フッ素化フェニルピリジン、フェニルピリミジン及びフェニルキノリンを伴うエレクトロルミネセントイリジウム化合物及びかかる化合物で作られたデバイス
【課題】改善された効率を示すエレクトロルミネセント化合物の提供。
【解決手段】本発明は一般に、エレクトロルミネセントIr(III)化合物、Ir(III)化合物を作るために使用される置換2−フェニルピリジン、フェニルピリミジン及びフェニルキノリン、ならびにIr(III)化合物で作られるデバイスに向けられている。
【解決手段】本発明は一般に、エレクトロルミネセントIr(III)化合物、Ir(III)化合物を作るために使用される置換2−フェニルピリジン、フェニルピリミジン及びフェニルキノリン、ならびにIr(III)化合物で作られるデバイスに向けられている。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、フッ素化フェニルピリジン、フェニルピリミジン及びフェニルキノリンに関する。これは同様に、活性層がエレクトロルミネセントIr(III)錯体を内含する電子デバイスにも関する。
【背景技術】
【0002】
本願は、米国特許仮出願第60/215362号(2000年6月30日出願)および同第60/224273号(2000年8月10日)に対する優先権を主張する国際出願第PCT/US01/20539号(2001年6月27日出願)の国内移行である、特願2002−507959号(国内移行日:2003年1月6日)に基づく分割出願である。
【0003】
表示装置を構成する発光ダイオードといったような光を発する有機電子デバイスが、さまざまな種類の電子機器の中に存在している。かかるデバイス全てにおいて、有機活性層は、2つの電気接点層の間にはさまれている。電気接点層の少なくとも1つは、光透過性であり、そのため、光は、電気接点層の中を通過することができる。有機活性層は、電気接点層を横断して電気を印加した時点で光透過性電気接点層を通して光を発出する。
【0004】
発光ダイオード内の活性成分として有機エレクトロルミネセント化合物を使用することは周知である。アントラセン、チアジアゾール誘導体及びクマリン誘導体といったような単純な有機分子が、エレクトロルミネッセンスを示すことが知られている。半導電性共役重合体も同様に、Friend et al. 米国特許第5,247,190号,Heeger et al., 米国特許第5,408,109号及びNakano et al., 公開された欧州特許出願第443,861号で開示されたように、エレクトロルミネセンス成分として使用されてきた。3価の金属イオン特にアンモニウムと8ヒドロキシキノレートの錯体が、例えば、Tang et al.,米国特許第5,552,678号の中で開示されてきたように、エレクトロルミネセンス成分として広く使用されてきた。
【0005】
Burrows 及び Thompson は、fac−トリス(2−フェニルピリジン)イリジウムを有機発光デバイス内で活性成分として使用できるということを報告した(Appl. Phys. Lett. 1999、75.4.)。イリジウム化合物がホスト導電性材料の中に存在する場合に、性能が最大となる。Thompsonは、活性層がfac−トリス〔2−(4’,5’−ジクロロフェニル)ピリジン−C12、N〕イリジウム(III)でドープされたポリ(N−ビニルカルバゾール)であるデバイスについてさらに報告した(Polymer Preprints 2000、41(1)、770)
【先行技術文献】
【特許文献】
【0006】
【特許文献1】米国特許第5,247,190号明細書
【特許文献2】米国特許第5,408,109号明細書
【特許文献3】欧州特許出願公開第443,861号明細書
【特許文献4】米国特許第5,552,678号明細書
【非特許文献】
【0007】
【非特許文献1】Appl. Phys. Lett. 1999、75.4.
【非特許文献2】Polymer Preprints 2000、41(1)、770
【非特許文献3】Synlett, 1999、45−48
【発明の概要】
【発明が解決しようとする課題】
【0008】
しかしながら、改善された効率を示すエレクトロルミネセント化合物に対するニーズがひき続き存在している。
【課題を解決するための手段】
【0009】
本発明は、配位子上に少なくとも1つのフッ素又はフッ素化された基が存在する少なくとも2つのフェニルピリジン配位子を有するイリジウム化合物(一般に「Ir(III)化合物」と呼ばれる)に向けられている。イリジウム化合物は、以下の第1の化学式を有する。
IrLaLbLcxL’yL’’z (第1化学式)
なお式中、
x=0又はy+z=0であり、y=2であるときz=0であることを条件として、x=0又は1、y=0、1又は2、及びz=0又は1であり;
L’が単座配位子であるときy+z=2であり、L’が二座配位子であるときz=0であることを条件として、L’=二座配位子又は単座配位子でありかつフェニルピリジン、フェニルピリミジン又はフェニルキノリンではなく;
L’’は、単座配位子であり、かつフェニルピリジン及びフェニルピリミジン又はフェニルキノリンではなく;
La、Lb及びLcは互いに同様であるか又は異なり、La、Lb及びLcの各々は
【0010】
【化1】

【0011】
という構造(I)を有し、式中、
R1−R4及びR5−R8の隣接対を接合させて5員環又は6員環を形成することができ、
R1−R8の少なくとも1つはF、CnF2n+1、OCnF2n+1及びOCF2Xから選択され、式中、n=1−6、X=H、Cl又はBrであり、
A=NであるときR1は存在しないことを条件として、A=C又はNである。
【0012】
もう1つの実施形態においては、本発明は、上述のIr(III)化合物を作る置換2−フェニルピリジン、フェニルピリミジン及びフェニルキノリン前駆体化合物に向けられる。前駆体化合物は、以下の構造(II)及び(III)を有する。
【0013】
【化2】

【0014】
(なお式中、A及びR1−R8は、上述の構造(I)に定義されている通りであり、R9はHである。)
【0015】
【化3】

【0016】
(なお式中、R10−R19のうちの少なくとも1つは、F、CnF2n+1、OCnF2n+1及びOCF2Xから選択され、n=1−6であり、X=H、Cl又はBr、R20はHである)。
【0017】
フェニル−ピリジン、フェニル−ピリミジン及びフェニル−キノリン結合を中心として自由な回転が存在することがわかる。しかしながら、本書の論述にあたっては、化合物を1つの配向に関して記述する。
【0018】
もう1つの実施形態においては、本発明は、上述のIr(III)化合物又は上述のIr(III)化合物の組合せを含む少なくとも1つの発光層を有する有機電子デバイスに向けられている。
【0019】
本書で使用される「化合物」という語は、物理的手段で分離できない原子でさらに構成されている分子から成る無帯電物質を意味するものとして意図されている。「配位子」という語は、金属イオンの配位圏に付着される分子、イオン又は原子を意味するものとして意図されている。「錯体」という語は、名詞として使用された場合、少なくとも1つのイオン及び少なくとも1つの配位子を有する化合物を意味するものとして意図されている。「基」という語は、1つの錯体内の配位子又は有機化合物内の置換基といった、1つの化合物の一部分を意味するものとして意図されている。「フェイシャル」という語は、3つの「a」基が全て隣接している、すなわち8面体の1面のコーナーにある、8面体の幾何形状を有する錯体Ma3b3の1つの異性体を意味することが意図されている。
【図面の簡単な説明】
【0020】
【図1】発光デバイス(LED)の概略図である。
【図2】LEDテスト器具の概略図である。
【発明を実施するための形態】
【0021】
本発明のIr(III)化合物は、上述の第1化学式Ir(III)LaLbLcxL’’yを有する。
【0022】
上述のIr(III)化合物は、往々にしてシクロメタレート化錯体と呼ばれる。すなわち、以下の第2化学式を有するIr(III)化合物は同様に往々にしてビス−シクロメタレート化錯体と呼ばれる。
IrLaLbL’yL’’z(第2化学式)
(なお式中、y、z、La、Lb、L’及びL’’は、上述の第1化学式で定義された通りである。
【0023】
以下の第3化学式を有するIr(III)も、往々にしてトリス−シクロメタレート化錯体と呼ばれる。
IrLaLbLc (第3化学式)
なお式中、
La、Lb及びLcは、上述の第1化学式に定義された通りである。
【0024】
好ましいシクロメタレート化錯体は中性かつ非イオン性であり、無傷の状態で昇華され得る。真空被着を介して得られたこれらの材料の薄膜は、良好乃至は優秀なエレクトロルミネセント特性を示す。イリジウム原子上の配位子内へのフッ素置換基の導入は、錯体の安定性及び揮発性の両方を増大させる。その結果、低温で真空被着を実施することができ、錯体の分解を回避することができる。配位子内へのフッ素置換基の導入により、往々にして非放射性崩壊速度及び固体状態での自己消光現象を低減させることができる。これらの低減は、エレクトロルミネセンス効率の増強を導く可能性がある。電子供与及び電子求引性特性を伴う置換基を変動させることで化合物のエレクトロルミネセント特性の微同調、ひいてはエレクトロルミネセントデバイスにおける明度及び効率の最適化が可能となる。
【0025】
理論による束縛を望むわけではないが、イリジウム化合物からの発光は、金属−配位子間の電荷移送の結果として配位子に基づくものであると考えられている。従って、エレクトロルミネセンスを示すことのできる化合物には、以上の第2化学式IrLaLbL’yL’’zの化合物、及び第3化学式IrLaLbLcの化合物が含まれ、ここでこの第3化学式中の全てのLa、Lb及びLcはフェニルピリジン、フェニルピリジン又はフェニルキノリンである。上述の構造(I)及び(II)のR1−R8基及び構造(III)のR10−R19基は、アルキル、アルコキシ、ハロゲン、ニトロ、及びシアノ基ならびにフルオロ、フッ素化アルキル及びフッ素化アルコキシ基といったような有機化合物のための従来の置換基から選択することができる。これらの基は、部分的に又は完全にフッ素化(過フッ素化)され得る。好ましいインジウム化合物の全てのR1−R8及びR16−R19置換基は、フルオロ、過フッ素化アルキル(CnF2n+1)及び過フッ素化アルキル基(OCnF2n+1)(なお、式中、過フッ素化アルキル及びアルコキシ基は、1〜6個の炭素原子を有する)か又は化学式(OCF2X)の基(式中、X=H、Cl又はBr)から選択されている。
【0026】
シクロメタレート化イリジウム錯体のエレクトロルミネセント特性は、R1−R8及びR10−R19基のうちのいずれか単数又は複数のものがニトロ基である場合により低いものとなる、ということがわかっている。従って、R1−R8及びR10−R19基のいずれもニトロ基でないことが好ましい。
【0027】
窒素含有環は、ピリジン環、ピリミジン環又はキノリン環であり得る。少なくとも1つのフッ素化置換基が、窒素含有環上にあることが好ましい(最も好ましくはCF3)。
【0028】
遷移金属配位化学にとって既知の従来のあらゆる配位子が、L’及びL’’配位子として適切である。二座配位子の例としては、置換可能なエチレンジアミン及びアセチルアセトネートといったような、2つの配位基を有する化合物が含まれる。単座配位子の例としては、塩化物及び硝酸塩イオン及びモノアミンが含まれる。イリジウム錯体は中性で昇華可能であることが好ましい。単一の二座配位子が使用される場合、マイナス1(−1)の正味電荷を有するはずである。2つの単座配位子が使用されている場合、これらは、マイナス1(−1)の組合せ正味電荷を有するはずである。ビス−シクロメタレート化錯体は、配位子全てが同じではないトリス−シクロメタレート化錯体を調製する上で有用であり得る。
【0029】
好ましい実施形態においては、イリジウム錯体は、上述のように第3化学式IrLaLbLcを有する。
【0030】
より好ましい実施形態においては、La=Lb=Lcである。これらのより好ましい化合物は好ましくは、イリジウムに配位された窒素原子がイリジウムに配位された炭素原子との関係においてトランスである、単結晶X線回折によって決定されるようなフェイシャル幾何形状を示すことが多い。これらのより好ましい化合物は、以下のような第4化学式を有する。
Fac−Ir(La)3 (第4化学式)
(式中、Laは、上述の構造(I)を有する)。
【0031】
化合物は同様に、イリジウムに配位された窒素原子のうちの2つが互いにトランスであるメリディオナル幾何形状を示す。これらの化合物は以下の第5化学式を有する:
mer−Ir(La)3 (第5化学式)
(式中、Laは上述の構造(I)を有する)。
【0032】
以上の第4化学式及び第5化学式の化合物の例は、下表1に示されている。
【0033】
【表1】

【0034】
上述の第2化学式IrLaLbL’yL’’zの化合物例としては、それぞれ以下の構造(IV)、(V)、(VI)、(IX)及び(X)を有する化合物1−n、1−o、1−p、1−w及び1−xが含まれる。
【0035】
【化4】

【0036】
【化5】

【0037】
上述の第3化学式IrLaLbLcのイリジウム錯体は一般に適切な置換2−フェニルピリジン、フェニルピリミジン又はフェニルキノリンから調製される。以上の構造(II)に示されているような置換2−フェニルピリジン;フェニルピリミジン及びフェニルキノリンは、O. Lohse, P.Thevenin, E.Waldvogel Synlett,1999、45−48に記述されているようにアリルホウ素酸と共に置換2−クロロピリジン、2−クロロピリミジン又は2−クロリキノリンのスズキカップリングを用いて、良好乃至優秀な収量で調製される。この反応は、以下の等式(1)の中で、X及びYが置換基を表わすものとしてピリジン誘導体について例示されている。
【0038】
【化6】

【0039】
上述の構造(II)を有する2−フェニルピリジン及び2−フェニルピリミジン 化合物の例は、下表2に示されている。
【0040】
【表2】

【0041】
上述の構造(II)を有する置換2−フェニルキノリン化合物の一例としては、R17=CF3及びR10−R16及びR18−R20=Hを有する化合物2−uがある。
【0042】
かくして調製された2−フェニルピリジン、ピリミジン及びキノリンは、シクロメタレート化イリジウム錯体の合成のために使用される。市販の三塩化イリジウム水和物及びトリフルオロ酢酸銀を利用する便利な1段階方法が開発されてきた。一般に反応は、3当量のAgOCOCF3の存在下で、溶剤無しで余剰の2−フェニルピリジン、ピリミジン又はキノリンを用いて実施される。この反応は、2−フェニルピリジンについて以下の等式(2)に例示されている:
【0043】
【化7】

【0044】
トリスシクロメタレート化イリジウム錯体は、単離、精製され、元素分析、1H及び19F NMRスペクトルデータそして化合物1−b、1−c及び1−eについては結晶X線回折によって完全に特徴づけされた。一部のケースでは、異性体混合物が得られた。往々にして、個々の異性体を単離することなく、混合物を使用することができる。
【0045】
一部のケースにおいては、上述の第2化学式IrLaLbL’yL’’zを有するイリジウム錯体を、上述の第3化学式IrLaLbLcを有する錯体の調製と同じ合成手順を用いて、反応混合物から単離することができる。錯体は同じく、まず最初に以下の構造(VII)を有する中間イリジウム二量体を調製することによって調製することもできる。
【0046】
【化8】

【0047】
(なお式中、B=H、CH3又はC2H5であり、La、Lb、Lc及びLdは互いに同じであっても異なっていてもよく、La、Lb、Lc及びLdの各々は上述の構造(I)を有する)
イリジウム二量体は一般に、まず最初に、2−フェニルピリジン、フェニルピリミジン又はフェニルキノリンと3塩化イリジウム水和物を反応させ、NaOBを添加することによって調製可能である。
【0048】
1つの特に有用なイリジウム二量体は、以下の構造(VIII)を有するヒドロキソイリジウム二量体である:
【0049】
【化9】

【0050】
この中間体は、アセト酢酸エチルを添加することによって化合物1−pを調製するために使用可能である。
【0051】
(電子デバイス)
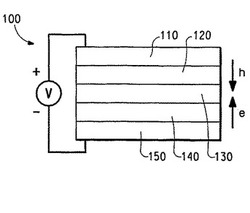
本発明は同様に、その少なくとも1つの層が本発明のイリジウム錯体を内含する、2つの電気接点層の間に位置づけされた少なくとも1つの光活性層を含む電子デバイスにも関する。デバイスは、付加的なホール輸送及び電子輸送層を有することが多い。標準的構造は図1に示されている。デバイス100は、陽極層110及び陰極層150を有する。陽極に隣接しているのは、ホール輸送材料を含む層120である。陰極に隣接しているのは、電子輸送材料を含む層140である。ホール輸送層と電子輸送層の間には、光活性層130がある。
【0052】
デバイス100の利用分野に応じて、光活性層130は、印加電圧により活性化される発光層(例えば発光ダイオード又は発光電気化学セルの場合)、放射エネルギーに応答し、印加されたバイアス電圧を伴って又は伴わずに信号を生成する材料層(例えば光検出機構の場合)でありうる。光検出機構の例としては、光伝導セル、光導電セル、フォトスイッチ、フォトトランジスタ及び光電管及び光電池が含まれる。なお、これらの用語はMarkus, John, エレクトロニクス及びヌクレオニクス辞典、470及び476(マグローヒル、Inc.1996)内で記述されている。
【0053】
本発明のイリジウム化合物は、層130中の光活性材料として又は層140中の電子輸送材料として有用である。好ましくは、本発明のイリジウム錯体は、ダイオード内に発光材料として使用されている。これらの利用分野では、本発明のフッ素化化合物は、有効であるために固体マトリクス希釈剤中にある必要はない。層の合計重量に基づいて20重量%以上最大で100%がイリジウム化合物である層を発光層として用いることができる。このことは、わずか6〜8重量%の量で発光層中に存在する場合に最大の効率を達成することが発見された非フッ素化イリジウム化合物つまりトリス(2−フェニルピリジン)イリジウム(III)とは対照的である。これは、自己消光効果を減少させるために必要であった。イリジウム化合物と共に、発光層中には、付加的な材料も存在し得る。例えば発光の色を変えるために、螢光染料が存在していてもよい。希釈剤を添加することも可能である。希釈剤は、ポリ(N−ビニルカルバゾル)及びポリシランといったような重合体材料であってもよい。それは、4、4’−N、N’−ジカルバゾルビフェニル又は第3級芳香族アミンといった小分子でもあり得る。希釈剤が使用される場合、イリジウム化合物は一般に、層の合計重量に基づいて、通常20重量%未満、好ましくは10重量%未満の少量で存在する。
【0054】
一部のケースでは、イリジウム錯体は、複数の異性体形態で存在することもでき、そうでなければ異なる錯体の混合物が存在していてもよい。OLEDについての以上の論述では、「イリジウム化合物」という語は化合物及び/又は異性体の混合物を包含することが意図されているということがわかるだろう。
【0055】
高効率LEDを実現するためには、ホール輸送材料のHOMO(最高占有分子軌道)は、陽極の仕事関数と整列しているべきであり、電子輸送材料のLUMO(最低未占有分子軌道)は、陰極の仕事関数と整列しているべきである。材料の化学的相容性及び昇華温度も又、電子及びホール輸送材料を選択する上で重要な考慮事項である。
【0056】
OLEDのその他の層は、かかる層において有用なものとして知られているあらゆる材料で作られていてよい。陽極110は、正電荷担体を注入するために特に効率の良い電極である。これは、例えば金属、混合金属、合金、金属酸化物又は混合金属酸化物を含有する材料で作られていてもよいし、或いは導電性重合体でもあり得る。適切な金属としては、第11群金属、第4群、5群及び6群の金属及び第8群〜10群の遷移金属が含まれる。陽極が、光透過性のものでなくてはならない場合には、インジウム、錫−酸化物といったような第12群、13群及び14群の金属の混合金属酸化物が一般に使用される。全体として、IUPAC付番システムが用いられ、ここでは、周期表からの群は、左から右へ1〜18と付番されている(CRC化学及び物理便覧)、2000年第81版)。陽極110は同様に、「可溶性導電性重合体から作られた可とう性発光ダイオード」Nature第357巻、p477〜479(1992年6月11日)の中で記述されているとおりのポリアニリンといったような有機材料をも含んでいてよい。陽極及び陰極のうちの少なくとも1つが少なくとも部分的に透明であって、生成された光を観察できるようになっているべきである。
【0057】
層120のためのホール輸送材料の例は、例えば、Y.WangのKirk−Othmer 化学技術百科事典、第4版、第18巻、p837〜860、1996年の中で要約されている。ホール輸送分子も重合体も、共に使用することができる。一般に使用されているホール輸送分子は、N,N’−ジフェニル−N,N’−ビス(3−メチルフェニル)−[1,1’−ビフェニル]−4,4’−ジアミン(TPD)、1,1−ビス[(ジ−4−トリルアミノ)フェニル]シクロヘキサン(TAPC)、N,N’−ビス(4−メチルフェニル)−N,N’−ビス(4−エチルフェニル)−[1,1’−(3,3’−ジメチル)ビフェニル]−4,4’−ジアミン(ETPD)、テトラキス−(3−メチルフェニル)−N,N,N’,N’−2,5−フェニレンジアミン (PDA)、 −フェニル−4−N,N−ジフェニルアミノスチレン(TPS)、p−(ジエチルアミノ)−ベンズアルデヒドジフェニルヒドラゾン(DEH)、トリフェニルアミン(TPA)、ビス[4−(N,N−ジエチルアミノ)−2−メチルフェニル](4−メチルフェニル)メタン(MPMP)、1−フェニル−3−[p−(ジエチルアミノ)スチリル]−5−[p−(ジエチルアミノ)フェニル]ピラゾリン(PPR又はDEASP)、1,2−トランス−ビス(9H−カルバゾル−9−イル)シクロブタン(DCZB)、N,N,N’,N’−テトラキス(4−メチルフェニル)−(1,1’−ビフェニル)−4,4’−ジアミン(TTB)、ポルフィリン化合物、例えば銅フタロシアニンといったものである。一般に使用されるホール輸送重合体は、ポリビニルカルバゾル、(フェニルメチル)ポリシラン及びポリアニリンである。ポリスチレン及びポリカーボネートといったような重合体内に上述のものといったようなホール輸送分子をドープすることによって、ホール輸送重合体を得ることも同様に可能である。
【0058】
層140のための電子輸送材料の例としては、トリス(8−ヒドロキシキノラト)アルミニウム(Alq3)、2,9−ジメチル−4,7−ジフェニル−1,10−フェナントロリン(DDPA)又は4,7−ジフェニル−1,10−フェナントロリン(DPA)といったフェナントロリンベースの化合物;及び、2−(4−ビフェニリル)−5−(4−t−ブチルフェニル)−1,3,4−オキサジアゾール(PBD)及び3−(4−ビフェニリル)−4−フェニル−5−(4−t−ブチルフェニル)−1,2,4−トリアゾール(TAZ)といったようなアゾル化合物が含まれる。層140は、電子輸送を容易にするためと同時に、層界面における励起子のクエンチングを防止するようバッファ層又は閉込め層としても役立つべく機能し得る。好ましくは、この層は、電子移動度を促進し、励起子クエンチングを低減させる。
【0059】
陰極150は、電子及び負の電荷担体を注入するのに特に効率が良い電極である。陰極は、陽極よりも低い仕事関数を有するあらゆる金属又は非金属でありうる。陰極用材料は、アクチニド及びランタニド及び希土類元素を含む第12群金属、第1群(例えばLi,Cs)、第2群(アルカリ土類)金属のアルカリ金属から選択され得る。アルミウニム、インジウム、カルシウム、バリウム、サマリウム及びマグネシウムといったような材料ならびにそれらの組合せも使用可能である。Li含有有機金属化合物も同様に、動作電圧を低下させるため有機層と陰極層の間に被着させることができる。
【0060】
有機電子デバイス内にその他の層を用いることも知られている。例えば、正電荷輸送及び/又は層の禁止帯幅整合を容易にするか又は保護層として機能するべく導電性重合体層120と活性層130の間に1つの層(図示せず)が存在し得る。同様にして、活性層130と陰極層150の間には、層間の負電荷輸送及び/又は禁止帯幅整合を容易にするか又は保護として機能するべく付加的な層(図示せず)が存在しうる。当該技術分野において既知の層を使用することができる。さらに、上述の層のいずれも、2層以上の層で作られていてよい。代替的には、無機陽極層110の一部又は全て、導電性重合体層120、活性層130及び陰極層150を表面処理して電荷担体輸送効率を高めることもできる。各々のコンポーネント層のための材料の選択は、好ましくは、高いデバイス効率でデバイスを提供するという最終目的のバランスをとることにより決定される。
【0061】
各々の機能層を複数の層で作ることもできるということも理解できる。
【0062】
デバイスは、適切な基板上に個々の層を順次蒸着させることによって調製できる。ガラス及び重合体膜といったような基板が利用可能である。熱蒸発、化学蒸着などといったような従来の蒸着技術を使用することができる。代替的には、従来のあらゆるコーティング技術を用いて、適切な溶剤中の溶液又は分散から、有機層をコーティングすることができる。一般的には、異なる層は以下のような厚み範囲を有することになる:陽極110、500〜5000Å、好ましくは1000〜2000Å;ホール輸送層120、50〜1000Å、好ましくは200〜800Å;発光層130、10〜1000Å好ましくは100〜800Å;電子輸送層140、50〜1000Å好ましくは200〜800Å;陰極150、200〜10000Å、好ましくは300〜5000Å。デバイス内の電子−ホール再結合ゾーンの場所ひいてはデバイスの発光スペクトルは、各層の相対的厚みによって影響され得る。かくして、電子−輸送層の厚みは、電子−ホール結合ゾーンが発光層内にくるように選択されるべきである。層厚みの望ましい比率は、使用される材料の正確な性質によって左右されることになる。
【0063】
本発明のイリジウム化合物で作られたデバイスの効率は、デバイス内のその他の層を最適化することによってさらに改善できるということがわかる。例えば、Ca、Ba又はLiFといったようなより効率の良い陰極を使用することもできる。動作電圧の低減を結果としてもたらすか又は量子効率を増大させる整形された基板及び新規輸送材料も同様に利用可能である。さまざまな層のエネルギーレベルを調整しエレクトロルミネセンスを容易にするために、付加的層をつけ加えることもできる。
【0064】
本発明のイリジウム錯体は往々にして、リン光性でかつホトルミネセントであり、OLED以外の利用分野でも有用であり得る。例えば、酸素感応性指示薬として、生物検定におけるリン光性指示薬として及び触媒として、イリジウムの有機金属錯体が使用されてきた。第3の配位子が同じであるか又は異なるものであるトリスシクロメタレート化錯体を合成するために、ビスシクロメタレート化錯体を使用することが可能である。
【実施例】
【0065】
以下の例は、本発明のいくつかの特長及び利点を例示する。これらは、本発明の一例として意図されているものであり、制限的意味を有するものではない。全ての百分率は、相反する指示のないかぎり重量百分率である。
【0066】
(実施例1)
この実施例は、イリジウム化合物を形成するために使用される2−フェニルピリジン及び2−フェニルピリミジンの調製を例示している。
【0067】
使用される一般的手順は、O.Lohse, P.Thevenin, E.Waldvogel Synlett, 1999、45−48の中で記述されたものである。標準的な実験においては、200mlの脱気水、20gの炭酸カリウム、150mlの1,2−ジメトキシエチレン、0.5gのPd(PPh3)4、0.05モルの置換2−クロロピリジン(キノリン又はビリミジン)及び0.05モルの置換フェニルホウ酸の混合物が、16〜30時間還流された(80〜90℃)。結果として得られた反応混合物を300mlの水で希釈し、CH2Cl2(2×100ml)で抽出した。組合さった有機層をMgSO4上で乾燥させ、溶剤を真空により除去した。分別真空蒸留によって液体生成物を精製した。固体材料をヘキサンから再結晶化させた。単離された材料の標準的純度は98%を超えていた。
【0068】
新しい材料の出発材料、収量、融点及び沸点は、下表3に示されている。NMRデータ及び分析データは下表4に示されている。
【0069】
【表3】

【0070】
【表4】

【0071】
【表5】

【0072】
【表6】

【0073】
(実施例2)
この実施例は、上述の第4化学式fac−Ir(La)3のイリジウム化合物の調製について例示している。
【0074】
標準的実験においては、IrCl3・nH2O(53〜55%Ir)、AgOCOCF3(Irあたり3.1当量)、2−アリルピリジン(余剰)及び(任意に)少量の水の混合物を、2〜8時間180〜195℃(油浴)でN2の下で勢いよくかき混ぜた。結果として得られた混合物を、抽出物が無色になるまでCH2Cl2で徹底的に抽出した。シリカカラムを通して抽出物を濾過して、透明で黄色の溶液を生成した。この溶液の蒸発により、残渣が得られ、これをメタノールで処理して有色の結晶質トリス−シクロメタレート化Ir錯体を生成した。錯体を濾過で分離し、メタノールで洗浄し、真空下で乾燥させ、(任意には)結晶化、真空昇華又はソックスレー抽出により精製した。収量:10〜82%。全ての材料は、NMR分光データ及び元素分析によって特徴づけされ、結果は下表5に示されている。シリーズの3つの錯体について単結晶X線構造を得た。
【0075】
(化合物1−b)
温度をゆっくりと(30分)185℃(油浴)まで上昇させながら、IrCl3・nH2O(54%Ir:508mg)、2−(4−フルオロフェニル)−5−トリフルオロメチルピリジン、化合物kk(2.20g)、AgOCOCF3(1.01g)及び水(1mL)の混合物をN2流の下で勢いよくかき混ぜた。185〜190℃で2時間後に、混合物は凝固した。混合物を室温まで冷却した。固体を、抽出物が脱色するまでジクロロメタンで抽出した。短かいシリカカラムを通して組合さったジクロロメタン溶液を濾過し蒸発させた。メタノール(50mL)を残渣に添加し、フラスコを−10℃に保ち一晩放置した。トリス−シクロメタレート化錯体の黄色沈殿物、化合物bを分離し、メタノールで洗浄し、真空下で乾燥させた。収量:1.07g(82%)。1,2−ジクロロエメタン中のその温かい溶液をゆっくり冷却することで錯体のX線品質の結晶を得た。
【0076】
(化合物1−e)
温度をゆっくりと(15分)192℃(油浴)まで上昇させながら、IrCl3・nH2O(54%Ir:504mg)、2−(3−トリフルオロメチルフェニル)−5−トリフルオロメチルピリジン、化合物bb(1.60g)及びAgOCOCF3(1.01g)の混合物をN2流の下で勢いよくかき混ぜた。190〜195℃で6時間後に、混合物は凝固した。混合物を室温まで冷却した。固体を、シリカカラム上に置き、これを、次に大量のジクロロメタンで洗浄した。濾過物の蒸発後の残渣をメタノールで処理して、黄色固体を生成した。固体を収集し、25−mLのマイクロ−ソックスレー抽出装置内でジクロロメタンでの抽出により精製した。トリス−シクロメタレート化 錯体の黄色沈殿物、化合物eを分離し、メタノールで洗浄し、真空下で乾燥させた。収量:0.59g(39%)。高温の1,2−ジクロロエタンから錯体のX線品質の結晶が得られた。
【0077】
(化合物1−d)
190〜195℃(油浴)で6時間15分の間、IrCl3・nH2O(54%Ir:508mg)、2−(2−フルオロフェニル)−5−トリフルオロメチルピリジン、化合物aa(1.53g)及びAgOCOCF3(1.01g)の混合物をN2流の下で勢いよくかき混ぜた。混合物を室温まで冷却し、次に、高温1,2−ジクロロエタンで抽出した。抽出物を短かいシリカカラムを通して濾過し、蒸発させた。メタノール(20mL)での残渣の処理は、望ましい生成物、化合物dの沈殿を結果としてもたらし、これを濾過により分離し、メタノールで洗浄し、真空下で乾燥させた。収量:0.63g(49%)。ジクロロメタン/メタノールから錯体のX線品質の結晶を得た。
【0078】
(化合物1−i)
190〜195℃(油浴)で2時間45分の間、IrCl3・nH2O(54%Ir:503mg)、2−(4−トリフルオロメトキシフェニル)−5−トリフルオロメチルピリジン、化合物ee(2.00g)及びAgOCOCF3(1.10g)の混合物をN2流の下で勢いよくかき混ぜた。混合物を室温まで冷却し、次に、ジクロロメタンで抽出した。抽出物を短かいシリカカラムを通して濾過し、蒸発させた。メタノール(20mL)での残渣の処理は、望ましい生成物、化合物iの沈殿を結果としてもたらし、これを濾過により分離し、メタノールで洗浄し、真空下で乾燥させた。収量は0.86gであった。さらに、母液を蒸発させ、残渣に石油エーテルを添加することにより0.27gの錯体を得た。全体的収量:1.13g(72%)。
【0079】
(化合物1−q)
温度をゆっくりと(30分)185℃(油浴)まで上昇させながら、IrCl3・nH2O(54%Ir:530mg)、2−(3−メトキシフェニル)−5−トリフルオロスメチルピリジン(2.50g)、AgOCOCF3(1.12g)及び水(1mL)の混合物をN2流の下で勢いよくかき混ぜた。185℃で1時間後に、混合物は凝固した。混合物を室温まで冷却した。固体を、抽出物が脱色するまでジクロロメタンで抽出した。短かいシリカカラムを通して組合さったジクロロメタン溶液を濾過し蒸発させた。残渣をヘキサンで洗浄し、次に1,2ジクロロエタン−ヘキサンから再結晶させた。収量:0.30g。19F NMR(CD2Cl2、20℃)、δ:−63(s)、1H NMR(CD2Cl2、20℃)、δ:8.1(1H)、7.9(1H)、7.8(1H)、7.4(1H)、6.6(2H)、4.8(3H)。1,2−ジクロロエタン−ヘキサンから、錯体(1,2−ジクロロエタン、ヘキサン溶媒和物)のX線品質の結晶を得た。このフェーシャル錯体は、オレンジ色光ルミネセントであった。
【0080】
同様の要領で、化合物1−a、1−c、1−f〜1−h、1−j〜1−m及び1−rを調製した。化合物 1−jの調製においては異性体の混合物が、R6又はR8位置のいずれかでフッ素と共に得られた。
【0081】
【表7】

【0082】
【表8】

【0083】
(実施例3)
この実施例は、上述の第2化学式 IrLaLbLcxL’yL’’zのイリジウム錯体の調製を例示するものである。
【0084】
(化合物1−n)
4時間190−195℃で、IrCl3・nH2O(54%Ir:510mg)、2−(3−トリフルオロメチルフェニル)−キノリン(1.80g)及びトリフルオロ酢酸銀(1.10g)の混合物を勢いよくかき混ぜた。結果として得た固体をジクロロメタンでシリカ上クロマトグラフィに付し、ジシクロメタレート化錯体と未反応配位子の混合物を生成した。温かいヘキサンでの抽出により、混合物から未反応配位子を除去した。抽出物が無色となった後、ヘキサン不溶性固体を収集し真空下で乾燥した。収量は、0.29gであった。19F NMR:−63.5(s.6F)、−76.5(s.3F)。この錯体の構造を、単結晶X線回折研究により立証した。
【0085】
(化合物1−o)
1.5時間190℃で、IrCl3・nH2O(54%Ir:500mg)、2−(2−フルオロフェニル)−3−クロロ−5−トリフルオロメチルピリジン(2.22g)、水(0.3mL)及びトリフルオロ酢酸銀(1.00g)の混合物を1.5時間190℃で撹拌した。固体生成物を、ジクロロメタンでシリカ上クロマトグラフィに付して、ジシクロメタレート化アクアトリフルオロアセタト錯体、化合物l−p及び未反応配位子の2:1の同時結晶化アダクツ0.33gを生成した。19F NMR:−63.0(9F)、−76.5(3F)、−87.7(2F)、−114.4(1F)。ジクロロメタン−ヘキサンから再結晶化により、同時結晶化されたフェニルピリジン配位子を除去した。アダクツと錯体の構造を単結晶X線回折研究により立証した。
【0086】
(実施例4)
この実施例は、上述の構造(VIII)を有するヒドロキソイリジウム二量体の調製を例示している。
【0087】
IrCl3・nH2O(54%Ir:510mg)、2−(4−フルオロフェニル)−5−トリフルオロメチルピリジン(725mg)、水(5mL)、及び2−エトキシエタノール(20mL)の混合物を、4、5時間還流下で勢いよくかき混ぜた。水(5mL)中のNaOH(2.3g)溶液を添加し、その後20mLの水を添加した後、混合物を2時間還流下でかき混ぜた。混合物を室温まで冷却し、50mLの水で希釈し、濾過した。固体を、30mLの1,2−ジクロロエタン及びNaOH水(水8mL中2.2g)を用いた還流の下で6時間勢いよくかき混ぜた。混合物から有機溶剤を蒸発させて、水相中のオレンジ色の固体の懸濁液を残した。オレンジ色の固体を濾過により分離し、水で徹底的に洗浄し、真空下で乾燥させて、0.94g(95%)のイリジウムヒドロキソ二量体(分光的に純粋のもの)を生成した。1H NMR(CD2Cl2):−1.0(s、1H、IrOH)、5.5(dd、2H)、6.6(dt、2H)、7.7(dd、2H)、7.9(dd、2H)、8.0(dd、2H)、9.1(d、2H)。19F NMR(CD2Cl2):−62.5(s、3F)、−109.0(ddd、1F)。
【0088】
(実施例5)
この実施例は、イリジウム二量体からのビス−シクロメタレート化錯体の調製を例示している。
【0089】
(化合物1−p)
実施例4からのイリジウムヒドロキソ二量体(100mg)アセト酢酸エチル(0.075mL;4倍余剰)及びジクロロメタン(4mL)の混合物を室温で一晩撹拌した。溶液を短かいシリカプラグを通して濾過し、蒸発させてオレンジ−黄色固体を得、これをヘキサンで洗浄して乾燥させた。錯体の収量は109mg(94%)であった。1H NMR(CD2Cl2):1.1(t、CH3)、3.9(dm、CH2)、4.8(s、CH3COCH)、5.9(m)、6.7(m)、7.7(m)、8.0(m)、8.8(d).19F NMR(CD2Cl2):−63.1(s、3F)、−63.2(s、3F)、−109.1(ddd、1F)、−109.5(ddd).分析:計算値:C、44.9;H、2.6;N、3.5.実際値C、44.4;H、2.6;N、3.3.
【0090】
(化合物1−w)
実施例4(0.20g)からのヒドロキソイリジウム二量体のTHF(6mL)溶液を、50mgのトリフルオロ酢酸で処理し、短かいシリカプラグを通して濾過し、計算上0.5mLまで蒸発させ、ヘキサン(8mL)で処理し、一晩放置した。黄色結晶固体を分離し、ヘキサンで洗浄し、真空下で乾燥させた。収量(1:1THF溶媒和物):0.24g(96%)。19F NMR(CD2Cl2、20℃)、δ:−63.2(s、3F)、−76.4(s、3F)、−107.3(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:9.2(br s、1H)、8.2(dd、1H)、8.1(d、1H)、7.7(m、1H)、6.7(m、1H)、5.8(dd、1H)、3.7(m、2H、THF)、1.8(m、2H、THF).
【0091】
(化合物1−x)
トリフルオロ酢酸中間物、化合物1−w(75mg)及び2−(4−ブロモフェニル)−5−ブロモピリジン(130mg)をN2下で150〜155℃で30分間撹拌した。結果として得られた固体を室温まで冷却し、CH2Cl2中で溶解させた。結果として得た溶液をシリカゲルを通して濾過し蒸発させた。残渣を数回温かいヘキサンで洗浄し、真空下で乾燥させて、黄色、黄色光ルミネセントの固体を残した。収量:74mg(86%)。19F NMR(CD2Cl2、20℃)、δ:−63.1(s、3F)、−63.3(s、3F)、−108.8(ddd、1F)、−109.1(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:8.2(s)、7.9(m)、7.7(m)、7.0(d)、6.7(m)、6.2(dd)、6.0(dd).錯体は、メリディオナル錯体であり、フッ素化配位子の窒素は、X線分析によって確認された通りトランスであった。
【0092】
(実施例6)
この実施例は、上述の第5化学式mer−Ir(La)3のイリジウム化合物の調製を例示するものである。
【0093】
(化合物1−s)
この錯体は、化合物1−nと類似の要領で合成された。NMR、TLC及びTGAデータによると、結果は、フェイシャル及びメリディオナル異性体のほぼ1:1の混合物であった。
【0094】
(化合物1−t)
温度をゆっくりと(30〜40分)165℃(油浴)まで上昇させながら、IrCl3・nH2O(54% Ir:0.40g)、2−(3,5−ジクロロフェニル)−5−トリフルオロメチルピリジン(1.40g)、AgOCOCF3(0.81g)及び水(0.5mL)の混合物をN2流の下で勢いよくかき混ぜた。165℃で40分後に、混合物は凝固した。混合物を室温まで冷却した。固体を、抽出物が脱色するまでジクロロメタンで抽出した。短かいシリカカラムを通して組合さったジクロロメタン溶液を濾過し蒸発させた。残渣をヘキサンで徹底的に洗浄し、真空下で乾燥させた。収量:0.53g(49%)。19F NMR(CD2Cl2、20℃)、δ:−63.55(s、3F)、−63.57(s、3F)、−63.67(s、3F)、−89.1(t、1F)、−100.6(t、1F)、102.8(dd、1F)、−118.6(ddd、1F)、−119.3(ddd、1F)、−123.3(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:8.4(s)、8.1(m)、7.9(m)、7.6(s)、7.5(m)、6.6(m)、6.4(m).錯体は、X線分析によっても確認された通り、メリディオナル錯体であった。
【0095】
(化合物1−u)
この錯体を、化合物1−qと類似の形で調製及び単離させ、次に1,2ジクロロエタン−ヘキサンから結晶化により精製した。精製された生成物は53%であった。錯体は、NMRデータから以下の通りmerである。19F NMR(CD2Cl2、20℃)、δ:−63.48(s、3F)、−63.52(s、6F)、−105.5(ddd、1F)、−105.9(ddd、1F)、−106.1(ddd、1F)、−107.4(t、1F)、−107.9(t、1F)、−109.3(t、1F).1H NMR(CD2Cl2、20℃)、δ:8.6(m)、8.3(s)、8.2(s)、8.1(m)、7.9(m)、7.6(m)、6.6(m)、6.4(m)、6.0(m)、5.8(m).
【0096】
(化合物1−v)
このmer−錯体を、トリフルオロアセテートジシクロメタレート化中間体、化合物1−x及び2−(4−フルオロフェニル)−5−トリフルオロメチルピリジンを用いて、化合物1−wと類似の要領で調製した。19F NMR(CD2Cl2、20℃)、δ:−63.30(s、3F)、−63.34(s、3F)、−63.37(s、3F)、−108.9(ddd、1F)、−109.0(ddd、1F)、−109.7(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:8.3−7.6(m)、6.7(m)、6.6(dd)、6.3(dd)、6.0(dd)。この黄色−ルミネセントメリディオナル錯体は、1気圧での昇華の時点で、緑色ルミネセントフェイシャル異性体つまり化合物1−bへと異性体化した。
【0097】
(実施例7)
この実施例は、本発明のイリジウム錯体を用いたOLEDの形成を例示している。
【0098】
熱蒸発技術を用いて、ホール輸送層(HT層)、エレクトロルミネセント層(EL層)及び少なくとも1つの電子輸送層(ET層)を含む薄膜OLEDデバイスを製造した。油拡散ポンプを伴うEdward Auto 306蒸発器を使用した。薄膜被着の全てについて基本真空は10-6 torr の範囲内であった。被着チャンバは、真空を中断させる必要なく、5枚の異なる膜を被着する能力を有していた。
【0099】
約1000−2000ÅのITO層を有するインジウム錫酸化物(ITO)でコーティングされたガラス基板を使用した。第1の電極パターンを形成するため、INのHCl溶液で望まれないITO部域をエッチングして除去することにより、まず最初に基板をパターン化した。パターン化されたITO基板を次に、洗剤水溶液中で超音波洗浄した。その後、基板をまずは精製水で洗い流し、その後最高3時間、トルエン蒸気で脱脂した。
【0100】
清浄し、パターン化したITO基板を次に真空チャンバ内に装入し、チャンバを10-6torrまでポンプダウンした。次に、約5〜10分間酸素プラズマを用いて、基板をさらに清浄した。清浄後、薄膜の多重層を熱蒸発により基板上に順次被着させた。最後に、Alのパターン化された金属電極をマスクを通して被着させた。水晶モニター(SyconSTC−200)を用いて、被着中、膜の厚みを測定した。実施例の中で報告されている全ての膜厚は、被着された材料の密度を1と仮定して計算された公称値である。完成したOLEDデバイスは次に真空チャンバから取出され、カプセル化せずに直ちに特徴づけされた。
【0101】
デバイス層及び厚みの要約が、表6に与えられている。全てのケースにおいて、陽極は、上述の通りITOであり、陰極は、700〜760Åの範囲内の厚みを有するAlであった。いくつかの標本において、2層の電子輸送層が使用された。最初に示された層は、EL層に隣接して塗布された。
【0102】
【表9】

【0103】
【表10】

【0104】
OLED標本は、それらの(1)電流−電圧(I−V)曲線、(2)エレクトロルミネセンス放射輝度と電圧の関係、及び(3)エレクトロルミネセンススペクトルと電圧の関係を測定することにより特徴づけされた。使用された器具200は、図2に示されている。OLED標本200のI−V曲線を、Keithleyソース測定ユニット237型、280で測定された。エレクトロルミネセンス放射輝度(Cd/m2単位)と電圧の関係は、Keithley SMUを用いて電圧を走査する間にMinolta LS−110ルミネセンス計210を用いて測定された。エレクトロルミネセンススペクトルは、電子シャッタ240を通して一対のレンズ230を用いて集光することによって得られ、スペクトログラフ250を通して分散され、その後ダイオードアレイ検出器260で測定された。3回の測定は全て同時に行なわれ、コンピュータ270により制御された。或る電圧におけるデバイスの効率は、デバイスをランさせるのに必要とされる電流密度でLEDのエレクトロルミネセンス放射輝度を除することによって決定される。単位はCd/Aである。
【0105】
結果は下表7に記されている:
【0106】
【表11】

【0107】
【表12】

【0108】
ピーク効率は、デバイス内のエレクトロルミネセント化合物の値を最も良く示すものである。それは、一定数の光子を出すために(放射輝度)デバイス内にどれほどの電子を入力しなければならないかの尺度を与える。それは、発光材料の固有の効率を反映する根本的に重要な数値である。より高い効率は、同じ放射輝度を達成するためにより少ない電子しか必要とされないことを意味し、そのこと自体より低い電力消費量を意味することから、実践的利用分野のためにもこれは重要である。より効率の高いデバイスは又、注入された電子が熱を発生するか又は望ましくない化学的副反応をひき起こす代りにより高い割合で光子に変換されることから、より長い寿命を有する傾向を有する。本発明のイリジウム錯体の大部分は、親fac−トリス(2−フェニルピリジン)イリジウム錯体に比べてはるかに高いピーク効率を有する。より低い効率を有する錯体も又、上述のように、リン光性又は光ルミネセント材料として又は触媒としての有用性を見い出すことができる。
【符号の説明】
【0109】
100 デバイス
110 陽極層
120 ホール輸送材料を含む層
130 光活性層
140 電子輸送材料を含む層
150 陰極層
200 器具
210 ルミネセンス計
230 レンズ
240 電子シャッタ
250 スペクトログラフ
260 ダイオードアレイ検出器
270 コンピュータ
【技術分野】
【0001】
本発明は、フッ素化フェニルピリジン、フェニルピリミジン及びフェニルキノリンに関する。これは同様に、活性層がエレクトロルミネセントIr(III)錯体を内含する電子デバイスにも関する。
【背景技術】
【0002】
本願は、米国特許仮出願第60/215362号(2000年6月30日出願)および同第60/224273号(2000年8月10日)に対する優先権を主張する国際出願第PCT/US01/20539号(2001年6月27日出願)の国内移行である、特願2002−507959号(国内移行日:2003年1月6日)に基づく分割出願である。
【0003】
表示装置を構成する発光ダイオードといったような光を発する有機電子デバイスが、さまざまな種類の電子機器の中に存在している。かかるデバイス全てにおいて、有機活性層は、2つの電気接点層の間にはさまれている。電気接点層の少なくとも1つは、光透過性であり、そのため、光は、電気接点層の中を通過することができる。有機活性層は、電気接点層を横断して電気を印加した時点で光透過性電気接点層を通して光を発出する。
【0004】
発光ダイオード内の活性成分として有機エレクトロルミネセント化合物を使用することは周知である。アントラセン、チアジアゾール誘導体及びクマリン誘導体といったような単純な有機分子が、エレクトロルミネッセンスを示すことが知られている。半導電性共役重合体も同様に、Friend et al. 米国特許第5,247,190号,Heeger et al., 米国特許第5,408,109号及びNakano et al., 公開された欧州特許出願第443,861号で開示されたように、エレクトロルミネセンス成分として使用されてきた。3価の金属イオン特にアンモニウムと8ヒドロキシキノレートの錯体が、例えば、Tang et al.,米国特許第5,552,678号の中で開示されてきたように、エレクトロルミネセンス成分として広く使用されてきた。
【0005】
Burrows 及び Thompson は、fac−トリス(2−フェニルピリジン)イリジウムを有機発光デバイス内で活性成分として使用できるということを報告した(Appl. Phys. Lett. 1999、75.4.)。イリジウム化合物がホスト導電性材料の中に存在する場合に、性能が最大となる。Thompsonは、活性層がfac−トリス〔2−(4’,5’−ジクロロフェニル)ピリジン−C12、N〕イリジウム(III)でドープされたポリ(N−ビニルカルバゾール)であるデバイスについてさらに報告した(Polymer Preprints 2000、41(1)、770)
【先行技術文献】
【特許文献】
【0006】
【特許文献1】米国特許第5,247,190号明細書
【特許文献2】米国特許第5,408,109号明細書
【特許文献3】欧州特許出願公開第443,861号明細書
【特許文献4】米国特許第5,552,678号明細書
【非特許文献】
【0007】
【非特許文献1】Appl. Phys. Lett. 1999、75.4.
【非特許文献2】Polymer Preprints 2000、41(1)、770
【非特許文献3】Synlett, 1999、45−48
【発明の概要】
【発明が解決しようとする課題】
【0008】
しかしながら、改善された効率を示すエレクトロルミネセント化合物に対するニーズがひき続き存在している。
【課題を解決するための手段】
【0009】
本発明は、配位子上に少なくとも1つのフッ素又はフッ素化された基が存在する少なくとも2つのフェニルピリジン配位子を有するイリジウム化合物(一般に「Ir(III)化合物」と呼ばれる)に向けられている。イリジウム化合物は、以下の第1の化学式を有する。
IrLaLbLcxL’yL’’z (第1化学式)
なお式中、
x=0又はy+z=0であり、y=2であるときz=0であることを条件として、x=0又は1、y=0、1又は2、及びz=0又は1であり;
L’が単座配位子であるときy+z=2であり、L’が二座配位子であるときz=0であることを条件として、L’=二座配位子又は単座配位子でありかつフェニルピリジン、フェニルピリミジン又はフェニルキノリンではなく;
L’’は、単座配位子であり、かつフェニルピリジン及びフェニルピリミジン又はフェニルキノリンではなく;
La、Lb及びLcは互いに同様であるか又は異なり、La、Lb及びLcの各々は
【0010】
【化1】

【0011】
という構造(I)を有し、式中、
R1−R4及びR5−R8の隣接対を接合させて5員環又は6員環を形成することができ、
R1−R8の少なくとも1つはF、CnF2n+1、OCnF2n+1及びOCF2Xから選択され、式中、n=1−6、X=H、Cl又はBrであり、
A=NであるときR1は存在しないことを条件として、A=C又はNである。
【0012】
もう1つの実施形態においては、本発明は、上述のIr(III)化合物を作る置換2−フェニルピリジン、フェニルピリミジン及びフェニルキノリン前駆体化合物に向けられる。前駆体化合物は、以下の構造(II)及び(III)を有する。
【0013】
【化2】

【0014】
(なお式中、A及びR1−R8は、上述の構造(I)に定義されている通りであり、R9はHである。)
【0015】
【化3】

【0016】
(なお式中、R10−R19のうちの少なくとも1つは、F、CnF2n+1、OCnF2n+1及びOCF2Xから選択され、n=1−6であり、X=H、Cl又はBr、R20はHである)。
【0017】
フェニル−ピリジン、フェニル−ピリミジン及びフェニル−キノリン結合を中心として自由な回転が存在することがわかる。しかしながら、本書の論述にあたっては、化合物を1つの配向に関して記述する。
【0018】
もう1つの実施形態においては、本発明は、上述のIr(III)化合物又は上述のIr(III)化合物の組合せを含む少なくとも1つの発光層を有する有機電子デバイスに向けられている。
【0019】
本書で使用される「化合物」という語は、物理的手段で分離できない原子でさらに構成されている分子から成る無帯電物質を意味するものとして意図されている。「配位子」という語は、金属イオンの配位圏に付着される分子、イオン又は原子を意味するものとして意図されている。「錯体」という語は、名詞として使用された場合、少なくとも1つのイオン及び少なくとも1つの配位子を有する化合物を意味するものとして意図されている。「基」という語は、1つの錯体内の配位子又は有機化合物内の置換基といった、1つの化合物の一部分を意味するものとして意図されている。「フェイシャル」という語は、3つの「a」基が全て隣接している、すなわち8面体の1面のコーナーにある、8面体の幾何形状を有する錯体Ma3b3の1つの異性体を意味することが意図されている。
【図面の簡単な説明】
【0020】
【図1】発光デバイス(LED)の概略図である。
【図2】LEDテスト器具の概略図である。
【発明を実施するための形態】
【0021】
本発明のIr(III)化合物は、上述の第1化学式Ir(III)LaLbLcxL’’yを有する。
【0022】
上述のIr(III)化合物は、往々にしてシクロメタレート化錯体と呼ばれる。すなわち、以下の第2化学式を有するIr(III)化合物は同様に往々にしてビス−シクロメタレート化錯体と呼ばれる。
IrLaLbL’yL’’z(第2化学式)
(なお式中、y、z、La、Lb、L’及びL’’は、上述の第1化学式で定義された通りである。
【0023】
以下の第3化学式を有するIr(III)も、往々にしてトリス−シクロメタレート化錯体と呼ばれる。
IrLaLbLc (第3化学式)
なお式中、
La、Lb及びLcは、上述の第1化学式に定義された通りである。
【0024】
好ましいシクロメタレート化錯体は中性かつ非イオン性であり、無傷の状態で昇華され得る。真空被着を介して得られたこれらの材料の薄膜は、良好乃至は優秀なエレクトロルミネセント特性を示す。イリジウム原子上の配位子内へのフッ素置換基の導入は、錯体の安定性及び揮発性の両方を増大させる。その結果、低温で真空被着を実施することができ、錯体の分解を回避することができる。配位子内へのフッ素置換基の導入により、往々にして非放射性崩壊速度及び固体状態での自己消光現象を低減させることができる。これらの低減は、エレクトロルミネセンス効率の増強を導く可能性がある。電子供与及び電子求引性特性を伴う置換基を変動させることで化合物のエレクトロルミネセント特性の微同調、ひいてはエレクトロルミネセントデバイスにおける明度及び効率の最適化が可能となる。
【0025】
理論による束縛を望むわけではないが、イリジウム化合物からの発光は、金属−配位子間の電荷移送の結果として配位子に基づくものであると考えられている。従って、エレクトロルミネセンスを示すことのできる化合物には、以上の第2化学式IrLaLbL’yL’’zの化合物、及び第3化学式IrLaLbLcの化合物が含まれ、ここでこの第3化学式中の全てのLa、Lb及びLcはフェニルピリジン、フェニルピリジン又はフェニルキノリンである。上述の構造(I)及び(II)のR1−R8基及び構造(III)のR10−R19基は、アルキル、アルコキシ、ハロゲン、ニトロ、及びシアノ基ならびにフルオロ、フッ素化アルキル及びフッ素化アルコキシ基といったような有機化合物のための従来の置換基から選択することができる。これらの基は、部分的に又は完全にフッ素化(過フッ素化)され得る。好ましいインジウム化合物の全てのR1−R8及びR16−R19置換基は、フルオロ、過フッ素化アルキル(CnF2n+1)及び過フッ素化アルキル基(OCnF2n+1)(なお、式中、過フッ素化アルキル及びアルコキシ基は、1〜6個の炭素原子を有する)か又は化学式(OCF2X)の基(式中、X=H、Cl又はBr)から選択されている。
【0026】
シクロメタレート化イリジウム錯体のエレクトロルミネセント特性は、R1−R8及びR10−R19基のうちのいずれか単数又は複数のものがニトロ基である場合により低いものとなる、ということがわかっている。従って、R1−R8及びR10−R19基のいずれもニトロ基でないことが好ましい。
【0027】
窒素含有環は、ピリジン環、ピリミジン環又はキノリン環であり得る。少なくとも1つのフッ素化置換基が、窒素含有環上にあることが好ましい(最も好ましくはCF3)。
【0028】
遷移金属配位化学にとって既知の従来のあらゆる配位子が、L’及びL’’配位子として適切である。二座配位子の例としては、置換可能なエチレンジアミン及びアセチルアセトネートといったような、2つの配位基を有する化合物が含まれる。単座配位子の例としては、塩化物及び硝酸塩イオン及びモノアミンが含まれる。イリジウム錯体は中性で昇華可能であることが好ましい。単一の二座配位子が使用される場合、マイナス1(−1)の正味電荷を有するはずである。2つの単座配位子が使用されている場合、これらは、マイナス1(−1)の組合せ正味電荷を有するはずである。ビス−シクロメタレート化錯体は、配位子全てが同じではないトリス−シクロメタレート化錯体を調製する上で有用であり得る。
【0029】
好ましい実施形態においては、イリジウム錯体は、上述のように第3化学式IrLaLbLcを有する。
【0030】
より好ましい実施形態においては、La=Lb=Lcである。これらのより好ましい化合物は好ましくは、イリジウムに配位された窒素原子がイリジウムに配位された炭素原子との関係においてトランスである、単結晶X線回折によって決定されるようなフェイシャル幾何形状を示すことが多い。これらのより好ましい化合物は、以下のような第4化学式を有する。
Fac−Ir(La)3 (第4化学式)
(式中、Laは、上述の構造(I)を有する)。
【0031】
化合物は同様に、イリジウムに配位された窒素原子のうちの2つが互いにトランスであるメリディオナル幾何形状を示す。これらの化合物は以下の第5化学式を有する:
mer−Ir(La)3 (第5化学式)
(式中、Laは上述の構造(I)を有する)。
【0032】
以上の第4化学式及び第5化学式の化合物の例は、下表1に示されている。
【0033】
【表1】

【0034】
上述の第2化学式IrLaLbL’yL’’zの化合物例としては、それぞれ以下の構造(IV)、(V)、(VI)、(IX)及び(X)を有する化合物1−n、1−o、1−p、1−w及び1−xが含まれる。
【0035】
【化4】

【0036】
【化5】

【0037】
上述の第3化学式IrLaLbLcのイリジウム錯体は一般に適切な置換2−フェニルピリジン、フェニルピリミジン又はフェニルキノリンから調製される。以上の構造(II)に示されているような置換2−フェニルピリジン;フェニルピリミジン及びフェニルキノリンは、O. Lohse, P.Thevenin, E.Waldvogel Synlett,1999、45−48に記述されているようにアリルホウ素酸と共に置換2−クロロピリジン、2−クロロピリミジン又は2−クロリキノリンのスズキカップリングを用いて、良好乃至優秀な収量で調製される。この反応は、以下の等式(1)の中で、X及びYが置換基を表わすものとしてピリジン誘導体について例示されている。
【0038】
【化6】

【0039】
上述の構造(II)を有する2−フェニルピリジン及び2−フェニルピリミジン 化合物の例は、下表2に示されている。
【0040】
【表2】

【0041】
上述の構造(II)を有する置換2−フェニルキノリン化合物の一例としては、R17=CF3及びR10−R16及びR18−R20=Hを有する化合物2−uがある。
【0042】
かくして調製された2−フェニルピリジン、ピリミジン及びキノリンは、シクロメタレート化イリジウム錯体の合成のために使用される。市販の三塩化イリジウム水和物及びトリフルオロ酢酸銀を利用する便利な1段階方法が開発されてきた。一般に反応は、3当量のAgOCOCF3の存在下で、溶剤無しで余剰の2−フェニルピリジン、ピリミジン又はキノリンを用いて実施される。この反応は、2−フェニルピリジンについて以下の等式(2)に例示されている:
【0043】
【化7】

【0044】
トリスシクロメタレート化イリジウム錯体は、単離、精製され、元素分析、1H及び19F NMRスペクトルデータそして化合物1−b、1−c及び1−eについては結晶X線回折によって完全に特徴づけされた。一部のケースでは、異性体混合物が得られた。往々にして、個々の異性体を単離することなく、混合物を使用することができる。
【0045】
一部のケースにおいては、上述の第2化学式IrLaLbL’yL’’zを有するイリジウム錯体を、上述の第3化学式IrLaLbLcを有する錯体の調製と同じ合成手順を用いて、反応混合物から単離することができる。錯体は同じく、まず最初に以下の構造(VII)を有する中間イリジウム二量体を調製することによって調製することもできる。
【0046】
【化8】

【0047】
(なお式中、B=H、CH3又はC2H5であり、La、Lb、Lc及びLdは互いに同じであっても異なっていてもよく、La、Lb、Lc及びLdの各々は上述の構造(I)を有する)
イリジウム二量体は一般に、まず最初に、2−フェニルピリジン、フェニルピリミジン又はフェニルキノリンと3塩化イリジウム水和物を反応させ、NaOBを添加することによって調製可能である。
【0048】
1つの特に有用なイリジウム二量体は、以下の構造(VIII)を有するヒドロキソイリジウム二量体である:
【0049】
【化9】

【0050】
この中間体は、アセト酢酸エチルを添加することによって化合物1−pを調製するために使用可能である。
【0051】
(電子デバイス)
本発明は同様に、その少なくとも1つの層が本発明のイリジウム錯体を内含する、2つの電気接点層の間に位置づけされた少なくとも1つの光活性層を含む電子デバイスにも関する。デバイスは、付加的なホール輸送及び電子輸送層を有することが多い。標準的構造は図1に示されている。デバイス100は、陽極層110及び陰極層150を有する。陽極に隣接しているのは、ホール輸送材料を含む層120である。陰極に隣接しているのは、電子輸送材料を含む層140である。ホール輸送層と電子輸送層の間には、光活性層130がある。
【0052】
デバイス100の利用分野に応じて、光活性層130は、印加電圧により活性化される発光層(例えば発光ダイオード又は発光電気化学セルの場合)、放射エネルギーに応答し、印加されたバイアス電圧を伴って又は伴わずに信号を生成する材料層(例えば光検出機構の場合)でありうる。光検出機構の例としては、光伝導セル、光導電セル、フォトスイッチ、フォトトランジスタ及び光電管及び光電池が含まれる。なお、これらの用語はMarkus, John, エレクトロニクス及びヌクレオニクス辞典、470及び476(マグローヒル、Inc.1996)内で記述されている。
【0053】
本発明のイリジウム化合物は、層130中の光活性材料として又は層140中の電子輸送材料として有用である。好ましくは、本発明のイリジウム錯体は、ダイオード内に発光材料として使用されている。これらの利用分野では、本発明のフッ素化化合物は、有効であるために固体マトリクス希釈剤中にある必要はない。層の合計重量に基づいて20重量%以上最大で100%がイリジウム化合物である層を発光層として用いることができる。このことは、わずか6〜8重量%の量で発光層中に存在する場合に最大の効率を達成することが発見された非フッ素化イリジウム化合物つまりトリス(2−フェニルピリジン)イリジウム(III)とは対照的である。これは、自己消光効果を減少させるために必要であった。イリジウム化合物と共に、発光層中には、付加的な材料も存在し得る。例えば発光の色を変えるために、螢光染料が存在していてもよい。希釈剤を添加することも可能である。希釈剤は、ポリ(N−ビニルカルバゾル)及びポリシランといったような重合体材料であってもよい。それは、4、4’−N、N’−ジカルバゾルビフェニル又は第3級芳香族アミンといった小分子でもあり得る。希釈剤が使用される場合、イリジウム化合物は一般に、層の合計重量に基づいて、通常20重量%未満、好ましくは10重量%未満の少量で存在する。
【0054】
一部のケースでは、イリジウム錯体は、複数の異性体形態で存在することもでき、そうでなければ異なる錯体の混合物が存在していてもよい。OLEDについての以上の論述では、「イリジウム化合物」という語は化合物及び/又は異性体の混合物を包含することが意図されているということがわかるだろう。
【0055】
高効率LEDを実現するためには、ホール輸送材料のHOMO(最高占有分子軌道)は、陽極の仕事関数と整列しているべきであり、電子輸送材料のLUMO(最低未占有分子軌道)は、陰極の仕事関数と整列しているべきである。材料の化学的相容性及び昇華温度も又、電子及びホール輸送材料を選択する上で重要な考慮事項である。
【0056】
OLEDのその他の層は、かかる層において有用なものとして知られているあらゆる材料で作られていてよい。陽極110は、正電荷担体を注入するために特に効率の良い電極である。これは、例えば金属、混合金属、合金、金属酸化物又は混合金属酸化物を含有する材料で作られていてもよいし、或いは導電性重合体でもあり得る。適切な金属としては、第11群金属、第4群、5群及び6群の金属及び第8群〜10群の遷移金属が含まれる。陽極が、光透過性のものでなくてはならない場合には、インジウム、錫−酸化物といったような第12群、13群及び14群の金属の混合金属酸化物が一般に使用される。全体として、IUPAC付番システムが用いられ、ここでは、周期表からの群は、左から右へ1〜18と付番されている(CRC化学及び物理便覧)、2000年第81版)。陽極110は同様に、「可溶性導電性重合体から作られた可とう性発光ダイオード」Nature第357巻、p477〜479(1992年6月11日)の中で記述されているとおりのポリアニリンといったような有機材料をも含んでいてよい。陽極及び陰極のうちの少なくとも1つが少なくとも部分的に透明であって、生成された光を観察できるようになっているべきである。
【0057】
層120のためのホール輸送材料の例は、例えば、Y.WangのKirk−Othmer 化学技術百科事典、第4版、第18巻、p837〜860、1996年の中で要約されている。ホール輸送分子も重合体も、共に使用することができる。一般に使用されているホール輸送分子は、N,N’−ジフェニル−N,N’−ビス(3−メチルフェニル)−[1,1’−ビフェニル]−4,4’−ジアミン(TPD)、1,1−ビス[(ジ−4−トリルアミノ)フェニル]シクロヘキサン(TAPC)、N,N’−ビス(4−メチルフェニル)−N,N’−ビス(4−エチルフェニル)−[1,1’−(3,3’−ジメチル)ビフェニル]−4,4’−ジアミン(ETPD)、テトラキス−(3−メチルフェニル)−N,N,N’,N’−2,5−フェニレンジアミン (PDA)、 −フェニル−4−N,N−ジフェニルアミノスチレン(TPS)、p−(ジエチルアミノ)−ベンズアルデヒドジフェニルヒドラゾン(DEH)、トリフェニルアミン(TPA)、ビス[4−(N,N−ジエチルアミノ)−2−メチルフェニル](4−メチルフェニル)メタン(MPMP)、1−フェニル−3−[p−(ジエチルアミノ)スチリル]−5−[p−(ジエチルアミノ)フェニル]ピラゾリン(PPR又はDEASP)、1,2−トランス−ビス(9H−カルバゾル−9−イル)シクロブタン(DCZB)、N,N,N’,N’−テトラキス(4−メチルフェニル)−(1,1’−ビフェニル)−4,4’−ジアミン(TTB)、ポルフィリン化合物、例えば銅フタロシアニンといったものである。一般に使用されるホール輸送重合体は、ポリビニルカルバゾル、(フェニルメチル)ポリシラン及びポリアニリンである。ポリスチレン及びポリカーボネートといったような重合体内に上述のものといったようなホール輸送分子をドープすることによって、ホール輸送重合体を得ることも同様に可能である。
【0058】
層140のための電子輸送材料の例としては、トリス(8−ヒドロキシキノラト)アルミニウム(Alq3)、2,9−ジメチル−4,7−ジフェニル−1,10−フェナントロリン(DDPA)又は4,7−ジフェニル−1,10−フェナントロリン(DPA)といったフェナントロリンベースの化合物;及び、2−(4−ビフェニリル)−5−(4−t−ブチルフェニル)−1,3,4−オキサジアゾール(PBD)及び3−(4−ビフェニリル)−4−フェニル−5−(4−t−ブチルフェニル)−1,2,4−トリアゾール(TAZ)といったようなアゾル化合物が含まれる。層140は、電子輸送を容易にするためと同時に、層界面における励起子のクエンチングを防止するようバッファ層又は閉込め層としても役立つべく機能し得る。好ましくは、この層は、電子移動度を促進し、励起子クエンチングを低減させる。
【0059】
陰極150は、電子及び負の電荷担体を注入するのに特に効率が良い電極である。陰極は、陽極よりも低い仕事関数を有するあらゆる金属又は非金属でありうる。陰極用材料は、アクチニド及びランタニド及び希土類元素を含む第12群金属、第1群(例えばLi,Cs)、第2群(アルカリ土類)金属のアルカリ金属から選択され得る。アルミウニム、インジウム、カルシウム、バリウム、サマリウム及びマグネシウムといったような材料ならびにそれらの組合せも使用可能である。Li含有有機金属化合物も同様に、動作電圧を低下させるため有機層と陰極層の間に被着させることができる。
【0060】
有機電子デバイス内にその他の層を用いることも知られている。例えば、正電荷輸送及び/又は層の禁止帯幅整合を容易にするか又は保護層として機能するべく導電性重合体層120と活性層130の間に1つの層(図示せず)が存在し得る。同様にして、活性層130と陰極層150の間には、層間の負電荷輸送及び/又は禁止帯幅整合を容易にするか又は保護として機能するべく付加的な層(図示せず)が存在しうる。当該技術分野において既知の層を使用することができる。さらに、上述の層のいずれも、2層以上の層で作られていてよい。代替的には、無機陽極層110の一部又は全て、導電性重合体層120、活性層130及び陰極層150を表面処理して電荷担体輸送効率を高めることもできる。各々のコンポーネント層のための材料の選択は、好ましくは、高いデバイス効率でデバイスを提供するという最終目的のバランスをとることにより決定される。
【0061】
各々の機能層を複数の層で作ることもできるということも理解できる。
【0062】
デバイスは、適切な基板上に個々の層を順次蒸着させることによって調製できる。ガラス及び重合体膜といったような基板が利用可能である。熱蒸発、化学蒸着などといったような従来の蒸着技術を使用することができる。代替的には、従来のあらゆるコーティング技術を用いて、適切な溶剤中の溶液又は分散から、有機層をコーティングすることができる。一般的には、異なる層は以下のような厚み範囲を有することになる:陽極110、500〜5000Å、好ましくは1000〜2000Å;ホール輸送層120、50〜1000Å、好ましくは200〜800Å;発光層130、10〜1000Å好ましくは100〜800Å;電子輸送層140、50〜1000Å好ましくは200〜800Å;陰極150、200〜10000Å、好ましくは300〜5000Å。デバイス内の電子−ホール再結合ゾーンの場所ひいてはデバイスの発光スペクトルは、各層の相対的厚みによって影響され得る。かくして、電子−輸送層の厚みは、電子−ホール結合ゾーンが発光層内にくるように選択されるべきである。層厚みの望ましい比率は、使用される材料の正確な性質によって左右されることになる。
【0063】
本発明のイリジウム化合物で作られたデバイスの効率は、デバイス内のその他の層を最適化することによってさらに改善できるということがわかる。例えば、Ca、Ba又はLiFといったようなより効率の良い陰極を使用することもできる。動作電圧の低減を結果としてもたらすか又は量子効率を増大させる整形された基板及び新規輸送材料も同様に利用可能である。さまざまな層のエネルギーレベルを調整しエレクトロルミネセンスを容易にするために、付加的層をつけ加えることもできる。
【0064】
本発明のイリジウム錯体は往々にして、リン光性でかつホトルミネセントであり、OLED以外の利用分野でも有用であり得る。例えば、酸素感応性指示薬として、生物検定におけるリン光性指示薬として及び触媒として、イリジウムの有機金属錯体が使用されてきた。第3の配位子が同じであるか又は異なるものであるトリスシクロメタレート化錯体を合成するために、ビスシクロメタレート化錯体を使用することが可能である。
【実施例】
【0065】
以下の例は、本発明のいくつかの特長及び利点を例示する。これらは、本発明の一例として意図されているものであり、制限的意味を有するものではない。全ての百分率は、相反する指示のないかぎり重量百分率である。
【0066】
(実施例1)
この実施例は、イリジウム化合物を形成するために使用される2−フェニルピリジン及び2−フェニルピリミジンの調製を例示している。
【0067】
使用される一般的手順は、O.Lohse, P.Thevenin, E.Waldvogel Synlett, 1999、45−48の中で記述されたものである。標準的な実験においては、200mlの脱気水、20gの炭酸カリウム、150mlの1,2−ジメトキシエチレン、0.5gのPd(PPh3)4、0.05モルの置換2−クロロピリジン(キノリン又はビリミジン)及び0.05モルの置換フェニルホウ酸の混合物が、16〜30時間還流された(80〜90℃)。結果として得られた反応混合物を300mlの水で希釈し、CH2Cl2(2×100ml)で抽出した。組合さった有機層をMgSO4上で乾燥させ、溶剤を真空により除去した。分別真空蒸留によって液体生成物を精製した。固体材料をヘキサンから再結晶化させた。単離された材料の標準的純度は98%を超えていた。
【0068】
新しい材料の出発材料、収量、融点及び沸点は、下表3に示されている。NMRデータ及び分析データは下表4に示されている。
【0069】
【表3】

【0070】
【表4】

【0071】
【表5】

【0072】
【表6】

【0073】
(実施例2)
この実施例は、上述の第4化学式fac−Ir(La)3のイリジウム化合物の調製について例示している。
【0074】
標準的実験においては、IrCl3・nH2O(53〜55%Ir)、AgOCOCF3(Irあたり3.1当量)、2−アリルピリジン(余剰)及び(任意に)少量の水の混合物を、2〜8時間180〜195℃(油浴)でN2の下で勢いよくかき混ぜた。結果として得られた混合物を、抽出物が無色になるまでCH2Cl2で徹底的に抽出した。シリカカラムを通して抽出物を濾過して、透明で黄色の溶液を生成した。この溶液の蒸発により、残渣が得られ、これをメタノールで処理して有色の結晶質トリス−シクロメタレート化Ir錯体を生成した。錯体を濾過で分離し、メタノールで洗浄し、真空下で乾燥させ、(任意には)結晶化、真空昇華又はソックスレー抽出により精製した。収量:10〜82%。全ての材料は、NMR分光データ及び元素分析によって特徴づけされ、結果は下表5に示されている。シリーズの3つの錯体について単結晶X線構造を得た。
【0075】
(化合物1−b)
温度をゆっくりと(30分)185℃(油浴)まで上昇させながら、IrCl3・nH2O(54%Ir:508mg)、2−(4−フルオロフェニル)−5−トリフルオロメチルピリジン、化合物kk(2.20g)、AgOCOCF3(1.01g)及び水(1mL)の混合物をN2流の下で勢いよくかき混ぜた。185〜190℃で2時間後に、混合物は凝固した。混合物を室温まで冷却した。固体を、抽出物が脱色するまでジクロロメタンで抽出した。短かいシリカカラムを通して組合さったジクロロメタン溶液を濾過し蒸発させた。メタノール(50mL)を残渣に添加し、フラスコを−10℃に保ち一晩放置した。トリス−シクロメタレート化錯体の黄色沈殿物、化合物bを分離し、メタノールで洗浄し、真空下で乾燥させた。収量:1.07g(82%)。1,2−ジクロロエメタン中のその温かい溶液をゆっくり冷却することで錯体のX線品質の結晶を得た。
【0076】
(化合物1−e)
温度をゆっくりと(15分)192℃(油浴)まで上昇させながら、IrCl3・nH2O(54%Ir:504mg)、2−(3−トリフルオロメチルフェニル)−5−トリフルオロメチルピリジン、化合物bb(1.60g)及びAgOCOCF3(1.01g)の混合物をN2流の下で勢いよくかき混ぜた。190〜195℃で6時間後に、混合物は凝固した。混合物を室温まで冷却した。固体を、シリカカラム上に置き、これを、次に大量のジクロロメタンで洗浄した。濾過物の蒸発後の残渣をメタノールで処理して、黄色固体を生成した。固体を収集し、25−mLのマイクロ−ソックスレー抽出装置内でジクロロメタンでの抽出により精製した。トリス−シクロメタレート化 錯体の黄色沈殿物、化合物eを分離し、メタノールで洗浄し、真空下で乾燥させた。収量:0.59g(39%)。高温の1,2−ジクロロエタンから錯体のX線品質の結晶が得られた。
【0077】
(化合物1−d)
190〜195℃(油浴)で6時間15分の間、IrCl3・nH2O(54%Ir:508mg)、2−(2−フルオロフェニル)−5−トリフルオロメチルピリジン、化合物aa(1.53g)及びAgOCOCF3(1.01g)の混合物をN2流の下で勢いよくかき混ぜた。混合物を室温まで冷却し、次に、高温1,2−ジクロロエタンで抽出した。抽出物を短かいシリカカラムを通して濾過し、蒸発させた。メタノール(20mL)での残渣の処理は、望ましい生成物、化合物dの沈殿を結果としてもたらし、これを濾過により分離し、メタノールで洗浄し、真空下で乾燥させた。収量:0.63g(49%)。ジクロロメタン/メタノールから錯体のX線品質の結晶を得た。
【0078】
(化合物1−i)
190〜195℃(油浴)で2時間45分の間、IrCl3・nH2O(54%Ir:503mg)、2−(4−トリフルオロメトキシフェニル)−5−トリフルオロメチルピリジン、化合物ee(2.00g)及びAgOCOCF3(1.10g)の混合物をN2流の下で勢いよくかき混ぜた。混合物を室温まで冷却し、次に、ジクロロメタンで抽出した。抽出物を短かいシリカカラムを通して濾過し、蒸発させた。メタノール(20mL)での残渣の処理は、望ましい生成物、化合物iの沈殿を結果としてもたらし、これを濾過により分離し、メタノールで洗浄し、真空下で乾燥させた。収量は0.86gであった。さらに、母液を蒸発させ、残渣に石油エーテルを添加することにより0.27gの錯体を得た。全体的収量:1.13g(72%)。
【0079】
(化合物1−q)
温度をゆっくりと(30分)185℃(油浴)まで上昇させながら、IrCl3・nH2O(54%Ir:530mg)、2−(3−メトキシフェニル)−5−トリフルオロスメチルピリジン(2.50g)、AgOCOCF3(1.12g)及び水(1mL)の混合物をN2流の下で勢いよくかき混ぜた。185℃で1時間後に、混合物は凝固した。混合物を室温まで冷却した。固体を、抽出物が脱色するまでジクロロメタンで抽出した。短かいシリカカラムを通して組合さったジクロロメタン溶液を濾過し蒸発させた。残渣をヘキサンで洗浄し、次に1,2ジクロロエタン−ヘキサンから再結晶させた。収量:0.30g。19F NMR(CD2Cl2、20℃)、δ:−63(s)、1H NMR(CD2Cl2、20℃)、δ:8.1(1H)、7.9(1H)、7.8(1H)、7.4(1H)、6.6(2H)、4.8(3H)。1,2−ジクロロエタン−ヘキサンから、錯体(1,2−ジクロロエタン、ヘキサン溶媒和物)のX線品質の結晶を得た。このフェーシャル錯体は、オレンジ色光ルミネセントであった。
【0080】
同様の要領で、化合物1−a、1−c、1−f〜1−h、1−j〜1−m及び1−rを調製した。化合物 1−jの調製においては異性体の混合物が、R6又はR8位置のいずれかでフッ素と共に得られた。
【0081】
【表7】

【0082】
【表8】

【0083】
(実施例3)
この実施例は、上述の第2化学式 IrLaLbLcxL’yL’’zのイリジウム錯体の調製を例示するものである。
【0084】
(化合物1−n)
4時間190−195℃で、IrCl3・nH2O(54%Ir:510mg)、2−(3−トリフルオロメチルフェニル)−キノリン(1.80g)及びトリフルオロ酢酸銀(1.10g)の混合物を勢いよくかき混ぜた。結果として得た固体をジクロロメタンでシリカ上クロマトグラフィに付し、ジシクロメタレート化錯体と未反応配位子の混合物を生成した。温かいヘキサンでの抽出により、混合物から未反応配位子を除去した。抽出物が無色となった後、ヘキサン不溶性固体を収集し真空下で乾燥した。収量は、0.29gであった。19F NMR:−63.5(s.6F)、−76.5(s.3F)。この錯体の構造を、単結晶X線回折研究により立証した。
【0085】
(化合物1−o)
1.5時間190℃で、IrCl3・nH2O(54%Ir:500mg)、2−(2−フルオロフェニル)−3−クロロ−5−トリフルオロメチルピリジン(2.22g)、水(0.3mL)及びトリフルオロ酢酸銀(1.00g)の混合物を1.5時間190℃で撹拌した。固体生成物を、ジクロロメタンでシリカ上クロマトグラフィに付して、ジシクロメタレート化アクアトリフルオロアセタト錯体、化合物l−p及び未反応配位子の2:1の同時結晶化アダクツ0.33gを生成した。19F NMR:−63.0(9F)、−76.5(3F)、−87.7(2F)、−114.4(1F)。ジクロロメタン−ヘキサンから再結晶化により、同時結晶化されたフェニルピリジン配位子を除去した。アダクツと錯体の構造を単結晶X線回折研究により立証した。
【0086】
(実施例4)
この実施例は、上述の構造(VIII)を有するヒドロキソイリジウム二量体の調製を例示している。
【0087】
IrCl3・nH2O(54%Ir:510mg)、2−(4−フルオロフェニル)−5−トリフルオロメチルピリジン(725mg)、水(5mL)、及び2−エトキシエタノール(20mL)の混合物を、4、5時間還流下で勢いよくかき混ぜた。水(5mL)中のNaOH(2.3g)溶液を添加し、その後20mLの水を添加した後、混合物を2時間還流下でかき混ぜた。混合物を室温まで冷却し、50mLの水で希釈し、濾過した。固体を、30mLの1,2−ジクロロエタン及びNaOH水(水8mL中2.2g)を用いた還流の下で6時間勢いよくかき混ぜた。混合物から有機溶剤を蒸発させて、水相中のオレンジ色の固体の懸濁液を残した。オレンジ色の固体を濾過により分離し、水で徹底的に洗浄し、真空下で乾燥させて、0.94g(95%)のイリジウムヒドロキソ二量体(分光的に純粋のもの)を生成した。1H NMR(CD2Cl2):−1.0(s、1H、IrOH)、5.5(dd、2H)、6.6(dt、2H)、7.7(dd、2H)、7.9(dd、2H)、8.0(dd、2H)、9.1(d、2H)。19F NMR(CD2Cl2):−62.5(s、3F)、−109.0(ddd、1F)。
【0088】
(実施例5)
この実施例は、イリジウム二量体からのビス−シクロメタレート化錯体の調製を例示している。
【0089】
(化合物1−p)
実施例4からのイリジウムヒドロキソ二量体(100mg)アセト酢酸エチル(0.075mL;4倍余剰)及びジクロロメタン(4mL)の混合物を室温で一晩撹拌した。溶液を短かいシリカプラグを通して濾過し、蒸発させてオレンジ−黄色固体を得、これをヘキサンで洗浄して乾燥させた。錯体の収量は109mg(94%)であった。1H NMR(CD2Cl2):1.1(t、CH3)、3.9(dm、CH2)、4.8(s、CH3COCH)、5.9(m)、6.7(m)、7.7(m)、8.0(m)、8.8(d).19F NMR(CD2Cl2):−63.1(s、3F)、−63.2(s、3F)、−109.1(ddd、1F)、−109.5(ddd).分析:計算値:C、44.9;H、2.6;N、3.5.実際値C、44.4;H、2.6;N、3.3.
【0090】
(化合物1−w)
実施例4(0.20g)からのヒドロキソイリジウム二量体のTHF(6mL)溶液を、50mgのトリフルオロ酢酸で処理し、短かいシリカプラグを通して濾過し、計算上0.5mLまで蒸発させ、ヘキサン(8mL)で処理し、一晩放置した。黄色結晶固体を分離し、ヘキサンで洗浄し、真空下で乾燥させた。収量(1:1THF溶媒和物):0.24g(96%)。19F NMR(CD2Cl2、20℃)、δ:−63.2(s、3F)、−76.4(s、3F)、−107.3(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:9.2(br s、1H)、8.2(dd、1H)、8.1(d、1H)、7.7(m、1H)、6.7(m、1H)、5.8(dd、1H)、3.7(m、2H、THF)、1.8(m、2H、THF).
【0091】
(化合物1−x)
トリフルオロ酢酸中間物、化合物1−w(75mg)及び2−(4−ブロモフェニル)−5−ブロモピリジン(130mg)をN2下で150〜155℃で30分間撹拌した。結果として得られた固体を室温まで冷却し、CH2Cl2中で溶解させた。結果として得た溶液をシリカゲルを通して濾過し蒸発させた。残渣を数回温かいヘキサンで洗浄し、真空下で乾燥させて、黄色、黄色光ルミネセントの固体を残した。収量:74mg(86%)。19F NMR(CD2Cl2、20℃)、δ:−63.1(s、3F)、−63.3(s、3F)、−108.8(ddd、1F)、−109.1(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:8.2(s)、7.9(m)、7.7(m)、7.0(d)、6.7(m)、6.2(dd)、6.0(dd).錯体は、メリディオナル錯体であり、フッ素化配位子の窒素は、X線分析によって確認された通りトランスであった。
【0092】
(実施例6)
この実施例は、上述の第5化学式mer−Ir(La)3のイリジウム化合物の調製を例示するものである。
【0093】
(化合物1−s)
この錯体は、化合物1−nと類似の要領で合成された。NMR、TLC及びTGAデータによると、結果は、フェイシャル及びメリディオナル異性体のほぼ1:1の混合物であった。
【0094】
(化合物1−t)
温度をゆっくりと(30〜40分)165℃(油浴)まで上昇させながら、IrCl3・nH2O(54% Ir:0.40g)、2−(3,5−ジクロロフェニル)−5−トリフルオロメチルピリジン(1.40g)、AgOCOCF3(0.81g)及び水(0.5mL)の混合物をN2流の下で勢いよくかき混ぜた。165℃で40分後に、混合物は凝固した。混合物を室温まで冷却した。固体を、抽出物が脱色するまでジクロロメタンで抽出した。短かいシリカカラムを通して組合さったジクロロメタン溶液を濾過し蒸発させた。残渣をヘキサンで徹底的に洗浄し、真空下で乾燥させた。収量:0.53g(49%)。19F NMR(CD2Cl2、20℃)、δ:−63.55(s、3F)、−63.57(s、3F)、−63.67(s、3F)、−89.1(t、1F)、−100.6(t、1F)、102.8(dd、1F)、−118.6(ddd、1F)、−119.3(ddd、1F)、−123.3(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:8.4(s)、8.1(m)、7.9(m)、7.6(s)、7.5(m)、6.6(m)、6.4(m).錯体は、X線分析によっても確認された通り、メリディオナル錯体であった。
【0095】
(化合物1−u)
この錯体を、化合物1−qと類似の形で調製及び単離させ、次に1,2ジクロロエタン−ヘキサンから結晶化により精製した。精製された生成物は53%であった。錯体は、NMRデータから以下の通りmerである。19F NMR(CD2Cl2、20℃)、δ:−63.48(s、3F)、−63.52(s、6F)、−105.5(ddd、1F)、−105.9(ddd、1F)、−106.1(ddd、1F)、−107.4(t、1F)、−107.9(t、1F)、−109.3(t、1F).1H NMR(CD2Cl2、20℃)、δ:8.6(m)、8.3(s)、8.2(s)、8.1(m)、7.9(m)、7.6(m)、6.6(m)、6.4(m)、6.0(m)、5.8(m).
【0096】
(化合物1−v)
このmer−錯体を、トリフルオロアセテートジシクロメタレート化中間体、化合物1−x及び2−(4−フルオロフェニル)−5−トリフルオロメチルピリジンを用いて、化合物1−wと類似の要領で調製した。19F NMR(CD2Cl2、20℃)、δ:−63.30(s、3F)、−63.34(s、3F)、−63.37(s、3F)、−108.9(ddd、1F)、−109.0(ddd、1F)、−109.7(ddd、1F).1H NMR(CD2Cl2、20℃)、δ:8.3−7.6(m)、6.7(m)、6.6(dd)、6.3(dd)、6.0(dd)。この黄色−ルミネセントメリディオナル錯体は、1気圧での昇華の時点で、緑色ルミネセントフェイシャル異性体つまり化合物1−bへと異性体化した。
【0097】
(実施例7)
この実施例は、本発明のイリジウム錯体を用いたOLEDの形成を例示している。
【0098】
熱蒸発技術を用いて、ホール輸送層(HT層)、エレクトロルミネセント層(EL層)及び少なくとも1つの電子輸送層(ET層)を含む薄膜OLEDデバイスを製造した。油拡散ポンプを伴うEdward Auto 306蒸発器を使用した。薄膜被着の全てについて基本真空は10-6 torr の範囲内であった。被着チャンバは、真空を中断させる必要なく、5枚の異なる膜を被着する能力を有していた。
【0099】
約1000−2000ÅのITO層を有するインジウム錫酸化物(ITO)でコーティングされたガラス基板を使用した。第1の電極パターンを形成するため、INのHCl溶液で望まれないITO部域をエッチングして除去することにより、まず最初に基板をパターン化した。パターン化されたITO基板を次に、洗剤水溶液中で超音波洗浄した。その後、基板をまずは精製水で洗い流し、その後最高3時間、トルエン蒸気で脱脂した。
【0100】
清浄し、パターン化したITO基板を次に真空チャンバ内に装入し、チャンバを10-6torrまでポンプダウンした。次に、約5〜10分間酸素プラズマを用いて、基板をさらに清浄した。清浄後、薄膜の多重層を熱蒸発により基板上に順次被着させた。最後に、Alのパターン化された金属電極をマスクを通して被着させた。水晶モニター(SyconSTC−200)を用いて、被着中、膜の厚みを測定した。実施例の中で報告されている全ての膜厚は、被着された材料の密度を1と仮定して計算された公称値である。完成したOLEDデバイスは次に真空チャンバから取出され、カプセル化せずに直ちに特徴づけされた。
【0101】
デバイス層及び厚みの要約が、表6に与えられている。全てのケースにおいて、陽極は、上述の通りITOであり、陰極は、700〜760Åの範囲内の厚みを有するAlであった。いくつかの標本において、2層の電子輸送層が使用された。最初に示された層は、EL層に隣接して塗布された。
【0102】
【表9】

【0103】
【表10】

【0104】
OLED標本は、それらの(1)電流−電圧(I−V)曲線、(2)エレクトロルミネセンス放射輝度と電圧の関係、及び(3)エレクトロルミネセンススペクトルと電圧の関係を測定することにより特徴づけされた。使用された器具200は、図2に示されている。OLED標本200のI−V曲線を、Keithleyソース測定ユニット237型、280で測定された。エレクトロルミネセンス放射輝度(Cd/m2単位)と電圧の関係は、Keithley SMUを用いて電圧を走査する間にMinolta LS−110ルミネセンス計210を用いて測定された。エレクトロルミネセンススペクトルは、電子シャッタ240を通して一対のレンズ230を用いて集光することによって得られ、スペクトログラフ250を通して分散され、その後ダイオードアレイ検出器260で測定された。3回の測定は全て同時に行なわれ、コンピュータ270により制御された。或る電圧におけるデバイスの効率は、デバイスをランさせるのに必要とされる電流密度でLEDのエレクトロルミネセンス放射輝度を除することによって決定される。単位はCd/Aである。
【0105】
結果は下表7に記されている:
【0106】
【表11】

【0107】
【表12】

【0108】
ピーク効率は、デバイス内のエレクトロルミネセント化合物の値を最も良く示すものである。それは、一定数の光子を出すために(放射輝度)デバイス内にどれほどの電子を入力しなければならないかの尺度を与える。それは、発光材料の固有の効率を反映する根本的に重要な数値である。より高い効率は、同じ放射輝度を達成するためにより少ない電子しか必要とされないことを意味し、そのこと自体より低い電力消費量を意味することから、実践的利用分野のためにもこれは重要である。より効率の高いデバイスは又、注入された電子が熱を発生するか又は望ましくない化学的副反応をひき起こす代りにより高い割合で光子に変換されることから、より長い寿命を有する傾向を有する。本発明のイリジウム錯体の大部分は、親fac−トリス(2−フェニルピリジン)イリジウム錯体に比べてはるかに高いピーク効率を有する。より低い効率を有する錯体も又、上述のように、リン光性又は光ルミネセント材料として又は触媒としての有用性を見い出すことができる。
【符号の説明】
【0109】
100 デバイス
110 陽極層
120 ホール輸送材料を含む層
130 光活性層
140 電子輸送材料を含む層
150 陰極層
200 器具
210 ルミネセンス計
230 レンズ
240 電子シャッタ
250 スペクトログラフ
260 ダイオードアレイ検出器
270 コンピュータ
【特許請求の範囲】
【請求項1】
以下の構造(II):
【化1】

を有し、式中、AおよびR1〜R9が、表2に示される2−a〜2−d、2−f〜2−r、2−t〜2−w及び2−y〜2−aa
【表1】

から選択されることを特徴とする化合物。
【請求項1】
以下の構造(II):
【化1】

を有し、式中、AおよびR1〜R9が、表2に示される2−a〜2−d、2−f〜2−r、2−t〜2−w及び2−y〜2−aa
【表1】

から選択されることを特徴とする化合物。
【図1】


【図2】




【図2】


【公開番号】特開2012−167124(P2012−167124A)
【公開日】平成24年9月6日(2012.9.6)
【国際特許分類】
【外国語出願】
【出願番号】特願2012−130172(P2012−130172)
【出願日】平成24年6月7日(2012.6.7)
【分割の表示】特願2002−507959(P2002−507959)の分割
【原出願日】平成13年6月27日(2001.6.27)
【出願人】(390023674)イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー (2,692)
【氏名又は名称原語表記】E.I.DU PONT DE NEMOURS AND COMPANY
【Fターム(参考)】
【公開日】平成24年9月6日(2012.9.6)
【国際特許分類】
【出願番号】特願2012−130172(P2012−130172)
【出願日】平成24年6月7日(2012.6.7)
【分割の表示】特願2002−507959(P2002−507959)の分割
【原出願日】平成13年6月27日(2001.6.27)
【出願人】(390023674)イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー (2,692)
【氏名又は名称原語表記】E.I.DU PONT DE NEMOURS AND COMPANY
【Fターム(参考)】
[ Back to top ]

