ブドウ培養細胞およびその培養方法
【課題】二次代謝産物を得るなどの所望の能力を持ったブドウ培養細胞を得るためには、適切なブドウ品種から培養細胞を作製し、それにあった培養条件を検討する必要があり、二次代謝産物の生合成の能力を維持したまま高い増殖力をもつブドウ培養細胞を作製し、その細胞の安定した培養を確立し、提供する。
【解決手段】白系ブドウ品種よりも赤系ブドウ品種の方が多く機能性成分を含んでいるため、赤系品種でなお且つ樹勢が強い品種「甲州」種から培養細胞を作製し、新規の本発明による培養条件により、増殖能力を高め、任意の二次代謝産物の生合成能力を付与することによりブドウ培養細胞を作製することができる。
【解決手段】白系ブドウ品種よりも赤系ブドウ品種の方が多く機能性成分を含んでいるため、赤系品種でなお且つ樹勢が強い品種「甲州」種から培養細胞を作製し、新規の本発明による培養条件により、増殖能力を高め、任意の二次代謝産物の生合成能力を付与することによりブドウ培養細胞を作製することができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、二次代謝産物生産のための植物培養細胞に関する。
【背景技術】
【0002】
近年、植物の二次代謝産物は医学、農学、食品の分野で利用されており、低コストで安定的に物質を得るために、植物培養細胞を用いた物質生産技術が考案されているブドウには、動脈硬化やアルツハイマー病、癌にポジティブな作用をもつリスベラトロールが含まれており、この物質を得るためにブドウ培養細胞に無作為メチル化β―シクロデキストリン (RMBCD) を処理し、細胞がレスベラトロールの合成および培地中への分泌を行う技術が開発されている (特表2005-514945)。さらに、植物培養細胞を用いた生産システムは、完全な閉鎖型培養を行うため、環境への負担が少なく、組み換え技術を用いた物質生産などが行えるため、組み換えタバコ培養細胞 (BY-2) による医療用タンパク質の生産技術も開発されている (特開2005-245228)。いずれの場合も、培養細胞には、細胞増殖の良さと植物体と同様な代謝システムの維持が求められる。
【0003】
しかしながら、ブドウ培養細胞は、現在実験で最もよく使われているタバコ培養細胞 (BY-2) と比較すると増殖能力が低い。これまでに代表的なブドウ品種であるカベルネソーヴィニヨンの培養細胞を作製したが、大変低い増殖能であった。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2005-245228号公報
【特許文献2】特表2005-514945号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
二次代謝産物を得るなどの所望の能力を持ったブドウ培養細胞を得るためには、適切なブドウ品種から培養細胞を作製し、それにあった培養条件を検討する必要があった。
本発明は、二次代謝産物の生合成の能力を維持したまま高い増殖力をもつブドウ培養細胞を作製し、その細胞の安定した培養方法を確立し、提供することを目的とする。
【課題を解決するための手段】
【0006】
白系ブドウ品種よりも赤系ブドウ品種の方が多く機能性成分を含んでいるため、赤系品種でなお且つ樹勢が強い品種「甲州」種から培養細胞を作製し、新規の本発明による培養条件により、増殖能力を高め、任意の二次代謝産物の生合成能力を付与することによりブドウ培養細胞を作製することができる。
【発明の効果】
【0007】
植物やその生産物を取得する場合、ある程度の栽培面積が必要で、気候や季節によって生産量が左右される。また、自然環境から植物を奪取することによる自然破壊が懸念される。しかし、植物培養細胞を用いれば、少ない培養面積で安定した生産が得られ、環境へのリスクが少なくなる。また、植物培養細胞は無機塩類を主とする培地で増殖できるので、低コスト化という効果も期待できる。
【0008】
本発明で確立したブドウ培養細胞は、高い増殖力と生存力を持つので、短期間に多くの
細胞が得られ、長期間生きたまま細胞を維持できる。また、ブドウの二次代謝産物は医療、農業、食品に広く利用されている。ブドウ培養細胞の二次代謝産物の生合成誘導や蓄積の機能は維持されているので、培養細胞に有効な物質を生産させることによって、少ない時間、労力、コストで大量に取得することが出来る。
【0009】
本ブドウ培養細胞に二次代謝産物の生合成を促進する遺伝子を導入すれば、より多くの物質を取得することが可能である。また、医療用タンパク質生産のための宿主細胞候補として、これまで高い増殖力をもつタバコ由来のBY-2が用いられているが、BY-2よりも高いバイオマス生産能力をもつ本培養細胞を用いれば、目的タンパク質をより大量に生産することが可能になる。また、ブドウ由来の培養細胞なので、動物由来と違い、医療や食品に安心して利用できる。
【図面の簡単な説明】
【0010】
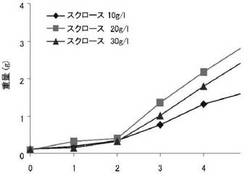
【図1】GV培地に含まれるショ糖濃度の違いによるブドウ培養細胞の増殖量
【図2】各温度および光条件下でのブドウ培養細胞の増殖量
【図3】各培地上でのブドウ培養細胞の増殖量(A:MM、GV、BSS培地上で培養 B:MM、GB、BSS培地上で培養)
【図4】甲州(A)とカベルネソーヴィニヨン(B)の培養細胞の増殖比較
【図5】甲州(A)とカベルネソーヴィニヨン(B)の培養細胞の増殖比較写真
【図6】ブドウ培養細胞とタバコ培養細胞の(BY−2)の増殖量の比較
【図7】ブドウ培養細胞を長期間培養したときの増殖量の変化
【図8】核小体内にGFPを発現するブドウ培養細胞の明視野像
【図9】図8のブドウ培養細胞の蛍光像(緑色蛍光はGFPを示す)
【発明を実施するための形態】
【0011】
本発明のブドウ培養細胞およびその培養方法は、最適な培地条件設定により、従来の植物培養細胞よりも高い増殖能を持つ。ブドウの種類は白系ブドウ品種よりも赤系ブドウ品種の方が多く機能性成分を含んでおり好ましく、赤系品種でなお且つ樹勢が強い品種「甲州」種が、特に好ましい。
【0012】
また遺伝子導入法には、アグロバクテリウム法、パーティクルガン法、エレクトロポーション法などの通常の導入方法を用いることができるが、本発明のブドウ培養細胞では、パーティクルガン法を用いることが好ましい。また導入される遺伝子群(ベクター)は、有用な二次代謝産物を合成する遺伝子群であれば、導入することができる。
【0013】
さらにブドウ細胞中に合成された二次代謝産物は、例えばジエチルエーテルまたはメタノール等の有機溶媒により抽出することができる。また細胞のまま、利用することができる。例えばブドウ培養細胞はリスベラトロールを合成することができるが、本発明の培養方法により、より高い合成速度を持つことができる。
【実施例1】
【0014】
カルス形成および培地の検討
樹勢の強い甲州種の新鞘から採集した腋芽を表面殺菌し、茎頂を摘出した。それを、1%ベンジルアデニンを含むムラシゲスクーグ(MS)培地上に置き、カルス形成を誘導した。カルス化した細胞を新鮮な培地に移し、培養細胞を作製した。同細胞株は、表1に示した培地で1〜2ヶ月毎に継代して培養した。従来のMM培地およびLS培地を基に最適条件の検討を行った。
【0015】
ショ糖濃度が、本細胞の増殖速度に大きな影響を与えることを見出し、最適なショ糖濃
度を検討した。ショ糖10 g/lのとき、培地上での増殖速度がもっとも低く、20、30 g/lのショ糖濃度の培地ではほぼ同じ増殖程度を示した (図1)。しかし、30 g/lの培地では、培養細胞の変色が観察されたため、ショ糖濃度は、20 g/lが適切であると判断した。また、LS培地上での培養細胞の増殖速度は、MM培地上よりも低かった。次に、光および温度の条件について検討した。結果を図2に示す。低い温度の場合、28℃での培養と比べて増殖速度が低くなった。また、明条件の方が暗条件よりもよい増殖が得られた。しかし、蛍光灯の光の種類によって増殖が著しく阻害されることや、明条件下では細胞の緑化や形態変化が見られたので、安定的な増殖のためには暗条件下での培養の方がよいと考えられる。MM培地、GV培地、BSS培地、GB培地上での細胞増殖を比較すると、BSS培地とGB培地で高い増殖を示した (図3A、B)。以上より、作製したブドウ培養細胞は、BSS培地およびGB培地 (ショ糖濃度20 g/l) 上で、28℃、暗条件で培養することを決定した。
【0016】
【表1】

【実施例2】
【0017】
増殖速度の評価
本発明において作製した甲州の培養細胞が、高い増殖力か否かを確かめるために、カベルネソーヴィニヨン由来培養細胞の増殖と比較した。その結果、いずれの培地上でも甲州由来培養細胞の方が、高い増殖であった (図4)。また培養細胞の様子を図5に示す。さらに、植物の培養細胞の中でも高い増殖能をもち、植物の細胞生物学的研究のstandard cell lineとなっているタバコ培養細胞 (BY-2) と比較したところ、ブドウ培養細胞は、BY-2よりもバイオマス生産能力が高かった (図6)。また、培養4週目ではBY-2の重量は減少し、細胞死が認められたが、ブドウ培養細胞は増殖を続けた。ブドウ培養細胞は、培養5週目では細胞増殖が認められたが、それ以降は停滞した(図7)。しかし、培養5週目での細胞死は認められなかった。以上のことから、新たに作製した培養細胞は、我々が決定した培養条件下において高い増殖能を持ち、さらに、BY-2よりも生存期間が長いという利点があることが分かった。
【実施例3】
【0018】
リスベラトロール合成の確認
ポリフェノールの一種であるリスベラトロールは、UV照射されたブドウによって合成・蓄積される。そこで、確立したブドウ培養細胞にUVを照射し、細胞内にリスベラトロールが蓄積されるか否か検討し、二次代謝産物の生合成能を確認した。結果を表2に示す。UV照射によって、リスベラトロールおよびその酸化誘導体 (ピセアタンノール)、オリゴマー体 (ビニフェリン) の蓄積が増加した。つまり、本ブドウ培養細胞は、二次代謝生産能を失っておらず、UVに対して植物体と同様な反応を示した。
【0019】
【表2】

【実施例4】
【0020】
遺伝子導入法の検討
液体培養4日目のブドウ細胞液1.5mlを、空シャーレ上の1/4にカットした円形ろ紙の上に落とした。この作業はクリーンベンチ内で行った。この時、ブドウ細胞がなるべく水平になるように置いた。シャーレにフタをしてクリーンベンチの外へ出し、パーティクルガン(バイオラッド社製)を用いて遺伝子導入を行った。パーティクルガンの遺伝子導入条件は、DNA 10 μg、金粒子量は 10 μgとした。また発射条件は、発射距離 3 cm、発射圧力 0.69 MPa とした。供試したベクターは、核小体でsynthetic green fluorescent protein gene (sGFP) を発現するように構成した遺伝子群を含む植物形質転換ベクターである。その後、すぐにクリーンベンチ内へ戻し、ろ紙ごとGM(ホルモン‐)固形培地の上に置き27℃インキュベーター内に静置させた。GM(ホルモン‐)培地の使用は、パーティクルガンで傷ついた細胞の修復促進を期待して選択した。
【0021】
2日後、カナマイシン濃度を10μg/ml、50μg/ml、100μg/ml、200μg/ml、400μg/mlとした各GB固定培地に細胞を移動させた。培地組成は表3に示す。この実験で用いたベクターにはカナマイシン耐性遺伝子が組み込まれている。この培地を用いて形質転換体の選択を行う。この作業はクリーンベンチ内で行った。火炎滅菌したスパチュラで、パーティクルガンが当たった部分およびその周辺を静かにすくい、固定培地に乗せた。この時、どの部分で形質転換体が得られるか不明なため、1つの固定培地に対して細胞を3〜4か所に乗せた。その後、27℃インキュベーター内で静置させた。
【0022】
16日後に細胞を観察したところ、カナマイシン濃度10μg/mlと50μg/mlへ移動させた細胞では、細胞塊表面は茶色くなっていたが、その内側では白い細胞が増殖していた。白い部分の細胞塊をBSS固定培地へ移動させ、27℃インキュベーター内で静置させた。BSS固定培地の使用は、細胞の成長促進を期待して選択した。100μg/ml、200μg/ml、400μg/mlでは、細胞塊全体が茶色くなり、細胞塊の大きさに変化がなかった。
【0023】
30日後、2種類のカナマイシン濃度からBSS固定培地へ移動させた細胞塊に成長が見られ、色も白かった。これらの細胞を採取してサンプルとし、蛍光顕微鏡で観察した。図 8、9に示す。その結果、核小体付近でGFP由来の蛍光が観察された。この結果は、本ブドウ細胞を用いて、目的とする細胞内小器官へ、目的のタンパク質を局所的に発現できることを意味する。
【0024】
【表3】

【産業上の利用可能性】
【0025】
本発明で確立したブドウ培養細胞は、高い増殖力と生存力を持ち、その二次代謝産物は医療、農業、食品に広く利用することができる。さらに植物培養細胞の遺伝子組み換え細胞として、本ブドウ培養細胞に二次代謝産物の生合成を促進する遺伝子を導入すれば、より多くの物質を生産・回収することが可能である。また医療用タンパク質生産のための宿主細胞候補として、これまで高い増殖力をもつBY-2が用いられているが、BY-2よりも高いバイオマス生産能力・生存力をもつ本培養細胞を用いれば、目的タンパク質をより大量に生産することが可能になる。
【技術分野】
【0001】
本発明は、二次代謝産物生産のための植物培養細胞に関する。
【背景技術】
【0002】
近年、植物の二次代謝産物は医学、農学、食品の分野で利用されており、低コストで安定的に物質を得るために、植物培養細胞を用いた物質生産技術が考案されているブドウには、動脈硬化やアルツハイマー病、癌にポジティブな作用をもつリスベラトロールが含まれており、この物質を得るためにブドウ培養細胞に無作為メチル化β―シクロデキストリン (RMBCD) を処理し、細胞がレスベラトロールの合成および培地中への分泌を行う技術が開発されている (特表2005-514945)。さらに、植物培養細胞を用いた生産システムは、完全な閉鎖型培養を行うため、環境への負担が少なく、組み換え技術を用いた物質生産などが行えるため、組み換えタバコ培養細胞 (BY-2) による医療用タンパク質の生産技術も開発されている (特開2005-245228)。いずれの場合も、培養細胞には、細胞増殖の良さと植物体と同様な代謝システムの維持が求められる。
【0003】
しかしながら、ブドウ培養細胞は、現在実験で最もよく使われているタバコ培養細胞 (BY-2) と比較すると増殖能力が低い。これまでに代表的なブドウ品種であるカベルネソーヴィニヨンの培養細胞を作製したが、大変低い増殖能であった。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2005-245228号公報
【特許文献2】特表2005-514945号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
二次代謝産物を得るなどの所望の能力を持ったブドウ培養細胞を得るためには、適切なブドウ品種から培養細胞を作製し、それにあった培養条件を検討する必要があった。
本発明は、二次代謝産物の生合成の能力を維持したまま高い増殖力をもつブドウ培養細胞を作製し、その細胞の安定した培養方法を確立し、提供することを目的とする。
【課題を解決するための手段】
【0006】
白系ブドウ品種よりも赤系ブドウ品種の方が多く機能性成分を含んでいるため、赤系品種でなお且つ樹勢が強い品種「甲州」種から培養細胞を作製し、新規の本発明による培養条件により、増殖能力を高め、任意の二次代謝産物の生合成能力を付与することによりブドウ培養細胞を作製することができる。
【発明の効果】
【0007】
植物やその生産物を取得する場合、ある程度の栽培面積が必要で、気候や季節によって生産量が左右される。また、自然環境から植物を奪取することによる自然破壊が懸念される。しかし、植物培養細胞を用いれば、少ない培養面積で安定した生産が得られ、環境へのリスクが少なくなる。また、植物培養細胞は無機塩類を主とする培地で増殖できるので、低コスト化という効果も期待できる。
【0008】
本発明で確立したブドウ培養細胞は、高い増殖力と生存力を持つので、短期間に多くの
細胞が得られ、長期間生きたまま細胞を維持できる。また、ブドウの二次代謝産物は医療、農業、食品に広く利用されている。ブドウ培養細胞の二次代謝産物の生合成誘導や蓄積の機能は維持されているので、培養細胞に有効な物質を生産させることによって、少ない時間、労力、コストで大量に取得することが出来る。
【0009】
本ブドウ培養細胞に二次代謝産物の生合成を促進する遺伝子を導入すれば、より多くの物質を取得することが可能である。また、医療用タンパク質生産のための宿主細胞候補として、これまで高い増殖力をもつタバコ由来のBY-2が用いられているが、BY-2よりも高いバイオマス生産能力をもつ本培養細胞を用いれば、目的タンパク質をより大量に生産することが可能になる。また、ブドウ由来の培養細胞なので、動物由来と違い、医療や食品に安心して利用できる。
【図面の簡単な説明】
【0010】
【図1】GV培地に含まれるショ糖濃度の違いによるブドウ培養細胞の増殖量
【図2】各温度および光条件下でのブドウ培養細胞の増殖量
【図3】各培地上でのブドウ培養細胞の増殖量(A:MM、GV、BSS培地上で培養 B:MM、GB、BSS培地上で培養)
【図4】甲州(A)とカベルネソーヴィニヨン(B)の培養細胞の増殖比較
【図5】甲州(A)とカベルネソーヴィニヨン(B)の培養細胞の増殖比較写真
【図6】ブドウ培養細胞とタバコ培養細胞の(BY−2)の増殖量の比較
【図7】ブドウ培養細胞を長期間培養したときの増殖量の変化
【図8】核小体内にGFPを発現するブドウ培養細胞の明視野像
【図9】図8のブドウ培養細胞の蛍光像(緑色蛍光はGFPを示す)
【発明を実施するための形態】
【0011】
本発明のブドウ培養細胞およびその培養方法は、最適な培地条件設定により、従来の植物培養細胞よりも高い増殖能を持つ。ブドウの種類は白系ブドウ品種よりも赤系ブドウ品種の方が多く機能性成分を含んでおり好ましく、赤系品種でなお且つ樹勢が強い品種「甲州」種が、特に好ましい。
【0012】
また遺伝子導入法には、アグロバクテリウム法、パーティクルガン法、エレクトロポーション法などの通常の導入方法を用いることができるが、本発明のブドウ培養細胞では、パーティクルガン法を用いることが好ましい。また導入される遺伝子群(ベクター)は、有用な二次代謝産物を合成する遺伝子群であれば、導入することができる。
【0013】
さらにブドウ細胞中に合成された二次代謝産物は、例えばジエチルエーテルまたはメタノール等の有機溶媒により抽出することができる。また細胞のまま、利用することができる。例えばブドウ培養細胞はリスベラトロールを合成することができるが、本発明の培養方法により、より高い合成速度を持つことができる。
【実施例1】
【0014】
カルス形成および培地の検討
樹勢の強い甲州種の新鞘から採集した腋芽を表面殺菌し、茎頂を摘出した。それを、1%ベンジルアデニンを含むムラシゲスクーグ(MS)培地上に置き、カルス形成を誘導した。カルス化した細胞を新鮮な培地に移し、培養細胞を作製した。同細胞株は、表1に示した培地で1〜2ヶ月毎に継代して培養した。従来のMM培地およびLS培地を基に最適条件の検討を行った。
【0015】
ショ糖濃度が、本細胞の増殖速度に大きな影響を与えることを見出し、最適なショ糖濃
度を検討した。ショ糖10 g/lのとき、培地上での増殖速度がもっとも低く、20、30 g/lのショ糖濃度の培地ではほぼ同じ増殖程度を示した (図1)。しかし、30 g/lの培地では、培養細胞の変色が観察されたため、ショ糖濃度は、20 g/lが適切であると判断した。また、LS培地上での培養細胞の増殖速度は、MM培地上よりも低かった。次に、光および温度の条件について検討した。結果を図2に示す。低い温度の場合、28℃での培養と比べて増殖速度が低くなった。また、明条件の方が暗条件よりもよい増殖が得られた。しかし、蛍光灯の光の種類によって増殖が著しく阻害されることや、明条件下では細胞の緑化や形態変化が見られたので、安定的な増殖のためには暗条件下での培養の方がよいと考えられる。MM培地、GV培地、BSS培地、GB培地上での細胞増殖を比較すると、BSS培地とGB培地で高い増殖を示した (図3A、B)。以上より、作製したブドウ培養細胞は、BSS培地およびGB培地 (ショ糖濃度20 g/l) 上で、28℃、暗条件で培養することを決定した。
【0016】
【表1】

【実施例2】
【0017】
増殖速度の評価
本発明において作製した甲州の培養細胞が、高い増殖力か否かを確かめるために、カベルネソーヴィニヨン由来培養細胞の増殖と比較した。その結果、いずれの培地上でも甲州由来培養細胞の方が、高い増殖であった (図4)。また培養細胞の様子を図5に示す。さらに、植物の培養細胞の中でも高い増殖能をもち、植物の細胞生物学的研究のstandard cell lineとなっているタバコ培養細胞 (BY-2) と比較したところ、ブドウ培養細胞は、BY-2よりもバイオマス生産能力が高かった (図6)。また、培養4週目ではBY-2の重量は減少し、細胞死が認められたが、ブドウ培養細胞は増殖を続けた。ブドウ培養細胞は、培養5週目では細胞増殖が認められたが、それ以降は停滞した(図7)。しかし、培養5週目での細胞死は認められなかった。以上のことから、新たに作製した培養細胞は、我々が決定した培養条件下において高い増殖能を持ち、さらに、BY-2よりも生存期間が長いという利点があることが分かった。
【実施例3】
【0018】
リスベラトロール合成の確認
ポリフェノールの一種であるリスベラトロールは、UV照射されたブドウによって合成・蓄積される。そこで、確立したブドウ培養細胞にUVを照射し、細胞内にリスベラトロールが蓄積されるか否か検討し、二次代謝産物の生合成能を確認した。結果を表2に示す。UV照射によって、リスベラトロールおよびその酸化誘導体 (ピセアタンノール)、オリゴマー体 (ビニフェリン) の蓄積が増加した。つまり、本ブドウ培養細胞は、二次代謝生産能を失っておらず、UVに対して植物体と同様な反応を示した。
【0019】
【表2】

【実施例4】
【0020】
遺伝子導入法の検討
液体培養4日目のブドウ細胞液1.5mlを、空シャーレ上の1/4にカットした円形ろ紙の上に落とした。この作業はクリーンベンチ内で行った。この時、ブドウ細胞がなるべく水平になるように置いた。シャーレにフタをしてクリーンベンチの外へ出し、パーティクルガン(バイオラッド社製)を用いて遺伝子導入を行った。パーティクルガンの遺伝子導入条件は、DNA 10 μg、金粒子量は 10 μgとした。また発射条件は、発射距離 3 cm、発射圧力 0.69 MPa とした。供試したベクターは、核小体でsynthetic green fluorescent protein gene (sGFP) を発現するように構成した遺伝子群を含む植物形質転換ベクターである。その後、すぐにクリーンベンチ内へ戻し、ろ紙ごとGM(ホルモン‐)固形培地の上に置き27℃インキュベーター内に静置させた。GM(ホルモン‐)培地の使用は、パーティクルガンで傷ついた細胞の修復促進を期待して選択した。
【0021】
2日後、カナマイシン濃度を10μg/ml、50μg/ml、100μg/ml、200μg/ml、400μg/mlとした各GB固定培地に細胞を移動させた。培地組成は表3に示す。この実験で用いたベクターにはカナマイシン耐性遺伝子が組み込まれている。この培地を用いて形質転換体の選択を行う。この作業はクリーンベンチ内で行った。火炎滅菌したスパチュラで、パーティクルガンが当たった部分およびその周辺を静かにすくい、固定培地に乗せた。この時、どの部分で形質転換体が得られるか不明なため、1つの固定培地に対して細胞を3〜4か所に乗せた。その後、27℃インキュベーター内で静置させた。
【0022】
16日後に細胞を観察したところ、カナマイシン濃度10μg/mlと50μg/mlへ移動させた細胞では、細胞塊表面は茶色くなっていたが、その内側では白い細胞が増殖していた。白い部分の細胞塊をBSS固定培地へ移動させ、27℃インキュベーター内で静置させた。BSS固定培地の使用は、細胞の成長促進を期待して選択した。100μg/ml、200μg/ml、400μg/mlでは、細胞塊全体が茶色くなり、細胞塊の大きさに変化がなかった。
【0023】
30日後、2種類のカナマイシン濃度からBSS固定培地へ移動させた細胞塊に成長が見られ、色も白かった。これらの細胞を採取してサンプルとし、蛍光顕微鏡で観察した。図 8、9に示す。その結果、核小体付近でGFP由来の蛍光が観察された。この結果は、本ブドウ細胞を用いて、目的とする細胞内小器官へ、目的のタンパク質を局所的に発現できることを意味する。
【0024】
【表3】

【産業上の利用可能性】
【0025】
本発明で確立したブドウ培養細胞は、高い増殖力と生存力を持ち、その二次代謝産物は医療、農業、食品に広く利用することができる。さらに植物培養細胞の遺伝子組み換え細胞として、本ブドウ培養細胞に二次代謝産物の生合成を促進する遺伝子を導入すれば、より多くの物質を生産・回収することが可能である。また医療用タンパク質生産のための宿主細胞候補として、これまで高い増殖力をもつBY-2が用いられているが、BY-2よりも高いバイオマス生産能力・生存力をもつ本培養細胞を用いれば、目的タンパク質をより大量に生産することが可能になる。
【特許請求の範囲】
【請求項1】
ブドウ品種である甲州種の新鞘から採取した腋芽を表面殺菌し、茎頂を摘出し、1%ベンジルアデニンを含むムラシゲスクーグ培地上に置き、カルス形成を誘導することにより作製されたブドウ培養細胞
【請求項2】
前記ブドウ培養細胞を、BSS培地またはGB培地において、ショ糖濃度10〜30g/Lであり、暗条件で培養することを特徴とするブドウ培養細胞の培養方法
【請求項3】
前記ブドウ培養細胞に、パーティクルガン法により遺伝子導入を行われることを特徴とする請求項2に記載のブドウ培養細胞の培養方法
【請求項4】
前記ブドウ培養細胞に、紫外線を照射し、前記ブドウ培養細胞内にリスベラトロールおよびその酸化誘導体 (ピセアタンノール)、オリゴマー体 (ビニフェリン)を合成・蓄積することを特徴とする請求項2に記載のブドウ培養細胞の培養方法
【請求項1】
ブドウ品種である甲州種の新鞘から採取した腋芽を表面殺菌し、茎頂を摘出し、1%ベンジルアデニンを含むムラシゲスクーグ培地上に置き、カルス形成を誘導することにより作製されたブドウ培養細胞
【請求項2】
前記ブドウ培養細胞を、BSS培地またはGB培地において、ショ糖濃度10〜30g/Lであり、暗条件で培養することを特徴とするブドウ培養細胞の培養方法
【請求項3】
前記ブドウ培養細胞に、パーティクルガン法により遺伝子導入を行われることを特徴とする請求項2に記載のブドウ培養細胞の培養方法
【請求項4】
前記ブドウ培養細胞に、紫外線を照射し、前記ブドウ培養細胞内にリスベラトロールおよびその酸化誘導体 (ピセアタンノール)、オリゴマー体 (ビニフェリン)を合成・蓄積することを特徴とする請求項2に記載のブドウ培養細胞の培養方法
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2013−5734(P2013−5734A)
【公開日】平成25年1月10日(2013.1.10)
【国際特許分類】
【出願番号】特願2011−139009(P2011−139009)
【出願日】平成23年6月23日(2011.6.23)
【出願人】(304023994)国立大学法人山梨大学 (223)
【Fターム(参考)】
【公開日】平成25年1月10日(2013.1.10)
【国際特許分類】
【出願日】平成23年6月23日(2011.6.23)
【出願人】(304023994)国立大学法人山梨大学 (223)
【Fターム(参考)】
[ Back to top ]

