プロスタサイクリン受容体拮抗薬の癌特異的導入剤による癌治療薬
【課題】本発明の課題は、癌増殖におけるEPCの関与について明らかにするとともに、EPCの機能及び増殖を抑制することにより、癌細胞の増殖を阻止することのできる、新しい癌治療剤を提供することにある。
【解決手段】 発明者らは、インビボでの実験により、IP欠損した骨髄細胞を移植したマウスでは、骨髄および末梢血中のEPCの機能が低下すること、また、同移植マウスにおいて、癌細胞増殖は正常骨髄細胞を移植したマウスと比較して、著しく抑えられること、さらに、単離した正常EPCの投与により、癌増殖性が回復することを見い出し、機能的EPCが癌増殖に不可欠であることを明らかにした。また、EPCの機能及び増殖がIP拮抗剤により抑制されることを見い出し、本発明を完成するに至った。
【解決手段】 発明者らは、インビボでの実験により、IP欠損した骨髄細胞を移植したマウスでは、骨髄および末梢血中のEPCの機能が低下すること、また、同移植マウスにおいて、癌細胞増殖は正常骨髄細胞を移植したマウスと比較して、著しく抑えられること、さらに、単離した正常EPCの投与により、癌増殖性が回復することを見い出し、機能的EPCが癌増殖に不可欠であることを明らかにした。また、EPCの機能及び増殖がIP拮抗剤により抑制されることを見い出し、本発明を完成するに至った。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、プロスタサイクリン受容体(IP)の拮抗剤を有効成分とする癌治療用組成物に関する。
【背景技術】
【0002】
近年、新しい癌治療戦略の一つとして血管新生制御による治療が注目されている。癌の増殖には、栄養供給路として腫瘍血管新生が必須であり、特に固形癌では、組織の直径1〜2mm以上に増殖するためには、既存血管から新生血管が延びて癌組織まで到達することが不可欠であることが知られている(非特許文献1)。また、癌組織が発達する際には、マクロファージ、繊維芽細胞、そして骨髄由来性血管内皮前駆細胞(EPC)を取り込みながら増殖していくことが明らかにされており、癌細胞の増殖や浸潤には様々な細胞が関与していると考えられている。なかでも、EPCは転移癌の初期の血管新生に非常に重要であることが示唆されているが(非特許文献2)、その役割の詳細については、いまだ不明な点が多く残されている。
【0003】
血管新生制御による癌治療法としては、既にVEGF/VEGFRファミリーに対する抗体療法や、チロシンリン酸化阻害薬を用いた治療法が開発されている(例えば、特許文献1)。しかし、腫瘍ごとに血管新生の際に依存する増殖因子の種類、程度が異なり、期待されるような治療効果がないのが現状である。また、癌増殖時に取り込まれる細胞群の多彩性も、血管増殖因子シグナルを標的とする治療効果を困難にしている。このため、癌種に依存せず普遍的な治療効果が期待できる、血管新生制御による癌治療法及び治療剤の開発が急がれている。
【0004】
最近、本願発明者らはEPCから産生されるプロスタサイクリン(PGI2としても知られる)が、細胞膜上の特異的プロスタサイクリン受容体(IP)を介して、EPCにオートクラインに作用し、EPCの増殖及び分化に深く関与することを明らかにした(特許文献2)。プロスタサイクリンは、生体内において主として血管内皮で産生される局所ホルモンであり、血管拡張作用、血圧降下作用、血小板凝集抑制作用等の生理活性を有している。そのため、プロスタサイクリンやそのアナログは、閉塞性動脈硬化、肺高血圧症、虚血性心疾患、糖尿病性大血管障害、糖尿病性腎症、糖尿病性網膜症等の治療に利用されている(例えば、特許文献3)。また、現在までにIPの拮抗剤(アンタゴニスト)として様々な物質が報告されており、抗炎症剤及び鎮痛剤として有用であることが知られているほか(例えば、特許文献4〜10)、心血管性疾患や(例えば、特許文献11)、神経障害性疾患の緩解に(特許文献12)、及び神経変性疾患の治療に(特許文献13)有用であることが示唆されている。しかし、癌増殖に及ぼすIP拮抗剤の影響については明らかにされておらず、IP拮抗剤が癌治療に有用である可能性は全く示唆されていなかった。
【0005】
【特許文献1】特開2007−045835号公報
【特許文献2】特願2007−281161号明細書
【特許文献3】特表2007−519604号公報
【特許文献4】特表2006−525254号公報
【特許文献5】国際公開第02/40453号パンフレット
【特許文献6】国際公開第02/070514号パンフレット
【特許文献7】国際公開第02/070500号パンフレット
【特許文献8】国際公開第01/68591号パンフレット
【特許文献9】欧州特許第0902018号明細書
【特許文献10】米国特許第6,184,242号明細書
【特許文献11】国際公開第79/00744号パンフレット
【特許文献12】国際公開第01/10433号パンフレット
【特許文献13】国際公開第01/10455号パンフレット
【非特許文献1】J. Folkman, J.Natl. Cancer Inst., 82: 4 (1990)
【非特許文献2】D. Gao et al., Science 319: 195-198 (2008)
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明の課題は、癌増殖におけるEPCの関与について明らかにするとともに、EPCの機能及び増殖を抑制することにより、癌細胞の増殖を阻止することのできる、新しい癌治療剤を提供することにある。
【課題を解決するための手段】
【0007】
発明者らは、インビボでの実験により、IP欠損した骨髄細胞を移植したマウスでは、骨髄および末梢血中のEPCの機能が低下すること、また、同移植マウスにおいて、癌細胞増殖は正常骨髄細胞を移植したマウスと比較して、著しく抑えられること、さらに、単離した正常EPCの投与により、癌増殖性が回復することを見い出し、機能的EPCが癌増殖に不可欠であることを明らかにした。また、EPCの機能及び増殖がIP拮抗剤により抑制されることを見い出し、本発明を完成するに至った。
【0008】
すなわち本発明は、(1)有効成分として1又は2以上のプロスタサイクリン受容体(IP)の拮抗剤を含むことを特徴とする癌治療用組成物や、(2)ドラッグデリバリーシステム(DDS)により、標的の癌細胞塊に特異的に取り込まれることを特徴とする上記(1)に記載の癌治療用組成物や、(3)DDS運搬体として、リポソームを用いることを特徴とする上記(2)に記載の癌治療用組成物や、(4)リポソームが、癌細胞を特異的に認識する抗体を結合させたターゲットリポソームであることを特徴とする上記(3)に記載の癌治療用組成物や、(5)IPの拮抗剤が、CAY10441であることを特徴とする上記(1)〜(4)いずれか記載の癌治療用組成物に関する。
【発明の効果】
【0009】
本発明のIP拮抗剤を含む癌治療用組成物は、癌組織における異常な血管新生を抑制することにより癌の増殖を抑えることができ、各種の癌に対して抗癌剤として使用することができる。
【発明を実施するための最良の形態】
【0010】
本発明のプロスタサイクリン受容体(IP)の拮抗剤としては、IPを介したプロスタサイクリンのシグナル伝達を阻害又は低下させる物質であれば特に制限されるものではなく、IPへのプロスタサイクリンの結合を阻害又は低下させる物質であっても、IPとプロスタサイクリンとの相互作用や、IPと関連するGタンパク質との相互作用に影響を及ぼすことにより、IP−プロスタサイクリン媒介性の細胞内シグナル伝達経路を阻害又は低下させる物質あってもよく、例えば、4,5−ジハイドロ−1H−イミダゾル−2−yl−4(4−イソプロポキシベンジル)フェニルアミン(4,5-dihydro-1H-imidazol-2-yl-4 (4-isopropoxybenzyl) phenylamine)や、欧州特許出願公開第09020l8号明細書に記載の2−(アリルフェニル)アミノ−イミダゾリン誘導体や、米国特許第6,184,242号明細書に記載の2−(置換されたフェニル)アミノ−イミダゾリン誘導体や、国際公開第02/070514号パンフレットに記載のアルコキシカルボニルアミノ・ヘテロアリール・カルボン酸誘導体や、国際公開第02/070500号パンフレットに記載のアルコキシカルボニルアミノ安息香酸またはアルコキシカルボニルアミノ・テトラゾリル・フェニル誘導体や、国際公開第02/40453号パンフレットに記載の2−フェニルアミノイミダゾリン・フェニルケトン誘導体や、国際公開第01/68591号パンフレットに記載のカルボン酸誘導体や、国際公開第01/10433号パンフレットに記載のアミノ−又はアミド−プロスタサイクリン誘導体合成物や、国際公開第01/10445号パンフレットに記載の15(R)イソカルバサイクリン又は15−デオキシイソカルバサイクリン誘導体や、国際公開第79/00744号パンフレットに記載の6,9-チアプロスタサイクリン類似体または誘導体;(5Z)-カルバサイクリン;FCE22176((5Z)-13,14−ジデヒドロ-20-メチル-カルボプロスタサイクリン)等を挙げることができ、なかでも、4,5−ジハイドロ−1H−イミダゾル−2−yl−4(4−イソプロポキシベンジル)フェニルアミン(4,5-dihydro-1H-imidazol-2-yl-4 (4-isopropoxybenzyl) phenylamine;CAY10441、Cayman Chemical社製)を好適に例示することができる。
【0011】
本発明の癌治療用が有効な癌としては、機能的EPCの存在が癌細胞増殖や癌組織形成に関与する癌であれば特に制限されず、例えば、肺癌、卵巣癌、膵臓癌、胃癌、胆嚢癌、腎臓癌、前立腺癌、乳癌、食道癌、肝臓癌、口腔癌、結腸癌、大腸癌、直腸癌、子宮癌、胆管癌、膵島細胞癌、副腎皮質癌、膀胱癌、精巣癌、睾丸腫瘍、甲状腺癌 、皮膚癌 、悪性カルチノイド腫瘍、メラノーマ、グリオーマ、骨肉腫、骨髄腫、軟部組織肉腫、神経芽細胞腫、悪性リンパ腫や白血病等の造血器腫瘍が挙げられるが、なかでも、肺癌を好適に例示することができる。
【0012】
本発明の癌治療用組成物は経口的又は非経口的に投与することができる。すなわち通常用いられる投与形態、例えば、粉末、顆粒、カプセル剤、シロップ剤、懸濁液等の剤型で経口的に投与することも、例えば、溶液、乳剤、懸濁液等の剤型にしたものを注射又はスプレーの型で非経口投与することもできるが、好ましい投与形態として、ドラッグデリバリーシステム(DDS)により標的の癌細胞塊に特異的に取り込まれるような投与形態を挙げることができ、特に好ましい投与形態として、ターゲティング(標的指向)DDSによる投与形態を挙げることができる。ここでドラッグデリバリーシステム(DDS)とは、癌細胞や標的組織等を狙い撃ちする薬物や遺伝子送達システムを意味するものであり、その中でも特にターゲティング(標的指向)DDSとは、薬物を「体内の必要な部位に」、「必要な量を」、「必要な時間だけ」送り込むといった概念である。ターゲティングDDSの代表的な運搬体として微粒子性キャリアーであるリポソームが挙げられる。この粒子に標的指向機能をもたせるために、リポソームの脂質の種類、組成比、粒子径、表面電荷を変化させるなどの受動的ターゲティング法があり、また、さらに高機能の能動的ターゲティング法として、リポソーム膜面上にリガンドを結合させ、標的組織の細胞膜面上に存在するレセプターに特異的に認識させることによって、積極的にターゲティングを可能にさせる方法が開発されている。この能動的ターゲティング法での標的となる細胞膜面上に存在するレセプターのリガンドとしては、抗原、抗体、ペプチド、糖脂質や糖蛋白質などを例示することができる。本発明の癌治療用組成物の投与に際しては、例えば、癌細胞を特異的に認識する抗体を結合させたターゲットリポソームを運搬体として用いることができ、上記癌細胞を特異的に認識する抗体としては、例えば、メラノーマ特異的モノクローナル抗体であるR24や、卵巣癌特異的モノクローナル抗体であるOvaRexや、大腸癌特異的モノクローナル抗体であるPanorexや、肺癌特異的モノクローナル抗体であるBEC2や、乳癌特異的モノクローナル抗体であるHerceptinや、急性骨髄性白血病(AML)特異的モノクローナル抗体であるSmartM195や、非ホジキンリンパ種(NHL)特異的モノクローナル抗体であるRituxanを好例として挙げることができる。
【0013】
以下、実施例により本発明をより具体的に説明するが、本発明の技術的範囲はこれらの例示に限定されるものではない。
【実施例1】
【0014】
[内皮前駆細胞(EPC)の単離]
野生型(WT)又はIP欠損型(IP−/−)マウスから骨髄を採取し、Histopaque 1083(登録商標)(Sigma社製)を用いて濃度勾配遠心分離を行い単核細胞を得た。次に、magnetic sorting system(Lineage deletion kit及びMulti-sorting system; Miltenyi Biotec社製)を用いて、骨髄単核細胞からlineage陰性(Lin-)、且つcKit/Sca1陽性(cKit+/Sca1+)の細胞を単離した。得られたLin-/cKit+/Sca1+細胞をEPCとして以後の実験で用いた。
【実施例2】
【0015】
[EPCの増殖・分化に及ぼすIPの影響]
実施例1で得られたEPCを、フィブロネクチンでコートしたプレートに播種し、α−MEM(GIBCO社製;#12571-063)培地[10質量%ウシ胎児血清、100μg/ml内皮細胞成長因子 E2759(Sigma社製)、100ng/mlマウス組換えVEGF(Sigma社製)、10U/mlヘパリン硫酸塩(Sigma社製)、100U/mlペニシリン、100μg/mlストレプトマイシン]を用い、5%CO2存在下、37℃で7日間培養した。培養細胞のコロニー形成能を、DiI-acLDL 及びFITC-lectinを用いた染色法により評価した結果、IP欠損EPCでは著明に低下していることが明らかとなった(図1a及び図1b)。また、長期間(2週間)培養後のそれぞれの細胞を、成熟内皮細胞マーカーであるvWFにより染色した結果、IP欠損EPCでは分化能が有意に低いことが示された(図1c及び図1d)。以上の結果から、IPがEPCの増殖及び分化に関与する可能性が示唆された。
【実施例3】
【0016】
[移植癌細胞の増殖に及ぼすEPCの影響]
致死的照射されたヌードマウス(ICRnu/nu)に、野生型(WT)又はIP欠損型(IP−/−)マウスから採取した骨髄細胞を移植した。4週間後に骨髄が生着したことを確認し、WT由来骨髄を移植されたマウス(BMT(WT))とIP−/−由来骨髄を移植されたマウス(BMT(IP))の背部皮下に、ヒト肺小細胞癌細胞SBC−1とMS−1−Lを接種した。癌細胞の移植後3週間にわたって、経時的な腫瘍体積の変化、血中EPC数、及び機能性EPC数の検討を行った。BMT(IP)群における移植腫瘍の体積は、BMT(WT)群と比較して有意に小さかった(図2)。また、移植3週間後のEPCの末梢血中数(%)は両群に差はなかったが、BMT(IP)群では機能性EPCの数が有意に低下していた(図3)。さらに、BMT(IP)マウスに、癌細胞移植と同時に、単離した正常EPCを補充した場合(BMT(IP)+EPC(WT))、癌細胞増殖能が回復することが明らかとなった(図2)。以上の結果は、腫瘍の形成及び増殖において、EPCが重要な役割を果たしており、IPの欠損によるEPC機能の抑制により、腫瘍の増殖が抑えられる可能性が示された。
【実施例4】
【0017】
[IP抑制薬剤によるEPC機能抑制作用]
単離したEPC(WT)を、実施例2と同様の条件で培養した。培養2日後(EPCが培養皿に付着した後)、IP拮抗薬(CAY10441)を含む新しい培養液に交換し、3〜4日後に細胞のAcetyl-LDL-DiIの貧食能およびLectin-FITCの結合能を評価することにより機能性EPCを同定した。その結果、IP拮抗薬の濃度に依存して、機能性EPCの増殖が抑えられた(図4)。
【0018】
以上の結果から、(1)EPCの分化・増殖にIPの関与すること、(2)癌細胞の増殖に機能的EPCが深く関与していること、さらに、(3)EPCの機能はIP拮抗薬により抑制されることが明らかとなり、IP拮抗薬が癌(腫瘍)の形成及び増殖を抑える作用を持つ可能性が示唆された。
【図面の簡単な説明】
【0019】
【図1】野生型(WT)又はIP欠損型(IP−/−)マウス由来のEPCの内皮細胞分化能を比較した結果を示す図である。
【図2】IP欠損EPCによる皮膚移植癌細胞増殖抑制効果を示す図である。
【図3】骨髄移植4週後の末梢血におけるEPC数と機能性EPC数を示す図である。
【図4】EPC機能に及ぼすIP拮抗剤の効果を示す図である。
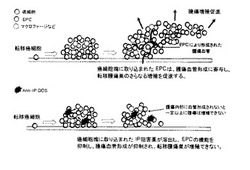
【図5】DDSによるIP抑制剤・拮抗剤の有用性を示す図である。
【図6】DDS運搬体である抗体を結合させたターゲットリポソームと、癌細胞に特異的なモノクローナル抗体を示す図である。
【技術分野】
【0001】
本発明は、プロスタサイクリン受容体(IP)の拮抗剤を有効成分とする癌治療用組成物に関する。
【背景技術】
【0002】
近年、新しい癌治療戦略の一つとして血管新生制御による治療が注目されている。癌の増殖には、栄養供給路として腫瘍血管新生が必須であり、特に固形癌では、組織の直径1〜2mm以上に増殖するためには、既存血管から新生血管が延びて癌組織まで到達することが不可欠であることが知られている(非特許文献1)。また、癌組織が発達する際には、マクロファージ、繊維芽細胞、そして骨髄由来性血管内皮前駆細胞(EPC)を取り込みながら増殖していくことが明らかにされており、癌細胞の増殖や浸潤には様々な細胞が関与していると考えられている。なかでも、EPCは転移癌の初期の血管新生に非常に重要であることが示唆されているが(非特許文献2)、その役割の詳細については、いまだ不明な点が多く残されている。
【0003】
血管新生制御による癌治療法としては、既にVEGF/VEGFRファミリーに対する抗体療法や、チロシンリン酸化阻害薬を用いた治療法が開発されている(例えば、特許文献1)。しかし、腫瘍ごとに血管新生の際に依存する増殖因子の種類、程度が異なり、期待されるような治療効果がないのが現状である。また、癌増殖時に取り込まれる細胞群の多彩性も、血管増殖因子シグナルを標的とする治療効果を困難にしている。このため、癌種に依存せず普遍的な治療効果が期待できる、血管新生制御による癌治療法及び治療剤の開発が急がれている。
【0004】
最近、本願発明者らはEPCから産生されるプロスタサイクリン(PGI2としても知られる)が、細胞膜上の特異的プロスタサイクリン受容体(IP)を介して、EPCにオートクラインに作用し、EPCの増殖及び分化に深く関与することを明らかにした(特許文献2)。プロスタサイクリンは、生体内において主として血管内皮で産生される局所ホルモンであり、血管拡張作用、血圧降下作用、血小板凝集抑制作用等の生理活性を有している。そのため、プロスタサイクリンやそのアナログは、閉塞性動脈硬化、肺高血圧症、虚血性心疾患、糖尿病性大血管障害、糖尿病性腎症、糖尿病性網膜症等の治療に利用されている(例えば、特許文献3)。また、現在までにIPの拮抗剤(アンタゴニスト)として様々な物質が報告されており、抗炎症剤及び鎮痛剤として有用であることが知られているほか(例えば、特許文献4〜10)、心血管性疾患や(例えば、特許文献11)、神経障害性疾患の緩解に(特許文献12)、及び神経変性疾患の治療に(特許文献13)有用であることが示唆されている。しかし、癌増殖に及ぼすIP拮抗剤の影響については明らかにされておらず、IP拮抗剤が癌治療に有用である可能性は全く示唆されていなかった。
【0005】
【特許文献1】特開2007−045835号公報
【特許文献2】特願2007−281161号明細書
【特許文献3】特表2007−519604号公報
【特許文献4】特表2006−525254号公報
【特許文献5】国際公開第02/40453号パンフレット
【特許文献6】国際公開第02/070514号パンフレット
【特許文献7】国際公開第02/070500号パンフレット
【特許文献8】国際公開第01/68591号パンフレット
【特許文献9】欧州特許第0902018号明細書
【特許文献10】米国特許第6,184,242号明細書
【特許文献11】国際公開第79/00744号パンフレット
【特許文献12】国際公開第01/10433号パンフレット
【特許文献13】国際公開第01/10455号パンフレット
【非特許文献1】J. Folkman, J.Natl. Cancer Inst., 82: 4 (1990)
【非特許文献2】D. Gao et al., Science 319: 195-198 (2008)
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明の課題は、癌増殖におけるEPCの関与について明らかにするとともに、EPCの機能及び増殖を抑制することにより、癌細胞の増殖を阻止することのできる、新しい癌治療剤を提供することにある。
【課題を解決するための手段】
【0007】
発明者らは、インビボでの実験により、IP欠損した骨髄細胞を移植したマウスでは、骨髄および末梢血中のEPCの機能が低下すること、また、同移植マウスにおいて、癌細胞増殖は正常骨髄細胞を移植したマウスと比較して、著しく抑えられること、さらに、単離した正常EPCの投与により、癌増殖性が回復することを見い出し、機能的EPCが癌増殖に不可欠であることを明らかにした。また、EPCの機能及び増殖がIP拮抗剤により抑制されることを見い出し、本発明を完成するに至った。
【0008】
すなわち本発明は、(1)有効成分として1又は2以上のプロスタサイクリン受容体(IP)の拮抗剤を含むことを特徴とする癌治療用組成物や、(2)ドラッグデリバリーシステム(DDS)により、標的の癌細胞塊に特異的に取り込まれることを特徴とする上記(1)に記載の癌治療用組成物や、(3)DDS運搬体として、リポソームを用いることを特徴とする上記(2)に記載の癌治療用組成物や、(4)リポソームが、癌細胞を特異的に認識する抗体を結合させたターゲットリポソームであることを特徴とする上記(3)に記載の癌治療用組成物や、(5)IPの拮抗剤が、CAY10441であることを特徴とする上記(1)〜(4)いずれか記載の癌治療用組成物に関する。
【発明の効果】
【0009】
本発明のIP拮抗剤を含む癌治療用組成物は、癌組織における異常な血管新生を抑制することにより癌の増殖を抑えることができ、各種の癌に対して抗癌剤として使用することができる。
【発明を実施するための最良の形態】
【0010】
本発明のプロスタサイクリン受容体(IP)の拮抗剤としては、IPを介したプロスタサイクリンのシグナル伝達を阻害又は低下させる物質であれば特に制限されるものではなく、IPへのプロスタサイクリンの結合を阻害又は低下させる物質であっても、IPとプロスタサイクリンとの相互作用や、IPと関連するGタンパク質との相互作用に影響を及ぼすことにより、IP−プロスタサイクリン媒介性の細胞内シグナル伝達経路を阻害又は低下させる物質あってもよく、例えば、4,5−ジハイドロ−1H−イミダゾル−2−yl−4(4−イソプロポキシベンジル)フェニルアミン(4,5-dihydro-1H-imidazol-2-yl-4 (4-isopropoxybenzyl) phenylamine)や、欧州特許出願公開第09020l8号明細書に記載の2−(アリルフェニル)アミノ−イミダゾリン誘導体や、米国特許第6,184,242号明細書に記載の2−(置換されたフェニル)アミノ−イミダゾリン誘導体や、国際公開第02/070514号パンフレットに記載のアルコキシカルボニルアミノ・ヘテロアリール・カルボン酸誘導体や、国際公開第02/070500号パンフレットに記載のアルコキシカルボニルアミノ安息香酸またはアルコキシカルボニルアミノ・テトラゾリル・フェニル誘導体や、国際公開第02/40453号パンフレットに記載の2−フェニルアミノイミダゾリン・フェニルケトン誘導体や、国際公開第01/68591号パンフレットに記載のカルボン酸誘導体や、国際公開第01/10433号パンフレットに記載のアミノ−又はアミド−プロスタサイクリン誘導体合成物や、国際公開第01/10445号パンフレットに記載の15(R)イソカルバサイクリン又は15−デオキシイソカルバサイクリン誘導体や、国際公開第79/00744号パンフレットに記載の6,9-チアプロスタサイクリン類似体または誘導体;(5Z)-カルバサイクリン;FCE22176((5Z)-13,14−ジデヒドロ-20-メチル-カルボプロスタサイクリン)等を挙げることができ、なかでも、4,5−ジハイドロ−1H−イミダゾル−2−yl−4(4−イソプロポキシベンジル)フェニルアミン(4,5-dihydro-1H-imidazol-2-yl-4 (4-isopropoxybenzyl) phenylamine;CAY10441、Cayman Chemical社製)を好適に例示することができる。
【0011】
本発明の癌治療用が有効な癌としては、機能的EPCの存在が癌細胞増殖や癌組織形成に関与する癌であれば特に制限されず、例えば、肺癌、卵巣癌、膵臓癌、胃癌、胆嚢癌、腎臓癌、前立腺癌、乳癌、食道癌、肝臓癌、口腔癌、結腸癌、大腸癌、直腸癌、子宮癌、胆管癌、膵島細胞癌、副腎皮質癌、膀胱癌、精巣癌、睾丸腫瘍、甲状腺癌 、皮膚癌 、悪性カルチノイド腫瘍、メラノーマ、グリオーマ、骨肉腫、骨髄腫、軟部組織肉腫、神経芽細胞腫、悪性リンパ腫や白血病等の造血器腫瘍が挙げられるが、なかでも、肺癌を好適に例示することができる。
【0012】
本発明の癌治療用組成物は経口的又は非経口的に投与することができる。すなわち通常用いられる投与形態、例えば、粉末、顆粒、カプセル剤、シロップ剤、懸濁液等の剤型で経口的に投与することも、例えば、溶液、乳剤、懸濁液等の剤型にしたものを注射又はスプレーの型で非経口投与することもできるが、好ましい投与形態として、ドラッグデリバリーシステム(DDS)により標的の癌細胞塊に特異的に取り込まれるような投与形態を挙げることができ、特に好ましい投与形態として、ターゲティング(標的指向)DDSによる投与形態を挙げることができる。ここでドラッグデリバリーシステム(DDS)とは、癌細胞や標的組織等を狙い撃ちする薬物や遺伝子送達システムを意味するものであり、その中でも特にターゲティング(標的指向)DDSとは、薬物を「体内の必要な部位に」、「必要な量を」、「必要な時間だけ」送り込むといった概念である。ターゲティングDDSの代表的な運搬体として微粒子性キャリアーであるリポソームが挙げられる。この粒子に標的指向機能をもたせるために、リポソームの脂質の種類、組成比、粒子径、表面電荷を変化させるなどの受動的ターゲティング法があり、また、さらに高機能の能動的ターゲティング法として、リポソーム膜面上にリガンドを結合させ、標的組織の細胞膜面上に存在するレセプターに特異的に認識させることによって、積極的にターゲティングを可能にさせる方法が開発されている。この能動的ターゲティング法での標的となる細胞膜面上に存在するレセプターのリガンドとしては、抗原、抗体、ペプチド、糖脂質や糖蛋白質などを例示することができる。本発明の癌治療用組成物の投与に際しては、例えば、癌細胞を特異的に認識する抗体を結合させたターゲットリポソームを運搬体として用いることができ、上記癌細胞を特異的に認識する抗体としては、例えば、メラノーマ特異的モノクローナル抗体であるR24や、卵巣癌特異的モノクローナル抗体であるOvaRexや、大腸癌特異的モノクローナル抗体であるPanorexや、肺癌特異的モノクローナル抗体であるBEC2や、乳癌特異的モノクローナル抗体であるHerceptinや、急性骨髄性白血病(AML)特異的モノクローナル抗体であるSmartM195や、非ホジキンリンパ種(NHL)特異的モノクローナル抗体であるRituxanを好例として挙げることができる。
【0013】
以下、実施例により本発明をより具体的に説明するが、本発明の技術的範囲はこれらの例示に限定されるものではない。
【実施例1】
【0014】
[内皮前駆細胞(EPC)の単離]
野生型(WT)又はIP欠損型(IP−/−)マウスから骨髄を採取し、Histopaque 1083(登録商標)(Sigma社製)を用いて濃度勾配遠心分離を行い単核細胞を得た。次に、magnetic sorting system(Lineage deletion kit及びMulti-sorting system; Miltenyi Biotec社製)を用いて、骨髄単核細胞からlineage陰性(Lin-)、且つcKit/Sca1陽性(cKit+/Sca1+)の細胞を単離した。得られたLin-/cKit+/Sca1+細胞をEPCとして以後の実験で用いた。
【実施例2】
【0015】
[EPCの増殖・分化に及ぼすIPの影響]
実施例1で得られたEPCを、フィブロネクチンでコートしたプレートに播種し、α−MEM(GIBCO社製;#12571-063)培地[10質量%ウシ胎児血清、100μg/ml内皮細胞成長因子 E2759(Sigma社製)、100ng/mlマウス組換えVEGF(Sigma社製)、10U/mlヘパリン硫酸塩(Sigma社製)、100U/mlペニシリン、100μg/mlストレプトマイシン]を用い、5%CO2存在下、37℃で7日間培養した。培養細胞のコロニー形成能を、DiI-acLDL 及びFITC-lectinを用いた染色法により評価した結果、IP欠損EPCでは著明に低下していることが明らかとなった(図1a及び図1b)。また、長期間(2週間)培養後のそれぞれの細胞を、成熟内皮細胞マーカーであるvWFにより染色した結果、IP欠損EPCでは分化能が有意に低いことが示された(図1c及び図1d)。以上の結果から、IPがEPCの増殖及び分化に関与する可能性が示唆された。
【実施例3】
【0016】
[移植癌細胞の増殖に及ぼすEPCの影響]
致死的照射されたヌードマウス(ICRnu/nu)に、野生型(WT)又はIP欠損型(IP−/−)マウスから採取した骨髄細胞を移植した。4週間後に骨髄が生着したことを確認し、WT由来骨髄を移植されたマウス(BMT(WT))とIP−/−由来骨髄を移植されたマウス(BMT(IP))の背部皮下に、ヒト肺小細胞癌細胞SBC−1とMS−1−Lを接種した。癌細胞の移植後3週間にわたって、経時的な腫瘍体積の変化、血中EPC数、及び機能性EPC数の検討を行った。BMT(IP)群における移植腫瘍の体積は、BMT(WT)群と比較して有意に小さかった(図2)。また、移植3週間後のEPCの末梢血中数(%)は両群に差はなかったが、BMT(IP)群では機能性EPCの数が有意に低下していた(図3)。さらに、BMT(IP)マウスに、癌細胞移植と同時に、単離した正常EPCを補充した場合(BMT(IP)+EPC(WT))、癌細胞増殖能が回復することが明らかとなった(図2)。以上の結果は、腫瘍の形成及び増殖において、EPCが重要な役割を果たしており、IPの欠損によるEPC機能の抑制により、腫瘍の増殖が抑えられる可能性が示された。
【実施例4】
【0017】
[IP抑制薬剤によるEPC機能抑制作用]
単離したEPC(WT)を、実施例2と同様の条件で培養した。培養2日後(EPCが培養皿に付着した後)、IP拮抗薬(CAY10441)を含む新しい培養液に交換し、3〜4日後に細胞のAcetyl-LDL-DiIの貧食能およびLectin-FITCの結合能を評価することにより機能性EPCを同定した。その結果、IP拮抗薬の濃度に依存して、機能性EPCの増殖が抑えられた(図4)。
【0018】
以上の結果から、(1)EPCの分化・増殖にIPの関与すること、(2)癌細胞の増殖に機能的EPCが深く関与していること、さらに、(3)EPCの機能はIP拮抗薬により抑制されることが明らかとなり、IP拮抗薬が癌(腫瘍)の形成及び増殖を抑える作用を持つ可能性が示唆された。
【図面の簡単な説明】
【0019】
【図1】野生型(WT)又はIP欠損型(IP−/−)マウス由来のEPCの内皮細胞分化能を比較した結果を示す図である。
【図2】IP欠損EPCによる皮膚移植癌細胞増殖抑制効果を示す図である。
【図3】骨髄移植4週後の末梢血におけるEPC数と機能性EPC数を示す図である。
【図4】EPC機能に及ぼすIP拮抗剤の効果を示す図である。
【図5】DDSによるIP抑制剤・拮抗剤の有用性を示す図である。
【図6】DDS運搬体である抗体を結合させたターゲットリポソームと、癌細胞に特異的なモノクローナル抗体を示す図である。
【特許請求の範囲】
【請求項1】
有効成分として1又は2以上のプロスタサイクリン受容体(IP)の拮抗剤を含むことを特徴とする癌治療用組成物。
【請求項2】
ドラッグデリバリーシステム(DDS)により、標的の癌細胞塊に特異的に取り込まれることを特徴とする請求項1に記載の癌治療用組成物。
【請求項3】
DDS運搬体として、リポソームを用いることを特徴とする請求項2に記載の癌治療用組成物。
【請求項4】
リポソームが、癌細胞を特異的に認識する抗体を結合させたターゲットリポソームであることを特徴とする請求項3に記載の癌治療用組成物。
【請求項5】
IPの拮抗剤が、CAY10441であることを特徴とする請求項1〜4いずれか記載の癌治療用組成物。
【請求項1】
有効成分として1又は2以上のプロスタサイクリン受容体(IP)の拮抗剤を含むことを特徴とする癌治療用組成物。
【請求項2】
ドラッグデリバリーシステム(DDS)により、標的の癌細胞塊に特異的に取り込まれることを特徴とする請求項1に記載の癌治療用組成物。
【請求項3】
DDS運搬体として、リポソームを用いることを特徴とする請求項2に記載の癌治療用組成物。
【請求項4】
リポソームが、癌細胞を特異的に認識する抗体を結合させたターゲットリポソームであることを特徴とする請求項3に記載の癌治療用組成物。
【請求項5】
IPの拮抗剤が、CAY10441であることを特徴とする請求項1〜4いずれか記載の癌治療用組成物。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2011−102242(P2011−102242A)
【公開日】平成23年5月26日(2011.5.26)
【国際特許分類】
【出願番号】特願2008−57250(P2008−57250)
【出願日】平成20年3月7日(2008.3.7)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 2007年10月15日日本肺癌学会発行 肺癌:第48回日本肺癌学会総会号(Vol.47 No.5)
【出願人】(505210115)国立大学法人旭川医科大学 (17)
【Fターム(参考)】
【公開日】平成23年5月26日(2011.5.26)
【国際特許分類】
【出願日】平成20年3月7日(2008.3.7)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 2007年10月15日日本肺癌学会発行 肺癌:第48回日本肺癌学会総会号(Vol.47 No.5)
【出願人】(505210115)国立大学法人旭川医科大学 (17)
【Fターム(参考)】
[ Back to top ]

