プロトン導電体及びその製造方法
【課題】高い導電率を示し、排ガス中の炭素含有成分を低温で十分に浄化することができるリン酸スズ系化合物からなるプロトン導電体及びその製造方法を提供すること。
【解決手段】純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体及びその製造方法である。プロトン導電体1は、これを導電性金属材2と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒3として用いられる。その製造にあたっては、水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてなるイオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得た後、沈殿物を焼成する。また、水溶性スズ塩の水溶液を中和して得られた中和物を解膠させ、リン酸を加えてゲル化させたゲルを乾燥して粉砕した後、粉砕粉を焼成しても得ることができる。
【解決手段】純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体及びその製造方法である。プロトン導電体1は、これを導電性金属材2と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒3として用いられる。その製造にあたっては、水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてなるイオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得た後、沈殿物を焼成する。また、水溶性スズ塩の水溶液を中和して得られた中和物を解膠させ、リン酸を加えてゲル化させたゲルを乾燥して粉砕した後、粉砕粉を焼成しても得ることができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、排ガスを浄化するために用いられる、リン酸スズ系化合物の粉末からなるプロトン導電体に関する。
【背景技術】
【0002】
従来から、自動車エンジンなどの内燃機関から排出される排ガス中に含まれるHC、CO、NOx等を浄化するために、排気管内には排ガス浄化用触媒体が設けられている。この排ガス浄化用触媒体としては、例えば多数のセルを有するハニカム構造のセラミック担体に触媒成分を担持させたものが用いられている。触媒成分としては、白金、パラジウム、及びロジウム等の貴金属成分をセリア/ジルコニア複合酸化物やアルミナ上に分散させた三元触媒が用いられている。
【0003】
貴金属等からなる上記三元触媒においては、理論空燃比に制御された排ガスの浄化は可能であるが、酸素過剰雰囲気にある例えばリーンバーンエンジンの排ガスの浄化性能が不十分であるという問題があった。また、例えば400℃を超える高温雰囲気でなければ、排ガスを十分に浄化できないという問題があった。
【0004】
そこで、リン酸スズ等のリン酸塩からなる触媒成分を含む排気ガス浄化用触媒が開発されている(特許文献1参照)。かかる排気ガス浄化用触媒を用いることにより、理論空燃比よりも高い空燃比で運転するリーンバーンエンジン等から排出される、酸素含有率が高い排ガスの浄化が可能になる。また、400℃以下の低温でも排ガスの浄化が可能になる。
また、リン酸化合物等からなるプロトン導電体を排気ガスの浄化に用いる技術が開発されている(特許文献2参照)。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2000−42415号公報
【特許文献2】特開2009−233618号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、リン酸スズ系化合物は、製造時に酸化スズ等の不純物を含みやすく、例えば95質量%以上という高純度のリン酸スズ系化合物を得ることは困難であった。そのため、リン酸スズ系化合物が本来有する優れた排ガスの浄化性能を十分に発揮させることができないという問題があった。特に、上記特許文献2に示すようにリン酸スズ系化合物をプロトン導電体として用いた排ガス浄化触媒を構成する場合には、リン酸スズ系化合物の純度が不十分であることに起因して導電率が不十分になり、低温での排ガスの浄化性能が不十分になるという問題があった。
【0007】
本発明はかかる問題点に鑑みてなされたものであって、高い導電率を示し、排ガス中の炭素含有成分を低温で十分に浄化することができるリン酸スズ系化合物からなるプロトン導電体及びその製造方法を提供しようとするものである。
【課題を解決するための手段】
【0008】
第1の発明は、導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
スズの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得る沈殿工程と、
上記沈殿物を焼成して上記プロトン導電体を得る焼成工程とを有することを特徴とするプロトン導電体の製造方法にある(請求項1)。
【0009】
第2の発明は、導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
水溶性スズ塩を水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液を中和して中和物を得る中和工程と、
上記中和物を解膠させることによりゾルを得るゾル化工程と、
上記ゾルとリン酸を混合してゲル化させてゲルを得るゲル化工程と、
上記ゲルを乾燥させ粉砕することにより粉砕粉を得る乾燥粉砕工程と、
上記粉砕粉を焼成する焼成工程とを有することを特徴とするプロトン導電体の製造方法にある(請求項4)。
【0010】
第3の発明は、導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、
純度95質量%以上のリン酸スズ系化合物の粉末からなることを特徴とするプロトン導電体にある(請求項6)。
【発明の効果】
【0011】
上記第1の発明の製造方法においては、上記イオン化工程と上記沈殿工程と上記焼成工程とを行うことにより、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体を製造する。
上記イオン化工程においては、上記特定の水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させる。これにより、液相の上記イオン水溶液中にスズイオンとリン酸イオンとを均一に分散させて溶解させることができる。そして、上記沈殿工程においては、上記イオン水溶液にスズイオンを還元する還元剤を添加する。これにより、SnとPとを含有する上記沈殿物を得ることができる。
次に、上記焼成工程においては、上記沈殿物を焼成する。これにより、上記沈殿物が酸化され、リン酸スズ系化合物の粉末からなる上記プロトン導電体を得ることができる。
【0012】
上記製造方法においては、上記イオン工程及び上記沈殿工程において、液相の上記イオン水溶液から、SnとPとを含むリン酸スズ系化合物の前駆体物質からなる上記沈殿物を沈殿させ、該沈殿物を上記焼成工程において焼成させている。そのため、不純物がほとんど残存又は生成せず、純度95質量%以上という従来にない高純度のリン酸スズ系化合物の粉末からなるプロトン導電体を製造することができる。かかる高純度のリン酸スズ系化合物の粉末からなるプロトン導電体は、上記第1の発明の製造方法により初めて製造可能となる。そして、上記プロトン導電体は、低温でも高い導電率を示し、上記プロトン導電体を導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。このとき、例えば400℃以下という低温でも排ガスを十分に浄化できるという優れた浄化性能を示すことができる。
【0013】
次に、上記第2の発明の製造方法においては、上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程と上記乾燥粉砕工程と上記焼成工程とを行うことにより、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体を製造する。
上記イオン化工程においては、上記水溶性スズ塩を水に溶解させてイオン水溶液を作製する。これにより、液相の上記イオン水溶液中にスズイオンを均一に分散させて溶解させることができる。そして、上記中和工程においては、上記イオン水溶液を中和させる。これにより、Snを含有する上記中和物を得ることができる。
【0014】
次に、上記ゾル化工程においては、上記中和物を解膠させる。これにより、Snが均一に分散したゾルを得ることができる。
次いで、上記ゲル化工程においては、上記ゾルとリン酸とを混合する。これにより、SnとPが均一に分散したゲルを得ることができる。
次に、上記乾燥粉砕工程においては、上記ゲルを乾燥させ粉砕する。これによりSnとPが均一に分散した粉砕粉を得る。そして、上記焼成工程においては、上記粉砕粉を焼成する。これにより、該粉砕粉が酸化され、リン酸スズ系化合物の粉末からなる上記プロトン導電体を得ることができる。
【0015】
上記製造方法においては、上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程とを行い、リン酸スズ系化合物の前駆体物質からなるゲルを生成させている。そして、上記乾燥粉砕工程において、乾燥及び粉砕させ、上記焼成工程において上記粉砕粉を焼成する。これにより、不純物がほとんど残存又は生成せず、純度95質量%以上という従来にない高純度のリン酸スズ系化合物の粉末からなるプロトン導電体を製造することができる。かかる高純度のリン酸スズ系化合物の粉末からなるプロトン導電体は、上記第2の発明の製造方法により初めて製造可能となる。該プロトン導電体は、低温でも高い導電率を示し、上記プロトン導電体を導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。このとき、例えば400℃以下という低温でも排ガスを十分に浄化できるという優れた浄化性能を示すことができる。
【0016】
第3の発明のプロトン導電体は、純度95質量%以上のリン酸スズ系化合物の粉末からなる。このような高純度のリン酸スズ系化合物粉末からなる上記プロトン導電体は、従来その製造方法が開発されていなかった。上記第1及び上記第2の発明により、その製造が可能になる。
かかる高純度のリン酸スズ系化合物粉末からなる上記プロトン導電体は、高い導電率を示し、上記プロトン導電体を導電性金属材に接触させて用いることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。このとき、排ガス中の炭素含有成分を例えば400℃以下の低温で十分に浄化することができる。
【図面の簡単な説明】
【0017】
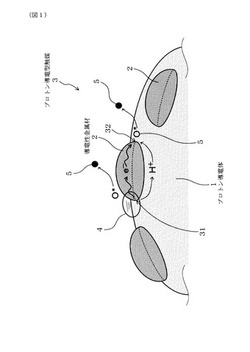
【図1】実施例1における、プロトン導電型触媒の構成を示す説明図。
【図2】実施例2における、リン酸スズ系化合物におけるxの値と、導電率との関係を示す説明図。
【図3】実施例3における、プロトン導電体の粉末の比表面積と、HC浄化性能との関係を示す説明図。
【発明を実施するための形態】
【0018】
次に、本発明の好ましい実施形態について説明する。
上記プロトン導電体は、該プロトン導電体を導電性金属材と接触させることにより、炭素含有成分及び水等を含有する排ガス中から炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。
上記導電性金属材としては、例えば、Pt、Ag、Cu、Fe、Cr、Ir、Ni、Co、Au、W、Mo、Pd、Rh、及びその合金材料等を用いることができる。
【0019】
以下、プロトン導電体と導電性金属材とを接触させたプロトン導電型触媒について説明する。
上記プロトン導電型触媒において、上記プロトン導電体と接触する上記導電性金属材は、互いに接触するアノード電極部とカソード電極部とを有する。上記プロトン導電型触媒は、上記アノード電極部によって、該アノード電極部と上記プロトン導電体との境界部分に接触したH2Oからプロトン(H+)を分離し、上記プロトン導電体に取り込む反応を促進すると共に、上記カソード電極部によって、該カソード電極部と上記プロトン導電体との境界部分において、該プロトン導電体から供給されるプロトンによる還元反応を促進するよう構成される。
【0020】
上記プロトン導電型触媒は、上記アノード電極部によって、該アノード電極部と上記プロトン導電体との境界部分に接触した排ガス中のH2Oからプロトン(H+)を分離し、上記プロトン導電体に取り込む反応が促進される。上記アノード電極部は、アノード反応を進行する電極材であり、高純度のリン酸スズ系化合物からなる上記プロトン導電体は、プロトンを通す性質を有すると共に、400℃以下という比較的低温において高い導電率を有する。
そのため、排ガス中のH2Oが上記アノード電極部と上記プロトン導電体との境界部分に接触すると、プロトン導電体、アノード電極、H2Oの三相界面(酸化サイト)において、例えば、H2O→H++OH-、H2O→2H++O2-等の反応が起きる。そのため、アノード電極部において、活性酸素種(例えばO2-、OH-、O2-、O22-等)が発生する。また、プロトン導電体は、発生したプロトンを自発的に取り込む。
【0021】
そして、アノード反応により発生した上記活性酸素種は、高い酸化能を有しているため、発生後すぐに、排ガス中の炭素含有成分を酸化する反応を起こす。例えば、CをCO又はCO2に、COをCO2に、CH4をCH3OH、CO2、CO等に、HCをCO2等に酸化が可能である。つまり、上記酸化サイトでは、アノード反応(2H2O+C→CO2+4H++4e-、2xH2O+CxHy→CxO2x+(4x+y)H++4xe-等)が起きていることとなる。
【0022】
炭素含有成分を酸化した際に発生した電子は、接触したアノード電極部及びカソード電極部中を自由に動き回る。
また、上記プロトン導電体は、高い導電率を有するため、上記アノード電極部と上記プロトン導電体との境界部分に接触したH2Oから分離されたプロトンを自発的に取り込む。そして、取り込まれたプロトンは、プロトン導電体中を自由に動きまわる。
【0023】
そして、上記カソード電極部によって、上記カソード電極部と上記プロトン導電体との境界部分において、上記プロトン導電体から供給されるプロトンによる還元反応が促進される。
上記カソード電極部は、カソード反応を進行する電極材であり、上記プロトン導電体は、上述したように、酸化サイトにおける反応で取り込んだプロトンが存在した状態となっている。
そのため、プロトン導電体、カソード電極、反応ガス(NO、NO2、O2等)の三相界面(還元サイト)ではプロトンによる反応ガスの還元反応(カソード反応)が起きる。具体的には、カソード極近傍にNO、NO2、O2が存在すれば、H2Oに還元することが出来る(2NO+4H++4e-→N2+2H2O、1/2O2+2H++2e-→H2O等)。また、カソード極近傍にH2OやO2があれば、H2O2及び活性酸素種(例えば・O2H、H3O+)を生成する(O2+2H++2e-→H2O2等)。そして、この活性酸素種は、上記と同様に、発生後すぐに排ガス中の炭素含有成分を酸化する反応を起こす。
【0024】
このように、上記プロトン導電型触媒は、排ガス中のH2Oを反応剤として用い、アノード極、カソード極の両極で活性酸素種を生成することができる。そして、両極より発生した活性酸素種が排ガス中の炭素含有成分の酸化を可能にするため、高い酸化性能で酸化を行うことができる。また、酸化性能が高いため、温度400℃以下という比較的低温でも、活性酸素種の発生、及び炭素含有成分の酸化が自発的に起こる。また、炭素含有成分の酸化だけでなく、NO、NO2等の還元も行うことができる。
【0025】
上記プロトン導電型触媒は、上記プロトン導電体と上記導電性金属材とが接触した状態で構成されていれば良く、例えば、粒状のプロトン導電体と粒状の導電性金属材とを混合して接触させた状態等がある。
【0026】
上記プロトン導電型触媒の製造方法としては、例えば、プロトン導電体とアノード反応及びカソード反応を進行する各種導電性金属材とを、乳鉢等で物理混合することにより得る方法がある。
また、溶液法にてアノード電極部及びカソード電極部を構成する材料をプロトン導電体に担持し混合する方法等により作製してもよい。
【0027】
上記アノード電極部と上記カソード電極部とは、異なる材料を用いてもよいし、同一の材料を用いてもよい。
上記アノード電極部と上記カソード電極部が異なる材料である場合には、アノード電極部とカソード電極部とを混合したものを導電性金属材とすればよい。
【0028】
上記アノード電極部と上記カソード電極部とが同一材料である場合には、上記アノード電極部及び上記カソード電極部を区別することなく、導電性金属材として1種の材料を用意すればよい。この場合には、導電性金属材において、プロトン導電体、H2Oとの三相界面を形成する部分が酸化サイトとなり上記アノード反応を促進する。一方、電極材料において、プロトン導電体、反応ガスとの三相界面を形成する部分が還元サイトとなって、上記カソード反応を促進する。
【0029】
上記プロトン導電型触媒は、これをコージェライト、SiC等からなるハニカム構造体に担持させて用いることができる。また、上記プロトン導電型触媒自体をハニカム状に成形して用いることもできる。
【0030】
次に、上記プロトン導電体は、純度95質量%以上のリン酸スズ系化合物の粉末からなる。
純度が95質量%未満の場合には、導電率が低くなり、低温での排ガスの浄化性能が不十分になるおそれがある。純度の測定は、X線回折(XRD)で結晶相を確認し、エネルギー分散型X線分光分析(EDX)により、P及びSの量を定量して算出することができる。
【0031】
上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなることが好ましい(請求項7)。
この場合には、上記リン酸スズ系化合物の導電率をより向上させることができる。
特に、MがAlの場合には、0.02≦x≦0.15がより好ましく、0.03≦x≦0.1がさらに好ましい。
また、MがInの場合には、0.04≦x≦0.15がより好ましく、0.05≦x≦0.13がよい。
【0032】
また、上記リン酸スズ系化合物の粉末の比表面積は10m2/g以上であることが好ましい(請求項8)。
この場合には、排ガス中の炭素含有成分に対する浄化性能をより向上させることができる。また、比表面積を大きくしすぎても上述の浄化性能の向上効果はほとんど得られなくなり、また大きな比表面積の粉末を得るための操作が煩雑になるという観点からは、上記リン酸スズ系化合物の粉末の比表面積は100m2/g以下が好ましく、50m2/g以下がより好ましい。
【0033】
上記プロトン導電体は、上記第1の発明のように、イオン化工程と沈殿工程と焼成工程とを行うことにより製造することができる。
上記第1の発明の上記イオン化工程においては、水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてイオン水溶液を作製する。
【0034】
上記第1の発明において、上記水溶性スズ塩としては、スズの硫酸塩(硫酸スズ)、硝酸塩(硝酸スズ)、塩化物塩(塩化スズ)、臭化物塩(臭化スズ)、及びヨウ化物塩(ヨウ化スズ)から選ばれる少なくとも1種を用いることができる。
また、上記水溶性リン酸塩としては、例えばリン酸アンモニウム、リン酸ナトリウム(リン酸ソーダ)等を用いることができる。
【0035】
上記沈殿工程においては、上記イオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得る。
上記還元剤としては、例えばアンモニア、尿素、アミン、及びヒドラジン等を用いることができる。
【0036】
また、上記第1の発明の上記焼成工程においては、上記沈殿物を焼成して上記プロトン導電体を得る。
上記沈殿物の焼成は、例えば温度650〜900℃で行うことができる。
【0037】
次に、上記第1の発明においては、上記沈殿工程と上記焼成工程との間に、上記沈殿物を水で洗浄する洗浄工程を行うことが好ましい(請求項3)。
この場合には、上記焼成工程後に得られる上記リン酸スズ系化合物の純度をより向上させることができる。
【0038】
また、上記第1の発明においては、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩及び上記水溶性リン酸塩の他に、アルミニウムの硫酸塩(硫酸アルミニウム)、硝酸塩(硝酸アルミニウム)、塩化物塩(塩化アルミニウム)、臭化物塩(臭化アルミニウム)、及びヨウ化物塩(ヨウ化アルミニウム)から選ばれる少なくとも1種の水溶性アルミニウム塩、又はインジウムの硫酸塩(硫酸インジウム)、硝酸塩(硝酸インジウム)、塩化物塩(塩化インジウム)、臭化物塩(臭化インジウム)、及びヨウ化物塩(ヨウ化インジウム)から選ばれる少なくとも1種の水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製し、上記沈殿工程においては、上記イオン水溶液中のSnイオンとAlイオン又はInイオンとを還元する上記還元剤を添加することが好ましい(請求項2)。
【0039】
この場合には、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)で表されるリン酸スズ系化合物からなる上記プロトン導電体を製造することができる。該プロトン導電体は、上述のごとく、低温でより優れた導電率を示すことができる。
SnイオンとAlイオン又はInイオンとを還元する上記還元剤としては、アンモニア、尿素などの上述の還元剤と同様のものを用いることができる。
【0040】
また、上記プロトン導電体は、上記第2の発明に示すごとく、イオン化工程と中和工程とゾル化工程とゲル化工程と乾燥粉砕工程と焼成工程とを行うことにより製造することができる。
上記第2の発明の上記イオン化工程においては、水溶性スズ塩を水に溶解させてイオン水溶液を作製する。
上記第2の発明においては、上記水溶性スズ塩として、例えばスズの水酸化物塩(水酸化スズ)、硫酸塩(硫酸スズ)、硝酸塩(硝酸スズ)、塩化物塩(塩化スズ)、臭化物塩(臭化スズ)及びヨウ化物塩(ヨウ化スズ)等を用いることができる。
【0041】
また、上記中和工程においては、上記第2の発明の上記イオン水溶液を中和して中和物を得る。具体的には、上記イオン水溶液がアルカリ性(塩基性)の場合には、例えば酢酸、乳酸等の酸を加えて中和させることができる。また、上記イオン水溶液が酸性の場合には、アンモニア、アンモニウム塩等の塩基を加えて中和させることができる。即ち、上記中和工程においては、中和させるイオン水溶液のpHに応じて酸又はアルカリ(塩基)を加えることができる。
【0042】
次に、上記ゾル化工程においては、上記中和物を解膠させることによりゾルを得る。
具体的には、酸や、水溶液が酸性を示す塩の水溶液を添加することにより上記中和物を解膠させることができる。
【0043】
次に、上記ゲル化工程においては、上記ゾルとリン酸とを混合してゲルを得る。また、上記乾燥粉砕工程においては、上記ゲルを乾燥させ粉砕することにより粉砕粉を得る。そして、上記焼成工程においては、上記粉砕粉を焼成する。
上記粉砕粉の焼成は、例えば温度800〜1000℃で行うことができる。
【0044】
また、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩の他に、水溶性アルミニウム塩又は水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製することが好ましい(請求項5)。
この場合には、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)で表されるリン酸スズ系化合物からなる上記プロトン導電体を製造することができる。該プロトン導電体は、上述のごとく低温でより優れた導電率を示すことができる。
【0045】
上記水溶性アルミニウム塩としては、例えばアルミニウムの水酸化物塩(水酸化アルミニウム)、硫酸塩(硫酸アルミニウム)、硝酸塩(硝酸アルミニウム)、塩化物塩(塩化アルミニウム)、臭化物塩(臭化アルミニウム)、及びヨウ化物塩(ヨウ化アルミニウム)等を用いることができる。
また、水溶性インジウム塩としては、例えばインジウムの水酸化物塩(水酸化インジウム)、硫酸塩(硫酸インジウム)、硝酸塩(硝酸インジウム)、塩化物塩(塩化インジウム)、臭化物塩(臭化インジウム)、及びヨウ化物塩(ヨウ化インジウム)等を用いることができる。
【実施例】
【0046】
(実施例1)
本発明の実施例にかかるプロトン導電体について説明する。
図1に示すごとく、本例のプロトン導電体1は、導電性金属材2と接触させることにより、排ガス中の炭素含有成分6を酸化して排ガスを浄化するプロトン導電型触媒3として用いられる。プロトン導電体1は、純度95質量%以上のリン酸スズ系化合物の粉末からなる。本例においては、リン酸スズ系化合物として、リン酸スズ化合物(SnP2O7)のSnの一部がAlで置換されたSn0.95Al0.05P2O7を採用する。
【0047】
本例のプロトン導電体は、次のようにして作製する。
即ち、まず、硫酸スズ(SnSO4)と硫酸アルミニウム(Al2(SO4)3)リン酸ソーダ(Na4P2O7)とを水に溶解させてイオン水溶液を作製した(イオン化工程)。次いで、このイオン水溶液に、Snの還元剤としてアンモニア(NH3)水溶液を添加し、沈殿物を得た(沈殿工程)。なお、各工程において原料の混合は、目的組成のSn0.95Al0.05P2O7が得られる化学量論比で行った。
【0048】
次に、得られた沈殿物を濾過して水で洗浄した後、乾燥させた。その後、大気雰囲気下、温度800℃で1時間焼成した(焼成工程)。このようにしてSn0.95Al0.05P2O7からなるプロトン導電体を得た。これを試料E1とする。
【0049】
また、本例においては、上記試料E1とは異なる方法により、Sn0.95Al0.05P2O7からなるプロトン導電体(試料E2及び試料C1)を作製した。
【0050】
試料E2のプロトン導電体の製造にあたっては、まず、水酸化スズ(Sn(OH)4)と水酸化アルミニウム(Al(OH)3)とを水に溶解させてイオン水溶液を作製した(イオン化工程)。次いで、イオン水溶液に酢酸を加えて中和し、中和物を得た(中和工程)。次に、乳酸を添加することにより中和物を解膠させてゾルを得た(ゾル化工程)。次いで、ゾルにリン酸を添加して混合することにより、ゲル化させてゲルを得た(ゲル化工程)。
各工程において原料の混合は、目的組成のSn0.95Al0.05P2O7が得られる化学量論比で行った。
【0051】
次に、ゲルを乾燥させ粉砕することにより粉砕粉を得た(乾燥粉砕工程)。次いで、粉砕粉を大気雰囲気下、温度900℃で1時間焼成した(焼成工程)。このようにしてSn0.95Al0.05P2O7からなるプロトン導電体を得た。これを試料E2とする。
【0052】
また、試料C1のプロトン導電体の製造にあたっては、まず、SnO2粉末、Al(OH)3粉末とをリン酸水溶液中に混合した。混合は、目的組成のSn0.95Al0.05P2O7が得られる化学量論比で行った。そして、混合液を大気雰囲気下温度200℃で乾燥させて泥漿(スラリー)を得た。次いで、得られた泥漿を大気雰囲気下温度650℃で2時間焼成した。このようにして、Sn0.95Al0.05P2O7を含む粉末からなるプロトン導電体を得た。これを試料C1とする。
【0053】
次に、上記のように作製した3種類のプロトン導電体(試料E1、試料E2、及び試料C1)について、Sn0.95Al0.05P2O7の純度、導電率、炭素含有成分に対する浄化性能の評価を行った。
【0054】
「純度」
純度の測定にあたっては、まずX線回折装置((株)リガク製のRINT2000)により、各試料がSnO2とSnP2O7の結晶相のみからなることを確認した。
次いで、電子顕微鏡(SEM:日本電子(株)製のJSM6700)での5000倍拡大下において、エネルギー分散型X線分光分析(EDX:日本電子(株)製のJED2000)を用いて各粉末試料についてランダムに10点のP量、Sn量を定量し、その平均nを求めた。測定したP量は全てSnP2O7になっており、測定したSnの量からSnP2O7に用いたSnの量を差し引いたSn量は全てSnO2であるとして、SnP2O7の純度を算出した。その結果を表1に示す。
【0055】
「導電率」
粉末状の各試料を厚みL(cm)のペレットに成形し、その両面にPt等からなる面積S(cm2)の導電性金属ペースト又は導電性金属箔を取り付けてセルを作製した。このセルについて、空気中で交流インピーダンス法によりオーミック抵抗Rohomic(Ω)を測定した。そして、導電率σをσ=L/S×Rohomicという式に基づいて算出した。その結果を表1に示す。
【0056】
「浄化性能」
浄化性能の測定にあたっては、まず、各試料のプロトン導電体1を導電性金属材料2に接触させてなるプロトン導電型触媒3を作製する(図1参照)。
具体的には、まず、導電性金属材料(アノード電極部及びカソード電極部)として、Ptを準備した。各試料のプロトン導電体90質量部と導電性金属材料10質量部とを乳鉢などで物理混合し、プロトン導電型触媒を得た。なお、本例においては、アノード電極部及びカソード電極部をいずれもPtで形成したが、異なる導電性金属材料で形成することもできる。また、本例においては、物理混合によりプロトン導電型触媒を作製したが、溶液法にてアノード電極部及びカソード電極部をプロトン導電体に担持させてプロトン導電型触媒を作製することもできる。
次に、プロトン導電型触媒1gを直径φ7.0mmの管状の反応器に充填した。そして、この反応器内に、HC:1000ppm、O2:1質量%、H2O:3質量%、N2:残部(質量%)からなるモデルガスを流速0.6L/minで通過させた。モデルガス通過前後におけるHCの変化量を温度280℃〜温度100℃の範囲内において測定した。HCの量は、ガスクロマトグラフィーにより測定した。そして、HC変化量が50%になるときの温度T50を求めた。その結果を表1に示す。
【0057】
【表1】

【0058】
表1より知られるごとく、試料E1及び試料E2は、95質量%以上という高純度のSn0.95Al0.05P2O7からなるプロトン導電体からなり、導電率に優れ、温度110℃という低温で炭素含有成分(HC)を50%浄化できるという優れた浄化性能を示した。即ち、上記イオン化工程と上記沈殿工程と上記焼成工程、又は上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程と上記乾燥粉砕工程と上記焼成工程とを行うことにより、95質量%以上の高純度のリン酸スズ系化合物からなるプロトン導電体(試料E1及び試料E2)を製造することができ、該プロトン導電体は、優れた導電率を示し、低温で炭素含有成分(HC)に対して優れた浄化性能を示すことができる。
【0059】
これに対し、固体粉末原料を混合して作製した試料C1のプロトン導電体は、Sn0.95Al0.05P2O7の純度が低く、SnO2を多く含有していた。そして、試料C1は、導電率が低く、低温での炭素含有成分(HC)に対する浄化性能が不十分であった。
【0060】
試料E1及び試料E2のプロトン導電体は、このプロトン導電体1を導電性金属材2と接触させることにより、炭素含有成分及び水等を含有する排ガス中から炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒3として用いられる(図1参照)。
図1に示すごとく、プロトン導電型触媒3において、プロトン導電体1に接触する導電性金属材2は、互いに接触するアノード電極部31及びカソード電極部32を有する。プロトン導電型触媒3は、アノード電極部31と上記プロトン導電体2との境界部分に接触した排ガス中のH2O4からアノード電極部31によってプロトン(H+)が分離され、プロトン導電体2に取り込む反応が促進されると共に、カソード電極部32と上記プロトン導電体2との境界部分において、カソード電極部32によって、プロトン導電体2から供給されるプロトンによる還元反応が促進されるよう構成される。
【0061】
プロトン導電型触媒3は、排ガス中のH2O4がアノード電極部31とプロトン導電体1との境界部分に接触すると、プロトン導電体1、アノード電極部31、H2O4の三相界面(酸化サイト)において、例えば、H2O→H++OH-、H2O→2H++O2-等の反応が起きる。そのため、アノード電極部31において、活性酸素種O*(例えばO2-、OH-、O2-、O22-等)が発生する。
そして、アノード反応により発生した上記活性酸素種O*は、高い酸化能を有しているため、発生後すぐに、排ガス中の炭素含有成分5を酸化する反応を起こす。例えば、CをCO又はCO2に、CH4をCH3OH、CO2、CO等に、HCをCO2等に酸化が可能である。つまり、上記酸化サイトでは、アノード反応(2H2O+C→CO2+4H++4e-、2xH2O+CxHy→CxO2x+(4x+y)H++4xe-等)が起きていることとなる。
【0062】
また、プロトン導電体1、カソード電極部32、排ガス(図示省略;NO、NO2、O2等)の三相界面(還元サイト)ではプロトンH+による反応ガスの還元反応(カソード反応)が起きる。具体的には、カソード電極部32近傍に排ガス中に含まれるNO、NO2、O2が存在すれば、これらをH2Oに還元することが出来る(2NO+4H++4e-→N2+2H2O、1/2O2+2H++2e-→H2O等)。また、カソード電極部32近傍にH2OやO2があれば、H2O2及び活性酸素種O*(例えば・O2H、H3O+)を生成する(O2+2H++2e-→H2O2等)。
【0063】
試料E1及び試料E2のプロトン導電体1は、上記のごとく、95質量%以上という高純度のSn0.95Al0.05P2O7からなる。そのため、これらのプロトン導電体1は、導電率に優れ、これを用いたプロトン導電型触媒3は、上述のごとく低温で炭素含有成分(HC)に対して優れた浄化性能を発揮することができる(表1参照)。
【0064】
(実施例2)
本例は、組成の異なる複数のリン酸スズ系化合物からなるプロトン導電体を作製する例である。
具体的には、実施例1の上記試料E2と同様にして、上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程と上記乾燥粉砕工程と上記焼成工程とを行ってSn1-xAlxP2O7又はSn1-xInxP2O7表されるプロトン導電体を作製した。
【0065】
本例においては、原料の配合比を変更してその他は上記試料E2と同様にしてSn1-xAlxP2O7(x=0、0.01、0.02、0.05、0.1、0.15、0.2、0.22、0.25)で表されるプロトン導電体、及びSn1-xInxP2O7((x=0、0.01、0.02、0.05、0.1、0.15、0.2、0.22、0.25))で表されるプロトン導電体を作製した。なお、Sn1-xInxP2O7で表されるプロトン導電体の作製にあたっては、試料E2の作製に用いた水酸化アルミニウム(Al(OH)3)の代わりに水酸化インジウム(In(OH)3)を用いた。
【0066】
このようにして作製したプロトン導電体について、実施例1と同様にして純度及び温度200℃における導電率を測定した。その結果を表2及び表3に示す。表2には、Sn1-xAlxP2O7で表されるプロトン導電体についてのxの値、純度、及び導電率を示す。また、表3には、Sn1-xInxP2O7で表されるプロトン導電体についてのxの値、純度、及び導電率を示す。
そして、Sn1-xAlxP2O7(0≦x≦0.25)及びSn1-xInxP2O7(0≦x≦0.25)におけるxの値と導電率との関係を図2に示す。同図において、横軸はSn1-xAlxP2O7又はSn1-xInxP2O7におけるxの値を示し、縦軸は温度200℃における導電率を示す。
【0067】
【表2】

【0068】
【表3】

【0069】
表2、表3、及び図2より知られるごとく、実施例1の上記試料E2と同様にして作製した本例のプロトン導電体は、いずれの組成においても、純度95質量%を超える高純度のリン酸スズ系化合物を製造することができた。また、これらのプロトン導電体は比較的高い導電率を示した。
特に、0.01≦x≦0.2の範囲においては、0.1S/cm以上の高い導電率を示した。したがって、Sn1-xAlxP2O7及びSn1-xInxP2O7において、0.01≦x≦0.2であることが好ましいことがわかる。
【0070】
(実施例3)
本例は、リン酸スズ系化合物の粉末からなるプロトン導電体の比表面積と浄化性能との関係を調べた例である。
本例においては、実施例1の試料E2と同様にしてSn0.95Al0.05P2O7の粉末からなるプロトン導電体を作製した。そして、このプロトン導電体の粉末をスタンプミルで15分間粉砕し、さらに乳鉢で調整後、遊星ボールミルで60分間湿式粉砕した。これにより一次粒子径(D50)が1μm弱の粉末を得た。
【0071】
次いで、粉末を温度450℃で仮焼し、所望の粒径にスタンプミルにて粉砕した。このようにして、比表面積が異なる複数のプロトン導電体の粉末を作製した。比表面積は、BET(N2吸着)で測定した。
【0072】
次に、比表面積が異なる複数のプロトン導電体について、それぞれ炭素含有成分の浄化性能の評価を行った。浄化性能の評価は、実施例1と同様にして行った。その結果を図3に示す。同図において、横軸はプロトン導電体粉末の比表面積(m2/g)を示し、縦軸はHC変化量が50%となるときの温度T50(℃)を示す。
【0073】
図3より知られるごとく、比表面積を10m2/g以上にすることにより、プロトン導電体の浄化性能をより一層向上できることがわかる。また、同図から、30m2/gを超えて比表面積を大きくしても浄化性能の向上効果はほとんど飽和してしまうことがわかる。
【0074】
以上のように、本例によれば、プロトン導電体粉末の比表面積は10m2/g以上が好ましく、プロトン導電体の排ガス中の炭素含有成分の浄化性能をより向上できることがわかる。
【符号の説明】
【0075】
1 プロトン導電体
2 導電性金属材
3 プロトン導電型触媒
【技術分野】
【0001】
本発明は、排ガスを浄化するために用いられる、リン酸スズ系化合物の粉末からなるプロトン導電体に関する。
【背景技術】
【0002】
従来から、自動車エンジンなどの内燃機関から排出される排ガス中に含まれるHC、CO、NOx等を浄化するために、排気管内には排ガス浄化用触媒体が設けられている。この排ガス浄化用触媒体としては、例えば多数のセルを有するハニカム構造のセラミック担体に触媒成分を担持させたものが用いられている。触媒成分としては、白金、パラジウム、及びロジウム等の貴金属成分をセリア/ジルコニア複合酸化物やアルミナ上に分散させた三元触媒が用いられている。
【0003】
貴金属等からなる上記三元触媒においては、理論空燃比に制御された排ガスの浄化は可能であるが、酸素過剰雰囲気にある例えばリーンバーンエンジンの排ガスの浄化性能が不十分であるという問題があった。また、例えば400℃を超える高温雰囲気でなければ、排ガスを十分に浄化できないという問題があった。
【0004】
そこで、リン酸スズ等のリン酸塩からなる触媒成分を含む排気ガス浄化用触媒が開発されている(特許文献1参照)。かかる排気ガス浄化用触媒を用いることにより、理論空燃比よりも高い空燃比で運転するリーンバーンエンジン等から排出される、酸素含有率が高い排ガスの浄化が可能になる。また、400℃以下の低温でも排ガスの浄化が可能になる。
また、リン酸化合物等からなるプロトン導電体を排気ガスの浄化に用いる技術が開発されている(特許文献2参照)。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2000−42415号公報
【特許文献2】特開2009−233618号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、リン酸スズ系化合物は、製造時に酸化スズ等の不純物を含みやすく、例えば95質量%以上という高純度のリン酸スズ系化合物を得ることは困難であった。そのため、リン酸スズ系化合物が本来有する優れた排ガスの浄化性能を十分に発揮させることができないという問題があった。特に、上記特許文献2に示すようにリン酸スズ系化合物をプロトン導電体として用いた排ガス浄化触媒を構成する場合には、リン酸スズ系化合物の純度が不十分であることに起因して導電率が不十分になり、低温での排ガスの浄化性能が不十分になるという問題があった。
【0007】
本発明はかかる問題点に鑑みてなされたものであって、高い導電率を示し、排ガス中の炭素含有成分を低温で十分に浄化することができるリン酸スズ系化合物からなるプロトン導電体及びその製造方法を提供しようとするものである。
【課題を解決するための手段】
【0008】
第1の発明は、導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
スズの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得る沈殿工程と、
上記沈殿物を焼成して上記プロトン導電体を得る焼成工程とを有することを特徴とするプロトン導電体の製造方法にある(請求項1)。
【0009】
第2の発明は、導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
水溶性スズ塩を水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液を中和して中和物を得る中和工程と、
上記中和物を解膠させることによりゾルを得るゾル化工程と、
上記ゾルとリン酸を混合してゲル化させてゲルを得るゲル化工程と、
上記ゲルを乾燥させ粉砕することにより粉砕粉を得る乾燥粉砕工程と、
上記粉砕粉を焼成する焼成工程とを有することを特徴とするプロトン導電体の製造方法にある(請求項4)。
【0010】
第3の発明は、導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、
純度95質量%以上のリン酸スズ系化合物の粉末からなることを特徴とするプロトン導電体にある(請求項6)。
【発明の効果】
【0011】
上記第1の発明の製造方法においては、上記イオン化工程と上記沈殿工程と上記焼成工程とを行うことにより、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体を製造する。
上記イオン化工程においては、上記特定の水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させる。これにより、液相の上記イオン水溶液中にスズイオンとリン酸イオンとを均一に分散させて溶解させることができる。そして、上記沈殿工程においては、上記イオン水溶液にスズイオンを還元する還元剤を添加する。これにより、SnとPとを含有する上記沈殿物を得ることができる。
次に、上記焼成工程においては、上記沈殿物を焼成する。これにより、上記沈殿物が酸化され、リン酸スズ系化合物の粉末からなる上記プロトン導電体を得ることができる。
【0012】
上記製造方法においては、上記イオン工程及び上記沈殿工程において、液相の上記イオン水溶液から、SnとPとを含むリン酸スズ系化合物の前駆体物質からなる上記沈殿物を沈殿させ、該沈殿物を上記焼成工程において焼成させている。そのため、不純物がほとんど残存又は生成せず、純度95質量%以上という従来にない高純度のリン酸スズ系化合物の粉末からなるプロトン導電体を製造することができる。かかる高純度のリン酸スズ系化合物の粉末からなるプロトン導電体は、上記第1の発明の製造方法により初めて製造可能となる。そして、上記プロトン導電体は、低温でも高い導電率を示し、上記プロトン導電体を導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。このとき、例えば400℃以下という低温でも排ガスを十分に浄化できるという優れた浄化性能を示すことができる。
【0013】
次に、上記第2の発明の製造方法においては、上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程と上記乾燥粉砕工程と上記焼成工程とを行うことにより、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体を製造する。
上記イオン化工程においては、上記水溶性スズ塩を水に溶解させてイオン水溶液を作製する。これにより、液相の上記イオン水溶液中にスズイオンを均一に分散させて溶解させることができる。そして、上記中和工程においては、上記イオン水溶液を中和させる。これにより、Snを含有する上記中和物を得ることができる。
【0014】
次に、上記ゾル化工程においては、上記中和物を解膠させる。これにより、Snが均一に分散したゾルを得ることができる。
次いで、上記ゲル化工程においては、上記ゾルとリン酸とを混合する。これにより、SnとPが均一に分散したゲルを得ることができる。
次に、上記乾燥粉砕工程においては、上記ゲルを乾燥させ粉砕する。これによりSnとPが均一に分散した粉砕粉を得る。そして、上記焼成工程においては、上記粉砕粉を焼成する。これにより、該粉砕粉が酸化され、リン酸スズ系化合物の粉末からなる上記プロトン導電体を得ることができる。
【0015】
上記製造方法においては、上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程とを行い、リン酸スズ系化合物の前駆体物質からなるゲルを生成させている。そして、上記乾燥粉砕工程において、乾燥及び粉砕させ、上記焼成工程において上記粉砕粉を焼成する。これにより、不純物がほとんど残存又は生成せず、純度95質量%以上という従来にない高純度のリン酸スズ系化合物の粉末からなるプロトン導電体を製造することができる。かかる高純度のリン酸スズ系化合物の粉末からなるプロトン導電体は、上記第2の発明の製造方法により初めて製造可能となる。該プロトン導電体は、低温でも高い導電率を示し、上記プロトン導電体を導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。このとき、例えば400℃以下という低温でも排ガスを十分に浄化できるという優れた浄化性能を示すことができる。
【0016】
第3の発明のプロトン導電体は、純度95質量%以上のリン酸スズ系化合物の粉末からなる。このような高純度のリン酸スズ系化合物粉末からなる上記プロトン導電体は、従来その製造方法が開発されていなかった。上記第1及び上記第2の発明により、その製造が可能になる。
かかる高純度のリン酸スズ系化合物粉末からなる上記プロトン導電体は、高い導電率を示し、上記プロトン導電体を導電性金属材に接触させて用いることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。このとき、排ガス中の炭素含有成分を例えば400℃以下の低温で十分に浄化することができる。
【図面の簡単な説明】
【0017】
【図1】実施例1における、プロトン導電型触媒の構成を示す説明図。
【図2】実施例2における、リン酸スズ系化合物におけるxの値と、導電率との関係を示す説明図。
【図3】実施例3における、プロトン導電体の粉末の比表面積と、HC浄化性能との関係を示す説明図。
【発明を実施するための形態】
【0018】
次に、本発明の好ましい実施形態について説明する。
上記プロトン導電体は、該プロトン導電体を導電性金属材と接触させることにより、炭素含有成分及び水等を含有する排ガス中から炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられる。
上記導電性金属材としては、例えば、Pt、Ag、Cu、Fe、Cr、Ir、Ni、Co、Au、W、Mo、Pd、Rh、及びその合金材料等を用いることができる。
【0019】
以下、プロトン導電体と導電性金属材とを接触させたプロトン導電型触媒について説明する。
上記プロトン導電型触媒において、上記プロトン導電体と接触する上記導電性金属材は、互いに接触するアノード電極部とカソード電極部とを有する。上記プロトン導電型触媒は、上記アノード電極部によって、該アノード電極部と上記プロトン導電体との境界部分に接触したH2Oからプロトン(H+)を分離し、上記プロトン導電体に取り込む反応を促進すると共に、上記カソード電極部によって、該カソード電極部と上記プロトン導電体との境界部分において、該プロトン導電体から供給されるプロトンによる還元反応を促進するよう構成される。
【0020】
上記プロトン導電型触媒は、上記アノード電極部によって、該アノード電極部と上記プロトン導電体との境界部分に接触した排ガス中のH2Oからプロトン(H+)を分離し、上記プロトン導電体に取り込む反応が促進される。上記アノード電極部は、アノード反応を進行する電極材であり、高純度のリン酸スズ系化合物からなる上記プロトン導電体は、プロトンを通す性質を有すると共に、400℃以下という比較的低温において高い導電率を有する。
そのため、排ガス中のH2Oが上記アノード電極部と上記プロトン導電体との境界部分に接触すると、プロトン導電体、アノード電極、H2Oの三相界面(酸化サイト)において、例えば、H2O→H++OH-、H2O→2H++O2-等の反応が起きる。そのため、アノード電極部において、活性酸素種(例えばO2-、OH-、O2-、O22-等)が発生する。また、プロトン導電体は、発生したプロトンを自発的に取り込む。
【0021】
そして、アノード反応により発生した上記活性酸素種は、高い酸化能を有しているため、発生後すぐに、排ガス中の炭素含有成分を酸化する反応を起こす。例えば、CをCO又はCO2に、COをCO2に、CH4をCH3OH、CO2、CO等に、HCをCO2等に酸化が可能である。つまり、上記酸化サイトでは、アノード反応(2H2O+C→CO2+4H++4e-、2xH2O+CxHy→CxO2x+(4x+y)H++4xe-等)が起きていることとなる。
【0022】
炭素含有成分を酸化した際に発生した電子は、接触したアノード電極部及びカソード電極部中を自由に動き回る。
また、上記プロトン導電体は、高い導電率を有するため、上記アノード電極部と上記プロトン導電体との境界部分に接触したH2Oから分離されたプロトンを自発的に取り込む。そして、取り込まれたプロトンは、プロトン導電体中を自由に動きまわる。
【0023】
そして、上記カソード電極部によって、上記カソード電極部と上記プロトン導電体との境界部分において、上記プロトン導電体から供給されるプロトンによる還元反応が促進される。
上記カソード電極部は、カソード反応を進行する電極材であり、上記プロトン導電体は、上述したように、酸化サイトにおける反応で取り込んだプロトンが存在した状態となっている。
そのため、プロトン導電体、カソード電極、反応ガス(NO、NO2、O2等)の三相界面(還元サイト)ではプロトンによる反応ガスの還元反応(カソード反応)が起きる。具体的には、カソード極近傍にNO、NO2、O2が存在すれば、H2Oに還元することが出来る(2NO+4H++4e-→N2+2H2O、1/2O2+2H++2e-→H2O等)。また、カソード極近傍にH2OやO2があれば、H2O2及び活性酸素種(例えば・O2H、H3O+)を生成する(O2+2H++2e-→H2O2等)。そして、この活性酸素種は、上記と同様に、発生後すぐに排ガス中の炭素含有成分を酸化する反応を起こす。
【0024】
このように、上記プロトン導電型触媒は、排ガス中のH2Oを反応剤として用い、アノード極、カソード極の両極で活性酸素種を生成することができる。そして、両極より発生した活性酸素種が排ガス中の炭素含有成分の酸化を可能にするため、高い酸化性能で酸化を行うことができる。また、酸化性能が高いため、温度400℃以下という比較的低温でも、活性酸素種の発生、及び炭素含有成分の酸化が自発的に起こる。また、炭素含有成分の酸化だけでなく、NO、NO2等の還元も行うことができる。
【0025】
上記プロトン導電型触媒は、上記プロトン導電体と上記導電性金属材とが接触した状態で構成されていれば良く、例えば、粒状のプロトン導電体と粒状の導電性金属材とを混合して接触させた状態等がある。
【0026】
上記プロトン導電型触媒の製造方法としては、例えば、プロトン導電体とアノード反応及びカソード反応を進行する各種導電性金属材とを、乳鉢等で物理混合することにより得る方法がある。
また、溶液法にてアノード電極部及びカソード電極部を構成する材料をプロトン導電体に担持し混合する方法等により作製してもよい。
【0027】
上記アノード電極部と上記カソード電極部とは、異なる材料を用いてもよいし、同一の材料を用いてもよい。
上記アノード電極部と上記カソード電極部が異なる材料である場合には、アノード電極部とカソード電極部とを混合したものを導電性金属材とすればよい。
【0028】
上記アノード電極部と上記カソード電極部とが同一材料である場合には、上記アノード電極部及び上記カソード電極部を区別することなく、導電性金属材として1種の材料を用意すればよい。この場合には、導電性金属材において、プロトン導電体、H2Oとの三相界面を形成する部分が酸化サイトとなり上記アノード反応を促進する。一方、電極材料において、プロトン導電体、反応ガスとの三相界面を形成する部分が還元サイトとなって、上記カソード反応を促進する。
【0029】
上記プロトン導電型触媒は、これをコージェライト、SiC等からなるハニカム構造体に担持させて用いることができる。また、上記プロトン導電型触媒自体をハニカム状に成形して用いることもできる。
【0030】
次に、上記プロトン導電体は、純度95質量%以上のリン酸スズ系化合物の粉末からなる。
純度が95質量%未満の場合には、導電率が低くなり、低温での排ガスの浄化性能が不十分になるおそれがある。純度の測定は、X線回折(XRD)で結晶相を確認し、エネルギー分散型X線分光分析(EDX)により、P及びSの量を定量して算出することができる。
【0031】
上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなることが好ましい(請求項7)。
この場合には、上記リン酸スズ系化合物の導電率をより向上させることができる。
特に、MがAlの場合には、0.02≦x≦0.15がより好ましく、0.03≦x≦0.1がさらに好ましい。
また、MがInの場合には、0.04≦x≦0.15がより好ましく、0.05≦x≦0.13がよい。
【0032】
また、上記リン酸スズ系化合物の粉末の比表面積は10m2/g以上であることが好ましい(請求項8)。
この場合には、排ガス中の炭素含有成分に対する浄化性能をより向上させることができる。また、比表面積を大きくしすぎても上述の浄化性能の向上効果はほとんど得られなくなり、また大きな比表面積の粉末を得るための操作が煩雑になるという観点からは、上記リン酸スズ系化合物の粉末の比表面積は100m2/g以下が好ましく、50m2/g以下がより好ましい。
【0033】
上記プロトン導電体は、上記第1の発明のように、イオン化工程と沈殿工程と焼成工程とを行うことにより製造することができる。
上記第1の発明の上記イオン化工程においては、水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてイオン水溶液を作製する。
【0034】
上記第1の発明において、上記水溶性スズ塩としては、スズの硫酸塩(硫酸スズ)、硝酸塩(硝酸スズ)、塩化物塩(塩化スズ)、臭化物塩(臭化スズ)、及びヨウ化物塩(ヨウ化スズ)から選ばれる少なくとも1種を用いることができる。
また、上記水溶性リン酸塩としては、例えばリン酸アンモニウム、リン酸ナトリウム(リン酸ソーダ)等を用いることができる。
【0035】
上記沈殿工程においては、上記イオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得る。
上記還元剤としては、例えばアンモニア、尿素、アミン、及びヒドラジン等を用いることができる。
【0036】
また、上記第1の発明の上記焼成工程においては、上記沈殿物を焼成して上記プロトン導電体を得る。
上記沈殿物の焼成は、例えば温度650〜900℃で行うことができる。
【0037】
次に、上記第1の発明においては、上記沈殿工程と上記焼成工程との間に、上記沈殿物を水で洗浄する洗浄工程を行うことが好ましい(請求項3)。
この場合には、上記焼成工程後に得られる上記リン酸スズ系化合物の純度をより向上させることができる。
【0038】
また、上記第1の発明においては、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩及び上記水溶性リン酸塩の他に、アルミニウムの硫酸塩(硫酸アルミニウム)、硝酸塩(硝酸アルミニウム)、塩化物塩(塩化アルミニウム)、臭化物塩(臭化アルミニウム)、及びヨウ化物塩(ヨウ化アルミニウム)から選ばれる少なくとも1種の水溶性アルミニウム塩、又はインジウムの硫酸塩(硫酸インジウム)、硝酸塩(硝酸インジウム)、塩化物塩(塩化インジウム)、臭化物塩(臭化インジウム)、及びヨウ化物塩(ヨウ化インジウム)から選ばれる少なくとも1種の水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製し、上記沈殿工程においては、上記イオン水溶液中のSnイオンとAlイオン又はInイオンとを還元する上記還元剤を添加することが好ましい(請求項2)。
【0039】
この場合には、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)で表されるリン酸スズ系化合物からなる上記プロトン導電体を製造することができる。該プロトン導電体は、上述のごとく、低温でより優れた導電率を示すことができる。
SnイオンとAlイオン又はInイオンとを還元する上記還元剤としては、アンモニア、尿素などの上述の還元剤と同様のものを用いることができる。
【0040】
また、上記プロトン導電体は、上記第2の発明に示すごとく、イオン化工程と中和工程とゾル化工程とゲル化工程と乾燥粉砕工程と焼成工程とを行うことにより製造することができる。
上記第2の発明の上記イオン化工程においては、水溶性スズ塩を水に溶解させてイオン水溶液を作製する。
上記第2の発明においては、上記水溶性スズ塩として、例えばスズの水酸化物塩(水酸化スズ)、硫酸塩(硫酸スズ)、硝酸塩(硝酸スズ)、塩化物塩(塩化スズ)、臭化物塩(臭化スズ)及びヨウ化物塩(ヨウ化スズ)等を用いることができる。
【0041】
また、上記中和工程においては、上記第2の発明の上記イオン水溶液を中和して中和物を得る。具体的には、上記イオン水溶液がアルカリ性(塩基性)の場合には、例えば酢酸、乳酸等の酸を加えて中和させることができる。また、上記イオン水溶液が酸性の場合には、アンモニア、アンモニウム塩等の塩基を加えて中和させることができる。即ち、上記中和工程においては、中和させるイオン水溶液のpHに応じて酸又はアルカリ(塩基)を加えることができる。
【0042】
次に、上記ゾル化工程においては、上記中和物を解膠させることによりゾルを得る。
具体的には、酸や、水溶液が酸性を示す塩の水溶液を添加することにより上記中和物を解膠させることができる。
【0043】
次に、上記ゲル化工程においては、上記ゾルとリン酸とを混合してゲルを得る。また、上記乾燥粉砕工程においては、上記ゲルを乾燥させ粉砕することにより粉砕粉を得る。そして、上記焼成工程においては、上記粉砕粉を焼成する。
上記粉砕粉の焼成は、例えば温度800〜1000℃で行うことができる。
【0044】
また、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩の他に、水溶性アルミニウム塩又は水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製することが好ましい(請求項5)。
この場合には、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)で表されるリン酸スズ系化合物からなる上記プロトン導電体を製造することができる。該プロトン導電体は、上述のごとく低温でより優れた導電率を示すことができる。
【0045】
上記水溶性アルミニウム塩としては、例えばアルミニウムの水酸化物塩(水酸化アルミニウム)、硫酸塩(硫酸アルミニウム)、硝酸塩(硝酸アルミニウム)、塩化物塩(塩化アルミニウム)、臭化物塩(臭化アルミニウム)、及びヨウ化物塩(ヨウ化アルミニウム)等を用いることができる。
また、水溶性インジウム塩としては、例えばインジウムの水酸化物塩(水酸化インジウム)、硫酸塩(硫酸インジウム)、硝酸塩(硝酸インジウム)、塩化物塩(塩化インジウム)、臭化物塩(臭化インジウム)、及びヨウ化物塩(ヨウ化インジウム)等を用いることができる。
【実施例】
【0046】
(実施例1)
本発明の実施例にかかるプロトン導電体について説明する。
図1に示すごとく、本例のプロトン導電体1は、導電性金属材2と接触させることにより、排ガス中の炭素含有成分6を酸化して排ガスを浄化するプロトン導電型触媒3として用いられる。プロトン導電体1は、純度95質量%以上のリン酸スズ系化合物の粉末からなる。本例においては、リン酸スズ系化合物として、リン酸スズ化合物(SnP2O7)のSnの一部がAlで置換されたSn0.95Al0.05P2O7を採用する。
【0047】
本例のプロトン導電体は、次のようにして作製する。
即ち、まず、硫酸スズ(SnSO4)と硫酸アルミニウム(Al2(SO4)3)リン酸ソーダ(Na4P2O7)とを水に溶解させてイオン水溶液を作製した(イオン化工程)。次いで、このイオン水溶液に、Snの還元剤としてアンモニア(NH3)水溶液を添加し、沈殿物を得た(沈殿工程)。なお、各工程において原料の混合は、目的組成のSn0.95Al0.05P2O7が得られる化学量論比で行った。
【0048】
次に、得られた沈殿物を濾過して水で洗浄した後、乾燥させた。その後、大気雰囲気下、温度800℃で1時間焼成した(焼成工程)。このようにしてSn0.95Al0.05P2O7からなるプロトン導電体を得た。これを試料E1とする。
【0049】
また、本例においては、上記試料E1とは異なる方法により、Sn0.95Al0.05P2O7からなるプロトン導電体(試料E2及び試料C1)を作製した。
【0050】
試料E2のプロトン導電体の製造にあたっては、まず、水酸化スズ(Sn(OH)4)と水酸化アルミニウム(Al(OH)3)とを水に溶解させてイオン水溶液を作製した(イオン化工程)。次いで、イオン水溶液に酢酸を加えて中和し、中和物を得た(中和工程)。次に、乳酸を添加することにより中和物を解膠させてゾルを得た(ゾル化工程)。次いで、ゾルにリン酸を添加して混合することにより、ゲル化させてゲルを得た(ゲル化工程)。
各工程において原料の混合は、目的組成のSn0.95Al0.05P2O7が得られる化学量論比で行った。
【0051】
次に、ゲルを乾燥させ粉砕することにより粉砕粉を得た(乾燥粉砕工程)。次いで、粉砕粉を大気雰囲気下、温度900℃で1時間焼成した(焼成工程)。このようにしてSn0.95Al0.05P2O7からなるプロトン導電体を得た。これを試料E2とする。
【0052】
また、試料C1のプロトン導電体の製造にあたっては、まず、SnO2粉末、Al(OH)3粉末とをリン酸水溶液中に混合した。混合は、目的組成のSn0.95Al0.05P2O7が得られる化学量論比で行った。そして、混合液を大気雰囲気下温度200℃で乾燥させて泥漿(スラリー)を得た。次いで、得られた泥漿を大気雰囲気下温度650℃で2時間焼成した。このようにして、Sn0.95Al0.05P2O7を含む粉末からなるプロトン導電体を得た。これを試料C1とする。
【0053】
次に、上記のように作製した3種類のプロトン導電体(試料E1、試料E2、及び試料C1)について、Sn0.95Al0.05P2O7の純度、導電率、炭素含有成分に対する浄化性能の評価を行った。
【0054】
「純度」
純度の測定にあたっては、まずX線回折装置((株)リガク製のRINT2000)により、各試料がSnO2とSnP2O7の結晶相のみからなることを確認した。
次いで、電子顕微鏡(SEM:日本電子(株)製のJSM6700)での5000倍拡大下において、エネルギー分散型X線分光分析(EDX:日本電子(株)製のJED2000)を用いて各粉末試料についてランダムに10点のP量、Sn量を定量し、その平均nを求めた。測定したP量は全てSnP2O7になっており、測定したSnの量からSnP2O7に用いたSnの量を差し引いたSn量は全てSnO2であるとして、SnP2O7の純度を算出した。その結果を表1に示す。
【0055】
「導電率」
粉末状の各試料を厚みL(cm)のペレットに成形し、その両面にPt等からなる面積S(cm2)の導電性金属ペースト又は導電性金属箔を取り付けてセルを作製した。このセルについて、空気中で交流インピーダンス法によりオーミック抵抗Rohomic(Ω)を測定した。そして、導電率σをσ=L/S×Rohomicという式に基づいて算出した。その結果を表1に示す。
【0056】
「浄化性能」
浄化性能の測定にあたっては、まず、各試料のプロトン導電体1を導電性金属材料2に接触させてなるプロトン導電型触媒3を作製する(図1参照)。
具体的には、まず、導電性金属材料(アノード電極部及びカソード電極部)として、Ptを準備した。各試料のプロトン導電体90質量部と導電性金属材料10質量部とを乳鉢などで物理混合し、プロトン導電型触媒を得た。なお、本例においては、アノード電極部及びカソード電極部をいずれもPtで形成したが、異なる導電性金属材料で形成することもできる。また、本例においては、物理混合によりプロトン導電型触媒を作製したが、溶液法にてアノード電極部及びカソード電極部をプロトン導電体に担持させてプロトン導電型触媒を作製することもできる。
次に、プロトン導電型触媒1gを直径φ7.0mmの管状の反応器に充填した。そして、この反応器内に、HC:1000ppm、O2:1質量%、H2O:3質量%、N2:残部(質量%)からなるモデルガスを流速0.6L/minで通過させた。モデルガス通過前後におけるHCの変化量を温度280℃〜温度100℃の範囲内において測定した。HCの量は、ガスクロマトグラフィーにより測定した。そして、HC変化量が50%になるときの温度T50を求めた。その結果を表1に示す。
【0057】
【表1】

【0058】
表1より知られるごとく、試料E1及び試料E2は、95質量%以上という高純度のSn0.95Al0.05P2O7からなるプロトン導電体からなり、導電率に優れ、温度110℃という低温で炭素含有成分(HC)を50%浄化できるという優れた浄化性能を示した。即ち、上記イオン化工程と上記沈殿工程と上記焼成工程、又は上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程と上記乾燥粉砕工程と上記焼成工程とを行うことにより、95質量%以上の高純度のリン酸スズ系化合物からなるプロトン導電体(試料E1及び試料E2)を製造することができ、該プロトン導電体は、優れた導電率を示し、低温で炭素含有成分(HC)に対して優れた浄化性能を示すことができる。
【0059】
これに対し、固体粉末原料を混合して作製した試料C1のプロトン導電体は、Sn0.95Al0.05P2O7の純度が低く、SnO2を多く含有していた。そして、試料C1は、導電率が低く、低温での炭素含有成分(HC)に対する浄化性能が不十分であった。
【0060】
試料E1及び試料E2のプロトン導電体は、このプロトン導電体1を導電性金属材2と接触させることにより、炭素含有成分及び水等を含有する排ガス中から炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒3として用いられる(図1参照)。
図1に示すごとく、プロトン導電型触媒3において、プロトン導電体1に接触する導電性金属材2は、互いに接触するアノード電極部31及びカソード電極部32を有する。プロトン導電型触媒3は、アノード電極部31と上記プロトン導電体2との境界部分に接触した排ガス中のH2O4からアノード電極部31によってプロトン(H+)が分離され、プロトン導電体2に取り込む反応が促進されると共に、カソード電極部32と上記プロトン導電体2との境界部分において、カソード電極部32によって、プロトン導電体2から供給されるプロトンによる還元反応が促進されるよう構成される。
【0061】
プロトン導電型触媒3は、排ガス中のH2O4がアノード電極部31とプロトン導電体1との境界部分に接触すると、プロトン導電体1、アノード電極部31、H2O4の三相界面(酸化サイト)において、例えば、H2O→H++OH-、H2O→2H++O2-等の反応が起きる。そのため、アノード電極部31において、活性酸素種O*(例えばO2-、OH-、O2-、O22-等)が発生する。
そして、アノード反応により発生した上記活性酸素種O*は、高い酸化能を有しているため、発生後すぐに、排ガス中の炭素含有成分5を酸化する反応を起こす。例えば、CをCO又はCO2に、CH4をCH3OH、CO2、CO等に、HCをCO2等に酸化が可能である。つまり、上記酸化サイトでは、アノード反応(2H2O+C→CO2+4H++4e-、2xH2O+CxHy→CxO2x+(4x+y)H++4xe-等)が起きていることとなる。
【0062】
また、プロトン導電体1、カソード電極部32、排ガス(図示省略;NO、NO2、O2等)の三相界面(還元サイト)ではプロトンH+による反応ガスの還元反応(カソード反応)が起きる。具体的には、カソード電極部32近傍に排ガス中に含まれるNO、NO2、O2が存在すれば、これらをH2Oに還元することが出来る(2NO+4H++4e-→N2+2H2O、1/2O2+2H++2e-→H2O等)。また、カソード電極部32近傍にH2OやO2があれば、H2O2及び活性酸素種O*(例えば・O2H、H3O+)を生成する(O2+2H++2e-→H2O2等)。
【0063】
試料E1及び試料E2のプロトン導電体1は、上記のごとく、95質量%以上という高純度のSn0.95Al0.05P2O7からなる。そのため、これらのプロトン導電体1は、導電率に優れ、これを用いたプロトン導電型触媒3は、上述のごとく低温で炭素含有成分(HC)に対して優れた浄化性能を発揮することができる(表1参照)。
【0064】
(実施例2)
本例は、組成の異なる複数のリン酸スズ系化合物からなるプロトン導電体を作製する例である。
具体的には、実施例1の上記試料E2と同様にして、上記イオン化工程と上記中和工程と上記ゾル化工程と上記ゲル化工程と上記乾燥粉砕工程と上記焼成工程とを行ってSn1-xAlxP2O7又はSn1-xInxP2O7表されるプロトン導電体を作製した。
【0065】
本例においては、原料の配合比を変更してその他は上記試料E2と同様にしてSn1-xAlxP2O7(x=0、0.01、0.02、0.05、0.1、0.15、0.2、0.22、0.25)で表されるプロトン導電体、及びSn1-xInxP2O7((x=0、0.01、0.02、0.05、0.1、0.15、0.2、0.22、0.25))で表されるプロトン導電体を作製した。なお、Sn1-xInxP2O7で表されるプロトン導電体の作製にあたっては、試料E2の作製に用いた水酸化アルミニウム(Al(OH)3)の代わりに水酸化インジウム(In(OH)3)を用いた。
【0066】
このようにして作製したプロトン導電体について、実施例1と同様にして純度及び温度200℃における導電率を測定した。その結果を表2及び表3に示す。表2には、Sn1-xAlxP2O7で表されるプロトン導電体についてのxの値、純度、及び導電率を示す。また、表3には、Sn1-xInxP2O7で表されるプロトン導電体についてのxの値、純度、及び導電率を示す。
そして、Sn1-xAlxP2O7(0≦x≦0.25)及びSn1-xInxP2O7(0≦x≦0.25)におけるxの値と導電率との関係を図2に示す。同図において、横軸はSn1-xAlxP2O7又はSn1-xInxP2O7におけるxの値を示し、縦軸は温度200℃における導電率を示す。
【0067】
【表2】

【0068】
【表3】

【0069】
表2、表3、及び図2より知られるごとく、実施例1の上記試料E2と同様にして作製した本例のプロトン導電体は、いずれの組成においても、純度95質量%を超える高純度のリン酸スズ系化合物を製造することができた。また、これらのプロトン導電体は比較的高い導電率を示した。
特に、0.01≦x≦0.2の範囲においては、0.1S/cm以上の高い導電率を示した。したがって、Sn1-xAlxP2O7及びSn1-xInxP2O7において、0.01≦x≦0.2であることが好ましいことがわかる。
【0070】
(実施例3)
本例は、リン酸スズ系化合物の粉末からなるプロトン導電体の比表面積と浄化性能との関係を調べた例である。
本例においては、実施例1の試料E2と同様にしてSn0.95Al0.05P2O7の粉末からなるプロトン導電体を作製した。そして、このプロトン導電体の粉末をスタンプミルで15分間粉砕し、さらに乳鉢で調整後、遊星ボールミルで60分間湿式粉砕した。これにより一次粒子径(D50)が1μm弱の粉末を得た。
【0071】
次いで、粉末を温度450℃で仮焼し、所望の粒径にスタンプミルにて粉砕した。このようにして、比表面積が異なる複数のプロトン導電体の粉末を作製した。比表面積は、BET(N2吸着)で測定した。
【0072】
次に、比表面積が異なる複数のプロトン導電体について、それぞれ炭素含有成分の浄化性能の評価を行った。浄化性能の評価は、実施例1と同様にして行った。その結果を図3に示す。同図において、横軸はプロトン導電体粉末の比表面積(m2/g)を示し、縦軸はHC変化量が50%となるときの温度T50(℃)を示す。
【0073】
図3より知られるごとく、比表面積を10m2/g以上にすることにより、プロトン導電体の浄化性能をより一層向上できることがわかる。また、同図から、30m2/gを超えて比表面積を大きくしても浄化性能の向上効果はほとんど飽和してしまうことがわかる。
【0074】
以上のように、本例によれば、プロトン導電体粉末の比表面積は10m2/g以上が好ましく、プロトン導電体の排ガス中の炭素含有成分の浄化性能をより向上できることがわかる。
【符号の説明】
【0075】
1 プロトン導電体
2 導電性金属材
3 プロトン導電型触媒
【特許請求の範囲】
【請求項1】
導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
スズの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得る沈殿工程と、
上記沈殿物を焼成して上記プロトン導電体を得る焼成工程とを有することを特徴とするプロトン導電体の製造方法。
【請求項2】
請求項1に記載の製造方法において、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩及び上記水溶性リン酸塩の他に、アルミニウムの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性アルミニウム塩、又はインジウムの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製し、上記沈殿工程においては、上記イオン水溶液中のSnイオンとAlイオン又はInイオンとを還元する上記還元剤を添加することを特徴とするプロトン導電体の製造方法。
【請求項3】
請求項1又は2に記載の製造方法において、上記沈殿工程と上記焼成工程との間に、上記沈殿物を水で洗浄する洗浄工程を行うことを特徴とするプロトン導電体の製造方法。
【請求項4】
導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
水溶性スズ塩を水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液を中和して中和物を得る中和工程と、
上記中和物を解膠させることによりゾルを得るゾル化工程と、
上記ゾルとリン酸を混合してゲル化させてゲルを得るゲル化工程と、
上記ゲルを乾燥させ粉砕することにより粉砕粉を得る乾燥粉砕工程と、
上記粉砕粉を焼成する焼成工程とを有することを特徴とするプロトン導電体の製造方法。
【請求項5】
請求項4に記載の製造方法において、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩の他に、水溶性アルミニウム塩又は水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製することを特徴とするプロトン導電体の製造方法。
【請求項6】
導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、
純度95質量%以上のリン酸スズ系化合物の粉末からなることを特徴とするプロトン導電体。
【請求項7】
請求項6に記載のプロトン導電体において、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなることを特徴とするプロトン導電体。
【請求項8】
請求項6又は7に記載のプロトン導電体において、上記リン酸スズ系化合物の粉末の比表面積は10m2/g以上であることを特徴とするプロトン導電体。
【請求項1】
導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
スズの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性スズ塩と、水溶性リン酸塩又はリン酸とを水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液にスズイオンを還元する還元剤を添加して沈殿物を得る沈殿工程と、
上記沈殿物を焼成して上記プロトン導電体を得る焼成工程とを有することを特徴とするプロトン導電体の製造方法。
【請求項2】
請求項1に記載の製造方法において、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩及び上記水溶性リン酸塩の他に、アルミニウムの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性アルミニウム塩、又はインジウムの硫酸塩、硝酸塩、塩化物塩、臭化物塩、及びヨウ化物塩から選ばれる少なくとも1種の水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製し、上記沈殿工程においては、上記イオン水溶液中のSnイオンとAlイオン又はInイオンとを還元する上記還元剤を添加することを特徴とするプロトン導電体の製造方法。
【請求項3】
請求項1又は2に記載の製造方法において、上記沈殿工程と上記焼成工程との間に、上記沈殿物を水で洗浄する洗浄工程を行うことを特徴とするプロトン導電体の製造方法。
【請求項4】
導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、純度95質量%以上のリン酸スズ系化合物の粉末からなるプロトン導電体の製造方法において、
水溶性スズ塩を水に溶解させてイオン水溶液を作製するイオン化工程と、
上記イオン水溶液を中和して中和物を得る中和工程と、
上記中和物を解膠させることによりゾルを得るゾル化工程と、
上記ゾルとリン酸を混合してゲル化させてゲルを得るゲル化工程と、
上記ゲルを乾燥させ粉砕することにより粉砕粉を得る乾燥粉砕工程と、
上記粉砕粉を焼成する焼成工程とを有することを特徴とするプロトン導電体の製造方法。
【請求項5】
請求項4に記載の製造方法において、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなり、上記イオン化工程においては、上記水溶性スズ塩の他に、水溶性アルミニウム塩又は水溶性インジウム塩を水に溶解させて上記イオン水溶液を作製することを特徴とするプロトン導電体の製造方法。
【請求項6】
導電性金属材と接触させることにより、排ガス中の炭素含有成分を酸化して排ガスを浄化するプロトン導電型触媒として用いられ、
純度95質量%以上のリン酸スズ系化合物の粉末からなることを特徴とするプロトン導電体。
【請求項7】
請求項6に記載のプロトン導電体において、上記リン酸スズ系化合物は、Sn1-xMxP2O7(0.01≦x≦0.2、MはAl又はIn)からなることを特徴とするプロトン導電体。
【請求項8】
請求項6又は7に記載のプロトン導電体において、上記リン酸スズ系化合物の粉末の比表面積は10m2/g以上であることを特徴とするプロトン導電体。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2012−20254(P2012−20254A)
【公開日】平成24年2月2日(2012.2.2)
【国際特許分類】
【出願番号】特願2010−161526(P2010−161526)
【出願日】平成22年7月16日(2010.7.16)
【出願人】(000004260)株式会社デンソー (27,639)
【出願人】(000004695)株式会社日本自動車部品総合研究所 (1,981)
【Fターム(参考)】
【公開日】平成24年2月2日(2012.2.2)
【国際特許分類】
【出願日】平成22年7月16日(2010.7.16)
【出願人】(000004260)株式会社デンソー (27,639)
【出願人】(000004695)株式会社日本自動車部品総合研究所 (1,981)
【Fターム(参考)】
[ Back to top ]

