ベータ型ゼオライトの製造方法
【課題】ゼオライトの結晶構造を破壊することなく、Si/Al比の高いベータ型ゼオライトを容易に製造できる方法を提供すること。
【解決手段】本発明のベータ型ゼオライトの製造方法は、原料ベータ型ゼオライトをイオン交換によってアンモニウム型となし、次いで該ベータ型ゼオライトを水蒸気に曝露し、曝露後の該ベータ型ゼオライトを酸処理に付して、Si/Al比が高められたベータ型ゼオライトを得ることを特徴とする。イオン交換に付される原料ベータ型ゼオライトが、構造規定剤を用いずに合成されたものであることが好適である。
【解決手段】本発明のベータ型ゼオライトの製造方法は、原料ベータ型ゼオライトをイオン交換によってアンモニウム型となし、次いで該ベータ型ゼオライトを水蒸気に曝露し、曝露後の該ベータ型ゼオライトを酸処理に付して、Si/Al比が高められたベータ型ゼオライトを得ることを特徴とする。イオン交換に付される原料ベータ型ゼオライトが、構造規定剤を用いずに合成されたものであることが好適である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、原料としてのベータ型ゼオライトから、Si/Al比が高められたベータ型ゼオライトを製造する方法に関する。
【背景技術】
【0002】
ベータ型ゼオライトは、固体酸触媒や吸着剤として有用なものであり、石油化学工業における触媒として、また内燃機関の排気ガス浄化用ハイドロカーボントラップとして、現在世界中で多量に使用されている。ベータ型ゼオライトの合成法は種々提案されている。一般的な方法はテトラエチルアンモニウムイオンを含む化合物を構造規定剤(以下「有機SDA」と略称する。)として用いる方法である。そのような方法は例えば以下の特許文献1に記載されている。しかしながら、テトラエチルアンモニウムイオンを含む化合物は高価である上に、ベータ型ゼオライトの結晶化終了後は過剰分のほとんどが分解してしまい、結晶に取りこまれた分も分解以外の方法で除去できないため、回収して再利用することは不可能である。そのために、この方法により製造したベータ型ゼオライトは高価である。更に、結晶中にテトラエチルアンモニウムイオンが取り込まれるため、吸着剤や触媒として使用する際には焼成により除去する必要がある。その際の排ガスは環境汚染の原因となり、また、合成母液の無害化処理のためにも多くの薬剤を必要とする。このように、テトラエチルアンモニウムイオンを用いるベータ型ゼオライトの合成方法は高価であるばかりでなく、環境負荷の大きい製造方法であることから、有機SDAを用いない製造方法の実現が望まれていた。
【0003】
このような状況の中で、最近、有機SDAを使用しないベータ型ゼオライトの合成方法が特許文献2において提案された。同文献においては、特定の組成の反応混合物となるように、シリカ源、アルミナ源、アルカリ源、及び水を混合し;SiO2/Al2O3比が8〜30であり、かつ平均粒子径が150nm以上である有機化合物を含まないベータ型ゼオライトを種結晶として用い、これを、前記反応混合物中のシリカ成分に対して0.1〜20質量%の割合で該反応混合物に添加し;前記種結晶が添加された前記反応混合物を100〜200℃で密閉加熱することで、有機SDAを使用せずにベータ型ゼオライトを合成している。
【0004】
ところで、ベータ型ゼオライトを、石油化学工業における触媒として用いる場合や、内燃機関の排気ガス浄化用ハイドロカーボントラップとして用いる場合には、そのSi/Al比を高めることが、性能向上の観点から有利である。ベータ型ゼオライトにおけるSi/Al比を高めるための手法としては、例えば特許文献3に記載されているとおり、水蒸気処理及び酸処理をこの順で行う方法が知られている。
【0005】
【特許文献1】米国特許第3,308,069号明細書
【特許文献2】国際公開2011/013560号パンフレット
【特許文献3】特開2010−215434号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかし、原料として用いるベータ型ゼオライトの種類によっては、Si/Al比を高めるための手法として、上述の処理を行った場合、ゼオライトの結晶構造が破壊されてしまう場合がある。
【0007】
本発明の課題は、前述した従来技術が有する種々の欠点を解消し得るベータ型ゼオライトの製造方法を提供することにある。
【課題を解決するための手段】
【0008】
本発明は、原料ベータ型ゼオライトをイオン交換によってアンモニウム型となし、次いで該ベータ型ゼオライトを水蒸気に曝露し、曝露後の該ベータ型ゼオライトを酸処理に付して、Si/Al比が高められたベータ型ゼオライトを得ることを特徴とするベータ型ゼオライトの製造方法を提供することによって、前記の課題を解決したものである。
【発明の効果】
【0009】
本発明によれば、ゼオライトの結晶構造を破壊することなく、Si/Al比の高いベータ型ゼオライトを容易に製造することができる。
【図面の簡単な説明】
【0010】
【図1】図1は、ベータ型ゼオライトの水蒸気曝露に用いられる装置を示す模式図である。
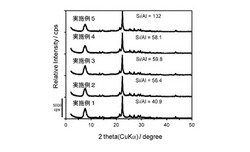
【図2】図2は、有機構造規定剤を用いずに合成されたベータ型ゼオライトを原料とし、実施例1ないし5で得られたベータ型ゼオライトのX線回折図である。
【図3】図3は、有機構造規定剤を用いて合成されたベータ型ゼオライトを原料とし、実施例6ないし10で得られたベータ型ゼオライトのX線回折図である。
【図4】図4は、比較例1及び2で得られたベータ型ゼオライトのX線回折図である。
【図5】図5は、実施例2及び7で得られたベータ型ゼオライトの触媒活性を評価するための装置の概略図である。
【発明を実施するための形態】
【0011】
本発明の製造方法は、(1)原料ベータ型ゼオライトのイオン交換処理工程、(2)イオン交換された原料ベータ型ゼオライトを水蒸気に曝露する工程、及び(3)水蒸気に曝露された原料ベータ型ゼオライトの酸処理工程の3つの工程を含んでいる。以下、これらの工程についてそれぞれ説明する。
【0012】
(1)原料ベータ型ゼオライトのイオン交換処理工程
原料ベータ型ゼオライトは、一般にナトリウム等のアルカリ金属を含んでいる。アルカリ金属を含むベータ型ゼオライトは、これを石油化学工業における触媒として用いる場合や、内燃機関の排気ガス浄化用ハイドロカーボントラップとして用いる場合に、所期の特性を発揮しにくいので、イオン交換によって除去し、アンモニウム型のベータ型ゼオライトとなす。
【0013】
イオン交換処理に付す原料ベータ型ゼオライトとしては、例えばSi/Al比が4〜100、好ましくは4〜8、更に好ましくは5〜7である低Si/Al比のものを用いる。低Si/Al比の原料ベータ型ゼオライトを用いることで、本発明の製造方法の効果が顕著なものとなる。
【0014】
原料ベータ型ゼオライトとしては、(イ)有機SDAを用いずに合成されたもの(以下「OSDAフリーベータ型ゼオライト」とも言う。)、及び(ロ)有機SDAを用いて合成されたもの(以下「OSDAベータ型ゼオライト」とも言う。)の双方を用いることができる。これら(イ)及び(ロ)のうち、(イ)のベータ型ゼオライトは、従来の手法によってSi/Alを高めると、ゼオライトの結晶構造が破壊されやすいことが、本発明者らの検討の結果判明した。しかし、本発明の方法によって(イ)のベータ型ゼオライトを処理すると、結晶構造の破壊を極力抑えた上で、Si/Alを高めることが可能となった。したがって、(イ)及び(ロ)のうち、(イ)のベータ型ゼオライトを原料として用いると、本発明の特徴が一層際だったものとなる。また、(イ)のベータ型ゼオライトを用いることは、有機SDAを用いないという点で、経済性の観点及び環境負荷の観点からも有利である。
【0015】
(イ)のベータ型ゼオライトを用いる場合、該ベータ型ゼオライトの合成方法としては、例えば国際公開2011/013560号パンフレットに記載の方法を採用することができる。また、中国特許出願公開第101249968A号明細書に記載の方法も採用することができる。更に、Chemistry of Materials, Vol.20, No.14, p.4533-4535 (2008)に記載の方法を採用することもできる。
【0016】
(イ)のベータ型ゼオライトの合成方法の一例を挙げるならば、以下のとおりである。
(i)以下に示すモル比で表される組成の反応混合物となるように、シリカ源、アルミナ源、アルカリ源、及び水を混合し、
SiO2/Al2O3=40〜200、特に44〜200
Na2O/SiO2=0.22〜0.4、特に0.24〜0.35
H2O/SiO2=10〜50、特に15〜25
(ii)SiO2/Al2O3比が8〜30であり、かつ平均粒子径が150nm以上、特に150〜1000nm、とりわけ200〜600nmである、有機化合物を含まないベータ型ゼオライトを種結晶として用い、これを、前記反応混合物中のシリカ成分に対して0.1〜20質量%の割合で該反応混合物に添加し、
(iii)前記種結晶が添加された前記反応混合物を100〜200℃、特に120〜180℃で密閉加熱する。
【0017】
(ロ)のベータ型ゼオライトは合成によって得てもよく、あるいは市販品を用いてもよい。(ロ)のベータ型ゼオライトを合成するには、例えば水酸化テトラエチルアンモニウム(有機構造規定剤)及び水酸化ナトリウムを含む水溶液に、コロイダルシリカ及び硫酸アルミニウムの水溶液を添加して混合し、オートクレーブ中で100〜200℃の加熱下に1〜10日にわたり反応を行うことで得られる。このようにして得られたベータ型ゼオライトには、その細孔中に水酸化テトラエチルアンモニウムが残存しているので、焼成によってこれを除去する。焼成は、大気雰囲気中で、500〜600℃の加熱下に1〜10時間にわたって行うことができる。
【0018】
原料ベータ型ゼオライトのイオン交換には、アンモニウム化合物が用いられ、特に硝酸アンモニウム、塩化アンモニウム、酢酸アンモニウム、硫酸アンモニウムを用いることが好ましい。硝酸アンモニウム、塩化アンモニウム等のアンモニウム化合物によってイオン交換を行う場合、原料ベータ型ゼオライト10gに対して、アンモニウムイオンの濃度が0.1〜10mol/Lである水溶液を、100〜1000mL、特に400〜600mL添加することが好ましい。イオン交換は、アンモニウムイオンを含む水溶液を加熱した状態下に、又は非加熱の状態下に行うことができる。アンモニウムイオンを含む水溶液を加熱する場合、加熱温度は40〜100℃、特に70〜90℃とすることが好ましい。原料ベータ型ゼオライトを、アンモニウムイオンを含む水溶液に分散させて分散液となし、この状態を所定時間保持してイオン交換を行う。保持時間は1〜48時間、特に12〜24時間とすることが好ましい。分散液は静置状態としてもよく、あるいは撹拌状態としてもよい。
【0019】
前記分散液を所定時間保持したら、該分散液を濾過し、原料ベータ型ゼオライトを分離し、水洗を行う。必要に応じ、前記のイオン交換処理と水洗との組み合わせを複数回行ってもよい。このようにしてイオン交換処理を行った後、原料ベータ型ゼオライトを乾燥させて、アンモニウム型のベータ型ゼオライトを得る。このアンモニウム型のベータ型ゼオライトは、それよってアルカリ金属イオンの含有量が極めて低減したものとなる。
【0020】
(2)イオン交換された原料ベータ型ゼオライトを水蒸気に曝露する工程
アンモニウム型の原料ベータ型ゼオライトを水蒸気に曝露するには、例えば、水蒸気雰囲気下に原料ベータ型ゼオライトを静置したり、水蒸気流中に原料ベータ型ゼオライトを配置したりすればよい。具体的には、図1に示す装置を用いて、原料ベータ型ゼオライトを水蒸気に曝露することができる。同図に示す装置10は、原料ベータ型ゼオライトが保持された保持管11を有している。保持管11の両端は開口している。下方の端部11aは大気に開放されている。保持管11の上方の端部11bは、水蒸気の流入口となっており、水蒸気の供給源12及び不活性ガスの供給源13と接続している。水蒸気の供給源12は、上方の端部が開口した有底筒体12aからなる。この筒体12a内には不活性ガスのバブリング管12bの一方の端部が挿入されている。バブリング管12bの他方の端部は、不活性ガスの供給源(図示せず)に接続されている。更に、この筒体12a内には水14が入れられている。水面の高さは、有底筒体12a内に挿入されているバブリング管12bの端部の位置よりも高くなっている。保持管11の周囲には加熱手段15が設置されている。加熱手段15は、保持管11内に保持された原料ベータ型ゼオライト及び保持管11内を流通する水蒸気の加熱が可能になっている。不活性ガスの供給源13からアルゴン等の不活性ガスを供給しつつ、水蒸気の供給源12におけるバブリング管12bを通じて不活性ガスをバブリングすることで、所定量の水蒸気が保持管11内に供給される。水蒸気の供給量は、不活性ガスの供給源13及び水蒸気の供給源12における不活性ガスの供給量のバランスで決定される。保持管11内に供給された水蒸気は、原料ベータ型ゼオライトとともに加熱手段15によって加熱される。そして、原料ベータ型ゼオライトは、所定温度に加熱された水蒸気に曝露される。この曝露によって、原料ベータ型ゼオライトを構成するアルミニウム原子が結晶格子内の所定のサイトから脱離し、脱離したサイトにケイ素原子がマイグレーションしてくると考えられる。しかし、水蒸気に曝露した時点では、原料ベータ型ゼオライトにおけるSi/Al比には変化は生じていない。また、原料ベータ型ゼオライトが水蒸気に曝露されることによって、該ゼオライトは、アンモニウム型からプロトン型に変換される。
【0021】
原料ベータ型ゼオライトの曝露に用いられる水蒸気の温度は、150〜1000℃、特に600〜900℃とすることが、ゼオライトの結晶構造の破壊を抑制しつつ、アルミニウムの脱離を促進し得る点から好ましい。同様の理由によって、水蒸気の曝露時間は、水蒸気の温度は上述の範囲内である場合には、1〜48時間、更に1〜24時間、特に12〜24時間であることが好ましい。原料ベータ型ゼオライトと水蒸気とが接触する時点における水蒸気の圧力(分圧)は、保持管11内の下方の端部が開放になっていることから大気圧又はそれ以下になっている。好ましい水蒸気の分圧は1〜101.3kPaである。
【0022】
(3)水蒸気に曝露された原料ベータ型ゼオライトの酸処理工程
水蒸気に曝露された原料ベータ型ゼオライトは、酸処理に付され、それによってベータ型ゼオライトからの脱アルミニウムが生じる。酸処理に用いられる酸としては、各種の鉱酸を用いることが好ましい。例えば硝酸、硫酸及び塩酸などを用いることができる。酸処理を行うときの酸の濃度が高いほど、脱アルミニウム化が進行してベータ型ゼオライトのSi/Al比が高くなる。したがって、所望のSi/Al比を有するベータ型ゼオライトを得るためには、酸の濃度を調整することが簡便である。この観点から、酸の濃度は、使用する酸の種類により異なるが、多くの場合、0.1〜100質量%、特に0.1〜60質量%であることが好ましい。例えば、鉱酸として硝酸を用いる場合、硝酸濃度は、0.1〜70質量%、特に0.5〜5質量%であることが好ましい。なお、酸の濃度が高ければ脱アルミニウム化が進行することは、上述のとおりであるところ、それに伴いゼオライトの結晶構造の破壊が起こりやすい。特に原料としてOSDAフリーベータ型ゼオライトを用いた場合には、結晶構造の破壊が起こりやすい。しかし本発明においては、酸処理に先立ち、上述の水蒸気曝露処理を行っていることに起因して、OSDAフリーベータ型ゼオライトを原料として用い、高濃度の酸で処理を行った場合であっても、ゼオライトの結晶構造の破壊が起こりにくくなっている。
【0023】
酸処理における酸の量は、原料ベータ型ゼオライト1g当たり、上述の濃度の酸を10〜500mL、特に100〜200mL用いることが、効率的な脱アルミニウム化が生じる点から好ましい。酸処理は、加熱下に行ってもよく、あるいは非加熱下に行ってもよい。加熱下に酸処理を行う場合、酸の温度は40〜100℃、特に70〜90℃に設定することが、効率的な脱アルミニウム化の点から好ましい。また、酸処理を加熱下に行う場合には、酸を環流させた状態にしてもよい。酸処理の時間は、酸の濃度及び温度が上述した範囲である場合、1〜24時間、特に2〜12時間とすることが、ゼオライトの結晶構造の破壊を抑制しつつ、効率的な脱アルミニウム化を行う点から好ましい。
【0024】
酸処理が完了したら固液分離を行い、濾別されたベータ型ゼオライトを1回又は複数回水洗し、その後乾燥させる。このようにして、原料ベータ型ゼオライトよりもSi/Al比が高められたベータ型ゼオライトが得られる。このベータ型ゼオライトは、先に述べたとおりプロトン型のものに変換されている。
【0025】
このようにしてSi/Al比が高められたベータ型ゼオライトが得られる。このベータ型ゼオライトにおけるSi/Al比は、5以上、好ましくは15以上、更に好ましくは15〜200、一層好ましくは40〜100という高い値になっている。このような高いSi/Al比でありながらも、本製造方法で得られたベータ型ゼオライトは、該ゼオライトの結晶構造が維持されたものになっている。
【0026】
本製造方法で得られたベータ型ゼオライトは、固体酸触媒や吸着剤として有望であり、例えば石油化学工業における長鎖炭化水素(例えばヘキサン)のクラッキング触媒、ガソリンエンジン及びディーゼルエンジン等の各種内燃機関の排気ガス浄化用ハイドロカーボントラップとして特に有望なものである。
【実施例】
【0027】
以下、実施例により本発明を更に詳細に説明する。しかしながら本発明の範囲は、かかる実施例に制限されない。特に断らない限り、「%」は「質量%」を意味する。
【0028】
〔実施例1〕
(1)種結晶の合成
水酸化テトラエチルアンモニウムを有機SDAとして用い、アルミン酸ナトリウムをアルミナ源、微粉状シリカ(Mizukasil P707)をシリカ源とする従来公知の方法により、165℃、96時間、攪拌加熱を行って、SiO2/Al2O3比が24.0のベータ型ゼオライトを合成した。これを電気炉中で空気を流通しながら550℃で10時間焼成して、有機物を含まない結晶を製造した。この結晶を走査型電子顕微鏡により観察した結果、平均粒子径は280nmであった。この有機物を含まないベータ型ゼオライトの結晶を、種結晶として使用した。
【0029】
(2)OSDAフリーベータ型ゼオライトの合成
純水13.9gに、アルミン酸ナトリウム0.235gと、36%水酸化ナトリウム1.828gを溶解した。微粉状シリカ(Cab−O−sil、M−5)2.024gと、前記の種結晶0.202gを混合したものを、少しずつ前記の水溶液に添加して攪拌混合し、反応混合物を得た。この反応混合物におけるSiO2/Al2O3比は70、Na2O/SiO2比は0.3、H2O/SiO2比は20であった。この反応混合物を60mLのステンレス製密閉容器に入れて、熟成及び攪拌することなしに140℃で34時間、自生圧力下で静置加熱した。密閉容器を冷却後、生成物を濾過、温水洗浄して白色粉末を得た。この生成物についてX線回折測定を行ったところ、不純物を含まないベータ型ゼオライトであることが確認された。組成分析の結果、そのSi/Alは6.4であった。
【0030】
(3)イオン交換処理
得られたOSDAフリーベータ型ゼオライトを原料として用い、これを硝酸アンモニウム水溶液中に分散させた。OSDAフリーベータ型ゼオライトと硝酸アンモニウムと水との質量比は1:2:50とした。この分散液を80℃に加熱した状態下に24時間にわたって静置してイオン交換を行った。その後、濾過を行い、ベータ型ゼオライトを濾別した。イオン交換及び濾過の操作をもう一度繰り返した後、水洗して80℃で乾燥して、アンモニウム型のベータ型ゼオライトを得た。
【0031】
(4)水蒸気による曝露
アンモニウム型のベータ型ゼオライトを図1に示す装置に充填した。充填量は1gとした。同図に示す加熱手段15によって700℃に加熱した状態下に、アルゴン−水蒸気の混合ガスを24時間にわたって連続して流通させた。水蒸気の分圧は12.2kPaとした。水蒸気による曝露で、ベータ型ゼオライトはアンモニウム型からプロトン型に変換された。
【0032】
(5)酸処理
水蒸気曝露後のベータ型ゼオライトを、0.1mol/Lの硝酸水溶液で酸処理した。硝酸水溶液の温度は80℃とした。硝酸水溶液は、ベータ型ゼオライト1gに対して10mL添加した。マグネチックスターラーで液を撹拌しながら2時間にわたって処理を行った。このようにして、目的とするベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図2に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0033】
〔実施例2ないし5〕
実施例1において、酸処理に用いた硝酸水溶液の濃度を0.5mol/L(実施例2)、1.0mol/L(実施例3)、2.0mol/L(実施例4)及び8.0mol/L(実施例5)とした。これ以外は実施例1と同様にして、Si/Al比が高められたベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図2に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0034】
〔実施例6〕
(1)OSDAベータ型ゼオライトの合成
水酸化テトラエチルアンモニウム(OSDA)及び水酸化ナトリウムを含む水溶液を室温下に撹拌し、そこにコロイダルシリカを添加した。コロイダルシリカとしては、Ludox HS-40(シリカ分40%)を用いた。コロイダルシリカを添加してから30分間にわたり撹拌を行った後、硫酸アルミニウム水溶液を添加し、更に30分間にわたり撹拌を行い、ゲルを得た。このゲルの組成は、SiO21モルに対して、Al2O3が0.033モル、水酸化ナトリウムが0.24モル、水酸化テトラエチルアンモニウムが0.50モル、水が20モルであった。このゲルをオートクレーブ中に入れて、150℃に加熱した状態下に7日間にわたり反応を行った。このようにしてベータ型ゼオライトを得た。このゼオライトを、大気雰囲気下に550℃で6時間にわたり加熱して、OSDAである水酸化テトラエチルアンモニウムを分解除去した。この生成物についてX線回折測定を行ったところ、不純物を含まないベータ型ゼオライトであることが確認された。組成分析の結果、そのSi/Alは13.1であった。
【0035】
(2)イオン交換、水蒸気曝露及び酸処理
実施例1と同様の条件で、イオン交換、水蒸気曝露及び酸処理を行った。このようにして、目的とするベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図3に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0036】
〔実施例7ないし10〕
実施例6において、酸処理に用いた硝酸水溶液の濃度を0.5mol/L(実施例7)、1.0mol/L(実施例8)、2.0mol/L(実施例9)及び8.0mol/L(実施例10)とした。これ以外は実施例6と同様にして、Si/Al比が高められたベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図3に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0037】
〔比較例1〕
実施例1において、イオン交換及び水蒸気曝露まで行い、かつ酸処理を行わずにベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図4に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0038】
〔比較例2〕
実施例1において、イオン交換及び水蒸気曝露は行わず、酸処理のみを行ってベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図4に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0039】
図2及び図3に示す結果から明らかなとおり、本発明の方法によって得られたベータ型ゼオライトは、該ゼオライトの結晶構造を維持しつつ、Si/Al比が高められたものであることが判る。これに対して、OSDAフリーベータ型ゼオライトを原料として用い、かつ酸処理を行わずに得られた比較例1のベータ型ゼオライトは、該ゼオライトの結晶構造は維持しているものの、Si/Al比の向上はみられなかった。また、OSDAフリーベータ型ゼオライトを原料として用い、かつイオン交換及び水蒸気曝露を行わず、酸処理のみを行って得られた比較例2のベータ型ゼオライトは、Si/Al比は高められているものの、該ゼオライトの結晶構造が破壊されていることが判る。
【0040】
〔実施例11及び12〕
実施例2及び7で得られたベータ型ゼオライトについて、ヘキサンのクラッキング反応における触媒活性を以下の手順で評価した。
触媒活性の評価に先立ち、粉末状のベータ型ゼオライトを成型・整粒した。具体的には、ベータ型ゼオライト粉末1〜2gを、内径20mmの錠剤成型器に詰めたのち、油圧プレスにて0.4MPaで加圧成型し、径が20mmのペレットを得た。このペレットをふるいの上で適度に粉砕し、500〜600μmに整粒してこれを触媒として用いた。
【0041】
本実施例における触媒反応は固定床常圧流通反応装置を用いて行った。装置の概略図を図5に示す。反応物であるヘキサンはシリンジポンプを用いてシリンジから供給し、キャリアガスである窒素(1%)−アルゴン混合ガスに導入した。シリンジポンプから供給されたヘキサンは、あらかじめ加熱した気化室に導入されるため蒸発して気体となり、この気体をキャリアガスに同伴した。反応装置のガスラインには内径2mmのステンレスパイプを用いて、ヒーターで外側から適温に加熱することで気化したヘキサンの凝縮を防いだ。反応管は内径8mmの石英管を用い、これに、先に整粒したベータ型ゼオライトト触媒を100mg詰め、石英ウールで触媒層を反応管中央部に保持した。反応前処理として、空気流通下で約7℃/minの昇温速度で650℃まで昇温し、この雰囲気で1時間保持した。その後、ヘリウム流通に切り替えてから5℃/minで450℃まで反応管温度を下げた。450℃で安定したのを確認してから、ヘキサンを同伴したメタン−ヘリウム混合ガスを触媒層に供給し、触媒反応を開始した。ヘキサンの分圧は5.0kPaであった。反応開始から5分経過後に六方バルブを切り替えて、サンプリングループに溜めた反応後の生成物をガスクロマトグラフへ導入し、キャピラリーカラムで分離後、水素炎検出器(FID)にて各生成物・未反応物の定性・定量を行った。所定時間(70分)経過後、触媒層へのヘキサンの供給をやめ、ヘリウム流通に切り替えた。その後で、1〜2℃/minで500℃まで昇温して温度が安定したところで、再びヘキサンを供給し、触媒反応を行った。同様の操作を550及び600℃でも続けて行った。触媒反応時のW/Fはいずれの反応温度でも、19.8g−catalyst h(mol−hexane)-1とした。600℃での触媒反応を停止した後には、ヘリウム流通下で自然放冷した。結果を、以下の表1に示す。各生成物への選択率はカーボンベース(炭素原子換算)で求めた。プロピレン(C3=)収率は、「転化率×プロピレン(C3=)への選択率」から求めた。なお、反応温度は、固定床常圧流通反応装置の石英製反応管を外側から加熱するように設置したヒーターと、反応管との間で測定したものである。
【0042】
【表1】

【0043】
表1に示す結果から明らかなように、実施例2及び7で得られたベータ型ゼオライトを触媒として用い、ヘキサンのクラッキングを行うと、化学原料として有用な物質であるC3=(プロピレン)が、高収率で生成することが判る。また、ベータ型ゼオライトの失活が観察されないことも判る。
【符号の説明】
【0044】
10 水蒸気曝露装置
11 保持管
12 水蒸気の供給源
13 不活性ガスの供給源
14 水
15 加熱手段
【技術分野】
【0001】
本発明は、原料としてのベータ型ゼオライトから、Si/Al比が高められたベータ型ゼオライトを製造する方法に関する。
【背景技術】
【0002】
ベータ型ゼオライトは、固体酸触媒や吸着剤として有用なものであり、石油化学工業における触媒として、また内燃機関の排気ガス浄化用ハイドロカーボントラップとして、現在世界中で多量に使用されている。ベータ型ゼオライトの合成法は種々提案されている。一般的な方法はテトラエチルアンモニウムイオンを含む化合物を構造規定剤(以下「有機SDA」と略称する。)として用いる方法である。そのような方法は例えば以下の特許文献1に記載されている。しかしながら、テトラエチルアンモニウムイオンを含む化合物は高価である上に、ベータ型ゼオライトの結晶化終了後は過剰分のほとんどが分解してしまい、結晶に取りこまれた分も分解以外の方法で除去できないため、回収して再利用することは不可能である。そのために、この方法により製造したベータ型ゼオライトは高価である。更に、結晶中にテトラエチルアンモニウムイオンが取り込まれるため、吸着剤や触媒として使用する際には焼成により除去する必要がある。その際の排ガスは環境汚染の原因となり、また、合成母液の無害化処理のためにも多くの薬剤を必要とする。このように、テトラエチルアンモニウムイオンを用いるベータ型ゼオライトの合成方法は高価であるばかりでなく、環境負荷の大きい製造方法であることから、有機SDAを用いない製造方法の実現が望まれていた。
【0003】
このような状況の中で、最近、有機SDAを使用しないベータ型ゼオライトの合成方法が特許文献2において提案された。同文献においては、特定の組成の反応混合物となるように、シリカ源、アルミナ源、アルカリ源、及び水を混合し;SiO2/Al2O3比が8〜30であり、かつ平均粒子径が150nm以上である有機化合物を含まないベータ型ゼオライトを種結晶として用い、これを、前記反応混合物中のシリカ成分に対して0.1〜20質量%の割合で該反応混合物に添加し;前記種結晶が添加された前記反応混合物を100〜200℃で密閉加熱することで、有機SDAを使用せずにベータ型ゼオライトを合成している。
【0004】
ところで、ベータ型ゼオライトを、石油化学工業における触媒として用いる場合や、内燃機関の排気ガス浄化用ハイドロカーボントラップとして用いる場合には、そのSi/Al比を高めることが、性能向上の観点から有利である。ベータ型ゼオライトにおけるSi/Al比を高めるための手法としては、例えば特許文献3に記載されているとおり、水蒸気処理及び酸処理をこの順で行う方法が知られている。
【0005】
【特許文献1】米国特許第3,308,069号明細書
【特許文献2】国際公開2011/013560号パンフレット
【特許文献3】特開2010−215434号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかし、原料として用いるベータ型ゼオライトの種類によっては、Si/Al比を高めるための手法として、上述の処理を行った場合、ゼオライトの結晶構造が破壊されてしまう場合がある。
【0007】
本発明の課題は、前述した従来技術が有する種々の欠点を解消し得るベータ型ゼオライトの製造方法を提供することにある。
【課題を解決するための手段】
【0008】
本発明は、原料ベータ型ゼオライトをイオン交換によってアンモニウム型となし、次いで該ベータ型ゼオライトを水蒸気に曝露し、曝露後の該ベータ型ゼオライトを酸処理に付して、Si/Al比が高められたベータ型ゼオライトを得ることを特徴とするベータ型ゼオライトの製造方法を提供することによって、前記の課題を解決したものである。
【発明の効果】
【0009】
本発明によれば、ゼオライトの結晶構造を破壊することなく、Si/Al比の高いベータ型ゼオライトを容易に製造することができる。
【図面の簡単な説明】
【0010】
【図1】図1は、ベータ型ゼオライトの水蒸気曝露に用いられる装置を示す模式図である。
【図2】図2は、有機構造規定剤を用いずに合成されたベータ型ゼオライトを原料とし、実施例1ないし5で得られたベータ型ゼオライトのX線回折図である。
【図3】図3は、有機構造規定剤を用いて合成されたベータ型ゼオライトを原料とし、実施例6ないし10で得られたベータ型ゼオライトのX線回折図である。
【図4】図4は、比較例1及び2で得られたベータ型ゼオライトのX線回折図である。
【図5】図5は、実施例2及び7で得られたベータ型ゼオライトの触媒活性を評価するための装置の概略図である。
【発明を実施するための形態】
【0011】
本発明の製造方法は、(1)原料ベータ型ゼオライトのイオン交換処理工程、(2)イオン交換された原料ベータ型ゼオライトを水蒸気に曝露する工程、及び(3)水蒸気に曝露された原料ベータ型ゼオライトの酸処理工程の3つの工程を含んでいる。以下、これらの工程についてそれぞれ説明する。
【0012】
(1)原料ベータ型ゼオライトのイオン交換処理工程
原料ベータ型ゼオライトは、一般にナトリウム等のアルカリ金属を含んでいる。アルカリ金属を含むベータ型ゼオライトは、これを石油化学工業における触媒として用いる場合や、内燃機関の排気ガス浄化用ハイドロカーボントラップとして用いる場合に、所期の特性を発揮しにくいので、イオン交換によって除去し、アンモニウム型のベータ型ゼオライトとなす。
【0013】
イオン交換処理に付す原料ベータ型ゼオライトとしては、例えばSi/Al比が4〜100、好ましくは4〜8、更に好ましくは5〜7である低Si/Al比のものを用いる。低Si/Al比の原料ベータ型ゼオライトを用いることで、本発明の製造方法の効果が顕著なものとなる。
【0014】
原料ベータ型ゼオライトとしては、(イ)有機SDAを用いずに合成されたもの(以下「OSDAフリーベータ型ゼオライト」とも言う。)、及び(ロ)有機SDAを用いて合成されたもの(以下「OSDAベータ型ゼオライト」とも言う。)の双方を用いることができる。これら(イ)及び(ロ)のうち、(イ)のベータ型ゼオライトは、従来の手法によってSi/Alを高めると、ゼオライトの結晶構造が破壊されやすいことが、本発明者らの検討の結果判明した。しかし、本発明の方法によって(イ)のベータ型ゼオライトを処理すると、結晶構造の破壊を極力抑えた上で、Si/Alを高めることが可能となった。したがって、(イ)及び(ロ)のうち、(イ)のベータ型ゼオライトを原料として用いると、本発明の特徴が一層際だったものとなる。また、(イ)のベータ型ゼオライトを用いることは、有機SDAを用いないという点で、経済性の観点及び環境負荷の観点からも有利である。
【0015】
(イ)のベータ型ゼオライトを用いる場合、該ベータ型ゼオライトの合成方法としては、例えば国際公開2011/013560号パンフレットに記載の方法を採用することができる。また、中国特許出願公開第101249968A号明細書に記載の方法も採用することができる。更に、Chemistry of Materials, Vol.20, No.14, p.4533-4535 (2008)に記載の方法を採用することもできる。
【0016】
(イ)のベータ型ゼオライトの合成方法の一例を挙げるならば、以下のとおりである。
(i)以下に示すモル比で表される組成の反応混合物となるように、シリカ源、アルミナ源、アルカリ源、及び水を混合し、
SiO2/Al2O3=40〜200、特に44〜200
Na2O/SiO2=0.22〜0.4、特に0.24〜0.35
H2O/SiO2=10〜50、特に15〜25
(ii)SiO2/Al2O3比が8〜30であり、かつ平均粒子径が150nm以上、特に150〜1000nm、とりわけ200〜600nmである、有機化合物を含まないベータ型ゼオライトを種結晶として用い、これを、前記反応混合物中のシリカ成分に対して0.1〜20質量%の割合で該反応混合物に添加し、
(iii)前記種結晶が添加された前記反応混合物を100〜200℃、特に120〜180℃で密閉加熱する。
【0017】
(ロ)のベータ型ゼオライトは合成によって得てもよく、あるいは市販品を用いてもよい。(ロ)のベータ型ゼオライトを合成するには、例えば水酸化テトラエチルアンモニウム(有機構造規定剤)及び水酸化ナトリウムを含む水溶液に、コロイダルシリカ及び硫酸アルミニウムの水溶液を添加して混合し、オートクレーブ中で100〜200℃の加熱下に1〜10日にわたり反応を行うことで得られる。このようにして得られたベータ型ゼオライトには、その細孔中に水酸化テトラエチルアンモニウムが残存しているので、焼成によってこれを除去する。焼成は、大気雰囲気中で、500〜600℃の加熱下に1〜10時間にわたって行うことができる。
【0018】
原料ベータ型ゼオライトのイオン交換には、アンモニウム化合物が用いられ、特に硝酸アンモニウム、塩化アンモニウム、酢酸アンモニウム、硫酸アンモニウムを用いることが好ましい。硝酸アンモニウム、塩化アンモニウム等のアンモニウム化合物によってイオン交換を行う場合、原料ベータ型ゼオライト10gに対して、アンモニウムイオンの濃度が0.1〜10mol/Lである水溶液を、100〜1000mL、特に400〜600mL添加することが好ましい。イオン交換は、アンモニウムイオンを含む水溶液を加熱した状態下に、又は非加熱の状態下に行うことができる。アンモニウムイオンを含む水溶液を加熱する場合、加熱温度は40〜100℃、特に70〜90℃とすることが好ましい。原料ベータ型ゼオライトを、アンモニウムイオンを含む水溶液に分散させて分散液となし、この状態を所定時間保持してイオン交換を行う。保持時間は1〜48時間、特に12〜24時間とすることが好ましい。分散液は静置状態としてもよく、あるいは撹拌状態としてもよい。
【0019】
前記分散液を所定時間保持したら、該分散液を濾過し、原料ベータ型ゼオライトを分離し、水洗を行う。必要に応じ、前記のイオン交換処理と水洗との組み合わせを複数回行ってもよい。このようにしてイオン交換処理を行った後、原料ベータ型ゼオライトを乾燥させて、アンモニウム型のベータ型ゼオライトを得る。このアンモニウム型のベータ型ゼオライトは、それよってアルカリ金属イオンの含有量が極めて低減したものとなる。
【0020】
(2)イオン交換された原料ベータ型ゼオライトを水蒸気に曝露する工程
アンモニウム型の原料ベータ型ゼオライトを水蒸気に曝露するには、例えば、水蒸気雰囲気下に原料ベータ型ゼオライトを静置したり、水蒸気流中に原料ベータ型ゼオライトを配置したりすればよい。具体的には、図1に示す装置を用いて、原料ベータ型ゼオライトを水蒸気に曝露することができる。同図に示す装置10は、原料ベータ型ゼオライトが保持された保持管11を有している。保持管11の両端は開口している。下方の端部11aは大気に開放されている。保持管11の上方の端部11bは、水蒸気の流入口となっており、水蒸気の供給源12及び不活性ガスの供給源13と接続している。水蒸気の供給源12は、上方の端部が開口した有底筒体12aからなる。この筒体12a内には不活性ガスのバブリング管12bの一方の端部が挿入されている。バブリング管12bの他方の端部は、不活性ガスの供給源(図示せず)に接続されている。更に、この筒体12a内には水14が入れられている。水面の高さは、有底筒体12a内に挿入されているバブリング管12bの端部の位置よりも高くなっている。保持管11の周囲には加熱手段15が設置されている。加熱手段15は、保持管11内に保持された原料ベータ型ゼオライト及び保持管11内を流通する水蒸気の加熱が可能になっている。不活性ガスの供給源13からアルゴン等の不活性ガスを供給しつつ、水蒸気の供給源12におけるバブリング管12bを通じて不活性ガスをバブリングすることで、所定量の水蒸気が保持管11内に供給される。水蒸気の供給量は、不活性ガスの供給源13及び水蒸気の供給源12における不活性ガスの供給量のバランスで決定される。保持管11内に供給された水蒸気は、原料ベータ型ゼオライトとともに加熱手段15によって加熱される。そして、原料ベータ型ゼオライトは、所定温度に加熱された水蒸気に曝露される。この曝露によって、原料ベータ型ゼオライトを構成するアルミニウム原子が結晶格子内の所定のサイトから脱離し、脱離したサイトにケイ素原子がマイグレーションしてくると考えられる。しかし、水蒸気に曝露した時点では、原料ベータ型ゼオライトにおけるSi/Al比には変化は生じていない。また、原料ベータ型ゼオライトが水蒸気に曝露されることによって、該ゼオライトは、アンモニウム型からプロトン型に変換される。
【0021】
原料ベータ型ゼオライトの曝露に用いられる水蒸気の温度は、150〜1000℃、特に600〜900℃とすることが、ゼオライトの結晶構造の破壊を抑制しつつ、アルミニウムの脱離を促進し得る点から好ましい。同様の理由によって、水蒸気の曝露時間は、水蒸気の温度は上述の範囲内である場合には、1〜48時間、更に1〜24時間、特に12〜24時間であることが好ましい。原料ベータ型ゼオライトと水蒸気とが接触する時点における水蒸気の圧力(分圧)は、保持管11内の下方の端部が開放になっていることから大気圧又はそれ以下になっている。好ましい水蒸気の分圧は1〜101.3kPaである。
【0022】
(3)水蒸気に曝露された原料ベータ型ゼオライトの酸処理工程
水蒸気に曝露された原料ベータ型ゼオライトは、酸処理に付され、それによってベータ型ゼオライトからの脱アルミニウムが生じる。酸処理に用いられる酸としては、各種の鉱酸を用いることが好ましい。例えば硝酸、硫酸及び塩酸などを用いることができる。酸処理を行うときの酸の濃度が高いほど、脱アルミニウム化が進行してベータ型ゼオライトのSi/Al比が高くなる。したがって、所望のSi/Al比を有するベータ型ゼオライトを得るためには、酸の濃度を調整することが簡便である。この観点から、酸の濃度は、使用する酸の種類により異なるが、多くの場合、0.1〜100質量%、特に0.1〜60質量%であることが好ましい。例えば、鉱酸として硝酸を用いる場合、硝酸濃度は、0.1〜70質量%、特に0.5〜5質量%であることが好ましい。なお、酸の濃度が高ければ脱アルミニウム化が進行することは、上述のとおりであるところ、それに伴いゼオライトの結晶構造の破壊が起こりやすい。特に原料としてOSDAフリーベータ型ゼオライトを用いた場合には、結晶構造の破壊が起こりやすい。しかし本発明においては、酸処理に先立ち、上述の水蒸気曝露処理を行っていることに起因して、OSDAフリーベータ型ゼオライトを原料として用い、高濃度の酸で処理を行った場合であっても、ゼオライトの結晶構造の破壊が起こりにくくなっている。
【0023】
酸処理における酸の量は、原料ベータ型ゼオライト1g当たり、上述の濃度の酸を10〜500mL、特に100〜200mL用いることが、効率的な脱アルミニウム化が生じる点から好ましい。酸処理は、加熱下に行ってもよく、あるいは非加熱下に行ってもよい。加熱下に酸処理を行う場合、酸の温度は40〜100℃、特に70〜90℃に設定することが、効率的な脱アルミニウム化の点から好ましい。また、酸処理を加熱下に行う場合には、酸を環流させた状態にしてもよい。酸処理の時間は、酸の濃度及び温度が上述した範囲である場合、1〜24時間、特に2〜12時間とすることが、ゼオライトの結晶構造の破壊を抑制しつつ、効率的な脱アルミニウム化を行う点から好ましい。
【0024】
酸処理が完了したら固液分離を行い、濾別されたベータ型ゼオライトを1回又は複数回水洗し、その後乾燥させる。このようにして、原料ベータ型ゼオライトよりもSi/Al比が高められたベータ型ゼオライトが得られる。このベータ型ゼオライトは、先に述べたとおりプロトン型のものに変換されている。
【0025】
このようにしてSi/Al比が高められたベータ型ゼオライトが得られる。このベータ型ゼオライトにおけるSi/Al比は、5以上、好ましくは15以上、更に好ましくは15〜200、一層好ましくは40〜100という高い値になっている。このような高いSi/Al比でありながらも、本製造方法で得られたベータ型ゼオライトは、該ゼオライトの結晶構造が維持されたものになっている。
【0026】
本製造方法で得られたベータ型ゼオライトは、固体酸触媒や吸着剤として有望であり、例えば石油化学工業における長鎖炭化水素(例えばヘキサン)のクラッキング触媒、ガソリンエンジン及びディーゼルエンジン等の各種内燃機関の排気ガス浄化用ハイドロカーボントラップとして特に有望なものである。
【実施例】
【0027】
以下、実施例により本発明を更に詳細に説明する。しかしながら本発明の範囲は、かかる実施例に制限されない。特に断らない限り、「%」は「質量%」を意味する。
【0028】
〔実施例1〕
(1)種結晶の合成
水酸化テトラエチルアンモニウムを有機SDAとして用い、アルミン酸ナトリウムをアルミナ源、微粉状シリカ(Mizukasil P707)をシリカ源とする従来公知の方法により、165℃、96時間、攪拌加熱を行って、SiO2/Al2O3比が24.0のベータ型ゼオライトを合成した。これを電気炉中で空気を流通しながら550℃で10時間焼成して、有機物を含まない結晶を製造した。この結晶を走査型電子顕微鏡により観察した結果、平均粒子径は280nmであった。この有機物を含まないベータ型ゼオライトの結晶を、種結晶として使用した。
【0029】
(2)OSDAフリーベータ型ゼオライトの合成
純水13.9gに、アルミン酸ナトリウム0.235gと、36%水酸化ナトリウム1.828gを溶解した。微粉状シリカ(Cab−O−sil、M−5)2.024gと、前記の種結晶0.202gを混合したものを、少しずつ前記の水溶液に添加して攪拌混合し、反応混合物を得た。この反応混合物におけるSiO2/Al2O3比は70、Na2O/SiO2比は0.3、H2O/SiO2比は20であった。この反応混合物を60mLのステンレス製密閉容器に入れて、熟成及び攪拌することなしに140℃で34時間、自生圧力下で静置加熱した。密閉容器を冷却後、生成物を濾過、温水洗浄して白色粉末を得た。この生成物についてX線回折測定を行ったところ、不純物を含まないベータ型ゼオライトであることが確認された。組成分析の結果、そのSi/Alは6.4であった。
【0030】
(3)イオン交換処理
得られたOSDAフリーベータ型ゼオライトを原料として用い、これを硝酸アンモニウム水溶液中に分散させた。OSDAフリーベータ型ゼオライトと硝酸アンモニウムと水との質量比は1:2:50とした。この分散液を80℃に加熱した状態下に24時間にわたって静置してイオン交換を行った。その後、濾過を行い、ベータ型ゼオライトを濾別した。イオン交換及び濾過の操作をもう一度繰り返した後、水洗して80℃で乾燥して、アンモニウム型のベータ型ゼオライトを得た。
【0031】
(4)水蒸気による曝露
アンモニウム型のベータ型ゼオライトを図1に示す装置に充填した。充填量は1gとした。同図に示す加熱手段15によって700℃に加熱した状態下に、アルゴン−水蒸気の混合ガスを24時間にわたって連続して流通させた。水蒸気の分圧は12.2kPaとした。水蒸気による曝露で、ベータ型ゼオライトはアンモニウム型からプロトン型に変換された。
【0032】
(5)酸処理
水蒸気曝露後のベータ型ゼオライトを、0.1mol/Lの硝酸水溶液で酸処理した。硝酸水溶液の温度は80℃とした。硝酸水溶液は、ベータ型ゼオライト1gに対して10mL添加した。マグネチックスターラーで液を撹拌しながら2時間にわたって処理を行った。このようにして、目的とするベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図2に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0033】
〔実施例2ないし5〕
実施例1において、酸処理に用いた硝酸水溶液の濃度を0.5mol/L(実施例2)、1.0mol/L(実施例3)、2.0mol/L(実施例4)及び8.0mol/L(実施例5)とした。これ以外は実施例1と同様にして、Si/Al比が高められたベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図2に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0034】
〔実施例6〕
(1)OSDAベータ型ゼオライトの合成
水酸化テトラエチルアンモニウム(OSDA)及び水酸化ナトリウムを含む水溶液を室温下に撹拌し、そこにコロイダルシリカを添加した。コロイダルシリカとしては、Ludox HS-40(シリカ分40%)を用いた。コロイダルシリカを添加してから30分間にわたり撹拌を行った後、硫酸アルミニウム水溶液を添加し、更に30分間にわたり撹拌を行い、ゲルを得た。このゲルの組成は、SiO21モルに対して、Al2O3が0.033モル、水酸化ナトリウムが0.24モル、水酸化テトラエチルアンモニウムが0.50モル、水が20モルであった。このゲルをオートクレーブ中に入れて、150℃に加熱した状態下に7日間にわたり反応を行った。このようにしてベータ型ゼオライトを得た。このゼオライトを、大気雰囲気下に550℃で6時間にわたり加熱して、OSDAである水酸化テトラエチルアンモニウムを分解除去した。この生成物についてX線回折測定を行ったところ、不純物を含まないベータ型ゼオライトであることが確認された。組成分析の結果、そのSi/Alは13.1であった。
【0035】
(2)イオン交換、水蒸気曝露及び酸処理
実施例1と同様の条件で、イオン交換、水蒸気曝露及び酸処理を行った。このようにして、目的とするベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図3に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0036】
〔実施例7ないし10〕
実施例6において、酸処理に用いた硝酸水溶液の濃度を0.5mol/L(実施例7)、1.0mol/L(実施例8)、2.0mol/L(実施例9)及び8.0mol/L(実施例10)とした。これ以外は実施例6と同様にして、Si/Al比が高められたベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図3に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0037】
〔比較例1〕
実施例1において、イオン交換及び水蒸気曝露まで行い、かつ酸処理を行わずにベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図4に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0038】
〔比較例2〕
実施例1において、イオン交換及び水蒸気曝露は行わず、酸処理のみを行ってベータ型ゼオライトを得た。得られたベータ型ゼオライトのX線回折図を図4に示す。また、元素分析から求めたSi/Al比を同図中に記載した。
【0039】
図2及び図3に示す結果から明らかなとおり、本発明の方法によって得られたベータ型ゼオライトは、該ゼオライトの結晶構造を維持しつつ、Si/Al比が高められたものであることが判る。これに対して、OSDAフリーベータ型ゼオライトを原料として用い、かつ酸処理を行わずに得られた比較例1のベータ型ゼオライトは、該ゼオライトの結晶構造は維持しているものの、Si/Al比の向上はみられなかった。また、OSDAフリーベータ型ゼオライトを原料として用い、かつイオン交換及び水蒸気曝露を行わず、酸処理のみを行って得られた比較例2のベータ型ゼオライトは、Si/Al比は高められているものの、該ゼオライトの結晶構造が破壊されていることが判る。
【0040】
〔実施例11及び12〕
実施例2及び7で得られたベータ型ゼオライトについて、ヘキサンのクラッキング反応における触媒活性を以下の手順で評価した。
触媒活性の評価に先立ち、粉末状のベータ型ゼオライトを成型・整粒した。具体的には、ベータ型ゼオライト粉末1〜2gを、内径20mmの錠剤成型器に詰めたのち、油圧プレスにて0.4MPaで加圧成型し、径が20mmのペレットを得た。このペレットをふるいの上で適度に粉砕し、500〜600μmに整粒してこれを触媒として用いた。
【0041】
本実施例における触媒反応は固定床常圧流通反応装置を用いて行った。装置の概略図を図5に示す。反応物であるヘキサンはシリンジポンプを用いてシリンジから供給し、キャリアガスである窒素(1%)−アルゴン混合ガスに導入した。シリンジポンプから供給されたヘキサンは、あらかじめ加熱した気化室に導入されるため蒸発して気体となり、この気体をキャリアガスに同伴した。反応装置のガスラインには内径2mmのステンレスパイプを用いて、ヒーターで外側から適温に加熱することで気化したヘキサンの凝縮を防いだ。反応管は内径8mmの石英管を用い、これに、先に整粒したベータ型ゼオライトト触媒を100mg詰め、石英ウールで触媒層を反応管中央部に保持した。反応前処理として、空気流通下で約7℃/minの昇温速度で650℃まで昇温し、この雰囲気で1時間保持した。その後、ヘリウム流通に切り替えてから5℃/minで450℃まで反応管温度を下げた。450℃で安定したのを確認してから、ヘキサンを同伴したメタン−ヘリウム混合ガスを触媒層に供給し、触媒反応を開始した。ヘキサンの分圧は5.0kPaであった。反応開始から5分経過後に六方バルブを切り替えて、サンプリングループに溜めた反応後の生成物をガスクロマトグラフへ導入し、キャピラリーカラムで分離後、水素炎検出器(FID)にて各生成物・未反応物の定性・定量を行った。所定時間(70分)経過後、触媒層へのヘキサンの供給をやめ、ヘリウム流通に切り替えた。その後で、1〜2℃/minで500℃まで昇温して温度が安定したところで、再びヘキサンを供給し、触媒反応を行った。同様の操作を550及び600℃でも続けて行った。触媒反応時のW/Fはいずれの反応温度でも、19.8g−catalyst h(mol−hexane)-1とした。600℃での触媒反応を停止した後には、ヘリウム流通下で自然放冷した。結果を、以下の表1に示す。各生成物への選択率はカーボンベース(炭素原子換算)で求めた。プロピレン(C3=)収率は、「転化率×プロピレン(C3=)への選択率」から求めた。なお、反応温度は、固定床常圧流通反応装置の石英製反応管を外側から加熱するように設置したヒーターと、反応管との間で測定したものである。
【0042】
【表1】

【0043】
表1に示す結果から明らかなように、実施例2及び7で得られたベータ型ゼオライトを触媒として用い、ヘキサンのクラッキングを行うと、化学原料として有用な物質であるC3=(プロピレン)が、高収率で生成することが判る。また、ベータ型ゼオライトの失活が観察されないことも判る。
【符号の説明】
【0044】
10 水蒸気曝露装置
11 保持管
12 水蒸気の供給源
13 不活性ガスの供給源
14 水
15 加熱手段
【特許請求の範囲】
【請求項1】
原料ベータ型ゼオライトをイオン交換によってアンモニウム型となし、次いで該ベータ型ゼオライトを水蒸気に曝露し、曝露後の該ベータ型ゼオライトを酸処理に付して、Si/Al比が高められたベータ型ゼオライトを得ることを特徴とするベータ型ゼオライトの製造方法。
【請求項2】
イオン交換に付される原料ベータ型ゼオライトが、構造規定剤を用いずに合成されたものである請求項1に記載の製造方法。
【請求項3】
イオン交換に付される原料ベータ型ゼオライトが、構造規定剤を用いて合成されたものである請求項1に記載の製造方法。
【請求項4】
イオン交換後の原料ベータ型ゼオライトを、150〜1000℃の水蒸気に、1〜48時間曝露する請求項1ないし3のいずれか一項に記載の製造方法。
【請求項5】
水蒸気に曝露した後の原料ベータ型ゼオライトを、鉱酸を用い、40〜100℃下に1〜24時間にわたり酸処理に付す請求項1ないし4のいずれか一項に記載の製造方法。
【請求項6】
Si/Al比が5以上のベータ型ゼオライトを得る請求項1ないし5のいずれか一項に記載の製造方法。
【請求項1】
原料ベータ型ゼオライトをイオン交換によってアンモニウム型となし、次いで該ベータ型ゼオライトを水蒸気に曝露し、曝露後の該ベータ型ゼオライトを酸処理に付して、Si/Al比が高められたベータ型ゼオライトを得ることを特徴とするベータ型ゼオライトの製造方法。
【請求項2】
イオン交換に付される原料ベータ型ゼオライトが、構造規定剤を用いずに合成されたものである請求項1に記載の製造方法。
【請求項3】
イオン交換に付される原料ベータ型ゼオライトが、構造規定剤を用いて合成されたものである請求項1に記載の製造方法。
【請求項4】
イオン交換後の原料ベータ型ゼオライトを、150〜1000℃の水蒸気に、1〜48時間曝露する請求項1ないし3のいずれか一項に記載の製造方法。
【請求項5】
水蒸気に曝露した後の原料ベータ型ゼオライトを、鉱酸を用い、40〜100℃下に1〜24時間にわたり酸処理に付す請求項1ないし4のいずれか一項に記載の製造方法。
【請求項6】
Si/Al比が5以上のベータ型ゼオライトを得る請求項1ないし5のいずれか一項に記載の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2013−112546(P2013−112546A)
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願番号】特願2011−258328(P2011−258328)
【出願日】平成23年11月25日(2011.11.25)
【出願人】(000230593)日本化学工業株式会社 (296)
【出願人】(504182255)国立大学法人横浜国立大学 (429)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【Fターム(参考)】
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願日】平成23年11月25日(2011.11.25)
【出願人】(000230593)日本化学工業株式会社 (296)
【出願人】(504182255)国立大学法人横浜国立大学 (429)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【Fターム(参考)】
[ Back to top ]

