ポリフェノールの定量法
【課題】過酸化水素がセリウムと反応して結晶性のセリウムペルヒドロキシド(CP)を形成することを利用して、植物や白血球における過酸化水素の局在を可視化する手法が報告されている。一方、カテキン類に代表されるポリフェノールは、中性からアルカリ性域で過酸化水素を発生することが報告されている。しかしながら、これまでポリフェノールの定量にこれ自体から生じる過酸化水素を利用したものはなく、また、過酸化水素とセリウムとが反応して形成される結晶物と、ポリフェノール濃度との間にどのような関係があるのか全く知られていない。したがって、簡便な操作で、迅速に試料中のポリフェノール濃度を測定できるポリフェノールの定量法を提供する。
【解決手段】ポリフェノールを含有する試料にセリウム化合物を作用させ、生成した結晶物を定量することによってポリフェノールの濃度を算出するポリフェノールの定量法。
【解決手段】ポリフェノールを含有する試料にセリウム化合物を作用させ、生成した結晶物を定量することによってポリフェノールの濃度を算出するポリフェノールの定量法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、セリウム化合物を用いたポリフェノールの定量法に関する。
【背景技術】
【0002】
ポリフェノールは、植物の果実や種子に含まれる色素、苦味成分の代表的なものとして知られ、古くから食品や化粧品に使われている。近年では、いわゆる「フレンチパラドックス」を背景とした赤ワインブームや、茶カテキン類の体脂肪蓄積抑制効果など、ポリフェノールの健康価値が注目されている(非特許文献1)。また、茶カテキン類に代表されるポリフェノールは、黄色ブドウ球菌や腸炎ビブリオ等の食中毒細菌、薬剤耐性細菌や植物病原菌に有効であることが報告されている(特許文献1−5)。
【0003】
試料中の総ポリフェノールを測定する方法としては、酒石酸鉄吸光光度法、フォーリン・デニス法及びフォーリン・チオカルト法が知られている。これらの方法は、試料中に含まれる総ポリフェノール量を発色的に定量する方法である。また、フラボノール類を測定する方法として、HPLCによる分離分析法が知られている(特許文献6)。
しかし、比色による方法では、試料液の着色が測定の障害になる場合があり、また反応に数時間要するといった欠点を有する。
【0004】
従来、過酸化水素がセリウムと反応して結晶性のセリウムペルヒドロキシド(CP)を形成することを利用して、植物や白血球における過酸化水素の局在を可視化する手法が報告されている。この手法では、電子顕微鏡により過酸化水素の発生の有無、発生部位及び発生量を定量することができる(非特許文献2−5)。
一方、カテキン類に代表されるポリフェノールは、中性からアルカリ性域で過酸化水素を発生することが報告されている(非特許文献6)。
しかしながら、これまでポリフェノールの定量にこれ自体から生じる過酸化水素を利用したものはなく、また、過酸化水素とセリウムとが反応して形成される結晶物と、ポリフェノール濃度との間にどのような関係があるのか全く知られていない。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開平2−276562号公報
【特許文献2】特開平2−117608号公報
【特許文献3】特開平3−246227号公報
【特許文献4】特開平8−38133号公報
【特許文献5】特開2000−328443号公報
【特許文献6】特開2009−000098号公報
【非特許文献】
【0006】
【非特許文献1】Shahidi F, Natural Antioxidant, Chemistry, Health Effects and Application, AOCS press, 1997
【非特許文献2】J. Electr. Microsc. Technol. Med. Biol.21(1), 7-11, 2007
【非特許文献3】医学生物学電子顕微鏡技術学会第24回予稿集 第19頁、平成20年
【非特許文献4】医学生物学電子顕微鏡技術学会第24回予稿集 第20頁、平成20年
【非特許文献5】医学生物学電子顕微鏡技術学会第23回予稿集 第45頁、平成19年
【非特許文献6】Biol. Pharm. Bull. 27(3), 277-281, 2004
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明は、簡便な操作で、迅速に試料中のポリフェノール濃度を測定できるポリフェノールの定量法を提供することに関する。
【課題を解決するための手段】
【0008】
本発明者らは、ポリフェノール濃度と、当該ポリフェノールから発生した過酸化水素とセリウムとが反応して形成される結晶物の量との間に極めて高い相関性があることを見出した。そして、ポリフェノールを含有する試料にセリウムを作用させて生成された結晶物の量を、予め求めた結晶物の量とポリフェノールの濃度との関係に照らし合わせることで、試料中のポリフェノール濃度を定量できることを見出した。
【0009】
すなわち、本発明は、ポリフェノールを含有する試料にセリウム化合物を作用させ、生成した結晶物を定量することによってポリフェノールの濃度を算出することを特徴とするポリフェノールの定量法を提供するものである。
【発明の効果】
【0010】
本発明によれば、試料中のポリフェノール濃度を簡便・迅速に算出することができる。
【図面の簡単な説明】
【0011】
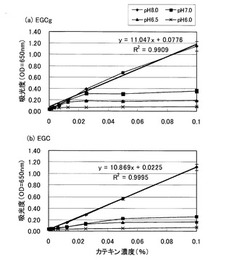
【図1−1】生成した結晶物の量とカテキン濃度との関係を示すグラフである。(a)EGCg、(b)EGC
【図1−2】生成した結晶物の量とカテキン濃度との関係を示すグラフである。(c)ECg、(d)EC
【図2】試料に塩化セリウム添加した後の吸光度の経時変化を示すグラフである。
【図3】生成した結晶物の量とクロロゲン酸濃度との関係を示すグラフである。
【図4】本発明方法によるEGCgの定量結果と既存法による定量結果を比較した図である。
【図5】本発明方法によるEGCgの定量値を100とした時の既存法による定量値を示す図である。
【図6】抗酸化剤存在下でのEGCgの定量結果を示すグラフである。(a)pH8.0、(b)pH5.0
【発明を実施するための形態】
【0012】
本発明に用いられるポリフェノールを含有する試料としては、ポリフェノールを含有するものであれば特に制限されず、例えば茶抽出液、果汁、コーヒー抽出液、ココア飲料その他飲食品などが挙げられる。ポリフェノールを含有する試料には、ポリフェノールの他に、例えば軟化剤、乳化剤、防腐剤、香科、安定剤、着色剤、紫外線吸収剤、抗酸化剤、保湿剤、増粘剤等の各種添加剤、食品素材等が含まれていてもよい。
試料中のポリフェノールの含有量は、特に限定されるものではないが、通常、試料中に溶解した状態で0.001質量%程度以上であるのが好適である。また、所望により、試料を緩衝液などの適当な溶媒に溶解又は分散させて用いてもよい。緩衝液としては、例えばHEPES Bufferなどのグッドバッファーが挙げられる。
【0013】
本発明の測定対象であるポリフェノールは過酸化水素を発生させるものである。そのようなポリフェノールとしては、フェニルカルボン酸系、リグナン系、クルクミン系、クマリン系又はフラボノイド系のポリフェノールが挙げられ、具体的には、フェニルカルボン酸系のポリフェノールとして、クロロゲン酸、カフェ酸又はフェルラ酸が挙げられる。また、フラボノイド系として、カテキン類、アピゲニン、ルチン、ルテオリン、ケルセチン、ケンフェロール、イソラムネチン又はヘスペレチンが挙げられる。
【0014】
なかでも、フラボノイド系のポリフェノールが好ましく、特にカテキン類が好ましい。カテキン類としては、カテキン、カテキンガレート、ガロカテキン及びガロカテキンガレート等の非エピ体カテキン類並びに、エピカテキン、エピガロカテキン、エピカテキンガレート及びエピガロカテキンガレート等のエピ体カテキン類の1種以上が挙げられる。また、カテキン類は、重合体であってもよい。
【0015】
本発明において用いられるセリウム化合物は、過酸化水素と反応して結晶物を形成するものであればよく、例えば酢酸セリウム、塩化セリウム、硝酸セリウム、硫酸セリウムなどが挙げられる。なかでも、取扱性・反応性の点から塩化セリウムが好ましい。
【0016】
ポリフェノールを含有する試料にセリウム化合物を作用させる方法は、特に制限されないが、例えば試料に最終濃度で0.001〜1質量%、好ましくは0.01〜0.5質量%のセリウム化合物を添加、混合することにより行うのが好ましい。これにより、ポリフェノールから発生する過酸化水素とセリウムが反応し、セリウムの結晶物が生成される。この際、セリウム化合物は、前記と同様の緩衝液、イオン交換水などの適当な溶媒に溶解又は分散させて用いてもよい。
【0017】
反応温度は0〜40℃、反応時間は10秒〜20分程度が好ましい。また、反応液のpHは6.5以上、特にpH8〜12の範囲とするのが、ポリフェノールからの過酸化水素発生が良好である点から好ましい。なお、反応液のpHは、水酸化ナトリウムなどにより調整することができる。
【0018】
本発明において、生成した結晶物を定量する方法は、特に限定されないが、反応液の濁度を測定することにより行うのが好ましい。濁度を測定するには、例えば所定の吸収波長における試料の吸光度を測定すればよい。吸光波長は、好ましくは600nm〜660nmである。
【0019】
上記により求めた結晶物の定量値を、予め既知濃度のポリフェノール試料を用いて求めた結晶物の量とポリフェノールの濃度との関係に照らし合わせることで、試料中のポリフェノール濃度を算出する。この両者の関係は、以下の方法により求めることができる。
先ず、既知濃度のポリフェノール試料に、前記と同様にセリウム化合物を添加、混合して結晶物を生成させる。ここで、ポリフェノール試料は、ポリフェノールを前記と同様の緩衝液などの適当な溶媒に溶解又は分散させて所定の濃度に希釈したものを用いることができる。
【0020】
次いで、生成した結晶物を定量し、該定量値とポリフェノールの濃度をプロットする。さらに、ポリフェノール試料の濃度を変えて同様の操作を数回行い、結晶物の量とポリフェノールの濃度との関係を示すグラフを作成し、検量線とする。後記実施例に示すように、ポリフェノールの濃度に応じて生成する結晶物の量は増大する。すなわち、結晶物の量とポリフェノールの濃度とは相関関係にある。
【0021】
従って、生成した結晶物の量とポリフェノールの濃度との関係を示す検量線や関係式を予め作製しておけば、同様な方法でポリフェノールを含有する試料から生成した結晶物を定量し、その定量値を前記検量線や関係式と照らし合わせることで試料中のポリフェノールの濃度を知ることができる。また、予めポリフェノールの特定濃度に相当する箇所に目盛りや印などを付しておけば、結晶物の量がその箇所を超えるか超えないかにより、半定量的に評価することもできる。なお、反応時のpHや定量したいポリフェノールの種類により結晶物の量は異なるので、一つの系に対して一つの検量線が必要である。
【0022】
上記方法を利用して定量可能なポリフェノールの濃度は特に規定されないが1000ppm以下が好ましく、更に500ppm以下がより好ましい。
【0023】
実施例
[試料]
EGCg;エピガロカテキンガレート(ニュートリションジャパン(株)商品名;テアビゴ)
EGC;エピガロカテキン(SIGMA社製)
ECg;エピカテキンガレート(SIGMA社製)
EC;エピカテキン(SIGMA社製)
CA;クロロゲン酸(Cayman CHEMICAL)
L(+)-アスコルビン酸ナトリウム 和光特級(和光純薬工業株式会社)
L(+)-アスコルビン酸 和光特級(和光純薬工業株式会社)
[緩衝液]
HEPES Buffer (Irvine Scientific)
【0024】
実施例1 検量線の作製
(1)EGCg、EGC、ECg、ECの4種のカテキン溶液を0.1、0.05、0.025、0.0125、0.00625、0質量%の濃度になるようにpH6.0〜8.0の10mM HEPES Buffer(Irvine Scientific)にそれぞれ溶解して試料を調製後、96穴タイタープレート(Falcon)に0.18mLずつ分注した。分注した試料に、イオン交換水に溶解し1.0質量%に調製したCeCl3溶液を0.02mLずつ添加し、室温(25℃、以下同じ)で0、5、10、20、30、60分間静置した後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0025】
得られた吸光度と対応するカテキンの濃度をそれぞれプロットし、グラフを作成して検量線とした。図1−1及び図1−2は、5分間反応させた、吸光度(生成した結晶物の量)とカテキン濃度との関係を示すグラフである。図1−1及び図1−2に示すように、吸光度とカテキン濃度の関係は用量依存的に変化し相関関係があることが確認された。また、最小二乗法による回帰分析を行い、相関係数と回帰式を求めたところ、高い相関係数が得られた。反応液はpH6.5以上であれば測定可能であった。また、pHが高いほどグラフの傾きが大きかった。
【0026】
CeCl3溶液を添加した後の吸光度を経時的に測定した結果を図2に示す(pH8.0)。添加直後から時間の経過とともに回帰式の傾きが小さくなり、さらには添加30分後にはカテキン濃度と吸光度の相関が低下した。
【0027】
(2)クロロゲン酸を0.05、0.025、0.0125、0.00625、0質量%の濃度になるようにpH8.0の10mM HEPES Buffer(Irvine Scientific)にそれぞれ溶解して試料を調製後、96穴タイタープレート(Falcon)に0.18mLずつ分注した。分注した溶液にpH8.0、10mM HEPES Buffer(Irvine Scientific)に溶解し1.0質量%に調製したCeCl3溶液を0.02mLずつ添加し、室温で5分間静置後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0028】
得られた吸光度と対応するクロロゲン酸の濃度をそれぞれプロットし、グラフを作成して検量線とした(図3)。
図3に示すように、吸光度(生成した結晶物の量)とクロロゲン酸濃度の関係は用量依存的に変化し相関関係があることが確認された。また、最小二乗法による回帰分析を行い、相関係数と回帰式を求めたところ、高い相関係数が得られた。
【0029】
実施例2 未知試料を用いたカテキン類の定量
(1)試料の調製
pH5.0の10mM HEPES Buffer(Irvine Scientific)に濃度未知となるようにEGCgを適宜溶解し試料(試料No.1〜No.3)を調製した。
【0030】
(2)検量線の作製
実施例1の方法に従いEGCgの検量線を作製した。
【0031】
(3)EGCgの定量
試料No.1〜No.3を96穴タイタープレート(Falcon)に0.18mLずつ分注した。分注した試料に、0.1N NaOHを0.01mLずつ添加しpHを8.0に調整し、更にイオン交換水に溶解し2.0質量%に調製したCeCl3溶液を0.01mLずつ添加し、室温で5分間静置後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0032】
(4)既存の方法による定量
試料No.1〜No.3中のEGCg濃度を既存の方法(特開2009-000098号公報参照)により以下の様に定量した。なお、EGCgの分解及び重合を考慮し、カテキン類及び没食子酸として検出されたものの合計をEGCgの値として濃度の算出を行った。
試料No.1〜No.3をそれぞれフィルター(0.45μm)で濾過し、島津製作所製、高速液体クロマトグラフ(型式SCL-10AVP)を用い、オクタデシル基導入液体クロマトグラフ用パックドカラムL−カラムTM ODS(4.6mmφ×250mm:財団法人 化学物質評価研究機構製)を装着し、カラム温度35℃でグラディエント法により行った。移動相A液は酢酸を0.1mol/L含有の蒸留水溶液、B液は酢酸を0.1mol/L含有のアセトニトリル溶液とし、流速は1mL/分、試料注入量は10μL、UV検出器波長は280nmの条件で行った。グラディエント条件は以下の通りである。
【0033】
時間(分) A液濃度(体積%) B液濃度
0 97% 3%
5 97% 3%
37 80% 20%
43 80% 20%
43.5 0% 100%
48.5 0% 100%
49 97% 3%
60 97% 3%
【0034】
(5)本発明方法と既存定量法の比較
pH8.0で塩化セリウムを作用させた本発明方法によるEGCgの定量結果と既存法による定量結果を比較した(図4)。
また、本発明方法によるEGCgの定量値を100とした時の既存法による定量値を表した結果を図5に示す。本発明方法と既存法の差は±10%以内であり、本発明方法によりポリフェノールの定量が可能であることが確認された。
【0035】
実施例3 抗酸化剤存在下でのカテキン類の定量
(1)試料の調製
抗酸化剤として0.05質量%のL(+)-アスコルビン酸ナトリウムを添加したpH8.0の10mM HEPES Buffer(Irvine Scientific)及び0.05質量%のL(+)-アスコルビン酸を添加したpH5.0の10mM HEPES Buffer(Irvine Scientific)に、それぞれEGCgを0.1、0.05、0.025、0.0125質量%の濃度になるように溶解し試料を調製した。コントロールとして、L(+)-アスコルビン酸ナトリウム未添加のpH8.0の10mM HEPES Buffer(Irvine Scientific)及びL(+)-アスコルビン酸未添加のpH5.0の10mM HEPES Buffer(Irvine Scientific)に、同様にEGCgを溶解した試料を調製した。
【0036】
(2)EGCgの定量
試料0.18mLを96穴タイタープレート(Falcon)に分注した。分注したpH8.0の試料に対しては、イオン交換水に溶解した1質量% CeCl3溶液を0.02mLずつ添加した。分注したpH5.0の試料に対しては、0.1N NaOHを0.01mL添加しpH8.0に調整し、イオン交換水に溶解した2質量% CeCl3溶液を0.01mLずつ添加した。室温で5分間静置後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0037】
得られた吸光度と対応するEGCgの濃度をそれぞれプロットし、グラフを作成して検量線とした(図6の▲)。一方、コントロール溶液も同様にして吸光度を測定し、その測定値と対応するEGCg濃度をそれぞれプロットし、グラフを作成して検量線とした(図6の◆)。
その結果、図6(a)、(b)に示すように、抗酸化剤を添加した試料においては吸光度が抗酸化剤未添加試料より低くなるものの吸光度とカテキン濃度の関係は用量依存的に変化し相関関係があることが確認された。また、最小二乗法による回帰分析を行い、相関係数と回帰式を求めたところ、高い相関係数が得られた。この結果から、抗酸化剤を含む試料中のポリフェノール濃度の測定は、試料と同濃度の抗酸化剤を含む緩衝液などで濃度既知のポリフェノール試料を調製し、その試料を用いて検量線を作製することで測定可能であることが示された。なお、試料中の抗酸化剤濃度は、常法に従って、HPLC法、滴定法、比色法等により測定できる。
【技術分野】
【0001】
本発明は、セリウム化合物を用いたポリフェノールの定量法に関する。
【背景技術】
【0002】
ポリフェノールは、植物の果実や種子に含まれる色素、苦味成分の代表的なものとして知られ、古くから食品や化粧品に使われている。近年では、いわゆる「フレンチパラドックス」を背景とした赤ワインブームや、茶カテキン類の体脂肪蓄積抑制効果など、ポリフェノールの健康価値が注目されている(非特許文献1)。また、茶カテキン類に代表されるポリフェノールは、黄色ブドウ球菌や腸炎ビブリオ等の食中毒細菌、薬剤耐性細菌や植物病原菌に有効であることが報告されている(特許文献1−5)。
【0003】
試料中の総ポリフェノールを測定する方法としては、酒石酸鉄吸光光度法、フォーリン・デニス法及びフォーリン・チオカルト法が知られている。これらの方法は、試料中に含まれる総ポリフェノール量を発色的に定量する方法である。また、フラボノール類を測定する方法として、HPLCによる分離分析法が知られている(特許文献6)。
しかし、比色による方法では、試料液の着色が測定の障害になる場合があり、また反応に数時間要するといった欠点を有する。
【0004】
従来、過酸化水素がセリウムと反応して結晶性のセリウムペルヒドロキシド(CP)を形成することを利用して、植物や白血球における過酸化水素の局在を可視化する手法が報告されている。この手法では、電子顕微鏡により過酸化水素の発生の有無、発生部位及び発生量を定量することができる(非特許文献2−5)。
一方、カテキン類に代表されるポリフェノールは、中性からアルカリ性域で過酸化水素を発生することが報告されている(非特許文献6)。
しかしながら、これまでポリフェノールの定量にこれ自体から生じる過酸化水素を利用したものはなく、また、過酸化水素とセリウムとが反応して形成される結晶物と、ポリフェノール濃度との間にどのような関係があるのか全く知られていない。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開平2−276562号公報
【特許文献2】特開平2−117608号公報
【特許文献3】特開平3−246227号公報
【特許文献4】特開平8−38133号公報
【特許文献5】特開2000−328443号公報
【特許文献6】特開2009−000098号公報
【非特許文献】
【0006】
【非特許文献1】Shahidi F, Natural Antioxidant, Chemistry, Health Effects and Application, AOCS press, 1997
【非特許文献2】J. Electr. Microsc. Technol. Med. Biol.21(1), 7-11, 2007
【非特許文献3】医学生物学電子顕微鏡技術学会第24回予稿集 第19頁、平成20年
【非特許文献4】医学生物学電子顕微鏡技術学会第24回予稿集 第20頁、平成20年
【非特許文献5】医学生物学電子顕微鏡技術学会第23回予稿集 第45頁、平成19年
【非特許文献6】Biol. Pharm. Bull. 27(3), 277-281, 2004
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明は、簡便な操作で、迅速に試料中のポリフェノール濃度を測定できるポリフェノールの定量法を提供することに関する。
【課題を解決するための手段】
【0008】
本発明者らは、ポリフェノール濃度と、当該ポリフェノールから発生した過酸化水素とセリウムとが反応して形成される結晶物の量との間に極めて高い相関性があることを見出した。そして、ポリフェノールを含有する試料にセリウムを作用させて生成された結晶物の量を、予め求めた結晶物の量とポリフェノールの濃度との関係に照らし合わせることで、試料中のポリフェノール濃度を定量できることを見出した。
【0009】
すなわち、本発明は、ポリフェノールを含有する試料にセリウム化合物を作用させ、生成した結晶物を定量することによってポリフェノールの濃度を算出することを特徴とするポリフェノールの定量法を提供するものである。
【発明の効果】
【0010】
本発明によれば、試料中のポリフェノール濃度を簡便・迅速に算出することができる。
【図面の簡単な説明】
【0011】
【図1−1】生成した結晶物の量とカテキン濃度との関係を示すグラフである。(a)EGCg、(b)EGC
【図1−2】生成した結晶物の量とカテキン濃度との関係を示すグラフである。(c)ECg、(d)EC
【図2】試料に塩化セリウム添加した後の吸光度の経時変化を示すグラフである。
【図3】生成した結晶物の量とクロロゲン酸濃度との関係を示すグラフである。
【図4】本発明方法によるEGCgの定量結果と既存法による定量結果を比較した図である。
【図5】本発明方法によるEGCgの定量値を100とした時の既存法による定量値を示す図である。
【図6】抗酸化剤存在下でのEGCgの定量結果を示すグラフである。(a)pH8.0、(b)pH5.0
【発明を実施するための形態】
【0012】
本発明に用いられるポリフェノールを含有する試料としては、ポリフェノールを含有するものであれば特に制限されず、例えば茶抽出液、果汁、コーヒー抽出液、ココア飲料その他飲食品などが挙げられる。ポリフェノールを含有する試料には、ポリフェノールの他に、例えば軟化剤、乳化剤、防腐剤、香科、安定剤、着色剤、紫外線吸収剤、抗酸化剤、保湿剤、増粘剤等の各種添加剤、食品素材等が含まれていてもよい。
試料中のポリフェノールの含有量は、特に限定されるものではないが、通常、試料中に溶解した状態で0.001質量%程度以上であるのが好適である。また、所望により、試料を緩衝液などの適当な溶媒に溶解又は分散させて用いてもよい。緩衝液としては、例えばHEPES Bufferなどのグッドバッファーが挙げられる。
【0013】
本発明の測定対象であるポリフェノールは過酸化水素を発生させるものである。そのようなポリフェノールとしては、フェニルカルボン酸系、リグナン系、クルクミン系、クマリン系又はフラボノイド系のポリフェノールが挙げられ、具体的には、フェニルカルボン酸系のポリフェノールとして、クロロゲン酸、カフェ酸又はフェルラ酸が挙げられる。また、フラボノイド系として、カテキン類、アピゲニン、ルチン、ルテオリン、ケルセチン、ケンフェロール、イソラムネチン又はヘスペレチンが挙げられる。
【0014】
なかでも、フラボノイド系のポリフェノールが好ましく、特にカテキン類が好ましい。カテキン類としては、カテキン、カテキンガレート、ガロカテキン及びガロカテキンガレート等の非エピ体カテキン類並びに、エピカテキン、エピガロカテキン、エピカテキンガレート及びエピガロカテキンガレート等のエピ体カテキン類の1種以上が挙げられる。また、カテキン類は、重合体であってもよい。
【0015】
本発明において用いられるセリウム化合物は、過酸化水素と反応して結晶物を形成するものであればよく、例えば酢酸セリウム、塩化セリウム、硝酸セリウム、硫酸セリウムなどが挙げられる。なかでも、取扱性・反応性の点から塩化セリウムが好ましい。
【0016】
ポリフェノールを含有する試料にセリウム化合物を作用させる方法は、特に制限されないが、例えば試料に最終濃度で0.001〜1質量%、好ましくは0.01〜0.5質量%のセリウム化合物を添加、混合することにより行うのが好ましい。これにより、ポリフェノールから発生する過酸化水素とセリウムが反応し、セリウムの結晶物が生成される。この際、セリウム化合物は、前記と同様の緩衝液、イオン交換水などの適当な溶媒に溶解又は分散させて用いてもよい。
【0017】
反応温度は0〜40℃、反応時間は10秒〜20分程度が好ましい。また、反応液のpHは6.5以上、特にpH8〜12の範囲とするのが、ポリフェノールからの過酸化水素発生が良好である点から好ましい。なお、反応液のpHは、水酸化ナトリウムなどにより調整することができる。
【0018】
本発明において、生成した結晶物を定量する方法は、特に限定されないが、反応液の濁度を測定することにより行うのが好ましい。濁度を測定するには、例えば所定の吸収波長における試料の吸光度を測定すればよい。吸光波長は、好ましくは600nm〜660nmである。
【0019】
上記により求めた結晶物の定量値を、予め既知濃度のポリフェノール試料を用いて求めた結晶物の量とポリフェノールの濃度との関係に照らし合わせることで、試料中のポリフェノール濃度を算出する。この両者の関係は、以下の方法により求めることができる。
先ず、既知濃度のポリフェノール試料に、前記と同様にセリウム化合物を添加、混合して結晶物を生成させる。ここで、ポリフェノール試料は、ポリフェノールを前記と同様の緩衝液などの適当な溶媒に溶解又は分散させて所定の濃度に希釈したものを用いることができる。
【0020】
次いで、生成した結晶物を定量し、該定量値とポリフェノールの濃度をプロットする。さらに、ポリフェノール試料の濃度を変えて同様の操作を数回行い、結晶物の量とポリフェノールの濃度との関係を示すグラフを作成し、検量線とする。後記実施例に示すように、ポリフェノールの濃度に応じて生成する結晶物の量は増大する。すなわち、結晶物の量とポリフェノールの濃度とは相関関係にある。
【0021】
従って、生成した結晶物の量とポリフェノールの濃度との関係を示す検量線や関係式を予め作製しておけば、同様な方法でポリフェノールを含有する試料から生成した結晶物を定量し、その定量値を前記検量線や関係式と照らし合わせることで試料中のポリフェノールの濃度を知ることができる。また、予めポリフェノールの特定濃度に相当する箇所に目盛りや印などを付しておけば、結晶物の量がその箇所を超えるか超えないかにより、半定量的に評価することもできる。なお、反応時のpHや定量したいポリフェノールの種類により結晶物の量は異なるので、一つの系に対して一つの検量線が必要である。
【0022】
上記方法を利用して定量可能なポリフェノールの濃度は特に規定されないが1000ppm以下が好ましく、更に500ppm以下がより好ましい。
【0023】
実施例
[試料]
EGCg;エピガロカテキンガレート(ニュートリションジャパン(株)商品名;テアビゴ)
EGC;エピガロカテキン(SIGMA社製)
ECg;エピカテキンガレート(SIGMA社製)
EC;エピカテキン(SIGMA社製)
CA;クロロゲン酸(Cayman CHEMICAL)
L(+)-アスコルビン酸ナトリウム 和光特級(和光純薬工業株式会社)
L(+)-アスコルビン酸 和光特級(和光純薬工業株式会社)
[緩衝液]
HEPES Buffer (Irvine Scientific)
【0024】
実施例1 検量線の作製
(1)EGCg、EGC、ECg、ECの4種のカテキン溶液を0.1、0.05、0.025、0.0125、0.00625、0質量%の濃度になるようにpH6.0〜8.0の10mM HEPES Buffer(Irvine Scientific)にそれぞれ溶解して試料を調製後、96穴タイタープレート(Falcon)に0.18mLずつ分注した。分注した試料に、イオン交換水に溶解し1.0質量%に調製したCeCl3溶液を0.02mLずつ添加し、室温(25℃、以下同じ)で0、5、10、20、30、60分間静置した後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0025】
得られた吸光度と対応するカテキンの濃度をそれぞれプロットし、グラフを作成して検量線とした。図1−1及び図1−2は、5分間反応させた、吸光度(生成した結晶物の量)とカテキン濃度との関係を示すグラフである。図1−1及び図1−2に示すように、吸光度とカテキン濃度の関係は用量依存的に変化し相関関係があることが確認された。また、最小二乗法による回帰分析を行い、相関係数と回帰式を求めたところ、高い相関係数が得られた。反応液はpH6.5以上であれば測定可能であった。また、pHが高いほどグラフの傾きが大きかった。
【0026】
CeCl3溶液を添加した後の吸光度を経時的に測定した結果を図2に示す(pH8.0)。添加直後から時間の経過とともに回帰式の傾きが小さくなり、さらには添加30分後にはカテキン濃度と吸光度の相関が低下した。
【0027】
(2)クロロゲン酸を0.05、0.025、0.0125、0.00625、0質量%の濃度になるようにpH8.0の10mM HEPES Buffer(Irvine Scientific)にそれぞれ溶解して試料を調製後、96穴タイタープレート(Falcon)に0.18mLずつ分注した。分注した溶液にpH8.0、10mM HEPES Buffer(Irvine Scientific)に溶解し1.0質量%に調製したCeCl3溶液を0.02mLずつ添加し、室温で5分間静置後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0028】
得られた吸光度と対応するクロロゲン酸の濃度をそれぞれプロットし、グラフを作成して検量線とした(図3)。
図3に示すように、吸光度(生成した結晶物の量)とクロロゲン酸濃度の関係は用量依存的に変化し相関関係があることが確認された。また、最小二乗法による回帰分析を行い、相関係数と回帰式を求めたところ、高い相関係数が得られた。
【0029】
実施例2 未知試料を用いたカテキン類の定量
(1)試料の調製
pH5.0の10mM HEPES Buffer(Irvine Scientific)に濃度未知となるようにEGCgを適宜溶解し試料(試料No.1〜No.3)を調製した。
【0030】
(2)検量線の作製
実施例1の方法に従いEGCgの検量線を作製した。
【0031】
(3)EGCgの定量
試料No.1〜No.3を96穴タイタープレート(Falcon)に0.18mLずつ分注した。分注した試料に、0.1N NaOHを0.01mLずつ添加しpHを8.0に調整し、更にイオン交換水に溶解し2.0質量%に調製したCeCl3溶液を0.01mLずつ添加し、室温で5分間静置後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0032】
(4)既存の方法による定量
試料No.1〜No.3中のEGCg濃度を既存の方法(特開2009-000098号公報参照)により以下の様に定量した。なお、EGCgの分解及び重合を考慮し、カテキン類及び没食子酸として検出されたものの合計をEGCgの値として濃度の算出を行った。
試料No.1〜No.3をそれぞれフィルター(0.45μm)で濾過し、島津製作所製、高速液体クロマトグラフ(型式SCL-10AVP)を用い、オクタデシル基導入液体クロマトグラフ用パックドカラムL−カラムTM ODS(4.6mmφ×250mm:財団法人 化学物質評価研究機構製)を装着し、カラム温度35℃でグラディエント法により行った。移動相A液は酢酸を0.1mol/L含有の蒸留水溶液、B液は酢酸を0.1mol/L含有のアセトニトリル溶液とし、流速は1mL/分、試料注入量は10μL、UV検出器波長は280nmの条件で行った。グラディエント条件は以下の通りである。
【0033】
時間(分) A液濃度(体積%) B液濃度
0 97% 3%
5 97% 3%
37 80% 20%
43 80% 20%
43.5 0% 100%
48.5 0% 100%
49 97% 3%
60 97% 3%
【0034】
(5)本発明方法と既存定量法の比較
pH8.0で塩化セリウムを作用させた本発明方法によるEGCgの定量結果と既存法による定量結果を比較した(図4)。
また、本発明方法によるEGCgの定量値を100とした時の既存法による定量値を表した結果を図5に示す。本発明方法と既存法の差は±10%以内であり、本発明方法によりポリフェノールの定量が可能であることが確認された。
【0035】
実施例3 抗酸化剤存在下でのカテキン類の定量
(1)試料の調製
抗酸化剤として0.05質量%のL(+)-アスコルビン酸ナトリウムを添加したpH8.0の10mM HEPES Buffer(Irvine Scientific)及び0.05質量%のL(+)-アスコルビン酸を添加したpH5.0の10mM HEPES Buffer(Irvine Scientific)に、それぞれEGCgを0.1、0.05、0.025、0.0125質量%の濃度になるように溶解し試料を調製した。コントロールとして、L(+)-アスコルビン酸ナトリウム未添加のpH8.0の10mM HEPES Buffer(Irvine Scientific)及びL(+)-アスコルビン酸未添加のpH5.0の10mM HEPES Buffer(Irvine Scientific)に、同様にEGCgを溶解した試料を調製した。
【0036】
(2)EGCgの定量
試料0.18mLを96穴タイタープレート(Falcon)に分注した。分注したpH8.0の試料に対しては、イオン交換水に溶解した1質量% CeCl3溶液を0.02mLずつ添加した。分注したpH5.0の試料に対しては、0.1N NaOHを0.01mL添加しpH8.0に調整し、イオン交換水に溶解した2質量% CeCl3溶液を0.01mLずつ添加した。室温で5分間静置後、撹拌し、直ちに吸光度測定器(SPECTRA MAX190 Molecular Devices)にて吸光度(650nm)を測定した。
【0037】
得られた吸光度と対応するEGCgの濃度をそれぞれプロットし、グラフを作成して検量線とした(図6の▲)。一方、コントロール溶液も同様にして吸光度を測定し、その測定値と対応するEGCg濃度をそれぞれプロットし、グラフを作成して検量線とした(図6の◆)。
その結果、図6(a)、(b)に示すように、抗酸化剤を添加した試料においては吸光度が抗酸化剤未添加試料より低くなるものの吸光度とカテキン濃度の関係は用量依存的に変化し相関関係があることが確認された。また、最小二乗法による回帰分析を行い、相関係数と回帰式を求めたところ、高い相関係数が得られた。この結果から、抗酸化剤を含む試料中のポリフェノール濃度の測定は、試料と同濃度の抗酸化剤を含む緩衝液などで濃度既知のポリフェノール試料を調製し、その試料を用いて検量線を作製することで測定可能であることが示された。なお、試料中の抗酸化剤濃度は、常法に従って、HPLC法、滴定法、比色法等により測定できる。
【特許請求の範囲】
【請求項1】
ポリフェノールを含有する試料にセリウム化合物を作用させ、生成した結晶物を定量することによってポリフェノールの濃度を算出するポリフェノールの定量法。
【請求項2】
ポリフェノールがカテキン類である請求項1記載のポリフェノールの定量法。
【請求項3】
セリウム化合物が塩化セリウムである請求項1又は2記載のポリフェノールの定量法。
【請求項4】
セリウム化合物をpH6.5以上の条件下で作用させる請求項1〜3のいずれか1項記載のポリフェノールの定量法。
【請求項5】
結晶物の定量を、反応液の濁度を測定することにより行う請求項1〜4のいずれか1項記載のポリフェノールの定量法。
【請求項1】
ポリフェノールを含有する試料にセリウム化合物を作用させ、生成した結晶物を定量することによってポリフェノールの濃度を算出するポリフェノールの定量法。
【請求項2】
ポリフェノールがカテキン類である請求項1記載のポリフェノールの定量法。
【請求項3】
セリウム化合物が塩化セリウムである請求項1又は2記載のポリフェノールの定量法。
【請求項4】
セリウム化合物をpH6.5以上の条件下で作用させる請求項1〜3のいずれか1項記載のポリフェノールの定量法。
【請求項5】
結晶物の定量を、反応液の濁度を測定することにより行う請求項1〜4のいずれか1項記載のポリフェノールの定量法。
【図1−1】


【図1−2】


【図2】


【図3】


【図4】


【図5】


【図6】




【図1−2】


【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2011−33347(P2011−33347A)
【公開日】平成23年2月17日(2011.2.17)
【国際特許分類】
【出願番号】特願2009−176726(P2009−176726)
【出願日】平成21年7月29日(2009.7.29)
【出願人】(000000918)花王株式会社 (8,290)
【出願人】(504145342)国立大学法人九州大学 (960)
【Fターム(参考)】
【公開日】平成23年2月17日(2011.2.17)
【国際特許分類】
【出願日】平成21年7月29日(2009.7.29)
【出願人】(000000918)花王株式会社 (8,290)
【出願人】(504145342)国立大学法人九州大学 (960)
【Fターム(参考)】
[ Back to top ]

