ポリペプチド及びその製造と利用
【課題】6PGL活性を示す新規で有用なポリペプチドと、その製造手段と、その利用形態を提供する。
【解決手段】特定のアミノ酸配列を有するポリペプチド。特定のアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチド。特定の塩基配列を有するポリヌクレオチド。このポリヌクレオチドを導入した形質転換体を利用するポリペプチドの製造方法。このポリペプチドを含有するリン酸化酵素測定用試薬。
【解決手段】特定のアミノ酸配列を有するポリペプチド。特定のアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチド。特定の塩基配列を有するポリヌクレオチド。このポリヌクレオチドを導入した形質転換体を利用するポリペプチドの製造方法。このポリペプチドを含有するリン酸化酵素測定用試薬。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はポリペプチド及びその製造と利用に関する。更に詳しくは本発明は、3−カルボキシ−シス,シス−ムコ酸環化酵素(3-Carboxy-cis,cis-muconate cyclase:以下「3−CMC」とも呼ぶ)のアミノ酸配列を有するにもかかわらず、機能的には6−ホスホグルコノラクトナーゼ(6-Phosphogluconolactonase:以下「6PGL」とも呼ぶ)として作用する新規なポリペプチドと、このポリペプチドをコードする遺伝子を導入した形質転換体による当該ポリペプチドの製造方法と、当該ポリペプチドの利用に関する。
【背景技術】
【0002】
6PGLは、エステル結合に作用する加水分解酵素の一種である。より具体的には、国際生化学分子生物学連合(IUBMB)酵素委員会が定めるEC番号3.1.1.31の「6-Phosphogluconolactonase」に分類されるものであって、当該EC番号の定義によれば、6PGLは、6−ホスホ−D−グルコノ−1,5−ラクトンが分子内加水分解によって6−ホスホ−D−グルコン酸になる反応を双方向的に触媒する酵素である。
【0003】
6PGLは、例えば、クレアチンキナーゼ(CK)やピルビン酸キナーゼ(PK)の測定において非常に有用である。即ち、CKやPKはヒト等の筋肉組織や脳に広範囲に存在し、それらの測定は各種の心疾患、筋疾患等の診断にルーチンに利用されている。そして、下記の特許文献1〜3に例示されるように、クレアチンキナーゼ測定用試薬やピルビン酸キナーゼ測定用試薬に6PGLを含ませると、高濃度にCKやPKを含む検体を希釈することなく、それらの測定が可能になるという利点が知られている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特許第2579082号公報 特許文献1は、「安定な6−ホスホグルコノラクトナーゼ、その製造方法および該酵素の使用」に関し、一定の特性を持った6PGL(EC 3.1.1.31)の画分と、この画分を使用する、6PGLに酵素的に変換できる反応相手又はその反応に含まれる酵素の測定方法を開示している。
【0005】
【特許文献2】特許第3045190号公報 特許文献2は、クレアチンリン酸、ADP(アデノシン5’−二リン酸)、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD(ニコチンアミドアデニンジヌクレオチド)又はNADP(ニコチンアミドアデニンジヌクレオチドリン酸)、グルコース−6−リン酸脱水素酵素、マグネシウム塩類、SH試薬を主要成分とし、かつ6PGLが含有されているクレアチンキナーゼ測定用試薬を開示している。
【0006】
【特許文献3】特許第3045191号公報 特許文献3は、ホスホエノールピルビン酸、ADP(アデノシン5’−二リン酸)、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD(ニコチンアミドアデニンジヌクレオチド)又はNADP(ニコチンアミドアデニンジヌクレオチドリン酸)、グルコース−6−リン酸脱水素酵素、マグネシウム塩類を主要成分とし、かつ6PGLが含有されているピルビン酸キナーゼ測定用試薬を開示している。 なお、上記した特許文献1〜3では、各発明に係る6PGLのアミノ酸配列を開示していない。6PGLのアミノ酸配列の公知例としては、Lactobacillus reuteri DSM20016由来の6PGLのアミノ酸配列が、「EC番号3.1.1.31」として、下記の周知のデータベースに開示されている。
【0007】
〔データベース〕
NCBI、BLAST検索
上記のデータベースに開示された6PGLのアミノ酸配列を以下の「化1」に示す。この6PGLを構成するアミノ酸の数は342個である。
【0008】
【化1】

【発明の概要】
【発明が解決しようとする課題】
【0009】
ところで、6PGLは上記のように有益な用途を伴う酵素であるが、上記した特許文献1〜3やデータベースに示されたものも含め、市場に提供されている6PGLの種類の多様性、提供量の豊富さ等の点で、必ずしも十分であるとは言えない。
【0010】
そこで本発明は、6PGL活性を示す新規で有用なポリペプチドと、その製造手段と、その利用形態とを提供することを、解決すべき技術的課題とする。
【課題を解決するための手段】
【0011】
(第1発明の構成)
上記課題を解決するための第1発明の構成は、配列表の配列番号1に示すアミノ酸配列を有するポリペプチドである。
【0012】
(第2発明の構成)
上記課題を解決するための第2発明の構成は、配列表の配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチドである。
【0013】
この第2発明も含めて、本願明細書で示すアミノ酸/塩基の配列相同性の数字(%)はIbis Biosciences社の配列解析プログラム(名称:BioEdit)の配列アライメントプログラムによって計算したものを言う。このプログラムの計算原理は、一般的にはClustalW multiple sequence alignment (interface internal, external
program by Des Higgins et. al.)と呼ばれる方法である。
【0014】
(第3発明の構成)
上記課題を解決するための第3発明の構成は、配列表の配列番号1に示す塩基配列を有するポリヌクレオチドである。なお、配列表の配列番号1に示す塩基配列において、最初に小文字表記で示す「gaattc」の6塩基はEcoRIの認識部位を示し、最後に小文字表記で示す「ggatcc」の6塩基はBamHIの認識部位を示す。
【0015】
(第4発明の構成)
上記課題を解決するための第4発明の構成は、以下の(1)及び(2)の一方又は双方に該当するポリヌクレオチドである。
【0016】
(1)第2発明に記載のポリペプチドをコードするポリヌクレオチド。
【0017】
(2)第3発明に記載のポリヌクレオチドについての相補的な塩基配列に対してストリンジェントな条件下でハイブリダイズする塩基配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチドをコードするポリヌクレオチド。
【0018】
この第4発明の(2)において、「ストリンジェントな条件下でハイブリダイズする」とは、コロニーハイブリダイゼーション法,プラークハイブリダイゼーション法又はサザンブロットハイブリダイゼーション法等の適宜なハイブリダイゼーション法において、以下の条件下で一方のポリヌクレオチド(DNA)又は該ポリヌクレオチドの断片に対し他方のポリヌクレオチド(DNA)がハイブリダイズできることを言う。即ち、フィルターに固定化された一方のポリヌクレオチド又は該ポリヌクレオチドの断片に対して、0.7〜1MのNaClの存在下、所定温度(X°C)下で他方のポリヌクレオチドのハイブリダイゼーションを行った後、0.1〜2倍程度のSSC溶液(1倍濃度のSSC溶液の組成は、150mM塩化ナトリウム,15mMクエン酸ナトリウムよりなる)を用いてX°Cの条件下でフィルターを洗浄した場合に、他方のポリヌクレオチドを同定できることを言う。そして上記の「X°C」とは、少なくとも50°C以上であり、より好ましくは60°C以上であり、更に好ましくは65°C以上である。
【0019】
(第5発明の構成)
上記課題を解決するための第5発明の構成は、第3発明又は第4発明に記載のポリヌクレオチドを含有する組み換えベクターである。
【0020】
(第6発明の構成)
上記課題を解決するための第6発明の構成は、第5発明に記載の組み換えベクターを宿主に導入してなる形質転換体である。
【0021】
(第7発明の構成)
上記課題を解決するための第7発明の構成は、前記第6発明に係る宿主が大腸菌(E. coli)である形質転換体である。
【0022】
(第8発明の構成)
上記課題を解決するための第8発明の構成は、第6発明又は第7発明に記載の形質転換体を培養して6−ホスホグルコノラクトナーゼの機能を示すポリペプチドを取得するポリペプチドの製造方法である。
【0023】
(第9発明の構成)
上記課題を解決するための第9発明の構成は、クレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬としての必須成分と共に、請求項1又は請求項2に記載のポリペプチドを含有する、リン酸化酵素測定用試薬である。
【0024】
この第9発明において「リン酸化酵素測定用試薬」とは、リンを含む基を転移する酵素を測定する試薬であって、より具体的には、クレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬を包含する概念である。又、クレアチンキナーゼ測定用試薬としての必須成分には、クレアチンリン酸、ADP(アデノシン5’−二リン酸)、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD(ニコチンアミドアデニンジヌクレオチド)又はNADP(ニコチンアミドアデニンジヌクレオチドリン酸)、グルコース−6−リン酸脱水素酵素、マグネシウム塩類、SH試薬が挙げられる。又、ピルビン酸キナーゼ測定用試薬としての必須成分には、ホスホエノールピルビン酸、ADP、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD又はNADP、グルコース−6−リン酸脱水素酵素、マグネシウム塩類が挙げられる。
【発明の効果】
【0025】
第1発明のポリペプチド、即ち配列表の配列番号1に示すアミノ酸配列を有するポリペプチドは、前記「化1」に示す公知6PGLのアミノ酸配列とは著しく異なる。即ち両者のアミノ酸配列の相同性は約47%という低い数値に止まる。
【0026】
加えて第1発明のポリペプチドは、前記のデータベース中において「EC番号5.5.1.5」として開示された3−カルボキシ−シス,シス−ムコ酸環化酵素(3-Carboxy-cis,cis-muconate
cyclase:Leuconostoc citreum
KM20株由来)のアミノ酸配列と実質的に同一と認め得るアミノ酸配列を有している。上記データベースに開示された3CMCのアミノ酸配列を以下の「化2」に示すが、「化2」のアミノ酸配列と第1発明のポリペプチドのアミノ酸配列との相違点はなく、同一である。
【0027】
【化2】

なお、図1において、「A」として6PGLが関与する触媒反応を示し、「B」として3CMCが関与する触媒反応を示す。これらは公知の事項である。
【0028】
以上のように、第1発明のポリペプチドは、そのアミノ酸配列において公知の6PGLとは全く異なると共に公知の3CMCとは実質的に同一であるが、驚いたことに有効な6PGL活性を示し、その半面、実施例では述べていないが、3CMC活性は示さないことがわかった。即ち、第1発明によって、6PGL活性を示す新規かつ有用なポリペプチドが提供される。
【0029】
又、第2発明によれば、第1発明のポリペプチドと同等の機能を有する、新規かつ有用なポリペプチドが提供される。後述の実施例においては第2発明のポリペプチドの具体例を提示していないが、第1発明のポリペプチドのアミノ酸配列に対して一部のアミノ酸が置換又は欠失されあるいは付加される変異を導入し、その結果として配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示す6PGL活性ポリペプチドを得ることは、当業者にとってはさして困難なことではない。
【0030】
第3発明によれば第1発明のポリペプチドをコードする塩基配列を有するポリヌクレオチドが提供され、第4発明によれば第2発明のポリペプチドをコードする塩基配列あるいは第1発明のポリペプチドと機能同等のポリペプチドをコードする塩基配列を有するポリヌクレオチドが提供される。
【0031】
これらのポリヌクレオチドは、例えば本発明のポリペプチドを効率的に生産するための、第5発明に係る組み換えベクターや、ひいては第6発明に係る形質転換体の作製に利用できる。形質転換体の宿主としては、特に大腸菌(E. coli)が好ましい。
【0032】
第8発明によれば、本発明のポリペプチドを上記の形質転換体を利用して製造するという、新規で効率的なポリペプチド製造方法が提供される。
【0033】
第9発明によれば、本発明の6PGL活性を有するポリペプチドを含んで構成される新規なクレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬であって、高い濃度にCKやPKを含む検体においても、それを希釈することなくCKやPKを正確に測定できるリン酸化酵素測定用試薬が提供される。
【図面の簡単な説明】
【0034】
【図1】6PGLと3CMCが各々関与する触媒反応を示す。
【図2】実施例におけるプラスミドの構築図を示す。
【図3】実施例におけるCK活性の測定結果を示す。
【発明を実施するための形態】
【0035】
次に、本発明の実施形態を、その最良の形態を含めて説明する。
【0036】
〔ポリペプチド〕
本発明ポリペプチドの第1のカテゴリーは配列表の配列番号1に示すアミノ酸配列を有するポリペプチドである。このポリペプチドは、公知の6PGLのアミノ酸配列とは大きく異なり、公知の3CMCのアミノ酸配列とは実質的に同一のアミノ酸配列を有するにもかかわらず、有効な6PGL活性を示し、一方、3CMC活性は示さない。
【0037】
本発明ポリペプチドの第2のカテゴリーは配列表の配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6PGLの機能を示すポリペプチドである。上記の配列相同性は、とりわけ85%以上であることが好ましい。
【0038】
〔ポリヌクレオチド〕
本発明ポリヌクレオチドの第1のカテゴリーは、配列表の配列番号1に示す塩基配列を有するポリヌクレオチドであって、これは前記した第1のカテゴリーに係るポリペプチドをコードしている。
【0039】
本発明のポリヌクレオチドの第2のカテゴリーは、以下の(1)及び(2)の一方又は双方に該当するポリヌクレオチドである。
【0040】
(1)前記した第1のカテゴリーに係るポリペプチドをコードするポリヌクレオチド。
【0041】
(2)上記の第1のカテゴリーに係るポリヌクレオチドについての相補的な塩基配列に対してストリンジェントな条件下でハイブリダイズする塩基配列を有し、6PGLの機能を示すポリペプチドをコードするポリヌクレオチド。
【0042】
〔組み換えベクター、形質転換体、ポリペプチドの製造方法〕
本発明の組み換えベクターは、本発明に係る前記いずれかのポリヌクレオチド(遺伝子)を含有する。
【0043】
本発明の形質転換体は、上記の組み換えベクターを宿主に導入してなるものである。宿主の種類は限定されず、バクテリア(Bacteria)、真菌(Eumycetes)、各種の酵母などの単細胞真核生物、又は動物あるいは植物の生細胞を任意に選択できるが、微生物が好ましく、特に大腸菌(E. coli)が好ましい。
【0044】
本発明に係るポリペプチドの製造方法は、上記の形質転換体を培養して6−ホスホグルコノラクトナーゼの機能を示すポリペプチドを取得するという方法である。
【0045】
一般的に形質転換体を利用する目的物の生産方法において認められることであるが、本発明のポリペプチドの製造方法においても、導入遺伝子の選択、導入すべき宿主の選択、発現ベクター等の導入手段とそれに適した DNA又はRNA の構築方法の選択、培地もしくはこれに対する添加物の種類や濃度の選択、形質転換体の培養条件あるいは生育条件の選択等の要因が、ポリペプチドの生産量に影響する場合がある。
【0046】
形質転換体の培養により生産された本発明のポリペプチドは、通常行われる細胞破砕物からの抽出だけでなく、場合によっては適当な抽出溶媒を用いて培養液からも直接に抽出できる。利用する宿主の種類によっては、ポリペプチドの少なくとも一部が宿主細胞内あるいは細胞表面に止まる場合があるが、細胞膜もしくは細胞壁の破壊や、適宜な抽出溶媒による抽出等の公知の各種操作を経て、採取することができる。
【0047】
本発明においては、少なくとも本発明のポリペプチドをコードするポリヌクレオチド(遺伝子)が宿主細胞に導入される。ここにおいて、「遺伝子を導入する」とは、遺伝子の機能を有するポリヌクレオチドを組換え核酸として宿主細胞に導入する全ての場合を含む。又、「ポリヌクレオチド」とは、1本鎖、2本鎖又は3本鎖のDNA DNA及び/又はRNAを言い、遺伝子の導入には、組み換えベクターによって導入する場合や、PCR フラグメント等で合成した核酸を用いて相同組換えによって導入する場合が含まれ得る。遺伝子は、より好ましくは、遺伝子の発現を強化する発現ベクターによって導入される。
【0048】
発現ベクターは、導入しようとする遺伝子を、その発現を強化する種々のDNA 断片又はRNA 断片と融合させたものである。好ましくは、発現ベクターは、遺伝子を恒常的又は誘導的に発現させるための転写プロモーターや、転写ターミネーター、組換え体選抜用マーカー遺伝子、エンハンサーを含み得る。一般的な発現ベクターの構築方法として、例えば、PCR 法等で調製した遺伝子断片を、適当な制限酵素とリガーゼを用いる既知の方法で発現ベクターに組み込むことができる。大腸菌(E. coli)での発現用の転写プロモーターとして、trp,lac ,trc ,tac 等を用いることができる。
【0049】
ベクターとしては、限定はされないが、大腸菌(E.
coli)を宿主とする場合に良く利用されるプラスミドpTRP、pSC101、pBR322、pHSG298、pVC18、pVC19、pTrc99A、pMal-c2、pGEX2T、pTV118N、pTV119N等を好ましく使用でき、その他にもS. cerevisiaeを宿主とする場合に良く利用されるpKG1、YEp13、YEp24、YCp50、pRS414、pRS415、pRS404、pAUR101等も利用でき、バシルス・ズブチリス(B. subtilis)を宿主とする場合に良く利用されるプラスミドpUB110、pC194等も利用できる。更に、pBI122、pBI1101その他の各種のものも限定なく使用できる。
【0050】
遺伝子を宿主細胞に導入するに当たり、種々の態様で宿主に適合した組換え核酸を利用することができる。例えば、大腸菌への外来遺伝子の導入法は、ハナハンの方法等の確立された幾つかの方法を利用できる。酵母への外来遺伝子の導入法は、リチウム法等の確立された幾つかの方法を利用できる。
【0051】
〔リン酸化酵素測定用試薬〕
本発明のリン酸化酵素測定用試薬は、具体的にはクレアチンキナーゼ(CK)測定用試薬又はピルビン酸キナーゼ(PK)測定用試薬であって、CK測定用試薬又はPK測定用試薬としての必須成分と共に、本発明に係る前記いずれかのポリペプチドを含有する測定用試薬である。リン酸化酵素測定用試薬には、上記の成分の他にも、緩衝液、賦活剤、防腐剤、安定剤等が含有され得る。
【0052】
前記したように、CK測定用試薬としての必須成分には、クレアチンリン酸、ADP、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD又はNADP、グルコース−6−リン酸脱水素酵素、マグネシウム塩類、SH試薬が含まれる。PK測定用試薬としての必須成分には、ホスホエノールピルビン酸、ADP、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD又はNADP、グルコース−6−リン酸脱水素酵素、マグネシウム塩類が含まれる。
【0053】
上記の成分の内、ヘキソキナーゼ又はグルコキナーゼ、あるいはグルコース−6−リン酸脱水素酵素としては、それらの給源は限定されず、パン酵母その他の各種微生物由来のものや、動物由来のもの等を任意に選択して使用することができる。
【0054】
マグネシウム塩類としては、例えば、酢酸マグネシウム、硫酸マグネシウム等を使用することができる。
【0055】
SH試薬としては、ジチオスレイトール、N−アセチルシステイン、ジチオエリスリトール、メルカプトエタノール、チオグリコール酸、システイン等を使用することができる。
【0056】
クレアチンリン酸、ADP、グルコース、NAD又はNADP等は、既存のCK測定用試薬やPK測定用試薬に使用されているものを使用できる。
【0057】
(CK測定用試薬の実施形態例)
ヘキソキナーゼ :0.2〜20ユニット/ml
グルコース−6−リン酸脱水素酵素:0.2〜20ユニット/ml
本発明のポリペプチド :0.1〜15ユニット/ml
クレアチンリン酸 :5〜40mM
ADP :0.2〜10mM
NAD又はNADP :0.2〜10mM
グルコース :2〜100mM
マグネシウム塩類 :2〜15mM
SH試薬 :2〜50μM
EDTA :0.2〜10mM
(PK測定用試薬の実施形態例)
ヘキソキナーゼ :0.2〜20ユニット/ml
グルコース−6−リン酸脱水素酵素:0.2〜20ユニット/ml
本発明のポリペプチド :0.1〜15ユニット/ml
ホスホエノールピルビン酸 :5〜40mM
ADP :0.2〜10mM
NAD又はNADP :0.1〜10mM
グルコース :2〜100mM
マグネシウム塩類 :2〜15mM
SH試薬 :2〜50μM
EDTA :0.2〜10mM
【実施例】
【0058】
次に本発明の実施例を説明する。本発明の技術的範囲は、以下の実施例によって限定されない。実施例では、本発明に係るポリペプチドを、そのアミノ酸配列に鑑みて「本発明3−CMC」と呼ぶ。
【0059】
〔実施例1:本発明3−CMC発現系の構築〕
まず、ロイコノストック・メセンテロイデス属菌由来の本発明3−CMCを大腸菌で発現させるためにプラスミドを構築し、本発明3−CMCの遺伝子配列を設計した。
【0060】
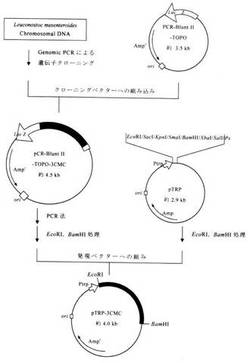
本発明3−CMCを挿入したプラスミドpTRP−3CMCを、図2に示す構築図にしたがって作製した。まず、ロイコノストック・メセンテロイデス属菌の染色体DNAを鋳型にして、5’末端側(センスプライマー)及び3’末端側(アンチセンスプライマー)にEcoRI及びBamHI制限酵素部位を設けた下記に示すプライマーを用いてPCRを行ない、アガロース電気泳動により約1.1kbのDNA断片を確認した。PCR反応組成は、(50μLあたり)1U KOD plus polymerase(TOYOBO)、10pg 鋳型DNA、0.3μM センスプライマー、0.3μM アンチセンスプライマー、0.2mM dNTP Mix、1mM
MgSO4、1×バッファーにて行なった。PCR反応は、94℃/2分(変性)、58℃/30秒(アニーリング)、68℃/1分30秒(伸長)を30サイクル繰り返した。
【0061】
上記したセンスプライマー(3CMC−EcoRI−ATG)の塩基配列を配列表の配列番号3に示し、アンチセンスプライマー(3CMC−BamHI−TAA)の塩基配列を配列表の配列番号4に示す。
【0062】
得られたPCR産物を制限酵素EcoRI及びBamHI(タカラバイオ社製)で処理を行ない、アガロース電気泳動後、GFXTM
PCR DNA and
Gel Band Purification
Kit(GEヘルスケアバイオサイエンス社製)により回収した。本発明3−CMC断片は、LigaFastTM
Rapid DNA Ligation System(プロメガ社製)を用いて、予め制限酵素EcoRI及びBamHI(タカラバイオ社製)で処理した発現ベクターpTRP(2.9kb)に導入した。大腸菌JM109株に形質転換し、大腸菌組換え体pTRP−3CMC/JM109を得た。このロイコノストック・メセンテロイデス属菌由来の本発明3−CMCの塩基配列およびアミノ酸配列を配列表の配列番号1に示し、そのアミノ酸配列をあらためて配列表の配列番号2に示す。
【0063】
〔実施例2:本発明3−CMCの大量培養〕
形質転換体の高密度培養によるロイコノストック・メセンテロイデス属菌由来の本発明3−CMCの大量生産(フェドバッチ培養による高密度培養)を以下の方法で実施した。
【0064】
プラスミドpTRP−3CMCを形質転換した大腸菌JM109株について、16L New Brunswick Scientific Fermentor SF−116(Edison,NJ,U.S.A.)を用いて高密度培養を行なった。温度(37℃)、pH(7.2)、撹拌速度(500rpm)、通気量(15mL/min)の培養パラメーターは、ML−4100(
Multi−loop microprocessor controller )によって制御した。pHの調整は、10% アンモニア水を添加して行なった。
【0065】
一晩前培養した培養液(160mL)を、50μg/mLのアンピシリンを含むLB培地(8L)へ植菌して2時間培養を行ない、その後10時間目まで添加培地を連続的に合計2L加えながら培養を続けた。
【0066】
添加培地の組成は以下に示す通りである。グルコース(10%)、酵母エキス(15%)、MgSO4・7H2O(0.1%)、L−グルタミン酸(0.75%)、L−スレオニン(0.75%)、L−チロシン(0.04%)、L−ヒスチジン(0.4%)、L−メチオニン(0.4%)、pH7.4。
【0067】
培地の添加は、100mL/hの速度で開始し、2時間ごとに200mL/h、300mL/h、400mL/hの順で増加させて行なった。集菌は、12時間目に遠心分離(11,000g×20min)により行なった。菌体の増殖は、培養液の600nmでの吸光度を測定して調べた。その結果、プラスミドpTRP−3CMCで形質転換した大腸菌JM109株の高密度培養菌体を得ることができた。
【0068】
発現量を確認するため、得られた湿菌体5gを3mLの抽出バッファー(20mM リン酸カリウムバッファー pH7.5)で懸濁し、超音波破砕後(MISONIX社製 astrason ULTRASONIC PROCESSOTR XL)、遠心分離し(18,000×g、15分、4℃ BECKMAN社製 Model J2−21
Centrifuge)粗抽出液を調製した。得られた粗抽出液中の本発明3−CMC発現量は、約3200U/mgタンパクであった。
【0069】
本発明3−CMCの活性測定は次のような方法で行なった。MESバッファー (30mM、pH6.5)、グルコース−6−リン酸(0.26mM、ロシュ社製)、NAD+(0.26mM、オリエンタル酵母工業社製)から構成される反応液にグルコース−6−リン酸脱水素酵素(30U、オリエンタル酵母工業社製)添加したのち、25℃で340nmの吸光度が変化しなくなるまで反応させる。その後、酵素溶液を添加したのち、340nmの吸光度変化を測定し本発明3−CMC活性を算出した。また、この反応条件における1分間あたりの1μmolのNADHの生成量を1単位とし、上記酵素活性を本発明3−CMC活性とした。
〔実施例3:本発明3−CMCの精製〕
大量精製を行なうため、得られた湿菌体170gを20mMリン酸カリウムバッファーに懸濁したのち、DINO−MILL(Typ KDL)にて菌体破砕を行ない、得られた破砕画分を遠心分離し(18,000×g、15分、4℃
BECKMAN社製 Model J2−21
Centrifuge)粗抽出液を調製した。得られた粗抽出液を用いて以下の方法で精製を行なった。
【0070】
バッファーA(10mM リン酸カリウムバッファー
pH7.5)で平衡化したDEAE−Cellulofine A−500(生化学工業株式会社製)に通じ、バッファーAで洗浄後、0−0.3M
NaClのリニア・グラジエントで目的タンパク質を溶出させた。
【0071】
活性画分に最終40%飽和になるように硫酸アンモニウムを加え、1時間攪拌した後、バッファーB(10mM
K−リン酸バッファー pH7.5、40%飽和硫酸アンモニウム)で平衡化したPhenyl−Sepharose
6Fast Flow(GEヘルスケアバイオサイエンス社製)に通じ、バッファーBで洗浄後、40−0% 硫酸アンモニウムのリニア・グラジエントで目的タンパク質を溶出させた。得られた目的画分をSephadex G−25(GEヘルスケアバイオサイエンス社製)に通じた。最終的に比活性6000U/mgタンパクである組換えタンパク質の精製標品を得た。この精製標品は、SDS−PAGE後CBBR−250で染色した結果、約38,000のほぼ単一バンドを示した。
〔実施例4:クレアチンキナーゼ測定用試薬における応用評価〕
CK測定用試薬を以下の方法で調製した。まず、イミダゾールバッファー(pH 6.6、134mM)、G6PDH(オリエンタル酵母工業社製、118U/mL)、HK(オリエンタル酵母工業社製、237U/mL)、本発明3−CMC(21U/mL)、ADP(2.68mM)、NADP(2.68mM)、グルコース(26.8mM)、酢酸マグネシウム(13.4mM)、EDTA(2.68mM)、NAC(26.8mM)より構成されるR1試薬を調製した。さらに、イミダゾールバッファー(pH6.6、10mM)、CP(154mM)からなるR2試薬を調製した(実施例)。また、別にR1試薬から本発明3−CMCを抜いた比較用R1試薬も調製し、比較例とすることとした。
【0072】
別に、試料として、大腸菌で組み換えたヒト由来のクレアチンキナーゼである「組換えヒトCK−MM(オリエンタル酵母工業社製)」を使用した。上記で調製したR1試薬、R2試薬及び比較用R1試薬を用いて日立自動分析装置7170形にてCK活性を測定した。その結果、実施例では1分間当りの吸光度変化量が4,000U/Lまで直線的に変化しているのに対して、本発明3−CMC無添加(比較例)では1,600U/Lまでしか直線的に変化していないことがわかった(図3参照)。このように、本発明3−CMCを添加することにより、測定範囲が広がることが示唆された。
【産業上の利用可能性】
【0073】
本発明により、6PGL活性を示す新規で有用なポリペプチドと、その製造手段と、その利用形態とが提供される。
【技術分野】
【0001】
本発明はポリペプチド及びその製造と利用に関する。更に詳しくは本発明は、3−カルボキシ−シス,シス−ムコ酸環化酵素(3-Carboxy-cis,cis-muconate cyclase:以下「3−CMC」とも呼ぶ)のアミノ酸配列を有するにもかかわらず、機能的には6−ホスホグルコノラクトナーゼ(6-Phosphogluconolactonase:以下「6PGL」とも呼ぶ)として作用する新規なポリペプチドと、このポリペプチドをコードする遺伝子を導入した形質転換体による当該ポリペプチドの製造方法と、当該ポリペプチドの利用に関する。
【背景技術】
【0002】
6PGLは、エステル結合に作用する加水分解酵素の一種である。より具体的には、国際生化学分子生物学連合(IUBMB)酵素委員会が定めるEC番号3.1.1.31の「6-Phosphogluconolactonase」に分類されるものであって、当該EC番号の定義によれば、6PGLは、6−ホスホ−D−グルコノ−1,5−ラクトンが分子内加水分解によって6−ホスホ−D−グルコン酸になる反応を双方向的に触媒する酵素である。
【0003】
6PGLは、例えば、クレアチンキナーゼ(CK)やピルビン酸キナーゼ(PK)の測定において非常に有用である。即ち、CKやPKはヒト等の筋肉組織や脳に広範囲に存在し、それらの測定は各種の心疾患、筋疾患等の診断にルーチンに利用されている。そして、下記の特許文献1〜3に例示されるように、クレアチンキナーゼ測定用試薬やピルビン酸キナーゼ測定用試薬に6PGLを含ませると、高濃度にCKやPKを含む検体を希釈することなく、それらの測定が可能になるという利点が知られている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特許第2579082号公報 特許文献1は、「安定な6−ホスホグルコノラクトナーゼ、その製造方法および該酵素の使用」に関し、一定の特性を持った6PGL(EC 3.1.1.31)の画分と、この画分を使用する、6PGLに酵素的に変換できる反応相手又はその反応に含まれる酵素の測定方法を開示している。
【0005】
【特許文献2】特許第3045190号公報 特許文献2は、クレアチンリン酸、ADP(アデノシン5’−二リン酸)、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD(ニコチンアミドアデニンジヌクレオチド)又はNADP(ニコチンアミドアデニンジヌクレオチドリン酸)、グルコース−6−リン酸脱水素酵素、マグネシウム塩類、SH試薬を主要成分とし、かつ6PGLが含有されているクレアチンキナーゼ測定用試薬を開示している。
【0006】
【特許文献3】特許第3045191号公報 特許文献3は、ホスホエノールピルビン酸、ADP(アデノシン5’−二リン酸)、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD(ニコチンアミドアデニンジヌクレオチド)又はNADP(ニコチンアミドアデニンジヌクレオチドリン酸)、グルコース−6−リン酸脱水素酵素、マグネシウム塩類を主要成分とし、かつ6PGLが含有されているピルビン酸キナーゼ測定用試薬を開示している。 なお、上記した特許文献1〜3では、各発明に係る6PGLのアミノ酸配列を開示していない。6PGLのアミノ酸配列の公知例としては、Lactobacillus reuteri DSM20016由来の6PGLのアミノ酸配列が、「EC番号3.1.1.31」として、下記の周知のデータベースに開示されている。
【0007】
〔データベース〕
NCBI、BLAST検索
上記のデータベースに開示された6PGLのアミノ酸配列を以下の「化1」に示す。この6PGLを構成するアミノ酸の数は342個である。
【0008】
【化1】

【発明の概要】
【発明が解決しようとする課題】
【0009】
ところで、6PGLは上記のように有益な用途を伴う酵素であるが、上記した特許文献1〜3やデータベースに示されたものも含め、市場に提供されている6PGLの種類の多様性、提供量の豊富さ等の点で、必ずしも十分であるとは言えない。
【0010】
そこで本発明は、6PGL活性を示す新規で有用なポリペプチドと、その製造手段と、その利用形態とを提供することを、解決すべき技術的課題とする。
【課題を解決するための手段】
【0011】
(第1発明の構成)
上記課題を解決するための第1発明の構成は、配列表の配列番号1に示すアミノ酸配列を有するポリペプチドである。
【0012】
(第2発明の構成)
上記課題を解決するための第2発明の構成は、配列表の配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチドである。
【0013】
この第2発明も含めて、本願明細書で示すアミノ酸/塩基の配列相同性の数字(%)はIbis Biosciences社の配列解析プログラム(名称:BioEdit)の配列アライメントプログラムによって計算したものを言う。このプログラムの計算原理は、一般的にはClustalW multiple sequence alignment (interface internal, external
program by Des Higgins et. al.)と呼ばれる方法である。
【0014】
(第3発明の構成)
上記課題を解決するための第3発明の構成は、配列表の配列番号1に示す塩基配列を有するポリヌクレオチドである。なお、配列表の配列番号1に示す塩基配列において、最初に小文字表記で示す「gaattc」の6塩基はEcoRIの認識部位を示し、最後に小文字表記で示す「ggatcc」の6塩基はBamHIの認識部位を示す。
【0015】
(第4発明の構成)
上記課題を解決するための第4発明の構成は、以下の(1)及び(2)の一方又は双方に該当するポリヌクレオチドである。
【0016】
(1)第2発明に記載のポリペプチドをコードするポリヌクレオチド。
【0017】
(2)第3発明に記載のポリヌクレオチドについての相補的な塩基配列に対してストリンジェントな条件下でハイブリダイズする塩基配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチドをコードするポリヌクレオチド。
【0018】
この第4発明の(2)において、「ストリンジェントな条件下でハイブリダイズする」とは、コロニーハイブリダイゼーション法,プラークハイブリダイゼーション法又はサザンブロットハイブリダイゼーション法等の適宜なハイブリダイゼーション法において、以下の条件下で一方のポリヌクレオチド(DNA)又は該ポリヌクレオチドの断片に対し他方のポリヌクレオチド(DNA)がハイブリダイズできることを言う。即ち、フィルターに固定化された一方のポリヌクレオチド又は該ポリヌクレオチドの断片に対して、0.7〜1MのNaClの存在下、所定温度(X°C)下で他方のポリヌクレオチドのハイブリダイゼーションを行った後、0.1〜2倍程度のSSC溶液(1倍濃度のSSC溶液の組成は、150mM塩化ナトリウム,15mMクエン酸ナトリウムよりなる)を用いてX°Cの条件下でフィルターを洗浄した場合に、他方のポリヌクレオチドを同定できることを言う。そして上記の「X°C」とは、少なくとも50°C以上であり、より好ましくは60°C以上であり、更に好ましくは65°C以上である。
【0019】
(第5発明の構成)
上記課題を解決するための第5発明の構成は、第3発明又は第4発明に記載のポリヌクレオチドを含有する組み換えベクターである。
【0020】
(第6発明の構成)
上記課題を解決するための第6発明の構成は、第5発明に記載の組み換えベクターを宿主に導入してなる形質転換体である。
【0021】
(第7発明の構成)
上記課題を解決するための第7発明の構成は、前記第6発明に係る宿主が大腸菌(E. coli)である形質転換体である。
【0022】
(第8発明の構成)
上記課題を解決するための第8発明の構成は、第6発明又は第7発明に記載の形質転換体を培養して6−ホスホグルコノラクトナーゼの機能を示すポリペプチドを取得するポリペプチドの製造方法である。
【0023】
(第9発明の構成)
上記課題を解決するための第9発明の構成は、クレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬としての必須成分と共に、請求項1又は請求項2に記載のポリペプチドを含有する、リン酸化酵素測定用試薬である。
【0024】
この第9発明において「リン酸化酵素測定用試薬」とは、リンを含む基を転移する酵素を測定する試薬であって、より具体的には、クレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬を包含する概念である。又、クレアチンキナーゼ測定用試薬としての必須成分には、クレアチンリン酸、ADP(アデノシン5’−二リン酸)、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD(ニコチンアミドアデニンジヌクレオチド)又はNADP(ニコチンアミドアデニンジヌクレオチドリン酸)、グルコース−6−リン酸脱水素酵素、マグネシウム塩類、SH試薬が挙げられる。又、ピルビン酸キナーゼ測定用試薬としての必須成分には、ホスホエノールピルビン酸、ADP、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD又はNADP、グルコース−6−リン酸脱水素酵素、マグネシウム塩類が挙げられる。
【発明の効果】
【0025】
第1発明のポリペプチド、即ち配列表の配列番号1に示すアミノ酸配列を有するポリペプチドは、前記「化1」に示す公知6PGLのアミノ酸配列とは著しく異なる。即ち両者のアミノ酸配列の相同性は約47%という低い数値に止まる。
【0026】
加えて第1発明のポリペプチドは、前記のデータベース中において「EC番号5.5.1.5」として開示された3−カルボキシ−シス,シス−ムコ酸環化酵素(3-Carboxy-cis,cis-muconate
cyclase:Leuconostoc citreum
KM20株由来)のアミノ酸配列と実質的に同一と認め得るアミノ酸配列を有している。上記データベースに開示された3CMCのアミノ酸配列を以下の「化2」に示すが、「化2」のアミノ酸配列と第1発明のポリペプチドのアミノ酸配列との相違点はなく、同一である。
【0027】
【化2】

なお、図1において、「A」として6PGLが関与する触媒反応を示し、「B」として3CMCが関与する触媒反応を示す。これらは公知の事項である。
【0028】
以上のように、第1発明のポリペプチドは、そのアミノ酸配列において公知の6PGLとは全く異なると共に公知の3CMCとは実質的に同一であるが、驚いたことに有効な6PGL活性を示し、その半面、実施例では述べていないが、3CMC活性は示さないことがわかった。即ち、第1発明によって、6PGL活性を示す新規かつ有用なポリペプチドが提供される。
【0029】
又、第2発明によれば、第1発明のポリペプチドと同等の機能を有する、新規かつ有用なポリペプチドが提供される。後述の実施例においては第2発明のポリペプチドの具体例を提示していないが、第1発明のポリペプチドのアミノ酸配列に対して一部のアミノ酸が置換又は欠失されあるいは付加される変異を導入し、その結果として配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示す6PGL活性ポリペプチドを得ることは、当業者にとってはさして困難なことではない。
【0030】
第3発明によれば第1発明のポリペプチドをコードする塩基配列を有するポリヌクレオチドが提供され、第4発明によれば第2発明のポリペプチドをコードする塩基配列あるいは第1発明のポリペプチドと機能同等のポリペプチドをコードする塩基配列を有するポリヌクレオチドが提供される。
【0031】
これらのポリヌクレオチドは、例えば本発明のポリペプチドを効率的に生産するための、第5発明に係る組み換えベクターや、ひいては第6発明に係る形質転換体の作製に利用できる。形質転換体の宿主としては、特に大腸菌(E. coli)が好ましい。
【0032】
第8発明によれば、本発明のポリペプチドを上記の形質転換体を利用して製造するという、新規で効率的なポリペプチド製造方法が提供される。
【0033】
第9発明によれば、本発明の6PGL活性を有するポリペプチドを含んで構成される新規なクレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬であって、高い濃度にCKやPKを含む検体においても、それを希釈することなくCKやPKを正確に測定できるリン酸化酵素測定用試薬が提供される。
【図面の簡単な説明】
【0034】
【図1】6PGLと3CMCが各々関与する触媒反応を示す。
【図2】実施例におけるプラスミドの構築図を示す。
【図3】実施例におけるCK活性の測定結果を示す。
【発明を実施するための形態】
【0035】
次に、本発明の実施形態を、その最良の形態を含めて説明する。
【0036】
〔ポリペプチド〕
本発明ポリペプチドの第1のカテゴリーは配列表の配列番号1に示すアミノ酸配列を有するポリペプチドである。このポリペプチドは、公知の6PGLのアミノ酸配列とは大きく異なり、公知の3CMCのアミノ酸配列とは実質的に同一のアミノ酸配列を有するにもかかわらず、有効な6PGL活性を示し、一方、3CMC活性は示さない。
【0037】
本発明ポリペプチドの第2のカテゴリーは配列表の配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6PGLの機能を示すポリペプチドである。上記の配列相同性は、とりわけ85%以上であることが好ましい。
【0038】
〔ポリヌクレオチド〕
本発明ポリヌクレオチドの第1のカテゴリーは、配列表の配列番号1に示す塩基配列を有するポリヌクレオチドであって、これは前記した第1のカテゴリーに係るポリペプチドをコードしている。
【0039】
本発明のポリヌクレオチドの第2のカテゴリーは、以下の(1)及び(2)の一方又は双方に該当するポリヌクレオチドである。
【0040】
(1)前記した第1のカテゴリーに係るポリペプチドをコードするポリヌクレオチド。
【0041】
(2)上記の第1のカテゴリーに係るポリヌクレオチドについての相補的な塩基配列に対してストリンジェントな条件下でハイブリダイズする塩基配列を有し、6PGLの機能を示すポリペプチドをコードするポリヌクレオチド。
【0042】
〔組み換えベクター、形質転換体、ポリペプチドの製造方法〕
本発明の組み換えベクターは、本発明に係る前記いずれかのポリヌクレオチド(遺伝子)を含有する。
【0043】
本発明の形質転換体は、上記の組み換えベクターを宿主に導入してなるものである。宿主の種類は限定されず、バクテリア(Bacteria)、真菌(Eumycetes)、各種の酵母などの単細胞真核生物、又は動物あるいは植物の生細胞を任意に選択できるが、微生物が好ましく、特に大腸菌(E. coli)が好ましい。
【0044】
本発明に係るポリペプチドの製造方法は、上記の形質転換体を培養して6−ホスホグルコノラクトナーゼの機能を示すポリペプチドを取得するという方法である。
【0045】
一般的に形質転換体を利用する目的物の生産方法において認められることであるが、本発明のポリペプチドの製造方法においても、導入遺伝子の選択、導入すべき宿主の選択、発現ベクター等の導入手段とそれに適した DNA又はRNA の構築方法の選択、培地もしくはこれに対する添加物の種類や濃度の選択、形質転換体の培養条件あるいは生育条件の選択等の要因が、ポリペプチドの生産量に影響する場合がある。
【0046】
形質転換体の培養により生産された本発明のポリペプチドは、通常行われる細胞破砕物からの抽出だけでなく、場合によっては適当な抽出溶媒を用いて培養液からも直接に抽出できる。利用する宿主の種類によっては、ポリペプチドの少なくとも一部が宿主細胞内あるいは細胞表面に止まる場合があるが、細胞膜もしくは細胞壁の破壊や、適宜な抽出溶媒による抽出等の公知の各種操作を経て、採取することができる。
【0047】
本発明においては、少なくとも本発明のポリペプチドをコードするポリヌクレオチド(遺伝子)が宿主細胞に導入される。ここにおいて、「遺伝子を導入する」とは、遺伝子の機能を有するポリヌクレオチドを組換え核酸として宿主細胞に導入する全ての場合を含む。又、「ポリヌクレオチド」とは、1本鎖、2本鎖又は3本鎖のDNA DNA及び/又はRNAを言い、遺伝子の導入には、組み換えベクターによって導入する場合や、PCR フラグメント等で合成した核酸を用いて相同組換えによって導入する場合が含まれ得る。遺伝子は、より好ましくは、遺伝子の発現を強化する発現ベクターによって導入される。
【0048】
発現ベクターは、導入しようとする遺伝子を、その発現を強化する種々のDNA 断片又はRNA 断片と融合させたものである。好ましくは、発現ベクターは、遺伝子を恒常的又は誘導的に発現させるための転写プロモーターや、転写ターミネーター、組換え体選抜用マーカー遺伝子、エンハンサーを含み得る。一般的な発現ベクターの構築方法として、例えば、PCR 法等で調製した遺伝子断片を、適当な制限酵素とリガーゼを用いる既知の方法で発現ベクターに組み込むことができる。大腸菌(E. coli)での発現用の転写プロモーターとして、trp,lac ,trc ,tac 等を用いることができる。
【0049】
ベクターとしては、限定はされないが、大腸菌(E.
coli)を宿主とする場合に良く利用されるプラスミドpTRP、pSC101、pBR322、pHSG298、pVC18、pVC19、pTrc99A、pMal-c2、pGEX2T、pTV118N、pTV119N等を好ましく使用でき、その他にもS. cerevisiaeを宿主とする場合に良く利用されるpKG1、YEp13、YEp24、YCp50、pRS414、pRS415、pRS404、pAUR101等も利用でき、バシルス・ズブチリス(B. subtilis)を宿主とする場合に良く利用されるプラスミドpUB110、pC194等も利用できる。更に、pBI122、pBI1101その他の各種のものも限定なく使用できる。
【0050】
遺伝子を宿主細胞に導入するに当たり、種々の態様で宿主に適合した組換え核酸を利用することができる。例えば、大腸菌への外来遺伝子の導入法は、ハナハンの方法等の確立された幾つかの方法を利用できる。酵母への外来遺伝子の導入法は、リチウム法等の確立された幾つかの方法を利用できる。
【0051】
〔リン酸化酵素測定用試薬〕
本発明のリン酸化酵素測定用試薬は、具体的にはクレアチンキナーゼ(CK)測定用試薬又はピルビン酸キナーゼ(PK)測定用試薬であって、CK測定用試薬又はPK測定用試薬としての必須成分と共に、本発明に係る前記いずれかのポリペプチドを含有する測定用試薬である。リン酸化酵素測定用試薬には、上記の成分の他にも、緩衝液、賦活剤、防腐剤、安定剤等が含有され得る。
【0052】
前記したように、CK測定用試薬としての必須成分には、クレアチンリン酸、ADP、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD又はNADP、グルコース−6−リン酸脱水素酵素、マグネシウム塩類、SH試薬が含まれる。PK測定用試薬としての必須成分には、ホスホエノールピルビン酸、ADP、グルコース、ヘキソキナーゼ又はグルコキナーゼ、NAD又はNADP、グルコース−6−リン酸脱水素酵素、マグネシウム塩類が含まれる。
【0053】
上記の成分の内、ヘキソキナーゼ又はグルコキナーゼ、あるいはグルコース−6−リン酸脱水素酵素としては、それらの給源は限定されず、パン酵母その他の各種微生物由来のものや、動物由来のもの等を任意に選択して使用することができる。
【0054】
マグネシウム塩類としては、例えば、酢酸マグネシウム、硫酸マグネシウム等を使用することができる。
【0055】
SH試薬としては、ジチオスレイトール、N−アセチルシステイン、ジチオエリスリトール、メルカプトエタノール、チオグリコール酸、システイン等を使用することができる。
【0056】
クレアチンリン酸、ADP、グルコース、NAD又はNADP等は、既存のCK測定用試薬やPK測定用試薬に使用されているものを使用できる。
【0057】
(CK測定用試薬の実施形態例)
ヘキソキナーゼ :0.2〜20ユニット/ml
グルコース−6−リン酸脱水素酵素:0.2〜20ユニット/ml
本発明のポリペプチド :0.1〜15ユニット/ml
クレアチンリン酸 :5〜40mM
ADP :0.2〜10mM
NAD又はNADP :0.2〜10mM
グルコース :2〜100mM
マグネシウム塩類 :2〜15mM
SH試薬 :2〜50μM
EDTA :0.2〜10mM
(PK測定用試薬の実施形態例)
ヘキソキナーゼ :0.2〜20ユニット/ml
グルコース−6−リン酸脱水素酵素:0.2〜20ユニット/ml
本発明のポリペプチド :0.1〜15ユニット/ml
ホスホエノールピルビン酸 :5〜40mM
ADP :0.2〜10mM
NAD又はNADP :0.1〜10mM
グルコース :2〜100mM
マグネシウム塩類 :2〜15mM
SH試薬 :2〜50μM
EDTA :0.2〜10mM
【実施例】
【0058】
次に本発明の実施例を説明する。本発明の技術的範囲は、以下の実施例によって限定されない。実施例では、本発明に係るポリペプチドを、そのアミノ酸配列に鑑みて「本発明3−CMC」と呼ぶ。
【0059】
〔実施例1:本発明3−CMC発現系の構築〕
まず、ロイコノストック・メセンテロイデス属菌由来の本発明3−CMCを大腸菌で発現させるためにプラスミドを構築し、本発明3−CMCの遺伝子配列を設計した。
【0060】
本発明3−CMCを挿入したプラスミドpTRP−3CMCを、図2に示す構築図にしたがって作製した。まず、ロイコノストック・メセンテロイデス属菌の染色体DNAを鋳型にして、5’末端側(センスプライマー)及び3’末端側(アンチセンスプライマー)にEcoRI及びBamHI制限酵素部位を設けた下記に示すプライマーを用いてPCRを行ない、アガロース電気泳動により約1.1kbのDNA断片を確認した。PCR反応組成は、(50μLあたり)1U KOD plus polymerase(TOYOBO)、10pg 鋳型DNA、0.3μM センスプライマー、0.3μM アンチセンスプライマー、0.2mM dNTP Mix、1mM
MgSO4、1×バッファーにて行なった。PCR反応は、94℃/2分(変性)、58℃/30秒(アニーリング)、68℃/1分30秒(伸長)を30サイクル繰り返した。
【0061】
上記したセンスプライマー(3CMC−EcoRI−ATG)の塩基配列を配列表の配列番号3に示し、アンチセンスプライマー(3CMC−BamHI−TAA)の塩基配列を配列表の配列番号4に示す。
【0062】
得られたPCR産物を制限酵素EcoRI及びBamHI(タカラバイオ社製)で処理を行ない、アガロース電気泳動後、GFXTM
PCR DNA and
Gel Band Purification
Kit(GEヘルスケアバイオサイエンス社製)により回収した。本発明3−CMC断片は、LigaFastTM
Rapid DNA Ligation System(プロメガ社製)を用いて、予め制限酵素EcoRI及びBamHI(タカラバイオ社製)で処理した発現ベクターpTRP(2.9kb)に導入した。大腸菌JM109株に形質転換し、大腸菌組換え体pTRP−3CMC/JM109を得た。このロイコノストック・メセンテロイデス属菌由来の本発明3−CMCの塩基配列およびアミノ酸配列を配列表の配列番号1に示し、そのアミノ酸配列をあらためて配列表の配列番号2に示す。
【0063】
〔実施例2:本発明3−CMCの大量培養〕
形質転換体の高密度培養によるロイコノストック・メセンテロイデス属菌由来の本発明3−CMCの大量生産(フェドバッチ培養による高密度培養)を以下の方法で実施した。
【0064】
プラスミドpTRP−3CMCを形質転換した大腸菌JM109株について、16L New Brunswick Scientific Fermentor SF−116(Edison,NJ,U.S.A.)を用いて高密度培養を行なった。温度(37℃)、pH(7.2)、撹拌速度(500rpm)、通気量(15mL/min)の培養パラメーターは、ML−4100(
Multi−loop microprocessor controller )によって制御した。pHの調整は、10% アンモニア水を添加して行なった。
【0065】
一晩前培養した培養液(160mL)を、50μg/mLのアンピシリンを含むLB培地(8L)へ植菌して2時間培養を行ない、その後10時間目まで添加培地を連続的に合計2L加えながら培養を続けた。
【0066】
添加培地の組成は以下に示す通りである。グルコース(10%)、酵母エキス(15%)、MgSO4・7H2O(0.1%)、L−グルタミン酸(0.75%)、L−スレオニン(0.75%)、L−チロシン(0.04%)、L−ヒスチジン(0.4%)、L−メチオニン(0.4%)、pH7.4。
【0067】
培地の添加は、100mL/hの速度で開始し、2時間ごとに200mL/h、300mL/h、400mL/hの順で増加させて行なった。集菌は、12時間目に遠心分離(11,000g×20min)により行なった。菌体の増殖は、培養液の600nmでの吸光度を測定して調べた。その結果、プラスミドpTRP−3CMCで形質転換した大腸菌JM109株の高密度培養菌体を得ることができた。
【0068】
発現量を確認するため、得られた湿菌体5gを3mLの抽出バッファー(20mM リン酸カリウムバッファー pH7.5)で懸濁し、超音波破砕後(MISONIX社製 astrason ULTRASONIC PROCESSOTR XL)、遠心分離し(18,000×g、15分、4℃ BECKMAN社製 Model J2−21
Centrifuge)粗抽出液を調製した。得られた粗抽出液中の本発明3−CMC発現量は、約3200U/mgタンパクであった。
【0069】
本発明3−CMCの活性測定は次のような方法で行なった。MESバッファー (30mM、pH6.5)、グルコース−6−リン酸(0.26mM、ロシュ社製)、NAD+(0.26mM、オリエンタル酵母工業社製)から構成される反応液にグルコース−6−リン酸脱水素酵素(30U、オリエンタル酵母工業社製)添加したのち、25℃で340nmの吸光度が変化しなくなるまで反応させる。その後、酵素溶液を添加したのち、340nmの吸光度変化を測定し本発明3−CMC活性を算出した。また、この反応条件における1分間あたりの1μmolのNADHの生成量を1単位とし、上記酵素活性を本発明3−CMC活性とした。
〔実施例3:本発明3−CMCの精製〕
大量精製を行なうため、得られた湿菌体170gを20mMリン酸カリウムバッファーに懸濁したのち、DINO−MILL(Typ KDL)にて菌体破砕を行ない、得られた破砕画分を遠心分離し(18,000×g、15分、4℃
BECKMAN社製 Model J2−21
Centrifuge)粗抽出液を調製した。得られた粗抽出液を用いて以下の方法で精製を行なった。
【0070】
バッファーA(10mM リン酸カリウムバッファー
pH7.5)で平衡化したDEAE−Cellulofine A−500(生化学工業株式会社製)に通じ、バッファーAで洗浄後、0−0.3M
NaClのリニア・グラジエントで目的タンパク質を溶出させた。
【0071】
活性画分に最終40%飽和になるように硫酸アンモニウムを加え、1時間攪拌した後、バッファーB(10mM
K−リン酸バッファー pH7.5、40%飽和硫酸アンモニウム)で平衡化したPhenyl−Sepharose
6Fast Flow(GEヘルスケアバイオサイエンス社製)に通じ、バッファーBで洗浄後、40−0% 硫酸アンモニウムのリニア・グラジエントで目的タンパク質を溶出させた。得られた目的画分をSephadex G−25(GEヘルスケアバイオサイエンス社製)に通じた。最終的に比活性6000U/mgタンパクである組換えタンパク質の精製標品を得た。この精製標品は、SDS−PAGE後CBBR−250で染色した結果、約38,000のほぼ単一バンドを示した。
〔実施例4:クレアチンキナーゼ測定用試薬における応用評価〕
CK測定用試薬を以下の方法で調製した。まず、イミダゾールバッファー(pH 6.6、134mM)、G6PDH(オリエンタル酵母工業社製、118U/mL)、HK(オリエンタル酵母工業社製、237U/mL)、本発明3−CMC(21U/mL)、ADP(2.68mM)、NADP(2.68mM)、グルコース(26.8mM)、酢酸マグネシウム(13.4mM)、EDTA(2.68mM)、NAC(26.8mM)より構成されるR1試薬を調製した。さらに、イミダゾールバッファー(pH6.6、10mM)、CP(154mM)からなるR2試薬を調製した(実施例)。また、別にR1試薬から本発明3−CMCを抜いた比較用R1試薬も調製し、比較例とすることとした。
【0072】
別に、試料として、大腸菌で組み換えたヒト由来のクレアチンキナーゼである「組換えヒトCK−MM(オリエンタル酵母工業社製)」を使用した。上記で調製したR1試薬、R2試薬及び比較用R1試薬を用いて日立自動分析装置7170形にてCK活性を測定した。その結果、実施例では1分間当りの吸光度変化量が4,000U/Lまで直線的に変化しているのに対して、本発明3−CMC無添加(比較例)では1,600U/Lまでしか直線的に変化していないことがわかった(図3参照)。このように、本発明3−CMCを添加することにより、測定範囲が広がることが示唆された。
【産業上の利用可能性】
【0073】
本発明により、6PGL活性を示す新規で有用なポリペプチドと、その製造手段と、その利用形態とが提供される。
【特許請求の範囲】
【請求項1】
配列表の配列番号1に示すアミノ酸配列を有するポリペプチド。
【請求項2】
配列表の配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチド。
【請求項3】
配列表の配列番号1に示す塩基配列を有するポリヌクレオチド。
【請求項4】
以下の(1)及び(2)の一方又は双方に該当するポリヌクレオチド。
(1)請求項2に記載のポリペプチドをコードするポリヌクレオチド。
(2)請求項3に記載のポリヌクレオチドについての相補的な塩基配列に対してストリンジェントな条件下でハイブリダイズする塩基配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチドをコードするポリヌクレオチド。
【請求項5】
請求項3又は請求項4に記載のポリヌクレオチドを含有する組み換えベクター。
【請求項6】
請求項5に記載の組み換えベクターを宿主に導入してなる形質転換体。
【請求項7】
前記宿主が大腸菌(E.
coli)である請求項6に記載の形質転換体。
【請求項8】
請求項6又は請求項7に記載の形質転換体を培養して6−ホスホグルコノラクトナーゼの機能を示すポリペプチドを取得するポリペプチドの製造方法。
【請求項9】
クレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬としての必須成分と共に、請求項1又は請求項2に記載のポリペプチドを含有するリン酸化酵素測定用試薬。
【請求項1】
配列表の配列番号1に示すアミノ酸配列を有するポリペプチド。
【請求項2】
配列表の配列番号1に示すアミノ酸配列に対して80%以上の配列相同性を示すアミノ酸配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチド。
【請求項3】
配列表の配列番号1に示す塩基配列を有するポリヌクレオチド。
【請求項4】
以下の(1)及び(2)の一方又は双方に該当するポリヌクレオチド。
(1)請求項2に記載のポリペプチドをコードするポリヌクレオチド。
(2)請求項3に記載のポリヌクレオチドについての相補的な塩基配列に対してストリンジェントな条件下でハイブリダイズする塩基配列を有し、6−ホスホグルコノラクトナーゼの機能を示すポリペプチドをコードするポリヌクレオチド。
【請求項5】
請求項3又は請求項4に記載のポリヌクレオチドを含有する組み換えベクター。
【請求項6】
請求項5に記載の組み換えベクターを宿主に導入してなる形質転換体。
【請求項7】
前記宿主が大腸菌(E.
coli)である請求項6に記載の形質転換体。
【請求項8】
請求項6又は請求項7に記載の形質転換体を培養して6−ホスホグルコノラクトナーゼの機能を示すポリペプチドを取得するポリペプチドの製造方法。
【請求項9】
クレアチンキナーゼ測定用試薬又はピルビン酸キナーゼ測定用試薬としての必須成分と共に、請求項1又は請求項2に記載のポリペプチドを含有するリン酸化酵素測定用試薬。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2011−92113(P2011−92113A)
【公開日】平成23年5月12日(2011.5.12)
【国際特許分類】
【出願番号】特願2009−250039(P2009−250039)
【出願日】平成21年10月30日(2009.10.30)
【出願人】(000103840)オリエンタル酵母工業株式会社 (60)
【Fターム(参考)】
【公開日】平成23年5月12日(2011.5.12)
【国際特許分類】
【出願日】平成21年10月30日(2009.10.30)
【出願人】(000103840)オリエンタル酵母工業株式会社 (60)
【Fターム(参考)】
[ Back to top ]

