ポリマー粒子およびその使用
本発明は、ポリマー粒子およびその使用に関する。特に本発明は、細胞媒介性免疫応答を引き出すに際しての、ならびに細胞内病原体により引き起こされるものを含めて疾患または症状の処置または防止における、機能性ポリマー粒子、その産生方法および使用に関する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む方法。
【請求項2】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが被験者における免疫応答を引き出し得る少なくとも1つの抗原を結合し得る結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項3】
病原体に対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む方法。
【請求項4】
病原体に対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが被験者における免疫応答を引き出し得る少なくとも1つの抗原を結合し得る結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項5】
前記免疫応答が細胞媒介性免疫応答を含む請求項1〜4のいずれか一項に記載の方法。
【請求項6】
前記免疫応答が体液性応答を含む請求項1〜5のいずれか一項に記載の方法。
【請求項7】
前記被験者が病原体に感染するかまたは病原体に対して免疫化されている請求項1〜6のいずれか一項に記載の方法。
【請求項8】
免疫応答を引き出し得る抗原を結合し得る前記結合ドメインが内因性抗原と結合する請求項2または4〜7のいずれか一項に記載の方法。
【請求項9】
免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項10】
免疫応答を引き出し得る抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項11】
前記抗原が細胞媒介性免疫応答を引き出し得る請求項9または請求項10記載のポリマー粒子。
【請求項12】
前記抗原が体液性免疫応答を引き出し得る請求項9〜11のいずれか一項に記載のポリマー粒子。
【請求項13】
前記ポリマー粒子が2つ以上の異なる融合ポリペプチドを含む請求項9〜12のいずれか一項に記載のポリマー粒子。
【請求項14】
前記ポリマー粒子が、2つ以上の異なる抗原、または抗原を結合し得る2つ以上の異なる結合ドメインを含む請求項9〜13のいずれか一項に記載のポリマー粒子。
【請求項15】
前記ポリマー粒子が、免疫応答を引き出し得る少なくとも1つの抗原ならびに細胞媒介性免疫応答を引き出し得る抗原を結合し得る少なくとも1つの結合ドメインを含む請求項9〜14のいずれか一項に記載のポリマー粒子。
【請求項16】
前記ポリマー粒子がさらに、前記ポリマー粒子に結合されるかまたは組み入れられる少なくとも1つの物質を含む請求項9〜15のいずれか一項に記載のポリマー粒子。
【請求項17】
前記物質が抗原、アジュバントまたは免疫刺激分子、あるいはその任意の2つ以上の組合せである請求項16記載のポリマー粒子。
【請求項18】
多価である請求項9〜17のいずれか一項に記載のポリマー粒子。
【請求項19】
前記物質が架橋によりポリマー粒子と結合される請求項16〜18のいずれか一項に記載のポリマー粒子。
【請求項20】
それを必要とする被験者における免疫応答を引き出すための、または病原体に対して被験者を免疫化するための、またはそれを必要とする被験者における病原体からの感染を診断するための、免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項21】
それを必要とする被験者における免疫応答を引き出すための、または病原体に対して被験者を免疫化するための、またはそれを必要とする被験者における病原体からの感染を診断するための、免疫応答を引き出し得る抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項22】
前記抗原が、マイコバクテリウム属(例えば、ウシ型結核菌、ヒト型結核菌、ライ菌、カンサシ菌、鳥結核菌、ヨーネ菌、マイコバクテリウム種)、リステリア属(例えば、リステリア・モノサイトゲネス、リステリア種)、サルモネラ属(例えば、チフス菌)、エルシニア属(例えば、ペスト菌、エルシニア・エンテロコリチカ、仮性結核菌)、炭疽菌Bacillus anthracis、レジオネラ属(例えば、レジオネラ・ニューモフィラ、レジオネラ・ロングビーチェ、レジオネラ・ボゼマニ、レジオネラ種)、リケッチア属(例えば、ロッキー山紅斑熱リケッチア、リケッチア痘菌、ボタン熱菌、シベリアチックチフス菌、オーストラリアチックチフス菌、日本紅斑熱菌、アフリカダニ熱菌、発疹チフス菌、発疹熱菌、リケッチア種)、クラミジア属(肺炎クラミジア菌、クラミジア・トラコマチス、クラミジア種)、クラミドフィラ属(例えば、クラミドフィラ・シタッシ、クラミドフィラ流産菌)、連鎖球菌属(例えば、肺炎連鎖球菌、化膿連鎖球菌、B群連鎖球菌)、ブドウ球菌属(黄色ブドウ球菌)、例えばメチシリン耐性黄色ブドウ球菌(MRSA)、エーリキア属(例えば、エーリキア・シャフェンシス、エーリキア・ファゴサイトフィラ・ゲノ群、エーリキア種)、コクシエラ・バーネッティCoxiella burnetii、リーシュマニア種、トキソプラズマ・ゴンジイ、トリパノソーマ・クルージ、ヒストプラズマ種、野兎病菌Francisella tularensis、ならびにウイルス、例えばC型肝炎ウイルス、アデノウイルス、ピコルナウイルス、例えばコクサッキーウイルス、A型肝炎ウイルス、ポリオウイルス、ヘルペスウイルス、例えばエプスタイン・バーウイルス、単純ヘルペスウイルス1型、単純ヘルペスウイルス2型、ヒトサイトメガロウイルス、ヒトヘルペスウイルス8型、水痘帯状疱疹ウイルス、ヘパドナウイルス、例えばB型肝炎ウイルス、フラビウイルス、例えばC型肝炎ウイルス、黄熱病ウイルス、デング熱ウイルス、西ナイルウイルス、レトロウイルス、例えばヒト免疫不全ウイルス(HIV)、オルトミクソウイルス、例えばインフルエンザウイルス、パラミクソウイルス、例えば麻疹ウイルス、流行性耳下腺炎ウイルス、パラインフルエンザウイルス、呼吸器合胞体ウイルス、パピローマウイルス属、例えばパピローマウイルス、ラブドウイルス、例えば狂犬病ウイルス、トガウイルス、例えば風疹ウイルス、ならびにその他のウイルス、例えばワクシニアウイルス、アビポックスウイルス、アデノ随伴ウイルス、修飾ワクシニアウイルスアンカラ株、セムリキ森林ウイルス、天然痘ウイルスおよびコロナウイルス、あるいは上記抗原のいずれかの少なくとも1つの抗原性部分またはT細胞エピトープからなる群から選択される生物体からの抗原である請求項1〜21のいずれか一項に記載のポリマー粒子。
【請求項23】
前記少なくとも1つのポリマー粒子が請求項9〜22のいずれか一項に記載のポリマー粒子である請求項1〜8のいずれか一項に記載の方法。
【請求項24】
請求項9〜22のいずれか一項に記載のポリマー粒子を含む組成物。
【請求項25】
それを必要とする被験者における免疫応答を引き出すための、またはそれを必要とする被験者にワクチン接種するための、または病原体に対してそれを必要とする被験者を免疫化するための、またはそれを必要とする被験者における病原体からの感染を診断するための、請求項25記載の組成物。
【請求項26】
前記組成物がワクチンである請求項25または請求項26記載の組成物。
【請求項27】
それを必要とする被験者における免疫応答を引き出すために、またはそれを必要とする被験者にワクチン接種するために、または病原体に対してそれを必要とする被験者を免疫化するために、またはそれを必要とする被験者における病原体からの感染を診断するために適した医薬剤の製造における請求項9〜22のいずれか一項に記載のポリマー粒子の使用。
【請求項28】
前記医薬剤がワクチンである請求項27記載の使用。
【請求項29】
以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列;ならびに
免疫応答を引き出し得る抗原をコードする少なくとも1つの核酸配列、あるいは免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列
を含む発現構築物。
【請求項30】
前記粒子形成タンパク質をコードする少なくとも1つの核酸配列、ならびに免疫応答を引き出し得る抗原をコードする少なくとも1つの核酸配列、または免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列が、単一オープンリーディングフレームとして存在する請求項29記載の発現構築物。
【請求項31】
粒子形成タンパク質、ならびに免疫応答を引き出し得る抗原、または免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする請求項29または30記載の発現構築物。
【請求項32】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. (i)および(ii)の両方
をコードする核酸をさらに含む請求項29〜31のいずれか一項に記載の発現構築物。
【請求項33】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. 少なくとも1つのポリマーシンターゼ、または
iv. 免疫応答を引き出し得る少なくとも1つの抗原、または
v. 免疫応答を引き出し得る少なくとも1つの抗原を結合し得る少なくとも1つの結合ドメイン、または
vi. 前記i)〜v)のうちの1つ以上を含む融合タンパク質、または
vii. 前記i)〜vi)の任意の組合せ
をコードする核酸を含む請求項29〜32のいずれか一項に記載の発現構築物。
【請求項34】
前記抗原が細胞媒介性免疫応答を引き出し得る抗原である請求項29〜33のいずれか一項に記載の発現構築物。
【請求項35】
ポリマー粒子の産生方法であって、少なくとも1つの発現構築物を含む宿主細胞(ここで、前記少なくとも1つの発現構築物は、免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列を含む)を提供すること、ならびに前記発現構築物の発現に適した条件下で前記宿主細胞を保持すること、ならびに前記宿主細胞から前記ポリマー粒子を分離することを包含する方法。
【請求項36】
病原体からの感染の診断方法であって、請求項9〜22のいずれか一項に記載の少なくとも1つのポリマー粒子を被験者に投与すること、そして前記病原体の存在を示す応答を検出することを包含する方法。
【請求項37】
前記病原体の存在を示す前記応答が遅延型過敏応答である請求項36記載の方法。
【請求項38】
前記病原体の存在を示す前記応答が、前記被験者から得られる試料中の前記病原体に対する抗体の存在の検出である請求項36記載の方法。
【請求項39】
前記病原体の存在を示す前記応答が、前記試料中の前記病原体に応答性の免疫細胞の存在の検出である請求項36記載の方法。
【請求項40】
ポリマー粒子の産生方法であって、以下の:
少なくとも1つの発現構築物を含む宿主細胞を提供すること(ここで、前記少なくとも1つの発現構築物は、以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列、および
ヒト型結核菌抗原またはヒト型結核菌抗原結合ドメインをコードする少なくとも1つの核酸配列
を含む);
前記発現構築物の発現に適した条件下で前記宿主細胞を保持すること;そして
前記宿主細胞から前記ポリマー粒子を分離すること
を包含する方法。
【請求項41】
前記発現構築物が高コピー数ベクター中である請求項40記載の方法。
【請求項42】
粒子形成タンパク質をコードする前記少なくとも1つの核酸配列が強プロモーターと操作可能的に連結される請求項40記載の方法。
【請求項43】
前記宿主細胞が、ポリマーシンターゼの基質、または基質混合物、例えば単量体基質、または宿主により代謝されてポリマーシンターゼの基質を形成し得る前駆体基質の存在下で保持される請求項40記載の方法。
【請求項44】
前記宿主細胞が、以下の:
粒子形成タンパク質および少なくとも1つのヒト型結核菌抗原をコードする核酸配列を含む発現構築物;または
粒子形成タンパク質および少なくとも1つのヒト型結核菌抗原結合ドメインをコードする核酸配列を含む発現構築物;または
アジュバントをコードする核酸配列を含む発現構築物;または
少なくとも1つのヒト型結核菌抗原をコードする核酸配列を含む発現構築物
からなる群から選択される少なくとも2つの異なる発現構築物を含む請求項40記載の方法。
【請求項45】
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列がESAT−6をコードする請求項40記載の方法。
【請求項46】
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列がAg85Aをコードする請求項40記載の方法。
【請求項47】
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列がESAT−6およびAg85Aをコードする請求項40記載の方法。
【請求項48】
少なくとも1つのヒト型結核菌抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項49】
少なくとも1つのヒト型結核菌抗原結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項50】
2つ以上の異なる融合ポリペプチドを含む請求項48または請求項49記載のポリマー粒子。
【請求項51】
2つ以上の異なるヒト型結核菌抗原または2つ以上の異なるヒト型結核菌抗原結合ドメインを含む請求項50記載のポリマー粒子。
【請求項52】
少なくとも1つのヒト型結核菌抗原および少なくとも1つのヒト型結核菌抗原結合ドメインを含む請求項50または請求項51記載のポリマー粒子。
【請求項53】
前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項48〜52のいずれか一項に記載のポリマー粒子。
【請求項54】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項53記載のポリマー粒子。
【請求項55】
多価である請求項48〜54のいずれか一項に記載のポリマー粒子。
【請求項56】
前記物質が架橋により前記ポリマー粒子に結合される請求項53〜55のいずれか一項に記載のポリマー。
【請求項57】
ヒト型結核菌ESAT−6抗原を含む請求項48〜56のいずれか一項に記載のポリマー粒子。
【請求項58】
ヒト型結核菌Ag85A抗原を含む請求項48〜57のいずれか一項に記載のポリマー粒子。
【請求項59】
融合ポリペプチドのうちの少なくとも1つがESAT−6抗原およびAg85A抗原を含む請求項58記載のポリマー粒子。
【請求項60】
以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列;ならびに
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列、あるいはヒト型結核菌抗原結合ドメインをコードする少なくとも1つの核酸配列
を含む発現構築物。
【請求項61】
前記粒子形成タンパク質をコードする少なくとも1つの核酸配列、ならびにヒト型結核菌抗原をコードする少なくとも1つの核酸配列、またはヒト型結核菌抗原結合ドメインをコードする少なくとも1つの核酸配列が、単一オープンリーディングフレームとして存在する請求項60記載の発現構築物。
【請求項62】
粒子形成タンパク質、ならびにヒト型結核菌抗原またはヒト型結核菌抗原結合ドメインを含む融合ポリペプチドをコードする請求項60または61記載の発現構築物。
【請求項63】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. (i)および(ii)の両方
をコードする核酸をさらに含む請求項60〜62のいずれか一項に記載の発現構築物。
【請求項64】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. 少なくとも1つのポリマーシンターゼ、または
iv. 細胞媒介性免疫応答を引き出し得る少なくとも1つの抗原、または
v. 細胞媒介性免疫応答を引き出し得る少なくとも1つの抗原を結合し得る少なくとも1つの結合ドメイン、または
vi. 前記i)〜v)のうちの1つ以上を含む融合タンパク質、または
vii. 前記i)〜vi)の任意の組合せ
をコードする核酸を含む請求項60〜63のいずれか一項に記載の発現構築物。
【請求項65】
結核に対して被験者を免疫化する方法であって、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原と融合される粒子形成タンパク質を含む方法。
【請求項66】
結核に対して被験者を免疫化する方法であって、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項67】
被験者における免疫応答を引き出す方法であって、1つ以上の融合ポリペプチドを含むポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原と融合される粒子形成タンパク質を含む方法。
【請求項68】
被験者における免疫応答を引き出す方法であって、1つ以上の融合ポリペプチドを含むポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項69】
前記被験者が結核に感染する請求項65〜68のいずれか一項に記載の方法。
【請求項70】
前記被験者が結核に対して免疫化されている請求項65〜69のいずれか一項に記載の方法。
【請求項71】
前記ヒト型結核菌抗原結合ドメインが内因性ヒト型結核菌抗原と結合する請求項66または68〜70のいずれか一項に記載の方法。
【請求項72】
前記ポリマー粒子のうちの少なくとも1つが2つ以上の異なる融合ポリペプチドを含む請求項65〜71のいずれか一項に記載の方法。
【請求項73】
前記ポリマー粒子のうちの少なくとも1つが、2つ以上の異なるヒト型結核菌抗原または2つ以上の異なるヒト型結核菌抗原結合ドメインを含む請求項65〜72のいずれか一項に記載の方法。
【請求項74】
前記ポリマー粒子のうちの少なくとも1つが、少なくとも1つのヒト型結核菌抗原および少なくとも1つのヒト型結核菌抗原結合ドメインを含む請求項65〜73のいずれか一項に記載の方法。
【請求項75】
前記ポリマー粒子のうちの少なくとも1つが、前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項65〜74のいずれか一項に記載の方法。
【請求項76】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項75記載の方法。
【請求項77】
前記ポリマー粒子が多価である請求項65〜74のいずれか一項に記載の方法。
【請求項78】
前記物質が架橋により前記ポリマー粒子に結合される請求項75〜77のいずれか一項に記載の方法。
【請求項79】
前記ポリマー粒子のうちの少なくとも1つがヒト型結核菌ESAT−6抗原を含む請求項65〜78のいずれか一項に記載の方法。
【請求項80】
前記ポリマー粒子のうちの少なくとも1つがヒト型結核菌Ag85A抗原を含む請求項65〜79のいずれか一項に記載の方法。
【請求項81】
前記ポリマー粒子のうちの少なくとも1つがESAT−6抗原およびAg85A抗原を含む融合ポリペプチドのうちの少なくとも1つを含む請求項65〜80のいずれか一項に記載の方法。
【請求項82】
前記ポリマー粒子のうちの少なくとも1つが、Ag85B(MPT59)、Ag85B、Ag85C、MPT32、MPT51、MPT59、MPT63、MPT64、MPT83、MPB5、MPB59、MPB64、MTC28、Mtb2、Mtb8.4、Mtb9.9、Mtb32A、Mtb39、Mtb41、TB10.4、TB10C、TB11B、TB12.5、TB13A、TB14、TB15、TB15A、TB16、TB16A、TB17、TB18、TB21、TB20.6、TB24、TB27B、TB32、TB32A、TB33、TB38、TB40.8、TB51、TB54、TB64、CFP6、CFP7、CFP7A、CFP7B、CFP8A、CFP8B、CFP9、CFP10、CFP11、CFP16、CFP17、CFP19、CFP19A、CFP19B、CFP20、CFP21、CFP22、CFP22A、CFP23、CFP23A、CFP23B、CFP25、CFP25A、CFP27、CFP28、CFP28B、CFP29、CFP30A、CFP30B、CFP50、CWP32、hspX(アルファ−結晶)、APA、ツベルクリン精製タンパク質誘導体(PPD)、ST−CF、PPE68、LppX、PstS−1、PstS−2、PstS−3、HBHA、GroEL、GroEL2、GrpES、LHP、19kDa リポタンパク質、71kDa、RD1−ORF2、RD1−ORF3、RD1−ORF4、RD1−ORF5、RD1−ORF8、RD1−ORF9A、RD1−ORF9B、Rv1984c、Rv0577、Rv1827、BfrB、Tpx. Rv1352、Rv1810、PpiA、Cut2、FbpB、FbpA、FbpC、DnaK、FecB、Ssb、RplL、FixA、FixB、AhpC2、Rv2626c、Rv1211、Mdh、Rv1626、Adk、ClpP、SucD(Belisle et al、2005;US 7,037,510;US 2004/0057963;US 2008/0199493; US 2008/0267990)、あるいは前記抗原のいずれかの少なくとも1つの抗原性部分またはT細胞エピトープからなる群から選択されるヒト型結核菌抗原を含む請求項65〜81のいずれか一項に記載の方法。
【請求項83】
肝炎またはインフルエンザに対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項84】
肝炎またはインフルエンザに対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と結合し得る結合ドメインと融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項85】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項86】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原を結合し得る結合ドメインと融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項87】
前記免疫応答が細胞媒介性免疫応答である請求項83〜86のいずれか一項に記載の方法。
【請求項88】
肝炎またはインフルエンザからの感染の診断方法であって、請求項9〜22のいずれか一項に記載の少なくとも1つのポリマー粒子を被験者に投与すること、そして前記肝炎またはインフルエンザウイルスの存在を示す応答を検出することを包含する方法。
【請求項89】
前記肝炎またはインフルエンザウイルスの存在を示す前記応答が、遅延型過敏応答である請求項88記載の方法。
【請求項90】
前記肝炎またはインフルエンザウイルスの存在を示す前記応答が、前記試料中の前記肝炎抗原またはインフルエンザ抗原に対する抗体の存在の検出である請求項88記載の方法。
【請求項91】
前記肝炎またはインフルエンザウイルスの存在を示す前記応答が、前記試料中の前記肝炎またはインフルエンザウイルスに応答性の免疫細胞の存在の検出である請求項88記載の方法。
【請求項92】
前記被験者が肝炎またはインフルエンザに感染する請求項88〜91のいずれか一項に記載の方法。
【請求項93】
前記被験者が肝炎またはインフルエンザに対して免疫化されている請求項88〜92のいずれか一項に記載の方法。
【請求項94】
肝炎抗原またはインフルエンザ抗原を結合し得る前記結合ドメインが内因性肝炎抗原またはインフルエンザ抗原と結合する請求項89または91〜93のいずれか一項に記載の方法。
【請求項95】
前記ポリマー粒子のうちの少なくとも1つが2つ以上の異なる融合ポリペプチドを含む請求項88〜94のいずれか一項に記載の方法。
【請求項96】
前記ポリマー粒子のうちの少なくとも1つが、2つ以上の異なる肝炎抗原、または2つ以上のインフルエンザ抗原、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る2つ以上の異なる結合ドメインを含む請求項88〜95のいずれか一項に記載の方法。
【請求項97】
前記ポリマー粒子のうちの少なくとも1つが、少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原、および肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインを含む請求項88〜96のいずれか一項に記載の方法。
【請求項98】
前記ポリマー粒子のうちの少なくとも1つが、前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項88〜97のいずれか一項に記載の方法。
【請求項99】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項98記載の方法。
【請求項100】
前記ポリマー粒子のうちの少なくとも1つが多価である請求項88〜99のいずれか一項に記載の方法。
【請求項101】
前記物質が架橋により前記ポリマー粒子に結合される請求項98〜100のいずれか一項に記載のポリマー。
【請求項102】
前記ポリマー粒子のうちの少なくとも1つが、少なくとも1つの抗原、または少なくとも1つの抗原を結合し得る少なくとも1つの結合ドメインを含む請求項88〜101のいずれか一項に記載の方法であって、前記抗原が、ウイルス、例えばC型肝炎ウイルス、アデノウイルス、ピコルナウイルス、例えばコクサッキーウイルス、A型肝炎ウイルス、ポリオウイルス、ヘルペスウイルス、例えばエプスタイン・バーウイルス、単純ヘルペスウイルス1型、単純ヘルペスウイルス2型、ヒトサイトメガロウイルス、ヒトヘルペスウイルス8型、水痘帯状疱疹ウイルス、ヘパドナウイルス、例えばB型肝炎ウイルス、フラビウイルス、例えばC型肝炎ウイルス、オルトミクソウイルス、例えばインフルエンザウイルス、あるいは上記抗原のいずれかの少なくとも1つの抗原性部分またはT細胞エピトープからなる群から選択される生物体からである方法。
【請求項103】
ポリマー粒子の産生方法であって、以下の:
少なくとも1つの発現構築物を含む宿主細胞を提供すること(ここで、前記少なくとも1つの発現構築物は、以下の:
肝炎抗原またはインフルエンザ抗原をコードする少なくとも1つの核酸配列、あるいは
肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列
を含む);
前記発現構築物の発現に適した条件下で前記宿主細胞を保持すること;そして
前記宿主細胞から前記ポリマー粒子を分離すること
を包含する方法。
【請求項104】
少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項105】
肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項106】
2つ以上の異なる融合ポリペプチドを含む請求項104または請求項105記載のポリマー粒子。
【請求項107】
2つ以上の異なる肝炎抗原または2つ以上の異なるインフルエンザ抗原、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る2つ以上の異なる結合ドメインを含む請求項106記載のポリマー粒子。
【請求項108】
少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原、ならびに肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインを含む請求項106または請求項107記載のポリマー粒子。
【請求項109】
前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項104〜108のいずれか一項に記載のポリマー粒子。
【請求項110】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項109記載のポリマー粒子。
【請求項111】
多価である請求項104〜110のいずれか一項に記載のポリマー粒子。
【請求項112】
前記物質が架橋により前記ポリマー粒子に結合される請求項109〜111のいずれか一項に記載のポリマー粒子。
【請求項113】
それを必要とする被験者における細胞媒介性免疫応答を引き出すための、あるいは肝炎またはインフルエンザに対して被験者を免疫化するための、あるいはそれを必要とする被験者における肝炎またはインフルエンザからの感染を診断するための、少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項114】
それを必要とする被験者における細胞媒介性免疫応答を引き出すための、あるいは肝炎またはインフルエンザに対して被験者を免疫化するための、あるいはそれを必要とする被験者における肝炎またはインフルエンザからの感染を診断するための、肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項115】
それを必要とする被験者における細胞媒介性免疫応答を引き出すために、あるいは肝炎またはインフルエンザに対して被験者を免疫化するために、あるいはそれを必要とする被験者における肝炎またはインフルエンザからの感染を診断するために適切である医薬剤の製造における請求項104〜114のいずれか一項に記載のポリマー粒子の使用。
【請求項116】
以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列;ならびに
肝炎抗原またはインフルエンザ抗原をコードする少なくとも1つの核酸配列、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列
を含む発現構築物。
【請求項117】
前記粒子形成タンパク質をコードする少なくとも1つの核酸配列、ならびに肝炎抗原またはインフルエンザ抗原をコードする少なくとも1つの核酸配列、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列が、単一オープンリーディングフレームとして存在する請求項116記載の発現構築物。
【請求項118】
前記粒子形成タンパク質ならびに肝炎抗原またはインフルエンザ抗原、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインを含む融合ポリペプチドをコードする請求項116または117記載の発現構築物。
【請求項119】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. (i)および(ii)の両方
をコードする核酸をさらに含む請求項116〜118のいずれか一項に記載の発現構築物。
【請求項120】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. 少なくとも1つのポリマーシンターゼ、または
iv. 少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原、または
v. 少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原を結合し得る少なくとも1つの結合ドメイン、または
vi. 前記i)〜v)のうちの1つ以上を含む融合タンパク質、または
vii. 前記i)〜vi)の任意の組合せ
をコードする核酸を含む請求項116〜119のいずれか一項に記載の発現構築物。
【請求項1】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む方法。
【請求項2】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが被験者における免疫応答を引き出し得る少なくとも1つの抗原を結合し得る結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項3】
病原体に対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む方法。
【請求項4】
病原体に対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが被験者における免疫応答を引き出し得る少なくとも1つの抗原を結合し得る結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項5】
前記免疫応答が細胞媒介性免疫応答を含む請求項1〜4のいずれか一項に記載の方法。
【請求項6】
前記免疫応答が体液性応答を含む請求項1〜5のいずれか一項に記載の方法。
【請求項7】
前記被験者が病原体に感染するかまたは病原体に対して免疫化されている請求項1〜6のいずれか一項に記載の方法。
【請求項8】
免疫応答を引き出し得る抗原を結合し得る前記結合ドメインが内因性抗原と結合する請求項2または4〜7のいずれか一項に記載の方法。
【請求項9】
免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項10】
免疫応答を引き出し得る抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項11】
前記抗原が細胞媒介性免疫応答を引き出し得る請求項9または請求項10記載のポリマー粒子。
【請求項12】
前記抗原が体液性免疫応答を引き出し得る請求項9〜11のいずれか一項に記載のポリマー粒子。
【請求項13】
前記ポリマー粒子が2つ以上の異なる融合ポリペプチドを含む請求項9〜12のいずれか一項に記載のポリマー粒子。
【請求項14】
前記ポリマー粒子が、2つ以上の異なる抗原、または抗原を結合し得る2つ以上の異なる結合ドメインを含む請求項9〜13のいずれか一項に記載のポリマー粒子。
【請求項15】
前記ポリマー粒子が、免疫応答を引き出し得る少なくとも1つの抗原ならびに細胞媒介性免疫応答を引き出し得る抗原を結合し得る少なくとも1つの結合ドメインを含む請求項9〜14のいずれか一項に記載のポリマー粒子。
【請求項16】
前記ポリマー粒子がさらに、前記ポリマー粒子に結合されるかまたは組み入れられる少なくとも1つの物質を含む請求項9〜15のいずれか一項に記載のポリマー粒子。
【請求項17】
前記物質が抗原、アジュバントまたは免疫刺激分子、あるいはその任意の2つ以上の組合せである請求項16記載のポリマー粒子。
【請求項18】
多価である請求項9〜17のいずれか一項に記載のポリマー粒子。
【請求項19】
前記物質が架橋によりポリマー粒子と結合される請求項16〜18のいずれか一項に記載のポリマー粒子。
【請求項20】
それを必要とする被験者における免疫応答を引き出すための、または病原体に対して被験者を免疫化するための、またはそれを必要とする被験者における病原体からの感染を診断するための、免疫応答を引き出し得る少なくとも1つの抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項21】
それを必要とする被験者における免疫応答を引き出すための、または病原体に対して被験者を免疫化するための、またはそれを必要とする被験者における病原体からの感染を診断するための、免疫応答を引き出し得る抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項22】
前記抗原が、マイコバクテリウム属(例えば、ウシ型結核菌、ヒト型結核菌、ライ菌、カンサシ菌、鳥結核菌、ヨーネ菌、マイコバクテリウム種)、リステリア属(例えば、リステリア・モノサイトゲネス、リステリア種)、サルモネラ属(例えば、チフス菌)、エルシニア属(例えば、ペスト菌、エルシニア・エンテロコリチカ、仮性結核菌)、炭疽菌Bacillus anthracis、レジオネラ属(例えば、レジオネラ・ニューモフィラ、レジオネラ・ロングビーチェ、レジオネラ・ボゼマニ、レジオネラ種)、リケッチア属(例えば、ロッキー山紅斑熱リケッチア、リケッチア痘菌、ボタン熱菌、シベリアチックチフス菌、オーストラリアチックチフス菌、日本紅斑熱菌、アフリカダニ熱菌、発疹チフス菌、発疹熱菌、リケッチア種)、クラミジア属(肺炎クラミジア菌、クラミジア・トラコマチス、クラミジア種)、クラミドフィラ属(例えば、クラミドフィラ・シタッシ、クラミドフィラ流産菌)、連鎖球菌属(例えば、肺炎連鎖球菌、化膿連鎖球菌、B群連鎖球菌)、ブドウ球菌属(黄色ブドウ球菌)、例えばメチシリン耐性黄色ブドウ球菌(MRSA)、エーリキア属(例えば、エーリキア・シャフェンシス、エーリキア・ファゴサイトフィラ・ゲノ群、エーリキア種)、コクシエラ・バーネッティCoxiella burnetii、リーシュマニア種、トキソプラズマ・ゴンジイ、トリパノソーマ・クルージ、ヒストプラズマ種、野兎病菌Francisella tularensis、ならびにウイルス、例えばC型肝炎ウイルス、アデノウイルス、ピコルナウイルス、例えばコクサッキーウイルス、A型肝炎ウイルス、ポリオウイルス、ヘルペスウイルス、例えばエプスタイン・バーウイルス、単純ヘルペスウイルス1型、単純ヘルペスウイルス2型、ヒトサイトメガロウイルス、ヒトヘルペスウイルス8型、水痘帯状疱疹ウイルス、ヘパドナウイルス、例えばB型肝炎ウイルス、フラビウイルス、例えばC型肝炎ウイルス、黄熱病ウイルス、デング熱ウイルス、西ナイルウイルス、レトロウイルス、例えばヒト免疫不全ウイルス(HIV)、オルトミクソウイルス、例えばインフルエンザウイルス、パラミクソウイルス、例えば麻疹ウイルス、流行性耳下腺炎ウイルス、パラインフルエンザウイルス、呼吸器合胞体ウイルス、パピローマウイルス属、例えばパピローマウイルス、ラブドウイルス、例えば狂犬病ウイルス、トガウイルス、例えば風疹ウイルス、ならびにその他のウイルス、例えばワクシニアウイルス、アビポックスウイルス、アデノ随伴ウイルス、修飾ワクシニアウイルスアンカラ株、セムリキ森林ウイルス、天然痘ウイルスおよびコロナウイルス、あるいは上記抗原のいずれかの少なくとも1つの抗原性部分またはT細胞エピトープからなる群から選択される生物体からの抗原である請求項1〜21のいずれか一項に記載のポリマー粒子。
【請求項23】
前記少なくとも1つのポリマー粒子が請求項9〜22のいずれか一項に記載のポリマー粒子である請求項1〜8のいずれか一項に記載の方法。
【請求項24】
請求項9〜22のいずれか一項に記載のポリマー粒子を含む組成物。
【請求項25】
それを必要とする被験者における免疫応答を引き出すための、またはそれを必要とする被験者にワクチン接種するための、または病原体に対してそれを必要とする被験者を免疫化するための、またはそれを必要とする被験者における病原体からの感染を診断するための、請求項25記載の組成物。
【請求項26】
前記組成物がワクチンである請求項25または請求項26記載の組成物。
【請求項27】
それを必要とする被験者における免疫応答を引き出すために、またはそれを必要とする被験者にワクチン接種するために、または病原体に対してそれを必要とする被験者を免疫化するために、またはそれを必要とする被験者における病原体からの感染を診断するために適した医薬剤の製造における請求項9〜22のいずれか一項に記載のポリマー粒子の使用。
【請求項28】
前記医薬剤がワクチンである請求項27記載の使用。
【請求項29】
以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列;ならびに
免疫応答を引き出し得る抗原をコードする少なくとも1つの核酸配列、あるいは免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列
を含む発現構築物。
【請求項30】
前記粒子形成タンパク質をコードする少なくとも1つの核酸配列、ならびに免疫応答を引き出し得る抗原をコードする少なくとも1つの核酸配列、または免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列が、単一オープンリーディングフレームとして存在する請求項29記載の発現構築物。
【請求項31】
粒子形成タンパク質、ならびに免疫応答を引き出し得る抗原、または免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする請求項29または30記載の発現構築物。
【請求項32】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. (i)および(ii)の両方
をコードする核酸をさらに含む請求項29〜31のいずれか一項に記載の発現構築物。
【請求項33】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. 少なくとも1つのポリマーシンターゼ、または
iv. 免疫応答を引き出し得る少なくとも1つの抗原、または
v. 免疫応答を引き出し得る少なくとも1つの抗原を結合し得る少なくとも1つの結合ドメイン、または
vi. 前記i)〜v)のうちの1つ以上を含む融合タンパク質、または
vii. 前記i)〜vi)の任意の組合せ
をコードする核酸を含む請求項29〜32のいずれか一項に記載の発現構築物。
【請求項34】
前記抗原が細胞媒介性免疫応答を引き出し得る抗原である請求項29〜33のいずれか一項に記載の発現構築物。
【請求項35】
ポリマー粒子の産生方法であって、少なくとも1つの発現構築物を含む宿主細胞(ここで、前記少なくとも1つの発現構築物は、免疫応答を引き出し得る抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列を含む)を提供すること、ならびに前記発現構築物の発現に適した条件下で前記宿主細胞を保持すること、ならびに前記宿主細胞から前記ポリマー粒子を分離することを包含する方法。
【請求項36】
病原体からの感染の診断方法であって、請求項9〜22のいずれか一項に記載の少なくとも1つのポリマー粒子を被験者に投与すること、そして前記病原体の存在を示す応答を検出することを包含する方法。
【請求項37】
前記病原体の存在を示す前記応答が遅延型過敏応答である請求項36記載の方法。
【請求項38】
前記病原体の存在を示す前記応答が、前記被験者から得られる試料中の前記病原体に対する抗体の存在の検出である請求項36記載の方法。
【請求項39】
前記病原体の存在を示す前記応答が、前記試料中の前記病原体に応答性の免疫細胞の存在の検出である請求項36記載の方法。
【請求項40】
ポリマー粒子の産生方法であって、以下の:
少なくとも1つの発現構築物を含む宿主細胞を提供すること(ここで、前記少なくとも1つの発現構築物は、以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列、および
ヒト型結核菌抗原またはヒト型結核菌抗原結合ドメインをコードする少なくとも1つの核酸配列
を含む);
前記発現構築物の発現に適した条件下で前記宿主細胞を保持すること;そして
前記宿主細胞から前記ポリマー粒子を分離すること
を包含する方法。
【請求項41】
前記発現構築物が高コピー数ベクター中である請求項40記載の方法。
【請求項42】
粒子形成タンパク質をコードする前記少なくとも1つの核酸配列が強プロモーターと操作可能的に連結される請求項40記載の方法。
【請求項43】
前記宿主細胞が、ポリマーシンターゼの基質、または基質混合物、例えば単量体基質、または宿主により代謝されてポリマーシンターゼの基質を形成し得る前駆体基質の存在下で保持される請求項40記載の方法。
【請求項44】
前記宿主細胞が、以下の:
粒子形成タンパク質および少なくとも1つのヒト型結核菌抗原をコードする核酸配列を含む発現構築物;または
粒子形成タンパク質および少なくとも1つのヒト型結核菌抗原結合ドメインをコードする核酸配列を含む発現構築物;または
アジュバントをコードする核酸配列を含む発現構築物;または
少なくとも1つのヒト型結核菌抗原をコードする核酸配列を含む発現構築物
からなる群から選択される少なくとも2つの異なる発現構築物を含む請求項40記載の方法。
【請求項45】
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列がESAT−6をコードする請求項40記載の方法。
【請求項46】
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列がAg85Aをコードする請求項40記載の方法。
【請求項47】
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列がESAT−6およびAg85Aをコードする請求項40記載の方法。
【請求項48】
少なくとも1つのヒト型結核菌抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項49】
少なくとも1つのヒト型結核菌抗原結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項50】
2つ以上の異なる融合ポリペプチドを含む請求項48または請求項49記載のポリマー粒子。
【請求項51】
2つ以上の異なるヒト型結核菌抗原または2つ以上の異なるヒト型結核菌抗原結合ドメインを含む請求項50記載のポリマー粒子。
【請求項52】
少なくとも1つのヒト型結核菌抗原および少なくとも1つのヒト型結核菌抗原結合ドメインを含む請求項50または請求項51記載のポリマー粒子。
【請求項53】
前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項48〜52のいずれか一項に記載のポリマー粒子。
【請求項54】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項53記載のポリマー粒子。
【請求項55】
多価である請求項48〜54のいずれか一項に記載のポリマー粒子。
【請求項56】
前記物質が架橋により前記ポリマー粒子に結合される請求項53〜55のいずれか一項に記載のポリマー。
【請求項57】
ヒト型結核菌ESAT−6抗原を含む請求項48〜56のいずれか一項に記載のポリマー粒子。
【請求項58】
ヒト型結核菌Ag85A抗原を含む請求項48〜57のいずれか一項に記載のポリマー粒子。
【請求項59】
融合ポリペプチドのうちの少なくとも1つがESAT−6抗原およびAg85A抗原を含む請求項58記載のポリマー粒子。
【請求項60】
以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列;ならびに
ヒト型結核菌抗原をコードする少なくとも1つの核酸配列、あるいはヒト型結核菌抗原結合ドメインをコードする少なくとも1つの核酸配列
を含む発現構築物。
【請求項61】
前記粒子形成タンパク質をコードする少なくとも1つの核酸配列、ならびにヒト型結核菌抗原をコードする少なくとも1つの核酸配列、またはヒト型結核菌抗原結合ドメインをコードする少なくとも1つの核酸配列が、単一オープンリーディングフレームとして存在する請求項60記載の発現構築物。
【請求項62】
粒子形成タンパク質、ならびにヒト型結核菌抗原またはヒト型結核菌抗原結合ドメインを含む融合ポリペプチドをコードする請求項60または61記載の発現構築物。
【請求項63】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. (i)および(ii)の両方
をコードする核酸をさらに含む請求項60〜62のいずれか一項に記載の発現構築物。
【請求項64】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. 少なくとも1つのポリマーシンターゼ、または
iv. 細胞媒介性免疫応答を引き出し得る少なくとも1つの抗原、または
v. 細胞媒介性免疫応答を引き出し得る少なくとも1つの抗原を結合し得る少なくとも1つの結合ドメイン、または
vi. 前記i)〜v)のうちの1つ以上を含む融合タンパク質、または
vii. 前記i)〜vi)の任意の組合せ
をコードする核酸を含む請求項60〜63のいずれか一項に記載の発現構築物。
【請求項65】
結核に対して被験者を免疫化する方法であって、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原と融合される粒子形成タンパク質を含む方法。
【請求項66】
結核に対して被験者を免疫化する方法であって、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項67】
被験者における免疫応答を引き出す方法であって、1つ以上の融合ポリペプチドを含むポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原と融合される粒子形成タンパク質を含む方法。
【請求項68】
被験者における免疫応答を引き出す方法であって、1つ以上の融合ポリペプチドを含むポリマー粒子を、それを必要とする被験者に投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つのヒト型結核菌抗原結合ドメインと融合される粒子形成タンパク質を含む方法。
【請求項69】
前記被験者が結核に感染する請求項65〜68のいずれか一項に記載の方法。
【請求項70】
前記被験者が結核に対して免疫化されている請求項65〜69のいずれか一項に記載の方法。
【請求項71】
前記ヒト型結核菌抗原結合ドメインが内因性ヒト型結核菌抗原と結合する請求項66または68〜70のいずれか一項に記載の方法。
【請求項72】
前記ポリマー粒子のうちの少なくとも1つが2つ以上の異なる融合ポリペプチドを含む請求項65〜71のいずれか一項に記載の方法。
【請求項73】
前記ポリマー粒子のうちの少なくとも1つが、2つ以上の異なるヒト型結核菌抗原または2つ以上の異なるヒト型結核菌抗原結合ドメインを含む請求項65〜72のいずれか一項に記載の方法。
【請求項74】
前記ポリマー粒子のうちの少なくとも1つが、少なくとも1つのヒト型結核菌抗原および少なくとも1つのヒト型結核菌抗原結合ドメインを含む請求項65〜73のいずれか一項に記載の方法。
【請求項75】
前記ポリマー粒子のうちの少なくとも1つが、前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項65〜74のいずれか一項に記載の方法。
【請求項76】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項75記載の方法。
【請求項77】
前記ポリマー粒子が多価である請求項65〜74のいずれか一項に記載の方法。
【請求項78】
前記物質が架橋により前記ポリマー粒子に結合される請求項75〜77のいずれか一項に記載の方法。
【請求項79】
前記ポリマー粒子のうちの少なくとも1つがヒト型結核菌ESAT−6抗原を含む請求項65〜78のいずれか一項に記載の方法。
【請求項80】
前記ポリマー粒子のうちの少なくとも1つがヒト型結核菌Ag85A抗原を含む請求項65〜79のいずれか一項に記載の方法。
【請求項81】
前記ポリマー粒子のうちの少なくとも1つがESAT−6抗原およびAg85A抗原を含む融合ポリペプチドのうちの少なくとも1つを含む請求項65〜80のいずれか一項に記載の方法。
【請求項82】
前記ポリマー粒子のうちの少なくとも1つが、Ag85B(MPT59)、Ag85B、Ag85C、MPT32、MPT51、MPT59、MPT63、MPT64、MPT83、MPB5、MPB59、MPB64、MTC28、Mtb2、Mtb8.4、Mtb9.9、Mtb32A、Mtb39、Mtb41、TB10.4、TB10C、TB11B、TB12.5、TB13A、TB14、TB15、TB15A、TB16、TB16A、TB17、TB18、TB21、TB20.6、TB24、TB27B、TB32、TB32A、TB33、TB38、TB40.8、TB51、TB54、TB64、CFP6、CFP7、CFP7A、CFP7B、CFP8A、CFP8B、CFP9、CFP10、CFP11、CFP16、CFP17、CFP19、CFP19A、CFP19B、CFP20、CFP21、CFP22、CFP22A、CFP23、CFP23A、CFP23B、CFP25、CFP25A、CFP27、CFP28、CFP28B、CFP29、CFP30A、CFP30B、CFP50、CWP32、hspX(アルファ−結晶)、APA、ツベルクリン精製タンパク質誘導体(PPD)、ST−CF、PPE68、LppX、PstS−1、PstS−2、PstS−3、HBHA、GroEL、GroEL2、GrpES、LHP、19kDa リポタンパク質、71kDa、RD1−ORF2、RD1−ORF3、RD1−ORF4、RD1−ORF5、RD1−ORF8、RD1−ORF9A、RD1−ORF9B、Rv1984c、Rv0577、Rv1827、BfrB、Tpx. Rv1352、Rv1810、PpiA、Cut2、FbpB、FbpA、FbpC、DnaK、FecB、Ssb、RplL、FixA、FixB、AhpC2、Rv2626c、Rv1211、Mdh、Rv1626、Adk、ClpP、SucD(Belisle et al、2005;US 7,037,510;US 2004/0057963;US 2008/0199493; US 2008/0267990)、あるいは前記抗原のいずれかの少なくとも1つの抗原性部分またはT細胞エピトープからなる群から選択されるヒト型結核菌抗原を含む請求項65〜81のいずれか一項に記載の方法。
【請求項83】
肝炎またはインフルエンザに対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項84】
肝炎またはインフルエンザに対して被験者を免疫化する方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含む少なくとも1つのポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と結合し得る結合ドメインと融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項85】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項86】
被験者における免疫応答を引き出す方法であって、それを必要とする被験者に、1つ以上の融合ポリペプチドを含むポリマー粒子を投与することを包含する方法であり、前記融合ポリペプチドのうちの少なくとも1つが少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原を結合し得る結合ドメインと融合される粒子形成タンパク質、好ましくはポリマーシンターゼを含む方法。
【請求項87】
前記免疫応答が細胞媒介性免疫応答である請求項83〜86のいずれか一項に記載の方法。
【請求項88】
肝炎またはインフルエンザからの感染の診断方法であって、請求項9〜22のいずれか一項に記載の少なくとも1つのポリマー粒子を被験者に投与すること、そして前記肝炎またはインフルエンザウイルスの存在を示す応答を検出することを包含する方法。
【請求項89】
前記肝炎またはインフルエンザウイルスの存在を示す前記応答が、遅延型過敏応答である請求項88記載の方法。
【請求項90】
前記肝炎またはインフルエンザウイルスの存在を示す前記応答が、前記試料中の前記肝炎抗原またはインフルエンザ抗原に対する抗体の存在の検出である請求項88記載の方法。
【請求項91】
前記肝炎またはインフルエンザウイルスの存在を示す前記応答が、前記試料中の前記肝炎またはインフルエンザウイルスに応答性の免疫細胞の存在の検出である請求項88記載の方法。
【請求項92】
前記被験者が肝炎またはインフルエンザに感染する請求項88〜91のいずれか一項に記載の方法。
【請求項93】
前記被験者が肝炎またはインフルエンザに対して免疫化されている請求項88〜92のいずれか一項に記載の方法。
【請求項94】
肝炎抗原またはインフルエンザ抗原を結合し得る前記結合ドメインが内因性肝炎抗原またはインフルエンザ抗原と結合する請求項89または91〜93のいずれか一項に記載の方法。
【請求項95】
前記ポリマー粒子のうちの少なくとも1つが2つ以上の異なる融合ポリペプチドを含む請求項88〜94のいずれか一項に記載の方法。
【請求項96】
前記ポリマー粒子のうちの少なくとも1つが、2つ以上の異なる肝炎抗原、または2つ以上のインフルエンザ抗原、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る2つ以上の異なる結合ドメインを含む請求項88〜95のいずれか一項に記載の方法。
【請求項97】
前記ポリマー粒子のうちの少なくとも1つが、少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原、および肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインを含む請求項88〜96のいずれか一項に記載の方法。
【請求項98】
前記ポリマー粒子のうちの少なくとも1つが、前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項88〜97のいずれか一項に記載の方法。
【請求項99】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項98記載の方法。
【請求項100】
前記ポリマー粒子のうちの少なくとも1つが多価である請求項88〜99のいずれか一項に記載の方法。
【請求項101】
前記物質が架橋により前記ポリマー粒子に結合される請求項98〜100のいずれか一項に記載のポリマー。
【請求項102】
前記ポリマー粒子のうちの少なくとも1つが、少なくとも1つの抗原、または少なくとも1つの抗原を結合し得る少なくとも1つの結合ドメインを含む請求項88〜101のいずれか一項に記載の方法であって、前記抗原が、ウイルス、例えばC型肝炎ウイルス、アデノウイルス、ピコルナウイルス、例えばコクサッキーウイルス、A型肝炎ウイルス、ポリオウイルス、ヘルペスウイルス、例えばエプスタイン・バーウイルス、単純ヘルペスウイルス1型、単純ヘルペスウイルス2型、ヒトサイトメガロウイルス、ヒトヘルペスウイルス8型、水痘帯状疱疹ウイルス、ヘパドナウイルス、例えばB型肝炎ウイルス、フラビウイルス、例えばC型肝炎ウイルス、オルトミクソウイルス、例えばインフルエンザウイルス、あるいは上記抗原のいずれかの少なくとも1つの抗原性部分またはT細胞エピトープからなる群から選択される生物体からである方法。
【請求項103】
ポリマー粒子の産生方法であって、以下の:
少なくとも1つの発現構築物を含む宿主細胞を提供すること(ここで、前記少なくとも1つの発現構築物は、以下の:
肝炎抗原またはインフルエンザ抗原をコードする少なくとも1つの核酸配列、あるいは
肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列
を含む);
前記発現構築物の発現に適した条件下で前記宿主細胞を保持すること;そして
前記宿主細胞から前記ポリマー粒子を分離すること
を包含する方法。
【請求項104】
少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項105】
肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項106】
2つ以上の異なる融合ポリペプチドを含む請求項104または請求項105記載のポリマー粒子。
【請求項107】
2つ以上の異なる肝炎抗原または2つ以上の異なるインフルエンザ抗原、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る2つ以上の異なる結合ドメインを含む請求項106記載のポリマー粒子。
【請求項108】
少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原、ならびに肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインを含む請求項106または請求項107記載のポリマー粒子。
【請求項109】
前記ポリマー粒子に結合されるかまたは組入れられる少なくとも1つの物質またはその組合せをさらに含む請求項104〜108のいずれか一項に記載のポリマー粒子。
【請求項110】
前記物質が抗原、アジュバントまたは免疫刺激分子である請求項109記載のポリマー粒子。
【請求項111】
多価である請求項104〜110のいずれか一項に記載のポリマー粒子。
【請求項112】
前記物質が架橋により前記ポリマー粒子に結合される請求項109〜111のいずれか一項に記載のポリマー粒子。
【請求項113】
それを必要とする被験者における細胞媒介性免疫応答を引き出すための、あるいは肝炎またはインフルエンザに対して被験者を免疫化するための、あるいはそれを必要とする被験者における肝炎またはインフルエンザからの感染を診断するための、少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原と融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項114】
それを必要とする被験者における細胞媒介性免疫応答を引き出すための、あるいは肝炎またはインフルエンザに対して被験者を免疫化するための、あるいはそれを必要とする被験者における肝炎またはインフルエンザからの感染を診断するための、肝炎抗原またはインフルエンザ抗原を結合し得る少なくとも1つの結合ドメインと融合される粒子形成タンパク質を含む1つ以上の融合ポリペプチドを含むポリマー粒子。
【請求項115】
それを必要とする被験者における細胞媒介性免疫応答を引き出すために、あるいは肝炎またはインフルエンザに対して被験者を免疫化するために、あるいはそれを必要とする被験者における肝炎またはインフルエンザからの感染を診断するために適切である医薬剤の製造における請求項104〜114のいずれか一項に記載のポリマー粒子の使用。
【請求項116】
以下の:
粒子形成タンパク質をコードする少なくとも1つの核酸配列;ならびに
肝炎抗原またはインフルエンザ抗原をコードする少なくとも1つの核酸配列、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列
を含む発現構築物。
【請求項117】
前記粒子形成タンパク質をコードする少なくとも1つの核酸配列、ならびに肝炎抗原またはインフルエンザ抗原をコードする少なくとも1つの核酸配列、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインをコードする少なくとも1つの核酸配列が、単一オープンリーディングフレームとして存在する請求項116記載の発現構築物。
【請求項118】
前記粒子形成タンパク質ならびに肝炎抗原またはインフルエンザ抗原、あるいは肝炎抗原またはインフルエンザ抗原を結合し得る結合ドメインを含む融合ポリペプチドをコードする請求項116または117記載の発現構築物。
【請求項119】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. (i)および(ii)の両方
をコードする核酸をさらに含む請求項116〜118のいずれか一項に記載の発現構築物。
【請求項120】
以下の:
i. 少なくとも1つのチオラーゼ、または
ii. 少なくとも1つのレダクターゼ、または
iii. 少なくとも1つのポリマーシンターゼ、または
iv. 少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原、または
v. 少なくとも1つの肝炎抗原または少なくとも1つのインフルエンザ抗原を結合し得る少なくとも1つの結合ドメイン、または
vi. 前記i)〜v)のうちの1つ以上を含む融合タンパク質、または
vii. 前記i)〜vi)の任意の組合せ
をコードする核酸を含む請求項116〜119のいずれか一項に記載の発現構築物。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


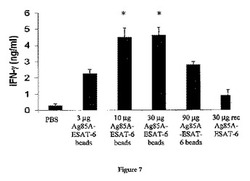
【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公表番号】特表2013−500329(P2013−500329A)
【公表日】平成25年1月7日(2013.1.7)
【国際特許分類】
【出願番号】特願2012−522328(P2012−522328)
【出願日】平成22年7月29日(2010.7.29)
【国際出願番号】PCT/IB2010/053465
【国際公開番号】WO2011/013097
【国際公開日】平成23年2月3日(2011.2.3)
【出願人】(512023063)
【出願人】(512023074)
【出願人】(512023085)
【出願人】(512023096)
【Fターム(参考)】
【公表日】平成25年1月7日(2013.1.7)
【国際特許分類】
【出願日】平成22年7月29日(2010.7.29)
【国際出願番号】PCT/IB2010/053465
【国際公開番号】WO2011/013097
【国際公開日】平成23年2月3日(2011.2.3)
【出願人】(512023063)

【出願人】(512023074)

【出願人】(512023085)

【出願人】(512023096)

【Fターム(参考)】
[ Back to top ]

