ポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体及びシリカ系無機構造体の製造方法
【課題】 製造コストが低く、有機物質の廃棄物が発生しないプロセスによる、多様な形状を有するポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体及びこれらを熱焼成して得られるシリカ系無機構造体の簡便な製造方法を提供すること。
【解決手段】 直鎖状ポリエチレンイミン骨格を有するポリマーの水性媒体中で形成する結晶性会合体を反応場として用い、それに予めpHを調製した水ガラスを混合させることによる、該ポリマーとシリカとがナノメートルオーダーで複合されたナノ構造体の製造方法、さらにはそのポリマー/シリカ複合構造体中に金属イオン、数ナノメートルオーダーの金属ナノ粒子が含まれるポリマー/金属類/シリカ複合構造体の製造方法、及びこれらを熱焼成して得られるシリカ系無機構造体の製造方法。
【解決手段】 直鎖状ポリエチレンイミン骨格を有するポリマーの水性媒体中で形成する結晶性会合体を反応場として用い、それに予めpHを調製した水ガラスを混合させることによる、該ポリマーとシリカとがナノメートルオーダーで複合されたナノ構造体の製造方法、さらにはそのポリマー/シリカ複合構造体中に金属イオン、数ナノメートルオーダーの金属ナノ粒子が含まれるポリマー/金属類/シリカ複合構造体の製造方法、及びこれらを熱焼成して得られるシリカ系無機構造体の製造方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、直鎖状ポリエチレンイミン骨格を有するポリマーの水性媒体中で形成する結晶性会合体を反応場として用い、それに水ガラスを混合させることによる、該ポリマーとシリカとがナノメートルオーダーで複合された構造体(以下、本発明においてナノ構造体と称す)の製造方法、さらにはそのポリマー/シリカ複合構造体中に金属イオン、数ナノメートルオーダーの金属ナノ粒子(以下、金属イオンと金属ナノ粒子をまとめて金属類と称す。)が含まれるポリマー/金属類/シリカ複合ナノ構造体の製造方法、及びこれらを熱焼成して得られるシリカ系無機構造体の製造方法に関する。
【背景技術】
【0002】
珪素は地殻上で酸素に次ぐ第二番目を誇る豊富な存在であり、自然界の石英、水晶、オパール、雲母、珪藻などはよく知られている珪素の酸化物である。規則的な空間構造やパターン構造を有するシリカ材料の創製は、材料科学分野において大きな研究課題であり、これに関する技術開発が大きく進歩している。
【0003】
シリカ材料にある種の構造を発現させるための方法としては、分子組織体をテンプレート(鋳型)として用い、その組織体周辺でシリカを固定化する方法が、該分野において広く用いられている。このテンプレートには、界面活性剤(例えば、非特許文献1参照。)、ブロックポリマー(例えば、非特許文献2参照。)、ウイルス、バクテリア(例えば、非特許文献3参照。)などが使用されており、これらをテンプレートとして合成されるナノ空洞を有するシリカ、例えば、MCM−41(メソポーラス)シリーズの材料は、触媒、電子材料、ナノフィルター、バイオ工学などへの応用が可能である。これら材料に関しては、より精密な構造の制御へ向けた研究がなされており、空洞の大きさ、並び方、あるいは球状のシリカ中での空洞制御などが検討されている。
【0004】
一方、このようなナノ空洞の制御と並行して、シリカの形状をナノからミクロンさらにはマクロスケールまでに制御する技術が注目されている。これは生態系でのバイオシリカに啓発されたことに一因がある(例えば、非特許文献4参照。)。自然界のバイオシリカとしては、珪藻類を取りあげることができる。珪藻類は、その体形をシリカで構成し、その上に複雑かつ精密な形状とパターンとを有する。そのシリカの構築には、タンパク質、またはポリペプチドが関わる(例えば、非特許文献5参照。)が、これらは、シリカの固定化反応の触媒として作用したり、シリカ形状成長の足場を提供したりする。このような生体系バイオシリカの形成において、欠かせない化学構造の一つが長鎖ポリアミンである。ポリアミンは、ペプチド構造に組み込まれることで働くか、または独自に一定分子量のポリアミンとしてポリペプチドと共に働くものである(例えば、非特許文献6参照。)。
【0005】
上記したように、ポリアミンの存在下で、例えば、珪酸、珪酸ナトリウムまたはアルコキシシラン等のシリカソースを、室温でシリカゲルとして固定化できることは、ここ数年広く知られるようになった。しかし、それらは通常ポリアミンを水中溶解させ、その水溶液中でのシリカソースのゾルゲル反応により行われるものであるため、シリカゲルが形成できても、そのシリカゲルの形状を制御することはできず、規則的な構造を有するシリカゲルの実現は困難であった。
【0006】
上記の方法とは異なり、本発明者らは、2級アミンで構成された直鎖状ポリエチレンイミンが水性媒体中で発現する特異な分子会合体をシリカ析出の反応場として用いることにより、シリカナノファイバーに代表されるさまざまな形状を有するシリカ含有ナノ構造体およびその製造法を見いだした(特許文献1〜4参照。)。これらの発明では、直鎖状ポリエチレンイミン骨格を有するポリマーを水中にて自発的に会合させた後、その会合体液中にアルコキシシラン類のシラン化合物を混合させると、そのシラン類が選択的にポリマー会合体表面で加水分解的に縮合され、ポリマーとシリカとが複合したナノ構造体が生成することを見出したことにより完成した発明である。このプロセスはシリカ系ナノ構造体の構造制御に高効率であるが、用いるシリカソースとしてはアルコキシシラン類である。従って、アルコキシシラン類が高価であることから、製造するナノ構造体の製造コストが高く、さらにはアルコキシシラン類の加水分解によりアルコール類が生じ、この廃棄処理のために、環境負荷への問題点も避けられない。シリカのナノ構造体を安価で、かつ無炭素の水ガラス等で構築することができれば、工業的には重要な意義を有する。
【0007】
【非特許文献1】C.T.Kresge et al.,Nature,1992,359,p.710
【非特許文献2】A.Monnier et al.,Science,1993,261,p1299
【非特許文献3】S.A.Davis et al.,Nature,1997,385,p420
【非特許文献4】W.E.G.Muller Ed.,Silicon Biomineralizattion:Biology−Biotechnology−Molecular Biology−Biotechnology,2003,Springer
【非特許文献5】N.Kroger et al.,Science,1999,286,p.1129
【非特許文献6】N.Kroger et al.,Proc.Natl.Acad.Sci.USA,2000,97,p14133
【特許文献1】特開2005−264421号公報
【特許文献2】特開2005−336440号公報
【特許文献3】特開2006−063097号公報
【特許文献4】特開2007−051056号公報
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明が解決しようとする課題は、製造コストが低く、有機物質の廃棄物が発生しないプロセスによる、多様な形状を有するポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体及びこれらを熱焼成して得られるシリカ系無機構造体の簡便な製造方法を提供することにある。
【課題を解決するための手段】
【0009】
上記の課題を解決するために、本発明者らは鋭意検討を行ったところ、特定のポリマーが水中で形成する結晶性会合体をテンプレートとし、それが安定に存在する条件下で予めpH調整した水ガラスと混合すると、水ガラスのケイ素が該会合体周辺でシリカとして析出し、有機物の発生がなく、ポリマーとシリカとが複合したナノ構造体が得られることを見出し、本発明を完成した。
【0010】
即ち、本発明は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を水性媒体中で結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合して、シリカ(b1)を析出させることを特徴とするポリマー/シリカ複合ナノ構造体の製造方法、更に該ポリマー/シリカ複合ナノ構造体に金属イオン(c1)又は金属ナノ粒子(c2)が含まれるポリマー/金属類/シリカ複合ナノ構造体の製造方法、及びこれらを熱焼成して得られるシリカ系無機構造体の製造方法を提供するものである。
【発明の効果】
【0011】
本発明の製造方法は、工業的に最も安く、汎用性の高い水ガラスをシリカソースとして用い、簡便で且つ有機物の廃棄がない方法でポリマー/シリカ複合ナノ構造体およびポリマー/金属類/シリカ複合ナノ構造体を得るものである。この製造方法から得られるナノ構造体は、ナノ次元のファイバー、ラメラのようなユニット構造が3次元空間に大きく広がり、さまざまな複雑形状と構造を有する、シリカを主成分とするシリカ系材料である。
【0012】
本発明で得られるポリマー/シリカ複合ナノ構造体は、シリカ内部に直鎖状ポリエチレンイミン骨格を有するポリマーが含まれるので、そのポリマーが固有する機能を生かすことができる。例えば、ポリエチレンイミンは金属イオンとポリマー金属錯体を形成することができるので、本発明のポリマー/シリカ複合ナノ構造体は金属イオンの濃縮・分離、金属錯体の固定に用いることができ、ポリマー/金属類/シリカ複合ナノ構造体を形成する。
【0013】
また、ポリエチレンイミンは酸性有機化合物や酸性の官能基を有する生体ポリマー等と酸/塩基複合体を形成することができるので、本発明のポリマー/シリカ複合ナノ構造体は多くの酸性物質の分離または固定に用いることができる。
【0014】
また、ポリエチレンイミンは殺菌、抗ウイルスの機能を有するので、本発明で得られるポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体は、例えば、防菌剤、殺菌剤、抗ウイルス、化粧品添加剤として用いることができる。
【0015】
更に、本発明で得られるポリマー/シリカ複合ナノ構造体は、シリカナノファイバーの絡み合いで構成する特徴を有するので、水、空気の浄化用ナノフィルターとして用いることもできる。
【0016】
又、前記ポリマー/シリカ複合ナノ構造体又はポリマー/金属類/シリカ複合ナノ構造体を焼成して得られるシリカ系無機構造体は、高い比表面積を有するためフィルター、触媒支持体、フィラー等に好適に用いることができるものである。
【発明を実施するための最良の形態】
【0017】
本発明は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を水性媒体中で結晶性会合体とし、これをテンプレートとして用いて、pHを8.5以上に調整した水ガラス(B)からシリカ(b1)を該会合体周辺に析出させることにより、ポリマー(A)とシリカ(b1)とを複合させ、ナノ構造体を得ることを特徴とする。
【0018】
シリカを含有する構造体の製造において、有機物質の環境への廃棄をなくすには、アルコキシシラン類を用いない反応を実現しなければならない。三次元空間で一定の形状と構造を有するシリカ含有ナノ構造体を構築するには、これは非常に困難である。
【0019】
ポリマーとシリカとが複合しているナノ構造体は、基本的にはポリマーが媒体中で形成する特定の構造が、シリカを析出させるテンプレートとして機能することによって生成するものである。そのポリマーテンプレートの形状が安定であれば安定であるほど、得られるポリマー/シリカ複合ナノ構造体は明確なナノ構造を有することになる。
【0020】
具体的に言えば、シリカをある特定形状に作り上げるためには、下記の三つの条件、(1)形状を誘導するポリマーテンプレートが安定に形成すること、(2)そのテンプレートがシリカソースを濃縮できること、(3)そのテンプレートがシリカソースの重合を促進させること、などをそろえる必要がある。この時、アルコキシシランをシリカソースに用いた場合には、比較的広範なポリマーに対してこの条件を満たすため、構造が制御された複合ナノ構造体を得るには好都合であった。アルコキシシランの代わりのシリカソースとしては、水溶性ケイ酸塩(珪酸ナトリウム、珪酸カリウムなど)または水分散シリカコロイド粒子といったものしかない。このようなシリカソースを用いると、アルコキシシランの加水分解によって生じるアルコール類の環境への廃棄問題は解決できると考えられる。しかしながら、水溶性ケイ酸塩類を用いる場合、特に濃厚溶液である水ガラスは水溶性であるが、水性媒体の微小な変化(例えば、pHの変動や添加物の混入等)により不安定化し、自発的に無規則なシリカの固まりとして析出してしまうため、ポリマーテンプレートと水ガラスとが安定に混合できない限り、該テンプレート表面にケイ酸塩を濃縮してシリカを析出させ、ポリマー/シリカ複合ナノ構造体を得ることは不可能である。
【0021】
本発明においては、上記の課題を解決するため、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)が水性媒体中で形成する結晶性会合体をテンプレートとして使用する。直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)は水中可溶であるが、室温では結晶性の分子会合体として存在する。ここにpHを8.5以上に調整した水ガラス(B)が混合されたときにも、この結晶性会合体の安定性が維持され、且つ該結晶性会合体を含有する水性媒体中におけるケイ酸塩自身の沈殿を防ぐことが可能であり、ケイ酸塩はこの結晶性会合体をテンプレートとして、選択的に該テンプレート周辺でシリカ(酸化ケイ素)(b1)として析出することを見出したことにより、本発明を完成するに至った。
【0022】
本発明で得られるナノ構造体は、直鎖状ポリエチレンイミン骨格を有するポリマー(A)とシリカ(b1)とが複合されたものであり、シリカ(b1)の固さにより、ナノ構造が空間に広がるさまざまな形状を有する。
【0023】
[直鎖状ポリエチレンイミン骨格を有するポリマー]
本発明でいう直鎖状ポリエチレンイミン骨格(a1)とは、二級アミンのエチレンイミン単位を主たる構造単位とするポリマー骨格である。該骨格(a1)中においては、エチレンイミン単位以外の構造単位が存在していてもよいが、結晶性会合体を形成させるためには、該ポリマー骨格(a1)中の一定鎖長が連続的なエチレンイミン単位であることが好ましい。該直鎖状ポリエチレンイミン骨格(a1)の長さは、該骨格を有するポリマー(A)が結晶を形成できる範囲であれば特に制限されないが、好適に結晶を形成するためには、該骨格(a1)部分のエチレンイミン単位の繰り返し単位数が10以上であることが好ましく、20〜10,000の範囲であることが特に好ましい。
【0024】
本発明において使用するポリマー(A)は、その構造中に直鎖状ポリエチレンイミン骨格(a1)を有するものであればよく、ポリマー(A)全体の形状が線状、星状または櫛状であっても、水または水と親水性有機溶媒との混合溶媒である水性媒体(以下、両者を併せて水性媒体という)中で結晶性会合体を与えることができる。
【0025】
また、これら線状、星状または櫛状のポリマーは、直鎖状ポリエチレンイミン骨格(a1)のみからなるものであっても、直鎖状ポリエチレンイミン骨格(a1)からなるブロック(以下、ポリエチレンイミンブロックと略記する。)と他のポリマーブロックとのブロックコポリマーからなるものであってもよい。他のポリマーブロックとしては、例えば、ポリエチレングリコール、ポリプロピオニルエチレンイミン、ポリアクリルアミドなどの水溶性のポリマーブロック、あるいは、ポリスチレン、ポリオキサゾリン類のポリフェニルオキサゾリン、ポリオクチルオキサゾリン、ポリドデシルオキサゾリン、ポリアクリレート類のポリメチルメタクリレート、ポリブチルメタクリレートなどの疎水性のポリマーブロック等を挙げることができる。これら他のポリマーブロックとのブロックコポリマーとすることで、ポリマーから形成する結晶性会合体の形状や得られるナノ構造体の特性を調整することができる。
【0026】
直鎖状ポリエチレンイミン骨格を有するポリマー(A)が、ブロックコポリマーである場合の該ポリマー(A)中における直鎖状ポリエチレンイミン骨格(a1)の割合は、結晶性会合体を形成できる範囲であれば特に制限されないが、好適に該会合体を形成するためには、ポリマー(A)中の直鎖状ポリエチレンイミン骨格(a1)の割合が40モル%以上であることが好ましく、50モル%以上であることがさらに好ましい。
【0027】
上記直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)は、その前駆体となるポリオキサゾリン類からなる直鎖状の骨格を有するポリマー(以下、前駆体ポリマーと略記する。)を、酸性条件下またはアルカリ条件下で加水分解することで容易に得ることができる。従って、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の線状、星状、または櫛状などの形状は、この前駆体ポリマーの形状を制御することで容易に設計することができる。また、重合度や末端構造も、前駆体ポリマーの重合度や末端機能団を制御することで容易に調整できる。さらに、直鎖状ポリエチレンイミン骨格(a1)を有するブロックコポリマーを形成する場合には、前駆体ポリマーをブロックコポリマーとし、該前駆体中のポリオキサゾリン類からなる直鎖状の骨格を選択的に加水分解することで得ることができる。
【0028】
前駆体ポリマーは、オキサゾリン類のモノマーを使用して、カチオン型の重合法、あるいは、マクロモノマー法などの合成方法により合成が可能であり、合成方法や開始剤を適宜選択することにより、線状、星状、あるいは櫛状などの各種形状の前駆体ポリマーを合成できる。
【0029】
ポリオキサゾリン類からなる直鎖状の骨格を形成するモノマーとしては、メチルオキサゾリン、エチルオキサゾリン、メチルビニルオキサゾリン、フェニルオキサゾリンなどのオキサゾリンモノマーを使用できる。
【0030】
重合開始剤としては、分子中に塩化アルキル基、臭化アルキル基、ヨウ化アルキル基、トルエンスルホニルオキシ基、あるいはトリフルオロメチルスルホニルオキシ基などの官能基を有する化合物を使用できる。これら重合開始剤は、多くのアルコール類化合物の水酸基を他の官能基に変換させることで得られる。なかでも、官能基変換として、臭素化、ヨウ素化、トルエンスルホン酸化、およびトリフルオロメチルスルホン酸化されたものは重合開始効率が高いため好ましく、特に臭化アルキル基、トルエンスルホン酸アルキル基とすることが好ましい。
【0031】
また、ポリ(エチレングリコール)の末端水酸基を臭素あるいはヨウ素に変換したもの、またはトルエンスルホニル基に変換したものを重合開始剤として使用することもできる。その場合、ポリ(エチレングリコール)の重合度は5〜100の範囲であることが好ましく、10〜50の範囲であれば特に好ましい。
【0032】
また、カチオン開環リビング重合開始能を有する官能基を有し、かつ光による発光機能、エネルギー移動機能、電子移動機能を有するポルフィリン骨格、フタロシアニン骨格、またはピレン骨格のいずれかの骨格を有する色素類は、得られるポリマー(A)及びナノ構造体に特殊な機能を付与することができる。
【0033】
線状の前駆体ポリマーは、上記オキサゾリンモノマーを1価または2価の官能基を有する重合開始剤により重合することで得られる。このような重合開始剤としては、例えば、塩化メチルベンゼン、臭化メチルベンゼン、ヨウ化メチルベンゼン、トルエンスルホン酸メチルベンゼン、トリフルオロメチルスルホン酸メチルベンゼン、臭化メタン、ヨウ化メタン、トルエンスルホン酸メタンまたはトルエンスルホン酸無水物、トリフルオロメチルスルホン酸無水物、5−(4−ブロモメチルフェニル)−10,15,20−トリ(フェニル)ポルフィリン、またはブロモメチルピレンなどの1価のもの、ジブロモメチルベンゼン、ジヨウ化メチルベンゼン、ジブロモメチルビフェニレン、またはジブロモメチルアゾベンゼンなどの2価のものが挙げられる。また、ポリ(メチルオキサゾリン)、ポリ(エチルオキサゾリン)、または、ポリ(メチルビニルオキサゾリン)などの工業的に使用されている線状のポリオキサゾリンを、そのまま前駆体ポリマーとして使用することもできる。
【0034】
星状の前駆体ポリマーは、上記したようなオキサゾリンモノマーを3価以上の官能基を有する重合開始剤により重合することで得られる。3価以上の重合開始剤としては、例えば、トリブロモメチルベンゼンなどの3価のもの、テトラブロモメチルベンゼン、テトラ(4−クロロメチルフェニル)ポルフィリン、テトラブロモエトキシフタロシアニンなどの4価のもの、ヘキサブロモメチルベンゼン、テトラ(3,5−ジトシリルエチルオキシフェニル)ポルフィリンなどの5価以上のものが挙げられる。
【0035】
櫛状の前駆体ポリマーを得るためには、多価の重合開始基を有する線状のポリマーを用いて、該重合開始基からオキサゾリンモノマーを重合させることにより得られるが、例えば、線状のエポキシ樹脂やポリビニルアルコールなどの側鎖に水酸基を複数有するポリマーの水酸基を、臭素やヨウ素等でハロゲン化するか、あるいはトルエンスルホニル基に変換させた後、該変換部分を重合開始基として用いることでも得ることができる。
【0036】
また、櫛状の前駆体ポリマーを得る方法として、ポリアミン型重合停止剤を用いることもできる。例えば、一価の重合開始剤を用い、オキサゾリンを重合させ、そのポリオキサゾリンの末端をポリエチレンイミン、ポリビニルアミン、ポリプロピルアミンなどのポリアミンのアミノ基に結合させることで、櫛状のポリオキサゾリンを得ることができる。
【0037】
上記により得られる前駆体ポリマーのポリオキサゾリン類からなる直鎖状の骨格部分の加水分解は、酸性条件下またはアルカリ条件下のいずれの条件下でもよい。酸性条件下での加水分解は、例えば、塩酸水溶液中で前駆体ポリマーを加熱下で攪拌することにより、ポリエチレンイミンの塩酸塩を得ることができる。得られた塩酸塩を過剰のアンモニウム水で処理することで、塩基性のポリエチレンイミン骨格を有するポリマーの結晶粉末を得ることができる。用いる塩酸水溶液は、濃塩酸でも、1mol/L程度の水溶液でもよいが、加水分解を効率的に行うには、5mol/Lの塩酸水溶液を用いることが望ましい。また、反応温度は80℃前後が望ましい。
【0038】
アルカリ条件下での加水分解は、例えば、水酸化ナトリウム水溶液を用いることで、ポリオキサゾリン類からなる骨格をポリエチレンイミン骨格に変換させることができる。アルカリ条件下で反応させた後、反応液を透析膜にて洗浄することで、過剰な水酸化ナトリウムを除去し、ポリエチレンイミン骨格を有するポリマーの結晶粉末を得ることができる。用いる水酸化ナトリウムの濃度は1〜10mol/Lの範囲であればよく、より効率的な反応を行うには3〜5mol/Lの範囲であることが好ましい。また、反応温度は80℃前後が好ましい。
【0039】
酸性条件下またはアルカリ条件下での加水分解における、酸またはアルカリの使用量としては、前駆体ポリマー中のオキサゾリン単位に対し、1〜10当量でよく、反応効率の向上と後処理の簡便化のためには、3当量程度とすることが好ましい。
【0040】
上記加水分解により、前駆体ポリマー中のポリオキサゾリン類からなる直鎖状の骨格が、直鎖状ポリエチレンイミン骨格(a1)となり、該ポリエチレンイミン骨格(a1)を有するポリマー(A)が得られる。
【0041】
また、直鎖状ポリエチレンイミンブロックと他のポリマーブロックとのブロックコポリマーを形成する場合には、前駆体ポリマーをポリオキサゾリン類からなる直鎖状のポリマーブロックと、他のポリマーブロックとからなるブロックコポリマーとし、該前駆体ポリマー中のポリオキサゾリン類からなる直鎖状のブロックを選択的に加水分解することで得ることができる。
【0042】
他のポリマーブロックが、ポリ(N−プロピオニルエチレンイミン)などの水溶性ポリマーブロックである場合には、ポリ(N−プロピオニルエチレンイミン)が、ポリ(N−ホルミルエチレンイミン)やポリ(N−アセチルエチレンイミン)に比べて、有機溶媒への溶解性が高いことを利用してブロックコポリマーを形成することができる。即ち、2−オキサゾリンまたは2−メチル−2−オキサゾリンを、前記した重合開始化合物の存在下でカチオン開環リビング重合した後、得られたリビングポリマーに、さらに2−エチル−2−オキサゾリンを重合させることによって、ポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとからなる前駆体ポリマーを得る。該前駆体ポリマーを水に溶解させ、該水溶液にポリ(N−プロピオニルエチレンイミン)ブロックを溶解する水とは非相溶の有機溶媒を混合して攪拌することによりエマルジョンを形成する。該エマルジョンの水相に、酸またはアルカリを添加することによりポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックを優先的に加水分解させることにより、直鎖状ポリエチレンイミンブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとを有するブロックコポリマーを形成できる。
【0043】
ここで使用する重合開始化合物の価数が1および2の場合には、直鎖状のブロックコポリマーとなり、それ以上の価数であれば星型のブロックコポリマーが得られる。また、前駆体ポリマーを多段のブロックコポリマーとすることで、得られるポリマーも多段のブロック構造とすることも可能である。
【0044】
[結晶性会合体]
上記直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)は、一次構造中の直鎖状ポリエチレンイミン骨格(a1)が、水性媒体中で結晶性を発現することにより該ポリマー(A)の結晶を誘導する。該ポリマー結晶は、水性媒体の存在下でのポリマー結晶同士の物理的な結合により三次元網目構造を有するヒドロゲルを形成することもでき、さらにポリマー結晶同士を架橋剤で架橋することにより化学的な架橋結合を有する架橋ヒドロゲルを形成することもできる。
【0045】
従来広く使用されてきたポリエチレンイミンは、環状エチレンイミンの開環重合により得られる分岐状ポリマーであり、その一次構造には一級アミン、二級アミン、三級アミンが存在する。従って、分岐状ポリエチレンイミンは水溶性であるが、結晶性は持たないため、分岐状ポリエチレンイミンを用いてヒドロゲルを作るためには、架橋剤による共有結合により網目構造を与えなくてはならない。しかしながら本発明に使用するポリマーが骨格として有する直鎖状ポリエチレンイミンは、二級アミンだけで構成されており、該二級アミン型の直鎖状ポリエチレンイミンは水溶性でありながら、優れた結晶性を有する。
【0046】
このような、直鎖状ポリエチレンイミンの結晶は、そのポリマーのエチレンイミン単位に含まれる結晶水数により、ポリマー結晶構造が大きく異なることが知られている(Y.Chatani et al.、Macromolecules、1981年、第14巻、p.315−321参照)。無水のポリエチレンイミンは二重螺旋構造を特徴とする結晶構造を優先するが、モノマー単位に2分子の水が含まれると、ポリマーはzigzag構造を特徴とする結晶体に成長することが知られている。実際、水中から得られる直鎖状ポリエチレンイミンの結晶は一つのモノマー単位に2分子水を含む結晶であり、その結晶は室温状態では水中不溶である。
【0047】
本発明における直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の結晶性会合体は、上記の場合と同様に直鎖状ポリエチレンイミン骨格(a1)の結晶発現により形成されるものであり、ポリマー形状が線状、星状、または櫛状などの形状であっても、一次構造に直鎖状ポリエチレンイミン骨格(a1)を有していれば、ポリマー(A)の結晶性会合体が得られる。
【0048】
本発明におけるポリマー(A)の結晶性会合体の存在は、例えば、X線散乱により確認でき、広角X線回折計(WAXS)における2θ角度値で20°,27°,28°にて散乱ピークを示す。
【0049】
また、本発明におけるポリマー(A)の結晶の示差走査熱量計(DSC)における融点は、該直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の構造にも依存するが、概ねその融点が45〜90℃で現れる。
【0050】
本発明におけるポリマー(A)の結晶性会合体は、その結晶を構成するポリマー(A)の幾何学的構造や、分子量、一次構造中に導入する非エチレンイミン部分、さらにはポリマー結晶の形成条件などの影響により各種形状を取り得ることができ、例えば束状、ブラシ状、星状などの形状を有する。
【0051】
上記結晶性会合体は、5〜30nm程度のナノメートルオーダーの繊維状構造を基本ユニットとするものであり、該繊維状構造表面に存在するフリーなエチレンイミン鎖により、繊維状構造同士が水素結合による物理的な結合で繋がれて空間に配置され、上記したような三次元形状に成長する。
【0052】
本発明の結晶性会合体は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)が室温の水に不溶である性質を利用し、該直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の水中での溶解−結晶変換により得ることができる。
【0053】
例えば、まず直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を一定量水性媒体中に分散し、該分散液を加熱することにより、ポリマー(A)の透明な溶液を得る。次いで、加熱状態のポリマー(A)の水性溶液を室温に冷やすことにより結晶性会合体が得られる。この際、ポリマー濃度が高いほど、結晶性会合体はアイスクリームのような状態を有し、多様な形状に造形させることが可能である。
【0054】
上記ポリマーの水性溶液の加熱温度は100℃以下が好ましく、90〜95℃の範囲であることがより好ましい。また、ポリマーの水性溶液中のポリマー含有量(濃度)は、特に限定されないが、0.01〜20質量%の範囲であることが好ましく、安定形状の結晶体からなる結晶性会合体を得るためには0.1〜10質量%の範囲がさらに好ましい。このように、本発明においては、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を使用すると、ごく少量のポリマー濃度でも結晶性会合体を形成することができる。
【0055】
上記ポリマーの水性溶液の温度を室温(25℃)まで低下させる過程により、得られる結晶性会合体中の結晶形状を調整することができる。例えば、該水性溶液を80℃に1時間保持した後、1時間かけて60℃にし、該温度でさらに1時間保持する。その後1時間かけて40℃まで低下させた後、自然に室温まで下げることで、水溶液の水が流動性をなくした状態のヒドロゲル結晶体を得ることができる。また、上記ポリマーの水性溶液を一気に氷点の氷り水、または氷点下のメタノール/ドライアイス、あるいはアセトン/ドライアイスの冷媒液にて冷却させた後、その状態のものを室温(25℃)の恒温槽にて保持させることで結晶性会合体を得ることができる。さらには、上記のポリマーの水性溶液を室温の恒温槽または室温の空気環境にて、室温まで温度を低下させることでも、結晶性会合体を得ることができる。
【0056】
上記ポリマーの水性溶液の温度を低下させる工程は、得られる結晶性会合体の形状に強く影響を与えるため、上記異なる工程により得られる結晶性会合体の形態は同一ではない。
【0057】
上記により得られる結晶性会合体は、室温中では不溶状態を保つが、結晶融点以上に加熱すると結晶が解離し、透明な溶液に変化してしまう。それを室温に戻すと再び結晶性会合体になる。従って、会合体を可逆的に変化させることが可能である。
【0058】
結晶性会合体の調整時に、他の水溶性ポリマーを加えることで、水溶性ポリマーを含有する結晶性会合体が得られる。該水溶性ポリマーとしては、例えば、ポリエチレングリコール、ポリビニルアルコール、ポリビニルピロリドン、ポリアクリルアミド、ポリ(N−イソプロピルアクリルアミド)、ポリヒドロキシエチルアクリレート、ポリメチルオキサゾリン、ポリエチルオキサゾリンなどをあげることができる。
【0059】
水溶性ポリマーの含有量は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の質量に対し、0.1〜5倍の範囲であることが好ましく、0.5〜2倍の範囲であればより好ましい。
【0060】
上記水溶性ポリマーを含有させることによっても、結晶会合体の形態を変えることができ、単純な系と異なる形態の結晶会合体を与えることができる。
【0061】
上記方法で得られた結晶性会合体を、ポリエチレンイミンのアミノ基と反応する官能基を2個以上を含む化合物で処理することで、会合体中のポリマー同士を化学結合でリンクさせて架橋化させることができる。
【0062】
前記アミノ基と室温状態で反応できる官能基を2個以上を含む化合物としては、アルデヒド類架橋剤、エポキシ類架橋剤、酸クロリド類、酸無水物、エステル類架橋剤を挙げることができる。アルデヒド類架橋剤としては、例えば、マロニルアルデヒド、スクシニルアルデヒド、グルタリルアルデヒド、フタロイルアルデヒド、イソフタロイルアルデヒド、テレフタロイルアルデヒドなどがあげられる。また、エポキシ類架橋剤としては、例えば、ポリエチレングリコールジグリシジルエーテル、ビスフェノールAジグリシジルエーテル、グリシジルクロライド、グリシジルブロマイドなどがあげられる。酸クロリド類としては、例えば、マロニル酸クロリド、スクシニル酸クロリド、グルタリル酸クロリド、フタロイル酸クロリド、イソフタロイル酸クロリド、テレフタロイル酸クロリドなどがあげられる。また、酸無水物としては、例えば、フタル酸無水物、スクシニル酸無水物、グルタリル酸無水物などがあげられる。また、エステル類架橋剤としては、マロニル酸メチルエステル、スクシニル酸メチルエステル、グルタリル酸メチルエステル、フタロイル酸メチルエステル、ポリエチレングリコールカルボン酸メチルエステルなどがあげられる。
【0063】
架橋反応は、得られた結晶性会合体を架橋剤の溶液に浸す方法にでも、架橋剤溶液を結晶性会合体中に加える方法でも可能である。この際、架橋剤は系内での浸透圧変化と共に、会合体内部へも浸透し、そこでポリマー(A)同士を水素結合で繋いだり、エチレンイミンの窒素原子との化学反応を引き起こしたりする。
【0064】
架橋反応は、結晶性会合体表面のフリーなエチレンイミンとの反応でも進行するが、それを保つためには、結晶性会合体の融点以下の温度で反応を行うことが望ましく、さらには架橋反応を室温で行うことが最も望ましい。
【0065】
架橋反応を室温で進行させる場合には、結晶性会合体を架橋剤溶液と混合した状態で放置しておくことで、架橋ヒドロゲルを得ることができる。架橋反応させる時間は、数分から数日でよく、概ね一晩放置することで好適に架橋が進行する。
【0066】
架橋剤量は、用いるポリエチレンイミン骨格(a1)を有するポリマー(A)中のエチレンイミンユニットのモル数に対し、0.05〜20モル%であればよく、それが1〜10モル%であればもっと好適である。
【0067】
[シリカソース]
本発明ではシリカソースとして、水ガラス(B)を用いる。水ガラス(ケイ酸ナトリウムまたはケイ酸リチウム)としては、一般式Na2O・xSiO2またはLi2O・xSiO2で示されるものであればよく、特に式中x=1,2,3であれば好適に用いることができる。
【0068】
上の式で示される水ガラス(B)は通常水溶性であるが、その安定性はpHに敏感に依存し、非常に狭いpH値の範囲でしか安定溶液にならない。例えば、珪酸ナトリウムの水溶液は、その水溶液のpHが6.5以上8.5未満では急速に固まり、構造上無規則のシリカゲルになる可能性が高い。本発明の製造方法では、水ガラス(B)を安定化させた状態で用いなければならない。そのためには、水ガラス(B)又は水ガラス(B)の水溶液のpHを8.5以上にすることを必須とする。高度な構造制御のためには、水ガラス(B)又は水ガラスの水溶液のpHを9〜11にすることがさらに好ましい。
【0069】
また、本発明の製造方法では、水ガラス(B)を予め0.01〜2.0モル/Lの範囲に希釈した水溶液として用いることが好ましく、特にポリマー(A)の結晶性会合体と混合した際の安定性を保持しやすい点から、0.1〜1.0モル/Lにすることが好ましい。
【0070】
[ポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体]
本発明で得られるポリマー/シリカ複合ナノ構造体は、上記のポリマー(A)の結晶性会合体の水性分散液またはヒドロゲル中に、予めpH調整をしておいた、シリカソースである水ガラス(B)又はその水溶液を混合し、その混合物を室温〜50℃の条件下で放置することにより容易に得ることができる。
【0071】
該ナノ構造体を与える上記混合物中、水ガラス(B)がシリカ(b1)へ変換するゾルゲル反応は、ポリマー(A)が形成する結晶性会合体が解いてない状態で進行させなければならない。即ち、シリカ析出反応は水性媒体中の任意の場所では起こらず、結晶性会合体の表面にて選択的に進行させる。これを満たす前提であれば、ナノ構造体生成の反応条件を任意に設定することができる。
【0072】
結晶性会合体の水性分散液またはヒドロゲルと、水ガラス(B)又はその水溶液を混合する工程において、水ガラス(B)又はその水溶液のpH、および濃度を調整することで、結晶性会合体を不溶状態に維持することができる。該pHは前述のように8.5以上にすることが必須であり、9〜11の範囲に調整することがより好ましい。濃度は0.1〜1.0モル/Lの範囲であることがより好ましい。
【0073】
また、上記混合工程において、用いるポリマー(A)中のエチレンイミンユニットに対し、シリカソースのケイ素の量を過剰とすれば好適にナノ構造体を形成できる。過剰の範囲として、エチレンイミンユニットに対しケイ素が10〜1000倍当量の範囲であることが好ましい。
【0074】
また、結晶会合体を形成する際、水性媒体中のポリマー(A)の濃度は、該ポリマー(A)中に含まれる直鎖状ポリエチレンイミン骨格(a1)の量を基準に、0.1〜30質量%にすることが好ましく、複合ナノ構造体の構造をもっとも有効に制御するためには、その濃度を0.5〜10質量%にすることが望ましい。
【0075】
シリカ(b1)の析出反応の時間は数分から数十時間まで様々であるが、基本的に10分〜10時間でよく、反応効率を上げることから、反応時間を30分〜5時間に設定すればさらに好適である。また、析出反応時の温度としては、結晶性会合体の融点以下の温度であれば好ましく設定できるが、基本的には70℃以下の温度で反応を行うことが望ましい。
【0076】
本発明で得られるポリマー/シリカ複合ナノ構造体は、多様な形状を有することが大きな特徴であるが、その形状は結晶性会合体の形状の拡大的な複写である。従って、シリカ(b1)の析出前に、水性媒体中でポリマー(A)の結晶を成長させ、結晶性会合体の形状を調整することにより得られるナノ構造体の形状を制御できる。
【0077】
得られるポリマー/シリカ複合ナノ構造体の形状は、マクロ構造的には様々な三次元形状に調整できる。これら複合体の大きさは数μm〜数mm程度の大きさとすることができるが、この大きさの形状は、基本ユニットと見られる20〜50nm太さの繊維状またはラメラ状複合体の会合と空間配置から形成された三次元形状である。この基本ユニットとなる20〜50nm太さの繊維状またはラメラ状複合体には数ナノ大きさの結晶性会合体が含まれる。
【0078】
これらの形状は、上記したようにポリマー(A)の幾何学構造や、分子量、一次構造中に導入できる非エチレンイミン部分、さらにはポリマー(A)の濃度、結晶化温度、後述するポリマー結晶形成時の金属イオンの添加など各種条件等により調整できる。
【0079】
例えば、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)として、重合度が300以上の直鎖状ポリエチレンイミンを使用し、80℃以上に加熱し、完全透明溶液を得た後、その溶液の温度を自然に常温まで低下させて結晶性会合体の水性分散液を得る。その後、該分散液にpH調整した水ガラス(B)の水溶液を加え、シリカ(b1)析出反応を進行させることにより、ナノファイバーのスポンジ状の構造体が得られる。
【0080】
また、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)として、ベンゼン環コアに4〜6本のポリエチレンイミンアームが結合した星型のポリマー(A)を使用すると、上記と同様な操作で、扇子形状のナノ構造体を得ることができる。
【0081】
さらに前記した結晶性会合体が化学結合で架橋された架橋ヒドロゲルを用いることにより、複合ナノ構造体のマクロな形状を制御して、該構造体を各種形状の成形体とすることもできる。その形状や大きさは、架橋ヒドロゲル調整時に用いた容器の大きさ及び形状と同一なものにすることができ、例えば、円盤状、円柱状、プレート状、球状などの任意の形状に調整できる。さらに、架橋ヒドロゲルを切断したり、削ったりすることにより、目的の形に成形することもできる。このように成形した架橋ヒドロゲルをシリカソースである水ガラス(B)の水溶液に浸せきさせることにより、ポリマー/シリカ複合ナノ構造体からなる成形体が簡単に得られる。この時、水ガラス(B)の水溶液に浸せきする時間としては、使用する水ガラス(B)水溶液の濃度、該水溶液のpHにより1時間〜1週間と様々であるため適宜調整する必要があるが、1〜48時間程度であれば好適である。
【0082】
本発明で得られるポリマー/シリカ複合ナノ構造体は、ポリマー(A)からなる結晶性会合体とシリカ(b1)とから構成され、複合ナノ構造体中のシリカ(b1)の含有量は、反応条件などにより調整可能であるが、ナノ構造体全体の30〜90質量%の範囲のものを得ることができる。該シリカ(b1)の含有率は、用いるポリマー(A)の濃度を高くしたり、また反応時間を長くしたりする事により高めることができる。
【0083】
また、ポリマー(A)を用いて、水性媒体中で結晶性会合体を形成させる際に、金属イオン(c1)を予め該水性媒体中に存在させておくことにより、該ポリマー(A)中の直鎖状ポリエチレンイミン骨格(a1)と金属イオン(c1)とが錯体を形成することから、金属イオン(c1)を含有する結晶性会合体の水性分散液を得ることができる。この分散液を用いて前述と同様にしてシリカ(b1)の析出反応を行うことにより、ポリマー/金属イオン/シリカ複合ナノ構造体を得ることができる。
【0084】
ポリマー(A)と金属イオン(c1)との混合液を調整する際、ポリマー(A)中のエチレンイミンユニットと金属イオン(c1)とのモル比が1/1〜100/1の範囲で任意に設定することができ、このモル比を調整することによって、得られるポリマー/金属イオン/シリカ複合ナノ構造体中のそれぞれの含有率を調整することが可能である。
【0085】
前記金属イオン(c1)の金属種としては、特に限定されるものではなく、例えば、アルカリ金属のNa,Li,K,Csなど、アルカリ土類金属のCa,Mgなど、遷移金属のFe,Mn,Co,Cr,Cu,Ru,Rh,V,Pd,Mo,Ti,Zr,Eu,Gd,Zn,Cdなど、半金属のAl,Ga,Sn,In,Pbなどを好適に用いることができる。
【0086】
前記で得られたポリマー/金属イオン/シリカ複合ナノ構造体中の金属イオン(c1)は、還元剤(D)を加えることで還元し、ナノメートルオーダーの金属ナノ粒子(c2)が含まれたポリマー/金属ナノ粒子/シリカ複合ナノ構造体とすることもできる。
【0087】
前記複合ナノ構造体中の金属イオン(c1)を金属ナノ粒子(c2)に還元する際に用いることができる還元剤(D)としては、低分子量の還元剤であることが好ましく、例えば、アスコルビン酸、クエン酸ナトリウム、水素化ホウ素ナトリウム、水素化ホウ素アンモニウム、水素、ヒドラジン、アルデヒドなどを挙げることができる。
【0088】
上記還元剤(D)の水溶液またはアルコール溶液とポリマー/金属イオン/シリカ複合ナノ構造体とを混合し、その混合物を室温〜60℃で0.5〜24時間撹拌することで、構造体中の金属イオン(c1)を金属ナノ粒子(c2)へ容易に還元できる。
【0089】
また、還元剤を使わず、前述のポリマー/シリカ複合ナノ構造体を、金、銀及び白金からなる群から選ばれる1種以上の金属イオン(c1’)を含有する溶液と混合することで、ポリマー(A)中の直鎖状ポリエチレンイミン骨格(a1)の還元作用及び自発還元によって、ポリマー/金属ナノ粒子/シリカ複合ナノ構造体を得ることもできる。金、銀、白金のイオンとして、例えば、塩化金酸、塩化金酸ナトリウム、硝酸銀、塩化白金酸、塩化白金酸ナトリウムの水溶液が挙げられ、これらの水溶液とポリマー/シリカ複合ナノ構造体とを混合し、それを室温〜60℃以下で撹拌することで、それぞれの金属のナノ粒子(c2’)が含まれたポリマー/金属ナノ粒子/シリカの複合ナノ構造体を得ることができる。この時、金属イオン(c1’)が金属ナノ粒子(c2’)と還元する途中では、金属イオン(c1’)と金属ナノ粒子(c2’)とが共存することになるが、本発明のポリマー/金属類/シリカ複合ナノ構造体は、この共存した状態のものも含む。
【0090】
[シリカ系無機構造体]
前述で得られたポリマー/シリカ複合ナノ構造体、ポリマー/金属イオン/シリカ複合ナノ構造体、ポリマー/金属ナノ粒子/シリカ複合ナノ構造体を加熱焼成することで、それぞれ、ポリマーが除去されたシリカ構造体、金属酸化物/シリカ複合体、金属ナノ粒子/シリカ複合体(本発明では、これらを総称してシリカ系無機構造体という。)を得ることができる。
【0091】
加熱焼成を行う際には、前述の複合ナノ構造体の粉末を電気炉中に放置し、炉内温度を500℃まで上昇させ、その温度で1〜3時間維持した後、自然に温度を室温まで降下させる方法が好ましい。この操作により、ポリマー(A)が除去されたシリカ系無機構造体を容易に得ることができる。得られる構造体は、それぞれ原料として用いたナノ構造体の中からポリマー(A)のみが除去された構造であり、基本ユニットと見られる20〜50nm太さの繊維状またはラメラ状の空間配置から形成された三次元形状であり、高い比表面積を有するものである。
【実施例】
【0092】
以下、合成例、実施例によって本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。特に断らない限り、「%」は「質量%」を表す。
【0093】
[X線回折法によるナノ構造体の分析]
単離乾燥したナノ構造体を測定試料用ホルダーにのせ、それを株式会社リガク製広角X線回折装置「Rint−Ultma」にセットし、Cu/Kα線、40kV/30mA、スキャンスピード1.0°/分、走査範囲10〜40°の条件で測定を行った。
【0094】
[TG−DTA(差動形示差熱天秤)によるナノ構造体の熱重量分析]
単離乾燥したナノ構造体を測定パッチにより秤量し、それをSIIナノテクノロジー株式会社製「TG−DTA 6300」にセットし、昇温速度を10℃/分として、50℃から500℃の温度範囲にて測定を行った。
【0095】
[X線蛍光分析によるナノ構造体の元素分析]
元素組成分析は株式会社リガク製X線蛍光分析にて行った。
【0096】
[固体29Si−NMRによるナノ構造体のケイ素分析]
ナノ構造体粉末を日本電子株式会社製NMR 「JNM−ECA600」にてCP/MAS方法で測定した。測定の際の外部標準物として、ポリジメチルシラン(−33.8ppm)を用いた。
【0097】
[走査電子顕微鏡によるナノ構造体の形状分析]
単離乾燥したナノ構造体をガラススライドに乗せ、それをキーエンス製表面観察装置VE−9800にて観察した。
【0098】
[透過電子顕微鏡によるナノ構造体の観察]
単離乾燥したナノ構造体を炭素蒸着された銅グリッドに乗せ、それを日本電子株式会社製透過型電子顕微鏡「JEM−2200FS」にて観察した。
【0099】
合成例1
<直鎖状のポリエチレンイミン(L−PEI)の合成>
市販のポリエチルオキサゾリン(数平均分子量500,000、平均重合度5,000、Aldrich社製)5gを、5モル/Lの塩酸20mLに溶解させた。その溶液をオイルバスにて90℃に加熱し、その温度で10時間攪拌した。反応液にアセトン50mLを加え、ポリマーを完全に沈殿させ、それを濾過し、メタノールで3回洗浄し、白色のポリエチレンイミンの粉末を得た。得られた粉末を1H−NMR(重水)にて同定したところ、ポリエチルオキサゾリンの側鎖エチル基に由来したピーク1.2ppm(CH3)と2.3ppm(CH2)が完全に消失していることが確認された。即ち、ポリエチルオキサゾリンが完全に加水分解され、ポリエチレンイミンに変換されたことが示された。
【0100】
その粉末を5mLの蒸留水に溶解し、攪拌しながら、その溶液に15%のアンモニア水50mLを滴下した。その混合液を一晩放置した後、沈殿した結晶粉末を濾過し、その結晶粉末を冷水で3回洗浄した。洗浄後の結晶粉末をデシケータ中で室温(25℃)乾燥し、直鎖状のポリエチレンイミン(L−PEI)を得た。収量は4.2g(結晶水含有)であった。ポリオキサゾリンの加水分解により得られるポリエチレンイミンは、側鎖だけが反応し、主鎖には変化がない。従って、L−PEIの重合度は加水分解前の5,000と同じである。
【0101】
合成例2
<ベンゼン環中心の星状ポリエチレンイミン(B−PEI)合成>
Jin,J.Mater.Chem.,13,672−675(2003)に示された方法に従い、前駆体ポリマーであるベンゼン環中心に6本のポリメチルオキサゾリンのアームが結合した星状ポリメチルオキサゾリンの合成を次の通り行った。
【0102】
磁気攪拌子がセットされたスリ口試験管中に、重合開始剤としてヘキサキス(ブロモメチル)ベンゼン0.021g(0.033mmol)を入れ、試験管の口に三方コックをつけた後、真空状態にしてから窒素置換を行った。窒素気流下で三方コックの導入口からシリンジを用いて2−メチル−2−オキサゾリン2.0ml(24mmol)、N,N−ジメチルアセトアミド4.0mlを順次加えた。試験管をオイルバス上で60℃まで加熱し、30分間保ったところ、混合液は透明になった。透明混合液をさらに100℃まで加熱し、その温度で20時間攪拌して、前駆体ポリマーを得た。この混合液の1H−NMR測定から、モノマーの転化率は98モル%、収量は1.8gであった。この転化率によりポリマーの平均重合度を見積もったところ、各アームの平均重合度は115であった。また、GPCによる分子量測定では、ポリマーの質量平均分子量は22,700であり、分子量分布は1.6であった。
【0103】
この前駆体ポリマーを用い、上記合成例1と同様な方法によりポリメチルオキサゾリンを加水分解し、6本のポリエチレンイミンがベンゼン環コアに結合した星状ポリエチレンイミンB−PEIを得た。1H−NMR(TMS外部標準、重水中)測定の結果、加水分解前の前駆体ポリマーの側鎖メチルに由来した1.98ppmのピークは完全に消失したことが確認された。
【0104】
その粉末を5mLの蒸留水に溶解し、攪拌しながら、その溶液に15%のアンモニア水50mLを滴下した。その混合液を一晩放置した後、沈殿した結晶粉末を濾過し、その結晶粉末を冷水で3回洗浄した。洗浄後の結晶粉末をデシケータ中で室温(25℃)乾燥し、6本のポリエチレンイミンがベンゼン環コアに結合した星状ポリエチレンイミン(B−PEI)を得た。収量は1.3g(結晶水含有)であった。
【0105】
合成例3
<ブロック共重合体PEG−b−PEIの合成>
数平均分子量が4,000のポリエチレングリコール(PEG)の片末端にトシレートが結合したポリマーを重合開始剤(PEG−I)として用い、前駆体ブロックポリマーであるPEGとポリオキサゾリンのブロック共重合体の合成を次の通り行った。
【0106】
磁気攪拌子がセットされたスリ口試験管中に、重合開始剤としてPEG−Iを1.5g(0.033mmol)取り入れ、試験管の口に三方コックをつけた後、真空状態にしてから窒素置換を行った。窒素気流下で三方コックの導入口からシリンジを用いて2−メチル−2−オキサゾリン6.0ml(72mmol)、N,N−ジメチルアセトアミド20.0mlを順次加えた。試験管をオイルバス上で100℃まで加熱し、その温度で24時間攪拌して前駆体ブロックポリマーを得た。得られた混合液の1H−NMR測定から、モノマーの転化率は100モル%であることがわかった。
【0107】
精製後の前駆体ブロックポリマーの収率は93%であった。また、1H−NMR測定において、ポリマー末端トシル基を基準とした各積分比を求めたが、PEGの重合度は45、ポリオキサゾリンの重合度は93であった。即ち、ブロックポリマーの平均重合度は138であった。また、GPCによる分子量測定では、ポリマーの数平均分子量は12,000であり、分子量分布は1.27であった。
【0108】
この前駆体ブロックポリマーを用い、上記合成例1と同様の方法によりポリオキサゾリンブロックを加水分解し、PEGにポリエチレンイミンが結合したブロック共重合体(PEG−b−PEI)を得た。1H−NMR(TMS外部標準、重水中)測定の結果、加水分解前の前駆体ポリマーの側鎖メチルに由来した1.98ppmのピークは完全に消失した。
【0109】
実施例1−1〜1−3、及び比較例1〜3
<直鎖状ポリエチレンイミンからのナノ構造体の製造>
合成例1で得られたL−PEI粉末を用い、蒸留水中に分散させた後、オイルバスにて90℃に加熱し、完全透明な水溶液を得た。その水溶液を室温に放置し、自然に室温までに冷やし、1%の不透明な結晶性会合体を得た。一方、水ガラス3号(キシダ化学株式会社製、pH=11.3)を用い、pH値が9.4(実施例1−1)、9.8(実施例1−2)、10(実施例1−3)、及びpHが2(比較例1)、4(比較例2)、6(比較例3)の0.2モル/Lの水ガラス水溶液を調整した。水ガラス水溶液のpH値調整には1モル/Lの塩酸と25%アンモニア水を用いた。
【0110】
上記で得られた濃度1%の結晶性会合体の水分散液10gと、0.2モル/Lの水ガラス水溶液20mlとを混合し、5分間撹拌した後、静置状態で50℃下2時間析出反応させ、白色の沈殿物を得た。反応液中の上澄みを除去し、沈殿物を蒸留水で洗浄した後、遠心分離にて3回繰り返し洗浄した。得られた固形物を室温で乾燥後、真空乾燥機にて60℃下12時間乾燥し、ナノ構造体(1−1)〜(1−3)及び比較例1〜3を得た。得られた粉末の収量を表1に示す。
【0111】
【表1】

【0112】
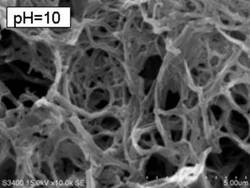
得られたナノ構造体の走査型顕微鏡写真(SEM)観察の結果を図1〜6に示した。pH値2〜6の水ガラス水溶液から得た構造体(1)〜(3)は、基本的にバルキーの固まりであったが、pH値を9.4〜10に調整した水ガラス水溶液から得たナノ構造体(1−1)〜(1−3)はファイバー状ネットワーク構造を有するスポンジであった。
【0113】
実施例1−3で得られたナノ構造体(1−3)の透過型電子顕微鏡(TEM)写真を図7に示した。非常に薄いラメラ状シリカ(左図)中には、一定的な陰(右図)のイメージが観察された。その陰はポリマーとシリカとが数ナノレベルで複合された部分によるコントラストであると推測される。
【0114】
実施例1−3で得られたナノ構造体(1−3)の固体29Si−NMR(CP/MAS)測定から、シリカ結合構造を示すQ4シグナルが−110ppm、Q3シグナルが−101ppmに現れ、Q4/Q3の積分比は1.00/0.68であった(図8参照)。Q2結合シグナルは現れなかった。このことは、ファイバー状ネットワークを形成しているシリカは高度なSi(0Si)4結合ユニットを有することを強く示唆する。
【0115】
さらに、実施例1−3で得られたナノ構造体(1−3)の元素分析の結果、Si:30%、C:15%、H:4.1%、N:8.2%、Na:0.8%であった。このことは、ナノ構造体(1−3)には、ケイ素以外の、直鎖状ポリエチレンイミンが複合され、その含有率が約27%であることが示唆された。即ち、得られたナノ構造体はシリカとポリマーとが複合された構造体である。
【0116】
実施例2
実施例1−3で得られたナノ構造体(1−3)0.1gアルミナ坩堝中に入れ、電気炉中にて500℃まで加熱し、その温度下1時間焼成した。収量は0.07gであった。を500℃にて1時間焼成して、シリカ系無機構造体を得た。SEM観察の結果、ファイバー構造には変わりがなく(図9参照)、29Si−NMR(CP/MAS)ではQ4/Q3の積分比は1.00/0.52であった(図10参照)。即ち、Q4構造成分がやや増える傾向であった。
【0117】
さらに、熱焼成前後の構造体の比表面積をN2/He 混合ガス(3/7体積比)の吸着−脱着実験法でFlow Sorb II 2300(Micromeritics)を用いて測定した結果、焼成前の149m2/gから焼成後の315m2/gまで2倍ほど大きく増大した。焼成によるポリマー除去が表面積を増大させることが示唆された。
【0118】
実施例3−1
<金ナノ粒子が含まれるナノ構造体>
実施例1−3で得られたナノ構造体(1−3)0.05gを2mLの0.1モル/L NaAuCl4溶液中に加え、室温(25℃)下で5分間撹拌後、そのまま25分間静置させた。得られた固形分を蒸留水で洗浄した後、室温乾燥した。これで得られた粉末のXRD測定から、金の結晶の存在を示す散乱ピーク(2θ)が38.1°、44.4°、64.5°、77.6°で確認された。また、TEM観察から、2〜3nmの大きさの金のナノ粒子がシリカ中に閉じ込まれていることが観測された(図11)。これは金属ナノ粒子が含まれてない図7のイメージと大きく異なるものであった。
【0119】
実施例3−2
<白金ナノ粒子が含まれるナノ構造体>
実施例1−3で得られたナノ構造体(1−3)0.05gを2mLの0.1モル/L Na2PtCl4溶液中に加え、室温下5分間撹拌後、そのまま25分間静置させた。得られた固形分を蒸留水で洗浄した後、室温乾燥した。これで得られた粉末のXRD測定から、白金の結晶の存在を示す散乱ピーク(2θ)が40.0°、46.4°、67.7°で観測された。また、TEM観察から、2〜3nm大きさの白金のナノ粒子がシリカ中に閉じ込まれていることが観測された(図12)。これは金属ナノ粒子が含まれてない図7のイメージと大きく異なるものであった。
【0120】
実施例4
<ベンゼン環中心のポリエチレンイミンからのナノ構造体>
合成例2で合成したB−PEIを使用し、実施例1と同様な方法により、2%のポリマーの結晶性会合体の分散液を調整した。この分散液10gに、pH値が9.6の0.2モル/L水ガラス水溶液20mLを加え、室温(25℃)で1時間放置した。上澄みを取り出し、固形物を蒸留水で洗浄した後、遠心分離機にて3回繰り返し洗浄した。得られた固形物を室温で乾燥後、真空乾燥機にて60℃下12時間乾燥し、白色のナノ構造体(4)を得た。収量は0.53gであった。
【0121】
上記で得られたナノ構造体(4)のSEM観察写真、TEM観察写真を図13と図14に示し。扇子状の複合ナノ構造体のイメージが明確に現れた。また、ナノ構造体(4)のXRD測定では、ポリマー結晶由来の散乱ピークが20.3°、27.3°、28.2°で確認された。
【0122】
実施例5−1〜5−4
<ブロック共重合体からのナノ構造体>
合成例3で得られたブロック共重合体(PEG−b−PEI)を用い、90℃に加温下、硝酸ナトリウム、硝酸銅、硝酸アルミニウムを含む2%のポリマー溶液3種類と金属イオンを含まないポリマー溶液を調整した。溶液中の各金属イオンとポリマー中のエチレンイミンユニット(EI)とのモル比を表2に示す。これら溶液を室温に6時間静置し、結晶性会合体を得た。それぞれの結晶性会合体の分散液10gに、pH値が9.6の0.2モル/L水ガラス水溶液20mLを加え、5分間撹拌後、室温で1時間静置した。析出した固形分を蒸留水で洗浄し、さらに遠心分離機にて3回繰り返し洗浄した。得られた固形物を室温で乾燥後、真空乾燥機にて60℃下12時間乾燥し、ポリマー/金属イオン/シリカ複合ナノ構造体(5−1)〜(5−4)を得た。収量は表2に示した。
【0123】
【表2】

【0124】
実施例5−1〜5−4で得られたナノ構造体(5−1)〜(5−4)のSEM観察写真を、図15〜図18に示す。金属イオンの存在により、得られた構造体の形状に大きな変化が起こることが示唆された。
【0125】
実施例6
実施例5−3の銅イオンが含まれたナノ構造体(5−3)のサンプル0.3gを10mLの0.1モル/Lの水素化ホウ素アンモニウム水溶液と混合し、窒素雰囲気下、40℃で1時間撹拌した。窒素雰囲気下、エタノールで洗浄し、窒素雰囲気下乾燥させた。これで得た粉末は元の青色が完全に消え、薄い銅色を示した。粉末XRD測定から、ゼロ価銅の存在を示す散乱ピーク2θ(°)が43.4,50.5,74.1が観測され、還元反応が起きたことを確認した。
【図面の簡単な説明】
【0126】
【図1】比較例1で得た構造体(1)の走査型電子顕微鏡写真である。
【図2】比較例2で得た構造体(2)の走査型電子顕微鏡写真である。
【図3】比較例3で得た構造体(3)の走査型電子顕微鏡写真である。
【図4】実施例1−1で得たナノ構造体(1−1)の走査型電子顕微鏡写真である。
【図5】実施例1−2で得たナノ構造体(1−2)の走査型電子顕微鏡写真である。
【図6】実施例1−3で得たナノ構造体(1−3)の走査型電子顕微鏡写真である。
【図7】実施例1−3で得たナノ構造体(1−3)の透過型電子顕微鏡写真である。右図は左図円形部分の高分解能イメージである。
【図8】実施例1−3で得たナノ構造体(1−3)の固体29Si−NMR(CP/MAS)スペクトルである。
【図9】実施例1−3で得たナノ構造体(1−3)の熱焼成前後の走査型電子顕微鏡写真である。
【図10】実施例1−3で得たナノ構造体(1−3)の熱焼成後の固体29Si−NMR(CP/MAS)スペクトルである。
【図11】実施例3−1で得た金ナノ粒子を含むナノ構造体(3−1)の透過型電子顕微鏡写真である。右図は左図円形部分の拡大イメージである。黒い斑点は2nm程度の金ナノ粒子の写真である。
【図12】実施例3−2で得た白金ナノ粒子を含むナノ構造体(3−2)の透過型電子顕微鏡写真である。右図は左図円形部分の拡大イメージである。黒い斑点は2nm程度の白金ナノ粒子の写真である。
【図13】実施例4で得たナノ構造体(4)の走査型電子顕微鏡写真である。
【図14】実施例4で得たナノ構造体(4)の透過型電子顕微鏡写真である。右図は左図の拡大図である。
【図15】実施例5−1で得たナノ構造体(5−1)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【図16】実施例5−2で得たナノ構造体(5−2)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【図17】実施例5−3で得たナノ構造体(5−3)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【図18】実施例5−4で得たナノ構造体(5−4)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【技術分野】
【0001】
本発明は、直鎖状ポリエチレンイミン骨格を有するポリマーの水性媒体中で形成する結晶性会合体を反応場として用い、それに水ガラスを混合させることによる、該ポリマーとシリカとがナノメートルオーダーで複合された構造体(以下、本発明においてナノ構造体と称す)の製造方法、さらにはそのポリマー/シリカ複合構造体中に金属イオン、数ナノメートルオーダーの金属ナノ粒子(以下、金属イオンと金属ナノ粒子をまとめて金属類と称す。)が含まれるポリマー/金属類/シリカ複合ナノ構造体の製造方法、及びこれらを熱焼成して得られるシリカ系無機構造体の製造方法に関する。
【背景技術】
【0002】
珪素は地殻上で酸素に次ぐ第二番目を誇る豊富な存在であり、自然界の石英、水晶、オパール、雲母、珪藻などはよく知られている珪素の酸化物である。規則的な空間構造やパターン構造を有するシリカ材料の創製は、材料科学分野において大きな研究課題であり、これに関する技術開発が大きく進歩している。
【0003】
シリカ材料にある種の構造を発現させるための方法としては、分子組織体をテンプレート(鋳型)として用い、その組織体周辺でシリカを固定化する方法が、該分野において広く用いられている。このテンプレートには、界面活性剤(例えば、非特許文献1参照。)、ブロックポリマー(例えば、非特許文献2参照。)、ウイルス、バクテリア(例えば、非特許文献3参照。)などが使用されており、これらをテンプレートとして合成されるナノ空洞を有するシリカ、例えば、MCM−41(メソポーラス)シリーズの材料は、触媒、電子材料、ナノフィルター、バイオ工学などへの応用が可能である。これら材料に関しては、より精密な構造の制御へ向けた研究がなされており、空洞の大きさ、並び方、あるいは球状のシリカ中での空洞制御などが検討されている。
【0004】
一方、このようなナノ空洞の制御と並行して、シリカの形状をナノからミクロンさらにはマクロスケールまでに制御する技術が注目されている。これは生態系でのバイオシリカに啓発されたことに一因がある(例えば、非特許文献4参照。)。自然界のバイオシリカとしては、珪藻類を取りあげることができる。珪藻類は、その体形をシリカで構成し、その上に複雑かつ精密な形状とパターンとを有する。そのシリカの構築には、タンパク質、またはポリペプチドが関わる(例えば、非特許文献5参照。)が、これらは、シリカの固定化反応の触媒として作用したり、シリカ形状成長の足場を提供したりする。このような生体系バイオシリカの形成において、欠かせない化学構造の一つが長鎖ポリアミンである。ポリアミンは、ペプチド構造に組み込まれることで働くか、または独自に一定分子量のポリアミンとしてポリペプチドと共に働くものである(例えば、非特許文献6参照。)。
【0005】
上記したように、ポリアミンの存在下で、例えば、珪酸、珪酸ナトリウムまたはアルコキシシラン等のシリカソースを、室温でシリカゲルとして固定化できることは、ここ数年広く知られるようになった。しかし、それらは通常ポリアミンを水中溶解させ、その水溶液中でのシリカソースのゾルゲル反応により行われるものであるため、シリカゲルが形成できても、そのシリカゲルの形状を制御することはできず、規則的な構造を有するシリカゲルの実現は困難であった。
【0006】
上記の方法とは異なり、本発明者らは、2級アミンで構成された直鎖状ポリエチレンイミンが水性媒体中で発現する特異な分子会合体をシリカ析出の反応場として用いることにより、シリカナノファイバーに代表されるさまざまな形状を有するシリカ含有ナノ構造体およびその製造法を見いだした(特許文献1〜4参照。)。これらの発明では、直鎖状ポリエチレンイミン骨格を有するポリマーを水中にて自発的に会合させた後、その会合体液中にアルコキシシラン類のシラン化合物を混合させると、そのシラン類が選択的にポリマー会合体表面で加水分解的に縮合され、ポリマーとシリカとが複合したナノ構造体が生成することを見出したことにより完成した発明である。このプロセスはシリカ系ナノ構造体の構造制御に高効率であるが、用いるシリカソースとしてはアルコキシシラン類である。従って、アルコキシシラン類が高価であることから、製造するナノ構造体の製造コストが高く、さらにはアルコキシシラン類の加水分解によりアルコール類が生じ、この廃棄処理のために、環境負荷への問題点も避けられない。シリカのナノ構造体を安価で、かつ無炭素の水ガラス等で構築することができれば、工業的には重要な意義を有する。
【0007】
【非特許文献1】C.T.Kresge et al.,Nature,1992,359,p.710
【非特許文献2】A.Monnier et al.,Science,1993,261,p1299
【非特許文献3】S.A.Davis et al.,Nature,1997,385,p420
【非特許文献4】W.E.G.Muller Ed.,Silicon Biomineralizattion:Biology−Biotechnology−Molecular Biology−Biotechnology,2003,Springer
【非特許文献5】N.Kroger et al.,Science,1999,286,p.1129
【非特許文献6】N.Kroger et al.,Proc.Natl.Acad.Sci.USA,2000,97,p14133
【特許文献1】特開2005−264421号公報
【特許文献2】特開2005−336440号公報
【特許文献3】特開2006−063097号公報
【特許文献4】特開2007−051056号公報
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明が解決しようとする課題は、製造コストが低く、有機物質の廃棄物が発生しないプロセスによる、多様な形状を有するポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体及びこれらを熱焼成して得られるシリカ系無機構造体の簡便な製造方法を提供することにある。
【課題を解決するための手段】
【0009】
上記の課題を解決するために、本発明者らは鋭意検討を行ったところ、特定のポリマーが水中で形成する結晶性会合体をテンプレートとし、それが安定に存在する条件下で予めpH調整した水ガラスと混合すると、水ガラスのケイ素が該会合体周辺でシリカとして析出し、有機物の発生がなく、ポリマーとシリカとが複合したナノ構造体が得られることを見出し、本発明を完成した。
【0010】
即ち、本発明は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を水性媒体中で結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合して、シリカ(b1)を析出させることを特徴とするポリマー/シリカ複合ナノ構造体の製造方法、更に該ポリマー/シリカ複合ナノ構造体に金属イオン(c1)又は金属ナノ粒子(c2)が含まれるポリマー/金属類/シリカ複合ナノ構造体の製造方法、及びこれらを熱焼成して得られるシリカ系無機構造体の製造方法を提供するものである。
【発明の効果】
【0011】
本発明の製造方法は、工業的に最も安く、汎用性の高い水ガラスをシリカソースとして用い、簡便で且つ有機物の廃棄がない方法でポリマー/シリカ複合ナノ構造体およびポリマー/金属類/シリカ複合ナノ構造体を得るものである。この製造方法から得られるナノ構造体は、ナノ次元のファイバー、ラメラのようなユニット構造が3次元空間に大きく広がり、さまざまな複雑形状と構造を有する、シリカを主成分とするシリカ系材料である。
【0012】
本発明で得られるポリマー/シリカ複合ナノ構造体は、シリカ内部に直鎖状ポリエチレンイミン骨格を有するポリマーが含まれるので、そのポリマーが固有する機能を生かすことができる。例えば、ポリエチレンイミンは金属イオンとポリマー金属錯体を形成することができるので、本発明のポリマー/シリカ複合ナノ構造体は金属イオンの濃縮・分離、金属錯体の固定に用いることができ、ポリマー/金属類/シリカ複合ナノ構造体を形成する。
【0013】
また、ポリエチレンイミンは酸性有機化合物や酸性の官能基を有する生体ポリマー等と酸/塩基複合体を形成することができるので、本発明のポリマー/シリカ複合ナノ構造体は多くの酸性物質の分離または固定に用いることができる。
【0014】
また、ポリエチレンイミンは殺菌、抗ウイルスの機能を有するので、本発明で得られるポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体は、例えば、防菌剤、殺菌剤、抗ウイルス、化粧品添加剤として用いることができる。
【0015】
更に、本発明で得られるポリマー/シリカ複合ナノ構造体は、シリカナノファイバーの絡み合いで構成する特徴を有するので、水、空気の浄化用ナノフィルターとして用いることもできる。
【0016】
又、前記ポリマー/シリカ複合ナノ構造体又はポリマー/金属類/シリカ複合ナノ構造体を焼成して得られるシリカ系無機構造体は、高い比表面積を有するためフィルター、触媒支持体、フィラー等に好適に用いることができるものである。
【発明を実施するための最良の形態】
【0017】
本発明は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を水性媒体中で結晶性会合体とし、これをテンプレートとして用いて、pHを8.5以上に調整した水ガラス(B)からシリカ(b1)を該会合体周辺に析出させることにより、ポリマー(A)とシリカ(b1)とを複合させ、ナノ構造体を得ることを特徴とする。
【0018】
シリカを含有する構造体の製造において、有機物質の環境への廃棄をなくすには、アルコキシシラン類を用いない反応を実現しなければならない。三次元空間で一定の形状と構造を有するシリカ含有ナノ構造体を構築するには、これは非常に困難である。
【0019】
ポリマーとシリカとが複合しているナノ構造体は、基本的にはポリマーが媒体中で形成する特定の構造が、シリカを析出させるテンプレートとして機能することによって生成するものである。そのポリマーテンプレートの形状が安定であれば安定であるほど、得られるポリマー/シリカ複合ナノ構造体は明確なナノ構造を有することになる。
【0020】
具体的に言えば、シリカをある特定形状に作り上げるためには、下記の三つの条件、(1)形状を誘導するポリマーテンプレートが安定に形成すること、(2)そのテンプレートがシリカソースを濃縮できること、(3)そのテンプレートがシリカソースの重合を促進させること、などをそろえる必要がある。この時、アルコキシシランをシリカソースに用いた場合には、比較的広範なポリマーに対してこの条件を満たすため、構造が制御された複合ナノ構造体を得るには好都合であった。アルコキシシランの代わりのシリカソースとしては、水溶性ケイ酸塩(珪酸ナトリウム、珪酸カリウムなど)または水分散シリカコロイド粒子といったものしかない。このようなシリカソースを用いると、アルコキシシランの加水分解によって生じるアルコール類の環境への廃棄問題は解決できると考えられる。しかしながら、水溶性ケイ酸塩類を用いる場合、特に濃厚溶液である水ガラスは水溶性であるが、水性媒体の微小な変化(例えば、pHの変動や添加物の混入等)により不安定化し、自発的に無規則なシリカの固まりとして析出してしまうため、ポリマーテンプレートと水ガラスとが安定に混合できない限り、該テンプレート表面にケイ酸塩を濃縮してシリカを析出させ、ポリマー/シリカ複合ナノ構造体を得ることは不可能である。
【0021】
本発明においては、上記の課題を解決するため、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)が水性媒体中で形成する結晶性会合体をテンプレートとして使用する。直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)は水中可溶であるが、室温では結晶性の分子会合体として存在する。ここにpHを8.5以上に調整した水ガラス(B)が混合されたときにも、この結晶性会合体の安定性が維持され、且つ該結晶性会合体を含有する水性媒体中におけるケイ酸塩自身の沈殿を防ぐことが可能であり、ケイ酸塩はこの結晶性会合体をテンプレートとして、選択的に該テンプレート周辺でシリカ(酸化ケイ素)(b1)として析出することを見出したことにより、本発明を完成するに至った。
【0022】
本発明で得られるナノ構造体は、直鎖状ポリエチレンイミン骨格を有するポリマー(A)とシリカ(b1)とが複合されたものであり、シリカ(b1)の固さにより、ナノ構造が空間に広がるさまざまな形状を有する。
【0023】
[直鎖状ポリエチレンイミン骨格を有するポリマー]
本発明でいう直鎖状ポリエチレンイミン骨格(a1)とは、二級アミンのエチレンイミン単位を主たる構造単位とするポリマー骨格である。該骨格(a1)中においては、エチレンイミン単位以外の構造単位が存在していてもよいが、結晶性会合体を形成させるためには、該ポリマー骨格(a1)中の一定鎖長が連続的なエチレンイミン単位であることが好ましい。該直鎖状ポリエチレンイミン骨格(a1)の長さは、該骨格を有するポリマー(A)が結晶を形成できる範囲であれば特に制限されないが、好適に結晶を形成するためには、該骨格(a1)部分のエチレンイミン単位の繰り返し単位数が10以上であることが好ましく、20〜10,000の範囲であることが特に好ましい。
【0024】
本発明において使用するポリマー(A)は、その構造中に直鎖状ポリエチレンイミン骨格(a1)を有するものであればよく、ポリマー(A)全体の形状が線状、星状または櫛状であっても、水または水と親水性有機溶媒との混合溶媒である水性媒体(以下、両者を併せて水性媒体という)中で結晶性会合体を与えることができる。
【0025】
また、これら線状、星状または櫛状のポリマーは、直鎖状ポリエチレンイミン骨格(a1)のみからなるものであっても、直鎖状ポリエチレンイミン骨格(a1)からなるブロック(以下、ポリエチレンイミンブロックと略記する。)と他のポリマーブロックとのブロックコポリマーからなるものであってもよい。他のポリマーブロックとしては、例えば、ポリエチレングリコール、ポリプロピオニルエチレンイミン、ポリアクリルアミドなどの水溶性のポリマーブロック、あるいは、ポリスチレン、ポリオキサゾリン類のポリフェニルオキサゾリン、ポリオクチルオキサゾリン、ポリドデシルオキサゾリン、ポリアクリレート類のポリメチルメタクリレート、ポリブチルメタクリレートなどの疎水性のポリマーブロック等を挙げることができる。これら他のポリマーブロックとのブロックコポリマーとすることで、ポリマーから形成する結晶性会合体の形状や得られるナノ構造体の特性を調整することができる。
【0026】
直鎖状ポリエチレンイミン骨格を有するポリマー(A)が、ブロックコポリマーである場合の該ポリマー(A)中における直鎖状ポリエチレンイミン骨格(a1)の割合は、結晶性会合体を形成できる範囲であれば特に制限されないが、好適に該会合体を形成するためには、ポリマー(A)中の直鎖状ポリエチレンイミン骨格(a1)の割合が40モル%以上であることが好ましく、50モル%以上であることがさらに好ましい。
【0027】
上記直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)は、その前駆体となるポリオキサゾリン類からなる直鎖状の骨格を有するポリマー(以下、前駆体ポリマーと略記する。)を、酸性条件下またはアルカリ条件下で加水分解することで容易に得ることができる。従って、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の線状、星状、または櫛状などの形状は、この前駆体ポリマーの形状を制御することで容易に設計することができる。また、重合度や末端構造も、前駆体ポリマーの重合度や末端機能団を制御することで容易に調整できる。さらに、直鎖状ポリエチレンイミン骨格(a1)を有するブロックコポリマーを形成する場合には、前駆体ポリマーをブロックコポリマーとし、該前駆体中のポリオキサゾリン類からなる直鎖状の骨格を選択的に加水分解することで得ることができる。
【0028】
前駆体ポリマーは、オキサゾリン類のモノマーを使用して、カチオン型の重合法、あるいは、マクロモノマー法などの合成方法により合成が可能であり、合成方法や開始剤を適宜選択することにより、線状、星状、あるいは櫛状などの各種形状の前駆体ポリマーを合成できる。
【0029】
ポリオキサゾリン類からなる直鎖状の骨格を形成するモノマーとしては、メチルオキサゾリン、エチルオキサゾリン、メチルビニルオキサゾリン、フェニルオキサゾリンなどのオキサゾリンモノマーを使用できる。
【0030】
重合開始剤としては、分子中に塩化アルキル基、臭化アルキル基、ヨウ化アルキル基、トルエンスルホニルオキシ基、あるいはトリフルオロメチルスルホニルオキシ基などの官能基を有する化合物を使用できる。これら重合開始剤は、多くのアルコール類化合物の水酸基を他の官能基に変換させることで得られる。なかでも、官能基変換として、臭素化、ヨウ素化、トルエンスルホン酸化、およびトリフルオロメチルスルホン酸化されたものは重合開始効率が高いため好ましく、特に臭化アルキル基、トルエンスルホン酸アルキル基とすることが好ましい。
【0031】
また、ポリ(エチレングリコール)の末端水酸基を臭素あるいはヨウ素に変換したもの、またはトルエンスルホニル基に変換したものを重合開始剤として使用することもできる。その場合、ポリ(エチレングリコール)の重合度は5〜100の範囲であることが好ましく、10〜50の範囲であれば特に好ましい。
【0032】
また、カチオン開環リビング重合開始能を有する官能基を有し、かつ光による発光機能、エネルギー移動機能、電子移動機能を有するポルフィリン骨格、フタロシアニン骨格、またはピレン骨格のいずれかの骨格を有する色素類は、得られるポリマー(A)及びナノ構造体に特殊な機能を付与することができる。
【0033】
線状の前駆体ポリマーは、上記オキサゾリンモノマーを1価または2価の官能基を有する重合開始剤により重合することで得られる。このような重合開始剤としては、例えば、塩化メチルベンゼン、臭化メチルベンゼン、ヨウ化メチルベンゼン、トルエンスルホン酸メチルベンゼン、トリフルオロメチルスルホン酸メチルベンゼン、臭化メタン、ヨウ化メタン、トルエンスルホン酸メタンまたはトルエンスルホン酸無水物、トリフルオロメチルスルホン酸無水物、5−(4−ブロモメチルフェニル)−10,15,20−トリ(フェニル)ポルフィリン、またはブロモメチルピレンなどの1価のもの、ジブロモメチルベンゼン、ジヨウ化メチルベンゼン、ジブロモメチルビフェニレン、またはジブロモメチルアゾベンゼンなどの2価のものが挙げられる。また、ポリ(メチルオキサゾリン)、ポリ(エチルオキサゾリン)、または、ポリ(メチルビニルオキサゾリン)などの工業的に使用されている線状のポリオキサゾリンを、そのまま前駆体ポリマーとして使用することもできる。
【0034】
星状の前駆体ポリマーは、上記したようなオキサゾリンモノマーを3価以上の官能基を有する重合開始剤により重合することで得られる。3価以上の重合開始剤としては、例えば、トリブロモメチルベンゼンなどの3価のもの、テトラブロモメチルベンゼン、テトラ(4−クロロメチルフェニル)ポルフィリン、テトラブロモエトキシフタロシアニンなどの4価のもの、ヘキサブロモメチルベンゼン、テトラ(3,5−ジトシリルエチルオキシフェニル)ポルフィリンなどの5価以上のものが挙げられる。
【0035】
櫛状の前駆体ポリマーを得るためには、多価の重合開始基を有する線状のポリマーを用いて、該重合開始基からオキサゾリンモノマーを重合させることにより得られるが、例えば、線状のエポキシ樹脂やポリビニルアルコールなどの側鎖に水酸基を複数有するポリマーの水酸基を、臭素やヨウ素等でハロゲン化するか、あるいはトルエンスルホニル基に変換させた後、該変換部分を重合開始基として用いることでも得ることができる。
【0036】
また、櫛状の前駆体ポリマーを得る方法として、ポリアミン型重合停止剤を用いることもできる。例えば、一価の重合開始剤を用い、オキサゾリンを重合させ、そのポリオキサゾリンの末端をポリエチレンイミン、ポリビニルアミン、ポリプロピルアミンなどのポリアミンのアミノ基に結合させることで、櫛状のポリオキサゾリンを得ることができる。
【0037】
上記により得られる前駆体ポリマーのポリオキサゾリン類からなる直鎖状の骨格部分の加水分解は、酸性条件下またはアルカリ条件下のいずれの条件下でもよい。酸性条件下での加水分解は、例えば、塩酸水溶液中で前駆体ポリマーを加熱下で攪拌することにより、ポリエチレンイミンの塩酸塩を得ることができる。得られた塩酸塩を過剰のアンモニウム水で処理することで、塩基性のポリエチレンイミン骨格を有するポリマーの結晶粉末を得ることができる。用いる塩酸水溶液は、濃塩酸でも、1mol/L程度の水溶液でもよいが、加水分解を効率的に行うには、5mol/Lの塩酸水溶液を用いることが望ましい。また、反応温度は80℃前後が望ましい。
【0038】
アルカリ条件下での加水分解は、例えば、水酸化ナトリウム水溶液を用いることで、ポリオキサゾリン類からなる骨格をポリエチレンイミン骨格に変換させることができる。アルカリ条件下で反応させた後、反応液を透析膜にて洗浄することで、過剰な水酸化ナトリウムを除去し、ポリエチレンイミン骨格を有するポリマーの結晶粉末を得ることができる。用いる水酸化ナトリウムの濃度は1〜10mol/Lの範囲であればよく、より効率的な反応を行うには3〜5mol/Lの範囲であることが好ましい。また、反応温度は80℃前後が好ましい。
【0039】
酸性条件下またはアルカリ条件下での加水分解における、酸またはアルカリの使用量としては、前駆体ポリマー中のオキサゾリン単位に対し、1〜10当量でよく、反応効率の向上と後処理の簡便化のためには、3当量程度とすることが好ましい。
【0040】
上記加水分解により、前駆体ポリマー中のポリオキサゾリン類からなる直鎖状の骨格が、直鎖状ポリエチレンイミン骨格(a1)となり、該ポリエチレンイミン骨格(a1)を有するポリマー(A)が得られる。
【0041】
また、直鎖状ポリエチレンイミンブロックと他のポリマーブロックとのブロックコポリマーを形成する場合には、前駆体ポリマーをポリオキサゾリン類からなる直鎖状のポリマーブロックと、他のポリマーブロックとからなるブロックコポリマーとし、該前駆体ポリマー中のポリオキサゾリン類からなる直鎖状のブロックを選択的に加水分解することで得ることができる。
【0042】
他のポリマーブロックが、ポリ(N−プロピオニルエチレンイミン)などの水溶性ポリマーブロックである場合には、ポリ(N−プロピオニルエチレンイミン)が、ポリ(N−ホルミルエチレンイミン)やポリ(N−アセチルエチレンイミン)に比べて、有機溶媒への溶解性が高いことを利用してブロックコポリマーを形成することができる。即ち、2−オキサゾリンまたは2−メチル−2−オキサゾリンを、前記した重合開始化合物の存在下でカチオン開環リビング重合した後、得られたリビングポリマーに、さらに2−エチル−2−オキサゾリンを重合させることによって、ポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとからなる前駆体ポリマーを得る。該前駆体ポリマーを水に溶解させ、該水溶液にポリ(N−プロピオニルエチレンイミン)ブロックを溶解する水とは非相溶の有機溶媒を混合して攪拌することによりエマルジョンを形成する。該エマルジョンの水相に、酸またはアルカリを添加することによりポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックを優先的に加水分解させることにより、直鎖状ポリエチレンイミンブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとを有するブロックコポリマーを形成できる。
【0043】
ここで使用する重合開始化合物の価数が1および2の場合には、直鎖状のブロックコポリマーとなり、それ以上の価数であれば星型のブロックコポリマーが得られる。また、前駆体ポリマーを多段のブロックコポリマーとすることで、得られるポリマーも多段のブロック構造とすることも可能である。
【0044】
[結晶性会合体]
上記直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)は、一次構造中の直鎖状ポリエチレンイミン骨格(a1)が、水性媒体中で結晶性を発現することにより該ポリマー(A)の結晶を誘導する。該ポリマー結晶は、水性媒体の存在下でのポリマー結晶同士の物理的な結合により三次元網目構造を有するヒドロゲルを形成することもでき、さらにポリマー結晶同士を架橋剤で架橋することにより化学的な架橋結合を有する架橋ヒドロゲルを形成することもできる。
【0045】
従来広く使用されてきたポリエチレンイミンは、環状エチレンイミンの開環重合により得られる分岐状ポリマーであり、その一次構造には一級アミン、二級アミン、三級アミンが存在する。従って、分岐状ポリエチレンイミンは水溶性であるが、結晶性は持たないため、分岐状ポリエチレンイミンを用いてヒドロゲルを作るためには、架橋剤による共有結合により網目構造を与えなくてはならない。しかしながら本発明に使用するポリマーが骨格として有する直鎖状ポリエチレンイミンは、二級アミンだけで構成されており、該二級アミン型の直鎖状ポリエチレンイミンは水溶性でありながら、優れた結晶性を有する。
【0046】
このような、直鎖状ポリエチレンイミンの結晶は、そのポリマーのエチレンイミン単位に含まれる結晶水数により、ポリマー結晶構造が大きく異なることが知られている(Y.Chatani et al.、Macromolecules、1981年、第14巻、p.315−321参照)。無水のポリエチレンイミンは二重螺旋構造を特徴とする結晶構造を優先するが、モノマー単位に2分子の水が含まれると、ポリマーはzigzag構造を特徴とする結晶体に成長することが知られている。実際、水中から得られる直鎖状ポリエチレンイミンの結晶は一つのモノマー単位に2分子水を含む結晶であり、その結晶は室温状態では水中不溶である。
【0047】
本発明における直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の結晶性会合体は、上記の場合と同様に直鎖状ポリエチレンイミン骨格(a1)の結晶発現により形成されるものであり、ポリマー形状が線状、星状、または櫛状などの形状であっても、一次構造に直鎖状ポリエチレンイミン骨格(a1)を有していれば、ポリマー(A)の結晶性会合体が得られる。
【0048】
本発明におけるポリマー(A)の結晶性会合体の存在は、例えば、X線散乱により確認でき、広角X線回折計(WAXS)における2θ角度値で20°,27°,28°にて散乱ピークを示す。
【0049】
また、本発明におけるポリマー(A)の結晶の示差走査熱量計(DSC)における融点は、該直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の構造にも依存するが、概ねその融点が45〜90℃で現れる。
【0050】
本発明におけるポリマー(A)の結晶性会合体は、その結晶を構成するポリマー(A)の幾何学的構造や、分子量、一次構造中に導入する非エチレンイミン部分、さらにはポリマー結晶の形成条件などの影響により各種形状を取り得ることができ、例えば束状、ブラシ状、星状などの形状を有する。
【0051】
上記結晶性会合体は、5〜30nm程度のナノメートルオーダーの繊維状構造を基本ユニットとするものであり、該繊維状構造表面に存在するフリーなエチレンイミン鎖により、繊維状構造同士が水素結合による物理的な結合で繋がれて空間に配置され、上記したような三次元形状に成長する。
【0052】
本発明の結晶性会合体は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)が室温の水に不溶である性質を利用し、該直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の水中での溶解−結晶変換により得ることができる。
【0053】
例えば、まず直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を一定量水性媒体中に分散し、該分散液を加熱することにより、ポリマー(A)の透明な溶液を得る。次いで、加熱状態のポリマー(A)の水性溶液を室温に冷やすことにより結晶性会合体が得られる。この際、ポリマー濃度が高いほど、結晶性会合体はアイスクリームのような状態を有し、多様な形状に造形させることが可能である。
【0054】
上記ポリマーの水性溶液の加熱温度は100℃以下が好ましく、90〜95℃の範囲であることがより好ましい。また、ポリマーの水性溶液中のポリマー含有量(濃度)は、特に限定されないが、0.01〜20質量%の範囲であることが好ましく、安定形状の結晶体からなる結晶性会合体を得るためには0.1〜10質量%の範囲がさらに好ましい。このように、本発明においては、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を使用すると、ごく少量のポリマー濃度でも結晶性会合体を形成することができる。
【0055】
上記ポリマーの水性溶液の温度を室温(25℃)まで低下させる過程により、得られる結晶性会合体中の結晶形状を調整することができる。例えば、該水性溶液を80℃に1時間保持した後、1時間かけて60℃にし、該温度でさらに1時間保持する。その後1時間かけて40℃まで低下させた後、自然に室温まで下げることで、水溶液の水が流動性をなくした状態のヒドロゲル結晶体を得ることができる。また、上記ポリマーの水性溶液を一気に氷点の氷り水、または氷点下のメタノール/ドライアイス、あるいはアセトン/ドライアイスの冷媒液にて冷却させた後、その状態のものを室温(25℃)の恒温槽にて保持させることで結晶性会合体を得ることができる。さらには、上記のポリマーの水性溶液を室温の恒温槽または室温の空気環境にて、室温まで温度を低下させることでも、結晶性会合体を得ることができる。
【0056】
上記ポリマーの水性溶液の温度を低下させる工程は、得られる結晶性会合体の形状に強く影響を与えるため、上記異なる工程により得られる結晶性会合体の形態は同一ではない。
【0057】
上記により得られる結晶性会合体は、室温中では不溶状態を保つが、結晶融点以上に加熱すると結晶が解離し、透明な溶液に変化してしまう。それを室温に戻すと再び結晶性会合体になる。従って、会合体を可逆的に変化させることが可能である。
【0058】
結晶性会合体の調整時に、他の水溶性ポリマーを加えることで、水溶性ポリマーを含有する結晶性会合体が得られる。該水溶性ポリマーとしては、例えば、ポリエチレングリコール、ポリビニルアルコール、ポリビニルピロリドン、ポリアクリルアミド、ポリ(N−イソプロピルアクリルアミド)、ポリヒドロキシエチルアクリレート、ポリメチルオキサゾリン、ポリエチルオキサゾリンなどをあげることができる。
【0059】
水溶性ポリマーの含有量は、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)の質量に対し、0.1〜5倍の範囲であることが好ましく、0.5〜2倍の範囲であればより好ましい。
【0060】
上記水溶性ポリマーを含有させることによっても、結晶会合体の形態を変えることができ、単純な系と異なる形態の結晶会合体を与えることができる。
【0061】
上記方法で得られた結晶性会合体を、ポリエチレンイミンのアミノ基と反応する官能基を2個以上を含む化合物で処理することで、会合体中のポリマー同士を化学結合でリンクさせて架橋化させることができる。
【0062】
前記アミノ基と室温状態で反応できる官能基を2個以上を含む化合物としては、アルデヒド類架橋剤、エポキシ類架橋剤、酸クロリド類、酸無水物、エステル類架橋剤を挙げることができる。アルデヒド類架橋剤としては、例えば、マロニルアルデヒド、スクシニルアルデヒド、グルタリルアルデヒド、フタロイルアルデヒド、イソフタロイルアルデヒド、テレフタロイルアルデヒドなどがあげられる。また、エポキシ類架橋剤としては、例えば、ポリエチレングリコールジグリシジルエーテル、ビスフェノールAジグリシジルエーテル、グリシジルクロライド、グリシジルブロマイドなどがあげられる。酸クロリド類としては、例えば、マロニル酸クロリド、スクシニル酸クロリド、グルタリル酸クロリド、フタロイル酸クロリド、イソフタロイル酸クロリド、テレフタロイル酸クロリドなどがあげられる。また、酸無水物としては、例えば、フタル酸無水物、スクシニル酸無水物、グルタリル酸無水物などがあげられる。また、エステル類架橋剤としては、マロニル酸メチルエステル、スクシニル酸メチルエステル、グルタリル酸メチルエステル、フタロイル酸メチルエステル、ポリエチレングリコールカルボン酸メチルエステルなどがあげられる。
【0063】
架橋反応は、得られた結晶性会合体を架橋剤の溶液に浸す方法にでも、架橋剤溶液を結晶性会合体中に加える方法でも可能である。この際、架橋剤は系内での浸透圧変化と共に、会合体内部へも浸透し、そこでポリマー(A)同士を水素結合で繋いだり、エチレンイミンの窒素原子との化学反応を引き起こしたりする。
【0064】
架橋反応は、結晶性会合体表面のフリーなエチレンイミンとの反応でも進行するが、それを保つためには、結晶性会合体の融点以下の温度で反応を行うことが望ましく、さらには架橋反応を室温で行うことが最も望ましい。
【0065】
架橋反応を室温で進行させる場合には、結晶性会合体を架橋剤溶液と混合した状態で放置しておくことで、架橋ヒドロゲルを得ることができる。架橋反応させる時間は、数分から数日でよく、概ね一晩放置することで好適に架橋が進行する。
【0066】
架橋剤量は、用いるポリエチレンイミン骨格(a1)を有するポリマー(A)中のエチレンイミンユニットのモル数に対し、0.05〜20モル%であればよく、それが1〜10モル%であればもっと好適である。
【0067】
[シリカソース]
本発明ではシリカソースとして、水ガラス(B)を用いる。水ガラス(ケイ酸ナトリウムまたはケイ酸リチウム)としては、一般式Na2O・xSiO2またはLi2O・xSiO2で示されるものであればよく、特に式中x=1,2,3であれば好適に用いることができる。
【0068】
上の式で示される水ガラス(B)は通常水溶性であるが、その安定性はpHに敏感に依存し、非常に狭いpH値の範囲でしか安定溶液にならない。例えば、珪酸ナトリウムの水溶液は、その水溶液のpHが6.5以上8.5未満では急速に固まり、構造上無規則のシリカゲルになる可能性が高い。本発明の製造方法では、水ガラス(B)を安定化させた状態で用いなければならない。そのためには、水ガラス(B)又は水ガラス(B)の水溶液のpHを8.5以上にすることを必須とする。高度な構造制御のためには、水ガラス(B)又は水ガラスの水溶液のpHを9〜11にすることがさらに好ましい。
【0069】
また、本発明の製造方法では、水ガラス(B)を予め0.01〜2.0モル/Lの範囲に希釈した水溶液として用いることが好ましく、特にポリマー(A)の結晶性会合体と混合した際の安定性を保持しやすい点から、0.1〜1.0モル/Lにすることが好ましい。
【0070】
[ポリマー/シリカ複合ナノ構造体、ポリマー/金属類/シリカ複合ナノ構造体]
本発明で得られるポリマー/シリカ複合ナノ構造体は、上記のポリマー(A)の結晶性会合体の水性分散液またはヒドロゲル中に、予めpH調整をしておいた、シリカソースである水ガラス(B)又はその水溶液を混合し、その混合物を室温〜50℃の条件下で放置することにより容易に得ることができる。
【0071】
該ナノ構造体を与える上記混合物中、水ガラス(B)がシリカ(b1)へ変換するゾルゲル反応は、ポリマー(A)が形成する結晶性会合体が解いてない状態で進行させなければならない。即ち、シリカ析出反応は水性媒体中の任意の場所では起こらず、結晶性会合体の表面にて選択的に進行させる。これを満たす前提であれば、ナノ構造体生成の反応条件を任意に設定することができる。
【0072】
結晶性会合体の水性分散液またはヒドロゲルと、水ガラス(B)又はその水溶液を混合する工程において、水ガラス(B)又はその水溶液のpH、および濃度を調整することで、結晶性会合体を不溶状態に維持することができる。該pHは前述のように8.5以上にすることが必須であり、9〜11の範囲に調整することがより好ましい。濃度は0.1〜1.0モル/Lの範囲であることがより好ましい。
【0073】
また、上記混合工程において、用いるポリマー(A)中のエチレンイミンユニットに対し、シリカソースのケイ素の量を過剰とすれば好適にナノ構造体を形成できる。過剰の範囲として、エチレンイミンユニットに対しケイ素が10〜1000倍当量の範囲であることが好ましい。
【0074】
また、結晶会合体を形成する際、水性媒体中のポリマー(A)の濃度は、該ポリマー(A)中に含まれる直鎖状ポリエチレンイミン骨格(a1)の量を基準に、0.1〜30質量%にすることが好ましく、複合ナノ構造体の構造をもっとも有効に制御するためには、その濃度を0.5〜10質量%にすることが望ましい。
【0075】
シリカ(b1)の析出反応の時間は数分から数十時間まで様々であるが、基本的に10分〜10時間でよく、反応効率を上げることから、反応時間を30分〜5時間に設定すればさらに好適である。また、析出反応時の温度としては、結晶性会合体の融点以下の温度であれば好ましく設定できるが、基本的には70℃以下の温度で反応を行うことが望ましい。
【0076】
本発明で得られるポリマー/シリカ複合ナノ構造体は、多様な形状を有することが大きな特徴であるが、その形状は結晶性会合体の形状の拡大的な複写である。従って、シリカ(b1)の析出前に、水性媒体中でポリマー(A)の結晶を成長させ、結晶性会合体の形状を調整することにより得られるナノ構造体の形状を制御できる。
【0077】
得られるポリマー/シリカ複合ナノ構造体の形状は、マクロ構造的には様々な三次元形状に調整できる。これら複合体の大きさは数μm〜数mm程度の大きさとすることができるが、この大きさの形状は、基本ユニットと見られる20〜50nm太さの繊維状またはラメラ状複合体の会合と空間配置から形成された三次元形状である。この基本ユニットとなる20〜50nm太さの繊維状またはラメラ状複合体には数ナノ大きさの結晶性会合体が含まれる。
【0078】
これらの形状は、上記したようにポリマー(A)の幾何学構造や、分子量、一次構造中に導入できる非エチレンイミン部分、さらにはポリマー(A)の濃度、結晶化温度、後述するポリマー結晶形成時の金属イオンの添加など各種条件等により調整できる。
【0079】
例えば、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)として、重合度が300以上の直鎖状ポリエチレンイミンを使用し、80℃以上に加熱し、完全透明溶液を得た後、その溶液の温度を自然に常温まで低下させて結晶性会合体の水性分散液を得る。その後、該分散液にpH調整した水ガラス(B)の水溶液を加え、シリカ(b1)析出反応を進行させることにより、ナノファイバーのスポンジ状の構造体が得られる。
【0080】
また、直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)として、ベンゼン環コアに4〜6本のポリエチレンイミンアームが結合した星型のポリマー(A)を使用すると、上記と同様な操作で、扇子形状のナノ構造体を得ることができる。
【0081】
さらに前記した結晶性会合体が化学結合で架橋された架橋ヒドロゲルを用いることにより、複合ナノ構造体のマクロな形状を制御して、該構造体を各種形状の成形体とすることもできる。その形状や大きさは、架橋ヒドロゲル調整時に用いた容器の大きさ及び形状と同一なものにすることができ、例えば、円盤状、円柱状、プレート状、球状などの任意の形状に調整できる。さらに、架橋ヒドロゲルを切断したり、削ったりすることにより、目的の形に成形することもできる。このように成形した架橋ヒドロゲルをシリカソースである水ガラス(B)の水溶液に浸せきさせることにより、ポリマー/シリカ複合ナノ構造体からなる成形体が簡単に得られる。この時、水ガラス(B)の水溶液に浸せきする時間としては、使用する水ガラス(B)水溶液の濃度、該水溶液のpHにより1時間〜1週間と様々であるため適宜調整する必要があるが、1〜48時間程度であれば好適である。
【0082】
本発明で得られるポリマー/シリカ複合ナノ構造体は、ポリマー(A)からなる結晶性会合体とシリカ(b1)とから構成され、複合ナノ構造体中のシリカ(b1)の含有量は、反応条件などにより調整可能であるが、ナノ構造体全体の30〜90質量%の範囲のものを得ることができる。該シリカ(b1)の含有率は、用いるポリマー(A)の濃度を高くしたり、また反応時間を長くしたりする事により高めることができる。
【0083】
また、ポリマー(A)を用いて、水性媒体中で結晶性会合体を形成させる際に、金属イオン(c1)を予め該水性媒体中に存在させておくことにより、該ポリマー(A)中の直鎖状ポリエチレンイミン骨格(a1)と金属イオン(c1)とが錯体を形成することから、金属イオン(c1)を含有する結晶性会合体の水性分散液を得ることができる。この分散液を用いて前述と同様にしてシリカ(b1)の析出反応を行うことにより、ポリマー/金属イオン/シリカ複合ナノ構造体を得ることができる。
【0084】
ポリマー(A)と金属イオン(c1)との混合液を調整する際、ポリマー(A)中のエチレンイミンユニットと金属イオン(c1)とのモル比が1/1〜100/1の範囲で任意に設定することができ、このモル比を調整することによって、得られるポリマー/金属イオン/シリカ複合ナノ構造体中のそれぞれの含有率を調整することが可能である。
【0085】
前記金属イオン(c1)の金属種としては、特に限定されるものではなく、例えば、アルカリ金属のNa,Li,K,Csなど、アルカリ土類金属のCa,Mgなど、遷移金属のFe,Mn,Co,Cr,Cu,Ru,Rh,V,Pd,Mo,Ti,Zr,Eu,Gd,Zn,Cdなど、半金属のAl,Ga,Sn,In,Pbなどを好適に用いることができる。
【0086】
前記で得られたポリマー/金属イオン/シリカ複合ナノ構造体中の金属イオン(c1)は、還元剤(D)を加えることで還元し、ナノメートルオーダーの金属ナノ粒子(c2)が含まれたポリマー/金属ナノ粒子/シリカ複合ナノ構造体とすることもできる。
【0087】
前記複合ナノ構造体中の金属イオン(c1)を金属ナノ粒子(c2)に還元する際に用いることができる還元剤(D)としては、低分子量の還元剤であることが好ましく、例えば、アスコルビン酸、クエン酸ナトリウム、水素化ホウ素ナトリウム、水素化ホウ素アンモニウム、水素、ヒドラジン、アルデヒドなどを挙げることができる。
【0088】
上記還元剤(D)の水溶液またはアルコール溶液とポリマー/金属イオン/シリカ複合ナノ構造体とを混合し、その混合物を室温〜60℃で0.5〜24時間撹拌することで、構造体中の金属イオン(c1)を金属ナノ粒子(c2)へ容易に還元できる。
【0089】
また、還元剤を使わず、前述のポリマー/シリカ複合ナノ構造体を、金、銀及び白金からなる群から選ばれる1種以上の金属イオン(c1’)を含有する溶液と混合することで、ポリマー(A)中の直鎖状ポリエチレンイミン骨格(a1)の還元作用及び自発還元によって、ポリマー/金属ナノ粒子/シリカ複合ナノ構造体を得ることもできる。金、銀、白金のイオンとして、例えば、塩化金酸、塩化金酸ナトリウム、硝酸銀、塩化白金酸、塩化白金酸ナトリウムの水溶液が挙げられ、これらの水溶液とポリマー/シリカ複合ナノ構造体とを混合し、それを室温〜60℃以下で撹拌することで、それぞれの金属のナノ粒子(c2’)が含まれたポリマー/金属ナノ粒子/シリカの複合ナノ構造体を得ることができる。この時、金属イオン(c1’)が金属ナノ粒子(c2’)と還元する途中では、金属イオン(c1’)と金属ナノ粒子(c2’)とが共存することになるが、本発明のポリマー/金属類/シリカ複合ナノ構造体は、この共存した状態のものも含む。
【0090】
[シリカ系無機構造体]
前述で得られたポリマー/シリカ複合ナノ構造体、ポリマー/金属イオン/シリカ複合ナノ構造体、ポリマー/金属ナノ粒子/シリカ複合ナノ構造体を加熱焼成することで、それぞれ、ポリマーが除去されたシリカ構造体、金属酸化物/シリカ複合体、金属ナノ粒子/シリカ複合体(本発明では、これらを総称してシリカ系無機構造体という。)を得ることができる。
【0091】
加熱焼成を行う際には、前述の複合ナノ構造体の粉末を電気炉中に放置し、炉内温度を500℃まで上昇させ、その温度で1〜3時間維持した後、自然に温度を室温まで降下させる方法が好ましい。この操作により、ポリマー(A)が除去されたシリカ系無機構造体を容易に得ることができる。得られる構造体は、それぞれ原料として用いたナノ構造体の中からポリマー(A)のみが除去された構造であり、基本ユニットと見られる20〜50nm太さの繊維状またはラメラ状の空間配置から形成された三次元形状であり、高い比表面積を有するものである。
【実施例】
【0092】
以下、合成例、実施例によって本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。特に断らない限り、「%」は「質量%」を表す。
【0093】
[X線回折法によるナノ構造体の分析]
単離乾燥したナノ構造体を測定試料用ホルダーにのせ、それを株式会社リガク製広角X線回折装置「Rint−Ultma」にセットし、Cu/Kα線、40kV/30mA、スキャンスピード1.0°/分、走査範囲10〜40°の条件で測定を行った。
【0094】
[TG−DTA(差動形示差熱天秤)によるナノ構造体の熱重量分析]
単離乾燥したナノ構造体を測定パッチにより秤量し、それをSIIナノテクノロジー株式会社製「TG−DTA 6300」にセットし、昇温速度を10℃/分として、50℃から500℃の温度範囲にて測定を行った。
【0095】
[X線蛍光分析によるナノ構造体の元素分析]
元素組成分析は株式会社リガク製X線蛍光分析にて行った。
【0096】
[固体29Si−NMRによるナノ構造体のケイ素分析]
ナノ構造体粉末を日本電子株式会社製NMR 「JNM−ECA600」にてCP/MAS方法で測定した。測定の際の外部標準物として、ポリジメチルシラン(−33.8ppm)を用いた。
【0097】
[走査電子顕微鏡によるナノ構造体の形状分析]
単離乾燥したナノ構造体をガラススライドに乗せ、それをキーエンス製表面観察装置VE−9800にて観察した。
【0098】
[透過電子顕微鏡によるナノ構造体の観察]
単離乾燥したナノ構造体を炭素蒸着された銅グリッドに乗せ、それを日本電子株式会社製透過型電子顕微鏡「JEM−2200FS」にて観察した。
【0099】
合成例1
<直鎖状のポリエチレンイミン(L−PEI)の合成>
市販のポリエチルオキサゾリン(数平均分子量500,000、平均重合度5,000、Aldrich社製)5gを、5モル/Lの塩酸20mLに溶解させた。その溶液をオイルバスにて90℃に加熱し、その温度で10時間攪拌した。反応液にアセトン50mLを加え、ポリマーを完全に沈殿させ、それを濾過し、メタノールで3回洗浄し、白色のポリエチレンイミンの粉末を得た。得られた粉末を1H−NMR(重水)にて同定したところ、ポリエチルオキサゾリンの側鎖エチル基に由来したピーク1.2ppm(CH3)と2.3ppm(CH2)が完全に消失していることが確認された。即ち、ポリエチルオキサゾリンが完全に加水分解され、ポリエチレンイミンに変換されたことが示された。
【0100】
その粉末を5mLの蒸留水に溶解し、攪拌しながら、その溶液に15%のアンモニア水50mLを滴下した。その混合液を一晩放置した後、沈殿した結晶粉末を濾過し、その結晶粉末を冷水で3回洗浄した。洗浄後の結晶粉末をデシケータ中で室温(25℃)乾燥し、直鎖状のポリエチレンイミン(L−PEI)を得た。収量は4.2g(結晶水含有)であった。ポリオキサゾリンの加水分解により得られるポリエチレンイミンは、側鎖だけが反応し、主鎖には変化がない。従って、L−PEIの重合度は加水分解前の5,000と同じである。
【0101】
合成例2
<ベンゼン環中心の星状ポリエチレンイミン(B−PEI)合成>
Jin,J.Mater.Chem.,13,672−675(2003)に示された方法に従い、前駆体ポリマーであるベンゼン環中心に6本のポリメチルオキサゾリンのアームが結合した星状ポリメチルオキサゾリンの合成を次の通り行った。
【0102】
磁気攪拌子がセットされたスリ口試験管中に、重合開始剤としてヘキサキス(ブロモメチル)ベンゼン0.021g(0.033mmol)を入れ、試験管の口に三方コックをつけた後、真空状態にしてから窒素置換を行った。窒素気流下で三方コックの導入口からシリンジを用いて2−メチル−2−オキサゾリン2.0ml(24mmol)、N,N−ジメチルアセトアミド4.0mlを順次加えた。試験管をオイルバス上で60℃まで加熱し、30分間保ったところ、混合液は透明になった。透明混合液をさらに100℃まで加熱し、その温度で20時間攪拌して、前駆体ポリマーを得た。この混合液の1H−NMR測定から、モノマーの転化率は98モル%、収量は1.8gであった。この転化率によりポリマーの平均重合度を見積もったところ、各アームの平均重合度は115であった。また、GPCによる分子量測定では、ポリマーの質量平均分子量は22,700であり、分子量分布は1.6であった。
【0103】
この前駆体ポリマーを用い、上記合成例1と同様な方法によりポリメチルオキサゾリンを加水分解し、6本のポリエチレンイミンがベンゼン環コアに結合した星状ポリエチレンイミンB−PEIを得た。1H−NMR(TMS外部標準、重水中)測定の結果、加水分解前の前駆体ポリマーの側鎖メチルに由来した1.98ppmのピークは完全に消失したことが確認された。
【0104】
その粉末を5mLの蒸留水に溶解し、攪拌しながら、その溶液に15%のアンモニア水50mLを滴下した。その混合液を一晩放置した後、沈殿した結晶粉末を濾過し、その結晶粉末を冷水で3回洗浄した。洗浄後の結晶粉末をデシケータ中で室温(25℃)乾燥し、6本のポリエチレンイミンがベンゼン環コアに結合した星状ポリエチレンイミン(B−PEI)を得た。収量は1.3g(結晶水含有)であった。
【0105】
合成例3
<ブロック共重合体PEG−b−PEIの合成>
数平均分子量が4,000のポリエチレングリコール(PEG)の片末端にトシレートが結合したポリマーを重合開始剤(PEG−I)として用い、前駆体ブロックポリマーであるPEGとポリオキサゾリンのブロック共重合体の合成を次の通り行った。
【0106】
磁気攪拌子がセットされたスリ口試験管中に、重合開始剤としてPEG−Iを1.5g(0.033mmol)取り入れ、試験管の口に三方コックをつけた後、真空状態にしてから窒素置換を行った。窒素気流下で三方コックの導入口からシリンジを用いて2−メチル−2−オキサゾリン6.0ml(72mmol)、N,N−ジメチルアセトアミド20.0mlを順次加えた。試験管をオイルバス上で100℃まで加熱し、その温度で24時間攪拌して前駆体ブロックポリマーを得た。得られた混合液の1H−NMR測定から、モノマーの転化率は100モル%であることがわかった。
【0107】
精製後の前駆体ブロックポリマーの収率は93%であった。また、1H−NMR測定において、ポリマー末端トシル基を基準とした各積分比を求めたが、PEGの重合度は45、ポリオキサゾリンの重合度は93であった。即ち、ブロックポリマーの平均重合度は138であった。また、GPCによる分子量測定では、ポリマーの数平均分子量は12,000であり、分子量分布は1.27であった。
【0108】
この前駆体ブロックポリマーを用い、上記合成例1と同様の方法によりポリオキサゾリンブロックを加水分解し、PEGにポリエチレンイミンが結合したブロック共重合体(PEG−b−PEI)を得た。1H−NMR(TMS外部標準、重水中)測定の結果、加水分解前の前駆体ポリマーの側鎖メチルに由来した1.98ppmのピークは完全に消失した。
【0109】
実施例1−1〜1−3、及び比較例1〜3
<直鎖状ポリエチレンイミンからのナノ構造体の製造>
合成例1で得られたL−PEI粉末を用い、蒸留水中に分散させた後、オイルバスにて90℃に加熱し、完全透明な水溶液を得た。その水溶液を室温に放置し、自然に室温までに冷やし、1%の不透明な結晶性会合体を得た。一方、水ガラス3号(キシダ化学株式会社製、pH=11.3)を用い、pH値が9.4(実施例1−1)、9.8(実施例1−2)、10(実施例1−3)、及びpHが2(比較例1)、4(比較例2)、6(比較例3)の0.2モル/Lの水ガラス水溶液を調整した。水ガラス水溶液のpH値調整には1モル/Lの塩酸と25%アンモニア水を用いた。
【0110】
上記で得られた濃度1%の結晶性会合体の水分散液10gと、0.2モル/Lの水ガラス水溶液20mlとを混合し、5分間撹拌した後、静置状態で50℃下2時間析出反応させ、白色の沈殿物を得た。反応液中の上澄みを除去し、沈殿物を蒸留水で洗浄した後、遠心分離にて3回繰り返し洗浄した。得られた固形物を室温で乾燥後、真空乾燥機にて60℃下12時間乾燥し、ナノ構造体(1−1)〜(1−3)及び比較例1〜3を得た。得られた粉末の収量を表1に示す。
【0111】
【表1】

【0112】
得られたナノ構造体の走査型顕微鏡写真(SEM)観察の結果を図1〜6に示した。pH値2〜6の水ガラス水溶液から得た構造体(1)〜(3)は、基本的にバルキーの固まりであったが、pH値を9.4〜10に調整した水ガラス水溶液から得たナノ構造体(1−1)〜(1−3)はファイバー状ネットワーク構造を有するスポンジであった。
【0113】
実施例1−3で得られたナノ構造体(1−3)の透過型電子顕微鏡(TEM)写真を図7に示した。非常に薄いラメラ状シリカ(左図)中には、一定的な陰(右図)のイメージが観察された。その陰はポリマーとシリカとが数ナノレベルで複合された部分によるコントラストであると推測される。
【0114】
実施例1−3で得られたナノ構造体(1−3)の固体29Si−NMR(CP/MAS)測定から、シリカ結合構造を示すQ4シグナルが−110ppm、Q3シグナルが−101ppmに現れ、Q4/Q3の積分比は1.00/0.68であった(図8参照)。Q2結合シグナルは現れなかった。このことは、ファイバー状ネットワークを形成しているシリカは高度なSi(0Si)4結合ユニットを有することを強く示唆する。
【0115】
さらに、実施例1−3で得られたナノ構造体(1−3)の元素分析の結果、Si:30%、C:15%、H:4.1%、N:8.2%、Na:0.8%であった。このことは、ナノ構造体(1−3)には、ケイ素以外の、直鎖状ポリエチレンイミンが複合され、その含有率が約27%であることが示唆された。即ち、得られたナノ構造体はシリカとポリマーとが複合された構造体である。
【0116】
実施例2
実施例1−3で得られたナノ構造体(1−3)0.1gアルミナ坩堝中に入れ、電気炉中にて500℃まで加熱し、その温度下1時間焼成した。収量は0.07gであった。を500℃にて1時間焼成して、シリカ系無機構造体を得た。SEM観察の結果、ファイバー構造には変わりがなく(図9参照)、29Si−NMR(CP/MAS)ではQ4/Q3の積分比は1.00/0.52であった(図10参照)。即ち、Q4構造成分がやや増える傾向であった。
【0117】
さらに、熱焼成前後の構造体の比表面積をN2/He 混合ガス(3/7体積比)の吸着−脱着実験法でFlow Sorb II 2300(Micromeritics)を用いて測定した結果、焼成前の149m2/gから焼成後の315m2/gまで2倍ほど大きく増大した。焼成によるポリマー除去が表面積を増大させることが示唆された。
【0118】
実施例3−1
<金ナノ粒子が含まれるナノ構造体>
実施例1−3で得られたナノ構造体(1−3)0.05gを2mLの0.1モル/L NaAuCl4溶液中に加え、室温(25℃)下で5分間撹拌後、そのまま25分間静置させた。得られた固形分を蒸留水で洗浄した後、室温乾燥した。これで得られた粉末のXRD測定から、金の結晶の存在を示す散乱ピーク(2θ)が38.1°、44.4°、64.5°、77.6°で確認された。また、TEM観察から、2〜3nmの大きさの金のナノ粒子がシリカ中に閉じ込まれていることが観測された(図11)。これは金属ナノ粒子が含まれてない図7のイメージと大きく異なるものであった。
【0119】
実施例3−2
<白金ナノ粒子が含まれるナノ構造体>
実施例1−3で得られたナノ構造体(1−3)0.05gを2mLの0.1モル/L Na2PtCl4溶液中に加え、室温下5分間撹拌後、そのまま25分間静置させた。得られた固形分を蒸留水で洗浄した後、室温乾燥した。これで得られた粉末のXRD測定から、白金の結晶の存在を示す散乱ピーク(2θ)が40.0°、46.4°、67.7°で観測された。また、TEM観察から、2〜3nm大きさの白金のナノ粒子がシリカ中に閉じ込まれていることが観測された(図12)。これは金属ナノ粒子が含まれてない図7のイメージと大きく異なるものであった。
【0120】
実施例4
<ベンゼン環中心のポリエチレンイミンからのナノ構造体>
合成例2で合成したB−PEIを使用し、実施例1と同様な方法により、2%のポリマーの結晶性会合体の分散液を調整した。この分散液10gに、pH値が9.6の0.2モル/L水ガラス水溶液20mLを加え、室温(25℃)で1時間放置した。上澄みを取り出し、固形物を蒸留水で洗浄した後、遠心分離機にて3回繰り返し洗浄した。得られた固形物を室温で乾燥後、真空乾燥機にて60℃下12時間乾燥し、白色のナノ構造体(4)を得た。収量は0.53gであった。
【0121】
上記で得られたナノ構造体(4)のSEM観察写真、TEM観察写真を図13と図14に示し。扇子状の複合ナノ構造体のイメージが明確に現れた。また、ナノ構造体(4)のXRD測定では、ポリマー結晶由来の散乱ピークが20.3°、27.3°、28.2°で確認された。
【0122】
実施例5−1〜5−4
<ブロック共重合体からのナノ構造体>
合成例3で得られたブロック共重合体(PEG−b−PEI)を用い、90℃に加温下、硝酸ナトリウム、硝酸銅、硝酸アルミニウムを含む2%のポリマー溶液3種類と金属イオンを含まないポリマー溶液を調整した。溶液中の各金属イオンとポリマー中のエチレンイミンユニット(EI)とのモル比を表2に示す。これら溶液を室温に6時間静置し、結晶性会合体を得た。それぞれの結晶性会合体の分散液10gに、pH値が9.6の0.2モル/L水ガラス水溶液20mLを加え、5分間撹拌後、室温で1時間静置した。析出した固形分を蒸留水で洗浄し、さらに遠心分離機にて3回繰り返し洗浄した。得られた固形物を室温で乾燥後、真空乾燥機にて60℃下12時間乾燥し、ポリマー/金属イオン/シリカ複合ナノ構造体(5−1)〜(5−4)を得た。収量は表2に示した。
【0123】
【表2】

【0124】
実施例5−1〜5−4で得られたナノ構造体(5−1)〜(5−4)のSEM観察写真を、図15〜図18に示す。金属イオンの存在により、得られた構造体の形状に大きな変化が起こることが示唆された。
【0125】
実施例6
実施例5−3の銅イオンが含まれたナノ構造体(5−3)のサンプル0.3gを10mLの0.1モル/Lの水素化ホウ素アンモニウム水溶液と混合し、窒素雰囲気下、40℃で1時間撹拌した。窒素雰囲気下、エタノールで洗浄し、窒素雰囲気下乾燥させた。これで得た粉末は元の青色が完全に消え、薄い銅色を示した。粉末XRD測定から、ゼロ価銅の存在を示す散乱ピーク2θ(°)が43.4,50.5,74.1が観測され、還元反応が起きたことを確認した。
【図面の簡単な説明】
【0126】
【図1】比較例1で得た構造体(1)の走査型電子顕微鏡写真である。
【図2】比較例2で得た構造体(2)の走査型電子顕微鏡写真である。
【図3】比較例3で得た構造体(3)の走査型電子顕微鏡写真である。
【図4】実施例1−1で得たナノ構造体(1−1)の走査型電子顕微鏡写真である。
【図5】実施例1−2で得たナノ構造体(1−2)の走査型電子顕微鏡写真である。
【図6】実施例1−3で得たナノ構造体(1−3)の走査型電子顕微鏡写真である。
【図7】実施例1−3で得たナノ構造体(1−3)の透過型電子顕微鏡写真である。右図は左図円形部分の高分解能イメージである。
【図8】実施例1−3で得たナノ構造体(1−3)の固体29Si−NMR(CP/MAS)スペクトルである。
【図9】実施例1−3で得たナノ構造体(1−3)の熱焼成前後の走査型電子顕微鏡写真である。
【図10】実施例1−3で得たナノ構造体(1−3)の熱焼成後の固体29Si−NMR(CP/MAS)スペクトルである。
【図11】実施例3−1で得た金ナノ粒子を含むナノ構造体(3−1)の透過型電子顕微鏡写真である。右図は左図円形部分の拡大イメージである。黒い斑点は2nm程度の金ナノ粒子の写真である。
【図12】実施例3−2で得た白金ナノ粒子を含むナノ構造体(3−2)の透過型電子顕微鏡写真である。右図は左図円形部分の拡大イメージである。黒い斑点は2nm程度の白金ナノ粒子の写真である。
【図13】実施例4で得たナノ構造体(4)の走査型電子顕微鏡写真である。
【図14】実施例4で得たナノ構造体(4)の透過型電子顕微鏡写真である。右図は左図の拡大図である。
【図15】実施例5−1で得たナノ構造体(5−1)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【図16】実施例5−2で得たナノ構造体(5−2)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【図17】実施例5−3で得たナノ構造体(5−3)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【図18】実施例5−4で得たナノ構造体(5−4)の走査型電子顕微鏡写真である。右図は左図の拡大図である。
【特許請求の範囲】
【請求項1】
直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を水性媒体中で結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合してシリカ(b1)を析出させることを特徴とするポリマー/シリカ複合ナノ構造体の製造方法。
【請求項2】
直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)と金属イオン(c1)とを水性媒体中で混合して金属イオン(c1)を含有する結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合してシリカ(b1)を析出させることを特徴とするポリマー/金属イオン/シリカ複合ナノ構造体の製造方法。
【請求項3】
直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)と金属イオン(c1)とを水性媒体中で混合して金属イオン(c1)を含有する結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合してシリカ(b1)を析出させ、更に金属イオン(c1)を還元剤(D)で還元して金属ナノ粒子(c2)とすることを特徴とするポリマー/金属ナノ粒子/シリカ複合ナノ構造体の製造方法。
【請求項4】
請求項1で得られるポリマー/シリカ複合ナノ構造体を、金、銀及び白金からなる群から選ばれる1種以上の金属イオン(c1’)を含有する水溶液と混合することにより、該金属イオン(c1’)をナノ構造体中のポリマー(A)に濃縮させながら、かつ自発的還元により金属ナノ粒子(c2’)とすることを特徴とするポリマー/金属ナノ粒子/シリカ複合ナノ構造体の製造方法。
【請求項5】
請求項1〜4の何れか1項記載の方法により得られたナノ構造体を、更に熱焼成させることを特徴とするシリカ系無機構造体の製造方法。
【請求項1】
直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)を水性媒体中で結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合してシリカ(b1)を析出させることを特徴とするポリマー/シリカ複合ナノ構造体の製造方法。
【請求項2】
直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)と金属イオン(c1)とを水性媒体中で混合して金属イオン(c1)を含有する結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合してシリカ(b1)を析出させることを特徴とするポリマー/金属イオン/シリカ複合ナノ構造体の製造方法。
【請求項3】
直鎖状ポリエチレンイミン骨格(a1)を有するポリマー(A)と金属イオン(c1)とを水性媒体中で混合して金属イオン(c1)を含有する結晶性会合体とし、これとpHを8.5以上に調整した水ガラス(B)とを混合してシリカ(b1)を析出させ、更に金属イオン(c1)を還元剤(D)で還元して金属ナノ粒子(c2)とすることを特徴とするポリマー/金属ナノ粒子/シリカ複合ナノ構造体の製造方法。
【請求項4】
請求項1で得られるポリマー/シリカ複合ナノ構造体を、金、銀及び白金からなる群から選ばれる1種以上の金属イオン(c1’)を含有する水溶液と混合することにより、該金属イオン(c1’)をナノ構造体中のポリマー(A)に濃縮させながら、かつ自発的還元により金属ナノ粒子(c2’)とすることを特徴とするポリマー/金属ナノ粒子/シリカ複合ナノ構造体の製造方法。
【請求項5】
請求項1〜4の何れか1項記載の方法により得られたナノ構造体を、更に熱焼成させることを特徴とするシリカ系無機構造体の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【公開番号】特開2009−24124(P2009−24124A)
【公開日】平成21年2月5日(2009.2.5)
【国際特許分類】
【出願番号】特願2007−190690(P2007−190690)
【出願日】平成19年7月23日(2007.7.23)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
【公開日】平成21年2月5日(2009.2.5)
【国際特許分類】
【出願日】平成19年7月23日(2007.7.23)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
[ Back to top ]

