マイクロチップ
【課題】 従来の大型装置と同等またはそれ以上の精度で、検体と試薬を混合して検査を行うことが可能なマイクロチップを提供する。
【解決手段】 その一端25に向けて検体を流すことができる微小な流路である検体流路21と、検体流路21の一端25に接続され、検体と反応する少なくとも一つの試薬を流すことができる微小な流路である試薬流路23と、検体流路21の一端25から延在し、合流した検体と試薬とを流すことができる微小な流路である合流流路27と、合流流路27の近傍に配置され、検体と試薬との反応を検出できるようにする検出部26と、検出部2において検体と試薬とを往復動させる力を付与する付与手段30を備える。
【解決手段】 その一端25に向けて検体を流すことができる微小な流路である検体流路21と、検体流路21の一端25に接続され、検体と反応する少なくとも一つの試薬を流すことができる微小な流路である試薬流路23と、検体流路21の一端25から延在し、合流した検体と試薬とを流すことができる微小な流路である合流流路27と、合流流路27の近傍に配置され、検体と試薬との反応を検出できるようにする検出部26と、検出部2において検体と試薬とを往復動させる力を付与する付与手段30を備える。
【発明の詳細な説明】
【0001】
【発明の属する技術分野】本発明は、マイクロチップに関し、詳しくは、検体と試薬との反応を検出するためのマイクロチップに関し、例えば血液凝固検査、免疫学的検査、生化学的検査、遺伝子検査等に好適に使用することができるマイクロチップに関する。
【0002】
【従来の技術】従来、例えば血液の凝固反応を測定する装置として、光散乱検出方式の装置や磁力センサー検出方式の装置が知られている。
【0003】光散乱検出方式の装置では、例えば図11に示すように、検体と試薬とを混合したキュベット7に光源5から光5aを照射し、検体と試薬との混合液からの散乱光5bを検出器6で検出する。検体と試薬との反応と、検出した散乱光5bの強度とは一定の相関関係があるので、検体の検査を行うことができる。この装置は、静止した混合液の変化を検出するものであり、検体と試薬の混合時に発生する泡によるノイズや血液の濁りなどの変化に弱い。
【0004】磁力センサー検出方式の装置では、例えば図12に示すように、検体と試薬との混合液とスチールボール8とが入ったキュベット7’を、垂直から少し傾いた軸を中心に回転し、スチールボール8の動きを磁力センサー8で検出する。例えば血液の凝固により混合液の粘稠度が変化すると、底に沈んでいたスチールボール8が動き出すことを利用して、混合液の粘稠度の変化を検出する。この装置では、キュベット7’を回転する必要があり、微小な粘稠度の変化まで検出することができない。
【0005】このような従来の装置(大型装置)は、ある程度の量の血液を採取する必要がある。また、据え置き型の装置であり、持ち運ぶことができないので、POC(Point Of Care、その場治療)に対応することができない。また、検査時間の短縮や検査精度の向上に限界がある。また、廃棄物の量も多い。
【0006】ところで、最近、マイクロマシン技術を応用して、化学分析や合成などの機器・手法を微細化して行うμ―TAS(μ−Total Analysis System)が注目されている。従来の装置に比べ微細化されたμ−TASでは、試料の量が少ない、反応時間が短い、廃棄物が少ないなどのメリットがある。また、医療分野に使用した場合、検体(血液)の量を少なくすることで患者への負担を軽減し、試薬の量を少なくすることで検査のコストを下げることが期待できる。
【0007】例えば、Roche Diagnostics社は、血液が毛細管現象により試薬チャンバー内を流れながら試薬と混合するマイクロチップを用い、血液の流動停止を散乱光の変化として捉え、流動停止までの時間を計測する装置を提供している。
【0008】
【発明が解決しようとする課題】この装置は、検体量は数十μリット程度とかなり少ないものの、試薬がドライ(マイクロチップに固定化されたもの)であるため、マイクロチップは高価である。また、測定精度は、従来の大型装置ほどは良くない。
【0009】したがって、本発明が解決しようとする技術的課題は、従来の大型装置と同等またはそれ以上の精度で、検体と試薬を混合して検査を行うことが可能なマイクロチップを提供することである。
【0010】
【課題を解決するための手段および作用・効果】本発明は、上記技術的課題を解決するために、以下の構成のマイクロチップを提供する。
【0011】マイクロチップは、微小な流路である検体流路、試薬流路、および合流流路と、検出部とを備える。上記検体流路は、その一端に向けて検体を流すことができる。上記試薬流路は、上記検体流路の上記一端に接続され、上記検体と反応する少なくとも一つの試薬を流すことができる。上記合流流路は、上記検体流路の上記一端から延在し、合流した上記検体と上記試薬とを流すことができる。上記検出部は、上記合流流路の近傍に配置され、上記検体と上記試薬との反応を検出できるようにする。更に、マイクロチップは、付与手段を備え、付与手段は上記検出部において上記検体と上記試薬とを往復動させる力を付与する。
【0012】上記構成において、「試薬」は、それ自体が直ちに検体と反応することができるもののみならず、2以上が混合して初めて検体と反応することができるようになるものをも含む。「検出部」は、例えば合流流路近傍の歪みや温度、電位等を検出することにより、検体と試薬との反応をそれ自体が直接検出するもの(例えば、圧電素子、熱電対、導電性を有する部分など)であっても、あるいは、それ自体は何ら検出するものではないが、マイクロチップの外部から検体と試薬との反応を検出することができるようにするもの(例えば、透明な部分)であってもよい。
【0013】上記構成によれば、検体と試薬を検体流路の一端に向けて流して合流させ、合流流路内を移動させる。合流した検体と試薬は、微小な合流流路内で極めて短時間で混合する。そして、混合した検体と試薬とが反応し、その反応を検出部で検出することができる。具体的には、混合した検体と試薬とは検出部において往復動しながら反応する。そして、この往復動の様子を観測乃至検出することで反応の様子を検出することができる。さらには、検体と試薬とともに含まれる微小な粒子の動きを検出するなどして、より高度な検査を行うことが可能になる。
【0014】上記構成によれば、検体と試料が極微量であっても反応は起こるので、従来の大型装置と同様の測定原理に基づいて検査を行うことができる。また、検体が極微量であれば、検体の濁りなどの影響も少なくなる。また、微小な反応を捉えるために検出感度(分解能)を上げ、検査精度を高めることも可能である。
【0015】したがって、従来の大型装置と同等、又はそれ以上の精度で検査を行うことができる。
【0016】なお、複数の試薬を用いる場合には、例えば試薬流路を枝分かれした構成として複数の試薬を流すようにしても、あるいは、検体流路の一端以外で検体流路に合流する微小な流路を設け、そこからも試薬を流すようにしてもよい。また、検体流路、試薬流路、又は合流流路の適宜位置で合流する微小な流路から、洗浄液や、検体や試薬と混合しても反応しないバッファ液などを流すようにしてもよい。
【0017】また、検体と試薬とは往復動をしながら反応するため、反応に要する経路長を短くすることができる。したがって、マイクロチップ自体の小型化、ひいては検出装置の小型化を実現できる。
【0018】また、本発明は、以下の構成のマイクロチップを提供する。
【0019】マイクロチップは、検体を流すことができる微小な流路である混合流路を備える。該混合流路は、上記検体に添加されて反応する試薬を保持する試薬添加部と、上記検体と上記試薬との反応を検出することができる検出部とを有する。更に、このマイクロチップは、上記検出部において上記検体と上記試薬とを往復動させるための力を付与する付与手段を備える。
【0020】上記構成において、試薬添加部は、検体に添加するまで試薬を仮固定し、検体と出会うことによって試薬が剥離したり溶解するようにしても、あるいは、単に試薬を収納しただけで移動自在な状態であってもよい。
【0021】上記構成によれば、混合流路に検体を流し、検体が試薬添加部に達すると、試薬は検体に添加され、検体とともに移動し、検体と混合しながら反応する。そして、検体と試薬との反応を、検出部を介して検出することができる。具体的には、混合した検体と試薬とは検出部において往復動しながら反応する。そして、この往復動の様子を観測乃至検出することで反応の様子を検出することができる。さらには、検体と試薬とともに含まれる微小な粒子の動きを検出するなどして、より高度な検査を行うことが可能になる。
【0022】上記構成によれば、検体と試料が極微量であっても反応は起こるので、従来の大型装置と同様の測定原理に基づいて検査を行うことができる。また、検体が極微量であれば、検体の濁りなどの影響も少なくなる。また、微小な反応を捉えるために検出感度(分解能)を上げ、検査精度を高めることも可能である。
【0023】したがって、従来の大型装置と同等、又はそれ以上の精度で検査を行うことができる。
【0024】上記の何れのマイクロチップにおいても、付与手段として種々な構成が採用できる。例えば、電気泳動を利用して検体、試薬を移動させる形態においては、電気的な力を付与する手段、例えば電極対、が採用できる。また、電気的な力ではなく、検体及び試薬を含む流体自体に往復動を生じさせる圧力を付与する手段、例えばマイクロポンプ、であってもよい。この場合、好ましくは、上記検体流路、上記試薬流路、上記合流流路および上記混合流路の少なくとも一つにマイクロポンプ、好ましくは双方向に吸込・吐出が可能なマイクロポンプ、を備える。
【0025】好ましくは、上記検出部は、マイクロチップの外部と上記合流流路又は上記混合流路とに隣接しかつ連続的に延在しかつ導光性を有する。
【0026】上記構成によれば、合流流路又は混合流路内から、検出部を通ってマイクロチップの外部に、光が出射するようにすることができる。これにより、例えば、検体と試薬との反応による発光を、マイクロチップの外部から検出することができる。また、合流流路又は混合流路内の検体と試薬とに光を当て、その散乱光、反射光、透過光、あるいは影像を捉え、それによって検体と試薬との反応の検出を行うことができる。
【0027】また、本発明は、以下のマイクロチップを提供する。
【0028】即ち、マイクロチップは、検体を含む液体を流すことができる微小な流路と、その一端側に第1ディフューザーを有すると共にその他端側に第2ディフューザーを有したポンプ室を備え前記第1ディフューザーが前記流路に接続されたマイクロポンプと、を備え、前記ポンプ室の圧力変化に対する、前記第1ディフューザーの流路インピーダンスの変化特性と前記第2ディフューザーの流路インピーダンスの変化特性とが互いに異なる。
【0029】上記構成によれば、第1ディフューザーと第2ディフューザーとが互いにその流路インピーダンスの、ポンプ室の圧力変化に対する変化特性が異なるため、ポンプ室の圧力変化を適宜調整するといった簡略な制御により、上記流路に液体を吐出することも上記流路から液体を吸入することもできる。したがって、流路内の液体を当該流路に沿って往復動させることができ、検体と試薬との反応に要する経路長を長く取らなくてもよく、マイクロチップ自体の小型化、ひいては検出装置の小型化を実現できる。
【0030】また、本発明は、以下の反応検出方法を提供する。
【0031】反応検出方法は、微小な流路を有するマイクロチップを用いて、検体と試薬の反応を検出するタイプの方法である。反応検出方法は、上記マイクロチップの上記流路内において、上記検体に、上記試薬と微小な粒子とを添加する第1ステップと、上記試薬および上記粒子が添加された上記検体に、上記流路に沿っ繰り返し往復動を行わせる力を与える第2ステップと、上記流路内における上記粒子の動きを検出し、該粒子の動きが停止するまでの時間を計測する第3ステップとを備える。
【0032】上記方法によれば、試薬および粒子が添加された検体を流路に沿って往復移動させることができる。この往復移動に伴なって粒子も移動する。しかし、検体と試薬との反応が進行し、試薬および粒子が添加された検体の粘度が高くなると、試薬および粒子が添加された検体を移動できなくなる。これにより、粒子の移動も停止する。この粒子の移動の停止までの時間を検出することによって、検体の反応を検出することができる。
【0033】微小な流路内で検体に試薬と粒子とを混合することにより、従来のスチールボールを用いる大型装置と同様の測定原理に基づいて粘稠度の変化を検出することができるが、スチールボールよりも小さい微小な粒子を用いることにより、従来の大型装置と同等、又はそれ以上の検出精度が得られる。
【0034】上記第2ステップにおいて、検体に往復動を行わせる力を付与するための具体的構成として種々な構成が採用できる。例えば、電気泳動を利用して検体、試薬を移動させる形態においては、電気的な力を付与する手段、例えば電極対、が採用できる。また、電気的な力ではなく、検体及び試薬を含む流体自体に往復動を生じさせるための所定の大きさの圧力を付与する手段、例えばマイクロポンプ、であってもよい。
【0035】
【発明の実施の形態】以下、本発明の一実施形態に係るマイクロチップについて、図面を参照しながら説明する。
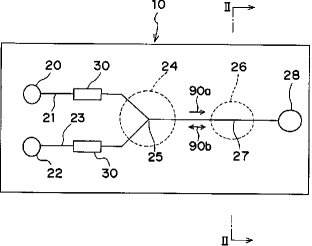
【0036】マイクロチップ10は、図1の模式的に図示した平面図および図2の断面図に示すように、大略、基板10b上に一点25で合流する微小な流路21,23,27が形成され、その上をカバー10aで覆われてなる。
【0037】例えば、マイクロチップ10の外形寸法は約20mm×40mm×0.5mmであり、流路21,23,27の幅は200μm、流路深さは約100μmである。マイクロチップ10の材料として用いることができるのは、PMMA(ポリメタクリル酸メチル)やPDMS(polydimethylsiloxane、ポリ・ジメチル・シロキサン)などの樹脂、感光性ガラスや耐熱ガラス、石英ガラスのなどのガラス材料にパリレンをコーティングした物、シリコンなどである。これらは、検体(血液)が付着しにくく、検体や試薬が流れることができる微小な流路を微細加工することが容易な材料である。例えば、基板10bには、エッチングにより微細加工が可能なシリコンを用いる。カバー10aには、透明な耐熱ガラスにパリレンをコーティングした物を用いる。
【0038】詳しくは、図1に示すように、流路21の端部には、液状の検体を供給するための検体供給口20が設けられている。流路23の端部には、液状の試薬を供給するための試薬供給口22が設けられている。流路27の端部には、空気抜きのための空気抜き穴28が設けられている。つまり、流路21は検体流路、流路23は試薬流路、流路27は合流流路である。
【0039】流路21,23には、マイクロポンプ30が組み込まれ、検体供給口22に供給された検体と試薬供給口22に供給された試薬とをそれぞれ送り出し、点線で示した合流部24で合流させ、混合するようになっている。合流した検体および試薬は、幅が狭い流路27内を層流状態で流れ、拡散により混合する。微小な流路27内における拡散による混合は非常に短時間で行われる。
【0040】マイクロポンプ30により送り出された検体と試薬とは、合流後、矢印90aで示すように、流路27を空気抜き穴28に向けて移動し、点線で示した検出部26において、検体と試薬との反応が検出される。
【0041】検体と試薬との反応を検出するため、マイクロチップ10は、不図示の検査装置に装填する。検査装置(本体)には、例えば図2に示すように、マイクロチップ10の検出部26の上部に、LEDなどの光源2と、フォトダイオードなどの光検出器4とが配置されるようになっている。光源2は、流路27に照射する光2aを発光する。光検出器4は、流路27内の粒子3による散乱光2bを受光する。光源2から流路27を経て光検出器4までの光路以外は、ノイズをなくすために遮光することが好ましい。
【0042】粒子3は、例えば血液凝固検査の場合、検体と試薬との混合液に添加された数μm程度のビーズである。このビーズには、シリカ(SiO2)などを用いることができる。ビーズは、試薬やバッファ液に予め混合しておいたり、流路21,23、27の適宜位置に予め配置したりすればよい。
【0043】図3は、マイクロポンプ30の断面図である。マイクロポンプ30はディフューザー型ポンプであり、振動板にPZTが貼り付けられていて、ユニモルフ駆動により送液を行うようになっている。
【0044】すなわち、カバー10aには、ポンプ室32に対向する部分に、セラミック圧電材料であるPZT[Pb(Zr,Ti)O3]38が固着されている。PZT38とカバー10aとの固着部分は、PZT38に電圧を印加することにより伸び、カバー10aのポンプ室32に対向する部分がポンプ室32側に湾曲し、ポンプ室32の体積が減少するようになっている。このとき、前後のデフューザー34,36の流路インピーダンスの差により、液体は、前後のデフューザー34,36のいずれか一方を通って、ポンプ室32から流出し、又はポンプ室32に流入する。
【0045】すなわち、前方のデフューザー36は、ポンプ室32の圧力変化が急激であっても緩やかであっても層流状態で液体が流れるので、流路インピーダンスの変化が相対的に小さい。これに対し、後方のデフューザー34は、流路インピーダンスの変化が相対的に大きい。すなわち、後方のデフューザー34は、ポンプ室32の圧力変化が急激な場合には、乱流が発生するために、流路インピーダンスが前方のデフューザー36よりも大きくなる。一方、ポンプ室32の圧力変化が緩やかな場合には、乱流が発生しないので、流路インピーダンスは前方のデフューザー36よりも小さくなる。
【0046】例えば、図4に示す進行波形70の駆動電圧をPZT38に印加し場合、70aに示した電圧の急激な変化により、ポンプ室32の体積が急激に小さくなる。このとき、図3において矢印70sで示すように、前方のデフューザー36から液体が吐出する。次に、図4R>4において70bで示した電圧の緩やかな変化により、ポンプ室32の体積はゆっくりと元に戻る。このとき、図3において70tで示すように、後方のデフューザー34からポンプ室32内に液体が吸い込まれる。この繰り返しにより、液体は前方に送り出される。
【0047】一方、図5に示す後退波形72の駆動電圧をPZT38に印加した場合、図5において72aで示した電圧の緩やかな変化により、ポンプ室32の体積は緩やかに小さくする。このとき、図3において矢印72sで示したように、後方のデフューザー34からポンプ室32の液体が吐出する。次に、図5において72bで示した急激な電圧変化により、ポンプ室32の体積は急激に元に戻る。このとき、図3において矢印72tで示すように、前方のデフューザー34から液体が吸い込まれる。この繰り返しにより、液体は後方に送り出される。
【0048】次に、マイクロチップ10を用いて、血液凝固の検査を行う手順について説明する。
【0049】まず、マイクロチップ10の検体供給口20に極微量の検体(血液)を供給し、試薬供給口22に極微量の試薬を供給する。
【0050】次に、マイクロチップ10のマイクロポンプ30のPZT38に、図13において符号Aで示したように、進行波形70の駆動電圧を繰り返し印加する。これにより、マイクロポンプ30は、検体および試薬を合流させ、流路27内を進行させる。これに伴なって、光検出器4で読み取る散乱光の強度Iは、図14において符号Kで示したように、ビーズの分布が一様になるまで、次第に増大する。
【0051】次に、図1において矢印90bで示すように、混合液を往復させ、光検出器4で散乱光の強度Iを読み取る。すなわち、図13において符号Bで示したように、例えば後退波形72の駆動電圧と進行波形70の駆動電圧とを所定回数(例えば100パルス)ずつ、交互にマイクロポンプ30に印加し、検出部26上の混合液を往復させる。これに伴なって、混合液中に適宜に添加されたビーズも動き、図14においてLで示すように、散乱光の強度Iが微妙に変化する。
【0052】時間が経つにつれ凝固が進み、混合液の粘凋度が高くなると、マイクロポンプ30の所定の出力によっては、混合液を動かすことができなくなる。そうなると、検体および試薬の混合液中のビーズも動かなくなり、図14に示すように、時間ts以降は、散乱光の強度Iが一定値となる。つまり、検体と試薬の反応をビーズからの散乱光の変化に基づいて検出することができる。光検出器4で、例えば散乱光の強度Iを0.1秒ごとに読み取り、凝固時間tsの計測を行う。
【0053】なお、血液の凝固の進行により、ビーズとは関係なく散乱光が増加するが、ビーズによる散乱光の変化は高周波成分となって現れるため、高周波成分だけを検出して変化を見ればよい。
【0054】以上説明したように、マイクロチップ10における微小流路内での反応のため、検体(血液)や試薬の量が極微量でよい。
【0055】また、液体の中にビーズ等を混ぜその動きを捉え血液凝固を測定するため、光学的な測定に比べ気泡等のノイズに強く、スチールボールによる測定よりも感度が良い。したがって、従来の大型装置と同等又はそれ以上の検出精度とすることが可能である。
【0056】また、光学的測定では血液を遠心分離等の作業で血漿に分離する必要があるが、全血で測定することができるので、POC(Point of Care)に適していて、家庭内での検査や救急車内などの緊急を要する場合にも使用することができる。
【0057】さらに、マイクロチップ10内にマイクロポンプ30を組み込んでいるため、デッドボリュームが少なく、検体や試薬を無駄にすることがない。マイクロポンプ30をマイクロチップ10に組み込むことで、検出装置(本体)側に送液装置やキュベットを回転させる装置を配置しなくてもよく、本体の小型化が図れ、開業医や一般家庭に置いても場所をとらない。
【0058】また、マイクロポンプ30は双方向(前後)に液を送ることができるので、検出部上で液を前後させることで検体・試薬の使用量を少なくすることができる。例えばコンマ数μリットル(例えば、0.2μリットル)の検体でも検出可能であり、数十μリットルの検体を必要とする従来のマイクロチップに比べも、検体の量を少なくすることができる。
【0059】なお、本発明は上記実施形態に限定されるものではなく、その他種々の態様で実施可能である。
【0060】例えば、図2のように光検出器4からの一つのデータの変化を検出する代わりに、図7に示したように、複数のデータが得られる撮像部4a(例えばCCDラインセンサやCCDエリアセンサなど)で流路27を撮像し、一定時間おきに撮り込んだ画像を比べると、血液が凝固すると画像に変化が見られなくなるので、凝固が検出できる。例えば、ビーズ入りの画像を画像処理部4bで二値化して差分をとるなど適宜に処理することにより、検体と試薬との反応に基づく流路27内のビーズ分布の変化を検出する。
【0061】また、図1ではマイクロポンプ30が検体流路21と試薬流路23の計2ケ所に配置されているが、図6のマイクロチップ12のように、合流流路27の1ヶ所にのみマイクロポンプ30を配置するようにしてもよい。
【0062】また、図1のマイクロチップは1つの検体と1つの試薬を用いるものであるが、1つの検体と2以上の試薬を用いるようにしてもよい。例えば図8に示した2試薬系のマイクロチップ14のように、検体を供給する一つの検体供給口40と、試薬を供給する2つの試薬供給口42,44を設け、検体および試薬をそれぞれマイクロポンプ30で送り出し、合流流路47で混合し、その混合液の変化を検出部46で検出する。なお、48は空気抜き穴である。
【0063】また、試薬のほかにバッファー液を用いるようにしてもよい。例えば図9に示したバッファ液を含む系のマイクロチップ16のように、検体を供給する検体供給口60と、試薬を供給する試薬供給口62と、バッファ液を供給するバッファ液供給口64とを設け、検体、試薬およびバッファ液をそれぞれマイクロポンプ30で送り出し、合流流路67で混合し、その混合液の変化を検出部66で検出する。なお、68は空気抜き穴である。
【0064】また、試薬は必ずしも液体である必要はなく、固体の試薬を流路の適宜位置に仮固定しておいてもよい。例えば図10に示したマイクロチップ18のように、検体供給口80と空気抜き穴84との間の流路81の適宜位置に、試薬固定部82、すなわち試薬添加部82を設け、試薬固定部82に、固体の試薬3を仮固定しておく。試薬固定部82に仮固定した試薬は、マイクロポンプ30で送り出された検体に触れると、例えば剥離したり溶解したりして、検体と混合するようにする。
【0065】また、図1のマイクロチップでは一組の検体および試薬からなる1つの検査系のみを含むが、互いに独立した、あるいは相互に関連した複数の検査系を一つのマイクロチップ内に配置してもよい。
【0066】また、ビーズなどの粒子を添加せずに、検体と試薬との反応を検出するようにしてもよい。例えば、検体と試薬との反応により生じる微小粒子の量を、散乱光の変化で検出するようにしてもよい。
【0067】また、散乱光2bを検出する代わりに、反射光や透過光を検出するようにしてもよい。あるいは、検体が試薬と反応するときの発光(例えば、蛍光)を検出するようにしてもよい。
【0068】また、マイクロポンプ30をなくし、マイクロチップ内の検体や試薬などを、マイクロチップの外部から移動させるようにしてもよい。例えば、検体供給口20と試薬供給口22とに、ステッピングモータで駆動するマイクロシリンダを接続し、検体と試薬を移動させるようにする。
【0069】また、本発明のマイクロチップは、血液凝固検査に限らず、種々の検査に用いることができる。
【図面の簡単な説明】
【図1】 本発明の第1実施形態のマイクロチップの平面図である。
【図2】 図1の線I−Iに沿って切断した断面図である。
【図3】 図1のマイクロチップの断面図である。
【図4】 電圧パルスの波形図である。
【図5】 電圧パルスの波形図である。
【図6】 変形例のマイクロチップの平面図である。
【図7】 他の変形例の断面図である。
【図8】 2試薬系のマイクロチップの平面図である。
【図9】 バッファ液を含む系のマイクロチップの平面図である。
【図10】 試薬を固定したマイクロチップの平面図である。
【図11】 従来例の検査の説明図である。
【図12】 他の従来例の検査の説明図である。
【図13】 駆動電圧のグラフである。
【図14】 散乱光の強度のグラフである。
【符号の説明】
3 粒子
4 光検出器(検出手段)
10,12,14,16 マイクロチップ
21 流路(検体流路)
23 流路(試薬流路)
26 検出部
27 流路(合流流路)
30 マイクロポンプ(付与手段)
82 試薬固定部(試薬添加部)
【0001】
【発明の属する技術分野】本発明は、マイクロチップに関し、詳しくは、検体と試薬との反応を検出するためのマイクロチップに関し、例えば血液凝固検査、免疫学的検査、生化学的検査、遺伝子検査等に好適に使用することができるマイクロチップに関する。
【0002】
【従来の技術】従来、例えば血液の凝固反応を測定する装置として、光散乱検出方式の装置や磁力センサー検出方式の装置が知られている。
【0003】光散乱検出方式の装置では、例えば図11に示すように、検体と試薬とを混合したキュベット7に光源5から光5aを照射し、検体と試薬との混合液からの散乱光5bを検出器6で検出する。検体と試薬との反応と、検出した散乱光5bの強度とは一定の相関関係があるので、検体の検査を行うことができる。この装置は、静止した混合液の変化を検出するものであり、検体と試薬の混合時に発生する泡によるノイズや血液の濁りなどの変化に弱い。
【0004】磁力センサー検出方式の装置では、例えば図12に示すように、検体と試薬との混合液とスチールボール8とが入ったキュベット7’を、垂直から少し傾いた軸を中心に回転し、スチールボール8の動きを磁力センサー8で検出する。例えば血液の凝固により混合液の粘稠度が変化すると、底に沈んでいたスチールボール8が動き出すことを利用して、混合液の粘稠度の変化を検出する。この装置では、キュベット7’を回転する必要があり、微小な粘稠度の変化まで検出することができない。
【0005】このような従来の装置(大型装置)は、ある程度の量の血液を採取する必要がある。また、据え置き型の装置であり、持ち運ぶことができないので、POC(Point Of Care、その場治療)に対応することができない。また、検査時間の短縮や検査精度の向上に限界がある。また、廃棄物の量も多い。
【0006】ところで、最近、マイクロマシン技術を応用して、化学分析や合成などの機器・手法を微細化して行うμ―TAS(μ−Total Analysis System)が注目されている。従来の装置に比べ微細化されたμ−TASでは、試料の量が少ない、反応時間が短い、廃棄物が少ないなどのメリットがある。また、医療分野に使用した場合、検体(血液)の量を少なくすることで患者への負担を軽減し、試薬の量を少なくすることで検査のコストを下げることが期待できる。
【0007】例えば、Roche Diagnostics社は、血液が毛細管現象により試薬チャンバー内を流れながら試薬と混合するマイクロチップを用い、血液の流動停止を散乱光の変化として捉え、流動停止までの時間を計測する装置を提供している。
【0008】
【発明が解決しようとする課題】この装置は、検体量は数十μリット程度とかなり少ないものの、試薬がドライ(マイクロチップに固定化されたもの)であるため、マイクロチップは高価である。また、測定精度は、従来の大型装置ほどは良くない。
【0009】したがって、本発明が解決しようとする技術的課題は、従来の大型装置と同等またはそれ以上の精度で、検体と試薬を混合して検査を行うことが可能なマイクロチップを提供することである。
【0010】
【課題を解決するための手段および作用・効果】本発明は、上記技術的課題を解決するために、以下の構成のマイクロチップを提供する。
【0011】マイクロチップは、微小な流路である検体流路、試薬流路、および合流流路と、検出部とを備える。上記検体流路は、その一端に向けて検体を流すことができる。上記試薬流路は、上記検体流路の上記一端に接続され、上記検体と反応する少なくとも一つの試薬を流すことができる。上記合流流路は、上記検体流路の上記一端から延在し、合流した上記検体と上記試薬とを流すことができる。上記検出部は、上記合流流路の近傍に配置され、上記検体と上記試薬との反応を検出できるようにする。更に、マイクロチップは、付与手段を備え、付与手段は上記検出部において上記検体と上記試薬とを往復動させる力を付与する。
【0012】上記構成において、「試薬」は、それ自体が直ちに検体と反応することができるもののみならず、2以上が混合して初めて検体と反応することができるようになるものをも含む。「検出部」は、例えば合流流路近傍の歪みや温度、電位等を検出することにより、検体と試薬との反応をそれ自体が直接検出するもの(例えば、圧電素子、熱電対、導電性を有する部分など)であっても、あるいは、それ自体は何ら検出するものではないが、マイクロチップの外部から検体と試薬との反応を検出することができるようにするもの(例えば、透明な部分)であってもよい。
【0013】上記構成によれば、検体と試薬を検体流路の一端に向けて流して合流させ、合流流路内を移動させる。合流した検体と試薬は、微小な合流流路内で極めて短時間で混合する。そして、混合した検体と試薬とが反応し、その反応を検出部で検出することができる。具体的には、混合した検体と試薬とは検出部において往復動しながら反応する。そして、この往復動の様子を観測乃至検出することで反応の様子を検出することができる。さらには、検体と試薬とともに含まれる微小な粒子の動きを検出するなどして、より高度な検査を行うことが可能になる。
【0014】上記構成によれば、検体と試料が極微量であっても反応は起こるので、従来の大型装置と同様の測定原理に基づいて検査を行うことができる。また、検体が極微量であれば、検体の濁りなどの影響も少なくなる。また、微小な反応を捉えるために検出感度(分解能)を上げ、検査精度を高めることも可能である。
【0015】したがって、従来の大型装置と同等、又はそれ以上の精度で検査を行うことができる。
【0016】なお、複数の試薬を用いる場合には、例えば試薬流路を枝分かれした構成として複数の試薬を流すようにしても、あるいは、検体流路の一端以外で検体流路に合流する微小な流路を設け、そこからも試薬を流すようにしてもよい。また、検体流路、試薬流路、又は合流流路の適宜位置で合流する微小な流路から、洗浄液や、検体や試薬と混合しても反応しないバッファ液などを流すようにしてもよい。
【0017】また、検体と試薬とは往復動をしながら反応するため、反応に要する経路長を短くすることができる。したがって、マイクロチップ自体の小型化、ひいては検出装置の小型化を実現できる。
【0018】また、本発明は、以下の構成のマイクロチップを提供する。
【0019】マイクロチップは、検体を流すことができる微小な流路である混合流路を備える。該混合流路は、上記検体に添加されて反応する試薬を保持する試薬添加部と、上記検体と上記試薬との反応を検出することができる検出部とを有する。更に、このマイクロチップは、上記検出部において上記検体と上記試薬とを往復動させるための力を付与する付与手段を備える。
【0020】上記構成において、試薬添加部は、検体に添加するまで試薬を仮固定し、検体と出会うことによって試薬が剥離したり溶解するようにしても、あるいは、単に試薬を収納しただけで移動自在な状態であってもよい。
【0021】上記構成によれば、混合流路に検体を流し、検体が試薬添加部に達すると、試薬は検体に添加され、検体とともに移動し、検体と混合しながら反応する。そして、検体と試薬との反応を、検出部を介して検出することができる。具体的には、混合した検体と試薬とは検出部において往復動しながら反応する。そして、この往復動の様子を観測乃至検出することで反応の様子を検出することができる。さらには、検体と試薬とともに含まれる微小な粒子の動きを検出するなどして、より高度な検査を行うことが可能になる。
【0022】上記構成によれば、検体と試料が極微量であっても反応は起こるので、従来の大型装置と同様の測定原理に基づいて検査を行うことができる。また、検体が極微量であれば、検体の濁りなどの影響も少なくなる。また、微小な反応を捉えるために検出感度(分解能)を上げ、検査精度を高めることも可能である。
【0023】したがって、従来の大型装置と同等、又はそれ以上の精度で検査を行うことができる。
【0024】上記の何れのマイクロチップにおいても、付与手段として種々な構成が採用できる。例えば、電気泳動を利用して検体、試薬を移動させる形態においては、電気的な力を付与する手段、例えば電極対、が採用できる。また、電気的な力ではなく、検体及び試薬を含む流体自体に往復動を生じさせる圧力を付与する手段、例えばマイクロポンプ、であってもよい。この場合、好ましくは、上記検体流路、上記試薬流路、上記合流流路および上記混合流路の少なくとも一つにマイクロポンプ、好ましくは双方向に吸込・吐出が可能なマイクロポンプ、を備える。
【0025】好ましくは、上記検出部は、マイクロチップの外部と上記合流流路又は上記混合流路とに隣接しかつ連続的に延在しかつ導光性を有する。
【0026】上記構成によれば、合流流路又は混合流路内から、検出部を通ってマイクロチップの外部に、光が出射するようにすることができる。これにより、例えば、検体と試薬との反応による発光を、マイクロチップの外部から検出することができる。また、合流流路又は混合流路内の検体と試薬とに光を当て、その散乱光、反射光、透過光、あるいは影像を捉え、それによって検体と試薬との反応の検出を行うことができる。
【0027】また、本発明は、以下のマイクロチップを提供する。
【0028】即ち、マイクロチップは、検体を含む液体を流すことができる微小な流路と、その一端側に第1ディフューザーを有すると共にその他端側に第2ディフューザーを有したポンプ室を備え前記第1ディフューザーが前記流路に接続されたマイクロポンプと、を備え、前記ポンプ室の圧力変化に対する、前記第1ディフューザーの流路インピーダンスの変化特性と前記第2ディフューザーの流路インピーダンスの変化特性とが互いに異なる。
【0029】上記構成によれば、第1ディフューザーと第2ディフューザーとが互いにその流路インピーダンスの、ポンプ室の圧力変化に対する変化特性が異なるため、ポンプ室の圧力変化を適宜調整するといった簡略な制御により、上記流路に液体を吐出することも上記流路から液体を吸入することもできる。したがって、流路内の液体を当該流路に沿って往復動させることができ、検体と試薬との反応に要する経路長を長く取らなくてもよく、マイクロチップ自体の小型化、ひいては検出装置の小型化を実現できる。
【0030】また、本発明は、以下の反応検出方法を提供する。
【0031】反応検出方法は、微小な流路を有するマイクロチップを用いて、検体と試薬の反応を検出するタイプの方法である。反応検出方法は、上記マイクロチップの上記流路内において、上記検体に、上記試薬と微小な粒子とを添加する第1ステップと、上記試薬および上記粒子が添加された上記検体に、上記流路に沿っ繰り返し往復動を行わせる力を与える第2ステップと、上記流路内における上記粒子の動きを検出し、該粒子の動きが停止するまでの時間を計測する第3ステップとを備える。
【0032】上記方法によれば、試薬および粒子が添加された検体を流路に沿って往復移動させることができる。この往復移動に伴なって粒子も移動する。しかし、検体と試薬との反応が進行し、試薬および粒子が添加された検体の粘度が高くなると、試薬および粒子が添加された検体を移動できなくなる。これにより、粒子の移動も停止する。この粒子の移動の停止までの時間を検出することによって、検体の反応を検出することができる。
【0033】微小な流路内で検体に試薬と粒子とを混合することにより、従来のスチールボールを用いる大型装置と同様の測定原理に基づいて粘稠度の変化を検出することができるが、スチールボールよりも小さい微小な粒子を用いることにより、従来の大型装置と同等、又はそれ以上の検出精度が得られる。
【0034】上記第2ステップにおいて、検体に往復動を行わせる力を付与するための具体的構成として種々な構成が採用できる。例えば、電気泳動を利用して検体、試薬を移動させる形態においては、電気的な力を付与する手段、例えば電極対、が採用できる。また、電気的な力ではなく、検体及び試薬を含む流体自体に往復動を生じさせるための所定の大きさの圧力を付与する手段、例えばマイクロポンプ、であってもよい。
【0035】
【発明の実施の形態】以下、本発明の一実施形態に係るマイクロチップについて、図面を参照しながら説明する。
【0036】マイクロチップ10は、図1の模式的に図示した平面図および図2の断面図に示すように、大略、基板10b上に一点25で合流する微小な流路21,23,27が形成され、その上をカバー10aで覆われてなる。
【0037】例えば、マイクロチップ10の外形寸法は約20mm×40mm×0.5mmであり、流路21,23,27の幅は200μm、流路深さは約100μmである。マイクロチップ10の材料として用いることができるのは、PMMA(ポリメタクリル酸メチル)やPDMS(polydimethylsiloxane、ポリ・ジメチル・シロキサン)などの樹脂、感光性ガラスや耐熱ガラス、石英ガラスのなどのガラス材料にパリレンをコーティングした物、シリコンなどである。これらは、検体(血液)が付着しにくく、検体や試薬が流れることができる微小な流路を微細加工することが容易な材料である。例えば、基板10bには、エッチングにより微細加工が可能なシリコンを用いる。カバー10aには、透明な耐熱ガラスにパリレンをコーティングした物を用いる。
【0038】詳しくは、図1に示すように、流路21の端部には、液状の検体を供給するための検体供給口20が設けられている。流路23の端部には、液状の試薬を供給するための試薬供給口22が設けられている。流路27の端部には、空気抜きのための空気抜き穴28が設けられている。つまり、流路21は検体流路、流路23は試薬流路、流路27は合流流路である。
【0039】流路21,23には、マイクロポンプ30が組み込まれ、検体供給口22に供給された検体と試薬供給口22に供給された試薬とをそれぞれ送り出し、点線で示した合流部24で合流させ、混合するようになっている。合流した検体および試薬は、幅が狭い流路27内を層流状態で流れ、拡散により混合する。微小な流路27内における拡散による混合は非常に短時間で行われる。
【0040】マイクロポンプ30により送り出された検体と試薬とは、合流後、矢印90aで示すように、流路27を空気抜き穴28に向けて移動し、点線で示した検出部26において、検体と試薬との反応が検出される。
【0041】検体と試薬との反応を検出するため、マイクロチップ10は、不図示の検査装置に装填する。検査装置(本体)には、例えば図2に示すように、マイクロチップ10の検出部26の上部に、LEDなどの光源2と、フォトダイオードなどの光検出器4とが配置されるようになっている。光源2は、流路27に照射する光2aを発光する。光検出器4は、流路27内の粒子3による散乱光2bを受光する。光源2から流路27を経て光検出器4までの光路以外は、ノイズをなくすために遮光することが好ましい。
【0042】粒子3は、例えば血液凝固検査の場合、検体と試薬との混合液に添加された数μm程度のビーズである。このビーズには、シリカ(SiO2)などを用いることができる。ビーズは、試薬やバッファ液に予め混合しておいたり、流路21,23、27の適宜位置に予め配置したりすればよい。
【0043】図3は、マイクロポンプ30の断面図である。マイクロポンプ30はディフューザー型ポンプであり、振動板にPZTが貼り付けられていて、ユニモルフ駆動により送液を行うようになっている。
【0044】すなわち、カバー10aには、ポンプ室32に対向する部分に、セラミック圧電材料であるPZT[Pb(Zr,Ti)O3]38が固着されている。PZT38とカバー10aとの固着部分は、PZT38に電圧を印加することにより伸び、カバー10aのポンプ室32に対向する部分がポンプ室32側に湾曲し、ポンプ室32の体積が減少するようになっている。このとき、前後のデフューザー34,36の流路インピーダンスの差により、液体は、前後のデフューザー34,36のいずれか一方を通って、ポンプ室32から流出し、又はポンプ室32に流入する。
【0045】すなわち、前方のデフューザー36は、ポンプ室32の圧力変化が急激であっても緩やかであっても層流状態で液体が流れるので、流路インピーダンスの変化が相対的に小さい。これに対し、後方のデフューザー34は、流路インピーダンスの変化が相対的に大きい。すなわち、後方のデフューザー34は、ポンプ室32の圧力変化が急激な場合には、乱流が発生するために、流路インピーダンスが前方のデフューザー36よりも大きくなる。一方、ポンプ室32の圧力変化が緩やかな場合には、乱流が発生しないので、流路インピーダンスは前方のデフューザー36よりも小さくなる。
【0046】例えば、図4に示す進行波形70の駆動電圧をPZT38に印加し場合、70aに示した電圧の急激な変化により、ポンプ室32の体積が急激に小さくなる。このとき、図3において矢印70sで示すように、前方のデフューザー36から液体が吐出する。次に、図4R>4において70bで示した電圧の緩やかな変化により、ポンプ室32の体積はゆっくりと元に戻る。このとき、図3において70tで示すように、後方のデフューザー34からポンプ室32内に液体が吸い込まれる。この繰り返しにより、液体は前方に送り出される。
【0047】一方、図5に示す後退波形72の駆動電圧をPZT38に印加した場合、図5において72aで示した電圧の緩やかな変化により、ポンプ室32の体積は緩やかに小さくする。このとき、図3において矢印72sで示したように、後方のデフューザー34からポンプ室32の液体が吐出する。次に、図5において72bで示した急激な電圧変化により、ポンプ室32の体積は急激に元に戻る。このとき、図3において矢印72tで示すように、前方のデフューザー34から液体が吸い込まれる。この繰り返しにより、液体は後方に送り出される。
【0048】次に、マイクロチップ10を用いて、血液凝固の検査を行う手順について説明する。
【0049】まず、マイクロチップ10の検体供給口20に極微量の検体(血液)を供給し、試薬供給口22に極微量の試薬を供給する。
【0050】次に、マイクロチップ10のマイクロポンプ30のPZT38に、図13において符号Aで示したように、進行波形70の駆動電圧を繰り返し印加する。これにより、マイクロポンプ30は、検体および試薬を合流させ、流路27内を進行させる。これに伴なって、光検出器4で読み取る散乱光の強度Iは、図14において符号Kで示したように、ビーズの分布が一様になるまで、次第に増大する。
【0051】次に、図1において矢印90bで示すように、混合液を往復させ、光検出器4で散乱光の強度Iを読み取る。すなわち、図13において符号Bで示したように、例えば後退波形72の駆動電圧と進行波形70の駆動電圧とを所定回数(例えば100パルス)ずつ、交互にマイクロポンプ30に印加し、検出部26上の混合液を往復させる。これに伴なって、混合液中に適宜に添加されたビーズも動き、図14においてLで示すように、散乱光の強度Iが微妙に変化する。
【0052】時間が経つにつれ凝固が進み、混合液の粘凋度が高くなると、マイクロポンプ30の所定の出力によっては、混合液を動かすことができなくなる。そうなると、検体および試薬の混合液中のビーズも動かなくなり、図14に示すように、時間ts以降は、散乱光の強度Iが一定値となる。つまり、検体と試薬の反応をビーズからの散乱光の変化に基づいて検出することができる。光検出器4で、例えば散乱光の強度Iを0.1秒ごとに読み取り、凝固時間tsの計測を行う。
【0053】なお、血液の凝固の進行により、ビーズとは関係なく散乱光が増加するが、ビーズによる散乱光の変化は高周波成分となって現れるため、高周波成分だけを検出して変化を見ればよい。
【0054】以上説明したように、マイクロチップ10における微小流路内での反応のため、検体(血液)や試薬の量が極微量でよい。
【0055】また、液体の中にビーズ等を混ぜその動きを捉え血液凝固を測定するため、光学的な測定に比べ気泡等のノイズに強く、スチールボールによる測定よりも感度が良い。したがって、従来の大型装置と同等又はそれ以上の検出精度とすることが可能である。
【0056】また、光学的測定では血液を遠心分離等の作業で血漿に分離する必要があるが、全血で測定することができるので、POC(Point of Care)に適していて、家庭内での検査や救急車内などの緊急を要する場合にも使用することができる。
【0057】さらに、マイクロチップ10内にマイクロポンプ30を組み込んでいるため、デッドボリュームが少なく、検体や試薬を無駄にすることがない。マイクロポンプ30をマイクロチップ10に組み込むことで、検出装置(本体)側に送液装置やキュベットを回転させる装置を配置しなくてもよく、本体の小型化が図れ、開業医や一般家庭に置いても場所をとらない。
【0058】また、マイクロポンプ30は双方向(前後)に液を送ることができるので、検出部上で液を前後させることで検体・試薬の使用量を少なくすることができる。例えばコンマ数μリットル(例えば、0.2μリットル)の検体でも検出可能であり、数十μリットルの検体を必要とする従来のマイクロチップに比べも、検体の量を少なくすることができる。
【0059】なお、本発明は上記実施形態に限定されるものではなく、その他種々の態様で実施可能である。
【0060】例えば、図2のように光検出器4からの一つのデータの変化を検出する代わりに、図7に示したように、複数のデータが得られる撮像部4a(例えばCCDラインセンサやCCDエリアセンサなど)で流路27を撮像し、一定時間おきに撮り込んだ画像を比べると、血液が凝固すると画像に変化が見られなくなるので、凝固が検出できる。例えば、ビーズ入りの画像を画像処理部4bで二値化して差分をとるなど適宜に処理することにより、検体と試薬との反応に基づく流路27内のビーズ分布の変化を検出する。
【0061】また、図1ではマイクロポンプ30が検体流路21と試薬流路23の計2ケ所に配置されているが、図6のマイクロチップ12のように、合流流路27の1ヶ所にのみマイクロポンプ30を配置するようにしてもよい。
【0062】また、図1のマイクロチップは1つの検体と1つの試薬を用いるものであるが、1つの検体と2以上の試薬を用いるようにしてもよい。例えば図8に示した2試薬系のマイクロチップ14のように、検体を供給する一つの検体供給口40と、試薬を供給する2つの試薬供給口42,44を設け、検体および試薬をそれぞれマイクロポンプ30で送り出し、合流流路47で混合し、その混合液の変化を検出部46で検出する。なお、48は空気抜き穴である。
【0063】また、試薬のほかにバッファー液を用いるようにしてもよい。例えば図9に示したバッファ液を含む系のマイクロチップ16のように、検体を供給する検体供給口60と、試薬を供給する試薬供給口62と、バッファ液を供給するバッファ液供給口64とを設け、検体、試薬およびバッファ液をそれぞれマイクロポンプ30で送り出し、合流流路67で混合し、その混合液の変化を検出部66で検出する。なお、68は空気抜き穴である。
【0064】また、試薬は必ずしも液体である必要はなく、固体の試薬を流路の適宜位置に仮固定しておいてもよい。例えば図10に示したマイクロチップ18のように、検体供給口80と空気抜き穴84との間の流路81の適宜位置に、試薬固定部82、すなわち試薬添加部82を設け、試薬固定部82に、固体の試薬3を仮固定しておく。試薬固定部82に仮固定した試薬は、マイクロポンプ30で送り出された検体に触れると、例えば剥離したり溶解したりして、検体と混合するようにする。
【0065】また、図1のマイクロチップでは一組の検体および試薬からなる1つの検査系のみを含むが、互いに独立した、あるいは相互に関連した複数の検査系を一つのマイクロチップ内に配置してもよい。
【0066】また、ビーズなどの粒子を添加せずに、検体と試薬との反応を検出するようにしてもよい。例えば、検体と試薬との反応により生じる微小粒子の量を、散乱光の変化で検出するようにしてもよい。
【0067】また、散乱光2bを検出する代わりに、反射光や透過光を検出するようにしてもよい。あるいは、検体が試薬と反応するときの発光(例えば、蛍光)を検出するようにしてもよい。
【0068】また、マイクロポンプ30をなくし、マイクロチップ内の検体や試薬などを、マイクロチップの外部から移動させるようにしてもよい。例えば、検体供給口20と試薬供給口22とに、ステッピングモータで駆動するマイクロシリンダを接続し、検体と試薬を移動させるようにする。
【0069】また、本発明のマイクロチップは、血液凝固検査に限らず、種々の検査に用いることができる。
【図面の簡単な説明】
【図1】 本発明の第1実施形態のマイクロチップの平面図である。
【図2】 図1の線I−Iに沿って切断した断面図である。
【図3】 図1のマイクロチップの断面図である。
【図4】 電圧パルスの波形図である。
【図5】 電圧パルスの波形図である。
【図6】 変形例のマイクロチップの平面図である。
【図7】 他の変形例の断面図である。
【図8】 2試薬系のマイクロチップの平面図である。
【図9】 バッファ液を含む系のマイクロチップの平面図である。
【図10】 試薬を固定したマイクロチップの平面図である。
【図11】 従来例の検査の説明図である。
【図12】 他の従来例の検査の説明図である。
【図13】 駆動電圧のグラフである。
【図14】 散乱光の強度のグラフである。
【符号の説明】
3 粒子
4 光検出器(検出手段)
10,12,14,16 マイクロチップ
21 流路(検体流路)
23 流路(試薬流路)
26 検出部
27 流路(合流流路)
30 マイクロポンプ(付与手段)
82 試薬固定部(試薬添加部)
【特許請求の範囲】
【請求項1】 その一端に向けて検体を流すことができる微小な流路である検体流路と、該検体流路の上記一端に接続され、上記検体と反応する少なくとも一つの試薬を流すことができる微小な流路である試薬流路と、上記検体流路の上記一端から延在し、合流した上記検体と上記試薬とを流すことができる微小な流路である合流流路と、該合流流路の近傍に配置され、上記検体と上記試薬との反応を検出できるようにする検出部と、前記検出部において上記検体と上記試薬とを往復動させる力を付与する付与手段と、を備えたことを特徴とする、マイクロチップ。
【請求項2】 検体を流すことができる微小な流路である混合流路であって、上記検体に添加されて反応する試薬を保持する試薬添加部と、上記検体と上記試薬との反応を検出することができる検出部とを有する混合流路と、上記検出部において上記検体と上記試薬とを往復動させるための力を付与する付与手段と、を備えたことを特徴とする、マイクロチップ。
【請求項3】 上記付与手段は少なくとも一つのマイクロポンプを含むことを特徴とする、請求項1又は2記載のマイクロチップ。
【請求項4】 上記マイクロポンプは、双方向に吸込・吐出が可能であることを特徴とする、請求項3記載のマイクロポンプ。
【請求項5】 上記検出部は、マイクロチップの外部と上記合流流路又は上記混合流路とに隣接しかつ連続的に延在しかつ導光性を有することを特徴とする、請求項1乃至4のいずれか一つに記載のマイクロチップ。
【請求項6】 検体を含む液体を流すことができる微小な流路と、その一端側に第1ディフューザーを有すると共にその他端側に第2ディフューザーを有したポンプ室を備え前記第1ディフューザーが前記流路に接続されたマイクロポンプと、を備え、前記ポンプ室の圧力変化に対する、前記第1ディフューザーの流路インピーダンスの変化特性と前記第2ディフューザーの流路インピーダンスの変化特性とが互いに異なることを特徴とする、マイクロチップ。
【請求項7】 微小な流路を有するマイクロチップを用いて、検体と試薬の反応を検出する反応検出方法であって、上記マイクロチップの上記流路内において、上記検体に、上記試薬と微小な粒子とを添加する第1ステップと、上記試薬および上記粒子が添加された上記検体に、上記流路に沿って繰り返し往復動を行わせる力を与える第2ステップと、上記流路内における上記粒子の動きを検出し、該粒子の動きが停止するまでの時間を計測する第3ステップと、を備えることを特徴とする、反応検出方法。
【請求項8】 前記第2ステップにおいて、上記検体に、所定の大きさの圧力を上記流路に沿って向きを変えながら繰り返し与えることを特徴とする、請求項7記載の反応検出方法。
【請求項1】 その一端に向けて検体を流すことができる微小な流路である検体流路と、該検体流路の上記一端に接続され、上記検体と反応する少なくとも一つの試薬を流すことができる微小な流路である試薬流路と、上記検体流路の上記一端から延在し、合流した上記検体と上記試薬とを流すことができる微小な流路である合流流路と、該合流流路の近傍に配置され、上記検体と上記試薬との反応を検出できるようにする検出部と、前記検出部において上記検体と上記試薬とを往復動させる力を付与する付与手段と、を備えたことを特徴とする、マイクロチップ。
【請求項2】 検体を流すことができる微小な流路である混合流路であって、上記検体に添加されて反応する試薬を保持する試薬添加部と、上記検体と上記試薬との反応を検出することができる検出部とを有する混合流路と、上記検出部において上記検体と上記試薬とを往復動させるための力を付与する付与手段と、を備えたことを特徴とする、マイクロチップ。
【請求項3】 上記付与手段は少なくとも一つのマイクロポンプを含むことを特徴とする、請求項1又は2記載のマイクロチップ。
【請求項4】 上記マイクロポンプは、双方向に吸込・吐出が可能であることを特徴とする、請求項3記載のマイクロポンプ。
【請求項5】 上記検出部は、マイクロチップの外部と上記合流流路又は上記混合流路とに隣接しかつ連続的に延在しかつ導光性を有することを特徴とする、請求項1乃至4のいずれか一つに記載のマイクロチップ。
【請求項6】 検体を含む液体を流すことができる微小な流路と、その一端側に第1ディフューザーを有すると共にその他端側に第2ディフューザーを有したポンプ室を備え前記第1ディフューザーが前記流路に接続されたマイクロポンプと、を備え、前記ポンプ室の圧力変化に対する、前記第1ディフューザーの流路インピーダンスの変化特性と前記第2ディフューザーの流路インピーダンスの変化特性とが互いに異なることを特徴とする、マイクロチップ。
【請求項7】 微小な流路を有するマイクロチップを用いて、検体と試薬の反応を検出する反応検出方法であって、上記マイクロチップの上記流路内において、上記検体に、上記試薬と微小な粒子とを添加する第1ステップと、上記試薬および上記粒子が添加された上記検体に、上記流路に沿って繰り返し往復動を行わせる力を与える第2ステップと、上記流路内における上記粒子の動きを検出し、該粒子の動きが停止するまでの時間を計測する第3ステップと、を備えることを特徴とする、反応検出方法。
【請求項8】 前記第2ステップにおいて、上記検体に、所定の大きさの圧力を上記流路に沿って向きを変えながら繰り返し与えることを特徴とする、請求項7記載の反応検出方法。
【図1】


【図2】


【図4】


【図5】


【図6】


【図12】


【図3】


【図7】


【図8】


【図9】


【図10】


【図11】


【図13】


【図14】




【図2】


【図4】


【図5】


【図6】


【図12】


【図3】


【図7】


【図8】


【図9】


【図10】


【図11】


【図13】


【図14】


【公開番号】特開2002−214241(P2002−214241A)
【公開日】平成14年7月31日(2002.7.31)
【国際特許分類】
【出願番号】特願2001−305237(P2001−305237)
【出願日】平成13年10月1日(2001.10.1)
【出願人】(000006079)ミノルタ株式会社 (155)
【Fターム(参考)】
【公開日】平成14年7月31日(2002.7.31)
【国際特許分類】
【出願日】平成13年10月1日(2001.10.1)
【出願人】(000006079)ミノルタ株式会社 (155)
【Fターム(参考)】
[ Back to top ]

