マイクロデバイス
【課題】点着部の先端を半球状に構成することで、試料液を点着部のみに付着させることができるマイクロデバイスを提供することを目的とする。
【解決手段】流路となる溝が掘られたベースプレート12にカバープレート11を重ね合わせて内部に毛細管キャビティ5を形成するとともに、基端が毛細管キャビティ5に接続され先端がカバープレート11から突出した点着部2を設け、点着部2の先端が、ベースプレート12の流路形成面から離れる方向に突出した半球状に形成されていることを特徴とする。
【解決手段】流路となる溝が掘られたベースプレート12にカバープレート11を重ね合わせて内部に毛細管キャビティ5を形成するとともに、基端が毛細管キャビティ5に接続され先端がカバープレート11から突出した点着部2を設け、点着部2の先端が、ベースプレート12の流路形成面から離れる方向に突出した半球状に形成されていることを特徴とする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、生物学的流体を電気化学的、もしくは光学的に分析するマイクロデバイスに関するものである。
【背景技術】
【0002】
従来、マイクロ流路を形成したマイクロデバイスを用いて生物学的流体を電気化学的にあるいは光学的に分析する方法がある。電気化学的に分析する方法としては、試料液中の特定の成分を分析するバイオセンサーとして、例えば、血液中のグルコースとセンサー中に担持したグルコースオキシダーゼ等の試薬との反応により得られる電流値を測定することにより、血糖値などを求めるものがある。
【0003】
また、マイクロデバイスを用いて分析する方法では、水平軸を有する回転装置を使って流体の制御をすることが可能であり、遠心力を利用して試料液の計量、細胞質材料の分離、分離された流体の移送分配、液体の混合/攪拌等を行うことができるため、種々の生物化学的な分析を行うことが可能である。
【0004】
マイクロデバイスに試料を導入するための従来の試料液採取方法としては、図7に示す電気化学式バイオセンサーがある。
これは絶縁基板205とカバー206を間にスペーサー207と試薬層210を挟んで貼り合わせたもので、試料液は、カバー206の吸引口208から毛細管現象によりキャビティ212内に導入される。絶縁基板205の上の作用極201、対極202と試薬層210のある位置まで導かれる。209は空気逃げ孔である。
【0005】
この時、キャビティ212の容積で試料の定量採取を行っている。そして作用極201、対極202での試料液と試薬との反応により生じる電流値は、リード203,204を通じて図示しない外部の測定装置に接続して読み取られる(例えば特許文献1参照)。
【0006】
また、図8に示す遠心移送式バイオセンサーでは、試料液は入り口313から毛細管現象により第1の毛細管キャビティ312内に定量採取され、次に遠心力を作用させることで、毛細管キャビティ312内の試料液は濾過材料315と第1の流路314と第2のキャビティ316および芯318を介して受入キャビティ317に移送され、受入キャビティ317で試薬と反応したものを遠心分離させ、第2のキャビティ316に溶液成分のみを毛細管力によって採取し、反応状態が光学的に読み取られる(例えば特許文献2参照)。
【0007】
また、図9に示す遠心移送式バイオセンサー400では、試料を入口ポート409から蛇行した連続微小導管401の中を出口ポート410まで毛細管力で移送し、各毛細管キャビティ404a〜404fを試料液で満たした後、バイオセンサーの回転によって発生する遠心力によって、それぞれの毛細管キャビティ内の試料液を各通気孔406a〜406gの位置で分配し、各連結微小導管407a〜407fを通って、次の処理室(図示省略)へ移送される(例えば特許文献3参照)。408a〜408fはバルブ機能部である。
【特許文献1】特開2001−159618号公報
【特許文献2】特表平4−504758号公報
【特許文献3】特表2004−529333号公報
【発明の開示】
【発明が解決しようとする課題】
【0008】
しかしながら、このような従来の構成では、点着部の先端が矩形状であるため、点着した際に試料液が点着部以外のマイクロデバイスの外壁面に付着してしまうという課題を有している。
【0009】
本発明は前記従来の課題を解決するもので、試料液を点着部のみに付着させることができるマイクロデバイスを提供することを目的とする。
【課題を解決するための手段】
【0010】
本発明の請求項1記載のマイクロデバイスは、流路となる溝が掘られたベースプレートにカバープレートを重ね合わせて内部に毛細管キャビティを形成するとともに、基端が前記毛細管キャビティに接続され先端がカバープレートから突出した点着部を設け、前記点着部の先端が、前記ベースプレートの流路形成面から離れる方向に突出した半球状に形成されていることを特徴とする。
【0011】
本発明の請求項2記載のマイクロデバイスは、請求項1において、前記毛細管キャビティの壁面は親水処理が施されていることを特徴とする。
本発明の請求項3記載のマイクロデバイスは、請求項1において、前記点着部より低く、隙間を空けて前記点着部を囲むリブを設けたことを特徴とする。
【0012】
本発明の請求項4記載のマイクロデバイスは、前記点着部の直径が、測定対象の試料液の液滴と同じかそれよりも僅かに大きいことを特徴とする。
【発明の効果】
【0013】
この構成によれば、点着部の先端を半球状に構成することで、試料液を点着部のみに付着させることができる。
【発明を実施するための最良の形態】
【0014】
以下、本発明の実施の形態のマイクロデバイスを図1〜図6に基づいて説明する。
図1はマイクロデバイス100の構成について示す。図2はマイクロデバイス100の分解図を示す。
【0015】
マイクロデバイス100は、図1と図2に示すように、カバープレート11とベースプレート12との貼り合わせで構成されており、ベースプレート12のカバープレート11と対向する面には、微細な凹凸形状をもつマイクロチャネル構造が形成されており、試料液の移送や、所定量の液量を保持するなど、それぞれの機能が働くようになっている。
【0016】
カバープレート11は、注入口1、リブ3、大気開放孔10で構成される。ベースプレート12は、点着部2、毛細管キャビティ5、保持チャンバー6、流路8、測定チャンバー7、流路9、出口4で構成される。
【0017】
マイクロデバイス100は、注入口1に注入された血液などの試料液が毛細管キャビティ5を介して所定量だけ保持チャンバー6に一時的に保持する。保持チャンバー6には、分析試薬(図示せず)が担持されている。そして、試料液と分析試薬とが混合され、この混合液が測定チャンバー7に毛細管キャビティ8を介して移送される。測定チャンバー7は、大気開放孔10を有する毛細管キャビティ9と連通している。測定チャンバー7に移送された試料液と分析試薬とが混合物は、光学的手法により所定の項目が測定され分析される。
【0018】
この実施の形態における点着部2の形状は、基端が毛細管キャビティ5に接続され先端がカバープレート11から突出しており、点着部2の先端形状は、ベースプレート12の流路形成面から離れる方向に突出した半球状に形成されている。具体的には、図2と図4に示すように、ベースプレート12の流路形成面に対して垂直に設けられた円柱形状であって、その先端は半球形状である。点着部2はリブ3との間に隙間が形成されており、この点着部2はリブ3との間に隙間が注入口1となっている。
【0019】
ここでカバープレート11をベースプレート12に重ねることで点着部2の先端がカバープレート11の注入口1より突出し試料液を点着しやすい形状を成す。
また、注入口1および点着部2の直径Dは、測定対象の試料液の液滴と同じかそれよりも僅かに大きく設定されており、試料液を点着した際に注入口1のどの部分からでも流入させることができる。このように設定することにより、点着した試料液をすべて毛細管キャビティ内に流入させることが出来る構造となっている。
【0020】
なお、ここで試料液の液滴径とは、試料液が血液の場合、指先を穿刺器具で刺して指先に現れる血液の量は約10μリットルであって、この分量の血液の滴の直径は4mm程度であって、注入口1および点着部2の直径Dは、血液の滴の直径の4mm程度と同じか僅かに大きな5mm程度に構成することが好ましい。
【0021】
また、カバープレート11には点着部2を囲むようにリブ3を設けることで、点着時に点着部2以外の位置に指などが接触して血液が付着するのを防ぐという効果がある。リブ3の高さは点着部2よりも低く設定する。リブ3の高さが点着部2より高いと指先を注入口1に押し当て注入口1を完全に塞いでしまうと試料液が吸い上がらなくなるためである。リブ3はカバープレート11と一体に樹脂成形されており、合成樹脂材料で成形されたリブ3の表面は、合成樹脂材料自身の撥水性で血液を弾く特性を有している。
【0022】
試薬と試料液との混合が所定のレベルに到達すると、保持チャンバー6内の試料液は、毛細管力により流路8内を通じて、測定チャンバー7の入口まで運ばれ、マイクロデバイス100を所定の回転数で回転して発生する遠心力を利用して測定チャンバー7へ移送される。そして移送された試料液は測定チャンバー7にて光学的に所定の項目が測定される。
【0023】
試料液の測定は、測定チャンバー7に光を照射して、検査すべき液体試料と分析試薬の反応状態を光学的に分析する。試料液と分析試薬との反応の割合で吸光度が変化するため照射する光の吸光度を測定することにより所定の項目が測定され、反応状態を分析することができる。本実施の形態では、試料液が毛細管力を利用して注入口1に通じる毛細管キャビティ5を介して保持チャンバー6に試料液を保持する。
【0024】
流路8,9の壁面に親水処理を行っており、親水処理方法としては、プラズマ、コロナ、オゾン、フッ素等の活性ガスを用いた表面処理方法や、界面活性剤や親水性ポリマーによる表面処理が挙げられる。ここで親水性とは水との接触角が90°未満のことをいう。
【0025】
本実施の形態における効果について説明する。
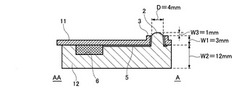
図4にマイクロデバイス100の具体的な寸法例について示す。
ここでは、注入口1及び点着部2の直径:D=4mm、点着部2の先端形状は半球形状で、リブ3からの点着部2の突出高さ:W3=1mmに形成した。カバープレート11のリブ3以外の部分の厚みは2mm、カバープレート11のリブ3の部分の厚み:W1=3mmとしている。マイクロデバイス100が一体構造となるベースプレート12の厚み:W2=12mm、マイクロデバイス100は略65mm角で構成する。
【0026】
このマイクロデバイス100の大きさは、試料液採取部として適当な大きさとするため、適宜変更することができる。また試料液の流路を形成する毛細管キャビティ5の厚さ、即ち、流路の深さは0.1mmである。一方、毛細菅キャビティ5と連結されマイクロデバイス100のベースプレート12に形成される保持チャンバー6の深さは、0.3mm〜0.5mmと毛細菅キャビティ5の厚み(即ち、流路となる深さ)より深く形成する。このように設定することにより、毛細管キャビティ5内に注入された試料液は、毛細管力だけでは、保持チャンバー6に進まず、マイクロデバイス100を回転して得られる遠心力を利用して、試料液を移送するためである。もちろん、毛細管キャビティ5の断面形状が矩形状以外でも毛細管力が作用する形状であれば、円形、楕円形状などいかなる形状でも同様の効果が得られることは当然である。
【0027】
ここで、本発明では、毛細管キャビティ5、流路8,9の深さは0.02mmから0.3mm未満で形成されているが、毛細管力で試料液が流れるのであれば、この寸法に限定されるものではない。一般的には、血液などの液体を測定し分析するので、0.02mmから0.3mm未満が望ましい。また、保持チャンバー6、測定チャンバー7の深さは、0.3mm〜0.5mmで形成しているが、これは、サンプル溶液の量や、吸光度を測定するための条件(光路長、測定波長、サンプル溶液の反応濃度、試薬の種類等)によって調整可能である。そして測定チャンバー7に移送された試料液を光学的に測定する。
【0028】
図5に点着時の様子について示す。
図5(a−1)(a−2)は本実施の形態、図5(b−1)(b−2)は従来例について示す。
【0029】
図5(a−1)(b−1)は点着前の図、図5(a−2)(b−2)は点着中の図を示す。また斜線は試料液であり、試料液を点着部2に近づけているのは指先を示している。
図5(a−1)では指先を点着部2に点着した場合、点着部2の先端を半球状に構成しているため、試料液が半球状の点着部2を伝い流れ、マイクロデバイス100の外壁に試料液が付着することなく点着することが出来る。しかし図5(b−1)では点着部2に指先をつけた場合、試料液が毛細管キャビティ5に導入される以外にマイクロデバイス100の外壁に試料液が付着してしまう様子が確認できる。よって本実施の形態の形状にすることでその効果を確認することができた。
【0030】
図6に点着部2の類似形状について示す。
図6(a)〜(d)に示すように、点着部2の先端の形状は何れも滑らかな曲線で構成していることがわかる。これは試料液がなじみやすくするためである。これらの形状であれば図1〜図4で示したような点着部2と同様の効果として、点着の際、試料液を点着部のみに付着させることが出来る。
【0031】
これらのことから点着部の先端を半球状に構成することで、試料液を点着部のみに付着させることが出来ることを確認した。
【産業上の利用可能性】
【0032】
本発明のマイクロデバイスは、電気化学式センサーや光学式センサーで生物学的流体の成分測定に使用する分析デバイス等として有用である。
【図面の簡単な説明】
【0033】
【図1】本発明の実施の形態におけるマイクロデバイスの斜視図
【図2】同実施の形態のマイクロデバイスの分解斜視図
【図3】同実施の形態のマイクロデバイスの正面図
【図4】図3のA−AA断面図
【図5】同実施の形態における点着時の様子と従来例の点着時の様子の説明図
【図6】本発明の実施の形態1における点着部の類似形状を示す図
【図7】従来例の電気化学式バイオセンサーの分解斜視図
【図8】従来例の遠心移送式バイオセンサーの構成を説明するための図
【図9】従来例の遠心移送式バイオセンサーの試料液分配構成を説明するための図
【符号の説明】
【0034】
1 注入口
2 点着部
3 リブ
4 出口
5 毛細管キャビティ
6 保持チャンバー
7 測定チャンバー
8,9 流路
10 大気開放孔
11 カバープレート
12 ベースプレート
100 マイクロデバイス
【技術分野】
【0001】
本発明は、生物学的流体を電気化学的、もしくは光学的に分析するマイクロデバイスに関するものである。
【背景技術】
【0002】
従来、マイクロ流路を形成したマイクロデバイスを用いて生物学的流体を電気化学的にあるいは光学的に分析する方法がある。電気化学的に分析する方法としては、試料液中の特定の成分を分析するバイオセンサーとして、例えば、血液中のグルコースとセンサー中に担持したグルコースオキシダーゼ等の試薬との反応により得られる電流値を測定することにより、血糖値などを求めるものがある。
【0003】
また、マイクロデバイスを用いて分析する方法では、水平軸を有する回転装置を使って流体の制御をすることが可能であり、遠心力を利用して試料液の計量、細胞質材料の分離、分離された流体の移送分配、液体の混合/攪拌等を行うことができるため、種々の生物化学的な分析を行うことが可能である。
【0004】
マイクロデバイスに試料を導入するための従来の試料液採取方法としては、図7に示す電気化学式バイオセンサーがある。
これは絶縁基板205とカバー206を間にスペーサー207と試薬層210を挟んで貼り合わせたもので、試料液は、カバー206の吸引口208から毛細管現象によりキャビティ212内に導入される。絶縁基板205の上の作用極201、対極202と試薬層210のある位置まで導かれる。209は空気逃げ孔である。
【0005】
この時、キャビティ212の容積で試料の定量採取を行っている。そして作用極201、対極202での試料液と試薬との反応により生じる電流値は、リード203,204を通じて図示しない外部の測定装置に接続して読み取られる(例えば特許文献1参照)。
【0006】
また、図8に示す遠心移送式バイオセンサーでは、試料液は入り口313から毛細管現象により第1の毛細管キャビティ312内に定量採取され、次に遠心力を作用させることで、毛細管キャビティ312内の試料液は濾過材料315と第1の流路314と第2のキャビティ316および芯318を介して受入キャビティ317に移送され、受入キャビティ317で試薬と反応したものを遠心分離させ、第2のキャビティ316に溶液成分のみを毛細管力によって採取し、反応状態が光学的に読み取られる(例えば特許文献2参照)。
【0007】
また、図9に示す遠心移送式バイオセンサー400では、試料を入口ポート409から蛇行した連続微小導管401の中を出口ポート410まで毛細管力で移送し、各毛細管キャビティ404a〜404fを試料液で満たした後、バイオセンサーの回転によって発生する遠心力によって、それぞれの毛細管キャビティ内の試料液を各通気孔406a〜406gの位置で分配し、各連結微小導管407a〜407fを通って、次の処理室(図示省略)へ移送される(例えば特許文献3参照)。408a〜408fはバルブ機能部である。
【特許文献1】特開2001−159618号公報
【特許文献2】特表平4−504758号公報
【特許文献3】特表2004−529333号公報
【発明の開示】
【発明が解決しようとする課題】
【0008】
しかしながら、このような従来の構成では、点着部の先端が矩形状であるため、点着した際に試料液が点着部以外のマイクロデバイスの外壁面に付着してしまうという課題を有している。
【0009】
本発明は前記従来の課題を解決するもので、試料液を点着部のみに付着させることができるマイクロデバイスを提供することを目的とする。
【課題を解決するための手段】
【0010】
本発明の請求項1記載のマイクロデバイスは、流路となる溝が掘られたベースプレートにカバープレートを重ね合わせて内部に毛細管キャビティを形成するとともに、基端が前記毛細管キャビティに接続され先端がカバープレートから突出した点着部を設け、前記点着部の先端が、前記ベースプレートの流路形成面から離れる方向に突出した半球状に形成されていることを特徴とする。
【0011】
本発明の請求項2記載のマイクロデバイスは、請求項1において、前記毛細管キャビティの壁面は親水処理が施されていることを特徴とする。
本発明の請求項3記載のマイクロデバイスは、請求項1において、前記点着部より低く、隙間を空けて前記点着部を囲むリブを設けたことを特徴とする。
【0012】
本発明の請求項4記載のマイクロデバイスは、前記点着部の直径が、測定対象の試料液の液滴と同じかそれよりも僅かに大きいことを特徴とする。
【発明の効果】
【0013】
この構成によれば、点着部の先端を半球状に構成することで、試料液を点着部のみに付着させることができる。
【発明を実施するための最良の形態】
【0014】
以下、本発明の実施の形態のマイクロデバイスを図1〜図6に基づいて説明する。
図1はマイクロデバイス100の構成について示す。図2はマイクロデバイス100の分解図を示す。
【0015】
マイクロデバイス100は、図1と図2に示すように、カバープレート11とベースプレート12との貼り合わせで構成されており、ベースプレート12のカバープレート11と対向する面には、微細な凹凸形状をもつマイクロチャネル構造が形成されており、試料液の移送や、所定量の液量を保持するなど、それぞれの機能が働くようになっている。
【0016】
カバープレート11は、注入口1、リブ3、大気開放孔10で構成される。ベースプレート12は、点着部2、毛細管キャビティ5、保持チャンバー6、流路8、測定チャンバー7、流路9、出口4で構成される。
【0017】
マイクロデバイス100は、注入口1に注入された血液などの試料液が毛細管キャビティ5を介して所定量だけ保持チャンバー6に一時的に保持する。保持チャンバー6には、分析試薬(図示せず)が担持されている。そして、試料液と分析試薬とが混合され、この混合液が測定チャンバー7に毛細管キャビティ8を介して移送される。測定チャンバー7は、大気開放孔10を有する毛細管キャビティ9と連通している。測定チャンバー7に移送された試料液と分析試薬とが混合物は、光学的手法により所定の項目が測定され分析される。
【0018】
この実施の形態における点着部2の形状は、基端が毛細管キャビティ5に接続され先端がカバープレート11から突出しており、点着部2の先端形状は、ベースプレート12の流路形成面から離れる方向に突出した半球状に形成されている。具体的には、図2と図4に示すように、ベースプレート12の流路形成面に対して垂直に設けられた円柱形状であって、その先端は半球形状である。点着部2はリブ3との間に隙間が形成されており、この点着部2はリブ3との間に隙間が注入口1となっている。
【0019】
ここでカバープレート11をベースプレート12に重ねることで点着部2の先端がカバープレート11の注入口1より突出し試料液を点着しやすい形状を成す。
また、注入口1および点着部2の直径Dは、測定対象の試料液の液滴と同じかそれよりも僅かに大きく設定されており、試料液を点着した際に注入口1のどの部分からでも流入させることができる。このように設定することにより、点着した試料液をすべて毛細管キャビティ内に流入させることが出来る構造となっている。
【0020】
なお、ここで試料液の液滴径とは、試料液が血液の場合、指先を穿刺器具で刺して指先に現れる血液の量は約10μリットルであって、この分量の血液の滴の直径は4mm程度であって、注入口1および点着部2の直径Dは、血液の滴の直径の4mm程度と同じか僅かに大きな5mm程度に構成することが好ましい。
【0021】
また、カバープレート11には点着部2を囲むようにリブ3を設けることで、点着時に点着部2以外の位置に指などが接触して血液が付着するのを防ぐという効果がある。リブ3の高さは点着部2よりも低く設定する。リブ3の高さが点着部2より高いと指先を注入口1に押し当て注入口1を完全に塞いでしまうと試料液が吸い上がらなくなるためである。リブ3はカバープレート11と一体に樹脂成形されており、合成樹脂材料で成形されたリブ3の表面は、合成樹脂材料自身の撥水性で血液を弾く特性を有している。
【0022】
試薬と試料液との混合が所定のレベルに到達すると、保持チャンバー6内の試料液は、毛細管力により流路8内を通じて、測定チャンバー7の入口まで運ばれ、マイクロデバイス100を所定の回転数で回転して発生する遠心力を利用して測定チャンバー7へ移送される。そして移送された試料液は測定チャンバー7にて光学的に所定の項目が測定される。
【0023】
試料液の測定は、測定チャンバー7に光を照射して、検査すべき液体試料と分析試薬の反応状態を光学的に分析する。試料液と分析試薬との反応の割合で吸光度が変化するため照射する光の吸光度を測定することにより所定の項目が測定され、反応状態を分析することができる。本実施の形態では、試料液が毛細管力を利用して注入口1に通じる毛細管キャビティ5を介して保持チャンバー6に試料液を保持する。
【0024】
流路8,9の壁面に親水処理を行っており、親水処理方法としては、プラズマ、コロナ、オゾン、フッ素等の活性ガスを用いた表面処理方法や、界面活性剤や親水性ポリマーによる表面処理が挙げられる。ここで親水性とは水との接触角が90°未満のことをいう。
【0025】
本実施の形態における効果について説明する。
図4にマイクロデバイス100の具体的な寸法例について示す。
ここでは、注入口1及び点着部2の直径:D=4mm、点着部2の先端形状は半球形状で、リブ3からの点着部2の突出高さ:W3=1mmに形成した。カバープレート11のリブ3以外の部分の厚みは2mm、カバープレート11のリブ3の部分の厚み:W1=3mmとしている。マイクロデバイス100が一体構造となるベースプレート12の厚み:W2=12mm、マイクロデバイス100は略65mm角で構成する。
【0026】
このマイクロデバイス100の大きさは、試料液採取部として適当な大きさとするため、適宜変更することができる。また試料液の流路を形成する毛細管キャビティ5の厚さ、即ち、流路の深さは0.1mmである。一方、毛細菅キャビティ5と連結されマイクロデバイス100のベースプレート12に形成される保持チャンバー6の深さは、0.3mm〜0.5mmと毛細菅キャビティ5の厚み(即ち、流路となる深さ)より深く形成する。このように設定することにより、毛細管キャビティ5内に注入された試料液は、毛細管力だけでは、保持チャンバー6に進まず、マイクロデバイス100を回転して得られる遠心力を利用して、試料液を移送するためである。もちろん、毛細管キャビティ5の断面形状が矩形状以外でも毛細管力が作用する形状であれば、円形、楕円形状などいかなる形状でも同様の効果が得られることは当然である。
【0027】
ここで、本発明では、毛細管キャビティ5、流路8,9の深さは0.02mmから0.3mm未満で形成されているが、毛細管力で試料液が流れるのであれば、この寸法に限定されるものではない。一般的には、血液などの液体を測定し分析するので、0.02mmから0.3mm未満が望ましい。また、保持チャンバー6、測定チャンバー7の深さは、0.3mm〜0.5mmで形成しているが、これは、サンプル溶液の量や、吸光度を測定するための条件(光路長、測定波長、サンプル溶液の反応濃度、試薬の種類等)によって調整可能である。そして測定チャンバー7に移送された試料液を光学的に測定する。
【0028】
図5に点着時の様子について示す。
図5(a−1)(a−2)は本実施の形態、図5(b−1)(b−2)は従来例について示す。
【0029】
図5(a−1)(b−1)は点着前の図、図5(a−2)(b−2)は点着中の図を示す。また斜線は試料液であり、試料液を点着部2に近づけているのは指先を示している。
図5(a−1)では指先を点着部2に点着した場合、点着部2の先端を半球状に構成しているため、試料液が半球状の点着部2を伝い流れ、マイクロデバイス100の外壁に試料液が付着することなく点着することが出来る。しかし図5(b−1)では点着部2に指先をつけた場合、試料液が毛細管キャビティ5に導入される以外にマイクロデバイス100の外壁に試料液が付着してしまう様子が確認できる。よって本実施の形態の形状にすることでその効果を確認することができた。
【0030】
図6に点着部2の類似形状について示す。
図6(a)〜(d)に示すように、点着部2の先端の形状は何れも滑らかな曲線で構成していることがわかる。これは試料液がなじみやすくするためである。これらの形状であれば図1〜図4で示したような点着部2と同様の効果として、点着の際、試料液を点着部のみに付着させることが出来る。
【0031】
これらのことから点着部の先端を半球状に構成することで、試料液を点着部のみに付着させることが出来ることを確認した。
【産業上の利用可能性】
【0032】
本発明のマイクロデバイスは、電気化学式センサーや光学式センサーで生物学的流体の成分測定に使用する分析デバイス等として有用である。
【図面の簡単な説明】
【0033】
【図1】本発明の実施の形態におけるマイクロデバイスの斜視図
【図2】同実施の形態のマイクロデバイスの分解斜視図
【図3】同実施の形態のマイクロデバイスの正面図
【図4】図3のA−AA断面図
【図5】同実施の形態における点着時の様子と従来例の点着時の様子の説明図
【図6】本発明の実施の形態1における点着部の類似形状を示す図
【図7】従来例の電気化学式バイオセンサーの分解斜視図
【図8】従来例の遠心移送式バイオセンサーの構成を説明するための図
【図9】従来例の遠心移送式バイオセンサーの試料液分配構成を説明するための図
【符号の説明】
【0034】
1 注入口
2 点着部
3 リブ
4 出口
5 毛細管キャビティ
6 保持チャンバー
7 測定チャンバー
8,9 流路
10 大気開放孔
11 カバープレート
12 ベースプレート
100 マイクロデバイス
【特許請求の範囲】
【請求項1】
流路となる溝が掘られたベースプレートにカバープレートを重ね合わせて内部に毛細管キャビティを形成するとともに、基端が前記毛細管キャビティに接続され先端がカバープレートから突出した点着部を設け、
前記点着部の先端が、前記ベースプレートの流路形成面から離れる方向に突出した半球状に形成されている
マイクロデバイス。
【請求項2】
前記毛細管キャビティの壁面は親水処理が施されていることを特徴とする
請求項1に記載のマイクロデバイス。
【請求項3】
前記点着部より低く、隙間を空けて前記点着部を囲むリブを設けたことを特徴とする
請求項1に記載のマイクロデバイス。
【請求項4】
前記点着部の直径が、測定対象の試料液の液滴と同じかそれよりも僅かに大きいことを特徴とする
請求項1に記載のマイクロデバイス。
【請求項1】
流路となる溝が掘られたベースプレートにカバープレートを重ね合わせて内部に毛細管キャビティを形成するとともに、基端が前記毛細管キャビティに接続され先端がカバープレートから突出した点着部を設け、
前記点着部の先端が、前記ベースプレートの流路形成面から離れる方向に突出した半球状に形成されている
マイクロデバイス。
【請求項2】
前記毛細管キャビティの壁面は親水処理が施されていることを特徴とする
請求項1に記載のマイクロデバイス。
【請求項3】
前記点着部より低く、隙間を空けて前記点着部を囲むリブを設けたことを特徴とする
請求項1に記載のマイクロデバイス。
【請求項4】
前記点着部の直径が、測定対象の試料液の液滴と同じかそれよりも僅かに大きいことを特徴とする
請求項1に記載のマイクロデバイス。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2009−229243(P2009−229243A)
【公開日】平成21年10月8日(2009.10.8)
【国際特許分類】
【出願番号】特願2008−74785(P2008−74785)
【出願日】平成20年3月24日(2008.3.24)
【出願人】(000005821)パナソニック株式会社 (73,050)
【Fターム(参考)】
【公開日】平成21年10月8日(2009.10.8)
【国際特許分類】
【出願日】平成20年3月24日(2008.3.24)
【出願人】(000005821)パナソニック株式会社 (73,050)
【Fターム(参考)】
[ Back to top ]

