マイクロ流体デバイス及び微量試料の注入方法
【課題】 流体試料を注入するデバイスおよびその方法において、荷電試料だけでなく非イオン性試料や気体試料にも適用可能で、非電解質液体媒体中、気体媒体中、または真空系への試料注入が可能であり、試料注入に複雑で大がかりな装置や複雑な制御を要することなく、簡易な操作で、極微量の試料を定量性よく、テーリングも少なく注入することが可能なマイクロ流体デバイス、およびそれを用いた試料注入方法を提供すること。
【解決手段】 第一流路と、その途中の分岐部にて分岐した第二流路と、分岐部近傍の第二流路中に設けられた弁と、分岐部近傍の第一流路の流路壁にあり、第一流路の外部からの圧力により第一流路の断面積を減少させる圧迫部とを有し、前記弁が常態では閉じており、且つ圧迫部を圧迫することにより開いて第一流路内の流体が第二流路内に流入する弁であるマイクロ流体デバイス。
【解決手段】 第一流路と、その途中の分岐部にて分岐した第二流路と、分岐部近傍の第二流路中に設けられた弁と、分岐部近傍の第一流路の流路壁にあり、第一流路の外部からの圧力により第一流路の断面積を減少させる圧迫部とを有し、前記弁が常態では閉じており、且つ圧迫部を圧迫することにより開いて第一流路内の流体が第二流路内に流入する弁であるマイクロ流体デバイス。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、マイクロ流体デバイス内に組み込まれた、又はマイクロ流体デバイス外に接続された機構に、極微量の試料を小さなスポットとして、又は極短時間にパルス状に注入することが出来るマイクロ流体デバイス、および、微量の流体の注入方法に関する。
【背景技術】
【0002】
マイクロ流体デバイスは、内部に有する微細な毛細管状の流路中で反応や分析を行うデバイスであり、マイクロ流体デバイスを使用することにより、反応や分析の迅速化、必要試料量の減少、省資源・省エネルギー、さらには廃棄物の減少が可能となる。このようなマイクロ流体デバイスを使用して、例えば、マイクロ電気泳動分析、マイクロクロマトグラフィー分析、マススペクトル分析の試料の前処理など、医療診断、生化学分析、化学分析の方面で微量の試料を分析する試みが行われている。
【0003】
しかしながら、マイクロ流体デバイスのスケールは、従来のポンプ、切り替えバルブ、シリンジ、ピペットなどの試料取り扱い手段や装置に比べて桁違いに小さいため、マイクロ流体デバイスの流路中に極微量の試料を注入することは相当困難であった。例えば、マイクロ・ガスクロマトグラフィー、マイクロ・液体クロマトグラフィー、マイクロ・アフィニティー・クロマトグラフィー、マイクロ・ゲル・パーミエーション・クロマトグラフィーなどのマイクロ・クロマトグラフィー分析においては、短い展開距離で迅速に高分解能の分析を行うためには、試料を短いスポットとして分離カラムに注入する必要があるが、マイクロシリンジやバルブによる流路切り替え法などの従来法による試料注入手段では注入試料の体積が過大になりがちであり、そのため、クロマトグラムのピークの広がりや、テーリングが生じ、良好に分離するためにはカラム長を太く或いは長くする必要があり、分析時間の伸長を招いていた。
【0004】
これを解決する方法として電気泳動分析に於いて、次の方法が試みられている(特許文献1参照。)。即ち、交差部に於いて交差する2本の流路の一方の一端に試料を注入し、該流路の両端に電圧を印加して電気泳動又は電気浸透流にて試料を移送し、試料が前記交差部を通過している時点で該電圧の印加を停止し、次いで、他方の流路の両端に電圧を印加することによって、交差部内の試料のみを他方の流路へ注入する方法である。
しかし、この方法では、分岐部の容積だけの極微量の試料を他方の流路に注入することが可能であるが、電気泳動による試料移送であるため、試料は荷電試料に限られ、また、媒体も電解質媒体に限られるため、ガスクロマトグラフィー、真空系へ試料を注入する質量分析装置、および多くの液体クロマトグラフィーには適用できなかった。
【0005】
また、サンプル分析の装置として、接合する二本のチャネルを有するデバイスを包含する装置が開示されている(特許文献2参照。)。該装置中のデバイスにおいては、デバイス内のチャネルに圧力勾配を適用させて、試料が注入されたチャネルから分離チャネルに試料を配置するものである。しかし、該方法においては、次のような点で、試料注入方法としては不十分なものであった。(1)質量分析装置のような真空系への試料注入は不可能なこと、(2)拡散速度の高い気体試料には適用が難しいこと、(3)試料注入用流路と電気泳動分析用流路の圧力や、その制御のタイミングを精密に行う必要があるため、ポンプやバルブなどの機構が複雑かつ大がかりとなりがちであること、(4)該公知文献にはクロマトグラフィーの試料注入については記載されていないが、本発明者等の検討によれば、二つの流路の圧力を厳密に制御する必要があり、制御装置が大がかりなものに成りがちであること、(5)注入試料がテーリングを生じがちであり、それを抑制するためには、更に複雑な機構や圧力制御操作が必要なこと。
【0006】
【特許文献1】特開平11−271273号公報
【特許文献2】特表2002−542489号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明が解決しようとする課題は、マイクロ流体デバイス内に組み込まれた、又はマイクロ流体デバイス外に接続された機構に、流体試料を注入するデバイスおよびその方法において、荷電試料だけでなく非イオン性試料や気体試料にも適用可能で、非電解質液体媒体中、気体媒体中、または真空系への試料注入が可能であり、試料注入に複雑で大がかりな装置や複雑な制御を要することなく、簡易な操作で、極微量の試料を定量性よく、テーリングも少なく注入することが可能なマイクロ流体デバイス、およびそれを用いた試料注入方法を提供すること。特に、マイクロ・クロマトグラフィーやマイクロ電気泳動分析用マイクロ流体デバイスへの試料注入方法、また、マイクロ流体デバイスに接続された質量分析装置などの分析装置への試料注入方法を提供すること。さらに、上記の機能を有しながら、安価で使い捨て可能なマイクロ流体デバイスを提供すること。
【課題を解決するための手段】
【0008】
本発明者らは、上記の課題を解決すべく鋭意検討した結果、第一流路(1)と、その途中の分岐部(3)にて分岐した第二流路(2)と、分岐部(3)近傍の第二流路(2)中に設けられた弁(4)と、分岐部(3)近傍の第一流路(1)の流路壁にあり、第一流路(1)の外部からの圧力により第一流路(1)の断面積を減少させる圧迫部(5)とを有し、前記弁(4)が常態では閉じており、且つ圧迫部(5)を圧迫することにより開いて第一流路(1)内の流体が第二流路(2)内に流入する弁であるマイクロ流体デバイスにより、上記課題を解決できることを見出し、本発明を完成するに至った。
【発明の効果】
【0009】
本発明のマイクロ流体デバイス及び試料注入方法は、マイクロ流体デバイス内に組み込まれた、又はマイクロ流体デバイス外に接続された機構に、極微量の流体試料を小さなスポットとして、又は極短時間にパルス状に注入することが出来るマイクロ流体デバイス、及びそれを用いた試料注入方法を提供できる。本発明は、荷電試料だけでなく非イオン性試料や気体試料にも適用可能であり、また、電解質液体媒体中への注入だけでなく、非電解質液体媒体中、気体媒体中、または真空系への試料注入が可能であるため、適用範囲が極めて広い。そのため、特に、マイクロ・ガスクロマトグラフィー、マイクロ・液体クロマトグラフィー、マイクロ・アフィニティー・クロマトグラフィー、マイクロ・ゲル・パーミエーション・クロマトグラフフィーなどのマイクロ・クロマトグラフィーの試料注入や、マイクロ流体デバイスに接続された質量分析装置への試料注入に用いると効果的である。
【0010】
また、本発明のマイクロ流体デバイス及び試料注入方法は、試料注入に複雑で大がかりな制御装置や複雑な制御を要せず、簡易な操作で試料を注入することが可能であり、マイクロ・トータル・アナリシス・システム(μ−TAS)に組み込んで使用することが容易である。
【0011】
さらに、本発明のマイクロ流体デバイスは、簡単な構造で容易に製作できるため、安価で使い捨て可能なマイクロ流体デバイスとすることが可能である。
【発明を実施するための最良の形態】
【0012】
以下、本発明について、詳細に説明する。
[マイクロ流体デバイス]
本発明のマイクロ流体デバイスは、部材内部に毛細管状の流路を有するデバイスである。マイクロ流体デバイスは、マイクロ流体デバイス、マイクロ・フルイディック・デバイス、マイクロ・ファブリケイテッド・デバイス、マイクロ流路、ラボ・オン・チップ、又はマイクロ・トータル・アナリシス・システム(μ−TAS)とも呼ばれるものを指し、該流路内で、化学反応、生化学反応、流体の温度変化、濃度調整、分離、測定などを行うデバイスである。
本発明のマイクロ流体デバイスの外形は、板状(柔軟なシート状を含む)、棒状(柔軟なひも状を含む)、チューブ状(毛細管状を含む)、塊状、又は、組み合わせ型マイクロ流体デバイスのコンポーネント(モジュール)となる形状、などの任意の形状であって良い。なかでも形状が板状のものは、製造が容易であり、流路などの構造に高い寸法精度や位置精度を持たせることができ、マイクロ流体デバイスの他の構造と一体化することが容易である上、使用時の温度調節や流路の観測が容易であるため好ましい。
【0013】
本発明のマイクロ流体デバイスを構成する材料は特に限定する必要がなく、例えば、ガラス、水晶等の結晶、シリコンなどの半導体、金属、セラミック、炭素、有機重合体(ポリジメチルシロキサンのように、無機元素を含有するものも含む。)、あるいはこれらの発泡体などを使用できる。また、例えば有機重合体などの上に金属やその他の物質を蒸着した複合材料なども使用できる。但し、後述のように、圧迫部においては、可撓性のある素材を使用する必要がある。なかでも、活性エネルギー線硬化性樹脂を使用すると、各種形状への成形が容易である。
【0014】
本発明のマイクロ流体デバイスは、毛細管状の流路[第一流路(1)と称する]、及び該第一流路(1)の途中の分岐部(3)から分岐した毛細管状の流路[第二流路(2)と称する]を有する。なお、本発明に於いては、特に言及しない限り、「第一流路(1)」は「分岐部(3)」を含むものとして説明する。
【0015】
[第一流路(1)]
第一流路の横断面、即ち、流体の流動方向に直角な断面(以下、該断面を単に「流路断面」と略記する。)の形状は特に限定されないが、矩形、台形、または半円形であることが、製造や内部の観察が容易であり好ましい。
【0016】
流路断面の寸法は任意であるが、幅、深さ共に1〜500μmであることが好ましい。但し、第一流路(1)をマイクロ・キャピラリー・クロマトグラフィー用の分離カラムとして使用する場合には、該流路の幅、深さの少なくとも一方は1〜50μmであことが好ましい。さらに、後述のように、これらの分離カラムが、流路内面の少なくとも一つの面に多孔質層を有するものである場合には、該断面中の任意の点をx、該点xと直線距離で最も近い多孔質層の部分をy、xy間の直線距離をrとし、rが該断面内でとり得る最大距離をrmaxとした際に、該rmaxが1〜50μmの範囲となるように設計することが好ましい。このような寸法とすることにより、流路内を流動する流体に含まれる分離対象物質が流路壁面や多孔質層と十分に相互作用を生じることができるため、高い分離能を実現することが出来る。勿論、流路の断面形状や断面寸法は流路の流れ方向で変化していて良い。
【0017】
但し、第一流路(1)をクロマトグラフィー用や電気泳動分析用の充填カラム或いはモノリス型多孔質カラムとする場合には、上記寸法の制約はなく、第一流路(1)の外部の直径は更に太くても良い。
【0018】
第一流路(1)の長さは任意であり、用途目的に応じて好適な長さをとり得る。例えば第一流路(1)の少なくとも一部をクロマトグラフィー用、或いは電気泳動分析用の分離カラムとして使用する場合には、1mm〜500mmが好ましく、5mm〜200mmが更に好ましい。上記下限以上とすることで、十分な分離能を得ることができ、上記上限以下とすることによって、マイクロ流体デバイスを小形化できる。
【0019】
第一流路(1)の流体の流動方向の形態も任意であり、直線であっても、曲線であってもよい。各流路の端はマイクロ流体デバイス外に連絡する開口部となっていてもよいし、マイクロ流体デバイス外の装置と接続するための配管が接続されていても良く、マイクロ流体デバイス内の他の機構に接続されていても良い。
【0020】
第一流路(1)は、分岐部(3)へ試料を導くための流路として用いることが出来る。第一流路(1)の一端は、試料を注入することが出来れば任意であり、例えば、マイクロ流体デバイス外に開口した開口部や、マイクロ流体デバイス外と連絡する配管が接続された配管接続部であって良いし、マイクロ流体デバイス中の他の機構、例えば貯液層、内部ポンプ、濾過機構、バルブなどに接続されていても良い。また、試料を電気泳動や電気浸透流によって移送する場合には電極を設置することができる。第一流路(1)の他端は任意であり、前記一端と同様の機構の他、試料溶液を吸引するための真空チャンバー、繊維充填型や多孔質型などの液体吸収部でありうる。即ち、前記一端から第一流路(1)に流入した試料溶液は、分岐部(3)を経て、他端から流出するように使用することが出来る。
【0021】
第一流路(1)の一端と分岐部(3)の間(以下、「分岐部(3)の上流側」と称する。)には、クロマトグラフィー用の分離カラムや電気泳動分析用の分離カラムが直列に設けられていてもよい。これらの分離カラムで分離された試料が分岐部(3)を経て移動するように使用することにより、分離された試料が分岐部に来たときに、選択的に第二流路(2)へ注入することが出来る。分離された試料が分岐部(3)に到達したことは、分岐部(3)またはその上流部分を光学的に観測することで判断できる。
【0022】
分岐部(3)と第一流路(1)の他端との間(以下、「分岐部(3)の下流側」と称する。)の第一流路に関しても、上記分岐部(3)の上流側の場合と同様である。例えば、前記のように分岐部(3)の上流側にクロマトグラフィー用の分離カラムなどを設け、分離された試料の内、不要のものを第二流路(2)へ除去し、残された試料を下流側の機構へ注入することも出来る。そのような必要がない場合には、単なる廃液用流路として使用できる。
【0023】
[弁]
本発明のマイクロ流体デバイスにおいては、分岐部(3)において第一流路(1)から分岐した第二流路(2)に、常態、即ち該弁に何らの操作も加えない状態では閉じていて、分岐部側の流路内圧力が一定値以上になると開く弁(以下、このような弁を単に弁(4)と称する)が設けられている。該弁(4)は分岐部(3)に接して設けることが好ましい。これにより、分岐部(3)と弁(4)間の死容積をなくすことが出来、第一流路を流れて分岐部(3)に到達した試料を死容積部分に滞留していた流体で希釈することないため、定量性良く、かつ濃度変化もなく、確実に第二流路(2)へ注入することが出来る。そのため、第一流路(1)の分岐部(3)の上流側に前記分離カラムが設けられている場合には、該弁(4)を分岐部(3)に接して設けることが特に好ましい。また、第二流路(2)にさらに別の流路(以下、第三流路(6)とする。)が設けられる場合には、該弁(4)は、第三流路(6)の近傍であることが好ましく、第三流路(6)接続部に接していることがさらに好ましい。この場合も、弁(4)と通過した流体を、該弁(4)と第三流路(6)接続部との間の第二流路(2)の死容積部分に滞留していた流体で希釈することないため、定量性良く、かつ濃度変化もなく、確実に第二流路(2)へ注入することが出来る。
【0024】
弁(4)は、常態では閉じていて、分岐部側の圧力が一定値以上で開けば、他の状態での動作は任意である。例えば、(a)分岐部(3)とは反対の側[第二流路(2)側と称する]の圧力がいくら高くなっても開かない逆止弁、(b)第二流路(2)側の圧力が一定値以上になると開くタイプのバルブ、(c)第二流路(2)側の圧力が下がることによって両側の圧力差が一定値以上になると開くタイプのバルブ、(d)第二流路(2)側の圧力がいくら低くなっても、開かないタイプのバルブ、などであって良い。これらは、用途目的に応じて選択できる。例えば、第二流路(2)が減圧される用途、例えば質量分析装置に接続される場合には、第二流路(2)側の圧力がいくら低くなっても開かないタイプのバルブとすることが必要である。
【0025】
弁(4)の構造は任意であり、例えば、本発明者らによる特開2003-139660に開示されているような、流路の途上に堰状構造が設けられて該流路は該部分で途切れており、該堰状構造は、堰の上面と流路壁が接触しているが接着していないため、常態では閉じていて、該堰状構造のいずれか一方又は両方の側の圧力が一定値以上になると開くが、いずれか一方又は両方の側の圧力がいくら低くなっても開かないタイプの弁を使用できる。
【0026】
[圧迫部]
本発明のマイクロ流体デバイスにおいては、第一流路(1)の分岐部(3)近傍に、流路壁を第一流路外から圧迫すると第一流路(1)の断面積が減少するような可撓性の材料で形成された圧迫部(5)が設けられている。該圧迫部(5)を圧迫することによって分岐部内の流体の圧力を高め、弁(4)を通して流体を第二流路へ注入することが出来る。
【0027】
圧迫部(5)を設ける領域としては、概ね分岐部(3)の領域のみの範囲であっても、分岐部(3)を含む広い範囲であっても良い。概ね分岐部(3)の領域のみに設ける場合には、該分岐部(3)において第一流路(1)は幅広となっていることが好ましい。幅広とすることで、該部分を圧迫したとき、分岐部の圧力を効果的に高めることができ、流体を弁(4)を通過して注入することが容易になる。
【0028】
また、圧迫部(5)が第一流路(1)の分岐部(3)を含む広い範囲に設けられている場合には、該広い範囲を圧迫することで、該圧迫部分の流路から逃げる液体の圧力損失によって、分岐部の圧力を効果的に高めることができ、流体を弁(4)を通して容易に注入することが出来るため好ましい。
【0029】
圧迫部(5)は、分岐部(3)をまたぐ両側の2つの圧迫部(5a)(5b)とその間の圧迫部(5)から成ることが好ましい。該圧迫部(5)を圧迫する際には、圧迫部(5a)(5b)を先に圧迫し、該圧迫を維持したまま、圧迫部(5)を圧迫する方法によって、確実にかつ定量的に試料を注入することが容易となる。圧迫部(5)は分岐部(3)に限定されず、その近傍であればよい。
【0030】
第一流路(1)の圧迫部(5)における断面の周囲を構成するいずれかの部分が可撓性材料で形成されるが、可撓性材料で形成される部分は任意であり、流路の底面、側壁、天井面の少なくとも一つであり得る。但し、最も柔軟な部分を直接圧迫する必要はなく、例えば両側壁が柔軟な材料で形成された第一流路(1)を可撓性ではあるが側壁より硬質の材料で形成された天井部から押圧することで、両側壁が変形しても良い。
【0031】
可撓性材料は任意であるが、架橋重合体であることが、クリープが少なく、繰り返し使用に耐えるため好ましい。可撓性材料は、引っ張り弾性率にして100GPa以下が好ましく、10GPa以下がさらに好ましく、1GPa以下が最も好ましい。引っ張り弾性率の下限は、自己保持できれば任意であるが、流路の耐圧性や取り扱いの容易さの面から、1KPa以上が好ましく、10KPa以上がより好ましい。引っ張り弾性率が10〜100GPaの素材は、圧迫部の面積を比較的大きく採り、厚みを薄くすることで使用できる。本発明に使用できる可撓性材料としては、有機重合体、金属、ガラス、結晶などを例示できるが、有機重合体が、引っ張り弾性率の選択範囲が広く、破断伸び率も大きいため好ましい。特に活性エネルギー線硬化性樹脂を使用した場合には、各種成形が容易であるため好ましい。
【0032】
圧迫部を機械的に押圧して圧迫する場合には、圧迫部の外表面に凸状構造を設けることも好ましい。これにより、平らな接触面を持つ圧迫用部材を用いて、該凸状構造を含む比較的広い範囲を圧迫すると、選択的に圧迫部が圧迫されるため、圧迫位置の正確な位置合わせが不要となる。
【0033】
また、圧迫機構にかかわらず、2つの圧迫部(5a)(5b)において、第一流路の高さ(即ち、圧迫により減少する方向の寸法)を他の部分より小さくすることが好ましい。このような構造により、圧迫に際し、該部分において流路が確実に閉鎖されることにより、注入量の定量性を向上させることができる。このような構造は、例えば、該部分において、第一流路の底を高くした構造、及び/又は、天井を低くした構造により実施できる。
【0034】
「第二流路」
本発明のマイクロ流体デバイスは、第一流路(1)の途中の分岐部(3)から分岐した毛細管状の流路[第二流路(2)と称する]を有する。第二流路の断面形状、寸法や流路方向の形態、長さに関しては第一流路(1)の場合と同様である。第二流路(2)をマイクロ・クロマトグラフィー用等の分離カラムとして使用する場合にも、第一流路(1)の場合と同様である。
【0035】
第二流路(2)は、流体の流動方向の形態も任意であり、直線であっても、曲線であってもよい。該流路の端はマイクロ流体デバイス外に連絡する開口部となっていてもよく、マイクロ流体デバイス外の装置と接続するための配管が接続されていても良く、マイクロ流体デバイス内の他の機構に接続されていても良い。
【0036】
第二流路(2)は、分岐部(3)から弁(4)を通して極微量の試料が注入される流路であり、反応や分析などを行うための流路として用いることが出来る。例えば、第二流路(2)は、該マイクロ流体デバイス内に設けられたクロマトグラフィー等の分離カラムとして使用されることも好ましい。或いは、該マイクロ流体デバイス外に設けられたクロマトグラフィー装置、電気泳動分析装置、質量分析装置、光学的その他の検出装置に接続されることが好ましい。また、第二流路は真空であっても良く、この場合には、第二流路へ注入された液体は直ちに気化して第二流路中を移送される。
【0037】
第二流路(2)には、他の流路(第三流路(6))が接続されていることも好ましい。第二流路(2)に、該マイクロ流体デバイス内に設けられたクロマトグラフィー等の分離カラムが接続されている場合には、該第三流路(6)の接続部(7)は分離カラム部より弁(4)側に設けられる。接続部(7)は前記弁(4)のなるべく近傍に設けることが、試料注入の定量性が増すため好ましい。第三流路(6)は、クロマトグラフィーの展開液注入路、電気泳動分析の導電路、第二流路へ注入された試料と混合すべき液体の注入路、などとして用いられる。
【0038】
本発明の試料注入方法は、本発明に成るマイクロ流体デバイスを用い、該マイクロ流体デバイスの第一流路(1)に試料を流し、前記圧迫部(5)を圧迫することによって前記第一流路(1)内の圧力を上昇させて、前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする。本発明の試料注入方法に適用できる試料の流体は任意であり、液体、超臨界流体、気体であり得るが、液体であることが、定量性が向上し好ましい。液体試料の種類は任意であり、単一液体、混合液体、溶液、分散液であり得る。溶質は任意であり、化学物質、生化学物質、有機物質、無機物質、揮発性物質、不揮発性物質、ノニオン性物質、カチオン性物質、アニオン性物質、両性イオン性物質、親水性物質、疎水性物質、両新馬異性物質、などであり得るし、溶媒は電解質、非電解質であり得る。
【0039】
圧迫する位置〔圧迫部(5)〕は分岐部(3)であっても良いし、分岐部(3)を含む第一流路(1)の広い範囲であっても良い。このとき、該圧迫部の流路から逃げる液体の圧力損失によって、分岐部の圧力を効果的に高めることができ、流体を弁(4)を通して容易に注入することが出来る。
【0040】
圧迫する位置〔圧迫部(5)〕は、分岐部(3)をまたぐ両側の2つの圧迫部(5a)(5b)とその間の圧迫部(5)であることが好ましい。該圧迫部(5)を圧迫する際には、圧迫部(5a)(5b)を先に圧迫し、該圧迫を維持したまま、圧迫部(5)を圧迫する方法によって、確実にかつ定量的に試料を注入することが容易となる。圧迫部(5)は分岐部(3)に限定されず、その近傍であればよい。
【0041】
圧迫方法は任意であり、アクチュエーターなどによるマイクロ流体デバイス外からの機械的な押圧、マイクロ流体デバイスの流路壁に接して設置した、または流路壁を構成するピエゾ素子による圧迫、マイクロ流体デバイスの流路壁に固定された強磁性体の磁力による駆動、該圧迫部における流路壁の、第一流路(1)と反対側にもうけられた圧力室への流体の導入による加圧、などを例示できる。これらの中で、マイクロ流体デバイス外からの機械的な押圧が、構造が単純であり、使い捨て可能なマイクロ流体デバイスを容易に作成できること、および、第一流路(1)や分岐部(3)の容積を小さくすることが容易なため、分岐部に供給される試料溶液が少ない場合にも適用可能であり、好ましい。それに次いで、強磁性体やピエゾ素子による迫が好ましい。
【0042】
本発明の試料注入方法は、クロマトグラフィーや電気泳動によって分離された試料スポットを選択的に第二流路(2)へ注入する方法であることも好ましい。この方法によって、例えば、該試料スポットを採取したり、質量分析装置などの分析装置へ注入することが出来る。或いは、該試料スポットの化合物を第二流路における反応に供することが出来る。この場合には、第一流路(1)の分岐部(3)より上流側にこれらの分離用キャピラリーや分離用カラムを設け、分離された試料スポットが分離部(4)に来たときに圧迫を行って第二流路へ注入する。このとき、第一流路(1)の前記分岐部(3)及び/又は前記分離カラムと前記分岐部(3)の間の部分に、第一流路(1)内の試料を光学的に観察する測定用の窓を設けたマイクロ流体デバイスを使用し、該窓を光学的に観察しつつ前記圧迫部(5)を圧迫することにより前記試料の一部を第二流路(2)へ注入することも好ましい。
上記の試料注入方法は、クロマトグラフィーや電気泳動によって分離された試料スポットを選択的に第二流路(2)へ除去し、残余を第一流路の分岐部より下流側へ注入する方法としても利用できる。この方法によって、例えば、特定の試料スポットを除去した試料を採取したり、該試料スポットを除去した試料を第一流路の下流側部における、或いは第一流路から流出させて反応に供することが出来る。
【0043】
本発明の試料注入方法は、クロマトグラフへの微量試料の注入方法であることも好ましい。この場合には、前記第二流路にこれらの分離用キャピラリーや分離用カラムを設けた、或いは接続したマイクロ流体デバイスを用い、注入すべき試料を第一流路に流して、その一部を第二流路に注入する。
【0044】
本発明の試料注入方法によれば、使用するマイクロ流体デバイス中の流路径や、圧迫部(5a)、(5b)の位置等の設計により、微少量、特に0.1pl(但し、pl=nm3)〜300nl(但し、nl=pm3)、さらに好ましくは1pl〜30nl、最も好ましくは10pl〜10nl程度の微少量の試料を定量的に注入することも可能である。さらに、圧迫部の圧迫操作をパルス的に行うことによって、複雑な制御を行わなくても、上記微少量の試料を最小のテーリングでもってパルス的に注入することが可能である。
【実施例】
【0045】
以下、実施例を用いて本発明を更に詳しく説明するが、本発明は、以下の実施例の範囲に限定されるものではない。本実施例における紫外線照射、および蛍光特性測定の方法を以下に示す。
【0046】
(紫外線ランプ1による照射)
3000Wメタルハライドランプを光源とするアイグラフィックス株式会社製のUE031−353CHC型UV照射装置を用い、365nmにおける紫外線強度が40mW/cm2の紫外線を特に指定が無い限り室温、窒素雰囲気中で照射した。
【0047】
(紫外線ランプ2による照射)
250W高圧水銀ランプを光源とするウシオ電機株式会社製のマルチライト250Wシリーズ露光装置用光源ユニットを用い、365nmにおける紫外線強度が50mW/cm2の紫外線を、特に指定が無い限り室温、窒素雰囲気中で照射した。
【0048】
(実施例1)
[組成物(X1)の調製]
エネルギー線重合性化合物(a)として平均分子量2000の3官能ウレタンアクリレートオリゴマー「ユニディックV−4263」(大日本インキ化学工業株式会社製)70部、ヘキサンジオールジアクリレート「ニューフロンティアHDDA」(第一工業製薬株式会社製)30部、光重合開始剤として1−ヒドロキシシクロヘキシルフェニルケトン「イルガキュアー184」(チバガイギー社製)3部、及び重合遅延剤として2,4−ジフェニル−4−メチル−1−ペンテン(関東化学株式会社製)0.5部を混合して、組成物(X1)を調製した。
【0049】
[組成物(X2)の調製]
エネルギー線重合性化合物として上記「ユニディックV−4263」80部、上記「ニューフロンティアHDDA」20部、光重合開始剤として上記「イルガキュアー184」2部を混合して、蓋用組成物を調製した。
【0050】
製膜液(Y1)の調製]
エネルギー線重合性化合物(b)として、上記「ユニディックV−4263」72質量部、ジシクロペンタニルジアクリレート「R−684」(日本化薬株式会社製)18質量部、メタクリル酸グリシジル(和光純薬工業株式会社製)10質量部、貧溶剤(R)としてデカン酸メチル(和光純薬工業株式会社製)を180質量部、揮発性の良溶剤としてアセトンを10質量部、紫外線重合開始剤として上記「イルガキュアー184」3質量部を、均一に混合して製膜液(Y1)を調製した。
【0051】
[多孔質層(12)の形成]
厚さ1mmのアクリル樹脂製の基板(10)にスピンコーターを用いて、組成物(X2)を塗布し、紫外線ランプ1にて 4秒間紫外線を照射して塗膜を半硬化させて樹脂層(11)とし、その上にスピンコーターにて製膜液(Y1)を塗工し、多孔質層(12)とする領域(12a)にフォトマスクを通して紫外線ランプ2により紫外線を40秒照射して該領域(12a)の製膜液(Y1)の塗膜(12)を硬化させ、n−ヘキサンで貧溶剤(R)を洗浄除去して多孔質層(12)を形成した。
【0052】
[流路となる溝の形成]
上記多孔質層(12)が形成された基板(10)の上に、バーコーターを用いて組成物(X1)を塗工し、第一流路(1)、第二流路(2)、及び第三流路(6)と成すべき部分以外の部分にフォトマスクを通して紫外線ランプ2による紫外線照射を120秒行って組成物(X1)の半硬化塗膜(13)を形成し、非照射部分の未硬化の前記組成物(X1)をエタノールで除去して、第一流路(1)、第二流路(2)、第三流路(6)および分岐部(3)となる溝を形成した。このとき、第二流路(2)が多孔質層形成領域(12a)とが重なった部分(6)の底面には多孔質層(12)が露出した状態となり、それ以外の多孔質層形成領域(12a)における多孔質層は組成物(X1)が充填されて硬化した。さらに、弁(4)となす部分のみに、フォトマスクを通して紫外線ランプ1により紫外線を120秒照射して硬化させた。
【0053】
[プローブDNAの固定]
(アミノ基の注入)
上記工程2で作製した溝に5質量%ポリアリルアミン(分子量15000、日東紡株式会社製)水溶液を接触させ、60℃、1時間反応させた(ポリアリルアミン中の一部のアミノ基を多孔質層中のエポキシ基と反応させた)後、流水で15分洗浄して、多孔質層へのアミノ基の注入を行った。
【0054】
(アルデヒド基の注入)
上記アミノ基を注入した後、支持体ごと5質量%のグルタルアルデヒド(和光純薬工業株式会社製)水溶液中に浸漬し、50℃に2時間保つことによって、ポリアリルアミンのほぼ全てのアミノ基をグルタルアルデヒドの一方のアルデヒド基と反応させた。その後、流水で10分洗浄して、多孔質層へのアルデヒド基を注入した。
【0055】
(DNAの固定)
上記アルデヒド基を注入した溝に、5’末端にアミノ修飾したDNA(N0と称する)(長さ20塩基、エスペックオリゴサービス株式会社製)水溶液(濃度50μM)を2μl滴下して、湿度100%、50℃にて15時間保つことにより、DNA(N0)の末端アミノ基を多孔質層のアルデヒド基と反応させた後、0.2質量%のテトラヒドロ硼酸ナトリウム水溶液中に入れ、5分間還元反応させ、次いで、0.2×SSC/0.1%SDS溶液でリンスし、次に、0.2×SSCと蒸留水でリンスして、自然乾燥して、第二流路(2)及び分岐部(3)となる溝の底面の多孔質層(12)にプローブDNAとしてDNA(N0)を固定した。(ここで、0.2×SSCは0.03M NaCl,3mMクエン酸ナトリウム水溶液であり、0.1%SDSは0.1質量%ドデシル硫酸ナトリウム水溶液である。)
【0056】
[蓋(14)の固着]
前記組成物(X2)を、片面がコロナ放電処理された厚さ30μmの2軸延伸ポリプロピレンシート(二村化学株式会社製)を一時的な支持体(図示略)の上に、バーコーターを用いて塗工し、紫外線ランプ1により紫外線を2秒照射し、前記組成物の半硬化塗膜(14)を形成し、弁(4)となす部分のみに、フォトマスクを通して紫外線ランプ1により紫外線を6秒照射して硬化させて、蓋用部材を作製した。
上記蓋用部材を前記溝を有する部材の溝形成面に、弁(4)となす部分を合わせて張り合わせ、紫外線ランプ1により紫外線を40秒照射して完全に硬化させて蓋(14)を固着した。但し、この時、弁(4)の部分は溝雅兄制された部材と蓋となる部材は接触しているが固着していない弁(4)が形成された。次いで、前記一時的な支持体を剥離除去して、毛細管状の第一流路(1)、第二流路(2)、第三流路(6)、分岐部(3)、弁(4)、及び第三流路接続部(8)を有するマイクロ流体デバイスを形成した。
【0057】
[その他の構造の形成]
この後、上記蓋(14)を貫通し第一流路(1)、第二流路(2)及び第三流路(6)の各端部に通じる直径0.5mmの孔(21)(22)(23)(24)を、ドリルを使用して形成し、各孔にルアーフィッティング(25)(26)(27)(28)を接着して接続部(25)(26)(27)(28)と成した。
このマイクロ流体デバイスの、接続部(25)と分岐部(3)との間の第一流路(1)を圧迫部(5a)とされており、分岐部(3)と接続部(26)との間の第一流路(1)を圧迫部(5)(5b)とされている。また、分岐部(3)から接続部(27)に至る流路は第二流路(2)とされ、該第二流路が多孔質層形成部範囲(12a)と重なる部分である長さ200mmの範囲は底面にDNAが固定された多孔質層(12)が露出しており、この範囲をアフィニティー・クロマトグラフィーの分離用キャピラリーとされている。そして、該分離用キャピラリーの接続口(27)側の透明部分が蛍光測定部(8)とされている。さらに、接続部(28)を基点とする第三流路(6)が弁(4)の部分で第二流路(2)に接続されている。以上のようにして、マイクロ流体デバイス(D1)を作製した。
【0058】
[流路の構造観察]
流路の断面を走査型電子顕微鏡にて観察したところ、流路は全て幅が約200μmであり、 第一流路(1)、第二流路(2)、第三流路(6)の深さは全て約30μm〔多孔質層(12)が形成された第二流路部分は多孔質層の厚みを含む〕で、第二流路のクロマト用伽歩ラリーとして使用する名川200mmの部分には、底面に厚み約5μmの多孔質層(12)が形成されていた。弁(4)を構成している、底面と天井が接触しているが固着していない部分の寸法は、幅、長さ共に約250μmであった。また、基板(10)の厚みは1mm、樹脂層(11)の厚みは10μm、樹脂層(13)の厚みは30μm、蓋(14)となる樹脂層(14)の厚みは100μmであった。
【0059】
[試料の調製]
(プローブDNAと相補的なDNA試料)
5’末端を蛍光色素FITCにて修飾し、プローブDNA(N0)に相補的な塩基配列を持つ長さ20塩基のDNA(F0と称する)(エスペックオリゴサービス株式会社製、濃度500μM)を0.2×SSC溶液で希釈して、濃度0.3μMのクロマトグラフィー測定用試料F0とした。
【0060】
(プローブDNAと一塩基ミスマッチを有するDNA試料)
DNAが、プローブDNA(N0)と1塩基ミスマッチとなる塩基配列を有するDNA(F1と称する)であること以外は、試料F0と同様にして試料F1を調製した。
【0061】
[試料注入試験]
〔試料F0のクロマトグラフィー〕
マイクロ流体デバイス(D1)を40℃に温度調節されたヒートブロック上に固定し、第一流路(1)の接続口(25)にマイクロシリンジポンプNo.1(図示略)を、また、第三流路(6)の接続口(28)にマイクロシリンジポンプNo.2(図示略)を接続し、シリンジポンプNo.2(図示略)から緩衝溶液(0.2×SSC)を2μl/分で送液した。第三流路(6)及び第二流路(2)に該緩衝溶液が充満した時点で、接続口(35)のルアーフィッティングをリザーバタンクとして使用し、その中にピペットで試料20μlを注入し、シリンジポンプNo.1(図示略)を3μl/分で吸引し、試料溶液が分岐部(3)及び圧迫部(5a)(5)(5b)を通過した時点で、硬質ゴムによる押圧部材(図示略)によって圧迫部(5a)(5b)を圧迫して該2箇所で第一流路(1)を遮断し、その状態を維持したまま直ちに圧迫部(5)を圧迫すると、微量の試料溶液が分岐部(3)から弁(4)を通過して、第二流路(2)にパルス状に注入された。その後、圧迫部(6a)(6b)(6c)の押圧を解除した。以上の押圧操作は全行程を約0.3秒で行った。
【0062】
シリンジポンプNo.1(図示略)を停止し、その後も引き続いてシリンジポンプNo.2(図示略)から、緩衝溶液を2μl/分で送液し、ニコン製蛍光実体顕微鏡を用いて、第二流路(2)の測定部(8)における蛍光強度変化を測定した。その結果、約65秒にピークを持つクロマトグラムが得られた。また、該クロマトグラムのピーク面積と検量線から、試料注入量は約5nlと計算された。
【0063】
〔試料F1のクロマトグラフィー〕
試料として試料F1を用いたこと以外は上記試料F0の場合と同様なクロマトグラフィー測定を行ったところ、約51秒にピークを持つクロマトグラムが得られた。また、該クロマトグラムのピーク面積と検量線から、試料注入量は約5nlと計算された。
【図面の簡単な説明】
【0064】
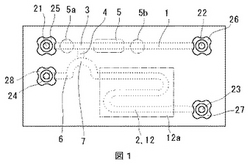
【図1】実施例に使用した本発明のマイクロ流体デバイスの平面図模式図である。
【図2】実施例に使用した本発明のマイクロ流体デバイスの側面図模式図である。
【符号の説明】
【0065】
1 第一流路
2 第二流路
3 分岐部
4 弁
5、5a、5b 圧迫部
6 第三流路
7 第三流路接続部
8 測定部
10 基板
11 樹脂層
12 多孔質層
12a 多孔質層形成領域
13 樹脂層
14 蓋、樹脂層
21、22、23、24 孔
25、26、27、28 ルアーフィッティング、接続部
【技術分野】
【0001】
本発明は、マイクロ流体デバイス内に組み込まれた、又はマイクロ流体デバイス外に接続された機構に、極微量の試料を小さなスポットとして、又は極短時間にパルス状に注入することが出来るマイクロ流体デバイス、および、微量の流体の注入方法に関する。
【背景技術】
【0002】
マイクロ流体デバイスは、内部に有する微細な毛細管状の流路中で反応や分析を行うデバイスであり、マイクロ流体デバイスを使用することにより、反応や分析の迅速化、必要試料量の減少、省資源・省エネルギー、さらには廃棄物の減少が可能となる。このようなマイクロ流体デバイスを使用して、例えば、マイクロ電気泳動分析、マイクロクロマトグラフィー分析、マススペクトル分析の試料の前処理など、医療診断、生化学分析、化学分析の方面で微量の試料を分析する試みが行われている。
【0003】
しかしながら、マイクロ流体デバイスのスケールは、従来のポンプ、切り替えバルブ、シリンジ、ピペットなどの試料取り扱い手段や装置に比べて桁違いに小さいため、マイクロ流体デバイスの流路中に極微量の試料を注入することは相当困難であった。例えば、マイクロ・ガスクロマトグラフィー、マイクロ・液体クロマトグラフィー、マイクロ・アフィニティー・クロマトグラフィー、マイクロ・ゲル・パーミエーション・クロマトグラフィーなどのマイクロ・クロマトグラフィー分析においては、短い展開距離で迅速に高分解能の分析を行うためには、試料を短いスポットとして分離カラムに注入する必要があるが、マイクロシリンジやバルブによる流路切り替え法などの従来法による試料注入手段では注入試料の体積が過大になりがちであり、そのため、クロマトグラムのピークの広がりや、テーリングが生じ、良好に分離するためにはカラム長を太く或いは長くする必要があり、分析時間の伸長を招いていた。
【0004】
これを解決する方法として電気泳動分析に於いて、次の方法が試みられている(特許文献1参照。)。即ち、交差部に於いて交差する2本の流路の一方の一端に試料を注入し、該流路の両端に電圧を印加して電気泳動又は電気浸透流にて試料を移送し、試料が前記交差部を通過している時点で該電圧の印加を停止し、次いで、他方の流路の両端に電圧を印加することによって、交差部内の試料のみを他方の流路へ注入する方法である。
しかし、この方法では、分岐部の容積だけの極微量の試料を他方の流路に注入することが可能であるが、電気泳動による試料移送であるため、試料は荷電試料に限られ、また、媒体も電解質媒体に限られるため、ガスクロマトグラフィー、真空系へ試料を注入する質量分析装置、および多くの液体クロマトグラフィーには適用できなかった。
【0005】
また、サンプル分析の装置として、接合する二本のチャネルを有するデバイスを包含する装置が開示されている(特許文献2参照。)。該装置中のデバイスにおいては、デバイス内のチャネルに圧力勾配を適用させて、試料が注入されたチャネルから分離チャネルに試料を配置するものである。しかし、該方法においては、次のような点で、試料注入方法としては不十分なものであった。(1)質量分析装置のような真空系への試料注入は不可能なこと、(2)拡散速度の高い気体試料には適用が難しいこと、(3)試料注入用流路と電気泳動分析用流路の圧力や、その制御のタイミングを精密に行う必要があるため、ポンプやバルブなどの機構が複雑かつ大がかりとなりがちであること、(4)該公知文献にはクロマトグラフィーの試料注入については記載されていないが、本発明者等の検討によれば、二つの流路の圧力を厳密に制御する必要があり、制御装置が大がかりなものに成りがちであること、(5)注入試料がテーリングを生じがちであり、それを抑制するためには、更に複雑な機構や圧力制御操作が必要なこと。
【0006】
【特許文献1】特開平11−271273号公報
【特許文献2】特表2002−542489号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明が解決しようとする課題は、マイクロ流体デバイス内に組み込まれた、又はマイクロ流体デバイス外に接続された機構に、流体試料を注入するデバイスおよびその方法において、荷電試料だけでなく非イオン性試料や気体試料にも適用可能で、非電解質液体媒体中、気体媒体中、または真空系への試料注入が可能であり、試料注入に複雑で大がかりな装置や複雑な制御を要することなく、簡易な操作で、極微量の試料を定量性よく、テーリングも少なく注入することが可能なマイクロ流体デバイス、およびそれを用いた試料注入方法を提供すること。特に、マイクロ・クロマトグラフィーやマイクロ電気泳動分析用マイクロ流体デバイスへの試料注入方法、また、マイクロ流体デバイスに接続された質量分析装置などの分析装置への試料注入方法を提供すること。さらに、上記の機能を有しながら、安価で使い捨て可能なマイクロ流体デバイスを提供すること。
【課題を解決するための手段】
【0008】
本発明者らは、上記の課題を解決すべく鋭意検討した結果、第一流路(1)と、その途中の分岐部(3)にて分岐した第二流路(2)と、分岐部(3)近傍の第二流路(2)中に設けられた弁(4)と、分岐部(3)近傍の第一流路(1)の流路壁にあり、第一流路(1)の外部からの圧力により第一流路(1)の断面積を減少させる圧迫部(5)とを有し、前記弁(4)が常態では閉じており、且つ圧迫部(5)を圧迫することにより開いて第一流路(1)内の流体が第二流路(2)内に流入する弁であるマイクロ流体デバイスにより、上記課題を解決できることを見出し、本発明を完成するに至った。
【発明の効果】
【0009】
本発明のマイクロ流体デバイス及び試料注入方法は、マイクロ流体デバイス内に組み込まれた、又はマイクロ流体デバイス外に接続された機構に、極微量の流体試料を小さなスポットとして、又は極短時間にパルス状に注入することが出来るマイクロ流体デバイス、及びそれを用いた試料注入方法を提供できる。本発明は、荷電試料だけでなく非イオン性試料や気体試料にも適用可能であり、また、電解質液体媒体中への注入だけでなく、非電解質液体媒体中、気体媒体中、または真空系への試料注入が可能であるため、適用範囲が極めて広い。そのため、特に、マイクロ・ガスクロマトグラフィー、マイクロ・液体クロマトグラフィー、マイクロ・アフィニティー・クロマトグラフィー、マイクロ・ゲル・パーミエーション・クロマトグラフフィーなどのマイクロ・クロマトグラフィーの試料注入や、マイクロ流体デバイスに接続された質量分析装置への試料注入に用いると効果的である。
【0010】
また、本発明のマイクロ流体デバイス及び試料注入方法は、試料注入に複雑で大がかりな制御装置や複雑な制御を要せず、簡易な操作で試料を注入することが可能であり、マイクロ・トータル・アナリシス・システム(μ−TAS)に組み込んで使用することが容易である。
【0011】
さらに、本発明のマイクロ流体デバイスは、簡単な構造で容易に製作できるため、安価で使い捨て可能なマイクロ流体デバイスとすることが可能である。
【発明を実施するための最良の形態】
【0012】
以下、本発明について、詳細に説明する。
[マイクロ流体デバイス]
本発明のマイクロ流体デバイスは、部材内部に毛細管状の流路を有するデバイスである。マイクロ流体デバイスは、マイクロ流体デバイス、マイクロ・フルイディック・デバイス、マイクロ・ファブリケイテッド・デバイス、マイクロ流路、ラボ・オン・チップ、又はマイクロ・トータル・アナリシス・システム(μ−TAS)とも呼ばれるものを指し、該流路内で、化学反応、生化学反応、流体の温度変化、濃度調整、分離、測定などを行うデバイスである。
本発明のマイクロ流体デバイスの外形は、板状(柔軟なシート状を含む)、棒状(柔軟なひも状を含む)、チューブ状(毛細管状を含む)、塊状、又は、組み合わせ型マイクロ流体デバイスのコンポーネント(モジュール)となる形状、などの任意の形状であって良い。なかでも形状が板状のものは、製造が容易であり、流路などの構造に高い寸法精度や位置精度を持たせることができ、マイクロ流体デバイスの他の構造と一体化することが容易である上、使用時の温度調節や流路の観測が容易であるため好ましい。
【0013】
本発明のマイクロ流体デバイスを構成する材料は特に限定する必要がなく、例えば、ガラス、水晶等の結晶、シリコンなどの半導体、金属、セラミック、炭素、有機重合体(ポリジメチルシロキサンのように、無機元素を含有するものも含む。)、あるいはこれらの発泡体などを使用できる。また、例えば有機重合体などの上に金属やその他の物質を蒸着した複合材料なども使用できる。但し、後述のように、圧迫部においては、可撓性のある素材を使用する必要がある。なかでも、活性エネルギー線硬化性樹脂を使用すると、各種形状への成形が容易である。
【0014】
本発明のマイクロ流体デバイスは、毛細管状の流路[第一流路(1)と称する]、及び該第一流路(1)の途中の分岐部(3)から分岐した毛細管状の流路[第二流路(2)と称する]を有する。なお、本発明に於いては、特に言及しない限り、「第一流路(1)」は「分岐部(3)」を含むものとして説明する。
【0015】
[第一流路(1)]
第一流路の横断面、即ち、流体の流動方向に直角な断面(以下、該断面を単に「流路断面」と略記する。)の形状は特に限定されないが、矩形、台形、または半円形であることが、製造や内部の観察が容易であり好ましい。
【0016】
流路断面の寸法は任意であるが、幅、深さ共に1〜500μmであることが好ましい。但し、第一流路(1)をマイクロ・キャピラリー・クロマトグラフィー用の分離カラムとして使用する場合には、該流路の幅、深さの少なくとも一方は1〜50μmであことが好ましい。さらに、後述のように、これらの分離カラムが、流路内面の少なくとも一つの面に多孔質層を有するものである場合には、該断面中の任意の点をx、該点xと直線距離で最も近い多孔質層の部分をy、xy間の直線距離をrとし、rが該断面内でとり得る最大距離をrmaxとした際に、該rmaxが1〜50μmの範囲となるように設計することが好ましい。このような寸法とすることにより、流路内を流動する流体に含まれる分離対象物質が流路壁面や多孔質層と十分に相互作用を生じることができるため、高い分離能を実現することが出来る。勿論、流路の断面形状や断面寸法は流路の流れ方向で変化していて良い。
【0017】
但し、第一流路(1)をクロマトグラフィー用や電気泳動分析用の充填カラム或いはモノリス型多孔質カラムとする場合には、上記寸法の制約はなく、第一流路(1)の外部の直径は更に太くても良い。
【0018】
第一流路(1)の長さは任意であり、用途目的に応じて好適な長さをとり得る。例えば第一流路(1)の少なくとも一部をクロマトグラフィー用、或いは電気泳動分析用の分離カラムとして使用する場合には、1mm〜500mmが好ましく、5mm〜200mmが更に好ましい。上記下限以上とすることで、十分な分離能を得ることができ、上記上限以下とすることによって、マイクロ流体デバイスを小形化できる。
【0019】
第一流路(1)の流体の流動方向の形態も任意であり、直線であっても、曲線であってもよい。各流路の端はマイクロ流体デバイス外に連絡する開口部となっていてもよいし、マイクロ流体デバイス外の装置と接続するための配管が接続されていても良く、マイクロ流体デバイス内の他の機構に接続されていても良い。
【0020】
第一流路(1)は、分岐部(3)へ試料を導くための流路として用いることが出来る。第一流路(1)の一端は、試料を注入することが出来れば任意であり、例えば、マイクロ流体デバイス外に開口した開口部や、マイクロ流体デバイス外と連絡する配管が接続された配管接続部であって良いし、マイクロ流体デバイス中の他の機構、例えば貯液層、内部ポンプ、濾過機構、バルブなどに接続されていても良い。また、試料を電気泳動や電気浸透流によって移送する場合には電極を設置することができる。第一流路(1)の他端は任意であり、前記一端と同様の機構の他、試料溶液を吸引するための真空チャンバー、繊維充填型や多孔質型などの液体吸収部でありうる。即ち、前記一端から第一流路(1)に流入した試料溶液は、分岐部(3)を経て、他端から流出するように使用することが出来る。
【0021】
第一流路(1)の一端と分岐部(3)の間(以下、「分岐部(3)の上流側」と称する。)には、クロマトグラフィー用の分離カラムや電気泳動分析用の分離カラムが直列に設けられていてもよい。これらの分離カラムで分離された試料が分岐部(3)を経て移動するように使用することにより、分離された試料が分岐部に来たときに、選択的に第二流路(2)へ注入することが出来る。分離された試料が分岐部(3)に到達したことは、分岐部(3)またはその上流部分を光学的に観測することで判断できる。
【0022】
分岐部(3)と第一流路(1)の他端との間(以下、「分岐部(3)の下流側」と称する。)の第一流路に関しても、上記分岐部(3)の上流側の場合と同様である。例えば、前記のように分岐部(3)の上流側にクロマトグラフィー用の分離カラムなどを設け、分離された試料の内、不要のものを第二流路(2)へ除去し、残された試料を下流側の機構へ注入することも出来る。そのような必要がない場合には、単なる廃液用流路として使用できる。
【0023】
[弁]
本発明のマイクロ流体デバイスにおいては、分岐部(3)において第一流路(1)から分岐した第二流路(2)に、常態、即ち該弁に何らの操作も加えない状態では閉じていて、分岐部側の流路内圧力が一定値以上になると開く弁(以下、このような弁を単に弁(4)と称する)が設けられている。該弁(4)は分岐部(3)に接して設けることが好ましい。これにより、分岐部(3)と弁(4)間の死容積をなくすことが出来、第一流路を流れて分岐部(3)に到達した試料を死容積部分に滞留していた流体で希釈することないため、定量性良く、かつ濃度変化もなく、確実に第二流路(2)へ注入することが出来る。そのため、第一流路(1)の分岐部(3)の上流側に前記分離カラムが設けられている場合には、該弁(4)を分岐部(3)に接して設けることが特に好ましい。また、第二流路(2)にさらに別の流路(以下、第三流路(6)とする。)が設けられる場合には、該弁(4)は、第三流路(6)の近傍であることが好ましく、第三流路(6)接続部に接していることがさらに好ましい。この場合も、弁(4)と通過した流体を、該弁(4)と第三流路(6)接続部との間の第二流路(2)の死容積部分に滞留していた流体で希釈することないため、定量性良く、かつ濃度変化もなく、確実に第二流路(2)へ注入することが出来る。
【0024】
弁(4)は、常態では閉じていて、分岐部側の圧力が一定値以上で開けば、他の状態での動作は任意である。例えば、(a)分岐部(3)とは反対の側[第二流路(2)側と称する]の圧力がいくら高くなっても開かない逆止弁、(b)第二流路(2)側の圧力が一定値以上になると開くタイプのバルブ、(c)第二流路(2)側の圧力が下がることによって両側の圧力差が一定値以上になると開くタイプのバルブ、(d)第二流路(2)側の圧力がいくら低くなっても、開かないタイプのバルブ、などであって良い。これらは、用途目的に応じて選択できる。例えば、第二流路(2)が減圧される用途、例えば質量分析装置に接続される場合には、第二流路(2)側の圧力がいくら低くなっても開かないタイプのバルブとすることが必要である。
【0025】
弁(4)の構造は任意であり、例えば、本発明者らによる特開2003-139660に開示されているような、流路の途上に堰状構造が設けられて該流路は該部分で途切れており、該堰状構造は、堰の上面と流路壁が接触しているが接着していないため、常態では閉じていて、該堰状構造のいずれか一方又は両方の側の圧力が一定値以上になると開くが、いずれか一方又は両方の側の圧力がいくら低くなっても開かないタイプの弁を使用できる。
【0026】
[圧迫部]
本発明のマイクロ流体デバイスにおいては、第一流路(1)の分岐部(3)近傍に、流路壁を第一流路外から圧迫すると第一流路(1)の断面積が減少するような可撓性の材料で形成された圧迫部(5)が設けられている。該圧迫部(5)を圧迫することによって分岐部内の流体の圧力を高め、弁(4)を通して流体を第二流路へ注入することが出来る。
【0027】
圧迫部(5)を設ける領域としては、概ね分岐部(3)の領域のみの範囲であっても、分岐部(3)を含む広い範囲であっても良い。概ね分岐部(3)の領域のみに設ける場合には、該分岐部(3)において第一流路(1)は幅広となっていることが好ましい。幅広とすることで、該部分を圧迫したとき、分岐部の圧力を効果的に高めることができ、流体を弁(4)を通過して注入することが容易になる。
【0028】
また、圧迫部(5)が第一流路(1)の分岐部(3)を含む広い範囲に設けられている場合には、該広い範囲を圧迫することで、該圧迫部分の流路から逃げる液体の圧力損失によって、分岐部の圧力を効果的に高めることができ、流体を弁(4)を通して容易に注入することが出来るため好ましい。
【0029】
圧迫部(5)は、分岐部(3)をまたぐ両側の2つの圧迫部(5a)(5b)とその間の圧迫部(5)から成ることが好ましい。該圧迫部(5)を圧迫する際には、圧迫部(5a)(5b)を先に圧迫し、該圧迫を維持したまま、圧迫部(5)を圧迫する方法によって、確実にかつ定量的に試料を注入することが容易となる。圧迫部(5)は分岐部(3)に限定されず、その近傍であればよい。
【0030】
第一流路(1)の圧迫部(5)における断面の周囲を構成するいずれかの部分が可撓性材料で形成されるが、可撓性材料で形成される部分は任意であり、流路の底面、側壁、天井面の少なくとも一つであり得る。但し、最も柔軟な部分を直接圧迫する必要はなく、例えば両側壁が柔軟な材料で形成された第一流路(1)を可撓性ではあるが側壁より硬質の材料で形成された天井部から押圧することで、両側壁が変形しても良い。
【0031】
可撓性材料は任意であるが、架橋重合体であることが、クリープが少なく、繰り返し使用に耐えるため好ましい。可撓性材料は、引っ張り弾性率にして100GPa以下が好ましく、10GPa以下がさらに好ましく、1GPa以下が最も好ましい。引っ張り弾性率の下限は、自己保持できれば任意であるが、流路の耐圧性や取り扱いの容易さの面から、1KPa以上が好ましく、10KPa以上がより好ましい。引っ張り弾性率が10〜100GPaの素材は、圧迫部の面積を比較的大きく採り、厚みを薄くすることで使用できる。本発明に使用できる可撓性材料としては、有機重合体、金属、ガラス、結晶などを例示できるが、有機重合体が、引っ張り弾性率の選択範囲が広く、破断伸び率も大きいため好ましい。特に活性エネルギー線硬化性樹脂を使用した場合には、各種成形が容易であるため好ましい。
【0032】
圧迫部を機械的に押圧して圧迫する場合には、圧迫部の外表面に凸状構造を設けることも好ましい。これにより、平らな接触面を持つ圧迫用部材を用いて、該凸状構造を含む比較的広い範囲を圧迫すると、選択的に圧迫部が圧迫されるため、圧迫位置の正確な位置合わせが不要となる。
【0033】
また、圧迫機構にかかわらず、2つの圧迫部(5a)(5b)において、第一流路の高さ(即ち、圧迫により減少する方向の寸法)を他の部分より小さくすることが好ましい。このような構造により、圧迫に際し、該部分において流路が確実に閉鎖されることにより、注入量の定量性を向上させることができる。このような構造は、例えば、該部分において、第一流路の底を高くした構造、及び/又は、天井を低くした構造により実施できる。
【0034】
「第二流路」
本発明のマイクロ流体デバイスは、第一流路(1)の途中の分岐部(3)から分岐した毛細管状の流路[第二流路(2)と称する]を有する。第二流路の断面形状、寸法や流路方向の形態、長さに関しては第一流路(1)の場合と同様である。第二流路(2)をマイクロ・クロマトグラフィー用等の分離カラムとして使用する場合にも、第一流路(1)の場合と同様である。
【0035】
第二流路(2)は、流体の流動方向の形態も任意であり、直線であっても、曲線であってもよい。該流路の端はマイクロ流体デバイス外に連絡する開口部となっていてもよく、マイクロ流体デバイス外の装置と接続するための配管が接続されていても良く、マイクロ流体デバイス内の他の機構に接続されていても良い。
【0036】
第二流路(2)は、分岐部(3)から弁(4)を通して極微量の試料が注入される流路であり、反応や分析などを行うための流路として用いることが出来る。例えば、第二流路(2)は、該マイクロ流体デバイス内に設けられたクロマトグラフィー等の分離カラムとして使用されることも好ましい。或いは、該マイクロ流体デバイス外に設けられたクロマトグラフィー装置、電気泳動分析装置、質量分析装置、光学的その他の検出装置に接続されることが好ましい。また、第二流路は真空であっても良く、この場合には、第二流路へ注入された液体は直ちに気化して第二流路中を移送される。
【0037】
第二流路(2)には、他の流路(第三流路(6))が接続されていることも好ましい。第二流路(2)に、該マイクロ流体デバイス内に設けられたクロマトグラフィー等の分離カラムが接続されている場合には、該第三流路(6)の接続部(7)は分離カラム部より弁(4)側に設けられる。接続部(7)は前記弁(4)のなるべく近傍に設けることが、試料注入の定量性が増すため好ましい。第三流路(6)は、クロマトグラフィーの展開液注入路、電気泳動分析の導電路、第二流路へ注入された試料と混合すべき液体の注入路、などとして用いられる。
【0038】
本発明の試料注入方法は、本発明に成るマイクロ流体デバイスを用い、該マイクロ流体デバイスの第一流路(1)に試料を流し、前記圧迫部(5)を圧迫することによって前記第一流路(1)内の圧力を上昇させて、前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする。本発明の試料注入方法に適用できる試料の流体は任意であり、液体、超臨界流体、気体であり得るが、液体であることが、定量性が向上し好ましい。液体試料の種類は任意であり、単一液体、混合液体、溶液、分散液であり得る。溶質は任意であり、化学物質、生化学物質、有機物質、無機物質、揮発性物質、不揮発性物質、ノニオン性物質、カチオン性物質、アニオン性物質、両性イオン性物質、親水性物質、疎水性物質、両新馬異性物質、などであり得るし、溶媒は電解質、非電解質であり得る。
【0039】
圧迫する位置〔圧迫部(5)〕は分岐部(3)であっても良いし、分岐部(3)を含む第一流路(1)の広い範囲であっても良い。このとき、該圧迫部の流路から逃げる液体の圧力損失によって、分岐部の圧力を効果的に高めることができ、流体を弁(4)を通して容易に注入することが出来る。
【0040】
圧迫する位置〔圧迫部(5)〕は、分岐部(3)をまたぐ両側の2つの圧迫部(5a)(5b)とその間の圧迫部(5)であることが好ましい。該圧迫部(5)を圧迫する際には、圧迫部(5a)(5b)を先に圧迫し、該圧迫を維持したまま、圧迫部(5)を圧迫する方法によって、確実にかつ定量的に試料を注入することが容易となる。圧迫部(5)は分岐部(3)に限定されず、その近傍であればよい。
【0041】
圧迫方法は任意であり、アクチュエーターなどによるマイクロ流体デバイス外からの機械的な押圧、マイクロ流体デバイスの流路壁に接して設置した、または流路壁を構成するピエゾ素子による圧迫、マイクロ流体デバイスの流路壁に固定された強磁性体の磁力による駆動、該圧迫部における流路壁の、第一流路(1)と反対側にもうけられた圧力室への流体の導入による加圧、などを例示できる。これらの中で、マイクロ流体デバイス外からの機械的な押圧が、構造が単純であり、使い捨て可能なマイクロ流体デバイスを容易に作成できること、および、第一流路(1)や分岐部(3)の容積を小さくすることが容易なため、分岐部に供給される試料溶液が少ない場合にも適用可能であり、好ましい。それに次いで、強磁性体やピエゾ素子による迫が好ましい。
【0042】
本発明の試料注入方法は、クロマトグラフィーや電気泳動によって分離された試料スポットを選択的に第二流路(2)へ注入する方法であることも好ましい。この方法によって、例えば、該試料スポットを採取したり、質量分析装置などの分析装置へ注入することが出来る。或いは、該試料スポットの化合物を第二流路における反応に供することが出来る。この場合には、第一流路(1)の分岐部(3)より上流側にこれらの分離用キャピラリーや分離用カラムを設け、分離された試料スポットが分離部(4)に来たときに圧迫を行って第二流路へ注入する。このとき、第一流路(1)の前記分岐部(3)及び/又は前記分離カラムと前記分岐部(3)の間の部分に、第一流路(1)内の試料を光学的に観察する測定用の窓を設けたマイクロ流体デバイスを使用し、該窓を光学的に観察しつつ前記圧迫部(5)を圧迫することにより前記試料の一部を第二流路(2)へ注入することも好ましい。
上記の試料注入方法は、クロマトグラフィーや電気泳動によって分離された試料スポットを選択的に第二流路(2)へ除去し、残余を第一流路の分岐部より下流側へ注入する方法としても利用できる。この方法によって、例えば、特定の試料スポットを除去した試料を採取したり、該試料スポットを除去した試料を第一流路の下流側部における、或いは第一流路から流出させて反応に供することが出来る。
【0043】
本発明の試料注入方法は、クロマトグラフへの微量試料の注入方法であることも好ましい。この場合には、前記第二流路にこれらの分離用キャピラリーや分離用カラムを設けた、或いは接続したマイクロ流体デバイスを用い、注入すべき試料を第一流路に流して、その一部を第二流路に注入する。
【0044】
本発明の試料注入方法によれば、使用するマイクロ流体デバイス中の流路径や、圧迫部(5a)、(5b)の位置等の設計により、微少量、特に0.1pl(但し、pl=nm3)〜300nl(但し、nl=pm3)、さらに好ましくは1pl〜30nl、最も好ましくは10pl〜10nl程度の微少量の試料を定量的に注入することも可能である。さらに、圧迫部の圧迫操作をパルス的に行うことによって、複雑な制御を行わなくても、上記微少量の試料を最小のテーリングでもってパルス的に注入することが可能である。
【実施例】
【0045】
以下、実施例を用いて本発明を更に詳しく説明するが、本発明は、以下の実施例の範囲に限定されるものではない。本実施例における紫外線照射、および蛍光特性測定の方法を以下に示す。
【0046】
(紫外線ランプ1による照射)
3000Wメタルハライドランプを光源とするアイグラフィックス株式会社製のUE031−353CHC型UV照射装置を用い、365nmにおける紫外線強度が40mW/cm2の紫外線を特に指定が無い限り室温、窒素雰囲気中で照射した。
【0047】
(紫外線ランプ2による照射)
250W高圧水銀ランプを光源とするウシオ電機株式会社製のマルチライト250Wシリーズ露光装置用光源ユニットを用い、365nmにおける紫外線強度が50mW/cm2の紫外線を、特に指定が無い限り室温、窒素雰囲気中で照射した。
【0048】
(実施例1)
[組成物(X1)の調製]
エネルギー線重合性化合物(a)として平均分子量2000の3官能ウレタンアクリレートオリゴマー「ユニディックV−4263」(大日本インキ化学工業株式会社製)70部、ヘキサンジオールジアクリレート「ニューフロンティアHDDA」(第一工業製薬株式会社製)30部、光重合開始剤として1−ヒドロキシシクロヘキシルフェニルケトン「イルガキュアー184」(チバガイギー社製)3部、及び重合遅延剤として2,4−ジフェニル−4−メチル−1−ペンテン(関東化学株式会社製)0.5部を混合して、組成物(X1)を調製した。
【0049】
[組成物(X2)の調製]
エネルギー線重合性化合物として上記「ユニディックV−4263」80部、上記「ニューフロンティアHDDA」20部、光重合開始剤として上記「イルガキュアー184」2部を混合して、蓋用組成物を調製した。
【0050】
製膜液(Y1)の調製]
エネルギー線重合性化合物(b)として、上記「ユニディックV−4263」72質量部、ジシクロペンタニルジアクリレート「R−684」(日本化薬株式会社製)18質量部、メタクリル酸グリシジル(和光純薬工業株式会社製)10質量部、貧溶剤(R)としてデカン酸メチル(和光純薬工業株式会社製)を180質量部、揮発性の良溶剤としてアセトンを10質量部、紫外線重合開始剤として上記「イルガキュアー184」3質量部を、均一に混合して製膜液(Y1)を調製した。
【0051】
[多孔質層(12)の形成]
厚さ1mmのアクリル樹脂製の基板(10)にスピンコーターを用いて、組成物(X2)を塗布し、紫外線ランプ1にて 4秒間紫外線を照射して塗膜を半硬化させて樹脂層(11)とし、その上にスピンコーターにて製膜液(Y1)を塗工し、多孔質層(12)とする領域(12a)にフォトマスクを通して紫外線ランプ2により紫外線を40秒照射して該領域(12a)の製膜液(Y1)の塗膜(12)を硬化させ、n−ヘキサンで貧溶剤(R)を洗浄除去して多孔質層(12)を形成した。
【0052】
[流路となる溝の形成]
上記多孔質層(12)が形成された基板(10)の上に、バーコーターを用いて組成物(X1)を塗工し、第一流路(1)、第二流路(2)、及び第三流路(6)と成すべき部分以外の部分にフォトマスクを通して紫外線ランプ2による紫外線照射を120秒行って組成物(X1)の半硬化塗膜(13)を形成し、非照射部分の未硬化の前記組成物(X1)をエタノールで除去して、第一流路(1)、第二流路(2)、第三流路(6)および分岐部(3)となる溝を形成した。このとき、第二流路(2)が多孔質層形成領域(12a)とが重なった部分(6)の底面には多孔質層(12)が露出した状態となり、それ以外の多孔質層形成領域(12a)における多孔質層は組成物(X1)が充填されて硬化した。さらに、弁(4)となす部分のみに、フォトマスクを通して紫外線ランプ1により紫外線を120秒照射して硬化させた。
【0053】
[プローブDNAの固定]
(アミノ基の注入)
上記工程2で作製した溝に5質量%ポリアリルアミン(分子量15000、日東紡株式会社製)水溶液を接触させ、60℃、1時間反応させた(ポリアリルアミン中の一部のアミノ基を多孔質層中のエポキシ基と反応させた)後、流水で15分洗浄して、多孔質層へのアミノ基の注入を行った。
【0054】
(アルデヒド基の注入)
上記アミノ基を注入した後、支持体ごと5質量%のグルタルアルデヒド(和光純薬工業株式会社製)水溶液中に浸漬し、50℃に2時間保つことによって、ポリアリルアミンのほぼ全てのアミノ基をグルタルアルデヒドの一方のアルデヒド基と反応させた。その後、流水で10分洗浄して、多孔質層へのアルデヒド基を注入した。
【0055】
(DNAの固定)
上記アルデヒド基を注入した溝に、5’末端にアミノ修飾したDNA(N0と称する)(長さ20塩基、エスペックオリゴサービス株式会社製)水溶液(濃度50μM)を2μl滴下して、湿度100%、50℃にて15時間保つことにより、DNA(N0)の末端アミノ基を多孔質層のアルデヒド基と反応させた後、0.2質量%のテトラヒドロ硼酸ナトリウム水溶液中に入れ、5分間還元反応させ、次いで、0.2×SSC/0.1%SDS溶液でリンスし、次に、0.2×SSCと蒸留水でリンスして、自然乾燥して、第二流路(2)及び分岐部(3)となる溝の底面の多孔質層(12)にプローブDNAとしてDNA(N0)を固定した。(ここで、0.2×SSCは0.03M NaCl,3mMクエン酸ナトリウム水溶液であり、0.1%SDSは0.1質量%ドデシル硫酸ナトリウム水溶液である。)
【0056】
[蓋(14)の固着]
前記組成物(X2)を、片面がコロナ放電処理された厚さ30μmの2軸延伸ポリプロピレンシート(二村化学株式会社製)を一時的な支持体(図示略)の上に、バーコーターを用いて塗工し、紫外線ランプ1により紫外線を2秒照射し、前記組成物の半硬化塗膜(14)を形成し、弁(4)となす部分のみに、フォトマスクを通して紫外線ランプ1により紫外線を6秒照射して硬化させて、蓋用部材を作製した。
上記蓋用部材を前記溝を有する部材の溝形成面に、弁(4)となす部分を合わせて張り合わせ、紫外線ランプ1により紫外線を40秒照射して完全に硬化させて蓋(14)を固着した。但し、この時、弁(4)の部分は溝雅兄制された部材と蓋となる部材は接触しているが固着していない弁(4)が形成された。次いで、前記一時的な支持体を剥離除去して、毛細管状の第一流路(1)、第二流路(2)、第三流路(6)、分岐部(3)、弁(4)、及び第三流路接続部(8)を有するマイクロ流体デバイスを形成した。
【0057】
[その他の構造の形成]
この後、上記蓋(14)を貫通し第一流路(1)、第二流路(2)及び第三流路(6)の各端部に通じる直径0.5mmの孔(21)(22)(23)(24)を、ドリルを使用して形成し、各孔にルアーフィッティング(25)(26)(27)(28)を接着して接続部(25)(26)(27)(28)と成した。
このマイクロ流体デバイスの、接続部(25)と分岐部(3)との間の第一流路(1)を圧迫部(5a)とされており、分岐部(3)と接続部(26)との間の第一流路(1)を圧迫部(5)(5b)とされている。また、分岐部(3)から接続部(27)に至る流路は第二流路(2)とされ、該第二流路が多孔質層形成部範囲(12a)と重なる部分である長さ200mmの範囲は底面にDNAが固定された多孔質層(12)が露出しており、この範囲をアフィニティー・クロマトグラフィーの分離用キャピラリーとされている。そして、該分離用キャピラリーの接続口(27)側の透明部分が蛍光測定部(8)とされている。さらに、接続部(28)を基点とする第三流路(6)が弁(4)の部分で第二流路(2)に接続されている。以上のようにして、マイクロ流体デバイス(D1)を作製した。
【0058】
[流路の構造観察]
流路の断面を走査型電子顕微鏡にて観察したところ、流路は全て幅が約200μmであり、 第一流路(1)、第二流路(2)、第三流路(6)の深さは全て約30μm〔多孔質層(12)が形成された第二流路部分は多孔質層の厚みを含む〕で、第二流路のクロマト用伽歩ラリーとして使用する名川200mmの部分には、底面に厚み約5μmの多孔質層(12)が形成されていた。弁(4)を構成している、底面と天井が接触しているが固着していない部分の寸法は、幅、長さ共に約250μmであった。また、基板(10)の厚みは1mm、樹脂層(11)の厚みは10μm、樹脂層(13)の厚みは30μm、蓋(14)となる樹脂層(14)の厚みは100μmであった。
【0059】
[試料の調製]
(プローブDNAと相補的なDNA試料)
5’末端を蛍光色素FITCにて修飾し、プローブDNA(N0)に相補的な塩基配列を持つ長さ20塩基のDNA(F0と称する)(エスペックオリゴサービス株式会社製、濃度500μM)を0.2×SSC溶液で希釈して、濃度0.3μMのクロマトグラフィー測定用試料F0とした。
【0060】
(プローブDNAと一塩基ミスマッチを有するDNA試料)
DNAが、プローブDNA(N0)と1塩基ミスマッチとなる塩基配列を有するDNA(F1と称する)であること以外は、試料F0と同様にして試料F1を調製した。
【0061】
[試料注入試験]
〔試料F0のクロマトグラフィー〕
マイクロ流体デバイス(D1)を40℃に温度調節されたヒートブロック上に固定し、第一流路(1)の接続口(25)にマイクロシリンジポンプNo.1(図示略)を、また、第三流路(6)の接続口(28)にマイクロシリンジポンプNo.2(図示略)を接続し、シリンジポンプNo.2(図示略)から緩衝溶液(0.2×SSC)を2μl/分で送液した。第三流路(6)及び第二流路(2)に該緩衝溶液が充満した時点で、接続口(35)のルアーフィッティングをリザーバタンクとして使用し、その中にピペットで試料20μlを注入し、シリンジポンプNo.1(図示略)を3μl/分で吸引し、試料溶液が分岐部(3)及び圧迫部(5a)(5)(5b)を通過した時点で、硬質ゴムによる押圧部材(図示略)によって圧迫部(5a)(5b)を圧迫して該2箇所で第一流路(1)を遮断し、その状態を維持したまま直ちに圧迫部(5)を圧迫すると、微量の試料溶液が分岐部(3)から弁(4)を通過して、第二流路(2)にパルス状に注入された。その後、圧迫部(6a)(6b)(6c)の押圧を解除した。以上の押圧操作は全行程を約0.3秒で行った。
【0062】
シリンジポンプNo.1(図示略)を停止し、その後も引き続いてシリンジポンプNo.2(図示略)から、緩衝溶液を2μl/分で送液し、ニコン製蛍光実体顕微鏡を用いて、第二流路(2)の測定部(8)における蛍光強度変化を測定した。その結果、約65秒にピークを持つクロマトグラムが得られた。また、該クロマトグラムのピーク面積と検量線から、試料注入量は約5nlと計算された。
【0063】
〔試料F1のクロマトグラフィー〕
試料として試料F1を用いたこと以外は上記試料F0の場合と同様なクロマトグラフィー測定を行ったところ、約51秒にピークを持つクロマトグラムが得られた。また、該クロマトグラムのピーク面積と検量線から、試料注入量は約5nlと計算された。
【図面の簡単な説明】
【0064】
【図1】実施例に使用した本発明のマイクロ流体デバイスの平面図模式図である。
【図2】実施例に使用した本発明のマイクロ流体デバイスの側面図模式図である。
【符号の説明】
【0065】
1 第一流路
2 第二流路
3 分岐部
4 弁
5、5a、5b 圧迫部
6 第三流路
7 第三流路接続部
8 測定部
10 基板
11 樹脂層
12 多孔質層
12a 多孔質層形成領域
13 樹脂層
14 蓋、樹脂層
21、22、23、24 孔
25、26、27、28 ルアーフィッティング、接続部
【特許請求の範囲】
【請求項1】
第一流路(1)と、その途中の分岐部(3)にて分岐した第二流路(2)と、分岐部(3)近傍の第二流路(2)中に設けられた弁(4)と、分岐部(3)近傍の第一流路(1)の流路壁にあり、第一流路(1)の外部からの圧力により第一流路(1)の断面積を減少させる圧迫部(5)とを有し、前記弁(4)が常態では閉じており、且つ圧迫部(5)を圧迫することにより開いて第一流路(1)内の流体が第二流路(2)内に流入する弁であるマイクロ流体デバイス。
【請求項2】
前記弁(4)が、前記第一流路(1)内の流体の減圧により開かない弁である請求項1に記載のマイクロ流体デバイス。
【請求項3】
前記第一流路(1)の分岐部(3)を挟む両側に、第一流路(1)の外部からの圧力により第一流路(1)の断面積を減少させる圧迫部(5a)および圧迫部(5b)が設けられた請求項1に記載のマイクロ流体デバイス。
【請求項4】
前記第二流路(2)の途中に、第三流路(6)が接続された請求項1に記載のマイクロ流体デバイス。
【請求項5】
前記第二流路(2)の前記第三流路(6)の接続部より下流側にクロマトグラフィー用分離カラムが直列に接続して設けられた請求項4に記載のマイクロ流体デバイス。
【請求項6】
前記第二流路(2)に質量分析装置への接続口が設けられた請求項1に記載のマイクロ流体デバイス。
【請求項7】
前記第一流路(1)の途上に直列にクロマトグラフィー用分離カラムが接続して設けられた請求項7に記載のマイクロ流体デバイス。
【請求項8】
前記第一流路(1)の前記分岐部(3)近傍に、前記第一流路(1)内の試料を光学的に観察する測定用の窓が設けられた請求項7に記載のマイクロ流体デバイス。
【請求項9】
請求項1に記載のマイクロ流体デバイスを用い、該マイクロ流体デバイスの第一流路(1)に試料を流し、前記圧迫部(5)を圧迫することによって前記第一流路(1)内の圧力を上昇させて、前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする微量試料の注入方法。
【請求項10】
請求項3に記載のマイクロ流体デバイスを使用し、前記分岐部(3)の両側の前記圧迫部(5’)、(5’’)を圧迫することにより前記第一流路(1)内の圧力を上昇させて、前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする微量試料の注入方法。
【請求項11】
請求項8に記載のマイクロ流体デバイスを使用し、前記分離カラムから前記分岐部(3)方向に液体を流し、前記分岐部(3)及び/又は前記分離カラムと前記分岐部(3)の間の部分を光学的に観察しつつ前記圧迫部(5)を圧迫することにより前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする微量試料の注入方法。
【請求項1】
第一流路(1)と、その途中の分岐部(3)にて分岐した第二流路(2)と、分岐部(3)近傍の第二流路(2)中に設けられた弁(4)と、分岐部(3)近傍の第一流路(1)の流路壁にあり、第一流路(1)の外部からの圧力により第一流路(1)の断面積を減少させる圧迫部(5)とを有し、前記弁(4)が常態では閉じており、且つ圧迫部(5)を圧迫することにより開いて第一流路(1)内の流体が第二流路(2)内に流入する弁であるマイクロ流体デバイス。
【請求項2】
前記弁(4)が、前記第一流路(1)内の流体の減圧により開かない弁である請求項1に記載のマイクロ流体デバイス。
【請求項3】
前記第一流路(1)の分岐部(3)を挟む両側に、第一流路(1)の外部からの圧力により第一流路(1)の断面積を減少させる圧迫部(5a)および圧迫部(5b)が設けられた請求項1に記載のマイクロ流体デバイス。
【請求項4】
前記第二流路(2)の途中に、第三流路(6)が接続された請求項1に記載のマイクロ流体デバイス。
【請求項5】
前記第二流路(2)の前記第三流路(6)の接続部より下流側にクロマトグラフィー用分離カラムが直列に接続して設けられた請求項4に記載のマイクロ流体デバイス。
【請求項6】
前記第二流路(2)に質量分析装置への接続口が設けられた請求項1に記載のマイクロ流体デバイス。
【請求項7】
前記第一流路(1)の途上に直列にクロマトグラフィー用分離カラムが接続して設けられた請求項7に記載のマイクロ流体デバイス。
【請求項8】
前記第一流路(1)の前記分岐部(3)近傍に、前記第一流路(1)内の試料を光学的に観察する測定用の窓が設けられた請求項7に記載のマイクロ流体デバイス。
【請求項9】
請求項1に記載のマイクロ流体デバイスを用い、該マイクロ流体デバイスの第一流路(1)に試料を流し、前記圧迫部(5)を圧迫することによって前記第一流路(1)内の圧力を上昇させて、前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする微量試料の注入方法。
【請求項10】
請求項3に記載のマイクロ流体デバイスを使用し、前記分岐部(3)の両側の前記圧迫部(5’)、(5’’)を圧迫することにより前記第一流路(1)内の圧力を上昇させて、前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする微量試料の注入方法。
【請求項11】
請求項8に記載のマイクロ流体デバイスを使用し、前記分離カラムから前記分岐部(3)方向に液体を流し、前記分岐部(3)及び/又は前記分離カラムと前記分岐部(3)の間の部分を光学的に観察しつつ前記圧迫部(5)を圧迫することにより前記試料の一部を、前記弁を通過させて前記第二流路(2)へ注入することを特徴とする微量試料の注入方法。
【図1】


【図2】




【図2】


【公開番号】特開2006−10327(P2006−10327A)
【公開日】平成18年1月12日(2006.1.12)
【国際特許分類】
【出願番号】特願2004−183577(P2004−183577)
【出願日】平成16年6月22日(2004.6.22)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
【公開日】平成18年1月12日(2006.1.12)
【国際特許分類】
【出願日】平成16年6月22日(2004.6.22)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
[ Back to top ]

