マイクロ流路チップ及びマイクロアレイチップ
【課題】周囲の機器の配置に制限されることなく容易に装着可能であり、且つ、製造コストが比較的安いマイクロ流路チップを提供する。
【解決手段】マイクロ流路チップは、凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダ及び前記反応基板を覆うように配置された第1のシートと、該第1のシートを覆うように配置された第2のシートと、を有する。反応基板は、前記反応チャンバに露出している第1の面と、前記基板ホルダの凹部に設けられた観察窓を介して外部に露出している第2の面と、を有し、前記反応基板の第1の面には微細構造からなる反応スポットが形成されており、該反応スポットは前記反応チャンバに露出されている。
【解決手段】マイクロ流路チップは、凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダ及び前記反応基板を覆うように配置された第1のシートと、該第1のシートを覆うように配置された第2のシートと、を有する。反応基板は、前記反応チャンバに露出している第1の面と、前記基板ホルダの凹部に設けられた観察窓を介して外部に露出している第2の面と、を有し、前記反応基板の第1の面には微細構造からなる反応スポットが形成されており、該反応スポットは前記反応チャンバに露出されている。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、遺伝子診断装置、遺伝子解析装置等の核酸分析装置にて使用して好適なマイクロ流路チップ及びマイクロアレイチップに関する。
【背景技術】
【0002】
近年、核酸分析装置において、ガラス基板等で作製された反応基板に多数のDNAプローブ又はポリメラーゼを固定し、塩基伸長反応を行うことで配列を決定する方法が提案されている。このような固定及び反応を行う領域を、以下「反応スポット」と呼ぶ。反応スポットの形成方法として、単一分子を固定する場合(単分子方式)や同一種複数分子を固定する場合(複数分子方式)がある。また多数の反応スポットを配置し、各々の反応スポットで並列して塩基伸長及び配列決定を行う超並列方式核酸分析装置が開発されている。
【0003】
非特許文献1には、反応スポットに単一分子を固定し、全反射エバネッセント照射検出方式を用いて単分子レベルのDNA配列解読を行う方法が記載されている。特許文献1には、局在型表面プラズモンの蛍光増強効果を利用して、塩基伸長反応を計測することが記載されている。特許文献2及び特許文献3には、ポリジメチルシロキサン(PDMS)基板又はシートを用いたマイクロ流路チップの製造方法の例が記載されている。特許文献4には、ナノチップを用いてPCR生成物であるサンプルを分析する方法が記載されている。特許文献5及び特許文献6には、インレットとアウトレットを有するマイクロ流路チップでの測定例が記載されている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2009-45057号公報
【特許文献2】特開2009-47438号公報
【特許文献3】特開2005-111567号公報
【特許文献4】特開2005-181145号公報
【特許文献5】特開2005-245317号公報
【特許文献6】特開2005-233802号公報
【非特許文献】
【0005】
【非特許文献1】Ido Braslavsky, ”Proc. Natl. Acad. Sci. USA”,2003年, Vol. 100, No. 7, pp. 3960-3964
【発明の概要】
【発明が解決しようとする課題】
【0006】
マイクロ流路チップは核酸分析装置等に装着され、溶液等の供給系と廃液を排出する排出系が接続される。マイクロ流路チップは、溶液供給系と廃液排出系を容易に接続できる構造であることが好ましい。更に、マイクロ流路チップの両面または片面には、照明装置及び検出装置が配置される。例えば、高倍率の対物レンズで観察する場合、対物レンズをマイクロ流路チップに近接させる必要がある。従って、マイクロ流路チップは、照明装置及び検出装置がどのような構造であっても、適合することが好ましい。
【0007】
マイクロ流路チップは反応スポットを備えた反応基板を有する。反応基板は半導体製造プロセス処理を用いて製造されるため、比較的高価である。反応基板の寸法は、できるだけ小さいほうがよく、理想的には観察すべき反応スポットが配置された領域と同等の寸法であれば無駄がない。
【0008】
本発明の目的は、周囲の機器の配置に制限されることなく容易に装着可能であり、且つ、製造コストが比較的安いマイクロ流路チップを提供することにある。
【課題を解決するための手段】
【0009】
本発明のマイクロ流路チップは、反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及びアウトレットをそれぞれ接続する供給流路及び排出流路と、を有する。
【0010】
本発明のマイクロ流路チップは、凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダ及び前記反応基板を覆うように配置された第1のシートと、該第1のシートを覆うように配置された第2のシートと、によって構成される。また、本発明のマイクロ流路チップは、反応基板と、該反応基板より大きく、少なくとも反応チャンバ部に相当する部分に貫通孔または凹部を有する第1のシートと、該第1のシートと接着する第2のシートと、によって構成される。
【0011】
本発明のマイクロ流路チップによると、前記反応基板と前記第1のシートの貫通孔と前記第2のシートによって前記反応チャンバが形成され、または、前記反応基板と前記第1のシートの凹部によって前記反応チャンバが形成され、前記インレット及びアウトレットは該反応基板より離れた外側に配置され、該反応チャンバと該インレット及びアウトレットを連結する流路が該第1のシートと第2のシートの間に形成される。
【発明の効果】
【0012】
本発明によると、周囲の機器の配置に制限されることなく容易に装着可能であり、且つ、製造コストが比較的安いマイクロ流路チップを提供することができる。
【図面の簡単な説明】
【0013】
【図1A】本発明のマイクロ流路チップの構成例(実施例1)を示す図である。
【図1B】本発明のマイクロ流路チップの流路シートの例を示す図である。
【図1C】本発明のマイクロ流路チップの反応室シートの例を示す図である。
【図1D】本発明のマイクロ流路チップの基板ホルダの例を示す図である。
【図1E】本発明のマイクロ流路チップの反応基板の例を示す図である。
【図2】本発明のマイクロ流路チップを用いたDNAシーケンサ装置の主要部を説明する図である。
【図3】本発明のマイクロ流路チップを用いた単一分子DNAシーケンサ装置の例を説明する図である。
【図4】本発明のマイクロ流路チップを用いた単一分子DNA配列解析方法の例を説明する図である。
【図5A】本発明のマイクロアレイチップの構成例(実施例2)を示す図である。
【図5B】本発明のマイクロアレイチップの流路シートの例を示す図である。
【図5C】本発明のマイクロアレイチップの基板ホルダの例を示す図である。
【図5D】本発明のマイクロアレイチップの反応基板の例を示す図である。
【図6A】本発明のマイクロアレイチップを遺伝子解析装置へ装着する方法を説明する図である。
【図6B】本発明のマイクロアレイチップを遺伝子解析装置へ装着する方法を説明する図である。
【図7】本発明のマイクロアレイチップを用いた遺伝子解析システムの構成例を説明する図である。
【図8】本発明のマイクロアレイチップを用いた遺伝子解析システムの操作方法の例を説明する図である。
【図9A】本発明のマイクロ流路チップの別の構成例(実施例3)を示す図である。
【図9B】本発明のマイクロ流路チップ図9Aのシート2の上面図である。
【図9C】本発明のマイクロ流路チップ図9Aのシート1の上面図である。
【図9D】本発明のマイクロ流路チップ図9Aの基板ホルダの上面図である。
【図10A】本発明のマイクロ流路チップの別の構成例(実施例4)を示す図である。
【図10B】本発明のマイクロ流路チップ図10Aの基板ホルダの上面図である。
【図11A】本発明のマイクロ流路チップの別の構成例(実施例5)を示す図である。
【図11B】本発明のマイクロ流路チップ図11Aのシート2の上面図である。
【図11C】本発明のマイクロ流路チップ図11Aのシート1の上面図である。
【図11D】本発明のマイクロ流路チップ図11Aのシート3の上面図である。
【図11E】本発明のマイクロ流路チップ図11Aの基板ホルダの上面図である。
【図12A】本発明のマイクロ流路チップの別の構成例(実施例6)を示す図である。
【図12B】本発明のマイクロ流路チップ図12Aのシート2の上面図である。
【図12C】本発明のマイクロ流路チップ図12Aのシート1の上面図である。
【図12D】本発明のマイクロ流路チップ図12Aの基板ホルダの上面図である。
【図13A】本発明のマイクロ流路チップの別の構成例(実施例7)を示す図である。
【図13B】本発明のマイクロ流路チップ図13Aのシート2の上面図である。
【図13C】本発明のマイクロ流路チップ図13Aのシート1の上面図である。
【図13D】本発明のマイクロ流路チップ図13Aの基板ホルダの上面図である。
【図14A】本発明のマイクロ流路チップの別の構成例(実施例8)のシート1の上面図である。
【図14B】本発明のマイクロ流路チップの別の構成例(実施例8)の基板ホルダの上面図である。
【図15A】本発明のマイクロ流路チップの別の構成例(実施例9)を示す図である。
【図15B】本発明のマイクロ流路チップ図15Aのシート2の上面図である。
【図15C】本発明のマイクロ流路チップ図15Aのシート1の上面図である。
【図15D】本発明のマイクロ流路チップ図15Aのシート3の上面図である。
【図15E】本発明のマイクロ流路チップ図15Aの基板ホルダの上面図である。
【発明を実施するための形態】
【0014】
[実施例1]
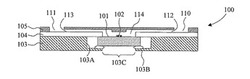
図1A、図1B、図1C、図1D及び図1Eを参照して本発明によるマイクロ流路チップの第1の例を説明する。図1Aに示すように、本例のマイクロ流路チップは、基板ホルダ103と、基板ホルダ103に装着された反応基板101と、基板ホルダ103及び反応基板101を覆うように配置された反応室シート104と、更にその上に配置された流路シート105とを有する。反応基板101、基板ホルダ103、反応室シート104、及び、流路シート105の2つの主面のうち、図1A、図1B、図1C、図1D及び図1Eにて上側の面を上面、下側の面を下面と称することとする。
【0015】
反応基板101の上面には、反応スポット102が形成されている。反応スポット102は、多数のDNAプローブ又はポリメラーゼを固定し、塩基伸長反応等を行う領域のことである。マイクロ流路チップの下面には照明窓103Cが形成されている。照明窓103Cを介して、反応基板101の下面が露出している。本例のマイクロ流路チップでは、図1Aの断面図において、下方から照明窓103Cを介して照明光を反応スポット102に照射し、上方から流路シート105を介して反応スポット102を観察する。従って、流路シート105、反応室シート104及び反応基板101は透明な材料によって形成される。
【0016】
マイクロ流路チップは、インレット110、供給流路112、反応チャンバ114、排出流路113、及び、アウトレット111を有する。供給流路112、反応チャンバ114、及び、排出流路113は、順に接続されており、密閉された通路を形成している。インレット110及びアウトレット111は、顕微鏡の対物レンズおよび励起光源光学系部品配置の障害とならないよう、反応スポット102から少なくとも約30mm離れた位置に形成されている。
【0017】
図1Eに示すように、反応基板101は、厚さが約0.7mm、一辺の寸法が約10mmの正方形の薄い板状部材からなる。しかしながら、反応基板101は、好ましくは、一辺の寸法が20mm以下の正方形の板状部材であってよく、更に、一辺の寸法が5mm〜500mmの正方形の板状部材であってもよい。更に、反応基板101は、正方形以外の形状、例えば、長方形、多角形、円形等の板状部材であってもよい。
【0018】
反応基板101は、石英によって形成される。反応基板101の上面には、遺伝子配列、遺伝子多型などを解析するための反応スポット102が形成されている。
【0019】
反応スポット102は、局在型表面プラズモンが発生し易いように微細構造を有することが好ましい。局在型表面プラズモンは局所的に蛍光を増加させる効果を有する。効果が及ぶ範囲は、10nmから20nm程度の極小領域である。このような極小領域に、ターゲットDNA分子を固定し、このターゲットDNA分子に蛍光標識したプライマー単一分子を結合させると、プライマー単一分子からの蛍光のみを局所的に増加させることができる。周囲に浮遊するプライマー単一分子からの蛍光は、局在型表面プラズモンによる蛍光増加効果の影響を受けないから、両者を峻別することができる。
【0020】
特許文献1には、局在型表面プラズモンが発生し易い微細構造の形成方法の例が記載されている。この文献に記載された例では、半導体製造プロセスによってウエハ上に微細構造を形成する。先ず、円形の石英基板(ウエハ)に、金属蒸着、エッチング、スパッタリング、ミリング等の半導体製造プロセス処理を行い、反応スポットを生成する。こうして多数の反応スポットが形成されたウエハを、ダイシング(裁断)して、所定の寸法の反応基板101を形成する。反応基板101は、マイクロ流路チップを構成する他の部品より比較的高価である。従って、反応基板101の寸法はできるだけ小さいことが好ましい。本発明によると、反応基板101は基板ホルダ103の凹部103Aに収納されるように構成されており、反応基板101の寸法を比較的小さくすることができる。それによって、マイクロ流路チップの価格を抑制することができる。
【0021】
図1Dに示すように、基板ホルダ103の上面には、反応基板101を収納するための凹部103Aが形成されている。凹部103Aの底面には、貫通孔が形成されている。この貫通孔によって、マイクロ流路チップの照明窓103Cが形成される。即ち、マイクロ流路チップの照明窓103Cにて、反応基板101の下面が露出する。照明窓103Cの周囲の部材によって、反応基板を保持するための反応基板保持部103Bが形成される。照明窓103Cの縦横寸法は、反応基板101の縦横寸法より小さい。従って、反応基板保持部103Bによって反応基板101を支持することができる。
【0022】
基板ホルダ103は、一般的なスライドグラスと同等の寸法を有する。即ち、縦横の寸法は、26mm×76mmである。厚さは好ましくは2mm程度であるが、0.1mm〜10mmでもよい。凹部103Aの縦横寸法は、反応基板の縦横寸法より大きく、凹部103Aの深さは、反応基板101の厚さと同一か又はそれより大きい。反応基板保持部103Bの厚さは、好ましくは、約0.5mmであるが、0.01mm〜5mmでもよい。
【0023】
基板ホルダ103は、ユーザによる不意の取り扱いミスや落下にも耐えうる材料によって形成される。このような材料として、ステンレス、アルミニウム、鉄などの金属、あるいは、プラスチック、エラストマーなどの樹脂がある。
【0024】
図1Cに示すように、反応室シート104は、基板ホルダ103の外形と同等の形状及び寸法を有する。反応室シート104の中心部には貫通孔104Aが形成されている。この貫通孔104Aによって、マイクロ流路チップの反応チャンバ114が形成される。即ち、反応チャンバ114の形状は、貫通孔104Aの形状に等しい。
【0025】
本例では、貫通孔104Aの形状は、六角形を反応室シートの長手方向に引き伸ばして得られる形状である。貫通孔104Aの両端104Bの角部は、反応室シート104の中心軸線に沿って配置されている。貫通孔104Aの形状は、中心軸線上の両端104Bが尖った形状が好ましい。それによって、反応チャンバ114に流れ込んだ液体が、両端の角部において、滞留することが回避される。しかしながら、図示の貫通孔104Aの形状は、例示であり、菱形、楕円、円、多角形、長方形等であってもよい。
【0026】
貫通孔104Aの寸法は、反応スポット102より大きいが、反応基板101より小さい。従って、反応チャンバ114の底面は、貫通孔104Aにて露出した反応基板101の上面によって形成される。検出光学系によって一度に観察できる領域を、以下に、「計測視野」と呼ぶ。反応チャンバ114の底面は、少なくとも、計測視野の寸法と同程度か又はそれより大きい。従って、貫通孔104Aの寸法は、計測視野の寸法と同程度か又はそれより大きい。
【0027】
反応室シート104の厚さは、好ましくは50μmであるが、5μm〜5mmでもよい。反応室シートは、耐熱性、耐寒性、耐候性、及び、耐薬品性を有する材料によって形成される。このような材料として、ポリジメチルシロキサン(PDMS)が好ましい。PDMSは自己吸着性を有するため、接着剤を使用しなくても他の部材と接着可能である利点を有する。尚、PDMSに対して用途に応じた表面処理が可能である。それにより、PDMSに、疎水性・親水性・自己吸着性を付与することができる。しかしながら、自己吸着性、又は、光化学反応による接着などが可能な材質であり、且つ、使用する試薬、実験系に不具合を与えなければ、PDMS以外の材料であってもよい。例えば、シリコン樹脂、ポリ塩化ビニル(PVC)などでもよい。
【0028】
図1Bに示すように、流路シート105は、基板ホルダ103の外形と同等の形状と寸法を有する。流路シート105には、中心軸線上に沿って、2つの貫通孔105Aが形成されている。貫通孔105Aは円形であり、流路シート105の両端近くに形成されている。流路シート105の下面には、2本の溝105Bが形成されている。これらの溝は、貫通孔105Aから、基板ホルダ103の中心軸線に沿って中心方向に延びており、他端には小さな円形の凹部105Cが形成されている。
【0029】
溝105Bの深さは約50μm、幅は約500μmである。凹部105Cの深さは、溝105Bの深さと同一であってよい。凹部105Cの径は、溝105Bの幅と同一であってもよいが、それより大きくてもよい。
【0030】
2つの貫通孔105Aによって、マイクロ流路チップのインレット110及びアウトレット111が形成される。2つの溝105Bによって、マイクロ流路チップの供給流路112及び排出流路113が形成される。
【0031】
上述のように、インレット110及びアウトレット111は、顕微鏡の対物レンズおよび励起光源光学系部品配置の障害とならないよう、反応スポットから少なくとも約30mm 離れた位置に形成されている。従って、2つの貫通孔105Aは、流路シート105の中心より、少なくとも30mm離れた位置に形成される。2本の溝105Bの内端の凹部105Cは、反応室シート104の貫通孔104Aの両端104Bに対応した位置にて、且つ、貫通孔104Aの内側の位置に形成されている。
【0032】
流路シート105の厚さは、好ましくは100μmであるが、5μm〜10mmでもよい。流路シート105は、反応室シートと同様に、耐熱性、耐寒性、耐候性、及び、耐薬品性を有する材料によって形成される。このような材料として、ポリジメチルシロキサン(PDMS)が好ましい。PDMSは自己吸着性を有するため、接着剤を使用しなくても他の部材と接着可能である利点を有する。例えば、流路シート105と反応室シート104の両者をPDMSによって形成することにより、自己吸着性を利用して両者を接合することができる。こうして、流路形成のために接着剤を用いた接合プロセスを省くことが可能となる。以下に、流路シート105と反応室シートの両者は、PDMSによって形成されているものとして説明する。
【0033】
本例のマイクロ流路チップの組立方法を説明する。先ず、基板ホルダ103の凹部103Aに反応基板101を配置する。このとき、基板ホルダ103と反応基板101の上面が共面となるように、配置する。基板ホルダ103の照明窓103Cの寸法より、反応基板101の寸法のほうが大きいから、反応基板101によって、照明窓103Cは塞がれる。反応基板101の下面は、照明窓103Cによって露出する。次に、基板ホルダの反応基板保持部103Bに、反応基板101を接着する。接着方法は、接着剤による接着であってもよいが、溶着であってもよい。次に、基板ホルダ103の上面に、反応室シート104を貼付する。本例では、反応室シート104は、PDMSによって形成されている。従って、PDMSの自己吸着性により、反応室シート104は、基板ホルダ103および反応基板101の上面に吸着する。反応室シート104の貫通孔104Aの寸法は、反応基板101の寸法より小さいから、貫通孔104Aの周囲にて、反応室シート104と反応基板101の間には隙間は形成されない。
【0034】
次に、反応室シート104の上に、さらに流路シート105を装着する。本例では、反応室シート104と流路シート105は、PDMSによって形成されている。従って、PDMSの自己吸着性により、流路シート105と反応室シート104は互いに吸着する。こうして、マイクロ流路チップが形成される。こうして形成されたマイクロ流路チップでは、流路シート105を天井面とし、反応基板101を底面とし、反応室シート104の貫通孔を側面とする反応チャンバ114が形成される。更に、流路シート105の溝105Bを通路とし、反応室シート104を底面とする供給流路112、及び、排出流路113が形成される。
【0035】
なお、本例では、流路シート105に溝105Bが形成されているが、流路シート105の代わりに反応室シート104に同様な溝を形成してもよい。
【0036】
マイクロ流路チップの特徴は、分析対象及び分析方法により、様々な反応スポットを有する反応基板101を用いることができるが、反応基板101以外の部材は共通である、即ち、同一である。従って、量産効果により、マイクロ流路チップの製造価格を安くすることが可能となる。
【0037】
図2を参照して、本発明のマイクロ流路チップを用いたDNAシーケンサ装置の主要部を説明する。マイクロ流路チップの構造は、図1Aに示したものと同様である。先ず、試薬供給及び排出系について説明する。マイクロ流路チップのインレット110には、パッキン131を介して、インレットチューブ213が接続されている。マイクロ流路チップのアウトレット111には、パッキン132を介して、アウトレットチューブ214が接続されている。パッキン131、132は、ゴム、シリコン、PDMS等により形成される。
【0038】
励起光源光学系、及び、検出光学系について説明する。図2では、検出光学系として対物レンズ231のみを示す。本例では、励起光源光学系として、全反射エバネッセント照射検出方式を用いる。反応基板101の下面には、全反射プリズム120が装着されている。全反射プリズム120は、一辺が数センチメートルの正方形の底面と、底面に対して傾斜した側面を有する。全反射プリズム120は、反応基板101の下面に接合されてよい。全反射プリズム120は、接着剤によって接合されてよいが、好ましくは、油侵によって接合される。全反射プリズム120は、反応基板101の下面のうち、照明窓によって露出された部分に装着されている。
【0039】
入射光路121に沿って導かれた励起用レーザ光は、全反射プリズム120の一方の傾斜面に入射され、反応基板101の上面に到達する。励起用レーザ光は、反応基板101の上面にて、全反射し、全反射プリズム120の他方の傾斜面から出射され、出射光路122に沿って導かれる。反応基板101の上側には、反応チャンバ114が形成されている。従って、反応基板101の上面は、屈折率境界面となる。屈折率境界面において全反射が起きると、およそ入射光の1波長程度の深さだけ低媒質側の内部に電磁波が浸透する。この光をエバネッセント光と呼ぶ。エバネッセント光により、反応スポット102に形成された金属構造体を含む極めて限定された領域のみが照明される。これは全反射エバネッセント照射と称される。エバネッセント光によって照射される領域をエバネッセント場と呼ぶ。
【0040】
本例の光学系では、更に、局在型表面プラズモンの蛍光増強効果を利用する。上述のように、反応スポット102には、局在型表面プラズモンが発生し易いように微細構造が形成されている。反応スポット102の微細構造にて、局在型表面プラズモンが発生すると、微細構造を含む極小領域において蛍光が増加する。
【0041】
反応スポット102には、ハイブリダイゼーション反応によって、蛍光標識された単一のプライマー分子が結合する。更に、塩基伸長反応によって、蛍光標識されたdNTP分子(NはA、C、G、Tのいずれかである)が取り込まれる。これらの蛍光色素は、エバネッセント光を励起光として発光する。更に、これらの蛍光色素からの発光は、局在型表面プラズモンにより、局部的に増加する。この発光は、反応基板101の上側に配置された対物レンズ231を含む検出光学系によって検出される。
【0042】
浮遊しているプライマー分子及びdNTP分子は、エバネッセント場外にあるから、エバネッセント光に起因する蛍光を発生しない。また、これらの浮遊分子は局在型表面プラズモンによる蛍光増加効果を受けない。従って、ハイブリダイゼーション反応又は塩基伸長反応によって結合した単一分子の位置を正確に検出することができる。
【0043】
本発明によるマイクロ流路チップの特徴は、インレット110とアウトレット111をマイクロ流路チップの上側に、即ち、照明窓103Cの反対側に設けたことにある。それによって次のような利点が得られる。先ず、アウトレットチューブ214とインレットチューブ213を、マイクロ流路チップの上側に配置することができる。即ち、アウトレットチューブ214とインレットチューブ213を、励起光源光学系とは反対側に配置することができる。それによって、マイクロ流路チップの上側に検出光学系を設け、マイクロ流路チップの下側に励起光源光学系を設けることができる。更に、励起光源光学系のためのスペースを確保することができる。従って、励起光源光学系の設計の自由度が高くなる。例えば励起光源光学系として、全反射エバネッセント照射検出方式を採用することが可能となる。全反射エバネッセント照射検出方式では、全反射プリズム120を用いるが、本例では、全反射プリズム120を反応基板の下面に直接装着することができる。更に、全反射エバネッセント照射検出方式では、全反射プリズム120に対する入射光と反射光を別個の光路に沿って導く必要がある。本例では、入射光路121と出射光路122を容易に別個に設けることができる。
【0044】
更に、本発明によるマイクロ流路チップの特徴は、インレット110とアウトレット111をマイクロ流路チップの両端近くに配置したことにある。それによって次のような利点が得られる。アウトレットチューブ214とインレットチューブ213の間に検出光学系のためのスペースを確保することができる。従って、検出光学系の設計の自由度が高くなる。例えば、倍率が40倍、あるいは60倍、あるいは100倍の顕微鏡用対物レンズを用いる場合、マイクロ流路チップの上面から対物レンズの先端までの距離を0.2mm程度に接近させる必要がある。本例では、対物レンズを、マイクロ流路チップに近接して配置することが可能となり、大口径すなわち高N/Aの対物レンズを使用することが可能となる。従って、検出感度を向上させることができる。
【0045】
図3を参照して、単一分子DNAシーケンサ装置の例を説明する。本例のDNAシーケンサ装置は、分析装置200と解析用コンピュータ241と出力装置242を有する。分析装置200は、マイクロ流路チップ100の上側に設けられた検出光学系と、マイクロ流路チップ100の下側に設けられた励起光源光学系と、マイクロ流路チップ100の右側に設けられた溶液供給系と、マイクロ流路チップ100の左側に設けられた廃液回収系と、装置制御用コンピュータ240を有する。装置制御用コンピュータ240は解析用コンピュータ241に接続されている。
【0046】
検出光学系は、対物レンズ231、蛍光波長フィルター232、結像レンズ233、2次元センサカメラ(検出器)234、及び、カメラコントローラ(検出器コントローラ)235を有する。励起光源光学系は、第1及び第2の励起光用レーザーユニット221、222、第1及び第2のλ/4波長板223、224、ミラー225、ダイクロイックミラー226、及び、ミラー227を有する。
【0047】
溶液供給系は、試薬保管ユニット211、分注ユニット212及びインレットチューブ213を有する。廃液回収系は、アウトレットチューブ214及び廃液容器215を有する。マイクロ流路チップの上側に、図示していない温度制御ユニットを設けてもよい。温度制御ユニットを設けることによって、反応チャンバ内に導入されるサンプル液、試薬、洗浄液等は、所定の温度に保持される。
【0048】
本例では、インレットチューブ213からの溶液が、マイクロ流路チップの反応チャンバ114に導入され、アウトレットチューブ214に排出されるとき、溶液が漏洩することはない。例えば、反応室シート104と反応基板101の間は密に接着され、両者の間から溶液が漏洩することはない。従って、溶液が、基板ホルダ103に接触することはない。
【0049】
図4を参照して、本発明によるマイクロ流路チップを用いた単一分子DNA配列解析方法の例を説明する。ここでは、図3に示したDNAシーケンサ装置を用いる。試薬保管ユニット211には、単一のターゲットDNA分子溶液、蛍光色素Cy3によって蛍光標識されたプライマー単一分子溶液、蛍光色素Cy5によって蛍光標識された一種類の塩基のdNTP(NはA、C、G、Tのいずれかである)とポリメラーゼを含む溶液、洗浄液、等が保管されている。第1の励起光用レーザーユニット221は、波長532nmのレーザ光は発生し、第2の励起光用レーザーユニット222は、波長635nmのレーザ光を発生する。蛍光色素Cy3は、波長532nmのレーザ光によって発光し、蛍光色素Cy5は波長635nmのレーザ光によって発光する。
【0050】
先ず、ステップS101にて、反応基板の上面に、単一のターゲットDNA分子を固定化し、反応スポットを形成する。ターゲットDNA分子の固定化には、ビオチン-アビジンのタンパク質結合を利用する。未反応の余剰なターゲットDNA分子を洗い流す。こうして、反応基板に所望の反応スポットを形成することができる。
【0051】
ステップS102にて、蛍光色素Cy3によって蛍光標識されたプライマーを含む溶液を、マイクロ流路チップに形成された流路に導入する。分注ユニット212の吸込み口を、試薬保管ユニット211に保管された蛍光色素Cy3によって蛍光標識されたプライマー単一分子溶液に接続する。このプライマー単一分子溶液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。プライマー単一分子は、反応スポットに固定されたターゲットDNA分子とハイブリダイズする。所定の時間、ハイブリダイゼーション反応を行う。
【0052】
ステップS103にて、未反応の余剰なプライマーを洗い流す。分注ユニット212の吸込み口を、試薬保管ユニット211の洗浄液に接続する。この洗浄液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。未反応の余剰なプライマーは洗浄液によって洗い流され、反応チャンバ114から、排出流路113、アウトレット111、及び、アウトレットチューブ214を介して、廃液容器215に排出される。
【0053】
ステップS104にて、532nmの励起光を用いた全反射エバネッセント照射により、Cy3の蛍光を検出する。Cy3の蛍光を検出することにより、反応スポットに固定されたターゲットDNA分子とハイブリダイズしたプライマー単一分子の位置を検出することができる。
【0054】
第1の励起光用レーザーユニット221からの波長532nmのレーザ光は、λ/4波長板223、ミラー225、及び、ダイクロイックミラー226、及び、ミラー227を経由して、全反射プリズム120に導入される。全反射プリズム120に導入されたレーザ光は、反応基板の上面にて全反射する。このとき、エバネッセント光により、反応スポット102に形成された金属構造体を含む極めて限定された領域のみが照明される。エバネッセント光によって、プライマー分子の蛍光色素Cy3が発光する。更に、反応スポット102に形成された金属構造体にて、局在型表面プラズモンが発生させ、蛍光を増加させることができる。
【0055】
この蛍光は、対物レンズ231、蛍光波長フィルター232、及び、結像レンズ233を介して、2次元センサカメラ(検出器)234によって検出される。2次元センサカメラ(検出器)234によって得られた2次元輝度信号は、カメラコントローラ(検出器コントローラ)235を介して、装置制御用コンピュータ240に送られ、更に、解析用コンピュータ241に送られる。
【0056】
ステップS105にて、Cy3を高出力の励起光で照射することによって蛍光退色させ、以降の蛍光発光を抑制する。即ち、第1の励起光用レーザーユニット221からのレーザ光の出力を増加し、蛍光色素Cy3を退色させる。
【0057】
ステップS106にて、蛍光色素Cy5によって蛍光標識された一種類の塩基のdNTP(NはA、C、G、Tのいずれかである)とポリメラーゼを含む溶液を、マイクロ流路チップに形成された流路に導入する。分注ユニット212の吸込み口を、試薬保管ユニット211に保管された蛍光色素Cy5によって蛍光標識された一種類の塩基のdNTP(NはA、C、G、Tのいずれかである)とポリメラーゼを含む溶液に接続する。この溶液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。ターゲットDNA分子に対して相補関係にあるdNTP(NはA、C、G、Tのいずれかである)は、反応スポットにおいて、プライマー分子の伸長鎖に取り込まれる。所定の時間、塩基伸長反応を行う。
【0058】
ステップS107にて、未反応の余剰なdNTPを洗い流す。分注ユニット212の吸込み口を、試薬保管ユニット211の洗浄液に接続する。この洗浄液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。未反応の余剰なdNTPは洗浄液によって洗い流され、反応チャンバ114から、排出流路113、アウトレット111、及び、アウトレットチューブ214を介して、廃液容器215に排出される。
【0059】
ステップS108にて、635nmの励起光を用いた全反射エバネッセント照射により、Cy5の蛍光を検出する。Cy5の蛍光を検出することにより、プライマー分子の伸長鎖に取り込まれたdNTPの位置を検出することができる。即ち、dNTP分子に対して相補関係にあるターゲットDNA分子の位置を検出することができる。
【0060】
第2の励起光用レーザーユニット222からの波長635nmのレーザ光は、λ/4波長板224、ダイクロイックミラー226及びミラー227を経由して、全反射プリズム120に導入される。全反射プリズム120に導入されたレーザ光は、反応基板の上面にて全反射する。このとき、エバネッセント光により、反応スポット102に形成された金属構造体を含む極めて限定された領域のみが照明される。エバネッセント光によって、dNTP分子の蛍光色素Cy5が発光する。更に、反応スポット102に形成された金属構造体にて、局在型表面プラズモンが発生させ、蛍光を増加させることができる。
【0061】
この蛍光は、対物レンズ231、蛍光波長フィルター232、及び、結像レンズ233を介して、2次元センサカメラ(検出器)234によって検出される。2次元センサカメラ(検出器)234によって得られた2次元輝度信号は、カメラコントローラ(検出器コントローラ)235を介して、装置制御用コンピュータ240に送られ、更に、解析用コンピュータ241に送られる。
【0062】
ステップS109にて、Cy5を高出力の励起光で照射することによって蛍光退色させ、以降の蛍光発光を抑制する。即ち、第2の励起光用レーザーユニット222からのレーザ光の出力を増加し、蛍光色素Cy5を退色させる。
【0063】
次に、dNTP(NはA、C、G、Tのいずれかである)における塩基の種類を例えばA>C>G>T>Aのように順次変更して、ステップS102〜ステップS109を繰り返す(段階的伸長反応)。解析用コンピュータ241は、ターゲットDNAに結合したプライマー分子の位置とdNTP分子の位置から、ターゲットDNA分子と相補関係にある塩基配列を決定する。
【0064】
[実施例2]
図5A、図5B、図5C及び図5Dを参照して、本発明のマイクロアレイチップの例を説明する。本例のマイクロアレイチップは、遺伝子解析用マイクロアレイチップとして用いられるように構成されている。即ち、微細電極パッドアレイにおける電気化学的結合によるハイブリダイゼーションを使用する診断装置を想定している。本例のマイクロアレイチップは、使い捨てを想定している。
【0065】
図5Aに示すように、本例のマイクロアレイチップ500は、基板ホルダ503と、基板ホルダ503に装着された反応基板501と、基板ホルダ503及び反応基板501を覆うように配置された流路シート505とを有する。反応基板501、基板ホルダ503、及び、流路シート505の2つの主面のうち、図5A、図5B、図5C及び図5Dにて上側の面を上面、下側の面を下面と称することとする。
【0066】
反応基板501の上面には、反応スポット502が形成されている。本例の遺伝子解析用マイクロアレイチップでは、図5Aの断面図において、上方から流路シート505を介して照明光を反応スポット502に照射し、上方から流路シート505を介して反応スポット502を観察する。従って、流路シート505は透明な材料によって形成される。
【0067】
マイクロアレイチップは、インレットチャンバ510、供給流路512、反応チャンバ514、排出流路513、及び、アウトレットチャンバ511を有する。インレットチャンバ510とアウトレットチャンバ511は、セプタ504によって封鎖されている。セプタ504は、ゴム、シリコン等の柔軟な材料によって形成された薄膜である。
【0068】
インレットチャンバ510、供給流路512、反応チャンバ514、排出流路513、及び、アウトレットチャンバ511は、順に接続されており、内部に密閉された通路を形成している。マイクロアレイチップでは、内部の空間が完全に密閉されており、そこに収納された溶液が漏洩することはない。従って、反応基板501に予め所望の反応スポット502が形成され、内部に溶液が充填されたマイクロアレイチップをそのまま搬送することができる。
【0069】
図5Dに反応基板501の例を示す。反応基板501の上面には、遺伝子配列、遺伝子多型などを解析するための反応スポット502が形成されている。
【0070】
本例の基板ホルダ503では、全反射エバネッセント照射検出方式を使用しないが、局在型表面プラズモンの局所的蛍光増加効果を利用してよい。従って、反応スポット502は、図1Eに示した例と同様に、局在型表面プラズモンが発生し易いように微細構造を有することが好ましい。
【0071】
本例の反応基板501は図1Eに示した反応基板101と比較すると、本例の反応基板の下面には、複数の制御電極501Aが設けられている点が異なる。制御電極501Aを設ける点以外は、本例の反応基板501は図1Eに示した反応基板101と同様であってよい。制御電極501Aを介して、反応スポット502に形成され微細電極に電圧を印加する。こうして、反応スポット502に形成された微細電極において、電気化学結合が生成される。
【0072】
図5Cに示すように、基板ホルダ503の下面には、反応基板501を収納するための凹部503Aが形成されている。この凹部503Aの底面には、貫通孔503Cが形成されている。貫通孔503Cの周囲の部材によって、反応基板を保持するための反応基板保持部503Bが形成される。
【0073】
貫通孔503Cによって、マイクロアレイチップの反応チャンバ514が形成される。即ち、反応チャンバ514の形状は、貫通孔503Cの形状に等しい。本例では、貫通孔503Cの形状は、六角形を流路シートの長手方向に引き伸ばして得られる形状である。貫通孔503Cの両端503Dの角部は、基板ホルダ503の中心軸線に沿って配置されている。貫通孔503Cの形状は、中心軸線上の両端503Dが尖った形状が好ましい。それによって、反応チャンバ514に流れ込んだ液体が、両端の角部において、滞留することが回避される。しかしながら、図示の貫通孔503Cの形状は、例示であり、菱形、楕円、円、多角形、長方形等であってもよい。
【0074】
貫通孔503Cの寸法は、反応スポット502より大きいが、反応基板501より小さい。従って、反応チャンバ514の底面は、貫通孔503Cにて露出した反応基板501の上面によって形成される。検出光学系によって一度に観察できる領域を、以下に、「計測視野」と呼ぶ。反応チャンバ514の底面は、少なくとも、計測視野の寸法と同程度か又はそれより大きい。従って、貫通孔503Cの寸法は、計測視野の寸法と同程度か又はそれより大きい。
【0075】
基板ホルダ503には、更に、中心軸線上に沿って、2つの貫通孔503Eが形成されている。貫通孔503Eは円形であり、基板ホルダ503の両端近くに形成されている。2つの貫通孔503Eによって、マイクロアレイチップのインレットチャンバ510及びアウトレットチャンバ511が形成される。
【0076】
基板ホルダ503は、一般的なスライドグラスと同等の寸法を有する。即ち、縦横の寸法は、26mm×76mmである。厚さは好ましくは2mm程度であるが、0.1mm〜10mmでもよい。凹部503Aの縦横寸法は、反応基板の縦横寸法より大きく、凹部503Aの深さは、反応基板501の厚さと同一か又はそれより大きい。反応基板保持部503Bの厚さは、好ましくは、約0.5mmであるが、0.01mm〜5mmでもよい。貫通孔503Cの縦横寸法は、反応基板501の縦横寸法より小さい。従って、反応基板保持部503Bにて反応基板501を装着することができる。本例の基板ホルダ503は、図1Dにて示した基板ホルダ103と同様な材料によって形成してよい。
【0077】
図5Bに示すように、流路シート505は、基板ホルダ503の外形と同等の形状と寸法を有してよい。但し、本例では、流路シート505の長手方向寸法は、基板ホルダ503の長手方向の寸法より僅かに小さい。流路シート505の下面には、中心軸線上に沿って、2つの凹部505Aが形成されている。凹部505Aは円形であり、流路シート505の両端近くに形成されている。流路シート505の下面には、2本の溝505Bが形成されている。これらの溝は、凹部505Aから、基板ホルダ503の中心軸線に沿って中心方向に延びており、他端には小さな円形の凹部505Cが形成されている。
【0078】
溝505Bの深さは約50μm、幅は約500μmである。凹部505A、505Cの深さは、溝505Bの深さと同一であってよい。凹部505Cの径は、溝505Bの幅と同一であってもよいが、それより大きくてもよい。
【0079】
基板ホルダ503の貫通孔503Eと流路シート505の凹部505Aによって、マイクロアレイチップのインレットチャンバ510及びアウトレットチャンバ511が形成される。流路シート505の2つの溝505Bによって、マイクロアレイチップの供給流路512及び排出流路513が形成される。
【0080】
2本の溝505Bの外端の凹部505Aは、基板ホルダ503の2つの貫通孔503Eに対応した位置に配置される。2本の溝505Bの内端の凹部505Cは、基板ホルダ503は貫通孔503Cの両端503Dに対応した位置にて、且つ、貫通孔503Cの内側の位置に形成されている。
【0081】
本例の流路シート505は、図1Bにて示した流路シート105と同様な材料によって形成してよい。
【0082】
本例のマイクロアレイチップの組立方法を説明する。基板ホルダ503の下面にて、貫通孔503Eにセプタ504を装着する。セプタ504によって、2つの貫通孔503Eの開口は完全に封鎖される。次に、基板ホルダ503の凹部503Aの反応基板保持部503Bに反応基板501を接着する。接着方法を説明する。先ず、反応基板501の下面の全面又は額縁状部分に、親水性処理を施してから、PDMSなどの樹脂皮膜を塗布する。親水性処理として、SiO2やTiO2等の超親水コート膜のコーティングを用いてよい。次に、こうして、親水性処理と樹脂皮膜を施した反応基板501を、基板ホルダ503の凹部503Aに貼付する。反応基板501のPDMS皮膜の自己吸着性により、反応基板501は、基板ホルダ503の凹部の反応基板保持部503Bに吸着する。
【0083】
本例では、基板ホルダ503の凹部503Aと反応基板501の間の接着面積は、図1Aに示した例と比較して、大きい。従って、反応基板501と基板ホルダ503は、両者の間の接着面において確実に密着される。反応チャンバ514に流れ込んだ液体が、反応基板501と基板ホルダ503の間より漏洩することはない。本例の接着方法では、接着剤を用いないことが好ましい。その理由は、反応チャンバ514に流れ込んだ液体が接着剤に接触する可能性を排除するためである。
【0084】
基板ホルダ503の貫通孔503Cの寸法は、反応基板501の寸法より小さいから、反応基板501によって、貫通孔503Cは塞がれる。貫通孔503Cの周囲にて、基板ホルダ503と反応基板501の間には隙間は形成されない。貫通孔503Cにて、反応基板501の上面が露出する。即ち、貫通孔503Cにて、反応基板501の上面の反応スポット502が露出する。反応基板501の下面は、基板ホルダ503の凹部503Aを介して外部に露出している。
【0085】
次に、基板ホルダ503の上面に、流路シート505を貼付する。本例では、流路シート505は、PDMSによって形成されている。従って、PDMSの自己吸着性により、流路シート505は、基板ホルダ503の上面に吸着する。こうして、マイクロアレイチップが形成される。こうして形成されたマイクロアレイチップでは、流路シート505を天井面とし、反応基板501を底面とし、基板ホルダ503の貫通孔503Cを側面とする反応チャンバ514が形成される。更に、流路シート505の溝505Bを通路とし、基板ホルダ503の上面を底面とする、供給流路512、及び、排出流路513が形成される。
【0086】
本例のマイクロアレイチップは、基板ホルダ503と流路シート505の2つの部材によって構成されており、図1Aに示す第1の例と比較して、構成部材が少ない。図1Aに示す第1の例では、マイクロ流路チップ内の流路を流れる溶液は、反応基板101、反応室シート104及び流路シート105に接触するが、基板ホルダ103には接触しない。しかしながら、本例のマイクロアレイチップでは、マイクロアレイチップ内の流路を流れる溶液は、反応基板501、流路シート505及び基板ホルダ503に接触する。即ち、基板ホルダ503と反応基板501の接着部に試薬等の溶液が直接接触する。従って、基板ホルダ503と反応基板501の間の接着面には接着剤は用いないことが好ましい。
【0087】
本例の遺伝子解析用マイクロアレイチップを用いた遺伝子解析の手順の例の概要を説明する。先ず、反応基板の反応スポットに、一端がビオチン化された塩基配列が既知のオリゴヌクレオチド(Capture Oligo)を供給し、制御電極を介して反応スポットの微細電極に電圧を印加する。オリゴヌクレオチド(Capture Oligo)は、微細電極に引き寄せられ、反応スポットの表面の透過層構造と接触する。オリゴヌクレオチド(Capture Oligo)のビオチン標識と透過層構造がavidin-biotin反応を起こし、オリゴヌクレオチド(Capture Oligo)は透過層構造に固定される。マイクロアレイチップの反応チャンバに洗浄液を供給し、未反応の余剰なオリゴヌクレオチド(Capture Oligo)を洗い流す。
【0088】
次に、別のオリゴヌクレオチド(Capture Oligo)を用いて上述の工程を繰り返す。それによって、反応スポットに、オリゴヌクレオチド(Capture Oligo)から成る所望のオリゴヌクレオチド・アレイが形成される。
【0089】
次に、マイクロアレイチップの反応チャンバに、一部の塩基配列が不明である分析対象のPCR生成物(Sample Oligos)を供給する。PCR生成物(Sample Oligos)は、反応スポットにて、相補的配列を有するオリゴヌクレオチド(Capture Oligo)とハイブリダイズする。このハイブリダイゼーション反応により、PCR生成物(Sample Oligos)は、オリゴヌクレオチド(Capture Oligo)によってキャプチャされ、反応スポットに固定される。洗浄液によって反応スポットを洗浄し、未反応の余剰なPCR生成物(Sample Oligos)を洗い流す。
【0090】
次にマイクロアレイチップの反応チャンバに、一端が蛍光標識されたオリゴヌクレオチド(Reporter Oligos)を供給する。このオリゴヌクレオチド(Reporter Oligos)は、反応スポットにて、相補的配列を有するPCR生成物(Sample Oligos)とハイブリダイズする。洗浄液によって反応スポットを洗浄し、未反応の余剰なオリゴヌクレオチド(Reporter Oligos)を洗い流す。
【0091】
マイクロアレイチップの反応基板の反応スポットに、励起光を照射する。この励起光により、PCR生成物(Sample Oligos)とハイブリダイズしたオリゴヌクレオチド(Reporter Oligos)から蛍光が発生する。この蛍光パターンを検出し、解析することで、PCR生成物(Sample Oligos)の塩基配列を分析することができる。
【0092】
図6A及び図6Bを参照して、本例の遺伝子解析用マイクロアレイチップを遺伝子解析装置へ装着する方法を説明する。図6Aに示すように、本例のマイクロアレイチップ500を、支持体610に装填する。マイクロアレイチップ500の両端を、支持体610の凹部611に、それぞれ係合させる。本例では、マイクロアレイチップ500の両端には、基板ホルダ503が露出している。従って、マイクロアレイチップ500の両端の基板ホルダ503の端部を、凹部611に、それぞれ係合させる。凹部611の幅は、基板ホルダ503の端部の厚さより大きい。基板ホルダ503の両端、即ち、マイクロアレイチップ500の両端は、支持体610の凹部611の下面上に配置されている。
【0093】
マイクロアレイチップの反応基板501には、診断目的に応じて、一端がビオチン化された塩基配列が既知のオリゴヌクレオチド(Capture Oligo)が既に結合されている。またオリゴヌクレオチドを安定して保存するため、マイクロアレイチップのインレットチャンバ510、供給流路512、反応チャンバ514、排出流路513、及び、アウトレットチャンバ511には、生理食塩水等のバッファが充填されている。
【0094】
マイクロアレイチップ500の下方には、インレットニードル701及びアウトレットニードル702が配置されている。インレットニードル701及びアウトレットニードル702は、支持体716によって支持されている。更に、マイクロアレイチップ500の下方には、電極703が設けられている。電極703は、支持体704に装着されている。支持体704は、ばね705によって支持体716に支持されている。
【0095】
インレットニードル701及びアウトレットニードル702はセプタ504の下方に配置されている。電極703は、反応基板501の下方に配置されている。
【0096】
図6Bに示すように、支持体716を上方に移動させる。インレットニードル701及びアウトレットニードル702と電極703が上昇する。インレットニードル701及びアウトレットニードル702はセプタ504を穿孔する。更に、支持体716を上方に移動させると、電極703が反応基板501の下面の制御電極501A(図5D参照)に係合し、電気回路が形成される。
【0097】
更に、支持体716を上方に移動させると、インレットニードル701及びアウトレットニードル702の先端は、マイクロアレイチップのインレットチャンバ510及びアウトレットチャンバ511内に配置される。セプタ504は、ゴム等の弾性変形可能な膜によって形成されているから、インレットニードル701及びアウトレットニードル702がセプタ504を穿孔しても、インレットニードル701及びアウトレットニードル702とセプタ504の間は密閉されている。即ち、インレットチャンバ510及びアウトレットチャンバ511の密閉性は確保される。インレットチャンバ510及びアウトレットチャンバ511内の液体が、インレットニードル701及びアウトレットニードル702とセプタ504の間から漏洩することはない。
【0098】
更に、支持体716を上方に移動させると、マイクロアレイチップ500は持ち上げられ、基板ホルダ503の両端、即ち、マイクロアレイチップ500の両端は、支持体610の凹部611の上面に当接する。更に、支持体716を上方に移動させると、ばね705が圧縮する。このとき、ばね705の圧縮力によって、電極703は、反応基板501の下面の制御電極501A(図5D参照)に押し付けられる。
【0099】
支持体610の凹部611の上面によって、マイクロアレイチップ500の基準位置が設定される。即ち、マイクロアレイチップ500の両端が、支持体610の凹部611の上面に当接しているとき、マイクロアレイチップ500は基準位置に配置されていると定義することができる。マイクロアレイチップ500の基準位置を設定することによって、光学観察系と、基板ホルダ503及び反応基板501の間の相対的な位置関係を所定の値に維持することが容易となる。
【0100】
こうして、アタッチメント操作が終了すると、遺伝子解析用の実験を行う。例えば、研究対象細胞の発現遺伝子等を蛍光色素等で標識した試薬を反応基板501の反応スポット502上でハイブリダイゼーションさせ、互いに相補的な核酸(DNA又はRNA)同士を結合させ、その箇所を蛍光色素等でラベルする。反応スポット502を照明装置621により照明し、CCDカメラ622により観察する。なお、カメラ622には予め蛍光波長のみを透過する光学バンドパスフィルタを装着し、蛍光信号のみを弁別し観察する。
【0101】
図7を参照して遺伝子解析システムの構成例を説明する。本例の遺伝子解析システムは、遺伝子解析装置700と解析用コンピュータ741と出力装置742とバーコードリーダ743を有する。分析装置200は、マイクロアレイチップ500の上側に設けられた検出光学系と、マイクロアレイチップ500の下側の右側に設けられた溶液供給系と、マイクロアレイチップ500の下側の左側に設けられた廃液回収系とを有する。
【0102】
検出光学系は、照明装置621、及び、CCDカメラ622を有し、カメラ622には所定の蛍光波長のみを透過する光学バンドパスフィルタが装着されている。
【0103】
溶液供給系は、サンプルトレイ711、洗浄水ボトル712、ヒスチジンボトル713、予備ボトル714、及び、4方向バルブ715を有する。サンプルトレイ711には、複数のサンプル又は試薬を保管することができる。サンプルトレイ711は、図示を省略したステージ装置により、X-Y-Z方向に移動可能である。ヒスチジンボトル713には、反応液として用いるヒスチジンが収納されている。
【0104】
サンプルトレイ711、洗浄水ボトル712、ヒスチジンボトル713、予備ボトル714は交換可能である。4方向バルブ715は、サンプルトレイ711、洗浄水ボトル712、ヒスチジンボトル713、及び、予備ボトル714の何れかと、マイクロアレイチップの反応チャンバ514を接続する。
【0105】
廃液回収系は、2方向バルブ717、吸引装置718及び廃液ボトル720を有する。2方向バルブ717は、マイクロアレイチップの反応チャンバ514と廃液ボトル720の何れかと、吸引装置718を接続する。吸引装置718はプランジャ718Aとシリンジ718Bを有する。
【0106】
本例の遺伝子解析システムの動作を説明する。先ず、4方向バルブ715によって、サンプルトレイ711の所定のサンプル保管部と、マイクロアレイチップの反応チャンバ514を接続する。2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。プランジャ718Aを下方に駆動することによって、マイクロアレイチップの反応チャンバ514と流路に充填されていた溶液は、シリンジ718Bに吸引され、代わりに、サンプルトレイ711に保管されていたサンプル溶液が、マイクロアレイチップの反応チャンバ514と流路を充填する。この動作をフィルと称する。
【0107】
次に、2方向バルブ717によって、廃液ボトル720と吸引装置718を接続する。プランジャ718Aを上方に駆動することによって、シリンジ718Bに充填されていた溶液は、廃液ボトル720に排出される。この動作をフラッシュと呼ぶ。
【0108】
次に、4方向バルブ715によって、洗浄水ボトル712と、マイクロアレイチップの反応チャンバ514を接続する。2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。プランジャ718Aを下方に駆動することによって、マイクロアレイチップの反応チャンバ514に充填されていた廃液は、シリンジ718Bに吸引され、代わりに、洗浄水ボトル712に保管されていた洗浄液が、マイクロアレイチップの反応チャンバ514と流路を充填する。即ち、洗浄液のフィルを行う。
【0109】
次に、2方向バルブ717によって、廃液ボトル720と吸引装置718を接続する。プランジャ718Aを上方に駆動することによって、シリンジ718Bに充填されていた廃液は、廃液ボトル720に排出される。即ち、廃液のフラッシュを行う。こうして、フィルとフラッシュを繰り返すことにより、所望の溶液の供給と排出を行うことができる。
【0110】
図8を参照して遺伝子解析システムの操作を説明する。ステップS701にて、遺伝子解析システムの電源を入れ、初期化を行う。初期化では、洗浄水ボトル712内の洗浄液の容量の確認とヒスチジンボトル713内のヒスチジンの容量の確認を行う。ステップS702にて、サンプル等の準備を行う。本例では、遺伝子解析用マイクロアレイチップ500の反応基板の反応スポットには、診断目的に応じて、一端がビオチン化された塩基配列が既知のオリゴヌクレオチド(Capture Oligo)が予め固定されている。遺伝子解析用マイクロアレイチップ500は、他の場所にて用意されたものであってもよい。サンプルトレイ711には、サンプルDNA(Sample Oligos)、レポータDNA(Reporter Oligos)等が保管されている。例えば、バーコードリーダ743により、サンプルトレイ711、各ボトル712、713、遺伝子解析用マイクロアレイチップ500又は基板ホルダ503に装着されたバーコードを読み取る。読み取った識別符号等は、解析用コンピュータ741に送られる。解析用コンピュータ741は、出力装置742に指示画面を表示し、ユーザへ所定の指示を行う。
【0111】
ステップS703にて、アタッチメントを行う。図6Aに示したように、マイクロアレイチップ500を、支持体610に装着する。インレットニードル701及びアウトレットニードル702と電極703を上昇させる。図6Bに示したように、インレットニードル701及びアウトレットニードル702はセプタ504を穿孔する。更に、支持体716を上方に移動させると、電極703が反応基板501の下面の制御電極501A(図5D参照)に係合する。
【0112】
ステップS704にて、サンプルDNAを、マイクロアレイチップの反応チャンバ514に導入する。先ず、サンプルトレイX-Y-Z駆動機構(図示なし)によりサンプルトレイ711を所望の位置に配置し、4方向バルブ715によって、サンプルトレイ711の所定のサンプルDNA溶液と、マイクロアレイチップの反応チャンバ514を接続する。次に、2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。フィルを行い、マイクロアレイチップの反応チャンバ514と流路に充填されていた溶液を、シリンジ718B内に吸引し、代わりに、サンプルトレイ711に保管されていたサンプルDNA溶液を、マイクロアレイチップの反応チャンバ514と流路を充填する。
【0113】
反応基板501の反応スポット502の目的の位置に、約0.2mAの電流を60秒印加する。電圧の印加によって、目的の位置にて電気的結合が起き、サンプルDNAがキャプチャされる。即ち、反応スポットに固定されたオリゴヌクレオチド(Capture Oligo)と相補配列を有するDNAのみが非特異的にハイブリダイズする。
【0114】
ハイブリダイゼーション反応が完了すると、次に、ステップS705にて、未反応のサンプルDNAを洗い流す。即ち、フラッシュを行い、マイクロアレイチップの反応チャンバ514内の液体を廃液ボトルに排出する。洗浄水のフィル及びフラッシュによりマイクロアレイチップの反応チャンバ514及び流路を洗浄する。
【0115】
ステップS706にて、蛍光標識されたレポータDNAを、マイクロアレイチップの反応基板の反応チャンバ514に導入する。先ず、サンプルトレイX-Y-Z駆動機構(図示なし)によりサンプルトレイ711を所望の位置に配置し、4方向バルブ715によって、サンプルトレイ711の所定のレポータDNA溶液と、マイクロアレイチップの反応チャンバ514を接続する。次に、2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。フィルを行い、マイクロアレイチップの反応チャンバ514と流路に充填されていた洗浄液を、シリンジ718B内に吸引し、代わりに、サンプルトレイ711に保管されていたレポータDNA溶液を、マイクロアレイチップの反応チャンバ514と流路を充填する。この状態でおよそ60秒維持する。これにより、キャプチャされたサンプルDNAとレポータDNAがハイブリダイズする。
【0116】
ハイブリダイゼーション反応が完了すると、ステップS707にて、未反応のレポータDNAを洗い流す。即ち、フラッシュを行い、マイクロアレイチップの反応チャンバ514内の液体を廃液ボトルに排出する。洗浄水のフィル及びフラッシュによりマイクロアレイチップの反応チャンバ514及び流路を洗浄する。洗浄が完了すると、洗浄水のフィルにより、マイクロアレイチップの反応チャンバ514及び流路を洗浄水によって充填する。
【0117】
ステップS708にて、CCDカメラで画像を取得する。先ず、照明装置621により励起光を反応基板の反応スポットに照射し、カメラ622により蛍光色素が発する蛍光の画像を取得する。蛍光の位置から、レポータDNA(Reporter Oligos)の位置を確認することができる。上述のステップにより、マイクロアレイチップの反応基板の反応スポットに予め固定されたオリゴヌクレオチド(Capture Oligo)にサンプルDNA(Sample Origos)が結合し、このサンプルDNA(Sample Origos)に更に、蛍光標識されたレポータDNA(Reporter Oligos)が結合している。レポータDNA(Reporter Oligos)の位置を検出することにより、サンプルDNA(Sample Origos)の位置を検出することができる。
【0118】
ステップS709にて、デタッチメントを行なう。画像取得完了後は、フラッシュを行い、マイクロアレイチップの反応チャンバ514及び流路に保持されていた洗浄水を廃棄する。更に、洗浄液のフィルおよびフラッシュを繰り返し、マイクロアレイチップの反応チャンバ、反応基板及び流路を洗浄する。洗浄が完了したのち、インレットニードル701及びアウトレットニードル702と電極703を下降させる。それにより、流路結合、および電気的結合が解除される。マイクロアレイチップ500を、支持体610より取り外す。
【0119】
ステップS710にて、終了処理を行う。装置内の各構成部品を初期位置に戻し、電源切断可能な状態とする。
【0120】
[実施例3]
本発明をさらに別の実施の形態例により説明する。
図9A、図9B、図9C、図9Dを参照して本発明によるマイクロ流路チップ900の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。図9Aに示すように、本例のマイクロ流路チップは、基板ホルダ903と、基板ホルダ903に装着された反応基板101と、基板ホルダ903及び反応基板101の上部に配置されたシート904と、更にその上に配置されたシート905とを有する。基板ホルダ903、シート904、及び、シート905の2つの主面のうち、図9A、図9B、図9C、図9Dにて上側の面を上面、下側の面を下面と称することとする。
【0121】
実施例1と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ903に支持され、またマイクロ流路チップの下面には照明窓903Cが形成されている。照明窓903Cを介して、反応基板101の下面が露出しており、その部分に全反射プリズムを光学的に接着、又は、配置させることができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。発する蛍光は、シート904、シート905を通して、上方より観察、集光、検出する。シート905、シート904及び反応基板101は透明な材料によって形成される。
【0122】
マイクロ流路チップは、インレット910、供給流路912、反応チャンバ914、排出流路913、及び、アウトレット911を有する。供給流路912、反応チャンバ914、及び、排出流路913は、順に接続されており、密閉された流路を形成している。
【0123】
インレット910及びアウトレット911は、顕微鏡の対物レンズおよび励起光源光学系部品配置の障害とならないよう、離れた位置に形成される。対物レンズの外径は通常約30mm程度であり、しかも高NAの対物レンズは基板表面に近接する必要がある。そのため、対物レンズの直下を含む近傍には反応基板・反応チャンバのカバー構造体以外配置できない状態になる。この場合、対物レンズとの干渉を避けるために、反応スポット102から少なくとも約15mm以上離れた位置にインレット910及びアウトレット911を形成する必要がある。
【0124】
本例ではインレット910及びアウトレット911を反応スポット102から20mmの距離に配置した。より正確には、対物レンズが測定視野を移動することも含み、測定視野範囲+対物レンズ外径を超える位置にインレット910及びアウトレット911を作成すればよい。本例では、反応スポットを中心としてその両側にインレット910及びアウトレット911を作成しており、その間隔は40mmとなり、対物レンズをその間に配置し、蛍光検出することができる。そのため、高NAの対物レンズを使用することができ高感度な蛍光検出することができる。DNA塩基配列解析装置のために、また、単分子方式DNA塩基配列解析装置に好適である。
【0125】
反応基板101は、石英ウェハから裁断した厚さが約0.725mm、一辺の寸法が約10mmの正方形の薄い石英ガラス板状部材とした。反応基板の上面には、少なくとも、その一部に、半導体製造プロセスによって、DNAなどが固定できる金属構造体などが作成されている。ただ、金属構造体などがなく、アミノ基、カルボキシル基、ビオチン、アビジンなどが結合されているものでも可能である。また、反応基板の形状は、正方形のほか、長方形、多角形、円形等であってもよい。また、大きさは、10mmの正方形に限らず、任意の大きさに対応できるが、小さな寸法にすることが望ましい。
【0126】
図9Dに示すように、基板ホルダ903の上面には、反応基板101を収納し、保持するための凹部903Aが形成されている。凹部903Aの底面には、反応基板保持部903Bと約9mm×9mmの貫通孔が形成されている。この貫通孔によって、マイクロ流路チップの照明窓903Cが形成される。反応基板101は反応基板保持部903Bに支えられ、照明窓903Cにて、反応基板101の下面が露出する。照明窓903Cの縦横寸法の少なくとも一方が反応基板101の縦横寸法より小さければよく、例えば、8mm×10mm、10mm×8mm等でもよい。これにより、反応基板保持部903Bによって反応基板101が支持される。なお、凹部903Aの縦横寸法は、なるべく近い寸法で、反応基板の縦横寸法より大きければよく、10.5mm×14mm程度でよい。凹部903Aの深さは、反応基板101の厚さと同一程度でよく、0.7mmとする。反応基板保持部903Bの厚さは、特に制約がないが、全反射照明する場合は、なるべく薄いほうがよく、0.1mmとする。0.05〜0.3mmでもよい。
【0127】
基板ホルダ903は、一般的なスライドグラスと同等の寸法を有する。即ち、縦横の寸法は、26mm×76mmである。厚さは上記により、0.8mmである。
基板ホルダ903は、ユーザによる不意の取り扱いミスや落下にも耐えうる材料によって形成される。このような材料として、ステンレス、アルミニウム、鉄などの金属、あるいは、アクリル、ポリスチレンなどの樹脂がある。
【0128】
図9Cに示すように、シート904は、基板ホルダ903の外形と同等または、やや小さい形状及び寸法を有する。厚みは100μmとする。シート904の中心部には凹部904A(下面側に開口、深さは50μm)が形成されている。シート904と反応基板が密着することで、凹部904Aの領域が反応チャンバ914になる。凹部904Aは反応スポット102の領域より大きく、反応基板101全体より小さいサイズとし、反応スポット102と凹部904Aの中心がほぼ一致するようにする。反応チャンバ914は、反応スポット102の上側に形成される。なお、検出光学系によって一度に観察できる領域を、以下に、「計測視野」と呼ぶ。反応チャンバ914の底面は、少なくとも、計測視野の寸法と同程度か又はそれより大きくする。凹部904Aの両端には貫通孔904Bがあり、上面に形成した2本の溝904Cと連結し、両端部904Dにつながる。溝904C、両端部904Dの深さは約50μm、溝904Cの幅は約500μm、両端部904Dは1mmφ、貫通孔904Bは1mmφである。
【0129】
図9Bに示すように、シート905は、シート904と同等の形状と寸法を有する。厚みは100μmとする。シート905には、シート904の両端部904Dと同じ位置に、2つの貫通孔905Aが形成されている。貫通孔905Aは円形であり2mmφである。シート904とシート905を密着させ、接着することで、シート904の上面の溝904Cとシート905の下面で流路912及び913が形成され、シート905の2つの貫通孔905Aがインレット910及びアウトレット911になる。
【0130】
これにより、インレット910、流路912、反応チャンバ914、流路913、アウトレット911とつながる流路が形成される。なお、図には記していないが、図2と同様に、インレット910、アウトレット911には、インレットチューブ、アウトレットチューブを接続して使用される。
【0131】
なお、シート905と904の厚さは、流路にかかる圧力による変形の影響を少なくするために、厚いほうがよい。ただし、シート904と905全体の厚みは対物レンズの結像が許容な範囲にする必要がある。最大の厚みは、対物レンズの倍率、NAなどによって異なるので、対物レンズにあわせればよい。材質は、耐熱性、耐寒性、耐候性、及び、耐薬品性を有する材料によって形成される。このような材料として、ポリジメチルシロキサン(PDMS)などのシリコーン樹脂が使用できる。PDMSは接着性を有するため、接着剤を使用しなくてもガラスなど他の部材と接着可能である利点を有する。また透明性が高く、光測定に有効である。接着などが可能な材質であり、且つ、使用する試薬、実験系に不具合を与えなければ、PDMS以外の材料であってもよい。
【0132】
なお、シート905は貫通孔以外の加工がされていないため、薄いガラス板であってもよい。シート904とはそのままで接着可能であり、流路にかかる圧力に耐性もあり、強度を高めることが可能である。
【0133】
また、流路912,913は、シート904の溝904Cとシート905の下面で形成したが、シート905の下面に溝904Cと同等の溝を作成して流路を構成してもよい。
【0134】
また、本例では、凹部904Aの形状は六角形としたが、形状は、例示であり、菱形、楕円、円、多角形、長方形等であってもよい。試薬などの液体が流れやすくするためのテーパなどがついていることが望ましい。
【0135】
なお、本図には記載されないが、本マイクロ流路チップを使った測定系には、励起光源光学系として、図2または図3と同様に、全反射エバネッセント照射検出方式を用いることができる。反応基板101の下面に、全反射プリズムをオイルカップリングにより光学的に接合する。照明窓より小さな全反射プリズムを使用して、照明窓によって露出された反応基板部分に直接接合してもよいし、または、照明窓より大きな全反射プリズムを使用して、反応基板保持部903Bと接触させ、反応基板保持部の厚みの空間にオイルなどを満たしてカップリングしてもよい。
【0136】
励起用のレーザ光は、全反射プリズムに入射し、オイルカップリング部を経由して反応基板内に導入され、上面の反応スポット部を照射する。反応基板、反応スポット部の上部の反応チャンバ内には反応試薬溶液、洗浄液などの水溶液で満たされている。反応基板の石英ガラスの屈折率は約1.46、水の屈折率は約1.33である。反応基板から反応チャンバへの入射角度が約66度で臨界角となり、それを超える角度で入射すると界面で全反射する。そのため界面での入射角度が68度前後になるように調整し、反応スポット部で全反射させ、反応スポット部の直上の反応チャンバ内にエバネッセントを形成させ、この範囲にある蛍光体を励起する。生じる蛍光は、前述のように対物レンズにより、上方より観察、集光、検出する。
【0137】
なお、全反射プリズムに代えて、対物レンズを使用してエバネッセント照明してもよい。反応基板として厚さ0.17mmの石英ガラス板を使用し、NA1.4以上の対物レンズを反応基板の下面に配置し、オイルカップリングにより、反応基板101の下面と光学的に接合する。対物レンズに入射するレーザ光の光路を調整することで、反応基板にレーザ光を導入し、上面の水溶液との界面で全反射するようにする。発する蛍光は、同じ対物レンズを使用して集光し、検出することができる。
【0138】
本実施例では、反応基板101のサイズが一辺約10mmの正方形に対して、試薬を導入し排出するためのインレット及びアウトレットの間隔が幅40mmと、基板サイズを超えて作成できる。これは、反応スポット上部の反応チャンバ914は基板面に接触する必要があるが、チャンバに試薬を導くための供給流路912、排出流路913は基板面と接触させる必要はないため、シート904とシート905の2層構造とし、その間に流路を構成することによって実現したものである。インレット及びアウトレットも反応基板と接触しない構造であり、インレット及びアウトレットの間隔を広げつつ、反応基板のサイズを最小にすることができる。
【0139】
本例によりチップを安価に作成することが可能になる。反応基板101は、石英ウェハから裁断したものを使用している。石英ウエハは高価であるため、コストを下げるには基板をより多く切り取る必要がある。実施例では反応基板のサイズを10mm角であり、8インチ径のウェハからは単純計算で約290枚程度得ることができる。実施例のように、マイクロ流路チップのインレット及びアウトレットの間隔を40mmにし、これを従来のように反応基板の上部に作成する場合、基板サイズは横45mm、縦10mm程度必要であり、この場合、58枚程度しか裁断できない。長辺の長さが20mmの基板であれば140枚に、25mmであれば110枚に裁断できるため、コスト低下が可能になる。本実施例の構造により、より多くの基板を得ることができ、より安価にチップを作成することができる。
【0140】
また、本実施例では、反応チャンバ914に試薬を導くための供給流路912、排出流路913は反応基板の面とは接触していない。そのため反応基板と基板ホルダとの間に隙間があっても液がその部分に漏れたり、しみだすことがなく、安定に、正確に液を流すことができる。本例では、反応基板の厚さが0.725mmで、基板ホルダの凹部の深さが0.7mmであるから、マイクロ流路チップを構築したときに、基板上面と基板ホルダ上面に段差ができる。しかしながら、このような構造でも、液を漏れたり、しみだすことがなく、送液することができる。単純に、供給流路または排出流路を反応基板及び基板ホルダとその上部のシートに形成した溝とで構築する場合、反応基板と液が接触するので、前記のような段差がある場合、液漏れするという問題がある。また、反応基板と基板ホルダとの間には隙間が必ず発生するため、隙間に液が入り込んでしまい、反応スポット領域への液の送液が困難になるという問題もある。隙間を接着剤などで埋める場合でも段差のないようにすることは困難であり、液漏れの可能性が高い。このように、本例によれば、インレット及びアウトレットの間隔を広げつつ、反応基板のサイズを最小にでき、液の漏れやしみだしのない安定で正確な送液を行うことが可能になる。
【0141】
[実施例4]
本発明をさらに別の実施の形態例により説明する。
図10A、図10Bを参照して本発明によるマイクロ流路チップ920の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。また、反応基板の上部に密着して配置されるシート904及び905は実施例3と同じものを使用する。図10Aに示すように、本例のマイクロ流路チップは、基板ホルダ923と、反応基板101と、反応基板上部に配置されたシート904と、更にその上に配置されたシート905とを有する。基板ホルダ923、シート904、及び、シート905の2つの主面のうち、図10A、図10Bにて上側の面を上面、下側の面を下面と称することとする。
【0142】
実施例3と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ923に設けられた貫通孔923A内に配置され、基板ホルダ923と反応基板101とに接着されるシート904によって保持される。シート904の上面にはシート905が接着される。反応基板101の下面は露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。シート905、シート904は透明材料により構成され、反応基板面より発する蛍光などを上方より観察、集光、検出する。
【0143】
実施例3と同様に、マイクロ流路チップは、インレット910、供給流路912、反応チャンバ914、排出流路913、及び、アウトレット911を有する。供給流路912、反応チャンバ914、及び、排出流路913は、順に接続されており、密閉された流路を形成する。インレット910及びアウトレット911は、反応スポット102からそれぞれ20mm離して配置され、インレット910とアウトレット911間は約40mm離れる。本構成により、液漏れすることなく、反応基板101(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に十分に広い間隔で設けられる。これにより、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。
【0144】
基板ホルダ923は、一般的なスライドグラスと同等の寸法を有する。縦横の寸法は、26mm×76mmである。厚さは反応基板と同等の厚さでよく、0.725mmとした。図9Dに示すように、基板ホルダ903は貫通孔923Aを有する。貫通孔は約11mm×11mmであり、反応基板101がその内部に入る大きさとする。
【0145】
反応基板はシート904にて吊り下げ保持される。そのため、反応基板と基板ホルダの上面に段差がなく、フラットにすることができる。シート904もシート905もフラットになり、シート905に強度の強いガラス板を使用することが可能である。なお、反応基板はシート904のほか、下面に配置される全反射プリズムによっても保持される。
本実施例によれば、流路構成が同じであり、実施例3と同等の効果が得られる。
【0146】
[実施例5]
本発明をさらに別の実施の形態例により説明する。
図11A、図11B、図11C、図11D、図11Eを参照して本発明によるマイクロ流路チップ930の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。また、反応基板の上部に密着して配置されるシート905は実施例3と同じものを使用する。図11Aに示すように、本例のマイクロ流路チップは、基板ホルダ933と、反応基板101と、反応基板上部に配置されたシート934と、更にその上に配置されたシート905と、反応基板101とシート934の間のシート936とを有する。基板ホルダ933、シート936、シート934、及び、シート905の2つの主面のうち、図11A、図11B、図11C、図11D、図11Eにて上側の面を上面、下側の面を下面と称することとする。
【0147】
実施例3と同様に、反応基板101(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の上面には、反応スポット102が形成されている。
【0148】
図11Eに示すように、基板ホルダ933の上面には、反応基板101を収納し、保持するための凹部933Aが形成されている。凹部933Aの底面には、反応基板保持部933Bと約9mm×9mmの貫通孔が形成されている。この貫通孔によって、マイクロ流路チップの照明窓933Cが形成される。反応基板101は反応基板保持部933Bに支えられ、照明窓933C部で反応基板101の下面が露出する。照明窓933Cの縦横寸法は、反応基板101の縦横寸法より小さく、9mm×9mm等でもよい。これにより、反応基板保持部933Bによって反応基板101が支持される。なお、凹部933Aの縦横寸法は、11mm×11mm程度でよい。凹部933Aの深さは、反応基板101の厚さと同一程度でよいが、0.82mmとする。反応基板保持部933Bの厚さは、0.1mmとする。基板ホルダ933の縦横の寸法は、26mm×76mmである。厚さは上記により、0.83mmである。
【0149】
反応基板101は凹部933A内の反応基板保持部933Bによって支持される。また、照明窓933Cを介して、反応基板101の下面が露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。
【0150】
発する蛍光は、シート934、シート905を通して、上方より観察、集光、検出する。シート905、シート934及び反応基板101は透明な材料によって形成される。
【0151】
反応基板101上部には、厚さ0.095mmのシート936を密着させている。それによって、反応基板101と凹部933Aの深さの間の寸法の差を埋め、基板ホルダ933の上面とシート936の上面を平らになる。これらの上にシート934、及び、シート905を配置して流路などを構築している。図11Dに示すように、シート934は、反応基板101とほぼ同一の大きさで、反応スポット領域に相当する位置に、反応スポット102の領域より大きく、反応基板101全体より小さいサイズの貫通孔936Aを有している。反応基板との接着は貫通孔の周辺部にて行う。
【0152】
図11Cに示すように、シート934は、基板ホルダ933の外形よりやや小さい形状及び寸法を有する。厚みは100μmとする。シート934とシート936、及び反応基板101が組み合わされて密着することで、貫通孔936Aの領域が反応チャンバ914になる。反応チャンバ914は、反応スポット102の上側に形成される。シート934には、シート936の貫通孔936Aの両端に相当する位置に、貫通孔934Bが形成されている。この貫通孔934Bは、上面に形成した2本の溝934Cと連結し、両端部934Dにつながる。溝934C、両端部934Dの深さは約50μm、溝934Cの幅は約500μm、両端部934Dは1mmφ、貫通孔934Bは1mmφである。
【0153】
図11Bに示すように、シート905は、シート934と同等の形状と寸法を有する。厚みは100μmとする。シート905には、シート934の両端部934Dと同じ位置に、2つの貫通孔905Aが形成されている。貫通孔905Aは円形であり2mmφである。シート934とシート905を密着させ、接着する。それにより、シート934の上面の溝934Cとシート905の下面によって、流路912及び913が形成され、シート905の2つの貫通孔905Aがインレット910及びアウトレット911になる。
【0154】
これにより、インレット910、流路912、反応チャンバ914、流路913、アウトレット911とつながる流路が形成される。
【0155】
なお、シート934と936の材料として、ポリジメチルシロキサン(PDMS)などのシリコーン樹脂が使用できる。PDMSは接着性を有するため、接着剤を使用しなくてもガラスなど他の部材と接着可能である利点を有する。また透明性が高く、光測定に有効である。接着などが可能な材質であり、且つ、使用する試薬、実験系に不具合を与えなければ、PDMS以外の材料であってもよい。シート936は不透明材料でも構わない。
【0156】
実施例3、4と同様に、マイクロ流路チップは、インレット910、供給流路912、反応チャンバ914、排出流路913、及び、アウトレット911を有する。供給流路912、反応チャンバ914、及び、排出流路913は、順に接続されており、密閉された流路を形成する。本構成により、液漏れすることなく、反応基板101(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に十分に広い間隔が設けられる。これにより、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。
【0157】
本実施例によれば、基板ホルダと反応基板の厚みが異なっていても、シート936が、その段差を吸収でき、基板などの設計が容易になる。
本実施例によれば、流路構成が同じであり、実施例3と同等の効果が得られる。
【0158】
[実施例6]
本発明をさらに別の実施の形態例により説明する。
図12A、図12B、図12C、図12Dを参照して本発明によるマイクロ流路チップ940の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。図12Aに示すように、本例のマイクロ流路チップは、基板ホルダ943と、反応基板101と、反応基板上部に配置されたシート944と、更にその上に配置されたシート945とを有する。
【0159】
実施例4と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ943に設けられた貫通孔943A内に配置され、基板ホルダ943と反応基板101とに接着されるシート944によって保持される。シート944の上面にはシート945が接着される。反応基板101の下面は露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。シート945、シート944は透明材料により構成され、反応基板面より発する蛍光などを上方より観察、集光、検出する。
【0160】
基板ホルダ943の寸法は、26mm×76mmである。厚さは反応基板と同等の厚さでよく、0.725mmとした。図12Dに示すように、基板ホルダ943は貫通孔943Aを有する。貫通孔の寸法は約11mm×11mmであり、反応基板101がその内部に入る大きさとする。また後述するインレット及び、アウトレット用に、シート944の貫通孔944Cと同じ位置に、貫通孔943Bが設けられている。
【0161】
図12Cに示すように、シート944は、基板ホルダ943の外形と同等または、やや小さい形状及び寸法を有する。厚みは100μmとする。シート944の中心部には貫通孔944Aが形成されている。シート944と反応基板が密着し、シート945で覆われることで、貫通孔944Aの領域が反応チャンバ954になる。貫通孔944Aは反応スポット102の領域より大きく、反応基板101全体より小さいサイズとし、反応スポット102と貫通孔944Aの中心がほぼ一致するようにする。反応チャンバ954は、反応スポット102の上側に形成される。シート944の貫通孔944Aの両端は、上面に形成した2本の溝944Bと連結し、両端部の貫通孔944Cにつながる。溝944Bの深さは約50μm、幅は約500μm、両端部の貫通孔944Cは1mmφである。なお、本シートは実施例3のシート904と同等の構造、つまり、貫通孔944Aの代わりに凹部904A(下面側に開口、深さは50μm程度)と同等の構造を設けて流路を形成してもよい。
【0162】
図12Bに示すように、シート945は、シート944と同等の寸法で、厚みが100μmのガラス板とする。すくなくとも、シート945の貫通孔、溝などをカバーするサイズであればよい。貫通孔、溝なども構造は不要である。シート944とシート945を密着させることによって、溝944Bに対応して流路952及び953が形成され、シート944の貫通孔944Cに対応してインレット950とアウトレット951が形成される。インレット950とアウトレット951は、シート944の貫通孔944C、及び、基板ホルダ943に設けられた貫通孔943Bによって構築される。
【0163】
これにより、インレット950、流路952、反応チャンバ954、流路953、アウトレット951とつながる流路が形成される。さらに、インレット950、アウトレット951には、インレットチューブ955、アウトレットチューブ956が接続され必要な液を供給及び排出する構成とする。
【0164】
実施例3、4などと同様に、マイクロ流路チップは、インレット、供給流路、反応チャンバ、排出流路、及び、アウトレットを有し、供給流路、反応チャンバ、及び、排出流路は、順に接続されており、密閉された流路を形成する。インレット及びアウトレットは、反応スポットからそれぞれ20mm離して配置され、インレットとアウトレット間は約40mm離れる。本構成により、液漏れすることなく、反応基板(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に十分に広い間隔が設けられる。これにより、小さな基板サイズのものでも、測定装置に必要な部品の配置に影響を与えることなく、使用することができる。
【0165】
上面は完全フラットであり、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。また、全反射プリズムを配置する際にも影響を与えることがない。また、下面から対物レンズで、全反射照明する場合でも障害となることはなくなる。
【0166】
本実施例では、孔、溝加工されていないガラス板をシート945に使用することができ、より容易に使用することができ、チップの強度を簡単に高めることができる。また、流路にかかる圧力に耐性もあり、流路、特に対物レンズの下方の観察窓になる面の変形が少なく、蛍光像を安定に計測することが可能になる。
【0167】
[実施例7]
本発明をさらに別の実施の形態例により説明する。
図13A、図13B、図13C、図13Dを参照して本発明によるマイクロ流路チップ960の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。
【0168】
実施例6と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ963に設けられた貫通孔963A内に配置され、基板ホルダ963と反応基板101とに接着されるシート964によって保持される。シート964の上面にはシート965が接着される。反応基板101の下面は露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。シート965、シート964は透明材料により構成され、反応基板面より発する蛍光などを上方より観察、集光、検出する。
【0169】
基板ホルダ963の形状は、実施例6の基板ホルダ943とほぼ同様で、図13Dに示すように、貫通孔963A、貫通孔963Bを有するが、貫通孔963Bは片側に設けられている。
【0170】
図13Cに示すように、シート964は、実施例6のシート944とほぼ同じ構造である。シート964には、貫通孔964A、貫通孔964Aと連結している溝964B、溝964Bの端部の貫通孔964Cが形成されている。シート964と反応基板が密着し、シート965で覆われることで、貫通孔964Aの領域が反応チャンバ974になる。反応チャンバ974は、反応スポット102の上側に形成される。ここで二つの貫通孔964Cはシートの片側に配置しており、そのため、片方の溝964Bもそれにあわせて、溝が180度向きを変えて、貫通孔964A端部に連結する構造としている。
【0171】
図13Bに示すように、シート965は、実施例6のシート945と同じものである。シート964とシート965を密着させることによって、溝964Bに対応して、流路972及び973が形成され、シート964の貫通孔964Cに対応してインレット970とアウトレット971(図示なし)が形成される。インレット970とアウトレット971は、二つの貫通孔964C及び、各貫通孔964Cと対応する基板ホルダ963に設けられた貫通孔963Bによって構築される。
【0172】
これにより、インレット970、流路972、反応チャンバ974、流路973、アウトレット971とつながる流路が形成される。さらに、インレット970、アウトレット971には、インレットチューブ、アウトレットチューブが接続され必要な液を供給及び排出する構成とする。
【0173】
実施例3、4などと同様に、マイクロ流路チップは、インレット、供給流路、反応チャンバ、排出流路、及び、アウトレットを有し、供給流路、反応チャンバ、及び、排出流路は、順に接続されており、密閉された流路を形成する。インレット及びアウトレットは、反応スポットから20mm離して配置されている。本構成により、液漏れすることなく、反応基板(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に離れて設けられる。これにより、小さな基板サイズのものでも、測定装置に必要な部品の配置に影響を与えることなく、使用することができる。
【0174】
上面は完全フラットであり、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。また、下面には、インレットチューブ、アウトレットチューブが接続されるが、反応スポットの位置から十分に離れて配置されており、また、片側に集中しているため、全反射プリズム等を配置する際にも影響を与えることがない。また、下面から対物レンズで、全反射照明する場合でも同様に対応できる。
【0175】
本実施例では、インレット、アウトレットが片側にまとまっているため、チップ表面の空間が寄り広く確保でき、装置構成が容易になる。また、接続するインレットチューブ、アウトレットチューブをまとめてハンドリングすることが容易にでき、装置構成が容易になる。
本実施例によれば、前記実施例などと同様の効果がある。
【0176】
[実施例8]
本発明をさらに別の実施の形態例により説明する。
図14A,図14Bを参照して本発明によるマイクロ流路チップの例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。
本実施例では、実施例7と同一の構成を有する。実施例7では、インレット、供給流路、反応チャンバ、排出流路、及び、アウトレットが一組であったが、本例では、同一反応基板に4組並列させて配置している。図14Aは実施例7の図13Cに相当するシート975の図であり、4組の流路を設けている。それぞれ、二つの貫通孔975C、反応チャンバとなる貫通孔975A、貫通孔975Cと975Aを連結し上面に作成された二つの溝975Bからなる。各貫通孔975Aは、横幅4mm、縦幅1mmの大きさで、2mmピッチで配置している。4つの貫通孔975Aは全体で横4mm、縦7mmの領域に形成され、反応基板(一辺の寸法が約10mmの正方形)上に4つの反応チャンバを形成する。なお、貫通孔975Aの大きさを変えれば、反応チャンバ数を変えることができる。
【0177】
また、各貫通孔975Cはφ1mm、各溝975Bは、深さ約50μm、幅約500μmである。各貫通孔975Cは2mm間隔で縦方向に並んでおり、全体の縦方向の寸法は15mmであり、基板ホルダのサイズ、26mm×76mmに収められている。
【0178】
図14Bは、実施例7の図13Dに相当する基板ホルダ976の図であり、反応基板を収める貫通孔976A、及び、シート975の貫通孔975Cと同じ配置の貫通孔976Bを有する。
【0179】
基板ホルダ976と反応基板と、シート975、及びシート965により、マイクロ流路チップが構成され、1反応基板に複数の反応チャンバと流路を構築することができ、多検体の解析を可能にする。
【0180】
[実施例9]
本発明をさらに別の実施の形態例により説明する。
図15A、図15B、図15C、図15D、図15Eを参照して本発明によるマイクロ流路チップ980の例を説明する。反応基板981には、厚さが約0.17mm、一辺の寸法が約12mmの正方形の石英ガラス基板を使用する。石英ガラス製の反応基板981には、前記実施例と同様に反応スポット982が形成されている。マイクロ流路チップ980は、反応基板981、基板ホルダ983、シート984、シート985、シート986で構成する。
【0181】
図15Eに示すように、基板ホルダ983は、反応基板981を固定するための貫通孔983Aを設け、またインレット及びアウトレットになる貫通孔983B(φ2mm)を有する。基板ホルダ983の寸法は縦26mm、横76mmであり、厚さは1mmとする。貫通孔983Aの寸法は10mm×10mmで、その下面に孔の中心と反応基板の中心とを合わせて、反応基板981を接着させて固定する。
【0182】
反応基板981の上側は、基板ホルダ983の貫通孔983Aの開口(厚さ1mm)が配置されている。この開口を埋めるようにシート986が反応基板981に接着される。シート986は図15Dに示すように、縦9mm、横9mm、厚さ1mmのPDMSシートであり、下面ほぼ中心に凹部986A(縦2mm、横4mmの六角形で、深さ0.05mm)が形成され、その端部にφ1mmの貫通孔986Bを有する。
【0183】
シート986の上面にはシート984が配置されている。このシート984は、シート986及び基板ホルダ983の上面と接着される。シート984は、図15Cに示すように、貫通孔986Bと位置を合わせた貫通孔984A(φ1mm)と、貫通孔983Bと位置を合わせた貫通孔984C(φ2mm)と、貫通孔984Aと貫通孔984Cとを連結し上面に作成された溝984Bとを有する。シート984の大きさは、縦26mm、横48mmであり、厚さは0.2mmである。溝984Bの深さは75μm、幅は400μmである。
【0184】
シート984の上面にはシート985を配置し、接着する。シート985は、図15Bに示すように、シート984と同じ大きさで厚さ0.5mmのガラス板を使用する。厚みは特に限定されない。また大きさは、シート984の貫通孔と溝の上部を覆えるだけのサイズであれば適用できる。
【0185】
反応基板981の上側に配置されたシート986の凹部986Aが反応チャンバ994となる。シート986の貫通孔986B、シート984の貫通孔984A、シート985、及び、シート984の溝984Bによって、流路992、及び993が構築される。基板ホルダ983の貫通孔983Bとシート984の貫通孔984Cによって、インレット990とアウトレット991(図示無し)が構築される。インレット990、流路992、反応チャンバ994、流路993、アウトレット991とつながる密閉された流路が形成される。本構成により、液漏れすることなく、反応基板981の外部から内部へ、また外部につながる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に設けることができる。具体的には反応基板中心から15mm以上離すこともできる。これにより、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。
【0186】
なお、本例では、蛍光検出用の対物レンズを反応基板下面に配置する。NA1.49の60倍対物レンズを使用し、オイルカップリングで、反応基板と光学的に接合する。励起光は、対物レンズを通して反応基板に導入し、反応スポット面にて入射角が臨界角となるように勝者し、エバネッセント励起とする。生じる蛍光は、同じ対物レンズにより集光され、検出される。
【0187】
本実施例では、薄い反応基板を使用することができ、プリズムエバネッセント照射のほか、対物エバネッセント照射が可能でとなる。
【0188】
本実施例によっても、より小さな基板で流路を構築することができ、チップの低コスト化が実現できる。
【0189】
以上本発明の例を説明したが本発明は上述の例に限定されるものではなく、特許請求の範囲に記載された発明の範囲にて様々な変更が可能であることは、当業者によって容易に理解されよう。
【符号の説明】
【0190】
100…マイクロ流路チップ、101…反応基板、102…反応スポット、103…基板ホルダ、104…反応室シート、105…流路シート、110…インレット、111…アウトレット、112…供給流路、113…排出流路、114…反応チャンバ、120…全反射プリズム、121…入射光路、122…出射光路、131…パッキン、200…分析装置、211…試薬保管ユニット、212…分注ユニット、213…インレットチューブ、214…アウトレットチューブ、215…廃液容器、221…励起光用レーザーユニット、222…励起光用レーザーユニット、223、224…λ/4波長版、225…ミラー、226…ダイクロイックミラー、227…ミラー、231…対物レンズ、232…フィルター、233…結像レンズ、234…2次元センサカメラ、235…カメラコントローラ、240…装置制御用コンピュータ、241…解析用コンピュータ、242…出力装置、500…マイクロアレイチップ、501…反応基板、502…反応スポット、503…基板ホルダ、504…セプタ、505…流路シート、510…インレットチャンバ、511…アウトレットチャンバ、512…供給流路、513…排出流路、514…反応チャンバ、610…支持体、611…凹部、622…カメラ、621…照明装置、700…分析装置、701…インレットニードル、702…アウトレットニードル、703…電極、711…サンプルトレイ、712…洗浄水ボトル、713…ヒスチジンボトル、714…予備ボトル、715…4方向バルブ、716…支持体、717…2方向バルブ、718…吸引装置、720…廃液ボトル、741…解析用コンピュータ、742…出力装置、743…バーコードリーダ、900…マイクロ流路チップ、903…基板ホルダ、903A…凹部、903B…反応基板保持部、903C…照明窓、904…シート、904A…凹部、904B…貫通孔、904C…溝、904D…両端部、905…シート、905A…貫通孔、910…インレット、911…アウトレット、912…供給流路、913…排出流路、914…反応チャンバ、920…マイクロ流路チップ、923…基板ホルダ、923A…貫通孔、930…マイクロ流路チップ、933…基板ホルダ、933A…凹部、933B…反応基板保持部、933C…照明窓、934…シート、934B…貫通孔、934C…溝、934D…両端部、935…シート、936…シート、936A…貫通孔、940…マイクロ流路チップ、943…基板ホルダ、943A…貫通孔、943B…貫通孔、944…シート、944A…貫通孔、944B…溝、944C…貫通孔、945…シート、950…インレット、951…アウトレット、952…供給流路、953…排出流路、954…反応チャンバ、955…インレットチューブ、956…アウトレットチューブ、960…マイクロ流路チップ、963…基板ホルダ、963A…貫通孔、963B…貫通孔、964…シート、964A…貫通孔、964B…溝、964C…貫通孔、965…シート、970…インレット、971…アウトレット、972…供給流路、973…排出流路、974…反応チャンバ、975…シート975、975A…貫通孔、975B…溝、975C…貫通孔、976…基板ホルダ、976A…貫通孔、976B…貫通孔、980…マイクロ流路チップ、981…反応基板、982…反応スポット、983…板ホルダ、983A…貫通孔、983B…貫通孔、984…シート、984A…貫通孔、984B…溝、984C…貫通孔、985…シート、986…シート、986A…凹部、986B…貫通孔、990…インレット、991…アウトレット、992…供給流路、993…排出流路、994…反応チャンバ。
【技術分野】
【0001】
本発明は、遺伝子診断装置、遺伝子解析装置等の核酸分析装置にて使用して好適なマイクロ流路チップ及びマイクロアレイチップに関する。
【背景技術】
【0002】
近年、核酸分析装置において、ガラス基板等で作製された反応基板に多数のDNAプローブ又はポリメラーゼを固定し、塩基伸長反応を行うことで配列を決定する方法が提案されている。このような固定及び反応を行う領域を、以下「反応スポット」と呼ぶ。反応スポットの形成方法として、単一分子を固定する場合(単分子方式)や同一種複数分子を固定する場合(複数分子方式)がある。また多数の反応スポットを配置し、各々の反応スポットで並列して塩基伸長及び配列決定を行う超並列方式核酸分析装置が開発されている。
【0003】
非特許文献1には、反応スポットに単一分子を固定し、全反射エバネッセント照射検出方式を用いて単分子レベルのDNA配列解読を行う方法が記載されている。特許文献1には、局在型表面プラズモンの蛍光増強効果を利用して、塩基伸長反応を計測することが記載されている。特許文献2及び特許文献3には、ポリジメチルシロキサン(PDMS)基板又はシートを用いたマイクロ流路チップの製造方法の例が記載されている。特許文献4には、ナノチップを用いてPCR生成物であるサンプルを分析する方法が記載されている。特許文献5及び特許文献6には、インレットとアウトレットを有するマイクロ流路チップでの測定例が記載されている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2009-45057号公報
【特許文献2】特開2009-47438号公報
【特許文献3】特開2005-111567号公報
【特許文献4】特開2005-181145号公報
【特許文献5】特開2005-245317号公報
【特許文献6】特開2005-233802号公報
【非特許文献】
【0005】
【非特許文献1】Ido Braslavsky, ”Proc. Natl. Acad. Sci. USA”,2003年, Vol. 100, No. 7, pp. 3960-3964
【発明の概要】
【発明が解決しようとする課題】
【0006】
マイクロ流路チップは核酸分析装置等に装着され、溶液等の供給系と廃液を排出する排出系が接続される。マイクロ流路チップは、溶液供給系と廃液排出系を容易に接続できる構造であることが好ましい。更に、マイクロ流路チップの両面または片面には、照明装置及び検出装置が配置される。例えば、高倍率の対物レンズで観察する場合、対物レンズをマイクロ流路チップに近接させる必要がある。従って、マイクロ流路チップは、照明装置及び検出装置がどのような構造であっても、適合することが好ましい。
【0007】
マイクロ流路チップは反応スポットを備えた反応基板を有する。反応基板は半導体製造プロセス処理を用いて製造されるため、比較的高価である。反応基板の寸法は、できるだけ小さいほうがよく、理想的には観察すべき反応スポットが配置された領域と同等の寸法であれば無駄がない。
【0008】
本発明の目的は、周囲の機器の配置に制限されることなく容易に装着可能であり、且つ、製造コストが比較的安いマイクロ流路チップを提供することにある。
【課題を解決するための手段】
【0009】
本発明のマイクロ流路チップは、反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及びアウトレットをそれぞれ接続する供給流路及び排出流路と、を有する。
【0010】
本発明のマイクロ流路チップは、凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダ及び前記反応基板を覆うように配置された第1のシートと、該第1のシートを覆うように配置された第2のシートと、によって構成される。また、本発明のマイクロ流路チップは、反応基板と、該反応基板より大きく、少なくとも反応チャンバ部に相当する部分に貫通孔または凹部を有する第1のシートと、該第1のシートと接着する第2のシートと、によって構成される。
【0011】
本発明のマイクロ流路チップによると、前記反応基板と前記第1のシートの貫通孔と前記第2のシートによって前記反応チャンバが形成され、または、前記反応基板と前記第1のシートの凹部によって前記反応チャンバが形成され、前記インレット及びアウトレットは該反応基板より離れた外側に配置され、該反応チャンバと該インレット及びアウトレットを連結する流路が該第1のシートと第2のシートの間に形成される。
【発明の効果】
【0012】
本発明によると、周囲の機器の配置に制限されることなく容易に装着可能であり、且つ、製造コストが比較的安いマイクロ流路チップを提供することができる。
【図面の簡単な説明】
【0013】
【図1A】本発明のマイクロ流路チップの構成例(実施例1)を示す図である。
【図1B】本発明のマイクロ流路チップの流路シートの例を示す図である。
【図1C】本発明のマイクロ流路チップの反応室シートの例を示す図である。
【図1D】本発明のマイクロ流路チップの基板ホルダの例を示す図である。
【図1E】本発明のマイクロ流路チップの反応基板の例を示す図である。
【図2】本発明のマイクロ流路チップを用いたDNAシーケンサ装置の主要部を説明する図である。
【図3】本発明のマイクロ流路チップを用いた単一分子DNAシーケンサ装置の例を説明する図である。
【図4】本発明のマイクロ流路チップを用いた単一分子DNA配列解析方法の例を説明する図である。
【図5A】本発明のマイクロアレイチップの構成例(実施例2)を示す図である。
【図5B】本発明のマイクロアレイチップの流路シートの例を示す図である。
【図5C】本発明のマイクロアレイチップの基板ホルダの例を示す図である。
【図5D】本発明のマイクロアレイチップの反応基板の例を示す図である。
【図6A】本発明のマイクロアレイチップを遺伝子解析装置へ装着する方法を説明する図である。
【図6B】本発明のマイクロアレイチップを遺伝子解析装置へ装着する方法を説明する図である。
【図7】本発明のマイクロアレイチップを用いた遺伝子解析システムの構成例を説明する図である。
【図8】本発明のマイクロアレイチップを用いた遺伝子解析システムの操作方法の例を説明する図である。
【図9A】本発明のマイクロ流路チップの別の構成例(実施例3)を示す図である。
【図9B】本発明のマイクロ流路チップ図9Aのシート2の上面図である。
【図9C】本発明のマイクロ流路チップ図9Aのシート1の上面図である。
【図9D】本発明のマイクロ流路チップ図9Aの基板ホルダの上面図である。
【図10A】本発明のマイクロ流路チップの別の構成例(実施例4)を示す図である。
【図10B】本発明のマイクロ流路チップ図10Aの基板ホルダの上面図である。
【図11A】本発明のマイクロ流路チップの別の構成例(実施例5)を示す図である。
【図11B】本発明のマイクロ流路チップ図11Aのシート2の上面図である。
【図11C】本発明のマイクロ流路チップ図11Aのシート1の上面図である。
【図11D】本発明のマイクロ流路チップ図11Aのシート3の上面図である。
【図11E】本発明のマイクロ流路チップ図11Aの基板ホルダの上面図である。
【図12A】本発明のマイクロ流路チップの別の構成例(実施例6)を示す図である。
【図12B】本発明のマイクロ流路チップ図12Aのシート2の上面図である。
【図12C】本発明のマイクロ流路チップ図12Aのシート1の上面図である。
【図12D】本発明のマイクロ流路チップ図12Aの基板ホルダの上面図である。
【図13A】本発明のマイクロ流路チップの別の構成例(実施例7)を示す図である。
【図13B】本発明のマイクロ流路チップ図13Aのシート2の上面図である。
【図13C】本発明のマイクロ流路チップ図13Aのシート1の上面図である。
【図13D】本発明のマイクロ流路チップ図13Aの基板ホルダの上面図である。
【図14A】本発明のマイクロ流路チップの別の構成例(実施例8)のシート1の上面図である。
【図14B】本発明のマイクロ流路チップの別の構成例(実施例8)の基板ホルダの上面図である。
【図15A】本発明のマイクロ流路チップの別の構成例(実施例9)を示す図である。
【図15B】本発明のマイクロ流路チップ図15Aのシート2の上面図である。
【図15C】本発明のマイクロ流路チップ図15Aのシート1の上面図である。
【図15D】本発明のマイクロ流路チップ図15Aのシート3の上面図である。
【図15E】本発明のマイクロ流路チップ図15Aの基板ホルダの上面図である。
【発明を実施するための形態】
【0014】
[実施例1]
図1A、図1B、図1C、図1D及び図1Eを参照して本発明によるマイクロ流路チップの第1の例を説明する。図1Aに示すように、本例のマイクロ流路チップは、基板ホルダ103と、基板ホルダ103に装着された反応基板101と、基板ホルダ103及び反応基板101を覆うように配置された反応室シート104と、更にその上に配置された流路シート105とを有する。反応基板101、基板ホルダ103、反応室シート104、及び、流路シート105の2つの主面のうち、図1A、図1B、図1C、図1D及び図1Eにて上側の面を上面、下側の面を下面と称することとする。
【0015】
反応基板101の上面には、反応スポット102が形成されている。反応スポット102は、多数のDNAプローブ又はポリメラーゼを固定し、塩基伸長反応等を行う領域のことである。マイクロ流路チップの下面には照明窓103Cが形成されている。照明窓103Cを介して、反応基板101の下面が露出している。本例のマイクロ流路チップでは、図1Aの断面図において、下方から照明窓103Cを介して照明光を反応スポット102に照射し、上方から流路シート105を介して反応スポット102を観察する。従って、流路シート105、反応室シート104及び反応基板101は透明な材料によって形成される。
【0016】
マイクロ流路チップは、インレット110、供給流路112、反応チャンバ114、排出流路113、及び、アウトレット111を有する。供給流路112、反応チャンバ114、及び、排出流路113は、順に接続されており、密閉された通路を形成している。インレット110及びアウトレット111は、顕微鏡の対物レンズおよび励起光源光学系部品配置の障害とならないよう、反応スポット102から少なくとも約30mm離れた位置に形成されている。
【0017】
図1Eに示すように、反応基板101は、厚さが約0.7mm、一辺の寸法が約10mmの正方形の薄い板状部材からなる。しかしながら、反応基板101は、好ましくは、一辺の寸法が20mm以下の正方形の板状部材であってよく、更に、一辺の寸法が5mm〜500mmの正方形の板状部材であってもよい。更に、反応基板101は、正方形以外の形状、例えば、長方形、多角形、円形等の板状部材であってもよい。
【0018】
反応基板101は、石英によって形成される。反応基板101の上面には、遺伝子配列、遺伝子多型などを解析するための反応スポット102が形成されている。
【0019】
反応スポット102は、局在型表面プラズモンが発生し易いように微細構造を有することが好ましい。局在型表面プラズモンは局所的に蛍光を増加させる効果を有する。効果が及ぶ範囲は、10nmから20nm程度の極小領域である。このような極小領域に、ターゲットDNA分子を固定し、このターゲットDNA分子に蛍光標識したプライマー単一分子を結合させると、プライマー単一分子からの蛍光のみを局所的に増加させることができる。周囲に浮遊するプライマー単一分子からの蛍光は、局在型表面プラズモンによる蛍光増加効果の影響を受けないから、両者を峻別することができる。
【0020】
特許文献1には、局在型表面プラズモンが発生し易い微細構造の形成方法の例が記載されている。この文献に記載された例では、半導体製造プロセスによってウエハ上に微細構造を形成する。先ず、円形の石英基板(ウエハ)に、金属蒸着、エッチング、スパッタリング、ミリング等の半導体製造プロセス処理を行い、反応スポットを生成する。こうして多数の反応スポットが形成されたウエハを、ダイシング(裁断)して、所定の寸法の反応基板101を形成する。反応基板101は、マイクロ流路チップを構成する他の部品より比較的高価である。従って、反応基板101の寸法はできるだけ小さいことが好ましい。本発明によると、反応基板101は基板ホルダ103の凹部103Aに収納されるように構成されており、反応基板101の寸法を比較的小さくすることができる。それによって、マイクロ流路チップの価格を抑制することができる。
【0021】
図1Dに示すように、基板ホルダ103の上面には、反応基板101を収納するための凹部103Aが形成されている。凹部103Aの底面には、貫通孔が形成されている。この貫通孔によって、マイクロ流路チップの照明窓103Cが形成される。即ち、マイクロ流路チップの照明窓103Cにて、反応基板101の下面が露出する。照明窓103Cの周囲の部材によって、反応基板を保持するための反応基板保持部103Bが形成される。照明窓103Cの縦横寸法は、反応基板101の縦横寸法より小さい。従って、反応基板保持部103Bによって反応基板101を支持することができる。
【0022】
基板ホルダ103は、一般的なスライドグラスと同等の寸法を有する。即ち、縦横の寸法は、26mm×76mmである。厚さは好ましくは2mm程度であるが、0.1mm〜10mmでもよい。凹部103Aの縦横寸法は、反応基板の縦横寸法より大きく、凹部103Aの深さは、反応基板101の厚さと同一か又はそれより大きい。反応基板保持部103Bの厚さは、好ましくは、約0.5mmであるが、0.01mm〜5mmでもよい。
【0023】
基板ホルダ103は、ユーザによる不意の取り扱いミスや落下にも耐えうる材料によって形成される。このような材料として、ステンレス、アルミニウム、鉄などの金属、あるいは、プラスチック、エラストマーなどの樹脂がある。
【0024】
図1Cに示すように、反応室シート104は、基板ホルダ103の外形と同等の形状及び寸法を有する。反応室シート104の中心部には貫通孔104Aが形成されている。この貫通孔104Aによって、マイクロ流路チップの反応チャンバ114が形成される。即ち、反応チャンバ114の形状は、貫通孔104Aの形状に等しい。
【0025】
本例では、貫通孔104Aの形状は、六角形を反応室シートの長手方向に引き伸ばして得られる形状である。貫通孔104Aの両端104Bの角部は、反応室シート104の中心軸線に沿って配置されている。貫通孔104Aの形状は、中心軸線上の両端104Bが尖った形状が好ましい。それによって、反応チャンバ114に流れ込んだ液体が、両端の角部において、滞留することが回避される。しかしながら、図示の貫通孔104Aの形状は、例示であり、菱形、楕円、円、多角形、長方形等であってもよい。
【0026】
貫通孔104Aの寸法は、反応スポット102より大きいが、反応基板101より小さい。従って、反応チャンバ114の底面は、貫通孔104Aにて露出した反応基板101の上面によって形成される。検出光学系によって一度に観察できる領域を、以下に、「計測視野」と呼ぶ。反応チャンバ114の底面は、少なくとも、計測視野の寸法と同程度か又はそれより大きい。従って、貫通孔104Aの寸法は、計測視野の寸法と同程度か又はそれより大きい。
【0027】
反応室シート104の厚さは、好ましくは50μmであるが、5μm〜5mmでもよい。反応室シートは、耐熱性、耐寒性、耐候性、及び、耐薬品性を有する材料によって形成される。このような材料として、ポリジメチルシロキサン(PDMS)が好ましい。PDMSは自己吸着性を有するため、接着剤を使用しなくても他の部材と接着可能である利点を有する。尚、PDMSに対して用途に応じた表面処理が可能である。それにより、PDMSに、疎水性・親水性・自己吸着性を付与することができる。しかしながら、自己吸着性、又は、光化学反応による接着などが可能な材質であり、且つ、使用する試薬、実験系に不具合を与えなければ、PDMS以外の材料であってもよい。例えば、シリコン樹脂、ポリ塩化ビニル(PVC)などでもよい。
【0028】
図1Bに示すように、流路シート105は、基板ホルダ103の外形と同等の形状と寸法を有する。流路シート105には、中心軸線上に沿って、2つの貫通孔105Aが形成されている。貫通孔105Aは円形であり、流路シート105の両端近くに形成されている。流路シート105の下面には、2本の溝105Bが形成されている。これらの溝は、貫通孔105Aから、基板ホルダ103の中心軸線に沿って中心方向に延びており、他端には小さな円形の凹部105Cが形成されている。
【0029】
溝105Bの深さは約50μm、幅は約500μmである。凹部105Cの深さは、溝105Bの深さと同一であってよい。凹部105Cの径は、溝105Bの幅と同一であってもよいが、それより大きくてもよい。
【0030】
2つの貫通孔105Aによって、マイクロ流路チップのインレット110及びアウトレット111が形成される。2つの溝105Bによって、マイクロ流路チップの供給流路112及び排出流路113が形成される。
【0031】
上述のように、インレット110及びアウトレット111は、顕微鏡の対物レンズおよび励起光源光学系部品配置の障害とならないよう、反応スポットから少なくとも約30mm 離れた位置に形成されている。従って、2つの貫通孔105Aは、流路シート105の中心より、少なくとも30mm離れた位置に形成される。2本の溝105Bの内端の凹部105Cは、反応室シート104の貫通孔104Aの両端104Bに対応した位置にて、且つ、貫通孔104Aの内側の位置に形成されている。
【0032】
流路シート105の厚さは、好ましくは100μmであるが、5μm〜10mmでもよい。流路シート105は、反応室シートと同様に、耐熱性、耐寒性、耐候性、及び、耐薬品性を有する材料によって形成される。このような材料として、ポリジメチルシロキサン(PDMS)が好ましい。PDMSは自己吸着性を有するため、接着剤を使用しなくても他の部材と接着可能である利点を有する。例えば、流路シート105と反応室シート104の両者をPDMSによって形成することにより、自己吸着性を利用して両者を接合することができる。こうして、流路形成のために接着剤を用いた接合プロセスを省くことが可能となる。以下に、流路シート105と反応室シートの両者は、PDMSによって形成されているものとして説明する。
【0033】
本例のマイクロ流路チップの組立方法を説明する。先ず、基板ホルダ103の凹部103Aに反応基板101を配置する。このとき、基板ホルダ103と反応基板101の上面が共面となるように、配置する。基板ホルダ103の照明窓103Cの寸法より、反応基板101の寸法のほうが大きいから、反応基板101によって、照明窓103Cは塞がれる。反応基板101の下面は、照明窓103Cによって露出する。次に、基板ホルダの反応基板保持部103Bに、反応基板101を接着する。接着方法は、接着剤による接着であってもよいが、溶着であってもよい。次に、基板ホルダ103の上面に、反応室シート104を貼付する。本例では、反応室シート104は、PDMSによって形成されている。従って、PDMSの自己吸着性により、反応室シート104は、基板ホルダ103および反応基板101の上面に吸着する。反応室シート104の貫通孔104Aの寸法は、反応基板101の寸法より小さいから、貫通孔104Aの周囲にて、反応室シート104と反応基板101の間には隙間は形成されない。
【0034】
次に、反応室シート104の上に、さらに流路シート105を装着する。本例では、反応室シート104と流路シート105は、PDMSによって形成されている。従って、PDMSの自己吸着性により、流路シート105と反応室シート104は互いに吸着する。こうして、マイクロ流路チップが形成される。こうして形成されたマイクロ流路チップでは、流路シート105を天井面とし、反応基板101を底面とし、反応室シート104の貫通孔を側面とする反応チャンバ114が形成される。更に、流路シート105の溝105Bを通路とし、反応室シート104を底面とする供給流路112、及び、排出流路113が形成される。
【0035】
なお、本例では、流路シート105に溝105Bが形成されているが、流路シート105の代わりに反応室シート104に同様な溝を形成してもよい。
【0036】
マイクロ流路チップの特徴は、分析対象及び分析方法により、様々な反応スポットを有する反応基板101を用いることができるが、反応基板101以外の部材は共通である、即ち、同一である。従って、量産効果により、マイクロ流路チップの製造価格を安くすることが可能となる。
【0037】
図2を参照して、本発明のマイクロ流路チップを用いたDNAシーケンサ装置の主要部を説明する。マイクロ流路チップの構造は、図1Aに示したものと同様である。先ず、試薬供給及び排出系について説明する。マイクロ流路チップのインレット110には、パッキン131を介して、インレットチューブ213が接続されている。マイクロ流路チップのアウトレット111には、パッキン132を介して、アウトレットチューブ214が接続されている。パッキン131、132は、ゴム、シリコン、PDMS等により形成される。
【0038】
励起光源光学系、及び、検出光学系について説明する。図2では、検出光学系として対物レンズ231のみを示す。本例では、励起光源光学系として、全反射エバネッセント照射検出方式を用いる。反応基板101の下面には、全反射プリズム120が装着されている。全反射プリズム120は、一辺が数センチメートルの正方形の底面と、底面に対して傾斜した側面を有する。全反射プリズム120は、反応基板101の下面に接合されてよい。全反射プリズム120は、接着剤によって接合されてよいが、好ましくは、油侵によって接合される。全反射プリズム120は、反応基板101の下面のうち、照明窓によって露出された部分に装着されている。
【0039】
入射光路121に沿って導かれた励起用レーザ光は、全反射プリズム120の一方の傾斜面に入射され、反応基板101の上面に到達する。励起用レーザ光は、反応基板101の上面にて、全反射し、全反射プリズム120の他方の傾斜面から出射され、出射光路122に沿って導かれる。反応基板101の上側には、反応チャンバ114が形成されている。従って、反応基板101の上面は、屈折率境界面となる。屈折率境界面において全反射が起きると、およそ入射光の1波長程度の深さだけ低媒質側の内部に電磁波が浸透する。この光をエバネッセント光と呼ぶ。エバネッセント光により、反応スポット102に形成された金属構造体を含む極めて限定された領域のみが照明される。これは全反射エバネッセント照射と称される。エバネッセント光によって照射される領域をエバネッセント場と呼ぶ。
【0040】
本例の光学系では、更に、局在型表面プラズモンの蛍光増強効果を利用する。上述のように、反応スポット102には、局在型表面プラズモンが発生し易いように微細構造が形成されている。反応スポット102の微細構造にて、局在型表面プラズモンが発生すると、微細構造を含む極小領域において蛍光が増加する。
【0041】
反応スポット102には、ハイブリダイゼーション反応によって、蛍光標識された単一のプライマー分子が結合する。更に、塩基伸長反応によって、蛍光標識されたdNTP分子(NはA、C、G、Tのいずれかである)が取り込まれる。これらの蛍光色素は、エバネッセント光を励起光として発光する。更に、これらの蛍光色素からの発光は、局在型表面プラズモンにより、局部的に増加する。この発光は、反応基板101の上側に配置された対物レンズ231を含む検出光学系によって検出される。
【0042】
浮遊しているプライマー分子及びdNTP分子は、エバネッセント場外にあるから、エバネッセント光に起因する蛍光を発生しない。また、これらの浮遊分子は局在型表面プラズモンによる蛍光増加効果を受けない。従って、ハイブリダイゼーション反応又は塩基伸長反応によって結合した単一分子の位置を正確に検出することができる。
【0043】
本発明によるマイクロ流路チップの特徴は、インレット110とアウトレット111をマイクロ流路チップの上側に、即ち、照明窓103Cの反対側に設けたことにある。それによって次のような利点が得られる。先ず、アウトレットチューブ214とインレットチューブ213を、マイクロ流路チップの上側に配置することができる。即ち、アウトレットチューブ214とインレットチューブ213を、励起光源光学系とは反対側に配置することができる。それによって、マイクロ流路チップの上側に検出光学系を設け、マイクロ流路チップの下側に励起光源光学系を設けることができる。更に、励起光源光学系のためのスペースを確保することができる。従って、励起光源光学系の設計の自由度が高くなる。例えば励起光源光学系として、全反射エバネッセント照射検出方式を採用することが可能となる。全反射エバネッセント照射検出方式では、全反射プリズム120を用いるが、本例では、全反射プリズム120を反応基板の下面に直接装着することができる。更に、全反射エバネッセント照射検出方式では、全反射プリズム120に対する入射光と反射光を別個の光路に沿って導く必要がある。本例では、入射光路121と出射光路122を容易に別個に設けることができる。
【0044】
更に、本発明によるマイクロ流路チップの特徴は、インレット110とアウトレット111をマイクロ流路チップの両端近くに配置したことにある。それによって次のような利点が得られる。アウトレットチューブ214とインレットチューブ213の間に検出光学系のためのスペースを確保することができる。従って、検出光学系の設計の自由度が高くなる。例えば、倍率が40倍、あるいは60倍、あるいは100倍の顕微鏡用対物レンズを用いる場合、マイクロ流路チップの上面から対物レンズの先端までの距離を0.2mm程度に接近させる必要がある。本例では、対物レンズを、マイクロ流路チップに近接して配置することが可能となり、大口径すなわち高N/Aの対物レンズを使用することが可能となる。従って、検出感度を向上させることができる。
【0045】
図3を参照して、単一分子DNAシーケンサ装置の例を説明する。本例のDNAシーケンサ装置は、分析装置200と解析用コンピュータ241と出力装置242を有する。分析装置200は、マイクロ流路チップ100の上側に設けられた検出光学系と、マイクロ流路チップ100の下側に設けられた励起光源光学系と、マイクロ流路チップ100の右側に設けられた溶液供給系と、マイクロ流路チップ100の左側に設けられた廃液回収系と、装置制御用コンピュータ240を有する。装置制御用コンピュータ240は解析用コンピュータ241に接続されている。
【0046】
検出光学系は、対物レンズ231、蛍光波長フィルター232、結像レンズ233、2次元センサカメラ(検出器)234、及び、カメラコントローラ(検出器コントローラ)235を有する。励起光源光学系は、第1及び第2の励起光用レーザーユニット221、222、第1及び第2のλ/4波長板223、224、ミラー225、ダイクロイックミラー226、及び、ミラー227を有する。
【0047】
溶液供給系は、試薬保管ユニット211、分注ユニット212及びインレットチューブ213を有する。廃液回収系は、アウトレットチューブ214及び廃液容器215を有する。マイクロ流路チップの上側に、図示していない温度制御ユニットを設けてもよい。温度制御ユニットを設けることによって、反応チャンバ内に導入されるサンプル液、試薬、洗浄液等は、所定の温度に保持される。
【0048】
本例では、インレットチューブ213からの溶液が、マイクロ流路チップの反応チャンバ114に導入され、アウトレットチューブ214に排出されるとき、溶液が漏洩することはない。例えば、反応室シート104と反応基板101の間は密に接着され、両者の間から溶液が漏洩することはない。従って、溶液が、基板ホルダ103に接触することはない。
【0049】
図4を参照して、本発明によるマイクロ流路チップを用いた単一分子DNA配列解析方法の例を説明する。ここでは、図3に示したDNAシーケンサ装置を用いる。試薬保管ユニット211には、単一のターゲットDNA分子溶液、蛍光色素Cy3によって蛍光標識されたプライマー単一分子溶液、蛍光色素Cy5によって蛍光標識された一種類の塩基のdNTP(NはA、C、G、Tのいずれかである)とポリメラーゼを含む溶液、洗浄液、等が保管されている。第1の励起光用レーザーユニット221は、波長532nmのレーザ光は発生し、第2の励起光用レーザーユニット222は、波長635nmのレーザ光を発生する。蛍光色素Cy3は、波長532nmのレーザ光によって発光し、蛍光色素Cy5は波長635nmのレーザ光によって発光する。
【0050】
先ず、ステップS101にて、反応基板の上面に、単一のターゲットDNA分子を固定化し、反応スポットを形成する。ターゲットDNA分子の固定化には、ビオチン-アビジンのタンパク質結合を利用する。未反応の余剰なターゲットDNA分子を洗い流す。こうして、反応基板に所望の反応スポットを形成することができる。
【0051】
ステップS102にて、蛍光色素Cy3によって蛍光標識されたプライマーを含む溶液を、マイクロ流路チップに形成された流路に導入する。分注ユニット212の吸込み口を、試薬保管ユニット211に保管された蛍光色素Cy3によって蛍光標識されたプライマー単一分子溶液に接続する。このプライマー単一分子溶液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。プライマー単一分子は、反応スポットに固定されたターゲットDNA分子とハイブリダイズする。所定の時間、ハイブリダイゼーション反応を行う。
【0052】
ステップS103にて、未反応の余剰なプライマーを洗い流す。分注ユニット212の吸込み口を、試薬保管ユニット211の洗浄液に接続する。この洗浄液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。未反応の余剰なプライマーは洗浄液によって洗い流され、反応チャンバ114から、排出流路113、アウトレット111、及び、アウトレットチューブ214を介して、廃液容器215に排出される。
【0053】
ステップS104にて、532nmの励起光を用いた全反射エバネッセント照射により、Cy3の蛍光を検出する。Cy3の蛍光を検出することにより、反応スポットに固定されたターゲットDNA分子とハイブリダイズしたプライマー単一分子の位置を検出することができる。
【0054】
第1の励起光用レーザーユニット221からの波長532nmのレーザ光は、λ/4波長板223、ミラー225、及び、ダイクロイックミラー226、及び、ミラー227を経由して、全反射プリズム120に導入される。全反射プリズム120に導入されたレーザ光は、反応基板の上面にて全反射する。このとき、エバネッセント光により、反応スポット102に形成された金属構造体を含む極めて限定された領域のみが照明される。エバネッセント光によって、プライマー分子の蛍光色素Cy3が発光する。更に、反応スポット102に形成された金属構造体にて、局在型表面プラズモンが発生させ、蛍光を増加させることができる。
【0055】
この蛍光は、対物レンズ231、蛍光波長フィルター232、及び、結像レンズ233を介して、2次元センサカメラ(検出器)234によって検出される。2次元センサカメラ(検出器)234によって得られた2次元輝度信号は、カメラコントローラ(検出器コントローラ)235を介して、装置制御用コンピュータ240に送られ、更に、解析用コンピュータ241に送られる。
【0056】
ステップS105にて、Cy3を高出力の励起光で照射することによって蛍光退色させ、以降の蛍光発光を抑制する。即ち、第1の励起光用レーザーユニット221からのレーザ光の出力を増加し、蛍光色素Cy3を退色させる。
【0057】
ステップS106にて、蛍光色素Cy5によって蛍光標識された一種類の塩基のdNTP(NはA、C、G、Tのいずれかである)とポリメラーゼを含む溶液を、マイクロ流路チップに形成された流路に導入する。分注ユニット212の吸込み口を、試薬保管ユニット211に保管された蛍光色素Cy5によって蛍光標識された一種類の塩基のdNTP(NはA、C、G、Tのいずれかである)とポリメラーゼを含む溶液に接続する。この溶液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。ターゲットDNA分子に対して相補関係にあるdNTP(NはA、C、G、Tのいずれかである)は、反応スポットにおいて、プライマー分子の伸長鎖に取り込まれる。所定の時間、塩基伸長反応を行う。
【0058】
ステップS107にて、未反応の余剰なdNTPを洗い流す。分注ユニット212の吸込み口を、試薬保管ユニット211の洗浄液に接続する。この洗浄液は、インレットチューブ213を介して、マイクロ流路チップの反応チャンバ114に導入される。未反応の余剰なdNTPは洗浄液によって洗い流され、反応チャンバ114から、排出流路113、アウトレット111、及び、アウトレットチューブ214を介して、廃液容器215に排出される。
【0059】
ステップS108にて、635nmの励起光を用いた全反射エバネッセント照射により、Cy5の蛍光を検出する。Cy5の蛍光を検出することにより、プライマー分子の伸長鎖に取り込まれたdNTPの位置を検出することができる。即ち、dNTP分子に対して相補関係にあるターゲットDNA分子の位置を検出することができる。
【0060】
第2の励起光用レーザーユニット222からの波長635nmのレーザ光は、λ/4波長板224、ダイクロイックミラー226及びミラー227を経由して、全反射プリズム120に導入される。全反射プリズム120に導入されたレーザ光は、反応基板の上面にて全反射する。このとき、エバネッセント光により、反応スポット102に形成された金属構造体を含む極めて限定された領域のみが照明される。エバネッセント光によって、dNTP分子の蛍光色素Cy5が発光する。更に、反応スポット102に形成された金属構造体にて、局在型表面プラズモンが発生させ、蛍光を増加させることができる。
【0061】
この蛍光は、対物レンズ231、蛍光波長フィルター232、及び、結像レンズ233を介して、2次元センサカメラ(検出器)234によって検出される。2次元センサカメラ(検出器)234によって得られた2次元輝度信号は、カメラコントローラ(検出器コントローラ)235を介して、装置制御用コンピュータ240に送られ、更に、解析用コンピュータ241に送られる。
【0062】
ステップS109にて、Cy5を高出力の励起光で照射することによって蛍光退色させ、以降の蛍光発光を抑制する。即ち、第2の励起光用レーザーユニット222からのレーザ光の出力を増加し、蛍光色素Cy5を退色させる。
【0063】
次に、dNTP(NはA、C、G、Tのいずれかである)における塩基の種類を例えばA>C>G>T>Aのように順次変更して、ステップS102〜ステップS109を繰り返す(段階的伸長反応)。解析用コンピュータ241は、ターゲットDNAに結合したプライマー分子の位置とdNTP分子の位置から、ターゲットDNA分子と相補関係にある塩基配列を決定する。
【0064】
[実施例2]
図5A、図5B、図5C及び図5Dを参照して、本発明のマイクロアレイチップの例を説明する。本例のマイクロアレイチップは、遺伝子解析用マイクロアレイチップとして用いられるように構成されている。即ち、微細電極パッドアレイにおける電気化学的結合によるハイブリダイゼーションを使用する診断装置を想定している。本例のマイクロアレイチップは、使い捨てを想定している。
【0065】
図5Aに示すように、本例のマイクロアレイチップ500は、基板ホルダ503と、基板ホルダ503に装着された反応基板501と、基板ホルダ503及び反応基板501を覆うように配置された流路シート505とを有する。反応基板501、基板ホルダ503、及び、流路シート505の2つの主面のうち、図5A、図5B、図5C及び図5Dにて上側の面を上面、下側の面を下面と称することとする。
【0066】
反応基板501の上面には、反応スポット502が形成されている。本例の遺伝子解析用マイクロアレイチップでは、図5Aの断面図において、上方から流路シート505を介して照明光を反応スポット502に照射し、上方から流路シート505を介して反応スポット502を観察する。従って、流路シート505は透明な材料によって形成される。
【0067】
マイクロアレイチップは、インレットチャンバ510、供給流路512、反応チャンバ514、排出流路513、及び、アウトレットチャンバ511を有する。インレットチャンバ510とアウトレットチャンバ511は、セプタ504によって封鎖されている。セプタ504は、ゴム、シリコン等の柔軟な材料によって形成された薄膜である。
【0068】
インレットチャンバ510、供給流路512、反応チャンバ514、排出流路513、及び、アウトレットチャンバ511は、順に接続されており、内部に密閉された通路を形成している。マイクロアレイチップでは、内部の空間が完全に密閉されており、そこに収納された溶液が漏洩することはない。従って、反応基板501に予め所望の反応スポット502が形成され、内部に溶液が充填されたマイクロアレイチップをそのまま搬送することができる。
【0069】
図5Dに反応基板501の例を示す。反応基板501の上面には、遺伝子配列、遺伝子多型などを解析するための反応スポット502が形成されている。
【0070】
本例の基板ホルダ503では、全反射エバネッセント照射検出方式を使用しないが、局在型表面プラズモンの局所的蛍光増加効果を利用してよい。従って、反応スポット502は、図1Eに示した例と同様に、局在型表面プラズモンが発生し易いように微細構造を有することが好ましい。
【0071】
本例の反応基板501は図1Eに示した反応基板101と比較すると、本例の反応基板の下面には、複数の制御電極501Aが設けられている点が異なる。制御電極501Aを設ける点以外は、本例の反応基板501は図1Eに示した反応基板101と同様であってよい。制御電極501Aを介して、反応スポット502に形成され微細電極に電圧を印加する。こうして、反応スポット502に形成された微細電極において、電気化学結合が生成される。
【0072】
図5Cに示すように、基板ホルダ503の下面には、反応基板501を収納するための凹部503Aが形成されている。この凹部503Aの底面には、貫通孔503Cが形成されている。貫通孔503Cの周囲の部材によって、反応基板を保持するための反応基板保持部503Bが形成される。
【0073】
貫通孔503Cによって、マイクロアレイチップの反応チャンバ514が形成される。即ち、反応チャンバ514の形状は、貫通孔503Cの形状に等しい。本例では、貫通孔503Cの形状は、六角形を流路シートの長手方向に引き伸ばして得られる形状である。貫通孔503Cの両端503Dの角部は、基板ホルダ503の中心軸線に沿って配置されている。貫通孔503Cの形状は、中心軸線上の両端503Dが尖った形状が好ましい。それによって、反応チャンバ514に流れ込んだ液体が、両端の角部において、滞留することが回避される。しかしながら、図示の貫通孔503Cの形状は、例示であり、菱形、楕円、円、多角形、長方形等であってもよい。
【0074】
貫通孔503Cの寸法は、反応スポット502より大きいが、反応基板501より小さい。従って、反応チャンバ514の底面は、貫通孔503Cにて露出した反応基板501の上面によって形成される。検出光学系によって一度に観察できる領域を、以下に、「計測視野」と呼ぶ。反応チャンバ514の底面は、少なくとも、計測視野の寸法と同程度か又はそれより大きい。従って、貫通孔503Cの寸法は、計測視野の寸法と同程度か又はそれより大きい。
【0075】
基板ホルダ503には、更に、中心軸線上に沿って、2つの貫通孔503Eが形成されている。貫通孔503Eは円形であり、基板ホルダ503の両端近くに形成されている。2つの貫通孔503Eによって、マイクロアレイチップのインレットチャンバ510及びアウトレットチャンバ511が形成される。
【0076】
基板ホルダ503は、一般的なスライドグラスと同等の寸法を有する。即ち、縦横の寸法は、26mm×76mmである。厚さは好ましくは2mm程度であるが、0.1mm〜10mmでもよい。凹部503Aの縦横寸法は、反応基板の縦横寸法より大きく、凹部503Aの深さは、反応基板501の厚さと同一か又はそれより大きい。反応基板保持部503Bの厚さは、好ましくは、約0.5mmであるが、0.01mm〜5mmでもよい。貫通孔503Cの縦横寸法は、反応基板501の縦横寸法より小さい。従って、反応基板保持部503Bにて反応基板501を装着することができる。本例の基板ホルダ503は、図1Dにて示した基板ホルダ103と同様な材料によって形成してよい。
【0077】
図5Bに示すように、流路シート505は、基板ホルダ503の外形と同等の形状と寸法を有してよい。但し、本例では、流路シート505の長手方向寸法は、基板ホルダ503の長手方向の寸法より僅かに小さい。流路シート505の下面には、中心軸線上に沿って、2つの凹部505Aが形成されている。凹部505Aは円形であり、流路シート505の両端近くに形成されている。流路シート505の下面には、2本の溝505Bが形成されている。これらの溝は、凹部505Aから、基板ホルダ503の中心軸線に沿って中心方向に延びており、他端には小さな円形の凹部505Cが形成されている。
【0078】
溝505Bの深さは約50μm、幅は約500μmである。凹部505A、505Cの深さは、溝505Bの深さと同一であってよい。凹部505Cの径は、溝505Bの幅と同一であってもよいが、それより大きくてもよい。
【0079】
基板ホルダ503の貫通孔503Eと流路シート505の凹部505Aによって、マイクロアレイチップのインレットチャンバ510及びアウトレットチャンバ511が形成される。流路シート505の2つの溝505Bによって、マイクロアレイチップの供給流路512及び排出流路513が形成される。
【0080】
2本の溝505Bの外端の凹部505Aは、基板ホルダ503の2つの貫通孔503Eに対応した位置に配置される。2本の溝505Bの内端の凹部505Cは、基板ホルダ503は貫通孔503Cの両端503Dに対応した位置にて、且つ、貫通孔503Cの内側の位置に形成されている。
【0081】
本例の流路シート505は、図1Bにて示した流路シート105と同様な材料によって形成してよい。
【0082】
本例のマイクロアレイチップの組立方法を説明する。基板ホルダ503の下面にて、貫通孔503Eにセプタ504を装着する。セプタ504によって、2つの貫通孔503Eの開口は完全に封鎖される。次に、基板ホルダ503の凹部503Aの反応基板保持部503Bに反応基板501を接着する。接着方法を説明する。先ず、反応基板501の下面の全面又は額縁状部分に、親水性処理を施してから、PDMSなどの樹脂皮膜を塗布する。親水性処理として、SiO2やTiO2等の超親水コート膜のコーティングを用いてよい。次に、こうして、親水性処理と樹脂皮膜を施した反応基板501を、基板ホルダ503の凹部503Aに貼付する。反応基板501のPDMS皮膜の自己吸着性により、反応基板501は、基板ホルダ503の凹部の反応基板保持部503Bに吸着する。
【0083】
本例では、基板ホルダ503の凹部503Aと反応基板501の間の接着面積は、図1Aに示した例と比較して、大きい。従って、反応基板501と基板ホルダ503は、両者の間の接着面において確実に密着される。反応チャンバ514に流れ込んだ液体が、反応基板501と基板ホルダ503の間より漏洩することはない。本例の接着方法では、接着剤を用いないことが好ましい。その理由は、反応チャンバ514に流れ込んだ液体が接着剤に接触する可能性を排除するためである。
【0084】
基板ホルダ503の貫通孔503Cの寸法は、反応基板501の寸法より小さいから、反応基板501によって、貫通孔503Cは塞がれる。貫通孔503Cの周囲にて、基板ホルダ503と反応基板501の間には隙間は形成されない。貫通孔503Cにて、反応基板501の上面が露出する。即ち、貫通孔503Cにて、反応基板501の上面の反応スポット502が露出する。反応基板501の下面は、基板ホルダ503の凹部503Aを介して外部に露出している。
【0085】
次に、基板ホルダ503の上面に、流路シート505を貼付する。本例では、流路シート505は、PDMSによって形成されている。従って、PDMSの自己吸着性により、流路シート505は、基板ホルダ503の上面に吸着する。こうして、マイクロアレイチップが形成される。こうして形成されたマイクロアレイチップでは、流路シート505を天井面とし、反応基板501を底面とし、基板ホルダ503の貫通孔503Cを側面とする反応チャンバ514が形成される。更に、流路シート505の溝505Bを通路とし、基板ホルダ503の上面を底面とする、供給流路512、及び、排出流路513が形成される。
【0086】
本例のマイクロアレイチップは、基板ホルダ503と流路シート505の2つの部材によって構成されており、図1Aに示す第1の例と比較して、構成部材が少ない。図1Aに示す第1の例では、マイクロ流路チップ内の流路を流れる溶液は、反応基板101、反応室シート104及び流路シート105に接触するが、基板ホルダ103には接触しない。しかしながら、本例のマイクロアレイチップでは、マイクロアレイチップ内の流路を流れる溶液は、反応基板501、流路シート505及び基板ホルダ503に接触する。即ち、基板ホルダ503と反応基板501の接着部に試薬等の溶液が直接接触する。従って、基板ホルダ503と反応基板501の間の接着面には接着剤は用いないことが好ましい。
【0087】
本例の遺伝子解析用マイクロアレイチップを用いた遺伝子解析の手順の例の概要を説明する。先ず、反応基板の反応スポットに、一端がビオチン化された塩基配列が既知のオリゴヌクレオチド(Capture Oligo)を供給し、制御電極を介して反応スポットの微細電極に電圧を印加する。オリゴヌクレオチド(Capture Oligo)は、微細電極に引き寄せられ、反応スポットの表面の透過層構造と接触する。オリゴヌクレオチド(Capture Oligo)のビオチン標識と透過層構造がavidin-biotin反応を起こし、オリゴヌクレオチド(Capture Oligo)は透過層構造に固定される。マイクロアレイチップの反応チャンバに洗浄液を供給し、未反応の余剰なオリゴヌクレオチド(Capture Oligo)を洗い流す。
【0088】
次に、別のオリゴヌクレオチド(Capture Oligo)を用いて上述の工程を繰り返す。それによって、反応スポットに、オリゴヌクレオチド(Capture Oligo)から成る所望のオリゴヌクレオチド・アレイが形成される。
【0089】
次に、マイクロアレイチップの反応チャンバに、一部の塩基配列が不明である分析対象のPCR生成物(Sample Oligos)を供給する。PCR生成物(Sample Oligos)は、反応スポットにて、相補的配列を有するオリゴヌクレオチド(Capture Oligo)とハイブリダイズする。このハイブリダイゼーション反応により、PCR生成物(Sample Oligos)は、オリゴヌクレオチド(Capture Oligo)によってキャプチャされ、反応スポットに固定される。洗浄液によって反応スポットを洗浄し、未反応の余剰なPCR生成物(Sample Oligos)を洗い流す。
【0090】
次にマイクロアレイチップの反応チャンバに、一端が蛍光標識されたオリゴヌクレオチド(Reporter Oligos)を供給する。このオリゴヌクレオチド(Reporter Oligos)は、反応スポットにて、相補的配列を有するPCR生成物(Sample Oligos)とハイブリダイズする。洗浄液によって反応スポットを洗浄し、未反応の余剰なオリゴヌクレオチド(Reporter Oligos)を洗い流す。
【0091】
マイクロアレイチップの反応基板の反応スポットに、励起光を照射する。この励起光により、PCR生成物(Sample Oligos)とハイブリダイズしたオリゴヌクレオチド(Reporter Oligos)から蛍光が発生する。この蛍光パターンを検出し、解析することで、PCR生成物(Sample Oligos)の塩基配列を分析することができる。
【0092】
図6A及び図6Bを参照して、本例の遺伝子解析用マイクロアレイチップを遺伝子解析装置へ装着する方法を説明する。図6Aに示すように、本例のマイクロアレイチップ500を、支持体610に装填する。マイクロアレイチップ500の両端を、支持体610の凹部611に、それぞれ係合させる。本例では、マイクロアレイチップ500の両端には、基板ホルダ503が露出している。従って、マイクロアレイチップ500の両端の基板ホルダ503の端部を、凹部611に、それぞれ係合させる。凹部611の幅は、基板ホルダ503の端部の厚さより大きい。基板ホルダ503の両端、即ち、マイクロアレイチップ500の両端は、支持体610の凹部611の下面上に配置されている。
【0093】
マイクロアレイチップの反応基板501には、診断目的に応じて、一端がビオチン化された塩基配列が既知のオリゴヌクレオチド(Capture Oligo)が既に結合されている。またオリゴヌクレオチドを安定して保存するため、マイクロアレイチップのインレットチャンバ510、供給流路512、反応チャンバ514、排出流路513、及び、アウトレットチャンバ511には、生理食塩水等のバッファが充填されている。
【0094】
マイクロアレイチップ500の下方には、インレットニードル701及びアウトレットニードル702が配置されている。インレットニードル701及びアウトレットニードル702は、支持体716によって支持されている。更に、マイクロアレイチップ500の下方には、電極703が設けられている。電極703は、支持体704に装着されている。支持体704は、ばね705によって支持体716に支持されている。
【0095】
インレットニードル701及びアウトレットニードル702はセプタ504の下方に配置されている。電極703は、反応基板501の下方に配置されている。
【0096】
図6Bに示すように、支持体716を上方に移動させる。インレットニードル701及びアウトレットニードル702と電極703が上昇する。インレットニードル701及びアウトレットニードル702はセプタ504を穿孔する。更に、支持体716を上方に移動させると、電極703が反応基板501の下面の制御電極501A(図5D参照)に係合し、電気回路が形成される。
【0097】
更に、支持体716を上方に移動させると、インレットニードル701及びアウトレットニードル702の先端は、マイクロアレイチップのインレットチャンバ510及びアウトレットチャンバ511内に配置される。セプタ504は、ゴム等の弾性変形可能な膜によって形成されているから、インレットニードル701及びアウトレットニードル702がセプタ504を穿孔しても、インレットニードル701及びアウトレットニードル702とセプタ504の間は密閉されている。即ち、インレットチャンバ510及びアウトレットチャンバ511の密閉性は確保される。インレットチャンバ510及びアウトレットチャンバ511内の液体が、インレットニードル701及びアウトレットニードル702とセプタ504の間から漏洩することはない。
【0098】
更に、支持体716を上方に移動させると、マイクロアレイチップ500は持ち上げられ、基板ホルダ503の両端、即ち、マイクロアレイチップ500の両端は、支持体610の凹部611の上面に当接する。更に、支持体716を上方に移動させると、ばね705が圧縮する。このとき、ばね705の圧縮力によって、電極703は、反応基板501の下面の制御電極501A(図5D参照)に押し付けられる。
【0099】
支持体610の凹部611の上面によって、マイクロアレイチップ500の基準位置が設定される。即ち、マイクロアレイチップ500の両端が、支持体610の凹部611の上面に当接しているとき、マイクロアレイチップ500は基準位置に配置されていると定義することができる。マイクロアレイチップ500の基準位置を設定することによって、光学観察系と、基板ホルダ503及び反応基板501の間の相対的な位置関係を所定の値に維持することが容易となる。
【0100】
こうして、アタッチメント操作が終了すると、遺伝子解析用の実験を行う。例えば、研究対象細胞の発現遺伝子等を蛍光色素等で標識した試薬を反応基板501の反応スポット502上でハイブリダイゼーションさせ、互いに相補的な核酸(DNA又はRNA)同士を結合させ、その箇所を蛍光色素等でラベルする。反応スポット502を照明装置621により照明し、CCDカメラ622により観察する。なお、カメラ622には予め蛍光波長のみを透過する光学バンドパスフィルタを装着し、蛍光信号のみを弁別し観察する。
【0101】
図7を参照して遺伝子解析システムの構成例を説明する。本例の遺伝子解析システムは、遺伝子解析装置700と解析用コンピュータ741と出力装置742とバーコードリーダ743を有する。分析装置200は、マイクロアレイチップ500の上側に設けられた検出光学系と、マイクロアレイチップ500の下側の右側に設けられた溶液供給系と、マイクロアレイチップ500の下側の左側に設けられた廃液回収系とを有する。
【0102】
検出光学系は、照明装置621、及び、CCDカメラ622を有し、カメラ622には所定の蛍光波長のみを透過する光学バンドパスフィルタが装着されている。
【0103】
溶液供給系は、サンプルトレイ711、洗浄水ボトル712、ヒスチジンボトル713、予備ボトル714、及び、4方向バルブ715を有する。サンプルトレイ711には、複数のサンプル又は試薬を保管することができる。サンプルトレイ711は、図示を省略したステージ装置により、X-Y-Z方向に移動可能である。ヒスチジンボトル713には、反応液として用いるヒスチジンが収納されている。
【0104】
サンプルトレイ711、洗浄水ボトル712、ヒスチジンボトル713、予備ボトル714は交換可能である。4方向バルブ715は、サンプルトレイ711、洗浄水ボトル712、ヒスチジンボトル713、及び、予備ボトル714の何れかと、マイクロアレイチップの反応チャンバ514を接続する。
【0105】
廃液回収系は、2方向バルブ717、吸引装置718及び廃液ボトル720を有する。2方向バルブ717は、マイクロアレイチップの反応チャンバ514と廃液ボトル720の何れかと、吸引装置718を接続する。吸引装置718はプランジャ718Aとシリンジ718Bを有する。
【0106】
本例の遺伝子解析システムの動作を説明する。先ず、4方向バルブ715によって、サンプルトレイ711の所定のサンプル保管部と、マイクロアレイチップの反応チャンバ514を接続する。2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。プランジャ718Aを下方に駆動することによって、マイクロアレイチップの反応チャンバ514と流路に充填されていた溶液は、シリンジ718Bに吸引され、代わりに、サンプルトレイ711に保管されていたサンプル溶液が、マイクロアレイチップの反応チャンバ514と流路を充填する。この動作をフィルと称する。
【0107】
次に、2方向バルブ717によって、廃液ボトル720と吸引装置718を接続する。プランジャ718Aを上方に駆動することによって、シリンジ718Bに充填されていた溶液は、廃液ボトル720に排出される。この動作をフラッシュと呼ぶ。
【0108】
次に、4方向バルブ715によって、洗浄水ボトル712と、マイクロアレイチップの反応チャンバ514を接続する。2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。プランジャ718Aを下方に駆動することによって、マイクロアレイチップの反応チャンバ514に充填されていた廃液は、シリンジ718Bに吸引され、代わりに、洗浄水ボトル712に保管されていた洗浄液が、マイクロアレイチップの反応チャンバ514と流路を充填する。即ち、洗浄液のフィルを行う。
【0109】
次に、2方向バルブ717によって、廃液ボトル720と吸引装置718を接続する。プランジャ718Aを上方に駆動することによって、シリンジ718Bに充填されていた廃液は、廃液ボトル720に排出される。即ち、廃液のフラッシュを行う。こうして、フィルとフラッシュを繰り返すことにより、所望の溶液の供給と排出を行うことができる。
【0110】
図8を参照して遺伝子解析システムの操作を説明する。ステップS701にて、遺伝子解析システムの電源を入れ、初期化を行う。初期化では、洗浄水ボトル712内の洗浄液の容量の確認とヒスチジンボトル713内のヒスチジンの容量の確認を行う。ステップS702にて、サンプル等の準備を行う。本例では、遺伝子解析用マイクロアレイチップ500の反応基板の反応スポットには、診断目的に応じて、一端がビオチン化された塩基配列が既知のオリゴヌクレオチド(Capture Oligo)が予め固定されている。遺伝子解析用マイクロアレイチップ500は、他の場所にて用意されたものであってもよい。サンプルトレイ711には、サンプルDNA(Sample Oligos)、レポータDNA(Reporter Oligos)等が保管されている。例えば、バーコードリーダ743により、サンプルトレイ711、各ボトル712、713、遺伝子解析用マイクロアレイチップ500又は基板ホルダ503に装着されたバーコードを読み取る。読み取った識別符号等は、解析用コンピュータ741に送られる。解析用コンピュータ741は、出力装置742に指示画面を表示し、ユーザへ所定の指示を行う。
【0111】
ステップS703にて、アタッチメントを行う。図6Aに示したように、マイクロアレイチップ500を、支持体610に装着する。インレットニードル701及びアウトレットニードル702と電極703を上昇させる。図6Bに示したように、インレットニードル701及びアウトレットニードル702はセプタ504を穿孔する。更に、支持体716を上方に移動させると、電極703が反応基板501の下面の制御電極501A(図5D参照)に係合する。
【0112】
ステップS704にて、サンプルDNAを、マイクロアレイチップの反応チャンバ514に導入する。先ず、サンプルトレイX-Y-Z駆動機構(図示なし)によりサンプルトレイ711を所望の位置に配置し、4方向バルブ715によって、サンプルトレイ711の所定のサンプルDNA溶液と、マイクロアレイチップの反応チャンバ514を接続する。次に、2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。フィルを行い、マイクロアレイチップの反応チャンバ514と流路に充填されていた溶液を、シリンジ718B内に吸引し、代わりに、サンプルトレイ711に保管されていたサンプルDNA溶液を、マイクロアレイチップの反応チャンバ514と流路を充填する。
【0113】
反応基板501の反応スポット502の目的の位置に、約0.2mAの電流を60秒印加する。電圧の印加によって、目的の位置にて電気的結合が起き、サンプルDNAがキャプチャされる。即ち、反応スポットに固定されたオリゴヌクレオチド(Capture Oligo)と相補配列を有するDNAのみが非特異的にハイブリダイズする。
【0114】
ハイブリダイゼーション反応が完了すると、次に、ステップS705にて、未反応のサンプルDNAを洗い流す。即ち、フラッシュを行い、マイクロアレイチップの反応チャンバ514内の液体を廃液ボトルに排出する。洗浄水のフィル及びフラッシュによりマイクロアレイチップの反応チャンバ514及び流路を洗浄する。
【0115】
ステップS706にて、蛍光標識されたレポータDNAを、マイクロアレイチップの反応基板の反応チャンバ514に導入する。先ず、サンプルトレイX-Y-Z駆動機構(図示なし)によりサンプルトレイ711を所望の位置に配置し、4方向バルブ715によって、サンプルトレイ711の所定のレポータDNA溶液と、マイクロアレイチップの反応チャンバ514を接続する。次に、2方向バルブ717によって、マイクロアレイチップの反応チャンバ514を吸引装置718に接続する。フィルを行い、マイクロアレイチップの反応チャンバ514と流路に充填されていた洗浄液を、シリンジ718B内に吸引し、代わりに、サンプルトレイ711に保管されていたレポータDNA溶液を、マイクロアレイチップの反応チャンバ514と流路を充填する。この状態でおよそ60秒維持する。これにより、キャプチャされたサンプルDNAとレポータDNAがハイブリダイズする。
【0116】
ハイブリダイゼーション反応が完了すると、ステップS707にて、未反応のレポータDNAを洗い流す。即ち、フラッシュを行い、マイクロアレイチップの反応チャンバ514内の液体を廃液ボトルに排出する。洗浄水のフィル及びフラッシュによりマイクロアレイチップの反応チャンバ514及び流路を洗浄する。洗浄が完了すると、洗浄水のフィルにより、マイクロアレイチップの反応チャンバ514及び流路を洗浄水によって充填する。
【0117】
ステップS708にて、CCDカメラで画像を取得する。先ず、照明装置621により励起光を反応基板の反応スポットに照射し、カメラ622により蛍光色素が発する蛍光の画像を取得する。蛍光の位置から、レポータDNA(Reporter Oligos)の位置を確認することができる。上述のステップにより、マイクロアレイチップの反応基板の反応スポットに予め固定されたオリゴヌクレオチド(Capture Oligo)にサンプルDNA(Sample Origos)が結合し、このサンプルDNA(Sample Origos)に更に、蛍光標識されたレポータDNA(Reporter Oligos)が結合している。レポータDNA(Reporter Oligos)の位置を検出することにより、サンプルDNA(Sample Origos)の位置を検出することができる。
【0118】
ステップS709にて、デタッチメントを行なう。画像取得完了後は、フラッシュを行い、マイクロアレイチップの反応チャンバ514及び流路に保持されていた洗浄水を廃棄する。更に、洗浄液のフィルおよびフラッシュを繰り返し、マイクロアレイチップの反応チャンバ、反応基板及び流路を洗浄する。洗浄が完了したのち、インレットニードル701及びアウトレットニードル702と電極703を下降させる。それにより、流路結合、および電気的結合が解除される。マイクロアレイチップ500を、支持体610より取り外す。
【0119】
ステップS710にて、終了処理を行う。装置内の各構成部品を初期位置に戻し、電源切断可能な状態とする。
【0120】
[実施例3]
本発明をさらに別の実施の形態例により説明する。
図9A、図9B、図9C、図9Dを参照して本発明によるマイクロ流路チップ900の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。図9Aに示すように、本例のマイクロ流路チップは、基板ホルダ903と、基板ホルダ903に装着された反応基板101と、基板ホルダ903及び反応基板101の上部に配置されたシート904と、更にその上に配置されたシート905とを有する。基板ホルダ903、シート904、及び、シート905の2つの主面のうち、図9A、図9B、図9C、図9Dにて上側の面を上面、下側の面を下面と称することとする。
【0121】
実施例1と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ903に支持され、またマイクロ流路チップの下面には照明窓903Cが形成されている。照明窓903Cを介して、反応基板101の下面が露出しており、その部分に全反射プリズムを光学的に接着、又は、配置させることができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。発する蛍光は、シート904、シート905を通して、上方より観察、集光、検出する。シート905、シート904及び反応基板101は透明な材料によって形成される。
【0122】
マイクロ流路チップは、インレット910、供給流路912、反応チャンバ914、排出流路913、及び、アウトレット911を有する。供給流路912、反応チャンバ914、及び、排出流路913は、順に接続されており、密閉された流路を形成している。
【0123】
インレット910及びアウトレット911は、顕微鏡の対物レンズおよび励起光源光学系部品配置の障害とならないよう、離れた位置に形成される。対物レンズの外径は通常約30mm程度であり、しかも高NAの対物レンズは基板表面に近接する必要がある。そのため、対物レンズの直下を含む近傍には反応基板・反応チャンバのカバー構造体以外配置できない状態になる。この場合、対物レンズとの干渉を避けるために、反応スポット102から少なくとも約15mm以上離れた位置にインレット910及びアウトレット911を形成する必要がある。
【0124】
本例ではインレット910及びアウトレット911を反応スポット102から20mmの距離に配置した。より正確には、対物レンズが測定視野を移動することも含み、測定視野範囲+対物レンズ外径を超える位置にインレット910及びアウトレット911を作成すればよい。本例では、反応スポットを中心としてその両側にインレット910及びアウトレット911を作成しており、その間隔は40mmとなり、対物レンズをその間に配置し、蛍光検出することができる。そのため、高NAの対物レンズを使用することができ高感度な蛍光検出することができる。DNA塩基配列解析装置のために、また、単分子方式DNA塩基配列解析装置に好適である。
【0125】
反応基板101は、石英ウェハから裁断した厚さが約0.725mm、一辺の寸法が約10mmの正方形の薄い石英ガラス板状部材とした。反応基板の上面には、少なくとも、その一部に、半導体製造プロセスによって、DNAなどが固定できる金属構造体などが作成されている。ただ、金属構造体などがなく、アミノ基、カルボキシル基、ビオチン、アビジンなどが結合されているものでも可能である。また、反応基板の形状は、正方形のほか、長方形、多角形、円形等であってもよい。また、大きさは、10mmの正方形に限らず、任意の大きさに対応できるが、小さな寸法にすることが望ましい。
【0126】
図9Dに示すように、基板ホルダ903の上面には、反応基板101を収納し、保持するための凹部903Aが形成されている。凹部903Aの底面には、反応基板保持部903Bと約9mm×9mmの貫通孔が形成されている。この貫通孔によって、マイクロ流路チップの照明窓903Cが形成される。反応基板101は反応基板保持部903Bに支えられ、照明窓903Cにて、反応基板101の下面が露出する。照明窓903Cの縦横寸法の少なくとも一方が反応基板101の縦横寸法より小さければよく、例えば、8mm×10mm、10mm×8mm等でもよい。これにより、反応基板保持部903Bによって反応基板101が支持される。なお、凹部903Aの縦横寸法は、なるべく近い寸法で、反応基板の縦横寸法より大きければよく、10.5mm×14mm程度でよい。凹部903Aの深さは、反応基板101の厚さと同一程度でよく、0.7mmとする。反応基板保持部903Bの厚さは、特に制約がないが、全反射照明する場合は、なるべく薄いほうがよく、0.1mmとする。0.05〜0.3mmでもよい。
【0127】
基板ホルダ903は、一般的なスライドグラスと同等の寸法を有する。即ち、縦横の寸法は、26mm×76mmである。厚さは上記により、0.8mmである。
基板ホルダ903は、ユーザによる不意の取り扱いミスや落下にも耐えうる材料によって形成される。このような材料として、ステンレス、アルミニウム、鉄などの金属、あるいは、アクリル、ポリスチレンなどの樹脂がある。
【0128】
図9Cに示すように、シート904は、基板ホルダ903の外形と同等または、やや小さい形状及び寸法を有する。厚みは100μmとする。シート904の中心部には凹部904A(下面側に開口、深さは50μm)が形成されている。シート904と反応基板が密着することで、凹部904Aの領域が反応チャンバ914になる。凹部904Aは反応スポット102の領域より大きく、反応基板101全体より小さいサイズとし、反応スポット102と凹部904Aの中心がほぼ一致するようにする。反応チャンバ914は、反応スポット102の上側に形成される。なお、検出光学系によって一度に観察できる領域を、以下に、「計測視野」と呼ぶ。反応チャンバ914の底面は、少なくとも、計測視野の寸法と同程度か又はそれより大きくする。凹部904Aの両端には貫通孔904Bがあり、上面に形成した2本の溝904Cと連結し、両端部904Dにつながる。溝904C、両端部904Dの深さは約50μm、溝904Cの幅は約500μm、両端部904Dは1mmφ、貫通孔904Bは1mmφである。
【0129】
図9Bに示すように、シート905は、シート904と同等の形状と寸法を有する。厚みは100μmとする。シート905には、シート904の両端部904Dと同じ位置に、2つの貫通孔905Aが形成されている。貫通孔905Aは円形であり2mmφである。シート904とシート905を密着させ、接着することで、シート904の上面の溝904Cとシート905の下面で流路912及び913が形成され、シート905の2つの貫通孔905Aがインレット910及びアウトレット911になる。
【0130】
これにより、インレット910、流路912、反応チャンバ914、流路913、アウトレット911とつながる流路が形成される。なお、図には記していないが、図2と同様に、インレット910、アウトレット911には、インレットチューブ、アウトレットチューブを接続して使用される。
【0131】
なお、シート905と904の厚さは、流路にかかる圧力による変形の影響を少なくするために、厚いほうがよい。ただし、シート904と905全体の厚みは対物レンズの結像が許容な範囲にする必要がある。最大の厚みは、対物レンズの倍率、NAなどによって異なるので、対物レンズにあわせればよい。材質は、耐熱性、耐寒性、耐候性、及び、耐薬品性を有する材料によって形成される。このような材料として、ポリジメチルシロキサン(PDMS)などのシリコーン樹脂が使用できる。PDMSは接着性を有するため、接着剤を使用しなくてもガラスなど他の部材と接着可能である利点を有する。また透明性が高く、光測定に有効である。接着などが可能な材質であり、且つ、使用する試薬、実験系に不具合を与えなければ、PDMS以外の材料であってもよい。
【0132】
なお、シート905は貫通孔以外の加工がされていないため、薄いガラス板であってもよい。シート904とはそのままで接着可能であり、流路にかかる圧力に耐性もあり、強度を高めることが可能である。
【0133】
また、流路912,913は、シート904の溝904Cとシート905の下面で形成したが、シート905の下面に溝904Cと同等の溝を作成して流路を構成してもよい。
【0134】
また、本例では、凹部904Aの形状は六角形としたが、形状は、例示であり、菱形、楕円、円、多角形、長方形等であってもよい。試薬などの液体が流れやすくするためのテーパなどがついていることが望ましい。
【0135】
なお、本図には記載されないが、本マイクロ流路チップを使った測定系には、励起光源光学系として、図2または図3と同様に、全反射エバネッセント照射検出方式を用いることができる。反応基板101の下面に、全反射プリズムをオイルカップリングにより光学的に接合する。照明窓より小さな全反射プリズムを使用して、照明窓によって露出された反応基板部分に直接接合してもよいし、または、照明窓より大きな全反射プリズムを使用して、反応基板保持部903Bと接触させ、反応基板保持部の厚みの空間にオイルなどを満たしてカップリングしてもよい。
【0136】
励起用のレーザ光は、全反射プリズムに入射し、オイルカップリング部を経由して反応基板内に導入され、上面の反応スポット部を照射する。反応基板、反応スポット部の上部の反応チャンバ内には反応試薬溶液、洗浄液などの水溶液で満たされている。反応基板の石英ガラスの屈折率は約1.46、水の屈折率は約1.33である。反応基板から反応チャンバへの入射角度が約66度で臨界角となり、それを超える角度で入射すると界面で全反射する。そのため界面での入射角度が68度前後になるように調整し、反応スポット部で全反射させ、反応スポット部の直上の反応チャンバ内にエバネッセントを形成させ、この範囲にある蛍光体を励起する。生じる蛍光は、前述のように対物レンズにより、上方より観察、集光、検出する。
【0137】
なお、全反射プリズムに代えて、対物レンズを使用してエバネッセント照明してもよい。反応基板として厚さ0.17mmの石英ガラス板を使用し、NA1.4以上の対物レンズを反応基板の下面に配置し、オイルカップリングにより、反応基板101の下面と光学的に接合する。対物レンズに入射するレーザ光の光路を調整することで、反応基板にレーザ光を導入し、上面の水溶液との界面で全反射するようにする。発する蛍光は、同じ対物レンズを使用して集光し、検出することができる。
【0138】
本実施例では、反応基板101のサイズが一辺約10mmの正方形に対して、試薬を導入し排出するためのインレット及びアウトレットの間隔が幅40mmと、基板サイズを超えて作成できる。これは、反応スポット上部の反応チャンバ914は基板面に接触する必要があるが、チャンバに試薬を導くための供給流路912、排出流路913は基板面と接触させる必要はないため、シート904とシート905の2層構造とし、その間に流路を構成することによって実現したものである。インレット及びアウトレットも反応基板と接触しない構造であり、インレット及びアウトレットの間隔を広げつつ、反応基板のサイズを最小にすることができる。
【0139】
本例によりチップを安価に作成することが可能になる。反応基板101は、石英ウェハから裁断したものを使用している。石英ウエハは高価であるため、コストを下げるには基板をより多く切り取る必要がある。実施例では反応基板のサイズを10mm角であり、8インチ径のウェハからは単純計算で約290枚程度得ることができる。実施例のように、マイクロ流路チップのインレット及びアウトレットの間隔を40mmにし、これを従来のように反応基板の上部に作成する場合、基板サイズは横45mm、縦10mm程度必要であり、この場合、58枚程度しか裁断できない。長辺の長さが20mmの基板であれば140枚に、25mmであれば110枚に裁断できるため、コスト低下が可能になる。本実施例の構造により、より多くの基板を得ることができ、より安価にチップを作成することができる。
【0140】
また、本実施例では、反応チャンバ914に試薬を導くための供給流路912、排出流路913は反応基板の面とは接触していない。そのため反応基板と基板ホルダとの間に隙間があっても液がその部分に漏れたり、しみだすことがなく、安定に、正確に液を流すことができる。本例では、反応基板の厚さが0.725mmで、基板ホルダの凹部の深さが0.7mmであるから、マイクロ流路チップを構築したときに、基板上面と基板ホルダ上面に段差ができる。しかしながら、このような構造でも、液を漏れたり、しみだすことがなく、送液することができる。単純に、供給流路または排出流路を反応基板及び基板ホルダとその上部のシートに形成した溝とで構築する場合、反応基板と液が接触するので、前記のような段差がある場合、液漏れするという問題がある。また、反応基板と基板ホルダとの間には隙間が必ず発生するため、隙間に液が入り込んでしまい、反応スポット領域への液の送液が困難になるという問題もある。隙間を接着剤などで埋める場合でも段差のないようにすることは困難であり、液漏れの可能性が高い。このように、本例によれば、インレット及びアウトレットの間隔を広げつつ、反応基板のサイズを最小にでき、液の漏れやしみだしのない安定で正確な送液を行うことが可能になる。
【0141】
[実施例4]
本発明をさらに別の実施の形態例により説明する。
図10A、図10Bを参照して本発明によるマイクロ流路チップ920の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。また、反応基板の上部に密着して配置されるシート904及び905は実施例3と同じものを使用する。図10Aに示すように、本例のマイクロ流路チップは、基板ホルダ923と、反応基板101と、反応基板上部に配置されたシート904と、更にその上に配置されたシート905とを有する。基板ホルダ923、シート904、及び、シート905の2つの主面のうち、図10A、図10Bにて上側の面を上面、下側の面を下面と称することとする。
【0142】
実施例3と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ923に設けられた貫通孔923A内に配置され、基板ホルダ923と反応基板101とに接着されるシート904によって保持される。シート904の上面にはシート905が接着される。反応基板101の下面は露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。シート905、シート904は透明材料により構成され、反応基板面より発する蛍光などを上方より観察、集光、検出する。
【0143】
実施例3と同様に、マイクロ流路チップは、インレット910、供給流路912、反応チャンバ914、排出流路913、及び、アウトレット911を有する。供給流路912、反応チャンバ914、及び、排出流路913は、順に接続されており、密閉された流路を形成する。インレット910及びアウトレット911は、反応スポット102からそれぞれ20mm離して配置され、インレット910とアウトレット911間は約40mm離れる。本構成により、液漏れすることなく、反応基板101(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に十分に広い間隔で設けられる。これにより、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。
【0144】
基板ホルダ923は、一般的なスライドグラスと同等の寸法を有する。縦横の寸法は、26mm×76mmである。厚さは反応基板と同等の厚さでよく、0.725mmとした。図9Dに示すように、基板ホルダ903は貫通孔923Aを有する。貫通孔は約11mm×11mmであり、反応基板101がその内部に入る大きさとする。
【0145】
反応基板はシート904にて吊り下げ保持される。そのため、反応基板と基板ホルダの上面に段差がなく、フラットにすることができる。シート904もシート905もフラットになり、シート905に強度の強いガラス板を使用することが可能である。なお、反応基板はシート904のほか、下面に配置される全反射プリズムによっても保持される。
本実施例によれば、流路構成が同じであり、実施例3と同等の効果が得られる。
【0146】
[実施例5]
本発明をさらに別の実施の形態例により説明する。
図11A、図11B、図11C、図11D、図11Eを参照して本発明によるマイクロ流路チップ930の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。また、反応基板の上部に密着して配置されるシート905は実施例3と同じものを使用する。図11Aに示すように、本例のマイクロ流路チップは、基板ホルダ933と、反応基板101と、反応基板上部に配置されたシート934と、更にその上に配置されたシート905と、反応基板101とシート934の間のシート936とを有する。基板ホルダ933、シート936、シート934、及び、シート905の2つの主面のうち、図11A、図11B、図11C、図11D、図11Eにて上側の面を上面、下側の面を下面と称することとする。
【0147】
実施例3と同様に、反応基板101(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の上面には、反応スポット102が形成されている。
【0148】
図11Eに示すように、基板ホルダ933の上面には、反応基板101を収納し、保持するための凹部933Aが形成されている。凹部933Aの底面には、反応基板保持部933Bと約9mm×9mmの貫通孔が形成されている。この貫通孔によって、マイクロ流路チップの照明窓933Cが形成される。反応基板101は反応基板保持部933Bに支えられ、照明窓933C部で反応基板101の下面が露出する。照明窓933Cの縦横寸法は、反応基板101の縦横寸法より小さく、9mm×9mm等でもよい。これにより、反応基板保持部933Bによって反応基板101が支持される。なお、凹部933Aの縦横寸法は、11mm×11mm程度でよい。凹部933Aの深さは、反応基板101の厚さと同一程度でよいが、0.82mmとする。反応基板保持部933Bの厚さは、0.1mmとする。基板ホルダ933の縦横の寸法は、26mm×76mmである。厚さは上記により、0.83mmである。
【0149】
反応基板101は凹部933A内の反応基板保持部933Bによって支持される。また、照明窓933Cを介して、反応基板101の下面が露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。
【0150】
発する蛍光は、シート934、シート905を通して、上方より観察、集光、検出する。シート905、シート934及び反応基板101は透明な材料によって形成される。
【0151】
反応基板101上部には、厚さ0.095mmのシート936を密着させている。それによって、反応基板101と凹部933Aの深さの間の寸法の差を埋め、基板ホルダ933の上面とシート936の上面を平らになる。これらの上にシート934、及び、シート905を配置して流路などを構築している。図11Dに示すように、シート934は、反応基板101とほぼ同一の大きさで、反応スポット領域に相当する位置に、反応スポット102の領域より大きく、反応基板101全体より小さいサイズの貫通孔936Aを有している。反応基板との接着は貫通孔の周辺部にて行う。
【0152】
図11Cに示すように、シート934は、基板ホルダ933の外形よりやや小さい形状及び寸法を有する。厚みは100μmとする。シート934とシート936、及び反応基板101が組み合わされて密着することで、貫通孔936Aの領域が反応チャンバ914になる。反応チャンバ914は、反応スポット102の上側に形成される。シート934には、シート936の貫通孔936Aの両端に相当する位置に、貫通孔934Bが形成されている。この貫通孔934Bは、上面に形成した2本の溝934Cと連結し、両端部934Dにつながる。溝934C、両端部934Dの深さは約50μm、溝934Cの幅は約500μm、両端部934Dは1mmφ、貫通孔934Bは1mmφである。
【0153】
図11Bに示すように、シート905は、シート934と同等の形状と寸法を有する。厚みは100μmとする。シート905には、シート934の両端部934Dと同じ位置に、2つの貫通孔905Aが形成されている。貫通孔905Aは円形であり2mmφである。シート934とシート905を密着させ、接着する。それにより、シート934の上面の溝934Cとシート905の下面によって、流路912及び913が形成され、シート905の2つの貫通孔905Aがインレット910及びアウトレット911になる。
【0154】
これにより、インレット910、流路912、反応チャンバ914、流路913、アウトレット911とつながる流路が形成される。
【0155】
なお、シート934と936の材料として、ポリジメチルシロキサン(PDMS)などのシリコーン樹脂が使用できる。PDMSは接着性を有するため、接着剤を使用しなくてもガラスなど他の部材と接着可能である利点を有する。また透明性が高く、光測定に有効である。接着などが可能な材質であり、且つ、使用する試薬、実験系に不具合を与えなければ、PDMS以外の材料であってもよい。シート936は不透明材料でも構わない。
【0156】
実施例3、4と同様に、マイクロ流路チップは、インレット910、供給流路912、反応チャンバ914、排出流路913、及び、アウトレット911を有する。供給流路912、反応チャンバ914、及び、排出流路913は、順に接続されており、密閉された流路を形成する。本構成により、液漏れすることなく、反応基板101(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に十分に広い間隔が設けられる。これにより、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。
【0157】
本実施例によれば、基板ホルダと反応基板の厚みが異なっていても、シート936が、その段差を吸収でき、基板などの設計が容易になる。
本実施例によれば、流路構成が同じであり、実施例3と同等の効果が得られる。
【0158】
[実施例6]
本発明をさらに別の実施の形態例により説明する。
図12A、図12B、図12C、図12Dを参照して本発明によるマイクロ流路チップ940の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。図12Aに示すように、本例のマイクロ流路チップは、基板ホルダ943と、反応基板101と、反応基板上部に配置されたシート944と、更にその上に配置されたシート945とを有する。
【0159】
実施例4と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ943に設けられた貫通孔943A内に配置され、基板ホルダ943と反応基板101とに接着されるシート944によって保持される。シート944の上面にはシート945が接着される。反応基板101の下面は露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。シート945、シート944は透明材料により構成され、反応基板面より発する蛍光などを上方より観察、集光、検出する。
【0160】
基板ホルダ943の寸法は、26mm×76mmである。厚さは反応基板と同等の厚さでよく、0.725mmとした。図12Dに示すように、基板ホルダ943は貫通孔943Aを有する。貫通孔の寸法は約11mm×11mmであり、反応基板101がその内部に入る大きさとする。また後述するインレット及び、アウトレット用に、シート944の貫通孔944Cと同じ位置に、貫通孔943Bが設けられている。
【0161】
図12Cに示すように、シート944は、基板ホルダ943の外形と同等または、やや小さい形状及び寸法を有する。厚みは100μmとする。シート944の中心部には貫通孔944Aが形成されている。シート944と反応基板が密着し、シート945で覆われることで、貫通孔944Aの領域が反応チャンバ954になる。貫通孔944Aは反応スポット102の領域より大きく、反応基板101全体より小さいサイズとし、反応スポット102と貫通孔944Aの中心がほぼ一致するようにする。反応チャンバ954は、反応スポット102の上側に形成される。シート944の貫通孔944Aの両端は、上面に形成した2本の溝944Bと連結し、両端部の貫通孔944Cにつながる。溝944Bの深さは約50μm、幅は約500μm、両端部の貫通孔944Cは1mmφである。なお、本シートは実施例3のシート904と同等の構造、つまり、貫通孔944Aの代わりに凹部904A(下面側に開口、深さは50μm程度)と同等の構造を設けて流路を形成してもよい。
【0162】
図12Bに示すように、シート945は、シート944と同等の寸法で、厚みが100μmのガラス板とする。すくなくとも、シート945の貫通孔、溝などをカバーするサイズであればよい。貫通孔、溝なども構造は不要である。シート944とシート945を密着させることによって、溝944Bに対応して流路952及び953が形成され、シート944の貫通孔944Cに対応してインレット950とアウトレット951が形成される。インレット950とアウトレット951は、シート944の貫通孔944C、及び、基板ホルダ943に設けられた貫通孔943Bによって構築される。
【0163】
これにより、インレット950、流路952、反応チャンバ954、流路953、アウトレット951とつながる流路が形成される。さらに、インレット950、アウトレット951には、インレットチューブ955、アウトレットチューブ956が接続され必要な液を供給及び排出する構成とする。
【0164】
実施例3、4などと同様に、マイクロ流路チップは、インレット、供給流路、反応チャンバ、排出流路、及び、アウトレットを有し、供給流路、反応チャンバ、及び、排出流路は、順に接続されており、密閉された流路を形成する。インレット及びアウトレットは、反応スポットからそれぞれ20mm離して配置され、インレットとアウトレット間は約40mm離れる。本構成により、液漏れすることなく、反応基板(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に十分に広い間隔が設けられる。これにより、小さな基板サイズのものでも、測定装置に必要な部品の配置に影響を与えることなく、使用することができる。
【0165】
上面は完全フラットであり、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。また、全反射プリズムを配置する際にも影響を与えることがない。また、下面から対物レンズで、全反射照明する場合でも障害となることはなくなる。
【0166】
本実施例では、孔、溝加工されていないガラス板をシート945に使用することができ、より容易に使用することができ、チップの強度を簡単に高めることができる。また、流路にかかる圧力に耐性もあり、流路、特に対物レンズの下方の観察窓になる面の変形が少なく、蛍光像を安定に計測することが可能になる。
【0167】
[実施例7]
本発明をさらに別の実施の形態例により説明する。
図13A、図13B、図13C、図13Dを参照して本発明によるマイクロ流路チップ960の例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。
【0168】
実施例6と同様に、反応基板101の上面には、反応スポット102が形成されている。反応基板101は基板ホルダ963に設けられた貫通孔963A内に配置され、基板ホルダ963と反応基板101とに接着されるシート964によって保持される。シート964の上面にはシート965が接着される。反応基板101の下面は露出しており、その部分に全反射プリズムを光学的に接着、又は、配置することができる。それによって、反応基板にレーザ光を導入し、反応スポット102面で全反射させ、エバネッセント場を形成し、蛍光体などを励起する。シート965、シート964は透明材料により構成され、反応基板面より発する蛍光などを上方より観察、集光、検出する。
【0169】
基板ホルダ963の形状は、実施例6の基板ホルダ943とほぼ同様で、図13Dに示すように、貫通孔963A、貫通孔963Bを有するが、貫通孔963Bは片側に設けられている。
【0170】
図13Cに示すように、シート964は、実施例6のシート944とほぼ同じ構造である。シート964には、貫通孔964A、貫通孔964Aと連結している溝964B、溝964Bの端部の貫通孔964Cが形成されている。シート964と反応基板が密着し、シート965で覆われることで、貫通孔964Aの領域が反応チャンバ974になる。反応チャンバ974は、反応スポット102の上側に形成される。ここで二つの貫通孔964Cはシートの片側に配置しており、そのため、片方の溝964Bもそれにあわせて、溝が180度向きを変えて、貫通孔964A端部に連結する構造としている。
【0171】
図13Bに示すように、シート965は、実施例6のシート945と同じものである。シート964とシート965を密着させることによって、溝964Bに対応して、流路972及び973が形成され、シート964の貫通孔964Cに対応してインレット970とアウトレット971(図示なし)が形成される。インレット970とアウトレット971は、二つの貫通孔964C及び、各貫通孔964Cと対応する基板ホルダ963に設けられた貫通孔963Bによって構築される。
【0172】
これにより、インレット970、流路972、反応チャンバ974、流路973、アウトレット971とつながる流路が形成される。さらに、インレット970、アウトレット971には、インレットチューブ、アウトレットチューブが接続され必要な液を供給及び排出する構成とする。
【0173】
実施例3、4などと同様に、マイクロ流路チップは、インレット、供給流路、反応チャンバ、排出流路、及び、アウトレットを有し、供給流路、反応チャンバ、及び、排出流路は、順に接続されており、密閉された流路を形成する。インレット及びアウトレットは、反応スポットから20mm離して配置されている。本構成により、液漏れすることなく、反応基板(厚さ:約0.725mm、一辺の寸法が約10mmの正方形)の領域の内側から外部に通じる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に離れて設けられる。これにより、小さな基板サイズのものでも、測定装置に必要な部品の配置に影響を与えることなく、使用することができる。
【0174】
上面は完全フラットであり、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。また、下面には、インレットチューブ、アウトレットチューブが接続されるが、反応スポットの位置から十分に離れて配置されており、また、片側に集中しているため、全反射プリズム等を配置する際にも影響を与えることがない。また、下面から対物レンズで、全反射照明する場合でも同様に対応できる。
【0175】
本実施例では、インレット、アウトレットが片側にまとまっているため、チップ表面の空間が寄り広く確保でき、装置構成が容易になる。また、接続するインレットチューブ、アウトレットチューブをまとめてハンドリングすることが容易にでき、装置構成が容易になる。
本実施例によれば、前記実施例などと同様の効果がある。
【0176】
[実施例8]
本発明をさらに別の実施の形態例により説明する。
図14A,図14Bを参照して本発明によるマイクロ流路チップの例を説明する。反応基板101は実施例1(図1E)と同様のものを使用する。
本実施例では、実施例7と同一の構成を有する。実施例7では、インレット、供給流路、反応チャンバ、排出流路、及び、アウトレットが一組であったが、本例では、同一反応基板に4組並列させて配置している。図14Aは実施例7の図13Cに相当するシート975の図であり、4組の流路を設けている。それぞれ、二つの貫通孔975C、反応チャンバとなる貫通孔975A、貫通孔975Cと975Aを連結し上面に作成された二つの溝975Bからなる。各貫通孔975Aは、横幅4mm、縦幅1mmの大きさで、2mmピッチで配置している。4つの貫通孔975Aは全体で横4mm、縦7mmの領域に形成され、反応基板(一辺の寸法が約10mmの正方形)上に4つの反応チャンバを形成する。なお、貫通孔975Aの大きさを変えれば、反応チャンバ数を変えることができる。
【0177】
また、各貫通孔975Cはφ1mm、各溝975Bは、深さ約50μm、幅約500μmである。各貫通孔975Cは2mm間隔で縦方向に並んでおり、全体の縦方向の寸法は15mmであり、基板ホルダのサイズ、26mm×76mmに収められている。
【0178】
図14Bは、実施例7の図13Dに相当する基板ホルダ976の図であり、反応基板を収める貫通孔976A、及び、シート975の貫通孔975Cと同じ配置の貫通孔976Bを有する。
【0179】
基板ホルダ976と反応基板と、シート975、及びシート965により、マイクロ流路チップが構成され、1反応基板に複数の反応チャンバと流路を構築することができ、多検体の解析を可能にする。
【0180】
[実施例9]
本発明をさらに別の実施の形態例により説明する。
図15A、図15B、図15C、図15D、図15Eを参照して本発明によるマイクロ流路チップ980の例を説明する。反応基板981には、厚さが約0.17mm、一辺の寸法が約12mmの正方形の石英ガラス基板を使用する。石英ガラス製の反応基板981には、前記実施例と同様に反応スポット982が形成されている。マイクロ流路チップ980は、反応基板981、基板ホルダ983、シート984、シート985、シート986で構成する。
【0181】
図15Eに示すように、基板ホルダ983は、反応基板981を固定するための貫通孔983Aを設け、またインレット及びアウトレットになる貫通孔983B(φ2mm)を有する。基板ホルダ983の寸法は縦26mm、横76mmであり、厚さは1mmとする。貫通孔983Aの寸法は10mm×10mmで、その下面に孔の中心と反応基板の中心とを合わせて、反応基板981を接着させて固定する。
【0182】
反応基板981の上側は、基板ホルダ983の貫通孔983Aの開口(厚さ1mm)が配置されている。この開口を埋めるようにシート986が反応基板981に接着される。シート986は図15Dに示すように、縦9mm、横9mm、厚さ1mmのPDMSシートであり、下面ほぼ中心に凹部986A(縦2mm、横4mmの六角形で、深さ0.05mm)が形成され、その端部にφ1mmの貫通孔986Bを有する。
【0183】
シート986の上面にはシート984が配置されている。このシート984は、シート986及び基板ホルダ983の上面と接着される。シート984は、図15Cに示すように、貫通孔986Bと位置を合わせた貫通孔984A(φ1mm)と、貫通孔983Bと位置を合わせた貫通孔984C(φ2mm)と、貫通孔984Aと貫通孔984Cとを連結し上面に作成された溝984Bとを有する。シート984の大きさは、縦26mm、横48mmであり、厚さは0.2mmである。溝984Bの深さは75μm、幅は400μmである。
【0184】
シート984の上面にはシート985を配置し、接着する。シート985は、図15Bに示すように、シート984と同じ大きさで厚さ0.5mmのガラス板を使用する。厚みは特に限定されない。また大きさは、シート984の貫通孔と溝の上部を覆えるだけのサイズであれば適用できる。
【0185】
反応基板981の上側に配置されたシート986の凹部986Aが反応チャンバ994となる。シート986の貫通孔986B、シート984の貫通孔984A、シート985、及び、シート984の溝984Bによって、流路992、及び993が構築される。基板ホルダ983の貫通孔983Bとシート984の貫通孔984Cによって、インレット990とアウトレット991(図示無し)が構築される。インレット990、流路992、反応チャンバ994、流路993、アウトレット991とつながる密閉された流路が形成される。本構成により、液漏れすることなく、反応基板981の外部から内部へ、また外部につながる流路が構成され、インレットとアウトレットを反応基板の大きさに縛られずに領域外部に設けることができる。具体的には反応基板中心から15mm以上離すこともできる。これにより、蛍光観察・集光用の高NAの対物レンズをマイクロ流路チップに近接して配置することが可能で、高感度な蛍光検出が可能になる。
【0186】
なお、本例では、蛍光検出用の対物レンズを反応基板下面に配置する。NA1.49の60倍対物レンズを使用し、オイルカップリングで、反応基板と光学的に接合する。励起光は、対物レンズを通して反応基板に導入し、反応スポット面にて入射角が臨界角となるように勝者し、エバネッセント励起とする。生じる蛍光は、同じ対物レンズにより集光され、検出される。
【0187】
本実施例では、薄い反応基板を使用することができ、プリズムエバネッセント照射のほか、対物エバネッセント照射が可能でとなる。
【0188】
本実施例によっても、より小さな基板で流路を構築することができ、チップの低コスト化が実現できる。
【0189】
以上本発明の例を説明したが本発明は上述の例に限定されるものではなく、特許請求の範囲に記載された発明の範囲にて様々な変更が可能であることは、当業者によって容易に理解されよう。
【符号の説明】
【0190】
100…マイクロ流路チップ、101…反応基板、102…反応スポット、103…基板ホルダ、104…反応室シート、105…流路シート、110…インレット、111…アウトレット、112…供給流路、113…排出流路、114…反応チャンバ、120…全反射プリズム、121…入射光路、122…出射光路、131…パッキン、200…分析装置、211…試薬保管ユニット、212…分注ユニット、213…インレットチューブ、214…アウトレットチューブ、215…廃液容器、221…励起光用レーザーユニット、222…励起光用レーザーユニット、223、224…λ/4波長版、225…ミラー、226…ダイクロイックミラー、227…ミラー、231…対物レンズ、232…フィルター、233…結像レンズ、234…2次元センサカメラ、235…カメラコントローラ、240…装置制御用コンピュータ、241…解析用コンピュータ、242…出力装置、500…マイクロアレイチップ、501…反応基板、502…反応スポット、503…基板ホルダ、504…セプタ、505…流路シート、510…インレットチャンバ、511…アウトレットチャンバ、512…供給流路、513…排出流路、514…反応チャンバ、610…支持体、611…凹部、622…カメラ、621…照明装置、700…分析装置、701…インレットニードル、702…アウトレットニードル、703…電極、711…サンプルトレイ、712…洗浄水ボトル、713…ヒスチジンボトル、714…予備ボトル、715…4方向バルブ、716…支持体、717…2方向バルブ、718…吸引装置、720…廃液ボトル、741…解析用コンピュータ、742…出力装置、743…バーコードリーダ、900…マイクロ流路チップ、903…基板ホルダ、903A…凹部、903B…反応基板保持部、903C…照明窓、904…シート、904A…凹部、904B…貫通孔、904C…溝、904D…両端部、905…シート、905A…貫通孔、910…インレット、911…アウトレット、912…供給流路、913…排出流路、914…反応チャンバ、920…マイクロ流路チップ、923…基板ホルダ、923A…貫通孔、930…マイクロ流路チップ、933…基板ホルダ、933A…凹部、933B…反応基板保持部、933C…照明窓、934…シート、934B…貫通孔、934C…溝、934D…両端部、935…シート、936…シート、936A…貫通孔、940…マイクロ流路チップ、943…基板ホルダ、943A…貫通孔、943B…貫通孔、944…シート、944A…貫通孔、944B…溝、944C…貫通孔、945…シート、950…インレット、951…アウトレット、952…供給流路、953…排出流路、954…反応チャンバ、955…インレットチューブ、956…アウトレットチューブ、960…マイクロ流路チップ、963…基板ホルダ、963A…貫通孔、963B…貫通孔、964…シート、964A…貫通孔、964B…溝、964C…貫通孔、965…シート、970…インレット、971…アウトレット、972…供給流路、973…排出流路、974…反応チャンバ、975…シート975、975A…貫通孔、975B…溝、975C…貫通孔、976…基板ホルダ、976A…貫通孔、976B…貫通孔、980…マイクロ流路チップ、981…反応基板、982…反応スポット、983…板ホルダ、983A…貫通孔、983B…貫通孔、984…シート、984A…貫通孔、984B…溝、984C…貫通孔、985…シート、986…シート、986A…凹部、986B…貫通孔、990…インレット、991…アウトレット、992…供給流路、993…排出流路、994…反応チャンバ。
【特許請求の範囲】
【請求項1】
反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及び前記アウトレットをそれぞれ接続する供給流路及び排出流路と、を有するマイクロ流路チップにおいて、
凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダ及び前記反応基板を覆うように配置された第1のシートと、該第1のシートを覆うように配置された第2のシートと、を有し、
前記第1のシートは貫通孔を有し、該貫通孔によって、前記第2のシートと前記反応基板の間に前記反応チャンバが形成され、
前記反応基板は、前記反応チャンバに露出している第1の面と、前記基板ホルダの凹部に設けられた観察窓を介して外部に露出している第2の面と、を有し、前記反応基板の第1の面には微細構造からなる反応スポットが形成されていることを特徴とするマイクロ流路チップ。
【請求項2】
請求項1記載のマイクロ流路チップにおいて、
前記インレットと前記アウトレットは、前記基板ホルダの観察窓が設けられた面とは反対側の面に設けられていることを特徴とするマイクロ流路チップ。
【請求項3】
請求項1記載のマイクロ流路チップにおいて、
前記インレットと前記アウトレットの間の流路は30mm以上であることを特徴とするマイクロ流路チップ。
【請求項4】
請求項1記載のマイクロ流路チップにおいて、
前記第1のシートと前記第2のシートの一方には溝が形成され、該溝によって、前記第1のシートと前記第2のシートの間に前記供給流路及び前記排出流路が形成されていることを特徴とするマイクロ流路チップ。
【請求項5】
請求項1記載のマイクロ流路チップにおいて、
前記第2のシートに形成された貫通孔によって、前記インレット及び前記アウトレットが形成されていることを特徴とするマイクロ流路チップ。
【請求項6】
請求項1記載のマイクロ流路チップにおいて、
前記第1のシート及び前記第2のシートは、ポリジメチルシロキサン(PDMS)によって構成されていることを特徴とするマイクロ流路チップ。
【請求項7】
請求項1記載のマイクロ流路チップにおいて、
前記反応基板は、半導体の製造プロセスを用いて製造されることを特徴とするマイクロ流路チップ。
【請求項8】
請求項1記載のマイクロ流路チップにおいて、
前記反応基板は、一辺の寸法が20mm以下の正方形の板状部材からなることを特徴とするマイクロ流路チップ。
【請求項9】
反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及び前記アウトレットをそれぞれ接続する供給流路及び排出流路と、を有するマイクロ流路チップの製造方法において、
微細構造からなる反応スポットが形成された第1の面と該第1の面と反対側の第2の面を有する反応基板を用意することと、
前記反応基板を、基板ホルダの凹部に配置することと、
前記基板ホルダと該基板ホルダの凹部に配置された前記反応基板を覆うように、第1のシートを貼付することと、
前記第1のシートを覆うように、第2のシートを貼付し、前記第2のシートと前記反応基板の間に、前記反応チャンバを形成することと、
を有し、
前記反応基板の第1の面に形成された前記反応スポットは、前記反応チャンバに露出しており、前記反応基板の第2の面は、前記基板ホルダの凹部に設けられた観察窓を介して外部に露出していることを特徴とするマイクロ流路チップの製造方法。
【請求項10】
請求項9記載のマイクロ流路チップの製造方法において、
前記第1のシートと前記第2のシートは、ポリジメチルシロキサン(PDMS)によって構成されており、前記第1のシートと前記第2のシートは、PDMSの自己吸着性を利用して互いに接着されていることを特徴とするマイクロ流路チップの製造方法。
【請求項11】
請求項9記載のマイクロ流路チップの製造方法において、
前記反応基板は、半導体製造プロセス技術を用いて製造されていることを特徴とするマイクロ流路チップの製造方法。
【請求項12】
反応基板を有するマイクロ流路チップと、該マイクロ流路チップに各種の溶液を供給する溶液供給系と、前記マイクロ流路チップから各種の廃液を回収する廃液回収系と、前記マイクロ流路チップの反応基板に励起光を照射する照射系と、前記マイクロ流路チップの反応基板からの蛍光を検出する検出光学系と、を有する核酸分析装置において、
前記反応基板は、反応スポットが形成された第1の面と該第1の面と反対側の第2の面を有し、
前記マイクロ流路チップは、第1の主面と該第1の主面と反対側の第2の主面を有し、
前記第1の主面には前記溶液供給系に接続されるインレットと前記廃液回収系に接続されるアウトレットとが設けられ、前記第2の主面には前記反応基板の第2の面を外部に露出させるための観察窓が設けられ、
前記検出光学系は前記マイクロ流路チップの第1の主面の側に配置され、前記照射系は前記マイクロ流路チップの第2の主面の側に配置されていることを特徴とする核酸分析装置。
【請求項13】
請求項12記載の核酸分析装置において、
前記反応基板の第2の面には、全反射プリズムが装着されており、前記照射系からの励起光は、前記全反射プリズムを経由して、前記反応基板の第1の面に導かれ、そこで全反射し、エバネッセント光を生成し、該エバネッセント光により、前記反応スポットにおける極めて限定された領域のみが照明されることを特徴とする核酸分析装置。
【請求項14】
請求項12記載の核酸分析装置において、
前記反応基板の反応スポットには、局在型表面プラズモンが発生し易いように微細構造が形成されていることを特徴とする核酸分析装置。
【請求項15】
反応チャンバと、インレットチャンバ及びアウトレットチャンバと、前記反応チャンバと前記インレットチャンバ及び前記アウトレットチャンバをそれぞれ接続する供給流路及び排出流路と、を有するマイクロアレイチップにおいて、
凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダの凹部が形成された面とは反対側の面を覆うように配置されたシートと、を有し、
前記基板ホルダの凹部は貫通孔を有し、該貫通孔によって露出した前記反応基板と前記シートの間に前記反応チャンバが形成され、
前記反応基板は、前記基板ホルダの凹部の貫通孔を介して前記反応チャンバに露出している第1の面と、前記基板ホルダの凹部を介して外部に露出している第2の面と、を有し、前記反応基板の第1の面には微細構造からなる反応スポットが形成されていることを特徴とするマイクロアレイチップ。
【請求項16】
請求項15記載のマイクロアレイチップにおいて、
前記インレットチャンバと前記アウトレットチャンバの開口はセプタによって封鎖されていることを特徴とするマイクロアレイチップ。
【請求項17】
請求項15記載のマイクロアレイチップにおいて、
前記反応基板の第2の面には、制御電極が設けられ、該制御電極を介して前記反応スポットに形成された微細電極に電圧を印加することができるように構成されていることを特徴とするマイクロアレイチップ。
【請求項18】
請求項15記載のマイクロアレイチップにおいて、
前記反応基板は、半導体の製造プロセスを用いて製造されることを特徴とするマイクロアレイチップ。
【請求項19】
反応基板を有する遺伝子解析用のマイクロアレイチップと、該マイクロアレイチップに各種の溶液を供給する溶液供給系と、前記マイクロアレイチップから各種の廃液を回収する廃液回収系と、前記マイクロアレイチップの反応基板に励起光を照射する照射系と、前記マイクロアレイチップの反応基板からの蛍光を検出する検出光学系と、を有する核酸分析装置において、
前記反応基板は、反応スポットが形成された第1の面と、該第1の面と反対側の第2の面を有し、該反応基板の第2の面には、前記反応スポットに形成された微細電極に電圧を印加するための制御電極が設けられ、
前記マイクロアレイチップは、第1の主面と該第1の主面と反対側の第2の主面を有し、前記第2の主面には前記溶液供給系に接続されるインレットチャンバと前記廃液回収系に接続されるアウトレットチャンバとが設けられ、前記第2の主面にて、前記反応基板の第2の面に設けられた制御電極が外部に露出しており、
前記照射系及び検出光学系は前記マイクロアレイチップの第1の主面の側に配置されていることを特徴とする核酸分析装置。
【請求項20】
請求項19記載の核酸分析装置において、
前記インレットチャンバ及び前記アウトレットチャンバはセプタによってそれぞれ封鎖されており、前記核酸分析装置は、更に、
前記マイクロアレイチップに対して可動なインレットニードル、アウトレットニードル、及び、電極を有し、前記インレットニードル、アウトレットニードル、及び、電極を前記マイクロアレイチップに向けて移動させることによって、前記インレットニードルによって、前記インレットチャンバを封鎖しているセプタが穿孔され、前記アウトレットニードルによって、前記アウトレットチャンバを封鎖しているセプタが穿孔され、前記電極が、前記反応基板の第2の面に形成された制御電極に接続するように構成されていることを特徴とする核酸分析装置。
【請求項21】
反応基板を有するマイクロ流路チップと、該マイクロ流路チップに各種の溶液を供給する溶液供給系と、前記マイクロ流路チップから各種の廃液を回収する廃液回収系と、前記マイクロ流路チップの反応基板に励起光を照射する照射系と、前記マイクロ流路チップの反応基板からの蛍光を検出する検出光学系と、を有する核酸分析装置において、
前記反応基板は、反応スポットが形成された第1の面と該第1の面と反対側の第2の面を有し、
前記マイクロ流路チップは、第1の主面と該第1の主面と反対側の第2の主面を有し、
前記第1の主面には前記溶液供給系に接続されるインレットと前記廃液回収系に接続されるアウトレットとが設けられ、前記第2の主面には前記反応基板の第2の面を外部に露出させるための観察窓が設けられ、
前記検出光学系及び前記照射系は前記マイクロ流路チップの第2の主面の側に配置されていることを特徴とする核酸分析装置。
【請求項22】
請求項12または21のいずれか記載の核酸分析装置において、
前記インレットと前記アウトレットの位置が、前記反応基板の外形より外側に配置されていることを特徴とする核酸分析装置。
【請求項23】
反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及び前記アウトレットをそれぞれ接続する供給流路及び排出流路と、を有するマイクロ流路チップにおいて、
その一部に反応スポットが配置された反応領域を有する反応基板と、
該反応基板より大きく、該反応基板を保持する凹部または少なくとも該反応基板が入る貫通孔を有する基板ホルダと、
該反応基板より大きく、少なくとも該反応領域部に相当する部分に貫通孔または凹部を有する第1のシートと、
該第1のシートと接着し、光学的に透明である、第2のシートと、
を有し、
該反応基板と、少なくとも該第1のシートにより、該反応領域面に反応チャンバが形成され、
該第1のシートと第2のシートの間に反応チャンバに連結する流路が形成され、
該流路の端部にインレット及びアウトレットが形成され、
該インレット及びアウトレットが該反応基板外形より離れた位置に形成されることを特徴とするマイクロ流路チップ。
【請求項24】
反応スポットが配置された反応領域を有する反応基板と、反応領域部の反応チャンバと、反応基板外形より離れた位置に設けたインレット及びアウトレットと、該反応チャンバと該インレット及びアウトレットを反応基板表面に接触しない流路で連結することを特徴とするマイクロ流路チップ。
【請求項25】
反応スポットが配置された反応領域を有する反応基板と、反応領域部の反応チャンバと、反応基板外形より離れた位置に設けたインレット・アウトレットを有するマイクロ流路チップ。
【請求項26】
請求項23から25のいずれか1項記載のマイクロ流路チップにおいて、
反応基板には反応領域が複数個所有し、複数のインレットおよびアウトレットを有することを特徴とするマイクロ流路チップ。
【請求項27】
請求項23記載のマイクロ流路チップにおいて、
前記反応基板とほぼ同じ大きさで、すくなくとも前記反応領域部の一部に貫通孔を有する第3のシートを、反応基板と前記第1のシートの間に配置することを特徴とするマイクロ流路チップ。
【請求項28】
請求項23または27記載のマイクロ流路チップにおいて、
前記第1のシート、または第2のシート、または第3のシートとして、接着性を有する樹脂、またはPDMSを使用することを特徴とするマイクロ流路チップ
【請求項29】
請求項23記載のマイクロ流路チップにおいて、
前記流路は、前記第1のシートまたは/および第2のシートに形成された凹部により形成されることを特徴とするマイクロ流路チップ。
【請求項30】
請求項23または29記載のマイクロ流路チップにおいて、
前記第2のシートはガラス板であることを特徴とするマイクロ流路チップ。
【請求項31】
請求項23または29記載のマイクロ流路チップにおいて、
前記第2のシートは厚さ0.02mmから0.2mmのガラス板であることを特徴とするマイクロ流路チップ。
【請求項32】
請求項23記載のマイクロ流路チップにおいて、
前記流路および前記インレット及びアウトレットは、第1のシートに形成されることを特徴とするマイクロ流路チップ。
【請求項33】
請求項23または32記載のマイクロ流路チップにおいて、
前記基板ホルダに、前記インレット及びアウトレットに相当する位置に、ほぼ同等の開口を有することを特徴とするマイクロ流路チップ。
【請求項34】
請求項23から26のいずれか1項記載のマイクロ流路チップにおいて、
前記インレット及びアウトレットは、前記反応領域から少なくとも15mm以上離れていることを特徴とするマイクロ流路チップ。
【請求項35】
請求項23または32または33または34のいずれか1項記載のマイクロ流路チップにおいて、
前記基板ホルダと第1のシートが同じ材質、または基板ホルダを第1のシートで兼用することを特徴とするマイクロ流路チップ。
【請求項36】
請求項23から26のいずれか1項記載のマイクロ流路チップにおいて、
前記反応基板の反応領域がエバネッセント照明されることを特徴とするマイクロ流路チップ。
【請求項1】
反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及び前記アウトレットをそれぞれ接続する供給流路及び排出流路と、を有するマイクロ流路チップにおいて、
凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダ及び前記反応基板を覆うように配置された第1のシートと、該第1のシートを覆うように配置された第2のシートと、を有し、
前記第1のシートは貫通孔を有し、該貫通孔によって、前記第2のシートと前記反応基板の間に前記反応チャンバが形成され、
前記反応基板は、前記反応チャンバに露出している第1の面と、前記基板ホルダの凹部に設けられた観察窓を介して外部に露出している第2の面と、を有し、前記反応基板の第1の面には微細構造からなる反応スポットが形成されていることを特徴とするマイクロ流路チップ。
【請求項2】
請求項1記載のマイクロ流路チップにおいて、
前記インレットと前記アウトレットは、前記基板ホルダの観察窓が設けられた面とは反対側の面に設けられていることを特徴とするマイクロ流路チップ。
【請求項3】
請求項1記載のマイクロ流路チップにおいて、
前記インレットと前記アウトレットの間の流路は30mm以上であることを特徴とするマイクロ流路チップ。
【請求項4】
請求項1記載のマイクロ流路チップにおいて、
前記第1のシートと前記第2のシートの一方には溝が形成され、該溝によって、前記第1のシートと前記第2のシートの間に前記供給流路及び前記排出流路が形成されていることを特徴とするマイクロ流路チップ。
【請求項5】
請求項1記載のマイクロ流路チップにおいて、
前記第2のシートに形成された貫通孔によって、前記インレット及び前記アウトレットが形成されていることを特徴とするマイクロ流路チップ。
【請求項6】
請求項1記載のマイクロ流路チップにおいて、
前記第1のシート及び前記第2のシートは、ポリジメチルシロキサン(PDMS)によって構成されていることを特徴とするマイクロ流路チップ。
【請求項7】
請求項1記載のマイクロ流路チップにおいて、
前記反応基板は、半導体の製造プロセスを用いて製造されることを特徴とするマイクロ流路チップ。
【請求項8】
請求項1記載のマイクロ流路チップにおいて、
前記反応基板は、一辺の寸法が20mm以下の正方形の板状部材からなることを特徴とするマイクロ流路チップ。
【請求項9】
反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及び前記アウトレットをそれぞれ接続する供給流路及び排出流路と、を有するマイクロ流路チップの製造方法において、
微細構造からなる反応スポットが形成された第1の面と該第1の面と反対側の第2の面を有する反応基板を用意することと、
前記反応基板を、基板ホルダの凹部に配置することと、
前記基板ホルダと該基板ホルダの凹部に配置された前記反応基板を覆うように、第1のシートを貼付することと、
前記第1のシートを覆うように、第2のシートを貼付し、前記第2のシートと前記反応基板の間に、前記反応チャンバを形成することと、
を有し、
前記反応基板の第1の面に形成された前記反応スポットは、前記反応チャンバに露出しており、前記反応基板の第2の面は、前記基板ホルダの凹部に設けられた観察窓を介して外部に露出していることを特徴とするマイクロ流路チップの製造方法。
【請求項10】
請求項9記載のマイクロ流路チップの製造方法において、
前記第1のシートと前記第2のシートは、ポリジメチルシロキサン(PDMS)によって構成されており、前記第1のシートと前記第2のシートは、PDMSの自己吸着性を利用して互いに接着されていることを特徴とするマイクロ流路チップの製造方法。
【請求項11】
請求項9記載のマイクロ流路チップの製造方法において、
前記反応基板は、半導体製造プロセス技術を用いて製造されていることを特徴とするマイクロ流路チップの製造方法。
【請求項12】
反応基板を有するマイクロ流路チップと、該マイクロ流路チップに各種の溶液を供給する溶液供給系と、前記マイクロ流路チップから各種の廃液を回収する廃液回収系と、前記マイクロ流路チップの反応基板に励起光を照射する照射系と、前記マイクロ流路チップの反応基板からの蛍光を検出する検出光学系と、を有する核酸分析装置において、
前記反応基板は、反応スポットが形成された第1の面と該第1の面と反対側の第2の面を有し、
前記マイクロ流路チップは、第1の主面と該第1の主面と反対側の第2の主面を有し、
前記第1の主面には前記溶液供給系に接続されるインレットと前記廃液回収系に接続されるアウトレットとが設けられ、前記第2の主面には前記反応基板の第2の面を外部に露出させるための観察窓が設けられ、
前記検出光学系は前記マイクロ流路チップの第1の主面の側に配置され、前記照射系は前記マイクロ流路チップの第2の主面の側に配置されていることを特徴とする核酸分析装置。
【請求項13】
請求項12記載の核酸分析装置において、
前記反応基板の第2の面には、全反射プリズムが装着されており、前記照射系からの励起光は、前記全反射プリズムを経由して、前記反応基板の第1の面に導かれ、そこで全反射し、エバネッセント光を生成し、該エバネッセント光により、前記反応スポットにおける極めて限定された領域のみが照明されることを特徴とする核酸分析装置。
【請求項14】
請求項12記載の核酸分析装置において、
前記反応基板の反応スポットには、局在型表面プラズモンが発生し易いように微細構造が形成されていることを特徴とする核酸分析装置。
【請求項15】
反応チャンバと、インレットチャンバ及びアウトレットチャンバと、前記反応チャンバと前記インレットチャンバ及び前記アウトレットチャンバをそれぞれ接続する供給流路及び排出流路と、を有するマイクロアレイチップにおいて、
凹部を有する基板ホルダと、該基板ホルダの凹部に装着された反応基板と、該基板ホルダの凹部が形成された面とは反対側の面を覆うように配置されたシートと、を有し、
前記基板ホルダの凹部は貫通孔を有し、該貫通孔によって露出した前記反応基板と前記シートの間に前記反応チャンバが形成され、
前記反応基板は、前記基板ホルダの凹部の貫通孔を介して前記反応チャンバに露出している第1の面と、前記基板ホルダの凹部を介して外部に露出している第2の面と、を有し、前記反応基板の第1の面には微細構造からなる反応スポットが形成されていることを特徴とするマイクロアレイチップ。
【請求項16】
請求項15記載のマイクロアレイチップにおいて、
前記インレットチャンバと前記アウトレットチャンバの開口はセプタによって封鎖されていることを特徴とするマイクロアレイチップ。
【請求項17】
請求項15記載のマイクロアレイチップにおいて、
前記反応基板の第2の面には、制御電極が設けられ、該制御電極を介して前記反応スポットに形成された微細電極に電圧を印加することができるように構成されていることを特徴とするマイクロアレイチップ。
【請求項18】
請求項15記載のマイクロアレイチップにおいて、
前記反応基板は、半導体の製造プロセスを用いて製造されることを特徴とするマイクロアレイチップ。
【請求項19】
反応基板を有する遺伝子解析用のマイクロアレイチップと、該マイクロアレイチップに各種の溶液を供給する溶液供給系と、前記マイクロアレイチップから各種の廃液を回収する廃液回収系と、前記マイクロアレイチップの反応基板に励起光を照射する照射系と、前記マイクロアレイチップの反応基板からの蛍光を検出する検出光学系と、を有する核酸分析装置において、
前記反応基板は、反応スポットが形成された第1の面と、該第1の面と反対側の第2の面を有し、該反応基板の第2の面には、前記反応スポットに形成された微細電極に電圧を印加するための制御電極が設けられ、
前記マイクロアレイチップは、第1の主面と該第1の主面と反対側の第2の主面を有し、前記第2の主面には前記溶液供給系に接続されるインレットチャンバと前記廃液回収系に接続されるアウトレットチャンバとが設けられ、前記第2の主面にて、前記反応基板の第2の面に設けられた制御電極が外部に露出しており、
前記照射系及び検出光学系は前記マイクロアレイチップの第1の主面の側に配置されていることを特徴とする核酸分析装置。
【請求項20】
請求項19記載の核酸分析装置において、
前記インレットチャンバ及び前記アウトレットチャンバはセプタによってそれぞれ封鎖されており、前記核酸分析装置は、更に、
前記マイクロアレイチップに対して可動なインレットニードル、アウトレットニードル、及び、電極を有し、前記インレットニードル、アウトレットニードル、及び、電極を前記マイクロアレイチップに向けて移動させることによって、前記インレットニードルによって、前記インレットチャンバを封鎖しているセプタが穿孔され、前記アウトレットニードルによって、前記アウトレットチャンバを封鎖しているセプタが穿孔され、前記電極が、前記反応基板の第2の面に形成された制御電極に接続するように構成されていることを特徴とする核酸分析装置。
【請求項21】
反応基板を有するマイクロ流路チップと、該マイクロ流路チップに各種の溶液を供給する溶液供給系と、前記マイクロ流路チップから各種の廃液を回収する廃液回収系と、前記マイクロ流路チップの反応基板に励起光を照射する照射系と、前記マイクロ流路チップの反応基板からの蛍光を検出する検出光学系と、を有する核酸分析装置において、
前記反応基板は、反応スポットが形成された第1の面と該第1の面と反対側の第2の面を有し、
前記マイクロ流路チップは、第1の主面と該第1の主面と反対側の第2の主面を有し、
前記第1の主面には前記溶液供給系に接続されるインレットと前記廃液回収系に接続されるアウトレットとが設けられ、前記第2の主面には前記反応基板の第2の面を外部に露出させるための観察窓が設けられ、
前記検出光学系及び前記照射系は前記マイクロ流路チップの第2の主面の側に配置されていることを特徴とする核酸分析装置。
【請求項22】
請求項12または21のいずれか記載の核酸分析装置において、
前記インレットと前記アウトレットの位置が、前記反応基板の外形より外側に配置されていることを特徴とする核酸分析装置。
【請求項23】
反応チャンバと、インレット及びアウトレットと、前記反応チャンバと前記インレット及び前記アウトレットをそれぞれ接続する供給流路及び排出流路と、を有するマイクロ流路チップにおいて、
その一部に反応スポットが配置された反応領域を有する反応基板と、
該反応基板より大きく、該反応基板を保持する凹部または少なくとも該反応基板が入る貫通孔を有する基板ホルダと、
該反応基板より大きく、少なくとも該反応領域部に相当する部分に貫通孔または凹部を有する第1のシートと、
該第1のシートと接着し、光学的に透明である、第2のシートと、
を有し、
該反応基板と、少なくとも該第1のシートにより、該反応領域面に反応チャンバが形成され、
該第1のシートと第2のシートの間に反応チャンバに連結する流路が形成され、
該流路の端部にインレット及びアウトレットが形成され、
該インレット及びアウトレットが該反応基板外形より離れた位置に形成されることを特徴とするマイクロ流路チップ。
【請求項24】
反応スポットが配置された反応領域を有する反応基板と、反応領域部の反応チャンバと、反応基板外形より離れた位置に設けたインレット及びアウトレットと、該反応チャンバと該インレット及びアウトレットを反応基板表面に接触しない流路で連結することを特徴とするマイクロ流路チップ。
【請求項25】
反応スポットが配置された反応領域を有する反応基板と、反応領域部の反応チャンバと、反応基板外形より離れた位置に設けたインレット・アウトレットを有するマイクロ流路チップ。
【請求項26】
請求項23から25のいずれか1項記載のマイクロ流路チップにおいて、
反応基板には反応領域が複数個所有し、複数のインレットおよびアウトレットを有することを特徴とするマイクロ流路チップ。
【請求項27】
請求項23記載のマイクロ流路チップにおいて、
前記反応基板とほぼ同じ大きさで、すくなくとも前記反応領域部の一部に貫通孔を有する第3のシートを、反応基板と前記第1のシートの間に配置することを特徴とするマイクロ流路チップ。
【請求項28】
請求項23または27記載のマイクロ流路チップにおいて、
前記第1のシート、または第2のシート、または第3のシートとして、接着性を有する樹脂、またはPDMSを使用することを特徴とするマイクロ流路チップ
【請求項29】
請求項23記載のマイクロ流路チップにおいて、
前記流路は、前記第1のシートまたは/および第2のシートに形成された凹部により形成されることを特徴とするマイクロ流路チップ。
【請求項30】
請求項23または29記載のマイクロ流路チップにおいて、
前記第2のシートはガラス板であることを特徴とするマイクロ流路チップ。
【請求項31】
請求項23または29記載のマイクロ流路チップにおいて、
前記第2のシートは厚さ0.02mmから0.2mmのガラス板であることを特徴とするマイクロ流路チップ。
【請求項32】
請求項23記載のマイクロ流路チップにおいて、
前記流路および前記インレット及びアウトレットは、第1のシートに形成されることを特徴とするマイクロ流路チップ。
【請求項33】
請求項23または32記載のマイクロ流路チップにおいて、
前記基板ホルダに、前記インレット及びアウトレットに相当する位置に、ほぼ同等の開口を有することを特徴とするマイクロ流路チップ。
【請求項34】
請求項23から26のいずれか1項記載のマイクロ流路チップにおいて、
前記インレット及びアウトレットは、前記反応領域から少なくとも15mm以上離れていることを特徴とするマイクロ流路チップ。
【請求項35】
請求項23または32または33または34のいずれか1項記載のマイクロ流路チップにおいて、
前記基板ホルダと第1のシートが同じ材質、または基板ホルダを第1のシートで兼用することを特徴とするマイクロ流路チップ。
【請求項36】
請求項23から26のいずれか1項記載のマイクロ流路チップにおいて、
前記反応基板の反応領域がエバネッセント照明されることを特徴とするマイクロ流路チップ。
【図1A】


【図1B】


【図1C】


【図1D】


【図1E】


【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図5D】


【図6A】


【図6B】


【図7】


【図8】


【図9A】


【図9B】


【図9C】


【図9D】


【図10A】


【図10B】


【図11A】


【図11B】


【図11C】


【図11D】


【図11E】


【図12A】


【図12B】


【図12C】


【図12D】


【図13A】


【図13B】


【図13C】


【図13D】


【図14A】


【図14B】


【図15A】


【図15B】


【図15C】


【図15D】


【図15E】




【図1B】


【図1C】


【図1D】


【図1E】


【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図5D】


【図6A】


【図6B】


【図7】


【図8】


【図9A】


【図9B】


【図9C】


【図9D】


【図10A】


【図10B】


【図11A】


【図11B】


【図11C】


【図11D】


【図11E】


【図12A】


【図12B】


【図12C】


【図12D】


【図13A】


【図13B】


【図13C】


【図13D】


【図14A】


【図14B】


【図15A】


【図15B】


【図15C】


【図15D】


【図15E】


【公開番号】特開2011−220996(P2011−220996A)
【公開日】平成23年11月4日(2011.11.4)
【国際特許分類】
【出願番号】特願2010−197992(P2010−197992)
【出願日】平成22年9月3日(2010.9.3)
【出願人】(501387839)株式会社日立ハイテクノロジーズ (4,325)
【Fターム(参考)】
【公開日】平成23年11月4日(2011.11.4)
【国際特許分類】
【出願日】平成22年9月3日(2010.9.3)
【出願人】(501387839)株式会社日立ハイテクノロジーズ (4,325)
【Fターム(参考)】
[ Back to top ]

