マイクロ遠心チューブとしての流体吸引/分配用先端部の使用
【課題】臨床分析器による分析前のサンプル処理能率を改善すること。
【解決手段】流体吸引/分配用部材は、サンプル獲得のためのサンプル用空洞部、およびシール可能な空洞部を含み、シール可能な空洞部は、いったんシールされると、遠心分離または他の分離方法の後、サンプル用空洞部内部の流体サンプル残部から、粒子を分離することを可能にする。流体吸引/分配用部材は、個別的、またはアレイの一部として、のいずれかで、臨床分析器による分析前のサンプル処理能率を増大させる。
【解決手段】流体吸引/分配用部材は、サンプル獲得のためのサンプル用空洞部、およびシール可能な空洞部を含み、シール可能な空洞部は、いったんシールされると、遠心分離または他の分離方法の後、サンプル用空洞部内部の流体サンプル残部から、粒子を分離することを可能にする。流体吸引/分配用部材は、個別的、またはアレイの一部として、のいずれかで、臨床分析器による分析前のサンプル処理能率を増大させる。
【発明の詳細な説明】
【開示の内容】
【0001】
〔本願の分野〕
本願は、単一の使い捨て可能な流体吸引/分配用部材の内部でサンプル収集および遠心分離するための装置および方法に関する。
【0002】
〔発明の背景〕
全血血清などの生物学的サンプルの試験をするための単一装置の中に「湿式」および「乾式」化学プラットフォームの両方を収容している組み合わせ臨床分析器が、現在、ほとんどの最新保健医療施設で広く使用されている。
【0003】
いわゆる「乾式」化学システムは、一般的に、サンプル供給部、多くのサンプル容器、計量/運搬機構、および例えば米国特許第3,992,158号に記載されているような複数の試験読取ステーションを有するインキュベータを含む。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする。典型的なプロトコルは、既知量のサンプルを流体吸引/分配用部材に吸引することから始まる。そしてサンプルの一定分量が、乾燥スライド要素上に分配され、この乾燥スライド要素はその後、インキュベータの中に装填される。適切なインキュベーションの後、サンプル中の少なくとも1つの分析対象の量または存在が、例えば電位計、反射計、または他の適当な試験デバイスを使用して決定される。
【0004】
一方、いわゆる「湿式」化学システムは、予め決定された容積測定量(volumetric quantities)のサンプル、試薬、および他の流体を受容するキュベットなどの反応容器を使用する。これらサンプル、試薬、および他の流体は、アッセイを行なうために適切に計量して反応容器内に入れられる。「湿式」化学システムは、一般的に、患者のサンプル流体をサンプル供給部から反応容器へ運搬するための計量機構を含む。1以上の反応が起こる予め決定されたインキュベーション期間の後、光測定デバイスなどの測定デバイスが、反応容器およびサンプルに一条の光線を通すために使用される。「湿式」化学システムで典型的に使用されるアッセイは、限定されるものではないが、終点反応分析(end point reaction analysis)および反応率分析などの分光光度的吸光度アッセイ(spectrophotometric absorbance assays)、濁度測定アッセイ、比濁分析アッセイ、放射エネルギー減衰アッセイ(例えば、米国特許第4,496,293号、および同第4,743,561号に記載されているアッセイ。これにより、これら特許の内容全体を参照によって本明細書に組み込んだものとする。)、イオン捕獲アッセイ、色彩(color)、計量的アッセイ(metric assays)、および蛍光測定アッセイ(fluorometric assay)、ならびにイムノアッセイを含み、これら全ては、当業界で周知である。
【0005】
湿式/乾式化学性能の臨床分析器への統合は、実験誤差を減らし、ワークフローを改善し、そして、人間の介入の必要性を制限することにより、ヒト病原体による研究室職員の汚染の危険性を減らす。湿式および乾式の化学システムの両方を利用している、市販の組み合わせ臨床分析器の一例が、Vitros 5,1 FS Chemistry Systemであり、これは、米国特許第7,250,303号、および米国特許出願公開第2003/0026733号にさらに詳細に記載されており(それぞれ、米国ニューヨーク州ロチェスターのOrtho-Clinical Diagnosticsに譲渡されている)、これら特許および特許出願公開の内容全体を参照によって本明細書に組み込んだものとする。
【0006】
進歩してきてはいるが、これらシステムは依然として、患者サンプルが臨床分析器へ送られる前に、まず微粒子成分を除去するために処理されることを必要とする。この処理ステップは相変わらず厄介で、時間がかかり、これら分析器の全体的な能率を制限している。
【0007】
この問題に取り組む試みに関連する情報が、米国特許第D453,573号;同第4,933,291号;同第5,384,239号;同第5,722,553号;同第5,753,186号;同第6,001,310号;同第6,334,842号;同第6,601,725号;同第6,622,882号;同第7,064,823号;米国特許出願公開第2001/0019842号;同第2005/0204832号;同第2005/0208676号;同第2007/0003443号,同第2007/0017927号;国際出願PCT/AU1992/000236号、および欧州特許第743095号に見出されうる。しかしながら、これら参考文献の各々は、以下の不都合な点の1つ以上を被っている:参考文献は、臨床分析前の患者サンプルの非能率的な処理を除去するものではなく、また、サンプル収集および遠心分離の両方を可能にする流体吸引/分配用部材を記載するものでもない。
【0008】
上述の理由によって、臨床分析器による分析前のサンプル処理能率を改善するための、未だ対処されていない必要性が本分野において存在する。
【0009】
〔本願の概要〕
本発明は、サンプル収集および遠心分離の両方に使用されうる、シール可能な端部を有する流体吸引/分配用部材に関連する。個々の流体部材、または複数の流体吸引/分配用部材を含むプレートのいずれかを用いて、サンプル収集および遠心分離を行なうための方法が記載される。
【0010】
一バージョンによれば、第1ポート、第1ポートと対向する第2ポート、およびキャップを含む、流体吸引/分配用部材が記載されている。このキャップは、第1ポートに取り付けられている場合、第1ポートを解放可能に閉じるように構成されている。流体吸引/分配用部材の内部体積(internal volume)は、第1ポートと第2ポートとの間のサンプル用空洞部、および第2ポートとサンプル用空洞部との間のシール可能な空洞部を含む。シール可能な空洞部のシールにより第2ポートがシールされて、サンプル用空洞部内に流体サンプルを保持し、かつサンプル中に懸濁されている粒子をサンプル残部から分離することを可能にするように構成された容器を作り出す。
【0011】
別の態様によれば、流体吸引/分配用部材は、粒子を流体サンプル残部から分離することができる試験装置の内部に設置されるように構成されている。この装置は、臨床分析器であってよい。粒子のサンプル残部からの分離は、例えば遠心分離の結果として起こりうる。
【0012】
一態様では、サンプル用空洞部の壁部は、先細になっているのに対し、シール可能な空洞部の壁部は、流体吸引/分配用部材の垂直軸に対して平行でありうる。
【0013】
流体吸引/分配用部材のシール可能な空洞部は、ヒートシール可能(heat-sealable)で、長さが1cm未満であることができ、壁部は2mm未満だけ離れていて流体吸引/分配用部材の垂直軸に対して平行である。
【0014】
一態様では、キャップは、吸引/分配用部材に取り外し可能に取り付けられている。
【0015】
吸引/分配用部材は、細胞懸濁液または血液でありうるサンプルの光学的または視覚的試験が可能であってよい。サンプル中の粒子は、赤血球でありうる。
【0016】
吸引/分配用部材は、各部材の内部体積内での凝集のために分離障壁または試薬をさらに収容できる。
【0017】
別のバージョンによれば、固体支持体に取り付けられた流体吸引/分配用部材のアレイを含む、流体吸引/分配用プレートが記載されている。吸引/分配用部材の各々は、第1ポート、および第1ポートに対向する第2ポートを含む。各流体吸引/分配用部材の内部体積は、第1ポートと第2ポートとの間のサンプル用空洞部、および第2ポートとサンプル用空洞部との間のシール可能な空洞部を含む。流体吸引/分配用部材の各々のシール可能な空洞部のシールにより、サンプル用空洞部内の流体サンプルを保持し、かつサンプル中に懸濁されている粒子のサンプル残部からの分離を可能にするように構成された、複数の容器が作り出される。
【0018】
一態様では、固体支持体は、平坦であり、流体吸引/分配用部材を支持するための手段を含むことができる。流体吸引/分配用プレートは、96個の流体吸引/分配用部材を有することができる。
【0019】
別の態様では、流体吸引/分配用部材は、固体支持体に可逆的(reversibly)に取り付けられる。
【0020】
別のバージョンでは、流体吸引/分配用プレートは、各流体吸引/分配用部材のサンプル残部から粒子を分離することができる試験装置の内部に設置されるように構成されている。この試験装置は、臨床分析器でありうる。
【0021】
サンプル残部からの粒子の分離は、遠心分離による分離の結果として起こりうる。
【0022】
流体吸引/分配用プレートのシール可能な空洞部は、ヒートシール可能な空洞部でありうる。
【0023】
別のバージョンでは、流体吸引/分配用プレートは、カバーを有し、このカバーが流体吸引/分配用プレートの第1ポート上に設置された場合、カバーは、第1ポートの各々を閉じるように構成されている。
【0024】
一態様では、プレートの流体吸引/分配用部材は、各部材の内部体積内部のサンプルの光学的または視覚的試験を可能にする。
【0025】
別の態様では、プレート上の吸引/分配用部材のアレイは、マイクロタイタープレートのウェル(wells)と整列している。マイクロタイタープレートの各ウェルは、プレート上の他のウェルの各々と異なるサンプルを保持でき、サンプルは、細胞懸濁液または血液でありうる。サンプル内部の粒子は、細胞でありうる。
【0026】
さらに別の態様では、プレート上の吸引/分配用部材は、各部材の内部体積内部での凝集のために分離障壁または試薬を収容できる。
【0027】
別の実施形態によれば、流体サンプル中の粒子を分離するための方法が記載されており、この方法は、(a)流体吸引/分配用部材を装置内へ装填するステップであって、この部材は、第1ポート、第2ポート、ならびに、第1ポートおよび第2ポートと流体連通しているサンプル用空洞部を含む、ステップと、(b)サンプルを、流体吸引/分配用部材の第2ポートを通してサンプル用空洞部内へ吸引するステップと、(c)流体容器を作り出すために流体吸引/分配用部材の第2ポートをシールするステップと、(d)第1ポートに解放可能に係合して第1ポートを覆うように寸法付けられたキャップを用いて第1ポートを閉じるステップと、(e)サンプル中の粒子をサンプル残部から分離するステップと、を含み、分離された粒子およびサンプルは、粒子またはサンプルの検出のために、流体吸引/分配用部材のサンプル用空洞部の内部に保持される。
【0028】
装置は臨床分析器でありうる。分離するステップは、例えば遠心分離によって行なわれうる。
【0029】
一態様によれば、装填するステップは、流体吸引/分配用部材を、装置の計量機構の管部(proboscis)に取り付けることを必要とする。
【0030】
別の態様では、流体吸引/分配用部材は、計量先端部である。
【0031】
一態様では、シールするステップは、流体吸引/分配用部材の第2ポートをヒートシールすることによって行なわれる。
【0032】
さらに別の実施形態によれば、複数の流体サンプル中の粒子を分離する方法が記載されており、この方法は、(a)流体吸引/分配用プレートを装置内に装填するステップであって、このプレートは、複数の流体吸引/分配用部材を含み、この部材の各々は、第1ポート、第2ポート、ならびに、第1ポートおよび第2ポートの各々と流体連通しているサンプル用空洞部を含む、ステップと、(b)複数のサンプルを、流体吸引/分配用部材の各々の第2ポートを通して、サンプル用空洞部内に吸引するステップと、(c)複数の流体容器を作り出すために流体吸引/分配用部材の各々の第2ポートをシールするステップと、(d)容器の各々の中において、サンプル中の粒子をサンプル残部から分離するステップと、を含み、粒子およびサンプルは、粒子またはサンプルの検出のために、流体吸引/分配用部材の各々のサンプル用空洞部の内部に保持される。
【0033】
一態様では、装置は臨床分析器である。
【0034】
分離するステップは、遠心分離により行なわれうる。
【0035】
一態様では、装填するステップは、流体吸引/分配用プレートを、装置の計量機構の複数の管部に取り付けることを必要とする。
【0036】
別の態様では、流体吸引/分配用部材は、計量先端部である。
【0037】
別の実施形態によれば、吸引するステップの後、流体吸引/分配用部材の各々の第1ポートは、蓋によって閉ざされ、蓋が流体吸引/分配用部材の第1ポートの上に設置されると、蓋は、流体吸引/分配用部材の各々の第1ポートを閉じるように構成されている。
【0038】
シールするステップは、流体吸引/分配用部材の各々の第2ポートをヒートシールすることによって行なわれうる。
【0039】
前述した実施形態は、個々の使い捨て可能な流体吸引/分配用部材、または複数の流体吸引/分配用部材を含む流体吸引/分配用プレートのいずれかを用いて、サンプル収集および粒子分離を行なう能力を含む、多くの利点を有する。本明細書に記載される方法は、取り扱いの誤り、および、臨床分析器による分析の前にサンプル処理に費やされる時間を減らす。したがって、本明細書に記載された流体吸引/分配用部材を用いたサンプル処理は、当業界で既知の従来方法よりも迅速である。
【0040】
本願は、この概要に開示された実施形態に制限されるものではなく、当分野における十分な技術の範囲内、かつ特許請求の範囲によって定められた範囲内の、修正および変形を含むように意図されていることが、理解されるべきである。
【0041】
〔詳細な説明〕
別段の定義がされていない限り、本明細書で使用される全ての技術用語および科学用語は、当業者によって一般的に理解されるのと同じ意味を有する。以下の定義は、本願の開示および特許請求の範囲を解釈するのを助けるために提供される。このセクションにおける定義が他の場合の定義と一致しない場合、このセクションに述べられる定義が、支配するであろう。
【0042】
本明細書に使用される「組み合わせ」分析器は、「乾式」および/または「湿式」化学システムの任意の組み合わせを包含することができる、少なくとも2つの化学システムを含む臨床分析器を指す。
【0043】
本明細書に使用される「臨床分析器」は、限定されるものではないが、臨床サンプルの「湿式」および/または「乾式」の自動化学分析のための分析器だけでなく免疫診断分析器を含む、臨床サンプルを分析することができる任意の装置を指す。「湿式」化学プラットフォームは典型的に、反応容器の中に1以上のサンプルおよび/または試薬を吸引および分配する自動流体取り扱いシステムを制御するマイクロプロセッサと、少なくとも1つのサンプル貯蔵器と、オプションの少なくとも1つの試薬貯蔵器と、少なくとも1つのインキュベータと、分光光度計などの少なくとも1つの検出器とを、含む。本願の流体吸引/分配用部材と共に使用するための典型的な分析器は、米国特許第6,096,561号、同第7,282,372号、および同第7,250,303号にさらに詳細に記載されており、これら特許全ての内容全体を参照によって本明細書に組み込んだものとする。好適な実施形態では、本明細書で使用される臨床分析器は、Ortho-Clinical Diagnostics, Inc.により製造されているVITROS 5,1 FS Chemistry Systemなどの市販の分析器を指す。
【0044】
流体が、毛管現象および/または重力によるなどして、ある要素から別の要素へ移動できる場合、一方の要素は、もう一方の要素と「流体連通」している。要素は、直接接触していてもよいが、直接接触の必要はない;すなわち、前記流体が通ることができる他の要素が介在していてもよい。流体が、毛管現象および/または重力により、ある要素から別の要素へ移動できない場合、一方の要素は、もう一方の要素と「流体連通していない」。典型的に、要素は、物理的に分離されている、すなわち離隔している。
【0045】
本明細書に使用される「流体吸引/分配用部材」は、2つ以上のシール可能な開口部と流体連通している1つ以上の内部空洞部を収容している計量先端部などのデバイスであり、米国特許第6,797,518号に記載されているようなサンプル収集および粒子分離の両方に使用される。これによりこの特許の内容全体を参照によって本明細書に組み込んだものとする。一実施形態では、粒子分離は、遠心分離の結果として起こる。流体吸引/分配用部材は典型的に、臨床分析器内部において、容積測定量のサンプルの吸引または分配を行なう。一実施形態では、流体吸引/分配用部材は、内部空洞部の変形を伴わずに遠心分離されうる、成型された固体材料から構成される。別の実施形態では、この材料は、生物学的サンプルの、流体吸引/分配用部材の内壁部への付着を促進しない。別の実施形態では、流体吸引/分配用部材は、典型的に押出しブロー成型により塑性材料から作られる。流体吸引/分配用部材は、その中への吸引後、流体内容物に光学的試験を行なうことを可能にする半透明または透明な特徴を好ましくは有する熱可塑性材料から作られうる。一実施形態では、流体吸引/分配用部材は、ポリプロピレンまたはポリエチレンなどの成型用プラスチックから作られる。別の実施形態では、流体吸引/分配用部材は、ホモポリマー、またはポリアロマーなどの共重合体から作られ、単量体の1つは、プロピレンである。さらに別の実施形態では、流体吸引/分配用部材は、ポリエチレンテレフタレートから作られる。
【0046】
本明細書に使用される「流体吸引/分配用プレート」は、固体支持体に取り付けられた複数の流体吸引/分配用部材のアレイを指す。各流体吸引/分配用部材は、サンプル収集および粒子分離の両方のために、2つ以上のシール可能な開口部と流体連通している1つ以上の内部空洞部を含む。流体吸引/分配用プレートは典型的に、臨床分析器内部において、容積測定量の1つ以上のサンプルの吸引または分配に使用される。一実施形態では、支持体は、平坦で、矩形または正方形の形状であるが、本明細書に記載される流体吸引/分配用プレートは、任意の形状を有してよい。別の実施形態では、流体吸引/分配用プレート上の流体吸引/分配用部材は、幾列にもなって配列されており、各列は、同数の流体吸引/分配用部材を有する。別の実施形態では、流体吸引/分配用プレートは、流体吸引/分配用部材のための支持体を含む。当業者であれば、この支持体は、臨床分析器内での遠心分離およびロボットによる取り扱いを容易にするように設計されうることを、認識するであろう。一実施形態では、流体吸引/分配用部材は、固体支持体に可逆的に固定される。別の実施形態では、複数の流体吸引/分配用部材は、マイクロタイタープレートのウェルと整列するような要領で、流体吸引/分配用プレート上に配列されている。さらに別の実施形態では、プレートは、1、2、5、10、25、50、75、100、またはそれ以上の流体吸引/分配用部材の可逆的な取り付けのための複数の場所を有する。プレート上の各場所は、流体吸引/分配用部材で充填されていても、充填されていなくてもよい。
【0047】
本明細書に使用される「サンプル残部からの粒子の分離」は、サンプルの固形微粒子相からサンプルの液体相を分離することを可能にする任意の手順を指す。一実施形態では、「サンプル残部からの粒子の分離」は、流体吸引/分配用部材のシール後、流体吸引/分配用部材のサンプル用空洞部の内部で、サンプル液体相からサンプルの固形微粒子相を部分的または完全に分離することを指す。別の実施形態では、分離は、遠心分離の結果として起こる。さらに別の実施形態では、分離は、サンプルに加えられた磁性粒子に働く磁場の結果として生じる。
【0048】
本明細書に使用される用語「シール可能な空洞部」は、サンプル用空洞部と流体吸引/分配用部材の底端部との間に位置する流体吸引/分配用部材の領域であって、例えばヒートシールによるか、または本明細書に定められるようなシーラントの適用の結果として、シールされうる、流体吸引/分配用部材の領域を指す。シールの結果、サンプル用空洞部はもはや、流体吸引/分配用部材の吸引/分配用端部と流体連通しておらず、ゆえに粒子分離のための流体容器を作り出す。一実施形態では、シール可能な空洞部は、熱可塑性の溶融−融合性材料(thermoplastic melt-fusible material)から作られる。別の実施形態では、熱可塑性の溶融−融合性材料は、当業者によって知られているようなヒートシールに適当な、ポリアロマーまたは類似の熱可塑性材料である。
【0049】
本明細書に使用される「ヒートシール」は、流体吸引/分配用部材のシール可能な空洞部の壁部を共に融合させるために、その壁部に十分な熱および圧力を加えることを指す。続く硬化、すなわち融合された熱可塑性壁部の強固化および凝固化が、シール可能な空洞部の圧力抵抗性シールを作り出し、この圧力抵抗性シールは、流体吸引/分配用部材のサンプル用空洞部とシール可能な吸引/分配用端部との間の流体連通を妨げる。ヒートシールのさらに詳細な記載は、米国特許第3,929,943号に見出されうる。これによりこの特許の内容全体を参照によって本明細書に組み込んだものとする。別の実施形態では、ヒートシールは、流体吸引/分配用プレート上に配列された複数の流体吸引/分配用部材のシール可能な空洞部に適用される。例えば、流体吸引/分配用部材のアレイの吸引/分配用端部は、整列させられ、金属製成型カップのアレイに挿入されうる。金属製成型カップは、そのカップ内に置かれたシール可能な空洞部の壁部の溶融および融合を促進する温度まで熱せられる。
【0050】
本明細書に使用される「シール(sealing)」は、流体吸引/分配用部材の吸引/分配用端部を恒久的に閉じることを指す。一実施形態では、シールはヒートシールを指す。別の実施形態では、シールは、流体吸引/分配用部材の吸引/分配用端部を密閉式に塞ぐ、例えばプラスチックまたは接着剤といったシーラントの適用を指す。別の例では、シーラントは、流体吸引/分配用部材の吸引/分配用端部を密閉式に閉じる、底部ねじぶたなどの底部キャップであってよい。
【0051】
本明細書に使用される「シーラント」は、本明細書に記載された流体吸引/分配用部材のシール可能な空洞部の壁部の間に連結結合を形成するために使用されうる接着剤などの任意の組成物を意味するものとする。一実施形態では、シーラントは、UV硬化性である。別の実施形態では、シーラントは、室温で硬化する。
【0052】
本明細書に使用される用語「ポリアロマー」は、通常ホモポリマーにのみ関連する結晶化度を呈する、1−オレフィンの共重合体を生成する任意の熱可塑性材料を指す。一実施形態では、ポリアロマーは、プロピレンとエチレンとのランダムブロック共重合体である。別の実施形態では、ポリアロマーは、「Tenite(登録商標) Polyallomer」という商品名でEastman Chemical Co.により販売されている、容易に融合可能な塑性材料である。
【0053】
本明細書に使用される用語「空洞部」は、記載された流体吸引/分配用部材の内部の任意の3次元の囲われた場所(enclosure)を指す。例示的実施形態では、1つ以上の空洞部が、互いに流体連通している。
【0054】
用語「複数」は、本明細書に使用されるように、2つ以上の数量を指す。
【0055】
本明細書に使用される「粒子」は、細胞であってよく、例えば、サンプル中に見出される細菌または赤血球または白血球である。別の実施形態では、粒子は、サンプル処理前に、サンプルに加えられる微細固形物であってよい。これらの粒子は、ビーズの形態の不活性固形物、ビーズのようになったゲル(beaded gels)、または微小球であってよいが、これら粒子は任意の形状を有してもよい。粒子のさらなる例は、限定されるものではないが、プラスチック粒子、セラミック粒子、カーボン粒子、ポリスチレンミクロビーズ、ラテックスビーズ、ガラスビーズ、磁気ビーズ、中空ガラス球体、金属粒子、複合組成物の粒子、微細加工またはマイクロ機械加工粒子(microfabricated or micromachined particles)を含む。不活性粒子は、ガラスもしくはセラミックスなどの任意の適した材料、カーボンもしくはプラスチックなどの有機材料、および/または、例えばナイロン、ポリテトラフルオロエチレン(TEFLON(商標))もしくはスチレン−ジビニルベンゼンポリマーなどの1種類以上のポリマーから、構成されうる。粒子サイズは、約0.1μm〜1000μmであってよい。好ましくは、粒子サイズは、約1μm〜約10μmである。原理上は、任意のリガンドが、例えば、HeamらによるMethods in Enzymology Vol. 35:102-117 (1987)に記載されているような既知の技術を用いて、固相マトリクス、またはアガロースビーズ(例えばセファロース・ファルマシア)などの粒子に共有結合してよい。一般的に、ビーズは、まず、グルタルアルデヒド、カルボニルジイミダゾール(carbonyldiimidizole)、臭化シアンヒドロキシスクシンイミド(cyanogen bromide hydroxysuccinimide)、塩化トシル(tosyl chloride)または同種のものなどの化学薬品によって、活性化される。その後、選択されたリガンドが、ビーズに共有結合し、その結果、リガンドのその支持体に対する非常に安定した結合を生じる。
【0056】
本明細書に使用される「細胞懸濁液」は、サンプル中に典型的に見出される、液体中の細胞の混合物を指す。細胞は、真核生物または原核生物の細胞でありうる。一実施形態では、細胞は、細菌である。別の実施形態では、細胞は、病原菌である。好適な実施形態では、細胞は、血液細胞である。別の好適な実施形態では、細胞は、赤血球である。
【0057】
本明細書に使用される用語「サンプル」は、少なくとも1つの分析対象を含有すると推測される材料を指す。サンプルは、ソースから獲得されたままで直接使用されうるか、またはサンプルの特徴を改変するための前処置に続いて、使用されうる。サンプルは、血液、血漿、唾液、眼球レンズ流体(ocular lens fluid)、脳脊髄液、汗、尿、乳汁、腹水(ascites fluid)、raucous、滑液、腹水(peritoneal fluid)、羊水、または同種のものを含む生理流体など、任意の生物学的ソースに由来するものでありうる。サンプルは、使用前に前処置されうる。例えば、全血は典型的に、血液凝固を防ぐためにヘパリンおよび同様のものなどポリアニオンで処置される。別の例では、粘性流体が希釈されうる。処置方法は、ろ過、蒸留、濃縮、干渉成分の不活性化、および試薬の添加を含むこともできる。生理流体のほかに、他の液体サンプルが使用されうる。加えて、分析対象を含有すると推測される固形材料が、サンプルとして使用されうる。いくつかの例では、固形サンプルを改変して、液体媒体を形成すること、または分析対象を放出することは有益でありうる。別の実施形態では、サンプルは、本明細書に定められるように、分析前または分析中にサンプルに加えられうる1種類以上の化合物を含むことが理解され、その1種類以上の化合物には、限定されるものではないが、緩衝剤、試薬、ペプチド、酵素、リガンド、リガンド結合分子、抗体、粒子、リガンド結合粒子、磁性粒子、および同様のものが含まれる。サンプルは、本明細書に定められるように、前記に定義されたような粒子を含有してよい。
【0058】
用語「分析対象」は、本明細書に使用されるように、検出または測定される、任意の化合物または組成物または存在物を指す。分析対象は、当業界で既知の臨床アッセイにより試験される、任意の、無機分子もしくは有機分子、または細胞成分、または細胞、または生物体でありうる。臨床アッセイは、分析対象の存在または不在のいずれかを試験してもよい。一実施形態では、分析対象は、少なくとも1つの、エピトープまたは結合部位またはリガンドを有する。別の実施形態では、分析対象は、任意の物質であって、この物質のための、自然発生的な結合メンバーが存在するか、またはこの物質のために結合メンバーが準備されうるような、任意の物質でありうる。さらに別の実施形態では、分析対象は、例えば、白血球、赤血球(ヘマトクリット)または血小板などの血液細胞といった細胞集団を指す。分析対象はまた、限定されるものではないが、代謝産物、毒素、無機または有機の化合物、タンパク質、ペプチド、サイトカイン、ケモカイン、酵素、アミノ酸、脂質、HDL/LDLコレステロール、トリグリセリド、多糖類、血糖、核酸、ホルモン(例えば、甲状腺刺激ホルモン(TSH)、副腎皮質刺激ホルモン(ACTH)、プロラクチン)、ステロイド(例えば、コルチゾールまたはテストステロンまたはエストロゲン)、ビタミン、電解質、薬剤、イオン(例えばpH測定のための)、微量金属、微生物(細菌、ウィルスまたは寄生生物、および同類のもの)、ウィルス粒子、上記の物質のいずれかの代謝産物、および上記の物質のいずれかに対する抗体を含むことができる。別の実施形態では、分析対象は、C反応性タンパク質、アルブミン、アミラーゼ、Dダイマー、ビリルビン、アルカリホスファターゼ、γグルタミルトランスフェラーゼ、尿素、クレアチン、血清鉄、トランスフェリン(transferring)、前立腺特異抗原(PSA)、αフェトプロテイン(AFP)、βヒト絨毛性性腺刺激ホルモン(bHCG)、α1−アンチトリプシン(AAT)、CA−125(CA12.5とも言う)、癌胎児性抗原(CEA)、フィブリノーゲン、または典型的に試験される、臨床サンプル中の任意の他の化合物である。用語「分析対象」は、任意の抗原性物質、ハプテン、抗体、巨大分子、およびこれらの組み合わせを含んでよい。別の実施形態では、分析対象は、酵素活性を測定することによって検出されうる酵素である。例えば、血液中での、クレアチンキナーゼ、グルタミン酸オキサロ酢酸トランスアミナーゼ(SGOT)、血清グルタミン酸ピルビン酸トランスアミナーゼ(SGPT)活性の試験は、肝臓または心臓の障害の指標として広く使用されている。
【0059】
本明細書に使用される「リガンド」は、リガンド結合分子に結合することができる任意の分子である。一実施形態では、リガンドは、抗体のエピトープである。免疫グロブリン分子に結合し、本願に使用される粒子に共有結合されうる、例えばプロテインA、プロテインG、プロテインA/GおよびKappaLock(商標)といった、多くのリガンドも知られている(米国特許第5,665,558号も参照のこと。この特許の内容全体を参照によって本明細書に組み込んだものとする)。リガンドは、使用されるか、または試験される、抗体のイソタイプに結合することができる。あるいは代替的に、リガンドは、例えば、IgM抗体に対して、IgG抗IgM(IgG anti-IgM)といったブリッジ抗体(bridging antibody)を使用することができる。ゆえに、IgG抗IgM抗体が、「ブリッジ」としてリガンドに結合され、IgM抗体が、IgG抗IgM抗体に結合するであろう。
【0060】
用語「リガンド結合」は、本明細書に使用されるように、結合対のメンバーを指し、すなわち2つの異なる分子であって、その分子の一方が、化学的手段または物理的手段により、第2分子に特異的に結合している、2つの異なる分子を指す。抗原および抗体の結合対メンバーに加えて、他の結合対は、限定するものではなく例として、ビオチンおよびアビジン、炭水化物およびレクチン、相補的ヌクレオチド配列、相補的ペプチド配列、多糖類およびレクチン、エフェクターおよびレセプター分子、酵素補因子および酵素、酵素阻害剤および酵素、ペプチド配列およびその配列またはタンパク質全体に対して特異的な抗体、ポリマー酸および塩基、色素およびタンパク質結合剤、ペプチドおよび特異的タンパク質結合剤(例えば、リボヌクレアーゼ、S−ぺプチド、およびリボヌクレアーゼS−タンパク質)、ならびに同様のものを含む。さらに、結合対は、例えば、組み換え技術または分子工学により作られる分析対象−類似体または結合メンバーといった、原型の結合メンバーの類似体であるメンバーを含むことができる。結合メンバーが免疫反応体(immunoreactant)である場合、その結合メンバーは、例えば、モノクロナール抗体またはポリクロナール抗体、組み換えタンパク質または組み替え抗体、キメラ抗体、上述の混合物もしくは断片、ならびに、結合メンバーとして使用するための適合性が当業者に周知である、そのような抗体、ペプチド、およびヌクレオチドの調製物でありうる。リガンド結合メンバーは、ポリペプチド親和性リガンドであってもよい(例えば米国特許第6,326,155号を参照のこと。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする)。一実施形態では、リガンド結合メンバーは、標識付けされている。標識は、蛍光ラベル、化学発光ラベルもしくは生物発光ラベル、酵素−抗体構造体(enzyme-antibody construct)、または当業界で既知の他の類似の適当なラベルから選択されてよい。
【0061】
本明細書に使用される「血液」は、全血、または、赤血球、白血球、血漿もしくは血清などの全血の任意の成分を広く含む。
【0062】
本明細書に使用される「遠心分離」は、回転軸の周りでの対象物の回転を指す。サンプルは、固定角ローターもしくはスイング・バケット・ローター(a fixed angle or swing bucket rotor)、または当業界で既知の任意の他のローターで遠心分離されうる。
【0063】
本明細書に使用される「STAT」は、直ちに、を意味するラテン語「statim」に由来する医学用語である。したがって、「STATレーン(STAT lane)」は、患者サンプルの至急または急ぐ処理を指す。
【0064】
本明細書に使用される「緊急サンプル」は、即時の処理を必要としている任意のサンプルを指す。緊急サンプルは典型的に、緊急治療室または他の救急手当施設で収集されたサンプルを含む。例えば、緊急治療室のサンプルは、緊急治療室内の患者から採取された血液サンプルでありうる。
【0065】
「凝集」は、本明細書に使用されるように、試薬、通常は抗体または他のリガンド結合する存在物による、細胞性抗原または微粒子抗原の懸濁液のクランピングを指す(例えば、米国特許第4,305,721号、同第5,650,068号、および同第5,552,064号を参照のこと。これにより、これら特許の内容全体を参照によって本明細書に組み込んだものとする)。一実施形態では、試薬は、クームス試薬(Coomb’s reagent)である。
【0066】
本明細書に使用される「クームス試薬」は、以下のヒト免疫グロブリン、補体、または特異的免疫グロブリンのうちの1つに対して向けられる、動物の体内で生じた抗体の調製物を指し、例えば、クームス試験に使用される抗ヒトIgGである。
【0067】
本明細書に使用される「検出」は、光検出器を用いた、光吸収または光散乱の検出を指す(例えば、米国特許第5,256,376号、および米国特許出願公開第2004/0166551号を参照のこと。これにより、これら特許および特許出願公開の内容全体を参照によって本明細書に組み込んだものとする)。一実施形態では、検出は、生物発光または化学発光または蛍光の検出を指す(例えば、米国特許第6,596,546号を参照のこと。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする)。
【0068】
本明細書に使用される用語「撹拌」は、流体吸引/分配用部材の内容物に働く力を指し、例えば、遠心力、または磁場によって誘起された力を指す。
【0069】
本明細書に使用される「計量デバイス」は、本明細書で使用されるように、管部によって流体吸引/分配用部材に可逆的に取り付くことができる臨床分析器の構成要素を指す。一実施形態では、オンボード・コンピュータにより制御される計量デバイスが、臨床分析器内部の、流体吸引/分配用部材または流体吸引/分配用プレートの移動および/または運搬を調整している。
【0070】
本明細書に使用される用語「管部(proboscis)」は、個別的、または流体吸引/分配用プレートの一部として、のいずれかで、1つ以上の吸引/分配用部材に取り付く臨床分析器の構成要素を指す。一実施形態では、管部は、計量機構の一部であり、円筒形の形状であってよく、流体吸引/分配用部材の管部レセプタクル領域の内壁部に対して管部自体を気密式に挿入するような(すなわち、管部の円筒形表面と壁部との間に実質的な空気の漏れが存在しない)要領で、1つ以上の流体吸引/分配用部材の各々の管部レセプタクル領域の内部に嵌まる。管部が流体吸引/分配用部材の各々の管部レセプタクル領域に密閉式に固定されると、計量機構を用いて、管部が各流体吸引/分配用部材の内部体積に減圧または圧力のいずれかを与え、それにより、各流体吸引/分配用部材の内部空洞部内部の既知分量の流体を移動させる。
【0071】
本明細書に使用される用語「分離障壁(separation barrier)」は、水不混和性で、典型的にチキソトロピーの、ゲル様またはビーズ様の材料であって、サンプルの軽い液体相に見出される密度と、サンプルの重い実質的に微粒子の相に見出される密度との間の中間の密度を有する、材料を指す。例えば、分離障壁は典型的に、流体吸引/分配用部材のサンプル用空洞部の中に配され、流体吸引/分配用部材はその後サンプルで充填される。遠心分離すると、サンプルは2つの相に傾斜分離され(gradient separated)、障壁材料は、相と相との間の界面に移行する。遠心分離が完了すると、分離障壁が、分離された相の相互間に物理的および化学的な障壁を形成し、それにより、相のいかなる混合も防ぐ。分離障壁は、例えば、シリコーン流体と微細な疎水性シリカ粉末との混合物、ポリエステル材料、またはポリブタン(polybutane)などの炭化水素ゲル様材料、または、当業界で既知の任意の他の材料でありうる。分離障壁材料の組成は、米国特許第4,190,535号;同第4,101,422号;同第4,818,418号、および同第4,147,628号にさらに詳細に記載されている。これにより、これら特許の内容全体を本明細書に組み込んだものとする。
【0072】
本明細書に使用される用語「抗体」は、ポリクロナール抗体およびモノクロナール抗体の両方を含み;完全な分子、そのフラグメント(Fv、Fd、Fab、Fab’およびF(ab)’2フラグメントなど)、あるいは、完全な分子および/またはフラグメントの多量体または集合体であってよく;自然発生するか、または、例えば免疫化、合成もしくは遺伝子操作によって生成されてもよい。本明細書に使用される抗体または抗原は、試験されている抗体または抗原によって決まる。例えば、血液型抗原の数、および、ゆえに識別されたそれら抗原に対する抗体の数は、非常に多く、さらなる抗原および抗体が、絶えず決定されている。国際輸血学会(The International Society of Blood Transfusion)は、Blood Group Terminology 1990, Vox. Sang. 58:152-169 (1990)に赤血球抗原の非排他的リストを公表しており、限定されるものではないが、抗体および抗原A、B、D、C、c、Cw、E、e、K、Fya、Fyb、Jka、Jkb、S、およびsを含む。
【0073】
本明細書に注記された前述の定義をふまえて、以下の記載は、本願のある好適な実施形態、および、化学分析前の患者サンプルの初期処理のための特定の方法論に関する。解説から容易に明らかになるであろうが、本明細書に記載された発明の概念は、患者サンプルの効果的な処理を必要とする他の方法にも適切に適用されうる。加えて、「上部」、「底部」、「側方」、「上方」、「下方」および同様のもののような用語もまた、添付の図面で使用するための便利な基準系を提供するために使用される。しかしながら、これらの用語は、別段に特記されていない限り、本発明を限定することを意図されていない。遠心分離または他の分離方法によりサンプル収集および粒子分離の両方を可能にし、それにより組み合わせ臨床分析器の湿式/乾式化学構成要素による分析の前の、サンプル処理の効率を増大させる、新規の流体吸引/分配用部材が、本明細書に記載されている。
【0074】
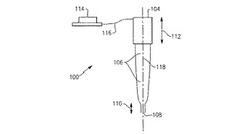
第1実施形態によれば、図1は、サンプル収集および粒子分離のためのシール可能な流体吸引/分配用部材100を示している。流体吸引/分配用部材100は典型的には、射出成型可能で、好ましくは透明な、熱可塑性材料から構成されており、その材料は、ポリプロピレン、ポリアロマー、ポリエチレンテレフタレート、ポリマーの共重合体もしくはブレンド、または当業界で既知の任意の他の適当な不活性材料などである。好ましくは、分析されているサンプルは、流体吸引/分配用部材100の内部体積の壁部に粘着せず、流体吸引/分配用部材100のこれらの表面は、サンプルまたは試薬の、流体吸引/分配用部材100の内部表面へのこのような粘着を避けるように処置されてよい。流体吸引/分配用部材100の内部体積は、約1μL〜約2000μL、またはそれを超えてもよい。一例では、内部体積は、約1μL〜約500μLである。好適な実施形態では、流体吸引/分配用部材100は、約1μL〜約300μLの内部体積を有する。流体吸引/分配用部材100の壁部の厚さは、変形することなく遠心分離に耐えることができるならば、重要ではない。典型的には、壁部は、約5mm〜約0.1mm、約2mm〜約0.5mm、または約1.5mm〜約0.75mmの厚さを有する。図1に示すように、流体吸引/分配用部材100は、上端部でインプットポート104により、そして下端部でシール可能なインプットポート108により、定められている。インプットポート104とインプットポート108との間には、サンプル用空洞部106を含む内部空洞部があり、サンプル用空洞部106は、インプットポート104および108と流体連通している。インプットポート104は、流体吸引/分配用部材100の内部体積から既知分量の空気を移動させるために、(この図には示されていない)計量機構の管部に密閉式に取り付くように構成されている。一実施形態では、管部320は、インプットポート104を通って流体吸引/分配用部材100の管部レセプタクル領域112の中へ密閉式に入り込む。シール可能なインプットポート108は、インプットポート108を介するサンプル用空洞部106内への流体の吸引または分配を可能にするように構成されている。シール可能な空洞部の壁部は、ヒートシールを容易にするためにサンプル用空洞部106の壁部よりも薄くてよい。一バージョンでは、流体吸引/分配用部材100の内部体積は、臨床分析のために必要とされる試薬で予め装填されていてよく、この試薬は、例えば、血液凝集または血液型検査のための試薬である。別の実施形態では、流体吸引/分配用部材100のサンプル用空洞部は、本明細書に定義されたような分離障壁を収容する。
【0075】
次に図1および図2を参照すると、本明細書に記載された流体吸引/分配用部材100は、つなぎ縄(tether)116により部材100の上端部に連結されたオプションのキャップ114を備えて、示されている。つなぎ縄116は、サンプル収集または粒子分離、すなわち遠心分離を妨げない限り、いかなる長さであってもよい。例えば、つなぎ縄116は、約0.5cm〜約2cmの長さ、または約0.5cm〜約1cmの長さであってもよい。つなぎ縄116を方向210に曲げることにより、キャップ114は、インプットポート104内に可逆的に挿入されうる。一バージョンでは、キャップ114は、(不図示の)流体吸引/分配用部材100に取り付けられておらず、したがって、遠心分離前にインプットポート104の中に直接挿入される。インプットポート104上へのキャップ114の設置は、流体吸引/分配用部材100の遠心分離および/または取り扱いの間にサンプル用空洞部106内の流体がインプットポート104を通って流出するのを防ぐ、密閉式シールを形成する。別のバージョンでは、流体吸引/分配用部材100は、キャップを必要としない。さらに別の実施形態では、インプットポート108は、シール可能な空洞部110の中に挿入された後に硬化される、本明細書に定められたようなシーラントを用いてシールされてもよい。
【0076】
図1、図2、および図3Aを参照すると、本明細書に記載された流体吸引/分配用部材100は、サンプル用空洞部106とシール可能なインプットポート108との間に配されるヒートシール可能な空洞部110を含む。ヒートシール可能な空洞部110へ熱を加えると、壁部の熱可塑性材料が溶融して融合し、ゆえにシール可能なインプットポート108をシールする。他の方法もまた、インプットポート108をシールするために利用されてよい。例えば、接着剤などのシーラントが、インプットポート108に適用され、冷却または、例えばUV放射に局所的に曝すなど他の手段により、硬化されてよい。別のバージョンでは、インプットポート108は、底部キャップ、例えば底部ねじぶた(不図示)を用いて、密閉式に閉ざされる。
【0077】
流体吸引/分配用部材100の上述の構造説明を伴って、次に、第2実施形態による流体吸引/分配用部材100内部でのサンプル収集および粒子分離に関する方法が記載される。
【0078】
図3Bを参照すると、計量機構350、より詳細には臨床分析器の管部320に取り付けられた場合の流体吸引/分配用部材100が示されている。管部は、分析器の計量機構の構成要素を形成している。適切なロボット命令が、計量システムに、管部320を流体吸引/分配用部材100のインプットポート220と整列させるように指示する。適切な整列の後、計量システムは、管部320を、開口インプットポート220を通して流体吸引/分配用部材100の管部レセプタクル領域112の中へ密閉式に挿入する。インプットポート108は、その後、サンプル330中に浸漬される。計量機構350の管部320は、流体吸引/分配用部材100の内部体積内部に制御された量の負圧を作り出す。インプットポート104を通る空気310の続く転位が、流体吸引/分配用部材100のサンプル用空洞部106内への、定められた分量のサンプル330の移動343を促進する。吸引されるサンプルの分量は、サンプル用空洞部106内部の利用可能な体積によって決まる。一例では、約1μL〜約1000μLの間の一定分量(aliquot)のサンプル330が、吸引される。別の例では、約1μL〜約300μLの一定分量のサンプル330が、吸引される。さらに別の例では、約1μL〜約50μLのサンプル330が、流体吸引/分配用部材100のサンプル用空洞部106の中へ吸引される。
【0079】
図3Cを参照すると、サンプル用空洞部106内へのサンプル330の吸引が完了した後、流体吸引/分配用部材100のインプットポート108は、サンプル330から取り除かれる。計量機構350の管部320は、再び、流体吸引/分配用部材100の内部体積の内部に制御された量の負圧を作り出し、この負圧により、空気347の小さな気泡がインプットポート108を通って吸引され、吸引されたサンプル345をインプットポート108から離してサンプル用空洞部106内へ適切に転位させる。管部320と流体吸引/分配用部材100の管部レセプタクル領域112との間の気密シールを維持することにより、サンプルは、インプットポート108のヒートシール前は、サンプル用空洞部106内部に保持される。この手順は、確かなシールと、分析前の吸引されたサンプル345のあらゆる温度上昇の制限との、両方を確実にする。
【0080】
図3Dを参照すると、流体吸引/分配用部材100のインプットポート104は、管部320が流体吸引/分配用部材100の管部レセプタクル領域112の中に密閉式に挿入されたままである間に、ヒートシールデバイス353内に設置される。その後、シール可能な空洞部110の壁部の熱可塑性材料が、その溶融温度まで急速に熱せられる。そのポリマーが溶融温度まで熱せられるべき速度は、上記で本明細書に組み込まれた米国特許第3,929,943号に詳細に記載されているように、ポリマーの固有粘度、シール可能な空洞部110の壁部の厚さおよび直径によって決まる。加熱の最大期間は、約1秒〜約30秒、または5秒〜約20秒、または約10秒〜約15秒でありうる。ヒートシールデバイスは、タングステン電球または石英灯などの高強度ラジエントヒーター(high-intensity radiant heater)でありうる。代替的に、誘導加熱器または超音波加熱器、または当業界で既知の任意の他の手段などのマイクロ波加熱器が利用されうる。溶融温度は、約200℃〜約350℃でありうるが、流体吸引/分配用部材100の熱可塑性特性によって決まる。ヒートシール可能な空洞部110の壁部が熱せられた後、その壁部は、プレス357によって方向362にプレスされ、壁部を共に押し付けて開口端部をシールする。一バージョンでは、プレス357の端部は、流体吸引/分配用部材100のインプットポート108を覆うように嵌まるカップ364の形態に成形されており、インプットポート108を融合および成型してシールされた端部355にすることを容易にする。一バージョンでは、金属プレス357は、適切な溶融温度まで熱せられ、シール可能なインプットポート108に直接適用される。シール後、インプットポート108は、融合された熱可塑性材料の凝固化を促進するために急速に冷却され、ゆえに密閉式にシールされた流体容器またはキュベットを生成する。その後、プレス357および計量デバイス320は、取り外される。
【0081】
図3E〜図3Gを参照すると、キャップ367は、インプットポート104を覆うように挿入されうる。その後、流体吸引/分配用部材360は、臨床分析器の遠心分離機の固定角ローターまたはスイング・バケット・ローター内にロボットにより設置され、垂直軸365の周りで方向370に回転させられる。ポート355は、密閉式にシールされ、前述されたヒートシール処置により圧力抵抗性にさせられる。それにより、吸引されたサンプル345が垂直軸365の周りを遠心分離している間、サンプル用空洞部106内部に留まることを確実にする。吸引されたサンプル345の微粒子相に働く遠心力の結果、サンプル内部の粒子が流体吸引/分配用部材100のサンプル用空洞部106の底部で蓄積してペレット375になる。遠心分離後、閉ざされたキャップ367は取り外されて、サンプルの上澄み380が臨床分析器の「湿式」および/または「乾式」化学構成要素のいずれかへの提供のために収集される。
【0082】
シールされる流体吸引/分配用部材100はまた、流体吸引/分配用部材100内部の流体内容物の光学的試験を可能にする透明な塑性材料から作られてもよい。サンプルの流体内容物の光学的読取(optical reading)に関する詳細は、米国特許第6,013,528号、および同第5,846,492号にさらに詳細に記載されている。これにより、これら特許の各々の内容全体を参照によって本明細書に組み込んだものとする。一例では、流体吸引/分配用部材の壁部は、蛍光リガンドの励起に必要とされる波長の電磁放射線、および、続く蛍光発光に特徴的な波長の電磁放射線を透過させることができる。
【0083】
別のバージョンによれば、流体吸引/分配用部材100は、本明細書で定められたような分離障壁材料で予め装填されていてよく、この分離障壁材料は、例えば遠心分離といった粒子分離の間、サンプルの液体相からの微粒子相の分離を容易にする。
【0084】
当業者は、記載された実施形態は、多くの方法で変更され、かつ依然として本願の意図される範囲に含まれることができると認識するであろう。例えば、本明細書に記載される流体吸引/分配用部材100は、ある連続の一部として使用されることができ、第2流体吸引/分配用部材100が、第1流体吸引/分配用部材100で処理された、遠心分離されたサンプルの上澄み380を収集するために使用される。例えば、患者由来の血液をヘパリン化したものなどのサンプルが、第1流体吸引/分配用部材100のサンプル用空洞部106の中に吸引されうる。シール可能な空洞部106のシール後、一定分量が、遠心分離され、サンプル用空洞部106の底部で血液細胞をペレットにする。その後、第2流体吸引/分配用部材100が、第2流体吸引/分配用部材100のサンプル用空洞部106の中に血清上澄み380を吸引するために使用されうる。第2流体吸引/分配用部材100のシール可能な空洞部110のシールは、追加の処理のために臨床分析器の湿式/乾式構成要素までロボットにより運搬されうる反応容器を作り出す。一バージョンでは、流体吸引/分配用部材100は、臨床分析のための1種類以上の試薬でサンプル用空洞部を予め装填することを可能にする管部320を有する計量機構350に取り付けられてよく、この試薬とは、例えば、凝集用試薬、すなわち抗ヒト免疫グロブリン(クームス試薬)、または血液型検査のための他の試薬である。サンプルを試薬と混合することは、適当な容器への吸引および分配を繰り返すことによって達成され、続いて、さらなる処理のために流体吸引/分配用部材100のサンプル用空洞部106の中に均質化された混合物を吸引することができる。
【0085】
十分な技能を有する者には容易に明らかとなるであろうが、さらに詳細に記載されるように、以下の記載は例示であり、したがって、例えば、ラテックスまたはアガロースビーズおよび同様のものなどの様々な粒子に取り付けられる分子をリガンド結合することを含むイムノアッセイの処理のために、流体吸引/分配用部材100を使用する可能性がある。免疫グロブリン分子に結合し、粒子に共有結合されうる、例えばプロテインA、プロテインG、プロテインA/G、Kappalockといった、多くのリガンドが知られている。一実施形態では、粒子は、例えばリガンド結合する存在物を表すバクテリオファージに結合されうる(例えば米国特許第6,979,534号を参照のこと。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする)。
【0086】
一バージョンによれば、流体吸引/分配用部材100と共に用いられるアッセイは、磁気ビーズなどの磁性粒子を含むことができる。磁性粒子は、サンプルと共にサンプル用空洞部106の中に吸引されうる。シール可能な空洞部110のシール後、粒子は、遠心分離がない場合、サンプル用空洞部に隣接して強力な磁石を単に配することにより、前述されたように、サンプルの残りの部分から分離される。細胞分離などの目的のために、細胞に磁性を与えることができる多くの方法が当業界で知られている。例えば、ビオチン化された抗体、または特定の細胞型の特徴を示す表面抗原に特異な他のリガンド結合分子と共に、細胞がインキュベートされうる。その後、添加のストレプトアビジン結合磁気ビーズ(Invitrogen/ Dynal Biotech)が、ビオチン化された抗体に結合し、それにより細胞に磁性を与え、したがって磁場を使用した細胞分離を施すことができる。磁気ビーズの制御された運搬の記載は、米国特許第7,217,561号に開示されており、これにより、この特許の内容全体を本明細書に組み込んだものとする。本発明に使用される細胞はまた、当業界で既知の標識抗体を使用してタグ付けされてもよい。例えば、標識抗体は、蛍光団結合抗体であってよい。凝集は、凝集された細胞から発光された蛍光の検出によって監視されうる。
【0087】
第3実施形態によれば、図4(A)および図4(B)は、複数のサンプルの、自動制御および高いスループットの分析をより受けやすい流体吸引/分配用部材組立体構成を図示している。図4(A)は、流体吸引/分配用プレート400を示しており、この流体吸引/分配用プレート400上には、96個の、図1の流体吸引/分配用部材100が、12個の流体吸引/分配用部材425を8列に並べることにより配列されている。図4(B)は、固体支持体414に取り付けられた12個の流体吸引/分配用部材425の列420を示す、プレート400の断面図を描いている。一バージョンでは、この取り付けは、可逆的であってよい。吸引/分配用部材425の各々は、インプットポート404、固体支持体414に取り付けられた管部レセプタクル領域412、サンプル用空洞部406、シール可能な空洞部410、およびシール可能なインプットポート408を含む。図5は、流体吸引/分配用プレート400のシール可能なインプットポート408が、どのようにマイクロタイタープレート500のウェル510と整列できるかを図示している。
【0088】
流体吸引/分配用部材の流体吸引/分配用プレート400の上述の構造説明に伴い、第4実施形態による流体吸引/分配用プレート400を使用するサンプル収集および粒子分離に関連する方法が次に記載される。
【0089】
図6Aを参照すると、図4(B)の流体吸引/分配用部材425の列420の断面図が描かれており、シール可能なインプットポート408がマイクロタイタープレート500のウェル510と整列させられている。適切なロボット命令が、計量機構603に、管部605を流体吸引/分配用プレート400のインプットポート404と整列させるように指示する。適切な整列後、計量システムは、管部605を、開口インプットポート404を通して流体吸引/分配用部材425の管部レセプタクル領域412の中に密閉式に挿入する。
【0090】
図6Bおよび図6Cを参照すると、計量機構はその後、流体吸引/分配用部材425のシール可能なインプットポート408をマイクロタイタープレート500のウェル510と整列させて、各ウェル510内部のサンプル607の中にシール可能なインプットポート408を浸す。計量機構603の管部605は、流体吸引/分配用部材425の各々の内部体積の内部に制御された量の負圧を作り出す。続いて起こる、インプットポート404を通る空気601の転位が、移動643を促進する。この移動643とは、定められた分量のサンプル607を、流体吸引/分配用部材425の各々のサンプル用空洞部406の中へ移動させることである。各流体吸引/分配用部材425内部の吸引されたサンプルの分量は、サンプル用空洞部406内部の利用可能な体積によって決まる。一例では、サンプル607の0.1〜1000μLの一定分量が、吸引される。別の例では、サンプル607の0.1〜300μLの一定分量が、吸引される。さらに別の例では、サンプル607の0.1〜50μLが、流体吸引/分配用部材425の各々のサンプル用空洞部406の中に吸引される。
【0091】
次に図6Dを参照すると、シール可能なインプットポート408は、ウェル510内のサンプル607から取り除かれる。ここでも、計量機構603の管部605は、流体吸引/分配用部材425の各々の内部体積の内部に制御された量の負圧を及ぼす。続いて、列402の流体吸引/分配用部材の内部空洞部内部の空気が方向625へ転位することにより、吸引されたサンプル620がサンプル用空洞部406の中へ適切に移動させられ、かつ、シール可能なインプットポート408のヒートシールの前に、測定された量の空気610が、シール可能なインプットポート408を通してシール可能な空洞部410中へ吸引される。この手順は、吸引されたサンプル620の加熱を回避し、確かなシールを確実にする。
【0092】
図6Eに示されているように、シール可能な空洞部410の壁部はその後、ヒートシールデバイス640の列を用いて、適切な溶融温度まで熱せられる。ヒートシール可能な空洞部410の壁部が熱せられた後、その壁部は、プレス630によって方向635にプレスされ、壁部を共に押し付けてシール可能なインプットポート408の開口端部をシールする。一バージョンでは、プレス630の端部は、シール可能なインプットポート408を覆うように嵌まるカップ645の形態に成形されており、それにより、図6Fに示されているように、インプットポート408を融合および成型してシールされた端部650にすることを容易にする。一バージョンでは、シール可能な空洞部410の壁部の溶融および融合のために、金属プレス630が、適切な溶融温度まで熱せられ、シール可能なインプットポート408に直接適用される。シール後、シール可能なインプットポート408は、融合された熱可塑性材料の凝固化を促進するために急速に冷却され、ゆえに密閉式にシールされた流体容器またはキュベットを生成する。プレス630および管部605はその後、取り外される。
【0093】
図6G〜図6Iを参照すると、オプションの蓋660が、流体吸引/分配用プレート400上に設置され、流体吸引/分配用部材のインプットポート404を密閉式にシールする。蓋660は、吸引されたサンプル620が各流体吸引/分配用部材のサンプル用空洞部406から漏れ出すことを防ぎ、また、吸引されたサンプル620の相互汚染を防ぐ。流体吸引/分配用プレート400はその後、遠心分離機の固定角ローターまたはスイング・バケット・ローターの中にロボットにより設置されて、吸引されたサンプル内部の粒子をサンプルの残りの部分から分離するのに必要とされる時間の間、垂直軸365の周りを方向370に回転させられる。遠心分離の終結で、吸引されたサンプル620内部の粒子が、サンプル用空洞部406の底部でペレット670を形成する。蓋660はその後、取り外されて、上澄み680が、収集されて、臨床分析器の湿式/乾式構成要素へ提供されることができる。
【0094】
代替バージョンでは、サンプル用空洞部406は、本明細書に定められたように、分離障壁材料で予め装填されて、遠心分離の間、吸引されたサンプル620の微粒子相を液体相から分離することを容易にすることができる。別のバージョンでは、サンプル用空洞部406は、試薬で予め装填されていてもよく、この試薬とは、例えば、凝集もしくは血液型検査のための試薬、またはイムノアッセイのための、本明細書に定められたような様々な粒子に取り付けられる抗体である。さらに別のバージョンでは、プレートの流体吸引/分配用部材の内部の吸引されたサンプル620は、磁性粒子を収容し、この磁性粒子は、当業界で周知のプロトコルにしたがって、このプレートを強力な磁石の上に設置することにより、吸引されたサンプル620の残りの部分から分離されうる。
【0095】
前記されたように、流体吸引/分配用部材のプレート内のサンプルの、本明細書に記載された処理は、救急手当施設でのSTATサンプルを迅速に処理するための自動化を特に受けやすい。サンプル処理は、臨床分析器の専用コンピュータ構成要素において動作する適切なソフトウェア・プログラムによって制御されうる。一バージョンでは、流体吸引/分配用部材のプレートの固体支持体414は、ロボットによる扱いを容易にするための付属物、および遠心分離用の適切なアダプターをさらに含む。
【0096】
本明細書における開示は、本開示の1つ以上の流体吸引/分配用部材を有するパッケージ・ユニットを含み、いくつかの実施形態では様々な試薬の容器を含む、キット形式をも提供する。キットはまた、以下のアイテムの1つ以上を収容してもよい:緩衝液、使用説明書、および、陰性対照または陽性対照。キットは、本明細書に記載された方法を実行するために適する比率で一緒に混合される試薬の容器を含んでもよい。試薬容器は好ましくは、本方法を実行するときに測定ステップを不要にする単位量で試薬を収容する。キットは、試薬で予め装填された流体吸引/分配用部材をさらに含んでもよい。
【0097】
本発明は、その好適な実施形態を参照して特に示され記載されてきたが、以下の添付の特許請求の範囲によって網羅される発明の意図される範囲から逸脱することなく、形態および詳細における様々な変更が施されうることは、当業者によって理解されるであろう。
【図面の簡単な説明】
【0098】
【図1】図1は、一実施形態にしたがって作られた流体吸引/分配用部材の断面図を示している。
【図2】図2は、図1の流体吸引/分配用部材のキャップの動きを図示している。
【図3A】図3Aは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3B】図3Bは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3C】図3Cは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3D】図3Dは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3E】図3Eは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3F】図3Fは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3G】図3Gは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図4】図4(A)は、第3実施形態にしたがう流体吸引/分配用部材のアレイを含む流体吸引/分配用プレートの図を示している。図4(B)は、図4(A)のプレートの流体吸引/分配用部材の列の断面図を示している。
【図5】図5は、マイクロタイタープレートとの、図4(A)の流体吸引/分配用部材のアレイの整列を図示している。
【図6A】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6B】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6C】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6D】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6E】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6F】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6G】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6H】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6I】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【開示の内容】
【0001】
〔本願の分野〕
本願は、単一の使い捨て可能な流体吸引/分配用部材の内部でサンプル収集および遠心分離するための装置および方法に関する。
【0002】
〔発明の背景〕
全血血清などの生物学的サンプルの試験をするための単一装置の中に「湿式」および「乾式」化学プラットフォームの両方を収容している組み合わせ臨床分析器が、現在、ほとんどの最新保健医療施設で広く使用されている。
【0003】
いわゆる「乾式」化学システムは、一般的に、サンプル供給部、多くのサンプル容器、計量/運搬機構、および例えば米国特許第3,992,158号に記載されているような複数の試験読取ステーションを有するインキュベータを含む。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする。典型的なプロトコルは、既知量のサンプルを流体吸引/分配用部材に吸引することから始まる。そしてサンプルの一定分量が、乾燥スライド要素上に分配され、この乾燥スライド要素はその後、インキュベータの中に装填される。適切なインキュベーションの後、サンプル中の少なくとも1つの分析対象の量または存在が、例えば電位計、反射計、または他の適当な試験デバイスを使用して決定される。
【0004】
一方、いわゆる「湿式」化学システムは、予め決定された容積測定量(volumetric quantities)のサンプル、試薬、および他の流体を受容するキュベットなどの反応容器を使用する。これらサンプル、試薬、および他の流体は、アッセイを行なうために適切に計量して反応容器内に入れられる。「湿式」化学システムは、一般的に、患者のサンプル流体をサンプル供給部から反応容器へ運搬するための計量機構を含む。1以上の反応が起こる予め決定されたインキュベーション期間の後、光測定デバイスなどの測定デバイスが、反応容器およびサンプルに一条の光線を通すために使用される。「湿式」化学システムで典型的に使用されるアッセイは、限定されるものではないが、終点反応分析(end point reaction analysis)および反応率分析などの分光光度的吸光度アッセイ(spectrophotometric absorbance assays)、濁度測定アッセイ、比濁分析アッセイ、放射エネルギー減衰アッセイ(例えば、米国特許第4,496,293号、および同第4,743,561号に記載されているアッセイ。これにより、これら特許の内容全体を参照によって本明細書に組み込んだものとする。)、イオン捕獲アッセイ、色彩(color)、計量的アッセイ(metric assays)、および蛍光測定アッセイ(fluorometric assay)、ならびにイムノアッセイを含み、これら全ては、当業界で周知である。
【0005】
湿式/乾式化学性能の臨床分析器への統合は、実験誤差を減らし、ワークフローを改善し、そして、人間の介入の必要性を制限することにより、ヒト病原体による研究室職員の汚染の危険性を減らす。湿式および乾式の化学システムの両方を利用している、市販の組み合わせ臨床分析器の一例が、Vitros 5,1 FS Chemistry Systemであり、これは、米国特許第7,250,303号、および米国特許出願公開第2003/0026733号にさらに詳細に記載されており(それぞれ、米国ニューヨーク州ロチェスターのOrtho-Clinical Diagnosticsに譲渡されている)、これら特許および特許出願公開の内容全体を参照によって本明細書に組み込んだものとする。
【0006】
進歩してきてはいるが、これらシステムは依然として、患者サンプルが臨床分析器へ送られる前に、まず微粒子成分を除去するために処理されることを必要とする。この処理ステップは相変わらず厄介で、時間がかかり、これら分析器の全体的な能率を制限している。
【0007】
この問題に取り組む試みに関連する情報が、米国特許第D453,573号;同第4,933,291号;同第5,384,239号;同第5,722,553号;同第5,753,186号;同第6,001,310号;同第6,334,842号;同第6,601,725号;同第6,622,882号;同第7,064,823号;米国特許出願公開第2001/0019842号;同第2005/0204832号;同第2005/0208676号;同第2007/0003443号,同第2007/0017927号;国際出願PCT/AU1992/000236号、および欧州特許第743095号に見出されうる。しかしながら、これら参考文献の各々は、以下の不都合な点の1つ以上を被っている:参考文献は、臨床分析前の患者サンプルの非能率的な処理を除去するものではなく、また、サンプル収集および遠心分離の両方を可能にする流体吸引/分配用部材を記載するものでもない。
【0008】
上述の理由によって、臨床分析器による分析前のサンプル処理能率を改善するための、未だ対処されていない必要性が本分野において存在する。
【0009】
〔本願の概要〕
本発明は、サンプル収集および遠心分離の両方に使用されうる、シール可能な端部を有する流体吸引/分配用部材に関連する。個々の流体部材、または複数の流体吸引/分配用部材を含むプレートのいずれかを用いて、サンプル収集および遠心分離を行なうための方法が記載される。
【0010】
一バージョンによれば、第1ポート、第1ポートと対向する第2ポート、およびキャップを含む、流体吸引/分配用部材が記載されている。このキャップは、第1ポートに取り付けられている場合、第1ポートを解放可能に閉じるように構成されている。流体吸引/分配用部材の内部体積(internal volume)は、第1ポートと第2ポートとの間のサンプル用空洞部、および第2ポートとサンプル用空洞部との間のシール可能な空洞部を含む。シール可能な空洞部のシールにより第2ポートがシールされて、サンプル用空洞部内に流体サンプルを保持し、かつサンプル中に懸濁されている粒子をサンプル残部から分離することを可能にするように構成された容器を作り出す。
【0011】
別の態様によれば、流体吸引/分配用部材は、粒子を流体サンプル残部から分離することができる試験装置の内部に設置されるように構成されている。この装置は、臨床分析器であってよい。粒子のサンプル残部からの分離は、例えば遠心分離の結果として起こりうる。
【0012】
一態様では、サンプル用空洞部の壁部は、先細になっているのに対し、シール可能な空洞部の壁部は、流体吸引/分配用部材の垂直軸に対して平行でありうる。
【0013】
流体吸引/分配用部材のシール可能な空洞部は、ヒートシール可能(heat-sealable)で、長さが1cm未満であることができ、壁部は2mm未満だけ離れていて流体吸引/分配用部材の垂直軸に対して平行である。
【0014】
一態様では、キャップは、吸引/分配用部材に取り外し可能に取り付けられている。
【0015】
吸引/分配用部材は、細胞懸濁液または血液でありうるサンプルの光学的または視覚的試験が可能であってよい。サンプル中の粒子は、赤血球でありうる。
【0016】
吸引/分配用部材は、各部材の内部体積内での凝集のために分離障壁または試薬をさらに収容できる。
【0017】
別のバージョンによれば、固体支持体に取り付けられた流体吸引/分配用部材のアレイを含む、流体吸引/分配用プレートが記載されている。吸引/分配用部材の各々は、第1ポート、および第1ポートに対向する第2ポートを含む。各流体吸引/分配用部材の内部体積は、第1ポートと第2ポートとの間のサンプル用空洞部、および第2ポートとサンプル用空洞部との間のシール可能な空洞部を含む。流体吸引/分配用部材の各々のシール可能な空洞部のシールにより、サンプル用空洞部内の流体サンプルを保持し、かつサンプル中に懸濁されている粒子のサンプル残部からの分離を可能にするように構成された、複数の容器が作り出される。
【0018】
一態様では、固体支持体は、平坦であり、流体吸引/分配用部材を支持するための手段を含むことができる。流体吸引/分配用プレートは、96個の流体吸引/分配用部材を有することができる。
【0019】
別の態様では、流体吸引/分配用部材は、固体支持体に可逆的(reversibly)に取り付けられる。
【0020】
別のバージョンでは、流体吸引/分配用プレートは、各流体吸引/分配用部材のサンプル残部から粒子を分離することができる試験装置の内部に設置されるように構成されている。この試験装置は、臨床分析器でありうる。
【0021】
サンプル残部からの粒子の分離は、遠心分離による分離の結果として起こりうる。
【0022】
流体吸引/分配用プレートのシール可能な空洞部は、ヒートシール可能な空洞部でありうる。
【0023】
別のバージョンでは、流体吸引/分配用プレートは、カバーを有し、このカバーが流体吸引/分配用プレートの第1ポート上に設置された場合、カバーは、第1ポートの各々を閉じるように構成されている。
【0024】
一態様では、プレートの流体吸引/分配用部材は、各部材の内部体積内部のサンプルの光学的または視覚的試験を可能にする。
【0025】
別の態様では、プレート上の吸引/分配用部材のアレイは、マイクロタイタープレートのウェル(wells)と整列している。マイクロタイタープレートの各ウェルは、プレート上の他のウェルの各々と異なるサンプルを保持でき、サンプルは、細胞懸濁液または血液でありうる。サンプル内部の粒子は、細胞でありうる。
【0026】
さらに別の態様では、プレート上の吸引/分配用部材は、各部材の内部体積内部での凝集のために分離障壁または試薬を収容できる。
【0027】
別の実施形態によれば、流体サンプル中の粒子を分離するための方法が記載されており、この方法は、(a)流体吸引/分配用部材を装置内へ装填するステップであって、この部材は、第1ポート、第2ポート、ならびに、第1ポートおよび第2ポートと流体連通しているサンプル用空洞部を含む、ステップと、(b)サンプルを、流体吸引/分配用部材の第2ポートを通してサンプル用空洞部内へ吸引するステップと、(c)流体容器を作り出すために流体吸引/分配用部材の第2ポートをシールするステップと、(d)第1ポートに解放可能に係合して第1ポートを覆うように寸法付けられたキャップを用いて第1ポートを閉じるステップと、(e)サンプル中の粒子をサンプル残部から分離するステップと、を含み、分離された粒子およびサンプルは、粒子またはサンプルの検出のために、流体吸引/分配用部材のサンプル用空洞部の内部に保持される。
【0028】
装置は臨床分析器でありうる。分離するステップは、例えば遠心分離によって行なわれうる。
【0029】
一態様によれば、装填するステップは、流体吸引/分配用部材を、装置の計量機構の管部(proboscis)に取り付けることを必要とする。
【0030】
別の態様では、流体吸引/分配用部材は、計量先端部である。
【0031】
一態様では、シールするステップは、流体吸引/分配用部材の第2ポートをヒートシールすることによって行なわれる。
【0032】
さらに別の実施形態によれば、複数の流体サンプル中の粒子を分離する方法が記載されており、この方法は、(a)流体吸引/分配用プレートを装置内に装填するステップであって、このプレートは、複数の流体吸引/分配用部材を含み、この部材の各々は、第1ポート、第2ポート、ならびに、第1ポートおよび第2ポートの各々と流体連通しているサンプル用空洞部を含む、ステップと、(b)複数のサンプルを、流体吸引/分配用部材の各々の第2ポートを通して、サンプル用空洞部内に吸引するステップと、(c)複数の流体容器を作り出すために流体吸引/分配用部材の各々の第2ポートをシールするステップと、(d)容器の各々の中において、サンプル中の粒子をサンプル残部から分離するステップと、を含み、粒子およびサンプルは、粒子またはサンプルの検出のために、流体吸引/分配用部材の各々のサンプル用空洞部の内部に保持される。
【0033】
一態様では、装置は臨床分析器である。
【0034】
分離するステップは、遠心分離により行なわれうる。
【0035】
一態様では、装填するステップは、流体吸引/分配用プレートを、装置の計量機構の複数の管部に取り付けることを必要とする。
【0036】
別の態様では、流体吸引/分配用部材は、計量先端部である。
【0037】
別の実施形態によれば、吸引するステップの後、流体吸引/分配用部材の各々の第1ポートは、蓋によって閉ざされ、蓋が流体吸引/分配用部材の第1ポートの上に設置されると、蓋は、流体吸引/分配用部材の各々の第1ポートを閉じるように構成されている。
【0038】
シールするステップは、流体吸引/分配用部材の各々の第2ポートをヒートシールすることによって行なわれうる。
【0039】
前述した実施形態は、個々の使い捨て可能な流体吸引/分配用部材、または複数の流体吸引/分配用部材を含む流体吸引/分配用プレートのいずれかを用いて、サンプル収集および粒子分離を行なう能力を含む、多くの利点を有する。本明細書に記載される方法は、取り扱いの誤り、および、臨床分析器による分析の前にサンプル処理に費やされる時間を減らす。したがって、本明細書に記載された流体吸引/分配用部材を用いたサンプル処理は、当業界で既知の従来方法よりも迅速である。
【0040】
本願は、この概要に開示された実施形態に制限されるものではなく、当分野における十分な技術の範囲内、かつ特許請求の範囲によって定められた範囲内の、修正および変形を含むように意図されていることが、理解されるべきである。
【0041】
〔詳細な説明〕
別段の定義がされていない限り、本明細書で使用される全ての技術用語および科学用語は、当業者によって一般的に理解されるのと同じ意味を有する。以下の定義は、本願の開示および特許請求の範囲を解釈するのを助けるために提供される。このセクションにおける定義が他の場合の定義と一致しない場合、このセクションに述べられる定義が、支配するであろう。
【0042】
本明細書に使用される「組み合わせ」分析器は、「乾式」および/または「湿式」化学システムの任意の組み合わせを包含することができる、少なくとも2つの化学システムを含む臨床分析器を指す。
【0043】
本明細書に使用される「臨床分析器」は、限定されるものではないが、臨床サンプルの「湿式」および/または「乾式」の自動化学分析のための分析器だけでなく免疫診断分析器を含む、臨床サンプルを分析することができる任意の装置を指す。「湿式」化学プラットフォームは典型的に、反応容器の中に1以上のサンプルおよび/または試薬を吸引および分配する自動流体取り扱いシステムを制御するマイクロプロセッサと、少なくとも1つのサンプル貯蔵器と、オプションの少なくとも1つの試薬貯蔵器と、少なくとも1つのインキュベータと、分光光度計などの少なくとも1つの検出器とを、含む。本願の流体吸引/分配用部材と共に使用するための典型的な分析器は、米国特許第6,096,561号、同第7,282,372号、および同第7,250,303号にさらに詳細に記載されており、これら特許全ての内容全体を参照によって本明細書に組み込んだものとする。好適な実施形態では、本明細書で使用される臨床分析器は、Ortho-Clinical Diagnostics, Inc.により製造されているVITROS 5,1 FS Chemistry Systemなどの市販の分析器を指す。
【0044】
流体が、毛管現象および/または重力によるなどして、ある要素から別の要素へ移動できる場合、一方の要素は、もう一方の要素と「流体連通」している。要素は、直接接触していてもよいが、直接接触の必要はない;すなわち、前記流体が通ることができる他の要素が介在していてもよい。流体が、毛管現象および/または重力により、ある要素から別の要素へ移動できない場合、一方の要素は、もう一方の要素と「流体連通していない」。典型的に、要素は、物理的に分離されている、すなわち離隔している。
【0045】
本明細書に使用される「流体吸引/分配用部材」は、2つ以上のシール可能な開口部と流体連通している1つ以上の内部空洞部を収容している計量先端部などのデバイスであり、米国特許第6,797,518号に記載されているようなサンプル収集および粒子分離の両方に使用される。これによりこの特許の内容全体を参照によって本明細書に組み込んだものとする。一実施形態では、粒子分離は、遠心分離の結果として起こる。流体吸引/分配用部材は典型的に、臨床分析器内部において、容積測定量のサンプルの吸引または分配を行なう。一実施形態では、流体吸引/分配用部材は、内部空洞部の変形を伴わずに遠心分離されうる、成型された固体材料から構成される。別の実施形態では、この材料は、生物学的サンプルの、流体吸引/分配用部材の内壁部への付着を促進しない。別の実施形態では、流体吸引/分配用部材は、典型的に押出しブロー成型により塑性材料から作られる。流体吸引/分配用部材は、その中への吸引後、流体内容物に光学的試験を行なうことを可能にする半透明または透明な特徴を好ましくは有する熱可塑性材料から作られうる。一実施形態では、流体吸引/分配用部材は、ポリプロピレンまたはポリエチレンなどの成型用プラスチックから作られる。別の実施形態では、流体吸引/分配用部材は、ホモポリマー、またはポリアロマーなどの共重合体から作られ、単量体の1つは、プロピレンである。さらに別の実施形態では、流体吸引/分配用部材は、ポリエチレンテレフタレートから作られる。
【0046】
本明細書に使用される「流体吸引/分配用プレート」は、固体支持体に取り付けられた複数の流体吸引/分配用部材のアレイを指す。各流体吸引/分配用部材は、サンプル収集および粒子分離の両方のために、2つ以上のシール可能な開口部と流体連通している1つ以上の内部空洞部を含む。流体吸引/分配用プレートは典型的に、臨床分析器内部において、容積測定量の1つ以上のサンプルの吸引または分配に使用される。一実施形態では、支持体は、平坦で、矩形または正方形の形状であるが、本明細書に記載される流体吸引/分配用プレートは、任意の形状を有してよい。別の実施形態では、流体吸引/分配用プレート上の流体吸引/分配用部材は、幾列にもなって配列されており、各列は、同数の流体吸引/分配用部材を有する。別の実施形態では、流体吸引/分配用プレートは、流体吸引/分配用部材のための支持体を含む。当業者であれば、この支持体は、臨床分析器内での遠心分離およびロボットによる取り扱いを容易にするように設計されうることを、認識するであろう。一実施形態では、流体吸引/分配用部材は、固体支持体に可逆的に固定される。別の実施形態では、複数の流体吸引/分配用部材は、マイクロタイタープレートのウェルと整列するような要領で、流体吸引/分配用プレート上に配列されている。さらに別の実施形態では、プレートは、1、2、5、10、25、50、75、100、またはそれ以上の流体吸引/分配用部材の可逆的な取り付けのための複数の場所を有する。プレート上の各場所は、流体吸引/分配用部材で充填されていても、充填されていなくてもよい。
【0047】
本明細書に使用される「サンプル残部からの粒子の分離」は、サンプルの固形微粒子相からサンプルの液体相を分離することを可能にする任意の手順を指す。一実施形態では、「サンプル残部からの粒子の分離」は、流体吸引/分配用部材のシール後、流体吸引/分配用部材のサンプル用空洞部の内部で、サンプル液体相からサンプルの固形微粒子相を部分的または完全に分離することを指す。別の実施形態では、分離は、遠心分離の結果として起こる。さらに別の実施形態では、分離は、サンプルに加えられた磁性粒子に働く磁場の結果として生じる。
【0048】
本明細書に使用される用語「シール可能な空洞部」は、サンプル用空洞部と流体吸引/分配用部材の底端部との間に位置する流体吸引/分配用部材の領域であって、例えばヒートシールによるか、または本明細書に定められるようなシーラントの適用の結果として、シールされうる、流体吸引/分配用部材の領域を指す。シールの結果、サンプル用空洞部はもはや、流体吸引/分配用部材の吸引/分配用端部と流体連通しておらず、ゆえに粒子分離のための流体容器を作り出す。一実施形態では、シール可能な空洞部は、熱可塑性の溶融−融合性材料(thermoplastic melt-fusible material)から作られる。別の実施形態では、熱可塑性の溶融−融合性材料は、当業者によって知られているようなヒートシールに適当な、ポリアロマーまたは類似の熱可塑性材料である。
【0049】
本明細書に使用される「ヒートシール」は、流体吸引/分配用部材のシール可能な空洞部の壁部を共に融合させるために、その壁部に十分な熱および圧力を加えることを指す。続く硬化、すなわち融合された熱可塑性壁部の強固化および凝固化が、シール可能な空洞部の圧力抵抗性シールを作り出し、この圧力抵抗性シールは、流体吸引/分配用部材のサンプル用空洞部とシール可能な吸引/分配用端部との間の流体連通を妨げる。ヒートシールのさらに詳細な記載は、米国特許第3,929,943号に見出されうる。これによりこの特許の内容全体を参照によって本明細書に組み込んだものとする。別の実施形態では、ヒートシールは、流体吸引/分配用プレート上に配列された複数の流体吸引/分配用部材のシール可能な空洞部に適用される。例えば、流体吸引/分配用部材のアレイの吸引/分配用端部は、整列させられ、金属製成型カップのアレイに挿入されうる。金属製成型カップは、そのカップ内に置かれたシール可能な空洞部の壁部の溶融および融合を促進する温度まで熱せられる。
【0050】
本明細書に使用される「シール(sealing)」は、流体吸引/分配用部材の吸引/分配用端部を恒久的に閉じることを指す。一実施形態では、シールはヒートシールを指す。別の実施形態では、シールは、流体吸引/分配用部材の吸引/分配用端部を密閉式に塞ぐ、例えばプラスチックまたは接着剤といったシーラントの適用を指す。別の例では、シーラントは、流体吸引/分配用部材の吸引/分配用端部を密閉式に閉じる、底部ねじぶたなどの底部キャップであってよい。
【0051】
本明細書に使用される「シーラント」は、本明細書に記載された流体吸引/分配用部材のシール可能な空洞部の壁部の間に連結結合を形成するために使用されうる接着剤などの任意の組成物を意味するものとする。一実施形態では、シーラントは、UV硬化性である。別の実施形態では、シーラントは、室温で硬化する。
【0052】
本明細書に使用される用語「ポリアロマー」は、通常ホモポリマーにのみ関連する結晶化度を呈する、1−オレフィンの共重合体を生成する任意の熱可塑性材料を指す。一実施形態では、ポリアロマーは、プロピレンとエチレンとのランダムブロック共重合体である。別の実施形態では、ポリアロマーは、「Tenite(登録商標) Polyallomer」という商品名でEastman Chemical Co.により販売されている、容易に融合可能な塑性材料である。
【0053】
本明細書に使用される用語「空洞部」は、記載された流体吸引/分配用部材の内部の任意の3次元の囲われた場所(enclosure)を指す。例示的実施形態では、1つ以上の空洞部が、互いに流体連通している。
【0054】
用語「複数」は、本明細書に使用されるように、2つ以上の数量を指す。
【0055】
本明細書に使用される「粒子」は、細胞であってよく、例えば、サンプル中に見出される細菌または赤血球または白血球である。別の実施形態では、粒子は、サンプル処理前に、サンプルに加えられる微細固形物であってよい。これらの粒子は、ビーズの形態の不活性固形物、ビーズのようになったゲル(beaded gels)、または微小球であってよいが、これら粒子は任意の形状を有してもよい。粒子のさらなる例は、限定されるものではないが、プラスチック粒子、セラミック粒子、カーボン粒子、ポリスチレンミクロビーズ、ラテックスビーズ、ガラスビーズ、磁気ビーズ、中空ガラス球体、金属粒子、複合組成物の粒子、微細加工またはマイクロ機械加工粒子(microfabricated or micromachined particles)を含む。不活性粒子は、ガラスもしくはセラミックスなどの任意の適した材料、カーボンもしくはプラスチックなどの有機材料、および/または、例えばナイロン、ポリテトラフルオロエチレン(TEFLON(商標))もしくはスチレン−ジビニルベンゼンポリマーなどの1種類以上のポリマーから、構成されうる。粒子サイズは、約0.1μm〜1000μmであってよい。好ましくは、粒子サイズは、約1μm〜約10μmである。原理上は、任意のリガンドが、例えば、HeamらによるMethods in Enzymology Vol. 35:102-117 (1987)に記載されているような既知の技術を用いて、固相マトリクス、またはアガロースビーズ(例えばセファロース・ファルマシア)などの粒子に共有結合してよい。一般的に、ビーズは、まず、グルタルアルデヒド、カルボニルジイミダゾール(carbonyldiimidizole)、臭化シアンヒドロキシスクシンイミド(cyanogen bromide hydroxysuccinimide)、塩化トシル(tosyl chloride)または同種のものなどの化学薬品によって、活性化される。その後、選択されたリガンドが、ビーズに共有結合し、その結果、リガンドのその支持体に対する非常に安定した結合を生じる。
【0056】
本明細書に使用される「細胞懸濁液」は、サンプル中に典型的に見出される、液体中の細胞の混合物を指す。細胞は、真核生物または原核生物の細胞でありうる。一実施形態では、細胞は、細菌である。別の実施形態では、細胞は、病原菌である。好適な実施形態では、細胞は、血液細胞である。別の好適な実施形態では、細胞は、赤血球である。
【0057】
本明細書に使用される用語「サンプル」は、少なくとも1つの分析対象を含有すると推測される材料を指す。サンプルは、ソースから獲得されたままで直接使用されうるか、またはサンプルの特徴を改変するための前処置に続いて、使用されうる。サンプルは、血液、血漿、唾液、眼球レンズ流体(ocular lens fluid)、脳脊髄液、汗、尿、乳汁、腹水(ascites fluid)、raucous、滑液、腹水(peritoneal fluid)、羊水、または同種のものを含む生理流体など、任意の生物学的ソースに由来するものでありうる。サンプルは、使用前に前処置されうる。例えば、全血は典型的に、血液凝固を防ぐためにヘパリンおよび同様のものなどポリアニオンで処置される。別の例では、粘性流体が希釈されうる。処置方法は、ろ過、蒸留、濃縮、干渉成分の不活性化、および試薬の添加を含むこともできる。生理流体のほかに、他の液体サンプルが使用されうる。加えて、分析対象を含有すると推測される固形材料が、サンプルとして使用されうる。いくつかの例では、固形サンプルを改変して、液体媒体を形成すること、または分析対象を放出することは有益でありうる。別の実施形態では、サンプルは、本明細書に定められるように、分析前または分析中にサンプルに加えられうる1種類以上の化合物を含むことが理解され、その1種類以上の化合物には、限定されるものではないが、緩衝剤、試薬、ペプチド、酵素、リガンド、リガンド結合分子、抗体、粒子、リガンド結合粒子、磁性粒子、および同様のものが含まれる。サンプルは、本明細書に定められるように、前記に定義されたような粒子を含有してよい。
【0058】
用語「分析対象」は、本明細書に使用されるように、検出または測定される、任意の化合物または組成物または存在物を指す。分析対象は、当業界で既知の臨床アッセイにより試験される、任意の、無機分子もしくは有機分子、または細胞成分、または細胞、または生物体でありうる。臨床アッセイは、分析対象の存在または不在のいずれかを試験してもよい。一実施形態では、分析対象は、少なくとも1つの、エピトープまたは結合部位またはリガンドを有する。別の実施形態では、分析対象は、任意の物質であって、この物質のための、自然発生的な結合メンバーが存在するか、またはこの物質のために結合メンバーが準備されうるような、任意の物質でありうる。さらに別の実施形態では、分析対象は、例えば、白血球、赤血球(ヘマトクリット)または血小板などの血液細胞といった細胞集団を指す。分析対象はまた、限定されるものではないが、代謝産物、毒素、無機または有機の化合物、タンパク質、ペプチド、サイトカイン、ケモカイン、酵素、アミノ酸、脂質、HDL/LDLコレステロール、トリグリセリド、多糖類、血糖、核酸、ホルモン(例えば、甲状腺刺激ホルモン(TSH)、副腎皮質刺激ホルモン(ACTH)、プロラクチン)、ステロイド(例えば、コルチゾールまたはテストステロンまたはエストロゲン)、ビタミン、電解質、薬剤、イオン(例えばpH測定のための)、微量金属、微生物(細菌、ウィルスまたは寄生生物、および同類のもの)、ウィルス粒子、上記の物質のいずれかの代謝産物、および上記の物質のいずれかに対する抗体を含むことができる。別の実施形態では、分析対象は、C反応性タンパク質、アルブミン、アミラーゼ、Dダイマー、ビリルビン、アルカリホスファターゼ、γグルタミルトランスフェラーゼ、尿素、クレアチン、血清鉄、トランスフェリン(transferring)、前立腺特異抗原(PSA)、αフェトプロテイン(AFP)、βヒト絨毛性性腺刺激ホルモン(bHCG)、α1−アンチトリプシン(AAT)、CA−125(CA12.5とも言う)、癌胎児性抗原(CEA)、フィブリノーゲン、または典型的に試験される、臨床サンプル中の任意の他の化合物である。用語「分析対象」は、任意の抗原性物質、ハプテン、抗体、巨大分子、およびこれらの組み合わせを含んでよい。別の実施形態では、分析対象は、酵素活性を測定することによって検出されうる酵素である。例えば、血液中での、クレアチンキナーゼ、グルタミン酸オキサロ酢酸トランスアミナーゼ(SGOT)、血清グルタミン酸ピルビン酸トランスアミナーゼ(SGPT)活性の試験は、肝臓または心臓の障害の指標として広く使用されている。
【0059】
本明細書に使用される「リガンド」は、リガンド結合分子に結合することができる任意の分子である。一実施形態では、リガンドは、抗体のエピトープである。免疫グロブリン分子に結合し、本願に使用される粒子に共有結合されうる、例えばプロテインA、プロテインG、プロテインA/GおよびKappaLock(商標)といった、多くのリガンドも知られている(米国特許第5,665,558号も参照のこと。この特許の内容全体を参照によって本明細書に組み込んだものとする)。リガンドは、使用されるか、または試験される、抗体のイソタイプに結合することができる。あるいは代替的に、リガンドは、例えば、IgM抗体に対して、IgG抗IgM(IgG anti-IgM)といったブリッジ抗体(bridging antibody)を使用することができる。ゆえに、IgG抗IgM抗体が、「ブリッジ」としてリガンドに結合され、IgM抗体が、IgG抗IgM抗体に結合するであろう。
【0060】
用語「リガンド結合」は、本明細書に使用されるように、結合対のメンバーを指し、すなわち2つの異なる分子であって、その分子の一方が、化学的手段または物理的手段により、第2分子に特異的に結合している、2つの異なる分子を指す。抗原および抗体の結合対メンバーに加えて、他の結合対は、限定するものではなく例として、ビオチンおよびアビジン、炭水化物およびレクチン、相補的ヌクレオチド配列、相補的ペプチド配列、多糖類およびレクチン、エフェクターおよびレセプター分子、酵素補因子および酵素、酵素阻害剤および酵素、ペプチド配列およびその配列またはタンパク質全体に対して特異的な抗体、ポリマー酸および塩基、色素およびタンパク質結合剤、ペプチドおよび特異的タンパク質結合剤(例えば、リボヌクレアーゼ、S−ぺプチド、およびリボヌクレアーゼS−タンパク質)、ならびに同様のものを含む。さらに、結合対は、例えば、組み換え技術または分子工学により作られる分析対象−類似体または結合メンバーといった、原型の結合メンバーの類似体であるメンバーを含むことができる。結合メンバーが免疫反応体(immunoreactant)である場合、その結合メンバーは、例えば、モノクロナール抗体またはポリクロナール抗体、組み換えタンパク質または組み替え抗体、キメラ抗体、上述の混合物もしくは断片、ならびに、結合メンバーとして使用するための適合性が当業者に周知である、そのような抗体、ペプチド、およびヌクレオチドの調製物でありうる。リガンド結合メンバーは、ポリペプチド親和性リガンドであってもよい(例えば米国特許第6,326,155号を参照のこと。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする)。一実施形態では、リガンド結合メンバーは、標識付けされている。標識は、蛍光ラベル、化学発光ラベルもしくは生物発光ラベル、酵素−抗体構造体(enzyme-antibody construct)、または当業界で既知の他の類似の適当なラベルから選択されてよい。
【0061】
本明細書に使用される「血液」は、全血、または、赤血球、白血球、血漿もしくは血清などの全血の任意の成分を広く含む。
【0062】
本明細書に使用される「遠心分離」は、回転軸の周りでの対象物の回転を指す。サンプルは、固定角ローターもしくはスイング・バケット・ローター(a fixed angle or swing bucket rotor)、または当業界で既知の任意の他のローターで遠心分離されうる。
【0063】
本明細書に使用される「STAT」は、直ちに、を意味するラテン語「statim」に由来する医学用語である。したがって、「STATレーン(STAT lane)」は、患者サンプルの至急または急ぐ処理を指す。
【0064】
本明細書に使用される「緊急サンプル」は、即時の処理を必要としている任意のサンプルを指す。緊急サンプルは典型的に、緊急治療室または他の救急手当施設で収集されたサンプルを含む。例えば、緊急治療室のサンプルは、緊急治療室内の患者から採取された血液サンプルでありうる。
【0065】
「凝集」は、本明細書に使用されるように、試薬、通常は抗体または他のリガンド結合する存在物による、細胞性抗原または微粒子抗原の懸濁液のクランピングを指す(例えば、米国特許第4,305,721号、同第5,650,068号、および同第5,552,064号を参照のこと。これにより、これら特許の内容全体を参照によって本明細書に組み込んだものとする)。一実施形態では、試薬は、クームス試薬(Coomb’s reagent)である。
【0066】
本明細書に使用される「クームス試薬」は、以下のヒト免疫グロブリン、補体、または特異的免疫グロブリンのうちの1つに対して向けられる、動物の体内で生じた抗体の調製物を指し、例えば、クームス試験に使用される抗ヒトIgGである。
【0067】
本明細書に使用される「検出」は、光検出器を用いた、光吸収または光散乱の検出を指す(例えば、米国特許第5,256,376号、および米国特許出願公開第2004/0166551号を参照のこと。これにより、これら特許および特許出願公開の内容全体を参照によって本明細書に組み込んだものとする)。一実施形態では、検出は、生物発光または化学発光または蛍光の検出を指す(例えば、米国特許第6,596,546号を参照のこと。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする)。
【0068】
本明細書に使用される用語「撹拌」は、流体吸引/分配用部材の内容物に働く力を指し、例えば、遠心力、または磁場によって誘起された力を指す。
【0069】
本明細書に使用される「計量デバイス」は、本明細書で使用されるように、管部によって流体吸引/分配用部材に可逆的に取り付くことができる臨床分析器の構成要素を指す。一実施形態では、オンボード・コンピュータにより制御される計量デバイスが、臨床分析器内部の、流体吸引/分配用部材または流体吸引/分配用プレートの移動および/または運搬を調整している。
【0070】
本明細書に使用される用語「管部(proboscis)」は、個別的、または流体吸引/分配用プレートの一部として、のいずれかで、1つ以上の吸引/分配用部材に取り付く臨床分析器の構成要素を指す。一実施形態では、管部は、計量機構の一部であり、円筒形の形状であってよく、流体吸引/分配用部材の管部レセプタクル領域の内壁部に対して管部自体を気密式に挿入するような(すなわち、管部の円筒形表面と壁部との間に実質的な空気の漏れが存在しない)要領で、1つ以上の流体吸引/分配用部材の各々の管部レセプタクル領域の内部に嵌まる。管部が流体吸引/分配用部材の各々の管部レセプタクル領域に密閉式に固定されると、計量機構を用いて、管部が各流体吸引/分配用部材の内部体積に減圧または圧力のいずれかを与え、それにより、各流体吸引/分配用部材の内部空洞部内部の既知分量の流体を移動させる。
【0071】
本明細書に使用される用語「分離障壁(separation barrier)」は、水不混和性で、典型的にチキソトロピーの、ゲル様またはビーズ様の材料であって、サンプルの軽い液体相に見出される密度と、サンプルの重い実質的に微粒子の相に見出される密度との間の中間の密度を有する、材料を指す。例えば、分離障壁は典型的に、流体吸引/分配用部材のサンプル用空洞部の中に配され、流体吸引/分配用部材はその後サンプルで充填される。遠心分離すると、サンプルは2つの相に傾斜分離され(gradient separated)、障壁材料は、相と相との間の界面に移行する。遠心分離が完了すると、分離障壁が、分離された相の相互間に物理的および化学的な障壁を形成し、それにより、相のいかなる混合も防ぐ。分離障壁は、例えば、シリコーン流体と微細な疎水性シリカ粉末との混合物、ポリエステル材料、またはポリブタン(polybutane)などの炭化水素ゲル様材料、または、当業界で既知の任意の他の材料でありうる。分離障壁材料の組成は、米国特許第4,190,535号;同第4,101,422号;同第4,818,418号、および同第4,147,628号にさらに詳細に記載されている。これにより、これら特許の内容全体を本明細書に組み込んだものとする。
【0072】
本明細書に使用される用語「抗体」は、ポリクロナール抗体およびモノクロナール抗体の両方を含み;完全な分子、そのフラグメント(Fv、Fd、Fab、Fab’およびF(ab)’2フラグメントなど)、あるいは、完全な分子および/またはフラグメントの多量体または集合体であってよく;自然発生するか、または、例えば免疫化、合成もしくは遺伝子操作によって生成されてもよい。本明細書に使用される抗体または抗原は、試験されている抗体または抗原によって決まる。例えば、血液型抗原の数、および、ゆえに識別されたそれら抗原に対する抗体の数は、非常に多く、さらなる抗原および抗体が、絶えず決定されている。国際輸血学会(The International Society of Blood Transfusion)は、Blood Group Terminology 1990, Vox. Sang. 58:152-169 (1990)に赤血球抗原の非排他的リストを公表しており、限定されるものではないが、抗体および抗原A、B、D、C、c、Cw、E、e、K、Fya、Fyb、Jka、Jkb、S、およびsを含む。
【0073】
本明細書に注記された前述の定義をふまえて、以下の記載は、本願のある好適な実施形態、および、化学分析前の患者サンプルの初期処理のための特定の方法論に関する。解説から容易に明らかになるであろうが、本明細書に記載された発明の概念は、患者サンプルの効果的な処理を必要とする他の方法にも適切に適用されうる。加えて、「上部」、「底部」、「側方」、「上方」、「下方」および同様のもののような用語もまた、添付の図面で使用するための便利な基準系を提供するために使用される。しかしながら、これらの用語は、別段に特記されていない限り、本発明を限定することを意図されていない。遠心分離または他の分離方法によりサンプル収集および粒子分離の両方を可能にし、それにより組み合わせ臨床分析器の湿式/乾式化学構成要素による分析の前の、サンプル処理の効率を増大させる、新規の流体吸引/分配用部材が、本明細書に記載されている。
【0074】
第1実施形態によれば、図1は、サンプル収集および粒子分離のためのシール可能な流体吸引/分配用部材100を示している。流体吸引/分配用部材100は典型的には、射出成型可能で、好ましくは透明な、熱可塑性材料から構成されており、その材料は、ポリプロピレン、ポリアロマー、ポリエチレンテレフタレート、ポリマーの共重合体もしくはブレンド、または当業界で既知の任意の他の適当な不活性材料などである。好ましくは、分析されているサンプルは、流体吸引/分配用部材100の内部体積の壁部に粘着せず、流体吸引/分配用部材100のこれらの表面は、サンプルまたは試薬の、流体吸引/分配用部材100の内部表面へのこのような粘着を避けるように処置されてよい。流体吸引/分配用部材100の内部体積は、約1μL〜約2000μL、またはそれを超えてもよい。一例では、内部体積は、約1μL〜約500μLである。好適な実施形態では、流体吸引/分配用部材100は、約1μL〜約300μLの内部体積を有する。流体吸引/分配用部材100の壁部の厚さは、変形することなく遠心分離に耐えることができるならば、重要ではない。典型的には、壁部は、約5mm〜約0.1mm、約2mm〜約0.5mm、または約1.5mm〜約0.75mmの厚さを有する。図1に示すように、流体吸引/分配用部材100は、上端部でインプットポート104により、そして下端部でシール可能なインプットポート108により、定められている。インプットポート104とインプットポート108との間には、サンプル用空洞部106を含む内部空洞部があり、サンプル用空洞部106は、インプットポート104および108と流体連通している。インプットポート104は、流体吸引/分配用部材100の内部体積から既知分量の空気を移動させるために、(この図には示されていない)計量機構の管部に密閉式に取り付くように構成されている。一実施形態では、管部320は、インプットポート104を通って流体吸引/分配用部材100の管部レセプタクル領域112の中へ密閉式に入り込む。シール可能なインプットポート108は、インプットポート108を介するサンプル用空洞部106内への流体の吸引または分配を可能にするように構成されている。シール可能な空洞部の壁部は、ヒートシールを容易にするためにサンプル用空洞部106の壁部よりも薄くてよい。一バージョンでは、流体吸引/分配用部材100の内部体積は、臨床分析のために必要とされる試薬で予め装填されていてよく、この試薬は、例えば、血液凝集または血液型検査のための試薬である。別の実施形態では、流体吸引/分配用部材100のサンプル用空洞部は、本明細書に定義されたような分離障壁を収容する。
【0075】
次に図1および図2を参照すると、本明細書に記載された流体吸引/分配用部材100は、つなぎ縄(tether)116により部材100の上端部に連結されたオプションのキャップ114を備えて、示されている。つなぎ縄116は、サンプル収集または粒子分離、すなわち遠心分離を妨げない限り、いかなる長さであってもよい。例えば、つなぎ縄116は、約0.5cm〜約2cmの長さ、または約0.5cm〜約1cmの長さであってもよい。つなぎ縄116を方向210に曲げることにより、キャップ114は、インプットポート104内に可逆的に挿入されうる。一バージョンでは、キャップ114は、(不図示の)流体吸引/分配用部材100に取り付けられておらず、したがって、遠心分離前にインプットポート104の中に直接挿入される。インプットポート104上へのキャップ114の設置は、流体吸引/分配用部材100の遠心分離および/または取り扱いの間にサンプル用空洞部106内の流体がインプットポート104を通って流出するのを防ぐ、密閉式シールを形成する。別のバージョンでは、流体吸引/分配用部材100は、キャップを必要としない。さらに別の実施形態では、インプットポート108は、シール可能な空洞部110の中に挿入された後に硬化される、本明細書に定められたようなシーラントを用いてシールされてもよい。
【0076】
図1、図2、および図3Aを参照すると、本明細書に記載された流体吸引/分配用部材100は、サンプル用空洞部106とシール可能なインプットポート108との間に配されるヒートシール可能な空洞部110を含む。ヒートシール可能な空洞部110へ熱を加えると、壁部の熱可塑性材料が溶融して融合し、ゆえにシール可能なインプットポート108をシールする。他の方法もまた、インプットポート108をシールするために利用されてよい。例えば、接着剤などのシーラントが、インプットポート108に適用され、冷却または、例えばUV放射に局所的に曝すなど他の手段により、硬化されてよい。別のバージョンでは、インプットポート108は、底部キャップ、例えば底部ねじぶた(不図示)を用いて、密閉式に閉ざされる。
【0077】
流体吸引/分配用部材100の上述の構造説明を伴って、次に、第2実施形態による流体吸引/分配用部材100内部でのサンプル収集および粒子分離に関する方法が記載される。
【0078】
図3Bを参照すると、計量機構350、より詳細には臨床分析器の管部320に取り付けられた場合の流体吸引/分配用部材100が示されている。管部は、分析器の計量機構の構成要素を形成している。適切なロボット命令が、計量システムに、管部320を流体吸引/分配用部材100のインプットポート220と整列させるように指示する。適切な整列の後、計量システムは、管部320を、開口インプットポート220を通して流体吸引/分配用部材100の管部レセプタクル領域112の中へ密閉式に挿入する。インプットポート108は、その後、サンプル330中に浸漬される。計量機構350の管部320は、流体吸引/分配用部材100の内部体積内部に制御された量の負圧を作り出す。インプットポート104を通る空気310の続く転位が、流体吸引/分配用部材100のサンプル用空洞部106内への、定められた分量のサンプル330の移動343を促進する。吸引されるサンプルの分量は、サンプル用空洞部106内部の利用可能な体積によって決まる。一例では、約1μL〜約1000μLの間の一定分量(aliquot)のサンプル330が、吸引される。別の例では、約1μL〜約300μLの一定分量のサンプル330が、吸引される。さらに別の例では、約1μL〜約50μLのサンプル330が、流体吸引/分配用部材100のサンプル用空洞部106の中へ吸引される。
【0079】
図3Cを参照すると、サンプル用空洞部106内へのサンプル330の吸引が完了した後、流体吸引/分配用部材100のインプットポート108は、サンプル330から取り除かれる。計量機構350の管部320は、再び、流体吸引/分配用部材100の内部体積の内部に制御された量の負圧を作り出し、この負圧により、空気347の小さな気泡がインプットポート108を通って吸引され、吸引されたサンプル345をインプットポート108から離してサンプル用空洞部106内へ適切に転位させる。管部320と流体吸引/分配用部材100の管部レセプタクル領域112との間の気密シールを維持することにより、サンプルは、インプットポート108のヒートシール前は、サンプル用空洞部106内部に保持される。この手順は、確かなシールと、分析前の吸引されたサンプル345のあらゆる温度上昇の制限との、両方を確実にする。
【0080】
図3Dを参照すると、流体吸引/分配用部材100のインプットポート104は、管部320が流体吸引/分配用部材100の管部レセプタクル領域112の中に密閉式に挿入されたままである間に、ヒートシールデバイス353内に設置される。その後、シール可能な空洞部110の壁部の熱可塑性材料が、その溶融温度まで急速に熱せられる。そのポリマーが溶融温度まで熱せられるべき速度は、上記で本明細書に組み込まれた米国特許第3,929,943号に詳細に記載されているように、ポリマーの固有粘度、シール可能な空洞部110の壁部の厚さおよび直径によって決まる。加熱の最大期間は、約1秒〜約30秒、または5秒〜約20秒、または約10秒〜約15秒でありうる。ヒートシールデバイスは、タングステン電球または石英灯などの高強度ラジエントヒーター(high-intensity radiant heater)でありうる。代替的に、誘導加熱器または超音波加熱器、または当業界で既知の任意の他の手段などのマイクロ波加熱器が利用されうる。溶融温度は、約200℃〜約350℃でありうるが、流体吸引/分配用部材100の熱可塑性特性によって決まる。ヒートシール可能な空洞部110の壁部が熱せられた後、その壁部は、プレス357によって方向362にプレスされ、壁部を共に押し付けて開口端部をシールする。一バージョンでは、プレス357の端部は、流体吸引/分配用部材100のインプットポート108を覆うように嵌まるカップ364の形態に成形されており、インプットポート108を融合および成型してシールされた端部355にすることを容易にする。一バージョンでは、金属プレス357は、適切な溶融温度まで熱せられ、シール可能なインプットポート108に直接適用される。シール後、インプットポート108は、融合された熱可塑性材料の凝固化を促進するために急速に冷却され、ゆえに密閉式にシールされた流体容器またはキュベットを生成する。その後、プレス357および計量デバイス320は、取り外される。
【0081】
図3E〜図3Gを参照すると、キャップ367は、インプットポート104を覆うように挿入されうる。その後、流体吸引/分配用部材360は、臨床分析器の遠心分離機の固定角ローターまたはスイング・バケット・ローター内にロボットにより設置され、垂直軸365の周りで方向370に回転させられる。ポート355は、密閉式にシールされ、前述されたヒートシール処置により圧力抵抗性にさせられる。それにより、吸引されたサンプル345が垂直軸365の周りを遠心分離している間、サンプル用空洞部106内部に留まることを確実にする。吸引されたサンプル345の微粒子相に働く遠心力の結果、サンプル内部の粒子が流体吸引/分配用部材100のサンプル用空洞部106の底部で蓄積してペレット375になる。遠心分離後、閉ざされたキャップ367は取り外されて、サンプルの上澄み380が臨床分析器の「湿式」および/または「乾式」化学構成要素のいずれかへの提供のために収集される。
【0082】
シールされる流体吸引/分配用部材100はまた、流体吸引/分配用部材100内部の流体内容物の光学的試験を可能にする透明な塑性材料から作られてもよい。サンプルの流体内容物の光学的読取(optical reading)に関する詳細は、米国特許第6,013,528号、および同第5,846,492号にさらに詳細に記載されている。これにより、これら特許の各々の内容全体を参照によって本明細書に組み込んだものとする。一例では、流体吸引/分配用部材の壁部は、蛍光リガンドの励起に必要とされる波長の電磁放射線、および、続く蛍光発光に特徴的な波長の電磁放射線を透過させることができる。
【0083】
別のバージョンによれば、流体吸引/分配用部材100は、本明細書で定められたような分離障壁材料で予め装填されていてよく、この分離障壁材料は、例えば遠心分離といった粒子分離の間、サンプルの液体相からの微粒子相の分離を容易にする。
【0084】
当業者は、記載された実施形態は、多くの方法で変更され、かつ依然として本願の意図される範囲に含まれることができると認識するであろう。例えば、本明細書に記載される流体吸引/分配用部材100は、ある連続の一部として使用されることができ、第2流体吸引/分配用部材100が、第1流体吸引/分配用部材100で処理された、遠心分離されたサンプルの上澄み380を収集するために使用される。例えば、患者由来の血液をヘパリン化したものなどのサンプルが、第1流体吸引/分配用部材100のサンプル用空洞部106の中に吸引されうる。シール可能な空洞部106のシール後、一定分量が、遠心分離され、サンプル用空洞部106の底部で血液細胞をペレットにする。その後、第2流体吸引/分配用部材100が、第2流体吸引/分配用部材100のサンプル用空洞部106の中に血清上澄み380を吸引するために使用されうる。第2流体吸引/分配用部材100のシール可能な空洞部110のシールは、追加の処理のために臨床分析器の湿式/乾式構成要素までロボットにより運搬されうる反応容器を作り出す。一バージョンでは、流体吸引/分配用部材100は、臨床分析のための1種類以上の試薬でサンプル用空洞部を予め装填することを可能にする管部320を有する計量機構350に取り付けられてよく、この試薬とは、例えば、凝集用試薬、すなわち抗ヒト免疫グロブリン(クームス試薬)、または血液型検査のための他の試薬である。サンプルを試薬と混合することは、適当な容器への吸引および分配を繰り返すことによって達成され、続いて、さらなる処理のために流体吸引/分配用部材100のサンプル用空洞部106の中に均質化された混合物を吸引することができる。
【0085】
十分な技能を有する者には容易に明らかとなるであろうが、さらに詳細に記載されるように、以下の記載は例示であり、したがって、例えば、ラテックスまたはアガロースビーズおよび同様のものなどの様々な粒子に取り付けられる分子をリガンド結合することを含むイムノアッセイの処理のために、流体吸引/分配用部材100を使用する可能性がある。免疫グロブリン分子に結合し、粒子に共有結合されうる、例えばプロテインA、プロテインG、プロテインA/G、Kappalockといった、多くのリガンドが知られている。一実施形態では、粒子は、例えばリガンド結合する存在物を表すバクテリオファージに結合されうる(例えば米国特許第6,979,534号を参照のこと。これにより、この特許の内容全体を参照によって本明細書に組み込んだものとする)。
【0086】
一バージョンによれば、流体吸引/分配用部材100と共に用いられるアッセイは、磁気ビーズなどの磁性粒子を含むことができる。磁性粒子は、サンプルと共にサンプル用空洞部106の中に吸引されうる。シール可能な空洞部110のシール後、粒子は、遠心分離がない場合、サンプル用空洞部に隣接して強力な磁石を単に配することにより、前述されたように、サンプルの残りの部分から分離される。細胞分離などの目的のために、細胞に磁性を与えることができる多くの方法が当業界で知られている。例えば、ビオチン化された抗体、または特定の細胞型の特徴を示す表面抗原に特異な他のリガンド結合分子と共に、細胞がインキュベートされうる。その後、添加のストレプトアビジン結合磁気ビーズ(Invitrogen/ Dynal Biotech)が、ビオチン化された抗体に結合し、それにより細胞に磁性を与え、したがって磁場を使用した細胞分離を施すことができる。磁気ビーズの制御された運搬の記載は、米国特許第7,217,561号に開示されており、これにより、この特許の内容全体を本明細書に組み込んだものとする。本発明に使用される細胞はまた、当業界で既知の標識抗体を使用してタグ付けされてもよい。例えば、標識抗体は、蛍光団結合抗体であってよい。凝集は、凝集された細胞から発光された蛍光の検出によって監視されうる。
【0087】
第3実施形態によれば、図4(A)および図4(B)は、複数のサンプルの、自動制御および高いスループットの分析をより受けやすい流体吸引/分配用部材組立体構成を図示している。図4(A)は、流体吸引/分配用プレート400を示しており、この流体吸引/分配用プレート400上には、96個の、図1の流体吸引/分配用部材100が、12個の流体吸引/分配用部材425を8列に並べることにより配列されている。図4(B)は、固体支持体414に取り付けられた12個の流体吸引/分配用部材425の列420を示す、プレート400の断面図を描いている。一バージョンでは、この取り付けは、可逆的であってよい。吸引/分配用部材425の各々は、インプットポート404、固体支持体414に取り付けられた管部レセプタクル領域412、サンプル用空洞部406、シール可能な空洞部410、およびシール可能なインプットポート408を含む。図5は、流体吸引/分配用プレート400のシール可能なインプットポート408が、どのようにマイクロタイタープレート500のウェル510と整列できるかを図示している。
【0088】
流体吸引/分配用部材の流体吸引/分配用プレート400の上述の構造説明に伴い、第4実施形態による流体吸引/分配用プレート400を使用するサンプル収集および粒子分離に関連する方法が次に記載される。
【0089】
図6Aを参照すると、図4(B)の流体吸引/分配用部材425の列420の断面図が描かれており、シール可能なインプットポート408がマイクロタイタープレート500のウェル510と整列させられている。適切なロボット命令が、計量機構603に、管部605を流体吸引/分配用プレート400のインプットポート404と整列させるように指示する。適切な整列後、計量システムは、管部605を、開口インプットポート404を通して流体吸引/分配用部材425の管部レセプタクル領域412の中に密閉式に挿入する。
【0090】
図6Bおよび図6Cを参照すると、計量機構はその後、流体吸引/分配用部材425のシール可能なインプットポート408をマイクロタイタープレート500のウェル510と整列させて、各ウェル510内部のサンプル607の中にシール可能なインプットポート408を浸す。計量機構603の管部605は、流体吸引/分配用部材425の各々の内部体積の内部に制御された量の負圧を作り出す。続いて起こる、インプットポート404を通る空気601の転位が、移動643を促進する。この移動643とは、定められた分量のサンプル607を、流体吸引/分配用部材425の各々のサンプル用空洞部406の中へ移動させることである。各流体吸引/分配用部材425内部の吸引されたサンプルの分量は、サンプル用空洞部406内部の利用可能な体積によって決まる。一例では、サンプル607の0.1〜1000μLの一定分量が、吸引される。別の例では、サンプル607の0.1〜300μLの一定分量が、吸引される。さらに別の例では、サンプル607の0.1〜50μLが、流体吸引/分配用部材425の各々のサンプル用空洞部406の中に吸引される。
【0091】
次に図6Dを参照すると、シール可能なインプットポート408は、ウェル510内のサンプル607から取り除かれる。ここでも、計量機構603の管部605は、流体吸引/分配用部材425の各々の内部体積の内部に制御された量の負圧を及ぼす。続いて、列402の流体吸引/分配用部材の内部空洞部内部の空気が方向625へ転位することにより、吸引されたサンプル620がサンプル用空洞部406の中へ適切に移動させられ、かつ、シール可能なインプットポート408のヒートシールの前に、測定された量の空気610が、シール可能なインプットポート408を通してシール可能な空洞部410中へ吸引される。この手順は、吸引されたサンプル620の加熱を回避し、確かなシールを確実にする。
【0092】
図6Eに示されているように、シール可能な空洞部410の壁部はその後、ヒートシールデバイス640の列を用いて、適切な溶融温度まで熱せられる。ヒートシール可能な空洞部410の壁部が熱せられた後、その壁部は、プレス630によって方向635にプレスされ、壁部を共に押し付けてシール可能なインプットポート408の開口端部をシールする。一バージョンでは、プレス630の端部は、シール可能なインプットポート408を覆うように嵌まるカップ645の形態に成形されており、それにより、図6Fに示されているように、インプットポート408を融合および成型してシールされた端部650にすることを容易にする。一バージョンでは、シール可能な空洞部410の壁部の溶融および融合のために、金属プレス630が、適切な溶融温度まで熱せられ、シール可能なインプットポート408に直接適用される。シール後、シール可能なインプットポート408は、融合された熱可塑性材料の凝固化を促進するために急速に冷却され、ゆえに密閉式にシールされた流体容器またはキュベットを生成する。プレス630および管部605はその後、取り外される。
【0093】
図6G〜図6Iを参照すると、オプションの蓋660が、流体吸引/分配用プレート400上に設置され、流体吸引/分配用部材のインプットポート404を密閉式にシールする。蓋660は、吸引されたサンプル620が各流体吸引/分配用部材のサンプル用空洞部406から漏れ出すことを防ぎ、また、吸引されたサンプル620の相互汚染を防ぐ。流体吸引/分配用プレート400はその後、遠心分離機の固定角ローターまたはスイング・バケット・ローターの中にロボットにより設置されて、吸引されたサンプル内部の粒子をサンプルの残りの部分から分離するのに必要とされる時間の間、垂直軸365の周りを方向370に回転させられる。遠心分離の終結で、吸引されたサンプル620内部の粒子が、サンプル用空洞部406の底部でペレット670を形成する。蓋660はその後、取り外されて、上澄み680が、収集されて、臨床分析器の湿式/乾式構成要素へ提供されることができる。
【0094】
代替バージョンでは、サンプル用空洞部406は、本明細書に定められたように、分離障壁材料で予め装填されて、遠心分離の間、吸引されたサンプル620の微粒子相を液体相から分離することを容易にすることができる。別のバージョンでは、サンプル用空洞部406は、試薬で予め装填されていてもよく、この試薬とは、例えば、凝集もしくは血液型検査のための試薬、またはイムノアッセイのための、本明細書に定められたような様々な粒子に取り付けられる抗体である。さらに別のバージョンでは、プレートの流体吸引/分配用部材の内部の吸引されたサンプル620は、磁性粒子を収容し、この磁性粒子は、当業界で周知のプロトコルにしたがって、このプレートを強力な磁石の上に設置することにより、吸引されたサンプル620の残りの部分から分離されうる。
【0095】
前記されたように、流体吸引/分配用部材のプレート内のサンプルの、本明細書に記載された処理は、救急手当施設でのSTATサンプルを迅速に処理するための自動化を特に受けやすい。サンプル処理は、臨床分析器の専用コンピュータ構成要素において動作する適切なソフトウェア・プログラムによって制御されうる。一バージョンでは、流体吸引/分配用部材のプレートの固体支持体414は、ロボットによる扱いを容易にするための付属物、および遠心分離用の適切なアダプターをさらに含む。
【0096】
本明細書における開示は、本開示の1つ以上の流体吸引/分配用部材を有するパッケージ・ユニットを含み、いくつかの実施形態では様々な試薬の容器を含む、キット形式をも提供する。キットはまた、以下のアイテムの1つ以上を収容してもよい:緩衝液、使用説明書、および、陰性対照または陽性対照。キットは、本明細書に記載された方法を実行するために適する比率で一緒に混合される試薬の容器を含んでもよい。試薬容器は好ましくは、本方法を実行するときに測定ステップを不要にする単位量で試薬を収容する。キットは、試薬で予め装填された流体吸引/分配用部材をさらに含んでもよい。
【0097】
本発明は、その好適な実施形態を参照して特に示され記載されてきたが、以下の添付の特許請求の範囲によって網羅される発明の意図される範囲から逸脱することなく、形態および詳細における様々な変更が施されうることは、当業者によって理解されるであろう。
【図面の簡単な説明】
【0098】
【図1】図1は、一実施形態にしたがって作られた流体吸引/分配用部材の断面図を示している。
【図2】図2は、図1の流体吸引/分配用部材のキャップの動きを図示している。
【図3A】図3Aは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3B】図3Bは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3C】図3Cは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3D】図3Dは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3E】図3Eは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3F】図3Fは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図3G】図3Gは、第2実施形態にしたがうサンプル収集および遠心分離の方法を表す、図1の流体吸引/分配用部材の連続断面図を示している。
【図4】図4(A)は、第3実施形態にしたがう流体吸引/分配用部材のアレイを含む流体吸引/分配用プレートの図を示している。図4(B)は、図4(A)のプレートの流体吸引/分配用部材の列の断面図を示している。
【図5】図5は、マイクロタイタープレートとの、図4(A)の流体吸引/分配用部材のアレイの整列を図示している。
【図6A】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6B】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6C】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6D】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6E】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6F】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6G】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6H】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【図6I】第4実施形態にしたがうサンプル収集および遠心分離の方法を表す、図4(A)の流体吸引/分配用部材のアレイの連続断面図を示している。
【特許請求の範囲】
【請求項1】
流体吸引/分配用部材において、
a)流体吸引/分配用部材の内部体積と流体連通している第1ポートと、
b)前記内部体積と流体連通している第2ポートであって、前記第2ポートは、前記第1ポートと対向している、第2ポートと、
c)前記第1ポートと前記第2ポートとの間に配された前記内部体積のサンプル用空洞部と、
d)前記第2ポートと前記サンプル用空洞部との間に配された前記内部体積のシール可能な空洞部と、
e)前記第1ポートに隣接して取り付けられるキャップであって、前記キャップが前記第1ポート上に設置されると、前記キャップは、前記第1ポートを閉じるように構成されている、キャップと、
を含み、
前記シール可能な空洞部をシールすることにより、前記第2ポートをシールして流体容器を作り出すことを可能にし、前記容器は、前記サンプル用空洞部内に流体サンプルを保持するように、かつ前記サンプル中に懸濁されている粒子を前記サンプルの残部から分離することを可能にするように、構成されている、流体吸引/分配用部材。
【請求項2】
請求項1に記載の吸引/分配用部材において、
前記サンプル残部から粒子を分離することができる試験装置の内部に設置されるようにさらに構成されている、吸引/分配用部材。
【請求項3】
請求項2に記載の吸引/分配用部材において、
前記装置は、臨床分析器である、吸引/分配用部材。
【請求項4】
請求項1に記載の吸引/分配用部材において、
前記サンプル残部からの前記粒子の前記分離は、遠心分離による分離の結果として起こる、吸引/分配用部材。
【請求項5】
請求項1に記載の吸引/分配用部材において、
前記サンプル用空洞部の壁部が、先細になっている、吸引/分配用部材。
【請求項6】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部の壁部は、前記部材の垂直軸に対して平行である、吸引/分配用部材。
【請求項7】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部は、ヒートシール可能である、吸引/分配用部材。
【請求項8】
請求項1に記載の吸引/分配用部材において、
前記キャップは、取り外し可能に取り付けられる、吸引/分配用部材。
【請求項9】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部の壁部は、2mm未満だけ離れている、吸引/分配用部材。
【請求項10】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部は、長さが1cm未満である、吸引/分配用部材。
【請求項11】
請求項1に記載の吸引/分配用部材において、
前記部材は、前記部材の前記内部体積の内部で、サンプルの光学的または視覚的試験を可能にする、吸引/分配用部材。
【請求項12】
請求項1に記載の吸引/分配用部材において、
前記サンプルは、細胞懸濁液を含む、吸引/分配用部材。
【請求項13】
請求項1に記載の吸引/分配用部材において、
前記サンプルは、血液を含む、吸引/分配用部材。
【請求項14】
請求項1に記載の吸引/分配用部材において、
前記粒子は、細胞である、吸引/分配用部材。
【請求項15】
請求項1に記載の吸引/分配用部材において、
前記部材の前記内部体積の中に配される分離障壁、
をさらに含む、吸引/分配用部材。
【請求項16】
請求項1に記載の吸引/分配用部材において、
前記サンプルは、粒子凝集のための試薬をさらに含む、吸引/分配用部材。
【請求項17】
流体吸引/分配用プレートにおいて、
固体支持体に取り付けられた流体吸引/分配用部材のアレイであって、前記吸引/分配用部材の各々は、
a)流体吸引/分配用部材の内部体積と流体連通している第1ポート、
b)前記内部体積と流体連通している第2ポートであって、前記第2ポートは、前記第1ポートと対向している、第2ポート、
c)前記第1ポートと前記第2ポートとの間に配された前記内部体積のサンプル用空洞部、および、
d)前記第2ポートと前記サンプル用空洞部との間に配された前記内部体積のシール可能な空洞部、を含む、アレイ、
を含み、
前記吸引/分配用部材の各々の前記シール可能な空洞部をシールすることにより、前記部材の各々の前記第2ポートをシールして複数の流体容器を作り出すことを可能にし、前記容器の各々は、前記サンプル用空洞部内に流体サンプルを保持するように、かつ前記サンプル中に懸濁されている粒子を前記サンプルの残部から分離することを可能にするように、構成されている、流体吸引/分配用プレート。
【請求項18】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記固体支持体は、平坦である、流体吸引/分配用プレート。
【請求項19】
請求項18に記載の流体吸引/分配用プレートにおいて、
前記支持体は、前記部材を支持するための手段をさらに含む、流体吸引/分配用プレート。
【請求項20】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記流体吸引/分配用部材は、前記固体支持体に可逆的に取り付けられる、流体吸引/分配用プレート。
【請求項21】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記プレートは、96個の流体吸引/分配用部材を含む、流体吸引/分配用プレート。
【請求項22】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記プレートは、各前記流体吸引/分配用部材の前記サンプル残部から粒子を分離することができる試験装置の内部に設置されるようにさらに構成されている、流体吸引/分配用プレート。
【請求項23】
請求項22に記載の流体吸引/分配用プレートにおいて、
前記試験装置は、臨床分析器である、流体吸引/分配用プレート。
【請求項24】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記サンプル残部からの前記粒子の前記分離は、遠心分離による分離の結果として起こる、流体吸引/分配用プレート。
【請求項25】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記シール可能な空洞部は、ヒートシール可能である、流体吸引/分配用プレート。
【請求項26】
請求項17に記載の流体吸引/分配用プレートにおいて、
カバーであって、前記カバーが前記第1ポート上に設置されると、前記カバーは、前記第1ポートの各々を閉じるように構成されている、カバー、
をさらに含む、流体吸引/分配用プレート。
【請求項27】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記流体吸引/分配用部材の前記各々は、前記部材の各々の前記内部体積の内部で、サンプルの光学的または視覚的試験を可能にする、流体吸引/分配用プレート。
【請求項28】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記吸引/分配用部材のアレイは、マイクロタイタープレートのウェルと整列させられうる、流体吸引/分配用プレート。
【請求項29】
請求項28に記載の流体吸引/分配用プレートにおいて、
前記マイクロタイタープレートの前記ウェルの各々は、その他のウェルの各々とは異なるサンプルを収容する、流体吸引/分配用プレート。
【請求項30】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記容器の各々の前記サンプルは、細胞懸濁液を含む、流体吸引/分配用プレート。
【請求項31】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記容器の各々の前記サンプルは、血液を含む、流体吸引/分配用プレート。
【請求項32】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記粒子は、細胞である、流体吸引/分配用プレート。
【請求項33】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記流体吸引/分配用部材の各々は、前記部材の各々の前記内部体積の中に配された分離障壁をさらに含む、流体吸引/分配用プレート。
【請求項34】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記容器の各々は、粒子凝集のための試薬をさらに含む、流体吸引/分配用プレート。
【請求項35】
流体サンプル中の粒子を分離する方法において、
前記方法は、
a)流体吸引/分配用部材を装置内へ装填するステップであって、前記部材は、第1ポート、第2ポート、ならびに、前記第1ポートおよび前記第2ポートの各々と流体連通しているサンプル用空洞部を含む、ステップと、
b)サンプルを、前記流体吸引/分配用部材の前記第2ポートを通して、前記サンプル用空洞部内へ吸引するステップと、
c)流体容器を作り出すために前記流体吸引/分配用部材の前記第2ポートをシールするステップと、
d)前記第1ポートに解放可能に係合して前記第1ポートを覆うように寸法付けられたキャップを用いて前記第1ポートを閉じるステップと、
e)前記サンプル中の粒子を前記サンプルの残部から分離するステップと、
を含み、
前記分離された粒子およびサンプルは、前記粒子またはサンプルの検出のために、前記流体吸引/分配用部材の前記サンプル用空洞部の内部に保持される、方法。
【請求項36】
請求項35に記載の方法において、
前記装填するステップは、前記流体吸引/分配用部材を管部に取り付けるステップを含む、方法。
【請求項37】
請求項35に記載の方法において、
前記流体吸引/分配用部材は、計量先端部である、方法、
【請求項38】
請求項35に記載の方法において、
前記装置は、臨床分析器である、方法。
【請求項39】
請求項35に記載の方法において、
前記分離するステップは、遠心分離によって行なわれる、方法。
【請求項40】
請求項35に記載の方法において、
前記シールするステップは、前記部材の前記第2ポートをヒートシールすることによって行なわれる、方法。
【請求項41】
複数の流体サンプル中の粒子を分離する方法において、
前記方法は、
(a)流体吸引/分配用プレートを装置内に装填するステップであって、前記プレートは、複数の流体吸引/分配用部材を含み、前記部材の各々は、第1ポート、第2ポート、ならびに、前記第1ポートおよび前記第2ポートの各々と流体連通しているサンプル用空洞部を含む、ステップと、
(b)複数のサンプルを、前記流体吸引/分配用部材の各々の前記第2ポートを通して、前記サンプル用空洞部内へ吸引するステップと、
(c)複数の流体容器を作り出すために前記流体吸引/分配用部材の各々の前記第2ポートをシールするステップと、
(d)前記容器の各々の中で、前記サンプル中の粒子を前記サンプルの残部から分離するステップと、
を含み、
前記分離された粒子およびサンプルは、前記粒子またはサンプルの検出のために、前記流体吸引/分配用部材の各々の前記サンプル用空洞部の内部に保持される、方法。
【請求項42】
請求項41に記載の方法において、
前記装填するステップは、前記流体吸引/分配用プレートを前記装置の複数の管部へ取り付けることを必要とし、前記管部は、計量機構の一部である、方法。
【請求項43】
請求項41に記載の方法において、
前記流体吸引/分配用部材は、計量先端部である、方法。
【請求項44】
請求項41に記載の方法において、
前記装置は、臨床分析器である、方法。
【請求項45】
請求項41に記載の方法において、
前記分離するステップは、遠心分離によって行なわれる、方法。
【請求項46】
請求項41に記載の方法において、
前記吸引するステップの後に、前記部材の各々の前記第1ポートが蓋によって閉ざされるステップであって、前記蓋が前記第1ポートの上に設置されると、前記蓋は、前記部材の各々の前記第1ポートを閉じるように構成されている、ステップ、
をさらに含む、方法。
【請求項47】
請求項41に記載の方法において、
前記シールするステップは、前記部材の各々の前記第2ポートをヒートシールすることによって行われる、方法。
【請求項1】
流体吸引/分配用部材において、
a)流体吸引/分配用部材の内部体積と流体連通している第1ポートと、
b)前記内部体積と流体連通している第2ポートであって、前記第2ポートは、前記第1ポートと対向している、第2ポートと、
c)前記第1ポートと前記第2ポートとの間に配された前記内部体積のサンプル用空洞部と、
d)前記第2ポートと前記サンプル用空洞部との間に配された前記内部体積のシール可能な空洞部と、
e)前記第1ポートに隣接して取り付けられるキャップであって、前記キャップが前記第1ポート上に設置されると、前記キャップは、前記第1ポートを閉じるように構成されている、キャップと、
を含み、
前記シール可能な空洞部をシールすることにより、前記第2ポートをシールして流体容器を作り出すことを可能にし、前記容器は、前記サンプル用空洞部内に流体サンプルを保持するように、かつ前記サンプル中に懸濁されている粒子を前記サンプルの残部から分離することを可能にするように、構成されている、流体吸引/分配用部材。
【請求項2】
請求項1に記載の吸引/分配用部材において、
前記サンプル残部から粒子を分離することができる試験装置の内部に設置されるようにさらに構成されている、吸引/分配用部材。
【請求項3】
請求項2に記載の吸引/分配用部材において、
前記装置は、臨床分析器である、吸引/分配用部材。
【請求項4】
請求項1に記載の吸引/分配用部材において、
前記サンプル残部からの前記粒子の前記分離は、遠心分離による分離の結果として起こる、吸引/分配用部材。
【請求項5】
請求項1に記載の吸引/分配用部材において、
前記サンプル用空洞部の壁部が、先細になっている、吸引/分配用部材。
【請求項6】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部の壁部は、前記部材の垂直軸に対して平行である、吸引/分配用部材。
【請求項7】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部は、ヒートシール可能である、吸引/分配用部材。
【請求項8】
請求項1に記載の吸引/分配用部材において、
前記キャップは、取り外し可能に取り付けられる、吸引/分配用部材。
【請求項9】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部の壁部は、2mm未満だけ離れている、吸引/分配用部材。
【請求項10】
請求項1に記載の吸引/分配用部材において、
前記シール可能な空洞部は、長さが1cm未満である、吸引/分配用部材。
【請求項11】
請求項1に記載の吸引/分配用部材において、
前記部材は、前記部材の前記内部体積の内部で、サンプルの光学的または視覚的試験を可能にする、吸引/分配用部材。
【請求項12】
請求項1に記載の吸引/分配用部材において、
前記サンプルは、細胞懸濁液を含む、吸引/分配用部材。
【請求項13】
請求項1に記載の吸引/分配用部材において、
前記サンプルは、血液を含む、吸引/分配用部材。
【請求項14】
請求項1に記載の吸引/分配用部材において、
前記粒子は、細胞である、吸引/分配用部材。
【請求項15】
請求項1に記載の吸引/分配用部材において、
前記部材の前記内部体積の中に配される分離障壁、
をさらに含む、吸引/分配用部材。
【請求項16】
請求項1に記載の吸引/分配用部材において、
前記サンプルは、粒子凝集のための試薬をさらに含む、吸引/分配用部材。
【請求項17】
流体吸引/分配用プレートにおいて、
固体支持体に取り付けられた流体吸引/分配用部材のアレイであって、前記吸引/分配用部材の各々は、
a)流体吸引/分配用部材の内部体積と流体連通している第1ポート、
b)前記内部体積と流体連通している第2ポートであって、前記第2ポートは、前記第1ポートと対向している、第2ポート、
c)前記第1ポートと前記第2ポートとの間に配された前記内部体積のサンプル用空洞部、および、
d)前記第2ポートと前記サンプル用空洞部との間に配された前記内部体積のシール可能な空洞部、を含む、アレイ、
を含み、
前記吸引/分配用部材の各々の前記シール可能な空洞部をシールすることにより、前記部材の各々の前記第2ポートをシールして複数の流体容器を作り出すことを可能にし、前記容器の各々は、前記サンプル用空洞部内に流体サンプルを保持するように、かつ前記サンプル中に懸濁されている粒子を前記サンプルの残部から分離することを可能にするように、構成されている、流体吸引/分配用プレート。
【請求項18】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記固体支持体は、平坦である、流体吸引/分配用プレート。
【請求項19】
請求項18に記載の流体吸引/分配用プレートにおいて、
前記支持体は、前記部材を支持するための手段をさらに含む、流体吸引/分配用プレート。
【請求項20】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記流体吸引/分配用部材は、前記固体支持体に可逆的に取り付けられる、流体吸引/分配用プレート。
【請求項21】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記プレートは、96個の流体吸引/分配用部材を含む、流体吸引/分配用プレート。
【請求項22】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記プレートは、各前記流体吸引/分配用部材の前記サンプル残部から粒子を分離することができる試験装置の内部に設置されるようにさらに構成されている、流体吸引/分配用プレート。
【請求項23】
請求項22に記載の流体吸引/分配用プレートにおいて、
前記試験装置は、臨床分析器である、流体吸引/分配用プレート。
【請求項24】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記サンプル残部からの前記粒子の前記分離は、遠心分離による分離の結果として起こる、流体吸引/分配用プレート。
【請求項25】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記シール可能な空洞部は、ヒートシール可能である、流体吸引/分配用プレート。
【請求項26】
請求項17に記載の流体吸引/分配用プレートにおいて、
カバーであって、前記カバーが前記第1ポート上に設置されると、前記カバーは、前記第1ポートの各々を閉じるように構成されている、カバー、
をさらに含む、流体吸引/分配用プレート。
【請求項27】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記流体吸引/分配用部材の前記各々は、前記部材の各々の前記内部体積の内部で、サンプルの光学的または視覚的試験を可能にする、流体吸引/分配用プレート。
【請求項28】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記吸引/分配用部材のアレイは、マイクロタイタープレートのウェルと整列させられうる、流体吸引/分配用プレート。
【請求項29】
請求項28に記載の流体吸引/分配用プレートにおいて、
前記マイクロタイタープレートの前記ウェルの各々は、その他のウェルの各々とは異なるサンプルを収容する、流体吸引/分配用プレート。
【請求項30】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記容器の各々の前記サンプルは、細胞懸濁液を含む、流体吸引/分配用プレート。
【請求項31】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記容器の各々の前記サンプルは、血液を含む、流体吸引/分配用プレート。
【請求項32】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記粒子は、細胞である、流体吸引/分配用プレート。
【請求項33】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記流体吸引/分配用部材の各々は、前記部材の各々の前記内部体積の中に配された分離障壁をさらに含む、流体吸引/分配用プレート。
【請求項34】
請求項17に記載の流体吸引/分配用プレートにおいて、
前記容器の各々は、粒子凝集のための試薬をさらに含む、流体吸引/分配用プレート。
【請求項35】
流体サンプル中の粒子を分離する方法において、
前記方法は、
a)流体吸引/分配用部材を装置内へ装填するステップであって、前記部材は、第1ポート、第2ポート、ならびに、前記第1ポートおよび前記第2ポートの各々と流体連通しているサンプル用空洞部を含む、ステップと、
b)サンプルを、前記流体吸引/分配用部材の前記第2ポートを通して、前記サンプル用空洞部内へ吸引するステップと、
c)流体容器を作り出すために前記流体吸引/分配用部材の前記第2ポートをシールするステップと、
d)前記第1ポートに解放可能に係合して前記第1ポートを覆うように寸法付けられたキャップを用いて前記第1ポートを閉じるステップと、
e)前記サンプル中の粒子を前記サンプルの残部から分離するステップと、
を含み、
前記分離された粒子およびサンプルは、前記粒子またはサンプルの検出のために、前記流体吸引/分配用部材の前記サンプル用空洞部の内部に保持される、方法。
【請求項36】
請求項35に記載の方法において、
前記装填するステップは、前記流体吸引/分配用部材を管部に取り付けるステップを含む、方法。
【請求項37】
請求項35に記載の方法において、
前記流体吸引/分配用部材は、計量先端部である、方法、
【請求項38】
請求項35に記載の方法において、
前記装置は、臨床分析器である、方法。
【請求項39】
請求項35に記載の方法において、
前記分離するステップは、遠心分離によって行なわれる、方法。
【請求項40】
請求項35に記載の方法において、
前記シールするステップは、前記部材の前記第2ポートをヒートシールすることによって行なわれる、方法。
【請求項41】
複数の流体サンプル中の粒子を分離する方法において、
前記方法は、
(a)流体吸引/分配用プレートを装置内に装填するステップであって、前記プレートは、複数の流体吸引/分配用部材を含み、前記部材の各々は、第1ポート、第2ポート、ならびに、前記第1ポートおよび前記第2ポートの各々と流体連通しているサンプル用空洞部を含む、ステップと、
(b)複数のサンプルを、前記流体吸引/分配用部材の各々の前記第2ポートを通して、前記サンプル用空洞部内へ吸引するステップと、
(c)複数の流体容器を作り出すために前記流体吸引/分配用部材の各々の前記第2ポートをシールするステップと、
(d)前記容器の各々の中で、前記サンプル中の粒子を前記サンプルの残部から分離するステップと、
を含み、
前記分離された粒子およびサンプルは、前記粒子またはサンプルの検出のために、前記流体吸引/分配用部材の各々の前記サンプル用空洞部の内部に保持される、方法。
【請求項42】
請求項41に記載の方法において、
前記装填するステップは、前記流体吸引/分配用プレートを前記装置の複数の管部へ取り付けることを必要とし、前記管部は、計量機構の一部である、方法。
【請求項43】
請求項41に記載の方法において、
前記流体吸引/分配用部材は、計量先端部である、方法。
【請求項44】
請求項41に記載の方法において、
前記装置は、臨床分析器である、方法。
【請求項45】
請求項41に記載の方法において、
前記分離するステップは、遠心分離によって行なわれる、方法。
【請求項46】
請求項41に記載の方法において、
前記吸引するステップの後に、前記部材の各々の前記第1ポートが蓋によって閉ざされるステップであって、前記蓋が前記第1ポートの上に設置されると、前記蓋は、前記部材の各々の前記第1ポートを閉じるように構成されている、ステップ、
をさらに含む、方法。
【請求項47】
請求項41に記載の方法において、
前記シールするステップは、前記部材の各々の前記第2ポートをヒートシールすることによって行われる、方法。
【図1】


【図2】


【図3A】


【図3B】


【図3C】


【図3D】


【図3E】


【図3F】


【図3G】


【図4】


【図5】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図6H】


【図6I】




【図2】


【図3A】


【図3B】


【図3C】


【図3D】


【図3E】


【図3F】


【図3G】


【図4】


【図5】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図6H】


【図6I】


【公開番号】特開2010−25937(P2010−25937A)
【公開日】平成22年2月4日(2010.2.4)
【国際特許分類】
【外国語出願】
【出願番号】特願2009−166307(P2009−166307)
【出願日】平成21年7月15日(2009.7.15)
【出願人】(501131014)オーソ−クリニカル・ダイアグノスティックス・インコーポレイテッド (30)
【氏名又は名称原語表記】Ortho−Clinical Diagnostics, Inc.
【住所又は居所原語表記】100 Indigo Creek Drive, Rochester, NY 14626−5101, U.S.A.
【Fターム(参考)】
【公開日】平成22年2月4日(2010.2.4)
【国際特許分類】
【出願番号】特願2009−166307(P2009−166307)
【出願日】平成21年7月15日(2009.7.15)
【出願人】(501131014)オーソ−クリニカル・ダイアグノスティックス・インコーポレイテッド (30)
【氏名又は名称原語表記】Ortho−Clinical Diagnostics, Inc.
【住所又は居所原語表記】100 Indigo Creek Drive, Rochester, NY 14626−5101, U.S.A.
【Fターム(参考)】
[ Back to top ]

