マニジピンの多形形態
本発明は、様々な新規多形形態のマニジピン及びその医薬として許容し得る塩に関する。本発明はまた、該多形形態のマニジピン及びその医薬として許容し得る塩の製造方法にも関する。
【発明の詳細な説明】
【技術分野】
【0001】
(発明の分野)
本発明は、新規多形形態のカルシウムチャンネル遮断薬及びその製造方法に関する。
特に、本発明は、新規多形形態のマニジピン及びその医薬として許容し得る塩に関する。また、本発明は、前記新規多形の製造方法に関する。
【背景技術】
【0002】
(背景)
マニジピン(化学的には、1,4-ジヒドロ-2,6-ジメチル-4-(3-ニトロフェニル)-3,5-ピリジンジカルボン酸2-[4-(ジフェニルメチル)-1-ピペラジニル]エチルメチルエステルと称される)は、ジヒドロピリジンカルシウムチャンネル遮断薬である。これは、フラニジピンとしても知られ、下記に示される構造(I)で表される。
【化1】

【0003】
マニジピンは、親油性でかつ高血管選択性の物質であり、高血圧治療に対して長期活性を有する。マニジピンは、軽度から中等度の高血圧患者において血圧を有効に低下させ、24時間の投与期間の間低下した血圧レベルを有効に維持するジヒドロピリジン(DHP)カルシウムチャンネルアンタゴニストである。それは、不耐性の所見なく長期間有効である。マニジピンは、軽度から中等度の高血圧患者における血圧低下の第1の選択肢を提供する。
【0004】
マニジピンの製造及び多形の存在は、EP0094159B1及びその対応のUS4892875に記載されている。また、Chem. Pharm. Bull., 1989, 37, (8), 2225-8には、光学活性モノカルボン酸のエステル化による鏡像異性(+)-及び(-)-マニジピン二塩酸塩の合成が記載されている。
Chem. Pharm. Bull., 1985, 33, (9), 3787-3797は、融点によって特徴付けられるマニジピン二塩酸塩の2つの結晶形態:α形態及びβ形態を開示している。
更に該文献のデータは、マニジピンが、結晶性塩基、及びマニジピン二塩酸塩一水和物形態で存在し得ることを示している。
【0005】
Eur J. Med. Chem., 33, 1998, 399-420は、マニジピンを開示しているが、特徴付けのデータは示されていない。
FR2924223は、ラマンスペクトルを使用するマニジピン二塩酸塩の多形純度の決定方法を開示している。これは、所定の多形純度を有するマニジピン二塩酸塩の製造に使用され得る。
結果として、増大した溶解度を有するマニジピンの結晶形態及びその医薬として許容し得る塩、並びにその製造方法、医薬組成物、及び使用方法を提供することは、当該分野に対する大きな貢献となり得る。
【0006】
(発明の目的)
本発明の目的は、様々な多形のマニジピン及びその医薬として許容し得る塩を提供することである。
本発明の別の目的は、新規多形のマニジピン及びその医薬として許容し得る塩の製造方法を提供することである。
本発明の更に別の目的は、産業上有利で、費用効率が良く、かつ環境に配慮した、高純度のマニジピンを高収率で製造するための方法を提供することである。
【図面の簡単な説明】
【0007】
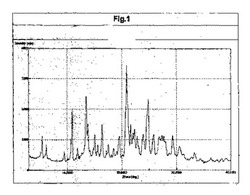
【図1】形態Iのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図2】形態IIのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図3】形態IIIのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図4】形態IVのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図5】非晶質形態Vのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図6】形態VIのマニジピン塩基のX線回折スペクトルを示す。
【図7】非晶質形態VIIのマニジピン塩基のX線回折スペクトルを示す。
【発明の概要】
【0008】
本発明は、形態I、形態II、形態III、形態IV、形態V、形態VI、及び形態VIIと称される新規多形形態のマニジピン二塩酸塩及び塩基を提供する。
したがって、本発明は、これら新規形態を高純度かつ高収率で製造するための方法も提供する。
該新規形態のそれぞれは、固有の粉末X線回折パターンによって識別される。
【0009】
本発明は更に、新規マニジピン形態I〜VIIを、1以上の医薬として許容し得る賦形剤とともに含む医薬組成物を提供する。
また、本発明は、新規マニジピン形態I〜VIIを含む医薬組成物を製造するための方法を提供する。
本発明は更に、マニジピン及びその医薬として許容し得る塩が有用である疾患又は症状の治療方法を提供する。
該方法の利点として、簡易性、環境保全性、及び商業利用への適合性が挙げられる。
【発明を実施するための形態】
【0010】
(発明の詳細な説明)
本発明は、新規結晶形態のマニジピン及びその医薬として許容し得る塩、該新規形態のマニジピン及びその医薬として許容し得る塩の高純度かつ高収率な製造方法、及びそれらを含む医薬組成物を提供する。該方法の利点として、簡易性、環境保全性、及び商業利用への適合性が挙げられる。
【0011】
多形は、主にX線回折図形のピーク位置によって最も確実に特徴付けられるので、本発明の多形は、特定の結晶形態のフィンガープリントを生成する粉末X線回折スペクトル法によって特徴付けられている。2θ値の測定値は典型的に、±0.2°の範囲内で正確である。全ての粉末回折パターンは、copper-K-α放射線源を備えた最新のX線粉末回折計Rigaku Dmax 2200で測定した。XRDパターンは2シータ値(2θ)及びパーセント強度(%)について表される。
【0012】
本発明で得られる全ての多形は、安定で、高純度であり、かつ少量の残留溶媒を有する。
本発明は、更に多形の製造方法を提供する。
【0013】
したがって、一態様において、本発明は、以後「形態I」と表される新規多形のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態Iのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態Iのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0014】
一実施態様において、該方法は、溶媒を含まない媒体における形態Iのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、結晶多形形態Iのマニジピン二塩酸塩は、10.94、13.50、20.90、21.14、及び24.86±0.2°2θにピークを有するXRDパターンを有する。該XRDパターンは、13.82、16.40、20.72、24.50、及び24.58°2θ±0.2°2θに更なるピークを含み得る。
【0015】
一実施態様において、結晶多形形態Iのマニジピン二塩酸塩は、表1に示されるように2θ値にピークを有するXRDパターンを有する。
【表1】

【0016】
別の実施態様において、結晶多形形態Iのマニジピン二塩酸塩のX線粉末回折スペクトルは、図1に示される。
【0017】
本発明の別の態様により、マニジピン二塩酸塩をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、沈殿した結晶形態Iのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態Iの製造方法が提供される。該方法によって製造される結晶形態Iのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、形態Iのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0018】
本発明の別の態様は、以後「形態II」と表される新規多形のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態IIのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態IIのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0019】
一実施態様において、該方法は、溶媒を含まない媒体における形態IIのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態IIは、10.94、22.02、22.74、及び22.84±0.2°2θにピークを有するX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、13.5、17.52、及び21.02 ±0.2°2θに更なるピークを含み得る。
【0020】
一実施態様において、結晶多形「形態II」のマニジピン二塩酸塩は、表2に示されるように2θ値にピークを有するXRDパターンを有する。
【表2】

【0021】
別の実施態様において、結晶多形形態IIのマニジピン二塩酸塩のX線粉末回折スペクトルは、図2に示される。
【0022】
本発明の別の態様により、マニジピン二塩酸塩をメタノールと変性エタノールとの混合物(1:1)に還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態IIの製造方法が提供される。該方法によって製造される結晶形態IIのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、形態IIのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0023】
本発明の更に別の態様は、以後「形態III」と表される新規多形形態のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態IIIのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態IIIのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0024】
一実施態様において、該方法は、溶媒を含まない媒体における形態IIIのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態IIIは、9.06、13.44、20.98、21.70、21.80、21.92、22.80、及び24.42±0.2°2θにピークを含むX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、10.90、14.28、15.80、18.28、27.60、及び27.70±0.2°2θに更なるピークを含み得る。
【0025】
一実施態様において、結晶多形形態IIIのマニジピン二塩酸塩は、表3に示されるように2θ値にピークを有するXRDパターンを有する。
【表3】

【0026】
別の実施態様において、結晶多形形態IIIのマニジピン二塩酸塩のX線粉末回折スペクトルは、図3に示される。
【0027】
本発明の別の態様により、マニジピン二塩酸塩をメタノールとトルエンとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態IIIの製造方法が提供される。該方法によって製造される結晶形態IIIのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、該形態IIIのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0028】
本発明の更に別の態様は、以後「形態IV」と表される新規多形形態のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態IVのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態IVのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0029】
一実施態様において、該方法は、溶媒を含まない媒体における形態IVのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態IVは、12.58、20.34、及び23.36±0.2°2θにピークを含むX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、7.90、10.10、18.98、22.28、26.62、及び28.32±0.2°2θに更なるピークを含み得る。
【0030】
一実施態様において、結晶多形形態IVのマニジピン二塩酸塩は、表4に示されるように2θ値にピークを有するXRDパターンを有する。
【表4】

【0031】
別の実施態様において、結晶多形形態IVのマニジピン二塩酸塩のX線粉末回折スペクトルは、図4に示される。
【0032】
本発明の別の態様により、マニジピン二塩酸塩をトルエンと変性エタノールとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IVのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態IVの製造方法が提供される。該方法によって製造される結晶形態IVのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、該形態IVのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0033】
本発明の更に別の態様において、以後「形態V」と表される非晶質形態のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態Vのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態Vのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0034】
一実施態様において、該方法は、溶媒を含まない媒体における形態Vのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態Vは、X線粉末回折スペクトルによって特徴付けられる。
【0035】
別の実施態様において、非晶質形態Vのマニジピン二塩酸塩は、図5に示されるXRDパターンを有することによって特徴付けられる。
本発明の別の態様により、マニジピン二塩酸塩をメタノールに還流で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質形態Vのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態Vの製造方法が提供される。該方法によって製造される非晶質形態Vのマニジピン二塩酸塩は、上記形態であり得る。
【0036】
好ましい実施態様において、形態Vのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
形態I、II、III、IV、又はVの製造に使用されるマニジピン二塩酸塩は、任意の多形形態であるか、又は任意の多形形態の混合物であり得る。
【0037】
更に別の態様において、本発明は、以後「形態VI」と表される結晶形態のマニジピン塩基を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態VIのマニジピン塩基の高収率かつ高純度な製造方法を提供する。また、本発明は、形態VIのマニジピン塩基を含む医薬組成物を提供する。
【0038】
一実施態様において、該方法は、溶媒を含まない媒体における形態VIのマニジピン塩基の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン塩基を生成することを含む。
一実施態様において、本発明の形態VIは、5.08、14.04、15.40、20.60、及び21.94±0.2°2θにピークを含むX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、15.08、18.96、19.44、及び22.26±0.2°2θに更なるピークを含み得る。
【0039】
一実施態様において、結晶多形形態VIのマニジピン塩基は、表5に示されるように2θ値にピークを有するXRDパターンを有する。
【表5】

【0040】
別の実施態様において、結晶多形形態VIのマニジピン塩基は、図6に示されるXRDパターンを有することによって特徴付けられる。
【0041】
本発明の別の態様により、マニジピン塩基をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、撹拌下でn-ヘプタンを加えること、10〜12時間撹拌すること、沈殿した結晶形態VIのマニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態VIの製造方法が提供される。該方法によって製造される結晶形態VIのマニジピン塩基は、上記形態であり得る。
好ましい実施態様において、形態VIのマニジピン塩基は、ラセミ体の形態で提供される。
【0042】
更に別の態様において、本発明は、以後「形態VII」と表される非晶質形態のマニジピン塩基を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態VIIのマニジピン塩基の高収率かつ高純度な製造方法を提供する。また、本発明は、形態VIIのマニジピン塩基を含む医薬組成物を提供する。
【0043】
一実施態様において、該方法は、溶媒を含まない媒体における形態VIIのマニジピン塩基の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン塩基を生成することを含む。
一実施態様において、本発明の形態VIIは、X線粉末回折スペクトルによって特徴付けられる。
別の実施態様において、結晶多形VIIのマニジピン塩基は、図7に示されるXRDパターンを有することによって特徴付けられる。
【0044】
本発明の別の態様により、マニジピン塩基を二塩化メチレンに約40℃で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質形態VIIのマニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態VIIの製造方法が提供される。該方法によって製造される非晶質形態VIIのマニジピン塩基は、上記形態であり得る。
【0045】
好ましい実施態様において、形態VIIのマニジピン塩基は、ラセミ体の形態で提供される。
形態VI又はVIIの製造に使用されるマニジピン塩基は、任意の多形形態であるか、又は任意の多形形態の混合物であり得る。
【0046】
本発明にしたがって得られる新規多形のマニジピンは、他の形態のマニジピンを実質的に含まない。他の形態のマニジピンを「実質的に含まない」とは、該多形のマニジピンが、10%未満、好ましくは5%未満の他の形態のマニジピン、及び1%未満の他の不純物、水又は溶媒を含むことを意味すると理解されたい。
発明の方法は、任意形態のマニジピンの精製方法として、及び新規多形の製造方法として使用され得る。
【0047】
本発明の別の態様により、上記多形形態のマニジピン又はその医薬として許容し得る塩を、1以上の医薬として許容し得る賦形剤とともに含む医薬組成物が提供される。医薬組成物の製造において使用されるマニジピン二塩酸塩は、実質的に上記形態I、II、III、IV又はVの1からなり得るか、又は実質的に前記形態の2以上の組み合わせからなり得る。医薬組成物の製造において使用されるマニジピン塩基は、実質的に上記形態V又はVIの1からなり得るか、又は実質的に前記形態の両方の組み合わせからなり得る。
【0048】
マニジピン又はその塩は、血圧上昇(高血圧)の制御に有効であることが見出されている。本発明の医薬組成物は、有効成分である新規多形I、II、III、IV、V、VI、又はVIIのマニジピンを、1以上の医薬として許容し得る担体、賦形剤、又は希釈剤とともに含む。医薬組成物及び本発明の剤形の製造には、任意の従来技術を使用することができる。
【0049】
マニジピンの多形I、II、III、IV、V、VI、及びVIIは、くるぶし浮腫を含む様々な疾患及び障害の治療に有用である。また、該薬剤は、高血圧、及び随伴性2型糖尿病、又は腎機能障害の患者の血圧を有意に低下させる。
したがって、本発明は、ヒトに有効量のマニジピンの形態を投与することによる、マニジピンの投与に応答することが公知の疾患又は障害に罹患しているヒトを治療する方法を提供する。
【0050】
本明細書中に開示される実施態様には、様々な修正がなされ得る。したがって、上記は、限定するものと解釈されるべきではなく、単なる実施態様の例示としてみなされるべきである。
ここで、本発明は、本発明の範囲を何ら限定しない下記実施例によって、更に例示される。
【実施例】
【0051】
(実施例1)
(マニジピン塩基の製造)
トルエン(35ml)中のベンズヒドリルピペラジン(7.28g)の溶液に、室温でジメチルホルムアミド(70ml)、2-クロロエタノール(5ml)及び炭酸カリウム(5g)を加えた。一定の撹拌を14〜16時間行いながら、該反応塊を還流まで加熱した。反応塊を冷却し、ろ過し、真空下で濃縮して2-(4-ベンズヒドリルピペラジン-1-イル)エタノール(収量:7.5g)を得た。
【0052】
トルエン(30ml)中の2,6-ジメチル-4-(3-ニトロ-フェニル)-1,4-ジヒドロ-ピリジン-3,5-ジカルボン酸モノメチルエステル(5g)、ジシクロヘキシルカルボジイミド(3.08g)、及びジメチルアミノピリジン(0.25g)の懸濁液に、室温で2-(4-ベンズヒドリルピペラジン-1-イル)エタノール(7.5g)を加えた。次いで、反応塊を70〜75℃に2時間加熱した。次いで、反応塊を室温まで冷却し、濾過した。トルエン層を真空下で濃縮して、マニジピン塩基(5g)を得た。
【0053】
(実施例2)
(マニジピン二塩酸塩の製造)
マニジピン塩基をアセトン(15ml)に溶解させた。一定の撹拌を行いながら、該溶液のpHをIPA-HCl溶液で1〜1.5に調整して、マニジピン二塩酸塩を得た。該反応塊をろ過し、2時間乾燥させた(収量:3g)。
【0054】
(実施例3)
(結晶形態Iのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(16g)をメタノール(320ml)に65℃で溶解させた。一定の撹拌を4時間行いながら、該溶液を室温まで冷却した。得られた固体をろ過し、メタノールで洗浄し、真空下、約40〜45℃で10〜12時間乾燥させて、形態Iの結晶(収量:14.6g)(純度:99.81%)を得た。該多形をXRDで特徴付けた。
【0055】
(実施例4)
(結晶形態IIのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(0.5g)をメタノールと変性エタノールとの混合物(1:1)(8ml)に65℃で溶解させた。該透明溶液をゆっくりと冷却し、室温で12〜14時間撹拌した。得られた固体をろ過し、メタノールで洗浄し、真空下、約40〜45℃で10〜12時間乾燥させて、形態IIの結晶(収量:0.4g)(純度:99.89%)を得た。該多形をXRDで特徴付けた。
【0056】
(実施例5)
(結晶形態IIIのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(0.5g)をメタノールとトルエンとの混合物(1:1)(4.5ml)に75℃で溶解させた。該透明溶液をゆっくりと冷却し、室温で12〜14時間撹拌した。次いで、得られた固体をろ過し、メタノールで洗浄し、真空下、約45℃で10〜12時間乾燥させて、形態IIIの結晶(収量:0.4g)(純度:99.81%)を得た。該多形をXRDで特徴付けた。
【0057】
(実施例6)
(結晶形態IVのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(0.5g)をトルエンと変性エタノールとの混合物(1:1)(9.5ml)に75〜80℃で溶解させた。該透明溶液をゆっくりと冷却し、室温で12〜14時間撹拌した。得られた固体をろ過し、変性エタノールで洗浄し、真空下、約45℃で10〜12時間乾燥させて、形態IVの結晶(収量:0.35g)(純度:99.87%)を得た。該多形をXRDで特徴付けた。
【0058】
(実施例7)
(非晶質形態Vのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(1g)をメタノール(20ml)に65℃で溶解させた。溶媒を真空下、50℃未満で完全に蒸留した。得られた固体を真空下、40〜45℃で少なくとも10時間乾燥させて、非晶質形態V(収量:0.9g)(純度:99.80%)を得た。該非晶質形態をXRDで特徴付けた。
【0059】
(実施例8)
(結晶形態VIのマニジピン塩基の製造)
マニジピン塩基(1g)をメタノール(2ml)に45℃で溶解させた。該溶液を室温まで冷却した。n-ヘプタン(20ml)を該透明溶液に加えた。撹拌を10〜12時間続け、沈殿物をろ過し、n-ヘプタンで洗浄した。単離した化合物を真空下、45〜50℃で10〜12時間乾燥させた(収量:0.8g)(純度:99.79%)。該多形形態VIをXRDで特徴付けた。
【0060】
(実施例9)
(非晶質形態VIIのマニジピン塩基の製造)
マニジピン塩基(1g)を二塩化メチレン(5ml)に60℃で溶解させた。溶媒を完全に蒸留した。次いで、得られた化合物を単離し、真空下、45〜50℃で10〜12時間乾燥させた(収量:0.9g)(純度:99.77%)。該非晶質形態VIIをXRDで特徴付けた。
【技術分野】
【0001】
(発明の分野)
本発明は、新規多形形態のカルシウムチャンネル遮断薬及びその製造方法に関する。
特に、本発明は、新規多形形態のマニジピン及びその医薬として許容し得る塩に関する。また、本発明は、前記新規多形の製造方法に関する。
【背景技術】
【0002】
(背景)
マニジピン(化学的には、1,4-ジヒドロ-2,6-ジメチル-4-(3-ニトロフェニル)-3,5-ピリジンジカルボン酸2-[4-(ジフェニルメチル)-1-ピペラジニル]エチルメチルエステルと称される)は、ジヒドロピリジンカルシウムチャンネル遮断薬である。これは、フラニジピンとしても知られ、下記に示される構造(I)で表される。
【化1】

【0003】
マニジピンは、親油性でかつ高血管選択性の物質であり、高血圧治療に対して長期活性を有する。マニジピンは、軽度から中等度の高血圧患者において血圧を有効に低下させ、24時間の投与期間の間低下した血圧レベルを有効に維持するジヒドロピリジン(DHP)カルシウムチャンネルアンタゴニストである。それは、不耐性の所見なく長期間有効である。マニジピンは、軽度から中等度の高血圧患者における血圧低下の第1の選択肢を提供する。
【0004】
マニジピンの製造及び多形の存在は、EP0094159B1及びその対応のUS4892875に記載されている。また、Chem. Pharm. Bull., 1989, 37, (8), 2225-8には、光学活性モノカルボン酸のエステル化による鏡像異性(+)-及び(-)-マニジピン二塩酸塩の合成が記載されている。
Chem. Pharm. Bull., 1985, 33, (9), 3787-3797は、融点によって特徴付けられるマニジピン二塩酸塩の2つの結晶形態:α形態及びβ形態を開示している。
更に該文献のデータは、マニジピンが、結晶性塩基、及びマニジピン二塩酸塩一水和物形態で存在し得ることを示している。
【0005】
Eur J. Med. Chem., 33, 1998, 399-420は、マニジピンを開示しているが、特徴付けのデータは示されていない。
FR2924223は、ラマンスペクトルを使用するマニジピン二塩酸塩の多形純度の決定方法を開示している。これは、所定の多形純度を有するマニジピン二塩酸塩の製造に使用され得る。
結果として、増大した溶解度を有するマニジピンの結晶形態及びその医薬として許容し得る塩、並びにその製造方法、医薬組成物、及び使用方法を提供することは、当該分野に対する大きな貢献となり得る。
【0006】
(発明の目的)
本発明の目的は、様々な多形のマニジピン及びその医薬として許容し得る塩を提供することである。
本発明の別の目的は、新規多形のマニジピン及びその医薬として許容し得る塩の製造方法を提供することである。
本発明の更に別の目的は、産業上有利で、費用効率が良く、かつ環境に配慮した、高純度のマニジピンを高収率で製造するための方法を提供することである。
【図面の簡単な説明】
【0007】
【図1】形態Iのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図2】形態IIのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図3】形態IIIのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図4】形態IVのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図5】非晶質形態Vのマニジピン二塩酸塩のX線回折スペクトルを示す。
【図6】形態VIのマニジピン塩基のX線回折スペクトルを示す。
【図7】非晶質形態VIIのマニジピン塩基のX線回折スペクトルを示す。
【発明の概要】
【0008】
本発明は、形態I、形態II、形態III、形態IV、形態V、形態VI、及び形態VIIと称される新規多形形態のマニジピン二塩酸塩及び塩基を提供する。
したがって、本発明は、これら新規形態を高純度かつ高収率で製造するための方法も提供する。
該新規形態のそれぞれは、固有の粉末X線回折パターンによって識別される。
【0009】
本発明は更に、新規マニジピン形態I〜VIIを、1以上の医薬として許容し得る賦形剤とともに含む医薬組成物を提供する。
また、本発明は、新規マニジピン形態I〜VIIを含む医薬組成物を製造するための方法を提供する。
本発明は更に、マニジピン及びその医薬として許容し得る塩が有用である疾患又は症状の治療方法を提供する。
該方法の利点として、簡易性、環境保全性、及び商業利用への適合性が挙げられる。
【発明を実施するための形態】
【0010】
(発明の詳細な説明)
本発明は、新規結晶形態のマニジピン及びその医薬として許容し得る塩、該新規形態のマニジピン及びその医薬として許容し得る塩の高純度かつ高収率な製造方法、及びそれらを含む医薬組成物を提供する。該方法の利点として、簡易性、環境保全性、及び商業利用への適合性が挙げられる。
【0011】
多形は、主にX線回折図形のピーク位置によって最も確実に特徴付けられるので、本発明の多形は、特定の結晶形態のフィンガープリントを生成する粉末X線回折スペクトル法によって特徴付けられている。2θ値の測定値は典型的に、±0.2°の範囲内で正確である。全ての粉末回折パターンは、copper-K-α放射線源を備えた最新のX線粉末回折計Rigaku Dmax 2200で測定した。XRDパターンは2シータ値(2θ)及びパーセント強度(%)について表される。
【0012】
本発明で得られる全ての多形は、安定で、高純度であり、かつ少量の残留溶媒を有する。
本発明は、更に多形の製造方法を提供する。
【0013】
したがって、一態様において、本発明は、以後「形態I」と表される新規多形のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態Iのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態Iのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0014】
一実施態様において、該方法は、溶媒を含まない媒体における形態Iのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、結晶多形形態Iのマニジピン二塩酸塩は、10.94、13.50、20.90、21.14、及び24.86±0.2°2θにピークを有するXRDパターンを有する。該XRDパターンは、13.82、16.40、20.72、24.50、及び24.58°2θ±0.2°2θに更なるピークを含み得る。
【0015】
一実施態様において、結晶多形形態Iのマニジピン二塩酸塩は、表1に示されるように2θ値にピークを有するXRDパターンを有する。
【表1】

【0016】
別の実施態様において、結晶多形形態Iのマニジピン二塩酸塩のX線粉末回折スペクトルは、図1に示される。
【0017】
本発明の別の態様により、マニジピン二塩酸塩をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、沈殿した結晶形態Iのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態Iの製造方法が提供される。該方法によって製造される結晶形態Iのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、形態Iのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0018】
本発明の別の態様は、以後「形態II」と表される新規多形のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態IIのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態IIのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0019】
一実施態様において、該方法は、溶媒を含まない媒体における形態IIのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態IIは、10.94、22.02、22.74、及び22.84±0.2°2θにピークを有するX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、13.5、17.52、及び21.02 ±0.2°2θに更なるピークを含み得る。
【0020】
一実施態様において、結晶多形「形態II」のマニジピン二塩酸塩は、表2に示されるように2θ値にピークを有するXRDパターンを有する。
【表2】

【0021】
別の実施態様において、結晶多形形態IIのマニジピン二塩酸塩のX線粉末回折スペクトルは、図2に示される。
【0022】
本発明の別の態様により、マニジピン二塩酸塩をメタノールと変性エタノールとの混合物(1:1)に還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態IIの製造方法が提供される。該方法によって製造される結晶形態IIのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、形態IIのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0023】
本発明の更に別の態様は、以後「形態III」と表される新規多形形態のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態IIIのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態IIIのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0024】
一実施態様において、該方法は、溶媒を含まない媒体における形態IIIのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態IIIは、9.06、13.44、20.98、21.70、21.80、21.92、22.80、及び24.42±0.2°2θにピークを含むX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、10.90、14.28、15.80、18.28、27.60、及び27.70±0.2°2θに更なるピークを含み得る。
【0025】
一実施態様において、結晶多形形態IIIのマニジピン二塩酸塩は、表3に示されるように2θ値にピークを有するXRDパターンを有する。
【表3】

【0026】
別の実施態様において、結晶多形形態IIIのマニジピン二塩酸塩のX線粉末回折スペクトルは、図3に示される。
【0027】
本発明の別の態様により、マニジピン二塩酸塩をメタノールとトルエンとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態IIIの製造方法が提供される。該方法によって製造される結晶形態IIIのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、該形態IIIのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0028】
本発明の更に別の態様は、以後「形態IV」と表される新規多形形態のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態IVのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態IVのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0029】
一実施態様において、該方法は、溶媒を含まない媒体における形態IVのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態IVは、12.58、20.34、及び23.36±0.2°2θにピークを含むX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、7.90、10.10、18.98、22.28、26.62、及び28.32±0.2°2θに更なるピークを含み得る。
【0030】
一実施態様において、結晶多形形態IVのマニジピン二塩酸塩は、表4に示されるように2θ値にピークを有するXRDパターンを有する。
【表4】

【0031】
別の実施態様において、結晶多形形態IVのマニジピン二塩酸塩のX線粉末回折スペクトルは、図4に示される。
【0032】
本発明の別の態様により、マニジピン二塩酸塩をトルエンと変性エタノールとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IVのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態IVの製造方法が提供される。該方法によって製造される結晶形態IVのマニジピン二塩酸塩は、上記形態であり得る。
好ましい実施態様において、該形態IVのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
【0033】
本発明の更に別の態様において、以後「形態V」と表される非晶質形態のマニジピン二塩酸塩を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態Vのマニジピン二塩酸塩の高収率かつ高純度な製造方法を提供する。また、本発明は、形態Vのマニジピン二塩酸塩を含む医薬組成物を提供する。
【0034】
一実施態様において、該方法は、溶媒を含まない媒体における形態Vのマニジピン二塩酸塩の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン二塩酸塩を生成することを含む。
一実施態様において、本発明の形態Vは、X線粉末回折スペクトルによって特徴付けられる。
【0035】
別の実施態様において、非晶質形態Vのマニジピン二塩酸塩は、図5に示されるXRDパターンを有することによって特徴付けられる。
本発明の別の態様により、マニジピン二塩酸塩をメタノールに還流で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質形態Vのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態Vの製造方法が提供される。該方法によって製造される非晶質形態Vのマニジピン二塩酸塩は、上記形態であり得る。
【0036】
好ましい実施態様において、形態Vのマニジピン二塩酸塩は、ラセミ体の形態で提供される。
形態I、II、III、IV、又はVの製造に使用されるマニジピン二塩酸塩は、任意の多形形態であるか、又は任意の多形形態の混合物であり得る。
【0037】
更に別の態様において、本発明は、以後「形態VI」と表される結晶形態のマニジピン塩基を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態VIのマニジピン塩基の高収率かつ高純度な製造方法を提供する。また、本発明は、形態VIのマニジピン塩基を含む医薬組成物を提供する。
【0038】
一実施態様において、該方法は、溶媒を含まない媒体における形態VIのマニジピン塩基の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン塩基を生成することを含む。
一実施態様において、本発明の形態VIは、5.08、14.04、15.40、20.60、及び21.94±0.2°2θにピークを含むX線粉末回折スペクトルによって特徴付けられる。該XRDパターンは、15.08、18.96、19.44、及び22.26±0.2°2θに更なるピークを含み得る。
【0039】
一実施態様において、結晶多形形態VIのマニジピン塩基は、表5に示されるように2θ値にピークを有するXRDパターンを有する。
【表5】

【0040】
別の実施態様において、結晶多形形態VIのマニジピン塩基は、図6に示されるXRDパターンを有することによって特徴付けられる。
【0041】
本発明の別の態様により、マニジピン塩基をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、撹拌下でn-ヘプタンを加えること、10〜12時間撹拌すること、沈殿した結晶形態VIのマニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態VIの製造方法が提供される。該方法によって製造される結晶形態VIのマニジピン塩基は、上記形態であり得る。
好ましい実施態様において、形態VIのマニジピン塩基は、ラセミ体の形態で提供される。
【0042】
更に別の態様において、本発明は、以後「形態VII」と表される非晶質形態のマニジピン塩基を提供し、これは実質的に非吸湿性であり、かつ良流動特性を有する。
別の態様において、本発明は、新規形態VIIのマニジピン塩基の高収率かつ高純度な製造方法を提供する。また、本発明は、形態VIIのマニジピン塩基を含む医薬組成物を提供する。
【0043】
一実施態様において、該方法は、溶媒を含まない媒体における形態VIIのマニジピン塩基の単離、したがって、溶媒を含まない又は溶媒の含有量を無視できるマニジピン塩基を生成することを含む。
一実施態様において、本発明の形態VIIは、X線粉末回折スペクトルによって特徴付けられる。
別の実施態様において、結晶多形VIIのマニジピン塩基は、図7に示されるXRDパターンを有することによって特徴付けられる。
【0044】
本発明の別の態様により、マニジピン塩基を二塩化メチレンに約40℃で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質形態VIIのマニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、形態VIIの製造方法が提供される。該方法によって製造される非晶質形態VIIのマニジピン塩基は、上記形態であり得る。
【0045】
好ましい実施態様において、形態VIIのマニジピン塩基は、ラセミ体の形態で提供される。
形態VI又はVIIの製造に使用されるマニジピン塩基は、任意の多形形態であるか、又は任意の多形形態の混合物であり得る。
【0046】
本発明にしたがって得られる新規多形のマニジピンは、他の形態のマニジピンを実質的に含まない。他の形態のマニジピンを「実質的に含まない」とは、該多形のマニジピンが、10%未満、好ましくは5%未満の他の形態のマニジピン、及び1%未満の他の不純物、水又は溶媒を含むことを意味すると理解されたい。
発明の方法は、任意形態のマニジピンの精製方法として、及び新規多形の製造方法として使用され得る。
【0047】
本発明の別の態様により、上記多形形態のマニジピン又はその医薬として許容し得る塩を、1以上の医薬として許容し得る賦形剤とともに含む医薬組成物が提供される。医薬組成物の製造において使用されるマニジピン二塩酸塩は、実質的に上記形態I、II、III、IV又はVの1からなり得るか、又は実質的に前記形態の2以上の組み合わせからなり得る。医薬組成物の製造において使用されるマニジピン塩基は、実質的に上記形態V又はVIの1からなり得るか、又は実質的に前記形態の両方の組み合わせからなり得る。
【0048】
マニジピン又はその塩は、血圧上昇(高血圧)の制御に有効であることが見出されている。本発明の医薬組成物は、有効成分である新規多形I、II、III、IV、V、VI、又はVIIのマニジピンを、1以上の医薬として許容し得る担体、賦形剤、又は希釈剤とともに含む。医薬組成物及び本発明の剤形の製造には、任意の従来技術を使用することができる。
【0049】
マニジピンの多形I、II、III、IV、V、VI、及びVIIは、くるぶし浮腫を含む様々な疾患及び障害の治療に有用である。また、該薬剤は、高血圧、及び随伴性2型糖尿病、又は腎機能障害の患者の血圧を有意に低下させる。
したがって、本発明は、ヒトに有効量のマニジピンの形態を投与することによる、マニジピンの投与に応答することが公知の疾患又は障害に罹患しているヒトを治療する方法を提供する。
【0050】
本明細書中に開示される実施態様には、様々な修正がなされ得る。したがって、上記は、限定するものと解釈されるべきではなく、単なる実施態様の例示としてみなされるべきである。
ここで、本発明は、本発明の範囲を何ら限定しない下記実施例によって、更に例示される。
【実施例】
【0051】
(実施例1)
(マニジピン塩基の製造)
トルエン(35ml)中のベンズヒドリルピペラジン(7.28g)の溶液に、室温でジメチルホルムアミド(70ml)、2-クロロエタノール(5ml)及び炭酸カリウム(5g)を加えた。一定の撹拌を14〜16時間行いながら、該反応塊を還流まで加熱した。反応塊を冷却し、ろ過し、真空下で濃縮して2-(4-ベンズヒドリルピペラジン-1-イル)エタノール(収量:7.5g)を得た。
【0052】
トルエン(30ml)中の2,6-ジメチル-4-(3-ニトロ-フェニル)-1,4-ジヒドロ-ピリジン-3,5-ジカルボン酸モノメチルエステル(5g)、ジシクロヘキシルカルボジイミド(3.08g)、及びジメチルアミノピリジン(0.25g)の懸濁液に、室温で2-(4-ベンズヒドリルピペラジン-1-イル)エタノール(7.5g)を加えた。次いで、反応塊を70〜75℃に2時間加熱した。次いで、反応塊を室温まで冷却し、濾過した。トルエン層を真空下で濃縮して、マニジピン塩基(5g)を得た。
【0053】
(実施例2)
(マニジピン二塩酸塩の製造)
マニジピン塩基をアセトン(15ml)に溶解させた。一定の撹拌を行いながら、該溶液のpHをIPA-HCl溶液で1〜1.5に調整して、マニジピン二塩酸塩を得た。該反応塊をろ過し、2時間乾燥させた(収量:3g)。
【0054】
(実施例3)
(結晶形態Iのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(16g)をメタノール(320ml)に65℃で溶解させた。一定の撹拌を4時間行いながら、該溶液を室温まで冷却した。得られた固体をろ過し、メタノールで洗浄し、真空下、約40〜45℃で10〜12時間乾燥させて、形態Iの結晶(収量:14.6g)(純度:99.81%)を得た。該多形をXRDで特徴付けた。
【0055】
(実施例4)
(結晶形態IIのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(0.5g)をメタノールと変性エタノールとの混合物(1:1)(8ml)に65℃で溶解させた。該透明溶液をゆっくりと冷却し、室温で12〜14時間撹拌した。得られた固体をろ過し、メタノールで洗浄し、真空下、約40〜45℃で10〜12時間乾燥させて、形態IIの結晶(収量:0.4g)(純度:99.89%)を得た。該多形をXRDで特徴付けた。
【0056】
(実施例5)
(結晶形態IIIのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(0.5g)をメタノールとトルエンとの混合物(1:1)(4.5ml)に75℃で溶解させた。該透明溶液をゆっくりと冷却し、室温で12〜14時間撹拌した。次いで、得られた固体をろ過し、メタノールで洗浄し、真空下、約45℃で10〜12時間乾燥させて、形態IIIの結晶(収量:0.4g)(純度:99.81%)を得た。該多形をXRDで特徴付けた。
【0057】
(実施例6)
(結晶形態IVのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(0.5g)をトルエンと変性エタノールとの混合物(1:1)(9.5ml)に75〜80℃で溶解させた。該透明溶液をゆっくりと冷却し、室温で12〜14時間撹拌した。得られた固体をろ過し、変性エタノールで洗浄し、真空下、約45℃で10〜12時間乾燥させて、形態IVの結晶(収量:0.35g)(純度:99.87%)を得た。該多形をXRDで特徴付けた。
【0058】
(実施例7)
(非晶質形態Vのマニジピン二塩酸塩の製造)
マニジピン二塩酸塩(1g)をメタノール(20ml)に65℃で溶解させた。溶媒を真空下、50℃未満で完全に蒸留した。得られた固体を真空下、40〜45℃で少なくとも10時間乾燥させて、非晶質形態V(収量:0.9g)(純度:99.80%)を得た。該非晶質形態をXRDで特徴付けた。
【0059】
(実施例8)
(結晶形態VIのマニジピン塩基の製造)
マニジピン塩基(1g)をメタノール(2ml)に45℃で溶解させた。該溶液を室温まで冷却した。n-ヘプタン(20ml)を該透明溶液に加えた。撹拌を10〜12時間続け、沈殿物をろ過し、n-ヘプタンで洗浄した。単離した化合物を真空下、45〜50℃で10〜12時間乾燥させた(収量:0.8g)(純度:99.79%)。該多形形態VIをXRDで特徴付けた。
【0060】
(実施例9)
(非晶質形態VIIのマニジピン塩基の製造)
マニジピン塩基(1g)を二塩化メチレン(5ml)に60℃で溶解させた。溶媒を完全に蒸留した。次いで、得られた化合物を単離し、真空下、45〜50℃で10〜12時間乾燥させた(収量:0.9g)(純度:99.77%)。該非晶質形態VIIをXRDで特徴付けた。
【特許請求の範囲】
【請求項1】
10.94、13.50、20.90、21.14、及び24.86±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態Iのマニジピン二塩酸塩。
【請求項2】
13.82、16.40、20.72、24.50、及び24.58°2θ±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項1記載の結晶多形形態Iのマニジピン二塩酸塩。
【請求項3】
図1に示されるXRDパターンを有することを特徴とする、結晶形態Iのマニジピン二塩酸塩。
【請求項4】
請求項1〜3のいずれか一項記載の結晶形態Iのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、沈殿した結晶形態Iのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項5】
前記形態Iのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項4記載の製造方法。
【請求項6】
請求項4又は5記載の方法によって製造された結晶形態Iのマニジピン二塩酸塩。
【請求項7】
10.94、22.02、22.74、及び22.84±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態IIのマニジピン二塩酸塩。
【請求項8】
13.5、17.52、及び21.02±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項7記載の結晶多形形態IIのマニジピン二塩酸塩。
【請求項9】
図2に示されるXRDパターンを有することを特徴とする、結晶形態IIのマニジピン二塩酸塩。
【請求項10】
請求項7〜9のいずれか一項記載の結晶形態IIのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールと変性エタノールとの混合物(1:1)に還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項11】
前記形態IIのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項10記載の製造方法。
【請求項12】
請求項10又は11記載の方法によって製造された結晶形態IIのマニジピン二塩酸塩。
【請求項13】
9.06、13.44、20.98、21.70、21.80、21.92、22.80、及び24.42±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態IIIのマニジピン二塩酸塩。
【請求項14】
10.90、14.28、15.80、18.28、27.60、及び27.70±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項13記載の結晶多形形態IIIのマニジピン二塩酸塩。
【請求項15】
図3に示されるXRDパターンを有することを特徴とする、結晶形態IIIのマニジピン二塩酸塩。
【請求項16】
請求項13〜15のいずれか一項記載の結晶形態IIIのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールとトルエンとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項17】
前記形態IIIのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項16記載の製造方法。
【請求項18】
請求項16又は17記載の方法によって製造された結晶形態IIIのマニジピン二塩酸塩。
【請求項19】
12.58、20.34、及び23.36±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態IVのマニジピン二塩酸塩。
【請求項20】
7.90、10.10、18.98、22.28、26.62、及び28.32± 0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項19記載の結晶多形形態IVのマニジピン二塩酸塩。
【請求項21】
図4に示されるXRDパターンを有することを特徴とする、結晶形態IVのマニジピン二塩酸塩。
【請求項22】
請求項19〜21のいずれか一項記載の結晶形態IVのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をトルエンと変性エタノールとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IVのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項23】
前記形態IVのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項22記載の製造方法。
【請求項24】
請求項22又は23記載の方法によって製造された結晶形態IVのマニジピン二塩酸塩。
【請求項25】
非晶質マニジピン二塩酸塩(形態V)。
【請求項26】
図5に示されるXRDパターンを有することを特徴とする、非晶質マニジピン二塩酸塩。
【請求項27】
請求項25又は26記載の非晶質マニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールに還流で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質マニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項28】
前記非晶質マニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項27記載の製造方法。
【請求項29】
請求項27又は28記載の方法によって製造された非晶質マニジピン二塩酸塩。
【請求項30】
5.08、14.04、15.40、20.60、及び21.94±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態VIのマニジピン塩基。
【請求項31】
15.08、18.96、19.44、及び22.26±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項30記載の結晶形態VIのマニジピン塩基。
【請求項32】
図6に示されるXRDパターンを有することを特徴とする、結晶形態VIのマニジピン塩基。
【請求項33】
請求項30〜32のいずれか一項記載の結晶形態VIのマニジピン塩基の製造方法であって、マニジピン塩基をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、撹拌下でn-ヘプタンを加えること、10〜12時間撹拌すること、沈殿した結晶形態VIのマニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項34】
前記形態VIのマニジピン塩基の製造に使用されるマニジピン塩基が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項33記載の製造方法。
【請求項35】
請求項33又は34記載の方法によって製造された結晶形態VIのマニジピン塩基。
【請求項36】
非晶質マニジピン塩基(形態VII)。
【請求項37】
図7に示されるXRDパターンを有することを特徴とする、非晶質マニジピン塩基。
【請求項38】
請求項36又は37に記載の非晶質マニジピン塩基の製造方法であって、二塩化メチレンに約40℃で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質マニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項39】
前記非晶質マニジピン塩基の製造に使用されるマニジピン塩基が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項38記載の製造方法。
【請求項40】
請求項38又は39記載の方法によって製造された非晶質マニジピン塩基。
【請求項41】
請求項1〜3又は6のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項42】
請求項7〜9又は12のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項43】
請求項13〜15又は18のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項44】
請求項19〜21又は24のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項45】
請求項25、26又は29のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項46】
請求項30〜32又は35のいずれか一項記載の多形形態のマニジピン塩基を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項47】
請求項36、37又は40のいずれか一項記載の多形形態のマニジピン塩基を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項1】
10.94、13.50、20.90、21.14、及び24.86±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態Iのマニジピン二塩酸塩。
【請求項2】
13.82、16.40、20.72、24.50、及び24.58°2θ±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項1記載の結晶多形形態Iのマニジピン二塩酸塩。
【請求項3】
図1に示されるXRDパターンを有することを特徴とする、結晶形態Iのマニジピン二塩酸塩。
【請求項4】
請求項1〜3のいずれか一項記載の結晶形態Iのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、沈殿した結晶形態Iのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項5】
前記形態Iのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項4記載の製造方法。
【請求項6】
請求項4又は5記載の方法によって製造された結晶形態Iのマニジピン二塩酸塩。
【請求項7】
10.94、22.02、22.74、及び22.84±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態IIのマニジピン二塩酸塩。
【請求項8】
13.5、17.52、及び21.02±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項7記載の結晶多形形態IIのマニジピン二塩酸塩。
【請求項9】
図2に示されるXRDパターンを有することを特徴とする、結晶形態IIのマニジピン二塩酸塩。
【請求項10】
請求項7〜9のいずれか一項記載の結晶形態IIのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールと変性エタノールとの混合物(1:1)に還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項11】
前記形態IIのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項10記載の製造方法。
【請求項12】
請求項10又は11記載の方法によって製造された結晶形態IIのマニジピン二塩酸塩。
【請求項13】
9.06、13.44、20.98、21.70、21.80、21.92、22.80、及び24.42±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態IIIのマニジピン二塩酸塩。
【請求項14】
10.90、14.28、15.80、18.28、27.60、及び27.70±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項13記載の結晶多形形態IIIのマニジピン二塩酸塩。
【請求項15】
図3に示されるXRDパターンを有することを特徴とする、結晶形態IIIのマニジピン二塩酸塩。
【請求項16】
請求項13〜15のいずれか一項記載の結晶形態IIIのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールとトルエンとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IIIのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項17】
前記形態IIIのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項16記載の製造方法。
【請求項18】
請求項16又は17記載の方法によって製造された結晶形態IIIのマニジピン二塩酸塩。
【請求項19】
12.58、20.34、及び23.36±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態IVのマニジピン二塩酸塩。
【請求項20】
7.90、10.10、18.98、22.28、26.62、及び28.32± 0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項19記載の結晶多形形態IVのマニジピン二塩酸塩。
【請求項21】
図4に示されるXRDパターンを有することを特徴とする、結晶形態IVのマニジピン二塩酸塩。
【請求項22】
請求項19〜21のいずれか一項記載の結晶形態IVのマニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をトルエンと変性エタノールとの混合物(1:1)に75〜80℃で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、12〜14時間撹拌すること、沈殿した結晶形態IVのマニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項23】
前記形態IVのマニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項22記載の製造方法。
【請求項24】
請求項22又は23記載の方法によって製造された結晶形態IVのマニジピン二塩酸塩。
【請求項25】
非晶質マニジピン二塩酸塩(形態V)。
【請求項26】
図5に示されるXRDパターンを有することを特徴とする、非晶質マニジピン二塩酸塩。
【請求項27】
請求項25又は26記載の非晶質マニジピン二塩酸塩の製造方法であって、マニジピン二塩酸塩をメタノールに還流で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質マニジピン二塩酸塩を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項28】
前記非晶質マニジピン二塩酸塩の製造に使用されるマニジピン二塩酸塩が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項27記載の製造方法。
【請求項29】
請求項27又は28記載の方法によって製造された非晶質マニジピン二塩酸塩。
【請求項30】
5.08、14.04、15.40、20.60、及び21.94±0.2°2θにピークを含むXRDパターンを有することを特徴とする、結晶形態VIのマニジピン塩基。
【請求項31】
15.08、18.96、19.44、及び22.26±0.2°2θに更にピークを含むXRDパターンを有することを特徴とする、請求項30記載の結晶形態VIのマニジピン塩基。
【請求項32】
図6に示されるXRDパターンを有することを特徴とする、結晶形態VIのマニジピン塩基。
【請求項33】
請求項30〜32のいずれか一項記載の結晶形態VIのマニジピン塩基の製造方法であって、マニジピン塩基をメタノールに還流で溶解させること、該反応塊を約25℃〜30℃の範囲の温度に冷却すること、撹拌下でn-ヘプタンを加えること、10〜12時間撹拌すること、沈殿した結晶形態VIのマニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項34】
前記形態VIのマニジピン塩基の製造に使用されるマニジピン塩基が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項33記載の製造方法。
【請求項35】
請求項33又は34記載の方法によって製造された結晶形態VIのマニジピン塩基。
【請求項36】
非晶質マニジピン塩基(形態VII)。
【請求項37】
図7に示されるXRDパターンを有することを特徴とする、非晶質マニジピン塩基。
【請求項38】
請求項36又は37に記載の非晶質マニジピン塩基の製造方法であって、二塩化メチレンに約40℃で溶解させること、真空下で乾燥するまで濃縮すること、沈殿した非晶質マニジピン塩基を単離すること、及び真空下、約40〜45℃で少なくとも10時間乾燥させることを含む、前記製造方法。
【請求項39】
前記非晶質マニジピン塩基の製造に使用されるマニジピン塩基が、任意の多形形態であるか、又は任意の多形形態の混合物である、請求項38記載の製造方法。
【請求項40】
請求項38又は39記載の方法によって製造された非晶質マニジピン塩基。
【請求項41】
請求項1〜3又は6のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項42】
請求項7〜9又は12のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項43】
請求項13〜15又は18のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項44】
請求項19〜21又は24のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項45】
請求項25、26又は29のいずれか一項記載の多形形態のマニジピン二塩酸塩を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項46】
請求項30〜32又は35のいずれか一項記載の多形形態のマニジピン塩基を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【請求項47】
請求項36、37又は40のいずれか一項記載の多形形態のマニジピン塩基を、任意に1以上の医薬として許容し得る賦形剤と組み合わせて含む、医薬組成物。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公表番号】特表2013−503145(P2013−503145A)
【公表日】平成25年1月31日(2013.1.31)
【国際特許分類】
【出願番号】特願2012−526115(P2012−526115)
【出願日】平成22年8月26日(2010.8.26)
【国際出願番号】PCT/GB2010/001615
【国際公開番号】WO2011/023954
【国際公開日】平成23年3月3日(2011.3.3)
【出願人】(511109180)シプラ・リミテッド (17)
【Fターム(参考)】
【公表日】平成25年1月31日(2013.1.31)
【国際特許分類】
【出願日】平成22年8月26日(2010.8.26)
【国際出願番号】PCT/GB2010/001615
【国際公開番号】WO2011/023954
【国際公開日】平成23年3月3日(2011.3.3)
【出願人】(511109180)シプラ・リミテッド (17)
【Fターム(参考)】
[ Back to top ]

