ミルナシプラン含有経皮吸収用医薬組成物
【課題】ミルナシプラン又はその薬学的に許容される塩の皮膚透過性を亢進させ、優れた薬理効果を発揮させるための新規な経皮吸収用医薬組成物及びこれを含有する医薬を提供する。
【解決手段】本発明は、ミルナシプラン又はその薬学的に許容される塩を有効成分とし、メントール、シネオール又はモノオレイン酸グリセリン或いはそれらのうちの2種以上の組合せを含有する新規な経皮吸収用医薬組成物及びこれを含有する医薬に関する。本発明組成物及び医薬は、うつ病の治療薬として広く臨床で使用され、慢性疼痛等用の鎮痛剤としての有用性も認められているミルナシプランを有効成分として含有するものであり、有効性と安全性に優れ、コンプライアンスよく長期間使用可能な経皮吸収型の抗うつ剤及び鎮痛剤として非常に有用性が高いものである。
【解決手段】本発明は、ミルナシプラン又はその薬学的に許容される塩を有効成分とし、メントール、シネオール又はモノオレイン酸グリセリン或いはそれらのうちの2種以上の組合せを含有する新規な経皮吸収用医薬組成物及びこれを含有する医薬に関する。本発明組成物及び医薬は、うつ病の治療薬として広く臨床で使用され、慢性疼痛等用の鎮痛剤としての有用性も認められているミルナシプランを有効成分として含有するものであり、有効性と安全性に優れ、コンプライアンスよく長期間使用可能な経皮吸収型の抗うつ剤及び鎮痛剤として非常に有用性が高いものである。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はミルナシプラン又はその薬学的に許容される塩を有効成分として含有する経皮吸収用医薬組成物又はこの組成物を含有する医薬に関する。
【背景技術】
【0002】
うつ病は、気分障害の一種であり、抑うつ気分(不安、焦燥など)、意欲の低下(無気力、億劫など)、精神活動の低下(考えがまとまらないなど)、各種の身体症状(不眠、易疲労感、頭重・頭痛、食欲不振など)を呈する精神疾患である。うつ病は、近年罹患者が増大しており、重症化すると日常生活に支障をきたし、自殺企図など生命に係ることもあることから、社会的にも重要な疾患である。そこで、その発症機序の解明が望まれているが、うつ病の発症には精神的な要因と脳神経科学的な要因が複雑に絡んでいると考えられ、十分な解明には至っていない。このうつ病の治療は、現在、薬物療法(抗うつ剤)と心理学的なケアを組み合わせて行われている。抗うつ剤としては、イミプラミンやアミトリプチリンなどの三環系抗うつ剤(第1世代)が先ず開発され使用されてきた。しかし、三環系抗うつ剤は、シナプス後部のヒスタミンH1受容体、アセチルコリン性ムスカリンM1受容体、アドレナリン性α1受容体なども遮断するため、抗コリン作用による便秘や排尿障害などの副作用が多かった。また、大量服用では致死的になるという問題があった。そこで、より副作用の少ない四環系抗うつ剤(第2世代)が開発されたが、抗うつ効果に物足りなさがあり、抗コリン作用もまだ残っていた。1980年代に、さらに抗コリン作用による副作用の少ないセロトニン選択的再取り込み阻害剤(SSRI)(第3世代)が開発されたが、SSRIは脳内や腸管のセロトニン受容体に対する刺激作用による吐気や嘔吐、服薬中断による離脱症候群などの新たな副作用を生じさせた。その後、1990年代になって、選択的セロトニン・ノルアドレナリン再取り込み阻害剤(SNRI)が開発され、胃腸症状はなお残るものの、抗コリン作用のない薬剤として、広く臨床現場で使用されている。
【0003】
うつ病の薬物療法では血中の薬剤濃度を有効濃度で一定に維持することが、副作用を低減して患者への治療効果を最大限もたらすために重要である。しかし、うつ病の治療では、服薬が長期にわたることやうつ症状が寛解・増悪を繰り返すため、うつ病の治療に一般的に使用されている経口剤を患者がコンプライアンス(医師から処方された薬剤を患者が指示通りに使用すること)よく服薬することが困難で、飲み忘れによる症状の悪化や過剰摂取による副作用を起こすことがある。特に、SSRIは1日1回の服用でよい製剤があるが、SNRIとして汎用されているミルナシプランは1日2〜3回服用する必要があり、さらにコンプライアンスよく服薬することが困難であった。
このような経口剤に対し、薬剤を経皮吸収させて投与する経皮剤は、薬剤が持続的に徐々に皮膚から吸収されるため、経口剤に比べて、有効血中濃度を持続的に維持することが可能である。その結果、特に1日2回以上服用する必要のあった薬剤を1日1回使用すればよい製剤にすることが可能となり、コンプライアンスが改善され得る。加えて、経皮剤の場合、最高血中濃度を低下させることができることから、副作用を回避し易くなる。また、経皮投与は、肝臓での薬剤の代謝による初回通過効果を回避できることから、経口投与より少量の薬剤で血中有効用量を維持できる可能性がある。さらに、薬剤を支持基材に塗布して貼付剤とした場合には、患者が薬剤を使用していることを患者のみならず、医師や看護師、家族などが容易に確認でき、副作用発生時にも貼付剤を剥すことによって以降の薬剤吸収を容易に中止できるメリットがある。従って、経皮剤は患者のコンプライアンス及びクオリティー・オブ・ライフ(QOL)の改善に非常に有用である。しかし、薬剤の種類によっては経皮吸収され難いものもあり、適切な経皮吸収製剤になり得る処方を見出すことが困難な場合も多い。
【0004】
ミルナシプラン〔(±)−シス−2−(アミノメチル)−N,N−ジエチル−1−フェニルシクロプロパンカルボキサミド〕は代表的なSNRIの一つで、脳内神経接合部においてセロトニンとノルアドレナリンの再取り込みを選択的に阻害することにより抗うつ作用を発揮することが知られている第4世代の抗うつ剤である。ミルナシプランは、三環系や四環系抗うつ剤のように神経伝達物質の受容体に結合しないことから抗コリン作用による副作用がなく、また、第3世代の抗うつ剤であるSSRIのように脳内や腸管でセロトニン受容体を刺激することによる吐気や嘔吐の副作用も少ない。効果的にも、セロトニンに加えてノルアドレナリンの再取り込みも阻害することから、セロトニンの再取り込みを選択的に阻害するSSRIより強い抗うつ作用を発揮し、特にSSRIではあまり効果のない意欲にも効果を有する。また、ミルナシプランは、抗うつ作用のみならず疼痛にも有効であり、神経因性疼痛、線維筋痛症、緊張型頭痛等に対する治療効果が報告されている。
なお、本発明において、便宜的にミルナシプランという場合でも、ミルナシプラン塩酸塩を指すことがある。
【0005】
ミルナシプランの経皮吸収剤に関しては、特許文献1の報告がある。しかしながら、これはミルナシプランの経粘膜投与剤に関すものであり、具体的にはミルナシプランの鼻腔内投与用の製剤を開示するのみのものである。粘膜が比較的薬物を透過しやすい組織であるのに対し、皮膚上皮は強力な薬物の透過阻止機能を有する。従って、経皮投与用製剤では、薬剤を経皮吸収させるための、より強力な吸収促進作用を有する処方を見出すことが必要となる。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】国際公開WO2007/086493号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明の目的は、有効成分であるミルナシプラン又はその薬学的に許容される塩の皮膚透過性を亢進させ、優れた薬理効果を発揮させるための、新規な経皮吸収用医薬組成物又はこれを含有する医薬を提供することにある。
【課題を解決するための手段】
【0008】
本発明者らは、経皮吸収が困難なミルナシプラン又はその薬学的に許容される塩の経皮吸収性を向上させることにより、経皮吸収剤として優れた薬理効果を発揮させるための製剤化について鋭意検討を行った。その結果、ミルナシプランに吸収促進剤としてメントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せを配合することにより、ミルナシプランの経皮吸収性が顕著に亢進されることを見出し、本発明を完成した。
【発明の効果】
【0009】
本発明医薬組成物は、ミルナシプラン又はその薬学的に許容される塩を経皮吸収により効果を発揮させることができるものである。従って、本発明医薬組成物を含有する医薬は、外用剤として有用である。特に貼付剤とした場合、コンプライアンスよく長期間使用可能な経皮吸収型の抗うつ薬又は鎮痛薬として非常に有用性が高いものである。
【図面の簡単な説明】
【0010】
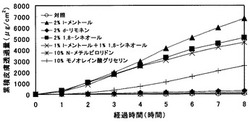
【図1】図1は、実施例1のインビトロ皮膚透過性試験において、ミルナシプランの累積皮膚透過量を経時的に示したグラフである。
【図2】図2は、実施例1のインビトロ皮膚透過性試験において、ミルナシプランの皮膚透過速度を示したグラフである。
【図3】図3は、実施例1のインビトロ皮膚透過性試験において、ミルナシプランの皮膚透過の遅延時間を示したグラフである。
【図4】図4は、実施例2のインビトロ皮膚透過性試験において、ミルナシプラン(MIL)の累積皮膚透過量を経時的に示したグラフである。
【図5】図5は、実施例2のインビトロ皮膚透過性試験において、ミルナシプラン(MIL)の皮膚透過速度を示したグラフである。
【図6】図6は、実施例3のインビボ強制水泳試験において、本発明医薬組成物が無動時間に及ぼす効果を示したグラフである。
【発明を実施するための形態】
【0011】
本発明は、ミルナシプラン又はその薬学的に許容される塩を有効成分とし、吸収促進剤としてメントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せを含有する新規な経皮吸収用医薬組成物又はこれを含有する医薬に関する。
【0012】
本発明医薬組成物又は医薬の有効成分は、ミルナシプラン又はその薬学的に許容される塩である。塩としては、薬学的に許容される酸付加塩であれば特に制限なく使用でき、例えば、塩酸塩、硫酸塩、硝酸塩、リン酸塩、フッ化水素酸塩、臭化水素酸塩等の無機酸塩や酢酸、酒石酸塩、乳酸塩、クエン酸塩、フマール酸塩、マレイン酸塩、メシル酸塩、コハク酸塩、メタンスルホン酸塩、ベンゼンスルホン酸塩、トルエンスルホン酸塩、ナフタレンスルホン酸塩、カンファースルホン酸塩等の有機酸塩を挙げることができる。好ましくは、市販され広く臨床的に用いられているミルナシプラン塩酸塩が挙げられる。また、本願においては、ミルナシプランの水和物や溶媒和物も本発明の有効成分であるミルナシプランに包含される。
【0013】
本発明医薬組成物又は医薬において有効成分として含有されるミルナシプラン又はその薬学的に許容される塩の重量%は、0.1乃至10重量%、好ましくは0.2乃至5重量%とすることができる。
【0014】
本発明医薬組成物で使用されるメントールは、その光学異性体であるl−メントール、dl−メントールを包含する。また、メントールを主成分とするハッカ油やハッカ水も本発明のメントールに包含される。使用されるメントールの量は、後述する剤形などによって異なるが、0.75乃至10重量%、好ましくは1乃至5重量%とすることができる。
【0015】
本発明医薬組成物で使用されるシネオールは、1,8−シネオール、1,8−エポキシ−p−メンタン又はユーカリプトールとも呼称され、シネオールを主成分とするユーカリ精油も本発明のシネオールに包含される。使用されるシネオールの量は、後述する剤形などによって異なるが、0.75乃至10重量%、好ましくは1乃至5重量%とすることができる。
【0016】
本発明医薬組成物においては、上記メントール及びシネオールを組合せて使用することもでき、使用されるメントール及びシネオールの量は、後述する剤形などによって異なるが、合わせて0.75乃至10重量%、好ましくは1乃至5重量%とすることができる。
【0017】
本発明医薬組成物で利用可能なグリセリン脂肪酸エステルとしては、脂肪酸の炭素数が5乃至25であるグリセリン脂肪酸エステル等が挙げられる。より具体的には、カプリル酸グリセリン、カプリン酸グリセリン、ラウリン酸グリセリン、パルミチン酸グリセリン、オレイン酸グリセリン、ステアリン酸グリセリン、ジカプリル酸グリセリン、トリカプリル酸グリセリン等が挙げられ、オレイン酸グリセリンが好ましい。グリセリン脂肪酸エステルの量は、後述する剤形などによって異なるが、2乃至30重量%、好ましくは5乃至20重量%とすることができる。
【0018】
本発明医薬組成物で使用される低級アルコールとしては、メタノール、エタノール、プロパノール、イソプロパノール、ブタノール、イソブタノール、2−ブタノール等の炭素数1乃至4のアルコールが挙げられる。使用される低級アルコールの量は、後述する剤形などによって異なるが、5乃至40重量%、好ましくは10乃至30重量%とすることができる。
【0019】
本発明に係る経皮吸収用医薬組成物を含有する医薬の具体的な剤形としては特に制限はなく、例えば、液剤、クリーム剤、軟膏剤、ゲル剤、ローション剤、スプレー剤、貼付剤、テープ剤等の外用剤として製剤化できる。製剤化に際しては、各剤形に適した添加剤や基剤を適宜使用し、日本薬局方の製剤総則などに記載される通常の方法に従って製造することができる。処方にあたっては、ミルナシプランと共に他の医薬活性成分との配合剤としてもよい。
【0020】
貼付剤の例としては、ヒドロゲルの形態の貼付剤(パップ剤)に製剤化することが挙げられる。ヒドロゲルの作成は、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、カルボキシビニルポリマー等の粘稠剤を用い、水で膨潤させて基剤とするという、通常行われている方法を利用でき、主薬であるミルナシプランや上記吸収促進剤を製剤中に均一に混合させるために、イソプロパノールやエタノール等の適当な溶剤を用いて製剤化することができる。
【0021】
本発明の経皮吸収用医薬組成物及び医薬は、うつ病又は慢性疼痛等で従来経口用ミルナシプランを投与されていた患者に用いることができる。鎮痛剤としては、慢性疼痛の他或いはこれに含まれるものとして、神経因性疼痛、頭痛、偏頭痛、緊張性頭痛、慢性骨盤痛、筋肉痛、関節痛、腰痛、線維筋痛症等の種々の痛みの治療に用いられ得る。また、他にも例えば、ミルナシプランの効果が報告されている腹圧性尿失禁等の疾患の治療にも用いられ得る。
【実施例】
【0022】
以下に、実施例により本発明を具体的に説明するが、本発明はこれらに限定されるものではない。
【0023】
実施例1.吸収促進剤の検討
(1)ミルナシプラン含有ヒドロゲルの作成
吸収促進剤が異なるミルナシプラン含有ヒドロゲルを以下の方法で作成した。なお、以下の本実施例においては、ミルナシプランの塩酸塩を用い、各組成成分の表示重量%は最終の総量(100重量%)に対するものである。
ヒドロキシエチルセルロース及びヒドロキシプロピルセルロースをそれぞれ1重量%となるように水に添加し、さらにミルナシプラン塩酸塩を2重量%となるように加えて一晩放置し基剤を膨潤させた。その後、吸収促進剤として2重量%のl−メントール、2重量%のd−リモネン、2重量%の1,8−シネオール、1重量%のl−メントールと1重量%の1,8−シネオールの組合せ、10重量%のN−メチルピロリドン又は10重量%のモノオレイン酸グリセリンを添加し、さらに20重量%のイソプロピルアルコールを添加して一晩静置して均一なヒドロゲルとした。なお、成分の配合量の増減に伴って使用する水の量を加減し、総量が100重量%となるようにした。さらに、対照として、吸収促進剤を添加しないミルナシプラン含有ヒドロゲルを同様に作成した。
【0024】
(2)インビトロ(in vitro)皮膚透過性試験
7週齢の雄性Hos;HR−1系ヘアレスマウス摘出皮膚(登録商標:ラボスキン、株式会社星野実験動物飼育所)を縦型拡散セル(有効拡散面積:2.01cm2、レシーバーセル体積16.0 mL)に皮膚角質層がドナー側、皮膚基底膜側がレシーバー側となるように装着した。上記のヒドロゲル1.0gをドナーセル内に適用し、レシーバーセルをpH 7.4のリン酸緩衝生理食塩液(PBS)で満たした。レシーバーセルから1時間ごとに0.2mLの溶液を分取して、ミルナシプランを高速液体クロマトグラフィー(HPLC)で定量した。また、分取後直ちに、0.2mLのPBSをレシーバーセルに補充した。HPLCは、移動相がリン酸二水素カリウム−水酸化カリウム緩衝液(pH5.5、イオン強度59mM):メタノール=60:40、カラムがYCM−Pack ODS−A(150mm×44.6mm)、波長が222nm、流速1.0mL/分、カラム温度が室温、注入量が90μLの条件にて実施した。なお、試験は各々3回行い、平均値±標準偏差を求めた。
【0025】
(3)ミルナシプラン皮膚透過性試験の結果
上記のインビトロ皮膚透過性試験により、各々の吸収促進剤を添加したミルナシプラン含有ヒドロゲルからのミルナシプランの単位面積当たりの累積皮膚透過量を経時的に測定した結果(累積透過量−時間曲線のグラフ)を図1に示した。また、上記測定値より求めたミルナシプランの皮膚透過速度(μg/cm2/h)〔皮膚透過速度は累積透過量−時間曲線のプロットを直線回帰して得られた回帰直線の傾きである〕を図2に示した。さらに、この回帰直線より求めた遅延時間〔皮膚透過速度が定常状態に達するまでの時間〕を図3に示した。
【0026】
図1及び図2から明らかなように、吸収促進剤を添加しないミルナシプラン含有組成物(対照)では、ほとんど皮膚透過性が認められなかったが、l−メントール(2重量%)又は1,8−シネオール(2重量%)を含有する組成物では顕著にミルナシプランの皮膚透過性が促進され、モノオレイン酸グリセリン(10重量%)を含有する組成物も、ミルナシプランの皮膚透過性が促進されることが示された。しかし、d−リモネン又はN−メチルピロリドンを含有する組成物では皮膚透過性の促進は認められなかった。特に、d−リモネンはl−メントールや1,8−シネオールと同様にモノテルペン類に属し、化学構造が類似しているにもかかわらず、ミルナシプランの吸収促進作用が認められなかった。このことは、ミルナシプランという薬物とこれに適した吸収促進剤の組合せが経皮吸収促進に重要であることを示すものである。
【0027】
また、l−メントール及び1,8−シネオールをそれぞれ1重量%ずつ含有する組成物では、l−メントール又は1,8−シネオールを各2重量%含有する組成物と同等にミルナシプランの皮膚透過性が促進された(図2)。なお、図3から明らかなように、l−メントール及び1,8−シネオールをそれぞれ1重量%ずつ配合した組成物では、l−メントール又は1,8−シネオールを2重量%含有する組成物よりもミルナシプランの皮膚透過遅延時間を短縮する効果が認められた。遅延時間が短い方が薬物の効果が現れるまでの時間が早くなることで、組成物として好ましい性質となり得る。
【0028】
実施例2.ミルナシプランの用量検討
(1)ミルナシプラン含有ヒドロゲルの作成
表1に示す処方のヒドロゲルを次の方法で作成した。すなわち、ミルナシプラン、ヒドロキシプロピルセルロース及びヒドロキシエチルセルロースに水を添加して一晩放置し基剤を膨潤させた。その後、イソプロピルアルコール(及びl−メントール)を添加して一晩静置して均一なヒドロゲルとした。なお、ミルナシプランとその他の成分の配合量の増減に伴って使用する水の量を加減し、総量が100重量%となるようにした。
【0029】
【表1】

【0030】
(2)ミルナシプラン皮膚透過性試験の結果
全組成物の重量を100重量%としたときのミルナシプランの添加量を1、2又は3重量%に設定し、l−メントールを添加しない場合と2重量%のl−メントールを添加した場合のミルナシプラン皮膚透過性を比較した。実施例1のインビトロ皮膚透過性試験と同様に、単位面積当たりのミルナシプランの累積皮膚透過量を経時的に測定した累積透過量−時間曲線のグラフを図4に示した。また、上記測定値より求めたミルナシプランの皮膚透過速度(μg/cm2/h)を図5に示した。図4及び図5から明らかなように、l−メントールを含有しない処方ではミルナシプランの濃度(用量)にかかわらず、ミルナシプランがほとんど皮膚透過しなかった。他方、l−メントールを含有する組成物では、時間の経過と共にミルナシプランの皮膚透過量の上昇が認められた(図4)。また、図5に示したとおり、同じミルナシプラン含有量(1%、2%及び3%)の組成物で比較した場合、l−メントール添加によりミルナシプランの皮膚透過性が有意に促進された(n=3、***P<0.001)。さらに、l−メントールを2重量%含有する各組成物では、1重量%のミルナシプランと比較したとき、ミルナシプランの濃度(用量)に依存して線形的に促進された(n=3、**P<0.01、***P<0.001)。これにより、ミルナシプランの含量を調整することにより、皮膚吸収速度を調整することが可能であることが示された。
【0031】
実施例3.インビボ(in vivo)強制水泳試験
ミルナシプランが皮膚を経由して生体内に送達されて薬理効果を発揮することを確認するため、下記の強制水泳試験を行った。なお、試験は各々5回行い、平均値±標準誤差を求めた。
【0032】
直径9.5cmのガラスシリンダーを適量の水で満たし、25℃水浴下で保温した。その後、ガラスシリンダー内で7週齢の雄性C57BL/6Jマウス(東京実験動物株式会社)を10分間強制水泳によるストレス負荷を行った。ストレス負荷12時間後に実施例1のミルナシプラン含有ヒドロゲルをマウス背部徐毛部に12時間適用した(有効拡散面積;0.16cm2)。12時間後、マウス背部よりヒドロゲルを除去し、再びガラスシリンダー内にて6分間の強制水泳を行った。このとき、終わり5分間のマウスの無動時間を測定し、無動時間の低下をミルナシプランの抗うつ作用として評価した。また、陽性対照として、ミルナシプラン60mg/kgを腹腔内(i.p.)投与したマウスにて同様に試験した。
【0033】
その結果を図6に示した。発症対照に対してミルナシプランを腹腔内投与した陽性対照の無動時間は有意に低下した(n=5、**P<0.01)。l−メントールを含まないヒドロゲルを適用した場合、ミルナシプランによる有意な効果は認められなかった。これに対して2重量%l−メントールを添加した各組成物では、2又は3重量%のミルナシプランを添加した本発明組成物の場合、l−メントールを添加しないものに比べて、ミルナシプランによる用量依存的な無動時間の低下が有意に認められ、陽性対照と同等の抗うつ作用が認められた(n=5、**P<0.01)。また、2重量%l−メントールを添加した組成物においては、ミルナシプランを添加しない組成物と比較して、2又は3重量%のミルナシプランを添加した本発明医薬組成物では、それぞれ有意な無動時間の低下が認められ(n=5、*P<0.05)、この無動時間の低下はミルナシプランの皮膚透過による薬効発現であることが示された。
【産業上の利用可能性】
【0034】
上記薬理試験の結果から明らかなように、適切な吸収促進剤を含有させることにより、ミルナシプランの経皮吸収性を促進し、顕著な薬理効果を発現させることが可能となった。吸収促進剤としては、メントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せが可能であり、メントール及びシネオールの組合せが好ましい。また、本発明医薬組成物においては、イソプロパノール又はエタノール等の低級アルコールをさらに添加することにより、より経皮吸収の優れた医薬製剤とすることが可能である。本発明医薬組成物含有する医薬は、うつ病治療薬として広く臨床で使用され、また鎮痛剤としての有用性も認められているミルナシプランを有効成分とするものであり、経皮吸収性に優れ、コンプライアンスよく長期間使用可能な経皮吸収型の抗うつ剤及び鎮痛剤として非常に有用性が高いものである。
【技術分野】
【0001】
本発明はミルナシプラン又はその薬学的に許容される塩を有効成分として含有する経皮吸収用医薬組成物又はこの組成物を含有する医薬に関する。
【背景技術】
【0002】
うつ病は、気分障害の一種であり、抑うつ気分(不安、焦燥など)、意欲の低下(無気力、億劫など)、精神活動の低下(考えがまとまらないなど)、各種の身体症状(不眠、易疲労感、頭重・頭痛、食欲不振など)を呈する精神疾患である。うつ病は、近年罹患者が増大しており、重症化すると日常生活に支障をきたし、自殺企図など生命に係ることもあることから、社会的にも重要な疾患である。そこで、その発症機序の解明が望まれているが、うつ病の発症には精神的な要因と脳神経科学的な要因が複雑に絡んでいると考えられ、十分な解明には至っていない。このうつ病の治療は、現在、薬物療法(抗うつ剤)と心理学的なケアを組み合わせて行われている。抗うつ剤としては、イミプラミンやアミトリプチリンなどの三環系抗うつ剤(第1世代)が先ず開発され使用されてきた。しかし、三環系抗うつ剤は、シナプス後部のヒスタミンH1受容体、アセチルコリン性ムスカリンM1受容体、アドレナリン性α1受容体なども遮断するため、抗コリン作用による便秘や排尿障害などの副作用が多かった。また、大量服用では致死的になるという問題があった。そこで、より副作用の少ない四環系抗うつ剤(第2世代)が開発されたが、抗うつ効果に物足りなさがあり、抗コリン作用もまだ残っていた。1980年代に、さらに抗コリン作用による副作用の少ないセロトニン選択的再取り込み阻害剤(SSRI)(第3世代)が開発されたが、SSRIは脳内や腸管のセロトニン受容体に対する刺激作用による吐気や嘔吐、服薬中断による離脱症候群などの新たな副作用を生じさせた。その後、1990年代になって、選択的セロトニン・ノルアドレナリン再取り込み阻害剤(SNRI)が開発され、胃腸症状はなお残るものの、抗コリン作用のない薬剤として、広く臨床現場で使用されている。
【0003】
うつ病の薬物療法では血中の薬剤濃度を有効濃度で一定に維持することが、副作用を低減して患者への治療効果を最大限もたらすために重要である。しかし、うつ病の治療では、服薬が長期にわたることやうつ症状が寛解・増悪を繰り返すため、うつ病の治療に一般的に使用されている経口剤を患者がコンプライアンス(医師から処方された薬剤を患者が指示通りに使用すること)よく服薬することが困難で、飲み忘れによる症状の悪化や過剰摂取による副作用を起こすことがある。特に、SSRIは1日1回の服用でよい製剤があるが、SNRIとして汎用されているミルナシプランは1日2〜3回服用する必要があり、さらにコンプライアンスよく服薬することが困難であった。
このような経口剤に対し、薬剤を経皮吸収させて投与する経皮剤は、薬剤が持続的に徐々に皮膚から吸収されるため、経口剤に比べて、有効血中濃度を持続的に維持することが可能である。その結果、特に1日2回以上服用する必要のあった薬剤を1日1回使用すればよい製剤にすることが可能となり、コンプライアンスが改善され得る。加えて、経皮剤の場合、最高血中濃度を低下させることができることから、副作用を回避し易くなる。また、経皮投与は、肝臓での薬剤の代謝による初回通過効果を回避できることから、経口投与より少量の薬剤で血中有効用量を維持できる可能性がある。さらに、薬剤を支持基材に塗布して貼付剤とした場合には、患者が薬剤を使用していることを患者のみならず、医師や看護師、家族などが容易に確認でき、副作用発生時にも貼付剤を剥すことによって以降の薬剤吸収を容易に中止できるメリットがある。従って、経皮剤は患者のコンプライアンス及びクオリティー・オブ・ライフ(QOL)の改善に非常に有用である。しかし、薬剤の種類によっては経皮吸収され難いものもあり、適切な経皮吸収製剤になり得る処方を見出すことが困難な場合も多い。
【0004】
ミルナシプラン〔(±)−シス−2−(アミノメチル)−N,N−ジエチル−1−フェニルシクロプロパンカルボキサミド〕は代表的なSNRIの一つで、脳内神経接合部においてセロトニンとノルアドレナリンの再取り込みを選択的に阻害することにより抗うつ作用を発揮することが知られている第4世代の抗うつ剤である。ミルナシプランは、三環系や四環系抗うつ剤のように神経伝達物質の受容体に結合しないことから抗コリン作用による副作用がなく、また、第3世代の抗うつ剤であるSSRIのように脳内や腸管でセロトニン受容体を刺激することによる吐気や嘔吐の副作用も少ない。効果的にも、セロトニンに加えてノルアドレナリンの再取り込みも阻害することから、セロトニンの再取り込みを選択的に阻害するSSRIより強い抗うつ作用を発揮し、特にSSRIではあまり効果のない意欲にも効果を有する。また、ミルナシプランは、抗うつ作用のみならず疼痛にも有効であり、神経因性疼痛、線維筋痛症、緊張型頭痛等に対する治療効果が報告されている。
なお、本発明において、便宜的にミルナシプランという場合でも、ミルナシプラン塩酸塩を指すことがある。
【0005】
ミルナシプランの経皮吸収剤に関しては、特許文献1の報告がある。しかしながら、これはミルナシプランの経粘膜投与剤に関すものであり、具体的にはミルナシプランの鼻腔内投与用の製剤を開示するのみのものである。粘膜が比較的薬物を透過しやすい組織であるのに対し、皮膚上皮は強力な薬物の透過阻止機能を有する。従って、経皮投与用製剤では、薬剤を経皮吸収させるための、より強力な吸収促進作用を有する処方を見出すことが必要となる。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】国際公開WO2007/086493号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明の目的は、有効成分であるミルナシプラン又はその薬学的に許容される塩の皮膚透過性を亢進させ、優れた薬理効果を発揮させるための、新規な経皮吸収用医薬組成物又はこれを含有する医薬を提供することにある。
【課題を解決するための手段】
【0008】
本発明者らは、経皮吸収が困難なミルナシプラン又はその薬学的に許容される塩の経皮吸収性を向上させることにより、経皮吸収剤として優れた薬理効果を発揮させるための製剤化について鋭意検討を行った。その結果、ミルナシプランに吸収促進剤としてメントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せを配合することにより、ミルナシプランの経皮吸収性が顕著に亢進されることを見出し、本発明を完成した。
【発明の効果】
【0009】
本発明医薬組成物は、ミルナシプラン又はその薬学的に許容される塩を経皮吸収により効果を発揮させることができるものである。従って、本発明医薬組成物を含有する医薬は、外用剤として有用である。特に貼付剤とした場合、コンプライアンスよく長期間使用可能な経皮吸収型の抗うつ薬又は鎮痛薬として非常に有用性が高いものである。
【図面の簡単な説明】
【0010】
【図1】図1は、実施例1のインビトロ皮膚透過性試験において、ミルナシプランの累積皮膚透過量を経時的に示したグラフである。
【図2】図2は、実施例1のインビトロ皮膚透過性試験において、ミルナシプランの皮膚透過速度を示したグラフである。
【図3】図3は、実施例1のインビトロ皮膚透過性試験において、ミルナシプランの皮膚透過の遅延時間を示したグラフである。
【図4】図4は、実施例2のインビトロ皮膚透過性試験において、ミルナシプラン(MIL)の累積皮膚透過量を経時的に示したグラフである。
【図5】図5は、実施例2のインビトロ皮膚透過性試験において、ミルナシプラン(MIL)の皮膚透過速度を示したグラフである。
【図6】図6は、実施例3のインビボ強制水泳試験において、本発明医薬組成物が無動時間に及ぼす効果を示したグラフである。
【発明を実施するための形態】
【0011】
本発明は、ミルナシプラン又はその薬学的に許容される塩を有効成分とし、吸収促進剤としてメントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せを含有する新規な経皮吸収用医薬組成物又はこれを含有する医薬に関する。
【0012】
本発明医薬組成物又は医薬の有効成分は、ミルナシプラン又はその薬学的に許容される塩である。塩としては、薬学的に許容される酸付加塩であれば特に制限なく使用でき、例えば、塩酸塩、硫酸塩、硝酸塩、リン酸塩、フッ化水素酸塩、臭化水素酸塩等の無機酸塩や酢酸、酒石酸塩、乳酸塩、クエン酸塩、フマール酸塩、マレイン酸塩、メシル酸塩、コハク酸塩、メタンスルホン酸塩、ベンゼンスルホン酸塩、トルエンスルホン酸塩、ナフタレンスルホン酸塩、カンファースルホン酸塩等の有機酸塩を挙げることができる。好ましくは、市販され広く臨床的に用いられているミルナシプラン塩酸塩が挙げられる。また、本願においては、ミルナシプランの水和物や溶媒和物も本発明の有効成分であるミルナシプランに包含される。
【0013】
本発明医薬組成物又は医薬において有効成分として含有されるミルナシプラン又はその薬学的に許容される塩の重量%は、0.1乃至10重量%、好ましくは0.2乃至5重量%とすることができる。
【0014】
本発明医薬組成物で使用されるメントールは、その光学異性体であるl−メントール、dl−メントールを包含する。また、メントールを主成分とするハッカ油やハッカ水も本発明のメントールに包含される。使用されるメントールの量は、後述する剤形などによって異なるが、0.75乃至10重量%、好ましくは1乃至5重量%とすることができる。
【0015】
本発明医薬組成物で使用されるシネオールは、1,8−シネオール、1,8−エポキシ−p−メンタン又はユーカリプトールとも呼称され、シネオールを主成分とするユーカリ精油も本発明のシネオールに包含される。使用されるシネオールの量は、後述する剤形などによって異なるが、0.75乃至10重量%、好ましくは1乃至5重量%とすることができる。
【0016】
本発明医薬組成物においては、上記メントール及びシネオールを組合せて使用することもでき、使用されるメントール及びシネオールの量は、後述する剤形などによって異なるが、合わせて0.75乃至10重量%、好ましくは1乃至5重量%とすることができる。
【0017】
本発明医薬組成物で利用可能なグリセリン脂肪酸エステルとしては、脂肪酸の炭素数が5乃至25であるグリセリン脂肪酸エステル等が挙げられる。より具体的には、カプリル酸グリセリン、カプリン酸グリセリン、ラウリン酸グリセリン、パルミチン酸グリセリン、オレイン酸グリセリン、ステアリン酸グリセリン、ジカプリル酸グリセリン、トリカプリル酸グリセリン等が挙げられ、オレイン酸グリセリンが好ましい。グリセリン脂肪酸エステルの量は、後述する剤形などによって異なるが、2乃至30重量%、好ましくは5乃至20重量%とすることができる。
【0018】
本発明医薬組成物で使用される低級アルコールとしては、メタノール、エタノール、プロパノール、イソプロパノール、ブタノール、イソブタノール、2−ブタノール等の炭素数1乃至4のアルコールが挙げられる。使用される低級アルコールの量は、後述する剤形などによって異なるが、5乃至40重量%、好ましくは10乃至30重量%とすることができる。
【0019】
本発明に係る経皮吸収用医薬組成物を含有する医薬の具体的な剤形としては特に制限はなく、例えば、液剤、クリーム剤、軟膏剤、ゲル剤、ローション剤、スプレー剤、貼付剤、テープ剤等の外用剤として製剤化できる。製剤化に際しては、各剤形に適した添加剤や基剤を適宜使用し、日本薬局方の製剤総則などに記載される通常の方法に従って製造することができる。処方にあたっては、ミルナシプランと共に他の医薬活性成分との配合剤としてもよい。
【0020】
貼付剤の例としては、ヒドロゲルの形態の貼付剤(パップ剤)に製剤化することが挙げられる。ヒドロゲルの作成は、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、カルボキシビニルポリマー等の粘稠剤を用い、水で膨潤させて基剤とするという、通常行われている方法を利用でき、主薬であるミルナシプランや上記吸収促進剤を製剤中に均一に混合させるために、イソプロパノールやエタノール等の適当な溶剤を用いて製剤化することができる。
【0021】
本発明の経皮吸収用医薬組成物及び医薬は、うつ病又は慢性疼痛等で従来経口用ミルナシプランを投与されていた患者に用いることができる。鎮痛剤としては、慢性疼痛の他或いはこれに含まれるものとして、神経因性疼痛、頭痛、偏頭痛、緊張性頭痛、慢性骨盤痛、筋肉痛、関節痛、腰痛、線維筋痛症等の種々の痛みの治療に用いられ得る。また、他にも例えば、ミルナシプランの効果が報告されている腹圧性尿失禁等の疾患の治療にも用いられ得る。
【実施例】
【0022】
以下に、実施例により本発明を具体的に説明するが、本発明はこれらに限定されるものではない。
【0023】
実施例1.吸収促進剤の検討
(1)ミルナシプラン含有ヒドロゲルの作成
吸収促進剤が異なるミルナシプラン含有ヒドロゲルを以下の方法で作成した。なお、以下の本実施例においては、ミルナシプランの塩酸塩を用い、各組成成分の表示重量%は最終の総量(100重量%)に対するものである。
ヒドロキシエチルセルロース及びヒドロキシプロピルセルロースをそれぞれ1重量%となるように水に添加し、さらにミルナシプラン塩酸塩を2重量%となるように加えて一晩放置し基剤を膨潤させた。その後、吸収促進剤として2重量%のl−メントール、2重量%のd−リモネン、2重量%の1,8−シネオール、1重量%のl−メントールと1重量%の1,8−シネオールの組合せ、10重量%のN−メチルピロリドン又は10重量%のモノオレイン酸グリセリンを添加し、さらに20重量%のイソプロピルアルコールを添加して一晩静置して均一なヒドロゲルとした。なお、成分の配合量の増減に伴って使用する水の量を加減し、総量が100重量%となるようにした。さらに、対照として、吸収促進剤を添加しないミルナシプラン含有ヒドロゲルを同様に作成した。
【0024】
(2)インビトロ(in vitro)皮膚透過性試験
7週齢の雄性Hos;HR−1系ヘアレスマウス摘出皮膚(登録商標:ラボスキン、株式会社星野実験動物飼育所)を縦型拡散セル(有効拡散面積:2.01cm2、レシーバーセル体積16.0 mL)に皮膚角質層がドナー側、皮膚基底膜側がレシーバー側となるように装着した。上記のヒドロゲル1.0gをドナーセル内に適用し、レシーバーセルをpH 7.4のリン酸緩衝生理食塩液(PBS)で満たした。レシーバーセルから1時間ごとに0.2mLの溶液を分取して、ミルナシプランを高速液体クロマトグラフィー(HPLC)で定量した。また、分取後直ちに、0.2mLのPBSをレシーバーセルに補充した。HPLCは、移動相がリン酸二水素カリウム−水酸化カリウム緩衝液(pH5.5、イオン強度59mM):メタノール=60:40、カラムがYCM−Pack ODS−A(150mm×44.6mm)、波長が222nm、流速1.0mL/分、カラム温度が室温、注入量が90μLの条件にて実施した。なお、試験は各々3回行い、平均値±標準偏差を求めた。
【0025】
(3)ミルナシプラン皮膚透過性試験の結果
上記のインビトロ皮膚透過性試験により、各々の吸収促進剤を添加したミルナシプラン含有ヒドロゲルからのミルナシプランの単位面積当たりの累積皮膚透過量を経時的に測定した結果(累積透過量−時間曲線のグラフ)を図1に示した。また、上記測定値より求めたミルナシプランの皮膚透過速度(μg/cm2/h)〔皮膚透過速度は累積透過量−時間曲線のプロットを直線回帰して得られた回帰直線の傾きである〕を図2に示した。さらに、この回帰直線より求めた遅延時間〔皮膚透過速度が定常状態に達するまでの時間〕を図3に示した。
【0026】
図1及び図2から明らかなように、吸収促進剤を添加しないミルナシプラン含有組成物(対照)では、ほとんど皮膚透過性が認められなかったが、l−メントール(2重量%)又は1,8−シネオール(2重量%)を含有する組成物では顕著にミルナシプランの皮膚透過性が促進され、モノオレイン酸グリセリン(10重量%)を含有する組成物も、ミルナシプランの皮膚透過性が促進されることが示された。しかし、d−リモネン又はN−メチルピロリドンを含有する組成物では皮膚透過性の促進は認められなかった。特に、d−リモネンはl−メントールや1,8−シネオールと同様にモノテルペン類に属し、化学構造が類似しているにもかかわらず、ミルナシプランの吸収促進作用が認められなかった。このことは、ミルナシプランという薬物とこれに適した吸収促進剤の組合せが経皮吸収促進に重要であることを示すものである。
【0027】
また、l−メントール及び1,8−シネオールをそれぞれ1重量%ずつ含有する組成物では、l−メントール又は1,8−シネオールを各2重量%含有する組成物と同等にミルナシプランの皮膚透過性が促進された(図2)。なお、図3から明らかなように、l−メントール及び1,8−シネオールをそれぞれ1重量%ずつ配合した組成物では、l−メントール又は1,8−シネオールを2重量%含有する組成物よりもミルナシプランの皮膚透過遅延時間を短縮する効果が認められた。遅延時間が短い方が薬物の効果が現れるまでの時間が早くなることで、組成物として好ましい性質となり得る。
【0028】
実施例2.ミルナシプランの用量検討
(1)ミルナシプラン含有ヒドロゲルの作成
表1に示す処方のヒドロゲルを次の方法で作成した。すなわち、ミルナシプラン、ヒドロキシプロピルセルロース及びヒドロキシエチルセルロースに水を添加して一晩放置し基剤を膨潤させた。その後、イソプロピルアルコール(及びl−メントール)を添加して一晩静置して均一なヒドロゲルとした。なお、ミルナシプランとその他の成分の配合量の増減に伴って使用する水の量を加減し、総量が100重量%となるようにした。
【0029】
【表1】

【0030】
(2)ミルナシプラン皮膚透過性試験の結果
全組成物の重量を100重量%としたときのミルナシプランの添加量を1、2又は3重量%に設定し、l−メントールを添加しない場合と2重量%のl−メントールを添加した場合のミルナシプラン皮膚透過性を比較した。実施例1のインビトロ皮膚透過性試験と同様に、単位面積当たりのミルナシプランの累積皮膚透過量を経時的に測定した累積透過量−時間曲線のグラフを図4に示した。また、上記測定値より求めたミルナシプランの皮膚透過速度(μg/cm2/h)を図5に示した。図4及び図5から明らかなように、l−メントールを含有しない処方ではミルナシプランの濃度(用量)にかかわらず、ミルナシプランがほとんど皮膚透過しなかった。他方、l−メントールを含有する組成物では、時間の経過と共にミルナシプランの皮膚透過量の上昇が認められた(図4)。また、図5に示したとおり、同じミルナシプラン含有量(1%、2%及び3%)の組成物で比較した場合、l−メントール添加によりミルナシプランの皮膚透過性が有意に促進された(n=3、***P<0.001)。さらに、l−メントールを2重量%含有する各組成物では、1重量%のミルナシプランと比較したとき、ミルナシプランの濃度(用量)に依存して線形的に促進された(n=3、**P<0.01、***P<0.001)。これにより、ミルナシプランの含量を調整することにより、皮膚吸収速度を調整することが可能であることが示された。
【0031】
実施例3.インビボ(in vivo)強制水泳試験
ミルナシプランが皮膚を経由して生体内に送達されて薬理効果を発揮することを確認するため、下記の強制水泳試験を行った。なお、試験は各々5回行い、平均値±標準誤差を求めた。
【0032】
直径9.5cmのガラスシリンダーを適量の水で満たし、25℃水浴下で保温した。その後、ガラスシリンダー内で7週齢の雄性C57BL/6Jマウス(東京実験動物株式会社)を10分間強制水泳によるストレス負荷を行った。ストレス負荷12時間後に実施例1のミルナシプラン含有ヒドロゲルをマウス背部徐毛部に12時間適用した(有効拡散面積;0.16cm2)。12時間後、マウス背部よりヒドロゲルを除去し、再びガラスシリンダー内にて6分間の強制水泳を行った。このとき、終わり5分間のマウスの無動時間を測定し、無動時間の低下をミルナシプランの抗うつ作用として評価した。また、陽性対照として、ミルナシプラン60mg/kgを腹腔内(i.p.)投与したマウスにて同様に試験した。
【0033】
その結果を図6に示した。発症対照に対してミルナシプランを腹腔内投与した陽性対照の無動時間は有意に低下した(n=5、**P<0.01)。l−メントールを含まないヒドロゲルを適用した場合、ミルナシプランによる有意な効果は認められなかった。これに対して2重量%l−メントールを添加した各組成物では、2又は3重量%のミルナシプランを添加した本発明組成物の場合、l−メントールを添加しないものに比べて、ミルナシプランによる用量依存的な無動時間の低下が有意に認められ、陽性対照と同等の抗うつ作用が認められた(n=5、**P<0.01)。また、2重量%l−メントールを添加した組成物においては、ミルナシプランを添加しない組成物と比較して、2又は3重量%のミルナシプランを添加した本発明医薬組成物では、それぞれ有意な無動時間の低下が認められ(n=5、*P<0.05)、この無動時間の低下はミルナシプランの皮膚透過による薬効発現であることが示された。
【産業上の利用可能性】
【0034】
上記薬理試験の結果から明らかなように、適切な吸収促進剤を含有させることにより、ミルナシプランの経皮吸収性を促進し、顕著な薬理効果を発現させることが可能となった。吸収促進剤としては、メントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せが可能であり、メントール及びシネオールの組合せが好ましい。また、本発明医薬組成物においては、イソプロパノール又はエタノール等の低級アルコールをさらに添加することにより、より経皮吸収の優れた医薬製剤とすることが可能である。本発明医薬組成物含有する医薬は、うつ病治療薬として広く臨床で使用され、また鎮痛剤としての有用性も認められているミルナシプランを有効成分とするものであり、経皮吸収性に優れ、コンプライアンスよく長期間使用可能な経皮吸収型の抗うつ剤及び鎮痛剤として非常に有用性が高いものである。
【特許請求の範囲】
【請求項1】
ミルナシプラン又はその薬学的に許容される塩を有効成分とし、吸収促進剤としてメントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せを含有する経皮吸収用医薬組成物。
【請求項2】
吸収促進剤がメントールである請求項1記載の組成物。
【請求項3】
吸収促進剤がl−メントールである請求項2記載の組成物。
【請求項4】
吸収促進剤がシネオールである請求項1記載の組成物。
【請求項5】
吸収促進剤がメントール及びシネオールの組合せである請求項1記載の組成物。
【請求項6】
吸収促進剤がl−メントール及び1,8−シネオールである請求項5記載の組成物。
【請求項7】
吸収促進剤の含有量が0.75乃至10重量%である請求項1乃至6のいずれか一項記載の組成物。
【請求項8】
吸収促進剤がグリセリン脂肪酸エステルである請求項1記載の組成物。
【請求項9】
吸収促進剤がモノオレイン酸グリセリンである請求項8記載の組成物。
【請求項10】
吸収促進剤の含有量が2乃至30重量%である請求項8又は9記載の組成物。
【請求項11】
有効成分がミルナシプラン塩酸塩である請求項1乃至10のいずれか一項記載の組成物。
【請求項12】
さらに低級アルコールを含有する請求項1乃至11のいずれか一項記載の組成物。
【請求項13】
低級アルコールがイソプロパノールである請求項12記載の組成物。
【請求項14】
低級アルコールの含有量が5乃至40重量%である請求項12又は13記載の組成物。
【請求項15】
ヒドロゲルの形態である請求項1乃至14のいずれか一項に記載の組成物。
【請求項16】
請求項1乃至14のいずれか一項に記載の組成物を含有する医薬。
【請求項17】
抗うつ剤である請求項16に記載の医薬。
【請求項18】
鎮痛剤である請求項16に記載の医薬。
【請求項19】
鎮痛剤が慢性疼痛、神経因性疼痛、頭痛、偏頭痛、緊張性頭痛、慢性骨盤痛、筋肉痛、関節痛、腰痛又は線維筋痛症の治療又は予防剤である請求項18記載の医薬。
【請求項20】
貼付剤の形態である請求項乃至16乃至19のいずれか一項に記載の医薬。
【請求項1】
ミルナシプラン又はその薬学的に許容される塩を有効成分とし、吸収促進剤としてメントール、シネオール又はグリセリン脂肪酸エステル或いはそれらのうちの2種以上の組合せを含有する経皮吸収用医薬組成物。
【請求項2】
吸収促進剤がメントールである請求項1記載の組成物。
【請求項3】
吸収促進剤がl−メントールである請求項2記載の組成物。
【請求項4】
吸収促進剤がシネオールである請求項1記載の組成物。
【請求項5】
吸収促進剤がメントール及びシネオールの組合せである請求項1記載の組成物。
【請求項6】
吸収促進剤がl−メントール及び1,8−シネオールである請求項5記載の組成物。
【請求項7】
吸収促進剤の含有量が0.75乃至10重量%である請求項1乃至6のいずれか一項記載の組成物。
【請求項8】
吸収促進剤がグリセリン脂肪酸エステルである請求項1記載の組成物。
【請求項9】
吸収促進剤がモノオレイン酸グリセリンである請求項8記載の組成物。
【請求項10】
吸収促進剤の含有量が2乃至30重量%である請求項8又は9記載の組成物。
【請求項11】
有効成分がミルナシプラン塩酸塩である請求項1乃至10のいずれか一項記載の組成物。
【請求項12】
さらに低級アルコールを含有する請求項1乃至11のいずれか一項記載の組成物。
【請求項13】
低級アルコールがイソプロパノールである請求項12記載の組成物。
【請求項14】
低級アルコールの含有量が5乃至40重量%である請求項12又は13記載の組成物。
【請求項15】
ヒドロゲルの形態である請求項1乃至14のいずれか一項に記載の組成物。
【請求項16】
請求項1乃至14のいずれか一項に記載の組成物を含有する医薬。
【請求項17】
抗うつ剤である請求項16に記載の医薬。
【請求項18】
鎮痛剤である請求項16に記載の医薬。
【請求項19】
鎮痛剤が慢性疼痛、神経因性疼痛、頭痛、偏頭痛、緊張性頭痛、慢性骨盤痛、筋肉痛、関節痛、腰痛又は線維筋痛症の治療又は予防剤である請求項18記載の医薬。
【請求項20】
貼付剤の形態である請求項乃至16乃至19のいずれか一項に記載の医薬。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2012−193176(P2012−193176A)
【公開日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願番号】特願2012−45291(P2012−45291)
【出願日】平成24年3月1日(2012.3.1)
【出願人】(000231796)日本臓器製薬株式会社 (23)
【Fターム(参考)】
【公開日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願日】平成24年3月1日(2012.3.1)
【出願人】(000231796)日本臓器製薬株式会社 (23)
【Fターム(参考)】
[ Back to top ]

