リアルタイム連続検出装置
【課題】一定量の可逆反応性の捕獲認識成分を連続的にリサイクルして、分析物質の濃度変化をリアルタイムに測定することができ、リアルタイム連続検出装置は、生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質や国防化生放測定物質などを検出、又は分析するのに活用可能なため、医療、公衆衛生、国防、環境、食品、獣医、バイオテクノロジー産業に応用することができる。
【解決手段】試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含む、リアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分及び試料内の分析物質−捕獲認識成分の結合体から発生した信号を探知するセンサーを含む分析物質のリアルタイム連続検出装置に関する。
【解決手段】試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含む、リアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分及び試料内の分析物質−捕獲認識成分の結合体から発生した信号を探知するセンサーを含む分析物質のリアルタイム連続検出装置に関する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、リアルタイム連続検出装置に関し、より具体的に、試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含む、リアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分及び試料内の分析物質−捕獲認識成分の結合体から発生した信号を探知するセンサーを含むことを特徴とする、分析物質のリアルタイム連続検出装置に関する。
【背景技術】
【0002】
保健医療分野だけでなく、食品、環境、獣医、国防といった様々な分野において、構造が複雑な有機物質、特に蛋白質、ホルモン、核酸、細胞などの探知に、抗原−抗体付着と核酸接合のような独特の認識反応を用いた分析方法が使用されている。これは、生体認識反応の高い特異性と親和力、そして分析原理の普遍性に起因し、これを応用して様々な形態の解析システムが開発されてきた。
【0003】
その例として、免疫分析システムの開発動向を見ると、マイクロタイタープレート(microtiter plate)を固定化マトリックスとして使用する固相免疫分析(例えば、enzyme−linked immunosorbent immunoassays;ELISA)方法の開発により様々な診断や分析分野に応用するきっかけとなっている(非特許文献1及び非特許文献2参照)。また、細孔性メンブレイン基板の無試薬属性診断キットの発売は、家庭などの場所で制限なく、免疫分析を可能にした(非特許文献3、非特許文献4、非特許文献5、非特許文献6、及び非特許文献7参照)。
【0004】
一方で、病院の臨床試験室など、専門機関で精密検査に使用する自動化診断機器が普及されており、核酸配列を決定したり、タンパク質の発現の程度を定量的に分析できるバイオセンサーアレイチップ、そして、更には、微細自動分析のために、試料の前処理など、順次連続プロセスを行うラップオンアチップの開発が盛んに研究されている(非特許文献8参照)。実用化の例として、CombiMatrix社(米国)のジノミックス研究用Custom Array、Nanosphere社(米国)の単一核酸変異(SNP)測定用のVerigene ID platform、AffyMetrix社(米国)のGeneChip System、Integrated NanoTechnologies社(米国)の現場分析用のBioDetect Test Cardなどが紹介されている。
【0005】
近年、ナノテクノロジーとバイオテクノロジーの技術が融合したナノバイオセンサー技術が、21世紀の最先端技術として脚光を浴びており、これに関連する源泉技術を確保しようと、国内を含む全世界的に研究が盛んに進められている。複数の機関でバイオセンサーの超高感度技術の開発に集中しているが、その技術水準がまだ初歩段階にあるナノセンサーの概念(非特許文献9及び非特許文献10参照)、及び振動型カンチレバー基板の免疫分析(非特許文献11参照)などが報告されている。
【0006】
このような、ほとんどの既存の分析システムに使用される抗体をはじめとする認識成分は、分析物質−認識成分の結合後、その結合体を分離するために、洗浄工程が不可欠である。この場合に形成された結合体の損失を最小化するために、脱着速度が非常に遅い認識成分を使用しなければならないので、一度結合した分析物質が認識成分から解離されず、ほとんどのセンサーを連続的に使用できずに、使い捨て用のみに使用する。
【0007】
最近になって、グルコースモニタリングにおいて、無侵襲センシング方法に対する研究が非常に盛んである(非特許文献12参照)。特に、病院の重症患者の病気に関連する指標物質に対する連続的な測定への要求が高まっているが、技術的な問題から要求を満たしていない。しかし、分析物質−認識成分間の反応を可逆的に運用できる場合、様々な疾患に対して、リアルタイムの連続モニタリングが可能になる。
【0008】
分析物質に対する連続測定が可能な場合、将来的には、人体に着用したり、体内の移植が可能なバイオセンサーを開発することができる。これらのセンサーを使用すると、生体情報を連続的に測定し、診断することにより、疾患が発生する確率が相対的に高い高危険群(慢性疾患者、高齢者など)の患者に対して、感染症や成人病などの好発疾患を早期に管理乃至監視することが可能になる。
したがって、これらの分析道具は、ユビキタスコンピューティング環境を基に、「いつ」、「どこでも」医療サービスを提供するヘルスケア環境を意味するU−ヘルスケアの時代で、将来の予防医療のための必須道具になると判断される(非特許文献13参照)。このようなU−ヘルスケアが実現されれば、病気の後に対応する「病院/治療中心」の既存のパラダイムから脱皮できるだけでなく、慢性疾患者や高齢者などが長期入院をする必要はない。
【先行技術文献】
【非特許文献】
【0009】
【非特許文献1】Irina Ionescu−Matiu等,J Virol Methods,Vol.6(1)、Page41-52,1983
【非特許文献2】Christopher Heeschen等、Clinical chemistry、Vol.45(10),Page 1789-1796,1999
【非特許文献3】R.Chen等,1987,Clin.Chem.Vol.33,Page 1521-1525
【非特許文献4】MPA Laitinen, 1996, Biosens.Bioelectron., Vol.11, 1207-1214
【非特許文献5】S.C.Lou等,1993,Clin.Chem.,Vol.39,619-624
【非特許文献6】S.H.Paek等、Methods Vol.22,Page 53-60,2000
【非特許文献7】S.H.Paek等,BioChip J.Vol.1,Page 1-16,2007
【非特許文献8】Kyeong−Sik Shin等、Analytical Chimica Acta Vol.573-574,Page 164-171,2006
【非特許文献9】Yi Cui等、Science,Vol.293,Page 1289-1292,2001
【非特許文献10】Jong−in Hahm等、Nano lett.,Vol.4,Page 51-54,2004
【非特許文献11】Y Arntz等、Nanotechnology,Vol.14,Page 86-90,2003
【非特許文献12】Ronald T.Kurnik等,Sensors and Actuators B:Chemical,Vol.60,Page 19-26,1999
【非特許文献13】Anthony PF Turner,Nature Biotechnology,Vol.15、Page 421-421,1997
【発明の概要】
【発明が解決しようとする課題】
【0010】
そこで、本発明者らは、前記従来技術の問題点を克服するために鋭意研究を重ねた結果、分析物質のリアルタイム検出装置に可逆反応性の捕獲認識成分を導入し、これを連続的にリサイクルする場合、反応に関与する分析物質の濃度に応じて、リアルタイムに信号を発生させて測定することにより、分析物質に対する連続測定が可能であることを確認し、本発明を完成するに至った。
【0011】
したがって、本発明の主な目的は、可逆反応性の捕獲認識成分が導入され、これを連続的にリサイクルできる分析物質のリアルタイム連続検出装置を提供することにある。
本発明の他の目的は、前記リアルタイム連続検出装置を用いた分析物質のリアルタイム連続検出方法を提供することにある。
また、本発明の更に他の目的は、前記リアルタイム連続検出装置に使用される可逆反応性の捕獲認識成分の選別方法を提供することにある。
【課題を解決するための手段】
【0012】
本発明の一様態によれば、本発明は、試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含む、リアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分10及び試料内の分析物質11−捕獲認識成分10の結合体から発生した信号を探知するセンサーを含むことを特徴とする、分析物質のリアルタイム連続検出装置を提供する(図1の(A)を参照)。
【0013】
本発明において、前記「分析物質」とは、試料の分析サイトに含まれているセンサーを使用して検出しようとする目的で、センサーの表面に注入する物質を意味する。前記「捕獲認識成分」とは、前記センサーのセンサーチップ上に固定化されており、分析物質と特異的に結合可能な物質を意味する。例えば、分析物質が、抗原又はリガンドである場合、捕獲認識成分は、各々その抗原に対する抗体、又はそのリガンドに対する受容体であり、反対に、分析物質が、抗原に対する抗体又はリガンドの受容体である場合、捕獲認識成分は、各々その抗原又はリガンドである。
【0014】
本発明において、前記可逆反応性の捕獲認識成分は、脱着及び付着速度が共に速い反応力学特性を持ち、かつ高親和力を持つ認識成分(例えば、抗体)を意味し、高い付着及び脱着速度定数値を有した捕獲認識成分を使用すれば、連続的に使用しても、高い分析感度を維持することができる。
ここで、「親和力」は、平衡付着定数として表示することができるが、平衡付着定数(KA)は、付着速度定数(ka)/脱着速度定数(kd)と定義される。本発明では、可逆反応特性と高親和力を同時に有する抗体を使用することにより、「高感度のリアルタイム連続検出」が可能になる。
【0015】
もし、可逆反応特徴のためだけに、親和力が、1×106L/mol以下の認識成分を使用することになると、検出装置の測定感度が、mmol/L水準に非常に低くて、ほとんどの病気や症状の徴候を示すバイオマーカー分析物質の検出には適用し難しいという問題がある。これは、認識成分の親和力が低いほど、測定可能な分析物質の濃度範囲が高くなるためである。例えば、可逆反応性の認識成分(例えば、抗体)の付着速度定数を下げたり、一定に維持しながら、脱着速度定数を高め過ぎた成分を使用すれば、親和力が1×106L/mol以下に低くなる。
したがって、本発明でのように、高親和力の可逆反応性の認識成分を得るためには、特別な選別方法が導入されなければならない。例えば、固定された抗原と認識成分とが結合した後、中性緩衝液で洗浄する際に、残存活性が認識成分濃度に比べて低い値を有する認識成分を一次選別し(実施例1を参照)、これに対して、再び抗原が固定されたセンサー(例えば、表面プラズモン共鳴センサー)を用いた付着速度定数、及び脱着速度定数を測定して、二次選別を実施することにより(実施例3を参照)、高親和力の可逆反応性の認識成分を効率よく生産することができる。
【0016】
したがって、前記可逆反応性の捕獲認識成分が、本発明の目的と符合するためには、速い反応力学特性を持ち、かつ平衡付着定数が1×107L/mol以上の高親和力を維持することが好ましく、より好ましくは、1×108L/mol〜1×1012L/molであり、更に好ましくは、1×109L/mol〜1×1012L/molの高親和力を維持することが好適である。
【0017】
本発明のリアルタイム連続検出装置において、前記可逆反応性の捕獲認識成分は、好ましくは、試料内の分析物質との反応時に、付着速度定数(ka)は、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、脱着速度定数(kd)は、1×10−3sec−1〜1×10−1sec−1の可逆反応特性を持ち、同時に2つの速度定数の割合(ka/kd)が、1×108L/mol以上の平衡付着定数(KA)を有することを特徴とする。
このような特徴を有した捕獲認識成分を連続検出装置に使用すれば、両付着及び脱着速度定数が共に高いため、検出装置の応答時間が早くて、分析物質のリアルタイム検出が可能になるだけでなく、平衡付着定数もまた高いため、高度の測定感度を提供するという利点がある。しかし、範囲から外れる場合、特に、脱着速度定数が更に低い場合は、捕獲認識成分と結合した分析物質の解離が難しくて、連続測定時に非常に長い応答時間がかかったり、解離を加速させるために、苛酷条件(例えば、酸性pH)の使用が不可避であり、リアルタイムの検出が根本的に不可能になる。また、付着及び脱着速度定数が、所定の範囲にあっても、平衡付着定数が設定された範囲よりも低い場合は、上述したように、分析感度が低くなって、実用的な応用が極めて制限される。
【0018】
前記可逆反応性の捕獲認識成分において、特定の分析物質に対する典型的な認識成分として、モノクローナル抗体は、一般的に分析物質に対して動物を免疫化するハイブリドーマ方法(Kohler.G等,Nature,Vol.256,Page 495−497,1975)、遺伝子組換え方法(HP Fell等,PNAS,Vol.86,Page 8507-8511,1989)、phage display方法(Nicholas A.Watkins等,Vox Sanguinis,Vol.78,Page 72-79,2000)などを通じて生産可能であるが、可逆反応性の抗体を選別するためには、特別な処理が要求される。
【0019】
抗体の選別方法として広く使用されている固相免疫分析では、反応後に残存する過剰成分を除去するために洗浄工程を使用するので、洗浄時に、反応結合体が容易に解離される可逆反応性抗体の場合は、選別が困難である。本発明では、これらの問題を解決するために、一例として、反応及び洗浄時にリアルタイムに反応結合を追跡できる表面プラズモン共鳴センサーのような非標識センサー付の選別システムを使用した。
前記分析物質をセンサーの表面に固定した後、生産された抗体を運搬溶液に希釈して連続的に注入した後、同一の運搬溶液で洗浄すれば、表面での抗原−抗体間の付着及び脱着反応によって形成され、解離される結合体の密度が、センサーからリアルタイムに測定される。
【0020】
本発明の具体的な一例では、前記可逆反応性の捕獲認識成分を選別するために、表面プラズモン共鳴センサー基板の選別システムを用いた。適宜に希釈された一定濃度の抗体溶液をシステム内に注入すると、結合反応によって信号が時間によって増加するが、洗浄時に、つまり、抗体濃度「0」で、結合体密度の変化は、各抗体の可逆反応特性に応じて変化する(図2を参照)。既存のほとんどの免疫分析では、洗浄工程を経る間、脱着されない非可逆性抗体(図2、20E7)が、容易に脱着される可逆性抗体1B5よりも絶対的に好まれた。これは、洗浄後、固相に残存した抗原−抗体結合体から分析物質の濃度に比例した信号を発生することができるからであるが、このような分析システムでは、抗体をリサイクルしにくく、連続測定が根本的に不可能である。しかし、試料内の分析物質の濃度と力学的平衡状態で付着及び脱着が迅速な可逆反応性抗体1B5を使用すれば、抗体を連続的にリサイクルすることができ、これにより、分析物質の連続モニタリングが可能になる。
【0021】
また、免疫分析の際に、抗体の反応特性の差異による連続測定の実現可能性の可否は、循環の繰り返して測定してみると、更に明らかになる(図3参照)。非可逆反応特性を示す抗体(図3、20E7;ka=1.10×104Lmol−1sec−1、kd=1.80×10−7sec−1)の場合、抗体の供給後、一定時間の間、固定された抗原と継続的な付着反応を示し、洗浄時には、脱着が完了されないので、循環の繰り返しに従って、抗原−抗体反応結合体は、次第に累積して増加するパターンを示す。その一方で、可逆反応特性を示す抗体(1B5;ka=4.13×106Lmol−1sec−1、kd=3.61×10−3sec−1)の場合、抗体の供給後に、信号が急激に増加して付着反応が平衡に達し、かつ洗浄時に、すぐに脱着され、信号が初期の基準線に戻ってくるが、このような付着/脱着可逆反応形態は、循環の繰り返し時にも高い再現性を示す。
【0022】
可逆反応性を示す抗体は、抗原−抗体結合体の脱着速度が速くて、親和力(平衡付着定数、KA)の減少による分析感度の低下が心配されるが、付着及び脱着速度が共に速ければ、親和力には影響を与えない。実際に、平衡付着定数(KA)=付着速度定数(ka)/脱着速度定数(kd)であるので、上述した方法により、適切な反応力学特性、つまり、高い付着及び脱着速度定数値を有した抗体を選別すれば、高い分析感度を維持することができる。これにより、高い感度を維持するためには、一般的に、KA>1×108Lmol−1の条件の抗体が必要とされるので、高親和力の可逆反応性抗体は、ka>1×105Lmol−1sec−1、及びkd>1×10−3sec−1の特性を有した抗体と定義することができる。
【0023】
一方、可逆反応性抗体の親和力をテストする他の方法として、抗体を標準濃度で連続して希釈して、表面プラズモン共鳴センサー上に固定されている抗原と反応させ、信号感知が可能な最低抗体濃度を決定してみると、抗体の親和力の予測が可能である(図4を参照)。特に、可逆反応性抗体1B5が、pg/mLの濃度範囲以下でも抗原と反応することが測定されているが、この結果は、既存の非可逆性抗体の場合と比較しても、非常に高い親和力を示したものである。更に、図4の結果から、使用された可逆反応性抗体は、比較的幅広い濃度範囲において固定された抗原とは異なる平衡状態で反応することからみて、バイオセンサーの製作に非常に適していることが分かる。
【0024】
本発明のリアルタイム連続検出装置において、前記可逆反応性の捕獲認識成分10は、試料内の分析物質11である生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質若しくは国防化生放測定物質と特異的に結合できる抗体、受容体、核酸、酵素、アプタマー、ペプチド又は分子印刷人工膜であることを特徴とする。
【0025】
本発明のリアルタイム連続検出装置において、前記センサーは、分析物質11−捕獲認識成分10の結合体から発生した信号を直接探知する非標識センサー12(図1の(A)を参照)、又は分析物質11−捕獲認識成分10の結合体の密度に比例して信号を発生する標識物質14を経由して探知する標識センサー15であることを特徴とする(図1の(B))。
【0026】
本発明において、前記非標識センサーは、分析物質−捕獲認識成分の結合体に比例して変化するセンサー上の質量、振動子の抵抗、電荷分布の変化による表面の歪み、エネルギーの伝達などを信号として測定する。センサー表面の結合体の質量変化に従って、光屈折の各差を示す表面プラズモン共鳴(surface Plasmon resonance;SPR)センサー(Robert Karlsson等、Journal of Immunological Methods,Vol.145,Page 229-240,1990)、振動子の抵抗や電荷分布を感知するカンチレバー(cantilever)センサー(Hans−Jurgen Butt、Journal of Colloid and Interface Science,Vol.180,Page 251-260,1996)、光導波路(evanescent)センサー(R.G.Eenink等、Analytica Chimica Acta,Vol.238,Page 317-321,1990)、更には、ナノ次元の線や間隔を用いたナノセンサー(Fengli Qu等、Biosensors and Bioelectronics,Vol.22,Page 1749-1755,2007)などが、非標識センサーとして使用されることができる。
また、前記標識センサーは、分析物質−捕獲認識成分の結合体に比例して信号を発生するために、標識物質が標識された探知認識成分を追加に反応させた後、標識物質からの信号を測定する。
【0027】
本発明において、前記「探知認識成分」とは、標識物質が、物理的又は化学的に結合されており、分析物質と特異的に反応可能な物質を意味する。ここで、探知認識成分が反応する分析物質の分子上の位置は、捕獲認識成分が反応する部位と異なり、両成分は、分析物質と同時に反応できる。
信号を発生する標識物質としては、例えば、蛍光体、発光体、酵素、金属粒子、プラスチック粒子、磁性粒子等が使用される。これから発生する蛍光、発光、発色、電気化学、磁場などを探知するセンサーが、標識センサーとして使用されることができる。
つまり、前記非標識センサーを用いる場合は、試料に含まれている分析物質は、流体チャンネルを通じて連続的にシステム内に流入され、捕獲認識成分と反応し、標識センサーを用いる場合は、試料内の分析物質は、標識物質が結合された探知認識成分と事前に反応した後、流体チャンネルを通じて連続的にシステム内に流入されて捕獲認識成分と反応する。
【0028】
本発明のリアルタイム連続検出装置において、前記試料の分析サイトは、試料内の分析物質11だけを選択的に透過させうる半透膜16で区切られ、捕獲認識成分10が固定されているセンサーの表面側に認識反応セル17を形成することを特徴とする。
前記認識反応セル17は、標識センサー15を用いる場合、前記認識反応セル17内に半透膜16を通過できないほどの大きさの標識物質14と結合した探知認識成分13を閉じ込めて、リサイクルすることを特徴とする。
【0029】
また、前記認識反応セル17内の探知認識成分13も捕獲認識成分10と共に連続的にリサイクルされるために、可逆反応特性を持つことを特徴とする。
具体的には、前記試料の分析サイトは、捕獲認識成分が固定されているセンサーの表面側を半透膜で区切って認識反応セルを形成でき(図1の(C)、(D))、試料に含まれている分析物質は、大きさが小さくて、この半透膜を介してセル内に拡散伝達されるが、試料内の大きさが大きい不純物は濾過されて、センサー表面の汚れを防ぐことができる。このような認識反応セルの設置は、特に標識方式の解析システムの場合(図1の(D))、大きさが大きい標識物質と結合した探知認識成分をセル内に閉じ込めてリサイクルする効果も提供する。
【0030】
本発明の他の様態によれば、本発明は、下記の段階を含む前記リアルタイム連続検出装置を用いた分析物質のリアルタイム連続検出方法を提供する。
(a)分析物質を含む試料を前記試料の流入チャンネルを通じて試料の分析サイト内に注入する段階と;
(b)前記分析物質を試料の分析サイト内の可逆反応性の捕獲認識成分10と結合させる段階と;
(c)前記分析物質と捕獲認識成分との結合によって発生する信号をセンサーで探知する段階と;
(d)試料の継続的な流入や洗浄液の流入により、前記分析物質と捕獲認識成分との結合が脱着して、分析物質が、前記試料の排出チャンネルを通じて排出される段階と;
(e)前記脱着された捕獲認識成分を連続的にリサイクルして、前記(b)乃至(d)の段階を繰り返すことにより、試料内の分析物質の濃度変化をリアルタイムに測定する段階。
【0031】
本発明のリアルタイム連続検出方法において、前記(c)の段階において、分析物質−捕獲認識成分の結合体から発生した信号を、非標識センサーを用いて直接探知するか、あるいは、分析物質−捕獲認識成分の結合体の密度に比例して信号を発生する標識物質を経由して、標識センサーを介して信号を測定することを特徴とする。
【0032】
本発明において、前記非標識センサーを用いる場合、試料に含まれている分析物質は、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応することを特徴とする。
【0033】
本発明において、前記標識センサーを用いる場合、試料内の分析物質が、標識物質が結合された探知認識成分と事前に反応した後、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応するか(連続流れ露出タイプ)、試料内の分析物質が、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入された後、認識反応セル内の標識物質と結合された探知認識成分及び捕獲認識成分と反応する(認識反応セルタイプ)ことを特徴とする。
【0034】
本発明において、前記探知認識成分は、連続流れ露出タイプの場合、分析物質と事前に反応して供給されるので、結合安定性の高い非可逆反応特性を持つか、あるいは、認識反応セルタイプの場合、捕獲認識成分と共に探知認識成分も連続的にリサイクルされるために、可逆反応特性を持つことを特徴とする。
【0035】
本発明において、認識反応セルタイプの標識センサーを用いる場合、近接していた蛍光物質(標識物質)と蛍光エネルギー受容体との間のエネルギー伝達が、捕獲認識成分と分析物質との反応によって妨げられ、蛍光信号が発生する原理を用いるか、又は酵素分子(標識物質)上に固定されている分析物質と認識成分とが結合すれば、活性が抑制されることが知られている酵素を、標識物質を用いて捕獲認識成分をセンサー上に固定させず、認識反応を液相で行えることを特徴とする。
【0036】
本発明の他の様態によれば、本発明は、下記の段階を含む前記リアルタイム連続検出装置に使用される可逆反応性の捕獲認識成分の選別方法を提供する。
(a)捕獲認識成分を用意する段階と;
(b)前記捕獲認識成分をセンサーの表面に固定されている分析物質と結合させる段階と;
(c)前記捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(d)洗浄液の流入により、前記捕獲認識成分と分析物質との結合を脱着させる段階と;
(e)前記脱着後、残りの捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(f)前記(e)の段階での探知信号は、前記(c)段階での探知信号よりも低くなる捕獲認識成分を選択する段階。
【0037】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記センサーは、表面プラズモン共鳴センサー、カンチレバーセンサー、光導波路センサー、光干渉センサー、及びナノセンサーから選ばれる非標識センサーであることを特徴とする。
【0038】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記捕獲認識成分は、センサーの表面に固定されている分析物質との反応時に、付着速度定数(ka)は、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、そして、脱着速度定数(kd)は、1×10−3sec−1〜1×10−1sec−1の範囲の可逆反応特性を持ち、同時に平衡付着定数(KA=ka/kd)が、1×108L/mol以上の高親和力を持つものを選択することを特徴とする。
【0039】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記(a)の段階において、前記捕獲認識成分は、運搬溶液で希釈して連続的に注入され、前記(f)の段階において、時間によって増加していた信号が減少する捕獲認識成分を選択することを特徴とする。
【0040】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記(a)の段階において、前記捕獲認識成分は、洗浄液と循環繰り返して注入され、前記(f)の段階において、時間によって信号が増加した後、最初の基準線に戻ってくる信号パターンが繰り返される捕獲認識成分を選択することを特徴とする。
【0041】
以上で説明する本発明に係る分析物質のリアルタイム検出装置、これを用いた分析物質のリアルタイム連続検出方法、及びこれに用いられる可逆反応性の捕獲認識成分の選別方法を用いる場合は、以下のような利点を奏する。
バイオセンサーやバイオチップの製作において、本発明でのように、分析物質の濃度に応じて迅速に可逆的に反応する抗体をリサイクルすれば、既存の使い捨ての診断チップに比べて、構成部品及び製作方法が大幅に単純化される。これは、既存の装置又はシステムで試薬の供給及び除去のために要求されてきた多数のバルブやポンプが最小化され、実際に身体に着用が可能な小型のマイクロ流体の流れ方式の連続診断システムの具現が可能である。
【0042】
このような新しい概念の検出方法(又は診断方式)は、病気や症状に関するリアルタイムのモニタリングを可能にするので、現存するほとんどすべての免疫分析システムが抱えている、一度使用した後に廃棄する使い捨ての性能の限界を克服することができ、人体の慢性疾患や高危険群患者に対する連続的な監視が可能になる。更に、現在の診断システムにおいて診断結果を得るために時間がかかり、また、患者状態の感知データを実験室で分析する必要がある場合、診察時点と診療結果が出てくる時間との差が多くて、正確な病気の診断やタイムリーな治療に難しさが多いという問題を解決することができる。
【0043】
したがって、本発明で開発された、リアルタイム連続検出装置及びこれを用いた検出方法は、早期診断概念の新たな予防医学の手法として、病院で需要の現場を中心に移動する診療パラダイムの変化を満たし、慢性疾患者や高齢者などの高危険群の患者の監視が常時可能な連続診断機器の開発と実用化を可能にする。特に、平均寿命が延長される共に、出生率の減少により高齢化社会への進入が加速されてあり、これに加えて、食生活パターンの西欧化により、様々な慢性成人病疾患が広まっており、早期診断により、健康な生活を営むのに役立つ。連続診断方法は、特に、今後到来するU−ヘルスケア時代において、診断システムを、携帯電話、病院、住宅などに内蔵したり、身体に装着して、生体情報をリアルタイムに測定し、診断するための基盤源泉技術として活用できる。
【0044】
また、本発明のリアルタイム連続検出装置及びこれを用いた検出方法は、生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質や国防化生放測定物質などを分析するのに活用可能であり、産業分野別の製品群を例として纏めると、以下の通りである。医療診断産業では、高危険群(慢性疾患者、高齢者、重症患者)の連続診断システム製品、糖尿病患者の感染症連続診断システム製品、心臓血管患者の再発連続監視システム製品は、癌治療患者の再発連続監視システム製品、そして、便座の健康モニタリングシステム製品などが挙げられる。人工臓器産業では、人工膵臓制御システム製品などの人工臓器の制御などに適用することができる。公衆衛生及び防衛産業では、生物テロ作用剤の連続探知システム製品、そして、鳥インフルエンザウイルス及びSARSウイルスなどの人獣共通感染症の病原体の連続探知システム製品などに応用することができる。環境産業では、川、沿岸、海洋汚染の連続監視システム製品などが挙げられる。生物及び食品産業では、生物工程の連続監視システム製品と食品の生産工程の連続監視システム製品などに適用することができる。
【発明の効果】
【0045】
本発明によると、一定量の可逆反応性の捕獲認識成分を連続的にリサイクルして、分析物質の濃度変化をリアルタイムに測定することができる。本発明のリアルタイム連続検出装置は、生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質や国防化生放測定物質などを検出、又は、分析するのに活用可能なので、医療、公衆衛生、国防、環境、食品、獣医、バイオテクノロジー産業に応用することができる。
【図面の簡単な説明】
【0046】
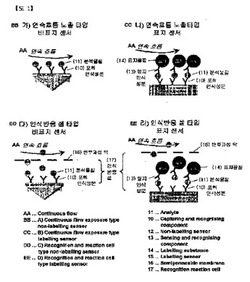
【図1】図1は、本発明に係る試料の分析サイト内で捕獲認識成分10を連続的にリサイクルして、分析物質の濃度変化を測定する(A)連続流れ露出タイプの非標識センサー;(B)連続流れ露出タイプの標識センサー;(C)認識反応セルタイプの非標識センサー、及び(D)認識反応セルタイプの標識センサーを示す模式図である。
【図2】図2は、本発明に係る捕獲認識成分の例示として、ネズミのハイブリドーマのクローンから生産された可逆反応性を示す抗体1B5と、典型的な非可逆反応性を示す抗体20E7に対する付着及び脱着反応特性を解析するために、センサーの表面に抗原、即ち、分析物質(α2−マクログロブリンをモデルとして使用)が固定されている表面プラズモン共鳴センサーシステムを使って測定したグラフ、及びこのことから決められた速度定数と付着平衡定数との比較である。
【図3】図3は、図2のセンサーシステムを用いて、2つの抗体1B5及び20E7の反応特性の差異による連続測定の実現可能性の可否をテストするための循環繰り返し測定の結果を比較したグラフである。
【図4】図4は、図2のセンサーシステムを用いて、可逆反応性抗体である1B5の抗原に対する親和力をテストするために、抗体を連続して希釈して、濃度の増減に従って、センサー上に固定されている抗原と反応させて得た結果である。
【図5】図5は、可逆反応性抗体である1B5が、医療臨床用の診断に使用可能か否かを評価するために、1B5抗体をセンサーの表面に固定させた後、抗原、つまり、分析物質を濃度の増加に従って固定されている抗体と反応させ、試料運搬液として(A)リン酸緩衝液、及び(B)ヒト血清を用いて得た結果の比較である。
【図6】図6は、図5のセンサーシステムの分析感度を向上させるために、標識物質14として直径が30nmの金コロイド粒子と探知認識成分13として非可逆反応性抗体20E7との重合体を追加に導入して得た信号増幅結果である。
【図7】図7は、図5のセンサーシステムを用いて、試料の使用量を最小化するために、センサーチップ内へのマイクロ流体の流れ速度を先行の実験条件の1/10に減速した条件下で、分析物質濃度の増減によるセンサーの応答結果である。
【図8】図8は、可逆反応性抗体のリサイクルを例示するために、センサー表面へ抗体1B5が固定されている表面プラズモン共鳴センサーシステムを連続測定モードで運用して、分析物質(α2−マクログロブリン)の濃度が連続して10倍ずつ増加して減少する2回の反復的な変化に対して、センサーから求めた(A)濃度応答の結果、及び(B)グラフで示した標準曲線である。
【図9】図9は、図8のセンサーシステムを用いて、分析物質の濃度が2倍、あるいは、それ以下に増加して減少する算術的な濃度変化に対するセンサーの濃度応答の結果である。
【発明を実施するための形態】
【0047】
以下、本発明の可逆反応性の捕獲認識成分を用いたリアルタイム連続検出装置について更に具体的に説明する。
【0048】
(1)非標識センサーを用いたリアルタイム連続検出デバイスの構築例示
リアルタイム連続検出装置(又はリアルタイム連続検出システム)を実装する際に、可逆反応性の認識成分のほか、重要な要素の一つがセンサー技術である。上述したように、センサーの種類としては、大きく非標識センサーと標識センサーとに分けられ、連続診断システムの構築時に、プラズモン共鳴センサー、カンチレバーセンサー、又は光導波路センサーのような非標識センサーを用いることが理論的に単純化する。
【0049】
連続検出装置の構成は、非常に多様であるが、本発明の有用性を容易に説明するために、プラズモン共鳴センサーチップ上に、可逆反応性抗体1B5を固定して製作した非標識センサー基板の連続検出装置を、図1を参照して例として説明すれば、以下の通りである。
【0050】
非標識センサーにより、金属と遺伝媒体の界面で光によって発生する電荷密度波長である表面プラズモン共鳴を測定する方法が代表的である。このような表面プラズモン共鳴は、金属表面に非常に近接して相互作用するので、この領域での認識反応などによる光学特性の変化は、表面プラズモン共鳴を引き起こす光の入射角に影響を与えることになる(J. Homola等,Sens.Actuators B, Vol.54、Page 3-15,1999)。これにより、センサー表面での分析物質と認識成分間の反応により、表面プラズモン共鳴を起こす光の入射角の変化を信号として測定する。
表面プラズモン共鳴センサー12上に可逆反応性抗体1B5;10を固定して構成した連続検出装置(図1の(A))に、リン酸緩衝液で希釈して、各々異なる濃度の分析物質(アルファ2−マクログロブリン)が含まれるように製造した標準溶液を10μL/分、マイクロ流体の流れ速度で順次に注入すると、濃度に比例した応答信号がセンサーから発生する(実施例6を参照)。各標準溶液は、信号を毎度基準線に戻してから注入したし、与えられた条件の下で、測定感度は、0.1ng/mLの水準以下と敏感しただけでなく、濃度の応答時間は、最終応答水準の95%を基準に640秒程度と非常に迅速した(図5の(A))。分析特異度をテストするために、同じ濃度範囲の分析物質を、医療臨床試料のヒト血清で希釈して製造した後、同じ実験を繰り返した結果、ほぼ類似した濃度応答が得られたので(図5の(B))は、構築された連続検出装置は、医療臨床用の診断に使用することができる。
【0051】
また、分析感度を向上させる方法として、標識物質14と結合した探知認識成分13を追加に導入して、分析物質11と捕獲認識成分10との間の認識反応結合体の質量変化を増加させる信号増幅方法が利用できる。探知認識成分13として非可逆反応性抗体20E7を選択して、直径が30nmの金コロイド粒子と物理的に結合し、この結合体を分析物質標準溶液と事前に反応させた後、センサー内に注入して、センサーの濃度応答を測定した(実施例7を参照)。参考として、非可逆反応性抗体20E7は、分析物質について、可逆反応性抗体1B5と同時に反応できる。その結果、信号増幅方法を利用すれば、最小0.001ng/mLの分析物質の探知が可能であり、これにより、分析感度が約100倍向上することが分かった(図6)。
【0052】
医療臨床試料の場合、特にその使用量を最小化することが必要とされるので、マイクロ流体の流れ速度を、先行の実験条件の1/10(つまり、1μL/分、又は1.44mL/日)に減速しようとし、同じ条件の下で、分析物質濃度の増減によるセンサーの応答を測定した(実施例8参照)。センサーの濃度応答を測定した結果、分析感度(0.1ng/mL)と応答時間(640秒、最終応答の95%基準)は、マイクロ流体の流れ速度に関係なく一定に維持されることが分かった(図7の(A))。また、マイクロ流体の流れ速度の変化によるセンサーの濃度応答パターンにも大きな変化がなくて、流体の流れ速度が10倍異なる条件で求めた2つの濃度応答曲線は、ほぼ一致していることが分かった(図7の(B))。しかも、分析物質の濃度の増加時に測定した濃度応答と、濃度の減少時に測定した濃度応答との間にも差がなかった。
【0053】
図5から図7に示すように、可逆反応性抗体が固定されているセンサーチップを用いて、分析物質の濃度変化に対するSPRセンサーの応答を求めるために、濃度変化時ごとに、毎回、初期条件、つまり分析物質が不在の状態に戻した後、測定を開始する「リセットモード」を使用した。
可逆反応性抗体のリサイクルを例示するために、「連続モード」を使用したが、分析物質の濃度が15分ごとに階段式に10倍ずつ増加して減少する2回の反復的な変更について(0.01ng/mL〜100ng/mLの範囲)、センサーから濃度応答を連続的に求めた(実施例9を参照)。与えられたマイクロ流体の流れ速度(1μL/分)でセンサー内に注入される分析物質の変化された濃度で、センサーの応答は15分以内に平衡状態に達し、2回の繰り返し時に高い再現性を示した(図8の(A))。このような連続測定方式で測定したセンサーの濃度応答を示した標準曲線(図8の(B))は、「リセットモード」で測定した曲線と多少違いがあることが分かるが、これは、センサーシステムの運用方式の違いによるものと判断される。
【0054】
分析物質の種類に従って、発症や症状の発現時に、濃度の増減変化パターン(指数的あるいは算術的)が異なることがあり得るので、2倍、又はそれ以下に増加して減少する算術的な濃度変化に対するセンサーの濃度応答を「連続モード」で測定した(実施例10を参照)。指数的な変化に対する応答と同様に、センサーは、算術的な分析物質の濃度変化に対しても類似した分析性能を示した(図9)。更に、小さな濃度変化に対しても敏感かつ迅速に反応することからみて、可逆反応性抗体基板のバイオセンサーは、今後、非常に正確な分析を要求する分析物質の測定に広く適用できると期待される。
【0055】
本発明では、連続診断を例示するための分析物質として、アルファ2−マクログロブリンを選択し、この物質に対して特異な可逆反応性の抗体を生産して、連続診断手法を例示した。アルファ2−マクログロブリンは、3種類の他の病気、特に新症候群の治療及び再発の確認、アルツハイマーの早期診断、そして人工臓器移植後の炎症反応と合併症の臨床診断にバイオマーカーとして使用することができる。
また、新症候群は、約90%が小児にのみ発生する病気で、尿にタンパク質が混じって出てくる腎臓疾患であって、腎臓の糸球体の異常により蛋白質が失われる(Daniel A.Blaustein等,Primary Care Update for OB/GYNS,Vol2,Page 204-206,1995)。患者は、身体や足に浮腫が生じて訪れる場合が大部分であり、状況に応じて、腎臓硬化症、腎不全、癌などに発展する場合もある。この病気の診断は、CBC(complete blood count)、肝機能検査、腎機能検査、マクログロブリンなど、血液中の蛋白検査、尿検査などによって実施される。新症候群と診断された時に、治療のために免疫抑制剤(prednisone)又はステロイド剤を1〜6ヶ月間投与するが、この期間の間、尿検査や血液検査を継続的に実施して変化を観察することで、治療効果を判断する。綿密な観察のために、定期的に病院を訪問して、血液と尿検査を実施しなければならないが、特に、新症候群の患者の90%が、表現力が弱い小児なので、症状変化などの身体の異常に対する継続的かつ徹底な検査や観察が必要である。これにより、小児の新症候群の治療効果及び再発確認のための未来の技術として、マクログロブリンなど、血蛋白に対する連続探知手法の開発は、非常に有用であると予測される。
【0056】
マクログロブリンのバイオマーカーへの活用に関する他の可能性として、アルツハイマーは、60〜70人に1人の割合で発生し、85歳以上は、50%が患っている老人性疾患であり、早期診断による予防が切実である。2006年にロンドンのキングスカレッジの研究チームが、血液検査によってアルツハイマー疾患にかかった患者から2種類の蛋白質、つまり、補体因子−Hの前駆体とアルファ2−マクログロブリンの濃度が増加したことを発見しており、このような蛋白質の濃度差の究明によって早期診断の可能性を提示した(A.Hye等, Brain.Vol.129,Page 3042-3050,2006)。このような目的で、マクログロブリンの連続探知によりアルツハイマー疾患を早期に診断すれば、症状の発現後に病院を訪問するよりも、疾患の予防及び治療が早期になされて、疾患の進行をはるかに緩和させ、生活の質の向上に大きく寄与すると期待される。
【0057】
マクログロブリンのバイオマーカーとしての活用に対するもう一つの可能性として、人工臓器の移植に伴う炎症反応や合併症の発生は、既知の事実であったが、その診断指標に関する研究結果が多くなかった。2005年米国のデューク大学医療センターで心臓手術に心肺機を使用した後、アルファ2−マクログロブリン濃度が50%増加した研究結果を提示した(Eric A.Williams等,J Thorac Cardiovasc Surg,Vol.129,Page 1098-1103,2005)。これは、全身的な炎症反応の一つの指標としてマクログロブリンの濃度変化が利用され得ることを示す。これにより、人工臓器移植後の予後観察の際に、炎症反応発現のバイオマーカーを連続探知することができる場合、定期的に病院訪問や合併症の症状の発現後の措置よりも、人工臓器の入れ替えや合併症の治療が早期に行えるという利点がある。
【0058】
前記で例示した病気を含めて、急慢性人体疾患は、一般的に時間や日単位で比較的ゆっくり進むので、疾患指標のバイオマーカーを測定するセンサーの応答時間として、通常分単位が要求される。これは、病気の進行時間と比較して、センサーの応答時間が10倍程度より速いとしたら、病気の進行がバイオマーカーの連続診断工程を支配する律速段階になるので、図8及び図9に示すセンサーのマクログロブリンの濃度応答時間(約15分、最終応答の95%基準)は、連続探知条件を満たす。より迅速なセンサーの応答時間(例えば、秒単位)は、連続診断時の分析性能に全く影響を与えず、単に概念のみが異なる使い捨てのセンサー(例えば、血糖値センサー)の場合、採取した試料の測定時間を短縮させるという効果を提供するだけである。
【0059】
(2)標識センサーを用いた診断システムの構築の可能性の例示
標識センサーの例として、蛍光体を信号発生源として使用する例が最も多く、捕獲認識成分10を固体表面に固定するか(図1の(B)及び(D))、あるいは、認識反応セル17内で液相反応によって探知が可能であり、この場合、信号発生源である蛍光物質(donor)から放射された光は、あるエネルギー受容体(acceptor)が非常に近接して存在する場合、吸収され、光が外部に放射されない原理を用いる(Shaw等,J.Clin.Pathol,Vol.30,Page 526-531,1977)。その応用として、抗原−抗体の付着のような認識反応が、蛍光物質とエネルギー受容体との間のエネルギー伝達を調節するように設計することができ、蛍光信号は、受光素子(フォトダイオード、charge−coupled device、photomultiplier tubeなど)を用いて探知される。
【0060】
標識センサーの他の例として、酵素を標識物質として使用することができ、センサーの表面に固定されている捕獲認識成分10を用いるか(図1の(B)及び(D))、又は酵素分子上に抗体が取り付けられる場合、活性が抑制されることが知られている数種類の酵素を用いると、認識反応セル17内で液相反応の遂行が可能である。これらの酵素を免疫分析に用いるために、分析物質(即ち、抗原)と結合させて抗体と反応させると、その酵素の活性が抑制されることが知られている(Se−Hwan Paek等、Biotechnology and bioengeering,Vol.56, Page 221-231,1997)。酵素からの信号は、選択した酵素と基質に応じて、吸光度測定センサー(スペクトロフォトメーター)、受光センサー(フォトダイオード、charge−coupled device、photomultiplier tubeなどの受光素子)、電気化学センサー(電極)などの様々な手段によって測定できる。
【0061】
標識センサーの他の例として、磁性粒子を標識物質として用いることができ、センサーの表面に固定されている捕獲認識成分10を用いると(図1の(B)及び(D))、分析物質との認識成分との間の反応に対する磁場測定が可能である(A. Perrin等,Journal of Immunological Methods,Vol.224, Page77-87,1999)。磁場測定センサーは、GMR/TMR及びHall素子が代表的であり、消費電力が少なく、大きさも小さく、軽くて、高集積化が可能である。
【0062】
以上で説明したように、可逆反応性抗体とセンサー技術とを組み合わせて、連続診断システムを構築すれば、分析感度の犠牲なしに、抗体を連続的にリサイクルして、分析物質をリアルタイムに測定することができる。例示された連続診断システムの濃度応答時間は、最終回答の95%を基準として10分台で、濃度が秒単位で変化する分析物質の測定には適用できず、分単位より相対的にゆっくり変化する分析物質の測定に適用することができる。特に、その濃度が定められた上限を超える場合、警報発令を必要とする分析の対象に適する。その適用可能な分野として、病気や症状に対する連続診断、及び人工臓器制御、生物テロ作用剤の連続探知、環境汚染の連続監視、及び生物工程の連続モニタリング分野などがある。
【実施例】
【0063】
以下、実施例に基づいて、本発明を更に詳細に説明する。これらの実施例は、本発明を例示するためのものなので、本発明の範囲が、これらの実施例によって制限されるものではない。
【0064】
<実験材料>
本発明の実施例のために使用された材料や購入先は、以下の通りである。表面プラズモン共鳴センサーチップ(BIACORE CM5;構成成分:ガラスマトリックス(母体)、30nm厚さの金薄膜、100nm厚さのdextran層)、amine couplingキット(100mM N−hydroxysuccinimide(NHS)、400mMのN−ethyl−N'−(dimethylaminopropyl)carbodiimide(EDC)、1Mのethanolamine hydrochloride、pH8.5を含む)、40%のグリセロール(glycerol)は、GE healthcare社(スウェーデン)から購入した。ネズミモノクローナル抗体(20E7、3D1;非可逆反応)とアルファ2−マクログロブリン(α2−macroglobulin、tetramer)は、エイビスフロンティア社(韓国)から供給された。牛血漿脂質蛋白質(bovine serum albumin)、sodium acetate、sodium phosphate、sodium chloride、glycine、ヒトAB型血清(human serum、AB plasma)、カゼイン(casein)、金ナノ粒子(gold nanoparticle、30nm)、抗ネズミヤギ抗体-horseradish peroxidase(HRP)重合体、及び3,3'、5,5'-tetramethylbenzidine(TMB)は、Sigma社(米国)から購入した。総IgG抗体定量キット(mouse IgG core ELISA)は、コマバイオテック社(韓国)から供給された。その他のすべての試薬は、分析用級に使用された。
【0065】
(実施例1)
−ネズミモノクローナル可逆反応性抗体の生産−
モノクローナル抗体を生産するハイブリドーマ細胞の作製は、通常の標準的な方法に基づいて実施した。具体的には、生後6週の雌BALB/cネズミの腹腔内にアルファ2−マクログロブリンを免疫原に注射して免疫させた後、2週間隔で3回ブースティングしている。三次ブースティング後、3日目にネズミを犠牲にして脾臓を摘出して得られた脾臓細胞を骨髄腫(myeloma)細胞株(Sp2/0-Ag14)との細胞融合を実施しており、このことからハイブリドーマ細胞を選別した。
【0066】
ハイブリドーマ細胞は、合計384種類のクローンが製作され、各クローンから生産された抗体含有培養液を用いて免疫原に対する反応性試験と総IgG抗体量の決定を行った。免疫原との抗体の反応性試験のために、10mMのリン酸緩衝液(140mMのNaClを含む;pH7.4)で希釈されたアルファ2−マクログロブリン(2.5μg/mL)が固定されている96−マイクロプレートウェル内にクローン培養液をそれぞれ移して反応させた。洗浄後、0.5%カゼイン含有10mMのリン酸緩衝液(カゼイン−PBS)で希釈された抗ネズミヤギ抗体−HRP重合体1/5、000)を反応させた。再度洗浄後、HRP基質溶液(3%過酸化水素水10μL)と10mg/mLのTMB(100μL;dimethyl sulfoxide溶媒に希釈)が含有された0.05Mの酢酸緩衝液、pH5.1(10mL)を各ウェルに加えて、酵素反応を行った後、15分間で2Mの硫酸を添加して停止させた。各ウェルで発生した発色信号は、マイクロプレート読み取り機器(VERSAmaxTM、Molecular Devices社製、米国)を用いて、450nm吸光度で測定された。また、総IgG抗体の量を決定するために、総IgG抗体定量キット(mouse IgG core ELISA)を使用して、メーカーから提供されたプロセスに基づいて分析した。
両分析結果から、抗体の反応性試験時の吸光度2.0以下(下位50%)、及び、総IgG抗体量0.1μg/mL以上(上位15%)の条件を同時に満足するハイブリドーマクローンの7種類を選別した。
【0067】
(実施例2)
−センサーチップの表面活性化及びリガンドの固定化−
表面プラズモン共鳴センサーチップとして購入されるBIACORE CM5は、メーカーから提供されたプロトコルに従って、100mMのNHSと400mMのEDCを用いて、チップの表面を活性化した。チップ表面に固定されるべきリガンド(抗原又は抗体)の量は、メーカーのプロトコル案内に従って計算して決定し、10mMのsodium acetate(pH4.0)緩衝液を用いて、リガンドを一定濃度で希釈した後、センサーチップ内に注入して(流速=5μL/分)、固定化を施した。20分後、1Mのethanolamine hydrochloride(pH8.5)溶液を6分間注入して、センサーの残りの表面を不活性化した。
表面プラズモン共鳴センサーシステム(BIACORE2000;GE healthcare社、スウェーデン)の運営は、メーカーから提供されたBIACORE 2000の使用プロトコルに従い、試料運搬液(running buffer)として、リン酸緩衝液、又はヒト血清を検査目的に従って選択して使用した。センサーシステム内に装着されるセンサーチップBIACORE CM5を購入して、このチップの1番の流体チャンネルには、対照群として牛血清アルブミンを付着させ、2番の流体チャンネルには、リガンドを化学的に固定させた。すべての実施例において同様に流体の流れ方向を1番の流体チャンネルから2番の流体チャンネルへ維持し、2番の流体チャンネルの信号値(resonance unit;RU)から1番の流体チャンネルのノイズ値を引くような方式で純粋な信号値を求めた。反応セル内の温度は、すべての実施例で同様に25℃に維持した。
【0068】
(実施例3)
−表面プラズモン共鳴測定システムを用いた可逆反応性抗体のスクリーニング−
可逆反応性抗体のスクリーニングを目的として、実施例2で説明したように、1番の流体チャンネルに100μg/mLの濃度で牛血清アルブミンを固定させ、2番の流体チャンネルに100μg/mLの濃度でアルファ2−マクログロブリンを固定させたセンサーチップを製造した。このように用意したセンサーチップを、表面プラズモン共鳴測定システムに装着した後、10mMのリン酸緩衝液を試料運搬液として用いて、5μL/分の速度で注入して、平衡状態を維持した。実施例1の抗体反応性試験と総IgG抗体量の決定から選別されたハイブリドーマクローン7種類を10mMのリン酸緩衝液(PBS、pH7.4)でそれぞれ適切に希釈した。メーカーから提供された分析プログラム(BIACORE operation 2000)に基づいて、各抗体試料35μLをセンサーシステム内に装着されているセンサーチップ内に420秒間注入して、付着反応を誘導した後、リン酸緩衝液を210秒間注入して、脱着反応を誘導した。同一種の抗体に対する分析が完了した後には、10mMのglycine緩衝液(pH1.5)15μLを180秒間一定に注入して、センサー表面を再生させた。付着及び脱着反応パターンは、メーカーから提供された編集プログラム(BIAevaluation 2.0)を用いて分析し、付着速度定数(ka)と脱着速度定数(kd)と平衡付着定数(KA)を計算した。以下の表は、テストされたハイブリドーマクローン7種類の付着速度定数(ka)と脱着速度定数(kd)と平衡付着定数(KA)を表したものである。
【0069】
二次選別されたハイブリドーマクローンの応答特性
【表1】

テストされたハイブリドーマクローン7種類のうち、2クローン1B5及び1F8が、高親和力の可逆反応性を示し、そのうち、1B5クローL/molよりも高い高親和力を示したので、本発明の目的に適するものと選定して、典型的な非可逆反応性を示す抗体である20E7と反応特性を比較した(図2)。付着反応時に、1B5抗体は、20E7より平衡状態に顕著に早く達しており、脱着反応時に、1B5抗体は、初期値に近接して落ちる形態のグラフを示したのに対し、20E7は、ほとんど脱着されていない形態のグラフを示した。このような特性の違いから、洗浄が要求される、既存の1回性の免疫分析において、洗浄時にも脱着されない非可逆反応の20E7抗体が好まれていた一方、抗体の濃度に応じて、力学的平衡反応により迅速に付着と脱着が迅速な1B5は、抗体のリサイクルによる連続測定に利用可能である。
したがって、本発明での基板素材である可逆反応性抗体の存在を提示し、既存の抗体とのその本質的な特性の差を一次証明した。参考事項として、1B5抗体と20E7抗体は、共にアルファ2−マクログロブリンに対して特異反応性を示し、この抗原分子上の他のエピトープ(epitope)に付着して、同じ抗原分子と同時に反応することができる。
【0070】
(実施例4)
−可逆反応性抗体の付着/脱着の繰り返し反応パターンの比較−
実施例3で製造したセンサーチップを用いて、同じ実験条件で可逆反応性1B5抗体の付着/脱着の繰り返し反応パターンを求めて、これを非可逆反応性20E7のパターンと比較した。10mMのリン酸緩衝液で希釈した抗体溶液(100ng/mLの1B5、又は20ng/mLの20E7)17.5μLを5μL/分の流速で210秒間、センサーチップ内に注入して付着反応を誘導し、その後、リン酸緩衝溶液を注入して、110秒間、脱着反応を誘導した。このような、同じ付着/脱着の反応条件下で、各抗体に対して、6回繰り返した。各抗体別に分析を完了した後、10mMのグリシン(pH1.5)の緩衝液15μLを180秒間に一定に注入して、センサーの表面を再生させた。BIACore 2000計測システムの運営とデータの編集は、実施例2の説明と同様である。
分析の結果、図3には、可逆反応特性を示すものと予測された1B5抗体は、抗体を供給してわずか1分以内に信号が増加して、固定された抗原との付着反応平衡状態に達し、かつ、リン酸緩衝液の供給時にすぐに着脱され、信号が初期値に戻ってきた。このような付着/脱着の可逆反応パターンは、6回繰り返し時に高い再現性を示した。非可逆反応特性を示すものと予測された20E7抗体は、抗体の供給後に一定時間の間、相対的に遅いが、継続的な付着反応を示し、リン酸緩衝液の供給時に脱着反応が完了していなかった。したがって、抗原−抗体反応結合体は、付着/着脱の繰り返し反応に従って順次累積され、信号が階段式に増加するパターンを示した。
【0071】
(実施例5)
−可逆反応性抗体の反応下限濃度の決定−
実施例3で製造したセンサーチップ及び同じ実験方法を用いて、可逆反応性1B5抗体の濃度変化に対する表面プラズモン共鳴センサーの応答を測定した。1B5抗体を、10mMのリン酸緩衝液を用いて、0.5pg/mL〜0.5μg/mLの範囲の濃度で希釈した。希釈した各抗体溶液17.5μLを5μL/分の流速で210秒間注入して付着反応を誘導し、その後、リン酸緩衝液を110秒間注入して脱着反応を誘導した。同じ条件下で、低濃度の抗体溶液から高濃度の溶液の順に分析し、また、逆順に分析して、1回循環テストした。循環試験が完了した後、実施例4の場合と同じ方法で、センサーの表面を再生させた。
【0072】
図4では、使用された抗体の濃度範囲内で、表面プラズモン共鳴センサーの信号は、抗体溶液の濃度が段階的に増加する際に比例して増加し、濃度が段階的に減少する際に比例して減少した。特に、抗体の濃度範囲が、pg/mL以下でもセンサーチップに固定されている抗原と反応することが分かったが、これは、既存の免疫分析に使用される非可逆反応性抗体と比較した場合、親和力の面で負けない結果である。したがって、1B5のような反応特性を有した抗体を搭載した免疫分析システムは、優れた分析感度を示すと予測され、また、その抗体がpg濃度単位からμg単位まで反応性を示すので、今後の免疫センサーの製作に利用する場合、広い測定範囲が予想される。
【0073】
(実施例6)
−可逆反応性抗体基板の非標識免疫センサーシステムの構築−
可逆反応性抗体を用いたアルファ2−マクログロブリン測定用の連続流れ露出タイプの非標識センサー(図1の(A))システムを構築するために、表面プラズモン共鳴センサーシステム(BIACORE 2000)と可逆反応性の抗体が固定されているBIACORE CM5センサーチップとを用いた。実施例2で説明したように、1番の流体チャンネルに牛血清アルブミンを100μg/mLの濃度で固定させ、2番の流体チャンネルに可逆反応性1B5抗体を10μg/mLの濃度で固定して、センサーチップを製造した。このように、センサーの表面に固定されている抗体と特異的に反応する分析物質であるマクログロブリンを10mMのリン酸緩衝液で希釈して、0〜10ng/mLの濃度範囲の標準試料を製造した。各標準試料(150μL)を10μL/分の流速で900秒間センサーシステム内に装着されているセンサーチップ内に注入して、付着反応を誘導した後、リン酸緩衝液を120秒間注入して、脱着反応を誘導した。各試料に対する分析が完了した後、実施例4のように、センサーの表面を再生させ、リン酸緩衝液の代わりに、ヒト血清を希釈液と試料運搬液として使用して、上述した同じ条件下で実験を繰り返した。
【0074】
表面プラズモン共鳴センサーを用いて、免疫分析分野で初めて、可逆反応性抗体基板の解析システムを構築し、この解析システムは、採択された分析物質濃度0.1〜10ng/mLの範囲で濃度応答を示し、測定感度に代表される探知下限濃度は、0.1ng/mL以下であることが分かった(図5の(A))。このシステムの分析特異性をテストするために、医療臨床の試験条件に近いヒト血清を試料運搬液及び標準試料希釈液として使用して測定した結果(図5の(B))、リン酸緩衝液を使用した場合(A)と非常に類似した濃度応答を示した。このことから、可逆反応性抗体である1B5基板のセンサーシステムは、測定感度と特異性の面で非常に優れており、更に、実際の医療臨床試験にも適用できると思われる。
【0075】
(実施例7)
−金ナノ粒子が標識された検出抗体を用いた信号増幅−
<実施例7.1 検出抗体−金ナノ粒子の重合体の製造>
金コロイド(直径:約30nm)懸濁液をクエン酸ナトリウム(sodium citrate)を還元剤として使用する標準方法で製造した(L.A.Dykman, A.A.Lyakhov, V.A.Bogatyrev,S.Y.Chchyogolev.Colloid,60,700,1998)。
具体的には、ガラスフラスコに3次脱イオン水1,000mLを入れた後、ここに1%塩化金溶液(tetrachloroauric acid)20mLを添加した。反応を助けるために、ホットプレートを使用して溶液を沸かし、金コロイドを作製するために、還元剤として、0.2μmのフィルターを使用して濾過した1%クエン酸ナトリウム溶液40mLを添加した。クエン酸ナトリウムの添加直後に、溶液は、淡黒色から赤色に変化した。10分間加熱した後、反応を停止させ、常温で徐々に冷却させた後、冷蔵保管しながら、以降の実験に使用した。
製造された金ナノ粒子懸濁液(1mL)に0.5Mのカーボネート緩衝液(pH9.6;1μL)を入れて、pH8.0程度に調整した。この溶液に、非可逆反応性抗体である20E7(図2参照)を10mMのリン酸緩衝液(PB;NaClを含まない)で150μg/mLの濃度(100μL)で希釈して添加した。室温で1時間反応させた後、5%カゼインが含まれているPB(カゼイン−PB;122μL)を添加し、室温で更に1時間反応させた。この混合物を16,000rpmで30分間遠心分離した後、上澄み液は捨てて、沈殿物にカゼイン−PB(400μL)を入れて溶解させた。再び16,000rpmで30分間遠心分離した後、上澄み液を捨てて、金粒子を基準に20倍濃縮されるように、カゼイン−PB(50μL)を入れて溶解させた。
【0076】
<実施例7.2 信号増幅の採択時の分析システムの濃度応答>
分析物質であるアルファ2−マクログロブリンをヒト血清で希釈して、0〜10ng/mLの濃度範囲の標準試料を製造し、各試料は、センサーシステムに搭載されたセンサーチップ内に注入される前に、実施例7.1で製造した探知抗体−金ナノ粒子の重合体10ng/mLと室温で10分間反応させた。この反応混合物(150μL)を実施例6で製造したセンサーチップ内に10μL/分の速度で900秒間注入して付着反応を誘導した後、ヒト血清を同じ流速で120秒間注入して、脱着反応を誘導した。各試料に対する分析が完了した後、実施例4でのように、センサーの表面を再生させた。図5において、前記信号増幅段階を採択した分析システムの濃度応答は、実施例6で求めた非標識センサーシステムの濃度応答と比較して、顕著に増加した形態を示しており、実際に分析感度は、0.1ng/mL水準(図5の(B)を参照)から0.001ng/mL水準に約100倍向上したことが分かった。
本発明で例示した信号増幅方法を用いれば、試料内に、非常に低い濃度で存在する分析物質も測定が可能であるので、可逆反応性抗体を用いた連続探知方法は、様々な分析物質の測定に広く適用できる。
【0077】
(実施例8)
−流速減少時の解析システムの濃度応答パターン−
医療臨床試料の場合、特にその使用量を最小化することが必要であるので、マイクロ流体の流れ速度を、先行の実験条件の1/10に減速して、分析システムの濃度応答を求めた。実施例6と同じセンサーチップを使用しており、流速の減少を除いて、同じ条件下で実験を行った。試料運搬液と標準試料希釈液としてヒト血清を使用し、流速は1μL/分に維持した。標準試料は、0〜100ng/mLの濃度範囲で用意し、試料(15μL)をセンサーチップ内に注入して、900秒間付着反応を誘導した後、リン酸緩衝溶液を注入して、420秒間、脱着反応を誘導した。標準試料を低濃度から高濃度の順に分析した後、再び低濃度に帰るという循環形態で分析した。分析システムの運営とデータの編集は、実施例4と同様に行っており、分析が完了した後は、提示のようにセンサーの表面を再生させた。
図1において、分析物質濃度の増減に伴うセンサーの応答は、分析物質の濃度に比例しており(図7の(A))、その応答パターンを、流速が10倍速い条件で得た結果(図5の(B))と比較してみると、分析感度は、約0.1ng/mL、そして応答時間は、640秒(最終回答の95%基準)と一定に維持されることが分かった。また、濃度応答をグラフとして作成して比較してみると(図7の(B))、テストされた流速範囲で顕著な差が示していなく、分析物質の濃度の増加時及び濃度の減少時に測定した濃度応答間にも差がなかった。特異事項として、流速が相対的に速い時(10μL/分)、高濃度の標準試料の分析時に現れた過剰応答の現象(図5、分析物質の濃度は、10ng/mLでの応答を参照)が、流速の減少時(1μL/分)に大幅に緩和されたことが分かった(図7、分析物質の濃度は、10ng/mL又はそれ以上での応答を参照)。
【0078】
(実施例9)
−指数的な濃度変化に対する連続測定−
前記実施例では、可逆反応性抗体の付着及び脱着反応を測定するために、各試料の分析間に試料運搬液(分析物質を含まない)が注入されるリセットモードを使用する一方で、本実施例では、可逆反応性抗体のリサイクルを例示するために、試料の連続分析モードを使用した。センサーチップは、実施例6で製造したものを使用しており、マクログロブリンをヒト血清で希釈して、0.01〜10,000ng/mLの範囲の標準試料を用意した。標準試料を順次1μL/分の流速でセンサーチップ内に注入し、分析物質の濃度が、900秒ごとに階段式に10倍ずつ増加して減少する循環変化2回繰り返しに対して、センサーからの濃度応答を連続的に求めた。センサーシステムの連続モードへの運営は、センサーシステムメーカーで設定したリセット分析工程とは異なり、試料の注入は、提供された注入口を通らず、試料運搬液供給通路を用いて行われた。試料の連続供給時、標準試料の注入中に絶えたり、空気が入らないように、以前の残りの試料溶液にあらかじめ定めた分析物質の濃縮液又は希釈液を添加して、次の試料の標準濃度で調整し、濃度が均一であるように持続的に混合した。
【0079】
分析の後、流出された試料は、分取装置で収集し、各分画は、マイクロウェルプレートを固定化マトリックスとして用いるサンドイッチ酵素免疫分析により標準試料の分析物質の濃度を確認した。分析方法は、10mMのリン酸緩衝液(140mMのNaClを含む;pH7.4)で希釈されたアルファ2−マクログロブリンに対して非可逆反応性である3D1モノクローナル抗体(1μg/mL;100μL)を各マイクロウェルに加えて固定させた。洗浄後、0.5%のカゼイン含有10mMのリン酸緩衝液(カゼイン−PBS)を200μL入れ、固定されていないウェルの残りの表面をブロッキングした。再度洗浄後、分取装置によって時間別に収集された分画溶液(30μL)に0.5%カゼイン、及び0.1%ツイン含有10mMのリン酸緩衝液(カゼイン−ツイン−PBS;70μL)を追加に注入して、全体試料(100μL)を抗体が固定されているウェルに入れて反応させた。洗浄後、アルファ2−マクログロブリンに対して非可逆反応性を持つ20E7のモノクローナル抗体にHRPが結合された20E7−HRP重合体(1μg/mL;100μL)をカゼイン−ツイン−PBSで希釈して、ウェルに注入して反応させた。再度洗浄後、HRPの基質溶液(実施例1を参照)を各ウェルに加えて酵素反応を行った後、15分間に2Mの硫酸を添加して停止させた。各ウェルで発生した発色信号は、マイクロプレート読み取り装置(VERSAmaxTM、 Molecular Devices社、米国)を用いて、450nmの吸光度で測定した。
【0080】
連続測定のために、事前に計算して設定した各標準試料の濃度を連続測定し、収集して、前記のように免疫分析を通じて実際の濃度を確認した結果、計算値と分析結果間の10%以内の差があったので、計算値をグラフの作成に用いた。与えられたマイクロ流体の流れ速度(1mL/分)でセンサー内に注入される標準試料内の分析物質濃度の増加又は減少に対するセンサーの応答は、ともに15分以内に平衡状態に達し、2回繰り返して循環する際に高い再現性を示した(図8の(A);0.01〜100ng/mLの濃度範囲でテストされた結果)。このような連続測定方式で測定したセンサーの濃度応答を示した標準曲線(図8の(B))は、リセットモードで測定した曲線と若干の差が生したが、これは、センサーシステムの運営の違いによるものと判断される。このような結果から、分析物質濃度の変化に対する連続測定が実際に可能であることが分かり、臨床試験への応用可能性も提示した。
【0081】
(実施例10)
−算術的な濃度変化に対する連続測定:小児腎臓癌マーカーの臨床濃度範囲への適用−
分析物質の種類に従って、発症や症状の発現時に、濃度の増減変化パターン(指数的あるいは算術的)が異なることがあり得るので、2倍、又はそれ以下に増加して減少する算術的な濃度変化に対するセンサーの濃度応答を、実施例9でのように連続モードで測定した。本実験では、モデル分析物質として選択したアルファ2−マクログロブリンをバイオマーカーとして使用できる小児腎臓癌の診断を究極的に念頭に置いた最適条件を使用した。つまり、血清試料の使用量を最小化できるように、分析物質をカゼイン−PBSで希釈して、標準試料を製造し、その濃度範囲は、分析性能を最適な状態で保持できる1〜20ng/mLの範囲で決定した。各標準試料を1,800秒間隔でセンサーチップ内に注入し、流速は、1μL/分に調節した。
【0082】
図9では、算術的な水準の連続的な濃度変化に対するセンサーの応答は、指数的な変化に関するものと同様に、迅速な応答時間と連続測定の再現性を示した。更に、小さな濃度変化に対しても敏感かつ迅速に反応することからみて、可逆反応性抗体基板のバイオセンサーは、今後、非常に正確な分析を必要とする分析物質の測定に広く適用できるものと期待される。特に、アルファ2−マクログロブリンの臨床的に有効な濃度変化の範囲は、3〜10mg/mLで、血清試料をそのまま連続測定に使用する場合、一日に1.44mL(1μL/分の注入速度基準)がかかる。
したがって、これらの試料量を最小化することが必要なので、本実施例では、106倍低い濃度範囲で希釈して、実際の臨床テストの際に、1.44nL/日の程度の極小量の血清の消耗を可能にした。更に、この解析条件下で、分析物質の濃度変化に対する信号変化幅の増加、つまり、分析精度も向上させることができる。
【産業上の利用可能性】
【0083】
以上述べたように、本発明によれば、一定量の可逆反応性の認識成分を連続的にリサイクルして、分析物質の濃度変化をリアルタイムに測定することができる。これは、分析物質の濃度に応じて迅速に可逆的に反応する抗体をリサイクルすると、既存の使い捨ての診断チップに比べて、構成部品及び製作方法を画期的に単純化できることを意味する。また、病気や症状に対するリアルタイムモニタリングを可能にするため、慢性疾患や高危険群患者への継続的な監視が可能になる。それだけでなく、人工臓器制御装置、生物テロ作用剤の連続探知システム製品は、人獣共通感染症の病原体の連続探知システム製品、環境汚染源の連続監視システム製品、生物工程、連続モニタリングシステム製品、食品生産工程の連続モニタリングシステム製品などに適用できる。
【符号の説明】
【0084】
10 捕獲認識成分
11 分析物質
12 非標識センサー
13 探知認識成分
14 標識物質
15 標識センサー
16 半透膜
17 認識反応セル
【技術分野】
【0001】
本発明は、リアルタイム連続検出装置に関し、より具体的に、試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含む、リアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分及び試料内の分析物質−捕獲認識成分の結合体から発生した信号を探知するセンサーを含むことを特徴とする、分析物質のリアルタイム連続検出装置に関する。
【背景技術】
【0002】
保健医療分野だけでなく、食品、環境、獣医、国防といった様々な分野において、構造が複雑な有機物質、特に蛋白質、ホルモン、核酸、細胞などの探知に、抗原−抗体付着と核酸接合のような独特の認識反応を用いた分析方法が使用されている。これは、生体認識反応の高い特異性と親和力、そして分析原理の普遍性に起因し、これを応用して様々な形態の解析システムが開発されてきた。
【0003】
その例として、免疫分析システムの開発動向を見ると、マイクロタイタープレート(microtiter plate)を固定化マトリックスとして使用する固相免疫分析(例えば、enzyme−linked immunosorbent immunoassays;ELISA)方法の開発により様々な診断や分析分野に応用するきっかけとなっている(非特許文献1及び非特許文献2参照)。また、細孔性メンブレイン基板の無試薬属性診断キットの発売は、家庭などの場所で制限なく、免疫分析を可能にした(非特許文献3、非特許文献4、非特許文献5、非特許文献6、及び非特許文献7参照)。
【0004】
一方で、病院の臨床試験室など、専門機関で精密検査に使用する自動化診断機器が普及されており、核酸配列を決定したり、タンパク質の発現の程度を定量的に分析できるバイオセンサーアレイチップ、そして、更には、微細自動分析のために、試料の前処理など、順次連続プロセスを行うラップオンアチップの開発が盛んに研究されている(非特許文献8参照)。実用化の例として、CombiMatrix社(米国)のジノミックス研究用Custom Array、Nanosphere社(米国)の単一核酸変異(SNP)測定用のVerigene ID platform、AffyMetrix社(米国)のGeneChip System、Integrated NanoTechnologies社(米国)の現場分析用のBioDetect Test Cardなどが紹介されている。
【0005】
近年、ナノテクノロジーとバイオテクノロジーの技術が融合したナノバイオセンサー技術が、21世紀の最先端技術として脚光を浴びており、これに関連する源泉技術を確保しようと、国内を含む全世界的に研究が盛んに進められている。複数の機関でバイオセンサーの超高感度技術の開発に集中しているが、その技術水準がまだ初歩段階にあるナノセンサーの概念(非特許文献9及び非特許文献10参照)、及び振動型カンチレバー基板の免疫分析(非特許文献11参照)などが報告されている。
【0006】
このような、ほとんどの既存の分析システムに使用される抗体をはじめとする認識成分は、分析物質−認識成分の結合後、その結合体を分離するために、洗浄工程が不可欠である。この場合に形成された結合体の損失を最小化するために、脱着速度が非常に遅い認識成分を使用しなければならないので、一度結合した分析物質が認識成分から解離されず、ほとんどのセンサーを連続的に使用できずに、使い捨て用のみに使用する。
【0007】
最近になって、グルコースモニタリングにおいて、無侵襲センシング方法に対する研究が非常に盛んである(非特許文献12参照)。特に、病院の重症患者の病気に関連する指標物質に対する連続的な測定への要求が高まっているが、技術的な問題から要求を満たしていない。しかし、分析物質−認識成分間の反応を可逆的に運用できる場合、様々な疾患に対して、リアルタイムの連続モニタリングが可能になる。
【0008】
分析物質に対する連続測定が可能な場合、将来的には、人体に着用したり、体内の移植が可能なバイオセンサーを開発することができる。これらのセンサーを使用すると、生体情報を連続的に測定し、診断することにより、疾患が発生する確率が相対的に高い高危険群(慢性疾患者、高齢者など)の患者に対して、感染症や成人病などの好発疾患を早期に管理乃至監視することが可能になる。
したがって、これらの分析道具は、ユビキタスコンピューティング環境を基に、「いつ」、「どこでも」医療サービスを提供するヘルスケア環境を意味するU−ヘルスケアの時代で、将来の予防医療のための必須道具になると判断される(非特許文献13参照)。このようなU−ヘルスケアが実現されれば、病気の後に対応する「病院/治療中心」の既存のパラダイムから脱皮できるだけでなく、慢性疾患者や高齢者などが長期入院をする必要はない。
【先行技術文献】
【非特許文献】
【0009】
【非特許文献1】Irina Ionescu−Matiu等,J Virol Methods,Vol.6(1)、Page41-52,1983
【非特許文献2】Christopher Heeschen等、Clinical chemistry、Vol.45(10),Page 1789-1796,1999
【非特許文献3】R.Chen等,1987,Clin.Chem.Vol.33,Page 1521-1525
【非特許文献4】MPA Laitinen, 1996, Biosens.Bioelectron., Vol.11, 1207-1214
【非特許文献5】S.C.Lou等,1993,Clin.Chem.,Vol.39,619-624
【非特許文献6】S.H.Paek等、Methods Vol.22,Page 53-60,2000
【非特許文献7】S.H.Paek等,BioChip J.Vol.1,Page 1-16,2007
【非特許文献8】Kyeong−Sik Shin等、Analytical Chimica Acta Vol.573-574,Page 164-171,2006
【非特許文献9】Yi Cui等、Science,Vol.293,Page 1289-1292,2001
【非特許文献10】Jong−in Hahm等、Nano lett.,Vol.4,Page 51-54,2004
【非特許文献11】Y Arntz等、Nanotechnology,Vol.14,Page 86-90,2003
【非特許文献12】Ronald T.Kurnik等,Sensors and Actuators B:Chemical,Vol.60,Page 19-26,1999
【非特許文献13】Anthony PF Turner,Nature Biotechnology,Vol.15、Page 421-421,1997
【発明の概要】
【発明が解決しようとする課題】
【0010】
そこで、本発明者らは、前記従来技術の問題点を克服するために鋭意研究を重ねた結果、分析物質のリアルタイム検出装置に可逆反応性の捕獲認識成分を導入し、これを連続的にリサイクルする場合、反応に関与する分析物質の濃度に応じて、リアルタイムに信号を発生させて測定することにより、分析物質に対する連続測定が可能であることを確認し、本発明を完成するに至った。
【0011】
したがって、本発明の主な目的は、可逆反応性の捕獲認識成分が導入され、これを連続的にリサイクルできる分析物質のリアルタイム連続検出装置を提供することにある。
本発明の他の目的は、前記リアルタイム連続検出装置を用いた分析物質のリアルタイム連続検出方法を提供することにある。
また、本発明の更に他の目的は、前記リアルタイム連続検出装置に使用される可逆反応性の捕獲認識成分の選別方法を提供することにある。
【課題を解決するための手段】
【0012】
本発明の一様態によれば、本発明は、試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含む、リアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分10及び試料内の分析物質11−捕獲認識成分10の結合体から発生した信号を探知するセンサーを含むことを特徴とする、分析物質のリアルタイム連続検出装置を提供する(図1の(A)を参照)。
【0013】
本発明において、前記「分析物質」とは、試料の分析サイトに含まれているセンサーを使用して検出しようとする目的で、センサーの表面に注入する物質を意味する。前記「捕獲認識成分」とは、前記センサーのセンサーチップ上に固定化されており、分析物質と特異的に結合可能な物質を意味する。例えば、分析物質が、抗原又はリガンドである場合、捕獲認識成分は、各々その抗原に対する抗体、又はそのリガンドに対する受容体であり、反対に、分析物質が、抗原に対する抗体又はリガンドの受容体である場合、捕獲認識成分は、各々その抗原又はリガンドである。
【0014】
本発明において、前記可逆反応性の捕獲認識成分は、脱着及び付着速度が共に速い反応力学特性を持ち、かつ高親和力を持つ認識成分(例えば、抗体)を意味し、高い付着及び脱着速度定数値を有した捕獲認識成分を使用すれば、連続的に使用しても、高い分析感度を維持することができる。
ここで、「親和力」は、平衡付着定数として表示することができるが、平衡付着定数(KA)は、付着速度定数(ka)/脱着速度定数(kd)と定義される。本発明では、可逆反応特性と高親和力を同時に有する抗体を使用することにより、「高感度のリアルタイム連続検出」が可能になる。
【0015】
もし、可逆反応特徴のためだけに、親和力が、1×106L/mol以下の認識成分を使用することになると、検出装置の測定感度が、mmol/L水準に非常に低くて、ほとんどの病気や症状の徴候を示すバイオマーカー分析物質の検出には適用し難しいという問題がある。これは、認識成分の親和力が低いほど、測定可能な分析物質の濃度範囲が高くなるためである。例えば、可逆反応性の認識成分(例えば、抗体)の付着速度定数を下げたり、一定に維持しながら、脱着速度定数を高め過ぎた成分を使用すれば、親和力が1×106L/mol以下に低くなる。
したがって、本発明でのように、高親和力の可逆反応性の認識成分を得るためには、特別な選別方法が導入されなければならない。例えば、固定された抗原と認識成分とが結合した後、中性緩衝液で洗浄する際に、残存活性が認識成分濃度に比べて低い値を有する認識成分を一次選別し(実施例1を参照)、これに対して、再び抗原が固定されたセンサー(例えば、表面プラズモン共鳴センサー)を用いた付着速度定数、及び脱着速度定数を測定して、二次選別を実施することにより(実施例3を参照)、高親和力の可逆反応性の認識成分を効率よく生産することができる。
【0016】
したがって、前記可逆反応性の捕獲認識成分が、本発明の目的と符合するためには、速い反応力学特性を持ち、かつ平衡付着定数が1×107L/mol以上の高親和力を維持することが好ましく、より好ましくは、1×108L/mol〜1×1012L/molであり、更に好ましくは、1×109L/mol〜1×1012L/molの高親和力を維持することが好適である。
【0017】
本発明のリアルタイム連続検出装置において、前記可逆反応性の捕獲認識成分は、好ましくは、試料内の分析物質との反応時に、付着速度定数(ka)は、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、脱着速度定数(kd)は、1×10−3sec−1〜1×10−1sec−1の可逆反応特性を持ち、同時に2つの速度定数の割合(ka/kd)が、1×108L/mol以上の平衡付着定数(KA)を有することを特徴とする。
このような特徴を有した捕獲認識成分を連続検出装置に使用すれば、両付着及び脱着速度定数が共に高いため、検出装置の応答時間が早くて、分析物質のリアルタイム検出が可能になるだけでなく、平衡付着定数もまた高いため、高度の測定感度を提供するという利点がある。しかし、範囲から外れる場合、特に、脱着速度定数が更に低い場合は、捕獲認識成分と結合した分析物質の解離が難しくて、連続測定時に非常に長い応答時間がかかったり、解離を加速させるために、苛酷条件(例えば、酸性pH)の使用が不可避であり、リアルタイムの検出が根本的に不可能になる。また、付着及び脱着速度定数が、所定の範囲にあっても、平衡付着定数が設定された範囲よりも低い場合は、上述したように、分析感度が低くなって、実用的な応用が極めて制限される。
【0018】
前記可逆反応性の捕獲認識成分において、特定の分析物質に対する典型的な認識成分として、モノクローナル抗体は、一般的に分析物質に対して動物を免疫化するハイブリドーマ方法(Kohler.G等,Nature,Vol.256,Page 495−497,1975)、遺伝子組換え方法(HP Fell等,PNAS,Vol.86,Page 8507-8511,1989)、phage display方法(Nicholas A.Watkins等,Vox Sanguinis,Vol.78,Page 72-79,2000)などを通じて生産可能であるが、可逆反応性の抗体を選別するためには、特別な処理が要求される。
【0019】
抗体の選別方法として広く使用されている固相免疫分析では、反応後に残存する過剰成分を除去するために洗浄工程を使用するので、洗浄時に、反応結合体が容易に解離される可逆反応性抗体の場合は、選別が困難である。本発明では、これらの問題を解決するために、一例として、反応及び洗浄時にリアルタイムに反応結合を追跡できる表面プラズモン共鳴センサーのような非標識センサー付の選別システムを使用した。
前記分析物質をセンサーの表面に固定した後、生産された抗体を運搬溶液に希釈して連続的に注入した後、同一の運搬溶液で洗浄すれば、表面での抗原−抗体間の付着及び脱着反応によって形成され、解離される結合体の密度が、センサーからリアルタイムに測定される。
【0020】
本発明の具体的な一例では、前記可逆反応性の捕獲認識成分を選別するために、表面プラズモン共鳴センサー基板の選別システムを用いた。適宜に希釈された一定濃度の抗体溶液をシステム内に注入すると、結合反応によって信号が時間によって増加するが、洗浄時に、つまり、抗体濃度「0」で、結合体密度の変化は、各抗体の可逆反応特性に応じて変化する(図2を参照)。既存のほとんどの免疫分析では、洗浄工程を経る間、脱着されない非可逆性抗体(図2、20E7)が、容易に脱着される可逆性抗体1B5よりも絶対的に好まれた。これは、洗浄後、固相に残存した抗原−抗体結合体から分析物質の濃度に比例した信号を発生することができるからであるが、このような分析システムでは、抗体をリサイクルしにくく、連続測定が根本的に不可能である。しかし、試料内の分析物質の濃度と力学的平衡状態で付着及び脱着が迅速な可逆反応性抗体1B5を使用すれば、抗体を連続的にリサイクルすることができ、これにより、分析物質の連続モニタリングが可能になる。
【0021】
また、免疫分析の際に、抗体の反応特性の差異による連続測定の実現可能性の可否は、循環の繰り返して測定してみると、更に明らかになる(図3参照)。非可逆反応特性を示す抗体(図3、20E7;ka=1.10×104Lmol−1sec−1、kd=1.80×10−7sec−1)の場合、抗体の供給後、一定時間の間、固定された抗原と継続的な付着反応を示し、洗浄時には、脱着が完了されないので、循環の繰り返しに従って、抗原−抗体反応結合体は、次第に累積して増加するパターンを示す。その一方で、可逆反応特性を示す抗体(1B5;ka=4.13×106Lmol−1sec−1、kd=3.61×10−3sec−1)の場合、抗体の供給後に、信号が急激に増加して付着反応が平衡に達し、かつ洗浄時に、すぐに脱着され、信号が初期の基準線に戻ってくるが、このような付着/脱着可逆反応形態は、循環の繰り返し時にも高い再現性を示す。
【0022】
可逆反応性を示す抗体は、抗原−抗体結合体の脱着速度が速くて、親和力(平衡付着定数、KA)の減少による分析感度の低下が心配されるが、付着及び脱着速度が共に速ければ、親和力には影響を与えない。実際に、平衡付着定数(KA)=付着速度定数(ka)/脱着速度定数(kd)であるので、上述した方法により、適切な反応力学特性、つまり、高い付着及び脱着速度定数値を有した抗体を選別すれば、高い分析感度を維持することができる。これにより、高い感度を維持するためには、一般的に、KA>1×108Lmol−1の条件の抗体が必要とされるので、高親和力の可逆反応性抗体は、ka>1×105Lmol−1sec−1、及びkd>1×10−3sec−1の特性を有した抗体と定義することができる。
【0023】
一方、可逆反応性抗体の親和力をテストする他の方法として、抗体を標準濃度で連続して希釈して、表面プラズモン共鳴センサー上に固定されている抗原と反応させ、信号感知が可能な最低抗体濃度を決定してみると、抗体の親和力の予測が可能である(図4を参照)。特に、可逆反応性抗体1B5が、pg/mLの濃度範囲以下でも抗原と反応することが測定されているが、この結果は、既存の非可逆性抗体の場合と比較しても、非常に高い親和力を示したものである。更に、図4の結果から、使用された可逆反応性抗体は、比較的幅広い濃度範囲において固定された抗原とは異なる平衡状態で反応することからみて、バイオセンサーの製作に非常に適していることが分かる。
【0024】
本発明のリアルタイム連続検出装置において、前記可逆反応性の捕獲認識成分10は、試料内の分析物質11である生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質若しくは国防化生放測定物質と特異的に結合できる抗体、受容体、核酸、酵素、アプタマー、ペプチド又は分子印刷人工膜であることを特徴とする。
【0025】
本発明のリアルタイム連続検出装置において、前記センサーは、分析物質11−捕獲認識成分10の結合体から発生した信号を直接探知する非標識センサー12(図1の(A)を参照)、又は分析物質11−捕獲認識成分10の結合体の密度に比例して信号を発生する標識物質14を経由して探知する標識センサー15であることを特徴とする(図1の(B))。
【0026】
本発明において、前記非標識センサーは、分析物質−捕獲認識成分の結合体に比例して変化するセンサー上の質量、振動子の抵抗、電荷分布の変化による表面の歪み、エネルギーの伝達などを信号として測定する。センサー表面の結合体の質量変化に従って、光屈折の各差を示す表面プラズモン共鳴(surface Plasmon resonance;SPR)センサー(Robert Karlsson等、Journal of Immunological Methods,Vol.145,Page 229-240,1990)、振動子の抵抗や電荷分布を感知するカンチレバー(cantilever)センサー(Hans−Jurgen Butt、Journal of Colloid and Interface Science,Vol.180,Page 251-260,1996)、光導波路(evanescent)センサー(R.G.Eenink等、Analytica Chimica Acta,Vol.238,Page 317-321,1990)、更には、ナノ次元の線や間隔を用いたナノセンサー(Fengli Qu等、Biosensors and Bioelectronics,Vol.22,Page 1749-1755,2007)などが、非標識センサーとして使用されることができる。
また、前記標識センサーは、分析物質−捕獲認識成分の結合体に比例して信号を発生するために、標識物質が標識された探知認識成分を追加に反応させた後、標識物質からの信号を測定する。
【0027】
本発明において、前記「探知認識成分」とは、標識物質が、物理的又は化学的に結合されており、分析物質と特異的に反応可能な物質を意味する。ここで、探知認識成分が反応する分析物質の分子上の位置は、捕獲認識成分が反応する部位と異なり、両成分は、分析物質と同時に反応できる。
信号を発生する標識物質としては、例えば、蛍光体、発光体、酵素、金属粒子、プラスチック粒子、磁性粒子等が使用される。これから発生する蛍光、発光、発色、電気化学、磁場などを探知するセンサーが、標識センサーとして使用されることができる。
つまり、前記非標識センサーを用いる場合は、試料に含まれている分析物質は、流体チャンネルを通じて連続的にシステム内に流入され、捕獲認識成分と反応し、標識センサーを用いる場合は、試料内の分析物質は、標識物質が結合された探知認識成分と事前に反応した後、流体チャンネルを通じて連続的にシステム内に流入されて捕獲認識成分と反応する。
【0028】
本発明のリアルタイム連続検出装置において、前記試料の分析サイトは、試料内の分析物質11だけを選択的に透過させうる半透膜16で区切られ、捕獲認識成分10が固定されているセンサーの表面側に認識反応セル17を形成することを特徴とする。
前記認識反応セル17は、標識センサー15を用いる場合、前記認識反応セル17内に半透膜16を通過できないほどの大きさの標識物質14と結合した探知認識成分13を閉じ込めて、リサイクルすることを特徴とする。
【0029】
また、前記認識反応セル17内の探知認識成分13も捕獲認識成分10と共に連続的にリサイクルされるために、可逆反応特性を持つことを特徴とする。
具体的には、前記試料の分析サイトは、捕獲認識成分が固定されているセンサーの表面側を半透膜で区切って認識反応セルを形成でき(図1の(C)、(D))、試料に含まれている分析物質は、大きさが小さくて、この半透膜を介してセル内に拡散伝達されるが、試料内の大きさが大きい不純物は濾過されて、センサー表面の汚れを防ぐことができる。このような認識反応セルの設置は、特に標識方式の解析システムの場合(図1の(D))、大きさが大きい標識物質と結合した探知認識成分をセル内に閉じ込めてリサイクルする効果も提供する。
【0030】
本発明の他の様態によれば、本発明は、下記の段階を含む前記リアルタイム連続検出装置を用いた分析物質のリアルタイム連続検出方法を提供する。
(a)分析物質を含む試料を前記試料の流入チャンネルを通じて試料の分析サイト内に注入する段階と;
(b)前記分析物質を試料の分析サイト内の可逆反応性の捕獲認識成分10と結合させる段階と;
(c)前記分析物質と捕獲認識成分との結合によって発生する信号をセンサーで探知する段階と;
(d)試料の継続的な流入や洗浄液の流入により、前記分析物質と捕獲認識成分との結合が脱着して、分析物質が、前記試料の排出チャンネルを通じて排出される段階と;
(e)前記脱着された捕獲認識成分を連続的にリサイクルして、前記(b)乃至(d)の段階を繰り返すことにより、試料内の分析物質の濃度変化をリアルタイムに測定する段階。
【0031】
本発明のリアルタイム連続検出方法において、前記(c)の段階において、分析物質−捕獲認識成分の結合体から発生した信号を、非標識センサーを用いて直接探知するか、あるいは、分析物質−捕獲認識成分の結合体の密度に比例して信号を発生する標識物質を経由して、標識センサーを介して信号を測定することを特徴とする。
【0032】
本発明において、前記非標識センサーを用いる場合、試料に含まれている分析物質は、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応することを特徴とする。
【0033】
本発明において、前記標識センサーを用いる場合、試料内の分析物質が、標識物質が結合された探知認識成分と事前に反応した後、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応するか(連続流れ露出タイプ)、試料内の分析物質が、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入された後、認識反応セル内の標識物質と結合された探知認識成分及び捕獲認識成分と反応する(認識反応セルタイプ)ことを特徴とする。
【0034】
本発明において、前記探知認識成分は、連続流れ露出タイプの場合、分析物質と事前に反応して供給されるので、結合安定性の高い非可逆反応特性を持つか、あるいは、認識反応セルタイプの場合、捕獲認識成分と共に探知認識成分も連続的にリサイクルされるために、可逆反応特性を持つことを特徴とする。
【0035】
本発明において、認識反応セルタイプの標識センサーを用いる場合、近接していた蛍光物質(標識物質)と蛍光エネルギー受容体との間のエネルギー伝達が、捕獲認識成分と分析物質との反応によって妨げられ、蛍光信号が発生する原理を用いるか、又は酵素分子(標識物質)上に固定されている分析物質と認識成分とが結合すれば、活性が抑制されることが知られている酵素を、標識物質を用いて捕獲認識成分をセンサー上に固定させず、認識反応を液相で行えることを特徴とする。
【0036】
本発明の他の様態によれば、本発明は、下記の段階を含む前記リアルタイム連続検出装置に使用される可逆反応性の捕獲認識成分の選別方法を提供する。
(a)捕獲認識成分を用意する段階と;
(b)前記捕獲認識成分をセンサーの表面に固定されている分析物質と結合させる段階と;
(c)前記捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(d)洗浄液の流入により、前記捕獲認識成分と分析物質との結合を脱着させる段階と;
(e)前記脱着後、残りの捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(f)前記(e)の段階での探知信号は、前記(c)段階での探知信号よりも低くなる捕獲認識成分を選択する段階。
【0037】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記センサーは、表面プラズモン共鳴センサー、カンチレバーセンサー、光導波路センサー、光干渉センサー、及びナノセンサーから選ばれる非標識センサーであることを特徴とする。
【0038】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記捕獲認識成分は、センサーの表面に固定されている分析物質との反応時に、付着速度定数(ka)は、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、そして、脱着速度定数(kd)は、1×10−3sec−1〜1×10−1sec−1の範囲の可逆反応特性を持ち、同時に平衡付着定数(KA=ka/kd)が、1×108L/mol以上の高親和力を持つものを選択することを特徴とする。
【0039】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記(a)の段階において、前記捕獲認識成分は、運搬溶液で希釈して連続的に注入され、前記(f)の段階において、時間によって増加していた信号が減少する捕獲認識成分を選択することを特徴とする。
【0040】
本発明の可逆反応性の捕獲認識成分の選別方法において、前記(a)の段階において、前記捕獲認識成分は、洗浄液と循環繰り返して注入され、前記(f)の段階において、時間によって信号が増加した後、最初の基準線に戻ってくる信号パターンが繰り返される捕獲認識成分を選択することを特徴とする。
【0041】
以上で説明する本発明に係る分析物質のリアルタイム検出装置、これを用いた分析物質のリアルタイム連続検出方法、及びこれに用いられる可逆反応性の捕獲認識成分の選別方法を用いる場合は、以下のような利点を奏する。
バイオセンサーやバイオチップの製作において、本発明でのように、分析物質の濃度に応じて迅速に可逆的に反応する抗体をリサイクルすれば、既存の使い捨ての診断チップに比べて、構成部品及び製作方法が大幅に単純化される。これは、既存の装置又はシステムで試薬の供給及び除去のために要求されてきた多数のバルブやポンプが最小化され、実際に身体に着用が可能な小型のマイクロ流体の流れ方式の連続診断システムの具現が可能である。
【0042】
このような新しい概念の検出方法(又は診断方式)は、病気や症状に関するリアルタイムのモニタリングを可能にするので、現存するほとんどすべての免疫分析システムが抱えている、一度使用した後に廃棄する使い捨ての性能の限界を克服することができ、人体の慢性疾患や高危険群患者に対する連続的な監視が可能になる。更に、現在の診断システムにおいて診断結果を得るために時間がかかり、また、患者状態の感知データを実験室で分析する必要がある場合、診察時点と診療結果が出てくる時間との差が多くて、正確な病気の診断やタイムリーな治療に難しさが多いという問題を解決することができる。
【0043】
したがって、本発明で開発された、リアルタイム連続検出装置及びこれを用いた検出方法は、早期診断概念の新たな予防医学の手法として、病院で需要の現場を中心に移動する診療パラダイムの変化を満たし、慢性疾患者や高齢者などの高危険群の患者の監視が常時可能な連続診断機器の開発と実用化を可能にする。特に、平均寿命が延長される共に、出生率の減少により高齢化社会への進入が加速されてあり、これに加えて、食生活パターンの西欧化により、様々な慢性成人病疾患が広まっており、早期診断により、健康な生活を営むのに役立つ。連続診断方法は、特に、今後到来するU−ヘルスケア時代において、診断システムを、携帯電話、病院、住宅などに内蔵したり、身体に装着して、生体情報をリアルタイムに測定し、診断するための基盤源泉技術として活用できる。
【0044】
また、本発明のリアルタイム連続検出装置及びこれを用いた検出方法は、生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質や国防化生放測定物質などを分析するのに活用可能であり、産業分野別の製品群を例として纏めると、以下の通りである。医療診断産業では、高危険群(慢性疾患者、高齢者、重症患者)の連続診断システム製品、糖尿病患者の感染症連続診断システム製品、心臓血管患者の再発連続監視システム製品は、癌治療患者の再発連続監視システム製品、そして、便座の健康モニタリングシステム製品などが挙げられる。人工臓器産業では、人工膵臓制御システム製品などの人工臓器の制御などに適用することができる。公衆衛生及び防衛産業では、生物テロ作用剤の連続探知システム製品、そして、鳥インフルエンザウイルス及びSARSウイルスなどの人獣共通感染症の病原体の連続探知システム製品などに応用することができる。環境産業では、川、沿岸、海洋汚染の連続監視システム製品などが挙げられる。生物及び食品産業では、生物工程の連続監視システム製品と食品の生産工程の連続監視システム製品などに適用することができる。
【発明の効果】
【0045】
本発明によると、一定量の可逆反応性の捕獲認識成分を連続的にリサイクルして、分析物質の濃度変化をリアルタイムに測定することができる。本発明のリアルタイム連続検出装置は、生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質や国防化生放測定物質などを検出、又は、分析するのに活用可能なので、医療、公衆衛生、国防、環境、食品、獣医、バイオテクノロジー産業に応用することができる。
【図面の簡単な説明】
【0046】
【図1】図1は、本発明に係る試料の分析サイト内で捕獲認識成分10を連続的にリサイクルして、分析物質の濃度変化を測定する(A)連続流れ露出タイプの非標識センサー;(B)連続流れ露出タイプの標識センサー;(C)認識反応セルタイプの非標識センサー、及び(D)認識反応セルタイプの標識センサーを示す模式図である。
【図2】図2は、本発明に係る捕獲認識成分の例示として、ネズミのハイブリドーマのクローンから生産された可逆反応性を示す抗体1B5と、典型的な非可逆反応性を示す抗体20E7に対する付着及び脱着反応特性を解析するために、センサーの表面に抗原、即ち、分析物質(α2−マクログロブリンをモデルとして使用)が固定されている表面プラズモン共鳴センサーシステムを使って測定したグラフ、及びこのことから決められた速度定数と付着平衡定数との比較である。
【図3】図3は、図2のセンサーシステムを用いて、2つの抗体1B5及び20E7の反応特性の差異による連続測定の実現可能性の可否をテストするための循環繰り返し測定の結果を比較したグラフである。
【図4】図4は、図2のセンサーシステムを用いて、可逆反応性抗体である1B5の抗原に対する親和力をテストするために、抗体を連続して希釈して、濃度の増減に従って、センサー上に固定されている抗原と反応させて得た結果である。
【図5】図5は、可逆反応性抗体である1B5が、医療臨床用の診断に使用可能か否かを評価するために、1B5抗体をセンサーの表面に固定させた後、抗原、つまり、分析物質を濃度の増加に従って固定されている抗体と反応させ、試料運搬液として(A)リン酸緩衝液、及び(B)ヒト血清を用いて得た結果の比較である。
【図6】図6は、図5のセンサーシステムの分析感度を向上させるために、標識物質14として直径が30nmの金コロイド粒子と探知認識成分13として非可逆反応性抗体20E7との重合体を追加に導入して得た信号増幅結果である。
【図7】図7は、図5のセンサーシステムを用いて、試料の使用量を最小化するために、センサーチップ内へのマイクロ流体の流れ速度を先行の実験条件の1/10に減速した条件下で、分析物質濃度の増減によるセンサーの応答結果である。
【図8】図8は、可逆反応性抗体のリサイクルを例示するために、センサー表面へ抗体1B5が固定されている表面プラズモン共鳴センサーシステムを連続測定モードで運用して、分析物質(α2−マクログロブリン)の濃度が連続して10倍ずつ増加して減少する2回の反復的な変化に対して、センサーから求めた(A)濃度応答の結果、及び(B)グラフで示した標準曲線である。
【図9】図9は、図8のセンサーシステムを用いて、分析物質の濃度が2倍、あるいは、それ以下に増加して減少する算術的な濃度変化に対するセンサーの濃度応答の結果である。
【発明を実施するための形態】
【0047】
以下、本発明の可逆反応性の捕獲認識成分を用いたリアルタイム連続検出装置について更に具体的に説明する。
【0048】
(1)非標識センサーを用いたリアルタイム連続検出デバイスの構築例示
リアルタイム連続検出装置(又はリアルタイム連続検出システム)を実装する際に、可逆反応性の認識成分のほか、重要な要素の一つがセンサー技術である。上述したように、センサーの種類としては、大きく非標識センサーと標識センサーとに分けられ、連続診断システムの構築時に、プラズモン共鳴センサー、カンチレバーセンサー、又は光導波路センサーのような非標識センサーを用いることが理論的に単純化する。
【0049】
連続検出装置の構成は、非常に多様であるが、本発明の有用性を容易に説明するために、プラズモン共鳴センサーチップ上に、可逆反応性抗体1B5を固定して製作した非標識センサー基板の連続検出装置を、図1を参照して例として説明すれば、以下の通りである。
【0050】
非標識センサーにより、金属と遺伝媒体の界面で光によって発生する電荷密度波長である表面プラズモン共鳴を測定する方法が代表的である。このような表面プラズモン共鳴は、金属表面に非常に近接して相互作用するので、この領域での認識反応などによる光学特性の変化は、表面プラズモン共鳴を引き起こす光の入射角に影響を与えることになる(J. Homola等,Sens.Actuators B, Vol.54、Page 3-15,1999)。これにより、センサー表面での分析物質と認識成分間の反応により、表面プラズモン共鳴を起こす光の入射角の変化を信号として測定する。
表面プラズモン共鳴センサー12上に可逆反応性抗体1B5;10を固定して構成した連続検出装置(図1の(A))に、リン酸緩衝液で希釈して、各々異なる濃度の分析物質(アルファ2−マクログロブリン)が含まれるように製造した標準溶液を10μL/分、マイクロ流体の流れ速度で順次に注入すると、濃度に比例した応答信号がセンサーから発生する(実施例6を参照)。各標準溶液は、信号を毎度基準線に戻してから注入したし、与えられた条件の下で、測定感度は、0.1ng/mLの水準以下と敏感しただけでなく、濃度の応答時間は、最終応答水準の95%を基準に640秒程度と非常に迅速した(図5の(A))。分析特異度をテストするために、同じ濃度範囲の分析物質を、医療臨床試料のヒト血清で希釈して製造した後、同じ実験を繰り返した結果、ほぼ類似した濃度応答が得られたので(図5の(B))は、構築された連続検出装置は、医療臨床用の診断に使用することができる。
【0051】
また、分析感度を向上させる方法として、標識物質14と結合した探知認識成分13を追加に導入して、分析物質11と捕獲認識成分10との間の認識反応結合体の質量変化を増加させる信号増幅方法が利用できる。探知認識成分13として非可逆反応性抗体20E7を選択して、直径が30nmの金コロイド粒子と物理的に結合し、この結合体を分析物質標準溶液と事前に反応させた後、センサー内に注入して、センサーの濃度応答を測定した(実施例7を参照)。参考として、非可逆反応性抗体20E7は、分析物質について、可逆反応性抗体1B5と同時に反応できる。その結果、信号増幅方法を利用すれば、最小0.001ng/mLの分析物質の探知が可能であり、これにより、分析感度が約100倍向上することが分かった(図6)。
【0052】
医療臨床試料の場合、特にその使用量を最小化することが必要とされるので、マイクロ流体の流れ速度を、先行の実験条件の1/10(つまり、1μL/分、又は1.44mL/日)に減速しようとし、同じ条件の下で、分析物質濃度の増減によるセンサーの応答を測定した(実施例8参照)。センサーの濃度応答を測定した結果、分析感度(0.1ng/mL)と応答時間(640秒、最終応答の95%基準)は、マイクロ流体の流れ速度に関係なく一定に維持されることが分かった(図7の(A))。また、マイクロ流体の流れ速度の変化によるセンサーの濃度応答パターンにも大きな変化がなくて、流体の流れ速度が10倍異なる条件で求めた2つの濃度応答曲線は、ほぼ一致していることが分かった(図7の(B))。しかも、分析物質の濃度の増加時に測定した濃度応答と、濃度の減少時に測定した濃度応答との間にも差がなかった。
【0053】
図5から図7に示すように、可逆反応性抗体が固定されているセンサーチップを用いて、分析物質の濃度変化に対するSPRセンサーの応答を求めるために、濃度変化時ごとに、毎回、初期条件、つまり分析物質が不在の状態に戻した後、測定を開始する「リセットモード」を使用した。
可逆反応性抗体のリサイクルを例示するために、「連続モード」を使用したが、分析物質の濃度が15分ごとに階段式に10倍ずつ増加して減少する2回の反復的な変更について(0.01ng/mL〜100ng/mLの範囲)、センサーから濃度応答を連続的に求めた(実施例9を参照)。与えられたマイクロ流体の流れ速度(1μL/分)でセンサー内に注入される分析物質の変化された濃度で、センサーの応答は15分以内に平衡状態に達し、2回の繰り返し時に高い再現性を示した(図8の(A))。このような連続測定方式で測定したセンサーの濃度応答を示した標準曲線(図8の(B))は、「リセットモード」で測定した曲線と多少違いがあることが分かるが、これは、センサーシステムの運用方式の違いによるものと判断される。
【0054】
分析物質の種類に従って、発症や症状の発現時に、濃度の増減変化パターン(指数的あるいは算術的)が異なることがあり得るので、2倍、又はそれ以下に増加して減少する算術的な濃度変化に対するセンサーの濃度応答を「連続モード」で測定した(実施例10を参照)。指数的な変化に対する応答と同様に、センサーは、算術的な分析物質の濃度変化に対しても類似した分析性能を示した(図9)。更に、小さな濃度変化に対しても敏感かつ迅速に反応することからみて、可逆反応性抗体基板のバイオセンサーは、今後、非常に正確な分析を要求する分析物質の測定に広く適用できると期待される。
【0055】
本発明では、連続診断を例示するための分析物質として、アルファ2−マクログロブリンを選択し、この物質に対して特異な可逆反応性の抗体を生産して、連続診断手法を例示した。アルファ2−マクログロブリンは、3種類の他の病気、特に新症候群の治療及び再発の確認、アルツハイマーの早期診断、そして人工臓器移植後の炎症反応と合併症の臨床診断にバイオマーカーとして使用することができる。
また、新症候群は、約90%が小児にのみ発生する病気で、尿にタンパク質が混じって出てくる腎臓疾患であって、腎臓の糸球体の異常により蛋白質が失われる(Daniel A.Blaustein等,Primary Care Update for OB/GYNS,Vol2,Page 204-206,1995)。患者は、身体や足に浮腫が生じて訪れる場合が大部分であり、状況に応じて、腎臓硬化症、腎不全、癌などに発展する場合もある。この病気の診断は、CBC(complete blood count)、肝機能検査、腎機能検査、マクログロブリンなど、血液中の蛋白検査、尿検査などによって実施される。新症候群と診断された時に、治療のために免疫抑制剤(prednisone)又はステロイド剤を1〜6ヶ月間投与するが、この期間の間、尿検査や血液検査を継続的に実施して変化を観察することで、治療効果を判断する。綿密な観察のために、定期的に病院を訪問して、血液と尿検査を実施しなければならないが、特に、新症候群の患者の90%が、表現力が弱い小児なので、症状変化などの身体の異常に対する継続的かつ徹底な検査や観察が必要である。これにより、小児の新症候群の治療効果及び再発確認のための未来の技術として、マクログロブリンなど、血蛋白に対する連続探知手法の開発は、非常に有用であると予測される。
【0056】
マクログロブリンのバイオマーカーへの活用に関する他の可能性として、アルツハイマーは、60〜70人に1人の割合で発生し、85歳以上は、50%が患っている老人性疾患であり、早期診断による予防が切実である。2006年にロンドンのキングスカレッジの研究チームが、血液検査によってアルツハイマー疾患にかかった患者から2種類の蛋白質、つまり、補体因子−Hの前駆体とアルファ2−マクログロブリンの濃度が増加したことを発見しており、このような蛋白質の濃度差の究明によって早期診断の可能性を提示した(A.Hye等, Brain.Vol.129,Page 3042-3050,2006)。このような目的で、マクログロブリンの連続探知によりアルツハイマー疾患を早期に診断すれば、症状の発現後に病院を訪問するよりも、疾患の予防及び治療が早期になされて、疾患の進行をはるかに緩和させ、生活の質の向上に大きく寄与すると期待される。
【0057】
マクログロブリンのバイオマーカーとしての活用に対するもう一つの可能性として、人工臓器の移植に伴う炎症反応や合併症の発生は、既知の事実であったが、その診断指標に関する研究結果が多くなかった。2005年米国のデューク大学医療センターで心臓手術に心肺機を使用した後、アルファ2−マクログロブリン濃度が50%増加した研究結果を提示した(Eric A.Williams等,J Thorac Cardiovasc Surg,Vol.129,Page 1098-1103,2005)。これは、全身的な炎症反応の一つの指標としてマクログロブリンの濃度変化が利用され得ることを示す。これにより、人工臓器移植後の予後観察の際に、炎症反応発現のバイオマーカーを連続探知することができる場合、定期的に病院訪問や合併症の症状の発現後の措置よりも、人工臓器の入れ替えや合併症の治療が早期に行えるという利点がある。
【0058】
前記で例示した病気を含めて、急慢性人体疾患は、一般的に時間や日単位で比較的ゆっくり進むので、疾患指標のバイオマーカーを測定するセンサーの応答時間として、通常分単位が要求される。これは、病気の進行時間と比較して、センサーの応答時間が10倍程度より速いとしたら、病気の進行がバイオマーカーの連続診断工程を支配する律速段階になるので、図8及び図9に示すセンサーのマクログロブリンの濃度応答時間(約15分、最終応答の95%基準)は、連続探知条件を満たす。より迅速なセンサーの応答時間(例えば、秒単位)は、連続診断時の分析性能に全く影響を与えず、単に概念のみが異なる使い捨てのセンサー(例えば、血糖値センサー)の場合、採取した試料の測定時間を短縮させるという効果を提供するだけである。
【0059】
(2)標識センサーを用いた診断システムの構築の可能性の例示
標識センサーの例として、蛍光体を信号発生源として使用する例が最も多く、捕獲認識成分10を固体表面に固定するか(図1の(B)及び(D))、あるいは、認識反応セル17内で液相反応によって探知が可能であり、この場合、信号発生源である蛍光物質(donor)から放射された光は、あるエネルギー受容体(acceptor)が非常に近接して存在する場合、吸収され、光が外部に放射されない原理を用いる(Shaw等,J.Clin.Pathol,Vol.30,Page 526-531,1977)。その応用として、抗原−抗体の付着のような認識反応が、蛍光物質とエネルギー受容体との間のエネルギー伝達を調節するように設計することができ、蛍光信号は、受光素子(フォトダイオード、charge−coupled device、photomultiplier tubeなど)を用いて探知される。
【0060】
標識センサーの他の例として、酵素を標識物質として使用することができ、センサーの表面に固定されている捕獲認識成分10を用いるか(図1の(B)及び(D))、又は酵素分子上に抗体が取り付けられる場合、活性が抑制されることが知られている数種類の酵素を用いると、認識反応セル17内で液相反応の遂行が可能である。これらの酵素を免疫分析に用いるために、分析物質(即ち、抗原)と結合させて抗体と反応させると、その酵素の活性が抑制されることが知られている(Se−Hwan Paek等、Biotechnology and bioengeering,Vol.56, Page 221-231,1997)。酵素からの信号は、選択した酵素と基質に応じて、吸光度測定センサー(スペクトロフォトメーター)、受光センサー(フォトダイオード、charge−coupled device、photomultiplier tubeなどの受光素子)、電気化学センサー(電極)などの様々な手段によって測定できる。
【0061】
標識センサーの他の例として、磁性粒子を標識物質として用いることができ、センサーの表面に固定されている捕獲認識成分10を用いると(図1の(B)及び(D))、分析物質との認識成分との間の反応に対する磁場測定が可能である(A. Perrin等,Journal of Immunological Methods,Vol.224, Page77-87,1999)。磁場測定センサーは、GMR/TMR及びHall素子が代表的であり、消費電力が少なく、大きさも小さく、軽くて、高集積化が可能である。
【0062】
以上で説明したように、可逆反応性抗体とセンサー技術とを組み合わせて、連続診断システムを構築すれば、分析感度の犠牲なしに、抗体を連続的にリサイクルして、分析物質をリアルタイムに測定することができる。例示された連続診断システムの濃度応答時間は、最終回答の95%を基準として10分台で、濃度が秒単位で変化する分析物質の測定には適用できず、分単位より相対的にゆっくり変化する分析物質の測定に適用することができる。特に、その濃度が定められた上限を超える場合、警報発令を必要とする分析の対象に適する。その適用可能な分野として、病気や症状に対する連続診断、及び人工臓器制御、生物テロ作用剤の連続探知、環境汚染の連続監視、及び生物工程の連続モニタリング分野などがある。
【実施例】
【0063】
以下、実施例に基づいて、本発明を更に詳細に説明する。これらの実施例は、本発明を例示するためのものなので、本発明の範囲が、これらの実施例によって制限されるものではない。
【0064】
<実験材料>
本発明の実施例のために使用された材料や購入先は、以下の通りである。表面プラズモン共鳴センサーチップ(BIACORE CM5;構成成分:ガラスマトリックス(母体)、30nm厚さの金薄膜、100nm厚さのdextran層)、amine couplingキット(100mM N−hydroxysuccinimide(NHS)、400mMのN−ethyl−N'−(dimethylaminopropyl)carbodiimide(EDC)、1Mのethanolamine hydrochloride、pH8.5を含む)、40%のグリセロール(glycerol)は、GE healthcare社(スウェーデン)から購入した。ネズミモノクローナル抗体(20E7、3D1;非可逆反応)とアルファ2−マクログロブリン(α2−macroglobulin、tetramer)は、エイビスフロンティア社(韓国)から供給された。牛血漿脂質蛋白質(bovine serum albumin)、sodium acetate、sodium phosphate、sodium chloride、glycine、ヒトAB型血清(human serum、AB plasma)、カゼイン(casein)、金ナノ粒子(gold nanoparticle、30nm)、抗ネズミヤギ抗体-horseradish peroxidase(HRP)重合体、及び3,3'、5,5'-tetramethylbenzidine(TMB)は、Sigma社(米国)から購入した。総IgG抗体定量キット(mouse IgG core ELISA)は、コマバイオテック社(韓国)から供給された。その他のすべての試薬は、分析用級に使用された。
【0065】
(実施例1)
−ネズミモノクローナル可逆反応性抗体の生産−
モノクローナル抗体を生産するハイブリドーマ細胞の作製は、通常の標準的な方法に基づいて実施した。具体的には、生後6週の雌BALB/cネズミの腹腔内にアルファ2−マクログロブリンを免疫原に注射して免疫させた後、2週間隔で3回ブースティングしている。三次ブースティング後、3日目にネズミを犠牲にして脾臓を摘出して得られた脾臓細胞を骨髄腫(myeloma)細胞株(Sp2/0-Ag14)との細胞融合を実施しており、このことからハイブリドーマ細胞を選別した。
【0066】
ハイブリドーマ細胞は、合計384種類のクローンが製作され、各クローンから生産された抗体含有培養液を用いて免疫原に対する反応性試験と総IgG抗体量の決定を行った。免疫原との抗体の反応性試験のために、10mMのリン酸緩衝液(140mMのNaClを含む;pH7.4)で希釈されたアルファ2−マクログロブリン(2.5μg/mL)が固定されている96−マイクロプレートウェル内にクローン培養液をそれぞれ移して反応させた。洗浄後、0.5%カゼイン含有10mMのリン酸緩衝液(カゼイン−PBS)で希釈された抗ネズミヤギ抗体−HRP重合体1/5、000)を反応させた。再度洗浄後、HRP基質溶液(3%過酸化水素水10μL)と10mg/mLのTMB(100μL;dimethyl sulfoxide溶媒に希釈)が含有された0.05Mの酢酸緩衝液、pH5.1(10mL)を各ウェルに加えて、酵素反応を行った後、15分間で2Mの硫酸を添加して停止させた。各ウェルで発生した発色信号は、マイクロプレート読み取り機器(VERSAmaxTM、Molecular Devices社製、米国)を用いて、450nm吸光度で測定された。また、総IgG抗体の量を決定するために、総IgG抗体定量キット(mouse IgG core ELISA)を使用して、メーカーから提供されたプロセスに基づいて分析した。
両分析結果から、抗体の反応性試験時の吸光度2.0以下(下位50%)、及び、総IgG抗体量0.1μg/mL以上(上位15%)の条件を同時に満足するハイブリドーマクローンの7種類を選別した。
【0067】
(実施例2)
−センサーチップの表面活性化及びリガンドの固定化−
表面プラズモン共鳴センサーチップとして購入されるBIACORE CM5は、メーカーから提供されたプロトコルに従って、100mMのNHSと400mMのEDCを用いて、チップの表面を活性化した。チップ表面に固定されるべきリガンド(抗原又は抗体)の量は、メーカーのプロトコル案内に従って計算して決定し、10mMのsodium acetate(pH4.0)緩衝液を用いて、リガンドを一定濃度で希釈した後、センサーチップ内に注入して(流速=5μL/分)、固定化を施した。20分後、1Mのethanolamine hydrochloride(pH8.5)溶液を6分間注入して、センサーの残りの表面を不活性化した。
表面プラズモン共鳴センサーシステム(BIACORE2000;GE healthcare社、スウェーデン)の運営は、メーカーから提供されたBIACORE 2000の使用プロトコルに従い、試料運搬液(running buffer)として、リン酸緩衝液、又はヒト血清を検査目的に従って選択して使用した。センサーシステム内に装着されるセンサーチップBIACORE CM5を購入して、このチップの1番の流体チャンネルには、対照群として牛血清アルブミンを付着させ、2番の流体チャンネルには、リガンドを化学的に固定させた。すべての実施例において同様に流体の流れ方向を1番の流体チャンネルから2番の流体チャンネルへ維持し、2番の流体チャンネルの信号値(resonance unit;RU)から1番の流体チャンネルのノイズ値を引くような方式で純粋な信号値を求めた。反応セル内の温度は、すべての実施例で同様に25℃に維持した。
【0068】
(実施例3)
−表面プラズモン共鳴測定システムを用いた可逆反応性抗体のスクリーニング−
可逆反応性抗体のスクリーニングを目的として、実施例2で説明したように、1番の流体チャンネルに100μg/mLの濃度で牛血清アルブミンを固定させ、2番の流体チャンネルに100μg/mLの濃度でアルファ2−マクログロブリンを固定させたセンサーチップを製造した。このように用意したセンサーチップを、表面プラズモン共鳴測定システムに装着した後、10mMのリン酸緩衝液を試料運搬液として用いて、5μL/分の速度で注入して、平衡状態を維持した。実施例1の抗体反応性試験と総IgG抗体量の決定から選別されたハイブリドーマクローン7種類を10mMのリン酸緩衝液(PBS、pH7.4)でそれぞれ適切に希釈した。メーカーから提供された分析プログラム(BIACORE operation 2000)に基づいて、各抗体試料35μLをセンサーシステム内に装着されているセンサーチップ内に420秒間注入して、付着反応を誘導した後、リン酸緩衝液を210秒間注入して、脱着反応を誘導した。同一種の抗体に対する分析が完了した後には、10mMのglycine緩衝液(pH1.5)15μLを180秒間一定に注入して、センサー表面を再生させた。付着及び脱着反応パターンは、メーカーから提供された編集プログラム(BIAevaluation 2.0)を用いて分析し、付着速度定数(ka)と脱着速度定数(kd)と平衡付着定数(KA)を計算した。以下の表は、テストされたハイブリドーマクローン7種類の付着速度定数(ka)と脱着速度定数(kd)と平衡付着定数(KA)を表したものである。
【0069】
二次選別されたハイブリドーマクローンの応答特性
【表1】

テストされたハイブリドーマクローン7種類のうち、2クローン1B5及び1F8が、高親和力の可逆反応性を示し、そのうち、1B5クローL/molよりも高い高親和力を示したので、本発明の目的に適するものと選定して、典型的な非可逆反応性を示す抗体である20E7と反応特性を比較した(図2)。付着反応時に、1B5抗体は、20E7より平衡状態に顕著に早く達しており、脱着反応時に、1B5抗体は、初期値に近接して落ちる形態のグラフを示したのに対し、20E7は、ほとんど脱着されていない形態のグラフを示した。このような特性の違いから、洗浄が要求される、既存の1回性の免疫分析において、洗浄時にも脱着されない非可逆反応の20E7抗体が好まれていた一方、抗体の濃度に応じて、力学的平衡反応により迅速に付着と脱着が迅速な1B5は、抗体のリサイクルによる連続測定に利用可能である。
したがって、本発明での基板素材である可逆反応性抗体の存在を提示し、既存の抗体とのその本質的な特性の差を一次証明した。参考事項として、1B5抗体と20E7抗体は、共にアルファ2−マクログロブリンに対して特異反応性を示し、この抗原分子上の他のエピトープ(epitope)に付着して、同じ抗原分子と同時に反応することができる。
【0070】
(実施例4)
−可逆反応性抗体の付着/脱着の繰り返し反応パターンの比較−
実施例3で製造したセンサーチップを用いて、同じ実験条件で可逆反応性1B5抗体の付着/脱着の繰り返し反応パターンを求めて、これを非可逆反応性20E7のパターンと比較した。10mMのリン酸緩衝液で希釈した抗体溶液(100ng/mLの1B5、又は20ng/mLの20E7)17.5μLを5μL/分の流速で210秒間、センサーチップ内に注入して付着反応を誘導し、その後、リン酸緩衝溶液を注入して、110秒間、脱着反応を誘導した。このような、同じ付着/脱着の反応条件下で、各抗体に対して、6回繰り返した。各抗体別に分析を完了した後、10mMのグリシン(pH1.5)の緩衝液15μLを180秒間に一定に注入して、センサーの表面を再生させた。BIACore 2000計測システムの運営とデータの編集は、実施例2の説明と同様である。
分析の結果、図3には、可逆反応特性を示すものと予測された1B5抗体は、抗体を供給してわずか1分以内に信号が増加して、固定された抗原との付着反応平衡状態に達し、かつ、リン酸緩衝液の供給時にすぐに着脱され、信号が初期値に戻ってきた。このような付着/脱着の可逆反応パターンは、6回繰り返し時に高い再現性を示した。非可逆反応特性を示すものと予測された20E7抗体は、抗体の供給後に一定時間の間、相対的に遅いが、継続的な付着反応を示し、リン酸緩衝液の供給時に脱着反応が完了していなかった。したがって、抗原−抗体反応結合体は、付着/着脱の繰り返し反応に従って順次累積され、信号が階段式に増加するパターンを示した。
【0071】
(実施例5)
−可逆反応性抗体の反応下限濃度の決定−
実施例3で製造したセンサーチップ及び同じ実験方法を用いて、可逆反応性1B5抗体の濃度変化に対する表面プラズモン共鳴センサーの応答を測定した。1B5抗体を、10mMのリン酸緩衝液を用いて、0.5pg/mL〜0.5μg/mLの範囲の濃度で希釈した。希釈した各抗体溶液17.5μLを5μL/分の流速で210秒間注入して付着反応を誘導し、その後、リン酸緩衝液を110秒間注入して脱着反応を誘導した。同じ条件下で、低濃度の抗体溶液から高濃度の溶液の順に分析し、また、逆順に分析して、1回循環テストした。循環試験が完了した後、実施例4の場合と同じ方法で、センサーの表面を再生させた。
【0072】
図4では、使用された抗体の濃度範囲内で、表面プラズモン共鳴センサーの信号は、抗体溶液の濃度が段階的に増加する際に比例して増加し、濃度が段階的に減少する際に比例して減少した。特に、抗体の濃度範囲が、pg/mL以下でもセンサーチップに固定されている抗原と反応することが分かったが、これは、既存の免疫分析に使用される非可逆反応性抗体と比較した場合、親和力の面で負けない結果である。したがって、1B5のような反応特性を有した抗体を搭載した免疫分析システムは、優れた分析感度を示すと予測され、また、その抗体がpg濃度単位からμg単位まで反応性を示すので、今後の免疫センサーの製作に利用する場合、広い測定範囲が予想される。
【0073】
(実施例6)
−可逆反応性抗体基板の非標識免疫センサーシステムの構築−
可逆反応性抗体を用いたアルファ2−マクログロブリン測定用の連続流れ露出タイプの非標識センサー(図1の(A))システムを構築するために、表面プラズモン共鳴センサーシステム(BIACORE 2000)と可逆反応性の抗体が固定されているBIACORE CM5センサーチップとを用いた。実施例2で説明したように、1番の流体チャンネルに牛血清アルブミンを100μg/mLの濃度で固定させ、2番の流体チャンネルに可逆反応性1B5抗体を10μg/mLの濃度で固定して、センサーチップを製造した。このように、センサーの表面に固定されている抗体と特異的に反応する分析物質であるマクログロブリンを10mMのリン酸緩衝液で希釈して、0〜10ng/mLの濃度範囲の標準試料を製造した。各標準試料(150μL)を10μL/分の流速で900秒間センサーシステム内に装着されているセンサーチップ内に注入して、付着反応を誘導した後、リン酸緩衝液を120秒間注入して、脱着反応を誘導した。各試料に対する分析が完了した後、実施例4のように、センサーの表面を再生させ、リン酸緩衝液の代わりに、ヒト血清を希釈液と試料運搬液として使用して、上述した同じ条件下で実験を繰り返した。
【0074】
表面プラズモン共鳴センサーを用いて、免疫分析分野で初めて、可逆反応性抗体基板の解析システムを構築し、この解析システムは、採択された分析物質濃度0.1〜10ng/mLの範囲で濃度応答を示し、測定感度に代表される探知下限濃度は、0.1ng/mL以下であることが分かった(図5の(A))。このシステムの分析特異性をテストするために、医療臨床の試験条件に近いヒト血清を試料運搬液及び標準試料希釈液として使用して測定した結果(図5の(B))、リン酸緩衝液を使用した場合(A)と非常に類似した濃度応答を示した。このことから、可逆反応性抗体である1B5基板のセンサーシステムは、測定感度と特異性の面で非常に優れており、更に、実際の医療臨床試験にも適用できると思われる。
【0075】
(実施例7)
−金ナノ粒子が標識された検出抗体を用いた信号増幅−
<実施例7.1 検出抗体−金ナノ粒子の重合体の製造>
金コロイド(直径:約30nm)懸濁液をクエン酸ナトリウム(sodium citrate)を還元剤として使用する標準方法で製造した(L.A.Dykman, A.A.Lyakhov, V.A.Bogatyrev,S.Y.Chchyogolev.Colloid,60,700,1998)。
具体的には、ガラスフラスコに3次脱イオン水1,000mLを入れた後、ここに1%塩化金溶液(tetrachloroauric acid)20mLを添加した。反応を助けるために、ホットプレートを使用して溶液を沸かし、金コロイドを作製するために、還元剤として、0.2μmのフィルターを使用して濾過した1%クエン酸ナトリウム溶液40mLを添加した。クエン酸ナトリウムの添加直後に、溶液は、淡黒色から赤色に変化した。10分間加熱した後、反応を停止させ、常温で徐々に冷却させた後、冷蔵保管しながら、以降の実験に使用した。
製造された金ナノ粒子懸濁液(1mL)に0.5Mのカーボネート緩衝液(pH9.6;1μL)を入れて、pH8.0程度に調整した。この溶液に、非可逆反応性抗体である20E7(図2参照)を10mMのリン酸緩衝液(PB;NaClを含まない)で150μg/mLの濃度(100μL)で希釈して添加した。室温で1時間反応させた後、5%カゼインが含まれているPB(カゼイン−PB;122μL)を添加し、室温で更に1時間反応させた。この混合物を16,000rpmで30分間遠心分離した後、上澄み液は捨てて、沈殿物にカゼイン−PB(400μL)を入れて溶解させた。再び16,000rpmで30分間遠心分離した後、上澄み液を捨てて、金粒子を基準に20倍濃縮されるように、カゼイン−PB(50μL)を入れて溶解させた。
【0076】
<実施例7.2 信号増幅の採択時の分析システムの濃度応答>
分析物質であるアルファ2−マクログロブリンをヒト血清で希釈して、0〜10ng/mLの濃度範囲の標準試料を製造し、各試料は、センサーシステムに搭載されたセンサーチップ内に注入される前に、実施例7.1で製造した探知抗体−金ナノ粒子の重合体10ng/mLと室温で10分間反応させた。この反応混合物(150μL)を実施例6で製造したセンサーチップ内に10μL/分の速度で900秒間注入して付着反応を誘導した後、ヒト血清を同じ流速で120秒間注入して、脱着反応を誘導した。各試料に対する分析が完了した後、実施例4でのように、センサーの表面を再生させた。図5において、前記信号増幅段階を採択した分析システムの濃度応答は、実施例6で求めた非標識センサーシステムの濃度応答と比較して、顕著に増加した形態を示しており、実際に分析感度は、0.1ng/mL水準(図5の(B)を参照)から0.001ng/mL水準に約100倍向上したことが分かった。
本発明で例示した信号増幅方法を用いれば、試料内に、非常に低い濃度で存在する分析物質も測定が可能であるので、可逆反応性抗体を用いた連続探知方法は、様々な分析物質の測定に広く適用できる。
【0077】
(実施例8)
−流速減少時の解析システムの濃度応答パターン−
医療臨床試料の場合、特にその使用量を最小化することが必要であるので、マイクロ流体の流れ速度を、先行の実験条件の1/10に減速して、分析システムの濃度応答を求めた。実施例6と同じセンサーチップを使用しており、流速の減少を除いて、同じ条件下で実験を行った。試料運搬液と標準試料希釈液としてヒト血清を使用し、流速は1μL/分に維持した。標準試料は、0〜100ng/mLの濃度範囲で用意し、試料(15μL)をセンサーチップ内に注入して、900秒間付着反応を誘導した後、リン酸緩衝溶液を注入して、420秒間、脱着反応を誘導した。標準試料を低濃度から高濃度の順に分析した後、再び低濃度に帰るという循環形態で分析した。分析システムの運営とデータの編集は、実施例4と同様に行っており、分析が完了した後は、提示のようにセンサーの表面を再生させた。
図1において、分析物質濃度の増減に伴うセンサーの応答は、分析物質の濃度に比例しており(図7の(A))、その応答パターンを、流速が10倍速い条件で得た結果(図5の(B))と比較してみると、分析感度は、約0.1ng/mL、そして応答時間は、640秒(最終回答の95%基準)と一定に維持されることが分かった。また、濃度応答をグラフとして作成して比較してみると(図7の(B))、テストされた流速範囲で顕著な差が示していなく、分析物質の濃度の増加時及び濃度の減少時に測定した濃度応答間にも差がなかった。特異事項として、流速が相対的に速い時(10μL/分)、高濃度の標準試料の分析時に現れた過剰応答の現象(図5、分析物質の濃度は、10ng/mLでの応答を参照)が、流速の減少時(1μL/分)に大幅に緩和されたことが分かった(図7、分析物質の濃度は、10ng/mL又はそれ以上での応答を参照)。
【0078】
(実施例9)
−指数的な濃度変化に対する連続測定−
前記実施例では、可逆反応性抗体の付着及び脱着反応を測定するために、各試料の分析間に試料運搬液(分析物質を含まない)が注入されるリセットモードを使用する一方で、本実施例では、可逆反応性抗体のリサイクルを例示するために、試料の連続分析モードを使用した。センサーチップは、実施例6で製造したものを使用しており、マクログロブリンをヒト血清で希釈して、0.01〜10,000ng/mLの範囲の標準試料を用意した。標準試料を順次1μL/分の流速でセンサーチップ内に注入し、分析物質の濃度が、900秒ごとに階段式に10倍ずつ増加して減少する循環変化2回繰り返しに対して、センサーからの濃度応答を連続的に求めた。センサーシステムの連続モードへの運営は、センサーシステムメーカーで設定したリセット分析工程とは異なり、試料の注入は、提供された注入口を通らず、試料運搬液供給通路を用いて行われた。試料の連続供給時、標準試料の注入中に絶えたり、空気が入らないように、以前の残りの試料溶液にあらかじめ定めた分析物質の濃縮液又は希釈液を添加して、次の試料の標準濃度で調整し、濃度が均一であるように持続的に混合した。
【0079】
分析の後、流出された試料は、分取装置で収集し、各分画は、マイクロウェルプレートを固定化マトリックスとして用いるサンドイッチ酵素免疫分析により標準試料の分析物質の濃度を確認した。分析方法は、10mMのリン酸緩衝液(140mMのNaClを含む;pH7.4)で希釈されたアルファ2−マクログロブリンに対して非可逆反応性である3D1モノクローナル抗体(1μg/mL;100μL)を各マイクロウェルに加えて固定させた。洗浄後、0.5%のカゼイン含有10mMのリン酸緩衝液(カゼイン−PBS)を200μL入れ、固定されていないウェルの残りの表面をブロッキングした。再度洗浄後、分取装置によって時間別に収集された分画溶液(30μL)に0.5%カゼイン、及び0.1%ツイン含有10mMのリン酸緩衝液(カゼイン−ツイン−PBS;70μL)を追加に注入して、全体試料(100μL)を抗体が固定されているウェルに入れて反応させた。洗浄後、アルファ2−マクログロブリンに対して非可逆反応性を持つ20E7のモノクローナル抗体にHRPが結合された20E7−HRP重合体(1μg/mL;100μL)をカゼイン−ツイン−PBSで希釈して、ウェルに注入して反応させた。再度洗浄後、HRPの基質溶液(実施例1を参照)を各ウェルに加えて酵素反応を行った後、15分間に2Mの硫酸を添加して停止させた。各ウェルで発生した発色信号は、マイクロプレート読み取り装置(VERSAmaxTM、 Molecular Devices社、米国)を用いて、450nmの吸光度で測定した。
【0080】
連続測定のために、事前に計算して設定した各標準試料の濃度を連続測定し、収集して、前記のように免疫分析を通じて実際の濃度を確認した結果、計算値と分析結果間の10%以内の差があったので、計算値をグラフの作成に用いた。与えられたマイクロ流体の流れ速度(1mL/分)でセンサー内に注入される標準試料内の分析物質濃度の増加又は減少に対するセンサーの応答は、ともに15分以内に平衡状態に達し、2回繰り返して循環する際に高い再現性を示した(図8の(A);0.01〜100ng/mLの濃度範囲でテストされた結果)。このような連続測定方式で測定したセンサーの濃度応答を示した標準曲線(図8の(B))は、リセットモードで測定した曲線と若干の差が生したが、これは、センサーシステムの運営の違いによるものと判断される。このような結果から、分析物質濃度の変化に対する連続測定が実際に可能であることが分かり、臨床試験への応用可能性も提示した。
【0081】
(実施例10)
−算術的な濃度変化に対する連続測定:小児腎臓癌マーカーの臨床濃度範囲への適用−
分析物質の種類に従って、発症や症状の発現時に、濃度の増減変化パターン(指数的あるいは算術的)が異なることがあり得るので、2倍、又はそれ以下に増加して減少する算術的な濃度変化に対するセンサーの濃度応答を、実施例9でのように連続モードで測定した。本実験では、モデル分析物質として選択したアルファ2−マクログロブリンをバイオマーカーとして使用できる小児腎臓癌の診断を究極的に念頭に置いた最適条件を使用した。つまり、血清試料の使用量を最小化できるように、分析物質をカゼイン−PBSで希釈して、標準試料を製造し、その濃度範囲は、分析性能を最適な状態で保持できる1〜20ng/mLの範囲で決定した。各標準試料を1,800秒間隔でセンサーチップ内に注入し、流速は、1μL/分に調節した。
【0082】
図9では、算術的な水準の連続的な濃度変化に対するセンサーの応答は、指数的な変化に関するものと同様に、迅速な応答時間と連続測定の再現性を示した。更に、小さな濃度変化に対しても敏感かつ迅速に反応することからみて、可逆反応性抗体基板のバイオセンサーは、今後、非常に正確な分析を必要とする分析物質の測定に広く適用できるものと期待される。特に、アルファ2−マクログロブリンの臨床的に有効な濃度変化の範囲は、3〜10mg/mLで、血清試料をそのまま連続測定に使用する場合、一日に1.44mL(1μL/分の注入速度基準)がかかる。
したがって、これらの試料量を最小化することが必要なので、本実施例では、106倍低い濃度範囲で希釈して、実際の臨床テストの際に、1.44nL/日の程度の極小量の血清の消耗を可能にした。更に、この解析条件下で、分析物質の濃度変化に対する信号変化幅の増加、つまり、分析精度も向上させることができる。
【産業上の利用可能性】
【0083】
以上述べたように、本発明によれば、一定量の可逆反応性の認識成分を連続的にリサイクルして、分析物質の濃度変化をリアルタイムに測定することができる。これは、分析物質の濃度に応じて迅速に可逆的に反応する抗体をリサイクルすると、既存の使い捨ての診断チップに比べて、構成部品及び製作方法を画期的に単純化できることを意味する。また、病気や症状に対するリアルタイムモニタリングを可能にするため、慢性疾患や高危険群患者への継続的な監視が可能になる。それだけでなく、人工臓器制御装置、生物テロ作用剤の連続探知システム製品は、人獣共通感染症の病原体の連続探知システム製品、環境汚染源の連続監視システム製品、生物工程、連続モニタリングシステム製品、食品生産工程の連続モニタリングシステム製品などに適用できる。
【符号の説明】
【0084】
10 捕獲認識成分
11 分析物質
12 非標識センサー
13 探知認識成分
14 標識物質
15 標識センサー
16 半透膜
17 認識反応セル
【特許請求の範囲】
【請求項1】
試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含むリアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分(reversibly reactive capturing an recognizing component)及び試料内の分析物質−捕獲認識成分の結合体から発生した信号を探知するセンサー(sensor)を含むことを特徴とする分析物質のリアルタイム連続検出装置。
【請求項2】
前記可逆反応性の捕獲認識成分が、試料内の分析物質との反応時に、付着速度定数(ka)が、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、脱着速度定数(kd)が、1×10−3sec−1〜1×10−1sec−1の可逆反応特性を持ち、同時に平衡付着定数(KA=ka/kd)が、1×108L/mol以上の高親和力を持つ請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項3】
前記可逆反応性の捕獲認識成分が、試料内の分析物質である生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質、若しくは国防化生放測定物質と特異的に結合可能な抗体、受容体、核酸、酵素、アプタマー、ペプチド、又は分子印刷人工膜である請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項4】
前記センサーが、分析物質−捕獲認識成分の結合体から発生した信号を直接探知する非標識センサー(label-free sensor)、又は分析物質−捕獲認識成分の結合体の密度に比例して信号を発生する標識物質(labeling material)を経由して探知する標識センサー(label senor)である請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項5】
前記非標識センサーが、表面プラズモン共鳴センサー、カンチレバーセンサー、光導波路センサー、光干渉センサー、又はナノセンサーである請求項4に記載の分析物質のリアルタイム連続検出装置。
【請求項6】
前記標識センサーが、標識物質として蛍光体、発光体、酵素、金属粒子、プラスチック粒子、磁性粒子、若しくはナノ粒子を使用する蛍光、発光、発色、電気化学、又は磁界探知センサーである請求項4に記載の分析物質のリアルタイム連続検出装置。
【請求項7】
前記試料の分析サイトが、試料内の分析物質だけを選択的に透過させうる半透膜(Semipermeable membrane)で区切られ、捕獲認識成分が固定されているセンサーの表面側に認識反応セル(recognizing reaction cell)を形成する請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項8】
標識センサーを用いる場合、前記認識反応セル内に半透膜を通過できないほどの大きさの標識物質(labeling material)と結合した探知認識成分(detecting and recognizing component)を閉じ込めて、リサイクルする請求項7に記載の分析物質のリアルタイム連続検出装置。
【請求項9】
前記認識反応セル内の探知認識成分も捕獲認識成分と共に連続的にリサイクルされるために、可逆反応(reversibly reactive)特性を持つ請求項8に記載の分析物質のリアルタイム連続検出装置。
【請求項10】
下記の段階を含む、請求項1から9のいずれかに記載のリアルタイム連続検出装置を用いた分析物質のリアルタイム連続検出方法。
(a)分析物質を含む試料を、前記試料の流入チャンネルを通じて試料の分析サイト内に注入する段階と;
(b)前記分析物質を試料の分析サイト内の可逆反応性の捕獲認識成分と結合させる段階と;
(c)前記分析物質と捕獲認識成分との結合によって発生する信号をセンサーで探知する段階と;
(d)試料の継続的な流入や洗浄液の流入により、前記分析物質と捕獲認識成分との結合が脱着して、分析物質が、前記試料の排出チャンネルを通じて排出される段階と;
(e)前記脱着された捕獲認識成分を連続的にリサイクルして、前記(b)乃至(d)の段階を繰り返すことにより、試料内の分析物質の濃度変化をリアルタイムに測定する段階。
【請求項11】
前記(c)の段階において、分析物質−捕獲認識成分の結合体から発生した信号を、非標識センサーを用いて直接探知するか、又は分析物質−捕獲認識成分の結合体の密度に比例して信号を発生する標識物質を経由して、標識センサーを介して信号を測定する請求項10に記載の分析物質のリアルタイム連続検出方法。
【請求項12】
前記非標識センサーを用いる場合、試料に含まれている分析物質が、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応する請求項11に記載の分析物質のリアルタイム連続検出方法。
【請求項13】
前記の標識センサーを用いる場合、試料内の分析物質が、標識物質が結合された探知認識成分と事前に反応した後、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応するか(連続流れ露出タイプ)、又は試料内の分析物質が、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入された後、認識反応セル内の標識物質と結合された探知認識成分及び捕獲認識成分と反応する(認識反応セルタイプ)ものである請求項11に記載の分析物質のリアルタイム連続検出方法。
【請求項14】
前記探知認識成分が、連続流れ露出タイプの場合、分析物質と事前に反応して供給されるので、結合安定性の高い非可逆反応(non-reversibly reactive)特性を持つか、又は認識反応セルタイプの場合、捕獲認識成分と共に探知認識成分も連続的にリサイクルされるために、可逆反応(reversibly reactive)特性を持つ請求項13に記載の分析物質のリアルタイム連続検出方法。
【請求項15】
認識反応セルタイプの標識センサーを用いる場合、近接していた蛍光物質(標識物質)と蛍光エネルギー受容体との間のエネルギーの伝達が、捕獲認識成分と分析物質との反応によって妨げられ、蛍光信号が発生する原理を用いるか、又は酵素分子(標識物質)上に固定されている分析物質と認識成分とが結合する場合、活性が抑制されることが知られている酵素を、標識物質を用いて捕獲認識成分をセンサー上に固定させず、認識反応を液相で行える請求項13に記載の分析物質のリアルタイム連続検出方法。
【請求項16】
下記の段階を含む、請求項1から9のいずれかに記載のリアルタイム連続検出装置に使用される可逆反応性の捕獲認識成分の選別方法。
(a)捕獲認識成分を用意する段階と;
(b)前記捕獲認識成分をセンサーの表面に固定されている分析物質と結合させる段階と;
(c)前記捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(d)洗浄液の流入により、前記捕獲認識成分と分析物質との結合を脱着させる段階と;
(e)前記脱着後、残りの捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(f)前記(e)の段階での探知信号が、前記(c)段階での探知信号よりも低くなる捕獲認識成分を選択する段階。
【請求項17】
前記センサーが、表面プラズモン共鳴センサー、カンチレバーセンサー、光導波路センサー、光干渉センサー、及びナノセンサーから選ばれる非標識センサーである請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【請求項18】
前記捕獲認識成分が、センサーの表面に固定されている分析物質との反応時に、付着速度定数(ka)が、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、脱着速度定数(kd)が、1×10−3sec−1〜1×10−1sec−1の可逆反応特性を持ち、同時に平衡付着定数(KA=ka/kd)が、1×108L/mol以上の高親和力を持つものを選択する請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【請求項19】
前記(a)の段階において、前記捕獲認識成分が、運搬溶液で希釈して連続的に注入され、前記(f)の段階において、時間によって増加していた信号が減少する捕獲認識成分を選択する請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【請求項20】
前記(a)の段階において、前記捕獲認識成分が、洗浄液と循環繰り返して注入され、前記(f)の段階において、時間によって信号が増加した後、最初の基準線に戻ってくる信号パターンが繰り返される捕獲認識成分を選択する請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【請求項1】
試料の流入チャンネル、試料の分析サイト、及び試料の排出チャンネルを含むリアルタイム検出装置において、前記試料の分析サイトは、可逆反応性の捕獲認識成分(reversibly reactive capturing an recognizing component)及び試料内の分析物質−捕獲認識成分の結合体から発生した信号を探知するセンサー(sensor)を含むことを特徴とする分析物質のリアルタイム連続検出装置。
【請求項2】
前記可逆反応性の捕獲認識成分が、試料内の分析物質との反応時に、付着速度定数(ka)が、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、脱着速度定数(kd)が、1×10−3sec−1〜1×10−1sec−1の可逆反応特性を持ち、同時に平衡付着定数(KA=ka/kd)が、1×108L/mol以上の高親和力を持つ請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項3】
前記可逆反応性の捕獲認識成分が、試料内の分析物質である生命体の代謝物質、蛋白質、ホルモン、核酸、細胞、食品検査対象物質、環境有害物質、若しくは国防化生放測定物質と特異的に結合可能な抗体、受容体、核酸、酵素、アプタマー、ペプチド、又は分子印刷人工膜である請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項4】
前記センサーが、分析物質−捕獲認識成分の結合体から発生した信号を直接探知する非標識センサー(label-free sensor)、又は分析物質−捕獲認識成分の結合体の密度に比例して信号を発生する標識物質(labeling material)を経由して探知する標識センサー(label senor)である請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項5】
前記非標識センサーが、表面プラズモン共鳴センサー、カンチレバーセンサー、光導波路センサー、光干渉センサー、又はナノセンサーである請求項4に記載の分析物質のリアルタイム連続検出装置。
【請求項6】
前記標識センサーが、標識物質として蛍光体、発光体、酵素、金属粒子、プラスチック粒子、磁性粒子、若しくはナノ粒子を使用する蛍光、発光、発色、電気化学、又は磁界探知センサーである請求項4に記載の分析物質のリアルタイム連続検出装置。
【請求項7】
前記試料の分析サイトが、試料内の分析物質だけを選択的に透過させうる半透膜(Semipermeable membrane)で区切られ、捕獲認識成分が固定されているセンサーの表面側に認識反応セル(recognizing reaction cell)を形成する請求項1に記載の分析物質のリアルタイム連続検出装置。
【請求項8】
標識センサーを用いる場合、前記認識反応セル内に半透膜を通過できないほどの大きさの標識物質(labeling material)と結合した探知認識成分(detecting and recognizing component)を閉じ込めて、リサイクルする請求項7に記載の分析物質のリアルタイム連続検出装置。
【請求項9】
前記認識反応セル内の探知認識成分も捕獲認識成分と共に連続的にリサイクルされるために、可逆反応(reversibly reactive)特性を持つ請求項8に記載の分析物質のリアルタイム連続検出装置。
【請求項10】
下記の段階を含む、請求項1から9のいずれかに記載のリアルタイム連続検出装置を用いた分析物質のリアルタイム連続検出方法。
(a)分析物質を含む試料を、前記試料の流入チャンネルを通じて試料の分析サイト内に注入する段階と;
(b)前記分析物質を試料の分析サイト内の可逆反応性の捕獲認識成分と結合させる段階と;
(c)前記分析物質と捕獲認識成分との結合によって発生する信号をセンサーで探知する段階と;
(d)試料の継続的な流入や洗浄液の流入により、前記分析物質と捕獲認識成分との結合が脱着して、分析物質が、前記試料の排出チャンネルを通じて排出される段階と;
(e)前記脱着された捕獲認識成分を連続的にリサイクルして、前記(b)乃至(d)の段階を繰り返すことにより、試料内の分析物質の濃度変化をリアルタイムに測定する段階。
【請求項11】
前記(c)の段階において、分析物質−捕獲認識成分の結合体から発生した信号を、非標識センサーを用いて直接探知するか、又は分析物質−捕獲認識成分の結合体の密度に比例して信号を発生する標識物質を経由して、標識センサーを介して信号を測定する請求項10に記載の分析物質のリアルタイム連続検出方法。
【請求項12】
前記非標識センサーを用いる場合、試料に含まれている分析物質が、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応する請求項11に記載の分析物質のリアルタイム連続検出方法。
【請求項13】
前記の標識センサーを用いる場合、試料内の分析物質が、標識物質が結合された探知認識成分と事前に反応した後、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入されて捕獲認識成分と反応するか(連続流れ露出タイプ)、又は試料内の分析物質が、試料の流入チャンネルを通じて連続的に試料の分析サイト内に流入された後、認識反応セル内の標識物質と結合された探知認識成分及び捕獲認識成分と反応する(認識反応セルタイプ)ものである請求項11に記載の分析物質のリアルタイム連続検出方法。
【請求項14】
前記探知認識成分が、連続流れ露出タイプの場合、分析物質と事前に反応して供給されるので、結合安定性の高い非可逆反応(non-reversibly reactive)特性を持つか、又は認識反応セルタイプの場合、捕獲認識成分と共に探知認識成分も連続的にリサイクルされるために、可逆反応(reversibly reactive)特性を持つ請求項13に記載の分析物質のリアルタイム連続検出方法。
【請求項15】
認識反応セルタイプの標識センサーを用いる場合、近接していた蛍光物質(標識物質)と蛍光エネルギー受容体との間のエネルギーの伝達が、捕獲認識成分と分析物質との反応によって妨げられ、蛍光信号が発生する原理を用いるか、又は酵素分子(標識物質)上に固定されている分析物質と認識成分とが結合する場合、活性が抑制されることが知られている酵素を、標識物質を用いて捕獲認識成分をセンサー上に固定させず、認識反応を液相で行える請求項13に記載の分析物質のリアルタイム連続検出方法。
【請求項16】
下記の段階を含む、請求項1から9のいずれかに記載のリアルタイム連続検出装置に使用される可逆反応性の捕獲認識成分の選別方法。
(a)捕獲認識成分を用意する段階と;
(b)前記捕獲認識成分をセンサーの表面に固定されている分析物質と結合させる段階と;
(c)前記捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(d)洗浄液の流入により、前記捕獲認識成分と分析物質との結合を脱着させる段階と;
(e)前記脱着後、残りの捕獲認識成分と分析物質との結合によって発生する信号をセンサーで探知する段階と;
(f)前記(e)の段階での探知信号が、前記(c)段階での探知信号よりも低くなる捕獲認識成分を選択する段階。
【請求項17】
前記センサーが、表面プラズモン共鳴センサー、カンチレバーセンサー、光導波路センサー、光干渉センサー、及びナノセンサーから選ばれる非標識センサーである請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【請求項18】
前記捕獲認識成分が、センサーの表面に固定されている分析物質との反応時に、付着速度定数(ka)が、1×105Lmol−1sec−1〜1×108Lmol−1sec−1であり、脱着速度定数(kd)が、1×10−3sec−1〜1×10−1sec−1の可逆反応特性を持ち、同時に平衡付着定数(KA=ka/kd)が、1×108L/mol以上の高親和力を持つものを選択する請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【請求項19】
前記(a)の段階において、前記捕獲認識成分が、運搬溶液で希釈して連続的に注入され、前記(f)の段階において、時間によって増加していた信号が減少する捕獲認識成分を選択する請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【請求項20】
前記(a)の段階において、前記捕獲認識成分が、洗浄液と循環繰り返して注入され、前記(f)の段階において、時間によって信号が増加した後、最初の基準線に戻ってくる信号パターンが繰り返される捕獲認識成分を選択する請求項16に記載の可逆反応性の捕獲認識成分の選別方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公表番号】特表2011−524982(P2011−524982A)
【公表日】平成23年9月8日(2011.9.8)
【国際特許分類】
【出願番号】特願2011−514486(P2011−514486)
【出願日】平成21年6月12日(2009.6.12)
【国際出願番号】PCT/KR2009/003174
【国際公開番号】WO2009/154377
【国際公開日】平成21年12月23日(2009.12.23)
【出願人】(510056353)コリア・ユニバーシティ・リサーチ・アンド・ビジネス・ファウンデーション (15)
【Fターム(参考)】
【公表日】平成23年9月8日(2011.9.8)
【国際特許分類】
【出願日】平成21年6月12日(2009.6.12)
【国際出願番号】PCT/KR2009/003174
【国際公開番号】WO2009/154377
【国際公開日】平成21年12月23日(2009.12.23)
【出願人】(510056353)コリア・ユニバーシティ・リサーチ・アンド・ビジネス・ファウンデーション (15)
【Fターム(参考)】
[ Back to top ]

