リガンド活性化転写レギュレータータンパク質
【課題】リガンド依存的転写に使用するための融合タンパク質を提供する。
【解決手段】細胞内受容体由来の改変されたリガンド結合ドメインと作動可能に連結したヌクレオチド結合ドメインを含む融合タンパク質、さらに転写制御ドメインも含む融合タンパク質、該融合タンパク質をコードするポリヌクレオチド、発現ベクター、およびトランスフェクションされた細胞。該ヌクレオチド結合ドメインは、約3ないし約18ヌクレオチドの隣接する標的ヌクレオチド配列に結合する亜鉛フィンガーペプチドである。該融合タンパク質は、遺伝子治療に用いられる。
【解決手段】細胞内受容体由来の改変されたリガンド結合ドメインと作動可能に連結したヌクレオチド結合ドメインを含む融合タンパク質、さらに転写制御ドメインも含む融合タンパク質、該融合タンパク質をコードするポリヌクレオチド、発現ベクター、およびトランスフェクションされた細胞。該ヌクレオチド結合ドメインは、約3ないし約18ヌクレオチドの隣接する標的ヌクレオチド配列に結合する亜鉛フィンガーペプチドである。該融合タンパク質は、遺伝子治療に用いられる。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
細胞内受容体由来の改変されたリガンド結合ドメイン(LBD)と作動可能に連結したヌクレオチド結合ドメイン(DBD)を含む融合タンパク質であって、
融合タンパク質が、リガンド活性化転写レギュレーターであり;
ヌクレオチド結合ドメインが、亜鉛フィンガーモジュラー部分を含む多指(polydactyl)亜鉛フィンガーであり;
ヌクレオチド結合ドメインの各モジュラー部分が、少なくとも3つのヌクレオチドの隣接するヌクレオチド配列と相互作用し;
LBDのリガンド特異性が、LBDが誘導された天然細胞内受容体のリガンド結合ドメインのリガンド特異性と比較してそのリガンド特異性が変化するように改変され、それによって融合タンパク質を活性化するリガンドがLBDが誘導されたレセプターを活性化するリガンドではなく、そして、
融合タンパク質が少なくとも6つの亜鉛フィンガーモジュラー部分を含む、
融合タンパク質。
【請求項2】
モノマーである、請求項1の融合タンパク質。
【請求項3】
第1のモノマーおよび第2のモノマーを有するダイマーである、請求項1または請求項2の融合タンパク質。
【請求項4】
ヘテロダイマーである、請求項3の融合タンパク質。
【請求項5】
ホモダイマーである、請求項3の融合タンパク質。
【請求項6】
作動可能に連結した転写制御ドメインをさらに含む、請求項1−5のいずれかの融合タンパク質。
【請求項7】
細胞内受容体が核ホルモン受容体である、請求項1−6のいずれかの融合タンパク質。
【請求項8】
亜鉛フィンガーが、式(GNN)n(ただし、Gはグアニジン、Nは任意のヌクレオチド、そしてnは3ないし6の整数である。)のヌクレオチド配列に結合する、請求項1−7のいずれかの融合タンパク質。
【請求項9】
DBDがC2H2亜鉛フィンガー由来の亜鉛フィンガーモジュラー部分を含む、請求項1−8のいずれかの融合タンパク質。
【請求項10】
細胞内受容体が、エストロゲン受容体、プロゲステロン受容体、グルココルチコイド−α受容体、グルココルチコイド−β受容体、ミネラルコルチコイド受容体、アンドロゲン受容体、甲状腺ホルモン受容体、レチノイン酸受容体、レチノイドX受容体、ビタミンD受容体、COUP−TF受容体、エクジソン受容体、Nurr−I受容体およびオーファン受容体からなる群から選択される核ホルモン受容体である、請求項1−9のいずれかの融合タンパク質。
【請求項11】
細胞内受容体がステロイド受容体である、請求項1−9のいずれかの融合タンパク質。
【請求項12】
ホルモン受容体が、プロゲステロン受容体変異体またはエストロゲン受容体変異体である、請求項10の融合タンパク質。
【請求項13】
転写制御ドメインが転写活性化ドメインを含む、請求項6の融合タンパク質。
【請求項14】
転写制御ドメインが、VP16、VP64、TA2、STAT−6、p65ならびにそれらの転写活性化活性を有する誘導体類、多量体および組合せからなる群から選択される、請求項6の融合タンパク質。
【請求項15】
転写制御ドメインが、核ホルモン受容体転写活性化ドメインまたはその転写活性化活性を有する変異体を含む、請求項6の融合タンパク質。
【請求項16】
転写制御ドメインが、ステロイドホルモン受容体転写活性化ドメインまたはその転写活性化活性を維持している変異体を含む、請求項6の融合タンパク質。
【請求項17】
転写制御ドメインが、ウイルス転写活性化ドメインまたはその転写活性化活性を維持している変異体を含む、請求項6の融合タンパク質。
【請求項18】
転写制御ドメインが、VP16転写活性化ドメインまたはその変異体を含む、請求項6の融合タンパク質。
【請求項19】
転写制御ドメインが、転写抑制ドメインを含む、請求項6の融合タンパク質。
【請求項20】
転写抑制ドメインが、ERD、KRAB、SID、デアセチラーゼ、ならびにそれらの誘導体類、多量体および組合せ、例えばKRAB−ERD、SID−ERD、(KRAB)2、(KRAB)3、KRAB−A、(KRAB−A)2、(SID)2、(KRAB−A)−SIDおよびSID−(KRAB−A)からなる群から選択される、請求項19の融合タンパク質。
【請求項21】
転写抑制ドメインが、KRAB−ERD、SID−ERD、(KRAB)2、(KRAB)3、KRAB−A、(KRAB−A)2、(SID)2、(KRAB−A)−SIDおよびSID−(KRAB−A)からなる群から選択されるドメインの組合せである、請求項19の融合タンパク質。
【請求項22】
配列番号1ないし配列番号18のいずれかに示すヌクレオチド配列にコードされるアミノ酸配列を含む、請求項1の融合タンパク質。
【請求項23】
核酸結合ドメインが、標的核酸分子と約1.0ナノモルより小さい解離定数で結合する、請求項1−22のいずれかの融合タンパク質。
【請求項24】
2つのリガンド結合ドメインを含む、請求項1−23のいずれかの融合タンパク質。
【請求項25】
リガンド結合ドメインが同じである、請求項24の融合タンパク質。
【請求項26】
リガンド結合ドメインが異なっている、請求項24の融合タンパク質。
【請求項27】
請求項1−26のいずれかの融合タンパク質をコードするヌクレオチド配列を含む核酸分子。
【請求項28】
請求項1−26のいずれかの融合タンパク質をコードするヌクレオチド配列を含むベクター。
【請求項29】
融合タンパク質をコードするヌクレオチド配列を含む請求項28のベクターであって、
融合タンパク質が細胞内受容体由来のリガンド結合ドメインと作動可能に連結したヌクレオチド結合ドメインを含み、ヌクレオチド結合ドメインが少なくとも18個のヌクレオチドの隣接するヌクレオチド配列と相互作用する多指C2H2亜鉛フィンガーペプチドまたはそのモジュラー部分であり、
融合タンパク質がリガンド活性化転写レギュレーターである、
ベクター。
【請求項30】
ウイルスベクターである、請求項28または請求項29のベクター。
【請求項31】
ウイルスベクターがDNAウイルスまたはレトロウイルスに由来する、請求項30のベクター。
【請求項32】
アデノウイルスベクター、アデノ随伴ウイルスベクター、ヘルペスウイルスベクター、ワクシニアウイルスベクターおよびレンチウイルスベクターからなる群から選択される、請求項30のベクター。
【請求項33】
請求項28−32のいずれかのベクターを含む単離細胞。
【請求項34】
真核生物細胞である、請求項33の細胞。
【請求項35】
有効量の請求項1−26のいずれかの融合タンパク質または融合タンパク質をコードするヌクレオチド配列を含む核酸分子;および医薬的に許容し得る賦形剤を含む、遺伝子発現を制御するための医薬組成物。
【請求項36】
単回投与用に製剤された、請求項35の医薬組成物。
【請求項37】
請求項1−26のいずれかの融合タンパク質または融合タンパク質をコードする核酸分子;および融合タンパク質または核酸分子の非ウイルス送達を達成するための試剤を含む、非ウイルス送達システム。
【請求項38】
発現カセットを含む核酸分子をさらに含み、該発現カセットは、融合タンパク質の核酸結合ドメインが相互作用するヌクレオチド配列を含有するものである、請求項37の非ウイルス送達システム。
【請求項39】
非ウイルス送達を達成するための試剤が、DNA−リガンド複合体、アデノウイルス−リガンド−DNA複合体、DNA直接注入用試剤、CaPO4沈殿用試剤、遺伝子銃法用試剤、エレクトロポレーション用試剤、リポソームおよびリポフェクション用試剤からなる群から選択される、請求項37または請求項38の非ウイルス送達システム。
【請求項40】
融合タンパク質のヌクレオチド結合ドメインが結合する核酸配列を含む遺伝子の転写を調節するための薬剤の製造における、請求項1−26のいずれかの融合タンパク質または請求項27の核酸分子の使用。
【請求項1】
細胞内受容体由来の改変されたリガンド結合ドメイン(LBD)と作動可能に連結したヌクレオチド結合ドメイン(DBD)を含む融合タンパク質であって、
融合タンパク質が、リガンド活性化転写レギュレーターであり;
ヌクレオチド結合ドメインが、亜鉛フィンガーモジュラー部分を含む多指(polydactyl)亜鉛フィンガーであり;
ヌクレオチド結合ドメインの各モジュラー部分が、少なくとも3つのヌクレオチドの隣接するヌクレオチド配列と相互作用し;
LBDのリガンド特異性が、LBDが誘導された天然細胞内受容体のリガンド結合ドメインのリガンド特異性と比較してそのリガンド特異性が変化するように改変され、それによって融合タンパク質を活性化するリガンドがLBDが誘導されたレセプターを活性化するリガンドではなく、そして、
融合タンパク質が少なくとも6つの亜鉛フィンガーモジュラー部分を含む、
融合タンパク質。
【請求項2】
モノマーである、請求項1の融合タンパク質。
【請求項3】
第1のモノマーおよび第2のモノマーを有するダイマーである、請求項1または請求項2の融合タンパク質。
【請求項4】
ヘテロダイマーである、請求項3の融合タンパク質。
【請求項5】
ホモダイマーである、請求項3の融合タンパク質。
【請求項6】
作動可能に連結した転写制御ドメインをさらに含む、請求項1−5のいずれかの融合タンパク質。
【請求項7】
細胞内受容体が核ホルモン受容体である、請求項1−6のいずれかの融合タンパク質。
【請求項8】
亜鉛フィンガーが、式(GNN)n(ただし、Gはグアニジン、Nは任意のヌクレオチド、そしてnは3ないし6の整数である。)のヌクレオチド配列に結合する、請求項1−7のいずれかの融合タンパク質。
【請求項9】
DBDがC2H2亜鉛フィンガー由来の亜鉛フィンガーモジュラー部分を含む、請求項1−8のいずれかの融合タンパク質。
【請求項10】
細胞内受容体が、エストロゲン受容体、プロゲステロン受容体、グルココルチコイド−α受容体、グルココルチコイド−β受容体、ミネラルコルチコイド受容体、アンドロゲン受容体、甲状腺ホルモン受容体、レチノイン酸受容体、レチノイドX受容体、ビタミンD受容体、COUP−TF受容体、エクジソン受容体、Nurr−I受容体およびオーファン受容体からなる群から選択される核ホルモン受容体である、請求項1−9のいずれかの融合タンパク質。
【請求項11】
細胞内受容体がステロイド受容体である、請求項1−9のいずれかの融合タンパク質。
【請求項12】
ホルモン受容体が、プロゲステロン受容体変異体またはエストロゲン受容体変異体である、請求項10の融合タンパク質。
【請求項13】
転写制御ドメインが転写活性化ドメインを含む、請求項6の融合タンパク質。
【請求項14】
転写制御ドメインが、VP16、VP64、TA2、STAT−6、p65ならびにそれらの転写活性化活性を有する誘導体類、多量体および組合せからなる群から選択される、請求項6の融合タンパク質。
【請求項15】
転写制御ドメインが、核ホルモン受容体転写活性化ドメインまたはその転写活性化活性を有する変異体を含む、請求項6の融合タンパク質。
【請求項16】
転写制御ドメインが、ステロイドホルモン受容体転写活性化ドメインまたはその転写活性化活性を維持している変異体を含む、請求項6の融合タンパク質。
【請求項17】
転写制御ドメインが、ウイルス転写活性化ドメインまたはその転写活性化活性を維持している変異体を含む、請求項6の融合タンパク質。
【請求項18】
転写制御ドメインが、VP16転写活性化ドメインまたはその変異体を含む、請求項6の融合タンパク質。
【請求項19】
転写制御ドメインが、転写抑制ドメインを含む、請求項6の融合タンパク質。
【請求項20】
転写抑制ドメインが、ERD、KRAB、SID、デアセチラーゼ、ならびにそれらの誘導体類、多量体および組合せ、例えばKRAB−ERD、SID−ERD、(KRAB)2、(KRAB)3、KRAB−A、(KRAB−A)2、(SID)2、(KRAB−A)−SIDおよびSID−(KRAB−A)からなる群から選択される、請求項19の融合タンパク質。
【請求項21】
転写抑制ドメインが、KRAB−ERD、SID−ERD、(KRAB)2、(KRAB)3、KRAB−A、(KRAB−A)2、(SID)2、(KRAB−A)−SIDおよびSID−(KRAB−A)からなる群から選択されるドメインの組合せである、請求項19の融合タンパク質。
【請求項22】
配列番号1ないし配列番号18のいずれかに示すヌクレオチド配列にコードされるアミノ酸配列を含む、請求項1の融合タンパク質。
【請求項23】
核酸結合ドメインが、標的核酸分子と約1.0ナノモルより小さい解離定数で結合する、請求項1−22のいずれかの融合タンパク質。
【請求項24】
2つのリガンド結合ドメインを含む、請求項1−23のいずれかの融合タンパク質。
【請求項25】
リガンド結合ドメインが同じである、請求項24の融合タンパク質。
【請求項26】
リガンド結合ドメインが異なっている、請求項24の融合タンパク質。
【請求項27】
請求項1−26のいずれかの融合タンパク質をコードするヌクレオチド配列を含む核酸分子。
【請求項28】
請求項1−26のいずれかの融合タンパク質をコードするヌクレオチド配列を含むベクター。
【請求項29】
融合タンパク質をコードするヌクレオチド配列を含む請求項28のベクターであって、
融合タンパク質が細胞内受容体由来のリガンド結合ドメインと作動可能に連結したヌクレオチド結合ドメインを含み、ヌクレオチド結合ドメインが少なくとも18個のヌクレオチドの隣接するヌクレオチド配列と相互作用する多指C2H2亜鉛フィンガーペプチドまたはそのモジュラー部分であり、
融合タンパク質がリガンド活性化転写レギュレーターである、
ベクター。
【請求項30】
ウイルスベクターである、請求項28または請求項29のベクター。
【請求項31】
ウイルスベクターがDNAウイルスまたはレトロウイルスに由来する、請求項30のベクター。
【請求項32】
アデノウイルスベクター、アデノ随伴ウイルスベクター、ヘルペスウイルスベクター、ワクシニアウイルスベクターおよびレンチウイルスベクターからなる群から選択される、請求項30のベクター。
【請求項33】
請求項28−32のいずれかのベクターを含む単離細胞。
【請求項34】
真核生物細胞である、請求項33の細胞。
【請求項35】
有効量の請求項1−26のいずれかの融合タンパク質または融合タンパク質をコードするヌクレオチド配列を含む核酸分子;および医薬的に許容し得る賦形剤を含む、遺伝子発現を制御するための医薬組成物。
【請求項36】
単回投与用に製剤された、請求項35の医薬組成物。
【請求項37】
請求項1−26のいずれかの融合タンパク質または融合タンパク質をコードする核酸分子;および融合タンパク質または核酸分子の非ウイルス送達を達成するための試剤を含む、非ウイルス送達システム。
【請求項38】
発現カセットを含む核酸分子をさらに含み、該発現カセットは、融合タンパク質の核酸結合ドメインが相互作用するヌクレオチド配列を含有するものである、請求項37の非ウイルス送達システム。
【請求項39】
非ウイルス送達を達成するための試剤が、DNA−リガンド複合体、アデノウイルス−リガンド−DNA複合体、DNA直接注入用試剤、CaPO4沈殿用試剤、遺伝子銃法用試剤、エレクトロポレーション用試剤、リポソームおよびリポフェクション用試剤からなる群から選択される、請求項37または請求項38の非ウイルス送達システム。
【請求項40】
融合タンパク質のヌクレオチド結合ドメインが結合する核酸配列を含む遺伝子の転写を調節するための薬剤の製造における、請求項1−26のいずれかの融合タンパク質または請求項27の核酸分子の使用。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


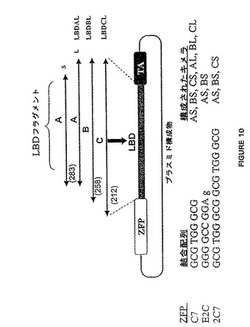
【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【公開番号】特開2009−273463(P2009−273463A)
【公開日】平成21年11月26日(2009.11.26)
【国際特許分類】
【出願番号】特願2009−147520(P2009−147520)
【出願日】平成21年6月22日(2009.6.22)
【分割の表示】特願2001−533840(P2001−533840)の分割
【原出願日】平成12年10月23日(2000.10.23)
【出願人】(593052785)ザ スクリップス リサーチ インスティテュート (91)
【Fターム(参考)】
【公開日】平成21年11月26日(2009.11.26)
【国際特許分類】
【出願日】平成21年6月22日(2009.6.22)
【分割の表示】特願2001−533840(P2001−533840)の分割
【原出願日】平成12年10月23日(2000.10.23)
【出願人】(593052785)ザ スクリップス リサーチ インスティテュート (91)
【Fターム(参考)】
[ Back to top ]

