リチウムイオン二次電池用負極及びその負極を用いたリチウムイオン二次電池
【課題】充放電時の内部抵抗を低減しイオン伝導性を向上させることで、その負極を用いたリチウムイオン二次電池のサイクル特性を向上させる。
【解決手段】負極活物質層には、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な前記元素の酸化物粒子と、バインダと、を含み、酸化物粒子の平均粒子径はLi吸蔵粒子の平均粒子径より小さい。バインダ被膜の内部まで電解液が浸入し易くなると考えられ、充放電時の反応抵抗が低く、繰り返し充放電後の内部抵抗の上昇も抑制される。
【解決手段】負極活物質層には、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な前記元素の酸化物粒子と、バインダと、を含み、酸化物粒子の平均粒子径はLi吸蔵粒子の平均粒子径より小さい。バインダ被膜の内部まで電解液が浸入し易くなると考えられ、充放電時の反応抵抗が低く、繰り返し充放電後の内部抵抗の上昇も抑制される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、リチウムイオン二次電池用負極及びその負極を用いたリチウムイオン二次電池に関するものである。
【背景技術】
【0002】
リチウムイオン二次電池は、充放電容量が高く、高出力化が可能な二次電池である。現在、主として携帯電子機器用の電源として用いられており、更に、今後普及が予想される電気自動車用の電源として期待されている。リチウムイオン二次電池は、リチウム(Li)を挿入および脱離することができる活物質を正極及び負極にそれぞれ有する。そして、両極間に設けられた電解液内をLiイオンが移動することによって動作する。
【0003】
リチウムイオン二次電池には、正極の活物質として主にリチウムコバルト複合酸化物等のリチウム含有金属複合酸化物が用いられ、負極の活物質としては多層構造を有する炭素材料が主に用いられている。
【0004】
リチウムイオン二次電池の性能は、二次電池を構成する正極、負極および電解質の材料に左右される。なかでも活物質を形成する活物質材料の研究開発が活発に行われている。現在、一般的に用いられている負極活物質として黒鉛などの炭素材料がある。黒鉛などを負極活物質とする炭素負極は、インターカレーション反応を有することから、サイクル特性は良いものの、高容量化が困難とされている。そこで負極活物質材料として、炭素よりも高容量なケイ素またはケイ素酸化物が検討されている。
【0005】
ケイ素を負極活物質として用いることにより、炭素材料を用いるよりも高容量の電池とすることができる。しかしながらケイ素は、充放電時のLiの吸蔵・放出に伴う体積変化が大きい。そのためケイ素が微粉化して集電体から脱落または剥離し、電池の充放電サイクル寿命が短いという問題点がある。そこでケイ素酸化物を負極活物質として用いることにより、ケイ素よりも充放電時のLiの吸蔵・放出に伴う体積変化を抑制することができる。
【0006】
例えば、負極活物質として、酸化ケイ素(SiOx:xは0.5≦x≦1.5程度)の使用が検討されている。SiOxは熱処理されると、SiとSiO2とに分解することが知られている。これは不均化反応といい、SiとOとの比が概ね1:1の均質な固体の一酸化ケイ素SiOであれば、固体の内部反応によりSi相とSiO2相の二相に分離する。分離して得られるSi相は非常に微細である。また、Si相を覆うSiO2相が電解液の分解を抑制する働きをもつ。したがって、SiとSiO2とに分解したSiOxからなる負極活物質を用いた二次電池は、サイクル特性に優れる。
【0007】
上記した負極活物質を含む負極は、例えば、負極活物質とバインダとを含むスラリーを集電体に塗布し、乾燥することにより作製される。このため活物質粒子どうしの結着と、活物質と集電体との結着とを担うバインダの性能が、負極の性能に大きく影響する。バインダの結着力が低い場合には、活物質粒子どうしの密着性及び活物質と集電体との密着性が低下し、集電性が低下する。そして上述のSiO系粒子からなる負極活物質を用いた負極でも、充放電反応時のリチウムの吸蔵及び放出に伴う体積変化が避けられない。このため、負極の活物質層に含まれるバインダには大きな応力が作用するので、バインダには強い結着力が求められている。
【0008】
また、SiO系粒子からなる活物質は導電性が低いため、導電材として黒鉛や非晶質の炭素材料を混合し、導電材粉末とSiOx粉末を点又は面で接触させることにより導電性をもたせている。しかし炭素材料を混合しても、結着力の強いバインダを用いた場合にはイオン伝導性の向上が僅かであり、さらなるイオン伝導性の向上が求められている。
【0009】
例えば特開2004-296108号公報には、負極にアルミナ、ジルコニア、シリカなどの金属酸化物微粒子を混合することで、大電流性能が優れたリチウムイオン二次電池となることが記載されている。
【0010】
ところでリチウムイオン二次電池では、初充電の際に非水電解液の一部が分解し、負極活物質表面に有機SEI被膜が形成されることが知られている。この有機SEI被膜によって、負極活物質の界面抵抗が上昇し、イオンの拡散が阻害される。そこで特開2008-041465号公報には、非水電解質二次電池の負極に、メジアン粒径が100nm以下のセラミックナノ粒子を含ませることが記載されている。有機SEIとセラミックナノ粒子とからなる複合被膜が負極活物質を覆うことで、イオン拡散性が向上する。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】特開2004-296108号公報
【特許文献2】特開2008-041465号公報
【発明の概要】
【発明が解決しようとする課題】
【0012】
しかし上記した各特許文献には、結着力の強いバインダを用いることに関する記載がない。本発明は、このような事情に鑑みてなされたものであり、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な元素の酸化物粒子と、バインダと、を含む負極活物質層をもつ負極において、充放電時の反応抵抗を低減するとともに、繰り返し充放電後の内部抵抗の上昇を抑制することで、イオン伝導性を向上させ、その負極を用いたリチウムイオン二次電池のサイクル特性を向上させることにある。
【課題を解決するための手段】
【0013】
上記課題を解決する本発明のリチウムイオン二次電池用負極の特徴は、集電体と、集電体に形成された負極活物質層と、からなるリチウムイオン二次電池用負極であって、
負極活物質層には、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な元素の酸化物粒子と、バインダと、を含み、酸化物粒子の平均粒子径はLi吸蔵粒子の平均粒子径より小さいことにある。
また上記課題を解決する本発明のリチウムイオン二次電池の特徴は、本発明の負極を用いたことにある。
【発明の効果】
【0014】
本発明のリチウムイオン二次電池用負極は、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子とリチウムと合金化反応可能な元素の酸化物粒子と、を含み、該酸化物粒子の平均粒子径はLi吸蔵粒子の平均粒子径より小さい。そのためバインダ被膜の内部まで電解液が浸入し易くなり、充放電時の反応抵抗が低減されるとともに、充放電繰り返し時の内部抵抗の上昇が抑制されることにより、リチウムイオン二次電池のサイクル特性が向上する。
【0015】
充放電時の反応抵抗が低減されるとともに内部抵抗の上昇が抑制される理由は明らかでは無いが、Li吸蔵粒子と該酸化物粒子との親和性が高いために、負極活物質層を形成する際のスラリー中において両粒子が凝集した比表面積の大きな凝集粒子が形成され、その凝集粒子の表面をバインダが被覆する。したがってバインダで被覆されたバインダ被覆粒子の表面も凹凸が大きく比表面積が大きい。そのため電解液とバインダ被覆粒子との接触面積が大きくなり、バインダ被膜の内部まで電解液が浸入し易くなると考えられる。
【図面の簡単な説明】
【0016】
【図1】サイクル数に対する放電容量維持率を示すグラフである。
【図2】ACインピーダンス測定結果を示すグラフである。
【発明を実施するための形態】
【0017】
本発明のリチウムイオン二次電池用負極は、Li吸蔵粒子と酸化物粒子とを含む。
【0018】
Li吸蔵粒子としては少なくともリチウムと合金化反応可能な元素を含むものであり、例えばシリコン(Si)、酸化ケイ素などを用いることができるが、SiOx(0.3≦x≦1.6)で表されるケイ素酸化物からなるSiO系粒子を用いることが望ましい。このSiO系粒子は、不均化反応によって微細なSiと、Siを覆うSiO2とに分解したSiOxからなる。xが下限値未満であると、Si比率が高くなるため充放電時の体積変化が大きくなりすぎてサイクル特性が低下する。またxが上限値を超えると、Si比率が低下してエネルギー密度が低下するようになる。0.5≦x≦1.5の範囲が好ましく、0.7≦x≦1.2の範囲がさらに望ましい。
【0019】
一般に、酸素を断った状態であれば800℃以上で、ほぼすべてのSiOが不均化して二相に分離すると言われている。具体的には、非結晶性のSiO粉末を含む原料酸化ケイ素粉末に対して、真空中または不活性ガス中などの不活性雰囲気中で800〜1200℃、1〜5時間の熱処理を行うことで、非結晶性のSiO2相および結晶性のSi相の二相を含むSiOx粒子からなる粉末が得られる。
【0020】
またLi吸蔵粒子は、SiO系粒子と、炭素材料からなりSiO系粒子の表面を被覆する被覆層と、からなることも好ましい。被覆層を有することでSiO系粒子とフッ酸などとの反応をさらに防止することができ、リチウムイオン二次電池のサイクル特性が向上する。被覆層の炭素材料としては、天然黒鉛、人造黒鉛、コークス、メソフェーズ炭素、気相成長炭素繊維、ピッチ系炭素繊維、PAN系炭素繊維などを用いることができる。また被覆層を形成するには、特許文献1に記載されたメカノヒュージョンなどの機械的表面融合処理法、CVD法などを用いることができる。
【0021】
被覆層の形成量は、SiO系粒子と被覆層の合計に対して1〜50質量%とすることができる。被覆層が1質量%未満では導電性向上の効果が得られず、50質量%を超えるとSiOxの割合が相対的に減少して負極容量が低下してしまう。被覆層の形成量は5〜30質量%の範囲が好ましく、5〜20質量%の範囲がさらに望ましい。
【0022】
Li吸蔵粒子はD50平均粒子径が1μm〜10μmの範囲にあることが望ましい。D50平均粒子径が10μmより大きいとリチウムイオン二次電池の充放電特性が低下し、D50平均粒子径が1μmより小さいと凝集して粗大な粒子となるため同様にリチウムイオン二次電池の充放電特性が低下する場合がある。
【0023】
酸化物粒子は、リチウムと合金化反応可能な前記元素の酸化物であり、例えばシリカ粒子が例示される。この酸化物粒子の平均粒子径は、Li吸蔵粒子の平均粒子径の1/100以下であることが望ましい。酸化物粒子の平均粒子径がこの範囲より大きくなると、Li吸蔵粒子と酸化物粒子とが凝集した凝集粒子の比表面積が小さくなるためと考えられ、充放電時の内部抵抗の上昇を抑制する効果が小さくなって本発明の効果が発現できない。なお酸化物粒子の平均粒子径がLi吸蔵粒子の平均粒子径の1/5000未満となると、凝集して粗大な粒子となり、抵抗が増加する場合があるため好ましくない。したがって酸化物粒子の平均粒子径は、Li吸蔵粒子の平均粒子径の1/5000以上とすることが好ましい。
【0024】
また負極活物質層における酸化物粒子の含有量は、体積%で、Li吸蔵粒子の含有量より少ないことが望ましい。酸化物粒子の含有量がLi吸蔵粒子の含有量より多くなると、抵抗が増加して放電容量が低下し実用的でない。
【0025】
負極活物質層には、さらに炭素系粒子を含むことが好ましい。この炭素系粒子としては、天然黒鉛、人造黒鉛、コークス、メソフェーズ炭素、気相成長炭素繊維、ピッチ系炭素繊維、PAN系炭素繊維などが例示されるが、緩衝性能に優れる黒鉛が好ましい。この炭素系粒子のD50平均粒子径は、Li吸蔵粒子としてSiOxを用いた場合には、1〜10μmであることが特に望ましい。
【0026】
負極活物質層における炭素系粒子の含有量は、体積%で、Li吸蔵粒子の含有量より少ないことが望ましい。炭素粒子の含有量がLi吸蔵粒子の含有量より多くなると、抵抗が増加して放電容量が低下し実用的でない。
【0027】
本発明のリチウムイオン二次電池の負極は、集電体と、集電体上に結着された負極活物質層と、を有する。負極活物質層は、例えばLi吸蔵粒子と、シリカ粒子と、炭素系粒子と、導電助剤と、バインダと、必要に応じ適量の有機溶剤を加えて混合しスラリーにしたものを、ロールコート法、ディップコート法、ドクターブレード法、スプレーコート法、カーテンコート法などの方法で集電体上に塗布し、プレスし、熱処理してバインダを硬化させることによって作製することができる。この負極活物質層の厚さ(t)は、従来と同様に10μm〜30μmとすることができる。
【0028】
集電体は、放電或いは充電の間、電極に電流を流し続けるための化学的に不活性な電子高伝導体のことである。集電体は箔、板等の形状を採用することができるが、目的に応じた形状であれば特に限定されない。集電体として、例えば銅箔やアルミニウム箔を好適に用いることができる。
【0029】
導電助剤は、電極の導電性を高めるために添加される。上記した炭素系粒子も導電助剤として機能するが、炭素質微粒子であるカーボンブラック、アセチレンブラック(AB)、ケッチェンブラック(KB)、気相法炭素繊維(Vapor Grown Carbon Fiber:VGCF)等を単独でまたは二種以上組み合わせて添加することができる。導電助剤の使用量については、特に限定的ではないが、例えば、Li吸蔵粒子100質量部に対して、20〜100質量部程度とすることができる。導電助剤の量が20質量部未満では効率のよい導電パスを形成できず、100質量部を超えると電極の成形性が悪化するとともにエネルギー密度が低くなる。なお炭素材料からなる被覆層をもつLi吸蔵粒子を用いる場合は、導電助剤の添加量を低減あるいは無しとすることができる。
【0030】
バインダは、活物質及び導電助剤を集電体に結着するための結着剤として用いられる。バインダはなるべく少ない量で活物質等を結着させることが求められ、その量は、負極活物質層の0.5wt%〜50wt%が望ましい。バインダ量が0.5wt%未満では電極の成形性が低下し、50wt%を超えると電極のエネルギー密度が低くなる。なお、バインダとしては、ポリフッ化ビニリデン(PVDF)、ポリテトラフルオロエチレン(PTFE)等のフッ素系ポリマー、スチレンブタジエンゴム(SBR)等のゴム、ポリイミド、ポリアミドイミド、ポリアミドイミドシリカハイブリッド等のイミド系ポリマー、アルコキシルシリル基含有樹脂、ポリアクリル酸、ポリメタクリル酸、ポリイタコン酸などが例示される。またアクリル酸と、メタクリル酸、イタコン酸、フマル酸、マレイン酸などの酸モノマーとの共重合物を用いることもできる。中でも結着性に優れた高結着性バインダが好ましく、ポリイミド、ポリアミドイミド、ポリアミドイミドシリカハイブリッド、ポリアクリル酸、カルボキシメチルセルロースから選ばれる少なくとも一種が望ましい。中でも、ポリアミドイミド樹脂あるいはポリアミドイミドシリカハイブリッドが特に望ましい。
【0031】
本発明のリチウムイオン二次電池における負極には、リチウムがプリドーピングされていることが望ましい。負極にリチウムをドープするには、例えば対極に金属リチウムを用いて半電池を組み、電気化学的にリチウムをドープする電極化成法などを利用することができる。リチウムのドープ量は特に制約されない。
【0032】
リチウムをドープすることにより、あるいは本発明のリチウムイオン二次電池の初回充電後には、負極活物質のSiO系粒子のSiO2相にLixSiyOzで表される酸化物系化合物が含まれている。LixSiyOzとしては、例えばx=0,y=1,z=2のSiO2、x=2,y=1,Z=3のLi2SiO3、x=4,y=1,z=4のLi4SiO4などが例示される。例えばx=4,y=1,z=4のLi4SiO4は下記の反応により生成し、クーロン効率は約77%と計算される。
【0033】
2SiO + 8.6Li+ + 8.6e− → 1.5Li4.4Si + 1/2Li4SiO4
また上記反応が途中で停止した場合には、下記の反応のようにx=2,y=1,Z=3のLi2SiO3とx=4,y=1,z=4のLi4SiO4の両者が生成し、この場合のクーロン効率も約77%と計算される。
2SiO + 7.35Li+ + 7.35e− → 1.42Li4Si + 1/3Li2SiO3 + 1/4Li4SiO4
【0034】
上記反応によって生成するLi4SiO4は、充放電時の電極反応に関与しない不活性な物質であり、充放電時の活物質の体積変化を緩和する働きをする。したがってSiO系粒子のSiO2相にLixSiyOzで表される酸化物系化合物が含まれる場合には、本発明のリチウムイオン二次電池はサイクル特性がさらに向上する。
【0035】
上記した負極を用いる本発明のリチウムイオン二次電池は、特に限定されない公知の正極、電解液、セパレータを用いることができる。正極は、リチウムイオン二次電池で使用可能なものであればよい。正極は、集電体と、集電体上に結着された正極活物質層とを有する。正極活物質層は、正極活物質と、バインダとを含み、さらには導電助剤を含んでも良い。正極活物質、導電助材およびバインダは、特に限定はなく、リチウムイオン二次電池で使用可能なものであればよい。
【0036】
正極活物質としては、金属リチウム、LiCoO2、LiNi1/3Co1/3Mn1/3O2、Li2MnO2、硫黄などが挙げられる。集電体は、アルミニウム、ニッケル、ステンレス鋼など、リチウムイオン二次電池の正極に一般的に使用されるものであればよい。導電助剤は上記の負極で記載したものと同様のものが使用できる。
【0037】
電解液は、有機溶媒に電解質であるリチウム金属塩を溶解させたものである。電解液は、特に限定されない。有機溶媒として、非プロトン性有機溶媒、たとえばプロピレンカーボネート(PC)、エチレンカーボネート(EC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、メチルエチルカーボネート(MEC)等から選ばれる一種以上を用いることができる。また、溶解させる電解質としては、LiPF6、LiBF4、LiAsF6、LiI、LiClO4、LiCF3SO3等の有機溶媒に可溶なリチウム金属塩を用いることができる。
【0038】
例えば、エチレンカーボネート、ジメチルカーボネート、プロピレンカーボネート、ジメチルカーボネートなどの有機溶媒にLiClO4、LiPF6、LiBF4、LiCF3SO3等のリチウム金属塩を0.5mol/lから1.7mol/l程度の濃度で溶解させた溶液を使用することができる。
【0039】
セパレータは、リチウムイオン二次電池に使用されることができるものであれば特に限定されない。セパレータは、正極と負極とを分離し電解液を保持するものであり、ポリエチレン、ポリプロピレン等の薄い微多孔膜を用いることができる。
【0040】
本発明のリチウムイオン二次電池は、形状に特に限定はなく、円筒型、積層型、コイン型等、種々の形状を採用することができる。いずれの形状を採る場合であっても、正極および負極にセパレータを挟装させ電極体とし、正極集電体および負極集電体から外部に通ずる正極端子および負極端子までの間を、集電用リード等を用いて接続した後、この電極体を電解液とともに電池ケースに密閉して電池となる。
【0041】
以上説明した本発明のリチウムイオン二次電池は、携帯電話、パソコン等の通信機器、情報関連機器の分野の他、自動車の分野においても好適に利用できる。たとえば、このリチウムイオン二次電池を車両に搭載すれば、リチウムイオン二次電池を電気自動車用の電源として使用できる。車両に搭載する場合には、一般に、複数の単電池を直列に連結した組電池として搭載され、インバータを介して電気モータ及び発電機に接続される。
【0042】
以下、実施例を挙げて本発明を更に詳しく説明する。
【実施例】
【0043】
<リチウムイオン二次電池用負極の作製>
SiO粉末(アルドリッチ社製)を900℃で2時間熱処理し、平均粒径5μmのSiOx粉末を調製した。この熱処理によって、SiとOとの比が概ね1:1の均質な固体の一酸化ケイ素SiOであれば、固体の内部反応によりSi相とSiO2相の二相に分離する。分離して得られるSi相は非常に微細である。
【0044】
得られたSiOx粉末42質量部と、天然黒鉛粉末40質量部と、ケッチェンブラック3質量部と、平均粒子径15nmのシリカ微粒子(比表面積180m2/g)1.5質量部と、バインダとしてのポリアミドイミド13.5質量部とを混合してスラリーを調製した。
【0045】
シリカ微粒子は、ポリアミドイミド樹脂がN-メチル-2-ピロリドン(NMP)に2.0質量%溶解した溶液中にシリカが14.0質量%分散したシリカ分散液(荒川化学工業社製「コンポセラン1102」)として供給されたものを用いた。またバインダは、ポリアミドイミド樹脂がN-メチル-2-ピロリドン(NMP)に30.0質量%溶解したバインダ溶液を用いた。
【0046】
各成分の混合方法は、先ずシリカ分散液とバインダ溶液とを均一に混合し、そこへSiOx粉末と、天然黒鉛粉末と、ケッチェンブラックとを混合して均一に撹拌した。
【0047】
このスラリーを、厚さ20μmの電解銅箔(集電体)の表面にドクターブレードを用いて塗布し、銅箔上に負極活物質層を形成した。その後、ロールプレス機により、集電体と負極活物質層を強固に密着接合させた。これを真空乾燥し、負極活物質層の厚さが16μmの負極を形成した。
【0048】
<正極の作製>
正極活物質としてのL333(Li[Mn1/3Ni1/3Co1/3]O2)と、導電助剤としてのアセチレンブラック(AB)と、バインダー樹脂としてのポリフッ化ビニリデン(PVdF)とを混合し、スラリー状の正極合材を調製した。スラリー中の各成分(固形分)の組成比は、L333:AB:PVdF=88:6:6(質量比)であった。このスラリーを集電体に塗布し、集電体上に正極合材層を積層形成した。具体的には、ドクターブレードを用いてこのスラリーを厚さ20μmのアルミニウム箔(集電体)の表面に塗布した。
【0049】
その後、80℃で20分間乾燥し、正極合材中から有機溶媒を揮発させて除去した。乾燥後、ロールプレス機により、電極密度を調整した。これを真空乾燥炉にて200℃で2時間加熱硬化させて、集電体の上層に厚さ50μm程度の正極合材層が積層されてなる正極を得た。
【0050】
<リチウムイオン二次電池の作製>
正極を30mm×25mm、負極を31mm×26mmに裁断し、ラミネートフィルムで収容した。この正極および負極の間に、セパレータとしてポリプロピレン樹脂からなる矩形状シート(40mm×40mm角、厚さ30μm)を挟装して極板群とした。この極板群を二枚一組のラミネートフィルムで覆い、三辺をシールした後、袋状となったラミネートフィルムに上記の電解液を注入した。その後、残りの一辺をシールすることで、四辺が気密にシールされ、極板群および電解液が密閉されたラミネートセルを得た。電解液にはEC(エチレンカーボネート)、MEC(メチルエチルカーボネート)、DMC(ジメチルカーボネート)=3:3:4(体積比)の混合溶液にLiPF6を1モル/Lとなる濃度で溶解したものを用いた。正極および負極は外部と電気的に接続可能なタブを備え、このタブの一部はラミネートセルの外側に延出した。以上の工程で、単層ラミネートセルのリチウムイオン二次電池を得た。
【0051】
[比較例]
シリカ微粒子1.5質量部に代えてポリアミドイミドを1.5質量部増量したこと以外は実施例と同様にして負極を形成した。すなわちシリカ分散液を用いることなく、バインダ溶液をシリカ当量分増量した。
この負極を用い、実施例と同様にしてリチウムイオン二次電池を作成した。
【0052】
<サイクル特性試験>
実施例及び比較例のリチウムイオン二次電池に対し、下記に示す条件で充放電を繰り返すのを300サイクル行った。
充電:4.2V 1C CC 55℃
放電:2.5V 1C CC 55℃
【0053】
そのときのサイクル数に対する放電容量維持率を測定し、結果を図1に示す。また300サイクル目の放電容量維持率と300サイクル時の内部抵抗上昇率を表1に示す。ここで放電維持率は、1サイクル目の放電容量を100としたときの各サイクル目における放電容量である。また内部抵抗上昇率は、1サイクル目の内部抵抗に対して、300サイクル時における内部抵抗が上昇した度合いの比率である。
【0054】
<評価>
【表1】

【0055】
図1から、実施例に係るリチウムイオン二次電池は比較例に比べてサイクル特性が向上していることがわかる。そして表1から、この理由は、実施例に係るリチウムイオン二次電池は比較例に比べて内部抵抗の上昇が抑制されたことに起因していることが明らかである。
【0056】
<ACインピーダンス測定試験>
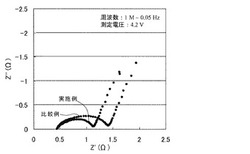
実施例及び比較例に係るリチウムイオン二次電池についてそれぞれACインピーダンス測定を行った。測定は、4.2V、1C、の条件でCCCV充電を行った後の電池を用い、東洋システム社製の測定器を用いて25℃で行った。結果を図2に示す。
【0057】
<評価>
図2より、実施例に係るリチウムイオン二次電池は比較例に係るリチウムイオン二次電池に比べて反応抵抗が小さいことが明らかであり、これはシリカ微粒子を含むことによる効果であることが明らかである。
【技術分野】
【0001】
本発明は、リチウムイオン二次電池用負極及びその負極を用いたリチウムイオン二次電池に関するものである。
【背景技術】
【0002】
リチウムイオン二次電池は、充放電容量が高く、高出力化が可能な二次電池である。現在、主として携帯電子機器用の電源として用いられており、更に、今後普及が予想される電気自動車用の電源として期待されている。リチウムイオン二次電池は、リチウム(Li)を挿入および脱離することができる活物質を正極及び負極にそれぞれ有する。そして、両極間に設けられた電解液内をLiイオンが移動することによって動作する。
【0003】
リチウムイオン二次電池には、正極の活物質として主にリチウムコバルト複合酸化物等のリチウム含有金属複合酸化物が用いられ、負極の活物質としては多層構造を有する炭素材料が主に用いられている。
【0004】
リチウムイオン二次電池の性能は、二次電池を構成する正極、負極および電解質の材料に左右される。なかでも活物質を形成する活物質材料の研究開発が活発に行われている。現在、一般的に用いられている負極活物質として黒鉛などの炭素材料がある。黒鉛などを負極活物質とする炭素負極は、インターカレーション反応を有することから、サイクル特性は良いものの、高容量化が困難とされている。そこで負極活物質材料として、炭素よりも高容量なケイ素またはケイ素酸化物が検討されている。
【0005】
ケイ素を負極活物質として用いることにより、炭素材料を用いるよりも高容量の電池とすることができる。しかしながらケイ素は、充放電時のLiの吸蔵・放出に伴う体積変化が大きい。そのためケイ素が微粉化して集電体から脱落または剥離し、電池の充放電サイクル寿命が短いという問題点がある。そこでケイ素酸化物を負極活物質として用いることにより、ケイ素よりも充放電時のLiの吸蔵・放出に伴う体積変化を抑制することができる。
【0006】
例えば、負極活物質として、酸化ケイ素(SiOx:xは0.5≦x≦1.5程度)の使用が検討されている。SiOxは熱処理されると、SiとSiO2とに分解することが知られている。これは不均化反応といい、SiとOとの比が概ね1:1の均質な固体の一酸化ケイ素SiOであれば、固体の内部反応によりSi相とSiO2相の二相に分離する。分離して得られるSi相は非常に微細である。また、Si相を覆うSiO2相が電解液の分解を抑制する働きをもつ。したがって、SiとSiO2とに分解したSiOxからなる負極活物質を用いた二次電池は、サイクル特性に優れる。
【0007】
上記した負極活物質を含む負極は、例えば、負極活物質とバインダとを含むスラリーを集電体に塗布し、乾燥することにより作製される。このため活物質粒子どうしの結着と、活物質と集電体との結着とを担うバインダの性能が、負極の性能に大きく影響する。バインダの結着力が低い場合には、活物質粒子どうしの密着性及び活物質と集電体との密着性が低下し、集電性が低下する。そして上述のSiO系粒子からなる負極活物質を用いた負極でも、充放電反応時のリチウムの吸蔵及び放出に伴う体積変化が避けられない。このため、負極の活物質層に含まれるバインダには大きな応力が作用するので、バインダには強い結着力が求められている。
【0008】
また、SiO系粒子からなる活物質は導電性が低いため、導電材として黒鉛や非晶質の炭素材料を混合し、導電材粉末とSiOx粉末を点又は面で接触させることにより導電性をもたせている。しかし炭素材料を混合しても、結着力の強いバインダを用いた場合にはイオン伝導性の向上が僅かであり、さらなるイオン伝導性の向上が求められている。
【0009】
例えば特開2004-296108号公報には、負極にアルミナ、ジルコニア、シリカなどの金属酸化物微粒子を混合することで、大電流性能が優れたリチウムイオン二次電池となることが記載されている。
【0010】
ところでリチウムイオン二次電池では、初充電の際に非水電解液の一部が分解し、負極活物質表面に有機SEI被膜が形成されることが知られている。この有機SEI被膜によって、負極活物質の界面抵抗が上昇し、イオンの拡散が阻害される。そこで特開2008-041465号公報には、非水電解質二次電池の負極に、メジアン粒径が100nm以下のセラミックナノ粒子を含ませることが記載されている。有機SEIとセラミックナノ粒子とからなる複合被膜が負極活物質を覆うことで、イオン拡散性が向上する。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】特開2004-296108号公報
【特許文献2】特開2008-041465号公報
【発明の概要】
【発明が解決しようとする課題】
【0012】
しかし上記した各特許文献には、結着力の強いバインダを用いることに関する記載がない。本発明は、このような事情に鑑みてなされたものであり、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な元素の酸化物粒子と、バインダと、を含む負極活物質層をもつ負極において、充放電時の反応抵抗を低減するとともに、繰り返し充放電後の内部抵抗の上昇を抑制することで、イオン伝導性を向上させ、その負極を用いたリチウムイオン二次電池のサイクル特性を向上させることにある。
【課題を解決するための手段】
【0013】
上記課題を解決する本発明のリチウムイオン二次電池用負極の特徴は、集電体と、集電体に形成された負極活物質層と、からなるリチウムイオン二次電池用負極であって、
負極活物質層には、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な元素の酸化物粒子と、バインダと、を含み、酸化物粒子の平均粒子径はLi吸蔵粒子の平均粒子径より小さいことにある。
また上記課題を解決する本発明のリチウムイオン二次電池の特徴は、本発明の負極を用いたことにある。
【発明の効果】
【0014】
本発明のリチウムイオン二次電池用負極は、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子とリチウムと合金化反応可能な元素の酸化物粒子と、を含み、該酸化物粒子の平均粒子径はLi吸蔵粒子の平均粒子径より小さい。そのためバインダ被膜の内部まで電解液が浸入し易くなり、充放電時の反応抵抗が低減されるとともに、充放電繰り返し時の内部抵抗の上昇が抑制されることにより、リチウムイオン二次電池のサイクル特性が向上する。
【0015】
充放電時の反応抵抗が低減されるとともに内部抵抗の上昇が抑制される理由は明らかでは無いが、Li吸蔵粒子と該酸化物粒子との親和性が高いために、負極活物質層を形成する際のスラリー中において両粒子が凝集した比表面積の大きな凝集粒子が形成され、その凝集粒子の表面をバインダが被覆する。したがってバインダで被覆されたバインダ被覆粒子の表面も凹凸が大きく比表面積が大きい。そのため電解液とバインダ被覆粒子との接触面積が大きくなり、バインダ被膜の内部まで電解液が浸入し易くなると考えられる。
【図面の簡単な説明】
【0016】
【図1】サイクル数に対する放電容量維持率を示すグラフである。
【図2】ACインピーダンス測定結果を示すグラフである。
【発明を実施するための形態】
【0017】
本発明のリチウムイオン二次電池用負極は、Li吸蔵粒子と酸化物粒子とを含む。
【0018】
Li吸蔵粒子としては少なくともリチウムと合金化反応可能な元素を含むものであり、例えばシリコン(Si)、酸化ケイ素などを用いることができるが、SiOx(0.3≦x≦1.6)で表されるケイ素酸化物からなるSiO系粒子を用いることが望ましい。このSiO系粒子は、不均化反応によって微細なSiと、Siを覆うSiO2とに分解したSiOxからなる。xが下限値未満であると、Si比率が高くなるため充放電時の体積変化が大きくなりすぎてサイクル特性が低下する。またxが上限値を超えると、Si比率が低下してエネルギー密度が低下するようになる。0.5≦x≦1.5の範囲が好ましく、0.7≦x≦1.2の範囲がさらに望ましい。
【0019】
一般に、酸素を断った状態であれば800℃以上で、ほぼすべてのSiOが不均化して二相に分離すると言われている。具体的には、非結晶性のSiO粉末を含む原料酸化ケイ素粉末に対して、真空中または不活性ガス中などの不活性雰囲気中で800〜1200℃、1〜5時間の熱処理を行うことで、非結晶性のSiO2相および結晶性のSi相の二相を含むSiOx粒子からなる粉末が得られる。
【0020】
またLi吸蔵粒子は、SiO系粒子と、炭素材料からなりSiO系粒子の表面を被覆する被覆層と、からなることも好ましい。被覆層を有することでSiO系粒子とフッ酸などとの反応をさらに防止することができ、リチウムイオン二次電池のサイクル特性が向上する。被覆層の炭素材料としては、天然黒鉛、人造黒鉛、コークス、メソフェーズ炭素、気相成長炭素繊維、ピッチ系炭素繊維、PAN系炭素繊維などを用いることができる。また被覆層を形成するには、特許文献1に記載されたメカノヒュージョンなどの機械的表面融合処理法、CVD法などを用いることができる。
【0021】
被覆層の形成量は、SiO系粒子と被覆層の合計に対して1〜50質量%とすることができる。被覆層が1質量%未満では導電性向上の効果が得られず、50質量%を超えるとSiOxの割合が相対的に減少して負極容量が低下してしまう。被覆層の形成量は5〜30質量%の範囲が好ましく、5〜20質量%の範囲がさらに望ましい。
【0022】
Li吸蔵粒子はD50平均粒子径が1μm〜10μmの範囲にあることが望ましい。D50平均粒子径が10μmより大きいとリチウムイオン二次電池の充放電特性が低下し、D50平均粒子径が1μmより小さいと凝集して粗大な粒子となるため同様にリチウムイオン二次電池の充放電特性が低下する場合がある。
【0023】
酸化物粒子は、リチウムと合金化反応可能な前記元素の酸化物であり、例えばシリカ粒子が例示される。この酸化物粒子の平均粒子径は、Li吸蔵粒子の平均粒子径の1/100以下であることが望ましい。酸化物粒子の平均粒子径がこの範囲より大きくなると、Li吸蔵粒子と酸化物粒子とが凝集した凝集粒子の比表面積が小さくなるためと考えられ、充放電時の内部抵抗の上昇を抑制する効果が小さくなって本発明の効果が発現できない。なお酸化物粒子の平均粒子径がLi吸蔵粒子の平均粒子径の1/5000未満となると、凝集して粗大な粒子となり、抵抗が増加する場合があるため好ましくない。したがって酸化物粒子の平均粒子径は、Li吸蔵粒子の平均粒子径の1/5000以上とすることが好ましい。
【0024】
また負極活物質層における酸化物粒子の含有量は、体積%で、Li吸蔵粒子の含有量より少ないことが望ましい。酸化物粒子の含有量がLi吸蔵粒子の含有量より多くなると、抵抗が増加して放電容量が低下し実用的でない。
【0025】
負極活物質層には、さらに炭素系粒子を含むことが好ましい。この炭素系粒子としては、天然黒鉛、人造黒鉛、コークス、メソフェーズ炭素、気相成長炭素繊維、ピッチ系炭素繊維、PAN系炭素繊維などが例示されるが、緩衝性能に優れる黒鉛が好ましい。この炭素系粒子のD50平均粒子径は、Li吸蔵粒子としてSiOxを用いた場合には、1〜10μmであることが特に望ましい。
【0026】
負極活物質層における炭素系粒子の含有量は、体積%で、Li吸蔵粒子の含有量より少ないことが望ましい。炭素粒子の含有量がLi吸蔵粒子の含有量より多くなると、抵抗が増加して放電容量が低下し実用的でない。
【0027】
本発明のリチウムイオン二次電池の負極は、集電体と、集電体上に結着された負極活物質層と、を有する。負極活物質層は、例えばLi吸蔵粒子と、シリカ粒子と、炭素系粒子と、導電助剤と、バインダと、必要に応じ適量の有機溶剤を加えて混合しスラリーにしたものを、ロールコート法、ディップコート法、ドクターブレード法、スプレーコート法、カーテンコート法などの方法で集電体上に塗布し、プレスし、熱処理してバインダを硬化させることによって作製することができる。この負極活物質層の厚さ(t)は、従来と同様に10μm〜30μmとすることができる。
【0028】
集電体は、放電或いは充電の間、電極に電流を流し続けるための化学的に不活性な電子高伝導体のことである。集電体は箔、板等の形状を採用することができるが、目的に応じた形状であれば特に限定されない。集電体として、例えば銅箔やアルミニウム箔を好適に用いることができる。
【0029】
導電助剤は、電極の導電性を高めるために添加される。上記した炭素系粒子も導電助剤として機能するが、炭素質微粒子であるカーボンブラック、アセチレンブラック(AB)、ケッチェンブラック(KB)、気相法炭素繊維(Vapor Grown Carbon Fiber:VGCF)等を単独でまたは二種以上組み合わせて添加することができる。導電助剤の使用量については、特に限定的ではないが、例えば、Li吸蔵粒子100質量部に対して、20〜100質量部程度とすることができる。導電助剤の量が20質量部未満では効率のよい導電パスを形成できず、100質量部を超えると電極の成形性が悪化するとともにエネルギー密度が低くなる。なお炭素材料からなる被覆層をもつLi吸蔵粒子を用いる場合は、導電助剤の添加量を低減あるいは無しとすることができる。
【0030】
バインダは、活物質及び導電助剤を集電体に結着するための結着剤として用いられる。バインダはなるべく少ない量で活物質等を結着させることが求められ、その量は、負極活物質層の0.5wt%〜50wt%が望ましい。バインダ量が0.5wt%未満では電極の成形性が低下し、50wt%を超えると電極のエネルギー密度が低くなる。なお、バインダとしては、ポリフッ化ビニリデン(PVDF)、ポリテトラフルオロエチレン(PTFE)等のフッ素系ポリマー、スチレンブタジエンゴム(SBR)等のゴム、ポリイミド、ポリアミドイミド、ポリアミドイミドシリカハイブリッド等のイミド系ポリマー、アルコキシルシリル基含有樹脂、ポリアクリル酸、ポリメタクリル酸、ポリイタコン酸などが例示される。またアクリル酸と、メタクリル酸、イタコン酸、フマル酸、マレイン酸などの酸モノマーとの共重合物を用いることもできる。中でも結着性に優れた高結着性バインダが好ましく、ポリイミド、ポリアミドイミド、ポリアミドイミドシリカハイブリッド、ポリアクリル酸、カルボキシメチルセルロースから選ばれる少なくとも一種が望ましい。中でも、ポリアミドイミド樹脂あるいはポリアミドイミドシリカハイブリッドが特に望ましい。
【0031】
本発明のリチウムイオン二次電池における負極には、リチウムがプリドーピングされていることが望ましい。負極にリチウムをドープするには、例えば対極に金属リチウムを用いて半電池を組み、電気化学的にリチウムをドープする電極化成法などを利用することができる。リチウムのドープ量は特に制約されない。
【0032】
リチウムをドープすることにより、あるいは本発明のリチウムイオン二次電池の初回充電後には、負極活物質のSiO系粒子のSiO2相にLixSiyOzで表される酸化物系化合物が含まれている。LixSiyOzとしては、例えばx=0,y=1,z=2のSiO2、x=2,y=1,Z=3のLi2SiO3、x=4,y=1,z=4のLi4SiO4などが例示される。例えばx=4,y=1,z=4のLi4SiO4は下記の反応により生成し、クーロン効率は約77%と計算される。
【0033】
2SiO + 8.6Li+ + 8.6e− → 1.5Li4.4Si + 1/2Li4SiO4
また上記反応が途中で停止した場合には、下記の反応のようにx=2,y=1,Z=3のLi2SiO3とx=4,y=1,z=4のLi4SiO4の両者が生成し、この場合のクーロン効率も約77%と計算される。
2SiO + 7.35Li+ + 7.35e− → 1.42Li4Si + 1/3Li2SiO3 + 1/4Li4SiO4
【0034】
上記反応によって生成するLi4SiO4は、充放電時の電極反応に関与しない不活性な物質であり、充放電時の活物質の体積変化を緩和する働きをする。したがってSiO系粒子のSiO2相にLixSiyOzで表される酸化物系化合物が含まれる場合には、本発明のリチウムイオン二次電池はサイクル特性がさらに向上する。
【0035】
上記した負極を用いる本発明のリチウムイオン二次電池は、特に限定されない公知の正極、電解液、セパレータを用いることができる。正極は、リチウムイオン二次電池で使用可能なものであればよい。正極は、集電体と、集電体上に結着された正極活物質層とを有する。正極活物質層は、正極活物質と、バインダとを含み、さらには導電助剤を含んでも良い。正極活物質、導電助材およびバインダは、特に限定はなく、リチウムイオン二次電池で使用可能なものであればよい。
【0036】
正極活物質としては、金属リチウム、LiCoO2、LiNi1/3Co1/3Mn1/3O2、Li2MnO2、硫黄などが挙げられる。集電体は、アルミニウム、ニッケル、ステンレス鋼など、リチウムイオン二次電池の正極に一般的に使用されるものであればよい。導電助剤は上記の負極で記載したものと同様のものが使用できる。
【0037】
電解液は、有機溶媒に電解質であるリチウム金属塩を溶解させたものである。電解液は、特に限定されない。有機溶媒として、非プロトン性有機溶媒、たとえばプロピレンカーボネート(PC)、エチレンカーボネート(EC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、メチルエチルカーボネート(MEC)等から選ばれる一種以上を用いることができる。また、溶解させる電解質としては、LiPF6、LiBF4、LiAsF6、LiI、LiClO4、LiCF3SO3等の有機溶媒に可溶なリチウム金属塩を用いることができる。
【0038】
例えば、エチレンカーボネート、ジメチルカーボネート、プロピレンカーボネート、ジメチルカーボネートなどの有機溶媒にLiClO4、LiPF6、LiBF4、LiCF3SO3等のリチウム金属塩を0.5mol/lから1.7mol/l程度の濃度で溶解させた溶液を使用することができる。
【0039】
セパレータは、リチウムイオン二次電池に使用されることができるものであれば特に限定されない。セパレータは、正極と負極とを分離し電解液を保持するものであり、ポリエチレン、ポリプロピレン等の薄い微多孔膜を用いることができる。
【0040】
本発明のリチウムイオン二次電池は、形状に特に限定はなく、円筒型、積層型、コイン型等、種々の形状を採用することができる。いずれの形状を採る場合であっても、正極および負極にセパレータを挟装させ電極体とし、正極集電体および負極集電体から外部に通ずる正極端子および負極端子までの間を、集電用リード等を用いて接続した後、この電極体を電解液とともに電池ケースに密閉して電池となる。
【0041】
以上説明した本発明のリチウムイオン二次電池は、携帯電話、パソコン等の通信機器、情報関連機器の分野の他、自動車の分野においても好適に利用できる。たとえば、このリチウムイオン二次電池を車両に搭載すれば、リチウムイオン二次電池を電気自動車用の電源として使用できる。車両に搭載する場合には、一般に、複数の単電池を直列に連結した組電池として搭載され、インバータを介して電気モータ及び発電機に接続される。
【0042】
以下、実施例を挙げて本発明を更に詳しく説明する。
【実施例】
【0043】
<リチウムイオン二次電池用負極の作製>
SiO粉末(アルドリッチ社製)を900℃で2時間熱処理し、平均粒径5μmのSiOx粉末を調製した。この熱処理によって、SiとOとの比が概ね1:1の均質な固体の一酸化ケイ素SiOであれば、固体の内部反応によりSi相とSiO2相の二相に分離する。分離して得られるSi相は非常に微細である。
【0044】
得られたSiOx粉末42質量部と、天然黒鉛粉末40質量部と、ケッチェンブラック3質量部と、平均粒子径15nmのシリカ微粒子(比表面積180m2/g)1.5質量部と、バインダとしてのポリアミドイミド13.5質量部とを混合してスラリーを調製した。
【0045】
シリカ微粒子は、ポリアミドイミド樹脂がN-メチル-2-ピロリドン(NMP)に2.0質量%溶解した溶液中にシリカが14.0質量%分散したシリカ分散液(荒川化学工業社製「コンポセラン1102」)として供給されたものを用いた。またバインダは、ポリアミドイミド樹脂がN-メチル-2-ピロリドン(NMP)に30.0質量%溶解したバインダ溶液を用いた。
【0046】
各成分の混合方法は、先ずシリカ分散液とバインダ溶液とを均一に混合し、そこへSiOx粉末と、天然黒鉛粉末と、ケッチェンブラックとを混合して均一に撹拌した。
【0047】
このスラリーを、厚さ20μmの電解銅箔(集電体)の表面にドクターブレードを用いて塗布し、銅箔上に負極活物質層を形成した。その後、ロールプレス機により、集電体と負極活物質層を強固に密着接合させた。これを真空乾燥し、負極活物質層の厚さが16μmの負極を形成した。
【0048】
<正極の作製>
正極活物質としてのL333(Li[Mn1/3Ni1/3Co1/3]O2)と、導電助剤としてのアセチレンブラック(AB)と、バインダー樹脂としてのポリフッ化ビニリデン(PVdF)とを混合し、スラリー状の正極合材を調製した。スラリー中の各成分(固形分)の組成比は、L333:AB:PVdF=88:6:6(質量比)であった。このスラリーを集電体に塗布し、集電体上に正極合材層を積層形成した。具体的には、ドクターブレードを用いてこのスラリーを厚さ20μmのアルミニウム箔(集電体)の表面に塗布した。
【0049】
その後、80℃で20分間乾燥し、正極合材中から有機溶媒を揮発させて除去した。乾燥後、ロールプレス機により、電極密度を調整した。これを真空乾燥炉にて200℃で2時間加熱硬化させて、集電体の上層に厚さ50μm程度の正極合材層が積層されてなる正極を得た。
【0050】
<リチウムイオン二次電池の作製>
正極を30mm×25mm、負極を31mm×26mmに裁断し、ラミネートフィルムで収容した。この正極および負極の間に、セパレータとしてポリプロピレン樹脂からなる矩形状シート(40mm×40mm角、厚さ30μm)を挟装して極板群とした。この極板群を二枚一組のラミネートフィルムで覆い、三辺をシールした後、袋状となったラミネートフィルムに上記の電解液を注入した。その後、残りの一辺をシールすることで、四辺が気密にシールされ、極板群および電解液が密閉されたラミネートセルを得た。電解液にはEC(エチレンカーボネート)、MEC(メチルエチルカーボネート)、DMC(ジメチルカーボネート)=3:3:4(体積比)の混合溶液にLiPF6を1モル/Lとなる濃度で溶解したものを用いた。正極および負極は外部と電気的に接続可能なタブを備え、このタブの一部はラミネートセルの外側に延出した。以上の工程で、単層ラミネートセルのリチウムイオン二次電池を得た。
【0051】
[比較例]
シリカ微粒子1.5質量部に代えてポリアミドイミドを1.5質量部増量したこと以外は実施例と同様にして負極を形成した。すなわちシリカ分散液を用いることなく、バインダ溶液をシリカ当量分増量した。
この負極を用い、実施例と同様にしてリチウムイオン二次電池を作成した。
【0052】
<サイクル特性試験>
実施例及び比較例のリチウムイオン二次電池に対し、下記に示す条件で充放電を繰り返すのを300サイクル行った。
充電:4.2V 1C CC 55℃
放電:2.5V 1C CC 55℃
【0053】
そのときのサイクル数に対する放電容量維持率を測定し、結果を図1に示す。また300サイクル目の放電容量維持率と300サイクル時の内部抵抗上昇率を表1に示す。ここで放電維持率は、1サイクル目の放電容量を100としたときの各サイクル目における放電容量である。また内部抵抗上昇率は、1サイクル目の内部抵抗に対して、300サイクル時における内部抵抗が上昇した度合いの比率である。
【0054】
<評価>
【表1】

【0055】
図1から、実施例に係るリチウムイオン二次電池は比較例に比べてサイクル特性が向上していることがわかる。そして表1から、この理由は、実施例に係るリチウムイオン二次電池は比較例に比べて内部抵抗の上昇が抑制されたことに起因していることが明らかである。
【0056】
<ACインピーダンス測定試験>
実施例及び比較例に係るリチウムイオン二次電池についてそれぞれACインピーダンス測定を行った。測定は、4.2V、1C、の条件でCCCV充電を行った後の電池を用い、東洋システム社製の測定器を用いて25℃で行った。結果を図2に示す。
【0057】
<評価>
図2より、実施例に係るリチウムイオン二次電池は比較例に係るリチウムイオン二次電池に比べて反応抵抗が小さいことが明らかであり、これはシリカ微粒子を含むことによる効果であることが明らかである。
【特許請求の範囲】
【請求項1】
集電体と、該集電体に形成された負極活物質層と、からなるリチウムイオン二次電池用負極であって、
該負極活物質層には、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な該元素の酸化物粒子と、バインダと、を含み、該酸化物粒子の平均粒子径は該Li吸蔵粒子の平均粒子径より小さいことを特徴とするリチウムイオン二次電池用負極。
【請求項2】
リチウムと合金化反応可能な前記元素はシリコン(Si)である請求項1に記載のリチウムイオン二次電池用負極。
【請求項3】
前記Li吸蔵粒子はSiO系粒子である請求項1又は請求項2に記載のリチウムイオン二次電池用負極。
【請求項4】
前記酸化物粒子の平均粒子径は前記Li吸蔵粒子の平均粒子径の1/100以下である請求項1〜請求項3のいずれかに記載のリチウムイオン二次電池用負極。
【請求項5】
前記バインダは、ポリイミド、ポリアミドイミド、ポリアミドイミドシリカハイブリッド、ポリアクリル酸、カルボキシメチルセルロースから選ばれる少なくとも一種である請求項1〜請求項4のいずれかに記載のリチウムイオン二次電池用負極。
【請求項6】
前記負極活物質層における前記酸化物粒子の含有量は、体積%で、前記負極活物質層における前記Li吸蔵粒子の含有量より少ない請求項1〜請求項5のいずれかに記載のリチウムイオン二次電池用負極。
【請求項7】
請求項1〜請求項6のいずれかに記載の負極を用いたことを特徴とするリチウムイオン二次電池。
【請求項8】
請求項7に記載のリチウムイオン二次電池を搭載したことを特徴とする車両。
【請求項1】
集電体と、該集電体に形成された負極活物質層と、からなるリチウムイオン二次電池用負極であって、
該負極活物質層には、少なくともリチウムと合金化反応可能な元素を含みリチウムイオンを吸蔵可能なLi吸蔵粒子と、リチウムと合金化反応可能な該元素の酸化物粒子と、バインダと、を含み、該酸化物粒子の平均粒子径は該Li吸蔵粒子の平均粒子径より小さいことを特徴とするリチウムイオン二次電池用負極。
【請求項2】
リチウムと合金化反応可能な前記元素はシリコン(Si)である請求項1に記載のリチウムイオン二次電池用負極。
【請求項3】
前記Li吸蔵粒子はSiO系粒子である請求項1又は請求項2に記載のリチウムイオン二次電池用負極。
【請求項4】
前記酸化物粒子の平均粒子径は前記Li吸蔵粒子の平均粒子径の1/100以下である請求項1〜請求項3のいずれかに記載のリチウムイオン二次電池用負極。
【請求項5】
前記バインダは、ポリイミド、ポリアミドイミド、ポリアミドイミドシリカハイブリッド、ポリアクリル酸、カルボキシメチルセルロースから選ばれる少なくとも一種である請求項1〜請求項4のいずれかに記載のリチウムイオン二次電池用負極。
【請求項6】
前記負極活物質層における前記酸化物粒子の含有量は、体積%で、前記負極活物質層における前記Li吸蔵粒子の含有量より少ない請求項1〜請求項5のいずれかに記載のリチウムイオン二次電池用負極。
【請求項7】
請求項1〜請求項6のいずれかに記載の負極を用いたことを特徴とするリチウムイオン二次電池。
【請求項8】
請求項7に記載のリチウムイオン二次電池を搭載したことを特徴とする車両。
【図1】


【図2】




【図2】


【公開番号】特開2013−98070(P2013−98070A)
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願番号】特願2011−240982(P2011−240982)
【出願日】平成23年11月2日(2011.11.2)
【出願人】(000003218)株式会社豊田自動織機 (4,162)
【Fターム(参考)】
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願日】平成23年11月2日(2011.11.2)
【出願人】(000003218)株式会社豊田自動織機 (4,162)
【Fターム(参考)】
[ Back to top ]

