リビングラジカル重合開始剤およびこれを用いた重合体
【課題】 核磁気共鳴装置を用いた測定で、重合体由来のプロトン吸収ケミカルシフト値と大きく異なるケミカルシフト値を有する開始剤を提供し、分子量の算出が容易となる重合体を提供することを目的とする。
【解決手段】 下記に示される化合物を重合開始剤とする。ここで、R1〜R2は水素原子、アルキル基を、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、アルキル基、アリール基、等を表し、mは0を含む3までの整数を表し、nは0を含む整数を表す。
【化1】

【解決手段】 下記に示される化合物を重合開始剤とする。ここで、R1〜R2は水素原子、アルキル基を、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、アルキル基、アリール基、等を表し、mは0を含む3までの整数を表し、nは0を含む整数を表す。
【化1】

【発明の詳細な説明】
【技術分野】
【0001】
本発明は、重合開始剤およびこれを用いた重合体に関し、特に原子移動型リビングラジカル重合で用いる開始剤およびこれを用いた重合体に関する。
【背景技術】
【0002】
従来、原子移動型リビングラジカル重合方法の1つであるATRP法(Atomic Transfer Radical Polymerization(ATRP)法)は、分子内に塩素原子または臭素原子を有する化合物を用いることで、簡便に狭分散重合体が得られる方法として知られている(例えば非特許文献1〜7参照)。
【非特許文献1】Jin-Shan Wang : J.Am.Chem.Soc. ,117,5614(1995)
【非特許文献2】Jin-Shan Wang : Macromolecules, 28,7572 (1995)
【非特許文献3】Virgil Percec : Macromolecules,28,7970(1995)
【非特許文献4】Mitsuru Kato : Macromolecules,28,1721(1995)
【非特許文献5】Jianhui Xia : Macromolecules, 32, 3531(1999)
【非特許文献6】Dong-Qi Qin : Macromolecules, 33, 6987(2000)
【非特許文献7】Shenmin Zhu : Macromolecules, 33, 8233(2000)
【発明の開示】
【発明が解決しようとする課題】
【0003】
重合体の分子量の測定方法として、核磁気共鳴装置(NMR)を用い、重合体末端の開始剤由来の吸収とそれ以外に由来するプロトンの吸収スペクトルの強度比を元に算出することは知られている。しかしながら、従来知られている開始剤では、開始剤に由来のケミカルシフト値と、それ以外の重合体のケミカルシフト値の差が小さいため、重合度が大きくなると重合体由来の吸収に紛れてしまい重合体分子量を正確に算出することが難しくなる点に問題があった。
【0004】
これに対し、本出願人は前述の問題点を解決するための化合物について既に出願しているが、スチレン類のような芳香族系の重合体では、芳香族環由来の吸収と開始剤のそれとが重なるために利用することが難しかった。
【0005】
本発明は、上述した実情を考慮してなされたもので、核磁気共鳴装置を用いた測定で、重合体由来のプロトン吸収ケミカルシフト値と大きく異なるケミカルシフト値を有する開始剤を提供し、分子量の算出が容易となる重合体を提供することを目的とする。
【課題を解決するための手段】
【0006】
上記の課題を解決するために、請求項1に記載の発明は、下記一般式(1)で示される化合物を特徴とする。
【0007】
【化1】

【0008】
一般式(1)において、R1〜R2はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表し、nは0を含む整数を表す。尚、mが2以上のとき、Y1は上記の何れかの置換基を表し、これらは同一でも異なっていてもよい。)
【0009】
また、請求項2に記載の発明は、請求項1記載の化合物が、請求項1記載の化合物が、下記一般式(2)で示される化合物を特徴とする。
【0010】
【化2】

【0011】
(一般式(2)において、R3〜R4は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X2はハロゲン原子を表し、Y2は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基の中から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y2は上記の何れかの置換基を表し、これら2以上のY2は同一でも異なっていてもよい。)
【0012】
また、請求項3に記載の発明は、請求項1記載の化合物が、下記一般式(3)で示される化合物を特徴とする。
【0013】
【化3】

【0014】
(一般式(3)において、R5〜R6はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X3はハロゲン原子を表し、Y3は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し、これら2以上のY3は同一でも異なっていてもよい。)
【0015】
また、請求項4に記載の発明は、請求項1から3の何れか1項に記載の化合物を開始剤とした重合方法を特徴とする。
【0016】
また、請求項5に記載の発明は、請求項1から3の何れか1項に記載の化合物由来の残基が含まれる重合体を特徴とする。
【0017】
また、請求項6に記載の発明は、請求項5記載の重合体において、繰り返し単位の1つが下記一般式(4)であらわされることを特徴とする。
【0018】
【化4】

【0019】
(一般式(4)において、R7、R8は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表す。)
【0020】
また、請求項7に記載の発明は、請求項5記載の重合体において、繰り返し単位の1つが前記一般式(5)で示される重合体を特徴とする。
【0021】
【化5】

【0022】
(一般式(5)において、R9は水素原子、置換もしくは未置換のアルキル基のいずれかを表し、Y4は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜5までの整数を表す。尚、mが2以上のとき、Y4は上記の何れかの置換基を表し、2以上のY4は同一でも異なっていてもよい。)
【0023】
また、請求項8に記載の発明は、請求項5から7のいずれか1項に記載の重合体をマクロ開始剤とする重合方法を特徴とする。
【0024】
また、請求項9に記載の発明は、請求項8記載の重合方法により得られるブロック重合体を特徴とする。
【発明の効果】
【0025】
本発明によれば、前記一般式(1)で示される化合物により、1,3−ベンゾ[d]オキソレン環2位のメチレン基由来のプロトン吸収帯と、スチレン類を代表とする芳香族環含有ビニル重合体由来のプロトン吸収帯と独立に観察できることが可能となる。
これらを開始材として合成した重合体は、分子量を正しく算出することが出来きることが明らかとなった。
本発明により、NMRによる分子量評価を目的とした新しい開始剤が提供でき、高真空下封止したアンプル等で合成することなく簡便な環境で重合体を合成する方法が提供できた。
【0026】
また、正確な分子量を評価した重合体が提供でき、マクロ開始剤が提供でき、作られたマクロ開始剤を用いたブロック重合体の合成方法が提供でき、NMRにより分子量を算出できるブロック共重合体が提供できた。
【発明を実施するための最良の形態】
【0027】
以下、図面を参照して、本発明の実施形態を詳細に説明する。
本発明は、下記一般式(1)で示される化合物を特徴とする。
【0028】
【化6】

【0029】
上記一般式(1)において、R1〜R2はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表し、nは0を含む整数を表す。尚、mが2以上のとき、Y1は上記の何れかの置換基を表し、これらは同一でも異なっていてもよい。
【0030】
前記アルキル基の具体例としては、メチル基、エチル基、n−プロピル基、n−ブチル基、n−ペンチル基、n−ヘキシル基、n−ヘプチル基、n−オクチル基、n−ノニル基、n−デシル基等の一級アルキル基、イソブチル基、イソアミル基、2−メチルブチル基、2−メチルペンチル基、3−メチルペンチル基、4−メチルペンチル基、2−エチルブチル基、2−メチルヘキシル基、3−メチルヘキシル基、4−メチルヘキシル基、5−メチルヘキシル基、2−エチルペンチル基、3−エチルペンチル基、2−メチルヘプチル基、3−メチルヘプチル基、4−メチルヘプチル基、5−メチルヘプチル基、2−エチルヘキシル基、3−エチルヘキシル基、イソプロピル基、sec−ブチル基、1−エチルプロピル基、1−メチルブチル基、1,2−ジメチルプロピル基、1−メチルヘプチル基、1−エチルブチル基、1,3−ジメチルブチル基、1,2−ジメチルブチル基、1−エチル−2−メチルプロピル基、1−メチルヘキシル基、1−エチルヘプチル基、1−プロピルブチル基、1−イソプロピル−2−メチルプロピル基、1−エチル−2−メチルブチル基、1−エチル−2−メチルブチル基、1−プロピル−2−メチルプロピル基、1−メチルヘプチル基、1−エチルヘキシル基、1−プロピルペンチル基、1−イソプロピルペンチル基、1−イソプロピル−2−メチルブチル基、1−イソプロピル−3−メチルブチル基、1−メチルオクチル基、1−エチルヘプチル基、1−プロピルヘキシル基、1−イソブチル−3−メチルブチル基等の二級アルキル基、ネオペンチル基、tert−ブチル基、tert−ヘキシル基、tert−アミル基、tert−オクチル基等の三級アルキル基、シクロヘキシル基、4−メチルシクロヘキシル基、4−エチルシクロヘキシル基、4−tert−ブチルシクロヘキシル基、4−(2−エチルヘキシル)シクロヘキシル基、ボルニル基、イソボルニル基(アダマンタン基)等のシクロアルキル基等が挙げられる。更に、これら一級及び二級アルキル基は、水酸基、ハロゲン原子、ニトロ基、カルボキシ基、シアノ基、置換又は未置換のアリール基、置換又は未置換の複素環残基等をもって置換されていてもよく、また酸素、硫黄、窒素等の原子を介して前記のアルキル基で置換されていてもよい。酸素を介して置換されているアルキル基としては、メトキシメチル基、メトキシエチル基、エトキシメチル基、エトキシエチル基、ブトキシエチル基、エトキシエトキシエチル基、フェノキシエチル基、メトキシプロピル基、エトキシプロピル基、ピペリジノ基、モルホリノ基等が、硫黄を介して置換されているアルキル基としては、メチルチオエチル基、エチルチオエチル基、エチルチオプロピル基、フェニルチオエチル基等が、窒素を介して置換されているアルキル基としては、ジメチルアミノエチル基、ジエチルアミノエチル基、ジエチルアミノプロピル基等が挙げられる。複素環残基の具体例としては、インドリル基、フリル基、チエニル基、ピリジル基、ピペリジル基、キノリル基、イソキノリル基、ピペリジノ基、モルホリノ基、ピロリル基等が挙げられる。
【0031】
ハロゲン原子の具体例は、塩素、臭素、ヨウ素等が挙げられる。
【0032】
一般式(2)において、R3〜R4はそれぞれ独立に水素原子、置換もしくは未置換のアルキル基を表し、X2はハロゲン原子を表し、Y2は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基を表し、mは0を含む3までの整数を表す。尚、mが2以上のとき、Y2は上記の何れかの置換基を表し同じである必要はない。
置換基の具体例は、前述のものと同じである。
【0033】
一般式(3)において、R5〜R6はそれぞれ独立に水素原子、置換もしくは未置換のアルキル基を表し、X3はハロゲン原子を表し、Y3は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基を表し、mは0を含む3までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し同じである必要はない。
置換基の具体例は、前述のものと同じである。
【0034】
請求項1に記載した開始剤は、その分子内に1,3ベンゾ[d]オキソレン環を有していることが特徴である。1,3−ベンゾ[d]オキソレン環のメチレン基のプロトンは、プロトンNMRスペクトルにおいてケミカルシフト値約6.0ppmに特徴的なシングレットの吸収帯を示す。多くの重合体のプロトン吸収帯と独立して観測することが出来るため、この開始剤を用いて合成した重合体は、NMR測定により平均分子量を簡便に算出することが出来る。
【0035】
特に、一般式(1)においてn=1のとき、即ち一般式(3)の化学構造であるとき、ベンゼン環とエステル基とに挟まれたメチレン基のプロトンは、約5.1ppmに特徴的なシングレットの吸収帯を示す。ケミカルシフト基5.1ppmに吸収を有する重合体はほぼ皆無のため極めて有効であることを確認した。
【0036】
一般的にATRP法による重合手順は、大体次のようなものである。
必要となる原材料をアンプル等の容器に入れ、液体窒素等の中に投入し内容物を凝固する。次に、真空ポンプ等により十分に脱気しコック等で密栓後、内容物を溶解し液体中の溶存気体を気相中に排出する。次に、容器内に窒素等の酸素を含まない気体で容器内を置換する。この一連の作業を数回繰り返した後、再度容器内をポンプ等で吸引し高真空状態にした後、容器を完全に密封する。この際、ガラス製の容器の口をバーナー等で焼き切り密封することが多い。この後、必要な温度に加熱することで、反応が開始される。
【0037】
ATRP法で用いられる開始剤の多くは沸点が低いため、脱気の際、液体窒素等に投入するなどして開始剤の蒸発を防止し、反応系内の化学量比が変わらないように工夫する必要がある。これに対し、一般式(1)〜(3)で示される開始剤は沸点が高いため、脱気による開始剤の蒸発を然程気にする必要がない。
【0038】
一般式(1)〜(3)で示される開始剤を用いた重合では、反応容器に原材料を入れ室温下、原材料および容器内から脱酸素後、アルゴン、窒素等のラジカルに影響しない不活性ガスで置換し、大気圧下、必要な加熱をすることで一般式(1)〜(3)の残基を開始末端とする重合体を得ることが出来る。
【0039】
このようにして得た重合体をNMRによりプロトンの吸収を観測すると、重合体に由来する吸収と異なる位置に開始剤由来の吸収を観測できるため、重合体の分子量を決定することが容易である。
【0040】
一般式(1)〜(3)で示した開始剤は、一般式(4)で示される繰り返し単位を持つアクリレート系重合体、および一般式(5)で示される繰り返し単位を持つスチレン系重合体において有利であった。
一般式(4)において、R7、R8はそれぞれ独立に水素原子、置換もしくは未置換のアルキル基を表す。
置換基の具体例は、前述のものと同じである。
【0041】
一般式(5)において、R9は水素原子、置換もしくは未置換のアルキル基を表し、Y4は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基を表し、mは0を含む5までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し同じである必要はない。
置換基の具体例は、前述のものと同じである。
【0042】
アクリレート系重合体を合成する際用いられる開始剤の多くは、分子量の小さなエステル系化合物である。このような開始剤を用いて合成した重合体の分子量特定は、エステル基の酸素と結合したメチル、メチレンもしくはメチン基のプロトン吸収と、重合体のエステル基の酸素と結合したメチル、メチレンもしくはメチン基のプロトン吸収との強度比により決定している。
【0043】
重合体の分子量が大きくなるに従い、開始剤由来の吸収が重合体の吸収に埋もれてしまい判断できない。また、HEMA(ヒドロキシエチルメタアクリレート)の重合体では、開始剤の由来の吸収が重合体の吸収に完全に重なるため、分子量を決定することが出来ない。
例として、2−ブロモ−2−メチルプロピオン酸エチルエステルを開始剤としたMMA(メチルメタアクリレート)重合体のNMRスペクトル図1に、同じ開始剤を用いたMMAとHEMAの共重合体のスペクトルを図2に示した。図1には開始剤由来のメチレン基の吸収が約4.1ppmに観察されている。開始剤由来の吸収とMMA由来の吸収が近いため、重合体の分子量が大きくなるに従い、開始剤の吸収が隠れてしまう。また、HEMAの存在する重合体では、図2が示すように開始剤由来のスペクトルが観察される4.1ppm付近に、HEMA由来の吸収があり開始剤由来の吸収と重なるため観測することが出来ない。
【0044】
これに対し、化合物例(1)を開始剤として重合したMMAとHEMAの重合体のスペクトルを図3に示した。開始剤由来の吸収が、5.99ppm、6.48ppm、6.57ppmおよび6.77ppmに観測される。この吸収帯と重合体由来の吸収帯の強度比により合成した重合体の平均分子量が確定できる。
【0045】
スチレン系重合体を合成する際用いられる開始剤は、前述のアクリレート系で用いられる分子量の小さなエステル系化合物や、分子量の小さなハロゲン化アルキルベンゼン等が用いられる。これらの開始剤は、前述のアクリレート系重合体のように開始剤由来の吸収と重合体由来の吸収が重なることはない。しかしながら、後述のように例えば、スチレン系重合体とアクリレート系重合体とのブロック共重合体を作成した場合、これらの開始剤由来の吸収は確認できなくなってしまう。
【0046】
このように、一般式(1)〜(3)で示される開始剤から合成された重合体は、その分子量を正確に決められるためマクロ開始剤として利用することに適している。分子量の決定されたマクロ開始剤を用いることで、必要となる触媒量を正確に投入出来るため、ブロック重合体の合成方法として優れている。
【0047】
例えば、化合物例(2)を開始剤に用いてポリスチレンを合成し、これをマクロ開始剤としてPSt−b−(PMMA−PHEMA)ブロック共重合体を合成した。このブロック共重合体のNMRスペクトルを図4に示した。開始剤由来の吸収が4.96ppmおよび5.98ppmに重合体由来の吸収に独立して観察されているため、このブロック重合体の平均分子量をNMRにて決定することが出来る(なおPStのPは、ポリの略であり、Stはスチレンのことである)。
【0048】
次に、実施例によって本発明をさらに詳細に説明する。ただし、本発明は以下の実施例によって限定されるものではない。
【実施例1】
【0049】
化合物例1の合成
反応容器にセサモール10.0g、脱水THF100ml、およびトリエチルアミン9.5gを投入し、氷浴にて5℃以下まで冷却した。この溶液に臭化2−ブロモ−2−メチルプロピオン酸18.3gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後、濾液を濃縮し水300mlに排出した。中和後、これをトルエンで抽出し、トルエン層を無水硫酸ナトリウムで乾燥後濃縮した。濃縮後蒸留し、下記化合物である目的物20.0g(化合物例1)を得た。
【0050】
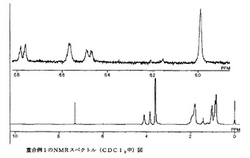
化合物例1の1H−NMRスペクトル(CDCl3中)を図5に示し、このスペクトルによるHの積分量と化学シフト値δHからの化学式との対比からの帰属を化7に、化合物例1の13C−NMRスペクトル(CDCl3中)を図6に示し、この図6のスペクトルと化合物例1の化学式中の各Cの図6から求めた化学シフト値δCからの帰属を化8に示す。
【0051】
【化7】

【0052】
【化8】

【実施例2】
【0053】
化合物例2の合成
反応容器にピペロニルアルコール10.0g、脱水THF100ml、およびトリエチルアミン8.7gを投入し、氷浴にて5℃以下まで冷却した。この溶液に臭化2−ブロモ−2−メチルプロピオン酸16.6gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後、濾液を濃縮し水300mlに排出した。中和後、これを酢酸エチルで抽出し、酢酸エチル層を水洗後、無水硫酸ナトリウムで乾燥し濃縮した。濃縮物はカラムクロマトグラフィー(シリカゲル/トルエン)により生成し、下記化合物である目的物18.8g(化合物例2)を得た。
図8は化合物例2の1H−NMRスペクトル(CDCl3中)を表し、このスペクトルからの積分値と化学シフト値δHからの化合物例2のスペクトル(CDCl3中)の帰属を化9に示す。
【0054】
【化9】

【0055】
また化合物例2の図8に示す13C−NMRからの化学シフトδCによる帰属を化10に示す。
【0056】
【化10】

【実施例3】
【0057】
化合物例3の合成
反応容器にセサモール10.0g、脱水THF100ml、およびトリエチルアミン9.5gを投入し、氷浴にて5℃以下まで冷却した。この溶液に塩化2−クロロプロピオン酸11.0gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後、濾液を濃縮し水300mlに排出した。中和後、これをジエチルエーテルで抽出し、このジエチルエーテル層を濃縮した。濃縮物はカラムクロマトグラフィー(シリカゲル/ヘキサン−酢酸エチル(5:1))により精製し、下記化合物である目的物18.8g(化合物例3)を得た。
図9に示す化合物例3の1H−NMRスペクトル(CDCl3中)からの化合物例3の積分値と化学シフト値δHから、化合物例3の帰属を化11に示す。
【0058】
【化11】

【0059】
また図10の13C−NMRスペクトル(CDCl3中)から、化合物例3の帰属を化12に示す。
【0060】
【化12】

【実施例4】
【0061】
化合物例4の合成
反応容器にピペロニルアルコール10.0g、脱水THF(テトラヒドロフラン)100ml、およびトリエチルアミン8.7gを投入し、氷浴にて5℃以下まで冷却した。この溶液に塩化2−クロロプロピオン酸10.0gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後濃縮し、濃縮したオイル状物質を水300mlに排出した。中和後、これをトルエンで抽出し、トルエン層を水洗後濃縮し、目的物18.3gを得た。
図11に示す1H−NMRスペクトル(CDCl3中)からの積分値と化学シフト値δHによる化合物例4の帰属を化13に示す。
【0062】
【化13】

【0063】
また、図12に示す化合物例4の13C−NMRスペクトル(CDCl3中)からの積分値と化学シフト値δCによる化合物例4のCの帰属を化14に示す。
【0064】
【化14】

【実施例5】
【0065】
重合例1の合成
冷却管及びアルゴンガスを充填した風船を取り付けた反応容器中に、MMA4.00g、HEMA1.30g、メチルエチルケトン6ml、1−プロパノール3mlを加えた。次に1,1,4,7,10,10−ヘキサメチルトリエチレンテトラミン0.0192g及び臭化第一銅0.0080gを添加し、銅塩が溶解するまで攪拌した。この溶液に化合物例1を0.0159g投入し、真空ポンプで反応系内を脱気後、系内をアルゴンガスで置換した。この作業を3回繰り返した後、大気圧アルゴンガス雰囲気下、40℃で8時間重合を行った。重合終了後、反応溶液をメタノール−水(1:3)中に排出し、析出したMMA−HEMAランダム共重合体を得た。
【0066】
Mn(NMR)=44,000
Mn(GPC:ゲルパーミエーションクロマトによる)=39,000
Mw(GPC)=51,000
Mw/Mn(GPC)=1.31 GPC:MMA換算
【実施例6】
【0067】
重合例2の合成
冷却管を取り付けた反応容器中に、St5.00g、DMF(ジメチルホルムアミド)4mlを加えた。次にトリ(2−ジメチルアミノエチル)アミン0.0205g及び臭化第一銅0.0098gを添加し、銅塩が溶解するまで攪拌した。銅塩溶解後、真空ポンプで反応系内を脱気後、系内を窒素ガスに置換し窒素ガスを通気した。次に反応容器内に化合物例2を0.0206g投入し、大気圧窒素ガス通気下、120℃で6時間重合を行った。重合終了後、反応溶液をメタノール中に排出し、ポリスチレン(PSt)を得た。
【0068】
Mn(NMR)=19,600
Mn(GPC)=19,100
Mw(GPC)=22,000
Mw/Mn(GPC)=1.15 GPC:St換算
【実施例7】
【0069】
重合例3の合成
反応容器中に重合例2を1.00g、MMA5.00g、HEMA1.5gおよびDMF8mlを加えた。次にトリ(2−ジメチルアミノエチル)アミン0.0141g及び塩化第一銅0.0051gを添加し、銅塩が溶解するまで攪拌した。銅塩溶解後、真空ポンプで反応系内を脱気後、反応容器の口を封かんし、40℃で10時間重合を行った。重合終了後、反応溶液をメタノール−水(1:1)中に排出し、PSt−b−(PMMA−PHEMA)のブロック共重合体を得た。
【0070】
Mn(NMR)=118,000
Mn(GPC)=109,000
Mw(GPC)=122,000
Mw/Mn(GPC)=1.12 GPC:St換算
【実施例8】
【0071】
重合例4の合成
冷却管及びアルゴンガスを充填した風船を取り付けた反応容器中に、重合例1を1.50g、4−ビニルピリジン2.5g、DMF5mlを加えた。次にトリ(2−ジメチルアミノエチル)アミン0.0105g及び塩化第一銅0.0034gを添加し、銅塩が溶解するまで攪拌した。銅塩溶解後、真空ポンプで反応系内を脱気後、系内をアルゴンガスで置換した。この作業を3回繰り返した後、大気圧アルゴンガス雰囲気下、40℃で5時間重合を行った。重合終了後、反応溶液をメタノール−水(1:2)中に排出し、析出したポリ4−ビニルピリジン−b−(PMMA−PHEMA)のブロック共重合体を得た。
【0072】
Mn(NMR)=87,700
Mn(GPC)=86,000
Mw(GPC)=114,000
Mw/Mn(GPC)=1.33 GPC:St換算
【0073】
上記実施例で使用した化合物例一般式を下記に示す。
【0074】
【化15】

【0075】
上記化合物例一般式のR1、R2、Z1,Z2,Z3、n、Xは、化合物例1〜8により下記表1に示すような基で構成した。
【0076】
【表1】

【図面の簡単な説明】
【0077】
【図1】従来例の開始剤由来の基のNMR吸収が重合体の吸収と重なる例のNMRスペクトル図である。
【図2】従来の開始剤由来の吸収が重なる他のNMRスペクトルである。
【図3】本発明の開始剤使用で重なりが無くなったNMRスペクトル図である。
【図4】本発明のブロック共重合体のNMRスペクトル図である。
【図5】化合物例1の1H−NMRスペクトル図である。
【図6】化合物例1の13C−NMRスペクトル図である。
【図7】化合物例2の1H−NMRスペクトル図である。
【図8】化合物例2の13C−NMRスペクトル図である。
【図9】化合物例3の1H−NMRスペクトル図である。
【図10】化合物例3の13C−NMRスペクトル図である。
【図11】化合物例4の1H−NMRスペクトル図である。
【図12】化合物例4の13C−NMRスペクトル図である。
【技術分野】
【0001】
本発明は、重合開始剤およびこれを用いた重合体に関し、特に原子移動型リビングラジカル重合で用いる開始剤およびこれを用いた重合体に関する。
【背景技術】
【0002】
従来、原子移動型リビングラジカル重合方法の1つであるATRP法(Atomic Transfer Radical Polymerization(ATRP)法)は、分子内に塩素原子または臭素原子を有する化合物を用いることで、簡便に狭分散重合体が得られる方法として知られている(例えば非特許文献1〜7参照)。
【非特許文献1】Jin-Shan Wang : J.Am.Chem.Soc. ,117,5614(1995)
【非特許文献2】Jin-Shan Wang : Macromolecules, 28,7572 (1995)
【非特許文献3】Virgil Percec : Macromolecules,28,7970(1995)
【非特許文献4】Mitsuru Kato : Macromolecules,28,1721(1995)
【非特許文献5】Jianhui Xia : Macromolecules, 32, 3531(1999)
【非特許文献6】Dong-Qi Qin : Macromolecules, 33, 6987(2000)
【非特許文献7】Shenmin Zhu : Macromolecules, 33, 8233(2000)
【発明の開示】
【発明が解決しようとする課題】
【0003】
重合体の分子量の測定方法として、核磁気共鳴装置(NMR)を用い、重合体末端の開始剤由来の吸収とそれ以外に由来するプロトンの吸収スペクトルの強度比を元に算出することは知られている。しかしながら、従来知られている開始剤では、開始剤に由来のケミカルシフト値と、それ以外の重合体のケミカルシフト値の差が小さいため、重合度が大きくなると重合体由来の吸収に紛れてしまい重合体分子量を正確に算出することが難しくなる点に問題があった。
【0004】
これに対し、本出願人は前述の問題点を解決するための化合物について既に出願しているが、スチレン類のような芳香族系の重合体では、芳香族環由来の吸収と開始剤のそれとが重なるために利用することが難しかった。
【0005】
本発明は、上述した実情を考慮してなされたもので、核磁気共鳴装置を用いた測定で、重合体由来のプロトン吸収ケミカルシフト値と大きく異なるケミカルシフト値を有する開始剤を提供し、分子量の算出が容易となる重合体を提供することを目的とする。
【課題を解決するための手段】
【0006】
上記の課題を解決するために、請求項1に記載の発明は、下記一般式(1)で示される化合物を特徴とする。
【0007】
【化1】

【0008】
一般式(1)において、R1〜R2はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表し、nは0を含む整数を表す。尚、mが2以上のとき、Y1は上記の何れかの置換基を表し、これらは同一でも異なっていてもよい。)
【0009】
また、請求項2に記載の発明は、請求項1記載の化合物が、請求項1記載の化合物が、下記一般式(2)で示される化合物を特徴とする。
【0010】
【化2】

【0011】
(一般式(2)において、R3〜R4は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X2はハロゲン原子を表し、Y2は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基の中から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y2は上記の何れかの置換基を表し、これら2以上のY2は同一でも異なっていてもよい。)
【0012】
また、請求項3に記載の発明は、請求項1記載の化合物が、下記一般式(3)で示される化合物を特徴とする。
【0013】
【化3】

【0014】
(一般式(3)において、R5〜R6はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X3はハロゲン原子を表し、Y3は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し、これら2以上のY3は同一でも異なっていてもよい。)
【0015】
また、請求項4に記載の発明は、請求項1から3の何れか1項に記載の化合物を開始剤とした重合方法を特徴とする。
【0016】
また、請求項5に記載の発明は、請求項1から3の何れか1項に記載の化合物由来の残基が含まれる重合体を特徴とする。
【0017】
また、請求項6に記載の発明は、請求項5記載の重合体において、繰り返し単位の1つが下記一般式(4)であらわされることを特徴とする。
【0018】
【化4】

【0019】
(一般式(4)において、R7、R8は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表す。)
【0020】
また、請求項7に記載の発明は、請求項5記載の重合体において、繰り返し単位の1つが前記一般式(5)で示される重合体を特徴とする。
【0021】
【化5】

【0022】
(一般式(5)において、R9は水素原子、置換もしくは未置換のアルキル基のいずれかを表し、Y4は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜5までの整数を表す。尚、mが2以上のとき、Y4は上記の何れかの置換基を表し、2以上のY4は同一でも異なっていてもよい。)
【0023】
また、請求項8に記載の発明は、請求項5から7のいずれか1項に記載の重合体をマクロ開始剤とする重合方法を特徴とする。
【0024】
また、請求項9に記載の発明は、請求項8記載の重合方法により得られるブロック重合体を特徴とする。
【発明の効果】
【0025】
本発明によれば、前記一般式(1)で示される化合物により、1,3−ベンゾ[d]オキソレン環2位のメチレン基由来のプロトン吸収帯と、スチレン類を代表とする芳香族環含有ビニル重合体由来のプロトン吸収帯と独立に観察できることが可能となる。
これらを開始材として合成した重合体は、分子量を正しく算出することが出来きることが明らかとなった。
本発明により、NMRによる分子量評価を目的とした新しい開始剤が提供でき、高真空下封止したアンプル等で合成することなく簡便な環境で重合体を合成する方法が提供できた。
【0026】
また、正確な分子量を評価した重合体が提供でき、マクロ開始剤が提供でき、作られたマクロ開始剤を用いたブロック重合体の合成方法が提供でき、NMRにより分子量を算出できるブロック共重合体が提供できた。
【発明を実施するための最良の形態】
【0027】
以下、図面を参照して、本発明の実施形態を詳細に説明する。
本発明は、下記一般式(1)で示される化合物を特徴とする。
【0028】
【化6】

【0029】
上記一般式(1)において、R1〜R2はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表し、nは0を含む整数を表す。尚、mが2以上のとき、Y1は上記の何れかの置換基を表し、これらは同一でも異なっていてもよい。
【0030】
前記アルキル基の具体例としては、メチル基、エチル基、n−プロピル基、n−ブチル基、n−ペンチル基、n−ヘキシル基、n−ヘプチル基、n−オクチル基、n−ノニル基、n−デシル基等の一級アルキル基、イソブチル基、イソアミル基、2−メチルブチル基、2−メチルペンチル基、3−メチルペンチル基、4−メチルペンチル基、2−エチルブチル基、2−メチルヘキシル基、3−メチルヘキシル基、4−メチルヘキシル基、5−メチルヘキシル基、2−エチルペンチル基、3−エチルペンチル基、2−メチルヘプチル基、3−メチルヘプチル基、4−メチルヘプチル基、5−メチルヘプチル基、2−エチルヘキシル基、3−エチルヘキシル基、イソプロピル基、sec−ブチル基、1−エチルプロピル基、1−メチルブチル基、1,2−ジメチルプロピル基、1−メチルヘプチル基、1−エチルブチル基、1,3−ジメチルブチル基、1,2−ジメチルブチル基、1−エチル−2−メチルプロピル基、1−メチルヘキシル基、1−エチルヘプチル基、1−プロピルブチル基、1−イソプロピル−2−メチルプロピル基、1−エチル−2−メチルブチル基、1−エチル−2−メチルブチル基、1−プロピル−2−メチルプロピル基、1−メチルヘプチル基、1−エチルヘキシル基、1−プロピルペンチル基、1−イソプロピルペンチル基、1−イソプロピル−2−メチルブチル基、1−イソプロピル−3−メチルブチル基、1−メチルオクチル基、1−エチルヘプチル基、1−プロピルヘキシル基、1−イソブチル−3−メチルブチル基等の二級アルキル基、ネオペンチル基、tert−ブチル基、tert−ヘキシル基、tert−アミル基、tert−オクチル基等の三級アルキル基、シクロヘキシル基、4−メチルシクロヘキシル基、4−エチルシクロヘキシル基、4−tert−ブチルシクロヘキシル基、4−(2−エチルヘキシル)シクロヘキシル基、ボルニル基、イソボルニル基(アダマンタン基)等のシクロアルキル基等が挙げられる。更に、これら一級及び二級アルキル基は、水酸基、ハロゲン原子、ニトロ基、カルボキシ基、シアノ基、置換又は未置換のアリール基、置換又は未置換の複素環残基等をもって置換されていてもよく、また酸素、硫黄、窒素等の原子を介して前記のアルキル基で置換されていてもよい。酸素を介して置換されているアルキル基としては、メトキシメチル基、メトキシエチル基、エトキシメチル基、エトキシエチル基、ブトキシエチル基、エトキシエトキシエチル基、フェノキシエチル基、メトキシプロピル基、エトキシプロピル基、ピペリジノ基、モルホリノ基等が、硫黄を介して置換されているアルキル基としては、メチルチオエチル基、エチルチオエチル基、エチルチオプロピル基、フェニルチオエチル基等が、窒素を介して置換されているアルキル基としては、ジメチルアミノエチル基、ジエチルアミノエチル基、ジエチルアミノプロピル基等が挙げられる。複素環残基の具体例としては、インドリル基、フリル基、チエニル基、ピリジル基、ピペリジル基、キノリル基、イソキノリル基、ピペリジノ基、モルホリノ基、ピロリル基等が挙げられる。
【0031】
ハロゲン原子の具体例は、塩素、臭素、ヨウ素等が挙げられる。
【0032】
一般式(2)において、R3〜R4はそれぞれ独立に水素原子、置換もしくは未置換のアルキル基を表し、X2はハロゲン原子を表し、Y2は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基を表し、mは0を含む3までの整数を表す。尚、mが2以上のとき、Y2は上記の何れかの置換基を表し同じである必要はない。
置換基の具体例は、前述のものと同じである。
【0033】
一般式(3)において、R5〜R6はそれぞれ独立に水素原子、置換もしくは未置換のアルキル基を表し、X3はハロゲン原子を表し、Y3は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基を表し、mは0を含む3までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し同じである必要はない。
置換基の具体例は、前述のものと同じである。
【0034】
請求項1に記載した開始剤は、その分子内に1,3ベンゾ[d]オキソレン環を有していることが特徴である。1,3−ベンゾ[d]オキソレン環のメチレン基のプロトンは、プロトンNMRスペクトルにおいてケミカルシフト値約6.0ppmに特徴的なシングレットの吸収帯を示す。多くの重合体のプロトン吸収帯と独立して観測することが出来るため、この開始剤を用いて合成した重合体は、NMR測定により平均分子量を簡便に算出することが出来る。
【0035】
特に、一般式(1)においてn=1のとき、即ち一般式(3)の化学構造であるとき、ベンゼン環とエステル基とに挟まれたメチレン基のプロトンは、約5.1ppmに特徴的なシングレットの吸収帯を示す。ケミカルシフト基5.1ppmに吸収を有する重合体はほぼ皆無のため極めて有効であることを確認した。
【0036】
一般的にATRP法による重合手順は、大体次のようなものである。
必要となる原材料をアンプル等の容器に入れ、液体窒素等の中に投入し内容物を凝固する。次に、真空ポンプ等により十分に脱気しコック等で密栓後、内容物を溶解し液体中の溶存気体を気相中に排出する。次に、容器内に窒素等の酸素を含まない気体で容器内を置換する。この一連の作業を数回繰り返した後、再度容器内をポンプ等で吸引し高真空状態にした後、容器を完全に密封する。この際、ガラス製の容器の口をバーナー等で焼き切り密封することが多い。この後、必要な温度に加熱することで、反応が開始される。
【0037】
ATRP法で用いられる開始剤の多くは沸点が低いため、脱気の際、液体窒素等に投入するなどして開始剤の蒸発を防止し、反応系内の化学量比が変わらないように工夫する必要がある。これに対し、一般式(1)〜(3)で示される開始剤は沸点が高いため、脱気による開始剤の蒸発を然程気にする必要がない。
【0038】
一般式(1)〜(3)で示される開始剤を用いた重合では、反応容器に原材料を入れ室温下、原材料および容器内から脱酸素後、アルゴン、窒素等のラジカルに影響しない不活性ガスで置換し、大気圧下、必要な加熱をすることで一般式(1)〜(3)の残基を開始末端とする重合体を得ることが出来る。
【0039】
このようにして得た重合体をNMRによりプロトンの吸収を観測すると、重合体に由来する吸収と異なる位置に開始剤由来の吸収を観測できるため、重合体の分子量を決定することが容易である。
【0040】
一般式(1)〜(3)で示した開始剤は、一般式(4)で示される繰り返し単位を持つアクリレート系重合体、および一般式(5)で示される繰り返し単位を持つスチレン系重合体において有利であった。
一般式(4)において、R7、R8はそれぞれ独立に水素原子、置換もしくは未置換のアルキル基を表す。
置換基の具体例は、前述のものと同じである。
【0041】
一般式(5)において、R9は水素原子、置換もしくは未置換のアルキル基を表し、Y4は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基を表し、mは0を含む5までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し同じである必要はない。
置換基の具体例は、前述のものと同じである。
【0042】
アクリレート系重合体を合成する際用いられる開始剤の多くは、分子量の小さなエステル系化合物である。このような開始剤を用いて合成した重合体の分子量特定は、エステル基の酸素と結合したメチル、メチレンもしくはメチン基のプロトン吸収と、重合体のエステル基の酸素と結合したメチル、メチレンもしくはメチン基のプロトン吸収との強度比により決定している。
【0043】
重合体の分子量が大きくなるに従い、開始剤由来の吸収が重合体の吸収に埋もれてしまい判断できない。また、HEMA(ヒドロキシエチルメタアクリレート)の重合体では、開始剤の由来の吸収が重合体の吸収に完全に重なるため、分子量を決定することが出来ない。
例として、2−ブロモ−2−メチルプロピオン酸エチルエステルを開始剤としたMMA(メチルメタアクリレート)重合体のNMRスペクトル図1に、同じ開始剤を用いたMMAとHEMAの共重合体のスペクトルを図2に示した。図1には開始剤由来のメチレン基の吸収が約4.1ppmに観察されている。開始剤由来の吸収とMMA由来の吸収が近いため、重合体の分子量が大きくなるに従い、開始剤の吸収が隠れてしまう。また、HEMAの存在する重合体では、図2が示すように開始剤由来のスペクトルが観察される4.1ppm付近に、HEMA由来の吸収があり開始剤由来の吸収と重なるため観測することが出来ない。
【0044】
これに対し、化合物例(1)を開始剤として重合したMMAとHEMAの重合体のスペクトルを図3に示した。開始剤由来の吸収が、5.99ppm、6.48ppm、6.57ppmおよび6.77ppmに観測される。この吸収帯と重合体由来の吸収帯の強度比により合成した重合体の平均分子量が確定できる。
【0045】
スチレン系重合体を合成する際用いられる開始剤は、前述のアクリレート系で用いられる分子量の小さなエステル系化合物や、分子量の小さなハロゲン化アルキルベンゼン等が用いられる。これらの開始剤は、前述のアクリレート系重合体のように開始剤由来の吸収と重合体由来の吸収が重なることはない。しかしながら、後述のように例えば、スチレン系重合体とアクリレート系重合体とのブロック共重合体を作成した場合、これらの開始剤由来の吸収は確認できなくなってしまう。
【0046】
このように、一般式(1)〜(3)で示される開始剤から合成された重合体は、その分子量を正確に決められるためマクロ開始剤として利用することに適している。分子量の決定されたマクロ開始剤を用いることで、必要となる触媒量を正確に投入出来るため、ブロック重合体の合成方法として優れている。
【0047】
例えば、化合物例(2)を開始剤に用いてポリスチレンを合成し、これをマクロ開始剤としてPSt−b−(PMMA−PHEMA)ブロック共重合体を合成した。このブロック共重合体のNMRスペクトルを図4に示した。開始剤由来の吸収が4.96ppmおよび5.98ppmに重合体由来の吸収に独立して観察されているため、このブロック重合体の平均分子量をNMRにて決定することが出来る(なおPStのPは、ポリの略であり、Stはスチレンのことである)。
【0048】
次に、実施例によって本発明をさらに詳細に説明する。ただし、本発明は以下の実施例によって限定されるものではない。
【実施例1】
【0049】
化合物例1の合成
反応容器にセサモール10.0g、脱水THF100ml、およびトリエチルアミン9.5gを投入し、氷浴にて5℃以下まで冷却した。この溶液に臭化2−ブロモ−2−メチルプロピオン酸18.3gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後、濾液を濃縮し水300mlに排出した。中和後、これをトルエンで抽出し、トルエン層を無水硫酸ナトリウムで乾燥後濃縮した。濃縮後蒸留し、下記化合物である目的物20.0g(化合物例1)を得た。
【0050】
化合物例1の1H−NMRスペクトル(CDCl3中)を図5に示し、このスペクトルによるHの積分量と化学シフト値δHからの化学式との対比からの帰属を化7に、化合物例1の13C−NMRスペクトル(CDCl3中)を図6に示し、この図6のスペクトルと化合物例1の化学式中の各Cの図6から求めた化学シフト値δCからの帰属を化8に示す。
【0051】
【化7】

【0052】
【化8】

【実施例2】
【0053】
化合物例2の合成
反応容器にピペロニルアルコール10.0g、脱水THF100ml、およびトリエチルアミン8.7gを投入し、氷浴にて5℃以下まで冷却した。この溶液に臭化2−ブロモ−2−メチルプロピオン酸16.6gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後、濾液を濃縮し水300mlに排出した。中和後、これを酢酸エチルで抽出し、酢酸エチル層を水洗後、無水硫酸ナトリウムで乾燥し濃縮した。濃縮物はカラムクロマトグラフィー(シリカゲル/トルエン)により生成し、下記化合物である目的物18.8g(化合物例2)を得た。
図8は化合物例2の1H−NMRスペクトル(CDCl3中)を表し、このスペクトルからの積分値と化学シフト値δHからの化合物例2のスペクトル(CDCl3中)の帰属を化9に示す。
【0054】
【化9】

【0055】
また化合物例2の図8に示す13C−NMRからの化学シフトδCによる帰属を化10に示す。
【0056】
【化10】

【実施例3】
【0057】
化合物例3の合成
反応容器にセサモール10.0g、脱水THF100ml、およびトリエチルアミン9.5gを投入し、氷浴にて5℃以下まで冷却した。この溶液に塩化2−クロロプロピオン酸11.0gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後、濾液を濃縮し水300mlに排出した。中和後、これをジエチルエーテルで抽出し、このジエチルエーテル層を濃縮した。濃縮物はカラムクロマトグラフィー(シリカゲル/ヘキサン−酢酸エチル(5:1))により精製し、下記化合物である目的物18.8g(化合物例3)を得た。
図9に示す化合物例3の1H−NMRスペクトル(CDCl3中)からの化合物例3の積分値と化学シフト値δHから、化合物例3の帰属を化11に示す。
【0058】
【化11】

【0059】
また図10の13C−NMRスペクトル(CDCl3中)から、化合物例3の帰属を化12に示す。
【0060】
【化12】

【実施例4】
【0061】
化合物例4の合成
反応容器にピペロニルアルコール10.0g、脱水THF(テトラヒドロフラン)100ml、およびトリエチルアミン8.7gを投入し、氷浴にて5℃以下まで冷却した。この溶液に塩化2−クロロプロピオン酸10.0gを滴下し、5時間攪拌を続けた。析出したトリエチルアミン塩酸塩を濾取後濃縮し、濃縮したオイル状物質を水300mlに排出した。中和後、これをトルエンで抽出し、トルエン層を水洗後濃縮し、目的物18.3gを得た。
図11に示す1H−NMRスペクトル(CDCl3中)からの積分値と化学シフト値δHによる化合物例4の帰属を化13に示す。
【0062】
【化13】

【0063】
また、図12に示す化合物例4の13C−NMRスペクトル(CDCl3中)からの積分値と化学シフト値δCによる化合物例4のCの帰属を化14に示す。
【0064】
【化14】

【実施例5】
【0065】
重合例1の合成
冷却管及びアルゴンガスを充填した風船を取り付けた反応容器中に、MMA4.00g、HEMA1.30g、メチルエチルケトン6ml、1−プロパノール3mlを加えた。次に1,1,4,7,10,10−ヘキサメチルトリエチレンテトラミン0.0192g及び臭化第一銅0.0080gを添加し、銅塩が溶解するまで攪拌した。この溶液に化合物例1を0.0159g投入し、真空ポンプで反応系内を脱気後、系内をアルゴンガスで置換した。この作業を3回繰り返した後、大気圧アルゴンガス雰囲気下、40℃で8時間重合を行った。重合終了後、反応溶液をメタノール−水(1:3)中に排出し、析出したMMA−HEMAランダム共重合体を得た。
【0066】
Mn(NMR)=44,000
Mn(GPC:ゲルパーミエーションクロマトによる)=39,000
Mw(GPC)=51,000
Mw/Mn(GPC)=1.31 GPC:MMA換算
【実施例6】
【0067】
重合例2の合成
冷却管を取り付けた反応容器中に、St5.00g、DMF(ジメチルホルムアミド)4mlを加えた。次にトリ(2−ジメチルアミノエチル)アミン0.0205g及び臭化第一銅0.0098gを添加し、銅塩が溶解するまで攪拌した。銅塩溶解後、真空ポンプで反応系内を脱気後、系内を窒素ガスに置換し窒素ガスを通気した。次に反応容器内に化合物例2を0.0206g投入し、大気圧窒素ガス通気下、120℃で6時間重合を行った。重合終了後、反応溶液をメタノール中に排出し、ポリスチレン(PSt)を得た。
【0068】
Mn(NMR)=19,600
Mn(GPC)=19,100
Mw(GPC)=22,000
Mw/Mn(GPC)=1.15 GPC:St換算
【実施例7】
【0069】
重合例3の合成
反応容器中に重合例2を1.00g、MMA5.00g、HEMA1.5gおよびDMF8mlを加えた。次にトリ(2−ジメチルアミノエチル)アミン0.0141g及び塩化第一銅0.0051gを添加し、銅塩が溶解するまで攪拌した。銅塩溶解後、真空ポンプで反応系内を脱気後、反応容器の口を封かんし、40℃で10時間重合を行った。重合終了後、反応溶液をメタノール−水(1:1)中に排出し、PSt−b−(PMMA−PHEMA)のブロック共重合体を得た。
【0070】
Mn(NMR)=118,000
Mn(GPC)=109,000
Mw(GPC)=122,000
Mw/Mn(GPC)=1.12 GPC:St換算
【実施例8】
【0071】
重合例4の合成
冷却管及びアルゴンガスを充填した風船を取り付けた反応容器中に、重合例1を1.50g、4−ビニルピリジン2.5g、DMF5mlを加えた。次にトリ(2−ジメチルアミノエチル)アミン0.0105g及び塩化第一銅0.0034gを添加し、銅塩が溶解するまで攪拌した。銅塩溶解後、真空ポンプで反応系内を脱気後、系内をアルゴンガスで置換した。この作業を3回繰り返した後、大気圧アルゴンガス雰囲気下、40℃で5時間重合を行った。重合終了後、反応溶液をメタノール−水(1:2)中に排出し、析出したポリ4−ビニルピリジン−b−(PMMA−PHEMA)のブロック共重合体を得た。
【0072】
Mn(NMR)=87,700
Mn(GPC)=86,000
Mw(GPC)=114,000
Mw/Mn(GPC)=1.33 GPC:St換算
【0073】
上記実施例で使用した化合物例一般式を下記に示す。
【0074】
【化15】

【0075】
上記化合物例一般式のR1、R2、Z1,Z2,Z3、n、Xは、化合物例1〜8により下記表1に示すような基で構成した。
【0076】
【表1】

【図面の簡単な説明】
【0077】
【図1】従来例の開始剤由来の基のNMR吸収が重合体の吸収と重なる例のNMRスペクトル図である。
【図2】従来の開始剤由来の吸収が重なる他のNMRスペクトルである。
【図3】本発明の開始剤使用で重なりが無くなったNMRスペクトル図である。
【図4】本発明のブロック共重合体のNMRスペクトル図である。
【図5】化合物例1の1H−NMRスペクトル図である。
【図6】化合物例1の13C−NMRスペクトル図である。
【図7】化合物例2の1H−NMRスペクトル図である。
【図8】化合物例2の13C−NMRスペクトル図である。
【図9】化合物例3の1H−NMRスペクトル図である。
【図10】化合物例3の13C−NMRスペクトル図である。
【図11】化合物例4の1H−NMRスペクトル図である。
【図12】化合物例4の13C−NMRスペクトル図である。
【特許請求の範囲】
【請求項1】
下記一般式(1)で示される化合物。
【化1】

(一般式(1)において、R1〜R2はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表し、nは0を含む整数を表す。尚、mが2以上のとき、Y1は上記の何れかの置換基を表し、これらは同一でも異なっていてもよい。)
【請求項2】
請求項1記載の化合物が、下記一般式(2)で示される化合物。
【化2】

(一般式(2)において、R3〜R4は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X2はハロゲン原子を表し、Y2は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基の中から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y2は上記の何れかの置換基を表し、これら2以上のY2は同一でも異なっていてもよい。)
【請求項3】
請求項1記載の化合物が、下記一般式(3)で示される化合物。
【化3】

(一般式(3)において、R5〜R6はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X3はハロゲン原子を表し、Y3は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し、これら2以上のY3は同一でも異なっていてもよい。)
【請求項4】
請求項1から3の何れか1項に記載の化合物を開始剤とした重合方法。
【請求項5】
請求項1から3の何れか1項に記載の化合物由来の残基が含まれる重合体。
【請求項6】
請求項5記載の重合体において、繰り返し単位の1つが下記一般式(4)で示される重合体。
【化4】

(一般式(4)において、R7、R8は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表す。)
【請求項7】
請求項5記載の重合体において、繰り返し単位の1つが下記一般式(5)で示される重合体。
【化5】

(一般式(5)において、R9は水素原子、置換もしくは未置換のアルキル基のいずれかを表し、Y4は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜5までの整数を表す。尚、mが2以上のとき、Y4は上記の何れかの置換基を表し、2以上のY4は同一でも異なっていてもよい。)
【請求項8】
請求項5から7のいずれか1項に記載の重合体をマクロ開始剤とする重合方法。
【請求項9】
請求項8記載の重合方法により得られるブロック重合体。
【請求項1】
下記一般式(1)で示される化合物。
【化1】

(一般式(1)において、R1〜R2はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X1はハロゲン原子を表し、Y1は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表し、nは0を含む整数を表す。尚、mが2以上のとき、Y1は上記の何れかの置換基を表し、これらは同一でも異なっていてもよい。)
【請求項2】
請求項1記載の化合物が、下記一般式(2)で示される化合物。
【化2】

(一般式(2)において、R3〜R4は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X2はハロゲン原子を表し、Y2は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基の中から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y2は上記の何れかの置換基を表し、これら2以上のY2は同一でも異なっていてもよい。)
【請求項3】
請求項1記載の化合物が、下記一般式(3)で示される化合物。
【化3】

(一般式(3)において、R5〜R6はそれぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表し、X3はハロゲン原子を表し、Y3は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜3までの整数を表す。尚、mが2以上のとき、Y3は上記の何れかの置換基を表し、これら2以上のY3は同一でも異なっていてもよい。)
【請求項4】
請求項1から3の何れか1項に記載の化合物を開始剤とした重合方法。
【請求項5】
請求項1から3の何れか1項に記載の化合物由来の残基が含まれる重合体。
【請求項6】
請求項5記載の重合体において、繰り返し単位の1つが下記一般式(4)で示される重合体。
【化4】

(一般式(4)において、R7、R8は、それぞれ独立に、水素原子、置換もしくは未置換のアルキル基のいずれかを表す。)
【請求項7】
請求項5記載の重合体において、繰り返し単位の1つが下記一般式(5)で示される重合体。
【化5】

(一般式(5)において、R9は水素原子、置換もしくは未置換のアルキル基のいずれかを表し、Y4は水素原子、ニトロ基、シアノ基、水酸基、カルボキシ基、アミノ基、置換もしくは未置換のアルキル基、置換もしくは未置換のアリール基、置換もしくは未置換のアルキルオキシ基、置換もしくは未置換のアリールオキシ基、置換もしくは未置換のアルキルアミノ基、置換もしくは未置換のアリールアミノ基、置換もしくは未置換のアルキルカルボニルアミノ基、置換もしくは未置換のアリールカルボニルアミノ基、カルバモイル基、置換もしくは未置換のアルキルカルバモイル基、置換もしくは未置換のアリールカルバモイル基、アルキルスルホニルアミノ基、アリールスルホニルアミノ基から選択される1つの基を表し、mは0〜5までの整数を表す。尚、mが2以上のとき、Y4は上記の何れかの置換基を表し、2以上のY4は同一でも異なっていてもよい。)
【請求項8】
請求項5から7のいずれか1項に記載の重合体をマクロ開始剤とする重合方法。
【請求項9】
請求項8記載の重合方法により得られるブロック重合体。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【公開番号】特開2006−257037(P2006−257037A)
【公開日】平成18年9月28日(2006.9.28)
【国際特許分類】
【出願番号】特願2005−78218(P2005−78218)
【出願日】平成17年3月17日(2005.3.17)
【出願人】(000006747)株式会社リコー (37,907)
【Fターム(参考)】
【公開日】平成18年9月28日(2006.9.28)
【国際特許分類】
【出願日】平成17年3月17日(2005.3.17)
【出願人】(000006747)株式会社リコー (37,907)
【Fターム(参考)】
[ Back to top ]

