リンゴを用いた水素ガス製造方法
【課題】病原性微生物を使用せず、種菌や活性汚泥などの発酵スターターを用いる必要もなく、バイオマスであるリンゴからバイオ水素の産生を行う方法を提供する。
【解決手段】水素発酵のための種菌をバイオマスに投与することなく、リンゴ搾り粕およびリンゴ汁、もしくはそれらの混合物を発酵させて水素ガスを生産する方法であり、種菌投与の作業が無くても発酵し、管理に関する手間の省略化を実現できる。また、発酵に関与する微生物は非病原性であるため、安全に発酵・水素製造・後処理作業を行うことができる。
【解決手段】水素発酵のための種菌をバイオマスに投与することなく、リンゴ搾り粕およびリンゴ汁、もしくはそれらの混合物を発酵させて水素ガスを生産する方法であり、種菌投与の作業が無くても発酵し、管理に関する手間の省略化を実現できる。また、発酵に関与する微生物は非病原性であるため、安全に発酵・水素製造・後処理作業を行うことができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、バイオマスであるリンゴ搾り粕、リンゴジュース、また、それらの混合物を原料として、非病原性細菌を用いて発酵させ、水素を得る技術に関する。
【背景技術】
【0002】
石油などの化石燃料の消費は大気中の二酸化炭素量を増加させ、地球温暖化を引き起こすとされている。これにより、カーボンニュートラル効果が得られることから、石油代替エネルギー源としてバイオマスを利用する方法が注目されている。
【0003】
なかでもバイオマス由来の水素は燃料電池の反応ガス等としても利用可能であり、発電時に生成する物質が水のみであるためクリーンなエネルギー物質とされ注目されている。
【0004】
バイオマスからの水素産生は、水素発酵を行う微生物により行うことが可能である。水素産生に用いられる微生物としては、クロストリジウム属菌や、エンテロバクター属菌、大腸菌属等の嫌気性細菌がある。しかしながらこれらの菌の多くはバイオセーフティレベルが2と病原性を有しており、発酵工程時の安全性に注意を要するものがほとんどである。
【0005】
また光合成細菌も水素発酵を行うことが知られているが、発酵には光エネルギーの供給が必要であり、太陽光を利用した場合は日中の晴天時にしか効率的に発酵しないという問題点がある。また、シアノバクテリアやクロレラ等も水素を産生することで知られているが、水素発生速度が遅く、実用化が困難であるとされている。
【0006】
バイオマスの種類としては様々なものがあるが、未利用バイオマスの一つとしてジュース製造時のリンゴ搾り粕(加工残渣)や、規格外や売れ残り等で農業廃棄物であるリンゴの活用も重要であるとされている。しかしながら、一部飼料粕としての利用はあるものの、バイオマスエネルギーとしての利用はほとんど報告されていない。
【先行技術文献】
【特許文献】
【0007】
【非特許文献1】電子とイオンと機能化学シリーズ,Vol.4,「固体高分子燃料電池のすべて」,第4節,バイオマス水素製造,p234,監修者 田村英雄,担当著者 谷生重晴,2003年10月1日,初版,(株)NTS発行
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は上記従来技術の不都合を解決するために創作されたものであり、その目的は病原性微生物を使用せず、種菌や活性汚泥などの発酵スターターを用いる必要もなく、バイオマスであるリンゴからバイオ水素の生産を行うことができる方法を提供するものである。
【課題を解決するための手段】
【0009】
上記課題を解決するために、本発明は、リンゴ果実を搾ったときの搾り粕とリンゴ汁のうち、前記搾り粕又は前記リンゴ汁のいずれか一方又は両方を含有し、pHが7以上のアルカリ性に調整された培養液を、前記リンゴ果実に付着する常在細菌によって発酵させて水素ガスを放出させる水素ガス製造方法である。
また、本発明は、前記培養液をpH6.5以上に調整する水素ガス製造方法である。
また、本発明は、前記培養液を30℃以上の温度に維持する水素ガス製造方法である。
【発明の効果】
【0010】
売れ残りのリンゴ果実や、リンゴ果実の搾り粕等のリンゴの農業廃棄物から水素ガスが得られる。
リンゴ果実の常在菌であるRhodosporidium属の酵母を利用して発酵するので、活性汚泥や種菌など外部から細菌を投与する工程が必要ない。
Rhodosporidium属の至適であるpH7以上又はpH7付近で発酵させると水素ガス集率が高い。
【図面の簡単な説明】
【0011】
【図1】本発明の水素ガス製造方法を実施できる水素収集装置の一例
【図2】リンゴ培養液の種類による培養日数と気体発生量の積算値との関係を示すグラフ
【図3】光と気体発生量の積算値との関係を示すグラフ
【図4】pHと気体発生量の積算値との関係を示すグラフ
【図5】滅菌処理と発酵との関係を示すグラフ
【図6】ブドウ、桃の培養日数と気体発生量の積算値との関係を示すグラフ
【図7】サン津軽(長野産)のpHと気体発生量の関係を示すグラフ
【図8】高pHでの水素ガス発生状況を示すグラフ
【図9】低pHで水素ガスが発生する場合の例を示すグラフ
【発明を実施するための形態】
【0012】
天然のリンゴには常在菌として、酵母であるRhodosporidium toruloidesがリンゴ果実に付着しており、常在菌を利用するため、バイオマス材料であるリンゴには消毒や加熱・殺菌・滅菌処理を施さず、その天然リンゴの常在菌を利用して水素発酵を行わせる。
【0013】
リンゴ搾り粕およびリンゴジュース、もしくはそれらの混合物から成る培養液は通常pHが4〜5程度の範囲であるが、このpHを7付近に調整することで、Rhodosporidium属の酵母が水素発酵できるような環境とし、発酵に供する。
本発明では、リンゴ搾り粕には、リンゴの皮の部分が含まれており、リンゴジュース(リンゴ搾り汁)は、リンゴ果実の皮を含む粉砕物を搾って取得している。
【0014】
リンゴ搾り粕およびリンゴジュース、もしくはそれらの混合物を、水とともに容器に入れる(以下、発酵溶液)。このリンゴ搾り粕およびリンゴジュース、もしくはそれらの混合物中には常在菌であるRhodosporidium toruloidesが含まれており、種菌や活性汚泥等の発酵スターターを添加する必要性がない。発酵溶液のpHは、未調整の場合は4〜5程度である。
【0015】
この条件では水素発酵が行われないため、pHをRhodosporidium toruloidesが水素発酵を行う条件であるpH7付近に調整して30℃程度の温度を維持しながら、24〜200時間程度放置すると、この発酵溶液から気体が発生する。発生した気体の中には水素と二酸化炭素とが含まれており、水素ガス(H2)濃度は30〜80%程度である。この水素濃度は、燃料電池を駆動させるのに十分な濃度であり、この発酵溶液から得られる気体を利用した発電、すなわちバイオマスエネルギーの利用が可能となる。発酵を行う際には、水素収集速度の観点からは、発酵液の温度は10℃以上40℃以下の範囲に維持することが望ましく、20℃以上35℃以下の範囲に維持することが、一層望ましい。
【0016】
また、発酵を行うために培養液の濃度は所望の値に調整できるが、1gの搾り粕を330mLの水に分散・溶解した培養液(0.3%)から、リンゴジュースを希釈しない培養液(100%)まで、任意の濃度の培養液を発酵させて水素産生を行うことが可能である。
但し、効率を考えた場合、10gの搾り粕を300mLの水に溶解した濃度(3%)以上の濃度の培養液が望ましい。
【0017】
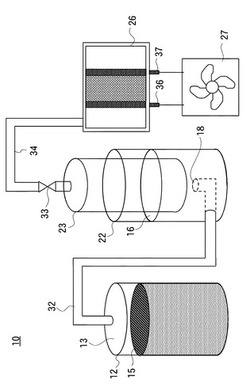
水素貯蔵には、例えば、図1に記載した水素収集装置10を用いることができる。
この水素収集装置10は、発酵槽12と捕集槽22を有しており、発酵槽12には、天井となる部分は蓋13によって閉塞されている。
蓋13には、捕集配管32の一端が接続され、捕集配管32の他端は、捕集槽22の内部に導入され、他端の先端の開口18が捕集槽22の底面の略中心の上方に配置されている。
発酵槽12内に、pH調整された培養液15が配置され、発酵して水素が発生すると、捕集配管32を通って、開口18から捕集槽22内に放出される。
【0018】
開口18の上方には、下端が捕集槽22の上端よりも下方に配置された貯蔵塔23が配置されている。貯蔵塔23の下端は開放され、容器状にされており、予め捕集槽22に捕集水16を注入し、貯蔵塔23の下端を、注入した捕集水16の水面化の位置に浸漬させておくと、開口18から放出された水素は、捕集水16内を泡となって上昇し、水上置換によって、貯蔵塔23内に捕集される。水素が捕集されると、その体積に応じて生じた浮力によって、貯蔵塔23が上昇する。
【0019】
貯蔵塔23の上方に向けられた底面には、サンプル管34の一端が接続され、貯蔵塔23に貯蔵された水素は、サンプル管34内を流れて燃料電池26の内部に導入されるようになっている。
サンプル管34の途中には、コック33が設けられており、開口18から放出された水素を貯蔵塔23の内部に貯蔵するときには、コック33を閉じておき、貯蔵された水素で燃料電池26を動作させるときには、コック33を開け、貯蔵塔23が重力で下降するときの圧力が貯蔵塔23内部の水素に印加され、その圧力で水素が燃料電池26に導入される。
【0020】
燃料電池26の燃料極36と酸素極37とには、ファンモータ27が接続されており、燃料電池26に水素が供給されて発電され、ファンモータ27に電圧が印加されると、ファンモータ27に接続されたプロペラが回転するようになっている。
【0021】
従って、プロペラの回転により、発酵槽12内での発酵による水素の発生から、貯蔵塔23による捕集を経て燃料電池26にて発電するまでの結果を視認することができるので、水素収集装置10は、リンゴの廃棄物を再利用するための教材としても用いることができるし、水素収集装置10を大型化すれば、廃棄物リサイクルによるエネルギーの多様化に寄与することもできる。
【実施例】
【0022】
リンゴ1個を水で軽く洗ってから4つに包丁で切断し、食品用のすりおろし器ですり下ろした。すり下ろしたリンゴは300mL容のガラスビーカー内にてプラスチック製ネット(台所用水切りネット)を用いて搾りとり、この搾り粕を試験に供した。なお、すり下ろしの作業は手の常在菌からのコンタミネーションを防ぐ目的で、ゴム手袋をはめて実施した。
【0023】
調製した搾り粕10gを容積300mLのガラス製三角フラスコ内に入れて脱イオン水を330mL投入した。これにKH2PO4を0.28g、K2HPO4を0.24g、HNaCO3を0.49g(割合はKH2PO40.85g、K2HPO40.75g、HNaCO31.5g/1Lとなる)投入し、pHを7付近に調製された培養液を作製した(上記試薬を投入するだけで、pH7付近となる)。また、培養前後の液体のpHはpHメーター((株)堀場製作所「B−212」)にて測定した。
【0024】
この溶液の入った三角フラスコにテフロンチューブ(テフロンは登録商標)を接続したシリコン栓を差し込み、三角フラスコを照明によって30℃付近(実測温度31℃)の温度に昇温させ、調整した恒温槽(水槽を利用、水は使用せず)内にフラスコを置き、培養液中の微生物を培養し、発酵させた。またテフロンチューブ(テフロンは登録商標)の先端を水の入れた水槽内に沈め、チューブ先端から発生した気体をガラス製メスシリンダー内に水上置換することで、発生気体の捕集を行った。
【0025】
培養日数と気体発生量の積算値との関係を図2に示す。サンフジのリンゴを使用した培養液と、フジのリンゴを使用した培養液とを、滅菌せずに別々に発酵させて発生気体を捕集した。
培養液からは1〜2日後から気体の発生が確認できた。
【0026】
メスシリンダー内に捕集した気体は、プラスチック製シリンジにて回収し、その後ガラスシリンジで空気によって100倍希釈してから、水素濃度を検知管法(水素検知管 U型 光明理化学工業(株)社製)にて水素濃度を測定した。測定した発生気体中の水素濃度を希釈前の濃度に換算すると、50%であった。
【0027】
さらに、シリンジで回収した発生気体は、10mLを燃料電池に投入し、接続したファンモーターが駆動するかどうかについても確認した。駆動時間は、サンフジの場合は6分2秒、フジの場合は7分11秒であった。
発生した気体を燃料電池に投入することで、ファンの駆動から発電が確認できた。これより、バイオマスであるリンゴから電気エネルギーを取り出せることが確認できた。
なお、燃料電池の水素投入口は2ヵ所あるが、投入に使用しない側の投入口には、投入した水素が燃料電池から拡散しないように、シリンジを別途接続しておいた。
【0028】
一方、比較対照として滅菌処理(高圧蒸気滅菌処理)したリンゴからも培養液を作成し、同じ条件で発酵を試みたが、気体は発生しなかった。これより、リンゴ中に含まれている微生物が水素発酵し、水素が産生されていることが確認できた。
また、リンゴバイオマスに加熱等の消毒・殺菌・滅菌処理等をおこなうと、常在菌が死滅するため、発酵が行われず水素産生が見られないことがわかった。
【0029】
<光試験>
フジのリンゴジュースで30%の濃度のものを用い、pHを6.5に調整して培養液を作製した。この培養液は、培養液を配置した発酵容器を遮光して発酵させたときと、光照射しながら発酵させたときとで、それぞれ気体発生量を測定した。培養液は30℃に維持して発酵させた。
【0030】
培養日数と気体発生量の積算値との関係を図3に示す。光照射の有無にかかわらず気体は発生している。この結果から、水素産生が光合成細菌によるものではないことがわかる。発生気体の水素濃度は、光照射したときには30%、光照射しなかったときには25%であった。
発生気体をシリンジで10mL抽出し、燃料電池に注入して動作させると、ファンモーターの回転時間は、光照射したときの発生気体の時と光非照射のときとで、10分以上であった。
【0031】
<pH試験(1)>
次に、フジのリンゴの搾り粕10gを脱イオン水330mLに投入し、pHを4.9、7.0、7.2にそれぞれ調整した培養液を作製し、各培養液を30℃で発酵させた。pH4.9はpH未調整である。
【0032】
初発(発酵開始時)のpH値と気体発生量の積算値との関係を図4に示す。pH未調整の4.9では気体発生が確認されなかったが、pH7付近(pH調整)では気体が発生し、水素濃度はpH7.0の培養液では40%、pH7.2の培養液では45%であった。これより、リンゴバイオマスはpH未調整の場合は水素産生がみられないが、pHを中性域に調整することにより、水素を産生させることが可能であることがわかった。
得られた発生気体をシリンジで5mL抽出し、燃料電池に注入して動作させると、ファンモーターは10分以上回転した。
【0033】
<発酵微生物の同定>
気体発生中の発酵溶液(発酵後48時間)を一部採取し、これをリンゴ寒天培地(リンゴ果汁をpH6.7に調整してから滅菌して調整した寒天平板培地。寒天濃度は1.5%)に塗沫して、発酵溶液中の微生物の釣菌を試みた。その結果、塗沫72時間後には寒天培地上に多数の赤色コロニーおよび少量の白色コロニーが確認された。
【0034】
発酵溶液中の赤色菌数は5×104個/mL程度、白色菌数は2×102個/mL程度であった。生えてきたコロニーの大半は赤色菌であったことから、水素産生に寄与している微生物は赤色菌と考え、この赤色菌の同定を試みた。
【0035】
赤色菌のDNAを抽出し、PCR法によりLarge subunit rRNAのD2領域のDNAを増幅した。増幅したDNAについてABI PRISM 310 Genetic Analyzer(Life technologies corporation)を用いて塩基配列を解析した。得られた配列を国際塩基配列データベース(DDBJ/EMBL/Genbank)に登録されている配列およびMicroseq ID Analysis Software Version 2.0(Life technologies corporation)のデータベースと相同性検索を行い、近縁種との系統樹を近隣結合法(NJ法)により作成した。
【0036】
その結果、Rhodosporidium toruloidesともっとも相同性が高く、その相同性は99.44%であった。この結果から、発酵溶液中の主要微生物である赤色菌はRhodosporidium toruloidesであることがわかった。Rhodosporidium toruloidesは植物、土壌、空気、動物、海水等から分離され、その不完全時代はRhodotorula rubescensである。
【0037】
滅菌リンゴの搾り汁の30%、pH6.7の培養液に、Rhodosporidium toruloidesのコロニーを3白金耳投入し、30℃で培養したところ、図5に示すとおり、気体が発生し水素も確認された。水素ガス濃度は30%であった。(図5のグラフでは、発酵開始3日目から8日目の間は、データを取得していない。)
発生気体をシリンジで5mL抽出し、燃料電池に注入して動作させると、ファンモーターの回転時間は2分30秒であった。
同じ培養液にコロニーを投入せずに30℃で培養した比較対象では、水素は発生しなかった。
【0038】
以上の結果により、リンゴバイオマス由来の水素発生にはRhodosporidium toruloidesが寄与していることが確認できた。
Rhodosporidium toruloidesはバイオセーフティレベルが1であり病原性がないとされている。これから、本微生物を用いたバイオ水素の産生は、発酵・水素製造・後処理作業時において、安全性が高いと言える。
【0039】
<発生ガスの解析>
発生したガスを検知管法にて解析をおこなった。結果の例を下記表1に示す。検知管はいずれも光明理化学工業株式会社製である。
【0040】
【表1】

【0041】
表1の結果は、複数回測定したときの測定結果例を示している。測定のタイミングや使用したリンゴの試験ロットは同一ではない。
ただし、水素、二酸化炭素が主要な発生ガスであり、硫化水素、酢酸、エチレン、アルコール類、アンモニアはほとんど含まれていないことがわかる。
【0042】
発生ガス中には燃料電池の触媒被毒原因物質である硫化水素が含まれていないことから、燃料電池への投入ガスとしては利点がある。アンモニア等の有害ガスも含まれていないことから、安全上も利点が高い。
【0043】
<発酵前後の発酵溶液中の糖質・有機酸・エタノール濃度>
発酵前後の発酵溶液中の糖質・有機酸濃度を測定した。
測定結果は、下記表2に示す。
【0044】
【表2】

【0045】
本試験時には40%の水素を含む気体が65mL産生した。
各成分は酵素法(ロシュ社 F−kit)にて測定した。その結果、ショ糖、麦芽糖、グルコース、フルクトースの糖質およびリンゴ酸は発酵前には比較的高濃度で含まれていたが、発酵後には著しく減少していることが確認できた。一方、エタノール、L/D−乳酸、酢酸は発酵前にはほとんど含まれていなかったが、発酵後には著しく増加していることが確認できた。この結果から、発酵溶液中では糖質およびリンゴ酸を栄養源として微生物が利用し、それにより水素発酵、エタノール発酵、乳酸発酵、酢酸発酵が行われていることがわかる。
pHは、発酵前は7.1であったが、発酵後は5.8にまで低下していた。これは、発酵により酢酸、乳酸などの有機酸が生成したことによることがわかる。
【0046】
<水素産生速度>
本発明における水素産生速度は、試験条件にも左右されるが、事例としては22mmol/L.h程度の結果が得られている。文献によると、非病原性である水素産生微生物の産生速度は、Oscillatoria sp.(ヨレモ)で0.4、Anabaena cylindrical(シアノバクテリア)で1.2、Rhdopseudomonas capslata(光合成細菌)で5.3mmol/L.hであった。これから、本発明による水素産生速度は非病原性微生物としては優れていることがわかる。また、病原性微生物においては、Clostridium beijerinkii(偏性嫌気性菌)で17、Enterobacter aerogenesで36mmol/L.hとなっており、本発明より早いケースはあるものの、本発明の方法は非病原性でありながらこれらの病原性微生物による産生速度とくらべても十分に比較可能なものであることがわかる。
【0047】
<比較例>
天然リンゴに替え、ブドウと桃についても、果実に付着している常在細菌によって発酵させた。その結果を図6に示す。
桃、ブドウについて気体が発生したが、桃の発生気体は75%の水素ガス濃度が検出されていたが、ブドウの発生気体には水素は検出されなかった。
ブドウについては、巨峰についての搾り粕40gを脱イオン水330mLに投入し、桃については白桃の搾り粕20gを脱イオン水330mLに投入し、pHを8.0にして培養液をそれぞれ作成し、30℃で発酵させた。
【0048】
桃、ブドウの発生気体をシリンジで5mL抽出して燃料電池に注入して動作させたところ、ファンモーターの回転時間は桃の発生気体では10分以上であり、ブドウの発生気体では、回転しなかった。
なお、水素発生を確認した時点では、発酵に寄与した常在細菌の特定はできていない。
【0049】
<pH試験(2)>
リンゴの産地と種類を変え、水素発生の試験を行った。
試験結果を下記表3に示す。
【0050】
【表3】

【0051】
上記表3から、発酵開始時のpHの値は、6pH以上8pH未満であれば、水素発生が可能なことが分かる。
次に、長野県産の「サン津軽」のリンゴの搾り粕10gを300mLの水に溶解し、濃度(3%)で、pH値が4.9、5.8、7.0、7.9の四種類の培養液を作成し、発酵させた。培養温度は30℃にした。
【0052】
各培養液についての培養日数と気体発生量積算値の関係を、図7に示す。図中の数値は、各培養液についての、発生ガス中の水素ガス濃度と、サンプル気体によるモータ回転時間とを示す値である(シリンジで5mL注入)。これらの試験結果から、pH5以上pH8未満の培養液について、水素発生が確認されている。
【0053】
次に、長野産に替え、会津産「サン津軽」のリンゴで、長野産と同じ濃度、体積で異なるpH値5.8、7.0、8.0、9.1の培養液を作成し、長野産と同じ条件で発酵させた。
その培養液の培養日数と気体発生量の積算値との関係を図8に示す。シリンジへの注入量は5mLである。pH7.0の培養液は水素ガス発生が確認できたが、pH5.8と、pH8〜9の培養液については水素ガス発生は確認できなかった。
【0054】
次に、低pH値でも、大量の水素ガスが発生する例を示す。
図9は、青森産のリンゴ「フジ」の搾り汁30%、pH6.5の培養液を光を照射して発酵させたときと、遮光して発酵させたときの、培養日数と気体発生量の積算値との関係を示すグラフである。光照射したときの水素ガス濃度は30%、遮光したときの水素ガス濃度は25%であった。シリンジで10mL注入したときのモータ駆動時間は、それぞれ10分以上であった。
このグラフの例から分かるように、pH6.5のときでも、水素ガスが大量発生する場合はある。
以上のことにより、水素ガス発生には、培養液のpH値は6以上8未満、発生量を考慮すると、6.5以上8.0未満が望ましい。
【符号の説明】
【0055】
10……水素収集装置
12……発酵槽
23……貯蔵塔
26……燃料電池
27……ファンモータ
【技術分野】
【0001】
本発明は、バイオマスであるリンゴ搾り粕、リンゴジュース、また、それらの混合物を原料として、非病原性細菌を用いて発酵させ、水素を得る技術に関する。
【背景技術】
【0002】
石油などの化石燃料の消費は大気中の二酸化炭素量を増加させ、地球温暖化を引き起こすとされている。これにより、カーボンニュートラル効果が得られることから、石油代替エネルギー源としてバイオマスを利用する方法が注目されている。
【0003】
なかでもバイオマス由来の水素は燃料電池の反応ガス等としても利用可能であり、発電時に生成する物質が水のみであるためクリーンなエネルギー物質とされ注目されている。
【0004】
バイオマスからの水素産生は、水素発酵を行う微生物により行うことが可能である。水素産生に用いられる微生物としては、クロストリジウム属菌や、エンテロバクター属菌、大腸菌属等の嫌気性細菌がある。しかしながらこれらの菌の多くはバイオセーフティレベルが2と病原性を有しており、発酵工程時の安全性に注意を要するものがほとんどである。
【0005】
また光合成細菌も水素発酵を行うことが知られているが、発酵には光エネルギーの供給が必要であり、太陽光を利用した場合は日中の晴天時にしか効率的に発酵しないという問題点がある。また、シアノバクテリアやクロレラ等も水素を産生することで知られているが、水素発生速度が遅く、実用化が困難であるとされている。
【0006】
バイオマスの種類としては様々なものがあるが、未利用バイオマスの一つとしてジュース製造時のリンゴ搾り粕(加工残渣)や、規格外や売れ残り等で農業廃棄物であるリンゴの活用も重要であるとされている。しかしながら、一部飼料粕としての利用はあるものの、バイオマスエネルギーとしての利用はほとんど報告されていない。
【先行技術文献】
【特許文献】
【0007】
【非特許文献1】電子とイオンと機能化学シリーズ,Vol.4,「固体高分子燃料電池のすべて」,第4節,バイオマス水素製造,p234,監修者 田村英雄,担当著者 谷生重晴,2003年10月1日,初版,(株)NTS発行
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は上記従来技術の不都合を解決するために創作されたものであり、その目的は病原性微生物を使用せず、種菌や活性汚泥などの発酵スターターを用いる必要もなく、バイオマスであるリンゴからバイオ水素の生産を行うことができる方法を提供するものである。
【課題を解決するための手段】
【0009】
上記課題を解決するために、本発明は、リンゴ果実を搾ったときの搾り粕とリンゴ汁のうち、前記搾り粕又は前記リンゴ汁のいずれか一方又は両方を含有し、pHが7以上のアルカリ性に調整された培養液を、前記リンゴ果実に付着する常在細菌によって発酵させて水素ガスを放出させる水素ガス製造方法である。
また、本発明は、前記培養液をpH6.5以上に調整する水素ガス製造方法である。
また、本発明は、前記培養液を30℃以上の温度に維持する水素ガス製造方法である。
【発明の効果】
【0010】
売れ残りのリンゴ果実や、リンゴ果実の搾り粕等のリンゴの農業廃棄物から水素ガスが得られる。
リンゴ果実の常在菌であるRhodosporidium属の酵母を利用して発酵するので、活性汚泥や種菌など外部から細菌を投与する工程が必要ない。
Rhodosporidium属の至適であるpH7以上又はpH7付近で発酵させると水素ガス集率が高い。
【図面の簡単な説明】
【0011】
【図1】本発明の水素ガス製造方法を実施できる水素収集装置の一例
【図2】リンゴ培養液の種類による培養日数と気体発生量の積算値との関係を示すグラフ
【図3】光と気体発生量の積算値との関係を示すグラフ
【図4】pHと気体発生量の積算値との関係を示すグラフ
【図5】滅菌処理と発酵との関係を示すグラフ
【図6】ブドウ、桃の培養日数と気体発生量の積算値との関係を示すグラフ
【図7】サン津軽(長野産)のpHと気体発生量の関係を示すグラフ
【図8】高pHでの水素ガス発生状況を示すグラフ
【図9】低pHで水素ガスが発生する場合の例を示すグラフ
【発明を実施するための形態】
【0012】
天然のリンゴには常在菌として、酵母であるRhodosporidium toruloidesがリンゴ果実に付着しており、常在菌を利用するため、バイオマス材料であるリンゴには消毒や加熱・殺菌・滅菌処理を施さず、その天然リンゴの常在菌を利用して水素発酵を行わせる。
【0013】
リンゴ搾り粕およびリンゴジュース、もしくはそれらの混合物から成る培養液は通常pHが4〜5程度の範囲であるが、このpHを7付近に調整することで、Rhodosporidium属の酵母が水素発酵できるような環境とし、発酵に供する。
本発明では、リンゴ搾り粕には、リンゴの皮の部分が含まれており、リンゴジュース(リンゴ搾り汁)は、リンゴ果実の皮を含む粉砕物を搾って取得している。
【0014】
リンゴ搾り粕およびリンゴジュース、もしくはそれらの混合物を、水とともに容器に入れる(以下、発酵溶液)。このリンゴ搾り粕およびリンゴジュース、もしくはそれらの混合物中には常在菌であるRhodosporidium toruloidesが含まれており、種菌や活性汚泥等の発酵スターターを添加する必要性がない。発酵溶液のpHは、未調整の場合は4〜5程度である。
【0015】
この条件では水素発酵が行われないため、pHをRhodosporidium toruloidesが水素発酵を行う条件であるpH7付近に調整して30℃程度の温度を維持しながら、24〜200時間程度放置すると、この発酵溶液から気体が発生する。発生した気体の中には水素と二酸化炭素とが含まれており、水素ガス(H2)濃度は30〜80%程度である。この水素濃度は、燃料電池を駆動させるのに十分な濃度であり、この発酵溶液から得られる気体を利用した発電、すなわちバイオマスエネルギーの利用が可能となる。発酵を行う際には、水素収集速度の観点からは、発酵液の温度は10℃以上40℃以下の範囲に維持することが望ましく、20℃以上35℃以下の範囲に維持することが、一層望ましい。
【0016】
また、発酵を行うために培養液の濃度は所望の値に調整できるが、1gの搾り粕を330mLの水に分散・溶解した培養液(0.3%)から、リンゴジュースを希釈しない培養液(100%)まで、任意の濃度の培養液を発酵させて水素産生を行うことが可能である。
但し、効率を考えた場合、10gの搾り粕を300mLの水に溶解した濃度(3%)以上の濃度の培養液が望ましい。
【0017】
水素貯蔵には、例えば、図1に記載した水素収集装置10を用いることができる。
この水素収集装置10は、発酵槽12と捕集槽22を有しており、発酵槽12には、天井となる部分は蓋13によって閉塞されている。
蓋13には、捕集配管32の一端が接続され、捕集配管32の他端は、捕集槽22の内部に導入され、他端の先端の開口18が捕集槽22の底面の略中心の上方に配置されている。
発酵槽12内に、pH調整された培養液15が配置され、発酵して水素が発生すると、捕集配管32を通って、開口18から捕集槽22内に放出される。
【0018】
開口18の上方には、下端が捕集槽22の上端よりも下方に配置された貯蔵塔23が配置されている。貯蔵塔23の下端は開放され、容器状にされており、予め捕集槽22に捕集水16を注入し、貯蔵塔23の下端を、注入した捕集水16の水面化の位置に浸漬させておくと、開口18から放出された水素は、捕集水16内を泡となって上昇し、水上置換によって、貯蔵塔23内に捕集される。水素が捕集されると、その体積に応じて生じた浮力によって、貯蔵塔23が上昇する。
【0019】
貯蔵塔23の上方に向けられた底面には、サンプル管34の一端が接続され、貯蔵塔23に貯蔵された水素は、サンプル管34内を流れて燃料電池26の内部に導入されるようになっている。
サンプル管34の途中には、コック33が設けられており、開口18から放出された水素を貯蔵塔23の内部に貯蔵するときには、コック33を閉じておき、貯蔵された水素で燃料電池26を動作させるときには、コック33を開け、貯蔵塔23が重力で下降するときの圧力が貯蔵塔23内部の水素に印加され、その圧力で水素が燃料電池26に導入される。
【0020】
燃料電池26の燃料極36と酸素極37とには、ファンモータ27が接続されており、燃料電池26に水素が供給されて発電され、ファンモータ27に電圧が印加されると、ファンモータ27に接続されたプロペラが回転するようになっている。
【0021】
従って、プロペラの回転により、発酵槽12内での発酵による水素の発生から、貯蔵塔23による捕集を経て燃料電池26にて発電するまでの結果を視認することができるので、水素収集装置10は、リンゴの廃棄物を再利用するための教材としても用いることができるし、水素収集装置10を大型化すれば、廃棄物リサイクルによるエネルギーの多様化に寄与することもできる。
【実施例】
【0022】
リンゴ1個を水で軽く洗ってから4つに包丁で切断し、食品用のすりおろし器ですり下ろした。すり下ろしたリンゴは300mL容のガラスビーカー内にてプラスチック製ネット(台所用水切りネット)を用いて搾りとり、この搾り粕を試験に供した。なお、すり下ろしの作業は手の常在菌からのコンタミネーションを防ぐ目的で、ゴム手袋をはめて実施した。
【0023】
調製した搾り粕10gを容積300mLのガラス製三角フラスコ内に入れて脱イオン水を330mL投入した。これにKH2PO4を0.28g、K2HPO4を0.24g、HNaCO3を0.49g(割合はKH2PO40.85g、K2HPO40.75g、HNaCO31.5g/1Lとなる)投入し、pHを7付近に調製された培養液を作製した(上記試薬を投入するだけで、pH7付近となる)。また、培養前後の液体のpHはpHメーター((株)堀場製作所「B−212」)にて測定した。
【0024】
この溶液の入った三角フラスコにテフロンチューブ(テフロンは登録商標)を接続したシリコン栓を差し込み、三角フラスコを照明によって30℃付近(実測温度31℃)の温度に昇温させ、調整した恒温槽(水槽を利用、水は使用せず)内にフラスコを置き、培養液中の微生物を培養し、発酵させた。またテフロンチューブ(テフロンは登録商標)の先端を水の入れた水槽内に沈め、チューブ先端から発生した気体をガラス製メスシリンダー内に水上置換することで、発生気体の捕集を行った。
【0025】
培養日数と気体発生量の積算値との関係を図2に示す。サンフジのリンゴを使用した培養液と、フジのリンゴを使用した培養液とを、滅菌せずに別々に発酵させて発生気体を捕集した。
培養液からは1〜2日後から気体の発生が確認できた。
【0026】
メスシリンダー内に捕集した気体は、プラスチック製シリンジにて回収し、その後ガラスシリンジで空気によって100倍希釈してから、水素濃度を検知管法(水素検知管 U型 光明理化学工業(株)社製)にて水素濃度を測定した。測定した発生気体中の水素濃度を希釈前の濃度に換算すると、50%であった。
【0027】
さらに、シリンジで回収した発生気体は、10mLを燃料電池に投入し、接続したファンモーターが駆動するかどうかについても確認した。駆動時間は、サンフジの場合は6分2秒、フジの場合は7分11秒であった。
発生した気体を燃料電池に投入することで、ファンの駆動から発電が確認できた。これより、バイオマスであるリンゴから電気エネルギーを取り出せることが確認できた。
なお、燃料電池の水素投入口は2ヵ所あるが、投入に使用しない側の投入口には、投入した水素が燃料電池から拡散しないように、シリンジを別途接続しておいた。
【0028】
一方、比較対照として滅菌処理(高圧蒸気滅菌処理)したリンゴからも培養液を作成し、同じ条件で発酵を試みたが、気体は発生しなかった。これより、リンゴ中に含まれている微生物が水素発酵し、水素が産生されていることが確認できた。
また、リンゴバイオマスに加熱等の消毒・殺菌・滅菌処理等をおこなうと、常在菌が死滅するため、発酵が行われず水素産生が見られないことがわかった。
【0029】
<光試験>
フジのリンゴジュースで30%の濃度のものを用い、pHを6.5に調整して培養液を作製した。この培養液は、培養液を配置した発酵容器を遮光して発酵させたときと、光照射しながら発酵させたときとで、それぞれ気体発生量を測定した。培養液は30℃に維持して発酵させた。
【0030】
培養日数と気体発生量の積算値との関係を図3に示す。光照射の有無にかかわらず気体は発生している。この結果から、水素産生が光合成細菌によるものではないことがわかる。発生気体の水素濃度は、光照射したときには30%、光照射しなかったときには25%であった。
発生気体をシリンジで10mL抽出し、燃料電池に注入して動作させると、ファンモーターの回転時間は、光照射したときの発生気体の時と光非照射のときとで、10分以上であった。
【0031】
<pH試験(1)>
次に、フジのリンゴの搾り粕10gを脱イオン水330mLに投入し、pHを4.9、7.0、7.2にそれぞれ調整した培養液を作製し、各培養液を30℃で発酵させた。pH4.9はpH未調整である。
【0032】
初発(発酵開始時)のpH値と気体発生量の積算値との関係を図4に示す。pH未調整の4.9では気体発生が確認されなかったが、pH7付近(pH調整)では気体が発生し、水素濃度はpH7.0の培養液では40%、pH7.2の培養液では45%であった。これより、リンゴバイオマスはpH未調整の場合は水素産生がみられないが、pHを中性域に調整することにより、水素を産生させることが可能であることがわかった。
得られた発生気体をシリンジで5mL抽出し、燃料電池に注入して動作させると、ファンモーターは10分以上回転した。
【0033】
<発酵微生物の同定>
気体発生中の発酵溶液(発酵後48時間)を一部採取し、これをリンゴ寒天培地(リンゴ果汁をpH6.7に調整してから滅菌して調整した寒天平板培地。寒天濃度は1.5%)に塗沫して、発酵溶液中の微生物の釣菌を試みた。その結果、塗沫72時間後には寒天培地上に多数の赤色コロニーおよび少量の白色コロニーが確認された。
【0034】
発酵溶液中の赤色菌数は5×104個/mL程度、白色菌数は2×102個/mL程度であった。生えてきたコロニーの大半は赤色菌であったことから、水素産生に寄与している微生物は赤色菌と考え、この赤色菌の同定を試みた。
【0035】
赤色菌のDNAを抽出し、PCR法によりLarge subunit rRNAのD2領域のDNAを増幅した。増幅したDNAについてABI PRISM 310 Genetic Analyzer(Life technologies corporation)を用いて塩基配列を解析した。得られた配列を国際塩基配列データベース(DDBJ/EMBL/Genbank)に登録されている配列およびMicroseq ID Analysis Software Version 2.0(Life technologies corporation)のデータベースと相同性検索を行い、近縁種との系統樹を近隣結合法(NJ法)により作成した。
【0036】
その結果、Rhodosporidium toruloidesともっとも相同性が高く、その相同性は99.44%であった。この結果から、発酵溶液中の主要微生物である赤色菌はRhodosporidium toruloidesであることがわかった。Rhodosporidium toruloidesは植物、土壌、空気、動物、海水等から分離され、その不完全時代はRhodotorula rubescensである。
【0037】
滅菌リンゴの搾り汁の30%、pH6.7の培養液に、Rhodosporidium toruloidesのコロニーを3白金耳投入し、30℃で培養したところ、図5に示すとおり、気体が発生し水素も確認された。水素ガス濃度は30%であった。(図5のグラフでは、発酵開始3日目から8日目の間は、データを取得していない。)
発生気体をシリンジで5mL抽出し、燃料電池に注入して動作させると、ファンモーターの回転時間は2分30秒であった。
同じ培養液にコロニーを投入せずに30℃で培養した比較対象では、水素は発生しなかった。
【0038】
以上の結果により、リンゴバイオマス由来の水素発生にはRhodosporidium toruloidesが寄与していることが確認できた。
Rhodosporidium toruloidesはバイオセーフティレベルが1であり病原性がないとされている。これから、本微生物を用いたバイオ水素の産生は、発酵・水素製造・後処理作業時において、安全性が高いと言える。
【0039】
<発生ガスの解析>
発生したガスを検知管法にて解析をおこなった。結果の例を下記表1に示す。検知管はいずれも光明理化学工業株式会社製である。
【0040】
【表1】

【0041】
表1の結果は、複数回測定したときの測定結果例を示している。測定のタイミングや使用したリンゴの試験ロットは同一ではない。
ただし、水素、二酸化炭素が主要な発生ガスであり、硫化水素、酢酸、エチレン、アルコール類、アンモニアはほとんど含まれていないことがわかる。
【0042】
発生ガス中には燃料電池の触媒被毒原因物質である硫化水素が含まれていないことから、燃料電池への投入ガスとしては利点がある。アンモニア等の有害ガスも含まれていないことから、安全上も利点が高い。
【0043】
<発酵前後の発酵溶液中の糖質・有機酸・エタノール濃度>
発酵前後の発酵溶液中の糖質・有機酸濃度を測定した。
測定結果は、下記表2に示す。
【0044】
【表2】

【0045】
本試験時には40%の水素を含む気体が65mL産生した。
各成分は酵素法(ロシュ社 F−kit)にて測定した。その結果、ショ糖、麦芽糖、グルコース、フルクトースの糖質およびリンゴ酸は発酵前には比較的高濃度で含まれていたが、発酵後には著しく減少していることが確認できた。一方、エタノール、L/D−乳酸、酢酸は発酵前にはほとんど含まれていなかったが、発酵後には著しく増加していることが確認できた。この結果から、発酵溶液中では糖質およびリンゴ酸を栄養源として微生物が利用し、それにより水素発酵、エタノール発酵、乳酸発酵、酢酸発酵が行われていることがわかる。
pHは、発酵前は7.1であったが、発酵後は5.8にまで低下していた。これは、発酵により酢酸、乳酸などの有機酸が生成したことによることがわかる。
【0046】
<水素産生速度>
本発明における水素産生速度は、試験条件にも左右されるが、事例としては22mmol/L.h程度の結果が得られている。文献によると、非病原性である水素産生微生物の産生速度は、Oscillatoria sp.(ヨレモ)で0.4、Anabaena cylindrical(シアノバクテリア)で1.2、Rhdopseudomonas capslata(光合成細菌)で5.3mmol/L.hであった。これから、本発明による水素産生速度は非病原性微生物としては優れていることがわかる。また、病原性微生物においては、Clostridium beijerinkii(偏性嫌気性菌)で17、Enterobacter aerogenesで36mmol/L.hとなっており、本発明より早いケースはあるものの、本発明の方法は非病原性でありながらこれらの病原性微生物による産生速度とくらべても十分に比較可能なものであることがわかる。
【0047】
<比較例>
天然リンゴに替え、ブドウと桃についても、果実に付着している常在細菌によって発酵させた。その結果を図6に示す。
桃、ブドウについて気体が発生したが、桃の発生気体は75%の水素ガス濃度が検出されていたが、ブドウの発生気体には水素は検出されなかった。
ブドウについては、巨峰についての搾り粕40gを脱イオン水330mLに投入し、桃については白桃の搾り粕20gを脱イオン水330mLに投入し、pHを8.0にして培養液をそれぞれ作成し、30℃で発酵させた。
【0048】
桃、ブドウの発生気体をシリンジで5mL抽出して燃料電池に注入して動作させたところ、ファンモーターの回転時間は桃の発生気体では10分以上であり、ブドウの発生気体では、回転しなかった。
なお、水素発生を確認した時点では、発酵に寄与した常在細菌の特定はできていない。
【0049】
<pH試験(2)>
リンゴの産地と種類を変え、水素発生の試験を行った。
試験結果を下記表3に示す。
【0050】
【表3】

【0051】
上記表3から、発酵開始時のpHの値は、6pH以上8pH未満であれば、水素発生が可能なことが分かる。
次に、長野県産の「サン津軽」のリンゴの搾り粕10gを300mLの水に溶解し、濃度(3%)で、pH値が4.9、5.8、7.0、7.9の四種類の培養液を作成し、発酵させた。培養温度は30℃にした。
【0052】
各培養液についての培養日数と気体発生量積算値の関係を、図7に示す。図中の数値は、各培養液についての、発生ガス中の水素ガス濃度と、サンプル気体によるモータ回転時間とを示す値である(シリンジで5mL注入)。これらの試験結果から、pH5以上pH8未満の培養液について、水素発生が確認されている。
【0053】
次に、長野産に替え、会津産「サン津軽」のリンゴで、長野産と同じ濃度、体積で異なるpH値5.8、7.0、8.0、9.1の培養液を作成し、長野産と同じ条件で発酵させた。
その培養液の培養日数と気体発生量の積算値との関係を図8に示す。シリンジへの注入量は5mLである。pH7.0の培養液は水素ガス発生が確認できたが、pH5.8と、pH8〜9の培養液については水素ガス発生は確認できなかった。
【0054】
次に、低pH値でも、大量の水素ガスが発生する例を示す。
図9は、青森産のリンゴ「フジ」の搾り汁30%、pH6.5の培養液を光を照射して発酵させたときと、遮光して発酵させたときの、培養日数と気体発生量の積算値との関係を示すグラフである。光照射したときの水素ガス濃度は30%、遮光したときの水素ガス濃度は25%であった。シリンジで10mL注入したときのモータ駆動時間は、それぞれ10分以上であった。
このグラフの例から分かるように、pH6.5のときでも、水素ガスが大量発生する場合はある。
以上のことにより、水素ガス発生には、培養液のpH値は6以上8未満、発生量を考慮すると、6.5以上8.0未満が望ましい。
【符号の説明】
【0055】
10……水素収集装置
12……発酵槽
23……貯蔵塔
26……燃料電池
27……ファンモータ
【特許請求の範囲】
【請求項1】
リンゴ果実を搾ったときの搾り粕とリンゴ汁のうち、前記搾り粕又は前記リンゴ汁のいずれか一方又は両方を含有し、pHが6以上8未満のアルカリ性に調整された培養液を、前記リンゴ果実に付着する常在細菌によって発酵させて水素ガスを放出させる水素ガス製造方法。
【請求項2】
前記培養液をpH6.5以上に調整する請求項1記載の水素ガス製造方法。
【請求項3】
前記培養液を30℃以上の温度に維持する請求項1又は請求項2のいずれか1項記載の水素ガス製造方法。
【請求項1】
リンゴ果実を搾ったときの搾り粕とリンゴ汁のうち、前記搾り粕又は前記リンゴ汁のいずれか一方又は両方を含有し、pHが6以上8未満のアルカリ性に調整された培養液を、前記リンゴ果実に付着する常在細菌によって発酵させて水素ガスを放出させる水素ガス製造方法。
【請求項2】
前記培養液をpH6.5以上に調整する請求項1記載の水素ガス製造方法。
【請求項3】
前記培養液を30℃以上の温度に維持する請求項1又は請求項2のいずれか1項記載の水素ガス製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2013−94140(P2013−94140A)
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願番号】特願2011−241637(P2011−241637)
【出願日】平成23年11月2日(2011.11.2)
【出願人】(390010364)光明理化学工業株式会社 (18)
【Fターム(参考)】
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願日】平成23年11月2日(2011.11.2)
【出願人】(390010364)光明理化学工業株式会社 (18)
【Fターム(参考)】
[ Back to top ]

