リン酸化型FMS関連チロシンキナーゼ3バイオマーカーアッセイ
試料におけるヒトpFLT3の存在を検出する方法が本明細書に提供される。本明細書に提供される典型的なアッセイは、ELISA法(例えば、サンドイッチELISA)である。また、試料におけるFLT3リン酸化を検出する方法、FLT3活性化突然変異を有する患者を診断する方法、ヒトFLT3リン酸化を活性化させる化合物又はさもなければヒトFLT3リン酸化のアゴニストである化合物を同定する方法、ヒトFLT3リン酸化を阻害する化合物又はさもなければヒトFLT3リン酸化のアンタゴニストである化合物を同定する方法、患者におけるヒトFLT3リン酸化を増大させ、低下させ、又はさもなければ調節する化合物の有効性を決定する方法も本明細書に提供される。さらに、前記方法を実施するキットが提供される。このようなキットは、固体支持体上に任意に固定化された少なくとも1つの総FLT3抗体と、標識済みpFLT3抗体とを含む。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
血液試料、血液溶解物試料、又は骨髄吸引物試料におけるヒトリン酸化型FMS関連チロシンキナーゼ3(pFLT3)の存在を検出する方法であって:
(a)該試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(d)結合していない第二の抗体を除去すること;及び
(e)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、ヒトpFLT3を欠失する対照試料と比較した、該試料に結合した第二の抗体の量の増加が、該試料におけるヒトpFLT3の存在を示す、前記方法。
【請求項2】
血液、血液溶解物、又は骨髄吸引物におけるFLT3リン酸化を検出する方法であって:
(a)前記試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体がヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるエピトープに免疫特異的に結合する;
(d)結合していない第二の抗体を除去すること;及び
(e)該試料に結合した該第二の抗体の存在を検出すること;を含み、
ここで、pFLT3を有さない対照試料と比較した、該試料に結合した第二の抗体の量の増加が、該試料におけるFLT3リン酸化を示す、前記方法。
【請求項3】
FLT3活性化突然変異を有する患者を診断する方法であって:
(a)患者由来の血液試料、血液溶解物試料、又は骨髄吸引物試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(d)結合していない第二の抗体を除去すること;及び
(e)該試料に結合した第二の抗体の存在を検出することを含む、前記方法。
【請求項4】
ヒトFLT3リン酸化を活性化させる試験化合物、又はさもなければ該リン酸化のアゴニストである試験化合物を同定する方法であって:
(a)該試験化合物の存在下及び不在下で、ヒトFLT3を含む血液試料、血液溶解物試料、又は骨髄吸引物試料を接触させること;
(b)該試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(c)結合していない試料を除去すること;
(d)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(e)結合していない第二の抗体を除去すること;及び
(f)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、該試験化合物の不在下の該試料に結合した第二の抗体の量と比較した、該試験化合物の存在下の該試料に結合した第二の抗体の量の増加が、該試験化合物がヒトFLT3リン酸化を活性化させることを示す、前記方法。
【請求項5】
ヒトFLT3リン酸化を阻害する試験化合物、又はさもなければ該リン酸化のアンタゴニストである試験化合物を同定する方法であって:
(a)該試験化合物の存在下及び不在下で、ヒトFLT3を含む試料を接触させること;
(b)該試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(c)結合していない試料を除去すること;
(d)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(e)結合していない第二の抗体を除去すること;及び
(f)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、試験化合物の不在下の試料に結合した第二の抗体の量と比較した、試験化合物の存在下の該試料に結合した第二の抗体の量の減少が、該試験化合物が、ヒトFLT3リン酸化を阻害することを示す、前記方法。
【請求項6】
前記試験化合物が、複数の試験化合物のうちの1つであって、ここで、該試験化合物のうちの少なくとも2つが互いに異なる、請求項4又は5記載の方法。
【請求項7】
前記複数の試験化合物が、1〜100,000の試験化合物、1〜35,000の試験化合物、1〜10,000の試験化合物、1〜1,000の試験化合物、1〜100の試験化合物、又は1〜10の試験化合物を含む、請求項6記載の方法。
【請求項8】
患者におけるヒトFLT3リン酸化を低下させる化合物の有効性を決定する方法であって:
(a)該化合物を該患者に投与すること;
(b)該患者由来の血液試料、血液溶解物試料、又は骨髄吸引物試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(c)結合していない試料を除去すること;
(d)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(e)結合していない第二の抗体を除去すること;及び
(f)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、該化合物の投与前の患者由来の対照試料と比較した、該試料に結合した第二の抗体の量の減少が、該患者におけるヒトFLT3リン酸化を低下させるための化合物の有効性を示す、前記方法。
【請求項9】
前記試料が患者に由来する、請求項1〜8のいずれか一項記載の方法。
【請求項10】
前記患者が、FLT3活性化突然変異を有する、請求項9記載の方法。
【請求項11】
前記第二の抗体が標識を含む、請求項1〜10のいずれか一項記載の方法。
【請求項12】
前記標識が、ビオチン、放射性核種、酵素、基質、蛍光マーカー、化学発光マーカー、又はルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルである、請求項11記載の方法。
【請求項13】
前記第一の抗体が、多重ウェルプレート又は多重ドメインプレートのうちの1つのウェルにおいて固定化されている、請求項1〜12のいずれか一項記載の方法。
【請求項14】
前記多重ウェルプレート又は多重ドメインプレートが、前記プレートの底部に電極を含む、請求項13記載の方法。
【請求項15】
前記第二の抗体がビオチン化されている、請求項13記載の方法。
【請求項16】
前記第二の抗体を標識済みストレプトアビジンと接触させ、並びに、結合していない第二の抗体を除去した後、かつ前記試料に結合した第二の抗体の存在を検出する前に、結合していない標識済みストレプトアビジンを除去することをさらに含む、請求項15記載の方法。
【請求項17】
前記標識済みストレプトアビジンが、ルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルを含む、請求項16記載の方法。
【請求項18】
前記試料に結合した第二の抗体の存在が、前記炭素電極の表面上のタグ付きストレプトアビジンのECLによって検出される、請求項17記載の方法。
【請求項19】
試料におけるヒトpFLT3の存在を検出する方法であって:
(a)該試料を、ヒトFLT3の細胞外ドメインに免疫特異的に結合する固定化された第一の抗体と接触させること、ここで、第一の抗体が、多重ウェルプレート又は多重ドメイン多重ウェルプレートの底部に電極を含む該プレートの上のウェルに固定化されており;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した該試料を、ビオチン化した第二の抗体と標識済みストレプトアビジンとの混合物と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合し、かつ該標識済みストレプトアビジンが、ルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルを含む;
(d)結合していない第二の抗体及び結合していない標識済みストレプトアビジンを除去すること;及び
(e)該試料に結合した第二の抗体の存在を、該電極の表面の標識済みストレプトアビジンのECLによって検出すること;を含み
ここで、ヒトpFLT3を欠失しているか又は検出不可能な量のヒトpFLT3を有するかのいずれかの対照試料と比較して、該試料に結合したより多量の第二の抗体が、該試料におけるヒトpFLT3の存在を示す、前記方法。
【請求項20】
前記固定化された第一の抗体が、前記ウェルに約0.1μg/mL〜約10μg/mLの範囲の濃度で添加される、請求項1〜19のいずれか一項記載の方法。
【請求項21】
約0.25ng〜約2.5μg、又は約2.5ng〜約250ngの第一の抗体が1ウェルあたりに添加される、請求項1〜19のいずれか一項記載の方法。
【請求項22】
前記第一の抗体が、ヒトFLT3 27-543の細胞外ドメインに免疫特異的に結合する、請求項1〜21のいずれか一項記載の方法。
【請求項23】
前記第一の抗体が、未変性型のヒトFLT3に免疫特異的に結合する、請求項1〜22のいずれか一項記載の方法。
【請求項24】
前記第一の抗体が、膜近傍ドメイン(アミノ酸572〜603配列番号1の配列)、キナーゼ挿入領域アミノ酸配列番号1の配列の711〜780、細胞外ドメインアミノ酸配列番号1の配列の564〜993、及びC末端(配列番号1の配列のアミノ酸974〜993)のうちの1つ以上に免疫特異的に結合しない、請求項1〜23のいずれか一項記載の方法。具体的な実施態様において、該第一の抗体は、ポリクローナル抗体ではない。
【請求項25】
前記第一の抗体が、ポリクローナル抗体ではない、請求項1〜24のいずれか一項記載の方法。
【請求項26】
前記第一の抗体が、マウスモノクローナル抗体である、請求項1〜25のいずれか一項記載の方法。
【請求項27】
前記第二の抗体が、pFLT3のリン酸化型チロシン残基589、591、597、599、726、842、及び955のうちの1つ以上に免疫特異的に結合する、請求項1〜26のいずれか一項記載の方法。
【請求項28】
前記第二の抗体が、前記リン酸化型チロシン残基589及び591のうちの1つ以上に単独で免疫特異的に結合しない、請求項1〜26のいずれか一項記載の方法。
【請求項29】
前記第二の抗体が、マウスモノクローナル抗体である、請求項1〜28のいずれか一項記載の方法。
【請求項30】
前記第二の抗体が、約0.1μg/mL〜約10μg/mLの範囲の濃度で前記試料と接触する、請求項1〜29のいずれか一項記載の方法。
【請求項31】
約0.25ng〜約2.5μg、又は約2.5ng〜約250ngの第二の抗体が、1ウェルあたりに添加される、請求項1〜30のいずれか一項記載の方法。
【請求項32】
1つ以上の容器にある、請求項1〜31のいずれか一項記載の方法を実施するキット。
【請求項33】
試料におけるヒトpFLT3の存在を検出するキットであって:
(a)多重ウェルプレート又は多重ドメインプレートの底部に電極を含む該プレート;
(b)ヒトFLT3の細胞外ドメインに免疫特異的に結合する第一の抗体であって、該プレートのウェルに任意に固定化される該第一の抗体;
(c)ヒトpFLT3に免疫特異的に結合し、かつ該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合し、かつ任意にビオチン化される第二の抗体;及び
(d)任意に、標識済みストレプトアビジンが、ルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルを含む、前記キット。
【請求項34】
必要な試薬並びに任意でポジティブコントロール及びネガティブコントロールをさらに含む、請求項32又は33に記載のキット。
【請求項1】
血液試料、血液溶解物試料、又は骨髄吸引物試料におけるヒトリン酸化型FMS関連チロシンキナーゼ3(pFLT3)の存在を検出する方法であって:
(a)該試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(d)結合していない第二の抗体を除去すること;及び
(e)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、ヒトpFLT3を欠失する対照試料と比較した、該試料に結合した第二の抗体の量の増加が、該試料におけるヒトpFLT3の存在を示す、前記方法。
【請求項2】
血液、血液溶解物、又は骨髄吸引物におけるFLT3リン酸化を検出する方法であって:
(a)前記試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体がヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるエピトープに免疫特異的に結合する;
(d)結合していない第二の抗体を除去すること;及び
(e)該試料に結合した該第二の抗体の存在を検出すること;を含み、
ここで、pFLT3を有さない対照試料と比較した、該試料に結合した第二の抗体の量の増加が、該試料におけるFLT3リン酸化を示す、前記方法。
【請求項3】
FLT3活性化突然変異を有する患者を診断する方法であって:
(a)患者由来の血液試料、血液溶解物試料、又は骨髄吸引物試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(d)結合していない第二の抗体を除去すること;及び
(e)該試料に結合した第二の抗体の存在を検出することを含む、前記方法。
【請求項4】
ヒトFLT3リン酸化を活性化させる試験化合物、又はさもなければ該リン酸化のアゴニストである試験化合物を同定する方法であって:
(a)該試験化合物の存在下及び不在下で、ヒトFLT3を含む血液試料、血液溶解物試料、又は骨髄吸引物試料を接触させること;
(b)該試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(c)結合していない試料を除去すること;
(d)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(e)結合していない第二の抗体を除去すること;及び
(f)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、該試験化合物の不在下の該試料に結合した第二の抗体の量と比較した、該試験化合物の存在下の該試料に結合した第二の抗体の量の増加が、該試験化合物がヒトFLT3リン酸化を活性化させることを示す、前記方法。
【請求項5】
ヒトFLT3リン酸化を阻害する試験化合物、又はさもなければ該リン酸化のアンタゴニストである試験化合物を同定する方法であって:
(a)該試験化合物の存在下及び不在下で、ヒトFLT3を含む試料を接触させること;
(b)該試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(c)結合していない試料を除去すること;
(d)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(e)結合していない第二の抗体を除去すること;及び
(f)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、試験化合物の不在下の試料に結合した第二の抗体の量と比較した、試験化合物の存在下の該試料に結合した第二の抗体の量の減少が、該試験化合物が、ヒトFLT3リン酸化を阻害することを示す、前記方法。
【請求項6】
前記試験化合物が、複数の試験化合物のうちの1つであって、ここで、該試験化合物のうちの少なくとも2つが互いに異なる、請求項4又は5記載の方法。
【請求項7】
前記複数の試験化合物が、1〜100,000の試験化合物、1〜35,000の試験化合物、1〜10,000の試験化合物、1〜1,000の試験化合物、1〜100の試験化合物、又は1〜10の試験化合物を含む、請求項6記載の方法。
【請求項8】
患者におけるヒトFLT3リン酸化を低下させる化合物の有効性を決定する方法であって:
(a)該化合物を該患者に投与すること;
(b)該患者由来の血液試料、血液溶解物試料、又は骨髄吸引物試料を、ヒト総FLT3に免疫特異的に結合する固定化された第一の抗体と接触させること;
(c)結合していない試料を除去すること;
(d)該固定化された第一の抗体に結合した該試料を、検出可能な第二の抗体と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合する;
(e)結合していない第二の抗体を除去すること;及び
(f)該試料に結合した第二の抗体の存在を検出すること;を含み、
ここで、該化合物の投与前の患者由来の対照試料と比較した、該試料に結合した第二の抗体の量の減少が、該患者におけるヒトFLT3リン酸化を低下させるための化合物の有効性を示す、前記方法。
【請求項9】
前記試料が患者に由来する、請求項1〜8のいずれか一項記載の方法。
【請求項10】
前記患者が、FLT3活性化突然変異を有する、請求項9記載の方法。
【請求項11】
前記第二の抗体が標識を含む、請求項1〜10のいずれか一項記載の方法。
【請求項12】
前記標識が、ビオチン、放射性核種、酵素、基質、蛍光マーカー、化学発光マーカー、又はルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルである、請求項11記載の方法。
【請求項13】
前記第一の抗体が、多重ウェルプレート又は多重ドメインプレートのうちの1つのウェルにおいて固定化されている、請求項1〜12のいずれか一項記載の方法。
【請求項14】
前記多重ウェルプレート又は多重ドメインプレートが、前記プレートの底部に電極を含む、請求項13記載の方法。
【請求項15】
前記第二の抗体がビオチン化されている、請求項13記載の方法。
【請求項16】
前記第二の抗体を標識済みストレプトアビジンと接触させ、並びに、結合していない第二の抗体を除去した後、かつ前記試料に結合した第二の抗体の存在を検出する前に、結合していない標識済みストレプトアビジンを除去することをさらに含む、請求項15記載の方法。
【請求項17】
前記標識済みストレプトアビジンが、ルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルを含む、請求項16記載の方法。
【請求項18】
前記試料に結合した第二の抗体の存在が、前記炭素電極の表面上のタグ付きストレプトアビジンのECLによって検出される、請求項17記載の方法。
【請求項19】
試料におけるヒトpFLT3の存在を検出する方法であって:
(a)該試料を、ヒトFLT3の細胞外ドメインに免疫特異的に結合する固定化された第一の抗体と接触させること、ここで、第一の抗体が、多重ウェルプレート又は多重ドメイン多重ウェルプレートの底部に電極を含む該プレートの上のウェルに固定化されており;
(b)結合していない試料を除去すること;
(c)該固定化された第一の抗体に結合した該試料を、ビオチン化した第二の抗体と標識済みストレプトアビジンとの混合物と接触させること、ここで、該第二の抗体が、ヒトpFLT3に免疫特異的に結合し、かつ該第二の抗体が、該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合し、かつ該標識済みストレプトアビジンが、ルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルを含む;
(d)結合していない第二の抗体及び結合していない標識済みストレプトアビジンを除去すること;及び
(e)該試料に結合した第二の抗体の存在を、該電極の表面の標識済みストレプトアビジンのECLによって検出すること;を含み
ここで、ヒトpFLT3を欠失しているか又は検出不可能な量のヒトpFLT3を有するかのいずれかの対照試料と比較して、該試料に結合したより多量の第二の抗体が、該試料におけるヒトpFLT3の存在を示す、前記方法。
【請求項20】
前記固定化された第一の抗体が、前記ウェルに約0.1μg/mL〜約10μg/mLの範囲の濃度で添加される、請求項1〜19のいずれか一項記載の方法。
【請求項21】
約0.25ng〜約2.5μg、又は約2.5ng〜約250ngの第一の抗体が1ウェルあたりに添加される、請求項1〜19のいずれか一項記載の方法。
【請求項22】
前記第一の抗体が、ヒトFLT3 27-543の細胞外ドメインに免疫特異的に結合する、請求項1〜21のいずれか一項記載の方法。
【請求項23】
前記第一の抗体が、未変性型のヒトFLT3に免疫特異的に結合する、請求項1〜22のいずれか一項記載の方法。
【請求項24】
前記第一の抗体が、膜近傍ドメイン(アミノ酸572〜603配列番号1の配列)、キナーゼ挿入領域アミノ酸配列番号1の配列の711〜780、細胞外ドメインアミノ酸配列番号1の配列の564〜993、及びC末端(配列番号1の配列のアミノ酸974〜993)のうちの1つ以上に免疫特異的に結合しない、請求項1〜23のいずれか一項記載の方法。具体的な実施態様において、該第一の抗体は、ポリクローナル抗体ではない。
【請求項25】
前記第一の抗体が、ポリクローナル抗体ではない、請求項1〜24のいずれか一項記載の方法。
【請求項26】
前記第一の抗体が、マウスモノクローナル抗体である、請求項1〜25のいずれか一項記載の方法。
【請求項27】
前記第二の抗体が、pFLT3のリン酸化型チロシン残基589、591、597、599、726、842、及び955のうちの1つ以上に免疫特異的に結合する、請求項1〜26のいずれか一項記載の方法。
【請求項28】
前記第二の抗体が、前記リン酸化型チロシン残基589及び591のうちの1つ以上に単独で免疫特異的に結合しない、請求項1〜26のいずれか一項記載の方法。
【請求項29】
前記第二の抗体が、マウスモノクローナル抗体である、請求項1〜28のいずれか一項記載の方法。
【請求項30】
前記第二の抗体が、約0.1μg/mL〜約10μg/mLの範囲の濃度で前記試料と接触する、請求項1〜29のいずれか一項記載の方法。
【請求項31】
約0.25ng〜約2.5μg、又は約2.5ng〜約250ngの第二の抗体が、1ウェルあたりに添加される、請求項1〜30のいずれか一項記載の方法。
【請求項32】
1つ以上の容器にある、請求項1〜31のいずれか一項記載の方法を実施するキット。
【請求項33】
試料におけるヒトpFLT3の存在を検出するキットであって:
(a)多重ウェルプレート又は多重ドメインプレートの底部に電極を含む該プレート;
(b)ヒトFLT3の細胞外ドメインに免疫特異的に結合する第一の抗体であって、該プレートのウェルに任意に固定化される該第一の抗体;
(c)ヒトpFLT3に免疫特異的に結合し、かつ該第一の抗体とは異なるFLT3エピトープに免疫特異的に結合し、かつ任意にビオチン化される第二の抗体;及び
(d)任意に、標識済みストレプトアビジンが、ルテニウム(II)トリ-ビピリジン-(4-メチルスルホナート)NHSエステルを含む、前記キット。
【請求項34】
必要な試薬並びに任意でポジティブコントロール及びネガティブコントロールをさらに含む、請求項32又は33に記載のキット。
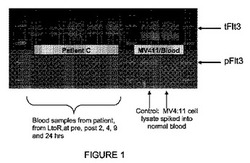
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【公表番号】特表2012−508367(P2012−508367A)
【公表日】平成24年4月5日(2012.4.5)
【国際特許分類】
【出願番号】特願2011−534927(P2011−534927)
【出願日】平成21年11月6日(2009.11.6)
【国際出願番号】PCT/US2009/063534
【国際公開番号】WO2010/054185
【国際公開日】平成22年5月14日(2010.5.14)
【出願人】(508278239)
【Fターム(参考)】
【公表日】平成24年4月5日(2012.4.5)
【国際特許分類】
【出願日】平成21年11月6日(2009.11.6)
【国際出願番号】PCT/US2009/063534
【国際公開番号】WO2010/054185
【国際公開日】平成22年5月14日(2010.5.14)
【出願人】(508278239)

【Fターム(参考)】
[ Back to top ]

