レチノール関連疾患を治療するための方法及び化合物
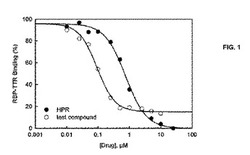
血清レチノールレベルを減少させる化合物は、視覚サイクルの経過中に蓄積する老廃物の過剰産生に関連する眼疾患を治療するのに用いられる。我々は、たとえば、黄斑変性及びジストロフィーを治療する、又はこのような眼疾患に関連する症状を軽減するための方法、化合物、及び組成物を記載する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
化学式(I)(化1)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物、及び
薬学的に許容可能な賦形剤を含む医薬組成物。
【化1】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H又は(化2)であり、
【化2】

Gは、−OR1、−(C1−C6)アルキル、−(C1−C6)アルキル−OR1、ハロゲン、−CO2R1、−(C1−C6)アルキル−CO2R1、NHR1、−(C1−C6)アルキル−NHR1、−(C=O)NHR1、−(C1−C6)アルキル−(C=O)NHR1、−NHR1(C=O)R1、又は−(C1−C6)アルキル−NHR1(C=O)R1であり、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンである。]
【請求項2】
化学式(II)(化3)の構造を有する化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を含むことを特徴とする請求項1記載の医薬組成物。
【化3】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H又は(化4)であり、
【化4】

Gは、−OR1、−(C1−C6)アルキル、−(C1−C6)アルキル−OR1、ハロゲン、−CO2R1、−(C1−C6)アルキル−CO2R1、NHR1、−(C1−C6)アルキル−NHR1、−(C=O)NHR1、−(C1−C6)アルキル−(C=O)NHR1、−NHR1(C=O)R1、又は−(C1−C6)アルキル−NHR1(C=O)R1であり、
R1は、H又は(C1−C6)アルキルである。]
【請求項3】
前記AがOであることを特徴とする請求項2記載の医薬組成物。
【請求項4】
前記Bは、−(CH2)nであり且つnが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項3記載の医薬組成物。
【請求項5】
前記Eは、(C=O)−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項4記載の医薬組成物。
【請求項6】
前記Rが(化5)であることを特徴とする請求項5記載の医薬組成物。
【化5】

【請求項7】
前記Eが(C=O)−ORであることを特徴とする請求項4記載の医薬組成物。
【請求項8】
前記RがHであることを特徴とする請求項7記載の医薬組成物。
【請求項9】
5−(2−tert−ブチル−4−クロロフェノキシ)−N−(4−ヒドロキシフェニル)ペンタンアミド、7−(2−tert−ブチル−4−クロロフェノキシ)−N−(4−ヒドロキシフェニル)ヘプタンアミド、4−(5−(2−tert−ブチル−4−クロロフェノキシ)ペンタンアミド)安息香酸、4−(3−((2−tert-ブチル−4−クロロフェノキシ)メチル)シクロペンタンアミド)安息香酸、5−(2−tert−ブチル−4−クロロフェノキシ)ペンタン酸、4−(2−tert−ブチル−4−クロロフェノキシ)ブタン酸、2−(3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロペンチル)酢酸、7−(2−tert−ブチル−4−クロロフェノキシ)ヘプタン酸、4−(5−(2−tert−ブチル−4−クロロフェノキシ)ペンタンアミド)ベンズアミド、3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロヘキサンカルボン酸、3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロペンタンカルボン酸、3−((2−tert−ブチル−4−クロロフェニルアミノ)メチル)シクロペンタンアミド、4−(3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロペンタンカルボキシアミド)安息香酸、及び5−(2−tert−ブチル−4−クロロフェニルチオ)ペンタン酸からなる群から選択されることを特徴とする請求項1記載の医薬組成物。
【請求項10】
レチノール−レチノール結合タンパク質−トランスサイレチン複合体の形成を抑制し、該抑制のIC50が約5μM未満であることを特徴とする請求項1記載の医薬組成物。
【請求項11】
前記抑制のIC50が約1μM未満であることを特徴とする請求項10記載の医薬組成物。
【請求項12】
シトクロムP450を約50%未満まで抑制することを特徴とする請求項1記載の医薬組成物。
【請求項13】
シトクロムP450を約10%未満まで抑制することを特徴とする請求項12記載の医薬組成物。
【請求項14】
前記化学式(I)の化合物が、硝子体網膜疾患の治療に使用されることを特徴とする請求項1記載の医薬組成物。
【請求項15】
前記硝子体網膜疾患が、乾性黄斑変性症、光受容体変性症、地図状萎縮症、黄斑ジストロフィー症、糖尿病性網膜症、湿性黄斑変性症、未熟児網膜症、及び網膜色素変性症からなる群から選択されることを特徴とする請求項1記載の医薬組成物。
【請求項16】
化学式(I)(化6)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物と、
薬学的に許容可能な賦形剤又は担体を含む医薬組成物。
【化6】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項17】
化学式(II)(化7)の構造を有する化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物と、
薬学的に許容可能な賦形剤又は担体を含むことを特徴とする請求項16記載の医薬組成物。
【化7】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、又は任意に置換されたヘテロアリールである。]
【請求項18】
前記組成物が、哺乳類における血清レチノール又は眼組織レチノールのレベル又は活性を下げるのに十分有効量含まれることを特徴とする請求項16記載の医薬組成物。
【請求項19】
治療的に有効量の化学式(I)(化8)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備える硝子体網膜疾患を治療する方法。
【化8】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項20】
治療的に有効量の化学式(II)(化9)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備えることを特徴とする請求項19記載の方法。
【化9】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項21】
前記化合物が、哺乳類におけるレチノール結合タンパク質のレベル又は活性を調節し、
前記レチノール結合タンパク質がRBP4であることを特徴とする請求項19又は20記載の方法。
【請求項22】
前記硝子体網膜疾患が、乾性黄斑変性症、光受容体変性症、地図状萎縮症、黄斑ジストロフィー症、糖尿病性網膜症、湿性黄斑変性症、未熟児網膜症、又は網膜色素変性症から選択されることを特徴とする請求項19記載の方法。
【請求項23】
哺乳類における血清レチノール結合タンパク質又はトランスサイレチンのレベル又は活性を下げる方法であって、
治療的に有効量の化学式(I)(化10)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備え、
前記化学式(I)(化10)の化合物が、哺乳類における血清レチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする方法。
【化10】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項24】
治療的に有効量の化学式(II)(化11)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)(化11)の化合物が、哺乳類における血清レチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする請求項23記載の方法。
【化11】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項25】
前記血清レチノール結合タンパク質がRBP4であることを特徴とする請求項23記載の方法。
【請求項26】
前記化学式(I)の化合物が、哺乳類におけるレチノール結合タンパク質又はトランスサイレチンの転写を抑制することを特徴とする請求項23記載の方法。
【請求項27】
前記化学式(I)の化合物が、哺乳類におけるレチノール結合タンパク質又はトランスサイレチンの翻訳を抑制することを特徴とする請求項23記載の方法。
【請求項28】
前記化学式(I)の化合物が、レチノール結合タンパク質へのレチノールの結合を抑制することを特徴とする請求項23記載の方法。
【請求項29】
前記化学式(I)の化合物が、トランスサイレチンへのレチノール結合タンパク質の結合を抑制することを特徴とする請求項23記載の方法。
【請求項30】
前記化学式(I)の化合物が、前記哺乳類におけるレチノール結合タンパク質又はトランスサイレチンのクリアランスを増大させることを特徴とする請求項23記載の方法。
【請求項31】
哺乳類におけるレチノール関連疾患を治療する方法であって、
治療的に有効量の化学式(I)(化12)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備えることを特徴とする方法。
【化12】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項32】
治療的に有効量の化学式(II)(化13)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備える請求項31記載の方法。
【化13】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項33】
前記レチノール関連疾患が、骨増殖症、特発性頭蓋内圧亢進症、アミロイドーシス、アルツハイマー病、及びアルストレム・ハルグレン症候群であることを特徴とする請求項31記載の方法。
【請求項34】
乾性加齢関連黄斑変性症を有する哺乳類において、血清レチノールレベルを下げるための方法であって、
該哺乳類に化学式(I)(化14)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(I)(化14)の化合物が、視覚サイクルにおいて酵素又はタンパク質の活性を直接的に調節しないことを特徴とする方法。
【化14】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項35】
治療的に有効量の化学式(II)(化15)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)(化15)の化合物が、視覚サイクルにおいて酵素又はタンパク質の活性を直接的に調節しないことを特徴とする請求項34記載の方法。
【化15】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項36】
前記化学式(I)の化合物が、視覚サイクルにおいて酵素又はタンパク質を直接的に抑制しない又は酵素又はタンパク質に直接的に結合しないことを特徴とする請求項34記載の方法。
【請求項37】
前記化学式(I)の化合物が、ロドプシン再生率に影響しないことを特徴とする請求項34記載の方法。
【請求項38】
前記化学式(I)の化合物が、暗順応の遅延を本質的に悪化させないことを特徴とする請求項34記載の方法。
【請求項39】
前記化学式(I)の化合物が、地図状萎縮、暗点、暗点もしくは病斑周囲の自己蛍光の輪、又は光受容体変性の広がりを制限することを特徴とする請求項34記載の方法。
【請求項40】
過剰レチノール血液状態(hyperretinolemia)を治療する方法であって、化学式(I)(化16)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備える方法。
【化16】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項41】
治療的に有効量の化学式(II)(化17)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグもしくは溶媒和物を投与する工程を備えることを特徴とする請求項40記載の方法。
【化17】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項42】
前記過剰レチノール血液状態が、硝子体網膜疾患に関連することを特徴とする請求項40記載の方法。
【請求項43】
前記過剰レチノール血液状態が、糖尿病又はアルツハイマー病に関連することを特徴とする請求項40記載の方法。
【請求項44】
哺乳類におけるレチノール関連疾患を治療する方法であって、
該哺乳類に、有効量の化学式(I)(化18)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(I)の化合物が、レチノール−レチノール結合タンパク質−トランスサイレチン複合体の形成を抑制し、
IC50抑制が、約5μM未満であることを特徴とする方法。
【化18】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項45】
治療的に有効量の化学式(II)(化19)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)の化合物が、レチノール−レチノール結合タンパク質−トランスサイレチン複合体の形成を抑制し、
IC50抑制が、約5μM未満であることを特徴とする請求項44記載の方法。
【化19】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項46】
前記IC50抑制が、約1μM未満であることを特徴とする請求項44記載の方法。
【請求項47】
化学式(I)の化合物が、さらにシトクロムP450を約50%未満に抑制することを特徴とする請求項44記載の方法。
【請求項48】
化学式(I)の化合物が、さらにシトクロムP450を約10%未満に抑制することを特徴とする請求項47記載の方法。
【請求項49】
哺乳類における1型又は2型糖尿病を治療する方法であって、
該哺乳類に、治療的に有効量の化学式(I)(化20)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(I)の化合物が、哺乳類におけるレチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする方法。
【化20】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項50】
前記哺乳類に、有効量の化学式(II)(化21)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)の化合物が、前記哺乳類におけるレチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする請求項49記載の方法。
【化21】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項51】
哺乳類における血清レチノール又は眼組織レチノールのレベルを下げる方法であって、
該哺乳類に、治療的に有効量の化学式(I)(化22)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備えることを特徴とする方法。
【化22】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項52】
前記哺乳類に、有効量の化学式(II)(化23)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備えることを特徴とする請求項51記載の方法。
【化23】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項53】
前記哺乳類がヒトであることを特徴とする請求項51記載の方法。
【請求項54】
前記血清レチノール又は眼組織レチノールのレベルが、少なくとも20%減少することを特徴とする請求項51記載の方法。
【請求項55】
少なくとも1つの追加的な薬剤を投与する工程をさらに含み、該追加的な薬剤が、一酸化窒素産生の誘導物質、抗炎症剤、生理的に許容可能な酸化防止剤、生理的に許容可能なミネラル、負に帯電したリン脂質、カロチノイド、スタチン、抗血管形成剤、マトリックスメタロプロテアーゼ阻害剤、レスベラトロルとその他のトランス−スチルベン化合物、及び13−シス−レチノイン酸からなる群から選択されることを特徴とする請求項51記載の方法。
【請求項56】
化学式(I)(化24)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を含む組成物。
【化24】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであるが、ただし、−(C2−C7)へテロアルキルは、窒素原子、−C(=O)−、−S−、−S(=O)−、−S(=O)2−、−NR1(C=O)−、−(C=O)NR1−、S(=O)2NR1−、−NR1S(=O)2、−O(C=O)NR1−、−NR1(C=O)O−、−O(C=O)O−、−NR1(C=O)NR1−、−(C=O)O−、又は−O(C=O)−を含まず、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、−(C1−C7)アルキル−(C=O)−NR1R、C1−C4アルキル、C2−C4アルキニル、C3−C6シクロアルキル、C1−C4アルキル−(C3−C6シクロアルキル)、アリール、置換アリール、アリールアルキル、−C(O)R2、ヒドロキシ−(C1−C6アルキル)、アールオキシ、ハロ、C1−C6−ハロアルキル、シアノ、ヒドロキシ、ニトロ、−O−C(O)NR2R3、−NR2R3(C=O)OR1、又は−SO2NR2R3であり、
R2及びR3は、H、C1−C6アルキル、及びC3−C6シクロアルキルから夫々独立して選択され、
Rは、H、任意に置換されたアリール、又は任意に置換されたヘテロアリールであるが、ただし、Bが−S−である時Rがピリミジンではなく、Bが−(C2−C7)アルキルである時Rがイミダゾールではなく、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンであり、
ただし、化学式(I)の化合物が二量体ではない。]
【請求項57】
前記Eが、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項56記載の組成物。
【請求項58】
前記XがClであり、
前記Dがイソプロピル、tert−ブチル、又はシクロプロピルであることを特徴とする請求項56記載の組成物。
【請求項59】
前記AがOであることを特徴とする請求項56記載の組成物。
【請求項60】
前記Bは、−(CH2)nであり且つ該nが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項56記載の組成物。
【請求項61】
請求項56に記載の化合物、及び薬学的に許容可能な担体もしくは賦形剤を含む医薬組成物。
【請求項62】
硝子体網膜疾患を治療するための方法であって、治療的に有効量の請求項56に記載の組成物を哺乳類に投与する工程を備えることを特徴とする方法。
【請求項63】
化学式(I)(化25)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物。
【化25】

[式中、Aは、Oであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであるが、ただし、−(C2−C7)へテロアルキルは、窒素原子、−C(=O)−、−S−、−S(=O)−、−S(=O)2−、−NR1(C=O)−、−(C=O)NR1−、S(=O)2NR1−、−NR1S(=O)2、−O(C=O)NR1−、−NR1(C=O)O−、−O(C=O)O−、−NR1(C=O)NR1−、−(C=O)O−、又は−O(C=O)−を含まず、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、−(C1−C7)アルキル−(C=O)−NR1R、C1−C4アルキル、C2−C4アルキニル、C3−C6シクロアルキル、C1−C4アルキル−(C3−C6シクロアルキル)、アリール、置換アリール、アリールアルキル、−C(O)R2、ヒドロキシ−(C1−C6アルキル)、アールオキシ、ハロ、C1−C6−ハロアルキル、シアノ、ヒドロキシ、ニトロ、−O−C(O)NR2R3、−NR2(C=O)OR1、又は−SO2NR2R3であり、
R2及びR3は、H、C1−C6アルキル、及びC3−C6シクロアルキルから夫々独立して選択され、
Rは、H、−(C2−C7アルキル)、任意に置換されたアリール、又は任意に置換されたヘテロアリールであるが、ただし、Bが−S−である時Rがピリミジンではなく、Bが−(C2−C7)アルキルである時Rがイミダゾールではなく、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンである。]
【請求項64】
前記Bは、−(CH2)n且つ該nが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項63記載の化合物。
【請求項65】
前記Eが、(C=O)−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項64記載の化合物。
【請求項66】
前記Eが、(C=O)−ORであることを特徴とする請求項65記載の化合物。
【請求項67】
前記Dがイソプロピル、tert−ブチル、又はシクロプロピルであることを特徴とする請求項66記載の化合物。
【請求項68】
前記XがClであり、前記Dがtert−ブチルであることを特徴とする請求項67記載の化合物。
【請求項69】
化学式(I)(化26)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物。
【化26】

[式中、Aは、NH又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、−(C1−C7)アルキル−(C=O)−NR1R、C1−C4アルキル、C2−C4アルキニル、C3−C6シクロアルキル、C1−C4アルキル−(C3−C6シクロアルキル)、アリール、置換アリール、アリールアルキル、−C(O)R2、ヒドロキシ−(C1−C6アルキル)、アールオキシ、ハロ、C1−C6−ハロアルキル、シアノ、ヒドロキシ、ニトロ、−O−C(O)NR2R3、−NR2(C=O)OR1、又は−SO2NR2R3であり、
R2及びR3は、H、C1−C6アルキル、及びC3−C6シクロアルキルから夫々独立して選択され、
Rは、H、−(C2−C7アルキル)、任意に置換されたアリール、又は任意に置換されたヘテロアリールであり、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンである。]
【請求項70】
前記Bは、−(CH2)nであり且つ該nが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項69記載の化合物。
【請求項71】
前記Eが、(C=O)−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項70記載の化合物。
【請求項72】
前記Eが、(C=O)−ORであることを特徴とする請求項71記載の化合物。
【請求項73】
前記Dが、イソプロピル、tert−ブチル、又はシクロプロピルであることを特徴とする請求項72記載の化合物。
【請求項74】
前記XがClであり、前記Dがtert−ブチルであることを特徴とする請求項73記載の化合物。
【請求項1】
化学式(I)(化1)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物、及び
薬学的に許容可能な賦形剤を含む医薬組成物。
【化1】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H又は(化2)であり、
【化2】

Gは、−OR1、−(C1−C6)アルキル、−(C1−C6)アルキル−OR1、ハロゲン、−CO2R1、−(C1−C6)アルキル−CO2R1、NHR1、−(C1−C6)アルキル−NHR1、−(C=O)NHR1、−(C1−C6)アルキル−(C=O)NHR1、−NHR1(C=O)R1、又は−(C1−C6)アルキル−NHR1(C=O)R1であり、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンである。]
【請求項2】
化学式(II)(化3)の構造を有する化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を含むことを特徴とする請求項1記載の医薬組成物。
【化3】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H又は(化4)であり、
【化4】

Gは、−OR1、−(C1−C6)アルキル、−(C1−C6)アルキル−OR1、ハロゲン、−CO2R1、−(C1−C6)アルキル−CO2R1、NHR1、−(C1−C6)アルキル−NHR1、−(C=O)NHR1、−(C1−C6)アルキル−(C=O)NHR1、−NHR1(C=O)R1、又は−(C1−C6)アルキル−NHR1(C=O)R1であり、
R1は、H又は(C1−C6)アルキルである。]
【請求項3】
前記AがOであることを特徴とする請求項2記載の医薬組成物。
【請求項4】
前記Bは、−(CH2)nであり且つnが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項3記載の医薬組成物。
【請求項5】
前記Eは、(C=O)−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項4記載の医薬組成物。
【請求項6】
前記Rが(化5)であることを特徴とする請求項5記載の医薬組成物。
【化5】

【請求項7】
前記Eが(C=O)−ORであることを特徴とする請求項4記載の医薬組成物。
【請求項8】
前記RがHであることを特徴とする請求項7記載の医薬組成物。
【請求項9】
5−(2−tert−ブチル−4−クロロフェノキシ)−N−(4−ヒドロキシフェニル)ペンタンアミド、7−(2−tert−ブチル−4−クロロフェノキシ)−N−(4−ヒドロキシフェニル)ヘプタンアミド、4−(5−(2−tert−ブチル−4−クロロフェノキシ)ペンタンアミド)安息香酸、4−(3−((2−tert-ブチル−4−クロロフェノキシ)メチル)シクロペンタンアミド)安息香酸、5−(2−tert−ブチル−4−クロロフェノキシ)ペンタン酸、4−(2−tert−ブチル−4−クロロフェノキシ)ブタン酸、2−(3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロペンチル)酢酸、7−(2−tert−ブチル−4−クロロフェノキシ)ヘプタン酸、4−(5−(2−tert−ブチル−4−クロロフェノキシ)ペンタンアミド)ベンズアミド、3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロヘキサンカルボン酸、3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロペンタンカルボン酸、3−((2−tert−ブチル−4−クロロフェニルアミノ)メチル)シクロペンタンアミド、4−(3−((2−tert−ブチル−4−クロロフェノキシ)メチル)シクロペンタンカルボキシアミド)安息香酸、及び5−(2−tert−ブチル−4−クロロフェニルチオ)ペンタン酸からなる群から選択されることを特徴とする請求項1記載の医薬組成物。
【請求項10】
レチノール−レチノール結合タンパク質−トランスサイレチン複合体の形成を抑制し、該抑制のIC50が約5μM未満であることを特徴とする請求項1記載の医薬組成物。
【請求項11】
前記抑制のIC50が約1μM未満であることを特徴とする請求項10記載の医薬組成物。
【請求項12】
シトクロムP450を約50%未満まで抑制することを特徴とする請求項1記載の医薬組成物。
【請求項13】
シトクロムP450を約10%未満まで抑制することを特徴とする請求項12記載の医薬組成物。
【請求項14】
前記化学式(I)の化合物が、硝子体網膜疾患の治療に使用されることを特徴とする請求項1記載の医薬組成物。
【請求項15】
前記硝子体網膜疾患が、乾性黄斑変性症、光受容体変性症、地図状萎縮症、黄斑ジストロフィー症、糖尿病性網膜症、湿性黄斑変性症、未熟児網膜症、及び網膜色素変性症からなる群から選択されることを特徴とする請求項1記載の医薬組成物。
【請求項16】
化学式(I)(化6)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物と、
薬学的に許容可能な賦形剤又は担体を含む医薬組成物。
【化6】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項17】
化学式(II)(化7)の構造を有する化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物と、
薬学的に許容可能な賦形剤又は担体を含むことを特徴とする請求項16記載の医薬組成物。
【化7】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、又は任意に置換されたヘテロアリールである。]
【請求項18】
前記組成物が、哺乳類における血清レチノール又は眼組織レチノールのレベル又は活性を下げるのに十分有効量含まれることを特徴とする請求項16記載の医薬組成物。
【請求項19】
治療的に有効量の化学式(I)(化8)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備える硝子体網膜疾患を治療する方法。
【化8】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項20】
治療的に有効量の化学式(II)(化9)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備えることを特徴とする請求項19記載の方法。
【化9】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項21】
前記化合物が、哺乳類におけるレチノール結合タンパク質のレベル又は活性を調節し、
前記レチノール結合タンパク質がRBP4であることを特徴とする請求項19又は20記載の方法。
【請求項22】
前記硝子体網膜疾患が、乾性黄斑変性症、光受容体変性症、地図状萎縮症、黄斑ジストロフィー症、糖尿病性網膜症、湿性黄斑変性症、未熟児網膜症、又は網膜色素変性症から選択されることを特徴とする請求項19記載の方法。
【請求項23】
哺乳類における血清レチノール結合タンパク質又はトランスサイレチンのレベル又は活性を下げる方法であって、
治療的に有効量の化学式(I)(化10)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備え、
前記化学式(I)(化10)の化合物が、哺乳類における血清レチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする方法。
【化10】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項24】
治療的に有効量の化学式(II)(化11)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)(化11)の化合物が、哺乳類における血清レチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする請求項23記載の方法。
【化11】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項25】
前記血清レチノール結合タンパク質がRBP4であることを特徴とする請求項23記載の方法。
【請求項26】
前記化学式(I)の化合物が、哺乳類におけるレチノール結合タンパク質又はトランスサイレチンの転写を抑制することを特徴とする請求項23記載の方法。
【請求項27】
前記化学式(I)の化合物が、哺乳類におけるレチノール結合タンパク質又はトランスサイレチンの翻訳を抑制することを特徴とする請求項23記載の方法。
【請求項28】
前記化学式(I)の化合物が、レチノール結合タンパク質へのレチノールの結合を抑制することを特徴とする請求項23記載の方法。
【請求項29】
前記化学式(I)の化合物が、トランスサイレチンへのレチノール結合タンパク質の結合を抑制することを特徴とする請求項23記載の方法。
【請求項30】
前記化学式(I)の化合物が、前記哺乳類におけるレチノール結合タンパク質又はトランスサイレチンのクリアランスを増大させることを特徴とする請求項23記載の方法。
【請求項31】
哺乳類におけるレチノール関連疾患を治療する方法であって、
治療的に有効量の化学式(I)(化12)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を、哺乳類に投与する工程を備えることを特徴とする方法。
【化12】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項32】
治療的に有効量の化学式(II)(化13)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備える請求項31記載の方法。
【化13】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項33】
前記レチノール関連疾患が、骨増殖症、特発性頭蓋内圧亢進症、アミロイドーシス、アルツハイマー病、及びアルストレム・ハルグレン症候群であることを特徴とする請求項31記載の方法。
【請求項34】
乾性加齢関連黄斑変性症を有する哺乳類において、血清レチノールレベルを下げるための方法であって、
該哺乳類に化学式(I)(化14)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(I)(化14)の化合物が、視覚サイクルにおいて酵素又はタンパク質の活性を直接的に調節しないことを特徴とする方法。
【化14】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項35】
治療的に有効量の化学式(II)(化15)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)(化15)の化合物が、視覚サイクルにおいて酵素又はタンパク質の活性を直接的に調節しないことを特徴とする請求項34記載の方法。
【化15】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項36】
前記化学式(I)の化合物が、視覚サイクルにおいて酵素又はタンパク質を直接的に抑制しない又は酵素又はタンパク質に直接的に結合しないことを特徴とする請求項34記載の方法。
【請求項37】
前記化学式(I)の化合物が、ロドプシン再生率に影響しないことを特徴とする請求項34記載の方法。
【請求項38】
前記化学式(I)の化合物が、暗順応の遅延を本質的に悪化させないことを特徴とする請求項34記載の方法。
【請求項39】
前記化学式(I)の化合物が、地図状萎縮、暗点、暗点もしくは病斑周囲の自己蛍光の輪、又は光受容体変性の広がりを制限することを特徴とする請求項34記載の方法。
【請求項40】
過剰レチノール血液状態(hyperretinolemia)を治療する方法であって、化学式(I)(化16)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備える方法。
【化16】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項41】
治療的に有効量の化学式(II)(化17)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグもしくは溶媒和物を投与する工程を備えることを特徴とする請求項40記載の方法。
【化17】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項42】
前記過剰レチノール血液状態が、硝子体網膜疾患に関連することを特徴とする請求項40記載の方法。
【請求項43】
前記過剰レチノール血液状態が、糖尿病又はアルツハイマー病に関連することを特徴とする請求項40記載の方法。
【請求項44】
哺乳類におけるレチノール関連疾患を治療する方法であって、
該哺乳類に、有効量の化学式(I)(化18)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(I)の化合物が、レチノール−レチノール結合タンパク質−トランスサイレチン複合体の形成を抑制し、
IC50抑制が、約5μM未満であることを特徴とする方法。
【化18】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項45】
治療的に有効量の化学式(II)(化19)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)の化合物が、レチノール−レチノール結合タンパク質−トランスサイレチン複合体の形成を抑制し、
IC50抑制が、約5μM未満であることを特徴とする請求項44記載の方法。
【化19】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項46】
前記IC50抑制が、約1μM未満であることを特徴とする請求項44記載の方法。
【請求項47】
化学式(I)の化合物が、さらにシトクロムP450を約50%未満に抑制することを特徴とする請求項44記載の方法。
【請求項48】
化学式(I)の化合物が、さらにシトクロムP450を約10%未満に抑制することを特徴とする請求項47記載の方法。
【請求項49】
哺乳類における1型又は2型糖尿病を治療する方法であって、
該哺乳類に、治療的に有効量の化学式(I)(化20)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(I)の化合物が、哺乳類におけるレチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする方法。
【化20】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項50】
前記哺乳類に、有効量の化学式(II)(化21)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備え、
前記化学式(II)の化合物が、前記哺乳類におけるレチノール結合タンパク質又はトランスサイレチンのレベル又は活性を調節することを特徴とする請求項49記載の方法。
【化21】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項51】
哺乳類における血清レチノール又は眼組織レチノールのレベルを下げる方法であって、
該哺乳類に、治療的に有効量の化学式(I)(化22)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備えることを特徴とする方法。
【化22】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールであり、
Xは、ハロゲンである。]
【請求項52】
前記哺乳類に、有効量の化学式(II)(化23)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を投与する工程を備えることを特徴とする請求項51記載の方法。
【化23】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであり、
Rは、H、任意に置換されたアリール、任意に置換されたヘテロシクロアルキル、又は任意に置換されたヘテロアリールである。]
【請求項53】
前記哺乳類がヒトであることを特徴とする請求項51記載の方法。
【請求項54】
前記血清レチノール又は眼組織レチノールのレベルが、少なくとも20%減少することを特徴とする請求項51記載の方法。
【請求項55】
少なくとも1つの追加的な薬剤を投与する工程をさらに含み、該追加的な薬剤が、一酸化窒素産生の誘導物質、抗炎症剤、生理的に許容可能な酸化防止剤、生理的に許容可能なミネラル、負に帯電したリン脂質、カロチノイド、スタチン、抗血管形成剤、マトリックスメタロプロテアーゼ阻害剤、レスベラトロルとその他のトランス−スチルベン化合物、及び13−シス−レチノイン酸からなる群から選択されることを特徴とする請求項51記載の方法。
【請求項56】
化学式(I)(化24)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物を含む組成物。
【化24】

[式中、Aは、O、NH、又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであるが、ただし、−(C2−C7)へテロアルキルは、窒素原子、−C(=O)−、−S−、−S(=O)−、−S(=O)2−、−NR1(C=O)−、−(C=O)NR1−、S(=O)2NR1−、−NR1S(=O)2、−O(C=O)NR1−、−NR1(C=O)O−、−O(C=O)O−、−NR1(C=O)NR1−、−(C=O)O−、又は−O(C=O)−を含まず、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、−(C1−C7)アルキル−(C=O)−NR1R、C1−C4アルキル、C2−C4アルキニル、C3−C6シクロアルキル、C1−C4アルキル−(C3−C6シクロアルキル)、アリール、置換アリール、アリールアルキル、−C(O)R2、ヒドロキシ−(C1−C6アルキル)、アールオキシ、ハロ、C1−C6−ハロアルキル、シアノ、ヒドロキシ、ニトロ、−O−C(O)NR2R3、−NR2R3(C=O)OR1、又は−SO2NR2R3であり、
R2及びR3は、H、C1−C6アルキル、及びC3−C6シクロアルキルから夫々独立して選択され、
Rは、H、任意に置換されたアリール、又は任意に置換されたヘテロアリールであるが、ただし、Bが−S−である時Rがピリミジンではなく、Bが−(C2−C7)アルキルである時Rがイミダゾールではなく、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンであり、
ただし、化学式(I)の化合物が二量体ではない。]
【請求項57】
前記Eが、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項56記載の組成物。
【請求項58】
前記XがClであり、
前記Dがイソプロピル、tert−ブチル、又はシクロプロピルであることを特徴とする請求項56記載の組成物。
【請求項59】
前記AがOであることを特徴とする請求項56記載の組成物。
【請求項60】
前記Bは、−(CH2)nであり且つ該nが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項56記載の組成物。
【請求項61】
請求項56に記載の化合物、及び薬学的に許容可能な担体もしくは賦形剤を含む医薬組成物。
【請求項62】
硝子体網膜疾患を治療するための方法であって、治療的に有効量の請求項56に記載の組成物を哺乳類に投与する工程を備えることを特徴とする方法。
【請求項63】
化学式(I)(化25)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物。
【化25】

[式中、Aは、Oであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであるが、ただし、−(C2−C7)へテロアルキルは、窒素原子、−C(=O)−、−S−、−S(=O)−、−S(=O)2−、−NR1(C=O)−、−(C=O)NR1−、S(=O)2NR1−、−NR1S(=O)2、−O(C=O)NR1−、−NR1(C=O)O−、−O(C=O)O−、−NR1(C=O)NR1−、−(C=O)O−、又は−O(C=O)−を含まず、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、−(C1−C7)アルキル−(C=O)−NR1R、C1−C4アルキル、C2−C4アルキニル、C3−C6シクロアルキル、C1−C4アルキル−(C3−C6シクロアルキル)、アリール、置換アリール、アリールアルキル、−C(O)R2、ヒドロキシ−(C1−C6アルキル)、アールオキシ、ハロ、C1−C6−ハロアルキル、シアノ、ヒドロキシ、ニトロ、−O−C(O)NR2R3、−NR2(C=O)OR1、又は−SO2NR2R3であり、
R2及びR3は、H、C1−C6アルキル、及びC3−C6シクロアルキルから夫々独立して選択され、
Rは、H、−(C2−C7アルキル)、任意に置換されたアリール、又は任意に置換されたヘテロアリールであるが、ただし、Bが−S−である時Rがピリミジンではなく、Bが−(C2−C7)アルキルである時Rがイミダゾールではなく、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンである。]
【請求項64】
前記Bは、−(CH2)n且つ該nが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項63記載の化合物。
【請求項65】
前記Eが、(C=O)−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項64記載の化合物。
【請求項66】
前記Eが、(C=O)−ORであることを特徴とする請求項65記載の化合物。
【請求項67】
前記Dがイソプロピル、tert−ブチル、又はシクロプロピルであることを特徴とする請求項66記載の化合物。
【請求項68】
前記XがClであり、前記Dがtert−ブチルであることを特徴とする請求項67記載の化合物。
【請求項69】
化学式(I)(化26)の化合物、その活性代謝産物、又はその薬学的に許容可能なプロドラッグ、塩もしくは溶媒和物。
【化26】

[式中、Aは、NH又はSであり、
Bは、単結合、−(C2−C7)アルキル、−(C2−C7)アルケニル、−(C3−C8)シクロアルキル、−(C2−C7)へテロアルキル、−(C3−C8)へテロシクロアルキル、−(C3−C8)シクロアルケニル、又は−(C3−C8)へテロシクロアルケニルであり、
Dは、イソプロピル、イソブチル、sec-ブチル、tert-ブチル、シクロプロピル、シクロブチル、シクロペンチル、メチレンシクロプロピル、メチレンシクロブチル、又はメチレンシクロペンチルであり、
Eは、(C=O)−OR、−O−(C=O)−R、−(C=O)−R、−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、NR1−(C=O)−R、−(C1−C7)アルキル−(C=O)−OR、−(C1−C7)アルキル−(C=O)−NR1R、C1−C4アルキル、C2−C4アルキニル、C3−C6シクロアルキル、C1−C4アルキル−(C3−C6シクロアルキル)、アリール、置換アリール、アリールアルキル、−C(O)R2、ヒドロキシ−(C1−C6アルキル)、アールオキシ、ハロ、C1−C6−ハロアルキル、シアノ、ヒドロキシ、ニトロ、−O−C(O)NR2R3、−NR2(C=O)OR1、又は−SO2NR2R3であり、
R2及びR3は、H、C1−C6アルキル、及びC3−C6シクロアルキルから夫々独立して選択され、
Rは、H、−(C2−C7アルキル)、任意に置換されたアリール、又は任意に置換されたヘテロアリールであり、
R1は、H又は(C1−C6)アルキルであり、
Xは、ハロゲンである。]
【請求項70】
前記Bは、−(CH2)nであり且つ該nが1−6である、又は−(C3−C8)シクロアルキルであることを特徴とする請求項69記載の化合物。
【請求項71】
前記Eが、(C=O)−OR、カルボン酸バイオイソスター、−(C=O)−NR1R、−(C1−C7)アルキル−(C=O)−OR、又は−(C1−C7)アルキル−(C=O)−NR1Rであることを特徴とする請求項70記載の化合物。
【請求項72】
前記Eが、(C=O)−ORであることを特徴とする請求項71記載の化合物。
【請求項73】
前記Dが、イソプロピル、tert−ブチル、又はシクロプロピルであることを特徴とする請求項72記載の化合物。
【請求項74】
前記XがClであり、前記Dがtert−ブチルであることを特徴とする請求項73記載の化合物。
【図1】


【図2】


【図3】


【図5】


【図7】


【図9】


【図10】


【図11】


【図4】


【図6】


【図8】




【図2】


【図3】


【図5】


【図7】


【図9】


【図10】


【図11】


【図4】


【図6】


【図8】


【公表番号】特表2010−540541(P2010−540541A)
【公表日】平成22年12月24日(2010.12.24)
【国際特許分類】
【出願番号】特願2010−527024(P2010−527024)
【出願日】平成20年9月16日(2008.9.16)
【国際出願番号】PCT/US2008/076499
【国際公開番号】WO2009/042444
【国際公開日】平成21年4月2日(2009.4.2)
【出願人】(510203762)リヴィジョン セラピューティクス,インク. (2)
【Fターム(参考)】
【公表日】平成22年12月24日(2010.12.24)
【国際特許分類】
【出願日】平成20年9月16日(2008.9.16)
【国際出願番号】PCT/US2008/076499
【国際公開番号】WO2009/042444
【国際公開日】平成21年4月2日(2009.4.2)
【出願人】(510203762)リヴィジョン セラピューティクス,インク. (2)
【Fターム(参考)】
[ Back to top ]

