レーザ誘起蒸気/プラズマ媒体の医療処置および装置
安全で有効な医療的応用のために改良した方法および装置が提供される。好ましい実施形態では、(信頼できる小型の固体状態の装置から発生する有効な電力などの)レーザダイオード固有の利益の使用に基づいて、プラズマおよび高エネルギーの蒸気は、医療的応用のために電力レベルおよび電力密度を十分に備えて生成されて、医学的適応に対処し、広域にわたる損傷の生成を回避する。様々な構造の送達手段を使用して、プラズマおよび高エネルギー蒸気を先端で引き起こすことができる、高電力密度を達成する。火花の少ないプラズマおよび高エネルギーの蒸気泡が形成されると、初めの波長に加えて他の波長も吸収されることがしばしば見受けられる。結果として、ダイオードまたはダイオード励起レーザによって発生されたより有効な他の波長は、治療効果を向上させるためにビームに追加され得る。たとえば、1470nmの波長を使用して、火花のないプラズマ泡を生成することができ、併せて980nmの波長を使用して、組織を気化し卓越した止血効果を引き起こすことができる。プラズマまたは高エネルギー蒸気が定位置に置かれると、この域からの放射線は組織効果を決定する。別の実施形態では、高尖頭出力のパルス放射線が使用される。1470nm、1940nm、または1550nmの波長が好ましい。さらに、高尖頭出力のパルス放射線は、水中で980nmなどの媒体吸収を備える別の波長との組合せに適用できる。別の実施形態では、同心二重コアファイバを使用して、点火放射線はほぼ単一モード、すなわち内核に誘導され、パルスを維持し高めるために使用される放射線は周囲の第2の外核に誘導される。
【発明の詳細な説明】
【背景技術】
【0001】
1.米国特許法第119条(e)下の国内優先権
本出願は、参照によって本明細書に組み込まれる、Wolfgang NeubergerおよびWalter Cecchettiによる「Diode Laser Induced Vapor/Plasma Mediated Medical Procedures and Device」という名称の2008年12月2日に出願された米国特許仮出願第61/119259号、ならびに同じくWolfgang NeubergerおよびWalter Cecchettiによる「Diode Laser Induced Vapor/Plasma Mediated Medical Procedures and Device」という名称の2009年12月2日に出願された米国特許出願第12/629313号の利益ならびに優先権を主張する。
【0002】
2.技術分野
本発明は、生物組織の治療のための低侵襲装置および方法に関する。より詳細には、本発明は、特異的効果を組織に達成させるために、ダイオードレーザ誘起蒸気/プラズマによって媒体される医療処置に関する。
【0003】
3.従来技術の説明
レーザ技術が医療処置のために市場に導入されて以来、多くのレーザ装置が組織の除去に対して提案されてきた。レーザエネルギーを使用して、その様々な有利な特徴を生かすことができる。結果として、組織を、レーザ放射線を通してエネルギー、電力、波長、その他などの様々な治療パラメータの使用によって蒸発させる、液化させる、凝固させる、その他が可能である。
【0004】
レーザエネルギーはまた、適切な放射パラメータおよび環境特性の使用によりプラズマ形成をもたらすことも可能である。プラズマ形成は、レーザ放射線が時間および空間を十分に凝縮されると生成される、非線形効果である光学分解を通して達成され、高密度電力を引き起こす。電磁エネルギーの光学分解中、イオン化状態またはプラズマが形成される。プラズマは、衝撃波の生成を急速に拡大させ、その後に空洞化または蒸気泡の形成が続き得る。さらに、空洞化または蒸気泡が崩れると、衝撃波の生成がもたらされる。結果として、レーザエネルギーを気体、液体または固体などの標的材料に焦点を合わせることによって、液体または固体は、一連の光学分解、プラズマ形成および衝撃波生成によって損傷する可能性がある。プラズマ現象および空洞化現象は、いずれも強力な光効果および熱切除効果に関連する。プラズマ泡内では、1000度を超える高温に上昇する。空洞化効果の存在は、衝撃波によって生成される通常のひび割れる音と常に関連している。このことを達成できる方法の一例は、たとえばFREDDY装置(この場合、フラッシュランプ励起の周波数逓倍パルスのYAGレーザによって提供される)として初期パルスを提供することによる。FREDDYレーザによって生成されるプラズマは、発泡するプラズマである。
【0005】
前述の作動の機構によると、レーザエネルギーは、組織の除去を達成させるために(プラズマ形成によって)2つの異なる方法で照射できる。間接的にレーザビームと組織との間に配置された標的にレーザエネルギーの焦点を合わせることによって、次いで光学分解に起因して振動し、組織を乳化するか、または組織の除去を達成するために直接標的組織に焦点を合わせる。
【0006】
間接的な方法の場合、レーザエネルギーは、振動運動を(ハンドピースの先端に配置される)標的にもたらす衝撃波を生成する光ファイバを通して送信され、次に乳化を引き起こすために組織に送信される。
【0007】
米国特許第5224942号において、Beuchatらは、光学分解、プラズマ形成および衝撃波の生成を達成させて体組織を乳化または破壊する、レーザによって駆動する外科用先端組立体を備えるハンドピースを含む、体組織破壊のためのレーザエネルギーを使用する方法および装置を開示している。レーザは、プラズマ形成に起因して振動する(ハンドピース内に配置された)標的に焦点を合わせるので、軽いエネルギーが組織に照射されてハンドピース先端部の機械的振動によって乳化のみがされる。結果として、このシステムの多様性は、軟組織の治療目的のときは、制限される。
【0008】
Dodickらによる米国特許第5324282号は、同様の原理に基づくシステムを教示している。パルス・レーザエネルギーは、金属標的を攻撃するように放出されて、電磁エネルギーを、治療する組織に向けた衝撃波に変換する変換機としての働きをする。機械的衝撃波は、組織の破壊を引き起こす。
【0009】
米国特許出願第2004/0167504号において、Thyzelらは、組織を保持する遠位操作ポートを含む、組織破壊のための外科用針を開示している。パルス・レーザエネルギーは、標的に光ファイバを通して照射され、プラズマ形成に起因する衝撃波を標的の光学分解から生成し、破壊される組織に衝突する。この特許は主に組織の破壊に焦点が絞られているので、ここでもまたシステムの多様性が制限される。
【0010】
上記の発明は、光学分解を機械的振動に変換させる、標的材料上へのプラズマ形成であることがわかる。結果として、この変換でエネルギー損失が生じ、治療効果を減少させる。さらに、機械的振動は、治療する細胞を選択できないため、効果は治療する細胞よりむしろ他の細胞に出現し得る。換言すると、所望の細胞のみが振動によって影響を受けるわけではない可能性がある。
【0011】
細胞の除去を達成するために、レーザ放射線の焦点を直接細胞に合わせると、放射線の標的は、今度は細胞自体になる。通常、除去される細胞は、液体に囲まれ閾値の強度レベルを超えたレーザ放射線に照射されて、衝撃波を生成する。したがって、細胞は溶融するのではなく、機械的エネルギーによって損傷を受ける。この方法は、体内の結石、石、石灰化組織を破壊するために広く使用される。たとえば、プラズマは、粘膜層の切除のためにイオン化アルゴンガスの形で医療に使用されてきた。このやり方で石は、周波数逓倍パルスのYAGレーザ(FREDDY)により、レーザパルスをフラッシュランプ励起から送達する光ファイバの先端でのプラズマ形成によって、開始される泡の崩壊に起因して、生成される衝撃波によって破壊されてきた。
【0012】
米国特許第5071422号において、Watsonらは、パルス色素レーザ源に基づいて、体内で材料を分解する方法を開示している。光ファイバは、治療する領域に挿入され、領域は液体に囲まれ、次いで衝撃波によって破壊を達成するためにパルス色素レーザエネルギーが放射される。この発明は基本的に結石および石の破壊を開示している。しかし色素レーザ放射線が石に吸収されない場合、プラズマ形成が生じず、レーザ破砕術は有効にはならない。色素レーザによって生成されるプラズマは、発泡するプラズマである。さらにパルス色素レーザ源が使用されると、この源は固体状態レーザではないため保守が頻繁に必要となり得る。
【0013】
Mullerらによる米国特許第5963575号は、レーザ破砕術用Q−スイッチ・レーザシステムを開示している。該システムは、より長いパルス幅を組み込み、プラズマ形成を増加させ、その結果衝撃波を生成する。レーザ源は、イオン結晶源であるNd:YAGレーザが好ましい。そのため、該システムは、低効率で寸法が大きく、液体冷却が必要である。その上、該システムは、レーザ放射線が光ファイバではなく鏡によって治療域に送達されるので、位置合わせを要する。さらにこの技術は、他のレーザ技術に比べて正確さに欠ける。
【0014】
米国特許第4960108号において、Reichelらは、赤外領域の近傍のパルスレーザ放射線が上昇する液体の水溶液で囲まれた、破壊される石に集中する、レーザ誘起破砕機を教示している。石は、衝撃波および空洞化を引き起こす、上昇する液体の分解(プラズマ)によって破壊される。上昇する液体は、前記分解に必要なエネルギーを低下させる金属化合物を含む。
【0015】
すべての前述の特許は、通常大量の、不正確な、非効率的なおよび/または頻繁な保守が求められ得るレーザ源の使用を開示しているに過ぎない。
【発明の概要】
【発明が解決しようとする課題】
【0016】
現在のプラズマ形成技術の不都合および多様性の欠落に起因して、それらの欠点に対処する迅速で安全な代替手段を提供する装置の存在が必要である。
【課題を解決するための手段】
【0017】
本発明の目的は、医療的応用のためのプラズマおよび蒸気を、電力レベルおよび電力密度を十分に使用するレーザダイオードによって生成する装置を提供して、様々な医学的適応に対処し、広域にわたる損傷の生成を回避することである。
【0018】
また、本発明の目的は、ダイオードレーザの有利な特徴を利用して、医療的応用のためのプラズマおよび蒸気を発生する装置を提供し、より効率的でより安全な治療をもたらすことである。
【0019】
本発明の別の目的は、医療的応用のためのプラズマおよび蒸気をレーザダイオードによって生成するシステムを提供して、実施可能な治療の多様性を高めることである。
【0020】
本発明のさらにべつの目的は、医療的応用のための火花の少ないプラズマおよび蒸気を、電力レベルおよび電力密度を十分に使用するレーザダイオードによって生成して、医学的適応に対処し、広域にわたる損傷の生成を回避する装置を提供することである。
【0021】
簡単に述べると、本発明は、安全で有効な医療的応用のために改良した方法および装置を提供する。好ましい実施形態では、(信頼できる小型の固体状態の装置から発生する有効な電力などの)レーザダイオード固有の利益の使用に基づいて、プラズマおよび高エネルギーの蒸気は、医療的応用のために電力レベルおよび電力密度を十分に備えて生成されて、医学的適応に対処し、広域にわたる損傷の生成を回避する。様々な構造の送達手段を使用して、プラズマおよび高エネルギー蒸気を先端で引き起こすことができる、高電力密度を達成する。一旦火花の少ないプラズマおよび高エネルギーの蒸気泡が形成されると、プラズマおよび高エネルギーの蒸気を先端で引き起こした波長に加えて他の波長も吸収されることがしばしば見受けられる。結果として、ダイオードまたはダイオード励起レーザによって発生されたより有効な他の波長は、治療効果を向上させるためにビームに追加され得る。たとえば、1470nmの波長を使用して、火花のないプラズマ泡を生成することができ、併せて980nmの波長を使用して、組織を気化し卓越した止血効果を引き起こすことができる。プラズマまたは高エネルギー蒸気が定位置に置かれると、この域からの放射線は組織効果を決定する。別の実施形態では、高尖頭出力のパルス放射線が使用される。1470nm、1940nm、または1550nmの波長が好ましい。さらに、高尖頭出力のパルス放射線は、水中で980nmなどの媒体吸収を備える別の波長との組合せに適用できる。別の実施形態では、同心二重コアファイバを使用して、点火放射線はほぼ単一モード、すなわち内核に誘導され、パルスを維持し高めるために使用される放射線は周囲の第2の外核に誘導される。
【0022】
本発明の上記ならびに他の目的、特徴および利点は、添付図面とともに読むと以下の説明から明確に理解されよう。
【図面の簡単な説明】
【0023】
【図1a】プラズマ泡がレーザ放射によって生成される、本発明の好ましい実施形態を示す図である。
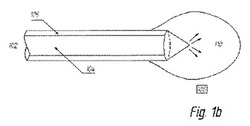
【図1b】プラズマ泡がレーザ放射によって生成される、本発明の好ましい実施形態を示す図である。
【図2】二波長レーザ放射によって組織上に得られた組合せ効果を表す図である。
【図3】円錐先端の光ファイバを通して送達されたレーザ放射により軟組織上に生成された溝を示す図である。
【発明を実施するための形態】
【0024】
ダイオードレーザは、吸収および凝固、ならびに気化を提供する代表的波長の好ましいレーザ組織の相互作用の恩恵により薬剤に使用されてきた。同じ出力電力に対して、ダイオードレーザは、特に非固体状態のレーザまたは周波数二重固体状態のレーザに比べてより小さく、より軽く、空冷で、高い信頼性があり、位置合わせおよび保守の必要がない。
【0025】
上記の技術、制限および問題の一部は、医療的応用のための火花の少ないプラズマおよび蒸気を生成するために、電力レベルおよび電力密度を十分に備えて、医学的適応に対処し、広域にわたる損傷の生成を回避する、(信頼できる小型の固体状態の装置から発生する有効な電力などの)レーザダイオードの固有の利益を使用することによって克服できる。
【0026】
上述のように、高電力密度は、プラズマ/蒸気の形成および/または高い吸収を標的上にもたらす必要がある。プラズマ/蒸気の形成をもたらす手段に焦点を絞って同様に使用することは可能であるが、一例では、円錐ファイバの先端をまず水環境に浸して使用し、放射線は前端部から水中に出る。
【0027】
高吸収の連続波放射線が含水物に照射されると、水分子は高温に急速に加熱される。このように急速に著しい高温加熱をすると、イオン化が急速に拡大し、火花の少ないプラズマ泡を生成して、数ミリメートル離れた場所を破壊し、数ミリ秒後にひび割れる音を発する。続いて数ミリ秒後に、該工程が繰り返され、泡の成長および破壊によって発するひび割れる音が聞こえる。これらの泡は、内部が1000度を超える温度に達する。結果として、泡は著しい熱切除効果を有し、周囲の水にそれらの熱エネルギーを放出する。そのため組織治療における高吸収の放射線レーザの止血効果は、レーザと組織自体との相互作用に直接関連しない。むしろ、止血効果は、熱エネルギーを水中に放出する、プラズマ泡の周囲に発生した蒸気および温水の熱スプレー効果に起因して引き起こされる。これがパラダイムスイッチである。
【0028】
図1aおよび1bは、コア104およびクラッド106を含む光ファイバ102が、プラズマ形成をもたらすためにレーザエネルギーを液体108に放射する、本発明の好ましい実施形態を示す。十分な吸収を環境にもたらすために波長および電力が適切に選択されると、泡110が形成され提供される。たとえば1470±60nmの波長は、水によく吸収されるので、電力濃度が十分であるときはこの目的に適切である。光ファイバ102の先端は、より大きな組織の切除を達成するために、円錐形であることが好ましい。高電力濃度の達成により、プラズマおよび高エネルギーの蒸気を先端で引き起こすことが可能になる。一旦プラズマおよび高エネルギーの蒸気が形成されると、プラズマおよび高エネルギーの蒸気を先端で引き起こした波長に加えて他の波長も吸収されることがしばしば見受けられる。結果としてダイオードまたはダイオード励起レーザ(たとえば980±60nm)によってより有効に生成された他の波長は、治療効果を向上させるためにビームに追加される。プラズマおよび/または高エネルギー蒸気が定位置に置かれると、この域からの放射線は、組織効果を決定する。媒体は放射線の非常に高い吸収係数を有するので、該媒体は放射線と組織との間の相互作用の媒体であり得る。プラズマによって放射される最大放射線波長は、可視範囲のスペクトルである傾向がしばしばあり、組織の分散に起因して、従来の赤外ダイオードレーザに比べて組織へのより高い吸収が見られることになる。
【0029】
さらに凝固は、一般に非常に高温の媒体スプレーの熱スプレーに依存し、媒体スプレーは「プラズマ」泡によって生成される。また、凝固は、プラズマによって放射された一部のスペクトル、および組織に送達される一部の元のレーザ放射線の十分な浸透、ならびに高エネルギー蒸気と組織の相互作用に起因して、組織で達成されることが可能である。
【0030】
上記の説明によれば、本発明は、その手段によって実行可能な様々な医療に関する実質的な多様性を実現する。
【0031】
好ましい実施形態として、本発明は、十分な量の水、または生理食塩水もしくは他の生体適合性液体によって提供される水性環境を含む細胞で実施される。
【0032】
本発明は、さらに以下の例によって説明されるが、それによって限定されない。
【0033】
実施例:
多波長レーザ細胞の切除および除去
マルチダイオードレーザ源は、1つまたは複数の同時波長、たとえば980nmと1470nmを一緒に、同一光ファイバで送達できる。1470nmでは水によく吸収され、したがって高エネルギーの泡をファイバの先端に形成する(空洞化効果および/または火花の少ないプラズマ効果)。この効果によって、軟組織の高速切除が可能になる。980nmでは水における吸収は低いが、血液によく吸収されるので、優れた止血効果が達成できる。BPH治療に使用されるマルチダイオードレーザを用いて、前立腺細胞の高速切除が優れた止血効果で実現できる。図2は、組織治療に対するこれら2つの波長を組み合わせた効果を示す。
【0034】
燃焼するファイバの側面の使用によって、前立腺組織の切除が非常に深い止血と組み合わせて、BPHレーザ治療中に可能になる。円錐先端の光ファイバを備えたマルチダイオードレーザを使用することによって、より大きい部分の前立腺組織の高速切除が、卓越した止血を伴ってBPHレーザ治療中に実現される。インビトロおよび臨床研究後、1470nmダイオードレーザは、もたらされた効果に関して卓越した能力を表すことが検証された。
【0035】
水中に浸され、1470nmのダイオードレーザ源に接続された光ファイバによってもたらされた効果は、同様の効果を1940nmのダイオードレーザで生み出す必要がある閾値に非常に近いプラズマ形成の閾値を有することが検証された。さらに、1470nmのダイオードレーザは、水中でツリウムレーザと同様の効果を生み出すので、生体物質でも同様の効果を生み出す。しかし、ダイオードレーザは、ツリウムレーザなどのイオン結晶レーザに比べると多くの利点を有する。たとえば、1470nmのダイオードレーザは、23%の効率を有するのに対して、ツリウムレーザの効率は6%である。加えて、同じ出力電力に対して、ダイオードレーザは、より小さく、より軽く、空冷で、より高い信頼性があり、位置合わせおよび保守の必要がより少ない。
【0036】
ダイオードレーザを使用して1470nmで連続モードで放射すると、水中に浸されたファイバの先端は、高エネルギーの泡を生成するのが観察され、調査後、火花の少ないプラズマ泡になった。これらのプラズマ泡には、時として火花が存在するので(300μ秒未満のパルス幅のHo:YAGレーザを使用するときは常に存在する)、我々はそれらの泡を「火花のない(sparkler−less)」泡または「火花の少ない(sparkless)」泡と呼んでいる。1470nmの放射線が、ファイバの先端に接触した水分子に衝突することによって、高速加熱を引き起こし、空洞化の泡を形成し、熱湯の熱スプレーをもたらす。すべての電磁エネルギーは、高吸収によって熱エネルギーに転換される。したがって、1mmの水の光学経路は、ほぼ100%の放射線を吸収する。
【0037】
この高速加熱は、急速に増大する熱湯を生成し、火花のないプラズマ泡を作り出し、その結果衝撃波を生成する。数ミリ秒後、この過程で再び関連したひび割れる音が発生する。火花のないプラズマ泡が衝撃波音を伴うが、より低いエネルギーで火花の出るプラズマ泡と同様の効果を生み出す。これらの泡は、熱切除効果に起因して非常に破壊的であり、それらが関連する熱エネルギーは、数ミリメートルの半径内で周囲の水に影響を与える。その結果、1470nmのダイオードレーザも、止血効果に貢献する。止血効果は、放射線と生体組織の直接の相互作用によって生み出されるのではなく、水が介在する。止血効果は、熱湯の熱スプレーによって生み出され、放出されたときに空洞化した泡からファイバの先端に生成され、熱エネルギーを周囲の水に送達する。
【0038】
前記の段落を考慮すると、プラズマ泡は、連続波源を使用して生成され、高エネルギーを有する熱切除効果が達成された。これは、従来技術に比べると特に新しい概念であり、概ねパルスレーザ源のみを開示する。
【0039】
1470nmのダイオードレーザの優れた効果により、1470nmの放射線の熱切除特性と980nmの放射線の止血特性を組合せた、二重帯域放射を有する新しい高電力ダイオードレーザが考えられ開発された(COMBOレーザ)。
【0040】
したがって、組織の高速切除のために1470nmの放射線と、組織に優れた浸透をし、制御され有効な止血効果を得るために980nmの放射線を使用して、光ファイバの移動速度に特に注意を払う必要がない、BHP治療のための高電力ダイオードレーザが開発された。また装置は、特定の外科的応用を実行するための単一波長が選択可能に設計された。
【0041】
高速切除を優れた止血効果と組み合わせて得るために、放出される電力は、それぞれ980nmおよび1470nm、両波長で放出される電力の合計として述べられる。たとえば、100Wのレーザ電力を使用するときは、70Wは980nm源からもたらされ、30Wは1470nm源からもたらされる。
【0042】
本発明の試作(COMBOレーザ)を使用した組織学的結果を含む臨床試験およびビトロ試験は、所望の組織効果、特に1470±60nmおよび980±60nmのダイオードレーザ用に、有効な火花のないプラズマ形成を達成するために2波長の組合せの効果を証明してきた。さらに水により、むしろより高吸収される1940±60nmのダイオードレーザは、前述のいずれの波長とも組み合わせて適切に使用できる。1470nmの波長が水中に浸された細い光ファイバによって送信されると、1470nmの波長は、火花のないプラズマ泡を600umのファイバで放出される電力2Wと同じ低い閾値レベルで生成する。1470nmによって生成されるプラズマは、薄い凝固ならびに硬組織の破裂を伴う軟組織の高速切除を引き起こすことが可能である。980nmの波長は、血液中で卓越して吸収され、水中で吸収されることがより少ない。980nmの波長は、透明白色で止血効果に関連した組織の蒸気化を引き起こすことができる。組織上での浸透は、約2〜3mmである。COMBOレーザを使用して1470nmの波長は、プラズマ泡を水に浸したファイバの先端に生成する。同じファイバの980nmの波長の同時放射がプラズマ泡内に達すると、波長は約70%が吸収され、残余30%はプラズマ泡から出る。その結果、980nmのエネルギーの70%は、プラズマに変換され、この波長の70%は、1470nmの波長によって生成されたプラズマ泡のためのポンプとしての働きをする。980nmの残余30%は、組織に達し、さらなる安定性を引き起こすことができる。このことをさらに実証すると、COMBOレーザが100Wの電力を放出しながら、75Wが980nmで計測され、29Wが1470nmで計測された。100Wが水に浸したファイバで送達されたとき、プラズマ泡がファイバの先端に発生し、980nmでプラズマ泡から出た残余16Wが計測された。プラズマ泡の電源は、980nmの70%すなわち60Wおよび1470nmで28Wである。その結果、プラズマ泡は、2つの放射線(980+1470nm)によって励起され、980nmの残余放射線は、プラズマ泡と重複する働きをして止血効果を向上させることができる。同様に(980+1940nm)の組合せ、または(1470+1940nm)の組合せも有効である。
【0043】
したがって、臨床試験およびインビボ試験は、1470nmの波長の低電力で、プラズマ泡を生成することができ、980nmの波長では、より低価格でより高い効率で、このプラズマ泡の増幅および増加が達成できることを示す。
【0044】
追加試験で、COMBOレーザを伴い1000umの円錐ファイバおよび120Wの電力を使用して、1470nmで35Wおよび980nmで93Wが計測されたことを示した。
【0045】
別の好ましい実施形態では、レーザ源の他の組合せを使用して、プラズマ点火手段およびパルス活性化手段を利用してプラズマを生成するためにダイオード励起レーザ装置を達成することができる。たとえば、点火放射線が単一モードコアおよびパルスを維持し高めるために使用する放射線に誘導される二重コアファイバは、周囲の第2のコアに誘導される。単一モードまたはほぼ単一モードの放射線は、1550±60nmのダイオード励起またはQ−スイッチでファイバレーザからもたらされ、ダイオード励起緑色レーザの細長いファイバパルスならびにエネルギーの大部分である、パルスの維持および強化のための放射線は、ダイオードレーザからもたらされることになる。1550nmのパルスは、915〜980nmまたは1480nmのレーザダイオード励起から生成することが可能である。
【0046】
ビトロ試験後、両側帯ダイオードレーザの卓越した効果は歴然としており、BPH処置でより迅速な治療がもたらされた。より多く組織の切除を各掃引で得るために、より大きな組織面に放射線を照射できる光ファイバを使用する可能性が着想された。結果として、前立腺組織上のより大きな面に照射するため、直径1000μmのコアを有する円錐形ファイバの使用が提案された。そのため、側面燃焼ファイバではなく、円錐形ファイバの使用によって、1470nmの放射線の高速熱切除効果の使用が可能になった。各掃引後、出血なしに大きく清潔な溝が得られた。得られた溝は、側面燃焼ファイバによって生成された溝より大きかったが、より深い凝固効果をもたらす。円錐ファイバの使用で、切除効果は、優れた止血効果と組み合わせられることによって、他の同様のレーザ治療より迅速に、さらには従来のTURP治療より迅速にBPH治療を完了することが可能になった。図3では、溝を誘発した円錐形ファイバが見られる。
【0047】
別の好ましい実施形態では、Neubergerにより米国特許出願第61/245484号に開示されたツイスターファイバなどの、非対称の軸外れ放射ファイバが利用され得る。これらのファイバによって、より良いねじれおよび操作が可能になる。
【0048】
質量50gr(約3.24g)の前立腺のBPH治療のために、100Wおよび110Wに設定した電力を使用すると、前立腺腺腫の切除のための総治療時間は、18〜20分であった。同じ質量の前立腺は、TURP治療では両側帯ダイオードレーザの治療より20%遅い25〜30分で治療され得ることを考慮されたい。
【0049】
治療後の患者は、痛みまたはあらゆる他の不便がないと述べた。出血がないことが観察され、カテーテルは同日に除去された。
【0050】
本発明の好ましい実施形態を添付図面を参照に説明したが、本発明は詳細な実施形態に限定されず、様々な変更および変形形態が、添付の特許請求で定義されているように本発明の範囲または精神から逸脱することなくその中で効果があることは、当業者には理解されたい。
【背景技術】
【0001】
1.米国特許法第119条(e)下の国内優先権
本出願は、参照によって本明細書に組み込まれる、Wolfgang NeubergerおよびWalter Cecchettiによる「Diode Laser Induced Vapor/Plasma Mediated Medical Procedures and Device」という名称の2008年12月2日に出願された米国特許仮出願第61/119259号、ならびに同じくWolfgang NeubergerおよびWalter Cecchettiによる「Diode Laser Induced Vapor/Plasma Mediated Medical Procedures and Device」という名称の2009年12月2日に出願された米国特許出願第12/629313号の利益ならびに優先権を主張する。
【0002】
2.技術分野
本発明は、生物組織の治療のための低侵襲装置および方法に関する。より詳細には、本発明は、特異的効果を組織に達成させるために、ダイオードレーザ誘起蒸気/プラズマによって媒体される医療処置に関する。
【0003】
3.従来技術の説明
レーザ技術が医療処置のために市場に導入されて以来、多くのレーザ装置が組織の除去に対して提案されてきた。レーザエネルギーを使用して、その様々な有利な特徴を生かすことができる。結果として、組織を、レーザ放射線を通してエネルギー、電力、波長、その他などの様々な治療パラメータの使用によって蒸発させる、液化させる、凝固させる、その他が可能である。
【0004】
レーザエネルギーはまた、適切な放射パラメータおよび環境特性の使用によりプラズマ形成をもたらすことも可能である。プラズマ形成は、レーザ放射線が時間および空間を十分に凝縮されると生成される、非線形効果である光学分解を通して達成され、高密度電力を引き起こす。電磁エネルギーの光学分解中、イオン化状態またはプラズマが形成される。プラズマは、衝撃波の生成を急速に拡大させ、その後に空洞化または蒸気泡の形成が続き得る。さらに、空洞化または蒸気泡が崩れると、衝撃波の生成がもたらされる。結果として、レーザエネルギーを気体、液体または固体などの標的材料に焦点を合わせることによって、液体または固体は、一連の光学分解、プラズマ形成および衝撃波生成によって損傷する可能性がある。プラズマ現象および空洞化現象は、いずれも強力な光効果および熱切除効果に関連する。プラズマ泡内では、1000度を超える高温に上昇する。空洞化効果の存在は、衝撃波によって生成される通常のひび割れる音と常に関連している。このことを達成できる方法の一例は、たとえばFREDDY装置(この場合、フラッシュランプ励起の周波数逓倍パルスのYAGレーザによって提供される)として初期パルスを提供することによる。FREDDYレーザによって生成されるプラズマは、発泡するプラズマである。
【0005】
前述の作動の機構によると、レーザエネルギーは、組織の除去を達成させるために(プラズマ形成によって)2つの異なる方法で照射できる。間接的にレーザビームと組織との間に配置された標的にレーザエネルギーの焦点を合わせることによって、次いで光学分解に起因して振動し、組織を乳化するか、または組織の除去を達成するために直接標的組織に焦点を合わせる。
【0006】
間接的な方法の場合、レーザエネルギーは、振動運動を(ハンドピースの先端に配置される)標的にもたらす衝撃波を生成する光ファイバを通して送信され、次に乳化を引き起こすために組織に送信される。
【0007】
米国特許第5224942号において、Beuchatらは、光学分解、プラズマ形成および衝撃波の生成を達成させて体組織を乳化または破壊する、レーザによって駆動する外科用先端組立体を備えるハンドピースを含む、体組織破壊のためのレーザエネルギーを使用する方法および装置を開示している。レーザは、プラズマ形成に起因して振動する(ハンドピース内に配置された)標的に焦点を合わせるので、軽いエネルギーが組織に照射されてハンドピース先端部の機械的振動によって乳化のみがされる。結果として、このシステムの多様性は、軟組織の治療目的のときは、制限される。
【0008】
Dodickらによる米国特許第5324282号は、同様の原理に基づくシステムを教示している。パルス・レーザエネルギーは、金属標的を攻撃するように放出されて、電磁エネルギーを、治療する組織に向けた衝撃波に変換する変換機としての働きをする。機械的衝撃波は、組織の破壊を引き起こす。
【0009】
米国特許出願第2004/0167504号において、Thyzelらは、組織を保持する遠位操作ポートを含む、組織破壊のための外科用針を開示している。パルス・レーザエネルギーは、標的に光ファイバを通して照射され、プラズマ形成に起因する衝撃波を標的の光学分解から生成し、破壊される組織に衝突する。この特許は主に組織の破壊に焦点が絞られているので、ここでもまたシステムの多様性が制限される。
【0010】
上記の発明は、光学分解を機械的振動に変換させる、標的材料上へのプラズマ形成であることがわかる。結果として、この変換でエネルギー損失が生じ、治療効果を減少させる。さらに、機械的振動は、治療する細胞を選択できないため、効果は治療する細胞よりむしろ他の細胞に出現し得る。換言すると、所望の細胞のみが振動によって影響を受けるわけではない可能性がある。
【0011】
細胞の除去を達成するために、レーザ放射線の焦点を直接細胞に合わせると、放射線の標的は、今度は細胞自体になる。通常、除去される細胞は、液体に囲まれ閾値の強度レベルを超えたレーザ放射線に照射されて、衝撃波を生成する。したがって、細胞は溶融するのではなく、機械的エネルギーによって損傷を受ける。この方法は、体内の結石、石、石灰化組織を破壊するために広く使用される。たとえば、プラズマは、粘膜層の切除のためにイオン化アルゴンガスの形で医療に使用されてきた。このやり方で石は、周波数逓倍パルスのYAGレーザ(FREDDY)により、レーザパルスをフラッシュランプ励起から送達する光ファイバの先端でのプラズマ形成によって、開始される泡の崩壊に起因して、生成される衝撃波によって破壊されてきた。
【0012】
米国特許第5071422号において、Watsonらは、パルス色素レーザ源に基づいて、体内で材料を分解する方法を開示している。光ファイバは、治療する領域に挿入され、領域は液体に囲まれ、次いで衝撃波によって破壊を達成するためにパルス色素レーザエネルギーが放射される。この発明は基本的に結石および石の破壊を開示している。しかし色素レーザ放射線が石に吸収されない場合、プラズマ形成が生じず、レーザ破砕術は有効にはならない。色素レーザによって生成されるプラズマは、発泡するプラズマである。さらにパルス色素レーザ源が使用されると、この源は固体状態レーザではないため保守が頻繁に必要となり得る。
【0013】
Mullerらによる米国特許第5963575号は、レーザ破砕術用Q−スイッチ・レーザシステムを開示している。該システムは、より長いパルス幅を組み込み、プラズマ形成を増加させ、その結果衝撃波を生成する。レーザ源は、イオン結晶源であるNd:YAGレーザが好ましい。そのため、該システムは、低効率で寸法が大きく、液体冷却が必要である。その上、該システムは、レーザ放射線が光ファイバではなく鏡によって治療域に送達されるので、位置合わせを要する。さらにこの技術は、他のレーザ技術に比べて正確さに欠ける。
【0014】
米国特許第4960108号において、Reichelらは、赤外領域の近傍のパルスレーザ放射線が上昇する液体の水溶液で囲まれた、破壊される石に集中する、レーザ誘起破砕機を教示している。石は、衝撃波および空洞化を引き起こす、上昇する液体の分解(プラズマ)によって破壊される。上昇する液体は、前記分解に必要なエネルギーを低下させる金属化合物を含む。
【0015】
すべての前述の特許は、通常大量の、不正確な、非効率的なおよび/または頻繁な保守が求められ得るレーザ源の使用を開示しているに過ぎない。
【発明の概要】
【発明が解決しようとする課題】
【0016】
現在のプラズマ形成技術の不都合および多様性の欠落に起因して、それらの欠点に対処する迅速で安全な代替手段を提供する装置の存在が必要である。
【課題を解決するための手段】
【0017】
本発明の目的は、医療的応用のためのプラズマおよび蒸気を、電力レベルおよび電力密度を十分に使用するレーザダイオードによって生成する装置を提供して、様々な医学的適応に対処し、広域にわたる損傷の生成を回避することである。
【0018】
また、本発明の目的は、ダイオードレーザの有利な特徴を利用して、医療的応用のためのプラズマおよび蒸気を発生する装置を提供し、より効率的でより安全な治療をもたらすことである。
【0019】
本発明の別の目的は、医療的応用のためのプラズマおよび蒸気をレーザダイオードによって生成するシステムを提供して、実施可能な治療の多様性を高めることである。
【0020】
本発明のさらにべつの目的は、医療的応用のための火花の少ないプラズマおよび蒸気を、電力レベルおよび電力密度を十分に使用するレーザダイオードによって生成して、医学的適応に対処し、広域にわたる損傷の生成を回避する装置を提供することである。
【0021】
簡単に述べると、本発明は、安全で有効な医療的応用のために改良した方法および装置を提供する。好ましい実施形態では、(信頼できる小型の固体状態の装置から発生する有効な電力などの)レーザダイオード固有の利益の使用に基づいて、プラズマおよび高エネルギーの蒸気は、医療的応用のために電力レベルおよび電力密度を十分に備えて生成されて、医学的適応に対処し、広域にわたる損傷の生成を回避する。様々な構造の送達手段を使用して、プラズマおよび高エネルギー蒸気を先端で引き起こすことができる、高電力密度を達成する。一旦火花の少ないプラズマおよび高エネルギーの蒸気泡が形成されると、プラズマおよび高エネルギーの蒸気を先端で引き起こした波長に加えて他の波長も吸収されることがしばしば見受けられる。結果として、ダイオードまたはダイオード励起レーザによって発生されたより有効な他の波長は、治療効果を向上させるためにビームに追加され得る。たとえば、1470nmの波長を使用して、火花のないプラズマ泡を生成することができ、併せて980nmの波長を使用して、組織を気化し卓越した止血効果を引き起こすことができる。プラズマまたは高エネルギー蒸気が定位置に置かれると、この域からの放射線は組織効果を決定する。別の実施形態では、高尖頭出力のパルス放射線が使用される。1470nm、1940nm、または1550nmの波長が好ましい。さらに、高尖頭出力のパルス放射線は、水中で980nmなどの媒体吸収を備える別の波長との組合せに適用できる。別の実施形態では、同心二重コアファイバを使用して、点火放射線はほぼ単一モード、すなわち内核に誘導され、パルスを維持し高めるために使用される放射線は周囲の第2の外核に誘導される。
【0022】
本発明の上記ならびに他の目的、特徴および利点は、添付図面とともに読むと以下の説明から明確に理解されよう。
【図面の簡単な説明】
【0023】
【図1a】プラズマ泡がレーザ放射によって生成される、本発明の好ましい実施形態を示す図である。
【図1b】プラズマ泡がレーザ放射によって生成される、本発明の好ましい実施形態を示す図である。
【図2】二波長レーザ放射によって組織上に得られた組合せ効果を表す図である。
【図3】円錐先端の光ファイバを通して送達されたレーザ放射により軟組織上に生成された溝を示す図である。
【発明を実施するための形態】
【0024】
ダイオードレーザは、吸収および凝固、ならびに気化を提供する代表的波長の好ましいレーザ組織の相互作用の恩恵により薬剤に使用されてきた。同じ出力電力に対して、ダイオードレーザは、特に非固体状態のレーザまたは周波数二重固体状態のレーザに比べてより小さく、より軽く、空冷で、高い信頼性があり、位置合わせおよび保守の必要がない。
【0025】
上記の技術、制限および問題の一部は、医療的応用のための火花の少ないプラズマおよび蒸気を生成するために、電力レベルおよび電力密度を十分に備えて、医学的適応に対処し、広域にわたる損傷の生成を回避する、(信頼できる小型の固体状態の装置から発生する有効な電力などの)レーザダイオードの固有の利益を使用することによって克服できる。
【0026】
上述のように、高電力密度は、プラズマ/蒸気の形成および/または高い吸収を標的上にもたらす必要がある。プラズマ/蒸気の形成をもたらす手段に焦点を絞って同様に使用することは可能であるが、一例では、円錐ファイバの先端をまず水環境に浸して使用し、放射線は前端部から水中に出る。
【0027】
高吸収の連続波放射線が含水物に照射されると、水分子は高温に急速に加熱される。このように急速に著しい高温加熱をすると、イオン化が急速に拡大し、火花の少ないプラズマ泡を生成して、数ミリメートル離れた場所を破壊し、数ミリ秒後にひび割れる音を発する。続いて数ミリ秒後に、該工程が繰り返され、泡の成長および破壊によって発するひび割れる音が聞こえる。これらの泡は、内部が1000度を超える温度に達する。結果として、泡は著しい熱切除効果を有し、周囲の水にそれらの熱エネルギーを放出する。そのため組織治療における高吸収の放射線レーザの止血効果は、レーザと組織自体との相互作用に直接関連しない。むしろ、止血効果は、熱エネルギーを水中に放出する、プラズマ泡の周囲に発生した蒸気および温水の熱スプレー効果に起因して引き起こされる。これがパラダイムスイッチである。
【0028】
図1aおよび1bは、コア104およびクラッド106を含む光ファイバ102が、プラズマ形成をもたらすためにレーザエネルギーを液体108に放射する、本発明の好ましい実施形態を示す。十分な吸収を環境にもたらすために波長および電力が適切に選択されると、泡110が形成され提供される。たとえば1470±60nmの波長は、水によく吸収されるので、電力濃度が十分であるときはこの目的に適切である。光ファイバ102の先端は、より大きな組織の切除を達成するために、円錐形であることが好ましい。高電力濃度の達成により、プラズマおよび高エネルギーの蒸気を先端で引き起こすことが可能になる。一旦プラズマおよび高エネルギーの蒸気が形成されると、プラズマおよび高エネルギーの蒸気を先端で引き起こした波長に加えて他の波長も吸収されることがしばしば見受けられる。結果としてダイオードまたはダイオード励起レーザ(たとえば980±60nm)によってより有効に生成された他の波長は、治療効果を向上させるためにビームに追加される。プラズマおよび/または高エネルギー蒸気が定位置に置かれると、この域からの放射線は、組織効果を決定する。媒体は放射線の非常に高い吸収係数を有するので、該媒体は放射線と組織との間の相互作用の媒体であり得る。プラズマによって放射される最大放射線波長は、可視範囲のスペクトルである傾向がしばしばあり、組織の分散に起因して、従来の赤外ダイオードレーザに比べて組織へのより高い吸収が見られることになる。
【0029】
さらに凝固は、一般に非常に高温の媒体スプレーの熱スプレーに依存し、媒体スプレーは「プラズマ」泡によって生成される。また、凝固は、プラズマによって放射された一部のスペクトル、および組織に送達される一部の元のレーザ放射線の十分な浸透、ならびに高エネルギー蒸気と組織の相互作用に起因して、組織で達成されることが可能である。
【0030】
上記の説明によれば、本発明は、その手段によって実行可能な様々な医療に関する実質的な多様性を実現する。
【0031】
好ましい実施形態として、本発明は、十分な量の水、または生理食塩水もしくは他の生体適合性液体によって提供される水性環境を含む細胞で実施される。
【0032】
本発明は、さらに以下の例によって説明されるが、それによって限定されない。
【0033】
実施例:
多波長レーザ細胞の切除および除去
マルチダイオードレーザ源は、1つまたは複数の同時波長、たとえば980nmと1470nmを一緒に、同一光ファイバで送達できる。1470nmでは水によく吸収され、したがって高エネルギーの泡をファイバの先端に形成する(空洞化効果および/または火花の少ないプラズマ効果)。この効果によって、軟組織の高速切除が可能になる。980nmでは水における吸収は低いが、血液によく吸収されるので、優れた止血効果が達成できる。BPH治療に使用されるマルチダイオードレーザを用いて、前立腺細胞の高速切除が優れた止血効果で実現できる。図2は、組織治療に対するこれら2つの波長を組み合わせた効果を示す。
【0034】
燃焼するファイバの側面の使用によって、前立腺組織の切除が非常に深い止血と組み合わせて、BPHレーザ治療中に可能になる。円錐先端の光ファイバを備えたマルチダイオードレーザを使用することによって、より大きい部分の前立腺組織の高速切除が、卓越した止血を伴ってBPHレーザ治療中に実現される。インビトロおよび臨床研究後、1470nmダイオードレーザは、もたらされた効果に関して卓越した能力を表すことが検証された。
【0035】
水中に浸され、1470nmのダイオードレーザ源に接続された光ファイバによってもたらされた効果は、同様の効果を1940nmのダイオードレーザで生み出す必要がある閾値に非常に近いプラズマ形成の閾値を有することが検証された。さらに、1470nmのダイオードレーザは、水中でツリウムレーザと同様の効果を生み出すので、生体物質でも同様の効果を生み出す。しかし、ダイオードレーザは、ツリウムレーザなどのイオン結晶レーザに比べると多くの利点を有する。たとえば、1470nmのダイオードレーザは、23%の効率を有するのに対して、ツリウムレーザの効率は6%である。加えて、同じ出力電力に対して、ダイオードレーザは、より小さく、より軽く、空冷で、より高い信頼性があり、位置合わせおよび保守の必要がより少ない。
【0036】
ダイオードレーザを使用して1470nmで連続モードで放射すると、水中に浸されたファイバの先端は、高エネルギーの泡を生成するのが観察され、調査後、火花の少ないプラズマ泡になった。これらのプラズマ泡には、時として火花が存在するので(300μ秒未満のパルス幅のHo:YAGレーザを使用するときは常に存在する)、我々はそれらの泡を「火花のない(sparkler−less)」泡または「火花の少ない(sparkless)」泡と呼んでいる。1470nmの放射線が、ファイバの先端に接触した水分子に衝突することによって、高速加熱を引き起こし、空洞化の泡を形成し、熱湯の熱スプレーをもたらす。すべての電磁エネルギーは、高吸収によって熱エネルギーに転換される。したがって、1mmの水の光学経路は、ほぼ100%の放射線を吸収する。
【0037】
この高速加熱は、急速に増大する熱湯を生成し、火花のないプラズマ泡を作り出し、その結果衝撃波を生成する。数ミリ秒後、この過程で再び関連したひび割れる音が発生する。火花のないプラズマ泡が衝撃波音を伴うが、より低いエネルギーで火花の出るプラズマ泡と同様の効果を生み出す。これらの泡は、熱切除効果に起因して非常に破壊的であり、それらが関連する熱エネルギーは、数ミリメートルの半径内で周囲の水に影響を与える。その結果、1470nmのダイオードレーザも、止血効果に貢献する。止血効果は、放射線と生体組織の直接の相互作用によって生み出されるのではなく、水が介在する。止血効果は、熱湯の熱スプレーによって生み出され、放出されたときに空洞化した泡からファイバの先端に生成され、熱エネルギーを周囲の水に送達する。
【0038】
前記の段落を考慮すると、プラズマ泡は、連続波源を使用して生成され、高エネルギーを有する熱切除効果が達成された。これは、従来技術に比べると特に新しい概念であり、概ねパルスレーザ源のみを開示する。
【0039】
1470nmのダイオードレーザの優れた効果により、1470nmの放射線の熱切除特性と980nmの放射線の止血特性を組合せた、二重帯域放射を有する新しい高電力ダイオードレーザが考えられ開発された(COMBOレーザ)。
【0040】
したがって、組織の高速切除のために1470nmの放射線と、組織に優れた浸透をし、制御され有効な止血効果を得るために980nmの放射線を使用して、光ファイバの移動速度に特に注意を払う必要がない、BHP治療のための高電力ダイオードレーザが開発された。また装置は、特定の外科的応用を実行するための単一波長が選択可能に設計された。
【0041】
高速切除を優れた止血効果と組み合わせて得るために、放出される電力は、それぞれ980nmおよび1470nm、両波長で放出される電力の合計として述べられる。たとえば、100Wのレーザ電力を使用するときは、70Wは980nm源からもたらされ、30Wは1470nm源からもたらされる。
【0042】
本発明の試作(COMBOレーザ)を使用した組織学的結果を含む臨床試験およびビトロ試験は、所望の組織効果、特に1470±60nmおよび980±60nmのダイオードレーザ用に、有効な火花のないプラズマ形成を達成するために2波長の組合せの効果を証明してきた。さらに水により、むしろより高吸収される1940±60nmのダイオードレーザは、前述のいずれの波長とも組み合わせて適切に使用できる。1470nmの波長が水中に浸された細い光ファイバによって送信されると、1470nmの波長は、火花のないプラズマ泡を600umのファイバで放出される電力2Wと同じ低い閾値レベルで生成する。1470nmによって生成されるプラズマは、薄い凝固ならびに硬組織の破裂を伴う軟組織の高速切除を引き起こすことが可能である。980nmの波長は、血液中で卓越して吸収され、水中で吸収されることがより少ない。980nmの波長は、透明白色で止血効果に関連した組織の蒸気化を引き起こすことができる。組織上での浸透は、約2〜3mmである。COMBOレーザを使用して1470nmの波長は、プラズマ泡を水に浸したファイバの先端に生成する。同じファイバの980nmの波長の同時放射がプラズマ泡内に達すると、波長は約70%が吸収され、残余30%はプラズマ泡から出る。その結果、980nmのエネルギーの70%は、プラズマに変換され、この波長の70%は、1470nmの波長によって生成されたプラズマ泡のためのポンプとしての働きをする。980nmの残余30%は、組織に達し、さらなる安定性を引き起こすことができる。このことをさらに実証すると、COMBOレーザが100Wの電力を放出しながら、75Wが980nmで計測され、29Wが1470nmで計測された。100Wが水に浸したファイバで送達されたとき、プラズマ泡がファイバの先端に発生し、980nmでプラズマ泡から出た残余16Wが計測された。プラズマ泡の電源は、980nmの70%すなわち60Wおよび1470nmで28Wである。その結果、プラズマ泡は、2つの放射線(980+1470nm)によって励起され、980nmの残余放射線は、プラズマ泡と重複する働きをして止血効果を向上させることができる。同様に(980+1940nm)の組合せ、または(1470+1940nm)の組合せも有効である。
【0043】
したがって、臨床試験およびインビボ試験は、1470nmの波長の低電力で、プラズマ泡を生成することができ、980nmの波長では、より低価格でより高い効率で、このプラズマ泡の増幅および増加が達成できることを示す。
【0044】
追加試験で、COMBOレーザを伴い1000umの円錐ファイバおよび120Wの電力を使用して、1470nmで35Wおよび980nmで93Wが計測されたことを示した。
【0045】
別の好ましい実施形態では、レーザ源の他の組合せを使用して、プラズマ点火手段およびパルス活性化手段を利用してプラズマを生成するためにダイオード励起レーザ装置を達成することができる。たとえば、点火放射線が単一モードコアおよびパルスを維持し高めるために使用する放射線に誘導される二重コアファイバは、周囲の第2のコアに誘導される。単一モードまたはほぼ単一モードの放射線は、1550±60nmのダイオード励起またはQ−スイッチでファイバレーザからもたらされ、ダイオード励起緑色レーザの細長いファイバパルスならびにエネルギーの大部分である、パルスの維持および強化のための放射線は、ダイオードレーザからもたらされることになる。1550nmのパルスは、915〜980nmまたは1480nmのレーザダイオード励起から生成することが可能である。
【0046】
ビトロ試験後、両側帯ダイオードレーザの卓越した効果は歴然としており、BPH処置でより迅速な治療がもたらされた。より多く組織の切除を各掃引で得るために、より大きな組織面に放射線を照射できる光ファイバを使用する可能性が着想された。結果として、前立腺組織上のより大きな面に照射するため、直径1000μmのコアを有する円錐形ファイバの使用が提案された。そのため、側面燃焼ファイバではなく、円錐形ファイバの使用によって、1470nmの放射線の高速熱切除効果の使用が可能になった。各掃引後、出血なしに大きく清潔な溝が得られた。得られた溝は、側面燃焼ファイバによって生成された溝より大きかったが、より深い凝固効果をもたらす。円錐ファイバの使用で、切除効果は、優れた止血効果と組み合わせられることによって、他の同様のレーザ治療より迅速に、さらには従来のTURP治療より迅速にBPH治療を完了することが可能になった。図3では、溝を誘発した円錐形ファイバが見られる。
【0047】
別の好ましい実施形態では、Neubergerにより米国特許出願第61/245484号に開示されたツイスターファイバなどの、非対称の軸外れ放射ファイバが利用され得る。これらのファイバによって、より良いねじれおよび操作が可能になる。
【0048】
質量50gr(約3.24g)の前立腺のBPH治療のために、100Wおよび110Wに設定した電力を使用すると、前立腺腺腫の切除のための総治療時間は、18〜20分であった。同じ質量の前立腺は、TURP治療では両側帯ダイオードレーザの治療より20%遅い25〜30分で治療され得ることを考慮されたい。
【0049】
治療後の患者は、痛みまたはあらゆる他の不便がないと述べた。出血がないことが観察され、カテーテルは同日に除去された。
【0050】
本発明の好ましい実施形態を添付図面を参照に説明したが、本発明は詳細な実施形態に限定されず、様々な変更および変形形態が、添付の特許請求で定義されているように本発明の範囲または精神から逸脱することなくその中で効果があることは、当業者には理解されたい。
【特許請求の範囲】
【請求項1】
医療を高めるための医療レーザ装置であって、
少なくとも1つのレーザ光源と、
遠位端および近位端を有する送信媒体であって、前記近位端は前記少なくとも1つの光源と光学接触し、前記遠位端は治療部位付近にある、送信媒体と、を含み、
前記少なくとも1つのダイオードレーザ源は、前記治療部位で優れた吸収をする少なくとも1つの波長を放射し、
操作中、プラズマおよび/または高エネルギー蒸気泡領域は、組織治療部位に著しく近位の前記送信媒体の前記遠位端で形成される、医療レーザ装置。
【請求項2】
たとえば尿路を通して、患者の体に入る手段をさらに含む、請求項1に記載の医療レーザ装置。
【請求項3】
前記送達媒体は、少なくとも1つの光ファイバである、請求項1に記載の医療レーザ装置。
【請求項4】
前記レーザ光源は、パルスモードで、連続モードでまたはこれらのモードの組合せで動作可能な、請求項1に記載の医療レーザ装置。
【請求項5】
前記レーザは、980±60nm、1470±60nm、または1940±60nmのいずれの周辺でも動作する、請求項1に記載の医療レーザ装置。
【請求項6】
前記少なくとも1つの光ファイバは、二重コア構造を有し、1つのレーザ波長は、内核の中に移動し、第2の波長は、外核の中に送達される、請求項3に記載のレーザシステム。
【請求項7】
少なくとも2つの好ましい前記波長は、980nmと1470nm;980nmと1940nmまたは1470nmと1940nmの組合せが利用される、請求項5に記載のレーザシステム。
【請求項8】
1つのレーザは、ファイバレーザであり第2のレーザは前記ファイバレーザのための励起レーザであり、両方のレーザからのビームは、少なくとも1つの光ファイバによって送達される、請求項3に記載のレーザシステム。
【請求項9】
前記少なくとも1つの光ファイバは、同心コア構造を有し、前記ファイバレーザ波長は、内核の中に移動し、励起レーザ波長は、外核の中に送達される、請求項8に記載のレーザシステム。
【請求項10】
前記ファイバレーザは、約1550nmで放射し、前記励起レーザは、約915〜980nmまたは約1480nmで放射する、請求項8に記載のレーザシステム。
【請求項11】
前記レーザ光源は、連続モードまたは半連続モードで動作するツリウムレーザである、請求項1に記載の医療レーザ装置。
【請求項12】
前記少なくとも1つの光ファイバは、ねじれファイバである、請求項3に記載の医療レーザシステム。
【請求項13】
強力なエネルギー源によって適切に発生したエネルギーを送達媒体を通してその遠位端に送達することによって、発生したプラズマおよび/または高エネルギー蒸気を利用する医療であって、治療される組織の近傍にあり、気化、凝固、切除、切断、または他の医療効果などの前記組織に所望の医療効果を達成する、医療。
【請求項14】
前記エネルギー源は、パルスモードで、連続モードでまたはこれらのモードの組合せで動作される、請求項13に記載の医療。
【請求項1】
医療を高めるための医療レーザ装置であって、
少なくとも1つのレーザ光源と、
遠位端および近位端を有する送信媒体であって、前記近位端は前記少なくとも1つの光源と光学接触し、前記遠位端は治療部位付近にある、送信媒体と、を含み、
前記少なくとも1つのダイオードレーザ源は、前記治療部位で優れた吸収をする少なくとも1つの波長を放射し、
操作中、プラズマおよび/または高エネルギー蒸気泡領域は、組織治療部位に著しく近位の前記送信媒体の前記遠位端で形成される、医療レーザ装置。
【請求項2】
たとえば尿路を通して、患者の体に入る手段をさらに含む、請求項1に記載の医療レーザ装置。
【請求項3】
前記送達媒体は、少なくとも1つの光ファイバである、請求項1に記載の医療レーザ装置。
【請求項4】
前記レーザ光源は、パルスモードで、連続モードでまたはこれらのモードの組合せで動作可能な、請求項1に記載の医療レーザ装置。
【請求項5】
前記レーザは、980±60nm、1470±60nm、または1940±60nmのいずれの周辺でも動作する、請求項1に記載の医療レーザ装置。
【請求項6】
前記少なくとも1つの光ファイバは、二重コア構造を有し、1つのレーザ波長は、内核の中に移動し、第2の波長は、外核の中に送達される、請求項3に記載のレーザシステム。
【請求項7】
少なくとも2つの好ましい前記波長は、980nmと1470nm;980nmと1940nmまたは1470nmと1940nmの組合せが利用される、請求項5に記載のレーザシステム。
【請求項8】
1つのレーザは、ファイバレーザであり第2のレーザは前記ファイバレーザのための励起レーザであり、両方のレーザからのビームは、少なくとも1つの光ファイバによって送達される、請求項3に記載のレーザシステム。
【請求項9】
前記少なくとも1つの光ファイバは、同心コア構造を有し、前記ファイバレーザ波長は、内核の中に移動し、励起レーザ波長は、外核の中に送達される、請求項8に記載のレーザシステム。
【請求項10】
前記ファイバレーザは、約1550nmで放射し、前記励起レーザは、約915〜980nmまたは約1480nmで放射する、請求項8に記載のレーザシステム。
【請求項11】
前記レーザ光源は、連続モードまたは半連続モードで動作するツリウムレーザである、請求項1に記載の医療レーザ装置。
【請求項12】
前記少なくとも1つの光ファイバは、ねじれファイバである、請求項3に記載の医療レーザシステム。
【請求項13】
強力なエネルギー源によって適切に発生したエネルギーを送達媒体を通してその遠位端に送達することによって、発生したプラズマおよび/または高エネルギー蒸気を利用する医療であって、治療される組織の近傍にあり、気化、凝固、切除、切断、または他の医療効果などの前記組織に所望の医療効果を達成する、医療。
【請求項14】
前記エネルギー源は、パルスモードで、連続モードでまたはこれらのモードの組合せで動作される、請求項13に記載の医療。
【図1a】


【図1b】


【図1c】


【図1d】


【図2】


【図3】




【図1b】


【図1c】


【図1d】


【図2】


【図3】


【公表番号】特表2012−510345(P2012−510345A)
【公表日】平成24年5月10日(2012.5.10)
【国際特許分類】
【出願番号】特願2011−539655(P2011−539655)
【出願日】平成21年12月2日(2009.12.2)
【国際出願番号】PCT/US2009/066421
【国際公開番号】WO2010/065645
【国際公開日】平成22年6月10日(2010.6.10)
【出願人】(511133381)セラモプテック インダストリーズ,インコーポレイテッド (2)
【Fターム(参考)】
【公表日】平成24年5月10日(2012.5.10)
【国際特許分類】
【出願日】平成21年12月2日(2009.12.2)
【国際出願番号】PCT/US2009/066421
【国際公開番号】WO2010/065645
【国際公開日】平成22年6月10日(2010.6.10)
【出願人】(511133381)セラモプテック インダストリーズ,インコーポレイテッド (2)
【Fターム(参考)】
[ Back to top ]

