両親媒性化合物およびその共重合体ならびに該共重合体を有効成分とする製紙用添加剤
【解決手段】 式(1)または(2)で表される新規両親媒性化合物、および共重合可能なモノマーとの共重合体、さらに(メタ)アクリルアミドとの共重合体を有効成分とする製紙用添加剤。

【効果】 合成樹脂原料として有用な新規両親媒性化合物およびその共重合体を提供することができる。

【効果】 合成樹脂原料として有用な新規両親媒性化合物およびその共重合体を提供することができる。
【発明の詳細な説明】
【0001】
【発明が属する技術分野】本発明は、コハク酸ハーフエステル構造を持つ新規の両親媒性ビニル化合物に関し、さらにこれらの新規ビニル化合物と共重合可能なビニル化合物との共重合体、およびこれらの新規ビニル化合物と(メタ)アクリルアミドとの水に可溶あるいは分散可能な共重合体および該共重合体を有効成分として含有する製紙用添加剤(以下PAM系サイズ剤と略称する)に関する。本発明による化合物およびこれらの化合物の共重合体は従来全く報告されていない新規な化合物である。
【0002】
【従来の技術】従来のサイズ剤はその使用により紙力強度が低下するものがほとんどであり、一部の表面サイズ剤は強度を向上させる能力を持つものが知られていたが、その効果については充分なものとは言えなかった。
【0003】
【発明が解決しようとする課題】本発明の目的は、新規なコハク酸ハーフエステル構造をもつ両親媒性アクリル酸エステル化合物(以下ASA−HAと略称する)あるいはコハク酸ハーフエステル構造をもつメタクリル酸エステル化合物(以下ASA−HMと略称する)および該化合物の共重合体を提供することである。さらには、ASA−HAあるいはASA−HMと(メタ)アクリルアミドを共重合することにより製造される、紙力強度を大幅に向上させる能力とサイズ性能を併せもつ、水に可溶あるいは分散可能な製紙用の添加剤に関する。
【0004】
【課題を解決するための手段】すなわち、本発明は、■ 式(1)または(2)〔化2〕で表される両親媒性化合物、
【0005】
【化2】

(式中、R1 は炭素数6〜48の直鎖状あるいは分岐状飽和炭化水素基、あるいは不飽和二重結合を1以上12以下含有する炭素数6〜48の直鎖状あるいは分岐状不飽和炭化水素基を表す。R2 は炭素数2〜6の直鎖状あるいは分岐状飽和炭化水素鎖を表し、R3 は水素原子またはメチル基を表す。Mは水素原子またはアルカリ金属、アルカリ土類金属、アンモニウム基、有機塩基を表す。)
■ ■記載の式(1)または(2)で表される両親媒性化合物からなる混合物、■ ■記載の式(1)または(2)で表される化合物またはそれらの混合物0.1〜90.0重量%と、共重合可能なビニル化合物10.0〜99.9重量%とを共重合することにより得られる、高分子化合物、■ ■記載の式(1)または(2)で表される化合物またはそれらの混合物0.1〜90.0重量%と、(メタ)アクリルアミド10.0〜99.9重量%とを共重合することにより得られる、水に可溶あるいは分散可能な共重合化合物、■ ■記載の水に可溶あるいは分散可能な共重合化合物を有効成分として含有する製紙用添加剤に関するものである。
【0006】
【発明の実施の形態】本発明のコハク酸ハーフエステル構造を持つ新規なビニル化合物は有機溶剤類に可溶な疎水性化合物であるが、分子内にカルボキシル基を持つため、pH、温度条件等により水溶性あるいは水分散性を示す両親媒性の化合物である。さらに、該化合物は分子内に二重結合を持つため、無溶剤系、水系あるいは有機溶剤系で種々のビニル化合物と重合可能であり、合成樹脂原料として有用な化合物である。
【0007】本発明の両親媒性化合物及びその共重合体の具体的な用途としては、可塑剤、耐熱性樹脂、潤滑剤、帯電防止剤、塗料、接着剤、分散剤、重合性界面活性剤、セメント用混和剤などへの利用が例示される。なかでも、本発明の両親媒性化合物と(メタ)アクリルアミドとの共重合体は水に可溶あるいは分散可能であり、紙力性能を大幅に向上させることができる新規のサイズ剤(製紙用添加剤)として利用価値が高いことが見いだされた。
【0008】本発明のASA−HAあるいはASA−HMは、エチレン、プロピレン、イソブテン、ブタジエン等から製造されるオレフィン類のオリゴマーと無水マレイン酸との反応により得られる化合物(以下ASAと略称する)を原料として、無溶剤系あるいは有機溶剤系でヒドロキシアルキルアクリレート(HA)あるいはヒドロキシアルキルメタクリレート(HM)と反応することにより製造できる。
【0009】本発明で使用されるASAは、(1)1−ヘキセン、1−オクテン、1−デセン、1−ドデセン、1−テトラデセン、1−ヘキサデセン、1−オクタデセン、1−ドコセンなどの炭素数が6〜48のα−オレフィン類あるいはそれらの混合物と無水マレイン酸との付加生成物、(2)炭素数が6〜48のα−オレフィン類あるいはそれらの混合物を触媒の存在下に異性化した内部オレフィンと無水マレイン酸との反応生成物、(3)炭素数が6〜48の直鎖状パラフィンあるいはその混合物を脱水素反応することにより得られる内部オレフィンと無水マレイン酸との反応生成物、(4)プロピレン、イソブテン、ブタジエンなどのオリゴマーで炭素数6〜48のものと無水マレイン酸との反応生成物等の公知技術により得られたもので、炭素数や、内部オレフィンの二重結合位置が異なるものの混合物であっても差し支えない。オレフィン類のオリゴマーの炭素数が6未満及び48を越える場合にはASA−HA及びASA−HMの両親媒的な性質が顕著ではなくなるため、本発明の目的には適合せず、あまり好ましくない。
【0010】本発明で使用するHAあるいはHMとしては、2−ヒドロキシエチルアクリレート、2−ヒドロキシエチルメタクリレート、2−ヒドロキシプロピルアクリレート、2−ヒドロキシプロピルメタクリレート、3−ヒドロキシプロピルアクリレート、3−ヒドロキシプロピルメタクリレート、2−ヒドロキシブチルアクリレート、2−ヒドロキシブチルメタクリレート、3−ヒドロキシブチルアクリレート、3−ヒドロキシブチルメタクリレート、4−ヒドロキシブチルアクリレート、4−ヒドロキシブチルメタクリレート、1−メチル−2−ヒドロキシプロピルアクリレート、1−メチル−2−ヒドロキシプロピルメタクリレート、2−メチル−2−ヒドロキシプロピルアクリレート、2−メチル−2−ヒドロキシプロピルメタクリレート、5−ヒドロキシペンチルアクリレート、5−ヒドロキシペンチルメタクリレート、1,2−ジメチル−2−ヒドロキシプロピルアクリレート、1,2−ジメチル−2−ヒドロキシプロピルメタクリレート、6−ヒドロキシヘキシルアクリレート、6−ヒドロキシヘキシルメタクリレート、1−メチル−4−ヒドロキシペンチルアクリレート、1−メチル−4−ヒドロキシペンチルメタクリレート、1,3−ジメチル−3−ヒドロキシブチルアクリレート、1,3−ジメチル−3−ヒドロキシブチルメタクリレート、1,1,2−トリメチル−2−ヒドロキシプロピルアクリレート、1,1,2−トリメチル−2−ヒドロキシプロピルメタクリレート、3−メチル−5−ヒドロキシペンチルアクリレート、3−メチル−5−ヒドロキシペンチルメタクリレートなどがあげられる。
【0011】ASAと上記HAあるいはHMとの反応は、通常はASAの有機溶剤溶液を撹拌しながら、HAあるいはHMを滴下して行われる。反応溶媒として利用可能な有機溶剤の例としてはASAとHA類をともに溶解する溶剤であればよく、アセトン、2−ブタノン、ベンゼン、トルエン、キシレン、ペンタン、ヘキサン、シクロヘキサン、DMF、DMSO、THF、ジエチルエーテル、ジオキサン、ジクロロメタン、ジクロロエタン、クロロホルムなどが例示される。メタノール、エタノール、イソプロパノール、メチルセロソルブ、エチルセロソルブ、2−エチルヘキサノール、シクロヘキサノールなどのアルコール系の溶剤は、コハク酸無水物との間でエステル化反応を生じるため好ましくない。
【0012】なお、炭素数が短いASAなどの常温で液状を示すASAに関しては、無溶剤系で反応することもできる。ASA−HAあるいはASA−HMを水系で利用する場合等のように、反応溶剤を除去する必要が生じるような場合には無溶剤系で反応するほうが好ましい。
【0013】反応は無触媒でも進行するが、反応を加速するために触媒を用いたほうが好ましい。本反応に使用する触媒については特に制限はなく、この種の反応に用いられている触媒を用いることができる。具体的には硫酸、塩酸、リン酸などの鉱酸類、あるいはこれらをシリカなどの無機担体に担持したもの、p−トルエンスルホン酸、メタンスルホン酸、ベンゼンスルホン酸等の有機酸類、酸性イオン交換樹脂等の固体酸類、その他塩化亜鉛、酢酸ナトリウム、ピリジンなどが例示され、これらの1種または2種以上を使用することができる。その使用量は用いる触媒により異なるので、一概に特定できないが、通常、原料のASAに対して0.001 重量%〜300 重量%、好ましくは0.01重量%〜30重量%の範囲である。
【0014】また、HA類の重合性が高いため、反応には重合禁止剤を用いる方が好ましい。重合禁止剤については特に制限はなく、HA類の重合禁止剤として用いることのできるものであればよい。具体的にはヒドロキノン、ヒドロキノンモノメチルエーテル、p-tert- ブチルカテコールなどのフェノール類;ニトロベンゾール、ニトロプロパンなどのニトロ化合物;p-フェニレンジアミン、N-ジフェニル-p-フェニレンジアミン、ジフェニルアミンなどのアミン類;ジフェニルピクリルヒドラジル、ガルビノキシル、フェルダジル、トリ-p- ニトロフェニルメチル、ジ-p- フルオロフェニルアミンなどの安定なラジカル類;亜硝酸ナトリウム、亜硝酸エチル、亜硝酸イソプロピルなどの亜硝酸化合物;その他硫黄、銅塩、チオ尿素化合物などがあげられ、これらの一種以上を使用することができる。その使用量は用いる重合禁止剤により異なるが、通常、原料のHA類に対して1ppm〜300重量%、好ましくは50ppm 〜5 重量%の範囲である。
【0015】HAあるいはHMの使用量は、ASAのコハク酸無水基に対して等モル量(すなわち、この場合酸無水物1モルに対し1モルのヒドロキシ基)を反応させる。等モル未満では未反応のASAが残存する。等モルを越えるとHA類が残存し、さらに触媒存在下では、HA類のヒドロキシ基がASA−HAあるいはASA−HMのカルボキシル基と反応してジエステル化合物をつくる可能性があるので好ましくない。
【0016】反応は常圧もしくは加圧下で、0℃〜150℃、好ましくは5℃〜130℃、さらに好ましくは10℃〜100℃の温度範囲で、30分〜20時間反応することで目的とするASA−HAあるいはASA−HMが高収率で得られる。反応中温度を一定に保つ必要はなく、反応速度を制御するあるいは反応液の粘度を調整するなどの目的で反応温度を変えても良い。
【0017】本発明の両親媒性化合物は、ASAの加水分解物であるコハク酸誘導体とHA、HMとのエステル化反応によっても製造可能であるが、ASAを原料とした方が反応性の面からより好ましい。
【0018】ASAは非対称化合物であるため、HA、HMとの反応物には置換基が結合している炭素側にエステルが結合している式(1)とその反対側にエステルが結合している式(2)が存在し、通常の反応条件ではそれらの混合物となる。エステルの位置異性体の存在は 1H−NMR及び13C−NMR分析法を用いると、対応する2種のカルボン酸エステル基が検出されることにより証明できる。HA、HMは置換基が結合していない炭素にエステル結合を形成する割合が高くなっており、その傾向は炭素数の多い置換基に顕著に認められる。これらの存在比は、ASAの置換基の鎖長や、反応溶媒、反応温度、反応濃度などの反応条件により決まるものと考えられるが、通常の使用目的では両者は分離することなく利用しても問題はない。
【0019】上記のASA−HA及びASA−HMと共重合可能なビニル化合物の例としては、芳香族ビニル化合物、シアン化ビニル化合物、ジエン化合物、不飽和カルボン酸エステル化合物、不飽和カルボン酸化合物、不飽和カルボン酸アミド化合物、アルキルビニルエーテル化合物、及びその他のビニル化合物からなる群より選択された一種以上の化合物である。
【0020】芳香族ビニル化合物としては、スチレン、α−メチルスチレン、α−クロルスチレン、p−tert−ブチルスチレン、p−メチルスチレン、p−クロルスチレン、o−クロルスチレン、2,5−ジクロルスチレン、3,4−ジクロルスチレン、ジビニルベンゼン等をあげることができる。
【0021】シアン化ビニル化合物としては、アクリロニトリル、メタクリロニトリル等をあげることができる。ジエン化合物としては、アレン、ブタジエン、イソプレン等のジオレフィン化合物および、クロロプレン等をあげることができる。
【0022】不飽和カルボン酸エステル化合物としては、メチルアクリレート、メチルメタクリレート、エチルアクリレート、エチルメタクリレート、プロピルアクリレート、プロピルメタクリレート、ブチルアクリレート、ブチルメタクリレート、2−エチルヘキシルアクリレート、2−エチルヘキシルメタクリレート、ラウリルアクリレート、ラウリルメタクリレート、ベンジルアクリレート、ベンジルメタクリレート、シクロヘキシルアクリレート、シクロヘキシルメタクリレート、グリシジルアクリレート、グリシジルメタクリレート、2−ヒドロキシエチルアクリレート、2−ヒドロキシエチルメタクリレート、3−ヒドロキシプロピルアクリレート、3−ヒドロキシプロピルメタクリレート、2−ヒドロキシプロピルアクリレート、2−ヒドロキシプロピルメタクリレート、ジメチルアミノエチルアクリレート、ジメチルアミノエチルメタクリレート、ジエチルアミノエチルアクリレート、ジエチルアミノエチルメタクリレート、エチレングリコールジアクリレート、エチレングリコールジメタクリレート、ジエチレングリコールジアクリレート、ジエチレングリコールジメタクリレート、トリエチレングリコールジアクリレート、トリエチレングリコールジメタクリレート、1,4−ブタンジオールジアクリレート、1,6−ヘキサンジオールアクリレート、ジメタクリル酸エチレングリコール、ジメタクリル酸トリエチレングリコール、ジメタクリル酸テトラエチレングリコール、ジメタクリル酸−1,3−ブチレングリコール、ポリエチレングリコール(メタ)アクリレート、メトキシポリエチレングリコール(メタ)アクリレート、エトキシポリエチレングリコール(メタ)アクリレート、プロポキシポリエチレングリコール(メタ)アクリレート、イソプロポキシポリエチレングリコール(メタ)アクリレート、フェノキシポリエチレングリコール(メタ)アクリレート、およびエポキシアクリレート類やウレタンアクリレート類のジビニル化合物等をあげることができる。
【0023】不飽和カルボン酸化合物としては、アクリル酸、メタクリル酸、クロトン酸、アンゲリカ酸、チグリン酸、2−ペンテン酸、β−メチルクロトン酸、β−メチルチグリン酸、α−メチル−2−ペンテン酸、β−メチル−2−ペンテン酸、マレイン酸、フマル酸、無水マレイン酸、イタコン酸、シトラコン酸、メサコン酸、グルタコン酸、α−ジヒドロムコン酸、2,3−ジメチルマレイン酸、2−メチルグルタコン酸、3−メチルグルタコン酸、2−メチル−α−ジヒドロムコン酸、2,3−ジメチル−α−ジヒドロムコン酸等の酸及びそれらのアルカリ金属塩、アンモニウム塩、有機アミン塩等をあげることができる。
【0024】不飽和カルボン酸アミド化合物としては、アクリルアミド、メタクリルアミド、ジアセトンアクリルアミド、N−メチルアクリルアミド、N−メチルメタクリルアミド、N,N−ジメチルアクリルアミド、N,N−ジメチルメタクリルアミド、N−エチルアクリルアミド、N−エチルメタクリルアミド、N,N−ジエチルアクリルアミド、N,N−ジエチルメタクリルアミド、N−プロピルアクリルアミド、N−アクリロイルピロリジン、N−アクリロイルピペリジン、N−アクリロイルモルホリン、N,N−ジ−n−プロピルアクリルアミド、N−n−ブチルアクリルアミド、N−n−ヘキシルアクリルアミド、N−n−ヘキシルメタクリルアミド、N−n−オクチルアクリルアミド、N−n−オクチルメタクリルアミド、N−tert−オクチルアクリルアミド、N−ドデシルアクリルアミド、N−n−ドデシルメタクリルアミド、N,N−ジグリシジルアクリルアミド、N,N−ジグリシジルメタクリルアミド、N−(4−グリシドキシブチル)アクリルアミド、N−(4−グリシドキシブチル)メタクリルアミド、N−(5−グリシドキシペンチル)アクリルアミド、N−(6−グリシドキシヘキシル)アクリルアミド、メチレンビスアクリルアミド、N,N’−エチレンビスアクリルアミド、N,N’−ヘキサメチレンビスアクリルアミド、N−メチロールアクリルアミド等をあげることができる。
【0025】アルキルビニルエーテル化合物としては、ビニルメチルエーテル、ビニルエチルエーテル、ビニルイソプロピルエーテル、ビニル−n−プロピルエーテル、ビニルイソブチルエーテル、ビニル−2−エチルヘキシルエーテル、ビニル−n−オクタデシルエーテル等をあげることができる。
【0026】その他のビニル化合物としては、酢酸ビニル、塩化ビニル、塩化ビニリデン、エチレン、プロピレン、ブテン、イソプレン、N−ビニル−2−ピロリドン、N−ビニルホルムアミド、N−ビニルアセトアミド、アジピン酸ジビニル、セバシン酸ジビニル等のジビニルエステル類、マレイミド、N−フェニルマレイミド、N−シクロヘキシルマレイミド、及びビニルスルホン酸、スチレンスルホン酸、2−アクリルアミド−2−フェニルプロパンスルホン酸、2−アクリルアミド−2−メチルプロパンスルホン酸等のスルホン酸及びそれらのアルカリ金属塩、アンモニウム塩、有機アミン塩等をあげることができる。
【0027】さらに、上記のビニル化合物以外にもアリルアミン、N−メチルアリルアミン、2−メチルアリルアミン、ジアリルアミン、ジメチルジアリルアンモニウムクロリドなどのアリルアミン類とそれらの塩、アリルスルホン酸、メタリルスルホン酸などのアリルスルホン酸類とそれらの塩、アリルアルコール、メタリルアルコール、ジアリルイソフタレート、ジアリルテレフタレート、ジエチレングリコールジアリルカーボネート、トリアリルシアヌレート等のようなアリル化合物を共重合することも可能である。
【0028】本発明のASA−HAまたはASA−HMと上記の共重合可能なビニル化合物の共重合比率は概ねASA−HAあるいはASA−HMが0.1 〜90.0重量%、共重合可能なビニル化合物が10.0〜99.9重量%の範囲にある。共重合可能なアリル化合物との共重合比率もビニル化合物の場合と同様であり、ビニル化合物とアリル化合物を組み合わせて使用しても差し支えない。
【0029】本発明のASA−HAまたはASA−HMと上記のビニル化合物の共重合方法に関しては特に制限はなく、公知の方法で共重合することができる。通常はラジカル重合開始剤の存在下、所定温度に保つことにより重合を行う。重合中同一温度に保つ必要はなく、重合の進行にともない適宜変えてよく、必要に応じて加熱あるいは除熱しながら行う。重合温度は使用するモノマーの種類や重合開始剤の種類などにより異なり、単一開始剤の場合には概ね30〜200℃の範囲であり、レドックス系重合開始剤の場合にはより低く、一括で重合を行う場合には概ね−5〜50℃であり、逐次添加する場合には概ね30〜90℃である。重合器内の雰囲気は特に限定はないが、重合を速やかに行わせるには窒素ガスのような不活性ガスで置換した方がよい。重合時間は特に限定はないが、概ね1〜40時間である。
【0030】重合溶媒としては上記のビニル化合物とASA−HAまたはASA−HMを均一に溶解するものであればよく、有機溶剤の例としては、ヘキサン、シクロヘキサン、デカリン、テトラリン、ジオキサン、四塩化炭素、トルエン、キシレン、クメン、エチルベンゼン、二硫化炭素、クロロホルム、酢酸エチル、酢酸、モルホリン、ベンゼン、テトラヒドロフラン、ピリジン、メチルエチルケトン、アセトン、メタノール、エタノール、プロパノール、ブタノール、メチルセロソルブ、エチルセロソルブ、ブチルセロソルブ、エチレングリコール等のアルコール類、ホルムアミド、ジメチルホルムアミド、ジメチルスルホキシドなどがあげられる。
【0031】ASA−HAあるいはASA−HMと相溶性のあるビニル化合物で、脱溶媒を必要とする用途については、プロセスを簡略化する目的で無溶剤系での共重合が好ましい場合もある。ASA−HAあるいはASA−HMは分子内のカルボキシル基をアルカリで中和すると水に可溶になる。水に可溶になるpHは置換基の鎖長などにより異なるが、例えば置換基の炭素数が16の場合ではpH8以上の条件で、水を溶媒とする均一重合が可能である。水に不溶なpH条件でも、界面活性剤の存在下で乳化重合することもできる。
【0032】重合開始剤としては一般の重合開始剤が使用できる。過酸化物系では、ベンゾイルパーオキサイド、ジクロルベンゾイルパーオキサイド、ジクミルパーオキサイド、ジ-tert-ブチルパーオキサイド、1,1,3,3,- テトラメチルブチルパーオキサイド、2,5-ジメチルヘキサン-2,5- ジハイドロパーオキサイド、クメンハイドロパーオキサイド、tert−ブチルパーベンゾエート、tert−ブチルパーアセテート、tert−ブチルパーフェニルアセテート、tert−ブチルパーオキシラウレート、クミルパービバレートまた、アゾ化合物としては、アゾビスイソブチロニトリル、2,2'- アゾビス(4-メトキシ-2,4- ジメチルバレロニトリル)、2,2'- アゾビス(2,4-ジメチルバレロニトリル)、2,2'- アゾビスイソブチロニトリル、1,1'- アゾビス(シクロヘキサン-1- カルボニトリル)、2-フェニルアゾ-4- メトキシ-2,4- ジメチルバレロニトリル、2,2'- アゾビス(2,4,4-トリメチルペンタン)、2,2'- アゾビス(2-メチルプロパン)、ジメチル2,2'- アゾビス(2-メチルプロピオネート)などを使用することができる。更に、上記した重合開始剤を2種以上併用することも可能である。
【0033】なお、水を溶媒とする場合の重合開始剤としては水溶性のものであれば特に制限はない。具体的には過酸化物系では、例えば過硫酸アンモニウム、過硫酸カリ、過酸化水素、tert−ブチルパーオキサイド等があげられる。この場合、単独でも使用できるが、還元剤と組み合わせてレドックス系重合開始剤としても使える。還元剤としては、例えば亜硫酸塩、亜硫酸水素塩、鉄、銅、コバルト等の低次のイオンの塩、次亜リン酸、次亜リン酸塩、N,N,N',N'-テトラメチルエチレンジアミン等の有機アミン、更にはアルドース、ケトース等の還元糖などをあげることができる。また、アゾ化合物としては、2,2'- アゾビス-2- アミジノプロパン塩酸塩、2,2'- アゾビス-2,4- ジメチルバレロニトリル、4,4'- アゾビス-4- シアノバレイン酸及びその塩などを使用することができる。更に上記した重合開始剤を2種以上併用してもよい。
【0034】重合開始剤の添加量は単量体に対して0.0001〜10重量%の範囲であり、好ましくは0.01〜8 重量%である。また、レドックス系の場合には、重合開始剤に対して還元剤の添加量はモル基準で0.1 〜100 %、好ましくは0.2 〜80%である。また、必要に応じてイソプロピルアルコール、α- チオグリセロール、メルカプトこはく酸、チオグリコール酸、トリエチルアミン、次亜りん酸ナトリウム等の連鎖移動剤を適宜使用することもできる。また、重合速度を調整するなどの目的で、エチレンジアミン4酢酸ナトリウム(EDTA−Na)やクエン酸、酒石酸、尿素、チオ尿素、L−アスコルビン酸、エチレントリチオカーボネート、フェノチアジン、ニコチン酸アミドなどの化合物を使用してもよい。連鎖移動剤や重合速度の調整剤などの使用量は、共重合体の使用目的に応じて異なるが、概ねモノマー全量に対して0.01ppm 〜5.0 %の範囲にある。
【0035】重合に供するモノマー類、重合開始剤、溶媒、連鎖移動剤などは重合を開始する時点で一度に反応容器に仕込んでもよいが、重合の進行に応じて、1種あるいはそれ以上の成分を、単独あるいは溶媒などに混合したものを逐次添加していってもよい。
【0036】かくして得られる本発明の高分子化合物は、可塑剤、耐熱性樹脂、帯電防止剤、潤滑剤、塗料、接着剤、分散剤、界面活性剤、セメント用混和剤などに利用される。その中でも、本発明の両親媒性化合物と(メタ)アクリルアミドとの共重合体は水に可溶あるいは分散可能であり、紙力性能を大幅に向上させることができる新規のPAM系サイズ剤として利用価値が高い。その作用については必ずしも明かとはなっていないが、塗工後乾燥過程で該共重合体のアミド基がセルロース繊維と水素結合を形成し、そのために紙力強度が大幅に向上し、それと同時に置換基が凝集して紙の表面側に配向することによりサイズ性能が発現されるものと考えられる。
【0037】具体的には、ASA−HAおよびASA−HMと(メタ)アクリルアミドの共重合体は、5〜30重量%濃度での25℃における粘度が、0.01〜500ポイズの範囲にある。本発明のPAM系サイズ剤(製紙用添加剤)は出発物質であるASAと異なり、それ自身で水分散性があるため、界面活性剤を使用して乳化する必要がなく、そのままの状態で利用できる。PAM系サイズ剤は紙の表面に塗工(外添)することにより、紙にサイズ性を付与し、紙力強度も大幅に向上する。紙に塗工する際の塗工液濃度は0.01〜10.0%、好ましくは0.10〜 8.0%の範囲にある。その塗工量は0.001 〜5.0g/m2 、好ましくは0.005 〜1.0g/m2 の範囲にある。
【0038】紙への塗工は、含浸、サイズプレス、ゲートロールコーター、カレンダー、ブレードコーター、スプレー等の一般的な方法が用いられる。塗工後の乾燥温度は水が蒸発する温度であればよく、好ましくは100℃から180℃の範囲にある。さらに本発明のPAM系サイズ剤は、従来より知られていた澱粉系、カルボキシメチルセルロース系、PVA系、PAM系等の表面塗工用の薬品類との組み合わせにより、表面強度や内部強度を一層向上させることもできる。
【0039】なお、ASA−HAあるいはASA−HMはカルボキシル基をもつアニオン性の疎水性モノマーであるためアクリルアミド系重合体(PAM)にアニオン性を付与する。従ってPAM系サイズ剤は、サイズ剤の歩留りを向上させる定着剤として広く利用されている硫酸アルミニウム、塩化アルミニウム、アルミン酸ナトリウムや、ポリエチレンイミン、ポリアクリルアミドのマンニッヒ変性物やホフマン変性物、ポリアルキレンポリアミン、カチオン化澱粉などのカチオン基を持つ水溶性高分子などとの相互作用によりパルプへの定着が可能であり、酸性抄紙用内添サイズ剤として利用できる。この場合、上記した共重合可能なビニル化合物の中で、アクリル酸、メタクリル酸、イタコン酸などの不飽和カルボン酸化合物あるいはビニルスルホン酸、スチレンスルホン酸、2−アクリルアミド−2−メチルプロパンスルホン酸などの不飽和スルホン酸化合物を共重合することにより同様の効果を高めることも可能である。
【0040】また、N,N−ジメチルアミノエチルアクリレート(DA)、N,N−ジメチルアミノエチルメタクリレート(DM)、N,N−ジメチルアミノプロピルアクリルアミド(DMAPAA)、N,N−ジメチルアミノプロピルメタクリルアミド(DMAPMA)、アリルアミン、ジアリルアミンなどの酸性〜弱酸性条件下でカチオン性を示すビニル化合物及びアリル化合物を共重合成分とすることにより、パルプへの定着性を一段と向上させることができる。
【0041】さらに、DA、DM、DMAPAA、DMAPMAなどをジメチル硫酸、メチルクロライドやメチルブロマイドなどのハロゲン化アルキル類、アリルクロライド、ベンジルクロライドやベンジルブロマイドなどのハロゲン化ベンジル類、エピクロヒドリンやエピブロモヒドリンなどのエピハロヒドリン類、プロピレンオキシドやスチレンオキシドなどのエポキシ類で四級化したビニル化合物や、ジメチルジアリルアンモニウムクロリドなどのアリル化合物を共重合成分とすると、中性〜弱アルカリ条件下でもパルプに定着できるようになり、中性抄紙用内添サイズ剤としての利用も可能になる。
【0042】このとき上記で例示したような硫酸アルミニウムをはじめとするサイズ剤の定着剤を併用してもよい。PAM系サイズ剤を内添サイズ剤として使用する場合には、パルプ重量に対して0.01〜4.0 重量%、好ましくは0.05〜2.0 重量%添加され、種箱やマシンチェストなどの通常の内添サイズ剤と同様の場所で添加すればよい。
【0043】本発明のPAM系サイズ剤は必要に応じて、消泡剤、防腐剤、防錆剤、防滑剤などを混合する、あるいは使用時に併用してもよい。
【0044】
【実施例】以下、実施例で本発明を詳細に説明するが、本発明はこれらの実施例に限定されるものではない。以下において%は重量基準であり、粘度は25℃においてB型粘度計により計測した値である。分子量はGPC分析法により、カラムはShodexOH-pak SB-80M +SB-804(昭和電工社製)、溶離液はNa2HPO4-KH2PO4(50mM)-NaNO3(0.1M)(pH6.5)を使用して測定を行った。NMR分析は試料を重水素化クロロホルムに約20%w/vの濃度になるように均一に溶かし、外径5mmφのNMRスペクトル測定用試料管に入れ、500MHzのNMRスペクトル測定装置A500(日本電子社製)を用いて 1H−および13C−NMRスペクトルを測定した。IR分析はKRS−5の窓板あるいはKBr錠剤法を用い、赤外線分析装置はFT/IR−8300(日本分光社製)を使用した。元素分析はCHN分析装置2400型(Perkin- Elmer 社製)を用いた。
【0045】(実施例1)撹拌機、還流冷却器、温度計、滴下ロートを取り付けた300ml の四つ口フラスコにASA(星光化学社製、C16タイプ、コロパールZ−100)100.0gと硫酸0.37g を入れ、撹拌しながら滴下ロートより2−ヒドロキシエチルメタクリレート(以下HEMAと略称する)40.4g とヒドロキノンモノメチルエーテル0.2gの混合液を30分で滴下した。滴下中反応温度は40℃になるように水浴で調整し、滴下終了後40℃で更に8時間撹拌を続け、トリエチルアミン0.73g を加えて硫酸を中和し、琥珀色の高粘性液体141.7gを得た。反応前のASAの粘度は96cpであったが、反応物(ASA−HEMA)の粘度は552cp であった。
【0046】元素分析値;C:68.99 %, H: 9.80 % (計算値:C26H44O6 )
C:68.65 %, H:10.02 % (実測値)
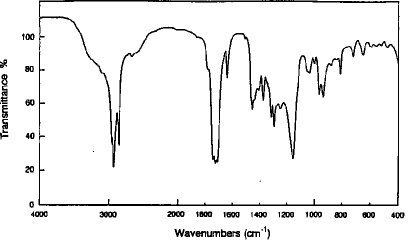
IR分析(図1)を行ったところ、原料ASAの1780cm-1および1860cm-1に認められる酸無水基の特性吸収帯(C =O 伸縮)が消失し、代って1710cm-1にカルボン酸(C =O 伸縮)、1740cm-1にエステル(C =O 伸縮)に由来する吸収帯が観測された。
【0047】図2および図3にASA−HEMAの 1H−NMRスペクトルおよび13C−NMRスペクトルを示した。横軸の磁場の強さはテトラメチルシランを基準(0ppm)としたppm単位で示した。
【0048】以下の実施例では、上記で得られたASA−HEMA20.0g 、40%苛性ソーダ水溶液4.4g、蒸留水175.6gを均一に溶解した水溶液(pH 10.62)を用いた。
【0049】(実施例2)撹拌機、還流冷却器および窒素導入管を取り付けた300ml の4つ口フラスコに実施例1で得られたASA−HEMAの10%水溶液15.0g 、50%アクリルアミド水溶液57.0g 、蒸留水221.4g、亜硫酸水素ナトリウム0.30g と次亜りん酸ナトリウム0.30g を加え、窒素気流下撹拌しながら30℃に加熱した。この溶液に、10%過硫酸アンモニウム(以下APS)水溶液6.0gを加えた。30℃で180 分間撹拌を続けた後、10%APS水溶液と10%亜硫酸水素ナトリウム水溶液をそれぞれ0.9gずつ加え、さらに120 分攪拌を続け、わずかに白く濁った水溶液を得た。得られた水溶液の不揮発分は10.8%、pHは8.43、粘度は176.2cp であり、重量平均分子量は418,600 であった。
【0050】(実施例3)撹拌機、還流冷却器および窒素導入管を取り付けた300ml の4つ口フラスコに実施例1で得られたASA−HEMAの10%水溶液30.0g 、50%アクリルアミド水溶液54.0g 、蒸留水209.1g、亜硫酸水素ナトリウム0.3gと次亜りん酸ナトリウム0.60g を加え、窒素気流下撹拌しながら30℃に加熱した。この溶液に10%APS水溶液6.0gを加えた。30℃で180 分間撹拌を続けた後、10%APS水溶液と10%亜硫酸水素ナトリウム水溶液をそれぞれ0.9gずつ加え、さらに120 分攪拌を続け、わずかに白く濁った水溶液を得た。得られた水溶液の不揮発分は10.9%、pHは8.64、粘度は448.0cp であり、重量平均分子量は186,100 であった。
【0051】(実施例4)撹拌機、還流冷却器および窒素導入管を取り付けた300ml の4つ口フラスコに実施例1で得られたASA−HEMAの10%水溶液45.0g 、50%アクリルアミド水溶液51.0g 、蒸留水196.2g、亜硫酸水素ナトリウム0.3gと次亜りん酸ナトリウム1.50g を加え、窒素気流下撹拌しながら30℃に加熱した。この溶液に10%APS水溶液6.0gを加えた。30℃で180 分間撹拌を続けた後、10%APS水溶液と10%亜硫酸水素ナトリウム水溶液をそれぞれ0.9gずつ加え、さらに120 分攪拌を続け、わずかに白く濁った水溶液を得た。得られた水溶液の不揮発分は11.1%、pHは8.78、粘度は65.9cpであり、重量平均分子量は85,400であった。
【0052】以下の塗工実施例は、何れも新聞用原紙(坪量50g/m2)を用いて行った。サイズ度はJIS P8122 のステキヒトサイズ試験法に準じて測定し、表面強度はRI−3型(明製作所社製)を用いてRIピックを(10点法の相対評価で点数が高いほど表面強度が高い)、Z軸強度はインターナルボンドテスター(熊谷理機工業社製)を用いて測定した。
【0053】(塗工実施例1〜3)実施例2〜4で得られた重合体溶液に被塗工原紙を1秒間浸漬し、2本のロールで搾った後に吸収された液量を秤量して塗工量を求めた。塗工量は重合体の不揮発分で 1.0g/m2となるように予め塗工液の濃度を調製した(重合体濃度:2.5wt %)。また、塗工液のpHは7.5 〜8.0 に調整した。塗工後直ちに表面温度を120℃に設定したドラムドライヤーで50秒間乾燥し、恒温恒湿室(20℃、湿度65%)中で24時間調湿後サイズ度と紙力強度を測定した。結果は表1に示した。
【0054】
【表1】

【0055】
【発明の効果】本発明のコハク酸ハーフエステル化合物は有機溶剤に可溶であるが、pHや温度条件等によっては水に対する溶解性にも優れた両親媒性化合物である。この化合物は分子内に重合可能な二重結合をもつため、重合性界面活性剤として種々の用途に利用できる。また、アクリルアミド系重合体の共重合成分として利用すると、実施例からも明らかなように紙力性能だけではなく、サイズ性能をもつ製紙用添加剤として有用である。
【図面の簡単な説明】
【図1】実施例1で得られた新規化合物の赤外線吸収スペクトル図
【図2】実施例1で得られた新規化合物の 1H−NMRスペクトル図
【図3】実施例1で得られた新規化合物の13C−NMRスペクトル図
【0001】
【発明が属する技術分野】本発明は、コハク酸ハーフエステル構造を持つ新規の両親媒性ビニル化合物に関し、さらにこれらの新規ビニル化合物と共重合可能なビニル化合物との共重合体、およびこれらの新規ビニル化合物と(メタ)アクリルアミドとの水に可溶あるいは分散可能な共重合体および該共重合体を有効成分として含有する製紙用添加剤(以下PAM系サイズ剤と略称する)に関する。本発明による化合物およびこれらの化合物の共重合体は従来全く報告されていない新規な化合物である。
【0002】
【従来の技術】従来のサイズ剤はその使用により紙力強度が低下するものがほとんどであり、一部の表面サイズ剤は強度を向上させる能力を持つものが知られていたが、その効果については充分なものとは言えなかった。
【0003】
【発明が解決しようとする課題】本発明の目的は、新規なコハク酸ハーフエステル構造をもつ両親媒性アクリル酸エステル化合物(以下ASA−HAと略称する)あるいはコハク酸ハーフエステル構造をもつメタクリル酸エステル化合物(以下ASA−HMと略称する)および該化合物の共重合体を提供することである。さらには、ASA−HAあるいはASA−HMと(メタ)アクリルアミドを共重合することにより製造される、紙力強度を大幅に向上させる能力とサイズ性能を併せもつ、水に可溶あるいは分散可能な製紙用の添加剤に関する。
【0004】
【課題を解決するための手段】すなわち、本発明は、
【0005】
【化2】

(式中、R1 は炭素数6〜48の直鎖状あるいは分岐状飽和炭化水素基、あるいは不飽和二重結合を1以上12以下含有する炭素数6〜48の直鎖状あるいは分岐状不飽和炭化水素基を表す。R2 は炭素数2〜6の直鎖状あるいは分岐状飽和炭化水素鎖を表し、R3 は水素原子またはメチル基を表す。Mは水素原子またはアルカリ金属、アルカリ土類金属、アンモニウム基、有機塩基を表す。)
【0006】
【発明の実施の形態】本発明のコハク酸ハーフエステル構造を持つ新規なビニル化合物は有機溶剤類に可溶な疎水性化合物であるが、分子内にカルボキシル基を持つため、pH、温度条件等により水溶性あるいは水分散性を示す両親媒性の化合物である。さらに、該化合物は分子内に二重結合を持つため、無溶剤系、水系あるいは有機溶剤系で種々のビニル化合物と重合可能であり、合成樹脂原料として有用な化合物である。
【0007】本発明の両親媒性化合物及びその共重合体の具体的な用途としては、可塑剤、耐熱性樹脂、潤滑剤、帯電防止剤、塗料、接着剤、分散剤、重合性界面活性剤、セメント用混和剤などへの利用が例示される。なかでも、本発明の両親媒性化合物と(メタ)アクリルアミドとの共重合体は水に可溶あるいは分散可能であり、紙力性能を大幅に向上させることができる新規のサイズ剤(製紙用添加剤)として利用価値が高いことが見いだされた。
【0008】本発明のASA−HAあるいはASA−HMは、エチレン、プロピレン、イソブテン、ブタジエン等から製造されるオレフィン類のオリゴマーと無水マレイン酸との反応により得られる化合物(以下ASAと略称する)を原料として、無溶剤系あるいは有機溶剤系でヒドロキシアルキルアクリレート(HA)あるいはヒドロキシアルキルメタクリレート(HM)と反応することにより製造できる。
【0009】本発明で使用されるASAは、(1)1−ヘキセン、1−オクテン、1−デセン、1−ドデセン、1−テトラデセン、1−ヘキサデセン、1−オクタデセン、1−ドコセンなどの炭素数が6〜48のα−オレフィン類あるいはそれらの混合物と無水マレイン酸との付加生成物、(2)炭素数が6〜48のα−オレフィン類あるいはそれらの混合物を触媒の存在下に異性化した内部オレフィンと無水マレイン酸との反応生成物、(3)炭素数が6〜48の直鎖状パラフィンあるいはその混合物を脱水素反応することにより得られる内部オレフィンと無水マレイン酸との反応生成物、(4)プロピレン、イソブテン、ブタジエンなどのオリゴマーで炭素数6〜48のものと無水マレイン酸との反応生成物等の公知技術により得られたもので、炭素数や、内部オレフィンの二重結合位置が異なるものの混合物であっても差し支えない。オレフィン類のオリゴマーの炭素数が6未満及び48を越える場合にはASA−HA及びASA−HMの両親媒的な性質が顕著ではなくなるため、本発明の目的には適合せず、あまり好ましくない。
【0010】本発明で使用するHAあるいはHMとしては、2−ヒドロキシエチルアクリレート、2−ヒドロキシエチルメタクリレート、2−ヒドロキシプロピルアクリレート、2−ヒドロキシプロピルメタクリレート、3−ヒドロキシプロピルアクリレート、3−ヒドロキシプロピルメタクリレート、2−ヒドロキシブチルアクリレート、2−ヒドロキシブチルメタクリレート、3−ヒドロキシブチルアクリレート、3−ヒドロキシブチルメタクリレート、4−ヒドロキシブチルアクリレート、4−ヒドロキシブチルメタクリレート、1−メチル−2−ヒドロキシプロピルアクリレート、1−メチル−2−ヒドロキシプロピルメタクリレート、2−メチル−2−ヒドロキシプロピルアクリレート、2−メチル−2−ヒドロキシプロピルメタクリレート、5−ヒドロキシペンチルアクリレート、5−ヒドロキシペンチルメタクリレート、1,2−ジメチル−2−ヒドロキシプロピルアクリレート、1,2−ジメチル−2−ヒドロキシプロピルメタクリレート、6−ヒドロキシヘキシルアクリレート、6−ヒドロキシヘキシルメタクリレート、1−メチル−4−ヒドロキシペンチルアクリレート、1−メチル−4−ヒドロキシペンチルメタクリレート、1,3−ジメチル−3−ヒドロキシブチルアクリレート、1,3−ジメチル−3−ヒドロキシブチルメタクリレート、1,1,2−トリメチル−2−ヒドロキシプロピルアクリレート、1,1,2−トリメチル−2−ヒドロキシプロピルメタクリレート、3−メチル−5−ヒドロキシペンチルアクリレート、3−メチル−5−ヒドロキシペンチルメタクリレートなどがあげられる。
【0011】ASAと上記HAあるいはHMとの反応は、通常はASAの有機溶剤溶液を撹拌しながら、HAあるいはHMを滴下して行われる。反応溶媒として利用可能な有機溶剤の例としてはASAとHA類をともに溶解する溶剤であればよく、アセトン、2−ブタノン、ベンゼン、トルエン、キシレン、ペンタン、ヘキサン、シクロヘキサン、DMF、DMSO、THF、ジエチルエーテル、ジオキサン、ジクロロメタン、ジクロロエタン、クロロホルムなどが例示される。メタノール、エタノール、イソプロパノール、メチルセロソルブ、エチルセロソルブ、2−エチルヘキサノール、シクロヘキサノールなどのアルコール系の溶剤は、コハク酸無水物との間でエステル化反応を生じるため好ましくない。
【0012】なお、炭素数が短いASAなどの常温で液状を示すASAに関しては、無溶剤系で反応することもできる。ASA−HAあるいはASA−HMを水系で利用する場合等のように、反応溶剤を除去する必要が生じるような場合には無溶剤系で反応するほうが好ましい。
【0013】反応は無触媒でも進行するが、反応を加速するために触媒を用いたほうが好ましい。本反応に使用する触媒については特に制限はなく、この種の反応に用いられている触媒を用いることができる。具体的には硫酸、塩酸、リン酸などの鉱酸類、あるいはこれらをシリカなどの無機担体に担持したもの、p−トルエンスルホン酸、メタンスルホン酸、ベンゼンスルホン酸等の有機酸類、酸性イオン交換樹脂等の固体酸類、その他塩化亜鉛、酢酸ナトリウム、ピリジンなどが例示され、これらの1種または2種以上を使用することができる。その使用量は用いる触媒により異なるので、一概に特定できないが、通常、原料のASAに対して0.001 重量%〜300 重量%、好ましくは0.01重量%〜30重量%の範囲である。
【0014】また、HA類の重合性が高いため、反応には重合禁止剤を用いる方が好ましい。重合禁止剤については特に制限はなく、HA類の重合禁止剤として用いることのできるものであればよい。具体的にはヒドロキノン、ヒドロキノンモノメチルエーテル、p-tert- ブチルカテコールなどのフェノール類;ニトロベンゾール、ニトロプロパンなどのニトロ化合物;p-フェニレンジアミン、N-ジフェニル-p-フェニレンジアミン、ジフェニルアミンなどのアミン類;ジフェニルピクリルヒドラジル、ガルビノキシル、フェルダジル、トリ-p- ニトロフェニルメチル、ジ-p- フルオロフェニルアミンなどの安定なラジカル類;亜硝酸ナトリウム、亜硝酸エチル、亜硝酸イソプロピルなどの亜硝酸化合物;その他硫黄、銅塩、チオ尿素化合物などがあげられ、これらの一種以上を使用することができる。その使用量は用いる重合禁止剤により異なるが、通常、原料のHA類に対して1ppm〜300重量%、好ましくは50ppm 〜5 重量%の範囲である。
【0015】HAあるいはHMの使用量は、ASAのコハク酸無水基に対して等モル量(すなわち、この場合酸無水物1モルに対し1モルのヒドロキシ基)を反応させる。等モル未満では未反応のASAが残存する。等モルを越えるとHA類が残存し、さらに触媒存在下では、HA類のヒドロキシ基がASA−HAあるいはASA−HMのカルボキシル基と反応してジエステル化合物をつくる可能性があるので好ましくない。
【0016】反応は常圧もしくは加圧下で、0℃〜150℃、好ましくは5℃〜130℃、さらに好ましくは10℃〜100℃の温度範囲で、30分〜20時間反応することで目的とするASA−HAあるいはASA−HMが高収率で得られる。反応中温度を一定に保つ必要はなく、反応速度を制御するあるいは反応液の粘度を調整するなどの目的で反応温度を変えても良い。
【0017】本発明の両親媒性化合物は、ASAの加水分解物であるコハク酸誘導体とHA、HMとのエステル化反応によっても製造可能であるが、ASAを原料とした方が反応性の面からより好ましい。
【0018】ASAは非対称化合物であるため、HA、HMとの反応物には置換基が結合している炭素側にエステルが結合している式(1)とその反対側にエステルが結合している式(2)が存在し、通常の反応条件ではそれらの混合物となる。エステルの位置異性体の存在は 1H−NMR及び13C−NMR分析法を用いると、対応する2種のカルボン酸エステル基が検出されることにより証明できる。HA、HMは置換基が結合していない炭素にエステル結合を形成する割合が高くなっており、その傾向は炭素数の多い置換基に顕著に認められる。これらの存在比は、ASAの置換基の鎖長や、反応溶媒、反応温度、反応濃度などの反応条件により決まるものと考えられるが、通常の使用目的では両者は分離することなく利用しても問題はない。
【0019】上記のASA−HA及びASA−HMと共重合可能なビニル化合物の例としては、芳香族ビニル化合物、シアン化ビニル化合物、ジエン化合物、不飽和カルボン酸エステル化合物、不飽和カルボン酸化合物、不飽和カルボン酸アミド化合物、アルキルビニルエーテル化合物、及びその他のビニル化合物からなる群より選択された一種以上の化合物である。
【0020】芳香族ビニル化合物としては、スチレン、α−メチルスチレン、α−クロルスチレン、p−tert−ブチルスチレン、p−メチルスチレン、p−クロルスチレン、o−クロルスチレン、2,5−ジクロルスチレン、3,4−ジクロルスチレン、ジビニルベンゼン等をあげることができる。
【0021】シアン化ビニル化合物としては、アクリロニトリル、メタクリロニトリル等をあげることができる。ジエン化合物としては、アレン、ブタジエン、イソプレン等のジオレフィン化合物および、クロロプレン等をあげることができる。
【0022】不飽和カルボン酸エステル化合物としては、メチルアクリレート、メチルメタクリレート、エチルアクリレート、エチルメタクリレート、プロピルアクリレート、プロピルメタクリレート、ブチルアクリレート、ブチルメタクリレート、2−エチルヘキシルアクリレート、2−エチルヘキシルメタクリレート、ラウリルアクリレート、ラウリルメタクリレート、ベンジルアクリレート、ベンジルメタクリレート、シクロヘキシルアクリレート、シクロヘキシルメタクリレート、グリシジルアクリレート、グリシジルメタクリレート、2−ヒドロキシエチルアクリレート、2−ヒドロキシエチルメタクリレート、3−ヒドロキシプロピルアクリレート、3−ヒドロキシプロピルメタクリレート、2−ヒドロキシプロピルアクリレート、2−ヒドロキシプロピルメタクリレート、ジメチルアミノエチルアクリレート、ジメチルアミノエチルメタクリレート、ジエチルアミノエチルアクリレート、ジエチルアミノエチルメタクリレート、エチレングリコールジアクリレート、エチレングリコールジメタクリレート、ジエチレングリコールジアクリレート、ジエチレングリコールジメタクリレート、トリエチレングリコールジアクリレート、トリエチレングリコールジメタクリレート、1,4−ブタンジオールジアクリレート、1,6−ヘキサンジオールアクリレート、ジメタクリル酸エチレングリコール、ジメタクリル酸トリエチレングリコール、ジメタクリル酸テトラエチレングリコール、ジメタクリル酸−1,3−ブチレングリコール、ポリエチレングリコール(メタ)アクリレート、メトキシポリエチレングリコール(メタ)アクリレート、エトキシポリエチレングリコール(メタ)アクリレート、プロポキシポリエチレングリコール(メタ)アクリレート、イソプロポキシポリエチレングリコール(メタ)アクリレート、フェノキシポリエチレングリコール(メタ)アクリレート、およびエポキシアクリレート類やウレタンアクリレート類のジビニル化合物等をあげることができる。
【0023】不飽和カルボン酸化合物としては、アクリル酸、メタクリル酸、クロトン酸、アンゲリカ酸、チグリン酸、2−ペンテン酸、β−メチルクロトン酸、β−メチルチグリン酸、α−メチル−2−ペンテン酸、β−メチル−2−ペンテン酸、マレイン酸、フマル酸、無水マレイン酸、イタコン酸、シトラコン酸、メサコン酸、グルタコン酸、α−ジヒドロムコン酸、2,3−ジメチルマレイン酸、2−メチルグルタコン酸、3−メチルグルタコン酸、2−メチル−α−ジヒドロムコン酸、2,3−ジメチル−α−ジヒドロムコン酸等の酸及びそれらのアルカリ金属塩、アンモニウム塩、有機アミン塩等をあげることができる。
【0024】不飽和カルボン酸アミド化合物としては、アクリルアミド、メタクリルアミド、ジアセトンアクリルアミド、N−メチルアクリルアミド、N−メチルメタクリルアミド、N,N−ジメチルアクリルアミド、N,N−ジメチルメタクリルアミド、N−エチルアクリルアミド、N−エチルメタクリルアミド、N,N−ジエチルアクリルアミド、N,N−ジエチルメタクリルアミド、N−プロピルアクリルアミド、N−アクリロイルピロリジン、N−アクリロイルピペリジン、N−アクリロイルモルホリン、N,N−ジ−n−プロピルアクリルアミド、N−n−ブチルアクリルアミド、N−n−ヘキシルアクリルアミド、N−n−ヘキシルメタクリルアミド、N−n−オクチルアクリルアミド、N−n−オクチルメタクリルアミド、N−tert−オクチルアクリルアミド、N−ドデシルアクリルアミド、N−n−ドデシルメタクリルアミド、N,N−ジグリシジルアクリルアミド、N,N−ジグリシジルメタクリルアミド、N−(4−グリシドキシブチル)アクリルアミド、N−(4−グリシドキシブチル)メタクリルアミド、N−(5−グリシドキシペンチル)アクリルアミド、N−(6−グリシドキシヘキシル)アクリルアミド、メチレンビスアクリルアミド、N,N’−エチレンビスアクリルアミド、N,N’−ヘキサメチレンビスアクリルアミド、N−メチロールアクリルアミド等をあげることができる。
【0025】アルキルビニルエーテル化合物としては、ビニルメチルエーテル、ビニルエチルエーテル、ビニルイソプロピルエーテル、ビニル−n−プロピルエーテル、ビニルイソブチルエーテル、ビニル−2−エチルヘキシルエーテル、ビニル−n−オクタデシルエーテル等をあげることができる。
【0026】その他のビニル化合物としては、酢酸ビニル、塩化ビニル、塩化ビニリデン、エチレン、プロピレン、ブテン、イソプレン、N−ビニル−2−ピロリドン、N−ビニルホルムアミド、N−ビニルアセトアミド、アジピン酸ジビニル、セバシン酸ジビニル等のジビニルエステル類、マレイミド、N−フェニルマレイミド、N−シクロヘキシルマレイミド、及びビニルスルホン酸、スチレンスルホン酸、2−アクリルアミド−2−フェニルプロパンスルホン酸、2−アクリルアミド−2−メチルプロパンスルホン酸等のスルホン酸及びそれらのアルカリ金属塩、アンモニウム塩、有機アミン塩等をあげることができる。
【0027】さらに、上記のビニル化合物以外にもアリルアミン、N−メチルアリルアミン、2−メチルアリルアミン、ジアリルアミン、ジメチルジアリルアンモニウムクロリドなどのアリルアミン類とそれらの塩、アリルスルホン酸、メタリルスルホン酸などのアリルスルホン酸類とそれらの塩、アリルアルコール、メタリルアルコール、ジアリルイソフタレート、ジアリルテレフタレート、ジエチレングリコールジアリルカーボネート、トリアリルシアヌレート等のようなアリル化合物を共重合することも可能である。
【0028】本発明のASA−HAまたはASA−HMと上記の共重合可能なビニル化合物の共重合比率は概ねASA−HAあるいはASA−HMが0.1 〜90.0重量%、共重合可能なビニル化合物が10.0〜99.9重量%の範囲にある。共重合可能なアリル化合物との共重合比率もビニル化合物の場合と同様であり、ビニル化合物とアリル化合物を組み合わせて使用しても差し支えない。
【0029】本発明のASA−HAまたはASA−HMと上記のビニル化合物の共重合方法に関しては特に制限はなく、公知の方法で共重合することができる。通常はラジカル重合開始剤の存在下、所定温度に保つことにより重合を行う。重合中同一温度に保つ必要はなく、重合の進行にともない適宜変えてよく、必要に応じて加熱あるいは除熱しながら行う。重合温度は使用するモノマーの種類や重合開始剤の種類などにより異なり、単一開始剤の場合には概ね30〜200℃の範囲であり、レドックス系重合開始剤の場合にはより低く、一括で重合を行う場合には概ね−5〜50℃であり、逐次添加する場合には概ね30〜90℃である。重合器内の雰囲気は特に限定はないが、重合を速やかに行わせるには窒素ガスのような不活性ガスで置換した方がよい。重合時間は特に限定はないが、概ね1〜40時間である。
【0030】重合溶媒としては上記のビニル化合物とASA−HAまたはASA−HMを均一に溶解するものであればよく、有機溶剤の例としては、ヘキサン、シクロヘキサン、デカリン、テトラリン、ジオキサン、四塩化炭素、トルエン、キシレン、クメン、エチルベンゼン、二硫化炭素、クロロホルム、酢酸エチル、酢酸、モルホリン、ベンゼン、テトラヒドロフラン、ピリジン、メチルエチルケトン、アセトン、メタノール、エタノール、プロパノール、ブタノール、メチルセロソルブ、エチルセロソルブ、ブチルセロソルブ、エチレングリコール等のアルコール類、ホルムアミド、ジメチルホルムアミド、ジメチルスルホキシドなどがあげられる。
【0031】ASA−HAあるいはASA−HMと相溶性のあるビニル化合物で、脱溶媒を必要とする用途については、プロセスを簡略化する目的で無溶剤系での共重合が好ましい場合もある。ASA−HAあるいはASA−HMは分子内のカルボキシル基をアルカリで中和すると水に可溶になる。水に可溶になるpHは置換基の鎖長などにより異なるが、例えば置換基の炭素数が16の場合ではpH8以上の条件で、水を溶媒とする均一重合が可能である。水に不溶なpH条件でも、界面活性剤の存在下で乳化重合することもできる。
【0032】重合開始剤としては一般の重合開始剤が使用できる。過酸化物系では、ベンゾイルパーオキサイド、ジクロルベンゾイルパーオキサイド、ジクミルパーオキサイド、ジ-tert-ブチルパーオキサイド、1,1,3,3,- テトラメチルブチルパーオキサイド、2,5-ジメチルヘキサン-2,5- ジハイドロパーオキサイド、クメンハイドロパーオキサイド、tert−ブチルパーベンゾエート、tert−ブチルパーアセテート、tert−ブチルパーフェニルアセテート、tert−ブチルパーオキシラウレート、クミルパービバレートまた、アゾ化合物としては、アゾビスイソブチロニトリル、2,2'- アゾビス(4-メトキシ-2,4- ジメチルバレロニトリル)、2,2'- アゾビス(2,4-ジメチルバレロニトリル)、2,2'- アゾビスイソブチロニトリル、1,1'- アゾビス(シクロヘキサン-1- カルボニトリル)、2-フェニルアゾ-4- メトキシ-2,4- ジメチルバレロニトリル、2,2'- アゾビス(2,4,4-トリメチルペンタン)、2,2'- アゾビス(2-メチルプロパン)、ジメチル2,2'- アゾビス(2-メチルプロピオネート)などを使用することができる。更に、上記した重合開始剤を2種以上併用することも可能である。
【0033】なお、水を溶媒とする場合の重合開始剤としては水溶性のものであれば特に制限はない。具体的には過酸化物系では、例えば過硫酸アンモニウム、過硫酸カリ、過酸化水素、tert−ブチルパーオキサイド等があげられる。この場合、単独でも使用できるが、還元剤と組み合わせてレドックス系重合開始剤としても使える。還元剤としては、例えば亜硫酸塩、亜硫酸水素塩、鉄、銅、コバルト等の低次のイオンの塩、次亜リン酸、次亜リン酸塩、N,N,N',N'-テトラメチルエチレンジアミン等の有機アミン、更にはアルドース、ケトース等の還元糖などをあげることができる。また、アゾ化合物としては、2,2'- アゾビス-2- アミジノプロパン塩酸塩、2,2'- アゾビス-2,4- ジメチルバレロニトリル、4,4'- アゾビス-4- シアノバレイン酸及びその塩などを使用することができる。更に上記した重合開始剤を2種以上併用してもよい。
【0034】重合開始剤の添加量は単量体に対して0.0001〜10重量%の範囲であり、好ましくは0.01〜8 重量%である。また、レドックス系の場合には、重合開始剤に対して還元剤の添加量はモル基準で0.1 〜100 %、好ましくは0.2 〜80%である。また、必要に応じてイソプロピルアルコール、α- チオグリセロール、メルカプトこはく酸、チオグリコール酸、トリエチルアミン、次亜りん酸ナトリウム等の連鎖移動剤を適宜使用することもできる。また、重合速度を調整するなどの目的で、エチレンジアミン4酢酸ナトリウム(EDTA−Na)やクエン酸、酒石酸、尿素、チオ尿素、L−アスコルビン酸、エチレントリチオカーボネート、フェノチアジン、ニコチン酸アミドなどの化合物を使用してもよい。連鎖移動剤や重合速度の調整剤などの使用量は、共重合体の使用目的に応じて異なるが、概ねモノマー全量に対して0.01ppm 〜5.0 %の範囲にある。
【0035】重合に供するモノマー類、重合開始剤、溶媒、連鎖移動剤などは重合を開始する時点で一度に反応容器に仕込んでもよいが、重合の進行に応じて、1種あるいはそれ以上の成分を、単独あるいは溶媒などに混合したものを逐次添加していってもよい。
【0036】かくして得られる本発明の高分子化合物は、可塑剤、耐熱性樹脂、帯電防止剤、潤滑剤、塗料、接着剤、分散剤、界面活性剤、セメント用混和剤などに利用される。その中でも、本発明の両親媒性化合物と(メタ)アクリルアミドとの共重合体は水に可溶あるいは分散可能であり、紙力性能を大幅に向上させることができる新規のPAM系サイズ剤として利用価値が高い。その作用については必ずしも明かとはなっていないが、塗工後乾燥過程で該共重合体のアミド基がセルロース繊維と水素結合を形成し、そのために紙力強度が大幅に向上し、それと同時に置換基が凝集して紙の表面側に配向することによりサイズ性能が発現されるものと考えられる。
【0037】具体的には、ASA−HAおよびASA−HMと(メタ)アクリルアミドの共重合体は、5〜30重量%濃度での25℃における粘度が、0.01〜500ポイズの範囲にある。本発明のPAM系サイズ剤(製紙用添加剤)は出発物質であるASAと異なり、それ自身で水分散性があるため、界面活性剤を使用して乳化する必要がなく、そのままの状態で利用できる。PAM系サイズ剤は紙の表面に塗工(外添)することにより、紙にサイズ性を付与し、紙力強度も大幅に向上する。紙に塗工する際の塗工液濃度は0.01〜10.0%、好ましくは0.10〜 8.0%の範囲にある。その塗工量は0.001 〜5.0g/m2 、好ましくは0.005 〜1.0g/m2 の範囲にある。
【0038】紙への塗工は、含浸、サイズプレス、ゲートロールコーター、カレンダー、ブレードコーター、スプレー等の一般的な方法が用いられる。塗工後の乾燥温度は水が蒸発する温度であればよく、好ましくは100℃から180℃の範囲にある。さらに本発明のPAM系サイズ剤は、従来より知られていた澱粉系、カルボキシメチルセルロース系、PVA系、PAM系等の表面塗工用の薬品類との組み合わせにより、表面強度や内部強度を一層向上させることもできる。
【0039】なお、ASA−HAあるいはASA−HMはカルボキシル基をもつアニオン性の疎水性モノマーであるためアクリルアミド系重合体(PAM)にアニオン性を付与する。従ってPAM系サイズ剤は、サイズ剤の歩留りを向上させる定着剤として広く利用されている硫酸アルミニウム、塩化アルミニウム、アルミン酸ナトリウムや、ポリエチレンイミン、ポリアクリルアミドのマンニッヒ変性物やホフマン変性物、ポリアルキレンポリアミン、カチオン化澱粉などのカチオン基を持つ水溶性高分子などとの相互作用によりパルプへの定着が可能であり、酸性抄紙用内添サイズ剤として利用できる。この場合、上記した共重合可能なビニル化合物の中で、アクリル酸、メタクリル酸、イタコン酸などの不飽和カルボン酸化合物あるいはビニルスルホン酸、スチレンスルホン酸、2−アクリルアミド−2−メチルプロパンスルホン酸などの不飽和スルホン酸化合物を共重合することにより同様の効果を高めることも可能である。
【0040】また、N,N−ジメチルアミノエチルアクリレート(DA)、N,N−ジメチルアミノエチルメタクリレート(DM)、N,N−ジメチルアミノプロピルアクリルアミド(DMAPAA)、N,N−ジメチルアミノプロピルメタクリルアミド(DMAPMA)、アリルアミン、ジアリルアミンなどの酸性〜弱酸性条件下でカチオン性を示すビニル化合物及びアリル化合物を共重合成分とすることにより、パルプへの定着性を一段と向上させることができる。
【0041】さらに、DA、DM、DMAPAA、DMAPMAなどをジメチル硫酸、メチルクロライドやメチルブロマイドなどのハロゲン化アルキル類、アリルクロライド、ベンジルクロライドやベンジルブロマイドなどのハロゲン化ベンジル類、エピクロヒドリンやエピブロモヒドリンなどのエピハロヒドリン類、プロピレンオキシドやスチレンオキシドなどのエポキシ類で四級化したビニル化合物や、ジメチルジアリルアンモニウムクロリドなどのアリル化合物を共重合成分とすると、中性〜弱アルカリ条件下でもパルプに定着できるようになり、中性抄紙用内添サイズ剤としての利用も可能になる。
【0042】このとき上記で例示したような硫酸アルミニウムをはじめとするサイズ剤の定着剤を併用してもよい。PAM系サイズ剤を内添サイズ剤として使用する場合には、パルプ重量に対して0.01〜4.0 重量%、好ましくは0.05〜2.0 重量%添加され、種箱やマシンチェストなどの通常の内添サイズ剤と同様の場所で添加すればよい。
【0043】本発明のPAM系サイズ剤は必要に応じて、消泡剤、防腐剤、防錆剤、防滑剤などを混合する、あるいは使用時に併用してもよい。
【0044】
【実施例】以下、実施例で本発明を詳細に説明するが、本発明はこれらの実施例に限定されるものではない。以下において%は重量基準であり、粘度は25℃においてB型粘度計により計測した値である。分子量はGPC分析法により、カラムはShodexOH-pak SB-80M +SB-804(昭和電工社製)、溶離液はNa2HPO4-KH2PO4(50mM)-NaNO3(0.1M)(pH6.5)を使用して測定を行った。NMR分析は試料を重水素化クロロホルムに約20%w/vの濃度になるように均一に溶かし、外径5mmφのNMRスペクトル測定用試料管に入れ、500MHzのNMRスペクトル測定装置A500(日本電子社製)を用いて 1H−および13C−NMRスペクトルを測定した。IR分析はKRS−5の窓板あるいはKBr錠剤法を用い、赤外線分析装置はFT/IR−8300(日本分光社製)を使用した。元素分析はCHN分析装置2400型(Perkin- Elmer 社製)を用いた。
【0045】(実施例1)撹拌機、還流冷却器、温度計、滴下ロートを取り付けた300ml の四つ口フラスコにASA(星光化学社製、C16タイプ、コロパールZ−100)100.0gと硫酸0.37g を入れ、撹拌しながら滴下ロートより2−ヒドロキシエチルメタクリレート(以下HEMAと略称する)40.4g とヒドロキノンモノメチルエーテル0.2gの混合液を30分で滴下した。滴下中反応温度は40℃になるように水浴で調整し、滴下終了後40℃で更に8時間撹拌を続け、トリエチルアミン0.73g を加えて硫酸を中和し、琥珀色の高粘性液体141.7gを得た。反応前のASAの粘度は96cpであったが、反応物(ASA−HEMA)の粘度は552cp であった。
【0046】元素分析値;C:68.99 %, H: 9.80 % (計算値:C26H44O6 )
C:68.65 %, H:10.02 % (実測値)
IR分析(図1)を行ったところ、原料ASAの1780cm-1および1860cm-1に認められる酸無水基の特性吸収帯(C =O 伸縮)が消失し、代って1710cm-1にカルボン酸(C =O 伸縮)、1740cm-1にエステル(C =O 伸縮)に由来する吸収帯が観測された。
【0047】図2および図3にASA−HEMAの 1H−NMRスペクトルおよび13C−NMRスペクトルを示した。横軸の磁場の強さはテトラメチルシランを基準(0ppm)としたppm単位で示した。
【0048】以下の実施例では、上記で得られたASA−HEMA20.0g 、40%苛性ソーダ水溶液4.4g、蒸留水175.6gを均一に溶解した水溶液(pH 10.62)を用いた。
【0049】(実施例2)撹拌機、還流冷却器および窒素導入管を取り付けた300ml の4つ口フラスコに実施例1で得られたASA−HEMAの10%水溶液15.0g 、50%アクリルアミド水溶液57.0g 、蒸留水221.4g、亜硫酸水素ナトリウム0.30g と次亜りん酸ナトリウム0.30g を加え、窒素気流下撹拌しながら30℃に加熱した。この溶液に、10%過硫酸アンモニウム(以下APS)水溶液6.0gを加えた。30℃で180 分間撹拌を続けた後、10%APS水溶液と10%亜硫酸水素ナトリウム水溶液をそれぞれ0.9gずつ加え、さらに120 分攪拌を続け、わずかに白く濁った水溶液を得た。得られた水溶液の不揮発分は10.8%、pHは8.43、粘度は176.2cp であり、重量平均分子量は418,600 であった。
【0050】(実施例3)撹拌機、還流冷却器および窒素導入管を取り付けた300ml の4つ口フラスコに実施例1で得られたASA−HEMAの10%水溶液30.0g 、50%アクリルアミド水溶液54.0g 、蒸留水209.1g、亜硫酸水素ナトリウム0.3gと次亜りん酸ナトリウム0.60g を加え、窒素気流下撹拌しながら30℃に加熱した。この溶液に10%APS水溶液6.0gを加えた。30℃で180 分間撹拌を続けた後、10%APS水溶液と10%亜硫酸水素ナトリウム水溶液をそれぞれ0.9gずつ加え、さらに120 分攪拌を続け、わずかに白く濁った水溶液を得た。得られた水溶液の不揮発分は10.9%、pHは8.64、粘度は448.0cp であり、重量平均分子量は186,100 であった。
【0051】(実施例4)撹拌機、還流冷却器および窒素導入管を取り付けた300ml の4つ口フラスコに実施例1で得られたASA−HEMAの10%水溶液45.0g 、50%アクリルアミド水溶液51.0g 、蒸留水196.2g、亜硫酸水素ナトリウム0.3gと次亜りん酸ナトリウム1.50g を加え、窒素気流下撹拌しながら30℃に加熱した。この溶液に10%APS水溶液6.0gを加えた。30℃で180 分間撹拌を続けた後、10%APS水溶液と10%亜硫酸水素ナトリウム水溶液をそれぞれ0.9gずつ加え、さらに120 分攪拌を続け、わずかに白く濁った水溶液を得た。得られた水溶液の不揮発分は11.1%、pHは8.78、粘度は65.9cpであり、重量平均分子量は85,400であった。
【0052】以下の塗工実施例は、何れも新聞用原紙(坪量50g/m2)を用いて行った。サイズ度はJIS P8122 のステキヒトサイズ試験法に準じて測定し、表面強度はRI−3型(明製作所社製)を用いてRIピックを(10点法の相対評価で点数が高いほど表面強度が高い)、Z軸強度はインターナルボンドテスター(熊谷理機工業社製)を用いて測定した。
【0053】(塗工実施例1〜3)実施例2〜4で得られた重合体溶液に被塗工原紙を1秒間浸漬し、2本のロールで搾った後に吸収された液量を秤量して塗工量を求めた。塗工量は重合体の不揮発分で 1.0g/m2となるように予め塗工液の濃度を調製した(重合体濃度:2.5wt %)。また、塗工液のpHは7.5 〜8.0 に調整した。塗工後直ちに表面温度を120℃に設定したドラムドライヤーで50秒間乾燥し、恒温恒湿室(20℃、湿度65%)中で24時間調湿後サイズ度と紙力強度を測定した。結果は表1に示した。
【0054】
【表1】

【0055】
【発明の効果】本発明のコハク酸ハーフエステル化合物は有機溶剤に可溶であるが、pHや温度条件等によっては水に対する溶解性にも優れた両親媒性化合物である。この化合物は分子内に重合可能な二重結合をもつため、重合性界面活性剤として種々の用途に利用できる。また、アクリルアミド系重合体の共重合成分として利用すると、実施例からも明らかなように紙力性能だけではなく、サイズ性能をもつ製紙用添加剤として有用である。
【図面の簡単な説明】
【図1】実施例1で得られた新規化合物の赤外線吸収スペクトル図
【図2】実施例1で得られた新規化合物の 1H−NMRスペクトル図
【図3】実施例1で得られた新規化合物の13C−NMRスペクトル図
【特許請求の範囲】
【請求項1】 式(1)または(2)〔化1〕で表される両親媒性化合物。
【化1】

(式中、R1 は炭素数6〜48の直鎖状あるいは分岐状飽和炭化水素基、あるいは不飽和二重結合を1以上12以下含有する炭素数6〜48の直鎖状あるいは分岐状不飽和炭化水素基を表す。R2 は炭素数2〜6の直鎖状あるいは分岐状飽和炭化水素鎖を表し、R3 は水素原子またはメチル基を表す。Mは水素原子またはアルカリ金属、アルカリ土類金属、アンモニウム基、有機塩基を表す。)
【請求項2】 請求項1記載の式(1)または(2)で表される両親媒性化合物からなる混合物。
【請求項3】 請求項1記載の式(1)または(2)で表される化合物またはそれらの混合物0.1 〜90.0重量%と、共重合可能なビニル化合物10.0〜99.9重量%とを共重合することにより得られる、高分子化合物。
【請求項4】 請求項1記載の式(1)または(2)で表される化合物またはそれらの混合物0.1 〜90.0重量%と、(メタ)アクリルアミド10.0〜99.9重量%とを共重合することにより得られる、水に可溶あるいは分散可能な共重合化合物。
【請求項5】 請求項4記載の水に可溶あるいは分散可能な共重合化合物を有効成分として含有する製紙用添加剤。
【請求項1】 式(1)または(2)〔化1〕で表される両親媒性化合物。
【化1】

(式中、R1 は炭素数6〜48の直鎖状あるいは分岐状飽和炭化水素基、あるいは不飽和二重結合を1以上12以下含有する炭素数6〜48の直鎖状あるいは分岐状不飽和炭化水素基を表す。R2 は炭素数2〜6の直鎖状あるいは分岐状飽和炭化水素鎖を表し、R3 は水素原子またはメチル基を表す。Mは水素原子またはアルカリ金属、アルカリ土類金属、アンモニウム基、有機塩基を表す。)
【請求項2】 請求項1記載の式(1)または(2)で表される両親媒性化合物からなる混合物。
【請求項3】 請求項1記載の式(1)または(2)で表される化合物またはそれらの混合物0.1 〜90.0重量%と、共重合可能なビニル化合物10.0〜99.9重量%とを共重合することにより得られる、高分子化合物。
【請求項4】 請求項1記載の式(1)または(2)で表される化合物またはそれらの混合物0.1 〜90.0重量%と、(メタ)アクリルアミド10.0〜99.9重量%とを共重合することにより得られる、水に可溶あるいは分散可能な共重合化合物。
【請求項5】 請求項4記載の水に可溶あるいは分散可能な共重合化合物を有効成分として含有する製紙用添加剤。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開平9−301926
【公開日】平成9年(1997)11月25日
【国際特許分類】
【出願番号】特願平8−121389
【出願日】平成8年(1996)5月16日
【出願人】(000003126)三井東圧化学株式会社 (49)
【公開日】平成9年(1997)11月25日
【国際特許分類】
【出願日】平成8年(1996)5月16日
【出願人】(000003126)三井東圧化学株式会社 (49)
[ Back to top ]

