並列反応用懸濁液、並列反応方法およびスクリーニング方法
【課題】 並列反応用の懸濁液、この懸濁液を用いた並列反応、更には並列反応を利用したスクリーンニング法を提供する。
【解決手段】
有機溶媒中に分散している低融点アガロースからなるゲル粒子は多糖鎖間の水素結合による網目構造を有し、その表面は半透膜で覆われている。この半透膜で覆われたゲル粒子内にはDNAと無細胞でタンパク質やペプチドの合成を行うための酵素が内包されている。これらDNA及び酵素は分子量が大きいため、半透膜を透過して外部に溶出しない。また、合成されたタンパク質、あるいはペプチドも分子量が大きいためゲル粒子内に保持される。
【解決手段】
有機溶媒中に分散している低融点アガロースからなるゲル粒子は多糖鎖間の水素結合による網目構造を有し、その表面は半透膜で覆われている。この半透膜で覆われたゲル粒子内にはDNAと無細胞でタンパク質やペプチドの合成を行うための酵素が内包されている。これらDNA及び酵素は分子量が大きいため、半透膜を透過して外部に溶出しない。また、合成されたタンパク質、あるいはペプチドも分子量が大きいためゲル粒子内に保持される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、多数のゲル粒子内で複数の化学反応、生化学反応を同時並行的に行うための懸濁液、この懸濁液を用いた並列反応方法およびこの並列反応を用いたスクリーニング方法に関する。
【背景技術】
【0002】
ランダムに変異が入った多くの候補タンパク質やペプチドの中から、目的の活性を有する酵素や生理活性ペプチドを探索したり、多くの候補物質の中から目的の活性を持つ触媒を探索する手法は、創薬や新規化学物質の探索においてしばしば用いられている。
例えば、非特許文献1には目的のタンパク質を発現する細胞をクローニングする際に、限界希釈法により1つの容器に1つの細胞が入る濃度から細胞を培養し、目的のタンパク質を発現するクローンを取得する方法が提案されている。
【0003】
また非特許文献2及び非特許文献3には、ある酵素の一部のアミノ酸をランダムに置換してライブラリーを作製し、このライブラリーから産業上有用な活性を有する酵素を探索することが開示されている。
【0004】
上記した手法では、一般的に96穴ウェルプレートなどの数百マイクロリットルから数ミリリットル程度の容積の反応器を使用している。
例えば、目的の細胞を含む細胞懸濁液を96穴ウェルプレートに分注し、抗体などを含む分析用試薬類を順次添加して細胞表面に発現した物質若しくは細胞から分泌される物質の量を定量したり、多様なアミノ酸置換を含む酵素を発現するライブラリーの中から活性の高い酵素を発現するクローンを選択する際に、96穴ウェルプレート等の反応器の中で酵素を発現させ、酵素の反応基質等を添加することにより酵素の活性を測定している。
つまり96穴ウェルプレート等を用いる場合には、多数の反応器(穴)に順次複数の試薬を分注する必要があり、分析対象となる酵素や細胞の数の増加に伴い必要となる反応器数が増大し、それに伴う溶液・試薬の分注操作が煩雑となる。
【0005】
非特許文献4には、半導体加工技術を利用して微小な反応容器を作製することが提案されているが、分注操作の問題は解消されていない。そこで、反応容器を更に小さくし且つ分注操作等も不要とする提案が特許文献1、2、3及び、非特許文献5、6に提案されている。
【0006】
特許文献1には、W/O型エマルションを構成する水滴中に、親水性分子と酵素などの機能性分子を別々に封じ込め、これら水滴を融合させることで、特異的な反応を誘導する内容が開示されている。また、この特許文献1には分子以外にDNAを封じ込めることも開示されている。
【0007】
特許文献2には、一方の荷電を有するベシクルに反応性物質を内包させ、他方の荷電を有するベシクルに前記反応性物質と反応する物質を内包させ、これら2つのベシクルを融合させ、融合した1つのベシクル内で反応を起こさせるようにしたことが開示されている。
【0008】
特許文献3には、エマルジョンの水相(水滴)内にPCR(ポリメラーゼ連鎖反応)用のプライマーが結合した固相担体を含ませ、水滴内でPCRを起こさせて固相担体に核酸複合体が連結させ、この後エマルジョンを破壊して固相担体−核酸複合体の結合体を回収し、この固相担体−核酸複合体を用いて無細胞タンパク質合成を行うことが開示されている。
【0009】
非特許文献5には、リン脂質二重層(リポソーム:Liposome)に目的とする分子を封じ込め、これらリン脂質二重層をレーザにより移動させて融合させる技術が開示されている。
【0010】
また非特許文献6には、ゲル粒子内でタンパク質合成反応を行わせるために、ゲル粒子表面の高分子皮膜を通してゲル粒子内に基質を供給する内容が開示されている。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】特開2000−271475号公報
【特許文献2】特開2008−29952号公報
【特許文献3】特開2009−178067号公報
【非特許文献】
【0012】
【非特許文献1】バイオ実験イラストレイテッド,6,128-130
【非特許文献2】AISTToday 5(4):18-19,2005
【非特許文献3】生化学,vol.72(12)pp.1430-1433,2000
【非特許文献4】Analytical Chemistry, vol.77(24)pp.8050-8056,2005
【非特許文献5】Nature Biotechnol.,16,652-656(1998)
【非特許文献6】Journal of Biotechnology, 143, 183-189(2000)
【発明の概要】
【発明が解決しようとする課題】
【0013】
特許文献1〜3或いは非特許文献5に開示されるような、ベシクル、エマルジョン或いはゲル粒子を反応容器とすることで、反応容器を小さくでき、多数の並列反応が可能になる。しかしながら、ゲル粒子などの微小容器内でタンパク質やペプチドの合成反応を起こさせ目的のタンパク質やペプチドを得たとしても、これらの物質が容易にゲル粒子などの微小反応容器から溶出してしまう問題がある。
【0014】
また、非特許文献6に開示されるようにゲル粒子表面を高分子皮膜で覆うことで、ゲル粒子内で合成されたタンパク質を内部に留めることが可能となる。しかしながら、非特許文献6にあってはゲル粒子に内包するDNAは一種類のみであり、異なる複数の合成反応を同時に行うものではない。
【課題を解決するための手段】
【0015】
上記課題を解決するため本発明は、ゲル粒子が分散した並列反応用懸濁液であって、このゲル粒子にはタンパク質合成酵素及びDNA(デオキシリボ核酸)が内包され、更にゲル粒子の表面は、ゲル粒子内へのタンパク質やペプチドの合成に必要な基質やエネルギー物質等の低分子の導入を許容するとともにゲル粒子内で合成されたタンパク質やペプチドの溶出を阻止する半透膜で覆われている。
ゲル粒子の大きさとしては、1〜500μmが適当であり、ゲル粒子の数としては、1016〜1012/mlが可能である。
【0016】
半透膜で覆われたゲル粒子を作製する方法としては、例えば、ゲル溶液とこれと反応して半透膜を形成する溶液とを隔壁を介して分離し、隔壁に形成した微細な穴からゲル溶液を微細な粒子として半透膜を形成する溶液中に押し出す方法、或いは細い流路を介してゲル溶液をこれと反応して半透膜を形成する溶液中に1粒ずつ送り出す方法などが適用される。
【0017】
このようにして作製したゲル粒子を基質やエネルギー物質等の低分子を含んだ溶液中に分散させることで懸濁液が得られる。基質としてはアミノ酸及び核酸、エネルギー物質はATP(アデノシン三リン酸)が考えられる。
【0018】
個々のゲル粒子内で異なる並列反応を同時に行わせるには、1つのゲル粒子中に1分子のDNAが含まれることが理想である。このためにはゲル粒子を作製する段階で、複数種のDNAを含む溶液を1つのゲル粒子に1分子のDNAが含まれる濃度まで限界希釈する。
【0019】
尚、実際には限界希釈しても1つのゲル粒子中に複数のDNA分子が包含されたり、1つのゲル粒子中に包含されるDNA分子がない場合も想定される。本発明における限界希釈の意味は、平均的に1つのゲル粒子に1つのDNAが包含される濃度である。
【0020】
このようにすることで、1つのゲル粒子で特定のタンパク質、あるいはペプチドのみが合成される。DNAがコードする目的物質としては、例えばプロテアーゼ、リパーゼ、アミラーゼ、セルラーゼ等の酵素タンパク質や蛍光タンパク質、あるいは、生理活性ペプチドが考えられる。
【0021】
前記ゲルとしては、アガロースやアルギン酸ナトリウムが挙げられ、前記半透膜としては、多価アニオンポリマーと多価カチオンポリマーによって構成されるポリイオンコンプレックス膜、例えば、Alg-PEI(アルギン酸−ポリエチレンイミン)が挙げられる。
【0022】
上記の懸濁液を用いた並列反応としては、懸濁液にタンパク質、およびペプチドの合成に必要な基質およびエネルギー物質を添加し、これら基質およびエネルギー物質をゲル粒子表面の半透膜を介してゲル粒子内に導入し、個々のゲル粒子中で個別の無細胞タンパク質合成反応を同時に並行して行う。
【0023】
また本発明に係るスクリーニング方法は、前記した並列反応に続いて、個々のゲル粒子内に包含されているタンパク質、あるいはペプチドの特性を検査し、目的の物質をコードするDNAを選別する。DNAの選別は例えば蛍光を発するゲル粒子を分取することで行う。また、分取の具体的な手段としては、フローサイトメトリーやマイクロマニュピュレータが挙げられる。
【発明の効果】
【0024】
本発明に係る並列反応用懸濁液を用いることで、例えば、1012〜1016個の反応を同時並列して行うことができる。
また、ゲル粒子からのDNAやタンパク質、ペプチドの溶出を防止し、ゲル粒子内での反応が効率よく行われ、且つ反応生成物であるタンパク質やペプチドの回収も効率よく行われる。
【図面の簡単な説明】
【0025】
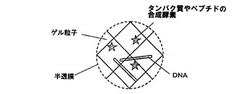
【図1】本発明に係る懸濁液中のゲル粒子の模式図
【図2】ゲル粒子にタンパク質やペプチドの無細胞合成に必要な物質の導入状態の模式図
【図3】ゲル粒子内でのタンパク質やペプチドの無細胞合成の模式図
【図4】半透膜で覆われたゲル粒子内での無細胞タンパク質合成。 (A)は基質を添加する前のゲル粒子の顕微鏡写真。 (B)は基質を添加する前のゲル粒子の蛍光顕微画像。 (C)はタンパク質合成後のゲル粒子の顕微鏡写真。 (D)はタンパク質合成後のゲル粒子の蛍光顕微画像。緑色蛍光タンパク質GFPの合成が蛍光として検出されている。
【図5】ゲル粒子内での一分子DNAからの無細胞タンパク質合成。 (A)は1分子のDNAが内包化されたゲル粒子の、タンパク質合成後の顕微鏡写真。 (B)は1分子のDNAが内包化されたゲル粒子の、タンパク質合成後の共焦点レーザ顕微鏡写真。矢印はDNAが内包化され、タンパク質合成反応によりGFPが合成されたゲル粒子を示している。GFPの合成は蛍光として検出されている。DNAが内包化されなかったゲル粒子は蛍光を有していない。
【発明を実施するための形態】
【0026】
図1に示すように、有機溶媒中に分散している低融点アガロースからなるゲル粒子は多糖鎖間の水素結合による網目構造を有し、その表面は半透膜で覆われている。この半透膜で覆われたゲル粒子内にはDNAと無細胞タンパク質合成を行うための酵素が内包されている。これらDNA及び酵素は分子量が大きいため、半透膜を透過して外部に溶出しない。
【0027】
上記の懸濁液を用いて、無細胞タンパク質合成、あるいは無細胞ペプチド合成を行うには、図1の状態の有機溶媒中に、タンパク質あるいはペプチドの合成に必要な物質、即ち、アミノ酸、核酸、ATP等を添加する。これらアミノ酸、核酸、ATPは低分子であるので、図2に示すように、ゲル粒子表面の半透膜を透過しゲル粒子内に侵入する。
【0028】
ゲル粒子内では、図3に示すようにタンパク質、あるいはペプチドの合成が行われる。具体的には、RNAポリメラーゼがDNAの二重螺旋の一部をほどいて塩基を剥き出しにし、剥き出しになった塩基を鋳型にしてmRNAが転写され、このmRNAの情報に基づいてtRNAが必要なアミノ酸を集めてリボソーム(ribosome)でタンパク質あるいはペプチドを合成する。そして、合成されたタンパク質やペプチドは半透膜を透過することができず、ゲル粒子内に保持される。
【0029】
以上が本発明に係る懸濁液中の1個のゲル粒子内の反応であるが、この懸濁液を用いた並列反応は、先ずDNAライブラリーを限界希釈し、ゲル粒子を作製する。希釈濃度およびゲル粒子の大きさは、ゲル粒子1つにDNAが1分子のみ入るようにする。現実にはゲル粒子の数は極めて多いため、すべてのゲル粒子にDNAが正確に1分子含まれる分けではなく、中にはDNAが入っていないものや複数入っているゲル粒子も存在するが、並列反応を行うには問題とならない。
【0030】
次いで、タンパク質、あるいはペプチドの合成に必要な物質をゲル粒子内に供給してゲル粒子内で無細胞合成を行い、目的とするタンパク質、あるいはペプチドが合成されているゲル粒子を他のゲル粒子と分けるため、FACS(登録商標)などのフローサイトメトリー(flow cytometory)を用いて分取する。具体的にはタンパク質、あるいはペプチドが内部で合成されているゲル粒子を1個ずつシース流に送り出し、流路の途中でレーザ光を照射する。目的のタンパク質、あるいはペプチドが内部で合成されているゲル粒子は蛍光抗体で染色され、他のゲルと区別されるので、そのゲル粒子を正に荷電し、下流側に負に荷電した偏向板によって他のゲルから分離して回収される。
【0031】
このようにして並行反応とスクリーニングを行うことで、目的のタンパク質、あるいはペプチドを合成するDNAを特定することができる。
【0032】
(実施例1)
1wt%アルギン酸ナトリウム、タンパク質合成酵素およびGFP(緑色蛍光タンパク質)の遺伝子をコードしたテンプレートDNA(30DNA分子/ゲル粒子)を含む水溶液を内水相として用いてW/O/W液滴を作製し、これを0.1mol/L塩化カルシウムおよび0.1wt% PEI(ポリエチレンイミン)を含む水溶液と混合することで、アルギン酸とPEIのポリイオンコンプレックスにより構成される半透膜で覆われたマイクロメートルサイズのゲル粒子を得た(図4A)。
遠心処理したサンプル25μLと、NTP・アミノ酸溶液25μLを混合し30℃で6時間インキュベートすることで、ゲル粒子内において無細胞タンパク質合成を行った。
この後、5℃で24時間静置した後、顕微鏡で観察した結果、ゲル粒子内から合成されたGFP由来の蛍光が検出することができた(図4B,4C)。
【0033】
(実施例2)
実施例1において、テンプレートDNAを1DNA分子/ゲル粒子の濃度になるよう限界希釈した点以外は実施例1と同様の操作を行い、個々のゲル粒子内で一分子のDNAからGFPの無細胞タンパク質合成を行った。顕微鏡で観察した結果、ゲル粒子内から合成されたGFP由来の蛍光が検出された(図5)。
【産業上の利用可能性】
【0034】
本発明に係る懸濁液は、多数の細胞の中から目的物質の分泌量の多い細胞を探索したり、ランダムに変異が入った多くの候補タンパク質、あるいはペプチドの中から目的とする活性を有する物質を探索する際の並列反応に利用できる。
【技術分野】
【0001】
本発明は、多数のゲル粒子内で複数の化学反応、生化学反応を同時並行的に行うための懸濁液、この懸濁液を用いた並列反応方法およびこの並列反応を用いたスクリーニング方法に関する。
【背景技術】
【0002】
ランダムに変異が入った多くの候補タンパク質やペプチドの中から、目的の活性を有する酵素や生理活性ペプチドを探索したり、多くの候補物質の中から目的の活性を持つ触媒を探索する手法は、創薬や新規化学物質の探索においてしばしば用いられている。
例えば、非特許文献1には目的のタンパク質を発現する細胞をクローニングする際に、限界希釈法により1つの容器に1つの細胞が入る濃度から細胞を培養し、目的のタンパク質を発現するクローンを取得する方法が提案されている。
【0003】
また非特許文献2及び非特許文献3には、ある酵素の一部のアミノ酸をランダムに置換してライブラリーを作製し、このライブラリーから産業上有用な活性を有する酵素を探索することが開示されている。
【0004】
上記した手法では、一般的に96穴ウェルプレートなどの数百マイクロリットルから数ミリリットル程度の容積の反応器を使用している。
例えば、目的の細胞を含む細胞懸濁液を96穴ウェルプレートに分注し、抗体などを含む分析用試薬類を順次添加して細胞表面に発現した物質若しくは細胞から分泌される物質の量を定量したり、多様なアミノ酸置換を含む酵素を発現するライブラリーの中から活性の高い酵素を発現するクローンを選択する際に、96穴ウェルプレート等の反応器の中で酵素を発現させ、酵素の反応基質等を添加することにより酵素の活性を測定している。
つまり96穴ウェルプレート等を用いる場合には、多数の反応器(穴)に順次複数の試薬を分注する必要があり、分析対象となる酵素や細胞の数の増加に伴い必要となる反応器数が増大し、それに伴う溶液・試薬の分注操作が煩雑となる。
【0005】
非特許文献4には、半導体加工技術を利用して微小な反応容器を作製することが提案されているが、分注操作の問題は解消されていない。そこで、反応容器を更に小さくし且つ分注操作等も不要とする提案が特許文献1、2、3及び、非特許文献5、6に提案されている。
【0006】
特許文献1には、W/O型エマルションを構成する水滴中に、親水性分子と酵素などの機能性分子を別々に封じ込め、これら水滴を融合させることで、特異的な反応を誘導する内容が開示されている。また、この特許文献1には分子以外にDNAを封じ込めることも開示されている。
【0007】
特許文献2には、一方の荷電を有するベシクルに反応性物質を内包させ、他方の荷電を有するベシクルに前記反応性物質と反応する物質を内包させ、これら2つのベシクルを融合させ、融合した1つのベシクル内で反応を起こさせるようにしたことが開示されている。
【0008】
特許文献3には、エマルジョンの水相(水滴)内にPCR(ポリメラーゼ連鎖反応)用のプライマーが結合した固相担体を含ませ、水滴内でPCRを起こさせて固相担体に核酸複合体が連結させ、この後エマルジョンを破壊して固相担体−核酸複合体の結合体を回収し、この固相担体−核酸複合体を用いて無細胞タンパク質合成を行うことが開示されている。
【0009】
非特許文献5には、リン脂質二重層(リポソーム:Liposome)に目的とする分子を封じ込め、これらリン脂質二重層をレーザにより移動させて融合させる技術が開示されている。
【0010】
また非特許文献6には、ゲル粒子内でタンパク質合成反応を行わせるために、ゲル粒子表面の高分子皮膜を通してゲル粒子内に基質を供給する内容が開示されている。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】特開2000−271475号公報
【特許文献2】特開2008−29952号公報
【特許文献3】特開2009−178067号公報
【非特許文献】
【0012】
【非特許文献1】バイオ実験イラストレイテッド,6,128-130
【非特許文献2】AISTToday 5(4):18-19,2005
【非特許文献3】生化学,vol.72(12)pp.1430-1433,2000
【非特許文献4】Analytical Chemistry, vol.77(24)pp.8050-8056,2005
【非特許文献5】Nature Biotechnol.,16,652-656(1998)
【非特許文献6】Journal of Biotechnology, 143, 183-189(2000)
【発明の概要】
【発明が解決しようとする課題】
【0013】
特許文献1〜3或いは非特許文献5に開示されるような、ベシクル、エマルジョン或いはゲル粒子を反応容器とすることで、反応容器を小さくでき、多数の並列反応が可能になる。しかしながら、ゲル粒子などの微小容器内でタンパク質やペプチドの合成反応を起こさせ目的のタンパク質やペプチドを得たとしても、これらの物質が容易にゲル粒子などの微小反応容器から溶出してしまう問題がある。
【0014】
また、非特許文献6に開示されるようにゲル粒子表面を高分子皮膜で覆うことで、ゲル粒子内で合成されたタンパク質を内部に留めることが可能となる。しかしながら、非特許文献6にあってはゲル粒子に内包するDNAは一種類のみであり、異なる複数の合成反応を同時に行うものではない。
【課題を解決するための手段】
【0015】
上記課題を解決するため本発明は、ゲル粒子が分散した並列反応用懸濁液であって、このゲル粒子にはタンパク質合成酵素及びDNA(デオキシリボ核酸)が内包され、更にゲル粒子の表面は、ゲル粒子内へのタンパク質やペプチドの合成に必要な基質やエネルギー物質等の低分子の導入を許容するとともにゲル粒子内で合成されたタンパク質やペプチドの溶出を阻止する半透膜で覆われている。
ゲル粒子の大きさとしては、1〜500μmが適当であり、ゲル粒子の数としては、1016〜1012/mlが可能である。
【0016】
半透膜で覆われたゲル粒子を作製する方法としては、例えば、ゲル溶液とこれと反応して半透膜を形成する溶液とを隔壁を介して分離し、隔壁に形成した微細な穴からゲル溶液を微細な粒子として半透膜を形成する溶液中に押し出す方法、或いは細い流路を介してゲル溶液をこれと反応して半透膜を形成する溶液中に1粒ずつ送り出す方法などが適用される。
【0017】
このようにして作製したゲル粒子を基質やエネルギー物質等の低分子を含んだ溶液中に分散させることで懸濁液が得られる。基質としてはアミノ酸及び核酸、エネルギー物質はATP(アデノシン三リン酸)が考えられる。
【0018】
個々のゲル粒子内で異なる並列反応を同時に行わせるには、1つのゲル粒子中に1分子のDNAが含まれることが理想である。このためにはゲル粒子を作製する段階で、複数種のDNAを含む溶液を1つのゲル粒子に1分子のDNAが含まれる濃度まで限界希釈する。
【0019】
尚、実際には限界希釈しても1つのゲル粒子中に複数のDNA分子が包含されたり、1つのゲル粒子中に包含されるDNA分子がない場合も想定される。本発明における限界希釈の意味は、平均的に1つのゲル粒子に1つのDNAが包含される濃度である。
【0020】
このようにすることで、1つのゲル粒子で特定のタンパク質、あるいはペプチドのみが合成される。DNAがコードする目的物質としては、例えばプロテアーゼ、リパーゼ、アミラーゼ、セルラーゼ等の酵素タンパク質や蛍光タンパク質、あるいは、生理活性ペプチドが考えられる。
【0021】
前記ゲルとしては、アガロースやアルギン酸ナトリウムが挙げられ、前記半透膜としては、多価アニオンポリマーと多価カチオンポリマーによって構成されるポリイオンコンプレックス膜、例えば、Alg-PEI(アルギン酸−ポリエチレンイミン)が挙げられる。
【0022】
上記の懸濁液を用いた並列反応としては、懸濁液にタンパク質、およびペプチドの合成に必要な基質およびエネルギー物質を添加し、これら基質およびエネルギー物質をゲル粒子表面の半透膜を介してゲル粒子内に導入し、個々のゲル粒子中で個別の無細胞タンパク質合成反応を同時に並行して行う。
【0023】
また本発明に係るスクリーニング方法は、前記した並列反応に続いて、個々のゲル粒子内に包含されているタンパク質、あるいはペプチドの特性を検査し、目的の物質をコードするDNAを選別する。DNAの選別は例えば蛍光を発するゲル粒子を分取することで行う。また、分取の具体的な手段としては、フローサイトメトリーやマイクロマニュピュレータが挙げられる。
【発明の効果】
【0024】
本発明に係る並列反応用懸濁液を用いることで、例えば、1012〜1016個の反応を同時並列して行うことができる。
また、ゲル粒子からのDNAやタンパク質、ペプチドの溶出を防止し、ゲル粒子内での反応が効率よく行われ、且つ反応生成物であるタンパク質やペプチドの回収も効率よく行われる。
【図面の簡単な説明】
【0025】
【図1】本発明に係る懸濁液中のゲル粒子の模式図
【図2】ゲル粒子にタンパク質やペプチドの無細胞合成に必要な物質の導入状態の模式図
【図3】ゲル粒子内でのタンパク質やペプチドの無細胞合成の模式図
【図4】半透膜で覆われたゲル粒子内での無細胞タンパク質合成。 (A)は基質を添加する前のゲル粒子の顕微鏡写真。 (B)は基質を添加する前のゲル粒子の蛍光顕微画像。 (C)はタンパク質合成後のゲル粒子の顕微鏡写真。 (D)はタンパク質合成後のゲル粒子の蛍光顕微画像。緑色蛍光タンパク質GFPの合成が蛍光として検出されている。
【図5】ゲル粒子内での一分子DNAからの無細胞タンパク質合成。 (A)は1分子のDNAが内包化されたゲル粒子の、タンパク質合成後の顕微鏡写真。 (B)は1分子のDNAが内包化されたゲル粒子の、タンパク質合成後の共焦点レーザ顕微鏡写真。矢印はDNAが内包化され、タンパク質合成反応によりGFPが合成されたゲル粒子を示している。GFPの合成は蛍光として検出されている。DNAが内包化されなかったゲル粒子は蛍光を有していない。
【発明を実施するための形態】
【0026】
図1に示すように、有機溶媒中に分散している低融点アガロースからなるゲル粒子は多糖鎖間の水素結合による網目構造を有し、その表面は半透膜で覆われている。この半透膜で覆われたゲル粒子内にはDNAと無細胞タンパク質合成を行うための酵素が内包されている。これらDNA及び酵素は分子量が大きいため、半透膜を透過して外部に溶出しない。
【0027】
上記の懸濁液を用いて、無細胞タンパク質合成、あるいは無細胞ペプチド合成を行うには、図1の状態の有機溶媒中に、タンパク質あるいはペプチドの合成に必要な物質、即ち、アミノ酸、核酸、ATP等を添加する。これらアミノ酸、核酸、ATPは低分子であるので、図2に示すように、ゲル粒子表面の半透膜を透過しゲル粒子内に侵入する。
【0028】
ゲル粒子内では、図3に示すようにタンパク質、あるいはペプチドの合成が行われる。具体的には、RNAポリメラーゼがDNAの二重螺旋の一部をほどいて塩基を剥き出しにし、剥き出しになった塩基を鋳型にしてmRNAが転写され、このmRNAの情報に基づいてtRNAが必要なアミノ酸を集めてリボソーム(ribosome)でタンパク質あるいはペプチドを合成する。そして、合成されたタンパク質やペプチドは半透膜を透過することができず、ゲル粒子内に保持される。
【0029】
以上が本発明に係る懸濁液中の1個のゲル粒子内の反応であるが、この懸濁液を用いた並列反応は、先ずDNAライブラリーを限界希釈し、ゲル粒子を作製する。希釈濃度およびゲル粒子の大きさは、ゲル粒子1つにDNAが1分子のみ入るようにする。現実にはゲル粒子の数は極めて多いため、すべてのゲル粒子にDNAが正確に1分子含まれる分けではなく、中にはDNAが入っていないものや複数入っているゲル粒子も存在するが、並列反応を行うには問題とならない。
【0030】
次いで、タンパク質、あるいはペプチドの合成に必要な物質をゲル粒子内に供給してゲル粒子内で無細胞合成を行い、目的とするタンパク質、あるいはペプチドが合成されているゲル粒子を他のゲル粒子と分けるため、FACS(登録商標)などのフローサイトメトリー(flow cytometory)を用いて分取する。具体的にはタンパク質、あるいはペプチドが内部で合成されているゲル粒子を1個ずつシース流に送り出し、流路の途中でレーザ光を照射する。目的のタンパク質、あるいはペプチドが内部で合成されているゲル粒子は蛍光抗体で染色され、他のゲルと区別されるので、そのゲル粒子を正に荷電し、下流側に負に荷電した偏向板によって他のゲルから分離して回収される。
【0031】
このようにして並行反応とスクリーニングを行うことで、目的のタンパク質、あるいはペプチドを合成するDNAを特定することができる。
【0032】
(実施例1)
1wt%アルギン酸ナトリウム、タンパク質合成酵素およびGFP(緑色蛍光タンパク質)の遺伝子をコードしたテンプレートDNA(30DNA分子/ゲル粒子)を含む水溶液を内水相として用いてW/O/W液滴を作製し、これを0.1mol/L塩化カルシウムおよび0.1wt% PEI(ポリエチレンイミン)を含む水溶液と混合することで、アルギン酸とPEIのポリイオンコンプレックスにより構成される半透膜で覆われたマイクロメートルサイズのゲル粒子を得た(図4A)。
遠心処理したサンプル25μLと、NTP・アミノ酸溶液25μLを混合し30℃で6時間インキュベートすることで、ゲル粒子内において無細胞タンパク質合成を行った。
この後、5℃で24時間静置した後、顕微鏡で観察した結果、ゲル粒子内から合成されたGFP由来の蛍光が検出することができた(図4B,4C)。
【0033】
(実施例2)
実施例1において、テンプレートDNAを1DNA分子/ゲル粒子の濃度になるよう限界希釈した点以外は実施例1と同様の操作を行い、個々のゲル粒子内で一分子のDNAからGFPの無細胞タンパク質合成を行った。顕微鏡で観察した結果、ゲル粒子内から合成されたGFP由来の蛍光が検出された(図5)。
【産業上の利用可能性】
【0034】
本発明に係る懸濁液は、多数の細胞の中から目的物質の分泌量の多い細胞を探索したり、ランダムに変異が入った多くの候補タンパク質、あるいはペプチドの中から目的とする活性を有する物質を探索する際の並列反応に利用できる。
【特許請求の範囲】
【請求項1】
ゲル粒子が分散した並列反応用懸濁液であって、このゲル粒子にはタンパク質合成酵素及びDNA(デオキシリボ核酸)が内包され、更にゲル粒子の表面は、ゲル粒子内へのタンパク質合成に必要な基質やエネルギー物質等の低分子の導入を許容するとともにゲル粒子内で合成されたタンパク質やペプチド等の目的物質の溶出を阻止する半透膜で覆われていることを特徴とする並列反応用懸濁液。
【請求項2】
請求項1に記載の並列反応用懸濁液において、前記懸濁液中に分散する個々のゲル粒子には平均1分子以下のDNAが内包されていることを特徴とする並列反応用懸濁液。
【請求項3】
請求項1に記載の並列反応用懸濁液において、前記半透膜は多価アニオンポリマーと多価カチオンポリマーによって構成されるポリイオンコンプレックス膜であることを特徴とする並列反応用懸濁液。
【請求項4】
請求項1に記載の並列反応用懸濁液において、前記ゲルはアガロースまたはアルギン酸ナトリウムによって構成されることを特徴とする並列反応用懸濁液。
【請求項5】
請求項1に記載の並列反応用懸濁液において、前記ゲル粒子の大きさは1〜500μmであることを特徴とする並列反応用懸濁液。
【請求項6】
請求項1乃至請求項5に記載の懸濁液にタンパク質やペプチドの合成に必要な基質およびエネルギー物質を添加し、これら基質およびエネルギー物質をゲル粒子表面の半透膜を介してゲル粒子内に導入し、個々のゲル粒子中で個別の無細胞合成反応を同時に並行して行うことを特徴とする並列反応方法。
【請求項7】
請求項6に記載の並列反応方法において、前記基質はアミノ酸と核酸であり、エネルギー物質はATP(アデノシン三リン酸)であることを特徴とする並列反応方法。
【請求項8】
請求項6または請求項7に記載した並列反応に続いて、個々のゲル粒子内に包含されているタンパク質、あるいはペプチドの特性を検査し、目的のタンパク質をコードするDNAを選別することを特徴とするスクリーニング方法。
【請求項9】
請求項8に記載のスクリーニング方法において、前記DNAの選別は蛍光を発するゲル粒子を分取することを特徴とするスクリーニング方法。
【請求項1】
ゲル粒子が分散した並列反応用懸濁液であって、このゲル粒子にはタンパク質合成酵素及びDNA(デオキシリボ核酸)が内包され、更にゲル粒子の表面は、ゲル粒子内へのタンパク質合成に必要な基質やエネルギー物質等の低分子の導入を許容するとともにゲル粒子内で合成されたタンパク質やペプチド等の目的物質の溶出を阻止する半透膜で覆われていることを特徴とする並列反応用懸濁液。
【請求項2】
請求項1に記載の並列反応用懸濁液において、前記懸濁液中に分散する個々のゲル粒子には平均1分子以下のDNAが内包されていることを特徴とする並列反応用懸濁液。
【請求項3】
請求項1に記載の並列反応用懸濁液において、前記半透膜は多価アニオンポリマーと多価カチオンポリマーによって構成されるポリイオンコンプレックス膜であることを特徴とする並列反応用懸濁液。
【請求項4】
請求項1に記載の並列反応用懸濁液において、前記ゲルはアガロースまたはアルギン酸ナトリウムによって構成されることを特徴とする並列反応用懸濁液。
【請求項5】
請求項1に記載の並列反応用懸濁液において、前記ゲル粒子の大きさは1〜500μmであることを特徴とする並列反応用懸濁液。
【請求項6】
請求項1乃至請求項5に記載の懸濁液にタンパク質やペプチドの合成に必要な基質およびエネルギー物質を添加し、これら基質およびエネルギー物質をゲル粒子表面の半透膜を介してゲル粒子内に導入し、個々のゲル粒子中で個別の無細胞合成反応を同時に並行して行うことを特徴とする並列反応方法。
【請求項7】
請求項6に記載の並列反応方法において、前記基質はアミノ酸と核酸であり、エネルギー物質はATP(アデノシン三リン酸)であることを特徴とする並列反応方法。
【請求項8】
請求項6または請求項7に記載した並列反応に続いて、個々のゲル粒子内に包含されているタンパク質、あるいはペプチドの特性を検査し、目的のタンパク質をコードするDNAを選別することを特徴とするスクリーニング方法。
【請求項9】
請求項8に記載のスクリーニング方法において、前記DNAの選別は蛍光を発するゲル粒子を分取することを特徴とするスクリーニング方法。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2012−170346(P2012−170346A)
【公開日】平成24年9月10日(2012.9.10)
【国際特許分類】
【出願番号】特願2011−32722(P2011−32722)
【出願日】平成23年2月18日(2011.2.18)
【出願人】(504171134)国立大学法人 筑波大学 (510)
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【Fターム(参考)】
【公開日】平成24年9月10日(2012.9.10)
【国際特許分類】
【出願日】平成23年2月18日(2011.2.18)
【出願人】(504171134)国立大学法人 筑波大学 (510)
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【Fターム(参考)】
[ Back to top ]

