乳酸エステルから酵素触媒を用いて乳酸の重合体を製造する方法
【課題】金属触媒を用いることなく、乳酸エステルの脱アルコールにより乳酸の重合体を得る乳酸重合体の製造方法を提供する。
【解決手段】乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。乳酸エステルは、乳酸と炭素数が4以上のアルコールとのエステルが好ましい。酵素として、カルボン酸エステル加水分解酵素、特にリパーゼ又はクチナーゼを用いることが好ましい。酵素として、固定化された酵素を用いることも好ましい。
【解決手段】乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。乳酸エステルは、乳酸と炭素数が4以上のアルコールとのエステルが好ましい。酵素として、カルボン酸エステル加水分解酵素、特にリパーゼ又はクチナーゼを用いることが好ましい。酵素として、固定化された酵素を用いることも好ましい。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、乳酸エステルから酵素触媒を用いて乳酸の重合体を製造する方法に関する。乳酸の重合体であるポリ乳酸は、植物等のバイオマスを原料とした生分解性プラスチック材料として注目されている。
【背景技術】
【0002】
ポリ乳酸の製造法としては、乳酸から乳酸の環状二量体であるラクチドを合成し、ラクチドの開環重合によってポリ乳酸を得る方法が知られている。この方法においては、例えば、まず、乳酸を減圧下(50〜30mmHg)加熱(135〜160℃)して乳酸オリゴマー(Mw:1170)を合成して、乳酸オリゴマーにスズ又はチタンなどの金属触媒を添加して、この混合物を減圧下(4〜5mmHg)加熱(190〜230℃)して、乳酸オリゴマーを解重合して、ラクチドを反応蒸発させる [Chem.Pharm.Bull., 47, 467-471 (1999)のExperimental] 。ラクチドを結晶化(例えば、特開平7−118259号公報、特開平7−138253号公報、特開平8−208638号公報)するか、又は精留(例えば、米国特許 5,142,023号明細書、米国特許 5,359,026号明細書)して、高純度ラクチドを得る。高純度ラクチドをスズやチタンなどの金属触媒を用いて開環重合して、ポリ乳酸を得る。
【0003】
また、ポリ乳酸の製造法として、最近、乳酸を直接脱水縮合する方法が開発されている。例えば、Polymer, 42, 5059-5062 (2001) には、乳酸を脱水して平均重合度8のオリゴ乳酸として、塩化スズ(II)及びp−トルエンスルホン酸触媒を用いて重縮合させてポリ乳酸を得ることが開示されている。
【0004】
上記従来の方法はいずれも、乳酸のフリー体を原料としており、且つスズ又はチタンなどの金属触媒を用いるものである。乳酸のフリー体は腐食性を有するので、工業化に際しては、反応容器や配管としては、耐食性の特殊材料から形成されたものか又は特殊材料でコーティングされたものを用いなければならない。このことは、ポリ乳酸の製造のコストアップに繋がる。そして、製造されたポリ乳酸中には金属触媒が残存している。金属触媒の残存は、ポリ乳酸の成形加工性に悪影響を与えるだけでなく、環境中に残存金属の拡散が起こる。
【0005】
ところで、バイオマスから乳酸を発酵法によって製造する方法は次の通りである。植物から得られるグルコース等の糖質を乳酸菌や、リゾプス等のカビ等の微生物を用いて乳酸発酵させて乳酸とする。この乳酸発酵の際には、生成した乳酸によって発酵液中のpHが低下すると微生物の活性が低下するので、水酸化カルシウム、炭酸カルシウム、水酸化ナトリウム、アンモニア等の塩基で中和しながら、発酵を進める。そのため、発酵法により得られる乳酸は、乳酸のカルシウム塩、ナトリウム塩、アンモニウム塩等の乳酸塩の形態である。
【0006】
水酸化カルシウム又は炭酸カルシウムを用いて中和を行うと、発酵液中において乳酸カルシウムが得られる。乳酸カルシウムの場合には、硫酸を用いて乳酸を遊離させ粗乳酸として、粗乳酸を目的に応じてエチル又はメチルエステル化し、乳酸エステルを蒸留する。蒸留された乳酸のエチル又はメチルエステルに水を加えて加水分解して乳酸に変換し、エチル又はメチルアルコールを蒸発させる。この方法は、工程が長い上に、多量の硫酸カルシウムが副生物として生産される。硫酸カルシウムは建材などとしての用途はあるが、副生物が多量に排出されるプロセスは好ましくない。
【0007】
アンモニア水を用いて中和を行うと、発酵液中において乳酸アンモニウムが得られる。特開平6−311886号公報には、アンモニアでの中和後の反応濃縮液にn−ブタノールを加え、ブタノールを還流させながらアンモニアを蒸発させ、乳酸ブチルを合成する。続いて、乳酸ブチルを蒸留し、得られた乳酸ブチルに水を添加して加水分解し、乳酸を得ることが開示されている。この方法では、蒸発捕集したアンモニアを再度、乳酸発酵の中和剤として利用できる。
【0008】
このように、バイオマスから乳酸を発酵法によって製造するに際しては、乳酸塩を乳酸のフリー体に変換するために別途の工程が必要である。このため、乳酸のフリー体を原料とする上述したラクチドの開環重合法や、乳酸の直接脱水縮合法では、ポリ乳酸の製造のさらなるコストアップに繋がる。
【0009】
また、ポリ乳酸の製造法として、乳酸エステルの脱アルコール縮合を行う方法が知られている。例えば、特開平7−173264号公報には、スズ等の金属触媒存在下で乳酸エステルを縮合し、ポリ乳酸を製造する方法が開示されている。特許3024907号公報には、スズ等の金属触媒存在下で乳酸エステルから生成するアルコールを除去しながら重縮合させ、ポリ乳酸を製造する方法が開示されている。特開平10−36366号公報には、乳酸エステルを合成し、乳酸エステルをスズ触媒存在下で脱アルコールして乳酸オリゴマーを合成し、続いてラクチドを合成する方法が開示されている。
【0010】
特開2002−300898号公報には、発酵により得られた乳酸アンモニウムから、乳酸エステルを経て重合物を得る方法が開示されている。
【0011】
いずれの方法においても、スズなどの金属触媒を用いる。製造されたポリ乳酸中には金属触媒が残存している。金属触媒の残存は、ポリ乳酸の成形加工性に悪影響を与えるだけでなく、環境中に残存金属の拡散が起こる。
【0012】
一方、World Journal of Microbiology & Biotechnology, 19, 859-865, (2003)には、リパーゼを触媒として乳酸を重合させたことが開示されている。
【0013】
Biotechnol. Prog., 22, 444-448 (2006) には、リパーゼを触媒として乳酸とブタノールとから乳酸ブチルを合成したことが開示されている。
【0014】
Chem. Lett., 1317-1318 (1999) には、リパーゼを触媒として環状ジエステルを開環重合させたことが開示されている。
【0015】
【非特許文献1】"Thermal Catalytic Depolymerization of Poly(L-Lactic Acid )Oligomer into LL-Lactide: Effects of Al, Ti, Zn and Zr Compounds as Catalysts", M. Noda and H. Okuyama, Chem. Pharm. Bull., 47, 467-471 (1999)
【非特許文献2】"Melt/solid polycondensation of L-lactic acid: an alternative route to poly(L-lactic acid) with high molecular weight", Y. Kimura et al., Polymer, 42, 5059-5062 (2001)
【非特許文献3】"Lipase-Catalysed polymerization of lactic acid and its film forming properties", S. Divakar et al., World Journal of Microbiology & Biotechnology, 19, 859-865, (2003)
【非特許文献4】"Lipase-Catalysed Transformations for the Synthesis of Butyl Lactate: A Comparison between Esterification and Transesterification", D. Pirozzi et al., Biotechnol. Prog., 22, 444-448 (2006)
【非特許文献5】"Lipase-Catalysed Ring-Opening Polymerization of Cyclic Diesters", S. Kobayashi et al., Chem. Lett., 1317-1318 (1999)
【特許文献1】特開平7−118259号公報
【特許文献2】特開平7−138253号公報
【特許文献3】特開平8−208638号公報
【特許文献4】米国特許 5,142,023号明細書
【特許文献5】米国特許 5,359,026号明細書
【特許文献6】特開平6−311886号公報
【特許文献7】特開平7−173264号公報
【特許文献8】特許3024907号公報
【特許文献9】特開平10−36366号公報
【特許文献10】特開2002−300898号公報
【発明の開示】
【発明が解決しようとする課題】
【0016】
バイオマスを出発原料とするポリ乳酸の製造を考えると、従来の方法では、上述のように、まず、バイオマスから乳酸を発酵法によって製造するに際して、乳酸塩を乳酸のフリー体に変換する工程が必要であり、ポリ乳酸製造の原料である乳酸のコストが高い。そして、乳酸のフリー体は腐食性を有するので、製造設備には耐食性の特殊材料を用いなければならず、ポリ乳酸製造のコストが高くなる。さらに、ポリ乳酸製造において金属触媒を用いるので、製造されたポリ乳酸中には金属触媒が残存しており、そのため、残存金属触媒がポリ乳酸の成形加工性に悪影響を与え、環境中に残存金属の拡散が起こる。
【0017】
本発明の目的は、上記従来技術の問題点を解決し、金属触媒を用いることなく、乳酸エステルの脱アルコールにより乳酸の重合体を得る乳酸重合体の製造方法を提供することにある。
【課題を解決するための手段】
【0018】
本発明には以下の発明が含まれる。
(1) 乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。
【0019】
(2) 乳酸エステルは、乳酸と炭素数が4以上のアルコールとのエステルである、上記(1)に記載の乳酸重合体の製造方法。
【0020】
(3) 乳酸エステルは、D−乳酸エステル、L−乳酸エステル、又はDL−乳酸エステルである、上記(1)又は(2)に記載の乳酸重合体の製造方法。
【0021】
(4) 脱アルコール反応を加熱条件及び/又は減圧条件で行う、上記(1)〜(3)のうちのいずれかに記載の乳酸重合体の製造方法。
【0022】
(5) 酵素として、カルボン酸エステル加水分解酵素を用いる、上記(1)〜(4)のうちのいずれかに記載の乳酸重合体の製造方法。
【0023】
(6) 酵素として、リパーゼ又はクチナーゼを用いる、上記(1)〜(4)のうちのいずれかに記載の乳酸重合体の製造方法。
【0024】
(7) 酵素として、固定化された酵素を用いる、上記(1)〜(6)のうちのいずれかに記載の乳酸重合体の製造方法。
【0025】
(8) 乳酸発酵で得られた乳酸アンモニウムとアルコールとを反応させ、乳酸エステルを合成し、
得られた乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。
【0026】
(9) 乳酸の重合体を光学選択的に得る、上記(1)〜(8)のうちのいずれかに記載の乳酸重合体の製造方法。
【発明の効果】
【0027】
本発明によれば、乳酸エステルを酵素触媒の存在下で脱アルコール縮合反応させ、乳酸の重合体を得る。酵素を触媒として用いるので、反応条件は温和であり製造上好ましい。得られる乳酸重合体には、金属触媒の残存はない。従って、乳酸重合体の成形加工性は良好であり、環境中への金属の拡散汚染は起こらない。
【0028】
本発明で用いる乳酸エステルは、バイオマスから乳酸を発酵法によって製造する際の中間製品として得ることができる。従って、乳酸塩を乳酸のフリー体に変換する別途の工程を行う必要がないので、乳酸を原料とする方法に比べて大幅な工程短縮が図られ、コストダウンが得られる。しかも、腐食性の乳酸を用いないので、製造設備の観点からもコストダウンが得られる。
【0029】
さらに、本発明によれば、光学選択的に乳酸の重合体を得ることができ、高い結晶性を有する乳酸重合体を得ることができる。
【発明を実施するための最良の形態】
【0030】
本発明において、乳酸エステルを酵素触媒の存在下で脱アルコール縮合反応させ、乳酸の重合体を得る。乳酸エステルとして、化学合成された乳酸を原料として合成されたものを用いてもよく、又はバイオマスから乳酸を発酵法によって製造する際の乳酸アンモニウムから合成されたものを用いてもよい。
【0031】
乳酸発酵はよく知られている。植物から得られる糖質、例えば、トウモロコシ、米、キャッサバなどのデンプンを加水分解して得られたグルコース、セルロースを硫酸や加圧熱水で加水分解して得られたグルコース; サトウキビやビートから得られたシュークロース; ヘミセルロースから得られたキシロース、アラビノース等の糖質を、乳酸菌や、リゾプス等のカビ等の微生物を用いて乳酸発酵させる。この乳酸発酵液のpHが低下すると微生物の活性が低下するので、アンモニア水又はアンモニアで中和しながら、発酵を進めると、乳酸アンモニウムが得られる。
【0032】
乳酸アンモニウムにアルコールを反応させると、乳酸とアルコールとのエステルが得られる。この際に用いるアルコールは特に限定されないが、炭素数が4以上のアルコールが好ましい。エタノールを用いると、エタノールの常圧での沸点が78℃と低いため反応温度を高くすることができず、乳酸アンモニウムとエタノールとの反応性は低く収率も低い。このため、エタノールを用いると、加圧条件下での反応が必要となる。炭素数が4以上のアルコールとしては、例えば、次の段落で挙げられているものを用いるとよい。
【0033】
本発明においては、乳酸エステルとして、乳酸と炭素数が4以上のアルコールとのエステルを用いることが好ましい。炭素数が4以上のアルコールとの乳酸エステルは、アルコール由来部分が疎水的であり、疎水性酵素触媒存在下での脱アルコール反応が起こりやすい。乳酸エステルとして、乳酸と炭素数が4以上12以下のアルコールとのエステルがより好ましく、このようなアルコールとしては、直鎖状又は分枝状であってもよく、ブタノール、ペンタノール、ヘキサノール、ヘプタノール、オクタノール、2−エチルヘキサノール、ノナノール、デカノール、ウンデカノール、ドデカノール等の一価アルコールが挙げられる。乳酸と炭素数が4以上6以下のアルコールとのエステル、すなわち、乳酸ブチル、乳酸ペンチル、乳酸ヘキシルがより好ましい。また、1,4−ブタンジオール、1,5−ペンタンジオール、1,6−ヘキサンジオール等の二価アルコールとのジエステルの使用も考えられる。
【0034】
また、乳酸エステルは、D−乳酸エステル、L−乳酸エステル、又はDL−乳酸エステルのいずれであってもよい。製造されるべき乳酸重合体の目的に応じて、適宜選択するとよい。
【0035】
触媒として用いる酵素としては、カルボン酸エステル加水分解酵素(EC3.1.1)が好ましい。カルボン酸エステル加水分解酵素(EC3.1.1)はエステラーゼ(EC3.1)の一種である。カルボン酸エステル加水分解酵素のなかでも、リパーゼ(EC3.1.1.3)が特に好適である。またクチナーゼ(EC3.1.1)も好適である。
【0036】
酵素を分離する微生物は特に限定されず、例えば、リパーゼに関しては、カンジダ アンタルチカ (Candida antartica)、カンジダ ルゴサ(Candida rugosa)、クリプトコッカス エスピー(Cryptococcus sp.)、プシュードモナス フルオレッセンス (Pseudomonas fluorescens)、プシュードモナス セパシア (Pseudomonas cepacia)、ブルコルデリア セパシア(Burkholderia cepacia)、アスペルギラス ナイガー (Aspergillus niger)、アスペルギラス オリザエ(Aspergillus oryzae)、ムコール ジャバニカス (Mucor javanicus)、ペニシリウム カメムベルチ(Penicillium camemberti)、リゾプス オリザエ (Rhizopus oryzae)、リゾプス デレマー(Rhizopus delemar)、ペニシリウム ロクエホルチ(Penicillium roqueforti)、リゾムコール ミエヘイ (Rhizomucor miehei)、リゾプス ジャポニカス(Rhizopus japonicus)、バチルス エスピー(Bacillus sp.)、カンジダ シリンドラシア(Candida cylindracea) などを給源とする微生物リパーゼを利用することができる。また、ブタ、ウシ、ラット等の動物を給源とする動物リパーゼ、ヒマシ、米ぬか、小麦、ダイズ、トウモロコシ等の植物を給源とする植物リパーゼを利用することもできる。これらに限定されることなく、乳酸エステルの脱アルコール縮合反応を触媒する機能を有する酵素を用いることができる。
【0037】
また、本発明において、固定化された酵素を用いてもよい。固定化酵素は、繰り返し使用できる点や、生成した乳酸重合体との分離が容易である点において好ましい。固定化担体としては、公知の各種のものを用いるとよく、例えば、アクリルアミド、セルロース、ビーズ、セラミック等が挙げられる。市販の固定化酵素としては、例えば、カンジダ アンタルチカ (Candida antartica)由来のリパーゼをポリアクリルアミドに固定化したノボノルディスク社のノボザイム435、ブルコルデリア セパシア(Burkholderia cepacia)由来のリパーゼをセラミックに固定化した天野エンザイム社のリパーゼPS−C「アマノ」I等が挙げられる。
【0038】
乳酸エステルの脱アルコール縮合反応は、乳酸エステルと酵素とを混合し、適切な反応温度、適切な減圧条件にて行うとよい。反応温度は、用いる酵素の至適温度により定められる。減圧は縮合により生成したアルコールを反応系外へ除去するために行う。すなわち、減圧度は、当該温度で除去しようとするアルコールの蒸気圧以下かつ基質である乳酸エステルの蒸気圧以上とする必要があり、通常は、当該温度で除去しようとするアルコールの蒸気圧よりも低い圧力かつ基質である乳酸エステルの蒸気圧よりも高い圧力とする。具体的には、加熱温度としては、用いる酵素の至適温度を考慮して、例えば60〜90℃程度、減圧度としては、乳酸ブチルの脱ブタノール縮合反応の場合、例えば5〜80mmHg程度とするとよい。反応時間は、特に限定されることはなく、重縮合の進行を考慮して定めるとよい。例えば30分間〜72時間、2時間〜48時間。もちろん、これらよりも長い反応時間としてもよい。
【0039】
用いる酵素の量は特に限定されるものではないが、乳酸エステルの100質量部に対して、例えば5〜200質量部、好ましくは10〜120質量部程度とするとよい。用いる酵素の触媒活性や、乳酸エステル中のアルキル基の長さ等を考慮して、適宜定めるとよい。
【0040】
乳酸エステルの脱アルコール縮合反応における酵素の触媒作用については、次のように考えられる。酵素中に含まれているセリン残基(Ser) の−OH基、又はトレオニン残基(Thr) の−OH基が、乳酸エステルのカルボニル基に求核付加し、脱アルコールによりアシル中間体(acyl intermediate) が生成する。このアシル中間体は活性エステル様であり、このアシルカルボニル基は、別の乳酸エステルの−OH基の求核付加を受けやすく、酵素が脱離して、乳酸エステル2分子から脱アルコール縮合した乳酸の二量体モノエステルが生成する。さらに、この反応が繰り返されることにより、乳酸の多量体モノエステルが得られる。リパーゼのような疎水性酵素との親和性を考慮すると、乳酸エステルは、炭素数が4以上の疎水的なアルコールとの乳酸エステルであることが有利である。反応スキームを示す。
【0041】
【化1】

【0042】
酵素の触媒作用の特徴として、基質特異性が挙げられる。すなわち、用いる酵素に応じて、乳酸エステルの特定の光学異性体(D体又はL体)のみが基質となり得る。そのため、ラセミ体の乳酸エステルを用いた場合であっても、高い光学純度を有する乳酸重合体か得られる。このように本発明によれば、光学選択的な乳酸重合体の製造方法が提供される。化学触媒では得られない利点である。
【実施例】
【0043】
以下、実施例により本発明をさらに具体的に説明するが、本発明はこれら実施例に限定されるものではない。
【0044】
[実施例1]
D,L−乳酸n−ブチル(関東化学製)0.5gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.5555gを加え、80℃、70mmHgで反応させた。反応開始後、2時間、6時間、12時間経過時に反応物のサンプリングを行い、以下のようにして、ガスクロマトグラフィーで分析を行った。
【0045】
(サンプル調製)
サンプリングした反応物5μlに、一晩冷蔵保存したBSTFA(N,O-Bis(trimethylsilyl)trifluoroacetamide, GL Sciences社製)0.1mlを加え、溶媒としてクロロホルム0.1mlを加えた。これをガスクロマトグラフィー分析のサンプル液とした。
【0046】
(ガスクロマトグラフィー分析条件)
ガスクロマトグラフ:島津製作所製GC−17A、
カラム:DB−5(Length 30m, I.D 0.25mm, Film 0.25 μm, Temperature limits 60℃〜 325℃/350℃, J&W Scientific製)、及び
検出器:Flame Ionization Detecter (FID)
を用いた。サンプル液を注入し、カラム温度を60℃から350℃に10℃/minの昇温速度で昇温し、FIDで検出し、クロマトグラムを得た。
【0047】
(乳酸重合度の決定)
FIDは、炭素原子を持つ有機化合物のみに応答を示し、そのイオン化機構は化学イオン化反応として知られている。化学イオン化反応によってイオン電流が生じ、有効炭素原子数 (Effective carbon number)が検出される。各種化合物の有効炭素原子数は以下の文献に示されているように既に知られている。
【0048】
1. "Gas chromatography", S ternberg, J. C., Gallaway, W. S., Jones, D. T. L., ed. N. Brenner et al., P231 (1962)
2. "Prediction of Gas Chromatography Flame Ionization Detector Response Factors from Molecular Structures", A. D. Jorgensen et al., Anal. Chem., 62, 683-689 (1990)
【0049】
まず、得られたクロマトグラムの各ピークについて、電子イオン化法 (EI;Electron Ionization)質量分析、及び化学イオン化法 (CI;Chemical Ionization)質量分析で質量を求め、各ピークの帰属を行った。これにより、乳酸のn量体(単量体〜n量体)の各ピークの帰属を行った。
【0050】
次に、乳酸のn量体のクロマトグラムのピークの面積をSnとして、
一方、乳酸のn量体の有効炭素原子数をEnとして(Enについては、上記文献に示された値を利用して算出した)、
乳酸のn量体の重量比率Rnは、下記の式で表される。この式において、mはガスクロマトグラフィーで検出される最も重合度の高い乳酸多量体のn数を表す。この式から、サンプル液に含まれている乳酸のn量体の重量比率を求めた。結果を表1に示す。
【0051】
【数1】

【0052】
【表1】

【0053】
この実施例において、反応時間が経つにつれて、乳酸エステルの重合が進んだことが分かる。
【0054】
[比較例]
実施例1と同じ温度、減圧条件では、D−乳酸n−ブチル、D,L−乳酸n−ブチル、L−乳酸n−ブチルのいずれを用いた場合においても、リパーゼ触媒が存在しなければ、重合体は得られなかった。
【0055】
[実施例2:光学選択性]
1.D−乳酸ブチルの重縮合
D−乳酸(PURAC社製)180gとn−ブタノール(関東化学製、特級)148gを混合し、110℃に加熱してエステル化させ、生成した水を反応系外へ除去した。その後、真空ポンプを用いて反応系を減圧し、乳酸ブチルを減圧蒸留した。このようにして、D−乳酸n−ブチルを調製した。
【0056】
試験管中において、得られたD−乳酸n−ブチル2.0gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、80℃に加熱し、攪拌子にて反応液を攪拌しながら、24時間反応させた。反応後、反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。
【0057】
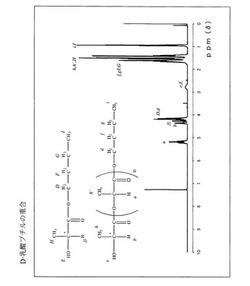
図1にD−乳酸ブチルの重縮合における500MHz 1HNMRチャートを示す。各プロトンピークの帰属は図中に示した通りである。
I(0.95ppm)、H(1.42ppm)、G(1.40ppm)、F(1.65ppm)、E(2.81ppm)、D(4.19ppm)、B(4.26ppm);
i(0.93ppm)、h,h’(1.50〜1.61ppm)、g(1.37ppm)、f(1.65ppm)、e(2.85ppm)、d(4.14ppm)、b(4.36ppm)、a(5.13〜5.25ppm)
【0058】
すなわち、乳酸ブチルのメチン基プロトンのピークBは4.26ppmであるが、重縮合により、OH末端のメチン基プロトンのピークbは4.36ppmにシフトし、それ以外のメチン基プロトンのピークaは5.2ppm付近(5.13〜5.25ppm)にシフトする。
【0059】
オリゴマーの5.2ppm付近(5.13〜5.25ppm)のメチン基に帰属するプロトンピークa、OH末端のメチン基プロトンのピークb(4.36ppm)、及び乳酸ブチルのメチン基プロトンのピークB(4.26ppm)の強度より、次のようにして、平均重合度(Degree of polymerization)と転換率(Conversion)を求めた。
【0060】
平均重合度:ピークbの積分値Hb を1とした時のピークaの積分値Ha を求め、ピークaの積分値Ha に1を加えた値である。すなわち、
平均重合度=(Ha +Hb )/Hb =(Ha /Hb )+1
転換率(%)=[(Ha +Hb )/(Ha +Hb +HB )]×100
ここで、HB は、ピークBの積分値を表す。
【0061】
1HNMR測定結果から、Ha =1.4、Hb =1.0、HB =2.7となり、平均重合度:2.4、転換率:47%であった。
【0062】
2.D,L−乳酸ブチルの重縮合
試験管中において、D,L−乳酸n−ブチル(関東化学製)2.0gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、80℃に加熱し、攪拌子にて反応液を攪拌しながら、24時間反応させた。反応後、反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。
【0063】
図2にD,L−乳酸ブチルの重縮合における500MHz 1HNMRチャートを示す。 1HNMR測定結果から、Ha =1.1、Hb =1.0、HB =3.3となり、平均重合度:2.1、転換率:39%であった。
【0064】
3.L−乳酸ブチルの重縮合
試験管中において、L−乳酸n−ブチル(アルドリッチ社製)2.0gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、80℃に加熱し、攪拌子にて反応液を攪拌しながら、24時間反応させた。反応後、反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。その結果、5.2ppm付近のメチン基に帰属するプロトンピークは確認されず、すなわち、重合は認められなかった。
【0065】
以上のように、 1HNMR測定により、D−乳酸ブチルを用いた場合、D,L−乳酸ブチルを用いた場合には、5.2ppm付近にメチン基に帰属するピークaが確認され、重合反応が進行したことが確認された。また、D−乳酸ブチルを用いた場合の重合度は、D,L−乳酸ブチルを用いた場合の重合度よりも高いことが分かった。
一方、L−乳酸ブチルを用いた場合には、5.2ppm付近にメチン基に帰属するピークaは見られず、重合反応は進行しなかった。
【0066】
[実施例3:各種乳酸エステルの重縮合]
この実施例においては、表2に示す7種のD−乳酸エステル、及び表3に示す7種のL−乳酸エステルの重縮合をそれぞれ行った。
【0067】
(原料の乳酸エステル)
L−乳酸エチル、L−乳酸n−ブチルについては、市販の試薬を用いた。
それ以外の乳酸エステルについては、市販のL−乳酸又はD−乳酸と、対応するアルコールとを硫酸触媒下に反応させることにより合成したものを用いた。
【0068】
(各種乳酸エステルの重縮合)
各乳酸エステル2.0gを試験管中に入れ、固定化リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、攪拌子にて反応液を攪拌しながら、80℃に加熱し、表2及び表3に示す各圧力下で24時間反応させた。
【0069】
ここで、表2及び表3に示す各圧力は、各乳酸エステルの酵素触媒反応における適切な減圧条件とされている。ただし、メチルエステルについては、常圧条件である。すなわち、上記の各圧力は、反応温度80℃において、原料の乳酸エステルはガス化しないが、縮合反応で脱離したアルコールはガス化し反応系外へ除去される圧力条件とされている。
【0070】
反応後、得られた反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。
【0071】
実施例2と同様にして、オリゴマーの5.2ppm付近のメチン基に帰属するプロトンピークaの積分値Ha 、OH末端のメチン基プロトンのピークb(4.36ppm)の積分値Hb 、及び乳酸エステルのメチン基プロトンのピークB(4.26ppm)の積分値HB より、平均重合度(Degree of polymerization)と転換率(Conversion)を求めた。
【0072】
さらに、得られた反応物の試料をESI−TOF−MSで質量分析し、反応物に含まれている重合物の分子量を測定した。重合物の最大分子量と、その重合度を求めた。
【0073】
この際のESI−TOF−MS測定はBrucker製の装置を用いて行った。反応物の試料2μlを溶離液2mlで溶解させ、この溶解液を親水性フィルターを通過させ測定した。溶離液としては、メタノール/水(50/50,v/v%)を脱気したものを用いた。
【0074】
ESI−TOF−MS測定結果の一例として、D−乳酸ブチル重合物についての結果を図3に示す。以上の結果を表2及び表3に示す。
【0075】
【表2】

【0076】
【表3】

【0077】
以上から、D−乳酸との各種エステルは、リパーゼ触媒により重合が認められ、これらの中でも、n−ブタノール及び iso−ブタノールとのエステルの重合性が最も高いことが分かった。一方、L−乳酸との各種エステルでは、リパーゼ触媒による重合は認められなかった。このように、リパーゼ触媒を用いた場合の乳酸エステルの光学選択性が明らかとなった。また、リパーゼ触媒を用いた場合に、種々のD−乳酸エステルを原料として使用できることが明らかとなった。
【図面の簡単な説明】
【0078】
【図1】実施例2において、D−乳酸ブチルの重縮合における500MHz 1HNMRチャートである。
【図2】実施例2において、D,L−乳酸ブチルの重縮合における500MHz 1HNMRチャートである。
【図3】実施例3において、D−乳酸ブチル重合物についてのESI−TOF−MS測定チャートである。
【技術分野】
【0001】
本発明は、乳酸エステルから酵素触媒を用いて乳酸の重合体を製造する方法に関する。乳酸の重合体であるポリ乳酸は、植物等のバイオマスを原料とした生分解性プラスチック材料として注目されている。
【背景技術】
【0002】
ポリ乳酸の製造法としては、乳酸から乳酸の環状二量体であるラクチドを合成し、ラクチドの開環重合によってポリ乳酸を得る方法が知られている。この方法においては、例えば、まず、乳酸を減圧下(50〜30mmHg)加熱(135〜160℃)して乳酸オリゴマー(Mw:1170)を合成して、乳酸オリゴマーにスズ又はチタンなどの金属触媒を添加して、この混合物を減圧下(4〜5mmHg)加熱(190〜230℃)して、乳酸オリゴマーを解重合して、ラクチドを反応蒸発させる [Chem.Pharm.Bull., 47, 467-471 (1999)のExperimental] 。ラクチドを結晶化(例えば、特開平7−118259号公報、特開平7−138253号公報、特開平8−208638号公報)するか、又は精留(例えば、米国特許 5,142,023号明細書、米国特許 5,359,026号明細書)して、高純度ラクチドを得る。高純度ラクチドをスズやチタンなどの金属触媒を用いて開環重合して、ポリ乳酸を得る。
【0003】
また、ポリ乳酸の製造法として、最近、乳酸を直接脱水縮合する方法が開発されている。例えば、Polymer, 42, 5059-5062 (2001) には、乳酸を脱水して平均重合度8のオリゴ乳酸として、塩化スズ(II)及びp−トルエンスルホン酸触媒を用いて重縮合させてポリ乳酸を得ることが開示されている。
【0004】
上記従来の方法はいずれも、乳酸のフリー体を原料としており、且つスズ又はチタンなどの金属触媒を用いるものである。乳酸のフリー体は腐食性を有するので、工業化に際しては、反応容器や配管としては、耐食性の特殊材料から形成されたものか又は特殊材料でコーティングされたものを用いなければならない。このことは、ポリ乳酸の製造のコストアップに繋がる。そして、製造されたポリ乳酸中には金属触媒が残存している。金属触媒の残存は、ポリ乳酸の成形加工性に悪影響を与えるだけでなく、環境中に残存金属の拡散が起こる。
【0005】
ところで、バイオマスから乳酸を発酵法によって製造する方法は次の通りである。植物から得られるグルコース等の糖質を乳酸菌や、リゾプス等のカビ等の微生物を用いて乳酸発酵させて乳酸とする。この乳酸発酵の際には、生成した乳酸によって発酵液中のpHが低下すると微生物の活性が低下するので、水酸化カルシウム、炭酸カルシウム、水酸化ナトリウム、アンモニア等の塩基で中和しながら、発酵を進める。そのため、発酵法により得られる乳酸は、乳酸のカルシウム塩、ナトリウム塩、アンモニウム塩等の乳酸塩の形態である。
【0006】
水酸化カルシウム又は炭酸カルシウムを用いて中和を行うと、発酵液中において乳酸カルシウムが得られる。乳酸カルシウムの場合には、硫酸を用いて乳酸を遊離させ粗乳酸として、粗乳酸を目的に応じてエチル又はメチルエステル化し、乳酸エステルを蒸留する。蒸留された乳酸のエチル又はメチルエステルに水を加えて加水分解して乳酸に変換し、エチル又はメチルアルコールを蒸発させる。この方法は、工程が長い上に、多量の硫酸カルシウムが副生物として生産される。硫酸カルシウムは建材などとしての用途はあるが、副生物が多量に排出されるプロセスは好ましくない。
【0007】
アンモニア水を用いて中和を行うと、発酵液中において乳酸アンモニウムが得られる。特開平6−311886号公報には、アンモニアでの中和後の反応濃縮液にn−ブタノールを加え、ブタノールを還流させながらアンモニアを蒸発させ、乳酸ブチルを合成する。続いて、乳酸ブチルを蒸留し、得られた乳酸ブチルに水を添加して加水分解し、乳酸を得ることが開示されている。この方法では、蒸発捕集したアンモニアを再度、乳酸発酵の中和剤として利用できる。
【0008】
このように、バイオマスから乳酸を発酵法によって製造するに際しては、乳酸塩を乳酸のフリー体に変換するために別途の工程が必要である。このため、乳酸のフリー体を原料とする上述したラクチドの開環重合法や、乳酸の直接脱水縮合法では、ポリ乳酸の製造のさらなるコストアップに繋がる。
【0009】
また、ポリ乳酸の製造法として、乳酸エステルの脱アルコール縮合を行う方法が知られている。例えば、特開平7−173264号公報には、スズ等の金属触媒存在下で乳酸エステルを縮合し、ポリ乳酸を製造する方法が開示されている。特許3024907号公報には、スズ等の金属触媒存在下で乳酸エステルから生成するアルコールを除去しながら重縮合させ、ポリ乳酸を製造する方法が開示されている。特開平10−36366号公報には、乳酸エステルを合成し、乳酸エステルをスズ触媒存在下で脱アルコールして乳酸オリゴマーを合成し、続いてラクチドを合成する方法が開示されている。
【0010】
特開2002−300898号公報には、発酵により得られた乳酸アンモニウムから、乳酸エステルを経て重合物を得る方法が開示されている。
【0011】
いずれの方法においても、スズなどの金属触媒を用いる。製造されたポリ乳酸中には金属触媒が残存している。金属触媒の残存は、ポリ乳酸の成形加工性に悪影響を与えるだけでなく、環境中に残存金属の拡散が起こる。
【0012】
一方、World Journal of Microbiology & Biotechnology, 19, 859-865, (2003)には、リパーゼを触媒として乳酸を重合させたことが開示されている。
【0013】
Biotechnol. Prog., 22, 444-448 (2006) には、リパーゼを触媒として乳酸とブタノールとから乳酸ブチルを合成したことが開示されている。
【0014】
Chem. Lett., 1317-1318 (1999) には、リパーゼを触媒として環状ジエステルを開環重合させたことが開示されている。
【0015】
【非特許文献1】"Thermal Catalytic Depolymerization of Poly(L-Lactic Acid )Oligomer into LL-Lactide: Effects of Al, Ti, Zn and Zr Compounds as Catalysts", M. Noda and H. Okuyama, Chem. Pharm. Bull., 47, 467-471 (1999)
【非特許文献2】"Melt/solid polycondensation of L-lactic acid: an alternative route to poly(L-lactic acid) with high molecular weight", Y. Kimura et al., Polymer, 42, 5059-5062 (2001)
【非特許文献3】"Lipase-Catalysed polymerization of lactic acid and its film forming properties", S. Divakar et al., World Journal of Microbiology & Biotechnology, 19, 859-865, (2003)
【非特許文献4】"Lipase-Catalysed Transformations for the Synthesis of Butyl Lactate: A Comparison between Esterification and Transesterification", D. Pirozzi et al., Biotechnol. Prog., 22, 444-448 (2006)
【非特許文献5】"Lipase-Catalysed Ring-Opening Polymerization of Cyclic Diesters", S. Kobayashi et al., Chem. Lett., 1317-1318 (1999)
【特許文献1】特開平7−118259号公報
【特許文献2】特開平7−138253号公報
【特許文献3】特開平8−208638号公報
【特許文献4】米国特許 5,142,023号明細書
【特許文献5】米国特許 5,359,026号明細書
【特許文献6】特開平6−311886号公報
【特許文献7】特開平7−173264号公報
【特許文献8】特許3024907号公報
【特許文献9】特開平10−36366号公報
【特許文献10】特開2002−300898号公報
【発明の開示】
【発明が解決しようとする課題】
【0016】
バイオマスを出発原料とするポリ乳酸の製造を考えると、従来の方法では、上述のように、まず、バイオマスから乳酸を発酵法によって製造するに際して、乳酸塩を乳酸のフリー体に変換する工程が必要であり、ポリ乳酸製造の原料である乳酸のコストが高い。そして、乳酸のフリー体は腐食性を有するので、製造設備には耐食性の特殊材料を用いなければならず、ポリ乳酸製造のコストが高くなる。さらに、ポリ乳酸製造において金属触媒を用いるので、製造されたポリ乳酸中には金属触媒が残存しており、そのため、残存金属触媒がポリ乳酸の成形加工性に悪影響を与え、環境中に残存金属の拡散が起こる。
【0017】
本発明の目的は、上記従来技術の問題点を解決し、金属触媒を用いることなく、乳酸エステルの脱アルコールにより乳酸の重合体を得る乳酸重合体の製造方法を提供することにある。
【課題を解決するための手段】
【0018】
本発明には以下の発明が含まれる。
(1) 乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。
【0019】
(2) 乳酸エステルは、乳酸と炭素数が4以上のアルコールとのエステルである、上記(1)に記載の乳酸重合体の製造方法。
【0020】
(3) 乳酸エステルは、D−乳酸エステル、L−乳酸エステル、又はDL−乳酸エステルである、上記(1)又は(2)に記載の乳酸重合体の製造方法。
【0021】
(4) 脱アルコール反応を加熱条件及び/又は減圧条件で行う、上記(1)〜(3)のうちのいずれかに記載の乳酸重合体の製造方法。
【0022】
(5) 酵素として、カルボン酸エステル加水分解酵素を用いる、上記(1)〜(4)のうちのいずれかに記載の乳酸重合体の製造方法。
【0023】
(6) 酵素として、リパーゼ又はクチナーゼを用いる、上記(1)〜(4)のうちのいずれかに記載の乳酸重合体の製造方法。
【0024】
(7) 酵素として、固定化された酵素を用いる、上記(1)〜(6)のうちのいずれかに記載の乳酸重合体の製造方法。
【0025】
(8) 乳酸発酵で得られた乳酸アンモニウムとアルコールとを反応させ、乳酸エステルを合成し、
得られた乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。
【0026】
(9) 乳酸の重合体を光学選択的に得る、上記(1)〜(8)のうちのいずれかに記載の乳酸重合体の製造方法。
【発明の効果】
【0027】
本発明によれば、乳酸エステルを酵素触媒の存在下で脱アルコール縮合反応させ、乳酸の重合体を得る。酵素を触媒として用いるので、反応条件は温和であり製造上好ましい。得られる乳酸重合体には、金属触媒の残存はない。従って、乳酸重合体の成形加工性は良好であり、環境中への金属の拡散汚染は起こらない。
【0028】
本発明で用いる乳酸エステルは、バイオマスから乳酸を発酵法によって製造する際の中間製品として得ることができる。従って、乳酸塩を乳酸のフリー体に変換する別途の工程を行う必要がないので、乳酸を原料とする方法に比べて大幅な工程短縮が図られ、コストダウンが得られる。しかも、腐食性の乳酸を用いないので、製造設備の観点からもコストダウンが得られる。
【0029】
さらに、本発明によれば、光学選択的に乳酸の重合体を得ることができ、高い結晶性を有する乳酸重合体を得ることができる。
【発明を実施するための最良の形態】
【0030】
本発明において、乳酸エステルを酵素触媒の存在下で脱アルコール縮合反応させ、乳酸の重合体を得る。乳酸エステルとして、化学合成された乳酸を原料として合成されたものを用いてもよく、又はバイオマスから乳酸を発酵法によって製造する際の乳酸アンモニウムから合成されたものを用いてもよい。
【0031】
乳酸発酵はよく知られている。植物から得られる糖質、例えば、トウモロコシ、米、キャッサバなどのデンプンを加水分解して得られたグルコース、セルロースを硫酸や加圧熱水で加水分解して得られたグルコース; サトウキビやビートから得られたシュークロース; ヘミセルロースから得られたキシロース、アラビノース等の糖質を、乳酸菌や、リゾプス等のカビ等の微生物を用いて乳酸発酵させる。この乳酸発酵液のpHが低下すると微生物の活性が低下するので、アンモニア水又はアンモニアで中和しながら、発酵を進めると、乳酸アンモニウムが得られる。
【0032】
乳酸アンモニウムにアルコールを反応させると、乳酸とアルコールとのエステルが得られる。この際に用いるアルコールは特に限定されないが、炭素数が4以上のアルコールが好ましい。エタノールを用いると、エタノールの常圧での沸点が78℃と低いため反応温度を高くすることができず、乳酸アンモニウムとエタノールとの反応性は低く収率も低い。このため、エタノールを用いると、加圧条件下での反応が必要となる。炭素数が4以上のアルコールとしては、例えば、次の段落で挙げられているものを用いるとよい。
【0033】
本発明においては、乳酸エステルとして、乳酸と炭素数が4以上のアルコールとのエステルを用いることが好ましい。炭素数が4以上のアルコールとの乳酸エステルは、アルコール由来部分が疎水的であり、疎水性酵素触媒存在下での脱アルコール反応が起こりやすい。乳酸エステルとして、乳酸と炭素数が4以上12以下のアルコールとのエステルがより好ましく、このようなアルコールとしては、直鎖状又は分枝状であってもよく、ブタノール、ペンタノール、ヘキサノール、ヘプタノール、オクタノール、2−エチルヘキサノール、ノナノール、デカノール、ウンデカノール、ドデカノール等の一価アルコールが挙げられる。乳酸と炭素数が4以上6以下のアルコールとのエステル、すなわち、乳酸ブチル、乳酸ペンチル、乳酸ヘキシルがより好ましい。また、1,4−ブタンジオール、1,5−ペンタンジオール、1,6−ヘキサンジオール等の二価アルコールとのジエステルの使用も考えられる。
【0034】
また、乳酸エステルは、D−乳酸エステル、L−乳酸エステル、又はDL−乳酸エステルのいずれであってもよい。製造されるべき乳酸重合体の目的に応じて、適宜選択するとよい。
【0035】
触媒として用いる酵素としては、カルボン酸エステル加水分解酵素(EC3.1.1)が好ましい。カルボン酸エステル加水分解酵素(EC3.1.1)はエステラーゼ(EC3.1)の一種である。カルボン酸エステル加水分解酵素のなかでも、リパーゼ(EC3.1.1.3)が特に好適である。またクチナーゼ(EC3.1.1)も好適である。
【0036】
酵素を分離する微生物は特に限定されず、例えば、リパーゼに関しては、カンジダ アンタルチカ (Candida antartica)、カンジダ ルゴサ(Candida rugosa)、クリプトコッカス エスピー(Cryptococcus sp.)、プシュードモナス フルオレッセンス (Pseudomonas fluorescens)、プシュードモナス セパシア (Pseudomonas cepacia)、ブルコルデリア セパシア(Burkholderia cepacia)、アスペルギラス ナイガー (Aspergillus niger)、アスペルギラス オリザエ(Aspergillus oryzae)、ムコール ジャバニカス (Mucor javanicus)、ペニシリウム カメムベルチ(Penicillium camemberti)、リゾプス オリザエ (Rhizopus oryzae)、リゾプス デレマー(Rhizopus delemar)、ペニシリウム ロクエホルチ(Penicillium roqueforti)、リゾムコール ミエヘイ (Rhizomucor miehei)、リゾプス ジャポニカス(Rhizopus japonicus)、バチルス エスピー(Bacillus sp.)、カンジダ シリンドラシア(Candida cylindracea) などを給源とする微生物リパーゼを利用することができる。また、ブタ、ウシ、ラット等の動物を給源とする動物リパーゼ、ヒマシ、米ぬか、小麦、ダイズ、トウモロコシ等の植物を給源とする植物リパーゼを利用することもできる。これらに限定されることなく、乳酸エステルの脱アルコール縮合反応を触媒する機能を有する酵素を用いることができる。
【0037】
また、本発明において、固定化された酵素を用いてもよい。固定化酵素は、繰り返し使用できる点や、生成した乳酸重合体との分離が容易である点において好ましい。固定化担体としては、公知の各種のものを用いるとよく、例えば、アクリルアミド、セルロース、ビーズ、セラミック等が挙げられる。市販の固定化酵素としては、例えば、カンジダ アンタルチカ (Candida antartica)由来のリパーゼをポリアクリルアミドに固定化したノボノルディスク社のノボザイム435、ブルコルデリア セパシア(Burkholderia cepacia)由来のリパーゼをセラミックに固定化した天野エンザイム社のリパーゼPS−C「アマノ」I等が挙げられる。
【0038】
乳酸エステルの脱アルコール縮合反応は、乳酸エステルと酵素とを混合し、適切な反応温度、適切な減圧条件にて行うとよい。反応温度は、用いる酵素の至適温度により定められる。減圧は縮合により生成したアルコールを反応系外へ除去するために行う。すなわち、減圧度は、当該温度で除去しようとするアルコールの蒸気圧以下かつ基質である乳酸エステルの蒸気圧以上とする必要があり、通常は、当該温度で除去しようとするアルコールの蒸気圧よりも低い圧力かつ基質である乳酸エステルの蒸気圧よりも高い圧力とする。具体的には、加熱温度としては、用いる酵素の至適温度を考慮して、例えば60〜90℃程度、減圧度としては、乳酸ブチルの脱ブタノール縮合反応の場合、例えば5〜80mmHg程度とするとよい。反応時間は、特に限定されることはなく、重縮合の進行を考慮して定めるとよい。例えば30分間〜72時間、2時間〜48時間。もちろん、これらよりも長い反応時間としてもよい。
【0039】
用いる酵素の量は特に限定されるものではないが、乳酸エステルの100質量部に対して、例えば5〜200質量部、好ましくは10〜120質量部程度とするとよい。用いる酵素の触媒活性や、乳酸エステル中のアルキル基の長さ等を考慮して、適宜定めるとよい。
【0040】
乳酸エステルの脱アルコール縮合反応における酵素の触媒作用については、次のように考えられる。酵素中に含まれているセリン残基(Ser) の−OH基、又はトレオニン残基(Thr) の−OH基が、乳酸エステルのカルボニル基に求核付加し、脱アルコールによりアシル中間体(acyl intermediate) が生成する。このアシル中間体は活性エステル様であり、このアシルカルボニル基は、別の乳酸エステルの−OH基の求核付加を受けやすく、酵素が脱離して、乳酸エステル2分子から脱アルコール縮合した乳酸の二量体モノエステルが生成する。さらに、この反応が繰り返されることにより、乳酸の多量体モノエステルが得られる。リパーゼのような疎水性酵素との親和性を考慮すると、乳酸エステルは、炭素数が4以上の疎水的なアルコールとの乳酸エステルであることが有利である。反応スキームを示す。
【0041】
【化1】

【0042】
酵素の触媒作用の特徴として、基質特異性が挙げられる。すなわち、用いる酵素に応じて、乳酸エステルの特定の光学異性体(D体又はL体)のみが基質となり得る。そのため、ラセミ体の乳酸エステルを用いた場合であっても、高い光学純度を有する乳酸重合体か得られる。このように本発明によれば、光学選択的な乳酸重合体の製造方法が提供される。化学触媒では得られない利点である。
【実施例】
【0043】
以下、実施例により本発明をさらに具体的に説明するが、本発明はこれら実施例に限定されるものではない。
【0044】
[実施例1]
D,L−乳酸n−ブチル(関東化学製)0.5gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.5555gを加え、80℃、70mmHgで反応させた。反応開始後、2時間、6時間、12時間経過時に反応物のサンプリングを行い、以下のようにして、ガスクロマトグラフィーで分析を行った。
【0045】
(サンプル調製)
サンプリングした反応物5μlに、一晩冷蔵保存したBSTFA(N,O-Bis(trimethylsilyl)trifluoroacetamide, GL Sciences社製)0.1mlを加え、溶媒としてクロロホルム0.1mlを加えた。これをガスクロマトグラフィー分析のサンプル液とした。
【0046】
(ガスクロマトグラフィー分析条件)
ガスクロマトグラフ:島津製作所製GC−17A、
カラム:DB−5(Length 30m, I.D 0.25mm, Film 0.25 μm, Temperature limits 60℃〜 325℃/350℃, J&W Scientific製)、及び
検出器:Flame Ionization Detecter (FID)
を用いた。サンプル液を注入し、カラム温度を60℃から350℃に10℃/minの昇温速度で昇温し、FIDで検出し、クロマトグラムを得た。
【0047】
(乳酸重合度の決定)
FIDは、炭素原子を持つ有機化合物のみに応答を示し、そのイオン化機構は化学イオン化反応として知られている。化学イオン化反応によってイオン電流が生じ、有効炭素原子数 (Effective carbon number)が検出される。各種化合物の有効炭素原子数は以下の文献に示されているように既に知られている。
【0048】
1. "Gas chromatography", S ternberg, J. C., Gallaway, W. S., Jones, D. T. L., ed. N. Brenner et al., P231 (1962)
2. "Prediction of Gas Chromatography Flame Ionization Detector Response Factors from Molecular Structures", A. D. Jorgensen et al., Anal. Chem., 62, 683-689 (1990)
【0049】
まず、得られたクロマトグラムの各ピークについて、電子イオン化法 (EI;Electron Ionization)質量分析、及び化学イオン化法 (CI;Chemical Ionization)質量分析で質量を求め、各ピークの帰属を行った。これにより、乳酸のn量体(単量体〜n量体)の各ピークの帰属を行った。
【0050】
次に、乳酸のn量体のクロマトグラムのピークの面積をSnとして、
一方、乳酸のn量体の有効炭素原子数をEnとして(Enについては、上記文献に示された値を利用して算出した)、
乳酸のn量体の重量比率Rnは、下記の式で表される。この式において、mはガスクロマトグラフィーで検出される最も重合度の高い乳酸多量体のn数を表す。この式から、サンプル液に含まれている乳酸のn量体の重量比率を求めた。結果を表1に示す。
【0051】
【数1】

【0052】
【表1】

【0053】
この実施例において、反応時間が経つにつれて、乳酸エステルの重合が進んだことが分かる。
【0054】
[比較例]
実施例1と同じ温度、減圧条件では、D−乳酸n−ブチル、D,L−乳酸n−ブチル、L−乳酸n−ブチルのいずれを用いた場合においても、リパーゼ触媒が存在しなければ、重合体は得られなかった。
【0055】
[実施例2:光学選択性]
1.D−乳酸ブチルの重縮合
D−乳酸(PURAC社製)180gとn−ブタノール(関東化学製、特級)148gを混合し、110℃に加熱してエステル化させ、生成した水を反応系外へ除去した。その後、真空ポンプを用いて反応系を減圧し、乳酸ブチルを減圧蒸留した。このようにして、D−乳酸n−ブチルを調製した。
【0056】
試験管中において、得られたD−乳酸n−ブチル2.0gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、80℃に加熱し、攪拌子にて反応液を攪拌しながら、24時間反応させた。反応後、反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。
【0057】
図1にD−乳酸ブチルの重縮合における500MHz 1HNMRチャートを示す。各プロトンピークの帰属は図中に示した通りである。
I(0.95ppm)、H(1.42ppm)、G(1.40ppm)、F(1.65ppm)、E(2.81ppm)、D(4.19ppm)、B(4.26ppm);
i(0.93ppm)、h,h’(1.50〜1.61ppm)、g(1.37ppm)、f(1.65ppm)、e(2.85ppm)、d(4.14ppm)、b(4.36ppm)、a(5.13〜5.25ppm)
【0058】
すなわち、乳酸ブチルのメチン基プロトンのピークBは4.26ppmであるが、重縮合により、OH末端のメチン基プロトンのピークbは4.36ppmにシフトし、それ以外のメチン基プロトンのピークaは5.2ppm付近(5.13〜5.25ppm)にシフトする。
【0059】
オリゴマーの5.2ppm付近(5.13〜5.25ppm)のメチン基に帰属するプロトンピークa、OH末端のメチン基プロトンのピークb(4.36ppm)、及び乳酸ブチルのメチン基プロトンのピークB(4.26ppm)の強度より、次のようにして、平均重合度(Degree of polymerization)と転換率(Conversion)を求めた。
【0060】
平均重合度:ピークbの積分値Hb を1とした時のピークaの積分値Ha を求め、ピークaの積分値Ha に1を加えた値である。すなわち、
平均重合度=(Ha +Hb )/Hb =(Ha /Hb )+1
転換率(%)=[(Ha +Hb )/(Ha +Hb +HB )]×100
ここで、HB は、ピークBの積分値を表す。
【0061】
1HNMR測定結果から、Ha =1.4、Hb =1.0、HB =2.7となり、平均重合度:2.4、転換率:47%であった。
【0062】
2.D,L−乳酸ブチルの重縮合
試験管中において、D,L−乳酸n−ブチル(関東化学製)2.0gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、80℃に加熱し、攪拌子にて反応液を攪拌しながら、24時間反応させた。反応後、反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。
【0063】
図2にD,L−乳酸ブチルの重縮合における500MHz 1HNMRチャートを示す。 1HNMR測定結果から、Ha =1.1、Hb =1.0、HB =3.3となり、平均重合度:2.1、転換率:39%であった。
【0064】
3.L−乳酸ブチルの重縮合
試験管中において、L−乳酸n−ブチル(アルドリッチ社製)2.0gに、リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、80℃に加熱し、攪拌子にて反応液を攪拌しながら、24時間反応させた。反応後、反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。その結果、5.2ppm付近のメチン基に帰属するプロトンピークは確認されず、すなわち、重合は認められなかった。
【0065】
以上のように、 1HNMR測定により、D−乳酸ブチルを用いた場合、D,L−乳酸ブチルを用いた場合には、5.2ppm付近にメチン基に帰属するピークaが確認され、重合反応が進行したことが確認された。また、D−乳酸ブチルを用いた場合の重合度は、D,L−乳酸ブチルを用いた場合の重合度よりも高いことが分かった。
一方、L−乳酸ブチルを用いた場合には、5.2ppm付近にメチン基に帰属するピークaは見られず、重合反応は進行しなかった。
【0066】
[実施例3:各種乳酸エステルの重縮合]
この実施例においては、表2に示す7種のD−乳酸エステル、及び表3に示す7種のL−乳酸エステルの重縮合をそれぞれ行った。
【0067】
(原料の乳酸エステル)
L−乳酸エチル、L−乳酸n−ブチルについては、市販の試薬を用いた。
それ以外の乳酸エステルについては、市販のL−乳酸又はD−乳酸と、対応するアルコールとを硫酸触媒下に反応させることにより合成したものを用いた。
【0068】
(各種乳酸エステルの重縮合)
各乳酸エステル2.0gを試験管中に入れ、固定化リパーゼ (Novozyme sp. 435R 、ノボノルディスク社製)0.2gを加え、攪拌子にて反応液を攪拌しながら、80℃に加熱し、表2及び表3に示す各圧力下で24時間反応させた。
【0069】
ここで、表2及び表3に示す各圧力は、各乳酸エステルの酵素触媒反応における適切な減圧条件とされている。ただし、メチルエステルについては、常圧条件である。すなわち、上記の各圧力は、反応温度80℃において、原料の乳酸エステルはガス化しないが、縮合反応で脱離したアルコールはガス化し反応系外へ除去される圧力条件とされている。
【0070】
反応後、得られた反応物10mgのサンプリングを行い、このサンプルを500MHz 1HNMR装置(Bruker ARX)により測定(CDCl3 、TMS:テトラメチルシラン)した。
【0071】
実施例2と同様にして、オリゴマーの5.2ppm付近のメチン基に帰属するプロトンピークaの積分値Ha 、OH末端のメチン基プロトンのピークb(4.36ppm)の積分値Hb 、及び乳酸エステルのメチン基プロトンのピークB(4.26ppm)の積分値HB より、平均重合度(Degree of polymerization)と転換率(Conversion)を求めた。
【0072】
さらに、得られた反応物の試料をESI−TOF−MSで質量分析し、反応物に含まれている重合物の分子量を測定した。重合物の最大分子量と、その重合度を求めた。
【0073】
この際のESI−TOF−MS測定はBrucker製の装置を用いて行った。反応物の試料2μlを溶離液2mlで溶解させ、この溶解液を親水性フィルターを通過させ測定した。溶離液としては、メタノール/水(50/50,v/v%)を脱気したものを用いた。
【0074】
ESI−TOF−MS測定結果の一例として、D−乳酸ブチル重合物についての結果を図3に示す。以上の結果を表2及び表3に示す。
【0075】
【表2】

【0076】
【表3】

【0077】
以上から、D−乳酸との各種エステルは、リパーゼ触媒により重合が認められ、これらの中でも、n−ブタノール及び iso−ブタノールとのエステルの重合性が最も高いことが分かった。一方、L−乳酸との各種エステルでは、リパーゼ触媒による重合は認められなかった。このように、リパーゼ触媒を用いた場合の乳酸エステルの光学選択性が明らかとなった。また、リパーゼ触媒を用いた場合に、種々のD−乳酸エステルを原料として使用できることが明らかとなった。
【図面の簡単な説明】
【0078】
【図1】実施例2において、D−乳酸ブチルの重縮合における500MHz 1HNMRチャートである。
【図2】実施例2において、D,L−乳酸ブチルの重縮合における500MHz 1HNMRチャートである。
【図3】実施例3において、D−乳酸ブチル重合物についてのESI−TOF−MS測定チャートである。
【特許請求の範囲】
【請求項1】
乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。
【請求項2】
乳酸エステルは、乳酸と炭素数が4以上のアルコールとのエステルである、請求項1に記載の乳酸重合体の製造方法。
【請求項3】
乳酸エステルは、D−乳酸エステル、L−乳酸エステル、又はDL−乳酸エステルである、請求項1又は2に記載の乳酸重合体の製造方法。
【請求項4】
脱アルコール反応を加熱条件及び/又は減圧条件で行う、請求項1〜3のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項5】
酵素として、カルボン酸エステル加水分解酵素を用いる、請求項1〜4のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項6】
酵素として、リパーゼ又はクチナーゼを用いる、請求項1〜4のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項7】
酵素として、固定化された酵素を用いる、請求項1〜6のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項8】
乳酸の重合体を光学選択的に得る、請求項1〜7のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項1】
乳酸エステルを酵素触媒の存在下で脱アルコール反応させ、乳酸の重合体を得る、乳酸重合体の製造方法。
【請求項2】
乳酸エステルは、乳酸と炭素数が4以上のアルコールとのエステルである、請求項1に記載の乳酸重合体の製造方法。
【請求項3】
乳酸エステルは、D−乳酸エステル、L−乳酸エステル、又はDL−乳酸エステルである、請求項1又は2に記載の乳酸重合体の製造方法。
【請求項4】
脱アルコール反応を加熱条件及び/又は減圧条件で行う、請求項1〜3のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項5】
酵素として、カルボン酸エステル加水分解酵素を用いる、請求項1〜4のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項6】
酵素として、リパーゼ又はクチナーゼを用いる、請求項1〜4のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項7】
酵素として、固定化された酵素を用いる、請求項1〜6のうちのいずれか1項に記載の乳酸重合体の製造方法。
【請求項8】
乳酸の重合体を光学選択的に得る、請求項1〜7のうちのいずれか1項に記載の乳酸重合体の製造方法。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2008−212147(P2008−212147A)
【公開日】平成20年9月18日(2008.9.18)
【国際特許分類】
【出願番号】特願2008−24235(P2008−24235)
【出願日】平成20年2月4日(2008.2.4)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成18年9月8日に頒布の国立大学法人京都工芸繊維大学発行の「京都工芸繊維大学 先端ファイブロ科学専攻 平成18年度修士論文中間発表会 論文集」に公開、平成18年9月26日に国立大学法人京都工芸繊維大学主催の「京都工芸繊維大学 先端ファイブロ科学専攻 平成18年度修士論文中間発表会」において文書をもって発表、社団法人日本生物工学会発行の「第59回日本生物工学会大会講演要旨集」(平成19年8月2日発行)に公開、社団法人高分子学会発行の「10th Pacific Polymer Conference(PPC 10)」(「第10回 環太平洋高分子国際会議(PPC 10)」)の予稿集CD−ROM(平成19年11月21日発行)に公開
【出願人】(000108993)ダイソー株式会社 (229)
【Fターム(参考)】
【公開日】平成20年9月18日(2008.9.18)
【国際特許分類】
【出願日】平成20年2月4日(2008.2.4)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成18年9月8日に頒布の国立大学法人京都工芸繊維大学発行の「京都工芸繊維大学 先端ファイブロ科学専攻 平成18年度修士論文中間発表会 論文集」に公開、平成18年9月26日に国立大学法人京都工芸繊維大学主催の「京都工芸繊維大学 先端ファイブロ科学専攻 平成18年度修士論文中間発表会」において文書をもって発表、社団法人日本生物工学会発行の「第59回日本生物工学会大会講演要旨集」(平成19年8月2日発行)に公開、社団法人高分子学会発行の「10th Pacific Polymer Conference(PPC 10)」(「第10回 環太平洋高分子国際会議(PPC 10)」)の予稿集CD−ROM(平成19年11月21日発行)に公開
【出願人】(000108993)ダイソー株式会社 (229)
【Fターム(参考)】
[ Back to top ]

