乳酸菌の免疫調整作用を相乗的に高める組成物
【課題】乳酸菌の持つ免疫調整作用、特に、IFN−γ産生促進能、IgE産生抑制能を相乗的に高める組成物やその製造法及びその飲食品及び飼料としての利用法、その乳酸菌との配合物を提供するものである。
【解決手段】植物処理物、中でもアスパラガスを処理したものを含有する培地に、乳酸菌、中でもラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)を接種し乳酸発酵して得られる培養物からなることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物。
【解決手段】植物処理物、中でもアスパラガスを処理したものを含有する培地に、乳酸菌、中でもラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)を接種し乳酸発酵して得られる培養物からなることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、乳酸菌の持つ免疫調整作用を相乗的に高める組成物、その製造法及びその飲食品及び飼料としての利用などに関するものである。
【背景技術】
【0002】
近年我が国では、花粉症、アトピー性皮膚炎、蕁麻疹、アレルギー性の鼻炎、結膜炎、喘息、アナフィラキシーショック、食物アレルギーといったアレルギー疾患の患者数が増加し、特に、花粉症は国民の2割近くが罹患しているとされており「国民病」の様相を呈している。
【0003】
一方、がんは国民の死亡原因の第1位であり、がんに対する有効な予防法が求められている。
【0004】
乳酸菌は有益な免疫調整作用を有することが知られており、抗アレルギー作用や抗腫瘍作用についても見出されている。
【0005】
花粉症やアレルギー性の鼻炎、結膜炎といった環境アレルギーは、I型アレルギーに分類される発症機構をもつことが知られており、抗原特異的IgE誘導とマスト細胞等からのヒスタミン等のケミカルメディエーターの放出を特徴とする。IgEはB細胞がクラススイッチされて産生されるが、そのクラススイッチを引き起こすのが、抗原を認識するヘルパーT細胞のうちTh2細胞から放出されるサイトカイン類(IL−4、IL−5、IL−6等)である。実際に、アレルギー患者ではリンパ球のTh2細胞が増加していることが分かっている。
【0006】
乳酸菌は、Th1細胞免疫を増強することで、Th2免疫を抑制し結果としてIgE量を低下させることが報告されている。また、Th1免疫を増強することは、インターフェロン−ガンマ(以下、IFN−γという。)やIL−12の産生を促し、NK細胞やマクロファージなどを含む細胞性免疫が活性化され、ガンの発生に対する抵抗力が増すことが明らかとなっている(特許文献1)。
【0007】
一方、積極的なIFN−γ産生誘導がIgEの産生を抑制することもすでに明らかになっており(特許文献2)、強力なIFN-γ誘導能やIgE産生抑制能をもつ乳酸菌は、抗腫瘍作用および抗アレルギー作用を有しているといえる。
【0008】
こうした乳酸菌としては、ラクトバチルス・ブレビス(特許文献3)、ラクトバチルス・アシドフィルス(L.acidphilus)AHU1402株、ラクトバチルス・カゼイ(L.casei)AHU1696株、ラクトバチルス・プランタラム(L.plantarum)L−137株、ストレプトコッカス・フェーカリス(Streptococcus faecalis)AHU1257株(特許文献1)、ラクトバチルス・パラカゼイ(L.paracasei)KW3110(特許文献4)、ラクトバチルス・ペントーサス(L.pentosus)S−PT84株(特許文献5)等が挙げられる。
【0009】
これらの乳酸菌は、サプリメントの形態か発酵物の形態で摂取されているが、必ずしも効果が満足できるものではなく、また、サプリメントの形態であれば必要な菌体量が多くなりコスト高になるという問題が、発酵物の形態であれば摂取量が多くなり継続摂取が困難であるという問題があった。
【0010】
これらの問題を解決する方法としては、他の免疫調整物質や、乳酸菌の効果を高めるとされる物質を併用する方法が試みられている。例えば、特開2003−38122号公報(特許文献6)では、アガリクス・ブラゼイを乳酸発酵させ、ビタミンB17および/または杏仁種子粉を含有させる方法が示されているが、その効果は各成分の効果の相加以下であり、満足いくものではない。また、アスコルビン酸と併用する方法(特許文献7)、ビタミンEと併用する方法(特許文献8)等が試みられているが、いまだ満足いくものではなかった。さらに、アスコルビン酸は熱に弱く、ビタミンEは脂溶性であり、扱いが難しいという問題点もあった。
【0011】
また、乳酸菌を大豆抽出液を含有する培地で培養すると乳酸菌自体の免疫賦活能が高まる(特許文献9)、乳酸発酵によって発酵物(乳酸菌体を除く)が免疫賦活能を有するようになることが報告されているが、上記問題を解決できるものではなかった。
【特許文献1】特開2002−80364号公報
【特許文献2】特開2005−139160号公報
【特許文献3】特公平7−55908号公報
【特許文献4】特開2005−137357号公報
【特許文献5】特開2005−333919号公報
【特許文献6】特開2003−38122号公報
【特許文献7】特開2001−64174号公報
【特許文献8】特開2002−80364号公報
【特許文献9】特開2004−357535号公報
【発明の開示】
【発明が解決しようとする課題】
【0012】
本発明は、乳酸菌の持つ免疫調整作用、特に、IFN−γ産生促進能、IgE産生抑制能を相乗的に高める組成物やその製造法及びその飲食品及び飼料としての利用法、その乳酸菌との配合物を提供するものである。
【課題を解決するための手段】
【0013】
本発明者らは、上記の課題を解決するために鋭意検討した結果、ラクトバチルス属の乳酸菌を用いて特定の野菜処理物を含有する培養液を乳酸発酵して得られた組成物に、免疫調整作用を有する乳酸菌の効果を相乗的に高める効果があることを見出し、本発明を完成させるに至った。本発明者らは、ラクトバチルス・ブレビス UAS−4株でアスパラガス処理物を含有する培養液を乳酸発酵して得られた組成物に、該組成物中に含まれる乳酸菌と同量の乳酸菌より強い免疫調整作用があることを既に報告しているが、本発明は該組成物の乳酸菌以外の成分を鋭意検討して見出されたものである。
【0014】
すなわち、本発明の第1は、植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物からなることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物を要旨とするものであり、好ましくは、培養物から乳酸菌を除いた成分が、免疫調製作用を有しない成分である前記の組成物であり、また好ましくは、免疫調整作用が、抗アレルギー作用、抗腫瘍作用、IFN−γ産生能を促進するもの、又はIgE抗体産生能を抑制するものである前記の組成物であり、また好ましくは、乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である前記の組成物であり、さらに好ましくは、植物処理物が、アスパラガスを処理したものである前記の組成物である。
【0015】
本発明の第2は、植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物から乳酸菌の免疫調整作用を相乗的に高める組成物を得ることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物の製造方法を要旨とするものである。
【0016】
本発明の第3は、本発明の第1の組成物と、免疫調整作用を有する乳酸菌とを含有することを特徴とする免疫調整作用を有する組成物を要旨とするものであり、好ましくは、免疫調整作用を有する乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である前記の組成物である。
【0017】
本発明の第4は、本発明の第1の組成物又は本発明の第3の組成物を含有することを特徴とする飲食品又は飼料を要旨とするものである。
【発明の効果】
【0018】
本発明によれば、乳酸菌の免疫調整作用を相乗的に高めることが可能となり、より優れた免疫調整作用を有する組成物の製造が可能となる。また、乳酸菌の摂取量を低減することが可能となり、継続摂取を容易にすることができる。
【発明を実施するための最良の形態】
【0019】
以下、本発明の第1及び第2について説明する。
【0020】
本発明に用いられる植物としては、食経験があり、その抽出液中で乳酸菌が増殖可能であればいかなるものでもよく、野菜類、果実類、穀類、いも類、豆類、藻類、キノコ類等が挙げられる。野菜類の例としては、アスパラガス、トマト、カボチャ、タケノコ、ゴボウ、ダイコン、ニンジン、キュウリ、ピーマン、カリフラワー、ブロッコリー、ナス、トウモロコシ、タマネギ、ラッキョウ、ニンニク、ネギ、レタス、キャベツ、ハクサイ、セロリ、ニラ、ホウレンソウ、コマツナ、シュンギク、ケール等が挙げられる。果実類の例としては、アケビ、アセロラ、アボガド、アンズ、イチゴ、イチジク、ウメ、ミカン、オレンジ、カキ、キウィ、グレープフルーツ、サクランボ、ザクロ、スイカ、モモ、スモモ、ナシ、パインアップル、バナナ、ブドウ、ビワ、マンゴー、マンゴスチン、メロン、ライチ、ラズベリー、ブルーベリー、リンゴ、レモン、ライム、ユズ、カボス、スダチ、アーモンド、ギンナン、クリ、クルミ、カシューナッツ、ココナッツ、マカダミアナッツ、ヘーゼルナッツ、ゴマ、ピスタチオ、ラッカセイ、松の実、蓮の実、カボチャの種等が挙げられる。穀類の例としては、米、麦、粟、ソバ、ひえ等が挙げられる。いも類の例としては、サツマイモ、ジャガイモ、サトイモ、ヤマイモ、キャッサバ、キクイモ等が挙げられる。豆類の例としては、アズキ、インゲンマメ、エンドウ、ソラマメ、ダイズ、ヒヨコマメ、レンズマメ等が挙げられる。藻類の例としては、コンブ、ワカメ、ヒジキ、ノリ、テングサ、モズク等が挙げられる。キノコ類の例としては、アガリクス、エノキタケ、キクラゲ、シイタケ、ホンシメジ、ブナシメジ、ハタケシメジ、ナメコ、エリンギ、ヒラタケ、マイタケ、マツタケ、マッシュルーム、ハナビラタケ等が挙げられる。これらの中でも、アスパラガスが、本発明の効果を発揮するのに最も好ましい。また、これらの植物は単独で用いてもよいし、2つ以上を組み合せて用いてもよい。
【0021】
本発明で用いられる植物処理物とは、上記したような植物を必要に応じて粉砕、細断、抽出、圧搾、濃縮、固液分離、加熱滅菌、濾過滅菌、酵素処理等公知の技術を単独或いは2つ以上組み合せて処理することで植物破砕物、磨砕物、粉砕物、搾汁、抽出物、酵素処理物が得られる。
【0022】
粉砕、細断とは物理的に植物体を細かく破砕する方法であり、粉砕は衝撃により、細断は切断によって破砕する。粉砕、細断は乳鉢や包丁、カッターナイフ、ハサミなどを用いて手作業で行っても良いが、大量の植物体を短時間で処理しようとする場合には装置を使用する。そのような装置としては、例えば、ミル、ハンマー式粉砕機、石臼式粉砕機、ミキサー、ブレンダーなどが挙げられ、また野菜用の細断機を用いてもよい。粉砕、細断された植物体の大きさは特に限定されないが、2cm以下が好ましく、5mm以下がより好ましい。
【0023】
抽出とは、溶媒を加え植物体の成分をそこに移行せしめる操作である。加える溶媒としては水が最も好ましいが、有機溶媒を併用してもよい。有機溶媒は、抽出時に水と併用してもよいし、抽出は有機溶媒単独で行い、その後水と混合してもよい。また、抽出は有機溶媒単独で行い、その後濃縮乾固等の操作により有機溶媒を除去した後、水を加えてもよい。有機溶媒の種類は特に限定されないが、食品に使用可能な点でエタノールが好ましい。抽出する際の溶媒の温度は、水の場合は0℃〜100℃が好ましく、10℃〜80℃がより好ましく、また、有機溶媒の場合は−20℃〜200℃が好ましく、0℃〜120℃がより好ましい。
【0024】
圧搾とは、植物体に物理的な圧力をかけて液を搾り出し、成分を搾汁に移行せしめる方法である。圧力は一方向のみにかけてもよいし、二以上の方向からかけてもよく、せん断力を伴わせることもできる。圧搾の操作は市販の圧搾機を用いれば容易であるが、手搾り、足踏み搾りなど機械を用いない方法で行ってもよい。このとき、植物体に水や湯を加えて圧搾してもよい。
【0025】
濃縮とは、他の成分を減少させること無く水分量、溶媒量を減らす操作であり、減圧濃縮、加熱濃縮、濾過膜を用いた濃縮などいかなる方法で行ってもよいが、20℃〜60℃の範囲での減圧濃縮を行うことが好ましい。
【0026】
固液分離とは、溶媒およびそこに溶解している成分と、不溶性の固形分を分離する方法であり、分離方法としては、例えばフィルター濾過、圧搾濾過、遠心分離、デカンテーションなどあらゆる方法が使用できる。清澄な植物抽出液を得る場合には、珪藻土などの濾過助剤を使用したフィルター濾過を行うことが好ましい。
【0027】
加熱滅菌とは、熱を加えて殺菌することであり、温度は60℃〜121℃が好ましく、70℃〜110℃がさらに好ましい。この温度範囲より低ければ、滅菌の効果が不十分になる問題があり、この温度範囲より高ければ有効成分が分解する問題がある。
【0028】
濾過滅菌とは、微生物が通過できないサイズの膜を、加圧或いは減圧して通過させることで除菌する操作である。膜の孔径としては0.1〜1.0μmが好ましく、より好ましくは0.2〜0.45μmである。
【0029】
酵素処理とは、植物体の構成成分の分解を促進する生体触媒で処理することであり、酵素の種類としては特に限定されないが、セルラーゼ、ペクチナーゼ、アラバナーゼ、プロテアーゼ等が好ましく例示される。酵素処理の条件は、各酵素に適した温度、pH、添加量で行えばよい。酵素処理後の反応物は、そのまま以後の発酵に用いてもよいが、失活させるのが好ましい。失活方法は、特に限定されないが、加熱処理が好ましい。
【0030】
本発明において植物処理物は、そのまま用いてもよいが、不溶物を取り除いたものを用いるのが好ましく、特に好ましくは、植物体を粉砕し水抽出した後に濾過滅菌したものを用いるのが好ましい。
【0031】
本発明においては、以上のような操作により得られた植物処理物を、そのままで培地として用いてもよいが、本発明の効果を損なわない限り、従来公知の乳酸菌用の培地と混合してもよい。かかる培地としては、GYP培地、市販のGAM培地(日水製薬)、MRS培地(Difco)等が挙げられる。これらの培地はその全成分を添加してもよいし、任意の1または複数の成分のみを添加してもよい。
【0032】
培地中に占める植物処理物の割合は、特に限定されるものではないが、植物処理物由来の不溶成分を除いた糖濃度(ブリックス(Brix)換算)が0.1〜40%であるのが好ましく、0.1〜20%であるのがより好ましく、0.5〜5%であるのがもっとも好ましい。糖濃度(Brix換算)がこの範囲を外れると、乳酸菌の増殖が極めて悪くなる。糖濃度(ブリックス(Brix)換算)が0.1%に満たない場合には、濃縮して大きくすることができる。糖濃度(ブリックス(Brix)換算)が40%を超える場合には、加水して少なくすればよい。
【0033】
次に、本発明において用いられる乳酸菌について説明する。本発明において用いられる乳酸菌は、その植物処理物を含む培地で培養することによって、免疫調整作用を有する乳酸菌の作用を相乗的に高める効果を有する成分を産生するものであればいかなるものでもよい。その効果の判定は、OVA感作したマウス脾臓細胞からのIFN−γ誘導能またはIgE産生抑制能を指標にすればよく、IFN−γを指標にする場合であれば植物処理物発酵物(菌体除く)と乳酸菌の両方を投与した場合のIFN−γ増加量が、各々単独投与時のIFN−γ増加量の和の1.0倍より高く、より好ましくは1.5倍以上、さらに好ましくは2.0倍以上であればよい。IgE産生抑制能を指標にする場合であれば植物処理物発酵物(菌体除く)と乳酸菌の両方を投与した場合のIgE減少量が、各々単独投与時のIgE減少量の和の1.0より高く、より好ましくは1.5倍以上であればよい。かかる乳酸菌としてはラクトバチルス(Lactobacillus)属に属するものが例示され、より好ましくはラクトバチルス・ブレビス(L.brevis)に属するもの、さらに好ましくは、L.brevis UAS−4(FERM P−20710)、L.brevis UAS−6(FERM P−20711)の菌株である。
【0034】
上記のL.brevis UAS−4(FERM P−20710)、L.brevis UAS−6(FERM P−20711)は、本発明者らがアスパラガスを分離源として分離した菌であり、以下の表1の様な性質を有する。
【0035】
【表1】

また、UAS−4及びUAS−6の16S rRNAのうち5’−末端側の約500塩基についてDNAシーケンサーを用いて特定した結果、いずれも全米バイオテクノロジー情報センター(National center for biotechnology information:NCBI)の保有するラクトバチルス・ブレビス(Lactobacillus brevis)の16S rRNA配列と99%以上の相同性を有していた。
【0036】
UAS−6株については、L−アラビノースの資化性が陰性であり、一般的なL.brevisがL−アラビノースを良好に資化することから鑑みると、この株に特徴的な性質である。また、UAS−4株及びUAS−6株のいずれも、後述するようにグルタミン酸又はグルタミン酸塩からγ−アミノ酪酸の産生能が従来公知のラクトバチルス・ブレビスと比較して顕著に高いことから、新規な乳酸菌であると判断し、独立行政法人産業技術総合研究所特許生物寄託センターに寄託手続を行い、UAS−4株は、受託番号FERM P−20710として、またUAS−6株は、受託番号FERM P−20711として、平成17年11月11日に受託された。
【0037】
本発明においては、上記したような培地に上記したような乳酸菌を接種し、次いで培養を行い乳酸発酵させる。以下、その条件について述べる。
【0038】
乳酸菌の添加方法は、上記のように調整された植物処理物を含有する培地に直接少量の菌体を接種することで増殖させることができるが、短期間で菌体濃度を上昇させる為には、前培養した菌液を接種することが好ましい。前培養液としては、本培養と同じ植物処理物を含有する培地でもよいし、前述の公知のあらゆる培地を使用することもできる。前培養した菌液を接種する量としては、本培養の培地量の100000分の1〜2分の1であり、1000分の1〜10分の1が好ましく、200分の1〜30分の1がさらに好ましい。この範囲より接種量が少なければ、菌体濃度の増加に時間がかかる問題があり、この範囲より多ければもはや前培養の時点で大きなスケールになっており、本培養を行う必要性がないということである。
【0039】
醗酵時の培養温度は用いる菌株にもよるが、5℃〜45℃であり、好ましくは15℃〜40℃であり、さらに好ましくは20℃〜35℃である。培養温度がこの温度範囲より高くても低くても著しく増殖速度が劣る問題がある。
【0040】
醗酵開始時の培地のpHは用いる菌株にもよるが、3.0〜9.0に調整することが好ましく、4.5〜7.5に調整することがより好ましい。pHがこの範囲を外れると、増殖速度が劣る問題がある。pH調整に用いる薬品はいかなる物も使用でき、例えば塩酸、硫酸、リン酸、硝酸、酢酸、酪酸、乳酸、蟻酸、コハク酸、マレイン酸、リンゴ酸、シュウ酸、クエン酸、水酸化ナトリウム、水酸化カリウム、水酸化カルシウム、アンモニア水等が挙げられる。
【0041】
発酵の際の酸素条件は、好気、嫌気のどちらでも構わない。
【0042】
発酵の培養時間は特に限定されないが、2時間〜10日間が好ましく、5時間〜5日間がより好ましく、8時間から〜3日間が最も好ましい。発酵時間がこの範囲を下回ると発酵が不十分になり、この範囲を上回っても、更なる効果は望めず、雑菌の混入や増殖の可能性も高くなる。
【0043】
以上の操作により得られる培養物に乳酸菌の免疫調整作用を相乗的に高める成分が含まれるようになり、この培養物がすなわち本発明の第1の乳酸菌の免疫調整作用を相乗的に高める組成物となる。この組成物はそのままで利用することも可能であるが、必要に応じて殺菌、除菌、固液分離、乾燥等の操作を行い、清澄液や粉末の形態にすることも可能である。また、適当な担体を添加した後常法により顆粒状、粒状、錠剤、カプセル、ゲル状、ペースト状、乳状、懸濁状、液状、飲料等の食用に適した形態に成形してもよい。
【0044】
固形状に調製する際には、賦形剤、結合剤、崩壊剤、滑沢剤、矯味矯臭剤、着色剤等常法で用いられているものを用いればよく、そのような担体の例としては、賦形剤としては乳糖、白糖、ブドウ糖、マンニット、ソルビット、デキストリン、デンプン、結晶セルロース、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、デキストラン、プルラン、無水ケイ酸、リン酸カルシウム、炭酸カルシウム、硫酸カルシウム等を、結合剤としては結晶セルロース、白糖、マンニトール、デキストリン、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ポリビニルピロリドン、アラビアゴム、デキストラン、プルラン、水、エタノール等を、崩壊剤としてはデンプン、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、デキストリン、結晶セルロース等を、滑沢剤としてはステアリン酸およびその金属塩、タルク、ホウ酸、脂肪酸ナトリウム塩、ラウリル硫酸ナトリウム、ラウリル硫酸マグネシウム、無水ケイ酸等を、矯味矯臭剤としては白糖、橙皮、クエン酸、酒石酸等を例示できる。
【0045】
液体状に調製する際には、乳化剤、可溶化剤、分散剤、懸濁化剤、粘調剤、緩衝剤、安定化剤、矯味矯臭剤等常法で用いられているものを用いればよく、乳化剤および可溶化剤としてはレシチン、ショ糖脂肪酸エステル、ソルビタン脂肪酸エステル、ラウリル硫酸ナトリウム等を、分散剤および懸濁化剤としては、レシチン、ショ糖脂肪酸エステル、メチルセルロース、アラビアゴム、ゼラチン等を、粘調剤としてはメチルセルロース、カルボキシメチルセルロース、アラビアゴム、ゼラチン等を、緩衝剤としてはクエン酸塩、コハク酸塩等を、安定化剤としてはレシチン、アラビアゴム、ゼラチン、メチルセルロースを、矯味矯臭剤としては上記したものを例示できる。
【0046】
また、味質の改善のために、糖類、糖アルコール類、塩類、油脂類、アミノ酸類、有機酸類、果汁、野菜汁、香料、香辛料、アルコール類、グリセリン等を添加することができる。また、pH調整のために、塩酸、硫酸、リン酸、酢酸、酪酸、乳酸、コハク酸、リンゴ酸、シュウ酸、クエン酸、水酸化ナトリウム、水酸化カリウム、水酸化カルシウム、アンモニア水等を添加することができる。
【0047】
次に、本発明の第3の免疫調整作用を有する組成物について説明する。該組成物は、本発明の第1の乳酸菌の免疫調整作用を相乗的に高める組成物と、免疫調整作用を有する乳酸菌とを含有する組成物である。
【0048】
ここで用いられる免疫調整作用を有する乳酸菌としては既知のいかなるものでもよく、かかる乳酸菌としては、ラクトバチルス属、ビフィドバクテリウム(Bifidobacterium)属、ストレプトコッカス(Streptococcus)属、テトラジェノコッカス(Tetragenococcus)属、ペディオコッカス(Pediococcus)属、ロイコノストック(Leuconostoc)属が例示され、さらにはラクトバチルス・ブレビス(L.brevis)、ラクトバチルス・パラカゼイ(L.paracasei)、ラクトバチルス・ペントーサス(L.pentosus)、ラクトバチルス・アシドフィルス(L.acidophilus)、ラクトバチルス・プランタラム(L.plantarum)、ラクトバチルス・カゼイ(L.casei)、ラクトバチルス・ロイテリ(L.reuteri)、ビフィドバクテリウム・ロンガム(B.longum)、ストレプトコッカス・フェーカリス(S.faecalis)、ストレプトコッカス・ラクティス(S.lactis)、テトラジェノコッカス・ハロフィラ(T.halophilus)、ペティオコッカス・ペントサセウス(P.pentosaseus)、ペディオコッカス・アシディラクティシ(P.acidilactici)、ペディオコッカス・セレビシエ(P.cerevisiae)、ロイコノストック・メセントロイデス(Leuconostoc mesenteroides)等が例示される。
【0049】
これらの中で、本発明者らがアスパラガスを分離源として分離した菌株である、L.brevis UAS−4(FERM P−20710)、L.brevis UAS−6(FERM P−20711)が好ましい。この2菌株の性質は前記した表1に示したとおりであり、新菌株として独立行政法人産業技術総合研究所特許生物寄託センターに寄託されている。
【0050】
免疫調整作用を有する乳酸菌の培養方法は、GYP培地、市販のGAM培地(日水製薬)、MRS培地(Difco)等、従来公知の乳酸菌用の培地を用い、培養方法も従来公知の方法によって行えばよい。
【0051】
そして、このようにして得られた培養液をそのままで、あるいは培養液から遠心または濾過等の固液分離操作によって集菌した菌体を、本発明の第1の組成物と混合する。本発明の第1の組成物との混合比率は、乾燥重量にして、免疫調整能を有する乳酸菌を1とした場合、本発明第1の組成物が0.1〜200、より好ましくは0.2〜100、さらに好ましくは0.5〜50である。
【0052】
また、混合の前後において適宜乾燥等の操作を行い粉末の形態にすることも可能であり、適当な担体を添加した後常法により顆粒状、粒状、錠剤、カプセル、ゲル状、ペースト状、乳状、懸濁状、液状、飲料等の食用に適した形態に成形してもよい。
【0053】
次に本発明の第4の飲食品又は飼料について説明する。
【0054】
本発明の飲食品又は飼料は、上述のようにして製造した本発明の第1又は第2の組成物を含有することを特徴とするものである。飲食品中又は飼料中における本発明の組成物の含有量は、特に限定されず本発明の組成物それ自身を飲食品又は飼料とすることも可能であるが、概ね本発明の第1の組成物の場合は1日当たり20〜1,000mgになるように配合することが好ましく、本発明の第2の組成物の場合は乳酸菌の乾燥重量として1日当たり10mg〜500mgになるように調整すればよい。この範囲より少ない場合は効果が望めない可能性があり、この範囲より多い場合はもはや効果の増大は見込ず、さらに日常摂取が困難な可能性がある。
【0055】
本発明の組成物を既存の飲食品或いは調味食品に含ませる場合は、ベースとなる飲食品或いは調味食品としては特に限定されないが、例えば、うどんやパスタ等の加工麺、ハム・ソーセージ等の食肉加工食品、かまぼこ・ちくわ等の水産加工食品、バター・粉乳・醗酵乳等の乳加工品、ゼリー・アイスクリーム等のデザート類、パン類、菓子類、調味料類等の加工食品、および、清涼飲料水、アルコール類、果汁飲料、野菜汁飲料、乳飲料、炭酸飲料、コーヒー飲料、アルコール類等の飲料が好ましい。
【0056】
飲食品或いは調味食品に含ませる本発明の組成物の形態は特に限定されず、飲料、グミ、キャンデーなどにおいては液体状の物を、錠剤、顆粒、カプセルなどにおいては粉末状の物を使用するなどすればよい。
【実施例】
【0057】
以下、実施例により本発明を具体的に説明するが、本発明は何らこれらに限定されるものではない。
【0058】
実験例1(植物処理物を発酵可能な乳酸菌株の単離、同定)
乳酸菌株は植物処理物中で増殖できることを条件に探索した。野菜、果物、漬物などの各種食品から被検試料を適量サンプリングし、生理食塩水にて希釈懸濁してGYP白亜寒天培地に混釈培養し、これから周囲に透明な層を形成する代表的コロニーを釣菌し、さらにこれをGYP寒天培地に画線し培養する操作を繰り返して乳酸菌の純粋分離を行なった。得られた分離乳酸菌株を以下の植物処理物中で30℃、24時間静置培養を行い、培養液の濁度(O.D.660の値)が2.0を超えたものだけを選別した。植物処理物は、アスパラガスに加水、ミルミキサーで粉砕し、加熱殺菌(85℃、30分)した後、珪藻土濾過して得られた清澄濾液をBrixが2.0%になるよう調整、オートクレーブ滅菌したものを用いた。この操作で乳酸菌株14株を得た。この14株の16SrRNA配列のうち5’−末端側の約500塩基について解読し、相同性検索を行ったところ、Lactobacillus brevisが4株、Lactobacillus pentosusが4株、Lactobacillus plantarumが3株、Lactobacillus hilgardiiが1株、Pediococcus petosaseusが2株であった。
【0059】
実験例2(免疫調整作用を有する乳酸菌の選抜)
実施例1で得られた14株の乳酸菌をアスパラガス処理物中で30℃、48時間静置培養した。アスパラガス処理物は実施例1の操作に加え、オートクレーブ前に酵母エキスを1重量%添加したものを用いた。培養終了後、100℃で5分間処理し、滅菌生理食塩水で2回遠心洗浄し、以下の試験のサンプルとした。なお、培養終了後の上清は実施例3、4で使用している。
【0060】
Balb/Cマウス雌性6週齢(日本チャールスリバー)に2mgの水酸化アルミニウムゲルに20μgの卵白アルブミン(以下、OVAという。)を吸収させた生理食塩水溶液200μlを腹腔内投与し、10日目に脾臓を回収した。脾臓細胞を調整し、20%FBSを含むRPMI−1640培溶液に懸濁し、100μg/mlのOVA共存下で分離乳酸菌体を10μg(乾燥重量)/mlとなるように添加して共培養した。7日後、培養上清を回収し、IFN−γをELISA法で定量した。単離乳酸菌株のIFN−γ誘導活性を表2に示した。結果、ラクトバチルス・ブレビスUAS−4株に強力なIFN−γ誘導活性が見出された。なお、この菌株は特許生物寄託センターへの寄託を行っており、その受託番号はFERM P−20710である。
【0061】
【表2】

実施例1(植物処理物発酵液が持つ、乳酸菌の免疫調整作用への影響)
強力なIFN−γ誘導能を有する乳酸菌株ラクトバチルス ブレビス UAS−4が得られたので、この菌株を指標にして、各菌株の植物処理物の発酵液が、免疫調整作用に及ぼす影響を比較した。
【0062】
植物処理物は、実験例2で作製したアスパラガス処理物の発酵液を85℃、30分殺菌処理後、珪藻土濾過し凍結乾燥したものを用いた(以下、AFと略す)。また、乳酸菌体は実験例2で作製したラクトバチルス ブレビス UAS−4の凍結乾燥物を用いた。
【0063】
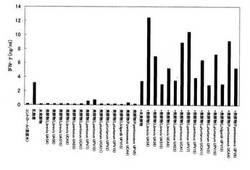
脾臓細胞からのIFN−γ産生量の測定実験は実験例2の方法に従って行い、サンプルとしてはラクトバチルス ブレビス UAS−4株菌体 5μg/ml、各菌株によるAF 5μg/mlのそれぞれを単独或いは混合して添加した。また、未発酵前のアスパラガス処理物(凍結乾燥物)についても、単独或いは乳酸菌株と混合した場合のIFN−γ生産能を調べた。結果を図1に示す。
【0064】
図1に示した通り、乳酸菌体を除いたAFには、全く或いはほとんどINF-γ産生能がないが、ラクトバチルス ブレビス UAS−4株と併用すると、いくつかの菌株によるAFでIFN−産生能に相乗効果が見られた。特にラクトバチルス ブレビス UAS−4株によって産生されたAFが最も相乗効果に優れており、IFN−γ産生量は3.97倍に達した。
【0065】
実施例2(植物処理物発酵物の効果の乳酸菌株による違い)
実施例1でAFがラクトバチルス ブレビス UAS−4株の免疫調整作用を相乗的に高めることが確認されたので、他の菌株に対するAFの効果を検証した。
【0066】
AFは実施例1で作製したもののうち、ラクトバチルス ブレビス UAS−4株によるもの、各乳酸菌体は実験例2で作製したものの凍結乾燥物を用いた。
【0067】
脾臓細胞からのIFN−γ産生量の測定実験は実施例2の方法に従って行い、サンプルとしては各乳酸菌体 5μg/ml、AF 5μg/mlのそれぞれを単独或いは混合して添加した。結果を図2に示す。
【0068】
図から明らかな通り、ラクトバチルス ブレビス UAS−4株の発酵により得られたAFは、その他の乳酸菌株に対しても相乗的に免疫調整作用を高めた。
【0069】
実施例3(植物による効果の違い)
次に、アスパラガス以外の植物処理物の発酵物に本発明の効果があるかを確認した。アスパラガス、ニンジン、トマト、キャベツ各1kgにそれぞれ水1Lを添加して家庭用のミキサーで粉砕し、85℃30分間加熱殺菌した。その後、珪藻土を添加し、濾紙(ADVANTEC東洋製No.5C)を用いて吸引濾過を行い、清澄な濾液を得た。この各濾液を濃縮或いは水で希釈しBrixを2.5%に調整した。次に、酵母エキスを1重量%溶解し85℃30分間再殺菌した。得られた培地1Lに、GYP培地のグルコースをフルクトースに換えたFYP培地で30℃、24時間静置して前培養したラクトバチルス ブレビス UAS−4株の前培養液を10ml接種した。30℃で48時間静置培養した後85℃30分間加熱殺菌した後、珪藻土濾過により除菌した清澄濾液を得、凍結乾燥した。アスパラガス、ニンジン、トマト、キャベツから得られたものは以下AF、CRF、TF、CBFと略す。また、乳酸菌体は実施例2で作製したラクトバチルス ブレビス UAS−4の凍結乾燥物を用いた。
【0070】
脾臓細胞からのIFN−γ産生量の測定実験は実施例2の方法に従って行い、サンプルとしてはラクトバチルス ブレビス UAS−4株菌体 5μg/ml、各植物発酵物 5μg/mlのそれぞれを単独或いは混合して添加した。結果を図3に示す。
【0071】
図から明らかな通り、各植物の発酵物は、いずれも乳酸菌のもつ免疫調整作用を相乗的に高めた。なかでも、アスパラガス発酵物が最も優れていた。
【0072】
試験例1<マウスにおける抗アレルギー作用の検討>
植物処理物発酵物に、乳酸菌のIFN−γ産生促進作用を相乗的に高めることが確認されたので、マウスアレルギーモデルを用いて血中IgEレベルが抑制されるか検討した。すなわち、Balb/Cマウス雌性6週齢(日本チャールスリバー)に2mgの水酸化アルミニウムゲルに20μgのOVAを吸収させた生理食塩水溶液100μlを腹腔内投与し、血中OVA特異的IgEを誘導した。OVAの腹腔内投与は0週目、2週目、5週目、8週目に行い、1)コントロール餌、2)AF入りの餌、3)乳酸菌体入りの餌、4)AFおよび乳酸菌体入りの餌を0週目からマウスに摂取させた。乳酸菌体はラクトバチルス ブレビス UAS−4株で実験例2と同じ方法で、AFは実施例3と同じ方法で作製したものを用いた。摂取量は乳酸菌体、AFともに5mg/1週目、3週目、6週目、9週目に採血して血清を調整し、血中OVA特異的IgEをELISA法により定量した。測定結果を図4に示す。この結果から、乳酸菌体単独でも有意差はなかったものの血中OVA特異的IgEの上昇が抑制される傾向にあり、AFと乳酸菌を併せて摂取した場合はさらに抑制され有意差を得られるほどであった。
【0073】
製造例1
以下に示す方法により、植物処理物発酵物を含有する医薬品(錠剤)を製造した。
【0074】
実施例3と同じ方法により製造したAFまたはCRF乾燥物60gを乳糖230gおよびステアリン酸マグネシウム1gとともに混合し、単発式打錠機にて打錠することにより、直径12mm、重量320mgの錠剤を製造した。
【0075】
製造例2
以下に示す方法により、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有する医薬品(錠剤)を製造した。
【0076】
実施例3と同じ方法により製造したAF乾燥物60g、実施例2と同じ方法で得たラクトバチルス ブレビス UAS−4株またはラクトバチルス ペントーサス UPV7株20g、乳糖230gおよびステアリン酸マグネシウム1gとともに混合し、単発式打錠機にて打錠することにより、直径12mm、重量320mgの錠剤を製造した。
【0077】
製造例3
以下に示す方法により、植物処理物発酵物を含有するウーロン茶を製造した。
実施例3と同じ方法により製造したAFまたはCRF乾燥物50gを日本粉末薬品(株)製「ウーロン茶エキスパウダー」950gと混合し、植物処理物発酵物を含有するウーロン茶粉末を製造した。このウーロン茶粉末5gを水500mlに溶解したところ、速やかに溶け、味も良好なものであった。
【0078】
製造例4
以下に示す方法により、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有するウーロン茶を製造した。
【0079】
実施例3と同じ方法により製造したAF乾燥物50g、実施例2と同じ方法で得たラクトバチルス ブレビス UAS−4株またはラクトバチルス ペントーサス UPV7株25gを日本粉末薬品(株)製「ウーロン茶エキスパウダー」925gと混合し、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有するウーロン茶粉末を製造した。このウーロン茶粉末5gを水500mlに溶解したところ、独特の触感のある、良好な味のするウーロン茶ができた。
【0080】
製造例5
以下の方法により、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有する醗酵乳飲料を製造した。
【0081】
脱脂粉乳20%、実施例5と同じ方法により製造したAFの、凍結乾燥前の清澄濾液を50%含有する培地1Lに、前培養して定常状態となっているラクトバチルス ブレビス UAS−4の菌体懸濁液を10mL添加して30℃、静置の条件で、36時間培養することにより、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有する醗酵乳飲料が得られた。
【0082】
製造例6
以下に示す方法により、植物処理物発酵物を含有する麺を製造した。
【0083】
実施例3と同じ方法により製造したAFまたはCRF乾燥物を1w/w%になるよう中力粉と混合し、うどんの麺を作製した。この麺を調理したうどんを食したところ、微かに甘味と爽やかな香りを感じる良好な麺であった。
【図面の簡単な説明】
【0084】
【図1】本発明の実施例1において、各種乳酸菌のアスパラガス処理物醗酵物、ラクトバチルス ブレビスUAS−4株菌体、およびそれらを併用したときのマウス脾臓細胞からのIFN−γ産生能を示す図である。
【図2】本発明の実施例2において、各種乳酸菌体、ラクトバチルス ブレビスUAS−4株によるアスパラガス処理物醗酵物(AF)、およびそれらを併用したときのマウス脾臓細胞からのIFN−γ産生能を示す図である。
【図3】本発明の実施例3において、ラクトバチルス ブレビスUAS−4株菌体、各種乳酸菌体による各種植物処理物醗酵物、およびそれらを併用したときのマウス脾臓細胞からのIFN−γ産生能を示す図である。
【図4】本発明の実施例4において、ラクトバチルス ブレビスUAS−4株菌体、アスパラガス処理物醗酵物、およびそれらを併用したときのマウスの血中OVA特異的IgE量を示す図である。
【技術分野】
【0001】
本発明は、乳酸菌の持つ免疫調整作用を相乗的に高める組成物、その製造法及びその飲食品及び飼料としての利用などに関するものである。
【背景技術】
【0002】
近年我が国では、花粉症、アトピー性皮膚炎、蕁麻疹、アレルギー性の鼻炎、結膜炎、喘息、アナフィラキシーショック、食物アレルギーといったアレルギー疾患の患者数が増加し、特に、花粉症は国民の2割近くが罹患しているとされており「国民病」の様相を呈している。
【0003】
一方、がんは国民の死亡原因の第1位であり、がんに対する有効な予防法が求められている。
【0004】
乳酸菌は有益な免疫調整作用を有することが知られており、抗アレルギー作用や抗腫瘍作用についても見出されている。
【0005】
花粉症やアレルギー性の鼻炎、結膜炎といった環境アレルギーは、I型アレルギーに分類される発症機構をもつことが知られており、抗原特異的IgE誘導とマスト細胞等からのヒスタミン等のケミカルメディエーターの放出を特徴とする。IgEはB細胞がクラススイッチされて産生されるが、そのクラススイッチを引き起こすのが、抗原を認識するヘルパーT細胞のうちTh2細胞から放出されるサイトカイン類(IL−4、IL−5、IL−6等)である。実際に、アレルギー患者ではリンパ球のTh2細胞が増加していることが分かっている。
【0006】
乳酸菌は、Th1細胞免疫を増強することで、Th2免疫を抑制し結果としてIgE量を低下させることが報告されている。また、Th1免疫を増強することは、インターフェロン−ガンマ(以下、IFN−γという。)やIL−12の産生を促し、NK細胞やマクロファージなどを含む細胞性免疫が活性化され、ガンの発生に対する抵抗力が増すことが明らかとなっている(特許文献1)。
【0007】
一方、積極的なIFN−γ産生誘導がIgEの産生を抑制することもすでに明らかになっており(特許文献2)、強力なIFN-γ誘導能やIgE産生抑制能をもつ乳酸菌は、抗腫瘍作用および抗アレルギー作用を有しているといえる。
【0008】
こうした乳酸菌としては、ラクトバチルス・ブレビス(特許文献3)、ラクトバチルス・アシドフィルス(L.acidphilus)AHU1402株、ラクトバチルス・カゼイ(L.casei)AHU1696株、ラクトバチルス・プランタラム(L.plantarum)L−137株、ストレプトコッカス・フェーカリス(Streptococcus faecalis)AHU1257株(特許文献1)、ラクトバチルス・パラカゼイ(L.paracasei)KW3110(特許文献4)、ラクトバチルス・ペントーサス(L.pentosus)S−PT84株(特許文献5)等が挙げられる。
【0009】
これらの乳酸菌は、サプリメントの形態か発酵物の形態で摂取されているが、必ずしも効果が満足できるものではなく、また、サプリメントの形態であれば必要な菌体量が多くなりコスト高になるという問題が、発酵物の形態であれば摂取量が多くなり継続摂取が困難であるという問題があった。
【0010】
これらの問題を解決する方法としては、他の免疫調整物質や、乳酸菌の効果を高めるとされる物質を併用する方法が試みられている。例えば、特開2003−38122号公報(特許文献6)では、アガリクス・ブラゼイを乳酸発酵させ、ビタミンB17および/または杏仁種子粉を含有させる方法が示されているが、その効果は各成分の効果の相加以下であり、満足いくものではない。また、アスコルビン酸と併用する方法(特許文献7)、ビタミンEと併用する方法(特許文献8)等が試みられているが、いまだ満足いくものではなかった。さらに、アスコルビン酸は熱に弱く、ビタミンEは脂溶性であり、扱いが難しいという問題点もあった。
【0011】
また、乳酸菌を大豆抽出液を含有する培地で培養すると乳酸菌自体の免疫賦活能が高まる(特許文献9)、乳酸発酵によって発酵物(乳酸菌体を除く)が免疫賦活能を有するようになることが報告されているが、上記問題を解決できるものではなかった。
【特許文献1】特開2002−80364号公報
【特許文献2】特開2005−139160号公報
【特許文献3】特公平7−55908号公報
【特許文献4】特開2005−137357号公報
【特許文献5】特開2005−333919号公報
【特許文献6】特開2003−38122号公報
【特許文献7】特開2001−64174号公報
【特許文献8】特開2002−80364号公報
【特許文献9】特開2004−357535号公報
【発明の開示】
【発明が解決しようとする課題】
【0012】
本発明は、乳酸菌の持つ免疫調整作用、特に、IFN−γ産生促進能、IgE産生抑制能を相乗的に高める組成物やその製造法及びその飲食品及び飼料としての利用法、その乳酸菌との配合物を提供するものである。
【課題を解決するための手段】
【0013】
本発明者らは、上記の課題を解決するために鋭意検討した結果、ラクトバチルス属の乳酸菌を用いて特定の野菜処理物を含有する培養液を乳酸発酵して得られた組成物に、免疫調整作用を有する乳酸菌の効果を相乗的に高める効果があることを見出し、本発明を完成させるに至った。本発明者らは、ラクトバチルス・ブレビス UAS−4株でアスパラガス処理物を含有する培養液を乳酸発酵して得られた組成物に、該組成物中に含まれる乳酸菌と同量の乳酸菌より強い免疫調整作用があることを既に報告しているが、本発明は該組成物の乳酸菌以外の成分を鋭意検討して見出されたものである。
【0014】
すなわち、本発明の第1は、植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物からなることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物を要旨とするものであり、好ましくは、培養物から乳酸菌を除いた成分が、免疫調製作用を有しない成分である前記の組成物であり、また好ましくは、免疫調整作用が、抗アレルギー作用、抗腫瘍作用、IFN−γ産生能を促進するもの、又はIgE抗体産生能を抑制するものである前記の組成物であり、また好ましくは、乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である前記の組成物であり、さらに好ましくは、植物処理物が、アスパラガスを処理したものである前記の組成物である。
【0015】
本発明の第2は、植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物から乳酸菌の免疫調整作用を相乗的に高める組成物を得ることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物の製造方法を要旨とするものである。
【0016】
本発明の第3は、本発明の第1の組成物と、免疫調整作用を有する乳酸菌とを含有することを特徴とする免疫調整作用を有する組成物を要旨とするものであり、好ましくは、免疫調整作用を有する乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である前記の組成物である。
【0017】
本発明の第4は、本発明の第1の組成物又は本発明の第3の組成物を含有することを特徴とする飲食品又は飼料を要旨とするものである。
【発明の効果】
【0018】
本発明によれば、乳酸菌の免疫調整作用を相乗的に高めることが可能となり、より優れた免疫調整作用を有する組成物の製造が可能となる。また、乳酸菌の摂取量を低減することが可能となり、継続摂取を容易にすることができる。
【発明を実施するための最良の形態】
【0019】
以下、本発明の第1及び第2について説明する。
【0020】
本発明に用いられる植物としては、食経験があり、その抽出液中で乳酸菌が増殖可能であればいかなるものでもよく、野菜類、果実類、穀類、いも類、豆類、藻類、キノコ類等が挙げられる。野菜類の例としては、アスパラガス、トマト、カボチャ、タケノコ、ゴボウ、ダイコン、ニンジン、キュウリ、ピーマン、カリフラワー、ブロッコリー、ナス、トウモロコシ、タマネギ、ラッキョウ、ニンニク、ネギ、レタス、キャベツ、ハクサイ、セロリ、ニラ、ホウレンソウ、コマツナ、シュンギク、ケール等が挙げられる。果実類の例としては、アケビ、アセロラ、アボガド、アンズ、イチゴ、イチジク、ウメ、ミカン、オレンジ、カキ、キウィ、グレープフルーツ、サクランボ、ザクロ、スイカ、モモ、スモモ、ナシ、パインアップル、バナナ、ブドウ、ビワ、マンゴー、マンゴスチン、メロン、ライチ、ラズベリー、ブルーベリー、リンゴ、レモン、ライム、ユズ、カボス、スダチ、アーモンド、ギンナン、クリ、クルミ、カシューナッツ、ココナッツ、マカダミアナッツ、ヘーゼルナッツ、ゴマ、ピスタチオ、ラッカセイ、松の実、蓮の実、カボチャの種等が挙げられる。穀類の例としては、米、麦、粟、ソバ、ひえ等が挙げられる。いも類の例としては、サツマイモ、ジャガイモ、サトイモ、ヤマイモ、キャッサバ、キクイモ等が挙げられる。豆類の例としては、アズキ、インゲンマメ、エンドウ、ソラマメ、ダイズ、ヒヨコマメ、レンズマメ等が挙げられる。藻類の例としては、コンブ、ワカメ、ヒジキ、ノリ、テングサ、モズク等が挙げられる。キノコ類の例としては、アガリクス、エノキタケ、キクラゲ、シイタケ、ホンシメジ、ブナシメジ、ハタケシメジ、ナメコ、エリンギ、ヒラタケ、マイタケ、マツタケ、マッシュルーム、ハナビラタケ等が挙げられる。これらの中でも、アスパラガスが、本発明の効果を発揮するのに最も好ましい。また、これらの植物は単独で用いてもよいし、2つ以上を組み合せて用いてもよい。
【0021】
本発明で用いられる植物処理物とは、上記したような植物を必要に応じて粉砕、細断、抽出、圧搾、濃縮、固液分離、加熱滅菌、濾過滅菌、酵素処理等公知の技術を単独或いは2つ以上組み合せて処理することで植物破砕物、磨砕物、粉砕物、搾汁、抽出物、酵素処理物が得られる。
【0022】
粉砕、細断とは物理的に植物体を細かく破砕する方法であり、粉砕は衝撃により、細断は切断によって破砕する。粉砕、細断は乳鉢や包丁、カッターナイフ、ハサミなどを用いて手作業で行っても良いが、大量の植物体を短時間で処理しようとする場合には装置を使用する。そのような装置としては、例えば、ミル、ハンマー式粉砕機、石臼式粉砕機、ミキサー、ブレンダーなどが挙げられ、また野菜用の細断機を用いてもよい。粉砕、細断された植物体の大きさは特に限定されないが、2cm以下が好ましく、5mm以下がより好ましい。
【0023】
抽出とは、溶媒を加え植物体の成分をそこに移行せしめる操作である。加える溶媒としては水が最も好ましいが、有機溶媒を併用してもよい。有機溶媒は、抽出時に水と併用してもよいし、抽出は有機溶媒単独で行い、その後水と混合してもよい。また、抽出は有機溶媒単独で行い、その後濃縮乾固等の操作により有機溶媒を除去した後、水を加えてもよい。有機溶媒の種類は特に限定されないが、食品に使用可能な点でエタノールが好ましい。抽出する際の溶媒の温度は、水の場合は0℃〜100℃が好ましく、10℃〜80℃がより好ましく、また、有機溶媒の場合は−20℃〜200℃が好ましく、0℃〜120℃がより好ましい。
【0024】
圧搾とは、植物体に物理的な圧力をかけて液を搾り出し、成分を搾汁に移行せしめる方法である。圧力は一方向のみにかけてもよいし、二以上の方向からかけてもよく、せん断力を伴わせることもできる。圧搾の操作は市販の圧搾機を用いれば容易であるが、手搾り、足踏み搾りなど機械を用いない方法で行ってもよい。このとき、植物体に水や湯を加えて圧搾してもよい。
【0025】
濃縮とは、他の成分を減少させること無く水分量、溶媒量を減らす操作であり、減圧濃縮、加熱濃縮、濾過膜を用いた濃縮などいかなる方法で行ってもよいが、20℃〜60℃の範囲での減圧濃縮を行うことが好ましい。
【0026】
固液分離とは、溶媒およびそこに溶解している成分と、不溶性の固形分を分離する方法であり、分離方法としては、例えばフィルター濾過、圧搾濾過、遠心分離、デカンテーションなどあらゆる方法が使用できる。清澄な植物抽出液を得る場合には、珪藻土などの濾過助剤を使用したフィルター濾過を行うことが好ましい。
【0027】
加熱滅菌とは、熱を加えて殺菌することであり、温度は60℃〜121℃が好ましく、70℃〜110℃がさらに好ましい。この温度範囲より低ければ、滅菌の効果が不十分になる問題があり、この温度範囲より高ければ有効成分が分解する問題がある。
【0028】
濾過滅菌とは、微生物が通過できないサイズの膜を、加圧或いは減圧して通過させることで除菌する操作である。膜の孔径としては0.1〜1.0μmが好ましく、より好ましくは0.2〜0.45μmである。
【0029】
酵素処理とは、植物体の構成成分の分解を促進する生体触媒で処理することであり、酵素の種類としては特に限定されないが、セルラーゼ、ペクチナーゼ、アラバナーゼ、プロテアーゼ等が好ましく例示される。酵素処理の条件は、各酵素に適した温度、pH、添加量で行えばよい。酵素処理後の反応物は、そのまま以後の発酵に用いてもよいが、失活させるのが好ましい。失活方法は、特に限定されないが、加熱処理が好ましい。
【0030】
本発明において植物処理物は、そのまま用いてもよいが、不溶物を取り除いたものを用いるのが好ましく、特に好ましくは、植物体を粉砕し水抽出した後に濾過滅菌したものを用いるのが好ましい。
【0031】
本発明においては、以上のような操作により得られた植物処理物を、そのままで培地として用いてもよいが、本発明の効果を損なわない限り、従来公知の乳酸菌用の培地と混合してもよい。かかる培地としては、GYP培地、市販のGAM培地(日水製薬)、MRS培地(Difco)等が挙げられる。これらの培地はその全成分を添加してもよいし、任意の1または複数の成分のみを添加してもよい。
【0032】
培地中に占める植物処理物の割合は、特に限定されるものではないが、植物処理物由来の不溶成分を除いた糖濃度(ブリックス(Brix)換算)が0.1〜40%であるのが好ましく、0.1〜20%であるのがより好ましく、0.5〜5%であるのがもっとも好ましい。糖濃度(Brix換算)がこの範囲を外れると、乳酸菌の増殖が極めて悪くなる。糖濃度(ブリックス(Brix)換算)が0.1%に満たない場合には、濃縮して大きくすることができる。糖濃度(ブリックス(Brix)換算)が40%を超える場合には、加水して少なくすればよい。
【0033】
次に、本発明において用いられる乳酸菌について説明する。本発明において用いられる乳酸菌は、その植物処理物を含む培地で培養することによって、免疫調整作用を有する乳酸菌の作用を相乗的に高める効果を有する成分を産生するものであればいかなるものでもよい。その効果の判定は、OVA感作したマウス脾臓細胞からのIFN−γ誘導能またはIgE産生抑制能を指標にすればよく、IFN−γを指標にする場合であれば植物処理物発酵物(菌体除く)と乳酸菌の両方を投与した場合のIFN−γ増加量が、各々単独投与時のIFN−γ増加量の和の1.0倍より高く、より好ましくは1.5倍以上、さらに好ましくは2.0倍以上であればよい。IgE産生抑制能を指標にする場合であれば植物処理物発酵物(菌体除く)と乳酸菌の両方を投与した場合のIgE減少量が、各々単独投与時のIgE減少量の和の1.0より高く、より好ましくは1.5倍以上であればよい。かかる乳酸菌としてはラクトバチルス(Lactobacillus)属に属するものが例示され、より好ましくはラクトバチルス・ブレビス(L.brevis)に属するもの、さらに好ましくは、L.brevis UAS−4(FERM P−20710)、L.brevis UAS−6(FERM P−20711)の菌株である。
【0034】
上記のL.brevis UAS−4(FERM P−20710)、L.brevis UAS−6(FERM P−20711)は、本発明者らがアスパラガスを分離源として分離した菌であり、以下の表1の様な性質を有する。
【0035】
【表1】

また、UAS−4及びUAS−6の16S rRNAのうち5’−末端側の約500塩基についてDNAシーケンサーを用いて特定した結果、いずれも全米バイオテクノロジー情報センター(National center for biotechnology information:NCBI)の保有するラクトバチルス・ブレビス(Lactobacillus brevis)の16S rRNA配列と99%以上の相同性を有していた。
【0036】
UAS−6株については、L−アラビノースの資化性が陰性であり、一般的なL.brevisがL−アラビノースを良好に資化することから鑑みると、この株に特徴的な性質である。また、UAS−4株及びUAS−6株のいずれも、後述するようにグルタミン酸又はグルタミン酸塩からγ−アミノ酪酸の産生能が従来公知のラクトバチルス・ブレビスと比較して顕著に高いことから、新規な乳酸菌であると判断し、独立行政法人産業技術総合研究所特許生物寄託センターに寄託手続を行い、UAS−4株は、受託番号FERM P−20710として、またUAS−6株は、受託番号FERM P−20711として、平成17年11月11日に受託された。
【0037】
本発明においては、上記したような培地に上記したような乳酸菌を接種し、次いで培養を行い乳酸発酵させる。以下、その条件について述べる。
【0038】
乳酸菌の添加方法は、上記のように調整された植物処理物を含有する培地に直接少量の菌体を接種することで増殖させることができるが、短期間で菌体濃度を上昇させる為には、前培養した菌液を接種することが好ましい。前培養液としては、本培養と同じ植物処理物を含有する培地でもよいし、前述の公知のあらゆる培地を使用することもできる。前培養した菌液を接種する量としては、本培養の培地量の100000分の1〜2分の1であり、1000分の1〜10分の1が好ましく、200分の1〜30分の1がさらに好ましい。この範囲より接種量が少なければ、菌体濃度の増加に時間がかかる問題があり、この範囲より多ければもはや前培養の時点で大きなスケールになっており、本培養を行う必要性がないということである。
【0039】
醗酵時の培養温度は用いる菌株にもよるが、5℃〜45℃であり、好ましくは15℃〜40℃であり、さらに好ましくは20℃〜35℃である。培養温度がこの温度範囲より高くても低くても著しく増殖速度が劣る問題がある。
【0040】
醗酵開始時の培地のpHは用いる菌株にもよるが、3.0〜9.0に調整することが好ましく、4.5〜7.5に調整することがより好ましい。pHがこの範囲を外れると、増殖速度が劣る問題がある。pH調整に用いる薬品はいかなる物も使用でき、例えば塩酸、硫酸、リン酸、硝酸、酢酸、酪酸、乳酸、蟻酸、コハク酸、マレイン酸、リンゴ酸、シュウ酸、クエン酸、水酸化ナトリウム、水酸化カリウム、水酸化カルシウム、アンモニア水等が挙げられる。
【0041】
発酵の際の酸素条件は、好気、嫌気のどちらでも構わない。
【0042】
発酵の培養時間は特に限定されないが、2時間〜10日間が好ましく、5時間〜5日間がより好ましく、8時間から〜3日間が最も好ましい。発酵時間がこの範囲を下回ると発酵が不十分になり、この範囲を上回っても、更なる効果は望めず、雑菌の混入や増殖の可能性も高くなる。
【0043】
以上の操作により得られる培養物に乳酸菌の免疫調整作用を相乗的に高める成分が含まれるようになり、この培養物がすなわち本発明の第1の乳酸菌の免疫調整作用を相乗的に高める組成物となる。この組成物はそのままで利用することも可能であるが、必要に応じて殺菌、除菌、固液分離、乾燥等の操作を行い、清澄液や粉末の形態にすることも可能である。また、適当な担体を添加した後常法により顆粒状、粒状、錠剤、カプセル、ゲル状、ペースト状、乳状、懸濁状、液状、飲料等の食用に適した形態に成形してもよい。
【0044】
固形状に調製する際には、賦形剤、結合剤、崩壊剤、滑沢剤、矯味矯臭剤、着色剤等常法で用いられているものを用いればよく、そのような担体の例としては、賦形剤としては乳糖、白糖、ブドウ糖、マンニット、ソルビット、デキストリン、デンプン、結晶セルロース、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、デキストラン、プルラン、無水ケイ酸、リン酸カルシウム、炭酸カルシウム、硫酸カルシウム等を、結合剤としては結晶セルロース、白糖、マンニトール、デキストリン、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ポリビニルピロリドン、アラビアゴム、デキストラン、プルラン、水、エタノール等を、崩壊剤としてはデンプン、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、デキストリン、結晶セルロース等を、滑沢剤としてはステアリン酸およびその金属塩、タルク、ホウ酸、脂肪酸ナトリウム塩、ラウリル硫酸ナトリウム、ラウリル硫酸マグネシウム、無水ケイ酸等を、矯味矯臭剤としては白糖、橙皮、クエン酸、酒石酸等を例示できる。
【0045】
液体状に調製する際には、乳化剤、可溶化剤、分散剤、懸濁化剤、粘調剤、緩衝剤、安定化剤、矯味矯臭剤等常法で用いられているものを用いればよく、乳化剤および可溶化剤としてはレシチン、ショ糖脂肪酸エステル、ソルビタン脂肪酸エステル、ラウリル硫酸ナトリウム等を、分散剤および懸濁化剤としては、レシチン、ショ糖脂肪酸エステル、メチルセルロース、アラビアゴム、ゼラチン等を、粘調剤としてはメチルセルロース、カルボキシメチルセルロース、アラビアゴム、ゼラチン等を、緩衝剤としてはクエン酸塩、コハク酸塩等を、安定化剤としてはレシチン、アラビアゴム、ゼラチン、メチルセルロースを、矯味矯臭剤としては上記したものを例示できる。
【0046】
また、味質の改善のために、糖類、糖アルコール類、塩類、油脂類、アミノ酸類、有機酸類、果汁、野菜汁、香料、香辛料、アルコール類、グリセリン等を添加することができる。また、pH調整のために、塩酸、硫酸、リン酸、酢酸、酪酸、乳酸、コハク酸、リンゴ酸、シュウ酸、クエン酸、水酸化ナトリウム、水酸化カリウム、水酸化カルシウム、アンモニア水等を添加することができる。
【0047】
次に、本発明の第3の免疫調整作用を有する組成物について説明する。該組成物は、本発明の第1の乳酸菌の免疫調整作用を相乗的に高める組成物と、免疫調整作用を有する乳酸菌とを含有する組成物である。
【0048】
ここで用いられる免疫調整作用を有する乳酸菌としては既知のいかなるものでもよく、かかる乳酸菌としては、ラクトバチルス属、ビフィドバクテリウム(Bifidobacterium)属、ストレプトコッカス(Streptococcus)属、テトラジェノコッカス(Tetragenococcus)属、ペディオコッカス(Pediococcus)属、ロイコノストック(Leuconostoc)属が例示され、さらにはラクトバチルス・ブレビス(L.brevis)、ラクトバチルス・パラカゼイ(L.paracasei)、ラクトバチルス・ペントーサス(L.pentosus)、ラクトバチルス・アシドフィルス(L.acidophilus)、ラクトバチルス・プランタラム(L.plantarum)、ラクトバチルス・カゼイ(L.casei)、ラクトバチルス・ロイテリ(L.reuteri)、ビフィドバクテリウム・ロンガム(B.longum)、ストレプトコッカス・フェーカリス(S.faecalis)、ストレプトコッカス・ラクティス(S.lactis)、テトラジェノコッカス・ハロフィラ(T.halophilus)、ペティオコッカス・ペントサセウス(P.pentosaseus)、ペディオコッカス・アシディラクティシ(P.acidilactici)、ペディオコッカス・セレビシエ(P.cerevisiae)、ロイコノストック・メセントロイデス(Leuconostoc mesenteroides)等が例示される。
【0049】
これらの中で、本発明者らがアスパラガスを分離源として分離した菌株である、L.brevis UAS−4(FERM P−20710)、L.brevis UAS−6(FERM P−20711)が好ましい。この2菌株の性質は前記した表1に示したとおりであり、新菌株として独立行政法人産業技術総合研究所特許生物寄託センターに寄託されている。
【0050】
免疫調整作用を有する乳酸菌の培養方法は、GYP培地、市販のGAM培地(日水製薬)、MRS培地(Difco)等、従来公知の乳酸菌用の培地を用い、培養方法も従来公知の方法によって行えばよい。
【0051】
そして、このようにして得られた培養液をそのままで、あるいは培養液から遠心または濾過等の固液分離操作によって集菌した菌体を、本発明の第1の組成物と混合する。本発明の第1の組成物との混合比率は、乾燥重量にして、免疫調整能を有する乳酸菌を1とした場合、本発明第1の組成物が0.1〜200、より好ましくは0.2〜100、さらに好ましくは0.5〜50である。
【0052】
また、混合の前後において適宜乾燥等の操作を行い粉末の形態にすることも可能であり、適当な担体を添加した後常法により顆粒状、粒状、錠剤、カプセル、ゲル状、ペースト状、乳状、懸濁状、液状、飲料等の食用に適した形態に成形してもよい。
【0053】
次に本発明の第4の飲食品又は飼料について説明する。
【0054】
本発明の飲食品又は飼料は、上述のようにして製造した本発明の第1又は第2の組成物を含有することを特徴とするものである。飲食品中又は飼料中における本発明の組成物の含有量は、特に限定されず本発明の組成物それ自身を飲食品又は飼料とすることも可能であるが、概ね本発明の第1の組成物の場合は1日当たり20〜1,000mgになるように配合することが好ましく、本発明の第2の組成物の場合は乳酸菌の乾燥重量として1日当たり10mg〜500mgになるように調整すればよい。この範囲より少ない場合は効果が望めない可能性があり、この範囲より多い場合はもはや効果の増大は見込ず、さらに日常摂取が困難な可能性がある。
【0055】
本発明の組成物を既存の飲食品或いは調味食品に含ませる場合は、ベースとなる飲食品或いは調味食品としては特に限定されないが、例えば、うどんやパスタ等の加工麺、ハム・ソーセージ等の食肉加工食品、かまぼこ・ちくわ等の水産加工食品、バター・粉乳・醗酵乳等の乳加工品、ゼリー・アイスクリーム等のデザート類、パン類、菓子類、調味料類等の加工食品、および、清涼飲料水、アルコール類、果汁飲料、野菜汁飲料、乳飲料、炭酸飲料、コーヒー飲料、アルコール類等の飲料が好ましい。
【0056】
飲食品或いは調味食品に含ませる本発明の組成物の形態は特に限定されず、飲料、グミ、キャンデーなどにおいては液体状の物を、錠剤、顆粒、カプセルなどにおいては粉末状の物を使用するなどすればよい。
【実施例】
【0057】
以下、実施例により本発明を具体的に説明するが、本発明は何らこれらに限定されるものではない。
【0058】
実験例1(植物処理物を発酵可能な乳酸菌株の単離、同定)
乳酸菌株は植物処理物中で増殖できることを条件に探索した。野菜、果物、漬物などの各種食品から被検試料を適量サンプリングし、生理食塩水にて希釈懸濁してGYP白亜寒天培地に混釈培養し、これから周囲に透明な層を形成する代表的コロニーを釣菌し、さらにこれをGYP寒天培地に画線し培養する操作を繰り返して乳酸菌の純粋分離を行なった。得られた分離乳酸菌株を以下の植物処理物中で30℃、24時間静置培養を行い、培養液の濁度(O.D.660の値)が2.0を超えたものだけを選別した。植物処理物は、アスパラガスに加水、ミルミキサーで粉砕し、加熱殺菌(85℃、30分)した後、珪藻土濾過して得られた清澄濾液をBrixが2.0%になるよう調整、オートクレーブ滅菌したものを用いた。この操作で乳酸菌株14株を得た。この14株の16SrRNA配列のうち5’−末端側の約500塩基について解読し、相同性検索を行ったところ、Lactobacillus brevisが4株、Lactobacillus pentosusが4株、Lactobacillus plantarumが3株、Lactobacillus hilgardiiが1株、Pediococcus petosaseusが2株であった。
【0059】
実験例2(免疫調整作用を有する乳酸菌の選抜)
実施例1で得られた14株の乳酸菌をアスパラガス処理物中で30℃、48時間静置培養した。アスパラガス処理物は実施例1の操作に加え、オートクレーブ前に酵母エキスを1重量%添加したものを用いた。培養終了後、100℃で5分間処理し、滅菌生理食塩水で2回遠心洗浄し、以下の試験のサンプルとした。なお、培養終了後の上清は実施例3、4で使用している。
【0060】
Balb/Cマウス雌性6週齢(日本チャールスリバー)に2mgの水酸化アルミニウムゲルに20μgの卵白アルブミン(以下、OVAという。)を吸収させた生理食塩水溶液200μlを腹腔内投与し、10日目に脾臓を回収した。脾臓細胞を調整し、20%FBSを含むRPMI−1640培溶液に懸濁し、100μg/mlのOVA共存下で分離乳酸菌体を10μg(乾燥重量)/mlとなるように添加して共培養した。7日後、培養上清を回収し、IFN−γをELISA法で定量した。単離乳酸菌株のIFN−γ誘導活性を表2に示した。結果、ラクトバチルス・ブレビスUAS−4株に強力なIFN−γ誘導活性が見出された。なお、この菌株は特許生物寄託センターへの寄託を行っており、その受託番号はFERM P−20710である。
【0061】
【表2】

実施例1(植物処理物発酵液が持つ、乳酸菌の免疫調整作用への影響)
強力なIFN−γ誘導能を有する乳酸菌株ラクトバチルス ブレビス UAS−4が得られたので、この菌株を指標にして、各菌株の植物処理物の発酵液が、免疫調整作用に及ぼす影響を比較した。
【0062】
植物処理物は、実験例2で作製したアスパラガス処理物の発酵液を85℃、30分殺菌処理後、珪藻土濾過し凍結乾燥したものを用いた(以下、AFと略す)。また、乳酸菌体は実験例2で作製したラクトバチルス ブレビス UAS−4の凍結乾燥物を用いた。
【0063】
脾臓細胞からのIFN−γ産生量の測定実験は実験例2の方法に従って行い、サンプルとしてはラクトバチルス ブレビス UAS−4株菌体 5μg/ml、各菌株によるAF 5μg/mlのそれぞれを単独或いは混合して添加した。また、未発酵前のアスパラガス処理物(凍結乾燥物)についても、単独或いは乳酸菌株と混合した場合のIFN−γ生産能を調べた。結果を図1に示す。
【0064】
図1に示した通り、乳酸菌体を除いたAFには、全く或いはほとんどINF-γ産生能がないが、ラクトバチルス ブレビス UAS−4株と併用すると、いくつかの菌株によるAFでIFN−産生能に相乗効果が見られた。特にラクトバチルス ブレビス UAS−4株によって産生されたAFが最も相乗効果に優れており、IFN−γ産生量は3.97倍に達した。
【0065】
実施例2(植物処理物発酵物の効果の乳酸菌株による違い)
実施例1でAFがラクトバチルス ブレビス UAS−4株の免疫調整作用を相乗的に高めることが確認されたので、他の菌株に対するAFの効果を検証した。
【0066】
AFは実施例1で作製したもののうち、ラクトバチルス ブレビス UAS−4株によるもの、各乳酸菌体は実験例2で作製したものの凍結乾燥物を用いた。
【0067】
脾臓細胞からのIFN−γ産生量の測定実験は実施例2の方法に従って行い、サンプルとしては各乳酸菌体 5μg/ml、AF 5μg/mlのそれぞれを単独或いは混合して添加した。結果を図2に示す。
【0068】
図から明らかな通り、ラクトバチルス ブレビス UAS−4株の発酵により得られたAFは、その他の乳酸菌株に対しても相乗的に免疫調整作用を高めた。
【0069】
実施例3(植物による効果の違い)
次に、アスパラガス以外の植物処理物の発酵物に本発明の効果があるかを確認した。アスパラガス、ニンジン、トマト、キャベツ各1kgにそれぞれ水1Lを添加して家庭用のミキサーで粉砕し、85℃30分間加熱殺菌した。その後、珪藻土を添加し、濾紙(ADVANTEC東洋製No.5C)を用いて吸引濾過を行い、清澄な濾液を得た。この各濾液を濃縮或いは水で希釈しBrixを2.5%に調整した。次に、酵母エキスを1重量%溶解し85℃30分間再殺菌した。得られた培地1Lに、GYP培地のグルコースをフルクトースに換えたFYP培地で30℃、24時間静置して前培養したラクトバチルス ブレビス UAS−4株の前培養液を10ml接種した。30℃で48時間静置培養した後85℃30分間加熱殺菌した後、珪藻土濾過により除菌した清澄濾液を得、凍結乾燥した。アスパラガス、ニンジン、トマト、キャベツから得られたものは以下AF、CRF、TF、CBFと略す。また、乳酸菌体は実施例2で作製したラクトバチルス ブレビス UAS−4の凍結乾燥物を用いた。
【0070】
脾臓細胞からのIFN−γ産生量の測定実験は実施例2の方法に従って行い、サンプルとしてはラクトバチルス ブレビス UAS−4株菌体 5μg/ml、各植物発酵物 5μg/mlのそれぞれを単独或いは混合して添加した。結果を図3に示す。
【0071】
図から明らかな通り、各植物の発酵物は、いずれも乳酸菌のもつ免疫調整作用を相乗的に高めた。なかでも、アスパラガス発酵物が最も優れていた。
【0072】
試験例1<マウスにおける抗アレルギー作用の検討>
植物処理物発酵物に、乳酸菌のIFN−γ産生促進作用を相乗的に高めることが確認されたので、マウスアレルギーモデルを用いて血中IgEレベルが抑制されるか検討した。すなわち、Balb/Cマウス雌性6週齢(日本チャールスリバー)に2mgの水酸化アルミニウムゲルに20μgのOVAを吸収させた生理食塩水溶液100μlを腹腔内投与し、血中OVA特異的IgEを誘導した。OVAの腹腔内投与は0週目、2週目、5週目、8週目に行い、1)コントロール餌、2)AF入りの餌、3)乳酸菌体入りの餌、4)AFおよび乳酸菌体入りの餌を0週目からマウスに摂取させた。乳酸菌体はラクトバチルス ブレビス UAS−4株で実験例2と同じ方法で、AFは実施例3と同じ方法で作製したものを用いた。摂取量は乳酸菌体、AFともに5mg/1週目、3週目、6週目、9週目に採血して血清を調整し、血中OVA特異的IgEをELISA法により定量した。測定結果を図4に示す。この結果から、乳酸菌体単独でも有意差はなかったものの血中OVA特異的IgEの上昇が抑制される傾向にあり、AFと乳酸菌を併せて摂取した場合はさらに抑制され有意差を得られるほどであった。
【0073】
製造例1
以下に示す方法により、植物処理物発酵物を含有する医薬品(錠剤)を製造した。
【0074】
実施例3と同じ方法により製造したAFまたはCRF乾燥物60gを乳糖230gおよびステアリン酸マグネシウム1gとともに混合し、単発式打錠機にて打錠することにより、直径12mm、重量320mgの錠剤を製造した。
【0075】
製造例2
以下に示す方法により、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有する医薬品(錠剤)を製造した。
【0076】
実施例3と同じ方法により製造したAF乾燥物60g、実施例2と同じ方法で得たラクトバチルス ブレビス UAS−4株またはラクトバチルス ペントーサス UPV7株20g、乳糖230gおよびステアリン酸マグネシウム1gとともに混合し、単発式打錠機にて打錠することにより、直径12mm、重量320mgの錠剤を製造した。
【0077】
製造例3
以下に示す方法により、植物処理物発酵物を含有するウーロン茶を製造した。
実施例3と同じ方法により製造したAFまたはCRF乾燥物50gを日本粉末薬品(株)製「ウーロン茶エキスパウダー」950gと混合し、植物処理物発酵物を含有するウーロン茶粉末を製造した。このウーロン茶粉末5gを水500mlに溶解したところ、速やかに溶け、味も良好なものであった。
【0078】
製造例4
以下に示す方法により、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有するウーロン茶を製造した。
【0079】
実施例3と同じ方法により製造したAF乾燥物50g、実施例2と同じ方法で得たラクトバチルス ブレビス UAS−4株またはラクトバチルス ペントーサス UPV7株25gを日本粉末薬品(株)製「ウーロン茶エキスパウダー」925gと混合し、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有するウーロン茶粉末を製造した。このウーロン茶粉末5gを水500mlに溶解したところ、独特の触感のある、良好な味のするウーロン茶ができた。
【0080】
製造例5
以下の方法により、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有する醗酵乳飲料を製造した。
【0081】
脱脂粉乳20%、実施例5と同じ方法により製造したAFの、凍結乾燥前の清澄濾液を50%含有する培地1Lに、前培養して定常状態となっているラクトバチルス ブレビス UAS−4の菌体懸濁液を10mL添加して30℃、静置の条件で、36時間培養することにより、植物処理物発酵物と免疫賦活作用を有する乳酸菌を含有する醗酵乳飲料が得られた。
【0082】
製造例6
以下に示す方法により、植物処理物発酵物を含有する麺を製造した。
【0083】
実施例3と同じ方法により製造したAFまたはCRF乾燥物を1w/w%になるよう中力粉と混合し、うどんの麺を作製した。この麺を調理したうどんを食したところ、微かに甘味と爽やかな香りを感じる良好な麺であった。
【図面の簡単な説明】
【0084】
【図1】本発明の実施例1において、各種乳酸菌のアスパラガス処理物醗酵物、ラクトバチルス ブレビスUAS−4株菌体、およびそれらを併用したときのマウス脾臓細胞からのIFN−γ産生能を示す図である。
【図2】本発明の実施例2において、各種乳酸菌体、ラクトバチルス ブレビスUAS−4株によるアスパラガス処理物醗酵物(AF)、およびそれらを併用したときのマウス脾臓細胞からのIFN−γ産生能を示す図である。
【図3】本発明の実施例3において、ラクトバチルス ブレビスUAS−4株菌体、各種乳酸菌体による各種植物処理物醗酵物、およびそれらを併用したときのマウス脾臓細胞からのIFN−γ産生能を示す図である。
【図4】本発明の実施例4において、ラクトバチルス ブレビスUAS−4株菌体、アスパラガス処理物醗酵物、およびそれらを併用したときのマウスの血中OVA特異的IgE量を示す図である。
【特許請求の範囲】
【請求項1】
植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物からなることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物。
【請求項2】
培養物から乳酸菌を除いた成分が、免疫調製作用を有しない成分である請求項1記載の組成物。
【請求項3】
免疫調整作用が、抗アレルギー作用である請求項1又は2記載の組成物。
【請求項4】
免疫調整作用が、抗腫瘍作用である請求項1又は2記載の組成物。
【請求項5】
免疫調整作用が、インターフェロン−ガンマ(IFN−γ)産生能を促進するものである請求項1〜4のいずれかに記載の組成物。
【請求項6】
免疫調整作用が、IgE抗体産生能を抑制するものである請求項1〜4のいずれかに記載の組成物。
【請求項7】
乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である請求項1〜8のいずれかに記載の組成物。
【請求項8】
植物処理物が、アスパラガスを処理したものである請求項1〜7のいずれかに記載の組成物。
【請求項9】
植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物から乳酸菌の免疫調整作用を相乗的に高める組成物を得ることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物の製造方法。
【請求項10】
請求項1〜8のいずれかに記載の組成物と、免疫調整作用を有する乳酸菌とを含有することを特徴とする免疫調整作用を有する組成物。
【請求項11】
免疫調整作用を有する乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である請求項10記載の組成物。
【請求項12】
請求項1〜8、10又は12のいずれかに記載の組成物を含有することを特徴とする飲食品又は飼料。
【請求項1】
植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物からなることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物。
【請求項2】
培養物から乳酸菌を除いた成分が、免疫調製作用を有しない成分である請求項1記載の組成物。
【請求項3】
免疫調整作用が、抗アレルギー作用である請求項1又は2記載の組成物。
【請求項4】
免疫調整作用が、抗腫瘍作用である請求項1又は2記載の組成物。
【請求項5】
免疫調整作用が、インターフェロン−ガンマ(IFN−γ)産生能を促進するものである請求項1〜4のいずれかに記載の組成物。
【請求項6】
免疫調整作用が、IgE抗体産生能を抑制するものである請求項1〜4のいずれかに記載の組成物。
【請求項7】
乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である請求項1〜8のいずれかに記載の組成物。
【請求項8】
植物処理物が、アスパラガスを処理したものである請求項1〜7のいずれかに記載の組成物。
【請求項9】
植物処理物を含有する培地に、乳酸菌を接種し乳酸発酵して得られる培養物から乳酸菌の免疫調整作用を相乗的に高める組成物を得ることを特徴とする、乳酸菌の免疫調整作用を相乗的に高める組成物の製造方法。
【請求項10】
請求項1〜8のいずれかに記載の組成物と、免疫調整作用を有する乳酸菌とを含有することを特徴とする免疫調整作用を有する組成物。
【請求項11】
免疫調整作用を有する乳酸菌が、ラクトバチルス・ブレビス(Lactobacillus brevis) UAS−4(FERM P−20710)又はUAS−6(FERM P−20711)である請求項10記載の組成物。
【請求項12】
請求項1〜8、10又は12のいずれかに記載の組成物を含有することを特徴とする飲食品又は飼料。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2007−302628(P2007−302628A)
【公開日】平成19年11月22日(2007.11.22)
【国際特許分類】
【出願番号】特願2006−134176(P2006−134176)
【出願日】平成18年5月12日(2006.5.12)
【出願人】(000004503)ユニチカ株式会社 (1,214)
【Fターム(参考)】
【公開日】平成19年11月22日(2007.11.22)
【国際特許分類】
【出願日】平成18年5月12日(2006.5.12)
【出願人】(000004503)ユニチカ株式会社 (1,214)
【Fターム(参考)】
[ Back to top ]

