乳酸菌生産物質とその製造方法
【課題】少量を摂取することで乳酸菌による効果を得ることができる乳酸菌生産物質およびその製造方法を提供する。
【解決手段】複数種の乳酸菌を第1次共生培養、第2次共生培養、第3次共生培養を介して、最終共生培養する。そして、この最終共生培養液をろ過し、菌体を除去したろ液を得る。このろ液を乳酸菌生産物質として、経口摂取する。このようにして得た乳酸菌生産物質の中には、多くの生産代謝物が含まれ、これら生産代謝物質が腸内の良性菌に好影響を与える。
【解決手段】複数種の乳酸菌を第1次共生培養、第2次共生培養、第3次共生培養を介して、最終共生培養する。そして、この最終共生培養液をろ過し、菌体を除去したろ液を得る。このろ液を乳酸菌生産物質として、経口摂取する。このようにして得た乳酸菌生産物質の中には、多くの生産代謝物が含まれ、これら生産代謝物質が腸内の良性菌に好影響を与える。
【発明の詳細な説明】
【0001】
【発明の属する技術分野】
この発明は、複数の乳酸菌を培養して得られる乳酸菌生産物質と、上記乳酸菌生産物質の製造方法に関する。
【0002】
【従来の技術】
乳酸菌は、腸内で腸内微生物の生育に大きな影響を与え、腸内環境を良好に保つことが知られている。この乳酸菌は人の腸内にいわゆる善玉菌として生息し、上記腸内環境を維持している。したがって、この乳酸菌数が低下したり、活性が低下したりすることによって上記腸内環境が崩れる原因になる。
そこで、近年乳酸菌の生菌を腸内に補給するために、その生菌を含むヨーグルトや飲料などが販売されている。そして、これらのヨーグルトや飲料を直接体内に取り入れて、腸内の乳酸菌量を増加させるようにしている。
なお、本願出願人は、先行技術調査をおこなうことなく、公知の技術を基に本願発明を開発したので、本件に係る先行技術文献情報はない。
【0003】
【発明が解決しようとする課題】
しかし、上記生菌を含むヨーグルトや飲料などの食料品を摂取したとしても、その生菌が腸に到達するまでに、胃酸で分解されたり、消化されたりして、生菌のほとんどが死滅してしまう。つまり、ヨーグルトや飲料などから生菌を摂取したとしても、生きたまま腸に到達する乳酸菌はほんのわずかな量になってしまう。
したがって、乳酸菌による期待通りの整腸作用が得られないことが多い。
【0004】
また、上記のように生菌の死滅を考慮すると、上記乳酸菌を含む食品を大量に摂取しなければならず、十分な整腸作用が得られない。しかしながら、ヨーグルトなどの飲食単位(ヨーグルト一瓶)に含まれている乳酸菌の量に限りがあるので、大量の乳酸菌を一度に摂取することは、かなり難しくなる。
この発明の目的は、少量を摂取することで乳酸菌による効果を得ることができる乳酸菌生産物質とその製造方法を提供することである。
【0005】
【課題を解決するための手段】
第1の発明は、複数種の乳酸菌を共生培養した培養液をろ過したろ液からなることを特徴とする。
第2の発明は、乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いたことを特徴とする。
【0006】
第3の発明は、複数種の乳酸菌を混合し、これを共生培養するとともに、この培養液をろ過してろ液を得ることを特徴とする。
第4の発明は、混合培養は、乳酸菌の少なくとも2種類を混合する第1次培養と、少なくともこの第1次培養した第1次培養菌を含む第2次培養と、少なくともこの第2次培養した第2次培養菌を含む第3次培養と、少なくともこの第3次培養した第3次培養菌を含む最終培養とを有することを特徴とする。
第5の発明は、乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いたことを特徴とする。
【0007】
【発明の実施の形態】
本願出願人は、乳酸菌の代謝産物に着目し、この乳酸菌の代謝産物が腸内環境の調整に役立つものと考えた。すなわち、上記乳酸菌の代謝産物が腸内に供給されることによって、これら代謝産物に含まれる成分が、腸内良性菌の栄養源となって、それら良性菌が活性化されるものとの仮説を立て、いろいろな実験を繰り返した。
【0008】
(実験例1)
そこで、先ず、複数の乳酸菌を共生培養し、その生産物質の中から乳酸菌を取り除くことによって、乳酸菌の代謝産物を含んだ乳酸菌生産物質を得た。
このようにして得た乳酸菌生産物質を次の条件の下で100人に経口摂取させた。すなわち、各人に、7mlずつ、朝、昼、夜の食間空腹時に、8週間継続的に摂取させた。その結果、表1に示すように、体のしびれ、便秘、腹部膨満、頭痛などの自覚感覚に対して、ある程度の好転が見られた。
【表1】

【0009】
このように自覚感覚に好転が見られたのは、菌の生存に関わりなく、多くの代謝産物が腸内に供給され、それが腸内良性菌の栄養源となって、良性菌が活性化されたものと考えられる。
【0010】
なお、上記複数の乳酸菌としては、次のものを用いた。
上記乳酸菌として連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた。また、上記連鎖球菌属としては、L.ラクティス(Lactococcus lactis subsp.lactis)、L.クレモリス(Lactococcus lactis subsp.cremoris)、E.フェカリス(Enterococcus fecalis)、S.サーモフィラス(Streptococcus thermophilus)を用いた。乳酸桿菌属としては、L.カゼイ(Lactobacillus casei、Lactobacillus acidophilus)、L.アシドフィラス(Lactobacillus acidophilus)、L.ファーメンタム(Lactobacillus fermentum)、L.ブルガリクス(Lactobacillus bulgaricus)、L.ガセリ(Lactobacillus gasseri)、L.デルブリッキ(Lactobacillus delbrueckii)、L.プランタラム(Lactobacillus plantarum)を用いた。ビフィズス菌属としては、B.ロンガム(Bifidobacterium longum)、B.ビフィダム(Bifidobacterium bifidum)、B.ブレーベ(Bifidobacterium breve)、B.インファンティス(Bifidobacterium infantis)、B.アドレセンス(Bifidobacterium adolescentis)を用いた。
なお、上記実験1は、北京中日友好医院中医内科に依頼したものである。
【0011】
(実験例2)
実験例2においては、血糖値の高い人に対して、実験例1と同様の乳酸菌生産物質を次の条件の下で50人に経口摂取させた。すなわち、各人に、7mlずつ、朝、昼、夜の食間空腹時に、16週間継続的に摂取させた。その結果、血糖値の顕著な低下が見られたが、その実験結果を示したのが表2である。なお、この表2は、上記50人の平均値を示したものである。実験結果は、「参照値±標準値」で表示した。
【0012】
【表2】

【0013】
上記表2に示したように、乳酸菌生産物質を経口摂取させることによって、静脈血糖値(GLU)および糖化ヘモグロビン(HbAlc)ともに明らかに低下したことが分かる。したがって、上記乳酸菌生産物質は、静脈血糖値(GLU)および糖化ヘモグロビン(HbAlc)に対して著しい効果作用があるといえる。
また、乳酸菌生産物質の摂取を止めてから1ヶ月後でも、これが再び上昇することがなかった。
【0014】
上記のような乳酸菌生産物質は、腸内環境を良好に保つとともに、腸内環境が整うことによって、腸内の栄養の吸収効率が上昇して、体内の恒常性を維持するものと考えられる。
なお、上記実験例2は、北京中日友好医院中医内科に依頼したものである。
【0015】
(実験例3)
実験例3においては、消化系腫瘍患者に対して、実験例1と同様の乳酸菌生産物質を次の条件の下で50人に経口摂取させた。すなわち、各人に、一日一回7mlを経口摂取させた。摂取期間は40日を1クールとした。その結果、食欲増加の自覚症状が23例あり、全体の46%を占めた。また、精神疲労が好転したという自覚症状が24例あり、全体の48%を占めた。
【0016】
さらに、足、腰の虚脱感が改善した例は24例であり、全体の48%を占めた。体重増加は22例で、全体の44%を占めた。また、生存品質(QOL)が向上したと観察された例は26例で52%を占めた。口の渇き改善例が17例であり34%を占めた。
これらの結果は乳酸菌生産物質が肝臓、脾臓に対して有益だということを示していると考えられる。
【0017】
また、血液検査の結果を表3に示している。
表3に示したように、血色素(Hb)の上昇、NK細胞活性の上昇、T細胞亜群CD3の上昇、CD4/CD8値の上昇が確認された。いずれの上昇率も著しいものであった。
さらに、白血球、血小板(BPC)の値も一定の上昇が確認できた。また、血糖値には改善の傾向があった。
なお、この実験例3は、北京中西医結合学会南陽腫瘍医、癌研究基金会興腫瘍医院、中日友好医院中医腫瘍科に依頼したものである。
【0018】
【表3】

【0019】
(実験例4)
実験例4においては、慢性腎炎患者に対して、実験例1と同様の乳酸菌生産物質を次の条件の下で30人に経口摂取させた。すなわち、各人に、一回7mlずつ、朝、昼、晩の食事の前に経口摂取させた。実験期間は2ヶ月とした。この結果を表4および表5に示した。
【0020】
【表4】

【0021】
【表5】

【0022】
上記表4に示したように、腫れ、高血圧、腰痛、脱力感の各症状について改善が見られた。また、上記表5は尿蛋白量を参照値±標準差で表示している。この表5のように、明らかに尿蛋白量が低減された。
なお、上記実験例4は、北京中日友好医院、河北省玉田具医院、北京慧忠医院、北京中医薬開発協会問診部に依頼したものである。
【0023】
(実験例5)
実験例5においては、アロキサン誘発糖尿病ラットに対して、実験例1と同様の乳酸菌生産物質を次の条件の下で経口投与した。まず、ラット15匹にストレプトゾトシン(STZ)を1mL/kgとなるようにクエン酸緩衝液で溶解した後、尾静脈より投与し、ラットの血糖値が180mg/dLとなるようにした。そして、これを5匹ずつ3つのグループに分け、これをグループ1〜3とした。
上記グループ1には蒸留水4mlを、グループ2には乳酸菌生産物質2ml+蒸留水2mlを、グループ3には乳酸菌生産物質4mlを経口投与した。経口投与は1日1回28日間おこなった。そして、これらのラットの血漿中グルコース濃度を測定した。測定結果は、平均値および標準誤差で示した。
【0024】
上記実験例5の結果、グループ1では試験期間を通して、200mg/dL以上という高い値を維持した。これに対して、乳酸菌生産物質を投与したグループ2では投与前の274.4±17.4に比べ、投与1週目には30%以上低下し178.2±27.6となり、2週目以降は、159.3±9.8とグループ1に対して優位な差が見られた。
また、乳酸菌生産物質を投与したグループ3では、投与1週目では153.8±7.6で、グループ1と比較して優位な差が見られた。2週目では160.1±5.5とその効果が持続された。さらに、3週目では95.2±2.2、試験最終日には103.2±11.1であった。これは、STZ処理していない健常のラットとほぼ同じ値であった。
以上のことから、乳酸菌生産物質は明らかに高血糖を正常値に改善することが分かった。
【0025】
また、上記試験の後、各グループの肝臓と十二指腸とをホルマリン固定して、組織切片を作成し、組織学的評価を行った。
その結果、グループ1ではランゲルハンス島β細胞の脱顆粒すなわち、顆粒の減少が見られ、細胞の空洞化などが確認された。またβ細胞数はSTD処理しないラットでは19以上であったが、このグループ1では7.0±2.0であり、β細胞数の減少も確認された。
これに対し、乳酸菌生産物質を投与したグループ2,3では容量依存的にβ細胞数減少の抑制が認められた。このときのβ細胞数は、10.3±2.3であった。
また、グループ2ではβ細胞の顆粒減少および細胞の空洞化が見られたが、グループ1に比べて少数であった。
【0026】
以上の結果から、乳酸菌生産物質は血糖値を濃度依存的に優位に低下させ、正常値に改善させるが、その機序としては1つの作用機序ではなく、複数の作用機序が存在する。それは、組織学的にランゲルハンス島β細胞の変性を改善させたがこれだけでは血糖値をほぼ正常値に回復させるには不十分と思われるからである。つまり、乳酸菌生産物質の投与によって、糖代謝に何らかの作用をもたらし、結果的に血糖値を正常値に改善させたものと考えられる。
なお、上記実験例5は、株式会社 薬物安全性試験センターに依頼したものである。
【0027】
【実施例】
この実施例では、乳酸菌として連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた。上記連鎖球菌属としては、L.ラクティス(Lactococcus lactis subsp.lactis)、L.クレモリス(Lactococcus lactis subsp.cremoris)、E.フェカリス(Enterococcus fecalis)、S.サーモフィラス(Streptococcus thermophilus)を用いた。乳酸桿菌属としては、L.カゼイ(Lactobacillus casei、Lactobacillus acidophilus)、L.アシドフィラス(Lactobacillus acidophilus)、L.ファーメンタム(Lactobacillus fermentum)、L.ブルガリクス(Lactobacillus bulgaricus)、L.ガセリ(Lactobacillus gasseri)、L.デルブリッキ(Lactobacillus delbrueckii)、L.プランタラム(Lactobacillus plantarum)を用いた。ビフィズス菌属としては、B.ロンガム(Bifidobacterium longum)、B.ビフィダム(Bifidobacterium bifidum)、B.ブレーベ(Bifidobacterium breve)、B.インファンティス(Bifidobacterium infantis)、B.アドレセンス(Bifidobacterium adolescentis)を用いた。
【0028】
これら各乳酸菌は次のようにして継代培養したものである。すなわち、各乳酸菌を、32℃で12時間培養した後、37℃で12時間培養し、さらに40℃で24時間培養した。そして、これら継代培養したものを、すぐに共生培養させないときには、それら乳酸菌を5℃で冷蔵保存しておいた。
【0029】
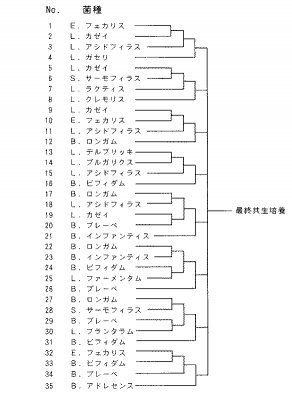
上記のようにして継代培養した各乳酸菌を用いて、図1に示す組み合わせの下で共生培養した。なお、この組み合わせ表に基づいて、各菌には1〜35のナンバーを付したので、以下には、共生培養のステップをこのナンバーを用いて説明する。
【0030】
No.1〜35の各乳酸菌を用いて、8つのバルクスターターを生成したが、次に、これら第1〜第8のバルクスターターの生成ステップを説明する。
第1のバルクスターターは、No.1〜4の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.1のE.フェカリスとNo.2のL.カゼイを用いて行った。第2次共生培養は、第1次共生培養液にNo.3のL.アシドフィラスを添加して行った。第3次共生培養は、第2次共生培養液にNO.4のL.ガセリを添加して行った。
【0031】
第2のバルクスターターは、No.5〜8の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.5のL.カゼイとNo.6のS.サーモフィラスを用いて行った。第2次共生培養は、第1次共生培養液にNo.7のL.ラクティスを添加して行った。第3次共生培養は、第2次共生培養液にNO.8のL.クレモリスを添加して行った。
【0032】
第3のバルクスターターは、No.9〜12の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.9のL.カゼイとNo.10のE.フェカリスを用いて行った。第2次共生培養は、第1次共生培養液にNo.11のL.アシドフィラスを添加して行った。第3次共生培養は、第2次共生培養液にNO.12のB.ロンガムを添加して行った。
【0033】
第4のバルクスターターは、No.13〜16の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.13のL.デルブリッキとNo.14のL.ブルガリクスを用いて行った。
第2次共生培養は、第1次共生培養液にNo.15のL.アシドフィラスを添加して行った。第3次共生培養は、第2次共生培養液にNO.16のB.ビフィダムを添加して行った。
【0034】
第5のバルクスターターは、No.17〜21の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.17のB.ロンガムとNo.18のL.アシドフィラスとの組み合わせと、No.19L.カゼイとNo.20B.ブレーベとの組み合わせを用いて行った。
第2次共生培養は、上記2組の第1次共生培養液同士をさらに共生培養して行ったものである。第3次共生培養は、第2次共生培養液にNo.21のB.インファンティスを添加して行った。
【0035】
第6のバルクスターターは、No.22〜26の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.22のB.ロンガムとNo.23のB.インファンティスとの組み合わせと、No.24のB.ビフィダムとNo.25のL.ファーメンタムとの組み合わせを用いて行った。
第2次共生培養は、上記2組の第1次共生培養液同士をさらに共生培養して行ったものである。第3次共生培養は、第2次共生培養液にNo.26のB.ブレーベを添加して行った。
【0036】
第7のバルクスターターは、No.27〜31の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.27のB.ロンガムとNo.28のS.サーモフィラスとの組み合わせと、No.29のB.ブレーベとNo.30のL.プランタラムとの組み合わせを用いて行った。
第2次共生培養は、上記2組の第1次共生培養液同士をさらに共生培養して行ったものである。第3次共生培養は、第2次共生培養液にNo.31のB.ビフィダムを添加して行った。
【0037】
第8のバルクスターターは、No.32〜35の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.32のE.フェカリスとNo.33のB.ビフィダムを用いて行った。
第2次共生培養は、第1次共生培養液にNo.34のB.ブレーベを添加して行った。第3次共生培養は、第2次共生培養液にNO.35のB.アドレセンスを添加して行った。
以上第1〜第8のバルクスターターをさらに最終共生培養して最終共生培養液を生成した。
【0038】
なお、上記第1〜第3次共生培養および最終培養において、培地と培養条件は次の通りである。
第1次共生培養は、半流動培地を用い、37℃でpH4.6になるまで約6〜12時間行った。第2次共生培養は、半流動培地を用い、37℃でpH4.6になるまで約4〜10時間行った。第3次共生培養では、培地として豆乳と脱脂乳とを1:1の割合で混合し、これにブドウ糖0.5%(w/v)、酵母エキス0.5%(w/v)を添加したものを用いた。そして、37℃でpH4.55になるまで約6〜10時間培養を行った。
【0039】
最終培養には、豆乳と脱脂乳とを5:1の割合で混合し、これに酵母エキス0.2%(w/v)、ブドウ糖0.5%(w/v)を添加し培地を用いた。そして、最初に32℃で24時間培養し、次に40℃で48時間培養し、さらに37℃で24時間培養し、最後に53℃で18時間培養し、これを最終培養とした。
【0040】
上記最終培養液は、高圧蒸気滅菌法を用いて65℃で40分間加熱し、最終培養液中の乳酸菌を殺菌する。そして、この殺菌した最終培養液を15℃まで冷却する。最終培養液を15℃に冷却することによって、脂肪分等の不要物を凝固させることができる。このように脂肪分を凝固させると、後で説明するろ過によってこれを除去できる。上記脂肪分を除去すれば、上記ろ過したときのろ液が懸濁するのを防止することができる。また、脂肪分が酸化することによって、ろ液の中に酸化物が増加するのを防止することもできる。
【0041】
さらに、上記冷却した培養液に12%無水エタノールを添加して、高速ホモジナイザーでミキシングする。このように無水エタノールを添加することによって、上記乳酸菌の菌体内の成分を抽出することができる。
【0042】
上記ミキシングした最終培養液は、ステンレス製のろ過器(濾紙3ミクロン)に注入して自然ろ過した後、0.1ミクロンの中空糸膜でろ過する。このとき、上記したように脂肪分が取り除かれる。また、上記のろ過でろ液の中から死菌も除去される。
このように最終培養液から、脂肪分や死菌を除去したものが乳酸菌生産物質となる。
【0043】
上記のようにして得られた乳酸菌生産物質の中には、大量の代謝産物が含まれている。この乳酸菌生産物質に含まれる代謝産物を示したのが表6である。
【0044】
【表6】

【0045】
上記表に示したように、乳酸菌生産物質に含まれる代謝産物は、微生物の栄養因子であることが分かる。したがって、上記乳酸菌生産物質を摂取することによって、上記栄養因子を腸内に供給することができる。腸内微生物は、上記栄養因子によって活性化し、腸内環境を良好に維持することができるものと推測される。このように腸内環境が良好に維持されれば、腸からの栄養吸収や排泄物の排泄がスムーズに行われ、その結果、自然治癒力が向上するものと考えられる。
また、複数種の乳酸菌を共生培養することによって、上記分析結果には表れない、各菌に特有の代謝産物も多く含まれていると思われる。これら代謝産物の豊富な種類も上記腸内細菌の活性化に寄与していると考えられる。
【0046】
また、上記のように乳酸菌生産物質の中には、大量の生産代謝物が含まれるので、これを摂取するときには、少量を摂取すれば十分であり、従来のように、大量の生菌を摂取する必要がない。
さらに、乳酸菌を加熱殺菌しているので、この乳酸菌が変質するのを防止することができる。乳酸菌の変質を防止することによって、乳酸菌生産物質の品質を一定に保つことができる。
【0047】
【発明の効果】
この発明によれば、複数の乳酸菌を培養して乳酸菌生産物質を得ることができるので、この乳酸菌生産物質には多くの種類の生産代謝物を大量に含有させることができる。この乳酸菌生産物質を摂取した場合には、上記生産代謝物によって、腸内良性菌が活性化し、腸内環境を良好にすることができる。つまり、乳酸菌の生菌を直接摂取することなく、乳酸菌の効果を得ることができる。
また、上記乳酸菌生産物質には大量の生産代謝産物が含まれているので、これを摂取するときにも、たくさん摂取する必要がない。
【図面の簡単な説明】
【図1】乳酸菌の共生培養の組み合わせを示した図である。
【0001】
【発明の属する技術分野】
この発明は、複数の乳酸菌を培養して得られる乳酸菌生産物質と、上記乳酸菌生産物質の製造方法に関する。
【0002】
【従来の技術】
乳酸菌は、腸内で腸内微生物の生育に大きな影響を与え、腸内環境を良好に保つことが知られている。この乳酸菌は人の腸内にいわゆる善玉菌として生息し、上記腸内環境を維持している。したがって、この乳酸菌数が低下したり、活性が低下したりすることによって上記腸内環境が崩れる原因になる。
そこで、近年乳酸菌の生菌を腸内に補給するために、その生菌を含むヨーグルトや飲料などが販売されている。そして、これらのヨーグルトや飲料を直接体内に取り入れて、腸内の乳酸菌量を増加させるようにしている。
なお、本願出願人は、先行技術調査をおこなうことなく、公知の技術を基に本願発明を開発したので、本件に係る先行技術文献情報はない。
【0003】
【発明が解決しようとする課題】
しかし、上記生菌を含むヨーグルトや飲料などの食料品を摂取したとしても、その生菌が腸に到達するまでに、胃酸で分解されたり、消化されたりして、生菌のほとんどが死滅してしまう。つまり、ヨーグルトや飲料などから生菌を摂取したとしても、生きたまま腸に到達する乳酸菌はほんのわずかな量になってしまう。
したがって、乳酸菌による期待通りの整腸作用が得られないことが多い。
【0004】
また、上記のように生菌の死滅を考慮すると、上記乳酸菌を含む食品を大量に摂取しなければならず、十分な整腸作用が得られない。しかしながら、ヨーグルトなどの飲食単位(ヨーグルト一瓶)に含まれている乳酸菌の量に限りがあるので、大量の乳酸菌を一度に摂取することは、かなり難しくなる。
この発明の目的は、少量を摂取することで乳酸菌による効果を得ることができる乳酸菌生産物質とその製造方法を提供することである。
【0005】
【課題を解決するための手段】
第1の発明は、複数種の乳酸菌を共生培養した培養液をろ過したろ液からなることを特徴とする。
第2の発明は、乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いたことを特徴とする。
【0006】
第3の発明は、複数種の乳酸菌を混合し、これを共生培養するとともに、この培養液をろ過してろ液を得ることを特徴とする。
第4の発明は、混合培養は、乳酸菌の少なくとも2種類を混合する第1次培養と、少なくともこの第1次培養した第1次培養菌を含む第2次培養と、少なくともこの第2次培養した第2次培養菌を含む第3次培養と、少なくともこの第3次培養した第3次培養菌を含む最終培養とを有することを特徴とする。
第5の発明は、乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いたことを特徴とする。
【0007】
【発明の実施の形態】
本願出願人は、乳酸菌の代謝産物に着目し、この乳酸菌の代謝産物が腸内環境の調整に役立つものと考えた。すなわち、上記乳酸菌の代謝産物が腸内に供給されることによって、これら代謝産物に含まれる成分が、腸内良性菌の栄養源となって、それら良性菌が活性化されるものとの仮説を立て、いろいろな実験を繰り返した。
【0008】
(実験例1)
そこで、先ず、複数の乳酸菌を共生培養し、その生産物質の中から乳酸菌を取り除くことによって、乳酸菌の代謝産物を含んだ乳酸菌生産物質を得た。
このようにして得た乳酸菌生産物質を次の条件の下で100人に経口摂取させた。すなわち、各人に、7mlずつ、朝、昼、夜の食間空腹時に、8週間継続的に摂取させた。その結果、表1に示すように、体のしびれ、便秘、腹部膨満、頭痛などの自覚感覚に対して、ある程度の好転が見られた。
【表1】

【0009】
このように自覚感覚に好転が見られたのは、菌の生存に関わりなく、多くの代謝産物が腸内に供給され、それが腸内良性菌の栄養源となって、良性菌が活性化されたものと考えられる。
【0010】
なお、上記複数の乳酸菌としては、次のものを用いた。
上記乳酸菌として連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた。また、上記連鎖球菌属としては、L.ラクティス(Lactococcus lactis subsp.lactis)、L.クレモリス(Lactococcus lactis subsp.cremoris)、E.フェカリス(Enterococcus fecalis)、S.サーモフィラス(Streptococcus thermophilus)を用いた。乳酸桿菌属としては、L.カゼイ(Lactobacillus casei、Lactobacillus acidophilus)、L.アシドフィラス(Lactobacillus acidophilus)、L.ファーメンタム(Lactobacillus fermentum)、L.ブルガリクス(Lactobacillus bulgaricus)、L.ガセリ(Lactobacillus gasseri)、L.デルブリッキ(Lactobacillus delbrueckii)、L.プランタラム(Lactobacillus plantarum)を用いた。ビフィズス菌属としては、B.ロンガム(Bifidobacterium longum)、B.ビフィダム(Bifidobacterium bifidum)、B.ブレーベ(Bifidobacterium breve)、B.インファンティス(Bifidobacterium infantis)、B.アドレセンス(Bifidobacterium adolescentis)を用いた。
なお、上記実験1は、北京中日友好医院中医内科に依頼したものである。
【0011】
(実験例2)
実験例2においては、血糖値の高い人に対して、実験例1と同様の乳酸菌生産物質を次の条件の下で50人に経口摂取させた。すなわち、各人に、7mlずつ、朝、昼、夜の食間空腹時に、16週間継続的に摂取させた。その結果、血糖値の顕著な低下が見られたが、その実験結果を示したのが表2である。なお、この表2は、上記50人の平均値を示したものである。実験結果は、「参照値±標準値」で表示した。
【0012】
【表2】

【0013】
上記表2に示したように、乳酸菌生産物質を経口摂取させることによって、静脈血糖値(GLU)および糖化ヘモグロビン(HbAlc)ともに明らかに低下したことが分かる。したがって、上記乳酸菌生産物質は、静脈血糖値(GLU)および糖化ヘモグロビン(HbAlc)に対して著しい効果作用があるといえる。
また、乳酸菌生産物質の摂取を止めてから1ヶ月後でも、これが再び上昇することがなかった。
【0014】
上記のような乳酸菌生産物質は、腸内環境を良好に保つとともに、腸内環境が整うことによって、腸内の栄養の吸収効率が上昇して、体内の恒常性を維持するものと考えられる。
なお、上記実験例2は、北京中日友好医院中医内科に依頼したものである。
【0015】
(実験例3)
実験例3においては、消化系腫瘍患者に対して、実験例1と同様の乳酸菌生産物質を次の条件の下で50人に経口摂取させた。すなわち、各人に、一日一回7mlを経口摂取させた。摂取期間は40日を1クールとした。その結果、食欲増加の自覚症状が23例あり、全体の46%を占めた。また、精神疲労が好転したという自覚症状が24例あり、全体の48%を占めた。
【0016】
さらに、足、腰の虚脱感が改善した例は24例であり、全体の48%を占めた。体重増加は22例で、全体の44%を占めた。また、生存品質(QOL)が向上したと観察された例は26例で52%を占めた。口の渇き改善例が17例であり34%を占めた。
これらの結果は乳酸菌生産物質が肝臓、脾臓に対して有益だということを示していると考えられる。
【0017】
また、血液検査の結果を表3に示している。
表3に示したように、血色素(Hb)の上昇、NK細胞活性の上昇、T細胞亜群CD3の上昇、CD4/CD8値の上昇が確認された。いずれの上昇率も著しいものであった。
さらに、白血球、血小板(BPC)の値も一定の上昇が確認できた。また、血糖値には改善の傾向があった。
なお、この実験例3は、北京中西医結合学会南陽腫瘍医、癌研究基金会興腫瘍医院、中日友好医院中医腫瘍科に依頼したものである。
【0018】
【表3】

【0019】
(実験例4)
実験例4においては、慢性腎炎患者に対して、実験例1と同様の乳酸菌生産物質を次の条件の下で30人に経口摂取させた。すなわち、各人に、一回7mlずつ、朝、昼、晩の食事の前に経口摂取させた。実験期間は2ヶ月とした。この結果を表4および表5に示した。
【0020】
【表4】

【0021】
【表5】

【0022】
上記表4に示したように、腫れ、高血圧、腰痛、脱力感の各症状について改善が見られた。また、上記表5は尿蛋白量を参照値±標準差で表示している。この表5のように、明らかに尿蛋白量が低減された。
なお、上記実験例4は、北京中日友好医院、河北省玉田具医院、北京慧忠医院、北京中医薬開発協会問診部に依頼したものである。
【0023】
(実験例5)
実験例5においては、アロキサン誘発糖尿病ラットに対して、実験例1と同様の乳酸菌生産物質を次の条件の下で経口投与した。まず、ラット15匹にストレプトゾトシン(STZ)を1mL/kgとなるようにクエン酸緩衝液で溶解した後、尾静脈より投与し、ラットの血糖値が180mg/dLとなるようにした。そして、これを5匹ずつ3つのグループに分け、これをグループ1〜3とした。
上記グループ1には蒸留水4mlを、グループ2には乳酸菌生産物質2ml+蒸留水2mlを、グループ3には乳酸菌生産物質4mlを経口投与した。経口投与は1日1回28日間おこなった。そして、これらのラットの血漿中グルコース濃度を測定した。測定結果は、平均値および標準誤差で示した。
【0024】
上記実験例5の結果、グループ1では試験期間を通して、200mg/dL以上という高い値を維持した。これに対して、乳酸菌生産物質を投与したグループ2では投与前の274.4±17.4に比べ、投与1週目には30%以上低下し178.2±27.6となり、2週目以降は、159.3±9.8とグループ1に対して優位な差が見られた。
また、乳酸菌生産物質を投与したグループ3では、投与1週目では153.8±7.6で、グループ1と比較して優位な差が見られた。2週目では160.1±5.5とその効果が持続された。さらに、3週目では95.2±2.2、試験最終日には103.2±11.1であった。これは、STZ処理していない健常のラットとほぼ同じ値であった。
以上のことから、乳酸菌生産物質は明らかに高血糖を正常値に改善することが分かった。
【0025】
また、上記試験の後、各グループの肝臓と十二指腸とをホルマリン固定して、組織切片を作成し、組織学的評価を行った。
その結果、グループ1ではランゲルハンス島β細胞の脱顆粒すなわち、顆粒の減少が見られ、細胞の空洞化などが確認された。またβ細胞数はSTD処理しないラットでは19以上であったが、このグループ1では7.0±2.0であり、β細胞数の減少も確認された。
これに対し、乳酸菌生産物質を投与したグループ2,3では容量依存的にβ細胞数減少の抑制が認められた。このときのβ細胞数は、10.3±2.3であった。
また、グループ2ではβ細胞の顆粒減少および細胞の空洞化が見られたが、グループ1に比べて少数であった。
【0026】
以上の結果から、乳酸菌生産物質は血糖値を濃度依存的に優位に低下させ、正常値に改善させるが、その機序としては1つの作用機序ではなく、複数の作用機序が存在する。それは、組織学的にランゲルハンス島β細胞の変性を改善させたがこれだけでは血糖値をほぼ正常値に回復させるには不十分と思われるからである。つまり、乳酸菌生産物質の投与によって、糖代謝に何らかの作用をもたらし、結果的に血糖値を正常値に改善させたものと考えられる。
なお、上記実験例5は、株式会社 薬物安全性試験センターに依頼したものである。
【0027】
【実施例】
この実施例では、乳酸菌として連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた。上記連鎖球菌属としては、L.ラクティス(Lactococcus lactis subsp.lactis)、L.クレモリス(Lactococcus lactis subsp.cremoris)、E.フェカリス(Enterococcus fecalis)、S.サーモフィラス(Streptococcus thermophilus)を用いた。乳酸桿菌属としては、L.カゼイ(Lactobacillus casei、Lactobacillus acidophilus)、L.アシドフィラス(Lactobacillus acidophilus)、L.ファーメンタム(Lactobacillus fermentum)、L.ブルガリクス(Lactobacillus bulgaricus)、L.ガセリ(Lactobacillus gasseri)、L.デルブリッキ(Lactobacillus delbrueckii)、L.プランタラム(Lactobacillus plantarum)を用いた。ビフィズス菌属としては、B.ロンガム(Bifidobacterium longum)、B.ビフィダム(Bifidobacterium bifidum)、B.ブレーベ(Bifidobacterium breve)、B.インファンティス(Bifidobacterium infantis)、B.アドレセンス(Bifidobacterium adolescentis)を用いた。
【0028】
これら各乳酸菌は次のようにして継代培養したものである。すなわち、各乳酸菌を、32℃で12時間培養した後、37℃で12時間培養し、さらに40℃で24時間培養した。そして、これら継代培養したものを、すぐに共生培養させないときには、それら乳酸菌を5℃で冷蔵保存しておいた。
【0029】
上記のようにして継代培養した各乳酸菌を用いて、図1に示す組み合わせの下で共生培養した。なお、この組み合わせ表に基づいて、各菌には1〜35のナンバーを付したので、以下には、共生培養のステップをこのナンバーを用いて説明する。
【0030】
No.1〜35の各乳酸菌を用いて、8つのバルクスターターを生成したが、次に、これら第1〜第8のバルクスターターの生成ステップを説明する。
第1のバルクスターターは、No.1〜4の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.1のE.フェカリスとNo.2のL.カゼイを用いて行った。第2次共生培養は、第1次共生培養液にNo.3のL.アシドフィラスを添加して行った。第3次共生培養は、第2次共生培養液にNO.4のL.ガセリを添加して行った。
【0031】
第2のバルクスターターは、No.5〜8の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.5のL.カゼイとNo.6のS.サーモフィラスを用いて行った。第2次共生培養は、第1次共生培養液にNo.7のL.ラクティスを添加して行った。第3次共生培養は、第2次共生培養液にNO.8のL.クレモリスを添加して行った。
【0032】
第3のバルクスターターは、No.9〜12の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.9のL.カゼイとNo.10のE.フェカリスを用いて行った。第2次共生培養は、第1次共生培養液にNo.11のL.アシドフィラスを添加して行った。第3次共生培養は、第2次共生培養液にNO.12のB.ロンガムを添加して行った。
【0033】
第4のバルクスターターは、No.13〜16の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.13のL.デルブリッキとNo.14のL.ブルガリクスを用いて行った。
第2次共生培養は、第1次共生培養液にNo.15のL.アシドフィラスを添加して行った。第3次共生培養は、第2次共生培養液にNO.16のB.ビフィダムを添加して行った。
【0034】
第5のバルクスターターは、No.17〜21の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.17のB.ロンガムとNo.18のL.アシドフィラスとの組み合わせと、No.19L.カゼイとNo.20B.ブレーベとの組み合わせを用いて行った。
第2次共生培養は、上記2組の第1次共生培養液同士をさらに共生培養して行ったものである。第3次共生培養は、第2次共生培養液にNo.21のB.インファンティスを添加して行った。
【0035】
第6のバルクスターターは、No.22〜26の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.22のB.ロンガムとNo.23のB.インファンティスとの組み合わせと、No.24のB.ビフィダムとNo.25のL.ファーメンタムとの組み合わせを用いて行った。
第2次共生培養は、上記2組の第1次共生培養液同士をさらに共生培養して行ったものである。第3次共生培養は、第2次共生培養液にNo.26のB.ブレーベを添加して行った。
【0036】
第7のバルクスターターは、No.27〜31の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.27のB.ロンガムとNo.28のS.サーモフィラスとの組み合わせと、No.29のB.ブレーベとNo.30のL.プランタラムとの組み合わせを用いて行った。
第2次共生培養は、上記2組の第1次共生培養液同士をさらに共生培養して行ったものである。第3次共生培養は、第2次共生培養液にNo.31のB.ビフィダムを添加して行った。
【0037】
第8のバルクスターターは、No.32〜35の乳酸菌を用いて、これらを第1次〜第3次共生培養して得たものである。上記第1次共生培養は、No.32のE.フェカリスとNo.33のB.ビフィダムを用いて行った。
第2次共生培養は、第1次共生培養液にNo.34のB.ブレーベを添加して行った。第3次共生培養は、第2次共生培養液にNO.35のB.アドレセンスを添加して行った。
以上第1〜第8のバルクスターターをさらに最終共生培養して最終共生培養液を生成した。
【0038】
なお、上記第1〜第3次共生培養および最終培養において、培地と培養条件は次の通りである。
第1次共生培養は、半流動培地を用い、37℃でpH4.6になるまで約6〜12時間行った。第2次共生培養は、半流動培地を用い、37℃でpH4.6になるまで約4〜10時間行った。第3次共生培養では、培地として豆乳と脱脂乳とを1:1の割合で混合し、これにブドウ糖0.5%(w/v)、酵母エキス0.5%(w/v)を添加したものを用いた。そして、37℃でpH4.55になるまで約6〜10時間培養を行った。
【0039】
最終培養には、豆乳と脱脂乳とを5:1の割合で混合し、これに酵母エキス0.2%(w/v)、ブドウ糖0.5%(w/v)を添加し培地を用いた。そして、最初に32℃で24時間培養し、次に40℃で48時間培養し、さらに37℃で24時間培養し、最後に53℃で18時間培養し、これを最終培養とした。
【0040】
上記最終培養液は、高圧蒸気滅菌法を用いて65℃で40分間加熱し、最終培養液中の乳酸菌を殺菌する。そして、この殺菌した最終培養液を15℃まで冷却する。最終培養液を15℃に冷却することによって、脂肪分等の不要物を凝固させることができる。このように脂肪分を凝固させると、後で説明するろ過によってこれを除去できる。上記脂肪分を除去すれば、上記ろ過したときのろ液が懸濁するのを防止することができる。また、脂肪分が酸化することによって、ろ液の中に酸化物が増加するのを防止することもできる。
【0041】
さらに、上記冷却した培養液に12%無水エタノールを添加して、高速ホモジナイザーでミキシングする。このように無水エタノールを添加することによって、上記乳酸菌の菌体内の成分を抽出することができる。
【0042】
上記ミキシングした最終培養液は、ステンレス製のろ過器(濾紙3ミクロン)に注入して自然ろ過した後、0.1ミクロンの中空糸膜でろ過する。このとき、上記したように脂肪分が取り除かれる。また、上記のろ過でろ液の中から死菌も除去される。
このように最終培養液から、脂肪分や死菌を除去したものが乳酸菌生産物質となる。
【0043】
上記のようにして得られた乳酸菌生産物質の中には、大量の代謝産物が含まれている。この乳酸菌生産物質に含まれる代謝産物を示したのが表6である。
【0044】
【表6】

【0045】
上記表に示したように、乳酸菌生産物質に含まれる代謝産物は、微生物の栄養因子であることが分かる。したがって、上記乳酸菌生産物質を摂取することによって、上記栄養因子を腸内に供給することができる。腸内微生物は、上記栄養因子によって活性化し、腸内環境を良好に維持することができるものと推測される。このように腸内環境が良好に維持されれば、腸からの栄養吸収や排泄物の排泄がスムーズに行われ、その結果、自然治癒力が向上するものと考えられる。
また、複数種の乳酸菌を共生培養することによって、上記分析結果には表れない、各菌に特有の代謝産物も多く含まれていると思われる。これら代謝産物の豊富な種類も上記腸内細菌の活性化に寄与していると考えられる。
【0046】
また、上記のように乳酸菌生産物質の中には、大量の生産代謝物が含まれるので、これを摂取するときには、少量を摂取すれば十分であり、従来のように、大量の生菌を摂取する必要がない。
さらに、乳酸菌を加熱殺菌しているので、この乳酸菌が変質するのを防止することができる。乳酸菌の変質を防止することによって、乳酸菌生産物質の品質を一定に保つことができる。
【0047】
【発明の効果】
この発明によれば、複数の乳酸菌を培養して乳酸菌生産物質を得ることができるので、この乳酸菌生産物質には多くの種類の生産代謝物を大量に含有させることができる。この乳酸菌生産物質を摂取した場合には、上記生産代謝物によって、腸内良性菌が活性化し、腸内環境を良好にすることができる。つまり、乳酸菌の生菌を直接摂取することなく、乳酸菌の効果を得ることができる。
また、上記乳酸菌生産物質には大量の生産代謝産物が含まれているので、これを摂取するときにも、たくさん摂取する必要がない。
【図面の簡単な説明】
【図1】乳酸菌の共生培養の組み合わせを示した図である。
【特許請求の範囲】
【請求項1】
複数種の乳酸菌を共生培養した培養液をろ過したろ液からなる乳酸菌生産物質。
【請求項2】
乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた請求項1記載の乳酸菌生産物質。
【請求項3】
複数種の乳酸菌を混合し、これを共生培養するとともに、この培養液をろ過してろ液を得る乳酸菌生産物質の製造方法。
【請求項4】
混合培養は、乳酸菌の少なくとも2種類を混合する第1次培養と、少なくともこの第1次培養した第1次培養菌を含む第2次培養と、少なくともこの第2次培養した第2次培養菌を含む第3次培養と、少なくともこの第3次培養した第3次培養液を含む最終培養とを有する請求項3記載の乳酸菌生産物質の製造方法。
【請求項5】
乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた請求項3または4記載の乳酸菌生産物質の製造方法。
【請求項1】
複数種の乳酸菌を共生培養した培養液をろ過したろ液からなる乳酸菌生産物質。
【請求項2】
乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた請求項1記載の乳酸菌生産物質。
【請求項3】
複数種の乳酸菌を混合し、これを共生培養するとともに、この培養液をろ過してろ液を得る乳酸菌生産物質の製造方法。
【請求項4】
混合培養は、乳酸菌の少なくとも2種類を混合する第1次培養と、少なくともこの第1次培養した第1次培養菌を含む第2次培養と、少なくともこの第2次培養した第2次培養菌を含む第3次培養と、少なくともこの第3次培養した第3次培養液を含む最終培養とを有する請求項3記載の乳酸菌生産物質の製造方法。
【請求項5】
乳酸菌として、連鎖球菌属、乳酸桿菌属、ビフィズス菌属を用いた請求項3または4記載の乳酸菌生産物質の製造方法。
【図1】




【公開番号】特開2004−137167(P2004−137167A)
【公開日】平成16年5月13日(2004.5.13)
【国際特許分類】
【出願番号】特願2002−301579(P2002−301579)
【出願日】平成14年10月16日(2002.10.16)
【出願人】(302057948)有限会社アーク技研 (2)
【Fターム(参考)】
【公開日】平成16年5月13日(2004.5.13)
【国際特許分類】
【出願日】平成14年10月16日(2002.10.16)
【出願人】(302057948)有限会社アーク技研 (2)
【Fターム(参考)】
[ Back to top ]

