事前固定式組織カセット
【課題】組織を支持するための第1の平坦な基準多孔質構造(116)と、圧縮抵抗を有する第2の多孔質構造(128)と、を含んでなる、組織を輸送するためのカセット(100)を提供すること。
【解決手段】第1の平坦な基準多孔質構造(116)及び第2の多孔質構造(128)は、その間で組織を固定するために、当接する位置に配置され、接触する位置又は接触しない位置にすることができる。
【解決手段】第1の平坦な基準多孔質構造(116)及び第2の多孔質構造(128)は、その間で組織を固定するために、当接する位置に配置され、接触する位置又は接触しない位置にすることができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、組織を摘出部位から病理学検査室に輸送するための装置に関し、限定はしないが、より具体的には、組織を摘出部位から病理学検査室に輸送するための組織カセットに関する。
【背景技術】
【0002】
本願は、2005年11月2日(係属中)に出願された継続中の仮出願番号第60/732549号の利益を主張し、該仮出願番号第60/732549号の開示は、この参照により本明細書に完全に組み込まれるものである。
【0003】
疾患の組織サンプルを検査することは、現代医療における極めて一般的な手法である。それ以外でも生体組織検査法(生検)として知られるように、患者は外科医や他の医療専門家によって体内から組織サンプルを摘出され、その組織サンプルは続いて、スライドプレパラート(slide preparation)、検査、及び診断のために、組織保存液で満たされた容器に入れられて病理学検査室(a pathology lab)に輸送される。組織が固定されずに組織保存液中に沈殿すると、その組織は硬化するときに丸くなったりねじれたりすることがある。丸くなりがちな組織の種類の例には結腸組織(colon tissue)や皮膚組織(skin tissue)があるが、他の種類の組織も同様に丸くなったりねじれたりする。
【0004】
より具体的には、外科医又は他の医療専門家が組織を摘出し、生検サンプルを取得すると、生検サンプルは続いて「固定液(fixing solution)」保存液として知られるものの中に置かれる。固定液又は保存液は一般には、ホルマリンとして知られる緩衝ホルムアルデヒドの溶液である。例えば、生検サンプルは一般に、鋭利な中空の針を使用して針の内腔内の組織を収集することによって摘出される。したがって、生検サンプルは一般には、長い皮状(skinny)であり、むしろ蛇のようである。保存液は、病理学検査室の作業者の安全性を保護するために病原体を死滅させる。組織は、球状に丸くなったり、他の三次元的なゆがみを生じたりすることがある。したがって、生検サンプルが病理学検査室に到着する頃には、生検サンプルはゆがんだ形状に硬化又は半硬化していることがある。
【0005】
組織サンプルは、切片化されて続いて診断されるためにパラフィンブロック(a paraffin block)に包埋されなければならない。生検サンプルは、パラフィン型において完全に平坦になるように再形成されなければならない。いかなるゆがんだ又は丸くなった生検サンプルも、パラフィンに包埋する前に直線状にされなければならない。組織サンプルを直線状にしなければ、後述する理由から誤診が生じることがある。これらの生検サンプルを直線状にすることは、高水準な精度が必要であり、且つサンプルの大きさがしばしば極めて小さいために困難である。
【0006】
サンプルが包埋されると、ミクロトーム(microtome)が使用され、生検サンプルとパラフィンとの結合体の切片が非常に薄くスライスされる。平均的な切片は通常3μmから5μmの厚さである。通常、技術者は、生検とパラフィンの結合体を約30回程度スライスする。これらの結合体切片すべてのパラフィンへの全体的な深さは約0.001インチ(25μm)である。したがって、生検サンプルがパラフィンに包埋される前に、生検サンプルが完全に平坦になるように正しく再配置されない場合、生検サンプルの一部が切片化されず、それによって病理医の次の検査から除外される可能性が非常に高くなる。
【0007】
多くの場合、生検サンプルを採る際に境界標表示器(landmark indicators)が使用される。境界標表示器は、患者の体に対する病巣の位置を医療専門家に示す。境界標表示器によって、腫瘍などの段階づけにおいて、その後の手術の際に追跡検査を正確に計画することができるようになる。ある種の境界標表示器とするために、縫合糸が生検サンプルに取り付けられてきた。しかしながら、縫合は、実施が困難で且つ時間を要することがある。現在、患者の解剖学的構造(anatomy)に対してサンプルの方向を識別するための、より時間を要さず且つより正確な方法に対する必要性が存在する。
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明は、これらの必要性、並びに、他の必要性に対処することを目的とする。
【課題を解決するための手段】
【0009】
本発明の一態様は、組織を保持するためのカセットである。そのカセットは、組織を支持するための第1の平坦な基準多孔質構造を有している。そのカセットはまた、圧縮抵抗を有する第2の多孔質構造を有している。第1の平坦な基準多孔質構造及び第2の多孔質構造は、その間に組織を固定するために、当接する位置に配置され得る。
【0010】
本発明の別の態様は、生検サンプルの切片の質を改善する方法である。その方法は、生検サンプルを組織カセット内に配置するステップと、組織カセットの平坦な基準表面に対して生検サンプルを平坦化させるように圧縮力を作用させるために、組織カセットの少なくとも一部を移動させるステップとを含む。
【0011】
本明細書に組み込まれると共に本明細書の一部を構成する添付の図面は、いくつかの実施形態を例示するものであり、また以下に記載した図示した実施形態の詳細な説明と共に、特許請求の範囲によってカバーされるいくつかの実施形態の説明に用いられるものである。
【発明を実施するための最良の形態】
【0012】
本出願は、生検が実施された後に組織を輸送するためのカセットに関する。一般に、カセットは、その間に組織サンプルを固定又は保持するための2つの対向する多孔質表面を有している。
【0013】
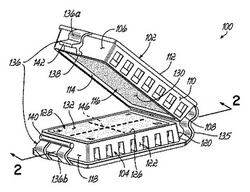
図面を参照すると、図1は組織カセット100を示している。組織カセット100は、生検組織サンプルが患者から摘出された後で病理医が視診のために生検組織サンプルを操作する前に、生検組織サンプルを保持するように構成及び配置されている。したがって、組織カセット100はホルマリン溶液などの組織保存液を入れるようになされた他の容器(図示せず)に配置されるように設計されており、この結果、溶液は、組織カセット100及びその中の任意の組織サンプルに十分に接し得る。組織カセット100は、第1の穿孔構造すなわちフレーム102及び第2の穿孔構造すなわちフレーム104を有している。本明細書において「孔のあいた」及び「多孔質」という語は、溶液が構造の孔又は穿孔を介して組織に達することができることを意味する類似又は同義の用語として使用されている。図1に示すように、第1の穿孔構造102及び第2の穿孔構造104は、概して同じ大きさのものであり、互いに対向して配置されている。このように配置することによって、第1の穿孔構造102及び第2の穿孔構造104は、それらの中に生検サンプルが挿入された後にそれに圧縮力を作用させるように突き合わせることが可能となる。第1の穿孔構造102は、前面106、後面108、及び2つの側面110を有している。これはまた、外面112も有している。後面108、及び他の任意の面は、まとめてそれらの面をなす複数の小さな面を有することができる。これら5つの面106、108、110、112は、一体となって第1の多孔質構造116を収容する内部領域114を画定している。ある実施形態においては、多孔質構造116は発泡パッドであるが、他の実施形態においては、他の種類の材料を使用してもよい。発泡パッド用の材料の種類には、連続気泡の網状構造を有するポリエステル又はポリウレタンがある。さらには、複雑なサンプルを確実に湿潤させるために、親水性を有する特殊な発泡体を使用することができる。加えて、1つの多孔質構造116が図1の内部領域114内に示されているが、他の実施形態においては2つ以上の多孔質構造を使用することができる。この図示した実施形態においては、内部領域114は実質的に箱の形状をなしているが、他の実施形態においては、第1の穿孔構造102は、形状の異なる内部領域114を有してもよい。例えば、内部領域114は楕円形状、円筒形状、矩形状、正方形状、又は当業者に容易に明らかである他の任意の領域であってもよい。したがって、内部領域114は様々な生検サンプルの大きさを受けるように大きさを決めてもよい。
【0014】
同様に、第2の穿孔構造すなわちフレーム104は、前面118、後面120、側面122、及び外面124を有している。これらの面118、120、122、124すべてを組み合わせると、第2の多孔質構造128を収容する内部領域126が画定され、その第2の多孔質構造128は発泡体又は他の材料から構成され得る。穿孔構造102、104は様々な材料から構成され得る。図示した実施例においては、穿孔構造102、104は、高密度ポリエチレン(HDPE)やアセテニルなどのプラスチック材料で構成されている。しかしながら、他の実施形態においては他の材料が使用され得る。加えて、多孔質構造116、128は、多孔質膜130、132を有してもよい。これらの多孔質膜130、132は、組織サンプルの損傷を防止するように、また組織サンプルにおける人為構造を最小限に又は防止するように構成され且つ配置されており、この結果、大きさが0.5mmに満たないものなど、極めて小さな生検サンプルを組織カセット100内で効果的に固定することが可能である。図示した実施形態においては、多孔質膜130、132はレンズペーパー又はろ紙から形成され得るが、当業者には、他の実施形態においては他の材料が使用され得ることが理解されよう。例えば、多孔質膜130、132は、熱可塑性の多孔質フィルムや網などの多孔質材料、綿又は他の天然もしくは合成の繊維材料でできた製織又は不織の材料、あるいは他の適切な材料とすることができる。1つの適切な材料が、米国デラウェア州ミドルタウンの Delstar Technologies, Inc.によってDelnet(登録商標)の名前で販売されており、この材料は、高密度ポリエチレンから形成された開口されたフィルム又は網であり、組織サンプルに面する平坦面を有している。膜130、132の一方又は両方は、望ましくない人為構造が多孔質構造116、128によって生検サンプルに形成されない限り、除去してもよい。膜130、132は、組織サンプルに対する固定液の到達及び吸上作用を妨げないようにするために、約0.001インチ(約25μm)厚としてもよい。加えて、膜130、132は約100μmから約400μmの穿孔を有しており、あるものは約200μmに近い穿孔を有している。膜130、132は、緊張状態を維持しなければならず、また温度、水分、及び試薬に対して安定な状態を維持しなければならない。加えて、膜130、132は、ホルマリン溶液などの試薬液中に置かれたときに分解してはならず、また、組織処理に使用される化学薬品にさらされたときに分解しないように設計又は調製され得る。さらにまた、膜130、132は、多孔質構造116、128もしくは穿孔構造102、104に熱かしめされ得、又は他の適切な方法によって適所に固定され得る。膜130、132は同一の材料である必要はない。例えば、膜130、132の一方をより薄く且つより伸展性のあるものとし、生検サンプルの起伏に適合させることができる。加えて、膜130、132の一方及び対応する多孔質構造116、128を単にその穿孔構造102、104に包み、それによって、必要に応じて厚い組織及び薄い組織に特に適合するようになされた浮動性の構成を可能にしてもよい。すなわち、多孔質膜130、132を避ける又は最小限にするこれらの人為構造は、生検サンプルに損傷を与えることを回避することに十分に対応するが、パラフィンなどの材料に包埋する前に生検サンプルを平坦化するのに十分に堅固である。
【0015】
多孔質構造116、128は異なるレベルの圧縮抵抗を有してもよい。しかしながら、いくつかの実施例は、同じレベルの圧縮抵抗を有する多孔質構造116、128を有している。一般に、圧縮抵抗は、約50%の圧縮において約0.5ポンド/平方インチ(約36.3g/平方センチメートル)から約4ポンド/平方インチ(約290.4g/平方センチメートル)の間で変動する。一方の多孔質構造116又は128は、より伸展性を有し、約0.5ポンド/平方インチの圧縮抵抗を有してもよい。他方の多孔質構造116又は128は、より伸展性が低く、約2ポンド/平方インチ(約145.2g/平方センチメートル)から4ポンド1平方インチの圧縮抵抗を有してもよい。より高い圧縮抵抗を有する多孔質構造116又は128はまた、基準構造として知られているものとすることができ、その対応する多孔質膜130、132は基準表面として知られているものとすることができる。多孔質構造116、128の一般的な穿孔は、およそ0.020インチ(約0.5mm)から0.025インチ(約0.625mm)の連続気泡孔である。加えて、いくつかの実施形態においては、湿潤性が十分に高く且つ孔径が十分に小さい場合、親水性を有するポリウレタン発泡体を多孔質膜なしで使用することができる。さらに、多孔質構造116、128は、ホルマリン中で、又は場合によっては組織処理に使用される化学薬品中で分解しない材料で形成されなければならない。より孔径を小さくすることによって、生検サンプルが組織カセット100内で捕捉され、また、湿潤性を高めることによって、より小さい孔径で生じうる欠点が克服される。
【0016】
図示した実施形態において、第2の多孔質構造128は、第1の多孔質構造116よりも高い圧縮抵抗を有している。よって、生検サンプルが組織カセット100内に導かれるとき、より高い圧縮抵抗を有する多孔質構造128によって、組織カセット100を閉じる際の変形に対する抵抗が得られる。したがって、生検サンプルの平坦な面が、多孔質膜132及び第2の多孔質構造128と接触する生検サンプルの表面に沿って形成される。
【0017】
組織カセット100はまた、伸展性ヒンジ135及び締め具136でできた接合装置を有している。しかしながら、当業者には、他の実施形態において他の接合装置を使用することができることが理解される。例えば、ある代替実施形態において、接合装置は、組織カセット100の各側部において互いにロックする2つの締め具とすることができる。さらに、他の実施形態において、接合装置134は、穿孔構造102、104の外周縁の周りに巻き付くゴムバンドであってもよい。したがって、多孔質構造116、128を一体に付勢するために使用することができる任意の構造が考えられる。さらに、弾性の多孔質構造116、128は、接合具を必要としない他の方式で十分な力を作用させることができるため、すべての組織カセットが接合具を必要とするわけではない。
【0018】
伸展性ヒンジ135は、後面108において第1の穿孔構造102に接合されている。伸展性ヒンジ135はまた、後面120において第2の穿孔構造104に接合されている。この配置によって、第1の穿孔構造102及び第2の穿孔構造104を互いに容易に分離すること、及び容易に締めつけることが可能となる「二枚貝(clam shell)」に似た設計が得られる。さらに、この配置によって、第1及び第2の穿孔構造102及び104の前端面106と118の間を最大限に分離することが可能となる。この配置により、使用者は、摘出器具を使用しまた必要に応じて医療専門家の助けを少しばかり借りて、内部領域114、126の内部に生検サンプルを容易に配置することが可能となる。
【0019】
図1に示す締め具136は、穿孔構造102、104を接合するのを助けることができる1つの構造であるが、当業者には、閉鎖の際に生検サンプルに作用させるべき圧縮力を他の機構が与える限り、その機構を使用してもよいことが理解されよう。図示した実施形態の締め具136は、上部部分136a及び下部部分136bを有している。上部部分136aは、上部部分136aの端部にラッチ138が設けられている。このラッチ138は、下部部分136bに配置されたバー140上で摺動し、続いてバー140の周りで後退して定位置に堅固にロックされる。加えて、上部部分136aはタブ142を有しており、このタブ142を利用することによって、医療専門家は、バー140の下方からラッチ138を後退させるように自身の親指又は指を単にタブ142の下側に押し付けることによって、必要なときに組織カセット100を容易に開くことが可能となる。締め具136は、対向する多孔質表面116、128の間に配置された生検サンプルに圧縮力を作用させるように、多孔質表面116、128を強制的に合わせる。締め具136はまた、組織カセット100が開かれ、且つ生検サンプルをパラフィンなどの材料内に包埋する準備ができるまで、その圧縮力を絶えず且つ均一に維持するために、ラッチ138及びバー140を有している。
【0020】
図2及び図3はそれぞれ、閉位置及び開位置にある生検カセット100を示している。外面112は複数の孔144を有していることがわかる。これらの孔144によって、ホルマリンなどの固定液を導くことが可能になる。多孔質構造116、128によって、流体は多孔質膜130、132に達することが可能となり、その結果、平坦化され且つ損傷を受けていない状態に生検サンプルを固定することができる。したがって、組織カセット100は視診用に生検サンプルを準備する。
【0021】
使用時に、組織カセット100は、その中に配置された生検サンプルを平坦化し且つ損傷を受けていない状態のままにする。最初に、医療専門家は患者に生検を実施して生検サンプルを得る。これは通常、針又は他の器具内に画定された内腔の内部で生検サンプルを採取するために、針又は他の中空の器具を使用して行われる。その生検サンプルは、続いて組織カセット100へと運ばれ、ここで多孔質膜130、132の一方に配置される。この時点で、生検サンプルは平坦でなくてもよい。生検サンプルは、多くの形状で丸くなったりゆがんだりすることがある。
【0022】
次に組織カセット100は閉じられ、多孔質膜130、132は均等で且つ一定の圧力を生検サンプルに作用させることができる。多孔質構造116、128の間で圧縮抵抗が異なり、結果として生検サンプルの一方の側が平坦化される。より高い圧縮抵抗を有する第2の多孔質構造128は、実質的に圧縮されず、第1の多孔質構造116は、生検サンプルに損傷を与えず且つ人為構造(artifact)をその中に導かないように圧縮される。第1の多孔質構造116は、第2の多孔質構造128に対する側面を除いて、組織サンプルのすべての側面を囲繞することができる。組織サンプルの一方の側面の平坦化は、多孔質膜130又は132の一方を緊張させることによって発生させることができる。加えて、他方の多孔質膜130又は132は、熱かしめされず単に多孔質構造116もしくは128上に載せられることによって、又は多孔質構造116もしくは128にのみ固定され、穿孔構造102、104には固定されないことによって、その穿孔構造102、104の内部で自由に動くことができる。同様に、多孔質構造116及び/又は128は、関連する穿孔構造102、104に固定されてもよく、又は固定されなくてもよい。したがって、生検サンプルは、生検サンプルが丸くなったりねじれたりすること、及び視認可能な縁辺が減少することを防止するために、平坦化され且つ固定され得る。
【0023】
組織カセット100は、固定液を充填した容器に浸漬してもよい。次に、生検サンプルは一方の側面で平坦に且つ視認可能な人為構造なく硬化され得る。平坦面を有することは、皮膚の生検サンプルには特に重要である。組織カセット100はその後、医療専門家によって開ける準備ができるまで保管することができる。組織カセット100を使用することによって、生検サンプルは、例えば0.0025インチ(約62.5μm)未満の変動で平坦に保持することが可能となることがある。サンプルは丸くならず、悪性組織の切除に対する縁辺を変形させないため、この水準の精度は皮膚組織の生検に重要となることがある。したがって、技術者が生検サンプルをパラフィンに投入し、次にミクロトームを使用してスライスする際、そのサンプルを取り扱う外科医又は他の医療専門家が意図する縁辺が組織学的な処理の間適切に保たれるため、生検サンプルが丸くなる又は変形することによる誤診の可能性が低下する。病理医は、摘出する医療専門家に引き渡される縁辺が医療専門家が意図したとおりとなることが保証される。
【0024】
ここで図4A〜図4Cを参照すると、境界標表示システム146が、例えば、圧縮抵抗がより高い多孔質構造128に関連する多孔質膜132に使用することができることが示されている。生検サンプルを摘出する医療専門家は、生検サンプルを多孔質膜132に配置し、境界標表示システム146を使用して、摘出された組織の解剖学的位置や生検サンプルに関する他の情報を伝える。境界標表示システム146は、ラベル150を使用して識別される4つの四半部(quadrants)148を有している。例示的な実施例が、以下で説明する図4A〜図4Cに示されている。図4A〜図4Cは境界標表示システム146のいくつかの使用法を示しているが、当業者には、境界標表示システム146を他の方式でも使用することができることが理解される。
【0025】
ここで図4Aを参照すると、境界標表示システム146が、前立腺から採られた生検サンプル152及び154と共に使用されている。生検サンプル152及び154は、生検中に医療専門家によって摘出された前立腺中心部を表している。生検サンプル152は、前立腺の左側から摘出された中心部を示している。したがって、「左側」ラベル150はこれを意味するために囲まれている。同様に、生検サンプル154は前立腺の右側から採られたものであり、したがって「右側」ラベル150が囲まれている。このようにして、組織技術者又は他の医療専門家は、パラフィン切片にラベルをつけて、中心部が摘出された前立腺の領域を正確に表すことが可能となる。
【0026】
図4Bは境界標表示システム146の他の使用法を示している。境界標表示システム146の中央には、指から採られた皮膚組織サンプル156がある。皮膚組織156は病巣158を有している。皮膚組織サンプル156の方向は、図4Bに示す「近位」及び「遠位」ラベル150を囲むことによって識別される。ここでも、皮膚組織サンプル156を摘出する医療専門家は、このシステムによって、皮膚サンプルの向きを患者の指の近位端及び遠位端に関して容易に知らせることができる。このようにして、誤認の可能性が減少する。
【0027】
図4Cは、多数の生検サンプル160を採って使用する境界標表示システム146を示している。組織カセット100は、閉じられると、生検サンプル160を定位置に保つ。したがって、外科医などの医療専門家は、外科報告を作成し、囲まれた「1」というラベル150に対応する四半部「1」の見出しの下に注釈を記すことができる。かかる注釈には、これらのサンプルの特徴を記載することができる。例えば、「1」のラベル150を有する四半部148にあるサンプル160はすべて膵臓からのものと仮定する。加えて、生検がさらに胆嚢、腎臓、及び肝臓からも採られたと仮定する。サンプル160を四半部148に編成することができ、次にその番号に対応するラベル150を囲むことができる。外科報告書は外科医によって記述され、ラベル150が「1」を有する四半部148のサンプルは膵臓から採られたものであり、「2」の下にあるものは胆嚢から採られたもの、などを示す情報を記すことができる。このようにして、境界標表示システム146は、多数の異なる方式で病理医や組織技術者に情報を提供することができる。
【0028】
病理医及び組織技術者は、その後に概略的な説明書を作成するとき、医療専門家が伝えたラベル150からの情報を使用することができる。概略的な説明書は、組織技術者又は病理医が組織カセット100を開き、組織を摘出した医療専門家が示した数、配置、大きさ、及び/又は解剖学的方向を観測することによって作成される。引き続き、組織カセット100は、包埋前に生検サンプルの付加的な操作を必要とすることなく、さらなる組織処理のために閉じることができる。組織カセット100は、組織固定処理の全体を通じて生検サンプルの方向を完全に維持する。
【0029】
包埋処理を実施するために、組織技術者又は病理医は組織カセット100から生検サンプルを取り出す。境界標表示システム146によって、解剖学的な摘出位置を容易に識別することが可能となり、また正しい方向に合わせ、標準的な包埋板内に整理することが可能となる。別法として、セクショナブルカセットを有するシステムを使用する場合、組織カセット100は、生検サンプルを平坦に保ち、境界標表示システム146を使用して生検サンプルの摘出方向を示す。組織は、事前に固定され(prefixed)且つ相当に硬化された後に、組織カセット100から取り出され、セクショナブルカセット、他の支持体、包埋する中間板などに配置される。
【0030】
ここで図5A及び図5B、並びに図6A及び図6Bを参照すると、図5A及び図6Aにそれぞれ示す第1のスライド162、164は、通常の組織保存容器から取り出され且つ保存溶液に自由に浸漬された生検サンプルを示している。図5B及び図6Bにそれぞれ示す第2のスライド166、168は、次に保存溶液に浸漬された組織カセット100から取り出された生検サンプルを示している。第2のスライド166、168は、明確で且つ全幅を有するサンプルを示している。スライドの切片の堅固性が改善されている。したがって、後の診断のために生検サンプルを包埋する間の誤認の余地が、組織カセット100によって大いに減じられている。
【0031】
図7Aは、パラフィンろうなどの材料で包埋する間に生検サンプル172を保持する型170を示している。型170は、サンプル172が図示の形状に硬化された後に、生検サンプル172を受ける。生検サンプル172は、曲がっており、高い位置174及び低い位置176を有している。生検サンプル172をパラフィンろうに包埋した後、ミクロトームを使用して生検サンプル172から複数の切片を取り出すことができる。線178は、生検サンプル172から切片が取り出される最も共通する領域を示している。生検サンプル172は、一群の癌細胞などの病巣180を有している。線178は病巣180の下方にある。図7Bを参照すると、線178に沿って切り取った切片が、スライド182の上に配置されたものとして示されている。組織サンプル172の3つの切片がスライド182に配置されている。第1の切片172aは、図7A及び図7Bに示す点Aと点Bとの間の生検サンプル172の長さに対応する。第2の切片172bは、点Cと点Dとの間の生検サンプル172の長さに対応する。第3の切片172cは、点Eと点Fとの間の生検サンプルの長さに対応する。病巣180は、高い点174に近い点DとEとの間にあるため現れない。したがって、診断は不正確になるであろう。
【0032】
ここで図8Aを参照すると、生検サンプル172’が、図1の組織カセット100から取り出されており、型170内に配置されている。生検サンプル172’を型170内に配置した後、生検サンプル172’はパラフィンろうなどの材料に包埋される。次に、例えば線178を通じて、ミクロトームで切片が取り出される。図1の組織カセットは、生検サンプル172’を平坦に形成していたため、線178は病巣180’を通過する。図8Bは、線178を通じて切り取られた切片を医療専門家が診断の準備の際にスライド182の上に配置したことを示している。生検サンプル172’は、生検サンプル172’の全長に沿って認識可能な平坦な切片172a’を有している。したがって、病巣180a’の切片は、平坦な切片172a’の内部に現れ、病理医又は他の医療専門家によって発見されよう。このようにして、組織カセット100は、生検サンプル172の適切な診断が実施されることを確実に導く。
【0033】
ここで図9〜図11及び図11Aを参照すると、第2の例示的実施形態による組織カセット100’が示されている。組織カセット100’は、第1の実施形態に関連して上述した特徴を有してもよい。以下の説明及び各図面の描写を検討することによって明らかとなるように、ある差異が第1と第2の実施形態との間に存在する。プライム符号(’)を有する同じ参照符号は、第1と第2の実施形態とにおけるそれぞれに対応する要素を示すために使用されおり、構造的及び/又は機能的差異は各図面の描写、説明文、又は双方を検討することによって明らかである。組織カセット100’は、蓋部102’及び基部104’を有する第1及び第2の穿孔構造を備えており、その蓋部102’及び基部104’は、一方の端部のヒンジ135’及び反対側の端部の締め具構造136’によって連結され得る。カセット100’内へ流体が流れるように、開口部144’が設けられている。締め具構造は、基部104’上の凹部136b’内で受けられる蓋部102’上の突起部136’を備えてもよい。蓋部102’はまた、ヒンジ135’に隣接して第2の締め具構造236を有している。この締め具構造236は、図10に開位置で、図11Aに閉位置で最良に示されるように、突起部236aと凹部236bとを備えている。蓋部102’が閉じられると、脆弱なヒンジは割れ、締め具構造236は、図11及び図11Aに示すように、締め具構造136’と共に閉位置で蓋部102’を基部104’に押し付けるように係合する。蓋部102’の側壁240、242は、基部104’(図10)の相補的受入れ領域246、248内で受容される。したがって、図9に示す閉位置において、組織サンプルは、カセット100’の側部並びに各締め具構造136’、236を有するカセット100’の端部から逃げるのを防止される。蓋部102’上のタブ200は、上向きの力を蓋部102’に作用させて締め具136’との結合を解除するために使用してもよい。
【0034】
図11及び図11Aに示すように、多孔質膜130’、132’は、突起部202を使用することによって穿孔構造102’、104’に熱かしめしてもよい。熱かしめ操作前の小さな円筒状要素としてのこれらの突起部202が図10に示されている。熱かしめの後、円筒状要素202はキノコのような形状の頭部を形成し、その頭部は、多孔質構造又は発泡体116’、128’の上面部に対して膜130’、132’の縁部を保持する。図11及び図11Aにさらに示すように、図11Aに示す矢印203の方向に蓋部102’と基部104’との間を流体(ホルマリンなど)が移動することが可能なように、完全に第1及び第2の穿孔構造102’、104’の間に流体路を形成してもよい。流体路は、穿孔構造102’、104’の付加的な部分102a’、102b’、104a’、104b’の間及び「キノコのような」突起部202の間に延在している。突起部202は、蓋部102’が閉じられたとき、図11Aに示すように整列する代わりに、互いに食い違い状となってもよい。この流体路によって、組織サンプルを完全に浸潤させることが可能となる。また、間隔204が上部及び下部の多孔質膜130’、132’の間に示されている。間隔204は、特定の用途の必要性に応じて、存在してもしなくてもよい。例えば、より大きい組織サンプルには、依然としてサンプルを適切に保持することが可能となる適切な寸法の間隔204が必要となることがあるが、その一方で、より小さい試料には間隔204が必要でないことがある。
【0035】
非付着性のコーティングを多孔質膜130’、132’の一方又は両方に処理してもよく、その結果、非付着性のコーティングを有する表面130’又は132’から1つ又は複数の組織サンプルを容易に取り出すことができることはさらに強調されるべきである。別法として、膜材料自体がPTFEなどの非付着性の材料を備えてもよい。他の別法として、1つ又は複数の組織サンプルを膜130’又は132’上に保持するために、その組織サンプルを多孔質膜130’又は132’の一方に接着剤で固定してもよい。ホルマリンなどの流体で固定した後、接着剤で固定された1つ又は複数の組織サンプルを有する膜は、カセット100’から切り取られ、パラフィンなどの材料に包埋するために包埋板又はセクショナブルカセットの底部に配置され得る。1つ又は複数の組織サンプルが膜の一方に接着剤で固定されるかどうかにかかわらず、蓋部102’は、1つ又は複数の生検サンプルを取り出す前又は取り出した後に、基部104’から完全に取り外されて破棄することができる。1つ又は複数の生検サンプルを通常のパラフィン型の底部に配置することができ、その型を融解した流動パラフィンで満たすことができる。パラフィンが依然として融解している間に、基部104’をパラフィンと接触させて配置することができる。続いてパラフィンは冷却し硬化する。続いて基部104’は、ミクロトームチャック内に保持するための固定具として使用され得る。次に、硬化したパラフィン上でミクロトーム操作を実施することができ、スライドプレパラート(slide preparation)及び分析を行うことができる。
【0036】
これらの実施形態についてかなり詳細に説明したが、かかる詳細に特許請求の範囲を制限するものではなく、或いは、いかなる形式であれ限定することは、本出願人の意図することではない。付加的な利点及び変形例は、当業者にとっては容易に明らかであろう。したがって、特許請求の範囲は、代表的なシステム、機器、及び方法の具体的な詳細、並びに図示し説明した例示的実施例に限定されない。したがって、本出願人の特許請求の範囲の精神及び範囲から逸脱することなく、かかる詳細な実施例を応用することが可能である。
【図面の簡単な説明】
【0037】
【図1】一実施形態による開位置にある組織カセットの斜視図である。
【図2】概ね図1の線2−2に沿って取られた組織カセットの断面図であるが、閉位置すなわちラッチ係合された位置を示す。
【図3】同様に概ね図1の線2−2に沿って取られた組織カセットの斜視断面図であり、開位置にあるカセットを示す。
【図4A】図1の組織カセットを使用した様々な用途における境界標表示システムを示す平面図である。
【図4B】図1の組織カセットを使用した様々な用途における境界標表示システムを示す平面図である。
【図4C】図1の組織カセットを使用した様々な用途における境界標表示システムを示す平面図である。
【図5A】第1の顕微鏡スライドを示す図であり、あらかじめ通常の生検容器内で保持された生検サンプルを示す。
【図5B】第2の顕微鏡スライドを示す図であり、図1の組織カセットで保持されたサンプルを示す。
【図6A】第1の顕微鏡スライドを示す図であり、あらかじめ通常の生検容器内でホルマリンと共に保持された生検サンプルを示す。
【図6B】第2の顕微鏡スライドを示す図であり、図1の組織カセットで保持されたサンプルを示す。
【図7A】通常の組織輸送容器又は生検容器から得られた組織サンプルを示す図であり、組織は包埋及び切片化に先立ってパラフィン型の中に配置されている。
【図7B】医療専門家による診断用にスライドの上に配置された図7Aの組織サンプルの一切片を示す図である。
【図8A】図1の組織カセットから得られた組織サンプルを示す図であり、組織は包埋及び切片化に先立ってパラフィン型の中に配置されている。
【図8B】医療専門家による診断用にスライドの上に配置された図8Aの組織サンプルの一切片を示す図である。
【図9】他の実施形態による組織カセットの斜視図であり、閉位置を示す。
【図10】図9に示す組織カセットの斜視図であるが、各多孔質膜を取り付ける前の状態を示す。
【図11】図9の線11−11に沿って取られた断面図である。
【図11A】図11に示す囲い部11Aの拡大図である。
【符号の説明】
【0038】
100、100’ 組織カセット
102、102’ 穿孔構造
104、104’ 穿孔構造
116 多孔質構造
128 多孔質構造
130 多孔質膜
132 多孔質膜
135、135’ 伸展性ヒンジ
136、136’ 締め具
144、144’ 孔
146 境界標表示システム
148 四半部
150 ラベル
152、154、160 生検サンプル
162、164、166、168、182 スライド
172、172’ 生検サンプル
180、180’ 病巣
236 締め具構造
【技術分野】
【0001】
本発明は、組織を摘出部位から病理学検査室に輸送するための装置に関し、限定はしないが、より具体的には、組織を摘出部位から病理学検査室に輸送するための組織カセットに関する。
【背景技術】
【0002】
本願は、2005年11月2日(係属中)に出願された継続中の仮出願番号第60/732549号の利益を主張し、該仮出願番号第60/732549号の開示は、この参照により本明細書に完全に組み込まれるものである。
【0003】
疾患の組織サンプルを検査することは、現代医療における極めて一般的な手法である。それ以外でも生体組織検査法(生検)として知られるように、患者は外科医や他の医療専門家によって体内から組織サンプルを摘出され、その組織サンプルは続いて、スライドプレパラート(slide preparation)、検査、及び診断のために、組織保存液で満たされた容器に入れられて病理学検査室(a pathology lab)に輸送される。組織が固定されずに組織保存液中に沈殿すると、その組織は硬化するときに丸くなったりねじれたりすることがある。丸くなりがちな組織の種類の例には結腸組織(colon tissue)や皮膚組織(skin tissue)があるが、他の種類の組織も同様に丸くなったりねじれたりする。
【0004】
より具体的には、外科医又は他の医療専門家が組織を摘出し、生検サンプルを取得すると、生検サンプルは続いて「固定液(fixing solution)」保存液として知られるものの中に置かれる。固定液又は保存液は一般には、ホルマリンとして知られる緩衝ホルムアルデヒドの溶液である。例えば、生検サンプルは一般に、鋭利な中空の針を使用して針の内腔内の組織を収集することによって摘出される。したがって、生検サンプルは一般には、長い皮状(skinny)であり、むしろ蛇のようである。保存液は、病理学検査室の作業者の安全性を保護するために病原体を死滅させる。組織は、球状に丸くなったり、他の三次元的なゆがみを生じたりすることがある。したがって、生検サンプルが病理学検査室に到着する頃には、生検サンプルはゆがんだ形状に硬化又は半硬化していることがある。
【0005】
組織サンプルは、切片化されて続いて診断されるためにパラフィンブロック(a paraffin block)に包埋されなければならない。生検サンプルは、パラフィン型において完全に平坦になるように再形成されなければならない。いかなるゆがんだ又は丸くなった生検サンプルも、パラフィンに包埋する前に直線状にされなければならない。組織サンプルを直線状にしなければ、後述する理由から誤診が生じることがある。これらの生検サンプルを直線状にすることは、高水準な精度が必要であり、且つサンプルの大きさがしばしば極めて小さいために困難である。
【0006】
サンプルが包埋されると、ミクロトーム(microtome)が使用され、生検サンプルとパラフィンとの結合体の切片が非常に薄くスライスされる。平均的な切片は通常3μmから5μmの厚さである。通常、技術者は、生検とパラフィンの結合体を約30回程度スライスする。これらの結合体切片すべてのパラフィンへの全体的な深さは約0.001インチ(25μm)である。したがって、生検サンプルがパラフィンに包埋される前に、生検サンプルが完全に平坦になるように正しく再配置されない場合、生検サンプルの一部が切片化されず、それによって病理医の次の検査から除外される可能性が非常に高くなる。
【0007】
多くの場合、生検サンプルを採る際に境界標表示器(landmark indicators)が使用される。境界標表示器は、患者の体に対する病巣の位置を医療専門家に示す。境界標表示器によって、腫瘍などの段階づけにおいて、その後の手術の際に追跡検査を正確に計画することができるようになる。ある種の境界標表示器とするために、縫合糸が生検サンプルに取り付けられてきた。しかしながら、縫合は、実施が困難で且つ時間を要することがある。現在、患者の解剖学的構造(anatomy)に対してサンプルの方向を識別するための、より時間を要さず且つより正確な方法に対する必要性が存在する。
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明は、これらの必要性、並びに、他の必要性に対処することを目的とする。
【課題を解決するための手段】
【0009】
本発明の一態様は、組織を保持するためのカセットである。そのカセットは、組織を支持するための第1の平坦な基準多孔質構造を有している。そのカセットはまた、圧縮抵抗を有する第2の多孔質構造を有している。第1の平坦な基準多孔質構造及び第2の多孔質構造は、その間に組織を固定するために、当接する位置に配置され得る。
【0010】
本発明の別の態様は、生検サンプルの切片の質を改善する方法である。その方法は、生検サンプルを組織カセット内に配置するステップと、組織カセットの平坦な基準表面に対して生検サンプルを平坦化させるように圧縮力を作用させるために、組織カセットの少なくとも一部を移動させるステップとを含む。
【0011】
本明細書に組み込まれると共に本明細書の一部を構成する添付の図面は、いくつかの実施形態を例示するものであり、また以下に記載した図示した実施形態の詳細な説明と共に、特許請求の範囲によってカバーされるいくつかの実施形態の説明に用いられるものである。
【発明を実施するための最良の形態】
【0012】
本出願は、生検が実施された後に組織を輸送するためのカセットに関する。一般に、カセットは、その間に組織サンプルを固定又は保持するための2つの対向する多孔質表面を有している。
【0013】
図面を参照すると、図1は組織カセット100を示している。組織カセット100は、生検組織サンプルが患者から摘出された後で病理医が視診のために生検組織サンプルを操作する前に、生検組織サンプルを保持するように構成及び配置されている。したがって、組織カセット100はホルマリン溶液などの組織保存液を入れるようになされた他の容器(図示せず)に配置されるように設計されており、この結果、溶液は、組織カセット100及びその中の任意の組織サンプルに十分に接し得る。組織カセット100は、第1の穿孔構造すなわちフレーム102及び第2の穿孔構造すなわちフレーム104を有している。本明細書において「孔のあいた」及び「多孔質」という語は、溶液が構造の孔又は穿孔を介して組織に達することができることを意味する類似又は同義の用語として使用されている。図1に示すように、第1の穿孔構造102及び第2の穿孔構造104は、概して同じ大きさのものであり、互いに対向して配置されている。このように配置することによって、第1の穿孔構造102及び第2の穿孔構造104は、それらの中に生検サンプルが挿入された後にそれに圧縮力を作用させるように突き合わせることが可能となる。第1の穿孔構造102は、前面106、後面108、及び2つの側面110を有している。これはまた、外面112も有している。後面108、及び他の任意の面は、まとめてそれらの面をなす複数の小さな面を有することができる。これら5つの面106、108、110、112は、一体となって第1の多孔質構造116を収容する内部領域114を画定している。ある実施形態においては、多孔質構造116は発泡パッドであるが、他の実施形態においては、他の種類の材料を使用してもよい。発泡パッド用の材料の種類には、連続気泡の網状構造を有するポリエステル又はポリウレタンがある。さらには、複雑なサンプルを確実に湿潤させるために、親水性を有する特殊な発泡体を使用することができる。加えて、1つの多孔質構造116が図1の内部領域114内に示されているが、他の実施形態においては2つ以上の多孔質構造を使用することができる。この図示した実施形態においては、内部領域114は実質的に箱の形状をなしているが、他の実施形態においては、第1の穿孔構造102は、形状の異なる内部領域114を有してもよい。例えば、内部領域114は楕円形状、円筒形状、矩形状、正方形状、又は当業者に容易に明らかである他の任意の領域であってもよい。したがって、内部領域114は様々な生検サンプルの大きさを受けるように大きさを決めてもよい。
【0014】
同様に、第2の穿孔構造すなわちフレーム104は、前面118、後面120、側面122、及び外面124を有している。これらの面118、120、122、124すべてを組み合わせると、第2の多孔質構造128を収容する内部領域126が画定され、その第2の多孔質構造128は発泡体又は他の材料から構成され得る。穿孔構造102、104は様々な材料から構成され得る。図示した実施例においては、穿孔構造102、104は、高密度ポリエチレン(HDPE)やアセテニルなどのプラスチック材料で構成されている。しかしながら、他の実施形態においては他の材料が使用され得る。加えて、多孔質構造116、128は、多孔質膜130、132を有してもよい。これらの多孔質膜130、132は、組織サンプルの損傷を防止するように、また組織サンプルにおける人為構造を最小限に又は防止するように構成され且つ配置されており、この結果、大きさが0.5mmに満たないものなど、極めて小さな生検サンプルを組織カセット100内で効果的に固定することが可能である。図示した実施形態においては、多孔質膜130、132はレンズペーパー又はろ紙から形成され得るが、当業者には、他の実施形態においては他の材料が使用され得ることが理解されよう。例えば、多孔質膜130、132は、熱可塑性の多孔質フィルムや網などの多孔質材料、綿又は他の天然もしくは合成の繊維材料でできた製織又は不織の材料、あるいは他の適切な材料とすることができる。1つの適切な材料が、米国デラウェア州ミドルタウンの Delstar Technologies, Inc.によってDelnet(登録商標)の名前で販売されており、この材料は、高密度ポリエチレンから形成された開口されたフィルム又は網であり、組織サンプルに面する平坦面を有している。膜130、132の一方又は両方は、望ましくない人為構造が多孔質構造116、128によって生検サンプルに形成されない限り、除去してもよい。膜130、132は、組織サンプルに対する固定液の到達及び吸上作用を妨げないようにするために、約0.001インチ(約25μm)厚としてもよい。加えて、膜130、132は約100μmから約400μmの穿孔を有しており、あるものは約200μmに近い穿孔を有している。膜130、132は、緊張状態を維持しなければならず、また温度、水分、及び試薬に対して安定な状態を維持しなければならない。加えて、膜130、132は、ホルマリン溶液などの試薬液中に置かれたときに分解してはならず、また、組織処理に使用される化学薬品にさらされたときに分解しないように設計又は調製され得る。さらにまた、膜130、132は、多孔質構造116、128もしくは穿孔構造102、104に熱かしめされ得、又は他の適切な方法によって適所に固定され得る。膜130、132は同一の材料である必要はない。例えば、膜130、132の一方をより薄く且つより伸展性のあるものとし、生検サンプルの起伏に適合させることができる。加えて、膜130、132の一方及び対応する多孔質構造116、128を単にその穿孔構造102、104に包み、それによって、必要に応じて厚い組織及び薄い組織に特に適合するようになされた浮動性の構成を可能にしてもよい。すなわち、多孔質膜130、132を避ける又は最小限にするこれらの人為構造は、生検サンプルに損傷を与えることを回避することに十分に対応するが、パラフィンなどの材料に包埋する前に生検サンプルを平坦化するのに十分に堅固である。
【0015】
多孔質構造116、128は異なるレベルの圧縮抵抗を有してもよい。しかしながら、いくつかの実施例は、同じレベルの圧縮抵抗を有する多孔質構造116、128を有している。一般に、圧縮抵抗は、約50%の圧縮において約0.5ポンド/平方インチ(約36.3g/平方センチメートル)から約4ポンド/平方インチ(約290.4g/平方センチメートル)の間で変動する。一方の多孔質構造116又は128は、より伸展性を有し、約0.5ポンド/平方インチの圧縮抵抗を有してもよい。他方の多孔質構造116又は128は、より伸展性が低く、約2ポンド/平方インチ(約145.2g/平方センチメートル)から4ポンド1平方インチの圧縮抵抗を有してもよい。より高い圧縮抵抗を有する多孔質構造116又は128はまた、基準構造として知られているものとすることができ、その対応する多孔質膜130、132は基準表面として知られているものとすることができる。多孔質構造116、128の一般的な穿孔は、およそ0.020インチ(約0.5mm)から0.025インチ(約0.625mm)の連続気泡孔である。加えて、いくつかの実施形態においては、湿潤性が十分に高く且つ孔径が十分に小さい場合、親水性を有するポリウレタン発泡体を多孔質膜なしで使用することができる。さらに、多孔質構造116、128は、ホルマリン中で、又は場合によっては組織処理に使用される化学薬品中で分解しない材料で形成されなければならない。より孔径を小さくすることによって、生検サンプルが組織カセット100内で捕捉され、また、湿潤性を高めることによって、より小さい孔径で生じうる欠点が克服される。
【0016】
図示した実施形態において、第2の多孔質構造128は、第1の多孔質構造116よりも高い圧縮抵抗を有している。よって、生検サンプルが組織カセット100内に導かれるとき、より高い圧縮抵抗を有する多孔質構造128によって、組織カセット100を閉じる際の変形に対する抵抗が得られる。したがって、生検サンプルの平坦な面が、多孔質膜132及び第2の多孔質構造128と接触する生検サンプルの表面に沿って形成される。
【0017】
組織カセット100はまた、伸展性ヒンジ135及び締め具136でできた接合装置を有している。しかしながら、当業者には、他の実施形態において他の接合装置を使用することができることが理解される。例えば、ある代替実施形態において、接合装置は、組織カセット100の各側部において互いにロックする2つの締め具とすることができる。さらに、他の実施形態において、接合装置134は、穿孔構造102、104の外周縁の周りに巻き付くゴムバンドであってもよい。したがって、多孔質構造116、128を一体に付勢するために使用することができる任意の構造が考えられる。さらに、弾性の多孔質構造116、128は、接合具を必要としない他の方式で十分な力を作用させることができるため、すべての組織カセットが接合具を必要とするわけではない。
【0018】
伸展性ヒンジ135は、後面108において第1の穿孔構造102に接合されている。伸展性ヒンジ135はまた、後面120において第2の穿孔構造104に接合されている。この配置によって、第1の穿孔構造102及び第2の穿孔構造104を互いに容易に分離すること、及び容易に締めつけることが可能となる「二枚貝(clam shell)」に似た設計が得られる。さらに、この配置によって、第1及び第2の穿孔構造102及び104の前端面106と118の間を最大限に分離することが可能となる。この配置により、使用者は、摘出器具を使用しまた必要に応じて医療専門家の助けを少しばかり借りて、内部領域114、126の内部に生検サンプルを容易に配置することが可能となる。
【0019】
図1に示す締め具136は、穿孔構造102、104を接合するのを助けることができる1つの構造であるが、当業者には、閉鎖の際に生検サンプルに作用させるべき圧縮力を他の機構が与える限り、その機構を使用してもよいことが理解されよう。図示した実施形態の締め具136は、上部部分136a及び下部部分136bを有している。上部部分136aは、上部部分136aの端部にラッチ138が設けられている。このラッチ138は、下部部分136bに配置されたバー140上で摺動し、続いてバー140の周りで後退して定位置に堅固にロックされる。加えて、上部部分136aはタブ142を有しており、このタブ142を利用することによって、医療専門家は、バー140の下方からラッチ138を後退させるように自身の親指又は指を単にタブ142の下側に押し付けることによって、必要なときに組織カセット100を容易に開くことが可能となる。締め具136は、対向する多孔質表面116、128の間に配置された生検サンプルに圧縮力を作用させるように、多孔質表面116、128を強制的に合わせる。締め具136はまた、組織カセット100が開かれ、且つ生検サンプルをパラフィンなどの材料内に包埋する準備ができるまで、その圧縮力を絶えず且つ均一に維持するために、ラッチ138及びバー140を有している。
【0020】
図2及び図3はそれぞれ、閉位置及び開位置にある生検カセット100を示している。外面112は複数の孔144を有していることがわかる。これらの孔144によって、ホルマリンなどの固定液を導くことが可能になる。多孔質構造116、128によって、流体は多孔質膜130、132に達することが可能となり、その結果、平坦化され且つ損傷を受けていない状態に生検サンプルを固定することができる。したがって、組織カセット100は視診用に生検サンプルを準備する。
【0021】
使用時に、組織カセット100は、その中に配置された生検サンプルを平坦化し且つ損傷を受けていない状態のままにする。最初に、医療専門家は患者に生検を実施して生検サンプルを得る。これは通常、針又は他の器具内に画定された内腔の内部で生検サンプルを採取するために、針又は他の中空の器具を使用して行われる。その生検サンプルは、続いて組織カセット100へと運ばれ、ここで多孔質膜130、132の一方に配置される。この時点で、生検サンプルは平坦でなくてもよい。生検サンプルは、多くの形状で丸くなったりゆがんだりすることがある。
【0022】
次に組織カセット100は閉じられ、多孔質膜130、132は均等で且つ一定の圧力を生検サンプルに作用させることができる。多孔質構造116、128の間で圧縮抵抗が異なり、結果として生検サンプルの一方の側が平坦化される。より高い圧縮抵抗を有する第2の多孔質構造128は、実質的に圧縮されず、第1の多孔質構造116は、生検サンプルに損傷を与えず且つ人為構造(artifact)をその中に導かないように圧縮される。第1の多孔質構造116は、第2の多孔質構造128に対する側面を除いて、組織サンプルのすべての側面を囲繞することができる。組織サンプルの一方の側面の平坦化は、多孔質膜130又は132の一方を緊張させることによって発生させることができる。加えて、他方の多孔質膜130又は132は、熱かしめされず単に多孔質構造116もしくは128上に載せられることによって、又は多孔質構造116もしくは128にのみ固定され、穿孔構造102、104には固定されないことによって、その穿孔構造102、104の内部で自由に動くことができる。同様に、多孔質構造116及び/又は128は、関連する穿孔構造102、104に固定されてもよく、又は固定されなくてもよい。したがって、生検サンプルは、生検サンプルが丸くなったりねじれたりすること、及び視認可能な縁辺が減少することを防止するために、平坦化され且つ固定され得る。
【0023】
組織カセット100は、固定液を充填した容器に浸漬してもよい。次に、生検サンプルは一方の側面で平坦に且つ視認可能な人為構造なく硬化され得る。平坦面を有することは、皮膚の生検サンプルには特に重要である。組織カセット100はその後、医療専門家によって開ける準備ができるまで保管することができる。組織カセット100を使用することによって、生検サンプルは、例えば0.0025インチ(約62.5μm)未満の変動で平坦に保持することが可能となることがある。サンプルは丸くならず、悪性組織の切除に対する縁辺を変形させないため、この水準の精度は皮膚組織の生検に重要となることがある。したがって、技術者が生検サンプルをパラフィンに投入し、次にミクロトームを使用してスライスする際、そのサンプルを取り扱う外科医又は他の医療専門家が意図する縁辺が組織学的な処理の間適切に保たれるため、生検サンプルが丸くなる又は変形することによる誤診の可能性が低下する。病理医は、摘出する医療専門家に引き渡される縁辺が医療専門家が意図したとおりとなることが保証される。
【0024】
ここで図4A〜図4Cを参照すると、境界標表示システム146が、例えば、圧縮抵抗がより高い多孔質構造128に関連する多孔質膜132に使用することができることが示されている。生検サンプルを摘出する医療専門家は、生検サンプルを多孔質膜132に配置し、境界標表示システム146を使用して、摘出された組織の解剖学的位置や生検サンプルに関する他の情報を伝える。境界標表示システム146は、ラベル150を使用して識別される4つの四半部(quadrants)148を有している。例示的な実施例が、以下で説明する図4A〜図4Cに示されている。図4A〜図4Cは境界標表示システム146のいくつかの使用法を示しているが、当業者には、境界標表示システム146を他の方式でも使用することができることが理解される。
【0025】
ここで図4Aを参照すると、境界標表示システム146が、前立腺から採られた生検サンプル152及び154と共に使用されている。生検サンプル152及び154は、生検中に医療専門家によって摘出された前立腺中心部を表している。生検サンプル152は、前立腺の左側から摘出された中心部を示している。したがって、「左側」ラベル150はこれを意味するために囲まれている。同様に、生検サンプル154は前立腺の右側から採られたものであり、したがって「右側」ラベル150が囲まれている。このようにして、組織技術者又は他の医療専門家は、パラフィン切片にラベルをつけて、中心部が摘出された前立腺の領域を正確に表すことが可能となる。
【0026】
図4Bは境界標表示システム146の他の使用法を示している。境界標表示システム146の中央には、指から採られた皮膚組織サンプル156がある。皮膚組織156は病巣158を有している。皮膚組織サンプル156の方向は、図4Bに示す「近位」及び「遠位」ラベル150を囲むことによって識別される。ここでも、皮膚組織サンプル156を摘出する医療専門家は、このシステムによって、皮膚サンプルの向きを患者の指の近位端及び遠位端に関して容易に知らせることができる。このようにして、誤認の可能性が減少する。
【0027】
図4Cは、多数の生検サンプル160を採って使用する境界標表示システム146を示している。組織カセット100は、閉じられると、生検サンプル160を定位置に保つ。したがって、外科医などの医療専門家は、外科報告を作成し、囲まれた「1」というラベル150に対応する四半部「1」の見出しの下に注釈を記すことができる。かかる注釈には、これらのサンプルの特徴を記載することができる。例えば、「1」のラベル150を有する四半部148にあるサンプル160はすべて膵臓からのものと仮定する。加えて、生検がさらに胆嚢、腎臓、及び肝臓からも採られたと仮定する。サンプル160を四半部148に編成することができ、次にその番号に対応するラベル150を囲むことができる。外科報告書は外科医によって記述され、ラベル150が「1」を有する四半部148のサンプルは膵臓から採られたものであり、「2」の下にあるものは胆嚢から採られたもの、などを示す情報を記すことができる。このようにして、境界標表示システム146は、多数の異なる方式で病理医や組織技術者に情報を提供することができる。
【0028】
病理医及び組織技術者は、その後に概略的な説明書を作成するとき、医療専門家が伝えたラベル150からの情報を使用することができる。概略的な説明書は、組織技術者又は病理医が組織カセット100を開き、組織を摘出した医療専門家が示した数、配置、大きさ、及び/又は解剖学的方向を観測することによって作成される。引き続き、組織カセット100は、包埋前に生検サンプルの付加的な操作を必要とすることなく、さらなる組織処理のために閉じることができる。組織カセット100は、組織固定処理の全体を通じて生検サンプルの方向を完全に維持する。
【0029】
包埋処理を実施するために、組織技術者又は病理医は組織カセット100から生検サンプルを取り出す。境界標表示システム146によって、解剖学的な摘出位置を容易に識別することが可能となり、また正しい方向に合わせ、標準的な包埋板内に整理することが可能となる。別法として、セクショナブルカセットを有するシステムを使用する場合、組織カセット100は、生検サンプルを平坦に保ち、境界標表示システム146を使用して生検サンプルの摘出方向を示す。組織は、事前に固定され(prefixed)且つ相当に硬化された後に、組織カセット100から取り出され、セクショナブルカセット、他の支持体、包埋する中間板などに配置される。
【0030】
ここで図5A及び図5B、並びに図6A及び図6Bを参照すると、図5A及び図6Aにそれぞれ示す第1のスライド162、164は、通常の組織保存容器から取り出され且つ保存溶液に自由に浸漬された生検サンプルを示している。図5B及び図6Bにそれぞれ示す第2のスライド166、168は、次に保存溶液に浸漬された組織カセット100から取り出された生検サンプルを示している。第2のスライド166、168は、明確で且つ全幅を有するサンプルを示している。スライドの切片の堅固性が改善されている。したがって、後の診断のために生検サンプルを包埋する間の誤認の余地が、組織カセット100によって大いに減じられている。
【0031】
図7Aは、パラフィンろうなどの材料で包埋する間に生検サンプル172を保持する型170を示している。型170は、サンプル172が図示の形状に硬化された後に、生検サンプル172を受ける。生検サンプル172は、曲がっており、高い位置174及び低い位置176を有している。生検サンプル172をパラフィンろうに包埋した後、ミクロトームを使用して生検サンプル172から複数の切片を取り出すことができる。線178は、生検サンプル172から切片が取り出される最も共通する領域を示している。生検サンプル172は、一群の癌細胞などの病巣180を有している。線178は病巣180の下方にある。図7Bを参照すると、線178に沿って切り取った切片が、スライド182の上に配置されたものとして示されている。組織サンプル172の3つの切片がスライド182に配置されている。第1の切片172aは、図7A及び図7Bに示す点Aと点Bとの間の生検サンプル172の長さに対応する。第2の切片172bは、点Cと点Dとの間の生検サンプル172の長さに対応する。第3の切片172cは、点Eと点Fとの間の生検サンプルの長さに対応する。病巣180は、高い点174に近い点DとEとの間にあるため現れない。したがって、診断は不正確になるであろう。
【0032】
ここで図8Aを参照すると、生検サンプル172’が、図1の組織カセット100から取り出されており、型170内に配置されている。生検サンプル172’を型170内に配置した後、生検サンプル172’はパラフィンろうなどの材料に包埋される。次に、例えば線178を通じて、ミクロトームで切片が取り出される。図1の組織カセットは、生検サンプル172’を平坦に形成していたため、線178は病巣180’を通過する。図8Bは、線178を通じて切り取られた切片を医療専門家が診断の準備の際にスライド182の上に配置したことを示している。生検サンプル172’は、生検サンプル172’の全長に沿って認識可能な平坦な切片172a’を有している。したがって、病巣180a’の切片は、平坦な切片172a’の内部に現れ、病理医又は他の医療専門家によって発見されよう。このようにして、組織カセット100は、生検サンプル172の適切な診断が実施されることを確実に導く。
【0033】
ここで図9〜図11及び図11Aを参照すると、第2の例示的実施形態による組織カセット100’が示されている。組織カセット100’は、第1の実施形態に関連して上述した特徴を有してもよい。以下の説明及び各図面の描写を検討することによって明らかとなるように、ある差異が第1と第2の実施形態との間に存在する。プライム符号(’)を有する同じ参照符号は、第1と第2の実施形態とにおけるそれぞれに対応する要素を示すために使用されおり、構造的及び/又は機能的差異は各図面の描写、説明文、又は双方を検討することによって明らかである。組織カセット100’は、蓋部102’及び基部104’を有する第1及び第2の穿孔構造を備えており、その蓋部102’及び基部104’は、一方の端部のヒンジ135’及び反対側の端部の締め具構造136’によって連結され得る。カセット100’内へ流体が流れるように、開口部144’が設けられている。締め具構造は、基部104’上の凹部136b’内で受けられる蓋部102’上の突起部136’を備えてもよい。蓋部102’はまた、ヒンジ135’に隣接して第2の締め具構造236を有している。この締め具構造236は、図10に開位置で、図11Aに閉位置で最良に示されるように、突起部236aと凹部236bとを備えている。蓋部102’が閉じられると、脆弱なヒンジは割れ、締め具構造236は、図11及び図11Aに示すように、締め具構造136’と共に閉位置で蓋部102’を基部104’に押し付けるように係合する。蓋部102’の側壁240、242は、基部104’(図10)の相補的受入れ領域246、248内で受容される。したがって、図9に示す閉位置において、組織サンプルは、カセット100’の側部並びに各締め具構造136’、236を有するカセット100’の端部から逃げるのを防止される。蓋部102’上のタブ200は、上向きの力を蓋部102’に作用させて締め具136’との結合を解除するために使用してもよい。
【0034】
図11及び図11Aに示すように、多孔質膜130’、132’は、突起部202を使用することによって穿孔構造102’、104’に熱かしめしてもよい。熱かしめ操作前の小さな円筒状要素としてのこれらの突起部202が図10に示されている。熱かしめの後、円筒状要素202はキノコのような形状の頭部を形成し、その頭部は、多孔質構造又は発泡体116’、128’の上面部に対して膜130’、132’の縁部を保持する。図11及び図11Aにさらに示すように、図11Aに示す矢印203の方向に蓋部102’と基部104’との間を流体(ホルマリンなど)が移動することが可能なように、完全に第1及び第2の穿孔構造102’、104’の間に流体路を形成してもよい。流体路は、穿孔構造102’、104’の付加的な部分102a’、102b’、104a’、104b’の間及び「キノコのような」突起部202の間に延在している。突起部202は、蓋部102’が閉じられたとき、図11Aに示すように整列する代わりに、互いに食い違い状となってもよい。この流体路によって、組織サンプルを完全に浸潤させることが可能となる。また、間隔204が上部及び下部の多孔質膜130’、132’の間に示されている。間隔204は、特定の用途の必要性に応じて、存在してもしなくてもよい。例えば、より大きい組織サンプルには、依然としてサンプルを適切に保持することが可能となる適切な寸法の間隔204が必要となることがあるが、その一方で、より小さい試料には間隔204が必要でないことがある。
【0035】
非付着性のコーティングを多孔質膜130’、132’の一方又は両方に処理してもよく、その結果、非付着性のコーティングを有する表面130’又は132’から1つ又は複数の組織サンプルを容易に取り出すことができることはさらに強調されるべきである。別法として、膜材料自体がPTFEなどの非付着性の材料を備えてもよい。他の別法として、1つ又は複数の組織サンプルを膜130’又は132’上に保持するために、その組織サンプルを多孔質膜130’又は132’の一方に接着剤で固定してもよい。ホルマリンなどの流体で固定した後、接着剤で固定された1つ又は複数の組織サンプルを有する膜は、カセット100’から切り取られ、パラフィンなどの材料に包埋するために包埋板又はセクショナブルカセットの底部に配置され得る。1つ又は複数の組織サンプルが膜の一方に接着剤で固定されるかどうかにかかわらず、蓋部102’は、1つ又は複数の生検サンプルを取り出す前又は取り出した後に、基部104’から完全に取り外されて破棄することができる。1つ又は複数の生検サンプルを通常のパラフィン型の底部に配置することができ、その型を融解した流動パラフィンで満たすことができる。パラフィンが依然として融解している間に、基部104’をパラフィンと接触させて配置することができる。続いてパラフィンは冷却し硬化する。続いて基部104’は、ミクロトームチャック内に保持するための固定具として使用され得る。次に、硬化したパラフィン上でミクロトーム操作を実施することができ、スライドプレパラート(slide preparation)及び分析を行うことができる。
【0036】
これらの実施形態についてかなり詳細に説明したが、かかる詳細に特許請求の範囲を制限するものではなく、或いは、いかなる形式であれ限定することは、本出願人の意図することではない。付加的な利点及び変形例は、当業者にとっては容易に明らかであろう。したがって、特許請求の範囲は、代表的なシステム、機器、及び方法の具体的な詳細、並びに図示し説明した例示的実施例に限定されない。したがって、本出願人の特許請求の範囲の精神及び範囲から逸脱することなく、かかる詳細な実施例を応用することが可能である。
【図面の簡単な説明】
【0037】
【図1】一実施形態による開位置にある組織カセットの斜視図である。
【図2】概ね図1の線2−2に沿って取られた組織カセットの断面図であるが、閉位置すなわちラッチ係合された位置を示す。
【図3】同様に概ね図1の線2−2に沿って取られた組織カセットの斜視断面図であり、開位置にあるカセットを示す。
【図4A】図1の組織カセットを使用した様々な用途における境界標表示システムを示す平面図である。
【図4B】図1の組織カセットを使用した様々な用途における境界標表示システムを示す平面図である。
【図4C】図1の組織カセットを使用した様々な用途における境界標表示システムを示す平面図である。
【図5A】第1の顕微鏡スライドを示す図であり、あらかじめ通常の生検容器内で保持された生検サンプルを示す。
【図5B】第2の顕微鏡スライドを示す図であり、図1の組織カセットで保持されたサンプルを示す。
【図6A】第1の顕微鏡スライドを示す図であり、あらかじめ通常の生検容器内でホルマリンと共に保持された生検サンプルを示す。
【図6B】第2の顕微鏡スライドを示す図であり、図1の組織カセットで保持されたサンプルを示す。
【図7A】通常の組織輸送容器又は生検容器から得られた組織サンプルを示す図であり、組織は包埋及び切片化に先立ってパラフィン型の中に配置されている。
【図7B】医療専門家による診断用にスライドの上に配置された図7Aの組織サンプルの一切片を示す図である。
【図8A】図1の組織カセットから得られた組織サンプルを示す図であり、組織は包埋及び切片化に先立ってパラフィン型の中に配置されている。
【図8B】医療専門家による診断用にスライドの上に配置された図8Aの組織サンプルの一切片を示す図である。
【図9】他の実施形態による組織カセットの斜視図であり、閉位置を示す。
【図10】図9に示す組織カセットの斜視図であるが、各多孔質膜を取り付ける前の状態を示す。
【図11】図9の線11−11に沿って取られた断面図である。
【図11A】図11に示す囲い部11Aの拡大図である。
【符号の説明】
【0038】
100、100’ 組織カセット
102、102’ 穿孔構造
104、104’ 穿孔構造
116 多孔質構造
128 多孔質構造
130 多孔質膜
132 多孔質膜
135、135’ 伸展性ヒンジ
136、136’ 締め具
144、144’ 孔
146 境界標表示システム
148 四半部
150 ラベル
152、154、160 生検サンプル
162、164、166、168、182 スライド
172、172’ 生検サンプル
180、180’ 病巣
236 締め具構造
【特許請求の範囲】
【請求項1】
組織を保持するためのカセットであって、
前記組織を支持するための第1の平坦な基準多孔質構造と、
圧縮抵抗を有する第2の多孔質構造を収容する内部領域を画定する第2の穿孔構造と、
を含んでなり、
前記第1の平坦な基準多孔質構造及び前記第2の多孔質構造が、その間に前記組織を固定するために当接する位置に配置され得ることを特徴とするカセット。
【請求項2】
第2の圧縮抵抗を有する前記第1の平坦な基準多孔質構造を収容する内部領域を画定する第1の穿孔構造をさらに含んでなることを特徴とする請求項1に記載のカセット。
【請求項3】
接合具が、前記第1の平坦な基準多孔質構造と前記第2の穿孔構造とを接合し、双方の前記構造を一体に圧縮して前記組織をその間に堅固に捕捉していることを特徴とする請求項1に記載のカセット。
【請求項4】
前記接合具が、締め具及びヒンジを使用して前記第1の平坦な基準多孔質構造と前記第2の穿孔構造とを接合していることを特徴とする請求項3に記載のカセット。
【請求項5】
前記第2の多孔質構造が、所定の圧縮抵抗をもたらす発泡体を含んでいることを特徴とする請求項1に記載のカセット。
【請求項6】
前記第2の多孔質構造が、人為構造を引き起こさない多孔質膜を含んでいることを特徴とする請求項1に記載のカセット。
【請求項7】
前記第1の平坦な基準多孔質構造の圧縮抵抗が、前記第2の多孔質構造の前記圧縮抵抗よりも大きいことを特徴とする請求項1に記載のカセット。
【請求項8】
前記第1の平坦な基準多孔質構造及び前記第2の穿孔構造が、二枚貝型の形状を形成するように配置されていることを特徴とする請求項1に記載のカセット。
【請求項9】
多孔質構造のうちの1つが、その上に記された境界標表示システムを有することを特徴とする請求項1に記載のカセット。
【請求項10】
組織サンプルを保持するための方法であって、
前記生検サンプルを組織カセット内に配置するステップと、
前記組織カセットの平坦な基準表面に対して前記生検サンプルを平坦化させるように圧縮力を作用させるために、前記組織カセットの少なくとも一部を移動させるステップと、
を含んでなることを特徴とする方法。
【請求項11】
前記組織サンプルが、前記組織カセット内に、前記組織サンプルの病巣の位置に対応する境界標表示システム上に配置されることを特徴とする請求項10に記載の方法。
【請求項12】
患者からの前記組織サンプルの病巣の位置又は方向に対応して、前記境界標表示システム上にラベルを記すステップをさらに含むことを特徴とする請求項11に記載の方法。
【請求項13】
前記組織カセットの移動が、前記組織カセットの一部を旋回軸の周りで回動させることによって生じることを特徴とする請求項10に記載の方法。
【請求項14】
前記平坦な基準表面と圧縮性の多孔質構造との間で前記組織サンプルを平坦化するステップをさらに含んでなることを特徴とする請求項10に記載の方法。
【請求項15】
組織を保持するためのカセットであって、
前記組織を支持するための第1の平坦な基準多孔質構造と、
圧縮抵抗を有する第2の多孔質構造と、
を含んでなり、
前記第1の平坦な基準多孔質構造及び前記第2の多孔質構造が、その間に前記組織を固定するために当接する位置に配置され得ることを特徴とするカセット。
【請求項1】
組織を保持するためのカセットであって、
前記組織を支持するための第1の平坦な基準多孔質構造と、
圧縮抵抗を有する第2の多孔質構造を収容する内部領域を画定する第2の穿孔構造と、
を含んでなり、
前記第1の平坦な基準多孔質構造及び前記第2の多孔質構造が、その間に前記組織を固定するために当接する位置に配置され得ることを特徴とするカセット。
【請求項2】
第2の圧縮抵抗を有する前記第1の平坦な基準多孔質構造を収容する内部領域を画定する第1の穿孔構造をさらに含んでなることを特徴とする請求項1に記載のカセット。
【請求項3】
接合具が、前記第1の平坦な基準多孔質構造と前記第2の穿孔構造とを接合し、双方の前記構造を一体に圧縮して前記組織をその間に堅固に捕捉していることを特徴とする請求項1に記載のカセット。
【請求項4】
前記接合具が、締め具及びヒンジを使用して前記第1の平坦な基準多孔質構造と前記第2の穿孔構造とを接合していることを特徴とする請求項3に記載のカセット。
【請求項5】
前記第2の多孔質構造が、所定の圧縮抵抗をもたらす発泡体を含んでいることを特徴とする請求項1に記載のカセット。
【請求項6】
前記第2の多孔質構造が、人為構造を引き起こさない多孔質膜を含んでいることを特徴とする請求項1に記載のカセット。
【請求項7】
前記第1の平坦な基準多孔質構造の圧縮抵抗が、前記第2の多孔質構造の前記圧縮抵抗よりも大きいことを特徴とする請求項1に記載のカセット。
【請求項8】
前記第1の平坦な基準多孔質構造及び前記第2の穿孔構造が、二枚貝型の形状を形成するように配置されていることを特徴とする請求項1に記載のカセット。
【請求項9】
多孔質構造のうちの1つが、その上に記された境界標表示システムを有することを特徴とする請求項1に記載のカセット。
【請求項10】
組織サンプルを保持するための方法であって、
前記生検サンプルを組織カセット内に配置するステップと、
前記組織カセットの平坦な基準表面に対して前記生検サンプルを平坦化させるように圧縮力を作用させるために、前記組織カセットの少なくとも一部を移動させるステップと、
を含んでなることを特徴とする方法。
【請求項11】
前記組織サンプルが、前記組織カセット内に、前記組織サンプルの病巣の位置に対応する境界標表示システム上に配置されることを特徴とする請求項10に記載の方法。
【請求項12】
患者からの前記組織サンプルの病巣の位置又は方向に対応して、前記境界標表示システム上にラベルを記すステップをさらに含むことを特徴とする請求項11に記載の方法。
【請求項13】
前記組織カセットの移動が、前記組織カセットの一部を旋回軸の周りで回動させることによって生じることを特徴とする請求項10に記載の方法。
【請求項14】
前記平坦な基準表面と圧縮性の多孔質構造との間で前記組織サンプルを平坦化するステップをさらに含んでなることを特徴とする請求項10に記載の方法。
【請求項15】
組織を保持するためのカセットであって、
前記組織を支持するための第1の平坦な基準多孔質構造と、
圧縮抵抗を有する第2の多孔質構造と、
を含んでなり、
前記第1の平坦な基準多孔質構造及び前記第2の多孔質構造が、その間に前記組織を固定するために当接する位置に配置され得ることを特徴とするカセット。
【図1】


【図2】


【図3】


【図4A】


【図4B】


【図4C】


【図5A】


【図5B】


【図6A】


【図6B】


【図7A】


【図7B】


【図8A】


【図8B】


【図9】


【図10】


【図11】


【図11A】




【図2】


【図3】


【図4A】


【図4B】


【図4C】


【図5A】


【図5B】


【図6A】


【図6B】


【図7A】


【図7B】


【図8A】


【図8B】


【図9】


【図10】


【図11】


【図11A】


【公開番号】特開2007−126457(P2007−126457A)
【公開日】平成19年5月24日(2007.5.24)
【国際特許分類】
【外国語出願】
【出願番号】特願2006−298137(P2006−298137)
【出願日】平成18年11月1日(2006.11.1)
【出願人】(505077404)バイオパス・オートメーション・エル・エル・シー (8)
【Fターム(参考)】
【公開日】平成19年5月24日(2007.5.24)
【国際特許分類】
【出願番号】特願2006−298137(P2006−298137)
【出願日】平成18年11月1日(2006.11.1)
【出願人】(505077404)バイオパス・オートメーション・エル・エル・シー (8)
【Fターム(参考)】
[ Back to top ]

