亜鉛イオンによって増強されたイソチアゾリノン殺生剤
本発明は、イソチアゾリノン、例えば1,2−ベンズイソチアゾリン−3−オン、および、亜鉛塩、酸化亜鉛、水酸化亜鉛、または、それらの組み合わせから選択される亜鉛化合物を含む抗菌性組成物に関する。有用な亜鉛塩としては、例えば、酸化物、硫酸塩、塩化物およびそれらの組み合わせが挙げられる。使用時において、このような亜鉛化合物からの亜鉛が、イソチアゾリン含有組成物の抗菌活性を増強する。このような増強は、イソチアゾリノンを亜鉛化合物の非存在下で使用した場合の濃度よりも低いイソチアゾリノン濃度で、望ましい抗菌活性の達成を可能にする。また本抗菌性組成物は、ピリチオン、例えばジンクピリチオンまたは銅ピリチオンのような補助殺生剤を含んでいてもよい。
【発明の詳細な説明】
【背景技術】
【0001】
発明の背景
1,2−ベンズイソチアゾリン−3−オン(また、「BIT」とも称される)のようなイソチアゾリノン類は、有効な抗菌剤として知られている。BIT、例えば欧州特許EP0703726で説明されている調合物において開示されているBITは、様々な用途で殺菌剤として広く用いられる。
【発明の開示】
【発明が解決しようとする課題】
【0002】
例として、英国特許公報GB2,230,190Aは、2,2’−ジチオピリジン−1,1’−二酸化物(「DTP」)と共に、BITおよび塩化亜鉛(「ZC」)の付加物を含む保存剤組成物を開示している。公報GB2,230,190Aの実施例3では、BIT、ZCおよびDTPを含む組成物と、コントロールとしてBITとZCだけを含む実施例とを比較している。この公報の実施例3および表3で示された結果によれば、DTPを包含させることによって、組成物中のBIT使用料の低減が可能になることが示される。それにもかかわらず、コントロール実施例で用いられたBITの量(2.5ppm)は、本発明者等によって、現実世界の用途における抗菌効果に関して不十分であることが見出された。
【0003】
BITは多様な用途において有用であることが証明されているが、市販品に添加することができるBITの有用な量は、有効性と経済上の考慮のために、さらにそれほどではないにせよ環境面や毒物学的な問題のために制限されている。従って、費用効率が高く、さらに不利な環境的および毒物学的な影響が生じる可能性を最小化するような湿潤状態での用途のための代替の抗菌性組成物が必要である。本発明は、このような代替物の1つを提供する。
【課題を解決するための手段】
【0004】
発明の要約
一形態において、本発明は、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む抗菌性組成物に関する。亜鉛塩の実例は、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせである。このような亜鉛化合物は、抗菌性組成物における金属イオンの源を提供する。本組成物において、イソチアゾリン−3−オンは、1〜500ppm(好ましくは5〜500ppm)の量で存在し、前記亜鉛化合物は、5〜200,000ppm(好ましくは5〜500ppm)の量で存在し、前記イソチアゾリン−3−オンの前記亜鉛化合物に対する重量比は、1:2000〜100:1(好ましくは1:100〜100:1)である。本抗菌性組成物はさらに、任意に、ピリチオン塩、または、ピリチオン酸を含んでいてもよい。有用なピリチオン塩としては、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオン、ピリチオンジスルフィドおよびそれらの組み合わせが挙げられる。
【0005】
その他の形態において、本発明は、水で希釈すると、機能性流体中で抗菌効果を提供する抗菌性組成物の濃縮物に関する。本濃縮物は、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む。本濃縮物において、成分(a)は、濃縮物の総重量に基づき、1〜95重量%の量で存在し、成分(b)は、1〜50重量%の量で存在するが、ここで(a)と(b)の合計の重量パーセントは100重量%を超えない。
【0006】
さらにその他の形態において、本発明は、ベースの媒体に加えて、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む機能性流体に関する。亜鉛塩の実例は、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせである。本組成物において、イソチアゾリン−3−オンは、1〜500ppm(好ましくは5〜500ppm)の量で存在し、前記金属化合物は、5〜200,00ppm(好ましくは5〜500ppm)の量で存在し、イソチアゾリン−3−オンの亜鉛イオンに対する重量比は、1:2000〜100:1(好ましくは100:1〜1:100)である。本抗菌性組成物はさらに、任意に、ピリチオン塩、または、ピリチオン酸を含んでいてもよい。有用なピリチオン塩としては、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオン、および、ピリチオンジスルフィドが挙げられる。このような機能性流体のためのベースの媒体は、例えば、ポリマーエマルジョンにおいて有用なポリマーであり得る。ポリマー系の例はラテックス系であり、例えば、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、上述のものコポリマーである。典型的な機能性流体としては、コーティング組成物が挙げられ、例えば、塗料、接着剤、シーラント、コーキング材、鉱物および顔料スラリー、印刷用インク、農業用殺虫剤、家庭用製品、パーソナルケア、金属加工用流体およびその他のベースが水性の系である。
【0007】
これらのおよびその他の形態は、以下の発明の詳細な説明を読むことによって明らかになると予想される。
【0008】
図面の簡単な説明
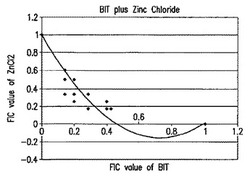
図1は、分別阻害濃度(Fractional Inhibitory Concentration)値に基づいた、1,2−ベンズイソチアゾリン−3−オン(「BIT」)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザ(Ps.aeruginosa)に対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0009】
図2は、分別阻害濃度値に基づいた、ケーソン(Kathon(R))(5−クロロ−2−メチル−4−イソチアゾリン−3−オン(「CIMIT」)、および、2−メチル−4−イソチアゾリン−3−オン(「MIT」)の混合物)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0010】
図3は、分別阻害濃度値に基づいた、MITおよび塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0011】
図4は、分別阻害濃度値に基づいた、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン(「BBIT」)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0012】
図5は、分別阻害濃度値に基づいた、BITおよび塩化ナトリウムの混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0013】
発明の詳細な説明
ここで驚くべきことに、本発明によれば、イソチアゾリン−3−オン、それに加えて、亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される亜鉛化合物を含む抗菌性組成物は、金属化合物を含まないイソチアゾリン含有組成物と比較して増強された抗菌効果を示すことが見出された。抗菌性組成物において、3〜12の広範なpHにわたって増強された効果が適切に提供される。
【0014】
本発明の抗菌性組成物は、機能性流体に適切に包含される。このような機能性流体は、適切には、ベースの媒体に加えて、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)有機酸の亜鉛塩、無機酸の亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む。亜鉛塩の実例としては、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛(また、「ヒドロキシ基を含む炭酸亜鉛」としても知られており、さらに「亜鉛ヒドロキシ炭酸塩」としても知られており、これは、Zn5(OH)6(CO3)2という実験式で示される)およびそれらの組み合わせが挙げられる。
【0015】
本発明においてにおいて有用なイソチアゾリノンは、好ましくは、以下から選択されるイソチアゾリン−3−オンである:1,2−ベンズイソチアゾリン−3−オン(「BIT」)、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン(「BBIT」)、4,5−ジクロロ−2−n−オクチル−4−イソチアゾリン−3−オン(「DCOIT」)、2−メチル−4−イソチアゾリン−3−オン(「MIT」)、5−クロロ−2−メチル−4−イソチアゾリン−3−オン(「ClMIT」)とMITの混合物(ローム・アンド・ハース社(Rohm and Haas Company,フィラデルフィア,ペンシルベニア州)よりケーソン(R)という商品名で入手可能)、ジチオ−2,2’−ビス(ベンズメチルアミド)およびそれらの組み合わせ。特に好ましいイソチアゾリンは、BIT、MIT、および、BBITおよびそれらの組み合わせである。
【0016】
本組成物において、イソチアゾリン−3−オンは、1〜500ppm(好ましくは5〜500ppm)の量で存在し、前記亜鉛化合物は、5〜200,000ppm(好ましくは5〜500ppm)の量で存在し、前記イソチアゾリン−3−オンの前記亜鉛化合物に対する重量比は、1:2000〜100:1(好ましくは100:1〜1:100)である。
【0017】
本抗菌性組成物はさらに、任意に、ピリチオン塩、または、ピリチオン酸を含んでいてもよい。有用なピリチオン塩としては、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオンが挙げられる。ピリチオン塩またはピリチオン酸が用いられる場合、これらは、適切には、本組成物中に約0.001重量%〜約1.0重量%の量で存在する。
【0018】
一実施態様において、本抗菌性組成物のための抗菌性の成分の組み合わせは、水で希釈すると、機能性流体中で抗菌効果を提供する抗菌性組成物の濃縮物の形態で提供することができる。本濃縮物は、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む。本濃縮物において、成分(a)は、1〜95重量%の量で存在し、成分(b)は、1〜50重量%の量で存在する。
【0019】
本発明の抗菌性組成物は、適切には、機能性流体中に用いられ、このような流体としては、例えば、湿潤状態と乾燥した被膜による保存の両方を付与するためのポリマーエマルジョンまたはその他のコーティング組成物が挙げられる。ベースの媒体は、例えば、ポリマーエマルジョンにおいて有用なポリマーが可能であり、ここでこのようなポリマーは、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、上述のものコポリマーからなる群より選択される。典型的な機能性流体としては、コーティング組成物が挙げられ、例えば、塗料、接着剤、シーラント、コーキング材、鉱物および顔料スラリー、印刷用インク、農業用殺虫剤、家庭用製品、パーソナルケア、金属加工用流体およびその他のベースが水性の系である。
【実施例】
【0020】
以下に示す実施例で本発明をさらに説明する。本明細書において示された全てのパーセンテージは、特に他の指定がない限り、組成物の総重量に基づく重量パーセントである。
【0021】
実施例1
この実施例において、抗菌添加剤を以下の表Iで示された量で含む、ハーロウ・ケミカル社(Harlow Chemical Company)から供給されているREVACRYL 1Aという商標名の市販の水性アクリルラテックス(pH8.1)のサンプルを、
シュードモナス・アエルギノーザ(Pseudomonas aeruginosa)、NCIMB8295、
プロビデンシア・レットゲリ(Providencia rettgeri)、NCIMB10842、
セラチア・マルセッセンス(Serratia marcescens)、NCIMB9523、
エロモナス・ヒドロフィラ(Aeromonas hydrophila)、NCIMB9233、
アルカリゲネス属(湿潤状態での保存単離物)、
バークホルデリア・セパシア(Burkholderia cepacia)、ATCC25416、
シュードモナス・プチダ(Pseudomonas putida)、NCIMB9494、
からなる細菌懸濁液で処理した。
【0022】
全ての試験用の種を栄養寒天上で培養し、30℃で24時間インキュベートした。この期間の後、各試験用有機体のそれぞれの懸濁液を、トーマ(Thoma)のカウントチャンバーを用いて食塩水中で106のコロニー形成単位/mlの濃度に調整した(これは、それぞれの懸濁液を等量混合することによって達成された)。各処理後の各アリコート中の細菌濃度は、2×106個/mlであった。
【0023】
試験を開始する前に、抗菌添加剤を含む塗料サンプルを40℃で7日保存した。この塗料サンプルを、上述した1%v/vの細菌懸濁液で処理した。全ての試験サンプルを試験の持続時間中30℃でインキュベートし、各処理の1、3および7日後に生存可能な細菌に関して試験した。栄養寒天上にアリコートを筋上に植菌して、続いて30℃で2日インキュベートすることによって生存可能な細菌を検出した。
【0024】
表Iに、1、3および7日目の3回の植菌の後に得られた結果を示す。
【表1】

【0025】
結果から、市販品、すなわちアーチ・ケミカルズ社(Arch Chemicals, Inc.)の製品であり、市販用ラテックスの保存のためにBITしか含まないプロキセル(PROXEL)BD20と比較した場合、BITだけを含むサンプルの場合は250ppmのBITが必要であったのに対して、亜鉛を含む塩の存在下ではわずか100ppmのBITしか必要としないという点で、亜鉛を含む塩と組み合わせるとBITの作用が増強されることが実証される。
【0026】
実施例2
シュードモナス・アエルギノーザに対する1,2−ベンズイソチアゾリン−3−オン(BIT)と塩化亜鉛(ZnCl2)との増強作用の調査。
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、BITとZnCl2との相乗効果を研究するために用いた。
【0027】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0028】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0029】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0030】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0031】
実施例2の結果
【表2】

BITは、アーチ社(Arch Limited)より入手可能な1,2−ベンズイソチアゾリン−3−オンであるプロキセル(R) GXLである。
【0032】
単独培養に対する活性の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表3に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0033】
【表3】

【0034】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(isobole;すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図1で示されるように、BITおよびZnCl2の組み合わせは、図1のグラフにおける凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0035】
実施例3
シュードモナス・アエルギノーザに対するケーソン(R)(ClMIT/MIT)と塩化亜鉛(ZnCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、ケーソン(R)およびZnCl2の相乗効果を研究するために用いた。
【0036】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0037】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0038】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0039】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0040】
実施例3の結果
【0041】
【表4】

CIMITおよびMITの混合物は、ローム・アンド・ハース社(フィラデルフィア,ペンシルベニア州)よりケーソン(R)という商品名で入手可能である。
【0042】
単独培養に対する相乗効果の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表5に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0043】
【表5】

【0044】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図2で示されるように、ケーソン(R)およびZnCl2の組み合わせは、図2における凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0045】
実施例4
シュードモナス・アエルギノーザに対するMITと塩化亜鉛(ZnCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、MITとZnCl2との相乗効果を研究するために用いた。
【0046】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0047】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0048】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0049】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0050】
実施例4の結果
【表6】

単独培養に対する相乗効果の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表7に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0051】
【表7】

【0052】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図3で示されるように、MITおよびZnCl2の組み合わせは、図3における凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0053】
実施例5
シュードモナス・アエルギノーザに対するBBITと塩化亜鉛(ZnCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、BBITとZnCl2との相乗効果を研究するために用いた。
【0054】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0055】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0056】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0057】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0058】
実施例5の結果
【表8】

BBITは、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オンである。
【0059】
単独培養に対する相乗効果の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表9に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0060】
【表9】

【0061】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図4で示されるように、BBITおよびZnCl2の組み合わせは、図4で示される凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0062】
比較例A
シュードモナス・アエルギノーザに対する1,2−ベンズイソチアゾリン−3−オン(BIT)と塩化亜鉛(ZnCl2)ととの相乗効果(実施例2)と比較した、シュードモナス・アエルギノーザに対する1.2−ベンズイソチアゾリン−3−オン(BIT)と塩化ナトリウム(NaCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、BITと塩化ナトリウムとの組み合わせの有効性を研究するために用いた。
【0063】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0064】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0065】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0066】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0067】
比較例Aの結果
【表10】

【0068】
BITは、アーチ社より入手可能な1,2−ベンズイソチアゾリン−3−オンであるプロキセル(R)GXLである。
【0069】
単独培養に対する増強作用の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表11に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0070】
【表11】

【0071】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図5で示されるように、BITおよびNaCl2の組み合わせは、図5における直線状の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して相加的である。加えて、この実施例の結果はさらに、実施例2で示されるように、イソチアゾリン−3−オン(例えばBIT)と亜鉛化合物(例えばZnCl2)との組み合わせは、シュードモナス・アエルギノーザに対して予想外の増強作用の結果を示すことも説明している。
【図面の簡単な説明】
【0072】
【図1】分別阻害濃度値に基づいた、1,2−ベンズイソチアゾリン−3−オンおよび塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図2】分別阻害濃度値に基づいた、ケーソン(5−クロロ−2−メチル−4−イソチアゾリン−3−オン(「CIMIT」)、および、2−メチル−4−イソチアゾリン−3−オン(「MIT」)の混合物)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図3】分別阻害濃度値に基づいた、MITおよび塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図4】分別阻害濃度値に基づいた、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン(「BBIT」)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図5】分別阻害濃度値に基づいた、BITおよび塩化ナトリウムの混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【背景技術】
【0001】
発明の背景
1,2−ベンズイソチアゾリン−3−オン(また、「BIT」とも称される)のようなイソチアゾリノン類は、有効な抗菌剤として知られている。BIT、例えば欧州特許EP0703726で説明されている調合物において開示されているBITは、様々な用途で殺菌剤として広く用いられる。
【発明の開示】
【発明が解決しようとする課題】
【0002】
例として、英国特許公報GB2,230,190Aは、2,2’−ジチオピリジン−1,1’−二酸化物(「DTP」)と共に、BITおよび塩化亜鉛(「ZC」)の付加物を含む保存剤組成物を開示している。公報GB2,230,190Aの実施例3では、BIT、ZCおよびDTPを含む組成物と、コントロールとしてBITとZCだけを含む実施例とを比較している。この公報の実施例3および表3で示された結果によれば、DTPを包含させることによって、組成物中のBIT使用料の低減が可能になることが示される。それにもかかわらず、コントロール実施例で用いられたBITの量(2.5ppm)は、本発明者等によって、現実世界の用途における抗菌効果に関して不十分であることが見出された。
【0003】
BITは多様な用途において有用であることが証明されているが、市販品に添加することができるBITの有用な量は、有効性と経済上の考慮のために、さらにそれほどではないにせよ環境面や毒物学的な問題のために制限されている。従って、費用効率が高く、さらに不利な環境的および毒物学的な影響が生じる可能性を最小化するような湿潤状態での用途のための代替の抗菌性組成物が必要である。本発明は、このような代替物の1つを提供する。
【課題を解決するための手段】
【0004】
発明の要約
一形態において、本発明は、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む抗菌性組成物に関する。亜鉛塩の実例は、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせである。このような亜鉛化合物は、抗菌性組成物における金属イオンの源を提供する。本組成物において、イソチアゾリン−3−オンは、1〜500ppm(好ましくは5〜500ppm)の量で存在し、前記亜鉛化合物は、5〜200,000ppm(好ましくは5〜500ppm)の量で存在し、前記イソチアゾリン−3−オンの前記亜鉛化合物に対する重量比は、1:2000〜100:1(好ましくは1:100〜100:1)である。本抗菌性組成物はさらに、任意に、ピリチオン塩、または、ピリチオン酸を含んでいてもよい。有用なピリチオン塩としては、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオン、ピリチオンジスルフィドおよびそれらの組み合わせが挙げられる。
【0005】
その他の形態において、本発明は、水で希釈すると、機能性流体中で抗菌効果を提供する抗菌性組成物の濃縮物に関する。本濃縮物は、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む。本濃縮物において、成分(a)は、濃縮物の総重量に基づき、1〜95重量%の量で存在し、成分(b)は、1〜50重量%の量で存在するが、ここで(a)と(b)の合計の重量パーセントは100重量%を超えない。
【0006】
さらにその他の形態において、本発明は、ベースの媒体に加えて、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む機能性流体に関する。亜鉛塩の実例は、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせである。本組成物において、イソチアゾリン−3−オンは、1〜500ppm(好ましくは5〜500ppm)の量で存在し、前記金属化合物は、5〜200,00ppm(好ましくは5〜500ppm)の量で存在し、イソチアゾリン−3−オンの亜鉛イオンに対する重量比は、1:2000〜100:1(好ましくは100:1〜1:100)である。本抗菌性組成物はさらに、任意に、ピリチオン塩、または、ピリチオン酸を含んでいてもよい。有用なピリチオン塩としては、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオン、および、ピリチオンジスルフィドが挙げられる。このような機能性流体のためのベースの媒体は、例えば、ポリマーエマルジョンにおいて有用なポリマーであり得る。ポリマー系の例はラテックス系であり、例えば、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、上述のものコポリマーである。典型的な機能性流体としては、コーティング組成物が挙げられ、例えば、塗料、接着剤、シーラント、コーキング材、鉱物および顔料スラリー、印刷用インク、農業用殺虫剤、家庭用製品、パーソナルケア、金属加工用流体およびその他のベースが水性の系である。
【0007】
これらのおよびその他の形態は、以下の発明の詳細な説明を読むことによって明らかになると予想される。
【0008】
図面の簡単な説明
図1は、分別阻害濃度(Fractional Inhibitory Concentration)値に基づいた、1,2−ベンズイソチアゾリン−3−オン(「BIT」)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザ(Ps.aeruginosa)に対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0009】
図2は、分別阻害濃度値に基づいた、ケーソン(Kathon(R))(5−クロロ−2−メチル−4−イソチアゾリン−3−オン(「CIMIT」)、および、2−メチル−4−イソチアゾリン−3−オン(「MIT」)の混合物)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0010】
図3は、分別阻害濃度値に基づいた、MITおよび塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0011】
図4は、分別阻害濃度値に基づいた、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン(「BBIT」)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0012】
図5は、分別阻害濃度値に基づいた、BITおよび塩化ナトリウムの混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【0013】
発明の詳細な説明
ここで驚くべきことに、本発明によれば、イソチアゾリン−3−オン、それに加えて、亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される亜鉛化合物を含む抗菌性組成物は、金属化合物を含まないイソチアゾリン含有組成物と比較して増強された抗菌効果を示すことが見出された。抗菌性組成物において、3〜12の広範なpHにわたって増強された効果が適切に提供される。
【0014】
本発明の抗菌性組成物は、機能性流体に適切に包含される。このような機能性流体は、適切には、ベースの媒体に加えて、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)有機酸の亜鉛塩、無機酸の亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む。亜鉛塩の実例としては、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛(また、「ヒドロキシ基を含む炭酸亜鉛」としても知られており、さらに「亜鉛ヒドロキシ炭酸塩」としても知られており、これは、Zn5(OH)6(CO3)2という実験式で示される)およびそれらの組み合わせが挙げられる。
【0015】
本発明においてにおいて有用なイソチアゾリノンは、好ましくは、以下から選択されるイソチアゾリン−3−オンである:1,2−ベンズイソチアゾリン−3−オン(「BIT」)、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン(「BBIT」)、4,5−ジクロロ−2−n−オクチル−4−イソチアゾリン−3−オン(「DCOIT」)、2−メチル−4−イソチアゾリン−3−オン(「MIT」)、5−クロロ−2−メチル−4−イソチアゾリン−3−オン(「ClMIT」)とMITの混合物(ローム・アンド・ハース社(Rohm and Haas Company,フィラデルフィア,ペンシルベニア州)よりケーソン(R)という商品名で入手可能)、ジチオ−2,2’−ビス(ベンズメチルアミド)およびそれらの組み合わせ。特に好ましいイソチアゾリンは、BIT、MIT、および、BBITおよびそれらの組み合わせである。
【0016】
本組成物において、イソチアゾリン−3−オンは、1〜500ppm(好ましくは5〜500ppm)の量で存在し、前記亜鉛化合物は、5〜200,000ppm(好ましくは5〜500ppm)の量で存在し、前記イソチアゾリン−3−オンの前記亜鉛化合物に対する重量比は、1:2000〜100:1(好ましくは100:1〜1:100)である。
【0017】
本抗菌性組成物はさらに、任意に、ピリチオン塩、または、ピリチオン酸を含んでいてもよい。有用なピリチオン塩としては、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオンが挙げられる。ピリチオン塩またはピリチオン酸が用いられる場合、これらは、適切には、本組成物中に約0.001重量%〜約1.0重量%の量で存在する。
【0018】
一実施態様において、本抗菌性組成物のための抗菌性の成分の組み合わせは、水で希釈すると、機能性流体中で抗菌効果を提供する抗菌性組成物の濃縮物の形態で提供することができる。本濃縮物は、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含む。本濃縮物において、成分(a)は、1〜95重量%の量で存在し、成分(b)は、1〜50重量%の量で存在する。
【0019】
本発明の抗菌性組成物は、適切には、機能性流体中に用いられ、このような流体としては、例えば、湿潤状態と乾燥した被膜による保存の両方を付与するためのポリマーエマルジョンまたはその他のコーティング組成物が挙げられる。ベースの媒体は、例えば、ポリマーエマルジョンにおいて有用なポリマーが可能であり、ここでこのようなポリマーは、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、上述のものコポリマーからなる群より選択される。典型的な機能性流体としては、コーティング組成物が挙げられ、例えば、塗料、接着剤、シーラント、コーキング材、鉱物および顔料スラリー、印刷用インク、農業用殺虫剤、家庭用製品、パーソナルケア、金属加工用流体およびその他のベースが水性の系である。
【実施例】
【0020】
以下に示す実施例で本発明をさらに説明する。本明細書において示された全てのパーセンテージは、特に他の指定がない限り、組成物の総重量に基づく重量パーセントである。
【0021】
実施例1
この実施例において、抗菌添加剤を以下の表Iで示された量で含む、ハーロウ・ケミカル社(Harlow Chemical Company)から供給されているREVACRYL 1Aという商標名の市販の水性アクリルラテックス(pH8.1)のサンプルを、
シュードモナス・アエルギノーザ(Pseudomonas aeruginosa)、NCIMB8295、
プロビデンシア・レットゲリ(Providencia rettgeri)、NCIMB10842、
セラチア・マルセッセンス(Serratia marcescens)、NCIMB9523、
エロモナス・ヒドロフィラ(Aeromonas hydrophila)、NCIMB9233、
アルカリゲネス属(湿潤状態での保存単離物)、
バークホルデリア・セパシア(Burkholderia cepacia)、ATCC25416、
シュードモナス・プチダ(Pseudomonas putida)、NCIMB9494、
からなる細菌懸濁液で処理した。
【0022】
全ての試験用の種を栄養寒天上で培養し、30℃で24時間インキュベートした。この期間の後、各試験用有機体のそれぞれの懸濁液を、トーマ(Thoma)のカウントチャンバーを用いて食塩水中で106のコロニー形成単位/mlの濃度に調整した(これは、それぞれの懸濁液を等量混合することによって達成された)。各処理後の各アリコート中の細菌濃度は、2×106個/mlであった。
【0023】
試験を開始する前に、抗菌添加剤を含む塗料サンプルを40℃で7日保存した。この塗料サンプルを、上述した1%v/vの細菌懸濁液で処理した。全ての試験サンプルを試験の持続時間中30℃でインキュベートし、各処理の1、3および7日後に生存可能な細菌に関して試験した。栄養寒天上にアリコートを筋上に植菌して、続いて30℃で2日インキュベートすることによって生存可能な細菌を検出した。
【0024】
表Iに、1、3および7日目の3回の植菌の後に得られた結果を示す。
【表1】

【0025】
結果から、市販品、すなわちアーチ・ケミカルズ社(Arch Chemicals, Inc.)の製品であり、市販用ラテックスの保存のためにBITしか含まないプロキセル(PROXEL)BD20と比較した場合、BITだけを含むサンプルの場合は250ppmのBITが必要であったのに対して、亜鉛を含む塩の存在下ではわずか100ppmのBITしか必要としないという点で、亜鉛を含む塩と組み合わせるとBITの作用が増強されることが実証される。
【0026】
実施例2
シュードモナス・アエルギノーザに対する1,2−ベンズイソチアゾリン−3−オン(BIT)と塩化亜鉛(ZnCl2)との増強作用の調査。
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、BITとZnCl2との相乗効果を研究するために用いた。
【0027】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0028】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0029】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0030】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0031】
実施例2の結果
【表2】

BITは、アーチ社(Arch Limited)より入手可能な1,2−ベンズイソチアゾリン−3−オンであるプロキセル(R) GXLである。
【0032】
単独培養に対する活性の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表3に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0033】
【表3】

【0034】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(isobole;すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図1で示されるように、BITおよびZnCl2の組み合わせは、図1のグラフにおける凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0035】
実施例3
シュードモナス・アエルギノーザに対するケーソン(R)(ClMIT/MIT)と塩化亜鉛(ZnCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、ケーソン(R)およびZnCl2の相乗効果を研究するために用いた。
【0036】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0037】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0038】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0039】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0040】
実施例3の結果
【0041】
【表4】

CIMITおよびMITの混合物は、ローム・アンド・ハース社(フィラデルフィア,ペンシルベニア州)よりケーソン(R)という商品名で入手可能である。
【0042】
単独培養に対する相乗効果の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表5に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0043】
【表5】

【0044】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図2で示されるように、ケーソン(R)およびZnCl2の組み合わせは、図2における凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0045】
実施例4
シュードモナス・アエルギノーザに対するMITと塩化亜鉛(ZnCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、MITとZnCl2との相乗効果を研究するために用いた。
【0046】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0047】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0048】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0049】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0050】
実施例4の結果
【表6】

単独培養に対する相乗効果の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表7に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0051】
【表7】

【0052】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図3で示されるように、MITおよびZnCl2の組み合わせは、図3における凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0053】
実施例5
シュードモナス・アエルギノーザに対するBBITと塩化亜鉛(ZnCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、BBITとZnCl2との相乗効果を研究するために用いた。
【0054】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0055】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0056】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0057】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0058】
実施例5の結果
【表8】

BBITは、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オンである。
【0059】
単独培養に対する相乗効果の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表9に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0060】
【表9】

【0061】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図4で示されるように、BBITおよびZnCl2の組み合わせは、図4で示される凹型の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して増強された作用を有する。
【0062】
比較例A
シュードモナス・アエルギノーザに対する1,2−ベンズイソチアゾリン−3−オン(BIT)と塩化亜鉛(ZnCl2)ととの相乗効果(実施例2)と比較した、シュードモナス・アエルギノーザに対する1.2−ベンズイソチアゾリン−3−オン(BIT)と塩化ナトリウム(NaCl2)との増強作用の調査
細菌
栄養寒天上で維持したシュードモナス・アエルギノーザ(NCIB10421)を、BITと塩化ナトリウムとの組み合わせの有効性を研究するために用いた。
【0063】
単独培養に対する最小阻止濃度の計算
細菌を、液体栄養培地中で定常期(約24時間)まで増殖させた(約109細菌/ml)。0.1%(v/v)の接種材料を用いて新しい培地に植菌し、続いて100μlの接種材料を、マイクロタイタープレートの各ウェルに添加した(ただし、第一のウェルには200μlを含ませた)。
【0064】
二倍希釈を用いて、調査対象の化合物濃度を、縦軸座標にそってウェルごとに様々に変化させた。37℃で24時間インキュベートした後に、増殖が起こったかどうかを目視検査によって記録した。
【0065】
単独培養に対する抗菌活性の計算
この分析のためのマイクロタイタープレートを用いた。2種の化合物の濃度を、10×10のアレイ中で2倍のMIC(最小阻止濃度)からゼロ濃度まで様々に変化させて簡単なマトリックスを構築した。このマイクロタイタープレートは96ウェルしかないため、両端の濃度(最高の濃度および最低の濃度)を構成する2種の化合物の組み合わせは省略した。上記化合物を蒸留水に予め溶解させた後に、液体培地を用いて最終濃度の2倍濃度の溶液を作製した。
【0066】
上記プレートに、各ウェル中の総体積が200μlになるようにこの混合物(100μl)を添加した。シュードモナス・アエルギノーザ用の液体栄養培地を用いた。プレートを37℃で16〜24時間インキュベートした。目視検査によって、増殖が起こったかどうかを決定した。
【0067】
比較例Aの結果
【表10】

【0068】
BITは、アーチ社より入手可能な1,2−ベンズイソチアゾリン−3−オンであるプロキセル(R)GXLである。
【0069】
単独培養に対する増強作用の計算
最小阻止濃度(MIC)は、単独で用いた場合に増殖阻害を示す殺生剤の最低濃度である。分別阻害濃度(FIC)を計算するために、単一の殺生剤では増殖を制御しなかった場合、MICを使用された最高濃度として採用した。分別阻害濃度は、増殖を制御した殺生剤の混合物中の濃度を、その殺生剤のMICで割った濃度である。混合物中の両方の化合物のFIC値を計算し、その結果を表11に示した。これらの2つの図を総合して、これら2種の殺生剤の作用の指標を得た。値が1未満の場合は増強された作用を示し、合計が1であるか、またはそれより大きい場合、作用は相加的であり、さらに、値が2より大きい場合、その殺生剤は拮抗作用を示す。
【0070】
【表11】

【0071】
2種の殺生剤に関する殺生剤の分別阻害濃度を一様目盛で示す軸を有するグラフを構築する場合、組み合わせが相加的であると、等効果曲線(すなわち、単独で用いられた殺生剤と等しい効果を示す濃度などの、等効果を示すあらゆる組み合わせを示すポイントを繋げたライン)は直線的であり、相乗作用を示す組み合わせは、凹型の等効果曲線を生じ、拮抗作用を示す組み合わせは、凸型の等効果曲線を生じる。図5で示されるように、BITおよびNaCl2の組み合わせは、図5における直線状の等効果曲線によって確認されるように、シュードモナス・アエルギノーザに対して相加的である。加えて、この実施例の結果はさらに、実施例2で示されるように、イソチアゾリン−3−オン(例えばBIT)と亜鉛化合物(例えばZnCl2)との組み合わせは、シュードモナス・アエルギノーザに対して予想外の増強作用の結果を示すことも説明している。
【図面の簡単な説明】
【0072】
【図1】分別阻害濃度値に基づいた、1,2−ベンズイソチアゾリン−3−オンおよび塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図2】分別阻害濃度値に基づいた、ケーソン(5−クロロ−2−メチル−4−イソチアゾリン−3−オン(「CIMIT」)、および、2−メチル−4−イソチアゾリン−3−オン(「MIT」)の混合物)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図3】分別阻害濃度値に基づいた、MITおよび塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図4】分別阻害濃度値に基づいた、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン(「BBIT」)および塩化亜鉛の混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【図5】分別阻害濃度値に基づいた、BITおよび塩化ナトリウムの混合物の、シュードモナス・アエルギノーザに対する抗菌活性を示すアイソボログラムの図式的な説明を示す。
【特許請求の範囲】
【請求項1】
抗菌性組成物であって、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含み、ここで前記イソチアゾリン−3−オンは、1〜500ppmの量で存在し、前記亜鉛化合物は、5〜200,000ppmの量で存在し、前記イソチアゾリン−3−オンの前記亜鉛化合物に対する重量比は、1:2000〜100:1である、上記抗菌性組成物。
【請求項2】
成分(a)が、1〜500ppmの量で存在し、成分(b)は、5〜200,000ppmの量で存在し、前記重量比は、1:100〜100:1である、請求項1に記載の組成物。
【請求項3】
成分(a)が、5〜500ppmの量で存在し、成分(b)は、5〜500ppmの量で存在する、請求項1に記載の組成物。
【請求項4】
前記イソチアゾリン−3−オンが、1,2−ベンズイソチアゾリン−3−オン、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン、4,5−ジクロロ−2−n−オクチル−4−イソチアゾリン−3−オン、2−メチル−4−イソチアゾリン−3−オン、5−クロロ−2−メチル−4−イソチアゾリン−3−オン(ClMIT)と2−メチル−4−イソチアゾリン−3−オンとの混合物、および、さらにジチオ−2,2’−ビス(ベンズメチルアミド)、ならびにそれらの組み合わせからなる群より選択される、請求項1に記載の抗菌性組成物。
【請求項5】
前記亜鉛塩が、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせからなる群より選択される、請求項1に記載の抗菌性組成物。
【請求項6】
前記亜鉛化合物が、塩化亜鉛である、請求項1に記載の抗菌性組成物。
【請求項7】
ピリチオン塩、ピリチオン酸およびそれらの組み合わせからなる群より選択される補助殺生剤(co−biocide)をさらに含み、ここで該補助殺生剤は、前記組成物中に、前記組成物の総重量に基づき約0.001〜約1重量%の量で存在する、請求項1に記載の抗菌性組成物。
【請求項8】
水で希釈すると請求項1で規定したような成分(a)および(b)の量が提供される抗菌性組成物の濃縮物であって、該濃縮物は、イソチアゾリン−3−オンを1〜95重量%の量で含む、上記濃縮物。
【請求項9】
ピリチオン塩、ピリチオン酸およびそれらの組み合わせからなる群より選択される補助殺生剤をさらに含み、ここで該補助殺生剤は、前記組成物中に、前記組成物の総重量に基づき約1〜約50重量%の量で存在する、請求項8に記載の抗菌性組成物の濃縮物。
【請求項10】
ポリマーエマルジョンを含む組成物であって、該組成物はさらに、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物の組み合わせを含む湿潤状態の保存剤を含み、ここで該組み合わせは、該組成物中に、約10ppm〜約400ppmの総量で存在し、ここで成分(a)の成分(b)に対するモル比は、約4:1〜約1:2である、上記組成物。
【請求項11】
前記ポリマーエマルジョンが、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、それらのコポリマーからなる群より選択されるポリマーを含む、請求項10に記載の組成物。
【請求項12】
前記亜鉛塩が、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせからなる群より選択される、請求項10に記載の抗菌性組成物。
【請求項13】
前記亜鉛塩が、塩化亜鉛である、請求項12に記載の抗菌性組成物。
【請求項14】
前記イソチアゾリン−3−オンが、1,2−ベンズイソチアゾリン−3−オン、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン、4,5−ジクロロ−2−n−オクチル−4−イソチアゾリン−3−オン、2−メチル−4−イソチアゾリン−3−オン、5−クロロ−2−メチル−4−イソチアゾリン−3−オン(ClMIT)と2−メチル−4−イソチアゾリン−3−オンとの混合物、および、さらにジチオ−2,2’−ビス(ベンズメチルアミド)、ならびにそれらの組み合わせからなる群より選択される、請求項10に記載の組成物。
【請求項15】
ピリチオン塩、ピリチオン酸およびそれらの組み合わせからなる群より選択される補助殺生剤をさらに含み、ここで該補助殺生剤は、該組成物中に、前記組成物の総重量に基づき約0.001〜約1.0重量%の量で存在する、請求項10に記載の組成物。
【請求項16】
前記ピリチオン塩が、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオンおよびそれらの組み合わせからなる群より選択される、請求項15に記載の組成物。
【請求項17】
塗料、接着剤、シーラント、コーキング材、鉱物および顔料スラリー、印刷用インク、農業用殺虫剤、家庭用コーティング製品、パーソナルケア製品、金属加工用流体およびそれらの組み合わせからなる群より選択されるコーティング組成物であって、該コーティング組成物は、液体ベースの媒体としてポリマーエマルジョン、および、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物の組み合わせを含む湿潤状態の保存剤を含み、ここで該組み合わせは、該組成物中に、約10ppm〜約400ppmの総量で存在し、ここで成分(a)の成分(b)に対するモル比は、約4:1〜約1:2である、上記組成物。
【請求項18】
前記液体ベースの媒体が、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、それらのコポリマーからなる群より選択される、請求項17に記載のコーティング組成物。
【請求項1】
抗菌性組成物であって、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物を含み、ここで前記イソチアゾリン−3−オンは、1〜500ppmの量で存在し、前記亜鉛化合物は、5〜200,000ppmの量で存在し、前記イソチアゾリン−3−オンの前記亜鉛化合物に対する重量比は、1:2000〜100:1である、上記抗菌性組成物。
【請求項2】
成分(a)が、1〜500ppmの量で存在し、成分(b)は、5〜200,000ppmの量で存在し、前記重量比は、1:100〜100:1である、請求項1に記載の組成物。
【請求項3】
成分(a)が、5〜500ppmの量で存在し、成分(b)は、5〜500ppmの量で存在する、請求項1に記載の組成物。
【請求項4】
前記イソチアゾリン−3−オンが、1,2−ベンズイソチアゾリン−3−オン、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン、4,5−ジクロロ−2−n−オクチル−4−イソチアゾリン−3−オン、2−メチル−4−イソチアゾリン−3−オン、5−クロロ−2−メチル−4−イソチアゾリン−3−オン(ClMIT)と2−メチル−4−イソチアゾリン−3−オンとの混合物、および、さらにジチオ−2,2’−ビス(ベンズメチルアミド)、ならびにそれらの組み合わせからなる群より選択される、請求項1に記載の抗菌性組成物。
【請求項5】
前記亜鉛塩が、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせからなる群より選択される、請求項1に記載の抗菌性組成物。
【請求項6】
前記亜鉛化合物が、塩化亜鉛である、請求項1に記載の抗菌性組成物。
【請求項7】
ピリチオン塩、ピリチオン酸およびそれらの組み合わせからなる群より選択される補助殺生剤(co−biocide)をさらに含み、ここで該補助殺生剤は、前記組成物中に、前記組成物の総重量に基づき約0.001〜約1重量%の量で存在する、請求項1に記載の抗菌性組成物。
【請求項8】
水で希釈すると請求項1で規定したような成分(a)および(b)の量が提供される抗菌性組成物の濃縮物であって、該濃縮物は、イソチアゾリン−3−オンを1〜95重量%の量で含む、上記濃縮物。
【請求項9】
ピリチオン塩、ピリチオン酸およびそれらの組み合わせからなる群より選択される補助殺生剤をさらに含み、ここで該補助殺生剤は、前記組成物中に、前記組成物の総重量に基づき約1〜約50重量%の量で存在する、請求項8に記載の抗菌性組成物の濃縮物。
【請求項10】
ポリマーエマルジョンを含む組成物であって、該組成物はさらに、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物の組み合わせを含む湿潤状態の保存剤を含み、ここで該組み合わせは、該組成物中に、約10ppm〜約400ppmの総量で存在し、ここで成分(a)の成分(b)に対するモル比は、約4:1〜約1:2である、上記組成物。
【請求項11】
前記ポリマーエマルジョンが、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、それらのコポリマーからなる群より選択されるポリマーを含む、請求項10に記載の組成物。
【請求項12】
前記亜鉛塩が、塩化亜鉛、硫化亜鉛、炭酸亜鉛、塩基性炭酸亜鉛およびそれらの組み合わせからなる群より選択される、請求項10に記載の抗菌性組成物。
【請求項13】
前記亜鉛塩が、塩化亜鉛である、請求項12に記載の抗菌性組成物。
【請求項14】
前記イソチアゾリン−3−オンが、1,2−ベンズイソチアゾリン−3−オン、N−(n−ブチル)−1,2−ベンズイソチアゾリン−3−オン、4,5−ジクロロ−2−n−オクチル−4−イソチアゾリン−3−オン、2−メチル−4−イソチアゾリン−3−オン、5−クロロ−2−メチル−4−イソチアゾリン−3−オン(ClMIT)と2−メチル−4−イソチアゾリン−3−オンとの混合物、および、さらにジチオ−2,2’−ビス(ベンズメチルアミド)、ならびにそれらの組み合わせからなる群より選択される、請求項10に記載の組成物。
【請求項15】
ピリチオン塩、ピリチオン酸およびそれらの組み合わせからなる群より選択される補助殺生剤をさらに含み、ここで該補助殺生剤は、該組成物中に、前記組成物の総重量に基づき約0.001〜約1.0重量%の量で存在する、請求項10に記載の組成物。
【請求項16】
前記ピリチオン塩が、銅ピリチオン、ジンクピリチオン、ナトリウムピリチオンおよびそれらの組み合わせからなる群より選択される、請求項15に記載の組成物。
【請求項17】
塗料、接着剤、シーラント、コーキング材、鉱物および顔料スラリー、印刷用インク、農業用殺虫剤、家庭用コーティング製品、パーソナルケア製品、金属加工用流体およびそれらの組み合わせからなる群より選択されるコーティング組成物であって、該コーティング組成物は、液体ベースの媒体としてポリマーエマルジョン、および、(a)少なくとも1種のイソチアゾリン−3−オン、および、(b)亜鉛塩、酸化亜鉛、水酸化亜鉛およびそれらの組み合わせからなる群より選択される少なくとも1種の亜鉛化合物の組み合わせを含む湿潤状態の保存剤を含み、ここで該組み合わせは、該組成物中に、約10ppm〜約400ppmの総量で存在し、ここで成分(a)の成分(b)に対するモル比は、約4:1〜約1:2である、上記組成物。
【請求項18】
前記液体ベースの媒体が、アクリル酸系誘導体および置換された(メタ)アクリラート、スチレン/ブタジエン、エチレン酢酸ビニル、ポリ酢酸ビニル、スチレン/ブタジエン/N−メチロールアクリルアミド、ニトリル、および、それらのコポリマーからなる群より選択される、請求項17に記載のコーティング組成物。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公表番号】特表2009−538319(P2009−538319A)
【公表日】平成21年11月5日(2009.11.5)
【国際特許分類】
【出願番号】特願2009−512168(P2009−512168)
【出願日】平成19年5月25日(2007.5.25)
【国際出願番号】PCT/US2007/012518
【国際公開番号】WO2007/139950
【国際公開日】平成19年12月6日(2007.12.6)
【出願人】(508154379)アーチ・ケミカルズ・インコーポレーテッド (4)
【Fターム(参考)】
【公表日】平成21年11月5日(2009.11.5)
【国際特許分類】
【出願日】平成19年5月25日(2007.5.25)
【国際出願番号】PCT/US2007/012518
【国際公開番号】WO2007/139950
【国際公開日】平成19年12月6日(2007.12.6)
【出願人】(508154379)アーチ・ケミカルズ・インコーポレーテッド (4)
【Fターム(参考)】
[ Back to top ]

