充填済みのマイクロスケール装置
【課題】床を構成する固相物質を備える微小流体装置において、床は乾燥状態で保管・輸送されることが望ましいが、乾燥、保管、輸送、再構成によって、床は機能不良と成り得る。
【解決手段】一つ、二つもしくはそれ以上のマイクロチャネル構造(101)を備える微小流体装置であって、該マイクロチャネル構造がそれぞれ濡れた多孔性床の形で固相物質を保持することを意図する微小反応空間(104a〜h)を備える微小流体装置。当該一つ、二つもしくはそれ以上のマイクロチャネル構造(101)はそれぞれ床の保存活性を有する一つもしくはそれ以上の化合物を含む床の保存剤と共に乾燥状態の固相物質を含む。
【解決手段】一つ、二つもしくはそれ以上のマイクロチャネル構造(101)を備える微小流体装置であって、該マイクロチャネル構造がそれぞれ濡れた多孔性床の形で固相物質を保持することを意図する微小反応空間(104a〜h)を備える微小流体装置。当該一つ、二つもしくはそれ以上のマイクロチャネル構造(101)はそれぞれ床の保存活性を有する一つもしくはそれ以上の化合物を含む床の保存剤と共に乾燥状態の固相物質を含む。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、それぞれが、固相物質(=支持体物質)および液体の中に存在する、溶質(SもしくはS')の間の相互作用を含む、実験を実施するための微小流体装置(microfluidic device)に関する。固相物質は、実験の間は多孔性床として装置の中に存在する。装置は、一つもしくはそれ以上の実験を装置内で平行して行うことができることを許容する。
【0002】
平行性とは、少なくとも溶質および固相物質の間の相互作用を、二つもしくはそれ以上の実験について平行して行うことを意味する。使用される試薬/反応物は異なり得る。
【0003】
用語“溶質”は、真の溶質、ウイルスを含む微生物、懸濁細胞、懸濁細胞部分および溶解されているかもしくはコロイド形であって、本明細書中で引用される、多孔性床を通して液流により輸送されるのに十分な程小さい、種々の他の反応物を含む。
【0004】
用語“微小流体装置”とは、装置が、その中でいろいろな種類の反応物、アナライト、生成物、試料、緩衝液等を輸送するために液流が使用される、一つもしくはそれ以上のマイクロチャネル構造を備えることを意味する。“マイクロチャネル構造”の中の用語“マイクロ”とは、≦103μm、好ましくは≦5×102μm、例えば≦102μmである断面積寸法を有する、一つもしくはそれ以上のキャビティおよび/もしくは導管があることを意図する。装置は、ナノリットル(nl)の範囲(ピコリットル(pl)の範囲を含む)の液体アリコートを加工する能力がある。nlの範囲は5,000nlの上端を有するが、大抵の場合には≦1,000nl、例えば≦500nlもしくは≦100nlの容積に関する。
【0005】
溶質および多孔性床の間の相互作用は、例えば、
a)液体から溶質の分離、即ち、多孔性床プラス溶質が液体から分離され得るという結果でもって溶質が固相物質上に保持される、
b)触媒反応、例えば酵素反応の一部としての相互作用、
c)固相合成、および/もしくは
d)固相誘導体化
を意図する。
本明細書中で引用される特許出版物(WOおよびUS出願ならびに発行された米国特許)は、出典明示によりその全体を本明細書の一部とする。
【背景技術】
【0006】
背景出版物
WO 02075312(Gyros AB)は、アフィニティー反応物に対する相手を固定化形に含む、固相物質に可溶性のアフィニティー反応物を結合することによる反応変数の特色化のためのアフィニティーアッセイに焦点を当てている。固相は、微小反応空間(reaction microcavity)の内壁によるかもしくは微小反応空間の中に置かれる多孔性床により代表される。
【0007】
WO 03093802(Gyros AB)は、固定化形で使用される触媒系の一つの部分で触媒アッセイを実施することを記載している。アッセイは酵素系で例示される。固定化技法および固相物質はWO 02075312(Gyros AB)にあるのと基本的に同一である。
【0008】
US 5,726,026(Univ. Pennsylvania)およびUS 5,928,880(Univ. Pennsylvania)は、粒子の形態で固相を含有する検出/反応ゾーンを含む、微小流体装置を副次的な文で記載している。ストレプトアビジンは粒子に固定化されている。粒子は乾燥されるかもしくは凍結乾燥され得る。
【0009】
US 6,479,299(Caliper)は、微小流体装置の製造の間に可溶性のおよび不溶性の試薬(アッセイ成分)の前分配を議論している。
【0010】
出願者は、それらのそれぞれが逆相固相物質(疎水性ビーズ)(WO 02075775(Gyros AB)およびWO 02075776(Gyros AB))のカラムを含有する、複数のマイクロチャネル構造を含有するマイクロスケール流体装置(Gyrolab MALDI SP1)を市販している。固相物質は乾燥状態にある。ビーズが保管および輸送の間に正確な位置に保持されることを保証するために、装置の包装は特別にデザインされている。
【0011】
WO 00056808(Gyros AB)、WO 01047437(Gyros AB)、WO 01054810(Gyros AB)、WO 02075775(Gyros AB)およびWO 02075776(Gyros AB)は、微小流体装置を乾燥形で配達することを一般的な用語で示唆している。
【0012】
US 5,354,654(Ligler et al)は、凍結安定剤と一緒に凍結乾燥された、固定化リガンド−受容体複合体を持つ固体支持体を含むキットを示唆している。マクロスケールカラム中の支持体の充填が示唆されている。
【0013】
US 5,998,155(Squibb)およびUS 5,691,152(Squibb)は、高いビオチンの結合活性を有する組成を記載している。ビオチンの結合部分はポリマー支持体に固定化されている。支持体は、ビーズ形であり得て、(a)ビーズを凍結での乾燥の間の損傷から守りかつビーズの再膨潤を手助けする充填剤、(b)凍結での乾燥および保管の間の化学反応を阻害する保護剤、(c)緩衝液等と一緒に凍結乾燥され得る。
【0014】
背景問題
市場に上で議論された型の微小流体装置を提供することに関連する数多くの技術的問題がある。我々は、顧客が装置の中に親水性の多孔性床を導入しようとする場合には、機能不良床を得る危険性が高いことを見出した。総じて、このことは、床/マイクロチャネル構造の性能において、装置間および装置内の変動の増加、構造内で行われるアッセイについての感度および再現性の減少等に至るであろう。
【0015】
マクロ世界では、一般的な傾向は、濡れた状態の床の形態で固相ベースの分離媒体を持つ充填済みのカラムを提供することであった。蒸発に因る保管中の液体の損失は典型的には、全体の容積に比べると低い。床容積が典型的にnl−範囲にあって、蒸発が吸い上げに因り容易に顕著になる、微小流体装置については状況は全く異なる。結果は、床の迅速な非制御乾燥についての高い危険性ならびに床の液流特性を乱すであろうチャネル、キャビティーおよび空気の混在の創造についての許容できない危険性である。生物活性反応物を含む固相物質については、活性の再生不可能なおよび不可逆的な変化に対する危険性がまた明らかである。微小流体装置の中の完全にもしくは部分的に乾燥した固相物質を、乾燥前に濡れた床が持っていたのと本質的に同一のチャネル間のおよび装置間の変動と共に液流特性ならびに結合活性を有する微細な整列してかつ均一な多孔性床/カラムへ再構成するには困難がある。
【0016】
これらの問題は、水中で膨潤しない疎水性についてよりも親水性のおよび/もしくは水に膨潤可能な固相物質について典型的にはさらに顕著である。図2a〜bおよび3を参照のこと。
【0017】
濡れた親水性の床での我々の経験は、床は制御条件下に乾燥されるべきであるという考えを植えつけた。しかしながら、望ましい方式で微細な多孔性床/カラムへ再構成できた乾燥固相物質を実現することは困難であるとさらに判った、例えば、
・固相物質は典型的に、乾燥、保管および輸送に感受性である反応物を保有する。
・微小流体装置の中で溶質の多孔性床への結合は、多孔性床に関連する検出窓を通して分光法によりモニターされ得る。望ましくないチャネル、キャビティーおよび空気の混在の創造は、検出に対するノイズレベルを増加して、かくしてまた感度および再現性を減少するであろう。
・多孔性床を備える微小流体装置の輸送の間には、固相物質がマイクロキャビティーから漏れ得るという顕著な危険性がある。マイクロチャネル構造内で不規定の位置における漏れた固相物質との反応による分配された試薬およびアナライトの損失に対する危険性が明らかである。
この種の問題は、もし床が粒子で造られているならば、最も深刻である。
【発明の概要】
【0018】
発明の目的
目的は、上で議論された問題を解決する改良された微小流体装置を提供することである。かくして、目的は、装置の保管および輸送の後で、乾燥状態に変換されなかった同一の固相物質の濡れた床と本質的に同一の性能を持った濡れた床に再構成され得る、乾燥状態の固相物質を備える微小流体装置を提供することを含む。もし固相物質が固定化反応物を含むならば、その活性、例えば、溶質を結合する能力のような結合活性は、乾燥状態への変換、保管、輸送および再構成により本質的に未変化であるであろう。これは特に流動条件下の活性に当てはまる。
目的は、装置の製造ならびに、とりわけ、分離および/もしくはアッセイの目的のための装置の使用のための方法を提供することを含む。
【図面の簡単な説明】
【0019】
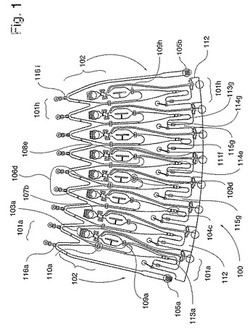
【図1】図1は、実験の部で利用される微小流体装置のマイクロチャネル構造(101a〜h)のサブグループ(100)を示す。
【0020】
【図2a】図2aおよびbは、微小反応空間(104a〜h)の中に置かれた粒子形(Superdex[登録商標]ペプチド、Amersham Biosciences, Uppsala, Sweden)の膨潤可能な固相物質を示す。図2aでは、粒子は凍結乾燥されている。粒子は、微小反応空間の中でひとまとめにされて、不規則に分散されている。充填床は何も用意されていない。
【図2b】図2aおよびbは、微小反応空間(104a〜h)の中に置かれた粒子形(Superdex[登録商標]ペプチド、Amersham Biosciences, Uppsala, Sweden)の膨潤可能な固相物質を示す。図2bでは、固相物質は整列して、濡れた多孔性床に再構築されている。
【0021】
【図3】図3は、多孔性床に充填されて、微小反応空間(104a〜h)の中で凍結乾燥された単分散の本質的に非膨潤可能でかつ親水性の粒子を示す。床は、再構成後に本質的に同一に見えた(図示していない)。
【0022】
【図4a】図4aおよびbは、リン酸カリウム緩衝液と一緒に乾燥(凍結乾燥)の、それにストレプトアビジンが固定化されている粒子の充填床の性能への影響を示す。蛍光強度は、典型的には出入り口におけるピークでもって床(床の長さ)を通して半径方向に示されている。流動方向は右から左へである。+4℃で一ヶ月の保管。影響は、ミオグロビンの四つの異なる濃度で蛍光ミオグロビン免疫アッセイ(下に示す)で測定されて、乾燥(凍結乾燥)されなかった(スラリー)同一の物質の床の性能と比較される。ミオグロビン濃度は、4.56nM(グラフ4)、22.8nM(グラフ3)、91.2nM(グラフ2)および273.6nM(グラフ1)であった。図4aは、リン酸カリウムと一緒に凍結乾燥および保管の後である。
【図4b】図4aおよびbは、リン酸カリウム緩衝液と一緒に乾燥(凍結乾燥)の、それにストレプトアビジンが固定化されている粒子の充填床の性能への影響を示す。蛍光強度は、典型的には出入り口におけるピークでもって床(床の長さ)を通して半径方向に示されている。流動方向は右から左へである。+4℃で一ヶ月の保管。影響は、ミオグロビンの四つの異なる濃度で蛍光ミオグロビン免疫アッセイ(下に示す)で測定されて、乾燥(凍結乾燥)されなかった(スラリー)同一の物質の床の性能と比較される。ミオグロビン濃度は、4.56nM(グラフ4)、22.8nM(グラフ3)、91.2nM(グラフ2)および273.6nM(グラフ1)であった。図4bは乾燥無しである。
【0023】
【図5a】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5aは乾燥無しである。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【図5b】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5bは大気圧での(吸い上げによる)乾燥である。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【図5c】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5cは真空での乾燥である。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【図5d】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5dは凍結乾燥である。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【0024】
【図6】図6は、ミオグロビンの試料(1%BSA添加のPBS中に希釈された、0〜274nMのミオグロビンの濃度)での実験の部で示される免疫アッセイのための標準曲線を示す。大気圧で乾燥された固相(100mMトレハロース中のPS−PheDex−ストレプトアビジン)、+4℃で一ヶ月の保管。y軸は蛍光を示して、x軸は対数での濃度を示す。
【発明を実施するための形態】
【0025】
本発明
固相物質と密接に混合されるときには、微小流体装置の中で微細な多孔性床として使用されることを意図する固相物質の前分配、乾燥、保管、輸送、再構成等の悪影響を減少するであろう特定の化合物および/もしくは化合物の組合せがあることが今や見出されている。これらの悪影響は、例えば:
a)チャネル、キャビティー、空気の混在等の許容できない形成および/もしくは、
b)マイクロチャネル構造内の望ましい位置からの固相物質の漏れ、および/もしくは
c)固定化反応物、例えばアフィニティー反応物、の結合活性の減少
である。
【0026】
これらの悪影響を減少する化合物もしくは化合物の組合せはこれ以後、これらが乾燥固相物質を効率的な濡れた多孔性床に復元するのを助けることから、“床の保存剤”もしくは単に“保存剤”と呼ばれるであろう。発明の原理にしたがって、床の保存剤は、乾燥/脱水前の濡れた固相物質の液体層の中に単に含まれる。乾燥は、微小流体装置の内部でもしくは外部で起こり得る。本明細書中で記載される、分布マニホールド(106a〜h)のような適切な入り口装置(102、103a〜h)および/もしくは単一の容積計量ユニット(108a〜h)を使用することにより、我々は、予め決められた容積の再構成された濡れた床の形成についての精度をさらに増加し得ることを見出した。充填済み固相物質の乾燥、保管、輸送および/もしくは再構成に因るチャネル間の変動を容易に最少に保つことができる。
【0027】
WO 02075312(Gyros AB)に規定されるような共通の流動制御が、微小流体装置のマイクロチャネル構造の少なくとも一つのサブセットの微小反応空間の中で平行して濡れた多孔性床の容積を復元するときに、精度を増加させるために有益であることがまた発見されている。遠心力は、例えば、もし床を沈降させてかつ復元するために適用されるならば、効率的な多孔性床の収率を改善するために有用である。
【0028】
第一の態様:微小流体装置
この態様は、そのそれぞれが多孔性床の形態で固相物質を保持することを意図した微小反応空間(104a〜h)を備える、一つ、二つもしくはそれ以上のマイクロチャネル構造(101)を備える、微小流体装置である。装置は、一つ、二つもしくはそれ以上のマイクロチャネル構造(101)の中の微小反応空間(104a〜h)が床の保存剤として作用する化合物もしくは化合物の組合せを含む乾燥状態の親水性の固相物質を含むことを特徴とする。かくしてこれらの化合物は、許容され得る濡れた多孔性床が、再構成液体が乾燥状態の固相物質を通過した後に復元され得ることを保障する。
床の保存剤(複数を含む)は、
a)おそらく固定化反応物(例えばアフィニティー反応物)を含む固相物質を
(i)固相物質の濡れた状態の乾燥状態への変換、および/もしくは
(ii)次の保管および/もしくは輸送
の間安定化させること、ならびに/または
b)乾燥状態の濡れた多孔性床への再構築を助けること
の能力がある。
【0029】
用語“許容され得る濡れた多孔性床”とは、床からの実験結果が使用され得る、即ち、床が機能性であることを意味する。用語“許容され得ない”とは、実験結果が廃棄されることを意味する。かくして、床の保存剤は、許容され得る床を得るための確率を増加させる。かくして、本発明の原理の使用は、微小流体装置上の機能性床またはマイクロチャネル構造の収率を微小流体装置の床またはマイクロチャネル構造の総数の≧70%、例えば≧80%もしくは≧90%もしくは≧95%もしくは≧98%になるように増加させることを助け得る。
【0030】
用語“乾燥状態”とは、乾燥後に残存する液体の量が、関係する液体で飽和されたとき(床の上端に現れる遊離の液体層が何も無い)の固相物質中に存在する液体の量の≦50%、例えば≦30%もしくは≦20%もしくは≦10%であることを意味する。多くの場合には、これは、乾燥および/もしくは保管後の固相物質の中の液体の量が、≦20%(w/w)、例えば≦10%もしくは≦5%であることを意味する。液体とは水を典型的に指す。
【0031】
床の保存剤(添加剤)
乾燥/脱水および保管の間の多孔性床の損傷は典型的には、生物学的に活性な物質についてと同様な様式で濡れた状態から乾燥状態への変換の間に誘発されるストレスに依存する。床の保存剤の選択は、乾燥条件、固相物質、固定化反応物の種類等に依存するであろう。同一の化合物(複数を含む)が一つの固相物質および/もしくは固定化反応物については床の保存剤として作用し得るが、他の組合せについては負に影響し得る。かくして、個別の保存剤の候補[単一の化合物としてもしくは化合物の組合せ(複数を含む)としてのいずれかで]ならびに乾燥状態への変換のための条件ならびに/または保管および/もしくは再構成のための条件を、候補を特定の固相物質のために使用する前に、試験することは極めて重要であろう。試験は、典型的に試行錯誤により行われ、そして
a)望ましくないチャネル、キャビティーおよび空気の混在を見出すための床の物理的検査、ならびに/もしくは
b)流動性、固定化反応物の活性、等の測定
を含み得る。
【0032】
固定化反応物/リガンドの活性の測定は、i)流動方向におけるおよび/もしくは流動方向に直角な活性プロフィール(例えば、床の中の活性の分布)、ii)例えば、標準型のアッセイでもしくは多孔性床の実際の将来の使用で床の挙動を試験することによる、床等の全活性の測定を含み得る。もしも固定化反応物が溶質を捕獲できるアフィニティー反応物であるならば、吸着(捕獲)後の床の中の溶質の分布を用いて、例えば反応物のチャネル、キャビティー、空気の混在もしくは局部的不活性化により引き起こされる異常な局部的挙動を見出し得る。吸着された溶質の総量は、全体像、例えば、再構成後の固定化反応物の平均状態の測定、を与え得る。試験に関する吸着は、流動、即ち、溶質を含有する液体が多孔性床を通って流れることができる、条件下に好ましく実施される。これらの種類の試験は典型的に、標準床および/もしくは
a)表示値
b)事前設定された規格
c)試験されるべき凍結乾燥された/乾燥された固相物質と同一の種類の凍結乾燥されていない/乾燥されていない固相物質から調製される床の挙動、等
により与えられ得る標準挙動との比較を含む。
【0033】
損傷の危険性が最も顕著である副工程は、主に乾燥工程(脱水工程)およびその状態での保管である。凍結乾燥が変換の一部である場合にはまた、凍結工程が顕著な損傷を引き起こし得る。生物学的に活性な物質については、特定の安定化剤がそれぞれの副工程に必要であり得ることが周知である。それ故に、安定化剤はそれらが活性である副工程の種類にしたがい名付けられ、例えば、冷凍安定化剤は凍結を指し、溶解安定化剤は脱水/乾燥を指し、そして長期安定化剤は保管を指す。例えば、Arakawa et al (Advanced Drug Delivery Reviews 46 (2001) 307-326)を参照されたい。本発明に関して、類似の分類が床の保存剤について用いられる。
乾燥固相物質の濡れた多孔性床への再構成を助ける化合物は、床の再構成剤と呼ばれ、また床の保存剤である。
【0034】
床の保存剤は、少なくとも一つから全部までの工程:乾燥/脱水、凍結、保管および再構成に関して活性であり得る。特定の薬剤の効力は、特定の工程の条件、固相物質および/もしくは安定化されるべき固定化反応物に依存するであろう。
【0035】
本発明で有用である床の保存剤は典型的には、それが水溶性であるという意味で親水性である。かくして、多くの床の保存剤は、典型的に酸素、窒素および硫黄から選択される一つもしくはそれ以上のヘテロ原子を有し、炭素原子の総数と酸素、窒素および硫黄原子の総数の間の比が≦6、例えば≦4もしくは≦2である。
【0036】
典型的な床の保存剤は、a)糖アルコール構造をまた含む炭水化物構造、b)ポリヒドロキシ構造(即ち、ポリヒドロキシポリマーをまた含む有機ポリオール)、c)ペプチド構造およびイミノ酸構造を含むアミノ酸構造、d)無機塩、e)有機塩特にカルボン酸塩、f)アミノ酸構造およびアンモニウム構造を含むアミン構造、h)等を示す化合物からなる群の中に見出され得る。
【0037】
炭水化物構造を持つ適当な化合物は、ショ糖、乳糖、グルコース、トレハロース、マルトース、イソマルトース、セロビオース、イノシトール、エチレングリコール、グリセロール、ソルビトール、キシリトール、マンニトール、場合によりその末端の一つもしくは両方で置換されたポリエチレングリコール、デキストラン、マルトデキストリン、単糖類、二糖類、オリゴ糖類を含む多糖類等の中で見出し得る。炭水化物構造を持つ化合物はまた、典型的にポリオールである。
【0038】
適当なポリオールは、多糖類、例えば場合によりアセテートもしくは低級ヒドロキシアルキル基(C2〜4)によってヒドロキシ基上で部分的に置換されたポリビニルアルコール、ポリ(低級ヒドロキシアルキル(C2〜4)アクリル酸エステル)ポリマーおよび相当するポリメタクリル酸エステルポリマー等のようなポリヒドロキシポリマー、ならびに二つもしくはそれ以上のヒドロキシ基を有する単量体化合物の中に見出され得る。典型的なポリオールにおいては、それぞれのヒドロキシ基は、sp3−混成炭素に直接結合している。
【0039】
適当なポリマーは、酸素および窒素から選択されるヘテロ原子を含む複数の官能基を有するポリマーの中に典型的に見出される。関連する官能基は、−O(CH2CH2O)n−(式中、nは≧2、例えば≧5である)、−CONH−もしくは−CONH2(式中、Hは適当な親水性の有機基で置換され得る)のようなアミド、ヒドロキシ(OH)、エステル(−COOR (式中、Rは適当な親水性の有機基である))、等である。特別な例は、ポリエチレングリコール、デキストランおよび他の多糖類、ポリビニルピロリドン、ポリペプチド、上述のポリアクリル酸エステルおよびメタクリル酸エステルポリマー、上述のポリビニルアルコール等である。
上の用語“ポリマー”はまた、言及される特異的なポリマーが一部であるコポリマーを含む。
【0040】
溶解安定剤である床の保存剤は、安定化されるべき固相物質に結合した水を置換することにより乾燥/脱水工程の間に作用すると信じられている。かくして、これらの床の保存剤は主として、固相物質との水素結合/配位に関与し得る化合物の中に見出される。現在の知識を持って、溶解安定化のための最も典型的な候補は、例えば、ポリマー構造および/もしくは炭水化物構造(オリゴマーはポリマーに含まれる)を持つ、ポリオール(ジオール、トリオール等を含む)の中に見出される。固相物質が、例えばペプチド構造を持つ、固定化反応物を含む場合には、最も有効な候補は、好ましくは二糖類である炭水化物構造を有し、ショ糖、乳糖、グルコース、トレハロース、マルトース、イソマルトース、セロビオース等の中に見出されると信じられている。
【0041】
何度も、溶解安定剤および長期保管のための安定剤のような、適当な床の保存剤は、場合により微小反応空間に存在する一つもしくはそれ以上の他の成分と混合して、微小反応空間の中でガラス状態で存在する能力がある。
【0042】
固相物質の乾燥状態で存在する床の保存剤は、典型的には非揮発性である。これは、揮発性の凍結安定剤が凍結乾燥の間に含まれることを除外しない。
【0043】
保護剤(添加剤)
乾燥状態にある固相物質はまた、固相物質および/もしくは固定化反応物の望ましくない化学反応を阻害する、一つもしくはそれ以上の所謂保護剤を含有し得る。適当な保護剤は、フリーラジカルの捕捉剤、抗酸化剤、還元剤等の中で見出される。
【0044】
他の添加剤
乾燥状態の固相物質はまた、非揮発性の緩衝成分を持つ、例えば、リン酸緩衝剤、クエン酸緩衝剤等におけるような、陰イオン性である緩衝成分の少なくとも一つもしくは二つを持つ緩衝剤のような、適切な緩衝剤を含有し得る。また他の緩衝剤を使用し得る。緩衝成分は典型的に、pH1〜13の範囲の適切なpH範囲内で、好ましくは3〜11の範囲で、高い緩衝能力を提供する。凍結乾燥される固相物質については、特にカリウムを対イオンとして持つ、リン酸塩緩衝剤が好まれる。
一つもしくはそれ以上の抗菌剤、例えば、静菌薬、殺菌剤、抗ウイルス薬等のような他の添加剤がまた含まれ得る。
【0045】
可能な充填剤が添加剤としてまた含まれ得る。充填剤は、床の保存剤について一般に上で議論されたように固相物質に対して床の保存効果を有し得る。
【0046】
マイクロキャビティーの密着剤(一種の床の保存剤)は、固相物質を微小反応空間の中に保持し、その結果、乾燥状態の固相物質を濡れた多孔性床へ復元することを助ける。この種の薬剤は、粒子をお互いにおよび/もしくは微小反応空間の内壁に密着させることにより作用する。マイクロキャビティーの密着剤は、上で議論された床の保存剤候補の中で、例えば、炭水化物のおよび/もしくはポリマーの構造を示す物の中で、見出され得る。
【0047】
種々の添加剤(床の保存剤、緩衝物質、保護剤、充填剤等)は、乾燥状態にある固相物質の中で、典型的に0.0001〜25%の範囲で、例えば≧0.001%もしくは≧0.01%もしくは≧0.1%および/または≦10%もしくは≦1%の量で存在する。これらの範囲は、それぞれの個別の添加剤ならびに添加剤の総量に適用され、ただし、総量が範囲の上限を超えるべきでない。有効量の最適な範囲および個別の床の保存剤の十分な床の保存効果の測定は、上で議論されたような実験的試験を必要とする。%値は、乾燥状態にある固相物質の総重量に対する添加剤(複数を含む)の重量を指す。
【0048】
添加剤(安定化剤、緩衝物質、保護剤、抗菌剤および/もしくは充填剤)は、それらが再構成された多孔性床から、例えば、液体を再構成された濡れた床を通して輸送すること(洗浄)により、容易に除去され得るように、典型的に水性媒体に可溶性である。
【0049】
微小反応空間(104a〜h)および固相物質
微小反応空間(104a〜h)は、その中に固相が存在するマイクロチャネル構造(101a〜h)の部分として規定される。これは、多孔性床の形態の固相について、床の容積および微小反応空間(104a〜h)が合致しそして同一の容積を有するであろうことを意味する。もしも固相がマイクロ導管の内壁であるならば、微小反応空間(104a〜h)は、固相の最上流のおよび最下流の末端の間の容積として規定される。
【0050】
微小反応空間(104a〜h)は、典型的に、連続的に広がりおよび/もしくは狭まり得るかまたはし得ない真直ぐなまたは曲がったマイクロ導管である。同一の装置において、全ての微小反応空間は典型的に、本質的に同一の形および/もしくはサイズを有する。形および/もしくはサイズが異なる本発明にしたがう微小反応空間を備える微小流体装置の中では、微小反応空間/マイクロチャネル構造(104a〜h/101a〜h)は、それぞれのグループが他のグループのいずれにも存在しない微小反応空間を含有するグループに分割され得る。それぞれのグループは、他のグループの小区域から分離している装置の小区域の中に位置し得る。
【0051】
微小反応空間(104a〜h)は、≦1,000μm、例えば≦500μmもしくは≦200μm(深さおよび/もしくは広さ)である、少なくとも一つの断面寸法を有する。最小の断面寸法は、典型的に≧5μmであり、例えば≧25μmもしくは≧50μmである。微小反応空間の総容積は、典型的にnlの範囲にあり、例えば≦5,000nl、例えば1,000nlもしくは≦500nlもしくは≦100nlもしくは≦50nlもしくは≦25nlである。
【0052】
多孔性床は、a)多孔性のもしくは非多孔性の粒子の集団、またはb)多孔性モノリス、である。
モノリスの床は、多孔性の膜もしくは多孔性のプラグの形態であり得る。
用語“多孔性の粒子”は、WO 02075312(Gyros AB)にあるのと同一の意味を有する。
【0053】
適当な粒子は球状でもしくは回転楕円形(ビーズ状)でまたは非球状である。固相として使用される粒子について適当な平均直径は、典型的に1〜100μmの範囲で見出され、好ましくは≧5μm、例えば≧10μmもしくは≧15μmおよび/または≦50μmである平均直径である。また、例えば0.1μm単位までの平均直径を持つ、さらに小さい粒子を使用することができる。微小反応空間(104a〜h)の出口末端(111a〜h)および粒子のデザインは、粒子が微小反応空間(104a〜h)の中に保持され得るようにお互いにマッチすべきである。特定の種類の粒子、特にコロイド寸法の粒子は塊状になり得る。これらの場合には、たとえ塊状になる粒子がそれ自体ではさらに小さくても、塊のサイズは、与えられた範囲の中にあるべきである。例えば、WO 02075312(Gyros AB)を参照されたい。直径とは“流体力学的な”直径を指す。
【0054】
使用される粒子は、WO 02075312(Gyros AB)にあるのと同一の意味で単分散で(モノサイズで)もしくは多分散で(ポリサイズで)あり得る。
固相物質は透明であり得るかもしくはあり得ない。
【0055】
固相の基材は無機のおよび/もしくは有機の物質から作成され得る。典型的な無機物質はガラスを含み、そして典型的な有機物質は有機ポリマーを含む。ポリマー物質は、ガラスおよびシリコンゴムのような、無機ポリマー、ならびに合成のもしくは生物の供給源(バイオポリマー)であり得る有機ポリマーを含む。用語のバイオポリマーは、その中に天然のバイオポリマーから誘導されるポリマーバックボーンがある半合成ポリマーを含む。典型的な合成の有機ポリマーは架橋されていて、重合可能な炭素−炭素二重結合を含む単量体の重合によりしばしば得られる。適当な単量体の例は、アクリル酸ヒドロキシアルキルおよび相当するメタクリル酸エステル、アクリルアミドおよびメタクリルアミド、ビニルおよびスチリルエーテル、アルケン置換のポリヒドロキシポリマー、スチレン等である。典型的なバイオポリマーは架橋され得るかもしくはされ得ない。大抵の場合には、それらは炭水化物構造、例えばアガロース、デキストラン、でん粉等を示す。
【0056】
多孔性床に関する用語“親水性の”とは、過剰の水と接触するときに、床の全部に渡って毛管現象(吸着)により広げられる水に対する細孔の表面の十分な湿潤性を意図する。この表現はまた、吸着の間に水と接触する床の内部表面は、それぞれが、例えば、酸素および窒素の中で選択されるヘテロ原子を有する複数の極性官能基を露出するものとすることを意味する。適切な官能基を、ヒドロキシ基、エチレンオキシド基(−X−[CH2CH2O−]n (式中、nは>1の整数であって、Xは窒素もしくは酸素である))、アミノ基、アミド基、エステル基、カルボキシ基、スルホン基等の中で選択することができ、好ましくはpHに無関係に、例えば2〜12の範囲内で本質的に荷電されないような基である。粒子形の固相物質については、これは粒子の少なくとも外側の表面が極性の官能基を示すべきであることを意味する。親水性の官能基は、所謂エクステンダーアーム(触手)の上に存在するかもしくはその一部であり得る。
【0057】
もしも固相物質の基材が疎水性であるかもしくは十分に親水性で無い、例えば、スチレン(コ)ポリマーに基づくならば、水性液体と接触するべき表面は親水性化され得る。典型的なプロトコルは、上で議論されたのと同一な型の極性官能基を示す化合物もしくは化合物の混合物で被膜すること、酸素プラズマによる処理等を含む。
【0058】
乾燥状態の固相物質は、再構成液体と接触するときに、膨潤可能であり得る。膨潤可能な物質は、(a)再構成後の収縮/膨潤、ならびに不均一な充填および/もしくは貫流ならびに/または(b)保管および輸送の間の乾燥粒子の漏れに関連した問題をさらに与えやすいように見える。これに関して、用語“膨潤可能な”とは、乾燥状態の物質(上で規定したような)が再構成液体(水のように水性であり得る)と接触するときに、物質(粒子それ自体もしくはモノリス)の容積の増加が検出され得ることを意味する。容積の増加は、例えば、乾燥状態の物質の容積の≧10%もしくは≧75%であり得る。この規定にしたがって膨潤可能でない固相物質は非−膨潤可能と考えられる。
固相物質は剛性であるかもしくは弾性であり得る。
【0059】
固相物質は、溶質との有機の、無機の、生化学の反応等に関与する能力がある、固定化反応物を含有してもしなくてもよい。状況ならびに反応物および溶質の種類に依存して、固定化反応物および溶質の間の相互作用は、分離加工法、触媒反応、固相合成、固相誘導体化等の一部であり得る。
【0060】
固定化反応物は、ここで、溶質(S)に対するアフィニティー相手(affinity counterpart)(ACS)であって、溶質とアフィニティー複合体(ACS−S)を形成する能力があるアフィニティー反応物で例示される。アフィニティー結合は典型的に、(a)静電気的相互作用、(b)疎水性相互作用、(c)電子−供与体受容体相互作用、および/もしくは(d)バイオアフィニティー結合:に基づいている。
バイオアフィニティー結合は典型的に複合的であって、上の(a)〜(c)のような、相互作用の組合せを含む。
【0061】
かくして、固定化アフィニティー相手(ACS)は:
(a)電気的に荷電されるかまたは荷電可能である、即ち、正に荷電した窒素(例えば、第一級の、第二級の、第三級のもしくは第四級のアンモニウム基、およびアミジニウム基)ならびに/または負に荷電した基(例えば、カルボキシレート基、ホスフェート基、ホスホネート基、スルフェート基およびスルホネート基)を含む;ならびに/または
(b)一つもしくはそれ以上のヒドロカルビル基および他の疎水性基を含む;ならびに/または
(c)場合により水素ならびに/またはsp−、sp2−および/もしくはsp3−混成炭素に結合している、一つまたはそれ以上のヘテロ原子(O、S、N)を含む;ならびに/または
(d)特徴(a)〜(c)の組合せを含む、
ことがあり得る。
【0062】
バイオアフィニティー反応物/リガンドは、バイオアフィニティー対のメンバーである。典型的なバイオアフィニティー対は、a)抗原/ハプテンおよび抗体、b)相補的な核酸、c)免疫グロブリン結合タンパク質ならびに免疫グロブリン(例えば、IgGまたはそのFc−部分およびタンパク質AもしくはG)、d)レクチンおよび相当する炭水化物、e)ビオチンおよび(ストレプト)アビジン、e)酵素系(酵素の基質、酵素の補因子、酵素の阻害剤等)のメンバー、f)IMAC基ならびにヒスチジルおよび/もしくはシステイニルならびに/またはリン酸エステル化残基のアミノ酸配列(即ちIMACモチーフ)、等である。抗体には、抗原結合フラグメントおよび抗体のミメティックが含まれる。用語“バイオアフィニティー対”は、その中で一つもしくは両方のメンバーが合成である、例えば、天然のバイオアフィニティー対の一つもしくは両方を模倣する、アフィニティー対(affinity pair)をまた含む。用語のIMACとは固定化金属キレートを意味する。
【0063】
用語“アフィニティー反応物”はまた、例えばジスルフィドの形成により、可逆的共有結合性結合が可能である反応物を含む。この種の反応物は典型的に、HS−または−S−SOn−基(n=0、1もしくは2、自由原子価は炭素に結合する)を示す。US 5,887,997(Batista)、US 4,175,073(Axen et al)、および4,563,304(Axen et al)を参照されたい。
【0064】
固定化反応物/リガンド(アフィニティー反応物)は、触媒系または、触媒、共触媒、補因子、基質もしくは補基質、阻害剤、促進剤等のような、触媒系のメンバーでまたあり得る。酵素系については、相当するメンバーは、酵素、共触媒、補因子、補酵素、基質、補基質等である。用語“触媒系”はまた、連鎖触媒系、例えば、その中で最初の系の生成物が第二の触媒系等の基質および全体の生物細胞もしくはそのような細胞の一部である一連の系を含む。
【0065】
固定化アフィニティー反応物(ACS)は、意図する応用に関して固相物質に対して興味のある溶質と相互作用するために適切な選択性および特異性を有するように選択されるべきである。アフィニティー反応物および反応条件の適切な選択についての一般方法ならびに基準は当分野で周知である。
【0066】
固定化アフィニティー反応物(ACS)および溶質(S)を含む複合体の形成についてのアフィニティー定数(KS−−AC=[S][ACS]/[S−−ACS])は、応用を最適化するための重要な基準であって、応用に依存して変わる。アフィニティーアッセイについては、アフィニティー定数は、典型的には≦10−8mole/lもしくは≦10−9mole/lである。この種のアッセイは典型的に、溶質が固定化ACSと流動条件下に反応しそして動物のもしくは生物の試料(動物のもしくは生物の試料は、ヒトおよび他の動物の患者のような、哺乳動物からの、ならびに実験動物からの試料を含む)の中のアナライトの量に関連することを含む。これは、さらに弱いアフィニティーを有するアフィニティー相手がこの種の試料、他の試料およびアフィニティーアッセイ、ならびに他の応用のために使用され得ることを除外しない。かくして、応用に依存して、アフィニティー定数は、10−3mole/lまでもしくは10−4mole/lまでもしくは10−5mole/lまでもしくは10−7mole/lまでのように、比較的大きく、または10−8mole/l以下もしくは10−11mole/l以下のように、比較的小さくあり得る。
【0067】
反応物/リガンドの固定化技法は、当分野で普通に既知である技法の中で選択され得る。かくして、固相物質への結合は、共有結合、アフィニティー結合(例えば、生物特異的アフィニティー結合)、物理的吸着等を介し得る。
【0068】
アフィニティー結合を介する固定化は、その中でメンバー(固定化リガンドもしくはL)の一つが固相物質に、例えば共有結合で、堅固に結合している固定化アフィニティー対(affinity pair)を利用し得る。対の他のメンバー(固定化結合剤、B)は、結合剤Bおよび溶質Sに対するアフィニティー相手ACSを含む結合体(固定化結合体)として使用される。固定化アフィニティー対の例は、a)ストレプトアビジン/アビジン/ニュートラビジンおよびビオチン化反応物(もしくは逆もまた同様)、b)抗体およびハプテン化反応物(もしくは逆もまた同様)、c)IMACグループならびに反応物に連結するかまたはその一部である、ヒスチジルおよび/もしくはシステイニルならびに/またはリン酸エステル化残基を含有するアミノ酸配列(即ちIMACモチーフ)等である。
【0069】
用語“結合体”とは主として、化学結合体および組換え的に製造される結合体のような共有結合性結合体(そこでは両方の部分はペプチド構造を有する)を指す。この用語はまた、所謂天然の結合体、即ち、お互いに離れて間隔を空けて、アフィニティーを二つの異なる分子要素のほうに向ける二つの結合部位を示すアフィニティー反応物、例えば、分子の一つの側(=部分)上に種およびクラス−特異的決定因子をならびにもう一つの側(=部分)上に抗原/ハプテンの結合部位を含む天然の抗体を含む。
【0070】
固定化リガンドLは固定化結合剤Bに対して二つもしくはそれ以上の結合部位を有し、そして/または固定化結合剤BはリガンドLに対して一つ、二つもしくはそれ以上の結合部位を有する(または逆もまた同様)ことは有利であると信じられている。
【0071】
好ましい固定化アフィニティー対(LおよびB)は典型的に、ストレプトアビジンおよびビオチンについての相当するアフィニティー定数にせいぜい同等であるかまたはそれより≦10倍もしくは≦102倍もしくは≦103倍さらに大きいアフィニティー定数(KL−−B=[L][B]/[L−−B])を有する。これは典型的に、それぞれ、ほぼ≦10−13mole/l、≦10−12mole/l、≦10−11mole/lおよび≦10−10mole/lであるアフィニティー定数を意味するであろう。好ましくは、LおよびBを、ビオチン結合化合物およびストレプトアビジン結合化合物の中で、それぞれ選択すること(もしくは逆もまた同様)である。
【0072】
上で議論されたアフィニティー定数とは、Biacore (Uppsala, Sweden)からのバイオセンサー(表面プラスモン共鳴)により、即ち、デキストランで被膜した金の表面に固定化されるアフィニティー反応物(ACSおよびL)で、得られる値を指す。
【0073】
本発明で使用されるべきアフィニティー対、特にバイオアフィニティー対、のメンバーの少なくとも一つは、a)ポリおよびオリゴペプチド構造のようなペプチド構造を含むアミノ酸構造、b)炭水化物構造、c)核酸構造を含むヌクレオチド構造、d)ステロイド構造、トリグリセリド構造等のような脂質構造:の中で選択される構造を典型的に示す。これに関して、用語のアフィニティー対とは、固定化アフィニティー対(LおよびB)、固定化アフィニティー反応物および溶質(ACSおよびS)ならびに使用され得る他のアフィニティー対を指す。
【0074】
乾燥状態にある固相物質は、他に活性化形であり得る。換言すれば、それは、望ましい反応物の官能基との反応による直接の共有結合性固定化への用意ができている。望ましい反応物の上で使用され得る官能基は、求電子性のおよび求核性の基の中で典型的に選択されて、活性化基が、それぞれ、求核性でもしくは求電子性であるかどうかに依存する。使用され得る官能基の例は、アミノ基および置換のもしくは未置換の−NH2、カルボキシ基(−COOH/−COO−)、ヒドロキシ基、チオール基、ケト基等を含む他の基である。
【0075】
微小流体装置の他の特徴
微小流体装置のマイクロチャネル構造(101a〜h)は、実験の全部のプロトコルを構造内で実施することを許容する機能性部分を備える。かくして、微小流体装置のマイクロチャネル構造(101a〜h)は、a)例えば、多分容積計量ユニット(106a〜h、108a〜h)と一緒に、入口/入口孔(105a〜b、107a〜h)を備える入り口装置(102、103a〜h)、b)液体輸送のためのマイクロ導管;c)微小反応空間(104a〜h);d)微小混合空間/ユニット;e)液体から粒子状物質を分離するためのユニット(入り口装置の中に存在し得る)、f)例えば、キャピラリー電気泳動、クロマトグラフィー等により、試料の中で溶解されたかもしくは懸濁された成分をお互いから分離するためのユニット;g)微小検出空間;h)廃液の導管/マイクロキャビティー(112、115a〜h);i)バルブ(109a〜h、110a〜h);j)環境外気への通気口(116a〜i);等:の中で選択される一つ、二つ、三つもしくはそれ以上の機能性部分を備え得る。機能性部分は、二つ以上の機能性を有し得る、例えば、微小反応空間(104a〜h)および微小検出空間が合致し得る。微小流体装置の中のいろいろな種類の機能性ユニットは、Gyros AB/Amersham Pharmacia Biotech AB:WO 99055827、WO 99058245、WO 02074438、WO 02075312、WO 03018198(US 20030044322)、WO 03034598、SE 03026507(SE 04000717、US SN 60/508,508)、SE 03015393(US SN 60/472,924)によりおよびTecan/Gamera Biosciences:WO 01087487、WO 01087486、WO 00079285、WO 00078455、WO 00069560、WO 98007019、WO 98053311により記載されている。
【0076】
有利な形において、親水性の多孔性床を意図する微小反応空間(104a〜h)は、それらのそれぞれが入口(105a〜b、107a〜h)および少なくとも一つの容積計量ユニット(106a〜h、108a〜h)を備える、一つもしくはそれ以上の入り口装置(上流方向)(102、103a〜h)に接続される。一つの有利な変形体において、マイクロチャネル構造(101a〜h)および固相物質を含有することを意図する微小反応空間(104a〜h)当り一つの別個の入り口装置(103a〜h)がある。もう一つの有利な変形体において、入り口装置(102)は、マイクロチャネル構造(101a〜h)および固相物質を含有することを意図する微小反応空間(104a〜h)の全部もしくはサブセット(100)に共通であって、サブセット(100)のそれぞれのマイクロチャネル構造/微小反応空間(101a〜h/104a〜h)について共通の入り口(105a〜b)および一つの容積計量ユニット(106a〜h)を持つ分布マニホールドを備える。
【0077】
両方の変形体において、容積計量ユニット(106a〜h、108a〜h)のそれぞれは順番に、そのマイクロチャネル構造(101a〜h)、例えば微小反応空間(104a〜h)の下流部分と通信(communicate)する。共通の入り口装置(102)および/もしくは共通の分布マニホールドにより一緒に連結されるマイクロチャネル構造は、マイクロチャネル構造のサブセット(100)のグループを規定する。それぞれの容積計量ユニット(106a〜h、108a〜h)は典型的に、その出口末端においてバルブ(109a〜h、110a〜h)を有する。このバルブは、例えば、親水性のおよび疎水性の表面の間の境界(疎水性表面切れ目)のような、出口末端における化学的表面特性(WO 99058245(Amersham Pharmacia Biotech AB))のおよび/もしくは幾何学的な/物理的な表面特性(WO 98007019(Gamera))の変化を利用して、典型的には受動的である。
【0078】
入口、容積計量ユニット、分布マニホールド、バルブ等を持つ典型的な入り口装置は、WO 02074438(Gyros AB)、WO 02075312(Gyros AB)、WO 02075775(Gyros AB)およびWO 02075776(Gyros AB)に提示されている。
【0079】
微小流体装置はまた、異なるマイクロチャネル構造を接続する他の共通のマイクロチャネル/マイクロ導管を備え得る。入口、出口、通気口、等のようなそれらの種々の部分を含む共通のチャネルは、それらが通信しているマイクロチャネル構造のそれぞれの部分と考えられている。
共通のマイクロチャネルは、その中でマイクロチャネル構造がネットワークを形成する微小流体装置を解釈することを可能にする。例えば、US 6,479,299(Caliper)を参照されたい。
【0080】
それぞれのマイクロチャネル構造は、液体用の少なくとも一つの入口孔(105a〜b、107a〜h)および過剰の空気用(通気口)(116a〜i)のおよび多分また液体用(廃液チャネル(112)の中の円)の少なくとも一つの出口孔を有する。
微小流体装置はまた、本発明にしたがって固相物質を保持するための微小反応空間を何も有しないマイクロチャネル構造を備え得る。
【0081】
微小流体装置は、本発明にしたがって固相を含有することを意図する複数のマイクロチャネル構造/装置を含有する。これに関して、複数とは、二つ、三つもしくはそれ以上のマイクロチャネル構造を意味して、典型的には≧10、例えば≧25もしくは≧90もしくは≧180もしくは≧270もしくは≧360である。上で議論されたように、装置のマイクロチャネル構造は、グループもしくはサブセット(100)に分割され得て、それらのそれぞれは、例えば、微小反応空間のサイズおよび/もしくは形により、マニホールド、共通の廃液チャネル(112)等を持つ共通の入り口装置(102)のような、共通のマイクロチャネル(102、112)により規定され得る。グループもしくはサブセットの中のマイクロチャネル構造の数は、典型的に、装置のマイクロチャネル構造の総数の1〜99%の範囲にあり、例えば5〜50%もしくは5〜25%もしくは10〜50%の範囲にある。これは典型的に、それぞれのグループが3〜15もしくは3〜25もしくは3〜50個のマイクロチャネル構造を典型的に備えることを意味する。それぞれのグループは、装置の特定な区域に位置し得る。
【0082】
異なる原理が、上述の機能性部分の二つもしくはそれ以上の間で微小流体装置/マイクロチャネル構造内で液体を輸送するために利用され得る。慣性力を、例えば、次の段落で議論されるようにディスクを回転させることにより、使用し得る。他の有用な力は、毛管力、動電力、毛管力、静水圧のような非動電力等である。
【0083】
微小流体装置は典型的にはディスクの形である。好ましい形式は、ディスク平面に直角であるかもしくはそれと合致する対称軸(Cn)[そこでは、nは≧2、3、4もしくは5の整数、好ましくは∞(C∞)である]を有する。換言すれば、ディスクは、正方形のような方形、および他の多角形の形であり得るが、好ましくは円形である。一旦適切なディスク形式が選択されてくると、液流を駆動させるために遠心力を使用し得る。典型的にはディスク平面に直角であるかもしくは平行である回転軸の周りに装置を回転することは、必要な遠心力を創造し得る。優先日での大抵の明白な変形体において、回転軸は上述の対称軸と合致する。
【0084】
好ましい遠心力ベースの変形体については、それぞれのマイクロチャネル構造は、下流セクション(回転軸から)よりさらに短いラジアル距離にある一つの上流セクションを含む。多孔性床を意図する微小反応空間は、典型的に二つのセクションに中間のラジアル位置にある。
【0085】
もし遠心力が粒子床の形成および/もしくは再構成のためにならびに/または床を通して液流を駆動するために使用されるならば、微小反応空間は、流れの方向を回転軸から放射状に外側に合わせて典型的に配置される。
【0086】
好ましい装置は、典型的に、従来のCD−形式と同様なサイズおよび/もしくは形、例えば、従来のCD−半径(12cm)を持つ円形ディスクの10%から300%までの範囲にあるサイズを持つディスク形である。ディスクの上方のおよび/もしくは下方の側は、平面であり得るかもしくはあり得ない。
【0087】
微小流体装置のマイクロチャネル/マイクロキャビティーは、次の工程でもう一つの本質的に平面な基板(蓋)により覆われる蓋のない形のチャネル/キャビティを示す、本質的に平面な基板表面から製造され得る。WO 91016966(Pharmacia Biotech AB)およびWO 01054810(Gyros AB)を参照されたい。両方の基板は、好ましくは、プラスティック物質、例えばプラスティックポリマー物質から製造される。
内部表面の付着活性および親水性は、応用に関して均衡させるべきである。例えば、WO 01047637(Gyros AB)を参照されたい。
【0088】
用語“湿潤性の(親水性の)”および“非−湿潤性の(疎水性の)”とは、表面が、それぞれ、≦90°もしくは≧90°の水接触角を有することを意図する。異なる機能性部分の間で液体の効率的な輸送を容易にするためには、個別の部分の内部表面は本来湿潤性であるべきであり、好ましくは≦60°、例えば≦50°もしくは≦40°もしくは≦30°もしくは≦20°の水接触角を有する。これらの湿潤性値はマイクロ導管の少なくとも一つ、二つ、三つもしくは四つの内壁に当てはまる。一つもしくはそれ以上の内壁がさらに高い水接触角を有する場合には、これは、内壁(複数を含む)に対するさらに低い水接触角により補償され得る。特に入り口装置の中の湿潤性は、一旦液体がキャビティに入り始めたならば、水性液体が毛管現象(自己吸引)により意図するマイクロキャビティーを満たすことが可能であるように、適応されるべきである。マイクロチャネル構造の中の親水性の内部表面は、例えば、受動性バルブ(passive valve)、抗−吸上げ手段(anti-wicking means)、環境大気等への通気口として単に機能する通気口(図1の方形)を導入するために、親水性の内壁の中で一つもしくはそれ以上の局部的な疎水性表面切れ目を含み得る。例えば、WO 99058245(Gyros AB)およびWO 02074438(Gyros AB)を参照されたい。
【0089】
接触角とは、使用温度、典型的には+25℃、での値を指して、静的でありそしてWO 00056808(Gyros AB)およびWO 01047637(Gyros AB)に例示される方法により測定されることができる。
【0090】
第二の態様:複数の濡れた多孔性床の、場合により複数の濡れた多孔性床へ再構成される乾燥/脱水状態への変換のための方法
この態様は、この章の見出しに規定されるような方法である。この方法は、
i)そのそれぞれが床の保存剤を含有する液体で飽和された親水性の多孔性床を含有する微小反応空間(104a〜h)を備える複数のマイクロチャネル構造(101)を備える微小流体装置を提供すること、
ii)それぞれの微小反応空間(104a〜h)の中の床を、微小反応空間の中に保持されながら、乾燥および/もしくは脱水状態にある固相物質へ変換すること、
iii)場合により、それぞれの微小反応空間(104a〜h)の中で、工程ii)で得られた固相物質を濡れた多孔性床に再構成すること:
の工程から成ることを特徴とする。
この態様はまた、再構成された多孔性床の性能に関して微小流体装置の中のチャネル間の変動を減少させるための方法に関係する。
【0091】
固相物質は、次に導入される液体アリコートの中の溶質と相互作用し得る反応物を示しても示さなくてもよい。種々の特性が下におよび本明細書中の他の所で議論されている。
工程(iii)は、例えば、好ましくは本発明の第三態様について議論されるような、床を通る滞留時間および流速を持つ流動条件下に行われる。
【0092】
多孔性の粒子床は、粒子の分散液を微小流体装置の微小反応空間(104a〜h)の全てのまたは一つもしくはそれ以上のサブセット(100)を通して流動させることにより創造されることができる。次いで、粒子が沈降して、それぞれのマイクロキャビティー(104a〜h)の出口末端(111a〜h)に多孔性床を形成する。床の形成は、重力の使用および/もしくは遠心力の使用により容易になり得て、後者が好ましくはそれぞれの微小反応空間(104a〜h)の流動方向に沿って作用する。上で議論されたような望ましい添加剤は、液体の分散液の中に存在するかおよび/もしくは形成された後に床に添加剤を含有する液体を通過させることにより導入される。添加剤を含有する液体で飽和した床と一緒に微小流体装置は、乾燥状態への変換まで保存される。
【0093】
多孔性のモノリスの床は、典型的に、装置の製造の間に、例えば、
a)重合により、もしくは
b)既製の多孔性のモノリスを置くことにより、
微小流体装置の微小反応空間(104a〜h)の少なくとも一つのサブセット(100)のそれぞれの中に導入される。
【0094】
選択肢のa)においては、好ましい変形体は、微小反応空間(104a〜h)および相当するマイクロチャネル構造(101a〜h)と共に重合を密閉形で行うことである。選択肢のb)においては、好ましい変形体は、少なくとも微小反応空間(104a〜h)は覆われない(そしてマイクロチャネル構造(101a〜h)の残りの部分は覆われれる)一方で、モノリスを挿入することである。多孔性床の導入および、必要であれば、マイクロキャビティーの密閉の後に、床を上で議論された保存剤を含む溶液で飽和して、乾燥状態への変換まで保存する。
【0095】
床の乾燥状態への変換は、減圧下に、例えば、床が飽和されている液体の凝固点以下でおよび/もしくは以上で、液体を除去することにより達成され得る。減圧下におよび凝固点以下での除去は典型的に凍結乾燥を意味する。これに代えて、液体は沈降した分散液から大気圧下に加温して又はしないで除去される。
装置が液体の輸送を遠心力により駆動するためにデザインされている場合には、所謂回転−乾燥を使用し得る。実験の部の図1の説明を参照されたい。
【0096】
微小反応空間の周りの壁の間の小さい寸法および内部エッジに因り、吸上げは、特に大気圧での、乾燥/脱水/蒸発において重要な因子であるであろう。
濡れた多孔性床の再構成とは、再構成液体が、乾燥状態の固相物質を含有する微小反応空間のそれぞれを通って流れることができることを意味する。実験の部を参照されたい。
【0097】
数個の構造の中で固相物質を均等におよび/もしくは平行して処理するための重要な道具は、それぞれのマイクロチャネル構造(101a〜h)に、第一の態様で議論されたように、好ましい変形体においてマイクロチャネル構造/微小反応空間(101a〜h/104a〜h)のグループ/サブセット(100)に共通(102)である入り口装置(102/103a〜h)を提供することである。かくして、この種のデザインは、固相物質の平行的な分配ならびに多孔性床の平行的な再構成およびコンディショニングを容易にするであろう。それにより、本発明の最良の利益を達成するためには、少なくとも入り口装置(102、103a〜h)、分布マニホールド、および/もしくは個別の容積計量ユニット(106a〜h、108a〜h)に本明細書中の他の所で議論された制限内で親水性の表面特性を、ならびにそれぞれの容積計量ユニット(106a〜h、108a〜h)の出口に、好ましくは、例えば局所的な疎水性表面切れ目の形で、受動的(可動部分を持たないという意味)であるバルブ機能(109a〜h、110a〜h)を提供することが重要である。
【0098】
本発明の第三の態様:装置の使用
革新的な微小流体装置の使用は、大まかに言えば、
(i)本発明の第一の態様にしたがって微小流体装置を提供すること;
(ii)予め決められた数のマイクロチャネル構造/微小反応空間(101a〜h/104a〜h)の中で、好ましくは流動条件下に、乾燥状態にある固相物質を濡れた多孔性床へ再構成すること、
(iii)濡れた多孔性床を含有する一つもしくはそれ以上のマイクロチャネル構造(101a〜h)の中で当該濡れた多孔性床の上流にある位置で溶質(S')を含有する液体を提供すること、
(vi)液体を当該一つもしくはそれ以上のマイクロチャネル構造(101a〜h)の少なくとも一つの中の当該濡れた床を通して輸送すること:
の工程から成っている。
【0099】
工程(i)および(ii)
これらの工程は、本発明の第一および第二の態様にしたがっている。
【0100】
工程(iii)および(iv)
溶質(S')は、典型的に濡れた多孔性床と相互作用する能力がある。
工程(iii)は、溶質(S')が装置/マイクロチャネル構造内で形成されるかもしくはマイクロチャネル構造に分配されることを含む。適用可能であれば、形成は、典型的に、濡れた多孔性床/微小反応空間(104a〜h)の上流位置でもしくはその内である。分配は、典型的には多孔性床/微小反応空間(104a〜h)の上流位置で入口(105a〜b、107a〜h)へである。
【0101】
工程(iii)および(iv)は、溶質(S')および多孔性床の間の相互作用が起こることを許容するために実施される。導入部で言及されたように、工程は、(a)分離方法、および/もしくは(b)触媒反応、(c)固相合成、ならびに/または(d)固相物質/多孔性床の誘導体化の一部であり得る。
【0102】
分離は他の中で、
i)捕獲、即ち、多孔性床は、溶質(S')に対する結合能力を持つアフィニティー構造(アフィニティーリガンド、アフィニティー反応物)(AC'S')を示す。溶質(S')を含有する液体が床を通過するときには、次いで、溶質(S')はAC'S'を介して多孔性床に捕獲され/結合されるであろう。多孔性床を通る通過後に、液体は、溶質(S')を欠如するかもしくは低減した量を有するであろう。AC'S'およびS'は、上で議論されたACSおよびSにそれぞれ相当するであろう。
ii)サイズ排除、即ち、多孔性床はさらに大きい分子に比較してさらに小さい分子を保持する傾向がさらに多くある。溶質(S')は、液の先端の移動に比して遅延して、それ故に濡れた多孔性床の中では初めは富化されるであろう。
iii)電気泳動、即ち、多孔性床は、抗−対流および/もしくは抗−拡散の手段として機能する。:
を含む。
多くの分離プロトコルについて、二つもしくはそれ以上の捕獲、サイズ排除、電気泳動等の組合せが連続した床の中でもしくは同一の床の中でのいずれかで利用される。
【0103】
分離は、液体の中に存在する溶質についての精製もしくは富化のプロトコルの部分であり得る。液体から分離される溶質は、精製されるべき、富化されるべき等の汚染物質もしくは要素であり得る。分離は、合成プロトコル、調製プロトコル、細胞ベースのアッセイ、核酸アッセイ、免疫アッセイ、酵素アッセイ等を含むいろいろな種類のアフィニティーアッセイの一部であり得る。
【0104】
溶質を固相物質に結合するために捕獲工程を利用するアフィニティーアッセイは典型的に、アッセイのアフィニティー反応に関与する反応変数の特色化を意図する。この文脈において反応変数は主として二つの型:1)アフィニティー反応物に関連した変数、および2)反応条件、を持つ。1型の変数は、二つの主なサブグループ、a)存在および/もしくは不存在を含む量、濃度、相対的な量、結合活性および酵素活性、等のような活性、ならびにb)例えばアフィニティー定数、特異性等のアフィニティーそれ自体を含むアフィニティー反応物の性質、を含む。WO 02075312(Gyros AB)を参照されたい。それについて1型の反応変数が特色化される分子要素はアナライトと呼ばれる。
【0105】
本発明の文脈における触媒反応は、固相物質が、利用される触媒系の一つもしくはそれ以上の固定化メンバー(例えば、アフィニティー構造、アフィニティーリガンド、アフィニティー反応物)を示す一方で、同一の系の他のメンバーは溶質であることを含む。触媒反応は、固定化メンバー(アフィニティー構造、アフィニティーリガンド、アフィニティー反応物)および少なくとも一つの溶質メンバーの間のアフィニティー複合体の形成を含む。少なくとも一つのメンバーは、触媒系のための基質に相当する。反応は、基質に比較して異なる化学組成および/もしくは構造を典型的に有する生成物をもたらす。生成物は、反応の間に床に固定化されてもされなくてもよい。
【0106】
用語“触媒系”は、単一の触媒系および一連の連結した単一の酵素系、細胞全体、酵素活性を示す細胞部分等を含むさらに複雑な変形体を含む。床は、酵素反応器のような、触媒反応器として機能し得る。
【0107】
その間に溶質との相互作用が起こる工程は、触媒系もしくは他の反応変数(例えば、反応条件)の一つもしくはそれ以上のメンバーを特色化するための、酵素アッセイのような、触媒アッセイの部分であり得る。アッセイは、液体試料の中の特定の触媒、基質、補基質、補因子、共触媒等の活性を測定するためであり得る。測定されるべき活性に相当する分子要素/複数の要素はアナライト/複数のアナライトと呼ばれる。例えば、WO 03093802(Gyros AB)を参照されたい。
【0108】
アッセイの文脈において、用語のアナライトは、元の試料の中で特色化されるべき要素ならびにアッセイの間に形成されて元の試料の中のアナライトに定量的に関連しているアナライト由来の要素を含む。上で議論された溶質は、元のアナライトもしくはアナライト由来の要素であり得る。
【0109】
固相合成は、例えば、オリゴペプチドおよびオリゴヌクレオチド合成のような、ポリマー合成ならびに固相物質上の他の小分子の合成を含む。ポリマー合成で用いられる固定化反応物は、例えば、ヌクレオチド、炭水化物のような相当する単量体の構造、アミノ酸構造、およびこれらの構造のミメティックを示し得る。コンビナトリアルライブラリーの固定化メンバーのライブラリーの合成がまた含まれる。そのようなメンバーは、比較的低い分子量(例えば、ポリマーバックボーンへの可能なスペーサーを含んで<10,000ダルトン)を有する。
【0110】
本発明の文脈において固相誘導体化は大抵の場合に、濡れた多孔性床の上に固定化反応物もしくは活性化された官能基を導入することを目標として有する。かくして、固相誘導体化は、共有結合を介してもしくはアフィニティー/吸着結合を介して望ましい反応物の固定化を許容する反応性の構造もしくは基の導入を含む。かくして、固定化リガンドLを露出する濡れた多孔性床から出発して、そして固定化結合体(B−R=S';Bは固定化アフィニティー結合剤Bであって、Rは固定化されるべき反応物Rである)を含有する液体を通過させて、反応物Rは、Lについて上で議論されたような多孔性床および固定化結合体B−ACSの上に堅固に結合しかつ露出されるであろう。もしRが溶質Sに対するアフィニティー相手ACS(B−R=B−ACS)であるならば、生じた多孔性床を、溶質Sを含有する液体から溶質Sを捕獲する/分離するために上で議論されたように使用することができる。
【0111】
工程(iv)の間の輸送は、液体が多孔性床を通って連続的に流れていることもしくは液体が床内にあるときには、液体の輸送が停止されることを含む。床の上に固定化された反応物および溶質の間の相互作用は、かくして、流動条件下にもしくは静的な条件下に、それぞれ、起こることができる。我々は、もしこの種の反応が流動条件下に起こっているならば、アフィニティー反応の中の反応変数に関してさらに多くの情報が得られ得ることを以前に見出した(WO 02075312(Gyros AB))。流速および/もしくは滞留時間は、例えば、固相に固定化されたアフィニティー相手ACSに結合されるように成っている溶質(S)の量が、拡散による最少の摂動(非拡散制限条件)をもって、固定化アフィニティー反応物、典型的にはACS、および溶質、典型的には溶質S、の間の実際の反応速度もしくはアフィニティーを反映するように調整され得る。
【0112】
これはまた本発明に当てはまるが、主な興味が結合される/捕獲される溶質の全量である応用については、拡散制限のもしくは非拡散制限の条件のいずれかを利用する流動条件の下で捕獲することが使用され得ることを除外しない。かくして、多孔性床を通る適切な流速は、多数の因子、例えば、固定化反応物および溶質ならびにそれらのサイズ、微小反応空間の容積、固相物質を含む多孔性床等、に依存する。典型的には、流速は、典型的に、1時間以下のように2時間以下である上限をもって、≧0.050秒もしくは≧0.1秒のように≧0.010秒の滞留時間を与えるべきである。例示的な流速は、0.01〜100nl/秒およびさらに典型的には0.1〜10nl/秒のように、0.01〜1000nl/秒以内にある。これらの流速の範囲は、1〜50nlもしくは1〜25nlのように、1〜200nlの範囲の床容積に有用であり得る。滞留時間とは、液体アリコートが微小反応空間の中で固相/多孔性床と接触するためにそれがかかる時間を指す。これらの範囲は、分離、触媒アッセイ、固相合成、固相誘導体化等を含む革新的な微小流体装置の他の使用にまた適用可能である。
【0113】
最良の形態
本出願の提出における本発明の最良の形態は、実験の部に与えられて、トレハロースを床の保存剤として、リン酸カリウムをさらに別の添加剤(緩衝剤)として示される固相物質を包含し、そしてマイクロチャネル構造を持つ微小流体装置を図1に示す。
【0114】
実験の部
実験に使用される微小流体装置は円形であって、従来のCD(コンパクトディスク)と同一の寸法を持っていた。この微小流体装置はさらに続けてCDと呼ばれるであろう。CDは、周辺部の近くにそれぞれのグループについて共通の廃液チャネル(112)を持つディスクの中心(回転軸)の周りの環状ゾーンに配置される8個のマイクロチャネル構造(101a〜h)の14個のグループ(100)を含有した。8個のマイクロチャネル構造(101a〜h)のグループ(100)は図1に示されていて、そしてWO 02075312(Gyros AB)の図1〜2ならびにWO 03024548(US 20030054563)(Gyros AB)およびWO 03024598(US 20030053934)(Gyros AB)の相当する図に図示されているマイクロチャネル構造のグループに似ていて、それと同一な様式で機能する。寸法は、これらの先の特許出願にあるのと同一のサイズを本質的に持つ。
【0115】
それぞれのサブセット(100)は、一つの共通の入り口装置(102)、マイクロチャネル構造当り一つの別個の入り口装置(103a〜h)およびマイクロチャネル構造当り一つの微小反応空間(104a〜h)を持つ8つのマイクロチャネル構造(101a〜h)を備える。共通の入り口装置は、それぞれのマイクロチャネル構造(101a〜h)についてa)過剰の液体の出口としてまた機能するであろう二つの共通の入口(105a〜b)、およびb)一つの容積計量ユニット(106a〜h)を備える。容積計量ユニット(106a〜h)は、マイクロチャネル構造の下流部分のための分布マニホールドとして機能するであろう。別個の入り口装置(103a〜h)のそれぞれは、唯一つのマイクロチャネル構造の部分であって、入口(107a〜h)および容積計量ユニット(108a〜h)を備える。それぞれの容積計量ユニット(106a〜h、108a〜h)およびそれらの下流部分の間には、それぞれ、好ましくは受動的な、バルブ機能(109a〜h、110a〜h)がある。マイクロチャネル構造(101a〜h)の微小反応空間(104a〜h)は、マイクロチャネル構造(101a〜h)の共通の入り口装置(102)および別個の入り口装置(103a〜h)の両方の下流に位置する。
【0116】
それぞれの微小反応空間の出口末端(111a〜h)においては、深度は二つの工程で100μmから10μmに下げられて、粒子が微小反応空間から漏れることを防止する。それぞれの微小反応空間(104a〜h)は、図1で外側の曲がりとして図示される出口マイクロ導管(113a〜h)に接続される下流方向にあり、そして廃液機能(115a〜h)に接続される出口末端(114a〜h)を有する。周辺において、共通の廃液チャネル(112)がある。バルブ(109a〜h、疎水性切れ目)と一緒に通気口(116a〜i、疎水性切れ目)は、それぞれの容積計量ユニット(106a〜h)から下流に分布されるべき液体アリコートの容積を規定する。
【0117】
適切な量の水性液体を入り口装置の入口に入れることにより、毛管現象が入口に接続される容積計量ユニット(複数を含む)を液体で満たすであろう。ディスクをその中心の周りに回転することにより、液体を容積計量ユニットおよび下流部分の間のバルブ(109a〜h、110a〜h)に強制的に通過させることができる。
【0118】
もし微小反応空間(104a〜h)が出口マイクロ導管(113)の出口末端(114)より回転軸からさらに短いラジアル距離に置かれるならば、濡れた充填床の回転−乾燥を使用することができる。これは、出口マイクロ導管(113)の形に依存しない。
【実施例】
【0119】
実験
計器装備
免疫アッセイは自動化システムの中で実施される。システム(レーザー誘起蛍光(LIF)モジュールを備えるGyrolabワークステーション2型試作機、Gyros AB, Uppsala, Sweden)を、CD−スピナー、マイクロタイタープレート(MTP)用の保持器および5個のシリンジポンプ、2および2、に接続される10個の毛管用の保持器を持つロボットのアームを備えた。毛管の二つは、全ての試薬および緩衝液をMTPからCDの中の二つの共通の入口(105a〜b)のいずれかへ移送した。他の8つの毛管は、個別の試料をMTPからCDの中の別個の個別の入口(107a〜h)へ移送した。
【0120】
Gyrolabワークステーションは、応用特異的ソフトウエアにより制御される完全に自動化されたロボットシステムである。ソフトウエア内の応用特異的方法は、CDの回転を正確に制御された速度で制御して、それによりマイクロ構造を通る液体の移動を、応用が進行するにつれて、制御する。特別なソフトウエアがバックグラウンドノイズを減少するために含まれた。
【0121】
WO 02075312(Gyros AB)、WO 03025548およびUS 20030054563(Gyros AB)、WO 03025585およびUS 200030055576(Gyros AB)、WO 03056517およびUS 200301156763(Gyros AB)ならびにまたwww.gyros.com.をまた参照されたい。
【0122】
固相、ストレプトアビジンの固定化、充填、乾燥/脱水および再構成
微小流体装置のマイクロ構造の中に充填される固相ビーズ物質は、多孔性もしくは固体の性質の何れであってもよい。例えば、ポリスチレン(PS)粒子(15μm、Dynal Biotech, Oslo, Norway)が固相のために選択された。ビーズをフェニル−デキストラン(PheDex)の受動的吸着により修飾して、親水性表面を作製し、そして引き続いてストレプトアビジン(Immunopure Streptavidin、Pierce, Perbio Science UK Limited, Cheshire, United Kingdom)と、CDAP化学(Kohn & Wilchek, Biochem. Biophys. Res. Commun. 107 (1982), 878-884)を用いて共有結合させた。SuperdexペプチドおよびSepharoseHP(Amersham Biosciences, Uppsala, Sweden)のような他の粒子はまた、ストレプトアビジンとCDAP化学(フェニル−デキストランの被膜無しで)を用いて共有結合している。ストレプトアビジン−ビオチンは周知のバイオアフィニティー対である。ポリスチレン粒子は固体であって使用される再構成液体の中では膨潤可能でない。SuperdexペプチドおよびSepharoseHPは多くのアフィニティー反応物に対して多孔性であって、使用される再構成液体の中で膨潤可能である。
【0123】
ストレプトアビジンとの結合後で、床の保存剤と共に(この場合には砂糖添加剤(10〜100mM))もしくは床の保存剤なしで、リン酸カリウム緩衝液(10mM)中の粒子の懸濁液を、入口(105a〜b)を介して共通の分布チャネルの中に分布して、遠心力により構造を通って移動させた。通気口(109a〜h、113a〜i)と組合せた遠心力は、懸濁液を共通の入り口装置(102)の中に同じ分量で分割して、それらのそれぞれは、それぞれの微小反応空間(104a〜h)の出口末端(111a〜h)における二相の深度(111a〜h)に対してそれぞれの微小反応空間(104a〜h)の中で充填された粒子の床(カラム)を形成する。カラムの凡その容積は15nlであった。カラム/床は三つの異なる方法により乾燥され/脱水された:
吸い上げの助けによる大気圧での乾燥:濡れた多孔性床を含有する微小流体装置を6000rpmで一分間回転して、可能なかぎりの液体を除去した後に、装置を宝石箱の中に入れて、ポリマーで被膜したアルミニウムのバッグの中に封入した。
真空乾燥:濡れた多孔性床を含有する微小流体装置をトレーの上に置いて、真空乾燥オーブン(Heraeus vacutherm VT6060M)の中に入れた。温度を25℃にセットして、真空により圧力を0.1ミリバールに減圧した。装置をこの圧力および温度で、生成物が乾燥するまで、半時間保持した。次いで、圧力を大気圧に到達させた。次いで、装置を宝石箱の中に入れて、ポリマーで被膜したアルミニウムのバッグの中に封入した。
凍結での乾燥(凍結乾燥):濡れた多孔性床を含有する微小流体装置をトレーの上に置いて、−80℃のフリーザーの中に入れた(装置をまた普通の−20℃のフリーザーの中に一時間置いてもよい)。2、3分後に装置の中の全てのカラムが冷凍されて、コンデンサーの温度が−57℃にセットされている凍結乾燥装置(Heto, LyoPro 3000)に、トレーを移した。圧力を0.1〜0.06ミリバールに(真空により)減圧した。装置をこの圧力および温度で、全ての氷が昇華してしまうまで(約12時間もしくは終夜)、保持した。次いで、圧力を2分間の間で大気圧に到達させた後に、チャンバーを開けて、凍結乾燥された生成物が装置の中に提供された。装置を宝石箱の中に入れて、ポリマーで被膜したアルミニウムのバッグの中に封入した。
【0124】
装置を+4℃で一ヶ月保管し、その後で、乾燥カラムを、0.15M NaCl、0.02% NaN3および0.01% Tween[登録商標]20を含有する15mM リン酸緩衝液(PBS)、pH7.4で、共通の分布チャネルを介しそして適切な速度で回転して、一回再湿潤し/再構成した。溶液のそれぞれの添加は200nlの液体を個別のカラム(104a〜h)に配達する。最後に、再構成された床の機能を四つの異なるアナライト(ミオグロビン)の濃度で下に示す免疫アッセイで試験して、乾燥/脱水されていない、相当する床と比較した。結果は図4〜5に提示されて、乾燥/脱水された固相物質を有効な濡れた多孔性床へ再構成するためには床の保存剤を含むことが多少とも必須であることを示している。
【0125】
免疫アッセイ
我々のミオグロビンアッセイの捕獲抗体(=ACS)、モノクローナル抗−ミオグロビン8E11.1(LabAS, Tartu, Estonia)をSulfo−NHS−LC−ビオチン(Pierce, prod # 21335, Perbio Science UK Limited, Cheshire, United Kingdom)を用いてビオチン化した。モノクローナル抗ミオグロビン8E11.1のタンパク質濃度は1〜10mg/mlであって、そしてそれを0.15M NaClを添加した15mMのPBS中でビオチン化試薬の3倍モル過剰と室温で1時間インキュベートした後、それをNAP−5カラム(Amersham Biosciences, Uppsala, Sweden)もしくはタンパク質脱塩スピンカラム(Protein Desalting Spin Column)(Pierce, # 89849-P, Perbio Science UK Limited, Cheshire, United Kingdom)のいずれかを通してゲルろ過した。
【0126】
ビオチン化抗体を持つストレプトアビジンで固定化した粒子を装填するために、抗体の0.2〜2mg/mlの濃度(どれだけのストレプトアビジンが充填されたカラムにあるかに依存して)での溶液を、入口(105a〜b)を介して共通の分布チャネルの中に分布して、遠心力により構造を通して移動した。カラムを通る流速を回転速度により制御した(回転流動1)。捕獲抗体がカラムに結合した後に、それらを、共通の分布チャネル(入口105aもしくはb)へのPBS(0.01%のTween20を添加した)の添加により一回洗浄して、引き続いて回転工程を行った。
【0127】
Gyrolabワークステーションの中でミオグロビンアッセイを実演するために、6点の標準曲線を創造した(図6)。0〜274nMの範囲の濃度を持つミオグロビンの試料(1%BSA添加のPBS中に希釈した)を個別の入口(107a〜h)に毛管により分布した。回転流動方法の最初の二工程の間、試料容積200nlを、容積計量ユニット(108a〜h)に規定した。捕獲工程(ミオグロビンを8E11.1に結合する)の下で好適な速度論的条件に到達するためには、試料の流速は1nl/秒を超えるべきでない。試料の流速を回転流動2により制御した。試料の捕獲後に、カラムを、共通の分布チャネル(入口105aもしくはb)へのPBS(0.01%のTween20を添加した)の添加により二回洗浄して、引き続いて回転工程を行った。過剰の検出抗体(モノクローナル抗ミオグロビン2F9.1(LabAs, Tartu, Estonia))を共通の分布チャネル(入口105aもしくはb)を介して次に加えて、同様の遅い流速(回転流動3)を用いた。検出抗体を蛍光体Alexa 633 (Molecular Probes, Eugene, USA)で標識した。過剰の標識抗体を、共通の分布チャネル(入口105aもしくはb)へのPBS(0.01%のTween20を添加した)の4回の添加により洗い流して、引き続いて回転工程を行った。
【0128】
完全なアッセイをレーザー誘起蛍光(LIF)検出モジュールの中で分析した。WO 02075312(Gyros AB)、WO 03025548およびUS 20030054563(Gyros AB)、ならびにWO 03056517および10/331,399(Gyros AB)をさらに参照されたい。
【0129】
システムの中で実施される運転方法の概観は表1に提示されている。
【0130】
【表1】

【0131】
本発明の特定の革新的な態様は、添付の請求の範囲にさらに詳細に規定されている。本発明およびその有利性は詳細に記述されているけれども、添付の請求の範囲に規定されているような本発明の精神および範囲から逸脱すること無しに、種々の変化、置換および変更が、ここでなされ得ることを理解するべきである。さらに、本出願の範囲は、本明細書中で記載されている加工法、機械、製造、物質の成分、手段、方法および工程の特定の実施態様に限定されることを意図していない。当業者によって本発明の開示から容易に認識されるため、本明細書中で記載されている相当する実施態様と実質的に同一の機能を実施するかもしくは実質的に同一の結果を達成する、現存するかまたは後で開発されるであろう加工法、機械、製造、物質の組成、手段、方法もしくは工程は、本発明にしたがって利用され得る。したがって、添付の請求の範囲は、そのような加工法、機械、製造、物質の組成、手段、方法もしくは工程をそれらの範囲内に含むことを意図する。
【技術分野】
【0001】
本発明は、それぞれが、固相物質(=支持体物質)および液体の中に存在する、溶質(SもしくはS')の間の相互作用を含む、実験を実施するための微小流体装置(microfluidic device)に関する。固相物質は、実験の間は多孔性床として装置の中に存在する。装置は、一つもしくはそれ以上の実験を装置内で平行して行うことができることを許容する。
【0002】
平行性とは、少なくとも溶質および固相物質の間の相互作用を、二つもしくはそれ以上の実験について平行して行うことを意味する。使用される試薬/反応物は異なり得る。
【0003】
用語“溶質”は、真の溶質、ウイルスを含む微生物、懸濁細胞、懸濁細胞部分および溶解されているかもしくはコロイド形であって、本明細書中で引用される、多孔性床を通して液流により輸送されるのに十分な程小さい、種々の他の反応物を含む。
【0004】
用語“微小流体装置”とは、装置が、その中でいろいろな種類の反応物、アナライト、生成物、試料、緩衝液等を輸送するために液流が使用される、一つもしくはそれ以上のマイクロチャネル構造を備えることを意味する。“マイクロチャネル構造”の中の用語“マイクロ”とは、≦103μm、好ましくは≦5×102μm、例えば≦102μmである断面積寸法を有する、一つもしくはそれ以上のキャビティおよび/もしくは導管があることを意図する。装置は、ナノリットル(nl)の範囲(ピコリットル(pl)の範囲を含む)の液体アリコートを加工する能力がある。nlの範囲は5,000nlの上端を有するが、大抵の場合には≦1,000nl、例えば≦500nlもしくは≦100nlの容積に関する。
【0005】
溶質および多孔性床の間の相互作用は、例えば、
a)液体から溶質の分離、即ち、多孔性床プラス溶質が液体から分離され得るという結果でもって溶質が固相物質上に保持される、
b)触媒反応、例えば酵素反応の一部としての相互作用、
c)固相合成、および/もしくは
d)固相誘導体化
を意図する。
本明細書中で引用される特許出版物(WOおよびUS出願ならびに発行された米国特許)は、出典明示によりその全体を本明細書の一部とする。
【背景技術】
【0006】
背景出版物
WO 02075312(Gyros AB)は、アフィニティー反応物に対する相手を固定化形に含む、固相物質に可溶性のアフィニティー反応物を結合することによる反応変数の特色化のためのアフィニティーアッセイに焦点を当てている。固相は、微小反応空間(reaction microcavity)の内壁によるかもしくは微小反応空間の中に置かれる多孔性床により代表される。
【0007】
WO 03093802(Gyros AB)は、固定化形で使用される触媒系の一つの部分で触媒アッセイを実施することを記載している。アッセイは酵素系で例示される。固定化技法および固相物質はWO 02075312(Gyros AB)にあるのと基本的に同一である。
【0008】
US 5,726,026(Univ. Pennsylvania)およびUS 5,928,880(Univ. Pennsylvania)は、粒子の形態で固相を含有する検出/反応ゾーンを含む、微小流体装置を副次的な文で記載している。ストレプトアビジンは粒子に固定化されている。粒子は乾燥されるかもしくは凍結乾燥され得る。
【0009】
US 6,479,299(Caliper)は、微小流体装置の製造の間に可溶性のおよび不溶性の試薬(アッセイ成分)の前分配を議論している。
【0010】
出願者は、それらのそれぞれが逆相固相物質(疎水性ビーズ)(WO 02075775(Gyros AB)およびWO 02075776(Gyros AB))のカラムを含有する、複数のマイクロチャネル構造を含有するマイクロスケール流体装置(Gyrolab MALDI SP1)を市販している。固相物質は乾燥状態にある。ビーズが保管および輸送の間に正確な位置に保持されることを保証するために、装置の包装は特別にデザインされている。
【0011】
WO 00056808(Gyros AB)、WO 01047437(Gyros AB)、WO 01054810(Gyros AB)、WO 02075775(Gyros AB)およびWO 02075776(Gyros AB)は、微小流体装置を乾燥形で配達することを一般的な用語で示唆している。
【0012】
US 5,354,654(Ligler et al)は、凍結安定剤と一緒に凍結乾燥された、固定化リガンド−受容体複合体を持つ固体支持体を含むキットを示唆している。マクロスケールカラム中の支持体の充填が示唆されている。
【0013】
US 5,998,155(Squibb)およびUS 5,691,152(Squibb)は、高いビオチンの結合活性を有する組成を記載している。ビオチンの結合部分はポリマー支持体に固定化されている。支持体は、ビーズ形であり得て、(a)ビーズを凍結での乾燥の間の損傷から守りかつビーズの再膨潤を手助けする充填剤、(b)凍結での乾燥および保管の間の化学反応を阻害する保護剤、(c)緩衝液等と一緒に凍結乾燥され得る。
【0014】
背景問題
市場に上で議論された型の微小流体装置を提供することに関連する数多くの技術的問題がある。我々は、顧客が装置の中に親水性の多孔性床を導入しようとする場合には、機能不良床を得る危険性が高いことを見出した。総じて、このことは、床/マイクロチャネル構造の性能において、装置間および装置内の変動の増加、構造内で行われるアッセイについての感度および再現性の減少等に至るであろう。
【0015】
マクロ世界では、一般的な傾向は、濡れた状態の床の形態で固相ベースの分離媒体を持つ充填済みのカラムを提供することであった。蒸発に因る保管中の液体の損失は典型的には、全体の容積に比べると低い。床容積が典型的にnl−範囲にあって、蒸発が吸い上げに因り容易に顕著になる、微小流体装置については状況は全く異なる。結果は、床の迅速な非制御乾燥についての高い危険性ならびに床の液流特性を乱すであろうチャネル、キャビティーおよび空気の混在の創造についての許容できない危険性である。生物活性反応物を含む固相物質については、活性の再生不可能なおよび不可逆的な変化に対する危険性がまた明らかである。微小流体装置の中の完全にもしくは部分的に乾燥した固相物質を、乾燥前に濡れた床が持っていたのと本質的に同一のチャネル間のおよび装置間の変動と共に液流特性ならびに結合活性を有する微細な整列してかつ均一な多孔性床/カラムへ再構成するには困難がある。
【0016】
これらの問題は、水中で膨潤しない疎水性についてよりも親水性のおよび/もしくは水に膨潤可能な固相物質について典型的にはさらに顕著である。図2a〜bおよび3を参照のこと。
【0017】
濡れた親水性の床での我々の経験は、床は制御条件下に乾燥されるべきであるという考えを植えつけた。しかしながら、望ましい方式で微細な多孔性床/カラムへ再構成できた乾燥固相物質を実現することは困難であるとさらに判った、例えば、
・固相物質は典型的に、乾燥、保管および輸送に感受性である反応物を保有する。
・微小流体装置の中で溶質の多孔性床への結合は、多孔性床に関連する検出窓を通して分光法によりモニターされ得る。望ましくないチャネル、キャビティーおよび空気の混在の創造は、検出に対するノイズレベルを増加して、かくしてまた感度および再現性を減少するであろう。
・多孔性床を備える微小流体装置の輸送の間には、固相物質がマイクロキャビティーから漏れ得るという顕著な危険性がある。マイクロチャネル構造内で不規定の位置における漏れた固相物質との反応による分配された試薬およびアナライトの損失に対する危険性が明らかである。
この種の問題は、もし床が粒子で造られているならば、最も深刻である。
【発明の概要】
【0018】
発明の目的
目的は、上で議論された問題を解決する改良された微小流体装置を提供することである。かくして、目的は、装置の保管および輸送の後で、乾燥状態に変換されなかった同一の固相物質の濡れた床と本質的に同一の性能を持った濡れた床に再構成され得る、乾燥状態の固相物質を備える微小流体装置を提供することを含む。もし固相物質が固定化反応物を含むならば、その活性、例えば、溶質を結合する能力のような結合活性は、乾燥状態への変換、保管、輸送および再構成により本質的に未変化であるであろう。これは特に流動条件下の活性に当てはまる。
目的は、装置の製造ならびに、とりわけ、分離および/もしくはアッセイの目的のための装置の使用のための方法を提供することを含む。
【図面の簡単な説明】
【0019】
【図1】図1は、実験の部で利用される微小流体装置のマイクロチャネル構造(101a〜h)のサブグループ(100)を示す。
【0020】
【図2a】図2aおよびbは、微小反応空間(104a〜h)の中に置かれた粒子形(Superdex[登録商標]ペプチド、Amersham Biosciences, Uppsala, Sweden)の膨潤可能な固相物質を示す。図2aでは、粒子は凍結乾燥されている。粒子は、微小反応空間の中でひとまとめにされて、不規則に分散されている。充填床は何も用意されていない。
【図2b】図2aおよびbは、微小反応空間(104a〜h)の中に置かれた粒子形(Superdex[登録商標]ペプチド、Amersham Biosciences, Uppsala, Sweden)の膨潤可能な固相物質を示す。図2bでは、固相物質は整列して、濡れた多孔性床に再構築されている。
【0021】
【図3】図3は、多孔性床に充填されて、微小反応空間(104a〜h)の中で凍結乾燥された単分散の本質的に非膨潤可能でかつ親水性の粒子を示す。床は、再構成後に本質的に同一に見えた(図示していない)。
【0022】
【図4a】図4aおよびbは、リン酸カリウム緩衝液と一緒に乾燥(凍結乾燥)の、それにストレプトアビジンが固定化されている粒子の充填床の性能への影響を示す。蛍光強度は、典型的には出入り口におけるピークでもって床(床の長さ)を通して半径方向に示されている。流動方向は右から左へである。+4℃で一ヶ月の保管。影響は、ミオグロビンの四つの異なる濃度で蛍光ミオグロビン免疫アッセイ(下に示す)で測定されて、乾燥(凍結乾燥)されなかった(スラリー)同一の物質の床の性能と比較される。ミオグロビン濃度は、4.56nM(グラフ4)、22.8nM(グラフ3)、91.2nM(グラフ2)および273.6nM(グラフ1)であった。図4aは、リン酸カリウムと一緒に凍結乾燥および保管の後である。
【図4b】図4aおよびbは、リン酸カリウム緩衝液と一緒に乾燥(凍結乾燥)の、それにストレプトアビジンが固定化されている粒子の充填床の性能への影響を示す。蛍光強度は、典型的には出入り口におけるピークでもって床(床の長さ)を通して半径方向に示されている。流動方向は右から左へである。+4℃で一ヶ月の保管。影響は、ミオグロビンの四つの異なる濃度で蛍光ミオグロビン免疫アッセイ(下に示す)で測定されて、乾燥(凍結乾燥)されなかった(スラリー)同一の物質の床の性能と比較される。ミオグロビン濃度は、4.56nM(グラフ4)、22.8nM(グラフ3)、91.2nM(グラフ2)および273.6nM(グラフ1)であった。図4bは乾燥無しである。
【0023】
【図5a】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5aは乾燥無しである。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【図5b】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5bは大気圧での(吸い上げによる)乾燥である。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【図5c】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5cは真空での乾燥である。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【図5d】図5a〜dは、床の保存剤(砂糖変形体、トレハロース)と共に三つの異なる乾燥手順の、それにストレプトアビジンが共有結合的に結合されている粒子の充填床の性能への影響を示す。保管および測定は、図4a〜bについてと同一である。図5dは凍結乾燥である。種々のグラフについてのミオグロビン濃度は、図4a〜bにあるのと同一である。
【0024】
【図6】図6は、ミオグロビンの試料(1%BSA添加のPBS中に希釈された、0〜274nMのミオグロビンの濃度)での実験の部で示される免疫アッセイのための標準曲線を示す。大気圧で乾燥された固相(100mMトレハロース中のPS−PheDex−ストレプトアビジン)、+4℃で一ヶ月の保管。y軸は蛍光を示して、x軸は対数での濃度を示す。
【発明を実施するための形態】
【0025】
本発明
固相物質と密接に混合されるときには、微小流体装置の中で微細な多孔性床として使用されることを意図する固相物質の前分配、乾燥、保管、輸送、再構成等の悪影響を減少するであろう特定の化合物および/もしくは化合物の組合せがあることが今や見出されている。これらの悪影響は、例えば:
a)チャネル、キャビティー、空気の混在等の許容できない形成および/もしくは、
b)マイクロチャネル構造内の望ましい位置からの固相物質の漏れ、および/もしくは
c)固定化反応物、例えばアフィニティー反応物、の結合活性の減少
である。
【0026】
これらの悪影響を減少する化合物もしくは化合物の組合せはこれ以後、これらが乾燥固相物質を効率的な濡れた多孔性床に復元するのを助けることから、“床の保存剤”もしくは単に“保存剤”と呼ばれるであろう。発明の原理にしたがって、床の保存剤は、乾燥/脱水前の濡れた固相物質の液体層の中に単に含まれる。乾燥は、微小流体装置の内部でもしくは外部で起こり得る。本明細書中で記載される、分布マニホールド(106a〜h)のような適切な入り口装置(102、103a〜h)および/もしくは単一の容積計量ユニット(108a〜h)を使用することにより、我々は、予め決められた容積の再構成された濡れた床の形成についての精度をさらに増加し得ることを見出した。充填済み固相物質の乾燥、保管、輸送および/もしくは再構成に因るチャネル間の変動を容易に最少に保つことができる。
【0027】
WO 02075312(Gyros AB)に規定されるような共通の流動制御が、微小流体装置のマイクロチャネル構造の少なくとも一つのサブセットの微小反応空間の中で平行して濡れた多孔性床の容積を復元するときに、精度を増加させるために有益であることがまた発見されている。遠心力は、例えば、もし床を沈降させてかつ復元するために適用されるならば、効率的な多孔性床の収率を改善するために有用である。
【0028】
第一の態様:微小流体装置
この態様は、そのそれぞれが多孔性床の形態で固相物質を保持することを意図した微小反応空間(104a〜h)を備える、一つ、二つもしくはそれ以上のマイクロチャネル構造(101)を備える、微小流体装置である。装置は、一つ、二つもしくはそれ以上のマイクロチャネル構造(101)の中の微小反応空間(104a〜h)が床の保存剤として作用する化合物もしくは化合物の組合せを含む乾燥状態の親水性の固相物質を含むことを特徴とする。かくしてこれらの化合物は、許容され得る濡れた多孔性床が、再構成液体が乾燥状態の固相物質を通過した後に復元され得ることを保障する。
床の保存剤(複数を含む)は、
a)おそらく固定化反応物(例えばアフィニティー反応物)を含む固相物質を
(i)固相物質の濡れた状態の乾燥状態への変換、および/もしくは
(ii)次の保管および/もしくは輸送
の間安定化させること、ならびに/または
b)乾燥状態の濡れた多孔性床への再構築を助けること
の能力がある。
【0029】
用語“許容され得る濡れた多孔性床”とは、床からの実験結果が使用され得る、即ち、床が機能性であることを意味する。用語“許容され得ない”とは、実験結果が廃棄されることを意味する。かくして、床の保存剤は、許容され得る床を得るための確率を増加させる。かくして、本発明の原理の使用は、微小流体装置上の機能性床またはマイクロチャネル構造の収率を微小流体装置の床またはマイクロチャネル構造の総数の≧70%、例えば≧80%もしくは≧90%もしくは≧95%もしくは≧98%になるように増加させることを助け得る。
【0030】
用語“乾燥状態”とは、乾燥後に残存する液体の量が、関係する液体で飽和されたとき(床の上端に現れる遊離の液体層が何も無い)の固相物質中に存在する液体の量の≦50%、例えば≦30%もしくは≦20%もしくは≦10%であることを意味する。多くの場合には、これは、乾燥および/もしくは保管後の固相物質の中の液体の量が、≦20%(w/w)、例えば≦10%もしくは≦5%であることを意味する。液体とは水を典型的に指す。
【0031】
床の保存剤(添加剤)
乾燥/脱水および保管の間の多孔性床の損傷は典型的には、生物学的に活性な物質についてと同様な様式で濡れた状態から乾燥状態への変換の間に誘発されるストレスに依存する。床の保存剤の選択は、乾燥条件、固相物質、固定化反応物の種類等に依存するであろう。同一の化合物(複数を含む)が一つの固相物質および/もしくは固定化反応物については床の保存剤として作用し得るが、他の組合せについては負に影響し得る。かくして、個別の保存剤の候補[単一の化合物としてもしくは化合物の組合せ(複数を含む)としてのいずれかで]ならびに乾燥状態への変換のための条件ならびに/または保管および/もしくは再構成のための条件を、候補を特定の固相物質のために使用する前に、試験することは極めて重要であろう。試験は、典型的に試行錯誤により行われ、そして
a)望ましくないチャネル、キャビティーおよび空気の混在を見出すための床の物理的検査、ならびに/もしくは
b)流動性、固定化反応物の活性、等の測定
を含み得る。
【0032】
固定化反応物/リガンドの活性の測定は、i)流動方向におけるおよび/もしくは流動方向に直角な活性プロフィール(例えば、床の中の活性の分布)、ii)例えば、標準型のアッセイでもしくは多孔性床の実際の将来の使用で床の挙動を試験することによる、床等の全活性の測定を含み得る。もしも固定化反応物が溶質を捕獲できるアフィニティー反応物であるならば、吸着(捕獲)後の床の中の溶質の分布を用いて、例えば反応物のチャネル、キャビティー、空気の混在もしくは局部的不活性化により引き起こされる異常な局部的挙動を見出し得る。吸着された溶質の総量は、全体像、例えば、再構成後の固定化反応物の平均状態の測定、を与え得る。試験に関する吸着は、流動、即ち、溶質を含有する液体が多孔性床を通って流れることができる、条件下に好ましく実施される。これらの種類の試験は典型的に、標準床および/もしくは
a)表示値
b)事前設定された規格
c)試験されるべき凍結乾燥された/乾燥された固相物質と同一の種類の凍結乾燥されていない/乾燥されていない固相物質から調製される床の挙動、等
により与えられ得る標準挙動との比較を含む。
【0033】
損傷の危険性が最も顕著である副工程は、主に乾燥工程(脱水工程)およびその状態での保管である。凍結乾燥が変換の一部である場合にはまた、凍結工程が顕著な損傷を引き起こし得る。生物学的に活性な物質については、特定の安定化剤がそれぞれの副工程に必要であり得ることが周知である。それ故に、安定化剤はそれらが活性である副工程の種類にしたがい名付けられ、例えば、冷凍安定化剤は凍結を指し、溶解安定化剤は脱水/乾燥を指し、そして長期安定化剤は保管を指す。例えば、Arakawa et al (Advanced Drug Delivery Reviews 46 (2001) 307-326)を参照されたい。本発明に関して、類似の分類が床の保存剤について用いられる。
乾燥固相物質の濡れた多孔性床への再構成を助ける化合物は、床の再構成剤と呼ばれ、また床の保存剤である。
【0034】
床の保存剤は、少なくとも一つから全部までの工程:乾燥/脱水、凍結、保管および再構成に関して活性であり得る。特定の薬剤の効力は、特定の工程の条件、固相物質および/もしくは安定化されるべき固定化反応物に依存するであろう。
【0035】
本発明で有用である床の保存剤は典型的には、それが水溶性であるという意味で親水性である。かくして、多くの床の保存剤は、典型的に酸素、窒素および硫黄から選択される一つもしくはそれ以上のヘテロ原子を有し、炭素原子の総数と酸素、窒素および硫黄原子の総数の間の比が≦6、例えば≦4もしくは≦2である。
【0036】
典型的な床の保存剤は、a)糖アルコール構造をまた含む炭水化物構造、b)ポリヒドロキシ構造(即ち、ポリヒドロキシポリマーをまた含む有機ポリオール)、c)ペプチド構造およびイミノ酸構造を含むアミノ酸構造、d)無機塩、e)有機塩特にカルボン酸塩、f)アミノ酸構造およびアンモニウム構造を含むアミン構造、h)等を示す化合物からなる群の中に見出され得る。
【0037】
炭水化物構造を持つ適当な化合物は、ショ糖、乳糖、グルコース、トレハロース、マルトース、イソマルトース、セロビオース、イノシトール、エチレングリコール、グリセロール、ソルビトール、キシリトール、マンニトール、場合によりその末端の一つもしくは両方で置換されたポリエチレングリコール、デキストラン、マルトデキストリン、単糖類、二糖類、オリゴ糖類を含む多糖類等の中で見出し得る。炭水化物構造を持つ化合物はまた、典型的にポリオールである。
【0038】
適当なポリオールは、多糖類、例えば場合によりアセテートもしくは低級ヒドロキシアルキル基(C2〜4)によってヒドロキシ基上で部分的に置換されたポリビニルアルコール、ポリ(低級ヒドロキシアルキル(C2〜4)アクリル酸エステル)ポリマーおよび相当するポリメタクリル酸エステルポリマー等のようなポリヒドロキシポリマー、ならびに二つもしくはそれ以上のヒドロキシ基を有する単量体化合物の中に見出され得る。典型的なポリオールにおいては、それぞれのヒドロキシ基は、sp3−混成炭素に直接結合している。
【0039】
適当なポリマーは、酸素および窒素から選択されるヘテロ原子を含む複数の官能基を有するポリマーの中に典型的に見出される。関連する官能基は、−O(CH2CH2O)n−(式中、nは≧2、例えば≧5である)、−CONH−もしくは−CONH2(式中、Hは適当な親水性の有機基で置換され得る)のようなアミド、ヒドロキシ(OH)、エステル(−COOR (式中、Rは適当な親水性の有機基である))、等である。特別な例は、ポリエチレングリコール、デキストランおよび他の多糖類、ポリビニルピロリドン、ポリペプチド、上述のポリアクリル酸エステルおよびメタクリル酸エステルポリマー、上述のポリビニルアルコール等である。
上の用語“ポリマー”はまた、言及される特異的なポリマーが一部であるコポリマーを含む。
【0040】
溶解安定剤である床の保存剤は、安定化されるべき固相物質に結合した水を置換することにより乾燥/脱水工程の間に作用すると信じられている。かくして、これらの床の保存剤は主として、固相物質との水素結合/配位に関与し得る化合物の中に見出される。現在の知識を持って、溶解安定化のための最も典型的な候補は、例えば、ポリマー構造および/もしくは炭水化物構造(オリゴマーはポリマーに含まれる)を持つ、ポリオール(ジオール、トリオール等を含む)の中に見出される。固相物質が、例えばペプチド構造を持つ、固定化反応物を含む場合には、最も有効な候補は、好ましくは二糖類である炭水化物構造を有し、ショ糖、乳糖、グルコース、トレハロース、マルトース、イソマルトース、セロビオース等の中に見出されると信じられている。
【0041】
何度も、溶解安定剤および長期保管のための安定剤のような、適当な床の保存剤は、場合により微小反応空間に存在する一つもしくはそれ以上の他の成分と混合して、微小反応空間の中でガラス状態で存在する能力がある。
【0042】
固相物質の乾燥状態で存在する床の保存剤は、典型的には非揮発性である。これは、揮発性の凍結安定剤が凍結乾燥の間に含まれることを除外しない。
【0043】
保護剤(添加剤)
乾燥状態にある固相物質はまた、固相物質および/もしくは固定化反応物の望ましくない化学反応を阻害する、一つもしくはそれ以上の所謂保護剤を含有し得る。適当な保護剤は、フリーラジカルの捕捉剤、抗酸化剤、還元剤等の中で見出される。
【0044】
他の添加剤
乾燥状態の固相物質はまた、非揮発性の緩衝成分を持つ、例えば、リン酸緩衝剤、クエン酸緩衝剤等におけるような、陰イオン性である緩衝成分の少なくとも一つもしくは二つを持つ緩衝剤のような、適切な緩衝剤を含有し得る。また他の緩衝剤を使用し得る。緩衝成分は典型的に、pH1〜13の範囲の適切なpH範囲内で、好ましくは3〜11の範囲で、高い緩衝能力を提供する。凍結乾燥される固相物質については、特にカリウムを対イオンとして持つ、リン酸塩緩衝剤が好まれる。
一つもしくはそれ以上の抗菌剤、例えば、静菌薬、殺菌剤、抗ウイルス薬等のような他の添加剤がまた含まれ得る。
【0045】
可能な充填剤が添加剤としてまた含まれ得る。充填剤は、床の保存剤について一般に上で議論されたように固相物質に対して床の保存効果を有し得る。
【0046】
マイクロキャビティーの密着剤(一種の床の保存剤)は、固相物質を微小反応空間の中に保持し、その結果、乾燥状態の固相物質を濡れた多孔性床へ復元することを助ける。この種の薬剤は、粒子をお互いにおよび/もしくは微小反応空間の内壁に密着させることにより作用する。マイクロキャビティーの密着剤は、上で議論された床の保存剤候補の中で、例えば、炭水化物のおよび/もしくはポリマーの構造を示す物の中で、見出され得る。
【0047】
種々の添加剤(床の保存剤、緩衝物質、保護剤、充填剤等)は、乾燥状態にある固相物質の中で、典型的に0.0001〜25%の範囲で、例えば≧0.001%もしくは≧0.01%もしくは≧0.1%および/または≦10%もしくは≦1%の量で存在する。これらの範囲は、それぞれの個別の添加剤ならびに添加剤の総量に適用され、ただし、総量が範囲の上限を超えるべきでない。有効量の最適な範囲および個別の床の保存剤の十分な床の保存効果の測定は、上で議論されたような実験的試験を必要とする。%値は、乾燥状態にある固相物質の総重量に対する添加剤(複数を含む)の重量を指す。
【0048】
添加剤(安定化剤、緩衝物質、保護剤、抗菌剤および/もしくは充填剤)は、それらが再構成された多孔性床から、例えば、液体を再構成された濡れた床を通して輸送すること(洗浄)により、容易に除去され得るように、典型的に水性媒体に可溶性である。
【0049】
微小反応空間(104a〜h)および固相物質
微小反応空間(104a〜h)は、その中に固相が存在するマイクロチャネル構造(101a〜h)の部分として規定される。これは、多孔性床の形態の固相について、床の容積および微小反応空間(104a〜h)が合致しそして同一の容積を有するであろうことを意味する。もしも固相がマイクロ導管の内壁であるならば、微小反応空間(104a〜h)は、固相の最上流のおよび最下流の末端の間の容積として規定される。
【0050】
微小反応空間(104a〜h)は、典型的に、連続的に広がりおよび/もしくは狭まり得るかまたはし得ない真直ぐなまたは曲がったマイクロ導管である。同一の装置において、全ての微小反応空間は典型的に、本質的に同一の形および/もしくはサイズを有する。形および/もしくはサイズが異なる本発明にしたがう微小反応空間を備える微小流体装置の中では、微小反応空間/マイクロチャネル構造(104a〜h/101a〜h)は、それぞれのグループが他のグループのいずれにも存在しない微小反応空間を含有するグループに分割され得る。それぞれのグループは、他のグループの小区域から分離している装置の小区域の中に位置し得る。
【0051】
微小反応空間(104a〜h)は、≦1,000μm、例えば≦500μmもしくは≦200μm(深さおよび/もしくは広さ)である、少なくとも一つの断面寸法を有する。最小の断面寸法は、典型的に≧5μmであり、例えば≧25μmもしくは≧50μmである。微小反応空間の総容積は、典型的にnlの範囲にあり、例えば≦5,000nl、例えば1,000nlもしくは≦500nlもしくは≦100nlもしくは≦50nlもしくは≦25nlである。
【0052】
多孔性床は、a)多孔性のもしくは非多孔性の粒子の集団、またはb)多孔性モノリス、である。
モノリスの床は、多孔性の膜もしくは多孔性のプラグの形態であり得る。
用語“多孔性の粒子”は、WO 02075312(Gyros AB)にあるのと同一の意味を有する。
【0053】
適当な粒子は球状でもしくは回転楕円形(ビーズ状)でまたは非球状である。固相として使用される粒子について適当な平均直径は、典型的に1〜100μmの範囲で見出され、好ましくは≧5μm、例えば≧10μmもしくは≧15μmおよび/または≦50μmである平均直径である。また、例えば0.1μm単位までの平均直径を持つ、さらに小さい粒子を使用することができる。微小反応空間(104a〜h)の出口末端(111a〜h)および粒子のデザインは、粒子が微小反応空間(104a〜h)の中に保持され得るようにお互いにマッチすべきである。特定の種類の粒子、特にコロイド寸法の粒子は塊状になり得る。これらの場合には、たとえ塊状になる粒子がそれ自体ではさらに小さくても、塊のサイズは、与えられた範囲の中にあるべきである。例えば、WO 02075312(Gyros AB)を参照されたい。直径とは“流体力学的な”直径を指す。
【0054】
使用される粒子は、WO 02075312(Gyros AB)にあるのと同一の意味で単分散で(モノサイズで)もしくは多分散で(ポリサイズで)あり得る。
固相物質は透明であり得るかもしくはあり得ない。
【0055】
固相の基材は無機のおよび/もしくは有機の物質から作成され得る。典型的な無機物質はガラスを含み、そして典型的な有機物質は有機ポリマーを含む。ポリマー物質は、ガラスおよびシリコンゴムのような、無機ポリマー、ならびに合成のもしくは生物の供給源(バイオポリマー)であり得る有機ポリマーを含む。用語のバイオポリマーは、その中に天然のバイオポリマーから誘導されるポリマーバックボーンがある半合成ポリマーを含む。典型的な合成の有機ポリマーは架橋されていて、重合可能な炭素−炭素二重結合を含む単量体の重合によりしばしば得られる。適当な単量体の例は、アクリル酸ヒドロキシアルキルおよび相当するメタクリル酸エステル、アクリルアミドおよびメタクリルアミド、ビニルおよびスチリルエーテル、アルケン置換のポリヒドロキシポリマー、スチレン等である。典型的なバイオポリマーは架橋され得るかもしくはされ得ない。大抵の場合には、それらは炭水化物構造、例えばアガロース、デキストラン、でん粉等を示す。
【0056】
多孔性床に関する用語“親水性の”とは、過剰の水と接触するときに、床の全部に渡って毛管現象(吸着)により広げられる水に対する細孔の表面の十分な湿潤性を意図する。この表現はまた、吸着の間に水と接触する床の内部表面は、それぞれが、例えば、酸素および窒素の中で選択されるヘテロ原子を有する複数の極性官能基を露出するものとすることを意味する。適切な官能基を、ヒドロキシ基、エチレンオキシド基(−X−[CH2CH2O−]n (式中、nは>1の整数であって、Xは窒素もしくは酸素である))、アミノ基、アミド基、エステル基、カルボキシ基、スルホン基等の中で選択することができ、好ましくはpHに無関係に、例えば2〜12の範囲内で本質的に荷電されないような基である。粒子形の固相物質については、これは粒子の少なくとも外側の表面が極性の官能基を示すべきであることを意味する。親水性の官能基は、所謂エクステンダーアーム(触手)の上に存在するかもしくはその一部であり得る。
【0057】
もしも固相物質の基材が疎水性であるかもしくは十分に親水性で無い、例えば、スチレン(コ)ポリマーに基づくならば、水性液体と接触するべき表面は親水性化され得る。典型的なプロトコルは、上で議論されたのと同一な型の極性官能基を示す化合物もしくは化合物の混合物で被膜すること、酸素プラズマによる処理等を含む。
【0058】
乾燥状態の固相物質は、再構成液体と接触するときに、膨潤可能であり得る。膨潤可能な物質は、(a)再構成後の収縮/膨潤、ならびに不均一な充填および/もしくは貫流ならびに/または(b)保管および輸送の間の乾燥粒子の漏れに関連した問題をさらに与えやすいように見える。これに関して、用語“膨潤可能な”とは、乾燥状態の物質(上で規定したような)が再構成液体(水のように水性であり得る)と接触するときに、物質(粒子それ自体もしくはモノリス)の容積の増加が検出され得ることを意味する。容積の増加は、例えば、乾燥状態の物質の容積の≧10%もしくは≧75%であり得る。この規定にしたがって膨潤可能でない固相物質は非−膨潤可能と考えられる。
固相物質は剛性であるかもしくは弾性であり得る。
【0059】
固相物質は、溶質との有機の、無機の、生化学の反応等に関与する能力がある、固定化反応物を含有してもしなくてもよい。状況ならびに反応物および溶質の種類に依存して、固定化反応物および溶質の間の相互作用は、分離加工法、触媒反応、固相合成、固相誘導体化等の一部であり得る。
【0060】
固定化反応物は、ここで、溶質(S)に対するアフィニティー相手(affinity counterpart)(ACS)であって、溶質とアフィニティー複合体(ACS−S)を形成する能力があるアフィニティー反応物で例示される。アフィニティー結合は典型的に、(a)静電気的相互作用、(b)疎水性相互作用、(c)電子−供与体受容体相互作用、および/もしくは(d)バイオアフィニティー結合:に基づいている。
バイオアフィニティー結合は典型的に複合的であって、上の(a)〜(c)のような、相互作用の組合せを含む。
【0061】
かくして、固定化アフィニティー相手(ACS)は:
(a)電気的に荷電されるかまたは荷電可能である、即ち、正に荷電した窒素(例えば、第一級の、第二級の、第三級のもしくは第四級のアンモニウム基、およびアミジニウム基)ならびに/または負に荷電した基(例えば、カルボキシレート基、ホスフェート基、ホスホネート基、スルフェート基およびスルホネート基)を含む;ならびに/または
(b)一つもしくはそれ以上のヒドロカルビル基および他の疎水性基を含む;ならびに/または
(c)場合により水素ならびに/またはsp−、sp2−および/もしくはsp3−混成炭素に結合している、一つまたはそれ以上のヘテロ原子(O、S、N)を含む;ならびに/または
(d)特徴(a)〜(c)の組合せを含む、
ことがあり得る。
【0062】
バイオアフィニティー反応物/リガンドは、バイオアフィニティー対のメンバーである。典型的なバイオアフィニティー対は、a)抗原/ハプテンおよび抗体、b)相補的な核酸、c)免疫グロブリン結合タンパク質ならびに免疫グロブリン(例えば、IgGまたはそのFc−部分およびタンパク質AもしくはG)、d)レクチンおよび相当する炭水化物、e)ビオチンおよび(ストレプト)アビジン、e)酵素系(酵素の基質、酵素の補因子、酵素の阻害剤等)のメンバー、f)IMAC基ならびにヒスチジルおよび/もしくはシステイニルならびに/またはリン酸エステル化残基のアミノ酸配列(即ちIMACモチーフ)、等である。抗体には、抗原結合フラグメントおよび抗体のミメティックが含まれる。用語“バイオアフィニティー対”は、その中で一つもしくは両方のメンバーが合成である、例えば、天然のバイオアフィニティー対の一つもしくは両方を模倣する、アフィニティー対(affinity pair)をまた含む。用語のIMACとは固定化金属キレートを意味する。
【0063】
用語“アフィニティー反応物”はまた、例えばジスルフィドの形成により、可逆的共有結合性結合が可能である反応物を含む。この種の反応物は典型的に、HS−または−S−SOn−基(n=0、1もしくは2、自由原子価は炭素に結合する)を示す。US 5,887,997(Batista)、US 4,175,073(Axen et al)、および4,563,304(Axen et al)を参照されたい。
【0064】
固定化反応物/リガンド(アフィニティー反応物)は、触媒系または、触媒、共触媒、補因子、基質もしくは補基質、阻害剤、促進剤等のような、触媒系のメンバーでまたあり得る。酵素系については、相当するメンバーは、酵素、共触媒、補因子、補酵素、基質、補基質等である。用語“触媒系”はまた、連鎖触媒系、例えば、その中で最初の系の生成物が第二の触媒系等の基質および全体の生物細胞もしくはそのような細胞の一部である一連の系を含む。
【0065】
固定化アフィニティー反応物(ACS)は、意図する応用に関して固相物質に対して興味のある溶質と相互作用するために適切な選択性および特異性を有するように選択されるべきである。アフィニティー反応物および反応条件の適切な選択についての一般方法ならびに基準は当分野で周知である。
【0066】
固定化アフィニティー反応物(ACS)および溶質(S)を含む複合体の形成についてのアフィニティー定数(KS−−AC=[S][ACS]/[S−−ACS])は、応用を最適化するための重要な基準であって、応用に依存して変わる。アフィニティーアッセイについては、アフィニティー定数は、典型的には≦10−8mole/lもしくは≦10−9mole/lである。この種のアッセイは典型的に、溶質が固定化ACSと流動条件下に反応しそして動物のもしくは生物の試料(動物のもしくは生物の試料は、ヒトおよび他の動物の患者のような、哺乳動物からの、ならびに実験動物からの試料を含む)の中のアナライトの量に関連することを含む。これは、さらに弱いアフィニティーを有するアフィニティー相手がこの種の試料、他の試料およびアフィニティーアッセイ、ならびに他の応用のために使用され得ることを除外しない。かくして、応用に依存して、アフィニティー定数は、10−3mole/lまでもしくは10−4mole/lまでもしくは10−5mole/lまでもしくは10−7mole/lまでのように、比較的大きく、または10−8mole/l以下もしくは10−11mole/l以下のように、比較的小さくあり得る。
【0067】
反応物/リガンドの固定化技法は、当分野で普通に既知である技法の中で選択され得る。かくして、固相物質への結合は、共有結合、アフィニティー結合(例えば、生物特異的アフィニティー結合)、物理的吸着等を介し得る。
【0068】
アフィニティー結合を介する固定化は、その中でメンバー(固定化リガンドもしくはL)の一つが固相物質に、例えば共有結合で、堅固に結合している固定化アフィニティー対(affinity pair)を利用し得る。対の他のメンバー(固定化結合剤、B)は、結合剤Bおよび溶質Sに対するアフィニティー相手ACSを含む結合体(固定化結合体)として使用される。固定化アフィニティー対の例は、a)ストレプトアビジン/アビジン/ニュートラビジンおよびビオチン化反応物(もしくは逆もまた同様)、b)抗体およびハプテン化反応物(もしくは逆もまた同様)、c)IMACグループならびに反応物に連結するかまたはその一部である、ヒスチジルおよび/もしくはシステイニルならびに/またはリン酸エステル化残基を含有するアミノ酸配列(即ちIMACモチーフ)等である。
【0069】
用語“結合体”とは主として、化学結合体および組換え的に製造される結合体のような共有結合性結合体(そこでは両方の部分はペプチド構造を有する)を指す。この用語はまた、所謂天然の結合体、即ち、お互いに離れて間隔を空けて、アフィニティーを二つの異なる分子要素のほうに向ける二つの結合部位を示すアフィニティー反応物、例えば、分子の一つの側(=部分)上に種およびクラス−特異的決定因子をならびにもう一つの側(=部分)上に抗原/ハプテンの結合部位を含む天然の抗体を含む。
【0070】
固定化リガンドLは固定化結合剤Bに対して二つもしくはそれ以上の結合部位を有し、そして/または固定化結合剤BはリガンドLに対して一つ、二つもしくはそれ以上の結合部位を有する(または逆もまた同様)ことは有利であると信じられている。
【0071】
好ましい固定化アフィニティー対(LおよびB)は典型的に、ストレプトアビジンおよびビオチンについての相当するアフィニティー定数にせいぜい同等であるかまたはそれより≦10倍もしくは≦102倍もしくは≦103倍さらに大きいアフィニティー定数(KL−−B=[L][B]/[L−−B])を有する。これは典型的に、それぞれ、ほぼ≦10−13mole/l、≦10−12mole/l、≦10−11mole/lおよび≦10−10mole/lであるアフィニティー定数を意味するであろう。好ましくは、LおよびBを、ビオチン結合化合物およびストレプトアビジン結合化合物の中で、それぞれ選択すること(もしくは逆もまた同様)である。
【0072】
上で議論されたアフィニティー定数とは、Biacore (Uppsala, Sweden)からのバイオセンサー(表面プラスモン共鳴)により、即ち、デキストランで被膜した金の表面に固定化されるアフィニティー反応物(ACSおよびL)で、得られる値を指す。
【0073】
本発明で使用されるべきアフィニティー対、特にバイオアフィニティー対、のメンバーの少なくとも一つは、a)ポリおよびオリゴペプチド構造のようなペプチド構造を含むアミノ酸構造、b)炭水化物構造、c)核酸構造を含むヌクレオチド構造、d)ステロイド構造、トリグリセリド構造等のような脂質構造:の中で選択される構造を典型的に示す。これに関して、用語のアフィニティー対とは、固定化アフィニティー対(LおよびB)、固定化アフィニティー反応物および溶質(ACSおよびS)ならびに使用され得る他のアフィニティー対を指す。
【0074】
乾燥状態にある固相物質は、他に活性化形であり得る。換言すれば、それは、望ましい反応物の官能基との反応による直接の共有結合性固定化への用意ができている。望ましい反応物の上で使用され得る官能基は、求電子性のおよび求核性の基の中で典型的に選択されて、活性化基が、それぞれ、求核性でもしくは求電子性であるかどうかに依存する。使用され得る官能基の例は、アミノ基および置換のもしくは未置換の−NH2、カルボキシ基(−COOH/−COO−)、ヒドロキシ基、チオール基、ケト基等を含む他の基である。
【0075】
微小流体装置の他の特徴
微小流体装置のマイクロチャネル構造(101a〜h)は、実験の全部のプロトコルを構造内で実施することを許容する機能性部分を備える。かくして、微小流体装置のマイクロチャネル構造(101a〜h)は、a)例えば、多分容積計量ユニット(106a〜h、108a〜h)と一緒に、入口/入口孔(105a〜b、107a〜h)を備える入り口装置(102、103a〜h)、b)液体輸送のためのマイクロ導管;c)微小反応空間(104a〜h);d)微小混合空間/ユニット;e)液体から粒子状物質を分離するためのユニット(入り口装置の中に存在し得る)、f)例えば、キャピラリー電気泳動、クロマトグラフィー等により、試料の中で溶解されたかもしくは懸濁された成分をお互いから分離するためのユニット;g)微小検出空間;h)廃液の導管/マイクロキャビティー(112、115a〜h);i)バルブ(109a〜h、110a〜h);j)環境外気への通気口(116a〜i);等:の中で選択される一つ、二つ、三つもしくはそれ以上の機能性部分を備え得る。機能性部分は、二つ以上の機能性を有し得る、例えば、微小反応空間(104a〜h)および微小検出空間が合致し得る。微小流体装置の中のいろいろな種類の機能性ユニットは、Gyros AB/Amersham Pharmacia Biotech AB:WO 99055827、WO 99058245、WO 02074438、WO 02075312、WO 03018198(US 20030044322)、WO 03034598、SE 03026507(SE 04000717、US SN 60/508,508)、SE 03015393(US SN 60/472,924)によりおよびTecan/Gamera Biosciences:WO 01087487、WO 01087486、WO 00079285、WO 00078455、WO 00069560、WO 98007019、WO 98053311により記載されている。
【0076】
有利な形において、親水性の多孔性床を意図する微小反応空間(104a〜h)は、それらのそれぞれが入口(105a〜b、107a〜h)および少なくとも一つの容積計量ユニット(106a〜h、108a〜h)を備える、一つもしくはそれ以上の入り口装置(上流方向)(102、103a〜h)に接続される。一つの有利な変形体において、マイクロチャネル構造(101a〜h)および固相物質を含有することを意図する微小反応空間(104a〜h)当り一つの別個の入り口装置(103a〜h)がある。もう一つの有利な変形体において、入り口装置(102)は、マイクロチャネル構造(101a〜h)および固相物質を含有することを意図する微小反応空間(104a〜h)の全部もしくはサブセット(100)に共通であって、サブセット(100)のそれぞれのマイクロチャネル構造/微小反応空間(101a〜h/104a〜h)について共通の入り口(105a〜b)および一つの容積計量ユニット(106a〜h)を持つ分布マニホールドを備える。
【0077】
両方の変形体において、容積計量ユニット(106a〜h、108a〜h)のそれぞれは順番に、そのマイクロチャネル構造(101a〜h)、例えば微小反応空間(104a〜h)の下流部分と通信(communicate)する。共通の入り口装置(102)および/もしくは共通の分布マニホールドにより一緒に連結されるマイクロチャネル構造は、マイクロチャネル構造のサブセット(100)のグループを規定する。それぞれの容積計量ユニット(106a〜h、108a〜h)は典型的に、その出口末端においてバルブ(109a〜h、110a〜h)を有する。このバルブは、例えば、親水性のおよび疎水性の表面の間の境界(疎水性表面切れ目)のような、出口末端における化学的表面特性(WO 99058245(Amersham Pharmacia Biotech AB))のおよび/もしくは幾何学的な/物理的な表面特性(WO 98007019(Gamera))の変化を利用して、典型的には受動的である。
【0078】
入口、容積計量ユニット、分布マニホールド、バルブ等を持つ典型的な入り口装置は、WO 02074438(Gyros AB)、WO 02075312(Gyros AB)、WO 02075775(Gyros AB)およびWO 02075776(Gyros AB)に提示されている。
【0079】
微小流体装置はまた、異なるマイクロチャネル構造を接続する他の共通のマイクロチャネル/マイクロ導管を備え得る。入口、出口、通気口、等のようなそれらの種々の部分を含む共通のチャネルは、それらが通信しているマイクロチャネル構造のそれぞれの部分と考えられている。
共通のマイクロチャネルは、その中でマイクロチャネル構造がネットワークを形成する微小流体装置を解釈することを可能にする。例えば、US 6,479,299(Caliper)を参照されたい。
【0080】
それぞれのマイクロチャネル構造は、液体用の少なくとも一つの入口孔(105a〜b、107a〜h)および過剰の空気用(通気口)(116a〜i)のおよび多分また液体用(廃液チャネル(112)の中の円)の少なくとも一つの出口孔を有する。
微小流体装置はまた、本発明にしたがって固相物質を保持するための微小反応空間を何も有しないマイクロチャネル構造を備え得る。
【0081】
微小流体装置は、本発明にしたがって固相を含有することを意図する複数のマイクロチャネル構造/装置を含有する。これに関して、複数とは、二つ、三つもしくはそれ以上のマイクロチャネル構造を意味して、典型的には≧10、例えば≧25もしくは≧90もしくは≧180もしくは≧270もしくは≧360である。上で議論されたように、装置のマイクロチャネル構造は、グループもしくはサブセット(100)に分割され得て、それらのそれぞれは、例えば、微小反応空間のサイズおよび/もしくは形により、マニホールド、共通の廃液チャネル(112)等を持つ共通の入り口装置(102)のような、共通のマイクロチャネル(102、112)により規定され得る。グループもしくはサブセットの中のマイクロチャネル構造の数は、典型的に、装置のマイクロチャネル構造の総数の1〜99%の範囲にあり、例えば5〜50%もしくは5〜25%もしくは10〜50%の範囲にある。これは典型的に、それぞれのグループが3〜15もしくは3〜25もしくは3〜50個のマイクロチャネル構造を典型的に備えることを意味する。それぞれのグループは、装置の特定な区域に位置し得る。
【0082】
異なる原理が、上述の機能性部分の二つもしくはそれ以上の間で微小流体装置/マイクロチャネル構造内で液体を輸送するために利用され得る。慣性力を、例えば、次の段落で議論されるようにディスクを回転させることにより、使用し得る。他の有用な力は、毛管力、動電力、毛管力、静水圧のような非動電力等である。
【0083】
微小流体装置は典型的にはディスクの形である。好ましい形式は、ディスク平面に直角であるかもしくはそれと合致する対称軸(Cn)[そこでは、nは≧2、3、4もしくは5の整数、好ましくは∞(C∞)である]を有する。換言すれば、ディスクは、正方形のような方形、および他の多角形の形であり得るが、好ましくは円形である。一旦適切なディスク形式が選択されてくると、液流を駆動させるために遠心力を使用し得る。典型的にはディスク平面に直角であるかもしくは平行である回転軸の周りに装置を回転することは、必要な遠心力を創造し得る。優先日での大抵の明白な変形体において、回転軸は上述の対称軸と合致する。
【0084】
好ましい遠心力ベースの変形体については、それぞれのマイクロチャネル構造は、下流セクション(回転軸から)よりさらに短いラジアル距離にある一つの上流セクションを含む。多孔性床を意図する微小反応空間は、典型的に二つのセクションに中間のラジアル位置にある。
【0085】
もし遠心力が粒子床の形成および/もしくは再構成のためにならびに/または床を通して液流を駆動するために使用されるならば、微小反応空間は、流れの方向を回転軸から放射状に外側に合わせて典型的に配置される。
【0086】
好ましい装置は、典型的に、従来のCD−形式と同様なサイズおよび/もしくは形、例えば、従来のCD−半径(12cm)を持つ円形ディスクの10%から300%までの範囲にあるサイズを持つディスク形である。ディスクの上方のおよび/もしくは下方の側は、平面であり得るかもしくはあり得ない。
【0087】
微小流体装置のマイクロチャネル/マイクロキャビティーは、次の工程でもう一つの本質的に平面な基板(蓋)により覆われる蓋のない形のチャネル/キャビティを示す、本質的に平面な基板表面から製造され得る。WO 91016966(Pharmacia Biotech AB)およびWO 01054810(Gyros AB)を参照されたい。両方の基板は、好ましくは、プラスティック物質、例えばプラスティックポリマー物質から製造される。
内部表面の付着活性および親水性は、応用に関して均衡させるべきである。例えば、WO 01047637(Gyros AB)を参照されたい。
【0088】
用語“湿潤性の(親水性の)”および“非−湿潤性の(疎水性の)”とは、表面が、それぞれ、≦90°もしくは≧90°の水接触角を有することを意図する。異なる機能性部分の間で液体の効率的な輸送を容易にするためには、個別の部分の内部表面は本来湿潤性であるべきであり、好ましくは≦60°、例えば≦50°もしくは≦40°もしくは≦30°もしくは≦20°の水接触角を有する。これらの湿潤性値はマイクロ導管の少なくとも一つ、二つ、三つもしくは四つの内壁に当てはまる。一つもしくはそれ以上の内壁がさらに高い水接触角を有する場合には、これは、内壁(複数を含む)に対するさらに低い水接触角により補償され得る。特に入り口装置の中の湿潤性は、一旦液体がキャビティに入り始めたならば、水性液体が毛管現象(自己吸引)により意図するマイクロキャビティーを満たすことが可能であるように、適応されるべきである。マイクロチャネル構造の中の親水性の内部表面は、例えば、受動性バルブ(passive valve)、抗−吸上げ手段(anti-wicking means)、環境大気等への通気口として単に機能する通気口(図1の方形)を導入するために、親水性の内壁の中で一つもしくはそれ以上の局部的な疎水性表面切れ目を含み得る。例えば、WO 99058245(Gyros AB)およびWO 02074438(Gyros AB)を参照されたい。
【0089】
接触角とは、使用温度、典型的には+25℃、での値を指して、静的でありそしてWO 00056808(Gyros AB)およびWO 01047637(Gyros AB)に例示される方法により測定されることができる。
【0090】
第二の態様:複数の濡れた多孔性床の、場合により複数の濡れた多孔性床へ再構成される乾燥/脱水状態への変換のための方法
この態様は、この章の見出しに規定されるような方法である。この方法は、
i)そのそれぞれが床の保存剤を含有する液体で飽和された親水性の多孔性床を含有する微小反応空間(104a〜h)を備える複数のマイクロチャネル構造(101)を備える微小流体装置を提供すること、
ii)それぞれの微小反応空間(104a〜h)の中の床を、微小反応空間の中に保持されながら、乾燥および/もしくは脱水状態にある固相物質へ変換すること、
iii)場合により、それぞれの微小反応空間(104a〜h)の中で、工程ii)で得られた固相物質を濡れた多孔性床に再構成すること:
の工程から成ることを特徴とする。
この態様はまた、再構成された多孔性床の性能に関して微小流体装置の中のチャネル間の変動を減少させるための方法に関係する。
【0091】
固相物質は、次に導入される液体アリコートの中の溶質と相互作用し得る反応物を示しても示さなくてもよい。種々の特性が下におよび本明細書中の他の所で議論されている。
工程(iii)は、例えば、好ましくは本発明の第三態様について議論されるような、床を通る滞留時間および流速を持つ流動条件下に行われる。
【0092】
多孔性の粒子床は、粒子の分散液を微小流体装置の微小反応空間(104a〜h)の全てのまたは一つもしくはそれ以上のサブセット(100)を通して流動させることにより創造されることができる。次いで、粒子が沈降して、それぞれのマイクロキャビティー(104a〜h)の出口末端(111a〜h)に多孔性床を形成する。床の形成は、重力の使用および/もしくは遠心力の使用により容易になり得て、後者が好ましくはそれぞれの微小反応空間(104a〜h)の流動方向に沿って作用する。上で議論されたような望ましい添加剤は、液体の分散液の中に存在するかおよび/もしくは形成された後に床に添加剤を含有する液体を通過させることにより導入される。添加剤を含有する液体で飽和した床と一緒に微小流体装置は、乾燥状態への変換まで保存される。
【0093】
多孔性のモノリスの床は、典型的に、装置の製造の間に、例えば、
a)重合により、もしくは
b)既製の多孔性のモノリスを置くことにより、
微小流体装置の微小反応空間(104a〜h)の少なくとも一つのサブセット(100)のそれぞれの中に導入される。
【0094】
選択肢のa)においては、好ましい変形体は、微小反応空間(104a〜h)および相当するマイクロチャネル構造(101a〜h)と共に重合を密閉形で行うことである。選択肢のb)においては、好ましい変形体は、少なくとも微小反応空間(104a〜h)は覆われない(そしてマイクロチャネル構造(101a〜h)の残りの部分は覆われれる)一方で、モノリスを挿入することである。多孔性床の導入および、必要であれば、マイクロキャビティーの密閉の後に、床を上で議論された保存剤を含む溶液で飽和して、乾燥状態への変換まで保存する。
【0095】
床の乾燥状態への変換は、減圧下に、例えば、床が飽和されている液体の凝固点以下でおよび/もしくは以上で、液体を除去することにより達成され得る。減圧下におよび凝固点以下での除去は典型的に凍結乾燥を意味する。これに代えて、液体は沈降した分散液から大気圧下に加温して又はしないで除去される。
装置が液体の輸送を遠心力により駆動するためにデザインされている場合には、所謂回転−乾燥を使用し得る。実験の部の図1の説明を参照されたい。
【0096】
微小反応空間の周りの壁の間の小さい寸法および内部エッジに因り、吸上げは、特に大気圧での、乾燥/脱水/蒸発において重要な因子であるであろう。
濡れた多孔性床の再構成とは、再構成液体が、乾燥状態の固相物質を含有する微小反応空間のそれぞれを通って流れることができることを意味する。実験の部を参照されたい。
【0097】
数個の構造の中で固相物質を均等におよび/もしくは平行して処理するための重要な道具は、それぞれのマイクロチャネル構造(101a〜h)に、第一の態様で議論されたように、好ましい変形体においてマイクロチャネル構造/微小反応空間(101a〜h/104a〜h)のグループ/サブセット(100)に共通(102)である入り口装置(102/103a〜h)を提供することである。かくして、この種のデザインは、固相物質の平行的な分配ならびに多孔性床の平行的な再構成およびコンディショニングを容易にするであろう。それにより、本発明の最良の利益を達成するためには、少なくとも入り口装置(102、103a〜h)、分布マニホールド、および/もしくは個別の容積計量ユニット(106a〜h、108a〜h)に本明細書中の他の所で議論された制限内で親水性の表面特性を、ならびにそれぞれの容積計量ユニット(106a〜h、108a〜h)の出口に、好ましくは、例えば局所的な疎水性表面切れ目の形で、受動的(可動部分を持たないという意味)であるバルブ機能(109a〜h、110a〜h)を提供することが重要である。
【0098】
本発明の第三の態様:装置の使用
革新的な微小流体装置の使用は、大まかに言えば、
(i)本発明の第一の態様にしたがって微小流体装置を提供すること;
(ii)予め決められた数のマイクロチャネル構造/微小反応空間(101a〜h/104a〜h)の中で、好ましくは流動条件下に、乾燥状態にある固相物質を濡れた多孔性床へ再構成すること、
(iii)濡れた多孔性床を含有する一つもしくはそれ以上のマイクロチャネル構造(101a〜h)の中で当該濡れた多孔性床の上流にある位置で溶質(S')を含有する液体を提供すること、
(vi)液体を当該一つもしくはそれ以上のマイクロチャネル構造(101a〜h)の少なくとも一つの中の当該濡れた床を通して輸送すること:
の工程から成っている。
【0099】
工程(i)および(ii)
これらの工程は、本発明の第一および第二の態様にしたがっている。
【0100】
工程(iii)および(iv)
溶質(S')は、典型的に濡れた多孔性床と相互作用する能力がある。
工程(iii)は、溶質(S')が装置/マイクロチャネル構造内で形成されるかもしくはマイクロチャネル構造に分配されることを含む。適用可能であれば、形成は、典型的に、濡れた多孔性床/微小反応空間(104a〜h)の上流位置でもしくはその内である。分配は、典型的には多孔性床/微小反応空間(104a〜h)の上流位置で入口(105a〜b、107a〜h)へである。
【0101】
工程(iii)および(iv)は、溶質(S')および多孔性床の間の相互作用が起こることを許容するために実施される。導入部で言及されたように、工程は、(a)分離方法、および/もしくは(b)触媒反応、(c)固相合成、ならびに/または(d)固相物質/多孔性床の誘導体化の一部であり得る。
【0102】
分離は他の中で、
i)捕獲、即ち、多孔性床は、溶質(S')に対する結合能力を持つアフィニティー構造(アフィニティーリガンド、アフィニティー反応物)(AC'S')を示す。溶質(S')を含有する液体が床を通過するときには、次いで、溶質(S')はAC'S'を介して多孔性床に捕獲され/結合されるであろう。多孔性床を通る通過後に、液体は、溶質(S')を欠如するかもしくは低減した量を有するであろう。AC'S'およびS'は、上で議論されたACSおよびSにそれぞれ相当するであろう。
ii)サイズ排除、即ち、多孔性床はさらに大きい分子に比較してさらに小さい分子を保持する傾向がさらに多くある。溶質(S')は、液の先端の移動に比して遅延して、それ故に濡れた多孔性床の中では初めは富化されるであろう。
iii)電気泳動、即ち、多孔性床は、抗−対流および/もしくは抗−拡散の手段として機能する。:
を含む。
多くの分離プロトコルについて、二つもしくはそれ以上の捕獲、サイズ排除、電気泳動等の組合せが連続した床の中でもしくは同一の床の中でのいずれかで利用される。
【0103】
分離は、液体の中に存在する溶質についての精製もしくは富化のプロトコルの部分であり得る。液体から分離される溶質は、精製されるべき、富化されるべき等の汚染物質もしくは要素であり得る。分離は、合成プロトコル、調製プロトコル、細胞ベースのアッセイ、核酸アッセイ、免疫アッセイ、酵素アッセイ等を含むいろいろな種類のアフィニティーアッセイの一部であり得る。
【0104】
溶質を固相物質に結合するために捕獲工程を利用するアフィニティーアッセイは典型的に、アッセイのアフィニティー反応に関与する反応変数の特色化を意図する。この文脈において反応変数は主として二つの型:1)アフィニティー反応物に関連した変数、および2)反応条件、を持つ。1型の変数は、二つの主なサブグループ、a)存在および/もしくは不存在を含む量、濃度、相対的な量、結合活性および酵素活性、等のような活性、ならびにb)例えばアフィニティー定数、特異性等のアフィニティーそれ自体を含むアフィニティー反応物の性質、を含む。WO 02075312(Gyros AB)を参照されたい。それについて1型の反応変数が特色化される分子要素はアナライトと呼ばれる。
【0105】
本発明の文脈における触媒反応は、固相物質が、利用される触媒系の一つもしくはそれ以上の固定化メンバー(例えば、アフィニティー構造、アフィニティーリガンド、アフィニティー反応物)を示す一方で、同一の系の他のメンバーは溶質であることを含む。触媒反応は、固定化メンバー(アフィニティー構造、アフィニティーリガンド、アフィニティー反応物)および少なくとも一つの溶質メンバーの間のアフィニティー複合体の形成を含む。少なくとも一つのメンバーは、触媒系のための基質に相当する。反応は、基質に比較して異なる化学組成および/もしくは構造を典型的に有する生成物をもたらす。生成物は、反応の間に床に固定化されてもされなくてもよい。
【0106】
用語“触媒系”は、単一の触媒系および一連の連結した単一の酵素系、細胞全体、酵素活性を示す細胞部分等を含むさらに複雑な変形体を含む。床は、酵素反応器のような、触媒反応器として機能し得る。
【0107】
その間に溶質との相互作用が起こる工程は、触媒系もしくは他の反応変数(例えば、反応条件)の一つもしくはそれ以上のメンバーを特色化するための、酵素アッセイのような、触媒アッセイの部分であり得る。アッセイは、液体試料の中の特定の触媒、基質、補基質、補因子、共触媒等の活性を測定するためであり得る。測定されるべき活性に相当する分子要素/複数の要素はアナライト/複数のアナライトと呼ばれる。例えば、WO 03093802(Gyros AB)を参照されたい。
【0108】
アッセイの文脈において、用語のアナライトは、元の試料の中で特色化されるべき要素ならびにアッセイの間に形成されて元の試料の中のアナライトに定量的に関連しているアナライト由来の要素を含む。上で議論された溶質は、元のアナライトもしくはアナライト由来の要素であり得る。
【0109】
固相合成は、例えば、オリゴペプチドおよびオリゴヌクレオチド合成のような、ポリマー合成ならびに固相物質上の他の小分子の合成を含む。ポリマー合成で用いられる固定化反応物は、例えば、ヌクレオチド、炭水化物のような相当する単量体の構造、アミノ酸構造、およびこれらの構造のミメティックを示し得る。コンビナトリアルライブラリーの固定化メンバーのライブラリーの合成がまた含まれる。そのようなメンバーは、比較的低い分子量(例えば、ポリマーバックボーンへの可能なスペーサーを含んで<10,000ダルトン)を有する。
【0110】
本発明の文脈において固相誘導体化は大抵の場合に、濡れた多孔性床の上に固定化反応物もしくは活性化された官能基を導入することを目標として有する。かくして、固相誘導体化は、共有結合を介してもしくはアフィニティー/吸着結合を介して望ましい反応物の固定化を許容する反応性の構造もしくは基の導入を含む。かくして、固定化リガンドLを露出する濡れた多孔性床から出発して、そして固定化結合体(B−R=S';Bは固定化アフィニティー結合剤Bであって、Rは固定化されるべき反応物Rである)を含有する液体を通過させて、反応物Rは、Lについて上で議論されたような多孔性床および固定化結合体B−ACSの上に堅固に結合しかつ露出されるであろう。もしRが溶質Sに対するアフィニティー相手ACS(B−R=B−ACS)であるならば、生じた多孔性床を、溶質Sを含有する液体から溶質Sを捕獲する/分離するために上で議論されたように使用することができる。
【0111】
工程(iv)の間の輸送は、液体が多孔性床を通って連続的に流れていることもしくは液体が床内にあるときには、液体の輸送が停止されることを含む。床の上に固定化された反応物および溶質の間の相互作用は、かくして、流動条件下にもしくは静的な条件下に、それぞれ、起こることができる。我々は、もしこの種の反応が流動条件下に起こっているならば、アフィニティー反応の中の反応変数に関してさらに多くの情報が得られ得ることを以前に見出した(WO 02075312(Gyros AB))。流速および/もしくは滞留時間は、例えば、固相に固定化されたアフィニティー相手ACSに結合されるように成っている溶質(S)の量が、拡散による最少の摂動(非拡散制限条件)をもって、固定化アフィニティー反応物、典型的にはACS、および溶質、典型的には溶質S、の間の実際の反応速度もしくはアフィニティーを反映するように調整され得る。
【0112】
これはまた本発明に当てはまるが、主な興味が結合される/捕獲される溶質の全量である応用については、拡散制限のもしくは非拡散制限の条件のいずれかを利用する流動条件の下で捕獲することが使用され得ることを除外しない。かくして、多孔性床を通る適切な流速は、多数の因子、例えば、固定化反応物および溶質ならびにそれらのサイズ、微小反応空間の容積、固相物質を含む多孔性床等、に依存する。典型的には、流速は、典型的に、1時間以下のように2時間以下である上限をもって、≧0.050秒もしくは≧0.1秒のように≧0.010秒の滞留時間を与えるべきである。例示的な流速は、0.01〜100nl/秒およびさらに典型的には0.1〜10nl/秒のように、0.01〜1000nl/秒以内にある。これらの流速の範囲は、1〜50nlもしくは1〜25nlのように、1〜200nlの範囲の床容積に有用であり得る。滞留時間とは、液体アリコートが微小反応空間の中で固相/多孔性床と接触するためにそれがかかる時間を指す。これらの範囲は、分離、触媒アッセイ、固相合成、固相誘導体化等を含む革新的な微小流体装置の他の使用にまた適用可能である。
【0113】
最良の形態
本出願の提出における本発明の最良の形態は、実験の部に与えられて、トレハロースを床の保存剤として、リン酸カリウムをさらに別の添加剤(緩衝剤)として示される固相物質を包含し、そしてマイクロチャネル構造を持つ微小流体装置を図1に示す。
【0114】
実験の部
実験に使用される微小流体装置は円形であって、従来のCD(コンパクトディスク)と同一の寸法を持っていた。この微小流体装置はさらに続けてCDと呼ばれるであろう。CDは、周辺部の近くにそれぞれのグループについて共通の廃液チャネル(112)を持つディスクの中心(回転軸)の周りの環状ゾーンに配置される8個のマイクロチャネル構造(101a〜h)の14個のグループ(100)を含有した。8個のマイクロチャネル構造(101a〜h)のグループ(100)は図1に示されていて、そしてWO 02075312(Gyros AB)の図1〜2ならびにWO 03024548(US 20030054563)(Gyros AB)およびWO 03024598(US 20030053934)(Gyros AB)の相当する図に図示されているマイクロチャネル構造のグループに似ていて、それと同一な様式で機能する。寸法は、これらの先の特許出願にあるのと同一のサイズを本質的に持つ。
【0115】
それぞれのサブセット(100)は、一つの共通の入り口装置(102)、マイクロチャネル構造当り一つの別個の入り口装置(103a〜h)およびマイクロチャネル構造当り一つの微小反応空間(104a〜h)を持つ8つのマイクロチャネル構造(101a〜h)を備える。共通の入り口装置は、それぞれのマイクロチャネル構造(101a〜h)についてa)過剰の液体の出口としてまた機能するであろう二つの共通の入口(105a〜b)、およびb)一つの容積計量ユニット(106a〜h)を備える。容積計量ユニット(106a〜h)は、マイクロチャネル構造の下流部分のための分布マニホールドとして機能するであろう。別個の入り口装置(103a〜h)のそれぞれは、唯一つのマイクロチャネル構造の部分であって、入口(107a〜h)および容積計量ユニット(108a〜h)を備える。それぞれの容積計量ユニット(106a〜h、108a〜h)およびそれらの下流部分の間には、それぞれ、好ましくは受動的な、バルブ機能(109a〜h、110a〜h)がある。マイクロチャネル構造(101a〜h)の微小反応空間(104a〜h)は、マイクロチャネル構造(101a〜h)の共通の入り口装置(102)および別個の入り口装置(103a〜h)の両方の下流に位置する。
【0116】
それぞれの微小反応空間の出口末端(111a〜h)においては、深度は二つの工程で100μmから10μmに下げられて、粒子が微小反応空間から漏れることを防止する。それぞれの微小反応空間(104a〜h)は、図1で外側の曲がりとして図示される出口マイクロ導管(113a〜h)に接続される下流方向にあり、そして廃液機能(115a〜h)に接続される出口末端(114a〜h)を有する。周辺において、共通の廃液チャネル(112)がある。バルブ(109a〜h、疎水性切れ目)と一緒に通気口(116a〜i、疎水性切れ目)は、それぞれの容積計量ユニット(106a〜h)から下流に分布されるべき液体アリコートの容積を規定する。
【0117】
適切な量の水性液体を入り口装置の入口に入れることにより、毛管現象が入口に接続される容積計量ユニット(複数を含む)を液体で満たすであろう。ディスクをその中心の周りに回転することにより、液体を容積計量ユニットおよび下流部分の間のバルブ(109a〜h、110a〜h)に強制的に通過させることができる。
【0118】
もし微小反応空間(104a〜h)が出口マイクロ導管(113)の出口末端(114)より回転軸からさらに短いラジアル距離に置かれるならば、濡れた充填床の回転−乾燥を使用することができる。これは、出口マイクロ導管(113)の形に依存しない。
【実施例】
【0119】
実験
計器装備
免疫アッセイは自動化システムの中で実施される。システム(レーザー誘起蛍光(LIF)モジュールを備えるGyrolabワークステーション2型試作機、Gyros AB, Uppsala, Sweden)を、CD−スピナー、マイクロタイタープレート(MTP)用の保持器および5個のシリンジポンプ、2および2、に接続される10個の毛管用の保持器を持つロボットのアームを備えた。毛管の二つは、全ての試薬および緩衝液をMTPからCDの中の二つの共通の入口(105a〜b)のいずれかへ移送した。他の8つの毛管は、個別の試料をMTPからCDの中の別個の個別の入口(107a〜h)へ移送した。
【0120】
Gyrolabワークステーションは、応用特異的ソフトウエアにより制御される完全に自動化されたロボットシステムである。ソフトウエア内の応用特異的方法は、CDの回転を正確に制御された速度で制御して、それによりマイクロ構造を通る液体の移動を、応用が進行するにつれて、制御する。特別なソフトウエアがバックグラウンドノイズを減少するために含まれた。
【0121】
WO 02075312(Gyros AB)、WO 03025548およびUS 20030054563(Gyros AB)、WO 03025585およびUS 200030055576(Gyros AB)、WO 03056517およびUS 200301156763(Gyros AB)ならびにまたwww.gyros.com.をまた参照されたい。
【0122】
固相、ストレプトアビジンの固定化、充填、乾燥/脱水および再構成
微小流体装置のマイクロ構造の中に充填される固相ビーズ物質は、多孔性もしくは固体の性質の何れであってもよい。例えば、ポリスチレン(PS)粒子(15μm、Dynal Biotech, Oslo, Norway)が固相のために選択された。ビーズをフェニル−デキストラン(PheDex)の受動的吸着により修飾して、親水性表面を作製し、そして引き続いてストレプトアビジン(Immunopure Streptavidin、Pierce, Perbio Science UK Limited, Cheshire, United Kingdom)と、CDAP化学(Kohn & Wilchek, Biochem. Biophys. Res. Commun. 107 (1982), 878-884)を用いて共有結合させた。SuperdexペプチドおよびSepharoseHP(Amersham Biosciences, Uppsala, Sweden)のような他の粒子はまた、ストレプトアビジンとCDAP化学(フェニル−デキストランの被膜無しで)を用いて共有結合している。ストレプトアビジン−ビオチンは周知のバイオアフィニティー対である。ポリスチレン粒子は固体であって使用される再構成液体の中では膨潤可能でない。SuperdexペプチドおよびSepharoseHPは多くのアフィニティー反応物に対して多孔性であって、使用される再構成液体の中で膨潤可能である。
【0123】
ストレプトアビジンとの結合後で、床の保存剤と共に(この場合には砂糖添加剤(10〜100mM))もしくは床の保存剤なしで、リン酸カリウム緩衝液(10mM)中の粒子の懸濁液を、入口(105a〜b)を介して共通の分布チャネルの中に分布して、遠心力により構造を通って移動させた。通気口(109a〜h、113a〜i)と組合せた遠心力は、懸濁液を共通の入り口装置(102)の中に同じ分量で分割して、それらのそれぞれは、それぞれの微小反応空間(104a〜h)の出口末端(111a〜h)における二相の深度(111a〜h)に対してそれぞれの微小反応空間(104a〜h)の中で充填された粒子の床(カラム)を形成する。カラムの凡その容積は15nlであった。カラム/床は三つの異なる方法により乾燥され/脱水された:
吸い上げの助けによる大気圧での乾燥:濡れた多孔性床を含有する微小流体装置を6000rpmで一分間回転して、可能なかぎりの液体を除去した後に、装置を宝石箱の中に入れて、ポリマーで被膜したアルミニウムのバッグの中に封入した。
真空乾燥:濡れた多孔性床を含有する微小流体装置をトレーの上に置いて、真空乾燥オーブン(Heraeus vacutherm VT6060M)の中に入れた。温度を25℃にセットして、真空により圧力を0.1ミリバールに減圧した。装置をこの圧力および温度で、生成物が乾燥するまで、半時間保持した。次いで、圧力を大気圧に到達させた。次いで、装置を宝石箱の中に入れて、ポリマーで被膜したアルミニウムのバッグの中に封入した。
凍結での乾燥(凍結乾燥):濡れた多孔性床を含有する微小流体装置をトレーの上に置いて、−80℃のフリーザーの中に入れた(装置をまた普通の−20℃のフリーザーの中に一時間置いてもよい)。2、3分後に装置の中の全てのカラムが冷凍されて、コンデンサーの温度が−57℃にセットされている凍結乾燥装置(Heto, LyoPro 3000)に、トレーを移した。圧力を0.1〜0.06ミリバールに(真空により)減圧した。装置をこの圧力および温度で、全ての氷が昇華してしまうまで(約12時間もしくは終夜)、保持した。次いで、圧力を2分間の間で大気圧に到達させた後に、チャンバーを開けて、凍結乾燥された生成物が装置の中に提供された。装置を宝石箱の中に入れて、ポリマーで被膜したアルミニウムのバッグの中に封入した。
【0124】
装置を+4℃で一ヶ月保管し、その後で、乾燥カラムを、0.15M NaCl、0.02% NaN3および0.01% Tween[登録商標]20を含有する15mM リン酸緩衝液(PBS)、pH7.4で、共通の分布チャネルを介しそして適切な速度で回転して、一回再湿潤し/再構成した。溶液のそれぞれの添加は200nlの液体を個別のカラム(104a〜h)に配達する。最後に、再構成された床の機能を四つの異なるアナライト(ミオグロビン)の濃度で下に示す免疫アッセイで試験して、乾燥/脱水されていない、相当する床と比較した。結果は図4〜5に提示されて、乾燥/脱水された固相物質を有効な濡れた多孔性床へ再構成するためには床の保存剤を含むことが多少とも必須であることを示している。
【0125】
免疫アッセイ
我々のミオグロビンアッセイの捕獲抗体(=ACS)、モノクローナル抗−ミオグロビン8E11.1(LabAS, Tartu, Estonia)をSulfo−NHS−LC−ビオチン(Pierce, prod # 21335, Perbio Science UK Limited, Cheshire, United Kingdom)を用いてビオチン化した。モノクローナル抗ミオグロビン8E11.1のタンパク質濃度は1〜10mg/mlであって、そしてそれを0.15M NaClを添加した15mMのPBS中でビオチン化試薬の3倍モル過剰と室温で1時間インキュベートした後、それをNAP−5カラム(Amersham Biosciences, Uppsala, Sweden)もしくはタンパク質脱塩スピンカラム(Protein Desalting Spin Column)(Pierce, # 89849-P, Perbio Science UK Limited, Cheshire, United Kingdom)のいずれかを通してゲルろ過した。
【0126】
ビオチン化抗体を持つストレプトアビジンで固定化した粒子を装填するために、抗体の0.2〜2mg/mlの濃度(どれだけのストレプトアビジンが充填されたカラムにあるかに依存して)での溶液を、入口(105a〜b)を介して共通の分布チャネルの中に分布して、遠心力により構造を通して移動した。カラムを通る流速を回転速度により制御した(回転流動1)。捕獲抗体がカラムに結合した後に、それらを、共通の分布チャネル(入口105aもしくはb)へのPBS(0.01%のTween20を添加した)の添加により一回洗浄して、引き続いて回転工程を行った。
【0127】
Gyrolabワークステーションの中でミオグロビンアッセイを実演するために、6点の標準曲線を創造した(図6)。0〜274nMの範囲の濃度を持つミオグロビンの試料(1%BSA添加のPBS中に希釈した)を個別の入口(107a〜h)に毛管により分布した。回転流動方法の最初の二工程の間、試料容積200nlを、容積計量ユニット(108a〜h)に規定した。捕獲工程(ミオグロビンを8E11.1に結合する)の下で好適な速度論的条件に到達するためには、試料の流速は1nl/秒を超えるべきでない。試料の流速を回転流動2により制御した。試料の捕獲後に、カラムを、共通の分布チャネル(入口105aもしくはb)へのPBS(0.01%のTween20を添加した)の添加により二回洗浄して、引き続いて回転工程を行った。過剰の検出抗体(モノクローナル抗ミオグロビン2F9.1(LabAs, Tartu, Estonia))を共通の分布チャネル(入口105aもしくはb)を介して次に加えて、同様の遅い流速(回転流動3)を用いた。検出抗体を蛍光体Alexa 633 (Molecular Probes, Eugene, USA)で標識した。過剰の標識抗体を、共通の分布チャネル(入口105aもしくはb)へのPBS(0.01%のTween20を添加した)の4回の添加により洗い流して、引き続いて回転工程を行った。
【0128】
完全なアッセイをレーザー誘起蛍光(LIF)検出モジュールの中で分析した。WO 02075312(Gyros AB)、WO 03025548およびUS 20030054563(Gyros AB)、ならびにWO 03056517および10/331,399(Gyros AB)をさらに参照されたい。
【0129】
システムの中で実施される運転方法の概観は表1に提示されている。
【0130】
【表1】

【0131】
本発明の特定の革新的な態様は、添付の請求の範囲にさらに詳細に規定されている。本発明およびその有利性は詳細に記述されているけれども、添付の請求の範囲に規定されているような本発明の精神および範囲から逸脱すること無しに、種々の変化、置換および変更が、ここでなされ得ることを理解するべきである。さらに、本出願の範囲は、本明細書中で記載されている加工法、機械、製造、物質の成分、手段、方法および工程の特定の実施態様に限定されることを意図していない。当業者によって本発明の開示から容易に認識されるため、本明細書中で記載されている相当する実施態様と実質的に同一の機能を実施するかもしくは実質的に同一の結果を達成する、現存するかまたは後で開発されるであろう加工法、機械、製造、物質の組成、手段、方法もしくは工程は、本発明にしたがって利用され得る。したがって、添付の請求の範囲は、そのような加工法、機械、製造、物質の組成、手段、方法もしくは工程をそれらの範囲内に含むことを意図する。
【特許請求の範囲】
【請求項1】
複数の濡れた多孔性ビーズを乾燥/脱水状態へ変換する方法であって、当該乾燥/脱水状態が所望により複数の濡れた多孔性ビーズに再構成され、当該方法が、
i) 複数のマイクロチャネル構造(101a〜h)を備える微小流体装置であって、該マイクロチャネル構造がそれぞれ、床の保存活性を有する一つもしくはそれ以上の化合物を含む床の保存剤を含む液体で飽和された親水性の多孔性床を含む微小反応空間(104a〜h)を含む、微小流体装置を提供すること;
ii) それぞれの微小反応空間(104a〜h)中の床を、微小反応空間中に保持しながら、乾燥および/または脱水状態である固相物質に変換すること;
iii) 所望により、それぞれの微小反応空間(104a〜h)中で、工程ii)で得られた固相物質を、濡れた多孔性床に再構成すること;
の工程を含むことを特徴とする、方法。
【請求項2】
工程(iii)が、流動条件下で行われる、請求項1に記載された方法。
【請求項3】
当該一つもしくはそれ以上の化合物の少なくとも一つがa)非イオン性であってもなくてもよい親水性基を示し、そしてb)水溶性であることを特徴とする、請求項1または2に記載された方法。
【請求項4】
当該一つもしくはそれ以上の化合物の少なくとも一つが、ポリオールであることを特徴とする、請求項1〜3のいずれか1項に記載された方法。
【請求項5】
当該一つもしくはそれ以上の化合物の少なくとも一つが、炭水化物構造、例えば多糖類構造もしくはオリゴ糖類構造を示すことを特徴とする、請求項1〜4のいずれか1項に記載された方法。
【請求項6】
当該一つもしくはそれ以上の化合物の少なくとも一つが、二糖類、好ましくはトレハロースであることを特徴とする、請求項1〜5のいずれか1項に記載された方法。
【請求項7】
当該化合物の少なくとも一つがマイクロキャビティーの密着剤であることを特徴とする、請求項1〜6のいずれか1項に記載された方法。
【請求項8】
当該液体が、非揮発性の緩衝剤、例えばカリウムイオンを対イオンとして含んでよいリン酸塩緩衝剤、を含むことを特徴とする、請求項1〜7のいずれか1項に記載された方法。
【請求項9】
当該乾燥状態への変換が、水性液体で飽和されている多孔性床から減圧下で、例えば、液体の凝固点以上でもしくは以下で、または水で飽和されている多孔性床を環境大気圧で加温して又はしないで乾燥することにより達成されることを特徴とする、請求項1〜8のいずれか1項に記載された方法。
【請求項10】
a)当該固相物質が多孔性のもしくは非多孔性の粒子の形態であり、そして
b)多孔性床がこれらの粒子の充填床である
ことを特徴とする、請求項1〜9のいずれか1項に記載された方法。
【請求項11】
当該固相物質が膨潤可能であるかもしくは膨潤可能でないことを特徴とする、請求項1〜10のいずれか1項に記載された方法。
【請求項12】
それぞれのマイクロチャネル構造(101)がその構造の少なくとも一部を通って遠心力により液流を駆動させるために設計されていることを特徴とする、請求項1〜11のいずれか1項に記載された方法。
【請求項13】
固相物質が固定化反応物、典型的には溶質Sをアフィニティー捕獲するためのアフィニティー反応物ACSを含むことを特徴とする、請求項1〜12のいずれか1項に記載された方法。
【請求項14】
固定化反応物がLおよびLに対するアフィニティー相手Bを含む固定化アフィニティー対のメンバーである、そしてACSが溶質Sに対するアフィニティー相手である、多孔性床への結合体B−ACSの固定化を意図する、固定化リガンドLであることを特徴とする、請求項13に記載された方法。
【請求項15】
溶質(S)および溶質に対するアフィニティー相手(ACS)の間の複合体(S−−AC)の形成についてのアフィニティー定数(KS−−AC)、即ち(KS−−AC)=[S][ACS]/[S−−ACS]が最大10−6mole/lであることを特徴とする、請求項14に記載された方法。
【請求項16】
固定化アフィニティー対のアフィニティー定数、即ちKL'−−B'=[L'][B']/[L'−−B']が、ストレプトアビジンおよびビオチンについての相当するアフィニティー定数より最大103倍大きいことを特徴とし、好ましくは、アフィニティー対のL'およびB'がそれぞれビオチン結合化合物およびストレプトアビジン結合化合物から選択される(もしくは逆)、請求項15に記載された方法。
【請求項17】
BがLに対して一つもしくはそれ以上の結合部位を有して、そしてLがBに対して二つもしくはそれ以上の結合部位を有するか、または逆であることを特徴とする、請求項16に記載された方法。
【請求項18】
少なくとも一つのSおよびACSならびに/または少なくとも一つのL、B、ACSおよびSが、ポリ/オリゴ−ペプチドを含むペプチド構造およびタンパク質構造、炭水化物構造、核酸構造を含むヌクレオチド構造、ならびに脂質構造の中で選択される構造を含むことを特徴とする、請求項13〜17のいずれか1項に記載された方法。
【請求項19】
工程(iii)が、
(iv) 濡れた多孔性床を含む一つもしくはそれ以上のマイクロチャネル構造(101a〜h)中で、当該濡れた多孔性床の上流位置に、溶質(S')を含有する液体を提供すること;
(v) 液体を、当該一つもしくはそれ以上のマイクロチャネル構造(101a〜h)の少なくとも一つの中の当該濡れた床を通して輸送すること:
の工程をさらに含むことを特徴とする方法によって行われる、請求項1〜18のいずれか1項に記載された方法。
【請求項20】
溶質(S')が、濡れた多孔性床と相互作用し得る、請求項19に記載された方法。
【請求項21】
溶質(S')が、微小流体装置/マイクロチャネル構造内で、好ましくは、濡れた多孔性床/微小反応空間(104a〜h)の上流位置またはその中で形成されるか;あるいは、マイクロチャネル構造に、好ましくは多孔性床/微小反応空間(104a〜h)の上流位置で、入口(105a〜b、107a〜h)に分配される、請求項19または20に記載された方法。
【請求項22】
工程(iv)または(v)が、(a)分離方法および/または(b)触媒反応、(c)固相合成、および/または(d)固相物質/多孔性床の誘導体化、の一部である、請求項19〜21のいずれか1項に記載された方法。
【請求項1】
複数の濡れた多孔性ビーズを乾燥/脱水状態へ変換する方法であって、当該乾燥/脱水状態が所望により複数の濡れた多孔性ビーズに再構成され、当該方法が、
i) 複数のマイクロチャネル構造(101a〜h)を備える微小流体装置であって、該マイクロチャネル構造がそれぞれ、床の保存活性を有する一つもしくはそれ以上の化合物を含む床の保存剤を含む液体で飽和された親水性の多孔性床を含む微小反応空間(104a〜h)を含む、微小流体装置を提供すること;
ii) それぞれの微小反応空間(104a〜h)中の床を、微小反応空間中に保持しながら、乾燥および/または脱水状態である固相物質に変換すること;
iii) 所望により、それぞれの微小反応空間(104a〜h)中で、工程ii)で得られた固相物質を、濡れた多孔性床に再構成すること;
の工程を含むことを特徴とする、方法。
【請求項2】
工程(iii)が、流動条件下で行われる、請求項1に記載された方法。
【請求項3】
当該一つもしくはそれ以上の化合物の少なくとも一つがa)非イオン性であってもなくてもよい親水性基を示し、そしてb)水溶性であることを特徴とする、請求項1または2に記載された方法。
【請求項4】
当該一つもしくはそれ以上の化合物の少なくとも一つが、ポリオールであることを特徴とする、請求項1〜3のいずれか1項に記載された方法。
【請求項5】
当該一つもしくはそれ以上の化合物の少なくとも一つが、炭水化物構造、例えば多糖類構造もしくはオリゴ糖類構造を示すことを特徴とする、請求項1〜4のいずれか1項に記載された方法。
【請求項6】
当該一つもしくはそれ以上の化合物の少なくとも一つが、二糖類、好ましくはトレハロースであることを特徴とする、請求項1〜5のいずれか1項に記載された方法。
【請求項7】
当該化合物の少なくとも一つがマイクロキャビティーの密着剤であることを特徴とする、請求項1〜6のいずれか1項に記載された方法。
【請求項8】
当該液体が、非揮発性の緩衝剤、例えばカリウムイオンを対イオンとして含んでよいリン酸塩緩衝剤、を含むことを特徴とする、請求項1〜7のいずれか1項に記載された方法。
【請求項9】
当該乾燥状態への変換が、水性液体で飽和されている多孔性床から減圧下で、例えば、液体の凝固点以上でもしくは以下で、または水で飽和されている多孔性床を環境大気圧で加温して又はしないで乾燥することにより達成されることを特徴とする、請求項1〜8のいずれか1項に記載された方法。
【請求項10】
a)当該固相物質が多孔性のもしくは非多孔性の粒子の形態であり、そして
b)多孔性床がこれらの粒子の充填床である
ことを特徴とする、請求項1〜9のいずれか1項に記載された方法。
【請求項11】
当該固相物質が膨潤可能であるかもしくは膨潤可能でないことを特徴とする、請求項1〜10のいずれか1項に記載された方法。
【請求項12】
それぞれのマイクロチャネル構造(101)がその構造の少なくとも一部を通って遠心力により液流を駆動させるために設計されていることを特徴とする、請求項1〜11のいずれか1項に記載された方法。
【請求項13】
固相物質が固定化反応物、典型的には溶質Sをアフィニティー捕獲するためのアフィニティー反応物ACSを含むことを特徴とする、請求項1〜12のいずれか1項に記載された方法。
【請求項14】
固定化反応物がLおよびLに対するアフィニティー相手Bを含む固定化アフィニティー対のメンバーである、そしてACSが溶質Sに対するアフィニティー相手である、多孔性床への結合体B−ACSの固定化を意図する、固定化リガンドLであることを特徴とする、請求項13に記載された方法。
【請求項15】
溶質(S)および溶質に対するアフィニティー相手(ACS)の間の複合体(S−−AC)の形成についてのアフィニティー定数(KS−−AC)、即ち(KS−−AC)=[S][ACS]/[S−−ACS]が最大10−6mole/lであることを特徴とする、請求項14に記載された方法。
【請求項16】
固定化アフィニティー対のアフィニティー定数、即ちKL'−−B'=[L'][B']/[L'−−B']が、ストレプトアビジンおよびビオチンについての相当するアフィニティー定数より最大103倍大きいことを特徴とし、好ましくは、アフィニティー対のL'およびB'がそれぞれビオチン結合化合物およびストレプトアビジン結合化合物から選択される(もしくは逆)、請求項15に記載された方法。
【請求項17】
BがLに対して一つもしくはそれ以上の結合部位を有して、そしてLがBに対して二つもしくはそれ以上の結合部位を有するか、または逆であることを特徴とする、請求項16に記載された方法。
【請求項18】
少なくとも一つのSおよびACSならびに/または少なくとも一つのL、B、ACSおよびSが、ポリ/オリゴ−ペプチドを含むペプチド構造およびタンパク質構造、炭水化物構造、核酸構造を含むヌクレオチド構造、ならびに脂質構造の中で選択される構造を含むことを特徴とする、請求項13〜17のいずれか1項に記載された方法。
【請求項19】
工程(iii)が、
(iv) 濡れた多孔性床を含む一つもしくはそれ以上のマイクロチャネル構造(101a〜h)中で、当該濡れた多孔性床の上流位置に、溶質(S')を含有する液体を提供すること;
(v) 液体を、当該一つもしくはそれ以上のマイクロチャネル構造(101a〜h)の少なくとも一つの中の当該濡れた床を通して輸送すること:
の工程をさらに含むことを特徴とする方法によって行われる、請求項1〜18のいずれか1項に記載された方法。
【請求項20】
溶質(S')が、濡れた多孔性床と相互作用し得る、請求項19に記載された方法。
【請求項21】
溶質(S')が、微小流体装置/マイクロチャネル構造内で、好ましくは、濡れた多孔性床/微小反応空間(104a〜h)の上流位置またはその中で形成されるか;あるいは、マイクロチャネル構造に、好ましくは多孔性床/微小反応空間(104a〜h)の上流位置で、入口(105a〜b、107a〜h)に分配される、請求項19または20に記載された方法。
【請求項22】
工程(iv)または(v)が、(a)分離方法および/または(b)触媒反応、(c)固相合成、および/または(d)固相物質/多孔性床の誘導体化、の一部である、請求項19〜21のいずれか1項に記載された方法。
【図1】


【図2a】


【図2b】


【図3】


【図4a】


【図4b】


【図5a】


【図5b】


【図5c】


【図5d】


【図6】




【図2a】


【図2b】


【図3】


【図4a】


【図4b】


【図5a】


【図5b】


【図5c】


【図5d】


【図6】


【公開番号】特開2010−112963(P2010−112963A)
【公開日】平成22年5月20日(2010.5.20)
【国際特許分類】
【出願番号】特願2010−13389(P2010−13389)
【出願日】平成22年1月25日(2010.1.25)
【分割の表示】特願2006−507978(P2006−507978)の分割
【原出願日】平成16年3月23日(2004.3.23)
【出願人】(505358004)ユィロス・パテント・アクチボラグ (22)
【氏名又は名称原語表記】Gyros Patent AB
【Fターム(参考)】
【公開日】平成22年5月20日(2010.5.20)
【国際特許分類】
【出願日】平成22年1月25日(2010.1.25)
【分割の表示】特願2006−507978(P2006−507978)の分割
【原出願日】平成16年3月23日(2004.3.23)
【出願人】(505358004)ユィロス・パテント・アクチボラグ (22)
【氏名又は名称原語表記】Gyros Patent AB
【Fターム(参考)】
[ Back to top ]

