充電可能な亜鉛イオン電池
本発明は充電可能な亜鉛イオン電池を開示し、正極、負極、電解質から構成されており、前記正極は亜鉛イオン(Zn2+)が可逆的なインサーション/エクストラクションを行うことができるマンガン酸化物材料二酸化マンガンを採用し、前記負極は亜鉛元素を主とする材料であり、前記電解質は亜鉛の可溶性塩基を溶質とし水を溶剤とし、かつイオン電気伝導性を有する液体またはゲル状の電解質である。前記充電可能な亜鉛イオン電池は、亜鉛イオン(Zn2+)が二酸化マンガンマンガン酸化物である正極材料の結晶構造に可逆的にインサーション及びエクストラクションし、同時に亜鉛元素を主とする負極材料で酸化或いは亜鉛イオン(Zn2+)が負極の表面で還元するというエネルギー貯蓄の原理を利用する。亜鉛イオン(Zn2+)が二酸化マンガンマンガン酸化物である正極材料の結晶構造に可逆的にインターカレーション及びデインターカレンションすることと、亜鉛イオンが負極の表面で酸化或いは還元することを利用しているため、前記電池は高容量と充電可能の特徴を有する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は電池技術領域に属し、具体的には亜鉛イオンが正極活性材料にインサーション/エクストラクションし、負極に還元或いは酸化する充電可能な亜鉛イオン電池に関する。
【背景技術】
【0002】
経済の継続発展は必然的に石油資源の欠如と環境の汚染を引き起こすため、新型のグリーンエネルギーの綜合的で高効率的な開発と利用が非常に必要な課題になっている。一次電池に比べ、二次電池は充放電サイクルを多数回繰り返すことができ、原材料をフルに利用できるため、より経済的で実用的である。最も有名な充電可能な電池(二次電池)はリチウムイオン電池である。リチウムイオン電池はリチウムイオンLi+をエネルギーの貯蓄媒体として利用し電気エネルギーを貯蓄するものであり、Li+イオンが正極と負極材料にインサーション或いはエクストラクションすることができ、充電時にリチウムイオンが正極材料からエクストラクションして電解液を経由して負極(一般的にはグラファイト)の層間にインサーションし、放電時にグラファイト負極にインサーションされたリチウムイオンが負極からエクストラクションして電解液を通じてまた正極に運動することを利用する。そのためリチウムイオン電池をイメージ的に揺り椅子となぞらえることができ、揺り椅子の両端は電池の正極と負極で、リチウムイオンが揺り椅子の両端に往復する。故にリチウムイオン電池はリチウムイオン揺り椅子電池(Rocking chair battery)とも呼ばれている。人類活動の増加と移動式電子製品の種類と数量の継続増加に従って、二次電池に対す需要も継続的に増加し、故に新型の充電可能な電池を開発することは非常に必要であり、重要な意義を有するものである。
【0003】
原材料の産出場所が広範で、値段が安く、毒性がないため、二酸化マンガンが広く使われているエネルギー貯蓄材料である。1865年からγ型二酸化マンガン(γ−MnO2)がすでに一次亜鉛マンガン電池の正極として使われ、この種類の亜鉛マンガン電池はγ−MnO2を正極とし、亜鉛板或いは亜鉛粉末を負極とし、電解液はZn2+とNH4+を含む水溶液であり、正極において以下の反応が発生する:
γ−MnO2 + NH4+ + e →MnOOH + NH3↑(1)
或いはMnO2 + H+ + e →MnOOH(2)
もし深く放電を行うと:
2MnOOH + 2H+→ MnO2 + Mn2+ + 2H2O (3)
亜鉛負極で発生する反応は、亜鉛の溶解である[夏熙、李清文、MnO2電極の充電可能性問題の検討(上)、電池、1992, 22: 177-180.]。20世紀の半ばに一次アルカリ亜鉛マンガン電池が開発され、その構造が一次亜鉛マンガン電池と同じで、ただ電解液はアルカリ性電解液になり、浅く放電(一電子放電)の時に[夏熙、李清文、MnO2電極の充電可能性問題の検討(上)、電池、1992, 22: 177-180.]:
γ−MnO2 + H2O + e →MnOOH + OH-(4)
深く放電の反応は:
MnOOH + H2O →Mn(OH)2 + OH-(5)
負極における反応は、亜鉛の溶解:Zn + 4OH-→ Zn[(OH)4]2- + 2e (6)
【0004】
このアルカリ亜鉛マンガン電池は価格が安く、性能が優れており、発売してすぐに一次電池の主要な地位を占め、アルカリ亜鉛マンガン電池の世界における生産量が100億個以上で、年売上が100億ドルを超えている[夏熙、二酸化マンガン電池の過去、現在と未来、電源技術、1996,20: 78-81;陳来茂、陳永▲しん▼、アルカリマンガン電池の発展の総括、電池工業、2006, 11: 119-124]。
【0005】
1977年になってKordeschが充電可能なアルカリ亜鉛マンガン電池[Kordesch, Karl Victor, United States Patent, 4091178]を開示し、それは負極活性材料の用量をコントロールすることによって正極材料である二酸化マンガンの反応を一電子の放電区間に抑える(等式4)ものである。充放電の時に正極に以下の反応が発生する[Y. shen, K. Kordesch, The mechanism of capacity fading of rechargeable alkaline manganese dioxide zinc cells, J. Power Sources, 2000, 87: 162.]:
γ−MnO2 + H2O + e →MnOOH + OH-(7)
負極の放電時に:
Zn + 4OH-= Zn[(OH)4]2- + 2e (8)
及びZnO + H2O + 2OH-= Zn[(OH)4]2- + 2e (9)
【0006】
二次アルカリ亜鉛マンガン電池の出現は原材料の利用率を大きく改善し、故にこの種類の充電電池は現在、小型一次と二次電池の半分を占めている。二次アルカリ亜鉛マンガン電池は充放電することができるが、その充電回数に限りがあり、かつ容量の減衰が非常に速いため、これらの要素がそのさらなる応用を制限した。
二酸化マンガンは非常に特殊なトンネル構造を有し、それは[MnO6]八面体を基本構造単元とし、Mnイオンは八面体の中心に位置し、酸素イオンが頂点位置を占める。[MnO6]八面体は共用頂点と辺を通じて一次元の[MnO6]八面体チェーンを構成することができ、このような[MnO6]八面体チェーンは頂点と辺を共用することによって一次元、二次元或いは三次元のトンネル構造を構成でき、これらの一次元、二次元或いは三次元のトンネル構造は水の分子或いは1価或いは2価の陽イオンによって充填されることができる。その中の一部のトンネルは大きいサイズの開放式構造を有し、トンネル内の陽イオンは水溶液中の陽イオンと交換を行うことができ、すなわちイオン交換能力を持ち、イオン交換のプロセスにおいてこれらのトンネル構造は安定を保つことができる。故に、我々は二酸化マンガンのトンネル構造の特徴に基づいて、二酸化マンガンのトンネルを利用して2価陽イオンを貯蓄し、エネルギー貯蓄の目的を達成することを初めて提案した。研究によって我々は、2価亜鉛イオン(Zn2+)の二酸化マンガン材料における可逆なインサーションとエクストラクション行為(図例1参照)と、Mn4+/Mn3+の可逆な変価に伴って電子(電気エネルギー)をストアとリリースすることを発見した:
δZn2+ + 2δe + MnO2 = ZnδMnO2 (10)
【0007】
このような亜鉛イオンのインサーション行為は容量が高く、可逆程度が良く、サイクル回数が長いなどの特徴を有し、この研究に基づいて、我々は亜鉛イオンをインサーションすることが可能な二酸化マンガンを正極とし、亜鉛を負極とし、亜鉛イオンを含む電解液とともに全く新しい亜鉛イオン電池を構成した。充電時に亜鉛イオンは二酸化マンガントンネルをエクストラクションして、電解液を経由してから負極に堆積し、放電時に負極の亜鉛は溶解して亜鉛イオンとなり、電解液を経由して二酸化マンガン正極材料のトンネルにインサーションする。故にこのような亜鉛イオン電池をイメージ的に揺り椅子となぞらえることができ、揺り椅子の両端は電池の正極と負極で、亜鉛イオンが揺り椅子の両端に往復する。
【0008】
このような亜鉛イオン電子が電子をストアする原理は以下である:
正極:δZn2+ + 2δe + MnO2 = ZnδMnO2(11)
負極:Zn = Zn2+ + 2e (12)
亜鉛イオンが正極材料における可逆なインサーション/エクストラクション行為を利用しているため、この充電可能な亜鉛イオン電池は容量が高く、サイクル寿命が長いなどの特徴を有し、かつこの電池の放電区間(図2参照)はアルカリ亜鉛マンガン電池の放電区間とだいたい同じであり、故にアルカリ亜鉛マンガン電池を使用する場合のすべてにおいてこの亜鉛イオン電池を使用することができ、個人のディジタルノート、電子手帳、携帯電話、無線電話、ポケットベル(登録商標)、電動玩具、ゲーム機、携帯式データターミナル、個人用オーディオ・ビデオ機器、実験装置、携帯情報端末(PDA)などの領域に広く応用できると予測できる。
【発明の概要】
【0009】
本発明の目的は、エネルギー密度が高く、仕事率密度が高く、サイクル寿命が長い二次電池を提案することにある。
【0010】
本発明が提案する充電可能な亜鉛イオン電池は、正極、負極、前記正極と前記負極の間に位置するセパレータ、及び陰陽イオンを含み、かつイオン電気伝導性を有する電解質から構成され、(1)正極活性材料は3価または4価のマンガンを主とする酸化物及びその水和物であって、1価の(H+,Li+、Na+、K+、Cu+、NH3+など)或いは2価の(Mg2+、Ca2+、Zn2+、Ba2+、Pb2+、Rb2+、Co2+、Cu2+、Fe2+など)の不純な陽イオンを含むことができ、(2)負極は亜鉛元素を主とする活性材料であり、(3)前記電解質は亜鉛の可溶性塩基を溶質とし、水を溶剤とし、かつイオン電気伝導性を有する液体またはゲル状材料であり、かつ酸、塩基或いは緩衝溶液を添加することによって電解質のpH値を3~10に調節できることを特徴とする。
【0011】
本発明が提案する充電可能な亜鉛イオン電池は、前記亜鉛イオンが正極活性材料の結晶構造内に可逆的にインサーション及びエクストラクションすることが可能であり、その亜鉛イオンのストア容量は100 mAh/g(正極活性物質の質量をもとに計算)以上であることを特徴とする。
【0012】
本発明が提案する充電可能な亜鉛イオン電池は、前記亜鉛の可溶性塩基は優先的に硝酸亜鉛、硫酸亜鉛及び塩化亜鉛などであることを特徴とする。
本発明が提案する充電可能な亜鉛イオン電池は、前記電解質は酸、塩基或いは緩衝溶液を添加することによって電解質のpH値を3~10に調節できることを特徴とする。
【0013】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料は亜鉛元素を主とする活性材料であり、亜鉛元素の含有量は10~100%であることを特徴とする。
【0014】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料は亜鉛粉末を含み、かつ亜鉛粉末を主とする膜状或いはクリーム状材料であることを特徴とする。
【0015】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料として亜鉛粉末を主とする膜状材料の中にさらに電子電気伝導剤、接着剤、酸化亜鉛(ZnO)または特定機能の添加剤を含み、その中、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であり、酸化亜鉛の添加量は負極膜の質量の50%以下であることを特徴とする。
【0016】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料として亜鉛粉末を主とするクリーム状材料の中にさらに電解液、増粘剤、酸化亜鉛粉末と特定機能の添加剤を含み、電解液は主に亜鉛イオン(Zn2+)を含む水溶液で、その添加量は負極の質量の40%以下であり、増粘剤は主にエステル類或いはカルボン酸類などで、例えばポリアクリル酸、アクリル酸ナトリウムなどであり、その添加量は負極の質量の10%以下であり、酸化亜鉛の添加量は負極膜の質量の50%以下であることを特徴とする。
本発明が提案する充電可能な亜鉛イオン電池は、前記負極の中に含まれる特定機能の添加剤は、亜鉛元素の水素発生反応を抑制または排除する防錆剤であり、インジウムの酸化物或いは水酸化物、及び金属銅であってもよく、その添加量は負極膜の質量の1%以下であることを特徴とする。
【0017】
本発明が提案する充電可能な亜鉛イオン電池は、前記正極の中で活性物質以外にさらに電子電気伝導剤、接着剤などを含み、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であることを特徴とする。
【0018】
本発明が提案する充電可能な亜鉛イオン電池は、前記電池構造がボタン式、円柱式、或いは方形構造であることを特徴とする。
【図面の簡単な説明】
【0019】
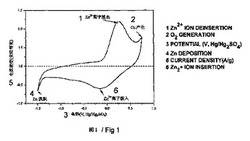
【図1】:正極活性材料が0.1 mol/L ZnSO4電解液の中でスキャン速度が1mV/s時の単電極サイクリックボルタモグラム。
【図2】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)における最初の放電と充電曲線。
【図3】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が1A/g(正極活性物質の質量をもとに計算)における放電と充電曲線。
【図4】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が異なる電流密度における放電容量(正極活性物質の質量をもとに計算)と能率。
【図5】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)固定電流における充放電サイクリック曲線。
【図6】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)におけるサイクル回数と容量及びクーロン能率の関係。
【図7】:二酸化マンガン電極の正極と、亜鉛板の負極と、NaOH溶液によってpH値が6.22に調節された0.1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)固定電流における充放電サイクリック曲線。
【図8】:二酸化マンガン電極の正極と、亜鉛板の負極と、NaOH溶液によってpH値が6.22に調節された0.1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)おけるサイクル回数と容量及びクーロン能率の関係。
【発明を実施するための形態】
【0020】
実施例1:
マイクロエマルション法を使って二酸化マンガン正極材料を製造する。一定量の表面活性剤であるスルホコハク酸塩ジオクチルナトリウム(sodium bis(2-ethylhexyl) sulfosuccinate,AOT)をイソオクタンに入れ、均一に撹拌し0.1 mol/Lの溶液を形成してから、撹拌しながら一定の濃度が0.1 mol/Lの過マンガン酸カリウム水溶液を加え、同時に所用の水と表面活性剤AOTのモル比が60になるようにして、全部の添加を終えてから、継続的に4時間撹拌する。その後、浸出を行い、水とエタノールを使ってそれぞれ5回ろ過し、ブラウン色のケーキ状ろ過物を得て、乾燥後、黒色の二酸化マンガン粉末を得る。この材料は部分結晶化のαMnO2構造であり、一定量の結合水を含む[徐成俊、李宝華、杜宏達、康飛宇、趙豊剛、曾毓群、ナノ二酸化マンガンの製造方法、中国特許、申請番号:200710032606.3]。
【0021】
分散剤として水を使い、製造した二酸化マンガンと、導電剤であるアセチレンブラックと、接着剤であるPTFE(ポリテトラフルオロエチレン)とを60:30:10の比例で混合してから、ステンレスメッシュの上に圧着し、一定のサイズに裁断し、真空の中で乾燥して二酸化マンガン電極板を得る。単電極計測は二酸化マンガン電極板を作用電極とし、白金電極を対極電極とし、Hg/Hg2SO4(in saturated K2SO4)を参照比較電極として計測を行った。二酸化マンガンと活性炭電極が0.1mol/L ZnSO4水溶液の中のサイクリックボルタモグラムが図1に示す通りであり、スキャン速度が2mV/sであり、0.2と−0.1V(vs. Hg/Hg2SO4)において2つの酸化還元峰が観測でき、この2つの酸化還元峰が亜鉛イオンが二酸化マンガンの結晶構造内のインサーションとエクストラクションに対応する。
【0022】
実施例2:
実施例1で製造したマンガン酸化物電極を正極とし、亜鉛箔(厚さ0.1mm)を負極とし、1mol L-1 ZnSO4水溶液を電解液としてボタン式電池を構成する。この亜鉛イオン電池の最初の放電と充電曲線は図2に示す通りである。放電電流が0.1A g-1(正極活性物質の質量をもとに計算)であり、亜鉛イオンの最初の放電フラットフォームが1.3V付近であることが観測できる。この二酸化マンガン電池が大電流1A g-1(正極活性物質の質量をもとに計算)における放充電曲線は図3に示す通りである。図4は異なる電流密度における放電容量とクーロン能率であり、この電池は優れた倍率性能と可逆性能を有することが観測できる。図5はこの電池の0.1A g-1電流における多数回の充放電サイクリック曲線であり、図6は30サイクルの容量及びクーロン能率とサイクル回数の関係であり、この電池は優れたサイクル性能を有することが観測できる。
【0023】
実施例3:
実施例1で製造したマンガン酸化物電極を正極とし、亜鉛箔(厚さ0.1mm)を負極とし、NaOH溶液によってpH値が6.22に調節された1mol L-1 ZnSO4水溶液を電解液としてボタン式亜鉛イオン電池を構成する。亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)固定電流における充放電サイクリック曲線は図7に示す通りであり、サイクル回数と容量及びクーロン能率の関係は図8に示す通りである。
【技術分野】
【0001】
本発明は電池技術領域に属し、具体的には亜鉛イオンが正極活性材料にインサーション/エクストラクションし、負極に還元或いは酸化する充電可能な亜鉛イオン電池に関する。
【背景技術】
【0002】
経済の継続発展は必然的に石油資源の欠如と環境の汚染を引き起こすため、新型のグリーンエネルギーの綜合的で高効率的な開発と利用が非常に必要な課題になっている。一次電池に比べ、二次電池は充放電サイクルを多数回繰り返すことができ、原材料をフルに利用できるため、より経済的で実用的である。最も有名な充電可能な電池(二次電池)はリチウムイオン電池である。リチウムイオン電池はリチウムイオンLi+をエネルギーの貯蓄媒体として利用し電気エネルギーを貯蓄するものであり、Li+イオンが正極と負極材料にインサーション或いはエクストラクションすることができ、充電時にリチウムイオンが正極材料からエクストラクションして電解液を経由して負極(一般的にはグラファイト)の層間にインサーションし、放電時にグラファイト負極にインサーションされたリチウムイオンが負極からエクストラクションして電解液を通じてまた正極に運動することを利用する。そのためリチウムイオン電池をイメージ的に揺り椅子となぞらえることができ、揺り椅子の両端は電池の正極と負極で、リチウムイオンが揺り椅子の両端に往復する。故にリチウムイオン電池はリチウムイオン揺り椅子電池(Rocking chair battery)とも呼ばれている。人類活動の増加と移動式電子製品の種類と数量の継続増加に従って、二次電池に対す需要も継続的に増加し、故に新型の充電可能な電池を開発することは非常に必要であり、重要な意義を有するものである。
【0003】
原材料の産出場所が広範で、値段が安く、毒性がないため、二酸化マンガンが広く使われているエネルギー貯蓄材料である。1865年からγ型二酸化マンガン(γ−MnO2)がすでに一次亜鉛マンガン電池の正極として使われ、この種類の亜鉛マンガン電池はγ−MnO2を正極とし、亜鉛板或いは亜鉛粉末を負極とし、電解液はZn2+とNH4+を含む水溶液であり、正極において以下の反応が発生する:
γ−MnO2 + NH4+ + e →MnOOH + NH3↑(1)
或いはMnO2 + H+ + e →MnOOH(2)
もし深く放電を行うと:
2MnOOH + 2H+→ MnO2 + Mn2+ + 2H2O (3)
亜鉛負極で発生する反応は、亜鉛の溶解である[夏熙、李清文、MnO2電極の充電可能性問題の検討(上)、電池、1992, 22: 177-180.]。20世紀の半ばに一次アルカリ亜鉛マンガン電池が開発され、その構造が一次亜鉛マンガン電池と同じで、ただ電解液はアルカリ性電解液になり、浅く放電(一電子放電)の時に[夏熙、李清文、MnO2電極の充電可能性問題の検討(上)、電池、1992, 22: 177-180.]:
γ−MnO2 + H2O + e →MnOOH + OH-(4)
深く放電の反応は:
MnOOH + H2O →Mn(OH)2 + OH-(5)
負極における反応は、亜鉛の溶解:Zn + 4OH-→ Zn[(OH)4]2- + 2e (6)
【0004】
このアルカリ亜鉛マンガン電池は価格が安く、性能が優れており、発売してすぐに一次電池の主要な地位を占め、アルカリ亜鉛マンガン電池の世界における生産量が100億個以上で、年売上が100億ドルを超えている[夏熙、二酸化マンガン電池の過去、現在と未来、電源技術、1996,20: 78-81;陳来茂、陳永▲しん▼、アルカリマンガン電池の発展の総括、電池工業、2006, 11: 119-124]。
【0005】
1977年になってKordeschが充電可能なアルカリ亜鉛マンガン電池[Kordesch, Karl Victor, United States Patent, 4091178]を開示し、それは負極活性材料の用量をコントロールすることによって正極材料である二酸化マンガンの反応を一電子の放電区間に抑える(等式4)ものである。充放電の時に正極に以下の反応が発生する[Y. shen, K. Kordesch, The mechanism of capacity fading of rechargeable alkaline manganese dioxide zinc cells, J. Power Sources, 2000, 87: 162.]:
γ−MnO2 + H2O + e →MnOOH + OH-(7)
負極の放電時に:
Zn + 4OH-= Zn[(OH)4]2- + 2e (8)
及びZnO + H2O + 2OH-= Zn[(OH)4]2- + 2e (9)
【0006】
二次アルカリ亜鉛マンガン電池の出現は原材料の利用率を大きく改善し、故にこの種類の充電電池は現在、小型一次と二次電池の半分を占めている。二次アルカリ亜鉛マンガン電池は充放電することができるが、その充電回数に限りがあり、かつ容量の減衰が非常に速いため、これらの要素がそのさらなる応用を制限した。
二酸化マンガンは非常に特殊なトンネル構造を有し、それは[MnO6]八面体を基本構造単元とし、Mnイオンは八面体の中心に位置し、酸素イオンが頂点位置を占める。[MnO6]八面体は共用頂点と辺を通じて一次元の[MnO6]八面体チェーンを構成することができ、このような[MnO6]八面体チェーンは頂点と辺を共用することによって一次元、二次元或いは三次元のトンネル構造を構成でき、これらの一次元、二次元或いは三次元のトンネル構造は水の分子或いは1価或いは2価の陽イオンによって充填されることができる。その中の一部のトンネルは大きいサイズの開放式構造を有し、トンネル内の陽イオンは水溶液中の陽イオンと交換を行うことができ、すなわちイオン交換能力を持ち、イオン交換のプロセスにおいてこれらのトンネル構造は安定を保つことができる。故に、我々は二酸化マンガンのトンネル構造の特徴に基づいて、二酸化マンガンのトンネルを利用して2価陽イオンを貯蓄し、エネルギー貯蓄の目的を達成することを初めて提案した。研究によって我々は、2価亜鉛イオン(Zn2+)の二酸化マンガン材料における可逆なインサーションとエクストラクション行為(図例1参照)と、Mn4+/Mn3+の可逆な変価に伴って電子(電気エネルギー)をストアとリリースすることを発見した:
δZn2+ + 2δe + MnO2 = ZnδMnO2 (10)
【0007】
このような亜鉛イオンのインサーション行為は容量が高く、可逆程度が良く、サイクル回数が長いなどの特徴を有し、この研究に基づいて、我々は亜鉛イオンをインサーションすることが可能な二酸化マンガンを正極とし、亜鉛を負極とし、亜鉛イオンを含む電解液とともに全く新しい亜鉛イオン電池を構成した。充電時に亜鉛イオンは二酸化マンガントンネルをエクストラクションして、電解液を経由してから負極に堆積し、放電時に負極の亜鉛は溶解して亜鉛イオンとなり、電解液を経由して二酸化マンガン正極材料のトンネルにインサーションする。故にこのような亜鉛イオン電池をイメージ的に揺り椅子となぞらえることができ、揺り椅子の両端は電池の正極と負極で、亜鉛イオンが揺り椅子の両端に往復する。
【0008】
このような亜鉛イオン電子が電子をストアする原理は以下である:
正極:δZn2+ + 2δe + MnO2 = ZnδMnO2(11)
負極:Zn = Zn2+ + 2e (12)
亜鉛イオンが正極材料における可逆なインサーション/エクストラクション行為を利用しているため、この充電可能な亜鉛イオン電池は容量が高く、サイクル寿命が長いなどの特徴を有し、かつこの電池の放電区間(図2参照)はアルカリ亜鉛マンガン電池の放電区間とだいたい同じであり、故にアルカリ亜鉛マンガン電池を使用する場合のすべてにおいてこの亜鉛イオン電池を使用することができ、個人のディジタルノート、電子手帳、携帯電話、無線電話、ポケットベル(登録商標)、電動玩具、ゲーム機、携帯式データターミナル、個人用オーディオ・ビデオ機器、実験装置、携帯情報端末(PDA)などの領域に広く応用できると予測できる。
【発明の概要】
【0009】
本発明の目的は、エネルギー密度が高く、仕事率密度が高く、サイクル寿命が長い二次電池を提案することにある。
【0010】
本発明が提案する充電可能な亜鉛イオン電池は、正極、負極、前記正極と前記負極の間に位置するセパレータ、及び陰陽イオンを含み、かつイオン電気伝導性を有する電解質から構成され、(1)正極活性材料は3価または4価のマンガンを主とする酸化物及びその水和物であって、1価の(H+,Li+、Na+、K+、Cu+、NH3+など)或いは2価の(Mg2+、Ca2+、Zn2+、Ba2+、Pb2+、Rb2+、Co2+、Cu2+、Fe2+など)の不純な陽イオンを含むことができ、(2)負極は亜鉛元素を主とする活性材料であり、(3)前記電解質は亜鉛の可溶性塩基を溶質とし、水を溶剤とし、かつイオン電気伝導性を有する液体またはゲル状材料であり、かつ酸、塩基或いは緩衝溶液を添加することによって電解質のpH値を3~10に調節できることを特徴とする。
【0011】
本発明が提案する充電可能な亜鉛イオン電池は、前記亜鉛イオンが正極活性材料の結晶構造内に可逆的にインサーション及びエクストラクションすることが可能であり、その亜鉛イオンのストア容量は100 mAh/g(正極活性物質の質量をもとに計算)以上であることを特徴とする。
【0012】
本発明が提案する充電可能な亜鉛イオン電池は、前記亜鉛の可溶性塩基は優先的に硝酸亜鉛、硫酸亜鉛及び塩化亜鉛などであることを特徴とする。
本発明が提案する充電可能な亜鉛イオン電池は、前記電解質は酸、塩基或いは緩衝溶液を添加することによって電解質のpH値を3~10に調節できることを特徴とする。
【0013】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料は亜鉛元素を主とする活性材料であり、亜鉛元素の含有量は10~100%であることを特徴とする。
【0014】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料は亜鉛粉末を含み、かつ亜鉛粉末を主とする膜状或いはクリーム状材料であることを特徴とする。
【0015】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料として亜鉛粉末を主とする膜状材料の中にさらに電子電気伝導剤、接着剤、酸化亜鉛(ZnO)または特定機能の添加剤を含み、その中、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であり、酸化亜鉛の添加量は負極膜の質量の50%以下であることを特徴とする。
【0016】
本発明が提案する充電可能な亜鉛イオン電池は、前記負極材料として亜鉛粉末を主とするクリーム状材料の中にさらに電解液、増粘剤、酸化亜鉛粉末と特定機能の添加剤を含み、電解液は主に亜鉛イオン(Zn2+)を含む水溶液で、その添加量は負極の質量の40%以下であり、増粘剤は主にエステル類或いはカルボン酸類などで、例えばポリアクリル酸、アクリル酸ナトリウムなどであり、その添加量は負極の質量の10%以下であり、酸化亜鉛の添加量は負極膜の質量の50%以下であることを特徴とする。
本発明が提案する充電可能な亜鉛イオン電池は、前記負極の中に含まれる特定機能の添加剤は、亜鉛元素の水素発生反応を抑制または排除する防錆剤であり、インジウムの酸化物或いは水酸化物、及び金属銅であってもよく、その添加量は負極膜の質量の1%以下であることを特徴とする。
【0017】
本発明が提案する充電可能な亜鉛イオン電池は、前記正極の中で活性物質以外にさらに電子電気伝導剤、接着剤などを含み、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であることを特徴とする。
【0018】
本発明が提案する充電可能な亜鉛イオン電池は、前記電池構造がボタン式、円柱式、或いは方形構造であることを特徴とする。
【図面の簡単な説明】
【0019】
【図1】:正極活性材料が0.1 mol/L ZnSO4電解液の中でスキャン速度が1mV/s時の単電極サイクリックボルタモグラム。
【図2】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)における最初の放電と充電曲線。
【図3】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が1A/g(正極活性物質の質量をもとに計算)における放電と充電曲線。
【図4】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が異なる電流密度における放電容量(正極活性物質の質量をもとに計算)と能率。
【図5】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)固定電流における充放電サイクリック曲線。
【図6】:二酸化マンガン電極の正極と、亜鉛板の負極と、1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)におけるサイクル回数と容量及びクーロン能率の関係。
【図7】:二酸化マンガン電極の正極と、亜鉛板の負極と、NaOH溶液によってpH値が6.22に調節された0.1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)固定電流における充放電サイクリック曲線。
【図8】:二酸化マンガン電極の正極と、亜鉛板の負極と、NaOH溶液によってpH値が6.22に調節された0.1 mol/L ZnSO4水溶液の電解液から構成された亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)おけるサイクル回数と容量及びクーロン能率の関係。
【発明を実施するための形態】
【0020】
実施例1:
マイクロエマルション法を使って二酸化マンガン正極材料を製造する。一定量の表面活性剤であるスルホコハク酸塩ジオクチルナトリウム(sodium bis(2-ethylhexyl) sulfosuccinate,AOT)をイソオクタンに入れ、均一に撹拌し0.1 mol/Lの溶液を形成してから、撹拌しながら一定の濃度が0.1 mol/Lの過マンガン酸カリウム水溶液を加え、同時に所用の水と表面活性剤AOTのモル比が60になるようにして、全部の添加を終えてから、継続的に4時間撹拌する。その後、浸出を行い、水とエタノールを使ってそれぞれ5回ろ過し、ブラウン色のケーキ状ろ過物を得て、乾燥後、黒色の二酸化マンガン粉末を得る。この材料は部分結晶化のαMnO2構造であり、一定量の結合水を含む[徐成俊、李宝華、杜宏達、康飛宇、趙豊剛、曾毓群、ナノ二酸化マンガンの製造方法、中国特許、申請番号:200710032606.3]。
【0021】
分散剤として水を使い、製造した二酸化マンガンと、導電剤であるアセチレンブラックと、接着剤であるPTFE(ポリテトラフルオロエチレン)とを60:30:10の比例で混合してから、ステンレスメッシュの上に圧着し、一定のサイズに裁断し、真空の中で乾燥して二酸化マンガン電極板を得る。単電極計測は二酸化マンガン電極板を作用電極とし、白金電極を対極電極とし、Hg/Hg2SO4(in saturated K2SO4)を参照比較電極として計測を行った。二酸化マンガンと活性炭電極が0.1mol/L ZnSO4水溶液の中のサイクリックボルタモグラムが図1に示す通りであり、スキャン速度が2mV/sであり、0.2と−0.1V(vs. Hg/Hg2SO4)において2つの酸化還元峰が観測でき、この2つの酸化還元峰が亜鉛イオンが二酸化マンガンの結晶構造内のインサーションとエクストラクションに対応する。
【0022】
実施例2:
実施例1で製造したマンガン酸化物電極を正極とし、亜鉛箔(厚さ0.1mm)を負極とし、1mol L-1 ZnSO4水溶液を電解液としてボタン式電池を構成する。この亜鉛イオン電池の最初の放電と充電曲線は図2に示す通りである。放電電流が0.1A g-1(正極活性物質の質量をもとに計算)であり、亜鉛イオンの最初の放電フラットフォームが1.3V付近であることが観測できる。この二酸化マンガン電池が大電流1A g-1(正極活性物質の質量をもとに計算)における放充電曲線は図3に示す通りである。図4は異なる電流密度における放電容量とクーロン能率であり、この電池は優れた倍率性能と可逆性能を有することが観測できる。図5はこの電池の0.1A g-1電流における多数回の充放電サイクリック曲線であり、図6は30サイクルの容量及びクーロン能率とサイクル回数の関係であり、この電池は優れたサイクル性能を有することが観測できる。
【0023】
実施例3:
実施例1で製造したマンガン酸化物電極を正極とし、亜鉛箔(厚さ0.1mm)を負極とし、NaOH溶液によってpH値が6.22に調節された1mol L-1 ZnSO4水溶液を電解液としてボタン式亜鉛イオン電池を構成する。亜鉛イオン電池が100mA/g(正極活性物質の質量をもとに計算)固定電流における充放電サイクリック曲線は図7に示す通りであり、サイクル回数と容量及びクーロン能率の関係は図8に示す通りである。
【特許請求の範囲】
【請求項1】
正極、負極、前記正極と前記負極の間に位置するセパレータ、及び陰陽イオンを含み、かつイオン電気伝導性を有する電解質から構成される充電可能な亜鉛イオン電池であって、
(1)正極活性材料は3価または4価のマンガンを主とする酸化物及びその水和物であって、1価の(H+,Li+、Na+、K+、Cu+、NH3+など)或いは2価の(Mg2+、Ca2+、Zn2+、Ba2+、Pb2+、Rb2+、Co2+、Cu2+、Fe2+など)の不純な陽イオンを含むことができ、
(2)負極は亜鉛元素を含む活性材料であり、
(3)前記電解質は亜鉛の可溶性塩基を溶質とし、水を溶剤とし、かつイオン電気伝導性を有する液体またはゲル状材料である
ことを特徴とする充電可能な亜鉛イオン電池。
【請求項2】
前記亜鉛の可溶性塩基は優先的に硝酸亜鉛、硫酸亜鉛及び塩化亜鉛などであることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項3】
前記負極材料の亜鉛元素の含有量は10〜100%であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項4】
前記負極材料は箔状、板状、円筒状、若しくはメッシュ状の純粋な亜鉛金属又は亜鉛合金であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項5】
前記負極材料は箔状、板状、円筒状、メッシュ状などの純粋な亜鉛金属或いは亜鉛合金であることを特徴とする請求項1と4に記載の充電可能な亜鉛イオン電池。
【請求項6】
前記負極材料は亜鉛粉末を含む膜状又はクリーム状材料であることを特徴とする請求項1と4に記載の充電可能な亜鉛イオン電池。
【請求項7】
前記負極材料として亜鉛粉末を主とする膜状材料の中にさらに電子電気伝導剤、接着剤、酸化亜鉛粉末(ZnO)や特定機能の添加剤を含み、その中、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であり、酸化亜鉛粉末の添加量は負極膜の質量の50%以下であることを特徴とする請求項1、4と6に記載の充電可能な亜鉛イオン電池。
【請求項8】
前記負極材料として亜鉛粉末を主とするクリーム状材料の中にさらに電解液、増粘剤、酸化亜鉛粉末と特定機能の添加剤を含み、電解液は主に亜鉛イオン(Zn2+)を含む水溶液で、その添加量は負極の質量の40%以下であり、増粘剤は主にエステル類或いはカルボン酸類などで、例えばポリアクリル酸、アクリル酸ナトリウムなどであり、その添加量は負極の質量の10%以下であり、酸化亜鉛の添加量は負極膜の質量の50%以下であることを特徴とする請求項1、4と6に記載の充電可能な亜鉛イオン電池。
【請求項9】
前記負極の中に含まれる特定機能の添加剤は、亜鉛元素の水素発生反応を抑制または排除する防錆剤であり、インジウムの酸化物或いは水酸化物、及び金属銅であってもよく、その添加量は負極膜の質量の1%以下であることを特徴とする請求項1、4、6、7と8に記載の充電可能な亜鉛イオン電池。
【請求項10】
前記正極は、さらに電子電気伝導剤、接着剤を含み、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項11】
前記電池構造がボタン式、円柱式、又は方形構造であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項1】
正極、負極、前記正極と前記負極の間に位置するセパレータ、及び陰陽イオンを含み、かつイオン電気伝導性を有する電解質から構成される充電可能な亜鉛イオン電池であって、
(1)正極活性材料は3価または4価のマンガンを主とする酸化物及びその水和物であって、1価の(H+,Li+、Na+、K+、Cu+、NH3+など)或いは2価の(Mg2+、Ca2+、Zn2+、Ba2+、Pb2+、Rb2+、Co2+、Cu2+、Fe2+など)の不純な陽イオンを含むことができ、
(2)負極は亜鉛元素を含む活性材料であり、
(3)前記電解質は亜鉛の可溶性塩基を溶質とし、水を溶剤とし、かつイオン電気伝導性を有する液体またはゲル状材料である
ことを特徴とする充電可能な亜鉛イオン電池。
【請求項2】
前記亜鉛の可溶性塩基は優先的に硝酸亜鉛、硫酸亜鉛及び塩化亜鉛などであることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項3】
前記負極材料の亜鉛元素の含有量は10〜100%であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項4】
前記負極材料は箔状、板状、円筒状、若しくはメッシュ状の純粋な亜鉛金属又は亜鉛合金であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項5】
前記負極材料は箔状、板状、円筒状、メッシュ状などの純粋な亜鉛金属或いは亜鉛合金であることを特徴とする請求項1と4に記載の充電可能な亜鉛イオン電池。
【請求項6】
前記負極材料は亜鉛粉末を含む膜状又はクリーム状材料であることを特徴とする請求項1と4に記載の充電可能な亜鉛イオン電池。
【請求項7】
前記負極材料として亜鉛粉末を主とする膜状材料の中にさらに電子電気伝導剤、接着剤、酸化亜鉛粉末(ZnO)や特定機能の添加剤を含み、その中、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であり、酸化亜鉛粉末の添加量は負極膜の質量の50%以下であることを特徴とする請求項1、4と6に記載の充電可能な亜鉛イオン電池。
【請求項8】
前記負極材料として亜鉛粉末を主とするクリーム状材料の中にさらに電解液、増粘剤、酸化亜鉛粉末と特定機能の添加剤を含み、電解液は主に亜鉛イオン(Zn2+)を含む水溶液で、その添加量は負極の質量の40%以下であり、増粘剤は主にエステル類或いはカルボン酸類などで、例えばポリアクリル酸、アクリル酸ナトリウムなどであり、その添加量は負極の質量の10%以下であり、酸化亜鉛の添加量は負極膜の質量の50%以下であることを特徴とする請求項1、4と6に記載の充電可能な亜鉛イオン電池。
【請求項9】
前記負極の中に含まれる特定機能の添加剤は、亜鉛元素の水素発生反応を抑制または排除する防錆剤であり、インジウムの酸化物或いは水酸化物、及び金属銅であってもよく、その添加量は負極膜の質量の1%以下であることを特徴とする請求項1、4、6、7と8に記載の充電可能な亜鉛イオン電池。
【請求項10】
前記正極は、さらに電子電気伝導剤、接着剤を含み、電子電気伝導剤はグラファイト、カーボンブラック、アセチレンブラック、炭素繊維またはカーボンナノチューブで、添加量は負極膜の質量の50%以下であり、接着剤はポリテトラフルオロエチレン(PTFE)、水溶性ゴム、ビニリデンPTFEまたはセルロースで、添加量は負極膜の質量の20%以下であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【請求項11】
前記電池構造がボタン式、円柱式、又は方形構造であることを特徴とする請求項1に記載の充電可能な亜鉛イオン電池。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公表番号】特表2012−524363(P2012−524363A)
【公表日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願番号】特願2012−505028(P2012−505028)
【出願日】平成21年6月17日(2009.6.17)
【国際出願番号】PCT/CN2009/072312
【国際公開番号】WO2010/118586
【国際公開日】平成22年10月21日(2010.10.21)
【出願人】(511233865)グラジュエート スクール アット シェンチェン、 ツィングワ ユニバーシティー (1)
【Fターム(参考)】
【公表日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願日】平成21年6月17日(2009.6.17)
【国際出願番号】PCT/CN2009/072312
【国際公開番号】WO2010/118586
【国際公開日】平成22年10月21日(2010.10.21)
【出願人】(511233865)グラジュエート スクール アット シェンチェン、 ツィングワ ユニバーシティー (1)
【Fターム(参考)】
[ Back to top ]

