光学式赤血球および白血球の弁別
【課題】光学式赤血球および白血球の弁別分析をすること。
【解決手段】試料における哺乳類赤血球の容積、ヘモグロビン濃度、成熟度、および赤血球形状を決定し、同時にシステム標準化をモニタするための方法および装置が開示される。
【解決手段】試料における哺乳類赤血球の容積、ヘモグロビン濃度、成熟度、および赤血球形状を決定し、同時にシステム標準化をモニタするための方法および装置が開示される。
【発明の詳細な説明】
【技術分野】
【0001】
(発明の概要)
試料中の哺乳類の赤血球の容積、ヘモグロビン濃度、成熟度、および赤血球形状を決定し、同時にシステム標準化をモニタするための方法および装置が開示される。赤血球分析の前に、赤血球を他の細胞粒子から区別するための方法も開示される。方法は、広範囲の可視スペクトルに対して正確に適用することができる。全血試料は、中性pHの等張緩衝溶液に非イオン性界面活性剤を含む試薬溶液で処理され、赤血球は、選択された波長で単一ファイルにおける光のビームを通過し、1つの光損失信号、選択された角度間隔での1つの前方角度光散乱信号、および第3の側方角度光散乱信号の結果として得られる大きさによって、あるいは、選択された角度間隔での2つの前方角度光散乱信号、および第3の側方角度光散乱信号の結果として得られる大きさによって、初期的なサイトグラムを獲得し、容積およびヘモグロビン濃度のグリッドラインを含む予め較正された三次元表面に、1点ずつサイトグラムを投影し、三次元グリッド表面への各投影された交差(インターセプト)の場所によって、赤血球容積およびヘモグロビン濃度の正確な値を決定する。
【0002】
本発明は、体液における哺乳類の赤血球(RBC)および白血球(WBC)の弁別の自動分析とシステム標準化の同時モニタとの方法および装置に関する。本発明は、特に、同一の光学式検出装置を使用してRBCおよびWBCの両方の弁別分析を行うことができる、マルチパラメータヘマトロジーアナライザーまたはフローサイトメータ等の多角光散乱および蛍光装置に関する。本発明は、より詳細には、(i)全血中における容積、ヘモグロビン含有量、細胞形状、および成熟度に関してRBCを分析するための方法、(ii)未熟RBC(網状赤血球)容積およびヘモグロビン含有量を決定するための正確な方法、(iii)RBC弁別のために血液試料が分析されている間に、システム標準化を継続してモニタすることができるRBC方法、(iv)1つの試薬を使用して、成熟RBCおよび網状赤血球の両方の容積およびヘモグロビン含有量を測定することができる方法、および(v)同一の光学式検出システムを使用して、WBCおよびRBCの両方の弁別分析を行うことができる装置とに関する。
【背景技術】
【0003】
従来のヘマトロジー方法、すなわち、細胞サイズ、細胞形状、色(ヘモグロビン含有量用)、および封入体に関するRBC形態学に関する患者血液塗抹標本の顕微鏡的検査は、診断へ導きかつ患者の臨床状態をモニタする豊富な情報を提供する。しかし、この手動方法は、非常に主観的であり、かつ時間がかかるものであるという事実に加えて、標準以下の血液フィルムから、きわめて誤解を招く恐れのある印象を引く可能性がある。過去30年の間に、大量の実験室作業量を取り扱いかつ労力を減少する、多数の自動ヘマトロジーアナライザーが利用可能になっている。これらの機器の大半は、電気インピーダンス測定によるか、または比色分析ヘモグロビン測定と組み合わされた光散乱光学式測定によって、赤血球の平均血球容積(MCV)および平均血球ヘモグロビン濃度(MCHC)を測定する。これらのシステムからの細胞分析における形態学的情報の不完全性またはあいまい性から、ヘマトロジー実験室における5から10パーセントの試料は、日常的に、顕微鏡的方法を使用して細胞形態学に関する塗抹標本検査を受ける。RBC形態学的分析の点におけるより進歩したヘマトロジーアナライザーは、テクニコンH*1(Technicon H*1)およびバイエルアドヴィア(Bayer ADVIA)である。両システムは、米国特許第4,735,504号に記載されたD.H.Tyckoの教示にしたがって、細胞1つずつに基づいて同時に赤血球の容積およびヘモグロビン濃度を測定するように構成されている。
【0004】
D.H.Tyckoに付与された米国特許第4,735,504号には、粒子の容積および屈折率を決定するための方法および装置が記載されている。VおよびHCを測定するための方法は、2つの選択された角度間隔の前方光散乱信号S1およびS2による卵形(ovolumetrically)形状のRBCであり、容積(V)およびヘモグロビン濃度(HC)を決定することが開示されている。この方法の欠点は、下記の通りである。1)RBCからのヘモグロビン吸収を避けるために、光源の波長が十分長くなければならず(たとえば633nm)、これによって、マルチパラメータ血液細胞分析用のより適切な光源(たとえば488nm光源)を選択することができない。2)二次元(2D)マトリクスは、異常な細胞形状に関するいずれの情報を提供しないが、それは、そのような細胞からの信号は、所定の二次元マトリクスでは誤った場所に入り、したがって、V&HCに関する不正確な臨床データを生成するからである。3)二次元マトリクスは、システム標準化におけるシフトに関するいずれの情報を提供せず、これは、一定の血液試料における凝血塊によって生じる流体素子工学的な通過における不安定性、またはシステムの電子工学における不安定性のため、いずれも警告無しで発生する可能性のある現象である。4)二次元散乱方法は、WBCおよび有核赤血球(NRBC)を、成熟RBCまたは染色された網状赤血球から識別してはっきりと分離することができない。WBCおよびNRBCは、その核のため、赤血球よりもかなり多くの散乱を生成し、VおよびHC分析の前に、RBC母集団からはっきりと除外されるのでなければ、MCV、ヘマトクリット(Hct)、MCHC、および平均血球ヘモグロビン(MCH)に関する臨床結果は、上昇WBCまたはNRBC試料では非常に誤解を招きやすい。
【0005】
D.H.Tyckoに付与された米国特許第5,194,909号には、赤血球のVおよびHCを測定するための方法および装置が教示されている。この技術と米国特許第4,735,504号における先の教示との相違は、長い波長(633nm)での1つの前方光散乱信号(予め選択される)と、抵抗パルスサイジング開口部からの第2の信号とを使用して、二次元マトリクスが形成されることである。この方法の欠点は下記の通りである。1)方法は、検出システムの2つの独立した源を必要とし、これは、2つの異なる検出システムからの2つの信号の同期等の不必要な複雑な状態を生み出す。2)RBCからのヘモグロビン吸収を避けるために、光源の波長が十分長くなければならず、これは、マルチパラメータ血液細胞分析用の光源の選択を限定する。3)二次元マトリクスは、異常な形状のRBCに関するいずれの情報を提供せず、したがって、V&HCに関する不正確な臨床データを生成する。4)二次元マトリクスは、システム標準化におけるシフトに関するいずれの情報を提供せず、これは上記に説明されたように、電子工学または流体素子工学における不安定性のため、いずれも警告無しで発生する可能性のある現象である。
【0006】
Fanらへ付与された米国特許第5,284,771号には、試薬組成物および細胞球形化におけるその使用が開示されている。試薬組成物は、向きによるノイズを排除するために赤血球を球形づけるための両性イオン界面活性剤と、網状赤血球を染色するためのOzxazine750とを含む。光学式検出システムの光源は633nmヘリウムネオンレーザであり、染色された網状赤血球は、光散乱/吸収技術によって識別される。網状赤血球の蛍光測定は、この特許では例示されていないか、または請求されていなかった。この開示の発明者らは、網状赤血球のV&HCの測定に関しては請求していなかったが、テクニコンH*1システムを使用して細胞1つずつに基づいて、赤血球の容積およびヘモグロビンを同時に測定する上述のTyckoの方法の使用を記載した。Fanらの教示において、網状赤血球の染色手順は、手動調製、手動供給、および2分以上の染色時間を必要とする。発明者らは、RBCおよび網状赤血球の両方のV&HCは、Tyckoの方法によって測定されるが、RBCおよび網状赤血球に使用される試薬は、組成が完全に異なると記載した。テクニコンH*1のRBCに関するTyckoの二次元マトリクスを作るために使用される試薬は、Tyckoの開示に記載されるように、RBCを球形にして固定し、一方、網状赤血球に関して使用される試薬は、いずれの固定剤を含まない緩衝液内でRBCを球形にする。その上、網状赤血球を染色するのに使用される青染料による吸収は、染色された細胞のV&HCの測定における散乱信号の大きさに干渉する。上述の問題は、Fanらの教示による網状赤血球のV&HCに関する誤った臨床データへ導く可能性がある。上述のように、V&HC測定に関するTyckoの方法は、ヘモグロビンが非常に透明である領域では単色光を発する光源を必要とする。これは、光源の利用可能性を制限する(λmaxは、600nmより大きくなければならない、赤ヘリウムネオンレーザ等)。別の制限は、吸収のためにまたは蛍光放射のために染料を励起するために、同一波長を使用しなければならないため、利用可能な染料の選択である。この条件下で、染料は、赤光を強力に吸収する青染料でなければならない。この特許では、網状赤血球のV&HCの測定に関しては、何の請求もされなかった。
【0007】
Collelaらに付与された米国特許第5,350,695号には、疑似吸収に関して測定された吸収信号を調整する方法が加えられていることを除いて、米国特許第5,284,771号で先に開示されたものと同一の網状赤血球を特徴づけるための方法および試薬が開示されている。この開示の第12欄、第1段落の記載によると、米国特許第5,284,771号に開示された方法の主要な問題は、テクニコンH*1機器の吸収信号が、吸収プリアンプのノイズと同一レベルであるということである。したがって、染色された網状赤血球からの吸収信号の信号対雑音(S/N)比を改良するために、数学的モデルを展開しなければならなかった。この特許に開示された数学的訂正を備えてさえ、染色された網状赤血球から吸収信号の満足のいくS/N比を生成することは、この方法の主要な問題であると思われる。その上、光吸収も、粒子の光散乱の大きさに干渉する。
【0008】
Fanらへ付与された米国特許第5,360,739号には、青の励起可能な蛍光染料、すなわちアクリジンオレンジが含まれることを除き、先の4つの特許に開示されたような方法および試薬が開示されている。この方法の教示を実行するために、2つの光源を必要とする。一方の光源は、青の励起可能な蛍光測定用(アルゴン/イオンレーザ)であり、他方の光源は、細胞の容積およびヘモグロビンの測定用(ヘリウムネオンレーザ)である。この方法の欠点は、同期および標準化のために検出システムが不必要に複雑になることであり、機器製造コストが非常に上昇する。
【0009】
Collelaらに付与された米国特許第5,438,003号には、全血における網状赤血球の識別および特徴づけに使用するために、先の4つの特許に示されたものと同一の試薬組成物が開示されている。この特許のすべての請求項は試薬組成物に関しており、網状赤血球のV&HCの測定の方法に関する請求はなされていない。しかし、ヘリウムネオン(633nm)光源を使用する光散乱/吸収によって、成熟RBCから網状赤血球を分離するにあたり、開示された方法では「疑似吸収」およびヘモグロビン干渉をどのように訂正しているかを、本文内で新規に非常に長く説明している。結果として、米国特許第5,438,003号に示されたサイトグラムは、成熟RBC信号から不十分に分離された網状赤血球信号を明らかにしている。開示された光散乱/吸収方法によって、成熟RBCから母集団がよく分離されない限り、網状赤血球のV&HCを正確に測定することは非常に困難である。さらに、この開示の例は、開示された方法が、V&HCの測定に関する二次元マップを作るのに使用される試薬とは、pH、浸透圧、球形剤、および緩衝液がまったく異なる、2つの試薬を必要とすることを明らかにしている。加えて、H*1RBC方法は、非常に短いインキュベーション時間を有し、一方、開示された試薬における網状赤血球の染色時間は2分である(30秒対120秒)。RBC球形づけプロセスは、非常に敏感な可逆的なプロセスであり、2つの選択された光散乱信号に基づいて、一貫して再現可能なV&HCデータを得るために、正確なタイミングを必要とする。Collelaらは、V&HCに関するいずれの時間検査データを開示していないし、この特許ではいずれの網状赤血球のV&HCデータも開示していない。
【発明の開示】
【発明が解決しようとする課題】
【0010】
先行技術のこれらの態様を考慮すると、完全なRBC弁別分析、およびより正確な網状赤血球計数、およびV&HC測定のための、改良された方法および装置を提供することが望ましい。本発明の目的は、単一の光源および光学式検出システムを使用して、WBCおよびRBCの両方の弁別分析を行うことができる装置を提供することである。本発明の別の目的は、細胞1つずつに基づいた臨床的に有用なMCHC測定、および異常な形状のRBCの検出および定量化を含む、より完全なRBC弁別分析を提供することである。本発明のさらに別の目的は、成熟RBCおよび網状赤血球の両方のV&HC測定のために使用することができる、単一の網状赤血球試薬を提供することである。本発明のさらなる目的は、非常に狭い範囲内に光源の選択を限定しない方法を提供することである。本発明のさらに別の目的は、システムの安定を継続してモニタするためのRBC/弁別方法を提供することである。本発明のこれらの目的およびさらなる目的は、下記の説明および図面から当業者には明らかになる。
【課題を解決するための手段】
【0011】
本発明は、(1)多角光散乱および蛍光ヘマトロジーアナライザーまたはフローサイトメータでRBC弁別を自動分析し、システム標準化を同時にモニタするための方法および装置に関し、(2)同一の光源および同一の光学式検出システムを使用して、WBCおよびRBCの両方の弁別分析を行うことができる装置に関し、(3)特に、全血または体液における、容積、ヘモグロビン含有量、細胞形状、および成熟度に関してRBCを分析するための方法に関し、(4)幼児および血液透析患者における鉄欠乏性貧血の診断に有用な、網状赤血球(未熟RBC)のV&HCを決定するための正確な方法に関し、(5)血液試料が分析されている間に、システム標準化を継続してモニタすることができるRBC方法に関し、特徴は、システムドリフトによって生じる誤った臨床データを報告する可能性を排除する。上記目的は、内蔵測定装置として明確な予め較正された三次元(3D)表面を使用して達成され、三次元表面は、理論的データ、および多角光散乱および/または光損失測定によって生成される実際のデータ(事象)の両方を使用して形成される。正常なRBCの各事象は、したがって、このごく薄い三次元表面に入らなければならない。細胞特徴の大半が、表面より下または上にあり、別の層を形成する場合には、電子工学的または流体素子工学的なシフトのいずれかのため、対象のチャネルが標準外であることが指摘される。3つまたはそれ以上の光散乱および/または光損失信号の多次元分析は、ある程度の内部一貫性を提供する。異常な形状のRBCは、表面からもっとも近い各事象の距離によって規定されるが、それは、すべての正常なRBC信号(CELL DYN4000希釈剤シースで球形づけられる)が、表面に近接するからである。網状赤血球は、CELL DYN4000網状赤血球試薬における核酸ステインで処理された各事象の蛍光強度によって規定される。細胞のV&HCは、ALL/IAS’/PSS、またはIAS/IAS’/PSSによって形成された、三次元マトリクスにおける各事象の場所に基づいて決定される。上記目的を達成するために、CELL DYN4000デテクタは、3つのゾーンを形成するように修正された。中心矩形ゾーン(ゾーン1)は、軸方向光損失(0度、ALL)用であり、2.24度から7.45度(IAS)である現在のCELL DYN4000中間角度(ゾーン2)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5度から5.5度(IAS’)である。修正されたデテクタは、本開示では3リングデテクタと称される。三次元表面は、前述の3リングデテクタによって生成された2つの角度(ALLおよびIAS’、またはIASおよびIAS’)、および90度偏光側方散乱(PSS)信号を使用して作られる。三次元の原則は、広い範囲の光源波長(たとえば、488nm、532nm、または633nm)を備えた光学式検出システムに適用可能である。
【0012】
本発明およびその利点をより完全に理解するために、添付の図面とともに取られた下記の説明が参照される。
【発明を実施するための最良の形態】
【0013】
A)装置
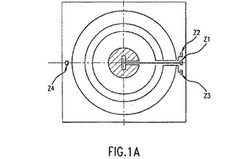
開示された装置の1つの実施態様は、米国特許第5,656,499号および第5,631,165号、発明の名称「自動分析を行うための方法および装置(METHOD AND APPARATUS FOR PERFORMING AUOMATED ANALYSIS)」に開示された、修正されたCELL DYN(登録商標)4000ヘマトロジーアナライザーである。本発明の開示された方法を行うために、CELL DYN(登録商標)4000システムデテクタおよびプリアンプボードは修正された。修正されたデテクタを示す図が、図1Aに表される。3つのゾーン(3リング)が形成される。中心矩形ゾーン(ゾーン1)は軸方向光損失(0度、ALL)用であり、中間ゾーン(ゾーン2、2.24から7.45度、IAS)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5から5.5度(IAS’)である。CELL DYN(登録商標)4000プリアンプボードも、図1Bに例示されるように修正された。修正されたプリアンプボードは、すべての3つのリングから信号を電気的に加算することによってIAS出力を形成する。この修正されたプリアンプボードからの可能な出力は、ALLおよびIASであるか、またはIAS’およびIASである(または配線し直すならば、ALLおよびIAS’である)。ALLチャネルのゲインが4に設定されるのであれば、IAS’は、ALLの代わりに、出力へルートづけられる。IAS’ゲインは、オンボードデュアルインラインパッケージ(DIP)スイッチによって設定される。ALLおよびIASは、WBC/弁別のために使用され、ALLおよびIAS’の組み合わせ、またはIAS’およびIASの組み合わせのいずれかが、RBC/弁別のために使用される。三次元RBC/弁別分析ために使用される第3の角度が、側方散乱信号であり、これは、125度円錐から構成される。これは、本質的にレーザ光の垂直偏光を保存するため、側方偏光散乱(PSS)と呼ばれる。125度全角度円錐の同一側方収集システムも、米国特許第5,691,204号に開示された試薬のRNAステインによって染色された網状赤血球の蛍光信号を収集する。この特徴は、単一の試薬および単一の光源から、網状赤血球の識別を可能にし、且つ成熟RBCおよび網状赤血球の両方のV&HC測定を可能にするものであり、これは、本発明の独特な特徴である。
【0014】
B)方法および試薬
WBC/弁別試薬
WBC弁別分析およびNRBC定量化に使用されるCELL DYN(登録商標)4000WBC試薬の組成物は、米国特許第5,516,695号に開示されており、NRBC分析の方法は、米国特許第5,559,037号に開示されている。
【0015】
RBC/弁別試薬
CELL DYN(登録商標)4000希釈剤シースの組成物は、米国特許第5,656,499号に開示されており、CELL DYN(登録商標)4000網状赤血球試薬組成物および方法は、米国特許第5,691,204号に開示されている。希釈剤シースおよび網状赤血球試薬の両方は、システムに予め存在する流体素子工学構成のため、開示された方法をCELL DYN(登録商標)4000システムで行うためのものであるが、2つの試薬を1つの試薬に化合して、開示された方法を行うことができる。
【0016】
方法
開示されたRBC弁別分析を修正されたCELL DYN(登録商標)4000で行うために、36.1μlの全血試料が、試料吸引プローブによって、約10.513μlの希釈剤シースを含んでいるRBCカップ内に置かれ、混合される。次いで、希釈された試料は、シース状インピーダンス開口部へ運ばれ、米国特許第5,656,499号および第5,631,165号、発明の名称「自動分析を行うための方法および装置」に記載されるように、試料の絶対RBC計数を電気的に決定する。次いで、約450μlの希釈された試料が、450μlの網状赤血球試薬を含んでいる網状赤血球カップ内に移され、ここで混合され、網状赤血球は染色される。次いで、準備された試料は、検出のために、シース状光学式フローセルへ運ばれる。細胞のストリームは、シースによって囲まれた層流の流体力学的に集束された試料ストリーム内で、本質的に一度に1細胞ずつ、フローセルを通って流れる。フロー軸に垂直な光のビームが、ストリームを照射する。照射された容積における細胞からの光散乱信号は、開示された3リングデテクタ(IASおよびIAS’)によって、および偏光側方散乱(PSS)および緑蛍光(FL1)を検出する2つの光電子増倍管(PMT)によって検出される。これらのパルスの振幅は、デジタル化され、リストモードデータとして保管される。本実施態様において、約20,000細胞が8秒間に計数される。
【0017】
RBC分析
第1に、図6Aに示されるFL1対IASサイトグラムにおいてRBCの左側に表れる信号は、血小板として識別される。第2のステップは、WBCおよびNRBC(もしあれば)を識別しラベルづけることであり、それらの信号は、FL1対IASサイトグラムにおいてRBCより上に表れる。FL1ヒストグラム(図6B)をスキャンして、サイトグラムにおけるRBCゲートの上部縁を決定する。ゲート内の事象は、成熟RBCおよび網状赤血球である。
【0018】
網状赤血球検出
本発明の方法は、十分に高いS/N比(染色された網状赤血球対染色されていない成熟RBC)を有するため、信号を分離するために数学的訂正は必要ない。先の開示(米国特許第5,691,204号)に記載されるように、ゲート内のRBC母集団のFL1ヒストグラムは、成熟RBCのピークに関してスキャンされ、このピークと第2のピーク(網状赤血球ピーク)との間の谷か、または傾斜の減少(網状赤血球「先端」)か、のいずれかに関してより高いFL1値でスキャンされ、そこで、網状赤血球を成熟赤血球から分離するために線が引かれる。この線より上の細胞は、網状赤血球とラベルづけられ、網状赤血球のパーセント(%R)は、合計RBC母集団の一部として決定され、RBCインピーダンス測定から決定されるように、この%Rに試料中のRBCの絶対濃度を掛けて、網状赤血球の絶対濃度を得る。
【0019】
RBC/弁別分析
ゲートされたRBCの3つの散乱信号が分析され、標準化三次元表面に表示される。三次元表面構造の詳細は、下記に説明される。
【0020】
RBC/弁別分析に関するシステムゲイン確立
最初に、MCVおよびMCHCに関する知られている参照値を備えた1セットの正常血液を、二重に流す。全読取値のMCVおよびMCHCの総平均が計算される。次いで、90fL(正規化された)のMCVおよび34(正規化された)のMCHC’を備えたRBC母集団の平均散乱信号が、チャネル125+/−3、すなわち各スケールの中心(CELL DYN(登録商標)4000は、全散乱チャネルに関する256チャネルリニアスケールを有する)になるように、各散乱チャネル(IAS、PSS、IAS’またはALL)に関するゲインが調整される。あるいは、適切な屈折率を有する安定したビーズか、または安定したヒトRBCが、標準化されたシステムの各散乱チャネル数の平均でラベル値割り当てされ、標準粒子として使用されることが可能である。
【0021】
三次元表面構造
第1のステップとして、三次元マップの理論的モデルが、ミー散乱理論に基づいて構成される。知られているMCVおよびMCHCを備えた赤血球の散乱信号を、完全に表面に適合させるために微調整が行われる(これは、吸収のため、488nmでヘモグロビン溶液の屈折率を正確に測定することが困難であるため、誤りが発生する可能性があるからである)。ミー散乱理論は、垂直に照射された均質な球形に関するマクスウェルの方程式の解法に基づいている。理論は、一定の屈折率を有する球形によって散乱される強度の計算方法を提供する(Kerker、Bohren、およびHuffman)。理論は、下記の入力パラメータを必要とする。
a)球形の屈折率。これは、球形が吸収するときに、複素数である。
b)媒体の屈折率(媒体は、光を吸収してはならない)。
c)照射に使用される光の波長および偏光。
d)容積から計算することができる球形の直径。
【0022】
モデルの仮定の1つは、球形は、固定された強度で照射されるということである。この近似は、球形を照射するビームの直径が、球形の直径よりも大きい(およそ10倍)場合に有効である。RBCのために行われる基本的な仮定は、RBCが球形であり、均質であるということである。これは、細胞の屈折率が、細胞のいずれの場所でも同一であることを意味する。ミー散乱理論アルゴリズムは、均一電磁場におけるマクスウェルの方程式の数値解法に基づいている。
【0023】
ミー理論アルゴリズムは、強度分布に角度シータを与えるだけである。これは、ビームが伝播する方向と観察の方向との間の角度である。これは、散乱強度プロファイルが前方方向で対称的であることを意味する。入射直線偏光に関する異なる角度によって収集される強度を計算するために使用される式は、式1によって与えられる。
【数1】

ここで、i1=|S1(θ)|2
i2=|S2(θ)|2
I=強度(相対数)
λ=波長(真空)
θ=レーザ方向と観察の方向との間の角度
φ=レーザ偏光と観察の方向との間の角度
i1、i2=2つの異なる偏光方向の強度
である。
【0024】
関数Si(θ)は、プログラムによって計算される。プログラムは、すべてに、0.3度で分離された角度で、0度から180度の間でこの関数の値を与える。各角度で、この角度の値は、絶対値の平方によって得られる。角度φは、偏光ベクトルと観察の方向との間の角度である。CD4000において、偏光方向は垂直軸である。したがって、関数I(θ,φ)は、細胞のまわりのすべての場所に散乱光の強度を提供する。前方IASデテクタによって収集される光の量を得るために、強度プロファイルは、収集された角度に対して積分することができる。プログラムに使用される積分の数値方法は、トラペジウム方法である。φは2πに対して積分されるため、前方角度における散乱に関する式は下記のようになる。
【数2】

ALLデテクタからの信号は、細胞がレーザビームを通過するときの最大強度低下に等しい。ALL信号は、合計光損失である。これは、散乱吸光係数とも呼ばれ、BohrenおよびHuffmanによって開発されたアルゴリズムによって計算することができる。
【0025】
デテクタが、各水平角度シータに関して異なる垂直角度ファイを収集する以外は、PSS信号の計算は簡単ではある。各水平角度φに関して、垂直角度φに関する積分が行われなければならない。この積分は正確であり、そのため近似を行う必要はない。各角度θは、円錐の形状に関連する自己の最小および最大φを有し、これは、CELL DYN(登録商標)4000の場合には円である。sin2(φ)の積分の解法は、式3によって与えられる。
【数3】

この式の中で角度φは半径方向に与えられ、上記公式の角度φよりも小さいπ/4である。これは、ファイが、90度プラスマイナスφmax(垂直収集角度)だからである。cos2(φ)の解法も同様であり、第2項の符号のみが異なる。各角度θに関して、垂直方向に収集される強度を計算することができる。水平最小および最大角度θに対する積分後に、PSSの値が得られる。
【0026】
前方散乱角度の選択
CELL DYN(登録商標)4000前方散乱角度デテクタ(空中でIAS3度から10度)は、容積に対して不感受性である。理論は、収集角度が懸濁媒体内で規定されなければならないことを必要とする。媒体(CELL DYN(登録商標)4000希釈剤シース)の屈折率は、λ25℃max488nmで1.339である。したがって、スネルの法則によって、希釈剤の収集角度は2.24から7.45である。図2Aおよび図2Bは、希釈剤における相対弁別クロス散乱対角度を表示する。弁別クロス散乱は、式2の積分より下の部分未満のものはない。
【0027】
曲線より下の区域は、容積(V)およびヘモグロビン濃度(HC)の相対強度を表す。33(g/dL)のHCで異なるVに関する曲線より下の区域は、2.24度から7.45度の間であまり変化しないが、これは、曲線が、4度より下では容積が高くなるにつれて下がり、4度より上では容積とともに上がるからである。最小ヘモグロビン干渉を有する容積を測定することができるために、4.5度から5.5度の間の角度が選択される。上記図2Aおよび図2B参照。
【0028】
異なる角度における測定は、修正された3リングデテクタを使用して達成される。デテクタは、2.24度から4.5度の角度をカバーする1つの内側リングと、4.5度から5.5度(IAS’)の角度をカバーする第2のリングと、5.5度から7.45度の角度をカバーする第3のリングとを有するように構成される。3つのリングは一緒に、WBC弁別分析に使用される現在のCELL DYN(登録商標)4000IASデテクタによって収集される角度を依然として与える。第2のリングのみから信号を収集することが可能であり、これは、4.5度から5.5度の間である。新しい角度と古い角度とを同時に使用することも可能である。この解決方法は、WBC/弁別およびRBC/弁別分析用に、2つの別個の光学式検出システムが使用される先行技術に対して利点を有する。本発明は、WBC/弁別およびRBC/弁別分析の両方に同時に同一の光学式検出システムを使用することを可能にする。この解決方法は、角度の異なるセットで散乱光を収集する様々な可能性を生み出す。
【0029】
三次元(3D)細胞分析
RBCが完全な球形であると仮定すると、3つの散乱信号、IAS、IAS’、およびPPS(またはALL、IAS’、およびPPS)は、主に、2つのRBCパラメータすなわちVおよびHCに応じる。すべての可能なVおよびHCの組み合わせが一緒に、空間に表面を形成する。空間におけるIAS’、ALL、およびPPSの表面の簡略にされた説明が、図3に示される。単一細胞のVおよびHCがどのように得られるかという原則を説明するために、三次元における表面の小さな部分のみが表示される。表面は実際には湾曲しているが、表面は平面であると仮定する。しかし、単一のRBCのVおよびHCを見出すために、同一の原則を表面に適用することができる。システムが完全に標準化されるときには、すべての球形RBCは、表面のまわりに非常に近接して分布される。鎌状細胞等の異常な形状のRBCは、表面からより離れている信号を生成する。このようにして、異常な細胞形状を識別するのに、RBC信号の表面からの距離を使用することができる。
【0030】
正確には表面上にない細胞のVおよびHC情報を見出す方法は、図3の細胞Mを使用して、下記に説明される。この細胞のVおよびHCをもっとも表す可能性がある表面上の点は、表面上のもっとも近接した点である。実際には現実の表面はないが、三次元における所与のVおよびHC値を備えた知られている点のセットの位置がある。図3の等V線および等HC線の交差は、これらの点を表す。正確にはこの表面にはない点のVおよびHC値を得るために、この表面上のもっとも近接した3点が見出される。この場合、3つのもっとも近接した点は、1、2、および3である。1から2へのベクトルおよび1から3へのベクトルは、法線を計算することができる表面の小さな部分を規定する。点Mを通って法線に平行なベクトルの表面との交差を計算して、点Iが見出される。点Iは、表面上の細胞の投影を表す。交差が見出されると、ベクトルaおよびbを計算することができる。aおよびbの長さを使用して、3点の値の間を補間し、細胞(点M)のVおよびHCを得ることができる。IAS方向のみにおける表面への距離のすべての細胞のヒストグラムを作ることによって、表面がIAS信号に関して正しい場所にあるか否かを見ることができる。表面がIAS信号に関して正しく設定される場合には、ヒストグラムのピークはチャネルゼロである。これは、同一数の細胞が表面の両側にあることを意味する。同一のことがALLおよびPPS信号に当てはまる。下記に示されるように、3つの信号方向における表面への距離に関する3つのヒストグラムが、正しい表面を見出すために有用なツールであることが判明した。
【0031】
三次元表面を見出す
ミー散乱理論は、知られている屈折率を有する完全球形からの信号を予測する。屈折率およびVの範囲に関する信号を計算することによって、表面上の点を見出すことができる。ミー理論は、信号強度の相対数のみを提供する。したがって、信号の三次元の正確なチャネル数は、これらを表面に正確に配置するために、ゲイン係数を掛けることによって計算されなければならない。これらの係数を見出すのを可能にするために、屈折率がヒト赤血球MCHCの臨床範囲内に入る3つの異なる炭化水素(ヘプタン、ノナン、およびドデカン)が使用された。3つの炭化水素の各々は、懸濁媒体内で強く混合されるときには、同一の屈折率を有する様々なサイズの滴を生成する。これらの3つのオイルの各々は、屈折率が異なるため(炭化水素は吸収がない)、互いに異なる、明確なV信号分布トラックを作る。次に、ミー理論によって作られる表面の正確度は、表面上のもっとも近接した点への実際の信号の距離を測定することによってチェックされる。たとえば、表面が3つの炭化水素によって生成される信号へ完全に適合するのであれば、3つのヒストグラムのピークの表面への距離はゼロである。
【0032】
血液試料に関する表面を作ることは、488nmでのヘモグロビンによる光吸収のため、より複雑である。吸収を訂正するために、炭化水素に関する三次元表面を形成するために使用されるシミュレーションに吸光度が加えられなければならない。理論値をチャネル数へ転換するために3つの炭化水素に関して使用されるすべてのゲイン設定は、一定に保たれる。このようにして、すべての可能なRBC事象を規定する完全な表面が形成される。正常な試料のRBCは、表面のまわりに正常に分布されなければならない。この表面は、機器の較正および標準化のための日常QCチェックに関してさらに努力することなく、試料が分析されている間にシステム標準化をモニタするツールも提供する。各試料に関して、表面のまわりのRBCの三次元ヒストグラムは、信号処理中に作られる。表面のまわりの正常なRBC分布が対称的ではない場合には、機器は標準化から外れる(たとえば、流体素子工学的なまたは電子工学的な問題)。
【0033】
例示のために、ここに検討された好適な実施態様の多数の使用が示される。下記の検討は、例示的な目的のためのみに提供され、この検討は網羅的ではない。具体的に下記に検討されるのは、統合された血液細胞分析、WBC弁別分析に使用されるのと同一の光学式検出システムを使用して、多角光散乱および蛍光ヘマトロジーアナライザーにおいて、容積、ヘモグロビン含有量、正常および異常な細胞形状、網状赤血球の容積、およびヘモグロビン含有量用のRBC弁別分析を行い、かつシステム標準化を同時にモニタするために開示された実施態様を使用する方法である。これは、請求される発明の範囲をいずれにも限定しない。
【0034】
例1.
開示された装置は、修正されたCELL DYN(登録商標)4000(CD4000)システムである。CD4000デテクタおよびプリアンプボードは、白血球弁別(WBC/弁別)分析と赤血球弁別(RBC/弁別)分析との両方に同一のデテクタを使用するために、修正される。修正されたデテクタを示す図は、図1Aに見られる。3つのゾーンが形成される。中心矩形ゾーン(ゾーン1)は軸方向光損失(0度、ALL)用である。中間ゾーン(ゾーン2、2.24から7.45度、IAS)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5から5.5度(IAS’)である。プリアンプボードは、図1Bに描かれるように修正された。修正されたプリアンプボードは、すべての3つのリングから信号を電気的に加算することによってIAS出力を形成する。この修正されたプリアンプボードからの可能な出力は、ALLおよびIASであるか、またはIAS’およびIASである(または配線し直すならば、ALLおよびIAS’である)。IAS’ゲインは、オンボードデュアルインラインパッケージ(DIP)スイッチによって設定される。ALLおよびIASは、WBC弁別のために使用され、ALLおよびIAS’か、またはIAS’およびIASかの組み合わせのいずれかが、RBC弁別分析のために使用される。三次元RBC弁別分析ために使用される第3の角度は、90度側方散乱である。
【0035】
例2.
この実験のために、米国特許第5,656,499号および第5,631,165号、発明の名称「自動分析を行うための方法および装置」に記載されたCD4000システムが、例1に記載されたように、3リングデテクタおよび新しいプリアンプボードを備えて修正された。約112.5μlの正常全血試料が、試料吸引プローブによって、約10.513μlのCD4000希釈剤シースを含んでいるRBCカップ内に置かれ、混合される。次いで、希釈された試料は、シース状インピーダンス開口部へ運ばれ、米国特許第5,656,499号および第5,631,165号に記載されるように、絶対RBC計数を電気的に決定する。約450μlの希釈された試料は、CD4000網状赤血球カップ内に移され、このカップは約450μlの網状赤血球試薬を含んでおり(米国特許第5,691,204号、1997年11月25日。「網状赤血球の迅速分析用の組成物および方法(Compositions and methods for the rapid analysis of reticulocytes)」)、混合される。次いで、準備された試料は、検出のために、シース状光学式フローセルへ運ばれる。WBCおよびNRBCは、RBCゲートによって排除され、網状赤血球は、米国特許第5,656,499号および第5,631,165号に記載されるように、識別され定量化される。同時に、3つの散乱信号は、各事象に関しても測定され、標準三次元表面に表示される。図4Aおよび図4Bは、三次元表面にきっちりと重なり合う正常血液の正面図および側面図を示す。完全に標準化され較正されたシステムで、図4Bに示されるように、約50%の信号が表面より上になり、50%が表面より下になる。
【0036】
例3.
鎌状細胞を含む臨床血液試料が、例2に記載された開示された装置を流れた。図5Aおよび図5Bは、それぞれ、試料の正面図および側面図を表示する。見ることができるように、異常な形状の鎌状細胞のため、細胞母集団はかなり分散しており、側面図は、信号が三次元表面から外れることを示す。各事象の表面からの距離に基づいて、本発明の方法は、異常な形状のRBCのパーセントを概算することができる。同一試料のTycko(バイエルH*1)による先行技術の二次元分布は、図5Cに表示される。図5Cから見ることができるように、二次元分布は、異常な細胞形状を球形の正赤血球から区別しない。その上、異常な形状を有するRBCの有意な数は、二次元マップから外れ、それによって容積測定から除外される。
【0037】
例4.
高WBC試料およびWBCのRBCゲートからの分離および除外のCD4000サイトグラム(FL1対IAS)は、染色された網状赤血球および成熟RBCを含み、図6Aに示される。図4Aに示されるように、本発明の方法は、RBC/弁別分析の前に、WBCをRBC母集団からはっきりと識別し排除する。ゲートされた母集団のFL1ヒストグラムは、図6Bに示される。逆に、Tycko(バイエルH*1)によって開示された先行技術は、WBCをRBC母集団からはっきりと区別しないかまたは分離しない(図6C参照、先行技術による同一試料のRBC分布)。したがって、先行技術の方法は、様々な白血病の患者、特に、慢性リンパ球性白血病(CLL)の患者からの上昇WBC試料では、誤った赤血球MCVおよびMCHC結果を生成する可能性があるが、それは、CLLのリンパ球が、RBCと同じほど小さいだけではなく、RBCと同じほど小さい光散乱を生成するには壊れ易いからである。
【0038】
例5.
小赤血球(図7A)、正赤血球(図7B)、および大赤血球(図7C)のRBC試料の細胞ヘモグロビン含有量(HC)対容積(V)の二変数分布が、本発明の方法によって分析された。2本の固定線が、正常範囲のまわりに垂直に且つ水平に引かれ、各試料におけるサイズおよびヘモグロビン含有量のRBC異常性の異なる組み合わせを識別し計数する。下記の表1a、1b、および1cは、各カテゴリーの細胞の概算されたパーセンテージを示す。提供された情報に基づいて、患者の状態の赤血球不同症、小赤血球症、大赤血球症、血色素減少症、および血色素増加症の重大度レベルを決定することができる。
【表1a】

【表1b】

【表1c】

【0039】
例6.
平均細胞容積(MCV)の回帰統計およびプロット。図8Aは、本発明対Tycko(バイエルH*1)による先行技術の結果を表し、図8Bは、正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCV結果(流体力学的に集束された細胞を使用した電気インピーダンス測定)の結果を表す。
【0040】
例7.
MCHCの回帰統計およびプロット。図9Aは、本発明対Tycko(バイエルH*1CHCM)による先行技術の結果を表示し、図9Bは、正常および臨床試料のセットにおける、本発明対CELL DYN4000MCHC(インピーダンスMCVおよびヘモグロビンのCELL DYN4000比色分析測定から計算された結果)の結果を表示する。
【0041】
例8.
MCHの回帰統計およびプロット。図10Aは、本発明対Tycko(バイエルH*1MCH)による先行技術の結果であり、図10Bは、正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCH(インピーダンスRBC計数およびヘモグロビンの比色分析測定から計算された)の結果である。
【0042】
例9.
開示された方法による正常および臨床試料のセットにおける平均網状赤血球容積(RETV)と合計RBCMCVとの比較が、図11Aに示され、開示された方法による正常および臨床試料の同一のセットにおける網状赤血球MCHC(RETHC)と合計RBCMCHCとの比較が、図11Bに示される。
【0043】
例10.
約1.67μLの全血試料が、試料吸引プローブによって、約2800μlの上記例2に使用されたものと同一の希釈剤を含んでいるRBCカップ内に置かれ、混合される。次いで、希釈された試料は、アボットCELL DYN3200シース状光学式フローセルへ運ばれ、細胞1つずつの容積およびヘモグロビン測定に関する信号を収集する。アボットCELL DYN3200の光源は、5mワットヘリウムネオンレーザであり、そのデテクタは、1度から3度、および3度から10度2つの前方光散乱信号、および90度+/−30度の側方散乱信号を収集するように構成される。試料のFSCファイルは較正された三次元表面で分析され、本発明の開示された方法を使用して、ヘリウムネオンシステムに関して作られる。157個の正常および臨床試料、および、浸透圧検査からの66個の試料がシステムに流され、結果の比較は図12Aおよび図12Bに示される。浸透圧実験は、血液を希釈するために使用される両方の試薬(CELL DYN3200およびH*1)の塩濃度を変えることによって行われた。検査された浸透圧範囲は、175mOsm/Lから500mOsm/Lであった。
【0044】
上記を考慮して、前述の記載から、先行技術に対して本発明の多くの利点が明らかである。一定の代表的な実施態様および詳細が、発明を例示する目的のために示されているが、特許請求の範囲に規定された本発明の範囲から逸脱せずに、様々な変更および修正を行うことができる。
【図面の簡単な説明】
【0045】
【図1A】白血球弁別(WBC/弁別)分析と赤血球弁別(RBC/弁別)との両方の分析に同一のデテクタを使用するために、修正されたCELL DYN(登録商標)4000デテクタを示す図である。3つのゾーンが形成される。中心矩形ゾーン(ゾーン1:ALL用に0度)は軸方向光損失用であり、中間ゾーン(ゾーン2:IAS用に2.24から7.45度)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5から5.5度(IAS’)である。
【図1B】CELL DYN(登録商標)4000プリアンプボードの修正を示す。IAS出力は、すべての3つのリングからの信号を電気的に加算することによって形成される。この修正されたプリアンプボードからの可能な出力は、ALLおよびIASであるか、またはIAS’およびIASである(または配線し直すならば、ALLおよびIAS’である)。WBC弁別および三次元RBC弁別の両方分析ために使用される第3の角度は、90度偏光側方散乱である。
【図2A】488nmの波長での容積およびヘモグロビン濃度の異なる値に関する前方角度における弁別クロス散乱を例示する。
【図2B】488nmの波長での容積およびヘモグロビン濃度の異なる値に関する前進角度における弁別クロス散乱を例示する。
【図3】細胞のV&HCデータがどのように三次元表面から得られるかの原則を説明するための三次元表面の小さな部分の例である。
【図4A】開示された三次元表面における正常血液の正面図である。米国特許第5,656,499号および第5,631,165号に開示されたCELL DYN(登録商標)4000システムが、例1に記載されたように、開示された3リングデテクタおよびプリアンプボードを備えて修正され、示されたデータを収集するために使用された。
【図4B】上記図4Aに示されたものと同一の正常な血液の側面図であり、三次元表面を囲む非常に密接な対称分布を示す。完全に標準化され較正されたシステムでは、示されるように、約50%の信号が表面より上になり、50%が表面より下になる。シンボル:Oは球形の成熟赤血球であり、Rは染色された網状赤血球であり、Xは非球形の異常形状の赤血球であり、Wは白血球であり、Pは血小板である。
【図5A】図4Aに示されたものと同一の三次元表面における鎌状細胞試料の正面図である。図示のように、細胞母集団は、異常な形状の鎌状細胞のためにかなり分散している。
【図5B】三次元表面における同一の鎌状細胞試料の側面図である。異常な形状の鎌状細胞からの散乱信号は、三次元表面から外れ、それによって、非対称分布になり、正常な赤血球よりも三次元表面からかなり離れる。シンボル:Oは球形の成熟赤血球であり、Rは染色された網状赤血球であり、Xは非球形の異常形状の赤血球であり、Wは白血球であり、Pは血小板である。
【図5C】Tyckoによって開示された先行技術(バイエルH*1)による、同一試料の二次元分布である。
【図6A】高いWBC試料のCELL DYN(登録商標)4000RBC/網状赤血球サイトグラム(FL1対IAS)を表示する。これは、染色された網状赤血球および成熟RBCを含むRBCゲートから、WBCのはっきりとした分離および除外を明らかにする。ゲートされたRBC母集団は、網状赤血球計数、および、成熟RBCおよび網状赤血球の両方のV&HCの測定のために使用される。
【図6B】成熟RBCに関するおよび網状赤血球に関する領域を示すゲートされたRBC母集団のFL1ヒストグラムである。
【図6C】Tyckoによって開示された先行技術によって分析された同一試料の二次元分布である。WBCはRBCからはっきりと分離されていない。
【図7A】小赤血球RBC試料のV&HCの二変数分布を表示する。
【図7B】正常なRBC試料のV&HCの二変数分布を示す。
【図7C】大赤血球RBC試料のV&HCの二変数分布を表示する。
【図8A】正常および臨床試料のセットにおける、本発明対Tyckoによる先行技術(バイエルH*1)の平均血球容積(MCV)の結果の回帰プロットを示す。
【図8B】図8Aと同一の正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCV結果(流体力学的に集束されたインピーダンス開口部を使用する電気抵抗測定)のMCV結果の回帰プロットを示す。
【図9A】図8Aと同一の正常および臨床試料のセットにおける、本発明対Tyckoによる先行技術(バイエルH*1CHCM)のMCHC結果を表示する。
【図9B】図8Aと同一の正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCHC(インピーダンスMCVおよびヘモグロビンのCELL DYN4000比色分析測定から計算された結果)のMCHC結果を表示する。
【図10A】図8Aと同一の正常および臨床試料のセットにおける、本発明対Tyckoによる先行技術(バイエルH*1MCH)のMCH結果を表示する。
【図10B】図8Aと同一の正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCH(インピーダンスRBC計数およびヘモグロビンの比色分析測定から計算される)のMCH結果を表示する。
【図11A】本発明の方法による正常および臨床試料のセットにおける、平均網状赤血球容積(RETV)と合計RBCMCVとの比較を示す。
【図11B】本発明の方法による同一の正常および臨床試料のセットにおける、網状赤血球MCHC(RETHC)と合計RBCMCHCとの比較を示す。
【図12A】157個の正常および臨床試料および66個の浸透圧試料(詳細は例10参照)を含むセットにおける、633nm(ヘリウムネオンレーザ)光源を使用する本発明対Tyckoによる先行技術(バイエルH*1)のMCVデータの回帰プロットを示す。
【図12B】同一のヘリウムネオンシステムからの本発明対先行技術(バイエルH*1CHCM)のMCHC結果を示す。
【技術分野】
【0001】
(発明の概要)
試料中の哺乳類の赤血球の容積、ヘモグロビン濃度、成熟度、および赤血球形状を決定し、同時にシステム標準化をモニタするための方法および装置が開示される。赤血球分析の前に、赤血球を他の細胞粒子から区別するための方法も開示される。方法は、広範囲の可視スペクトルに対して正確に適用することができる。全血試料は、中性pHの等張緩衝溶液に非イオン性界面活性剤を含む試薬溶液で処理され、赤血球は、選択された波長で単一ファイルにおける光のビームを通過し、1つの光損失信号、選択された角度間隔での1つの前方角度光散乱信号、および第3の側方角度光散乱信号の結果として得られる大きさによって、あるいは、選択された角度間隔での2つの前方角度光散乱信号、および第3の側方角度光散乱信号の結果として得られる大きさによって、初期的なサイトグラムを獲得し、容積およびヘモグロビン濃度のグリッドラインを含む予め較正された三次元表面に、1点ずつサイトグラムを投影し、三次元グリッド表面への各投影された交差(インターセプト)の場所によって、赤血球容積およびヘモグロビン濃度の正確な値を決定する。
【0002】
本発明は、体液における哺乳類の赤血球(RBC)および白血球(WBC)の弁別の自動分析とシステム標準化の同時モニタとの方法および装置に関する。本発明は、特に、同一の光学式検出装置を使用してRBCおよびWBCの両方の弁別分析を行うことができる、マルチパラメータヘマトロジーアナライザーまたはフローサイトメータ等の多角光散乱および蛍光装置に関する。本発明は、より詳細には、(i)全血中における容積、ヘモグロビン含有量、細胞形状、および成熟度に関してRBCを分析するための方法、(ii)未熟RBC(網状赤血球)容積およびヘモグロビン含有量を決定するための正確な方法、(iii)RBC弁別のために血液試料が分析されている間に、システム標準化を継続してモニタすることができるRBC方法、(iv)1つの試薬を使用して、成熟RBCおよび網状赤血球の両方の容積およびヘモグロビン含有量を測定することができる方法、および(v)同一の光学式検出システムを使用して、WBCおよびRBCの両方の弁別分析を行うことができる装置とに関する。
【背景技術】
【0003】
従来のヘマトロジー方法、すなわち、細胞サイズ、細胞形状、色(ヘモグロビン含有量用)、および封入体に関するRBC形態学に関する患者血液塗抹標本の顕微鏡的検査は、診断へ導きかつ患者の臨床状態をモニタする豊富な情報を提供する。しかし、この手動方法は、非常に主観的であり、かつ時間がかかるものであるという事実に加えて、標準以下の血液フィルムから、きわめて誤解を招く恐れのある印象を引く可能性がある。過去30年の間に、大量の実験室作業量を取り扱いかつ労力を減少する、多数の自動ヘマトロジーアナライザーが利用可能になっている。これらの機器の大半は、電気インピーダンス測定によるか、または比色分析ヘモグロビン測定と組み合わされた光散乱光学式測定によって、赤血球の平均血球容積(MCV)および平均血球ヘモグロビン濃度(MCHC)を測定する。これらのシステムからの細胞分析における形態学的情報の不完全性またはあいまい性から、ヘマトロジー実験室における5から10パーセントの試料は、日常的に、顕微鏡的方法を使用して細胞形態学に関する塗抹標本検査を受ける。RBC形態学的分析の点におけるより進歩したヘマトロジーアナライザーは、テクニコンH*1(Technicon H*1)およびバイエルアドヴィア(Bayer ADVIA)である。両システムは、米国特許第4,735,504号に記載されたD.H.Tyckoの教示にしたがって、細胞1つずつに基づいて同時に赤血球の容積およびヘモグロビン濃度を測定するように構成されている。
【0004】
D.H.Tyckoに付与された米国特許第4,735,504号には、粒子の容積および屈折率を決定するための方法および装置が記載されている。VおよびHCを測定するための方法は、2つの選択された角度間隔の前方光散乱信号S1およびS2による卵形(ovolumetrically)形状のRBCであり、容積(V)およびヘモグロビン濃度(HC)を決定することが開示されている。この方法の欠点は、下記の通りである。1)RBCからのヘモグロビン吸収を避けるために、光源の波長が十分長くなければならず(たとえば633nm)、これによって、マルチパラメータ血液細胞分析用のより適切な光源(たとえば488nm光源)を選択することができない。2)二次元(2D)マトリクスは、異常な細胞形状に関するいずれの情報を提供しないが、それは、そのような細胞からの信号は、所定の二次元マトリクスでは誤った場所に入り、したがって、V&HCに関する不正確な臨床データを生成するからである。3)二次元マトリクスは、システム標準化におけるシフトに関するいずれの情報を提供せず、これは、一定の血液試料における凝血塊によって生じる流体素子工学的な通過における不安定性、またはシステムの電子工学における不安定性のため、いずれも警告無しで発生する可能性のある現象である。4)二次元散乱方法は、WBCおよび有核赤血球(NRBC)を、成熟RBCまたは染色された網状赤血球から識別してはっきりと分離することができない。WBCおよびNRBCは、その核のため、赤血球よりもかなり多くの散乱を生成し、VおよびHC分析の前に、RBC母集団からはっきりと除外されるのでなければ、MCV、ヘマトクリット(Hct)、MCHC、および平均血球ヘモグロビン(MCH)に関する臨床結果は、上昇WBCまたはNRBC試料では非常に誤解を招きやすい。
【0005】
D.H.Tyckoに付与された米国特許第5,194,909号には、赤血球のVおよびHCを測定するための方法および装置が教示されている。この技術と米国特許第4,735,504号における先の教示との相違は、長い波長(633nm)での1つの前方光散乱信号(予め選択される)と、抵抗パルスサイジング開口部からの第2の信号とを使用して、二次元マトリクスが形成されることである。この方法の欠点は下記の通りである。1)方法は、検出システムの2つの独立した源を必要とし、これは、2つの異なる検出システムからの2つの信号の同期等の不必要な複雑な状態を生み出す。2)RBCからのヘモグロビン吸収を避けるために、光源の波長が十分長くなければならず、これは、マルチパラメータ血液細胞分析用の光源の選択を限定する。3)二次元マトリクスは、異常な形状のRBCに関するいずれの情報を提供せず、したがって、V&HCに関する不正確な臨床データを生成する。4)二次元マトリクスは、システム標準化におけるシフトに関するいずれの情報を提供せず、これは上記に説明されたように、電子工学または流体素子工学における不安定性のため、いずれも警告無しで発生する可能性のある現象である。
【0006】
Fanらへ付与された米国特許第5,284,771号には、試薬組成物および細胞球形化におけるその使用が開示されている。試薬組成物は、向きによるノイズを排除するために赤血球を球形づけるための両性イオン界面活性剤と、網状赤血球を染色するためのOzxazine750とを含む。光学式検出システムの光源は633nmヘリウムネオンレーザであり、染色された網状赤血球は、光散乱/吸収技術によって識別される。網状赤血球の蛍光測定は、この特許では例示されていないか、または請求されていなかった。この開示の発明者らは、網状赤血球のV&HCの測定に関しては請求していなかったが、テクニコンH*1システムを使用して細胞1つずつに基づいて、赤血球の容積およびヘモグロビンを同時に測定する上述のTyckoの方法の使用を記載した。Fanらの教示において、網状赤血球の染色手順は、手動調製、手動供給、および2分以上の染色時間を必要とする。発明者らは、RBCおよび網状赤血球の両方のV&HCは、Tyckoの方法によって測定されるが、RBCおよび網状赤血球に使用される試薬は、組成が完全に異なると記載した。テクニコンH*1のRBCに関するTyckoの二次元マトリクスを作るために使用される試薬は、Tyckoの開示に記載されるように、RBCを球形にして固定し、一方、網状赤血球に関して使用される試薬は、いずれの固定剤を含まない緩衝液内でRBCを球形にする。その上、網状赤血球を染色するのに使用される青染料による吸収は、染色された細胞のV&HCの測定における散乱信号の大きさに干渉する。上述の問題は、Fanらの教示による網状赤血球のV&HCに関する誤った臨床データへ導く可能性がある。上述のように、V&HC測定に関するTyckoの方法は、ヘモグロビンが非常に透明である領域では単色光を発する光源を必要とする。これは、光源の利用可能性を制限する(λmaxは、600nmより大きくなければならない、赤ヘリウムネオンレーザ等)。別の制限は、吸収のためにまたは蛍光放射のために染料を励起するために、同一波長を使用しなければならないため、利用可能な染料の選択である。この条件下で、染料は、赤光を強力に吸収する青染料でなければならない。この特許では、網状赤血球のV&HCの測定に関しては、何の請求もされなかった。
【0007】
Collelaらに付与された米国特許第5,350,695号には、疑似吸収に関して測定された吸収信号を調整する方法が加えられていることを除いて、米国特許第5,284,771号で先に開示されたものと同一の網状赤血球を特徴づけるための方法および試薬が開示されている。この開示の第12欄、第1段落の記載によると、米国特許第5,284,771号に開示された方法の主要な問題は、テクニコンH*1機器の吸収信号が、吸収プリアンプのノイズと同一レベルであるということである。したがって、染色された網状赤血球からの吸収信号の信号対雑音(S/N)比を改良するために、数学的モデルを展開しなければならなかった。この特許に開示された数学的訂正を備えてさえ、染色された網状赤血球から吸収信号の満足のいくS/N比を生成することは、この方法の主要な問題であると思われる。その上、光吸収も、粒子の光散乱の大きさに干渉する。
【0008】
Fanらへ付与された米国特許第5,360,739号には、青の励起可能な蛍光染料、すなわちアクリジンオレンジが含まれることを除き、先の4つの特許に開示されたような方法および試薬が開示されている。この方法の教示を実行するために、2つの光源を必要とする。一方の光源は、青の励起可能な蛍光測定用(アルゴン/イオンレーザ)であり、他方の光源は、細胞の容積およびヘモグロビンの測定用(ヘリウムネオンレーザ)である。この方法の欠点は、同期および標準化のために検出システムが不必要に複雑になることであり、機器製造コストが非常に上昇する。
【0009】
Collelaらに付与された米国特許第5,438,003号には、全血における網状赤血球の識別および特徴づけに使用するために、先の4つの特許に示されたものと同一の試薬組成物が開示されている。この特許のすべての請求項は試薬組成物に関しており、網状赤血球のV&HCの測定の方法に関する請求はなされていない。しかし、ヘリウムネオン(633nm)光源を使用する光散乱/吸収によって、成熟RBCから網状赤血球を分離するにあたり、開示された方法では「疑似吸収」およびヘモグロビン干渉をどのように訂正しているかを、本文内で新規に非常に長く説明している。結果として、米国特許第5,438,003号に示されたサイトグラムは、成熟RBC信号から不十分に分離された網状赤血球信号を明らかにしている。開示された光散乱/吸収方法によって、成熟RBCから母集団がよく分離されない限り、網状赤血球のV&HCを正確に測定することは非常に困難である。さらに、この開示の例は、開示された方法が、V&HCの測定に関する二次元マップを作るのに使用される試薬とは、pH、浸透圧、球形剤、および緩衝液がまったく異なる、2つの試薬を必要とすることを明らかにしている。加えて、H*1RBC方法は、非常に短いインキュベーション時間を有し、一方、開示された試薬における網状赤血球の染色時間は2分である(30秒対120秒)。RBC球形づけプロセスは、非常に敏感な可逆的なプロセスであり、2つの選択された光散乱信号に基づいて、一貫して再現可能なV&HCデータを得るために、正確なタイミングを必要とする。Collelaらは、V&HCに関するいずれの時間検査データを開示していないし、この特許ではいずれの網状赤血球のV&HCデータも開示していない。
【発明の開示】
【発明が解決しようとする課題】
【0010】
先行技術のこれらの態様を考慮すると、完全なRBC弁別分析、およびより正確な網状赤血球計数、およびV&HC測定のための、改良された方法および装置を提供することが望ましい。本発明の目的は、単一の光源および光学式検出システムを使用して、WBCおよびRBCの両方の弁別分析を行うことができる装置を提供することである。本発明の別の目的は、細胞1つずつに基づいた臨床的に有用なMCHC測定、および異常な形状のRBCの検出および定量化を含む、より完全なRBC弁別分析を提供することである。本発明のさらに別の目的は、成熟RBCおよび網状赤血球の両方のV&HC測定のために使用することができる、単一の網状赤血球試薬を提供することである。本発明のさらなる目的は、非常に狭い範囲内に光源の選択を限定しない方法を提供することである。本発明のさらに別の目的は、システムの安定を継続してモニタするためのRBC/弁別方法を提供することである。本発明のこれらの目的およびさらなる目的は、下記の説明および図面から当業者には明らかになる。
【課題を解決するための手段】
【0011】
本発明は、(1)多角光散乱および蛍光ヘマトロジーアナライザーまたはフローサイトメータでRBC弁別を自動分析し、システム標準化を同時にモニタするための方法および装置に関し、(2)同一の光源および同一の光学式検出システムを使用して、WBCおよびRBCの両方の弁別分析を行うことができる装置に関し、(3)特に、全血または体液における、容積、ヘモグロビン含有量、細胞形状、および成熟度に関してRBCを分析するための方法に関し、(4)幼児および血液透析患者における鉄欠乏性貧血の診断に有用な、網状赤血球(未熟RBC)のV&HCを決定するための正確な方法に関し、(5)血液試料が分析されている間に、システム標準化を継続してモニタすることができるRBC方法に関し、特徴は、システムドリフトによって生じる誤った臨床データを報告する可能性を排除する。上記目的は、内蔵測定装置として明確な予め較正された三次元(3D)表面を使用して達成され、三次元表面は、理論的データ、および多角光散乱および/または光損失測定によって生成される実際のデータ(事象)の両方を使用して形成される。正常なRBCの各事象は、したがって、このごく薄い三次元表面に入らなければならない。細胞特徴の大半が、表面より下または上にあり、別の層を形成する場合には、電子工学的または流体素子工学的なシフトのいずれかのため、対象のチャネルが標準外であることが指摘される。3つまたはそれ以上の光散乱および/または光損失信号の多次元分析は、ある程度の内部一貫性を提供する。異常な形状のRBCは、表面からもっとも近い各事象の距離によって規定されるが、それは、すべての正常なRBC信号(CELL DYN4000希釈剤シースで球形づけられる)が、表面に近接するからである。網状赤血球は、CELL DYN4000網状赤血球試薬における核酸ステインで処理された各事象の蛍光強度によって規定される。細胞のV&HCは、ALL/IAS’/PSS、またはIAS/IAS’/PSSによって形成された、三次元マトリクスにおける各事象の場所に基づいて決定される。上記目的を達成するために、CELL DYN4000デテクタは、3つのゾーンを形成するように修正された。中心矩形ゾーン(ゾーン1)は、軸方向光損失(0度、ALL)用であり、2.24度から7.45度(IAS)である現在のCELL DYN4000中間角度(ゾーン2)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5度から5.5度(IAS’)である。修正されたデテクタは、本開示では3リングデテクタと称される。三次元表面は、前述の3リングデテクタによって生成された2つの角度(ALLおよびIAS’、またはIASおよびIAS’)、および90度偏光側方散乱(PSS)信号を使用して作られる。三次元の原則は、広い範囲の光源波長(たとえば、488nm、532nm、または633nm)を備えた光学式検出システムに適用可能である。
【0012】
本発明およびその利点をより完全に理解するために、添付の図面とともに取られた下記の説明が参照される。
【発明を実施するための最良の形態】
【0013】
A)装置
開示された装置の1つの実施態様は、米国特許第5,656,499号および第5,631,165号、発明の名称「自動分析を行うための方法および装置(METHOD AND APPARATUS FOR PERFORMING AUOMATED ANALYSIS)」に開示された、修正されたCELL DYN(登録商標)4000ヘマトロジーアナライザーである。本発明の開示された方法を行うために、CELL DYN(登録商標)4000システムデテクタおよびプリアンプボードは修正された。修正されたデテクタを示す図が、図1Aに表される。3つのゾーン(3リング)が形成される。中心矩形ゾーン(ゾーン1)は軸方向光損失(0度、ALL)用であり、中間ゾーン(ゾーン2、2.24から7.45度、IAS)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5から5.5度(IAS’)である。CELL DYN(登録商標)4000プリアンプボードも、図1Bに例示されるように修正された。修正されたプリアンプボードは、すべての3つのリングから信号を電気的に加算することによってIAS出力を形成する。この修正されたプリアンプボードからの可能な出力は、ALLおよびIASであるか、またはIAS’およびIASである(または配線し直すならば、ALLおよびIAS’である)。ALLチャネルのゲインが4に設定されるのであれば、IAS’は、ALLの代わりに、出力へルートづけられる。IAS’ゲインは、オンボードデュアルインラインパッケージ(DIP)スイッチによって設定される。ALLおよびIASは、WBC/弁別のために使用され、ALLおよびIAS’の組み合わせ、またはIAS’およびIASの組み合わせのいずれかが、RBC/弁別のために使用される。三次元RBC/弁別分析ために使用される第3の角度が、側方散乱信号であり、これは、125度円錐から構成される。これは、本質的にレーザ光の垂直偏光を保存するため、側方偏光散乱(PSS)と呼ばれる。125度全角度円錐の同一側方収集システムも、米国特許第5,691,204号に開示された試薬のRNAステインによって染色された網状赤血球の蛍光信号を収集する。この特徴は、単一の試薬および単一の光源から、網状赤血球の識別を可能にし、且つ成熟RBCおよび網状赤血球の両方のV&HC測定を可能にするものであり、これは、本発明の独特な特徴である。
【0014】
B)方法および試薬
WBC/弁別試薬
WBC弁別分析およびNRBC定量化に使用されるCELL DYN(登録商標)4000WBC試薬の組成物は、米国特許第5,516,695号に開示されており、NRBC分析の方法は、米国特許第5,559,037号に開示されている。
【0015】
RBC/弁別試薬
CELL DYN(登録商標)4000希釈剤シースの組成物は、米国特許第5,656,499号に開示されており、CELL DYN(登録商標)4000網状赤血球試薬組成物および方法は、米国特許第5,691,204号に開示されている。希釈剤シースおよび網状赤血球試薬の両方は、システムに予め存在する流体素子工学構成のため、開示された方法をCELL DYN(登録商標)4000システムで行うためのものであるが、2つの試薬を1つの試薬に化合して、開示された方法を行うことができる。
【0016】
方法
開示されたRBC弁別分析を修正されたCELL DYN(登録商標)4000で行うために、36.1μlの全血試料が、試料吸引プローブによって、約10.513μlの希釈剤シースを含んでいるRBCカップ内に置かれ、混合される。次いで、希釈された試料は、シース状インピーダンス開口部へ運ばれ、米国特許第5,656,499号および第5,631,165号、発明の名称「自動分析を行うための方法および装置」に記載されるように、試料の絶対RBC計数を電気的に決定する。次いで、約450μlの希釈された試料が、450μlの網状赤血球試薬を含んでいる網状赤血球カップ内に移され、ここで混合され、網状赤血球は染色される。次いで、準備された試料は、検出のために、シース状光学式フローセルへ運ばれる。細胞のストリームは、シースによって囲まれた層流の流体力学的に集束された試料ストリーム内で、本質的に一度に1細胞ずつ、フローセルを通って流れる。フロー軸に垂直な光のビームが、ストリームを照射する。照射された容積における細胞からの光散乱信号は、開示された3リングデテクタ(IASおよびIAS’)によって、および偏光側方散乱(PSS)および緑蛍光(FL1)を検出する2つの光電子増倍管(PMT)によって検出される。これらのパルスの振幅は、デジタル化され、リストモードデータとして保管される。本実施態様において、約20,000細胞が8秒間に計数される。
【0017】
RBC分析
第1に、図6Aに示されるFL1対IASサイトグラムにおいてRBCの左側に表れる信号は、血小板として識別される。第2のステップは、WBCおよびNRBC(もしあれば)を識別しラベルづけることであり、それらの信号は、FL1対IASサイトグラムにおいてRBCより上に表れる。FL1ヒストグラム(図6B)をスキャンして、サイトグラムにおけるRBCゲートの上部縁を決定する。ゲート内の事象は、成熟RBCおよび網状赤血球である。
【0018】
網状赤血球検出
本発明の方法は、十分に高いS/N比(染色された網状赤血球対染色されていない成熟RBC)を有するため、信号を分離するために数学的訂正は必要ない。先の開示(米国特許第5,691,204号)に記載されるように、ゲート内のRBC母集団のFL1ヒストグラムは、成熟RBCのピークに関してスキャンされ、このピークと第2のピーク(網状赤血球ピーク)との間の谷か、または傾斜の減少(網状赤血球「先端」)か、のいずれかに関してより高いFL1値でスキャンされ、そこで、網状赤血球を成熟赤血球から分離するために線が引かれる。この線より上の細胞は、網状赤血球とラベルづけられ、網状赤血球のパーセント(%R)は、合計RBC母集団の一部として決定され、RBCインピーダンス測定から決定されるように、この%Rに試料中のRBCの絶対濃度を掛けて、網状赤血球の絶対濃度を得る。
【0019】
RBC/弁別分析
ゲートされたRBCの3つの散乱信号が分析され、標準化三次元表面に表示される。三次元表面構造の詳細は、下記に説明される。
【0020】
RBC/弁別分析に関するシステムゲイン確立
最初に、MCVおよびMCHCに関する知られている参照値を備えた1セットの正常血液を、二重に流す。全読取値のMCVおよびMCHCの総平均が計算される。次いで、90fL(正規化された)のMCVおよび34(正規化された)のMCHC’を備えたRBC母集団の平均散乱信号が、チャネル125+/−3、すなわち各スケールの中心(CELL DYN(登録商標)4000は、全散乱チャネルに関する256チャネルリニアスケールを有する)になるように、各散乱チャネル(IAS、PSS、IAS’またはALL)に関するゲインが調整される。あるいは、適切な屈折率を有する安定したビーズか、または安定したヒトRBCが、標準化されたシステムの各散乱チャネル数の平均でラベル値割り当てされ、標準粒子として使用されることが可能である。
【0021】
三次元表面構造
第1のステップとして、三次元マップの理論的モデルが、ミー散乱理論に基づいて構成される。知られているMCVおよびMCHCを備えた赤血球の散乱信号を、完全に表面に適合させるために微調整が行われる(これは、吸収のため、488nmでヘモグロビン溶液の屈折率を正確に測定することが困難であるため、誤りが発生する可能性があるからである)。ミー散乱理論は、垂直に照射された均質な球形に関するマクスウェルの方程式の解法に基づいている。理論は、一定の屈折率を有する球形によって散乱される強度の計算方法を提供する(Kerker、Bohren、およびHuffman)。理論は、下記の入力パラメータを必要とする。
a)球形の屈折率。これは、球形が吸収するときに、複素数である。
b)媒体の屈折率(媒体は、光を吸収してはならない)。
c)照射に使用される光の波長および偏光。
d)容積から計算することができる球形の直径。
【0022】
モデルの仮定の1つは、球形は、固定された強度で照射されるということである。この近似は、球形を照射するビームの直径が、球形の直径よりも大きい(およそ10倍)場合に有効である。RBCのために行われる基本的な仮定は、RBCが球形であり、均質であるということである。これは、細胞の屈折率が、細胞のいずれの場所でも同一であることを意味する。ミー散乱理論アルゴリズムは、均一電磁場におけるマクスウェルの方程式の数値解法に基づいている。
【0023】
ミー理論アルゴリズムは、強度分布に角度シータを与えるだけである。これは、ビームが伝播する方向と観察の方向との間の角度である。これは、散乱強度プロファイルが前方方向で対称的であることを意味する。入射直線偏光に関する異なる角度によって収集される強度を計算するために使用される式は、式1によって与えられる。
【数1】

ここで、i1=|S1(θ)|2
i2=|S2(θ)|2
I=強度(相対数)
λ=波長(真空)
θ=レーザ方向と観察の方向との間の角度
φ=レーザ偏光と観察の方向との間の角度
i1、i2=2つの異なる偏光方向の強度
である。
【0024】
関数Si(θ)は、プログラムによって計算される。プログラムは、すべてに、0.3度で分離された角度で、0度から180度の間でこの関数の値を与える。各角度で、この角度の値は、絶対値の平方によって得られる。角度φは、偏光ベクトルと観察の方向との間の角度である。CD4000において、偏光方向は垂直軸である。したがって、関数I(θ,φ)は、細胞のまわりのすべての場所に散乱光の強度を提供する。前方IASデテクタによって収集される光の量を得るために、強度プロファイルは、収集された角度に対して積分することができる。プログラムに使用される積分の数値方法は、トラペジウム方法である。φは2πに対して積分されるため、前方角度における散乱に関する式は下記のようになる。
【数2】

ALLデテクタからの信号は、細胞がレーザビームを通過するときの最大強度低下に等しい。ALL信号は、合計光損失である。これは、散乱吸光係数とも呼ばれ、BohrenおよびHuffmanによって開発されたアルゴリズムによって計算することができる。
【0025】
デテクタが、各水平角度シータに関して異なる垂直角度ファイを収集する以外は、PSS信号の計算は簡単ではある。各水平角度φに関して、垂直角度φに関する積分が行われなければならない。この積分は正確であり、そのため近似を行う必要はない。各角度θは、円錐の形状に関連する自己の最小および最大φを有し、これは、CELL DYN(登録商標)4000の場合には円である。sin2(φ)の積分の解法は、式3によって与えられる。
【数3】

この式の中で角度φは半径方向に与えられ、上記公式の角度φよりも小さいπ/4である。これは、ファイが、90度プラスマイナスφmax(垂直収集角度)だからである。cos2(φ)の解法も同様であり、第2項の符号のみが異なる。各角度θに関して、垂直方向に収集される強度を計算することができる。水平最小および最大角度θに対する積分後に、PSSの値が得られる。
【0026】
前方散乱角度の選択
CELL DYN(登録商標)4000前方散乱角度デテクタ(空中でIAS3度から10度)は、容積に対して不感受性である。理論は、収集角度が懸濁媒体内で規定されなければならないことを必要とする。媒体(CELL DYN(登録商標)4000希釈剤シース)の屈折率は、λ25℃max488nmで1.339である。したがって、スネルの法則によって、希釈剤の収集角度は2.24から7.45である。図2Aおよび図2Bは、希釈剤における相対弁別クロス散乱対角度を表示する。弁別クロス散乱は、式2の積分より下の部分未満のものはない。
【0027】
曲線より下の区域は、容積(V)およびヘモグロビン濃度(HC)の相対強度を表す。33(g/dL)のHCで異なるVに関する曲線より下の区域は、2.24度から7.45度の間であまり変化しないが、これは、曲線が、4度より下では容積が高くなるにつれて下がり、4度より上では容積とともに上がるからである。最小ヘモグロビン干渉を有する容積を測定することができるために、4.5度から5.5度の間の角度が選択される。上記図2Aおよび図2B参照。
【0028】
異なる角度における測定は、修正された3リングデテクタを使用して達成される。デテクタは、2.24度から4.5度の角度をカバーする1つの内側リングと、4.5度から5.5度(IAS’)の角度をカバーする第2のリングと、5.5度から7.45度の角度をカバーする第3のリングとを有するように構成される。3つのリングは一緒に、WBC弁別分析に使用される現在のCELL DYN(登録商標)4000IASデテクタによって収集される角度を依然として与える。第2のリングのみから信号を収集することが可能であり、これは、4.5度から5.5度の間である。新しい角度と古い角度とを同時に使用することも可能である。この解決方法は、WBC/弁別およびRBC/弁別分析用に、2つの別個の光学式検出システムが使用される先行技術に対して利点を有する。本発明は、WBC/弁別およびRBC/弁別分析の両方に同時に同一の光学式検出システムを使用することを可能にする。この解決方法は、角度の異なるセットで散乱光を収集する様々な可能性を生み出す。
【0029】
三次元(3D)細胞分析
RBCが完全な球形であると仮定すると、3つの散乱信号、IAS、IAS’、およびPPS(またはALL、IAS’、およびPPS)は、主に、2つのRBCパラメータすなわちVおよびHCに応じる。すべての可能なVおよびHCの組み合わせが一緒に、空間に表面を形成する。空間におけるIAS’、ALL、およびPPSの表面の簡略にされた説明が、図3に示される。単一細胞のVおよびHCがどのように得られるかという原則を説明するために、三次元における表面の小さな部分のみが表示される。表面は実際には湾曲しているが、表面は平面であると仮定する。しかし、単一のRBCのVおよびHCを見出すために、同一の原則を表面に適用することができる。システムが完全に標準化されるときには、すべての球形RBCは、表面のまわりに非常に近接して分布される。鎌状細胞等の異常な形状のRBCは、表面からより離れている信号を生成する。このようにして、異常な細胞形状を識別するのに、RBC信号の表面からの距離を使用することができる。
【0030】
正確には表面上にない細胞のVおよびHC情報を見出す方法は、図3の細胞Mを使用して、下記に説明される。この細胞のVおよびHCをもっとも表す可能性がある表面上の点は、表面上のもっとも近接した点である。実際には現実の表面はないが、三次元における所与のVおよびHC値を備えた知られている点のセットの位置がある。図3の等V線および等HC線の交差は、これらの点を表す。正確にはこの表面にはない点のVおよびHC値を得るために、この表面上のもっとも近接した3点が見出される。この場合、3つのもっとも近接した点は、1、2、および3である。1から2へのベクトルおよび1から3へのベクトルは、法線を計算することができる表面の小さな部分を規定する。点Mを通って法線に平行なベクトルの表面との交差を計算して、点Iが見出される。点Iは、表面上の細胞の投影を表す。交差が見出されると、ベクトルaおよびbを計算することができる。aおよびbの長さを使用して、3点の値の間を補間し、細胞(点M)のVおよびHCを得ることができる。IAS方向のみにおける表面への距離のすべての細胞のヒストグラムを作ることによって、表面がIAS信号に関して正しい場所にあるか否かを見ることができる。表面がIAS信号に関して正しく設定される場合には、ヒストグラムのピークはチャネルゼロである。これは、同一数の細胞が表面の両側にあることを意味する。同一のことがALLおよびPPS信号に当てはまる。下記に示されるように、3つの信号方向における表面への距離に関する3つのヒストグラムが、正しい表面を見出すために有用なツールであることが判明した。
【0031】
三次元表面を見出す
ミー散乱理論は、知られている屈折率を有する完全球形からの信号を予測する。屈折率およびVの範囲に関する信号を計算することによって、表面上の点を見出すことができる。ミー理論は、信号強度の相対数のみを提供する。したがって、信号の三次元の正確なチャネル数は、これらを表面に正確に配置するために、ゲイン係数を掛けることによって計算されなければならない。これらの係数を見出すのを可能にするために、屈折率がヒト赤血球MCHCの臨床範囲内に入る3つの異なる炭化水素(ヘプタン、ノナン、およびドデカン)が使用された。3つの炭化水素の各々は、懸濁媒体内で強く混合されるときには、同一の屈折率を有する様々なサイズの滴を生成する。これらの3つのオイルの各々は、屈折率が異なるため(炭化水素は吸収がない)、互いに異なる、明確なV信号分布トラックを作る。次に、ミー理論によって作られる表面の正確度は、表面上のもっとも近接した点への実際の信号の距離を測定することによってチェックされる。たとえば、表面が3つの炭化水素によって生成される信号へ完全に適合するのであれば、3つのヒストグラムのピークの表面への距離はゼロである。
【0032】
血液試料に関する表面を作ることは、488nmでのヘモグロビンによる光吸収のため、より複雑である。吸収を訂正するために、炭化水素に関する三次元表面を形成するために使用されるシミュレーションに吸光度が加えられなければならない。理論値をチャネル数へ転換するために3つの炭化水素に関して使用されるすべてのゲイン設定は、一定に保たれる。このようにして、すべての可能なRBC事象を規定する完全な表面が形成される。正常な試料のRBCは、表面のまわりに正常に分布されなければならない。この表面は、機器の較正および標準化のための日常QCチェックに関してさらに努力することなく、試料が分析されている間にシステム標準化をモニタするツールも提供する。各試料に関して、表面のまわりのRBCの三次元ヒストグラムは、信号処理中に作られる。表面のまわりの正常なRBC分布が対称的ではない場合には、機器は標準化から外れる(たとえば、流体素子工学的なまたは電子工学的な問題)。
【0033】
例示のために、ここに検討された好適な実施態様の多数の使用が示される。下記の検討は、例示的な目的のためのみに提供され、この検討は網羅的ではない。具体的に下記に検討されるのは、統合された血液細胞分析、WBC弁別分析に使用されるのと同一の光学式検出システムを使用して、多角光散乱および蛍光ヘマトロジーアナライザーにおいて、容積、ヘモグロビン含有量、正常および異常な細胞形状、網状赤血球の容積、およびヘモグロビン含有量用のRBC弁別分析を行い、かつシステム標準化を同時にモニタするために開示された実施態様を使用する方法である。これは、請求される発明の範囲をいずれにも限定しない。
【0034】
例1.
開示された装置は、修正されたCELL DYN(登録商標)4000(CD4000)システムである。CD4000デテクタおよびプリアンプボードは、白血球弁別(WBC/弁別)分析と赤血球弁別(RBC/弁別)分析との両方に同一のデテクタを使用するために、修正される。修正されたデテクタを示す図は、図1Aに見られる。3つのゾーンが形成される。中心矩形ゾーン(ゾーン1)は軸方向光損失(0度、ALL)用である。中間ゾーン(ゾーン2、2.24から7.45度、IAS)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5から5.5度(IAS’)である。プリアンプボードは、図1Bに描かれるように修正された。修正されたプリアンプボードは、すべての3つのリングから信号を電気的に加算することによってIAS出力を形成する。この修正されたプリアンプボードからの可能な出力は、ALLおよびIASであるか、またはIAS’およびIASである(または配線し直すならば、ALLおよびIAS’である)。IAS’ゲインは、オンボードデュアルインラインパッケージ(DIP)スイッチによって設定される。ALLおよびIASは、WBC弁別のために使用され、ALLおよびIAS’か、またはIAS’およびIASかの組み合わせのいずれかが、RBC弁別分析のために使用される。三次元RBC弁別分析ために使用される第3の角度は、90度側方散乱である。
【0035】
例2.
この実験のために、米国特許第5,656,499号および第5,631,165号、発明の名称「自動分析を行うための方法および装置」に記載されたCD4000システムが、例1に記載されたように、3リングデテクタおよび新しいプリアンプボードを備えて修正された。約112.5μlの正常全血試料が、試料吸引プローブによって、約10.513μlのCD4000希釈剤シースを含んでいるRBCカップ内に置かれ、混合される。次いで、希釈された試料は、シース状インピーダンス開口部へ運ばれ、米国特許第5,656,499号および第5,631,165号に記載されるように、絶対RBC計数を電気的に決定する。約450μlの希釈された試料は、CD4000網状赤血球カップ内に移され、このカップは約450μlの網状赤血球試薬を含んでおり(米国特許第5,691,204号、1997年11月25日。「網状赤血球の迅速分析用の組成物および方法(Compositions and methods for the rapid analysis of reticulocytes)」)、混合される。次いで、準備された試料は、検出のために、シース状光学式フローセルへ運ばれる。WBCおよびNRBCは、RBCゲートによって排除され、網状赤血球は、米国特許第5,656,499号および第5,631,165号に記載されるように、識別され定量化される。同時に、3つの散乱信号は、各事象に関しても測定され、標準三次元表面に表示される。図4Aおよび図4Bは、三次元表面にきっちりと重なり合う正常血液の正面図および側面図を示す。完全に標準化され較正されたシステムで、図4Bに示されるように、約50%の信号が表面より上になり、50%が表面より下になる。
【0036】
例3.
鎌状細胞を含む臨床血液試料が、例2に記載された開示された装置を流れた。図5Aおよび図5Bは、それぞれ、試料の正面図および側面図を表示する。見ることができるように、異常な形状の鎌状細胞のため、細胞母集団はかなり分散しており、側面図は、信号が三次元表面から外れることを示す。各事象の表面からの距離に基づいて、本発明の方法は、異常な形状のRBCのパーセントを概算することができる。同一試料のTycko(バイエルH*1)による先行技術の二次元分布は、図5Cに表示される。図5Cから見ることができるように、二次元分布は、異常な細胞形状を球形の正赤血球から区別しない。その上、異常な形状を有するRBCの有意な数は、二次元マップから外れ、それによって容積測定から除外される。
【0037】
例4.
高WBC試料およびWBCのRBCゲートからの分離および除外のCD4000サイトグラム(FL1対IAS)は、染色された網状赤血球および成熟RBCを含み、図6Aに示される。図4Aに示されるように、本発明の方法は、RBC/弁別分析の前に、WBCをRBC母集団からはっきりと識別し排除する。ゲートされた母集団のFL1ヒストグラムは、図6Bに示される。逆に、Tycko(バイエルH*1)によって開示された先行技術は、WBCをRBC母集団からはっきりと区別しないかまたは分離しない(図6C参照、先行技術による同一試料のRBC分布)。したがって、先行技術の方法は、様々な白血病の患者、特に、慢性リンパ球性白血病(CLL)の患者からの上昇WBC試料では、誤った赤血球MCVおよびMCHC結果を生成する可能性があるが、それは、CLLのリンパ球が、RBCと同じほど小さいだけではなく、RBCと同じほど小さい光散乱を生成するには壊れ易いからである。
【0038】
例5.
小赤血球(図7A)、正赤血球(図7B)、および大赤血球(図7C)のRBC試料の細胞ヘモグロビン含有量(HC)対容積(V)の二変数分布が、本発明の方法によって分析された。2本の固定線が、正常範囲のまわりに垂直に且つ水平に引かれ、各試料におけるサイズおよびヘモグロビン含有量のRBC異常性の異なる組み合わせを識別し計数する。下記の表1a、1b、および1cは、各カテゴリーの細胞の概算されたパーセンテージを示す。提供された情報に基づいて、患者の状態の赤血球不同症、小赤血球症、大赤血球症、血色素減少症、および血色素増加症の重大度レベルを決定することができる。
【表1a】

【表1b】

【表1c】

【0039】
例6.
平均細胞容積(MCV)の回帰統計およびプロット。図8Aは、本発明対Tycko(バイエルH*1)による先行技術の結果を表し、図8Bは、正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCV結果(流体力学的に集束された細胞を使用した電気インピーダンス測定)の結果を表す。
【0040】
例7.
MCHCの回帰統計およびプロット。図9Aは、本発明対Tycko(バイエルH*1CHCM)による先行技術の結果を表示し、図9Bは、正常および臨床試料のセットにおける、本発明対CELL DYN4000MCHC(インピーダンスMCVおよびヘモグロビンのCELL DYN4000比色分析測定から計算された結果)の結果を表示する。
【0041】
例8.
MCHの回帰統計およびプロット。図10Aは、本発明対Tycko(バイエルH*1MCH)による先行技術の結果であり、図10Bは、正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCH(インピーダンスRBC計数およびヘモグロビンの比色分析測定から計算された)の結果である。
【0042】
例9.
開示された方法による正常および臨床試料のセットにおける平均網状赤血球容積(RETV)と合計RBCMCVとの比較が、図11Aに示され、開示された方法による正常および臨床試料の同一のセットにおける網状赤血球MCHC(RETHC)と合計RBCMCHCとの比較が、図11Bに示される。
【0043】
例10.
約1.67μLの全血試料が、試料吸引プローブによって、約2800μlの上記例2に使用されたものと同一の希釈剤を含んでいるRBCカップ内に置かれ、混合される。次いで、希釈された試料は、アボットCELL DYN3200シース状光学式フローセルへ運ばれ、細胞1つずつの容積およびヘモグロビン測定に関する信号を収集する。アボットCELL DYN3200の光源は、5mワットヘリウムネオンレーザであり、そのデテクタは、1度から3度、および3度から10度2つの前方光散乱信号、および90度+/−30度の側方散乱信号を収集するように構成される。試料のFSCファイルは較正された三次元表面で分析され、本発明の開示された方法を使用して、ヘリウムネオンシステムに関して作られる。157個の正常および臨床試料、および、浸透圧検査からの66個の試料がシステムに流され、結果の比較は図12Aおよび図12Bに示される。浸透圧実験は、血液を希釈するために使用される両方の試薬(CELL DYN3200およびH*1)の塩濃度を変えることによって行われた。検査された浸透圧範囲は、175mOsm/Lから500mOsm/Lであった。
【0044】
上記を考慮して、前述の記載から、先行技術に対して本発明の多くの利点が明らかである。一定の代表的な実施態様および詳細が、発明を例示する目的のために示されているが、特許請求の範囲に規定された本発明の範囲から逸脱せずに、様々な変更および修正を行うことができる。
【図面の簡単な説明】
【0045】
【図1A】白血球弁別(WBC/弁別)分析と赤血球弁別(RBC/弁別)との両方の分析に同一のデテクタを使用するために、修正されたCELL DYN(登録商標)4000デテクタを示す図である。3つのゾーンが形成される。中心矩形ゾーン(ゾーン1:ALL用に0度)は軸方向光損失用であり、中間ゾーン(ゾーン2:IAS用に2.24から7.45度)は、3つのサブゾーンに分割され、中心ゾーン(ゾーン3)は4.5から5.5度(IAS’)である。
【図1B】CELL DYN(登録商標)4000プリアンプボードの修正を示す。IAS出力は、すべての3つのリングからの信号を電気的に加算することによって形成される。この修正されたプリアンプボードからの可能な出力は、ALLおよびIASであるか、またはIAS’およびIASである(または配線し直すならば、ALLおよびIAS’である)。WBC弁別および三次元RBC弁別の両方分析ために使用される第3の角度は、90度偏光側方散乱である。
【図2A】488nmの波長での容積およびヘモグロビン濃度の異なる値に関する前方角度における弁別クロス散乱を例示する。
【図2B】488nmの波長での容積およびヘモグロビン濃度の異なる値に関する前進角度における弁別クロス散乱を例示する。
【図3】細胞のV&HCデータがどのように三次元表面から得られるかの原則を説明するための三次元表面の小さな部分の例である。
【図4A】開示された三次元表面における正常血液の正面図である。米国特許第5,656,499号および第5,631,165号に開示されたCELL DYN(登録商標)4000システムが、例1に記載されたように、開示された3リングデテクタおよびプリアンプボードを備えて修正され、示されたデータを収集するために使用された。
【図4B】上記図4Aに示されたものと同一の正常な血液の側面図であり、三次元表面を囲む非常に密接な対称分布を示す。完全に標準化され較正されたシステムでは、示されるように、約50%の信号が表面より上になり、50%が表面より下になる。シンボル:Oは球形の成熟赤血球であり、Rは染色された網状赤血球であり、Xは非球形の異常形状の赤血球であり、Wは白血球であり、Pは血小板である。
【図5A】図4Aに示されたものと同一の三次元表面における鎌状細胞試料の正面図である。図示のように、細胞母集団は、異常な形状の鎌状細胞のためにかなり分散している。
【図5B】三次元表面における同一の鎌状細胞試料の側面図である。異常な形状の鎌状細胞からの散乱信号は、三次元表面から外れ、それによって、非対称分布になり、正常な赤血球よりも三次元表面からかなり離れる。シンボル:Oは球形の成熟赤血球であり、Rは染色された網状赤血球であり、Xは非球形の異常形状の赤血球であり、Wは白血球であり、Pは血小板である。
【図5C】Tyckoによって開示された先行技術(バイエルH*1)による、同一試料の二次元分布である。
【図6A】高いWBC試料のCELL DYN(登録商標)4000RBC/網状赤血球サイトグラム(FL1対IAS)を表示する。これは、染色された網状赤血球および成熟RBCを含むRBCゲートから、WBCのはっきりとした分離および除外を明らかにする。ゲートされたRBC母集団は、網状赤血球計数、および、成熟RBCおよび網状赤血球の両方のV&HCの測定のために使用される。
【図6B】成熟RBCに関するおよび網状赤血球に関する領域を示すゲートされたRBC母集団のFL1ヒストグラムである。
【図6C】Tyckoによって開示された先行技術によって分析された同一試料の二次元分布である。WBCはRBCからはっきりと分離されていない。
【図7A】小赤血球RBC試料のV&HCの二変数分布を表示する。
【図7B】正常なRBC試料のV&HCの二変数分布を示す。
【図7C】大赤血球RBC試料のV&HCの二変数分布を表示する。
【図8A】正常および臨床試料のセットにおける、本発明対Tyckoによる先行技術(バイエルH*1)の平均血球容積(MCV)の結果の回帰プロットを示す。
【図8B】図8Aと同一の正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCV結果(流体力学的に集束されたインピーダンス開口部を使用する電気抵抗測定)のMCV結果の回帰プロットを示す。
【図9A】図8Aと同一の正常および臨床試料のセットにおける、本発明対Tyckoによる先行技術(バイエルH*1CHCM)のMCHC結果を表示する。
【図9B】図8Aと同一の正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCHC(インピーダンスMCVおよびヘモグロビンのCELL DYN4000比色分析測定から計算された結果)のMCHC結果を表示する。
【図10A】図8Aと同一の正常および臨床試料のセットにおける、本発明対Tyckoによる先行技術(バイエルH*1MCH)のMCH結果を表示する。
【図10B】図8Aと同一の正常および臨床試料のセットにおける、本発明対CELL DYN(登録商標)4000MCH(インピーダンスRBC計数およびヘモグロビンの比色分析測定から計算される)のMCH結果を表示する。
【図11A】本発明の方法による正常および臨床試料のセットにおける、平均網状赤血球容積(RETV)と合計RBCMCVとの比較を示す。
【図11B】本発明の方法による同一の正常および臨床試料のセットにおける、網状赤血球MCHC(RETHC)と合計RBCMCHCとの比較を示す。
【図12A】157個の正常および臨床試料および66個の浸透圧試料(詳細は例10参照)を含むセットにおける、633nm(ヘリウムネオンレーザ)光源を使用する本発明対Tyckoによる先行技術(バイエルH*1)のMCVデータの回帰プロットを示す。
【図12B】同一のヘリウムネオンシステムからの本発明対先行技術(バイエルH*1CHCM)のMCHC結果を示す。
【特許請求の範囲】
【請求項1】
個別の赤血球の容積Vおよびヘモグロビン含有量HCを決定するための三次元光学式方法であって、
a)抗凝固全血試料を、球形剤および中性緩衝等張塩水を含む試薬溶液で処理するステップと、
b)前記試料から分離された赤血球を、選択された波長で光路に沿って方向づけられた光ビームを通過させるステップと、
c)各赤血球からの第1の前方角度光散乱信号、第2の中間角度光散乱信号、および第3の側方角度光散乱信号の結果として得られる大きさを測定するステップと、
d)VおよびHCのグリッドラインを含む予め較正された三次元表面に、各赤血球からの前記光散乱信号の三次元座標を投影するステップと、
e)前記三次元グリッド表面に各投影された交差の場所によって、VおよびHCの値を決定するステップとを含む、方法。
【請求項2】
前記散乱信号が、各赤血球の容積およびヘモグロビン濃度によって決定され、前記ヘモグロビン濃度が、前記光のビームの波長におけるヘモグロビンの屈折率に応じて決定される、請求項1に記載の方法。
【請求項3】
前記選択された波長が、400nmから800nmの範囲の可視光に対応する、請求項1に記載の方法。
【請求項4】
前記三次元表面が、ミー散乱理論に基づいて計算され、前記光ビームの角度に対する前記第3の側方角度光散乱信号の角度、前記光ビームの波長、および前記波長におけるヘモグロビンの屈折率に応じる、請求項1に記載の方法。
【請求項5】
前記試薬溶液が、核酸ステインをさらに含み、核酸ステインが、第4の蛍光信号によって、前記血液試料の成熟赤血球から網状赤血球を分離することを可能にする、請求項1に記載の方法。
【請求項6】
白血球、血小板、および有核赤血球を含む他の細胞状粒子を除外するための赤血球ゲートをさらに含み、前記ゲートが、前方散乱および蛍光の二次元サイトグラムを作ることによって確立される、請求項5に記載の方法。
【請求項7】
白血球、血小板、および有核赤血球を含む他の細胞状粒子を除外するための赤血球ゲートをさらに含み、前記ゲートが、光損失および蛍光の二次元サイトグラムを作ることによって確立される、請求項5に記載の方法。
【請求項8】
三次元表面グリッド方法が、前記網状赤血球の容積およびヘモグロビン濃度を決定するために適用される、請求項5に記載の方法。
【請求項9】
前記グリッド表面の法線方向で測定された、前記三次元グリッド表面から赤血球点のもっとも近い距離を決定することによって、異常な形状の赤血球を識別することを含む、請求項1に記載の方法。
【請求項10】
前記試料の個別の赤血球の容積およびヘモグロビン濃度の二変数分布から、前記血液試料における大赤血球、小赤血球、血色素減少細胞、血色素増加細胞、またはそれらの組み合わせのパーセントを定量化することができる、請求項1に記載の方法。
【請求項11】
前記三次元グリッド表面から細胞母集団の距離の対称性程度を決定することによって、システム標準化を継続してモニタすることを含む、請求項1に記載の方法。
【請求項12】
個別の赤血球の容積Vおよびヘモグロビン含有量HCを決定するための三次元光学式方法であって、
a)抗凝固全血試料を、球形剤および中性緩衝等張塩水を含む試薬溶液で処理するステップと、
b)前記試料から分離された赤血球を、選択された波長で光路に沿って方向づけられた光ビームを通過させるステップと、
c)各赤血球からの1つの前方角度光散乱信号、1つの光損失信号、および第3の側方角度光散乱信号の結果として得られる大きさを測定するステップと、
d)VおよびHCのグリッドラインを含む予め較正された三次元表面に、各細胞からの前記光散乱信号の三次元座標を投影するステップと、
e)前記三次元グリッド表面に各投影された交差の場所によって、VおよびHCの値を決定するステップとを含む、方法。
【請求項13】
白血球および赤血球の弁別を同時に決定するための装置であって、
a)光路に沿って光のビームを方向づける手段と、
b)細胞を前記光ビームに通過させて、所望の角度間隔の光散乱パターンを作る手段と、
c)所定の角度間隔に対応する、多数の別々の領域を備えた光学式デテクタと、
d)それぞれ前記白血球および赤血球の弁別分析に関して、所望の角度間隔を選択的に分離するための電子プリアンプ手段と、
e)それぞれ前記角度間隔内の散乱した光の強度に対応する、各角度間隔からの信号を同時に生成する手段と、
f)前記赤血球の細胞1つずつに基づいて容積およびヘモグロビン濃度を決定し、かつ前記白血球のサイズおよび複雑度を決定するための手段とを具備する、装置。
【請求項14】
決定ステップが、複数の前記赤血球を1度に1つずつ前記光のビームを通過させて、前記赤血球の各々が、少なくとも第1の前方角度光散乱信号、第2の中間角度光散乱信号、および第3の側方角度光散乱信号を展開して、容積、ヘモグロビン濃度、および赤血球形状異常度を決定することを含む、請求項13に記載の装置。
【請求項15】
決定ステップが、複数の前記赤血球を1度に1つずつ前記光のビームを通過させて、前記赤血球の各々が、少なくとも1つ光損失信号、第2の中間角度光散乱信号、および第3の側方角度光散乱信号とを展開して、容積、ヘモグロビン濃度、および赤血球形状異常度を決定することを含む、請求項13に記載の装置。
【請求項16】
さらなる決定ステップが、各赤血球の成熟度を決定するために、前記赤血球の第4の同時蛍光信号を展開するための手段を含む、請求項14に記載の装置。
【請求項17】
決定ステップが、複数の白血球を1度に1つずつ前記光のビームを通過させて、前記白血球の各々が、少なくとも第1の前方角度光散乱信号、第2の中間角度光散乱信号、第3の側方角度偏光散乱信号、および第4の側方角度偏光解消散乱信号を展開して、各白血球のサイズ、白血球内部複雑度、および粒度を決定することを含む、請求項13に記載の装置。
【請求項18】
決定ステップが、複数の白血球を1度に1つずつ前記光のビームを通過させて、前記白血球の各々が、少なくとも1つの光損失信号、第2の中間角度光散乱信号、第3の側方角度偏光散乱信号、および第4の側方角度偏光解消散乱信号を展開して、各白血球のサイズ、白血球内部複雑度、および粒度を決定することを含む、請求項13に記載の装置。
【請求項19】
前記光ビームが、400nmから800nmの範囲の可視スペクトルから選択される、請求項13に記載の装置。
【請求項20】
前記光源が、
a)488nmでのアルゴンイオンガスレーザと、
b)532nmでの固定レーザと、
b)632nmでのヘリウムネオンガスレーザと、
c)赤色ダイオードレーザと、
d)緑色ダイオードレーザと、
e)青色ダイオードレーザと
からなる群から選択される、請求項19に記載の装置。
【請求項21】
前記球形剤が、非イオン性界面活性剤である、請求項1または12に記載の方法。
【請求項1】
個別の赤血球の容積Vおよびヘモグロビン含有量HCを決定するための三次元光学式方法であって、
a)抗凝固全血試料を、球形剤および中性緩衝等張塩水を含む試薬溶液で処理するステップと、
b)前記試料から分離された赤血球を、選択された波長で光路に沿って方向づけられた光ビームを通過させるステップと、
c)各赤血球からの第1の前方角度光散乱信号、第2の中間角度光散乱信号、および第3の側方角度光散乱信号の結果として得られる大きさを測定するステップと、
d)VおよびHCのグリッドラインを含む予め較正された三次元表面に、各赤血球からの前記光散乱信号の三次元座標を投影するステップと、
e)前記三次元グリッド表面に各投影された交差の場所によって、VおよびHCの値を決定するステップとを含む、方法。
【請求項2】
前記散乱信号が、各赤血球の容積およびヘモグロビン濃度によって決定され、前記ヘモグロビン濃度が、前記光のビームの波長におけるヘモグロビンの屈折率に応じて決定される、請求項1に記載の方法。
【請求項3】
前記選択された波長が、400nmから800nmの範囲の可視光に対応する、請求項1に記載の方法。
【請求項4】
前記三次元表面が、ミー散乱理論に基づいて計算され、前記光ビームの角度に対する前記第3の側方角度光散乱信号の角度、前記光ビームの波長、および前記波長におけるヘモグロビンの屈折率に応じる、請求項1に記載の方法。
【請求項5】
前記試薬溶液が、核酸ステインをさらに含み、核酸ステインが、第4の蛍光信号によって、前記血液試料の成熟赤血球から網状赤血球を分離することを可能にする、請求項1に記載の方法。
【請求項6】
白血球、血小板、および有核赤血球を含む他の細胞状粒子を除外するための赤血球ゲートをさらに含み、前記ゲートが、前方散乱および蛍光の二次元サイトグラムを作ることによって確立される、請求項5に記載の方法。
【請求項7】
白血球、血小板、および有核赤血球を含む他の細胞状粒子を除外するための赤血球ゲートをさらに含み、前記ゲートが、光損失および蛍光の二次元サイトグラムを作ることによって確立される、請求項5に記載の方法。
【請求項8】
三次元表面グリッド方法が、前記網状赤血球の容積およびヘモグロビン濃度を決定するために適用される、請求項5に記載の方法。
【請求項9】
前記グリッド表面の法線方向で測定された、前記三次元グリッド表面から赤血球点のもっとも近い距離を決定することによって、異常な形状の赤血球を識別することを含む、請求項1に記載の方法。
【請求項10】
前記試料の個別の赤血球の容積およびヘモグロビン濃度の二変数分布から、前記血液試料における大赤血球、小赤血球、血色素減少細胞、血色素増加細胞、またはそれらの組み合わせのパーセントを定量化することができる、請求項1に記載の方法。
【請求項11】
前記三次元グリッド表面から細胞母集団の距離の対称性程度を決定することによって、システム標準化を継続してモニタすることを含む、請求項1に記載の方法。
【請求項12】
個別の赤血球の容積Vおよびヘモグロビン含有量HCを決定するための三次元光学式方法であって、
a)抗凝固全血試料を、球形剤および中性緩衝等張塩水を含む試薬溶液で処理するステップと、
b)前記試料から分離された赤血球を、選択された波長で光路に沿って方向づけられた光ビームを通過させるステップと、
c)各赤血球からの1つの前方角度光散乱信号、1つの光損失信号、および第3の側方角度光散乱信号の結果として得られる大きさを測定するステップと、
d)VおよびHCのグリッドラインを含む予め較正された三次元表面に、各細胞からの前記光散乱信号の三次元座標を投影するステップと、
e)前記三次元グリッド表面に各投影された交差の場所によって、VおよびHCの値を決定するステップとを含む、方法。
【請求項13】
白血球および赤血球の弁別を同時に決定するための装置であって、
a)光路に沿って光のビームを方向づける手段と、
b)細胞を前記光ビームに通過させて、所望の角度間隔の光散乱パターンを作る手段と、
c)所定の角度間隔に対応する、多数の別々の領域を備えた光学式デテクタと、
d)それぞれ前記白血球および赤血球の弁別分析に関して、所望の角度間隔を選択的に分離するための電子プリアンプ手段と、
e)それぞれ前記角度間隔内の散乱した光の強度に対応する、各角度間隔からの信号を同時に生成する手段と、
f)前記赤血球の細胞1つずつに基づいて容積およびヘモグロビン濃度を決定し、かつ前記白血球のサイズおよび複雑度を決定するための手段とを具備する、装置。
【請求項14】
決定ステップが、複数の前記赤血球を1度に1つずつ前記光のビームを通過させて、前記赤血球の各々が、少なくとも第1の前方角度光散乱信号、第2の中間角度光散乱信号、および第3の側方角度光散乱信号を展開して、容積、ヘモグロビン濃度、および赤血球形状異常度を決定することを含む、請求項13に記載の装置。
【請求項15】
決定ステップが、複数の前記赤血球を1度に1つずつ前記光のビームを通過させて、前記赤血球の各々が、少なくとも1つ光損失信号、第2の中間角度光散乱信号、および第3の側方角度光散乱信号とを展開して、容積、ヘモグロビン濃度、および赤血球形状異常度を決定することを含む、請求項13に記載の装置。
【請求項16】
さらなる決定ステップが、各赤血球の成熟度を決定するために、前記赤血球の第4の同時蛍光信号を展開するための手段を含む、請求項14に記載の装置。
【請求項17】
決定ステップが、複数の白血球を1度に1つずつ前記光のビームを通過させて、前記白血球の各々が、少なくとも第1の前方角度光散乱信号、第2の中間角度光散乱信号、第3の側方角度偏光散乱信号、および第4の側方角度偏光解消散乱信号を展開して、各白血球のサイズ、白血球内部複雑度、および粒度を決定することを含む、請求項13に記載の装置。
【請求項18】
決定ステップが、複数の白血球を1度に1つずつ前記光のビームを通過させて、前記白血球の各々が、少なくとも1つの光損失信号、第2の中間角度光散乱信号、第3の側方角度偏光散乱信号、および第4の側方角度偏光解消散乱信号を展開して、各白血球のサイズ、白血球内部複雑度、および粒度を決定することを含む、請求項13に記載の装置。
【請求項19】
前記光ビームが、400nmから800nmの範囲の可視スペクトルから選択される、請求項13に記載の装置。
【請求項20】
前記光源が、
a)488nmでのアルゴンイオンガスレーザと、
b)532nmでの固定レーザと、
b)632nmでのヘリウムネオンガスレーザと、
c)赤色ダイオードレーザと、
d)緑色ダイオードレーザと、
e)青色ダイオードレーザと
からなる群から選択される、請求項19に記載の装置。
【請求項21】
前記球形剤が、非イオン性界面活性剤である、請求項1または12に記載の方法。
【図1A】


【図1B】


【図2A】


【図2B】


【図3】


【図4A】


【図4B】


【図5A】


【図5B】


【図5C】


【図6A】


【図6B】


【図6C】


【図7A】


【図7B】


【図7C】


【図8A】


【図8B】


【図9A】


【図9B】


【図10A】


【図10B】


【図11A】


【図11B】


【図12A】


【図12B】




【図1B】


【図2A】


【図2B】


【図3】


【図4A】


【図4B】


【図5A】


【図5B】


【図5C】


【図6A】


【図6B】


【図6C】


【図7A】


【図7B】


【図7C】


【図8A】


【図8B】


【図9A】


【図9B】


【図10A】


【図10B】


【図11A】


【図11B】


【図12A】


【図12B】


【公開番号】特開2008−268230(P2008−268230A)
【公開日】平成20年11月6日(2008.11.6)
【国際特許分類】
【外国語出願】
【出願番号】特願2008−159875(P2008−159875)
【出願日】平成20年6月19日(2008.6.19)
【分割の表示】特願2003−502455(P2003−502455)の分割
【原出願日】平成14年5月31日(2002.5.31)
【出願人】(391008788)アボット・ラボラトリーズ (650)
【氏名又は名称原語表記】ABBOTT LABORATORIES
【Fターム(参考)】
【公開日】平成20年11月6日(2008.11.6)
【国際特許分類】
【出願番号】特願2008−159875(P2008−159875)
【出願日】平成20年6月19日(2008.6.19)
【分割の表示】特願2003−502455(P2003−502455)の分割
【原出願日】平成14年5月31日(2002.5.31)
【出願人】(391008788)アボット・ラボラトリーズ (650)
【氏名又は名称原語表記】ABBOTT LABORATORIES
【Fターム(参考)】
[ Back to top ]

