光学活性体分析システム
【課題】目的成分である対掌体を特定でき、標準品を用いずに光学活性体の分析を実現するシステムを提供する。
【解決手段】光学活性体を分離できるクロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器を連結する。光学活性体を分離できるクロマトグラフが、キラルカラムを接続した高速液体クロマトグラフであり、光学活性体が区別できる検出器が、円二色性分光計3である光学活性体分析システム。
【解決手段】光学活性体を分離できるクロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器を連結する。光学活性体を分離できるクロマトグラフが、キラルカラムを接続した高速液体クロマトグラフであり、光学活性体が区別できる検出器が、円二色性分光計3である光学活性体分析システム。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、光学活性体を分離できるクロマトグラフと、光学活性体が区別できる検出器と化学構造を区別できる分光器を連結することを特徴とする光学活性体分析システムに関する。
【背景技術】
【0002】
医薬品や農薬の分野において、特定の光学異性体のみが望む活性を有し、対掌体が活性を有しない、もしくは、深刻な副作用などの望まない活性を示す例が知られている。そのため、工業プロセスで単一な光学活性体を製造することはますます重要になっており、プロセス管理上、光学活性体分析の重要度も高まっている。光学活性体の分析には、キラル液体クロマトグラフが最も広く用いられている。しかしながら、本手法ではピークを同定に光学活性体とその対掌体の標準品が必要であり、これらの調製に多大な労力とコストを要していた。
このような背景から、標準品の調製を必要としない分析システムが考案されている。いずれのシステムも、分析手法を組み合わせて反応混合物中などに微量に含まれる対掌体を特定することを特徴としている。
具体的には、1)一方の立体配置のキラルセレクターを担持したキラルカラムと、逆の立体配置のキラルセレクターを担持したキラルカラムで、試料中に含まれる対掌体同士の溶出位置が入れ替わることを利用して、高速液体クロマトグラフ質量分析計を用いて、対掌体を特定する分析システム(非特許文献1)、
2)キラルカラムを接続した高速液体クロマトグラフと旋光度分析計と質量分析計を接続し、得られたピークの中から、旋光度が逆符号でかつ同一の質量スペクトルを持つものを対掌体として特定する分析システム(非特許文献2)や
3)キラル高速液体クロマトグラフと核磁気共鳴分光計と接続した分析システム、キラル高速液体クロマトグラフと円二色性分光計と接続した分析システムを用いて、別々に得られた各スペクトルからコットン効果曲線が逆符号でかつ同一の核磁気共鳴スペクトルを持つものを対掌体として特定する分析システム(非特許文献3)などが挙げられる。
【先行技術文献】
【非特許文献】
【0003】
【非特許文献1】Analytical Chemistry 2007, 79, 6013-6019.
【非特許文献2】Journal of Chromatography A 2000, 878, 35-43.
【非特許文献3】Analytical Chemistry, 1999, 71, 2838-2843.
【発明の概要】
【発明が解決しようとする課題】
【0004】
しかしながら、上記1)の分析システムは、通常入手が困難な逆の立体配置を有するキラルセレクターを担持したカラムが必要であるため汎用性が低い点や、反応混合物のような不純物を多く含む試料では、不純物と対掌体のピークが重複して特定できないといった点が問題であった。また上記2)の分析システムは、分子量によって対掌体と不純物を区別する方法であるが、同一の分子量を与える幾何異性体、位置異性体などを対掌体と区別することが困難であった。上記3)の分析システムでは、複数回の測定が必要であり、別々の装置で得られた各スペクトルのピークをひとつずつ帰属させる作業の煩雑さが大きな問題であった。さらに、不純物を多く含む試料では、各測定間で保持時間が微妙に変化しただけでピークの帰属が困難になる場合も多く、分析の再現性を高める方法が強く望まれていた。また移動相や試料を多く必要とすることも問題であった。
【0005】
本発明の目的は、目的成分である対掌体を明確に特定でき、標準品を用いずに光学活性体の分析を実現するシステムを提供することにある。
【課題を解決するための手段】
【0006】
このような状況下、本発明者らは鋭意検討を行った結果、本発明に至った。すなわち本発明は、光学活性体を分離できるクロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器とを連結することを特徴とする光学活性体分析システムを提供するものである。
【発明の効果】
【0007】
本発明によれば、光学活性体の分析において、標準品を用いずに当該光学活性体の分析を実現できる。また光学活性体を区別できる検出器を用いることで、光学不活性な不純物は検出されないため、夾雑物の影響を受けない。さらに、対掌体同士が完全に分離せず単一のピークとして検出される場合においても、対掌体を特定できる。
【図面の簡単な説明】
【0008】
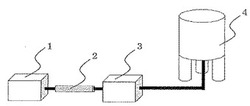
【図1】本発明の装置構成の一例である。
【図2】実施例1のクロマトグラム(円二色性、254 nm)
【図3】実施例1の各ピークの核磁気共鳴スペクトルの比較
【図4】実施例2のクロマトグラム(紫外吸光、254 nm)
【図5】実施例2の各ピークの核磁気共鳴スペクトルの比較
【発明を実施するための形態】
【0009】
本発明において、クロマトグラフは目的の対掌体が分離できる手法であればよく、例えば光学活性体が分離できる媒体を接続した液体クロマトグラフ、ガスクロマトグラフ、超臨界流体クロマトグラフ、キャピラリー電気泳動、キャピラリー電気クロマトグラフ、光学活性固定相を固定化した薄層クロマトグラフなどが用いられる。
【0010】
本発明において、液体クロマトグラフには、低圧クロマトグラフ、中圧クロマトグラフ、高速液体クロマトグラフなどを用いることができる。なお、より好ましくは分離性能の優れた高速液体クロマトグラフが挙げられる。
【0011】
本発明において、液体クロマトグラフに接続する光学活性体が分離できる媒体には、光学活性固定相をガラスや金属製管内に充填したパックドカラム、キャピラリー内部表面に被覆もしくは共有結合させたキャピラリーカラム、マイクロチップ上の微細流路内部表面に被覆もしくは共有結合させたマイクロ分離チップなどを用いることができる。なお、パックドカラムは入手の容易さの面では好ましい。
【0012】
本発明において、液体クロマトグラフに接続するパックドカラムには、例えば水素結合型・電荷移動型として、住化分析センター製SUMICHIRAL OA-2000、SUMICHIRAL OA-2000I、SUMICHIRAL OA-2500、SUMICHIRAL OA-2500I、SUMICHIRAL OA-3100、SUMICHIRAL OA-3200、SUMICHIRAL OA-3300、SUMICHIRAL OA-4000、SUMICHIRAL OA-4100、SUMICHIRAL OA-4400、SUMICHIRAL OA-4500、SUMICHIRAL OA-4600、SUMICHIRAL OA-4700、SUMICHIRAL OA-4800、SUMICHIRAL OA-4900 、Eka Chemicals製Kromasil CHI-DMB、Kromasil CHI-TBB、MACHEREY-NAGEL製NUCLEOSIL CHIRAL-2、NUCLEOSIL CHIRAL-3、ZirChrom製ZirChrom-Chiral (S) LEU、ZirChrom-Chiral (R) NESA、ZirChrom-Chiral (S) NESA、ZirChrom-Chiral (S) PG、ZirChrom-Chiral (R) PG、Regis Technologies製 (R,R)-Whelk-O 1、(S,S)-Whelk-O 1、(R,R)-Whelk-O 2、(R,R)-Whelk-O 2、(R,R)-ULMO、(S,S)-ULMO、(R,R)-DACH-DNB、(S,S)-DACH-DNB、(3R,4S)-Pirkle 1-J、(3S,4R)-Pirkle 1-J、(R,R)-α-Burke 2、(S,S)-α-Burke 2、(R,R)-β-Gem 1、(S,S)-β-Gem 1、D-Leucine、L-Leucine、D-Phenylglycine、L-Phenylglycine、L-Naphthylleucineなど、配位子交換型として、住化分析センター製SUMICHIRAL OA-5000、SUMICHIRAL OA-6000、SUMICHIRAL OA-6100、ダイセル化学工業製CHIRALPAK WH、CHIRALPAK MA(+)、MACHEREY-NAGEL製NUCLEOSIL CHIRAL-1、Regis Technologies製Davankovなど、ホストゲスト型として、住化分析センター製SUMICHIRAL OA-7000、SUMICHIRAL OA-7100、SUMICHIRAL OA-7500、SUMICHIRAL OA-8000、ダイセル化学工業製CROWNPAK CR(+)、CROWNPAK CR(-)、MACHEREY-NAGEL製NUCLEODEX β-OH、NUCLEODEX α-PM、NUCLEODEX β-PM、NUCLEODEX γ-PM、信和化工製ULTRON ES-CD、ULTRON ES-PhCD、資生堂製Chiral CD-Ph、昭和電工製ORpak CDA-453 HQ、ORpak CDB-453 HQ、ORpak CDC-453 HQ、ORpak CDBS-453、ORpak CRX-853、Regis Technologies製 Chirosil RCA(+)、Chirosil SCA(+)など、アフィニティー型として、住化分析センター製SUMICHIRAL AGP、SUMICHIRAL CBH、SUMICHIRAL HSA 、CHIRAL AGP、MACHEREY-NAGEL製RESOLVOSIL BSA-7、信和化工製ULTRON ES-OVM、ULTRON ES-PEPSIN、ULTRON ES-BSA、昭和電工製AFpak ABA-894、Chrom Tech製Chiral AGP、Chiral CBH、Chiral HSAなど、らせん高分子型として、ダイセル化学工業製CHIRALPAK IA、CHIRALPAK IB、CHIRALPAK IC、CHIRALPAK AD-H、CHIRALPAK AD、CHIRALPAK AS-H、CHIRALPAK AS、CHIRALCEL OD-H、CHIRALCEL OD、CHIRALCEL OJ-H、CHIRALCEL OJ、CHIRALCEL OA、CHIRALCEL OB-H、CHIRALCEL OB、CHIRALCEL OC、CHIRALCEL OF、CHIRALCEL OG、CHIRALCEL OK、CHIRALPAK OT(+)、CHIRALPAK OP(+)、CHIRALPAK AD-RH、CHIRALPAK AS-RH、CHIRALCEL OD-RH、CHIRALCEL OJ-RH、Eka Chemicals製Kromasil CelluCoat、Kromasil AmyCoat、Kromasil CelluCoat RP、Kromasil AmyCoat RP 、東京化成製TCI Chiral BP-S、TCI Chiral CH-S、TCI Chiral MB-Sなど、上記以外のキラルカラムとして、例えば、光学活性な金属錯体を固定した資生堂製Ceramospher RU-1、Ceramospher RU-2や、イオン交換能を有する光学活性固定相を結合したダイセル化学工業製CHIRALPAK QN-AX、CHIRALPAK QD-AXや、前述の型を組み合わせた複合型キラルカラムなどを用いることができる。
【0013】
本発明において、液体クロマトグラフの移動相には、例えば炭化水素溶媒としては、ペンタン、ヘキサン、ヘプタン、ノナン、デカン、シクロヘキサンなどが、芳香族炭化水素としては、ベンゼン、トルエン、o-キシレン、m-キシレンなどが、ハロゲン溶媒としては、ジクロロメタン、クロロホルム、四塩化炭素、トリクロロエチレン、テトラクロロエチレン、塩化n-ブチル、クロロベンゼンなどが、エステル系移動相としては、酢酸メチル、酢酸エチル、酢酸n-ブチルなどが、ケトン溶媒としては、アセトン、エチルメチルケトン、イソブチルメチルケトンなどが、エーテル溶媒としては、ジエチルエーテル、テトラヒドロフラン、1,4-ジオキサンなどが、アルコール溶媒としては、メタノール、エタノール、1-プロパノール、2-プロパノール、1-メトキシエタノール、2-メトキシエタノール、1-ブタノールなどが、含窒素溶媒としては、アセトニトリル、ジエチルアミン、ピリジン、ジメチルホルムアミド、ジメチルアセトアミド、上記以外の溶媒としては、二硫化炭素、炭酸プロピレン、ジメチルスルホキシド、ギ酸、酢酸、トリフルオロ酢酸、リン酸、水、各種緩衝液、及び上記の重水素化溶媒、もしくはこれらを組み合わせたものなどを用いることができる。
【0014】
本発明において、ガスクロマトグラフに接続する光学活性体を分離する媒体には、光学活性固定相をガラスや金属製管内に充填したパックドカラム、キャピラリー内部表面に被覆もしくは共有結合させたキャピラリーカラム、マイクロチップ上の微細流路内部表面に被覆もしくは共有結合させたマイクロ分離チップなどを用いることができる。なお、キャピラリーカラムは入手の容易さの面では好ましい。
【0015】
本発明において、ガスクロマトグラフに用いられるパックドカラムもしくはキャピラリーカラムの光学活性固定相には、例えば、D,L−バリン誘導体、D,L−ロイシン誘導体、D,L−フェニルグリシン誘導体、D,L−ナフチルアラニン誘導体、D,L−ナフチルグリシン誘導体などのアミノ酸誘導体型の固定相や、α−シクロデキストリン誘導体、β−シクロデキストリン誘導体、γ−シクロデキストリン誘導体などの糖誘導体型の固定相などを用いることができる。
【0016】
本発明において、ガスクロマトグラフに用いられるキャピラリーカラムには、例えば、アミノ酸誘導体型としては、バリアン製CP-Chirasil-D-Val、CP-Chirasil-L-Val、などが、糖誘導体型としては、RESTEK製Rt-β-DEXm、Rt-β-DEXsm、Rt-β-DEXsp、Rt-β-DEXsa、Rt-β-DEXcst、Rt-γ-DEXsa、SGE製CYDEX-B、アジレント製HP-Chiral β、バリアン製CP-Cyclodextrin-β-2,3,6-M-19、CP-Chirasil-DEX CB、スペルコ製α-DEX 120、β-DEX 110、β-DEX 120、γ-DEX 120、α-DEX 225、β-DEX 225、γ-DEX 225、α-DEX 325、β-DEX 325、γ-DEX 325、J&W製Cyclodex-β、Cyclosil-β、GLサイエンス製Inertcap CHIRAMIX、Advanced Separations Technologies製CHIRALDEX G-BP、CHIRALDEX A-DA、CHIRALDEX B-DA、CHIRALDEX G-DA、CHIRALDEX B-DM、CHIRALDEX G-DM、CHIRALDEX B-DP、CHIRALDEX G-DP、CHIRALDEX A-PH、CHIRALDEX B-PH、CHIRALDEX B-PM、CHIRALDEX G-PN、CHIRALDEX A-TA、CHIRALDEX B-TA、CHIRALDEX G-TAなどを用いることができる。
【0017】
本発明において、超臨界流体クロマトグラフに接続する光学活性体を分離する媒体には、光学活性固定相を充填したパックドカラムやキャピラリーカラム内部表面に被覆もしくは共有結合させたキャピラリーカラムなどを用いることができる。なお、パックドカラムは入手の容易さの面では好ましい。
【0018】
本発明において、超臨界流体クロマトグラフに接続するパックドカラムには、らせん高分子型のダイセル化学工業製CHIRALPAK IA/SFC、CHIRALPAK IB/SFC、CHIRALPAK IC/SFC、CHIRALPAK AD-H/SFC、CHIRALPAK AS-H/SFC、CHIRALCEL OD-H/SFC、CHIRALCEL OJ-H/SFCなどを用いることができる。
【0019】
本発明において、超臨界流体クロマトグラフの移動相には、例えば二酸化炭素、亜酸化窒素、アンモニア、イソオクタン、ペンタン、ヘキサン、ヘプタン、ブタン、プロパン、エタン、エチレン、メタン、イソプロピルエーテル、ジエチルエーテル、キセノン、六フッ化硫黄、フロン類、水などを用いることができる。
【0020】
本発明において、超臨界流体クロマトグラフのモディファイヤーには、例えば、2-プロパノール、ジオキサン、アセトニトリル、テトラヒドロフラン、ジイソプロピルエーテル、ジメチルスルホキシド、メタノール、エタノール、上記の重水素化溶媒などを用いることができる。
【0021】
本発明において、キャピラリー電気泳動に接続する光学活性体を分離する媒体には、光学活性移動相もしくは擬似固定相を用いるキャピラリーなどが用いられる。
【0022】
本発明において、キャピラリー電気泳動に用いる光学活性移動相としては、例えば、らせん高分子型としては、α-シクロデキストリン、β-シクロデキストリン、γ-シクロデキストリン、シクロデキストリンの各種誘導体など、抗生物質型としては、バンコマイシン、テイコプラニン、リファマイシン、リストセチン、A82846B、MDL63,246など、配位子交換型として、銅―ヒドロキシプロリン複合体のような金属―アミノ酸もしくは金属―ペプチド複合体など、アフィニティー型としてはα-AGP、BSA、HSAなどのタンパク質を用いることができる。
【0023】
擬似固定相としては、例えば、N,N−ジデシル−L−アラニン、ポリウンデセノイル−L−バリン、N−ドデカノイル−L−アラ二ン、N−ドデカノイル−L−バリン、N−ドデカノイル−L−グルタミン酸、N−ドデカノイル−L−セリン、N−ドデカノイル−L−アスパラギン酸、N−テトラデカノイル−L−グルタメート、(S)−ドデコキシカルボニル−L−バリン、(R)−ドデコキシカルボニル−L−バリン、(S)−2−[(ドデコキシカルボニル)アミノ] −3−(S)−メチル−1−スルホキシペンタン、(R)−ドデコキシカルボニルプロリン、ドデシル−β−D−グルコピラノシド−6−リン酸エステル、n−ドデシル−β−D−グルコピラノシド−4,6−リン酸エステル、(2R,4R)−N−アセチル−2−ウンデシル−4−チアゾリジンカルボン酸、(2S,4S)−N−アセチル−2−ウンデシル−4−チアゾリジンカルボン酸、6−アミノペニシリン酸誘導体、(2R,3R)−ジ−n−ブチル酒石酸などの塩やN,N−ビス(3−D−グルコアミドプロピル)コールアミド、N,N−ビス(3−D−グルコアミドプロピル)デオキシコールアミドなどのキラル界面活性剤などを用いることができる。
【0024】
本発明において、キャピラリー電気クロマトグラフに接続する光学活性体を分離する媒体には、光学活性固定相で被膜もしくは共有結合させたキャピラリーなどが用いられる。
【0025】
本発明において、キャピラリー電気クロマトグラフに用いられる光学活性固定相としては、例えば、シクロデキストリン、クラウンエーテル、カリックスアレーン、各種抗生物質、タンパク質などを固定させた固定相、分子インプリンティング型の固定相などが挙げられる。
【0026】
本発明において、薄層クロマトグラフに用いられる光学活性固定相は、例えばセルロース、トリアセチルセルロース、シクロデキストリン、バンコマイシン、エリスロマイシン、L-アミノ酸などを用いることができる。
【0027】
本発明において、薄層クロマトグラフには、キラル移動相を用いることもでき、移動相としては、バンコマイシンなどの各種抗生物質や、BSA、HSAなどの各種タンパク質を用いることができる。
【0028】
光学活性体を分離する媒体を固定化した薄層クロマトグラフは、例えば加圧装置を用いる加圧薄層クロマトグラフ装置や、遠心薄層クロマトグラフなどと接続して用いることができる。
【0029】
検出器は、エナンチオマーを区別できるものであれば良く、円二色性分光計、赤外円二色性分光計及び旋光度計などを用いることができる。
【0030】
円二色性分光計の検出波長範囲は、通常220〜420 nmであり、目的とする光学活性体に応じて最適な波長を選択する。
【0031】
赤外円二色性分光計の検出波長範囲は、通常900〜3200 cm-1であり、目的とする光学活性体に応じて最適な波長を選択する。
【0032】
本発明において、光学活性体を区別できる検出器に加えて、汎用的な化学検出器を連結してもよい。これにより光学活性体を区別できる検出器では感度が得られない成分や光学不活性で検出されない不純物の溶出位置を確認することができる。
【0033】
汎用的な化学検出器としては、紫外吸光検出器、示差屈折度検出器、蛍光検出器などを用いることができる。なお、紫外吸光検出器は汎用性の面では好ましい。
【0034】
本発明において、化学構造の違いを区別できる分光器には、核磁気共鳴分光計や赤外分光計などを用いることができる。
【0035】
核磁気共鳴分光計の観測核には、1H、2H、3H、6Li、7Li、10B、11B、13C、14N、15N、17O、19F、23Na、27Al、29Si、31P、33S、35Cl、37Cl、59Co、77Se、103Rh、113Cd、119Sn、183W、195Pt、207Pbなどがあるが、1Hが感度及び汎用性の面では好ましい。
【0036】
赤外分光計の検出波長範囲は、通常400〜4000 cm-1であり、目的とする光学活性体に応じて最適な波長範囲を選択する。
【0037】
本発明において、クロマトグラフ、検出器及び分光器の接続方法は、直列もしくはスプリッターなどを用いて並列に接続してもよく、検出器及び分光器がクロマトグラフの下流であれば、どのような順番で接続されていてもよい。また少なくとも光学活性体を区別できる検出器及び分光器がそれぞれ一つ以上接続されていれば、検出器及び分光器の個数、種類をどのように組み合わせてもよい。
【0038】
本発明において、クロマトグラフ、検出器及び分光器はマイクロチップ上に一部もしくは全部を集約したものでもよい。
【実施例】
【0039】
以下に実施例により本発明を詳細に説明するが、本発明はこれらに限定されるものではない。
[実施例1]
装置の設定
高速液体クロマトグラフにキラルカラム、円二色性検出器及び核磁気共鳴装置を図1に示したように連結した。
【0040】
<HPLC条件>
ポンプ:バリアン Prostar model 230
円二色性検出器:日本分光 CD-2095
カラムオーブン:日本ウォーターズ Model 1122
カラム:CHIRALCEL OJ-RH(4.6×150 mm、5 μm)
移動相:10 mM リン酸重水緩衝液(pH 3.0)/アセトニトリル混液(75:25)
流速:1.0 mL/min
カラム温度:40 ℃
検出波長:254 nm(円二色性スペクトル)
<NMR条件>
分光器:バリアンINOVA-500(500MHz)
プローブ:フローセルプローブ(60 μL)
【0041】
Boc−3−(3−ピリジル)−L−アラニンベンジルエステルを主成分に、対掌体であるBoc−3−(3−ピリジル)−D−アラニンベンジルエステル及び、位置異性体であるBoc−3−(2−ピリジル)−L−アラニンベンジルエステル、Boc−3−(2−ピリジル)−D−アラニンベンジルエステル、Boc−3−(4−ピリジル)− L−アラニンベンジルエステル、Boc−3−(4−ピリジル)−D−アラニンベンジルエステルを微量成分とする試料を用いて測定を行なった。
【0042】
得られたクロマトグラムを図2、NMRスペクトルの比較を図3に示した。保持時間、スペクトルパターン、検出波長254 nmにおける円二色性スペクトルのコットン効果曲線の符号について表1に示した。
【0043】
【表1】

【0044】
表1に示したように、液体クロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器を連結することで、主成分とNMRパターンが等しく、コットン効果曲線の符号が逆となるピーク6が対掌体であると、一度の測定で一義的に決定することができた。
【0045】
[実施例2]
実施例1の円二色性検出器の下流に紫外吸光検出器(バリアン Prostar model 335)を接続し、検出波長を254 nmとして、その他は同条件で測定を行った。その結果、実施例1と同様の円二色性クロマトグラムに加えて、紫外吸収クロマトグラム(図4)が得られ、感度の低い円二色性クロマトグラムのみの場合よりもピーク6の溶出位置を明確に確認することができた。主成分とのNMRパターンの比較(図5)、及び、コットン効果曲線の符号からピーク6が対掌体であると決定できた。
【0046】
[比較例1]
液体クロマトグラフ質量分析計と液体クロマトグラフ円二色性検出器を別々に用いた既存の分析方法で、実施例と同様の試料を分析した。各ピークの分子量、検出波長254 nmにおける円二色性スペクトルのコットン効果曲線の符号について表2に示した。
【0047】
【表2】

(分子量測定の移動相には、10mM 酢酸アンモニウム緩衝液/アセトニトリルを使用)
【0048】
質量分析計を用いた既存の方法では、主成分と分子量が等しく、かつコットン効果曲線の符号が逆となるピークが5、6、8と複数存在し、対掌体の特定には至らなかった。
【符号の説明】
【0049】
1.ポンプ
2.カラム
3.円二色性検出器
4.核磁気共鳴分光計
【技術分野】
【0001】
本発明は、光学活性体を分離できるクロマトグラフと、光学活性体が区別できる検出器と化学構造を区別できる分光器を連結することを特徴とする光学活性体分析システムに関する。
【背景技術】
【0002】
医薬品や農薬の分野において、特定の光学異性体のみが望む活性を有し、対掌体が活性を有しない、もしくは、深刻な副作用などの望まない活性を示す例が知られている。そのため、工業プロセスで単一な光学活性体を製造することはますます重要になっており、プロセス管理上、光学活性体分析の重要度も高まっている。光学活性体の分析には、キラル液体クロマトグラフが最も広く用いられている。しかしながら、本手法ではピークを同定に光学活性体とその対掌体の標準品が必要であり、これらの調製に多大な労力とコストを要していた。
このような背景から、標準品の調製を必要としない分析システムが考案されている。いずれのシステムも、分析手法を組み合わせて反応混合物中などに微量に含まれる対掌体を特定することを特徴としている。
具体的には、1)一方の立体配置のキラルセレクターを担持したキラルカラムと、逆の立体配置のキラルセレクターを担持したキラルカラムで、試料中に含まれる対掌体同士の溶出位置が入れ替わることを利用して、高速液体クロマトグラフ質量分析計を用いて、対掌体を特定する分析システム(非特許文献1)、
2)キラルカラムを接続した高速液体クロマトグラフと旋光度分析計と質量分析計を接続し、得られたピークの中から、旋光度が逆符号でかつ同一の質量スペクトルを持つものを対掌体として特定する分析システム(非特許文献2)や
3)キラル高速液体クロマトグラフと核磁気共鳴分光計と接続した分析システム、キラル高速液体クロマトグラフと円二色性分光計と接続した分析システムを用いて、別々に得られた各スペクトルからコットン効果曲線が逆符号でかつ同一の核磁気共鳴スペクトルを持つものを対掌体として特定する分析システム(非特許文献3)などが挙げられる。
【先行技術文献】
【非特許文献】
【0003】
【非特許文献1】Analytical Chemistry 2007, 79, 6013-6019.
【非特許文献2】Journal of Chromatography A 2000, 878, 35-43.
【非特許文献3】Analytical Chemistry, 1999, 71, 2838-2843.
【発明の概要】
【発明が解決しようとする課題】
【0004】
しかしながら、上記1)の分析システムは、通常入手が困難な逆の立体配置を有するキラルセレクターを担持したカラムが必要であるため汎用性が低い点や、反応混合物のような不純物を多く含む試料では、不純物と対掌体のピークが重複して特定できないといった点が問題であった。また上記2)の分析システムは、分子量によって対掌体と不純物を区別する方法であるが、同一の分子量を与える幾何異性体、位置異性体などを対掌体と区別することが困難であった。上記3)の分析システムでは、複数回の測定が必要であり、別々の装置で得られた各スペクトルのピークをひとつずつ帰属させる作業の煩雑さが大きな問題であった。さらに、不純物を多く含む試料では、各測定間で保持時間が微妙に変化しただけでピークの帰属が困難になる場合も多く、分析の再現性を高める方法が強く望まれていた。また移動相や試料を多く必要とすることも問題であった。
【0005】
本発明の目的は、目的成分である対掌体を明確に特定でき、標準品を用いずに光学活性体の分析を実現するシステムを提供することにある。
【課題を解決するための手段】
【0006】
このような状況下、本発明者らは鋭意検討を行った結果、本発明に至った。すなわち本発明は、光学活性体を分離できるクロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器とを連結することを特徴とする光学活性体分析システムを提供するものである。
【発明の効果】
【0007】
本発明によれば、光学活性体の分析において、標準品を用いずに当該光学活性体の分析を実現できる。また光学活性体を区別できる検出器を用いることで、光学不活性な不純物は検出されないため、夾雑物の影響を受けない。さらに、対掌体同士が完全に分離せず単一のピークとして検出される場合においても、対掌体を特定できる。
【図面の簡単な説明】
【0008】
【図1】本発明の装置構成の一例である。
【図2】実施例1のクロマトグラム(円二色性、254 nm)
【図3】実施例1の各ピークの核磁気共鳴スペクトルの比較
【図4】実施例2のクロマトグラム(紫外吸光、254 nm)
【図5】実施例2の各ピークの核磁気共鳴スペクトルの比較
【発明を実施するための形態】
【0009】
本発明において、クロマトグラフは目的の対掌体が分離できる手法であればよく、例えば光学活性体が分離できる媒体を接続した液体クロマトグラフ、ガスクロマトグラフ、超臨界流体クロマトグラフ、キャピラリー電気泳動、キャピラリー電気クロマトグラフ、光学活性固定相を固定化した薄層クロマトグラフなどが用いられる。
【0010】
本発明において、液体クロマトグラフには、低圧クロマトグラフ、中圧クロマトグラフ、高速液体クロマトグラフなどを用いることができる。なお、より好ましくは分離性能の優れた高速液体クロマトグラフが挙げられる。
【0011】
本発明において、液体クロマトグラフに接続する光学活性体が分離できる媒体には、光学活性固定相をガラスや金属製管内に充填したパックドカラム、キャピラリー内部表面に被覆もしくは共有結合させたキャピラリーカラム、マイクロチップ上の微細流路内部表面に被覆もしくは共有結合させたマイクロ分離チップなどを用いることができる。なお、パックドカラムは入手の容易さの面では好ましい。
【0012】
本発明において、液体クロマトグラフに接続するパックドカラムには、例えば水素結合型・電荷移動型として、住化分析センター製SUMICHIRAL OA-2000、SUMICHIRAL OA-2000I、SUMICHIRAL OA-2500、SUMICHIRAL OA-2500I、SUMICHIRAL OA-3100、SUMICHIRAL OA-3200、SUMICHIRAL OA-3300、SUMICHIRAL OA-4000、SUMICHIRAL OA-4100、SUMICHIRAL OA-4400、SUMICHIRAL OA-4500、SUMICHIRAL OA-4600、SUMICHIRAL OA-4700、SUMICHIRAL OA-4800、SUMICHIRAL OA-4900 、Eka Chemicals製Kromasil CHI-DMB、Kromasil CHI-TBB、MACHEREY-NAGEL製NUCLEOSIL CHIRAL-2、NUCLEOSIL CHIRAL-3、ZirChrom製ZirChrom-Chiral (S) LEU、ZirChrom-Chiral (R) NESA、ZirChrom-Chiral (S) NESA、ZirChrom-Chiral (S) PG、ZirChrom-Chiral (R) PG、Regis Technologies製 (R,R)-Whelk-O 1、(S,S)-Whelk-O 1、(R,R)-Whelk-O 2、(R,R)-Whelk-O 2、(R,R)-ULMO、(S,S)-ULMO、(R,R)-DACH-DNB、(S,S)-DACH-DNB、(3R,4S)-Pirkle 1-J、(3S,4R)-Pirkle 1-J、(R,R)-α-Burke 2、(S,S)-α-Burke 2、(R,R)-β-Gem 1、(S,S)-β-Gem 1、D-Leucine、L-Leucine、D-Phenylglycine、L-Phenylglycine、L-Naphthylleucineなど、配位子交換型として、住化分析センター製SUMICHIRAL OA-5000、SUMICHIRAL OA-6000、SUMICHIRAL OA-6100、ダイセル化学工業製CHIRALPAK WH、CHIRALPAK MA(+)、MACHEREY-NAGEL製NUCLEOSIL CHIRAL-1、Regis Technologies製Davankovなど、ホストゲスト型として、住化分析センター製SUMICHIRAL OA-7000、SUMICHIRAL OA-7100、SUMICHIRAL OA-7500、SUMICHIRAL OA-8000、ダイセル化学工業製CROWNPAK CR(+)、CROWNPAK CR(-)、MACHEREY-NAGEL製NUCLEODEX β-OH、NUCLEODEX α-PM、NUCLEODEX β-PM、NUCLEODEX γ-PM、信和化工製ULTRON ES-CD、ULTRON ES-PhCD、資生堂製Chiral CD-Ph、昭和電工製ORpak CDA-453 HQ、ORpak CDB-453 HQ、ORpak CDC-453 HQ、ORpak CDBS-453、ORpak CRX-853、Regis Technologies製 Chirosil RCA(+)、Chirosil SCA(+)など、アフィニティー型として、住化分析センター製SUMICHIRAL AGP、SUMICHIRAL CBH、SUMICHIRAL HSA 、CHIRAL AGP、MACHEREY-NAGEL製RESOLVOSIL BSA-7、信和化工製ULTRON ES-OVM、ULTRON ES-PEPSIN、ULTRON ES-BSA、昭和電工製AFpak ABA-894、Chrom Tech製Chiral AGP、Chiral CBH、Chiral HSAなど、らせん高分子型として、ダイセル化学工業製CHIRALPAK IA、CHIRALPAK IB、CHIRALPAK IC、CHIRALPAK AD-H、CHIRALPAK AD、CHIRALPAK AS-H、CHIRALPAK AS、CHIRALCEL OD-H、CHIRALCEL OD、CHIRALCEL OJ-H、CHIRALCEL OJ、CHIRALCEL OA、CHIRALCEL OB-H、CHIRALCEL OB、CHIRALCEL OC、CHIRALCEL OF、CHIRALCEL OG、CHIRALCEL OK、CHIRALPAK OT(+)、CHIRALPAK OP(+)、CHIRALPAK AD-RH、CHIRALPAK AS-RH、CHIRALCEL OD-RH、CHIRALCEL OJ-RH、Eka Chemicals製Kromasil CelluCoat、Kromasil AmyCoat、Kromasil CelluCoat RP、Kromasil AmyCoat RP 、東京化成製TCI Chiral BP-S、TCI Chiral CH-S、TCI Chiral MB-Sなど、上記以外のキラルカラムとして、例えば、光学活性な金属錯体を固定した資生堂製Ceramospher RU-1、Ceramospher RU-2や、イオン交換能を有する光学活性固定相を結合したダイセル化学工業製CHIRALPAK QN-AX、CHIRALPAK QD-AXや、前述の型を組み合わせた複合型キラルカラムなどを用いることができる。
【0013】
本発明において、液体クロマトグラフの移動相には、例えば炭化水素溶媒としては、ペンタン、ヘキサン、ヘプタン、ノナン、デカン、シクロヘキサンなどが、芳香族炭化水素としては、ベンゼン、トルエン、o-キシレン、m-キシレンなどが、ハロゲン溶媒としては、ジクロロメタン、クロロホルム、四塩化炭素、トリクロロエチレン、テトラクロロエチレン、塩化n-ブチル、クロロベンゼンなどが、エステル系移動相としては、酢酸メチル、酢酸エチル、酢酸n-ブチルなどが、ケトン溶媒としては、アセトン、エチルメチルケトン、イソブチルメチルケトンなどが、エーテル溶媒としては、ジエチルエーテル、テトラヒドロフラン、1,4-ジオキサンなどが、アルコール溶媒としては、メタノール、エタノール、1-プロパノール、2-プロパノール、1-メトキシエタノール、2-メトキシエタノール、1-ブタノールなどが、含窒素溶媒としては、アセトニトリル、ジエチルアミン、ピリジン、ジメチルホルムアミド、ジメチルアセトアミド、上記以外の溶媒としては、二硫化炭素、炭酸プロピレン、ジメチルスルホキシド、ギ酸、酢酸、トリフルオロ酢酸、リン酸、水、各種緩衝液、及び上記の重水素化溶媒、もしくはこれらを組み合わせたものなどを用いることができる。
【0014】
本発明において、ガスクロマトグラフに接続する光学活性体を分離する媒体には、光学活性固定相をガラスや金属製管内に充填したパックドカラム、キャピラリー内部表面に被覆もしくは共有結合させたキャピラリーカラム、マイクロチップ上の微細流路内部表面に被覆もしくは共有結合させたマイクロ分離チップなどを用いることができる。なお、キャピラリーカラムは入手の容易さの面では好ましい。
【0015】
本発明において、ガスクロマトグラフに用いられるパックドカラムもしくはキャピラリーカラムの光学活性固定相には、例えば、D,L−バリン誘導体、D,L−ロイシン誘導体、D,L−フェニルグリシン誘導体、D,L−ナフチルアラニン誘導体、D,L−ナフチルグリシン誘導体などのアミノ酸誘導体型の固定相や、α−シクロデキストリン誘導体、β−シクロデキストリン誘導体、γ−シクロデキストリン誘導体などの糖誘導体型の固定相などを用いることができる。
【0016】
本発明において、ガスクロマトグラフに用いられるキャピラリーカラムには、例えば、アミノ酸誘導体型としては、バリアン製CP-Chirasil-D-Val、CP-Chirasil-L-Val、などが、糖誘導体型としては、RESTEK製Rt-β-DEXm、Rt-β-DEXsm、Rt-β-DEXsp、Rt-β-DEXsa、Rt-β-DEXcst、Rt-γ-DEXsa、SGE製CYDEX-B、アジレント製HP-Chiral β、バリアン製CP-Cyclodextrin-β-2,3,6-M-19、CP-Chirasil-DEX CB、スペルコ製α-DEX 120、β-DEX 110、β-DEX 120、γ-DEX 120、α-DEX 225、β-DEX 225、γ-DEX 225、α-DEX 325、β-DEX 325、γ-DEX 325、J&W製Cyclodex-β、Cyclosil-β、GLサイエンス製Inertcap CHIRAMIX、Advanced Separations Technologies製CHIRALDEX G-BP、CHIRALDEX A-DA、CHIRALDEX B-DA、CHIRALDEX G-DA、CHIRALDEX B-DM、CHIRALDEX G-DM、CHIRALDEX B-DP、CHIRALDEX G-DP、CHIRALDEX A-PH、CHIRALDEX B-PH、CHIRALDEX B-PM、CHIRALDEX G-PN、CHIRALDEX A-TA、CHIRALDEX B-TA、CHIRALDEX G-TAなどを用いることができる。
【0017】
本発明において、超臨界流体クロマトグラフに接続する光学活性体を分離する媒体には、光学活性固定相を充填したパックドカラムやキャピラリーカラム内部表面に被覆もしくは共有結合させたキャピラリーカラムなどを用いることができる。なお、パックドカラムは入手の容易さの面では好ましい。
【0018】
本発明において、超臨界流体クロマトグラフに接続するパックドカラムには、らせん高分子型のダイセル化学工業製CHIRALPAK IA/SFC、CHIRALPAK IB/SFC、CHIRALPAK IC/SFC、CHIRALPAK AD-H/SFC、CHIRALPAK AS-H/SFC、CHIRALCEL OD-H/SFC、CHIRALCEL OJ-H/SFCなどを用いることができる。
【0019】
本発明において、超臨界流体クロマトグラフの移動相には、例えば二酸化炭素、亜酸化窒素、アンモニア、イソオクタン、ペンタン、ヘキサン、ヘプタン、ブタン、プロパン、エタン、エチレン、メタン、イソプロピルエーテル、ジエチルエーテル、キセノン、六フッ化硫黄、フロン類、水などを用いることができる。
【0020】
本発明において、超臨界流体クロマトグラフのモディファイヤーには、例えば、2-プロパノール、ジオキサン、アセトニトリル、テトラヒドロフラン、ジイソプロピルエーテル、ジメチルスルホキシド、メタノール、エタノール、上記の重水素化溶媒などを用いることができる。
【0021】
本発明において、キャピラリー電気泳動に接続する光学活性体を分離する媒体には、光学活性移動相もしくは擬似固定相を用いるキャピラリーなどが用いられる。
【0022】
本発明において、キャピラリー電気泳動に用いる光学活性移動相としては、例えば、らせん高分子型としては、α-シクロデキストリン、β-シクロデキストリン、γ-シクロデキストリン、シクロデキストリンの各種誘導体など、抗生物質型としては、バンコマイシン、テイコプラニン、リファマイシン、リストセチン、A82846B、MDL63,246など、配位子交換型として、銅―ヒドロキシプロリン複合体のような金属―アミノ酸もしくは金属―ペプチド複合体など、アフィニティー型としてはα-AGP、BSA、HSAなどのタンパク質を用いることができる。
【0023】
擬似固定相としては、例えば、N,N−ジデシル−L−アラニン、ポリウンデセノイル−L−バリン、N−ドデカノイル−L−アラ二ン、N−ドデカノイル−L−バリン、N−ドデカノイル−L−グルタミン酸、N−ドデカノイル−L−セリン、N−ドデカノイル−L−アスパラギン酸、N−テトラデカノイル−L−グルタメート、(S)−ドデコキシカルボニル−L−バリン、(R)−ドデコキシカルボニル−L−バリン、(S)−2−[(ドデコキシカルボニル)アミノ] −3−(S)−メチル−1−スルホキシペンタン、(R)−ドデコキシカルボニルプロリン、ドデシル−β−D−グルコピラノシド−6−リン酸エステル、n−ドデシル−β−D−グルコピラノシド−4,6−リン酸エステル、(2R,4R)−N−アセチル−2−ウンデシル−4−チアゾリジンカルボン酸、(2S,4S)−N−アセチル−2−ウンデシル−4−チアゾリジンカルボン酸、6−アミノペニシリン酸誘導体、(2R,3R)−ジ−n−ブチル酒石酸などの塩やN,N−ビス(3−D−グルコアミドプロピル)コールアミド、N,N−ビス(3−D−グルコアミドプロピル)デオキシコールアミドなどのキラル界面活性剤などを用いることができる。
【0024】
本発明において、キャピラリー電気クロマトグラフに接続する光学活性体を分離する媒体には、光学活性固定相で被膜もしくは共有結合させたキャピラリーなどが用いられる。
【0025】
本発明において、キャピラリー電気クロマトグラフに用いられる光学活性固定相としては、例えば、シクロデキストリン、クラウンエーテル、カリックスアレーン、各種抗生物質、タンパク質などを固定させた固定相、分子インプリンティング型の固定相などが挙げられる。
【0026】
本発明において、薄層クロマトグラフに用いられる光学活性固定相は、例えばセルロース、トリアセチルセルロース、シクロデキストリン、バンコマイシン、エリスロマイシン、L-アミノ酸などを用いることができる。
【0027】
本発明において、薄層クロマトグラフには、キラル移動相を用いることもでき、移動相としては、バンコマイシンなどの各種抗生物質や、BSA、HSAなどの各種タンパク質を用いることができる。
【0028】
光学活性体を分離する媒体を固定化した薄層クロマトグラフは、例えば加圧装置を用いる加圧薄層クロマトグラフ装置や、遠心薄層クロマトグラフなどと接続して用いることができる。
【0029】
検出器は、エナンチオマーを区別できるものであれば良く、円二色性分光計、赤外円二色性分光計及び旋光度計などを用いることができる。
【0030】
円二色性分光計の検出波長範囲は、通常220〜420 nmであり、目的とする光学活性体に応じて最適な波長を選択する。
【0031】
赤外円二色性分光計の検出波長範囲は、通常900〜3200 cm-1であり、目的とする光学活性体に応じて最適な波長を選択する。
【0032】
本発明において、光学活性体を区別できる検出器に加えて、汎用的な化学検出器を連結してもよい。これにより光学活性体を区別できる検出器では感度が得られない成分や光学不活性で検出されない不純物の溶出位置を確認することができる。
【0033】
汎用的な化学検出器としては、紫外吸光検出器、示差屈折度検出器、蛍光検出器などを用いることができる。なお、紫外吸光検出器は汎用性の面では好ましい。
【0034】
本発明において、化学構造の違いを区別できる分光器には、核磁気共鳴分光計や赤外分光計などを用いることができる。
【0035】
核磁気共鳴分光計の観測核には、1H、2H、3H、6Li、7Li、10B、11B、13C、14N、15N、17O、19F、23Na、27Al、29Si、31P、33S、35Cl、37Cl、59Co、77Se、103Rh、113Cd、119Sn、183W、195Pt、207Pbなどがあるが、1Hが感度及び汎用性の面では好ましい。
【0036】
赤外分光計の検出波長範囲は、通常400〜4000 cm-1であり、目的とする光学活性体に応じて最適な波長範囲を選択する。
【0037】
本発明において、クロマトグラフ、検出器及び分光器の接続方法は、直列もしくはスプリッターなどを用いて並列に接続してもよく、検出器及び分光器がクロマトグラフの下流であれば、どのような順番で接続されていてもよい。また少なくとも光学活性体を区別できる検出器及び分光器がそれぞれ一つ以上接続されていれば、検出器及び分光器の個数、種類をどのように組み合わせてもよい。
【0038】
本発明において、クロマトグラフ、検出器及び分光器はマイクロチップ上に一部もしくは全部を集約したものでもよい。
【実施例】
【0039】
以下に実施例により本発明を詳細に説明するが、本発明はこれらに限定されるものではない。
[実施例1]
装置の設定
高速液体クロマトグラフにキラルカラム、円二色性検出器及び核磁気共鳴装置を図1に示したように連結した。
【0040】
<HPLC条件>
ポンプ:バリアン Prostar model 230
円二色性検出器:日本分光 CD-2095
カラムオーブン:日本ウォーターズ Model 1122
カラム:CHIRALCEL OJ-RH(4.6×150 mm、5 μm)
移動相:10 mM リン酸重水緩衝液(pH 3.0)/アセトニトリル混液(75:25)
流速:1.0 mL/min
カラム温度:40 ℃
検出波長:254 nm(円二色性スペクトル)
<NMR条件>
分光器:バリアンINOVA-500(500MHz)
プローブ:フローセルプローブ(60 μL)
【0041】
Boc−3−(3−ピリジル)−L−アラニンベンジルエステルを主成分に、対掌体であるBoc−3−(3−ピリジル)−D−アラニンベンジルエステル及び、位置異性体であるBoc−3−(2−ピリジル)−L−アラニンベンジルエステル、Boc−3−(2−ピリジル)−D−アラニンベンジルエステル、Boc−3−(4−ピリジル)− L−アラニンベンジルエステル、Boc−3−(4−ピリジル)−D−アラニンベンジルエステルを微量成分とする試料を用いて測定を行なった。
【0042】
得られたクロマトグラムを図2、NMRスペクトルの比較を図3に示した。保持時間、スペクトルパターン、検出波長254 nmにおける円二色性スペクトルのコットン効果曲線の符号について表1に示した。
【0043】
【表1】

【0044】
表1に示したように、液体クロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器を連結することで、主成分とNMRパターンが等しく、コットン効果曲線の符号が逆となるピーク6が対掌体であると、一度の測定で一義的に決定することができた。
【0045】
[実施例2]
実施例1の円二色性検出器の下流に紫外吸光検出器(バリアン Prostar model 335)を接続し、検出波長を254 nmとして、その他は同条件で測定を行った。その結果、実施例1と同様の円二色性クロマトグラムに加えて、紫外吸収クロマトグラム(図4)が得られ、感度の低い円二色性クロマトグラムのみの場合よりもピーク6の溶出位置を明確に確認することができた。主成分とのNMRパターンの比較(図5)、及び、コットン効果曲線の符号からピーク6が対掌体であると決定できた。
【0046】
[比較例1]
液体クロマトグラフ質量分析計と液体クロマトグラフ円二色性検出器を別々に用いた既存の分析方法で、実施例と同様の試料を分析した。各ピークの分子量、検出波長254 nmにおける円二色性スペクトルのコットン効果曲線の符号について表2に示した。
【0047】
【表2】

(分子量測定の移動相には、10mM 酢酸アンモニウム緩衝液/アセトニトリルを使用)
【0048】
質量分析計を用いた既存の方法では、主成分と分子量が等しく、かつコットン効果曲線の符号が逆となるピークが5、6、8と複数存在し、対掌体の特定には至らなかった。
【符号の説明】
【0049】
1.ポンプ
2.カラム
3.円二色性検出器
4.核磁気共鳴分光計
【特許請求の範囲】
【請求項1】
光学活性体を分離できるクロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器を連結することを特徴とする光学活性体分析システム。
【請求項2】
請求項1に記載の光学活性体を分離できるクロマトグラフが、キラルカラムを接続した高速液体クロマトグラフである請求項1に記載の光学活性体分析システム。
【請求項3】
光学活性体が区別できる検出器が、円二色性分光計である請求項1又は2に記載の光学活性体分析システム。
【請求項4】
化学構造の違いを区別できる分光器が、核磁気共鳴分光計である請求項1、2又は3に記載の光学活性体分析システム。
【請求項5】
請求項1〜4のいずれかに記載の光学活性体分析システムに、更に紫外吸光検出器を連結した光学活性体分析システム。
【請求項1】
光学活性体を分離できるクロマトグラフと光学活性体が区別できる検出器と化学構造を区別できる分光器を連結することを特徴とする光学活性体分析システム。
【請求項2】
請求項1に記載の光学活性体を分離できるクロマトグラフが、キラルカラムを接続した高速液体クロマトグラフである請求項1に記載の光学活性体分析システム。
【請求項3】
光学活性体が区別できる検出器が、円二色性分光計である請求項1又は2に記載の光学活性体分析システム。
【請求項4】
化学構造の違いを区別できる分光器が、核磁気共鳴分光計である請求項1、2又は3に記載の光学活性体分析システム。
【請求項5】
請求項1〜4のいずれかに記載の光学活性体分析システムに、更に紫外吸光検出器を連結した光学活性体分析システム。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2010−249558(P2010−249558A)
【公開日】平成22年11月4日(2010.11.4)
【国際特許分類】
【出願番号】特願2009−96699(P2009−96699)
【出願日】平成21年4月13日(2009.4.13)
【出願人】(000002093)住友化学株式会社 (8,981)
【公開日】平成22年11月4日(2010.11.4)
【国際特許分類】
【出願日】平成21年4月13日(2009.4.13)
【出願人】(000002093)住友化学株式会社 (8,981)
[ Back to top ]

