光触媒用酸化チタニウム粒子およびその製造方法
【課題】
光触媒活性の高い酸化チタニウム粒子およびその製造方法を提供する。
【解決手段】
本発明は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子、およびその製造方法であってチタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、当該有機酸を、当該有機酸と水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程(S100)と、混合溶液を50〜100℃の範囲に保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程(S200)と、加水分解・結晶化工程後の溶液から当該溶液に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程(S300)と、固体生成物を200〜350℃の範囲で加熱する加熱工程(S400)と、を含む光触媒用酸化チタニウム粒子の製造方法に関する。
光触媒活性の高い酸化チタニウム粒子およびその製造方法を提供する。
【解決手段】
本発明は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子、およびその製造方法であってチタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、当該有機酸を、当該有機酸と水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程(S100)と、混合溶液を50〜100℃の範囲に保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程(S200)と、加水分解・結晶化工程後の溶液から当該溶液に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程(S300)と、固体生成物を200〜350℃の範囲で加熱する加熱工程(S400)と、を含む光触媒用酸化チタニウム粒子の製造方法に関する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、光触媒用酸化チタニウム粒子およびその製造方法に関する。
【背景技術】
【0002】
光触媒は、紫外線等の照射によってその表面に発生するヒドロキシラジカル等により、該表面に存在する有害物質を分解する機能を有する触媒である。酸化チタニウムは、光触媒として最もポピュラーな材料であり、アナターゼ型の結晶体の触媒活性が最も大きいことが知られている。酸化チタニウムの製造法は、気相法(塩素法ともいう)、液相法に大別され、液相法も水熱法、硫酸法、ゾル・ゲル法等の多数の製造法に分けられる。
【0003】
例えば、気相法(塩素法)および液相法に属する硫酸法は、共に、酸化チタニウム粒子の工業的製法として確立されている製造法である。塩素法は、四塩化チタニウムを高温で焼成して酸化チタニウム粒子を製造する方法である。硫酸法は、例えば硫酸チタニルを加水分解して含水酸化チタニウムを生成し、これを焼成して酸化チタニウム粒子を製造する方法である。塩素法の場合、800℃以上の高温下で気相反応させる必要から、酸化チタニウム粒子同士の焼結が生じ、比表面積が小さくなり、触媒活性が低くなる。これに対して、硫酸法の場合、塩素法よりも低温で酸化チタニウムを製造できるものの、アナターゼ型の結晶割合を高め、また不純物を揮発除去するには、400℃以上の高温にて焼成する必要がある。加えて、硫酸法の場合には、加熱後に、濾過、洗浄などの工程が必要となり、工程が煩雑となるという問題もある。
【0004】
かかる理由から、塩素法および硫酸法よりも低温にて、アナターゼ型の結晶体を主とする酸化チタニウムを製造できる水熱法が着目されている。例えば、有機溶剤への耐性の低い部材への酸化チタニウム含有スラリーのコーティングを可能とし、低温にて比表面積の大きなアナターゼ型を主とした酸化チタニウム粒子を製造することを目的に、有機溶剤を含まない水系のチタニアゾル水溶液、チタニアゲル体又はチタニアゾル・ゲル混合体を、密閉容器内で加熱および加圧処理し、乾燥することによって酸化チタニウムを製造する方法が知られている(例えば、特許文献1を参照)。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2000−233928号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかし、上記例示の製造法にて得られた酸化チタニウム粒子には、次のような問題がある。上記製造法では、300℃以下の温度で加熱しているため、粒子同士の焼結が抑制され、比較的高い比表面積を有する酸化チタニウム粒子が得られる。しかし、その比表面積は50〜100m2/gの範囲に留まっており、さらなる高比表面積を有し、光触媒活性をより高めた酸化チタニウム粒子が望まれている。また、酸化チタニウム粒子の結晶相がアナターゼ型を主としつつも、ブルッカイト型の結晶相も含まれており、アナターゼ型単一相であって光触媒活性のより高い酸化チタニウム粒子が望まれている。
【0007】
本発明は、上記問題を解決するためになされたものであり、光触媒活性の高い酸化チタニウム粒子およびその製造方法を提供することを目的とする。
【課題を解決するための手段】
【0008】
上記目的を達成するための本発明の一形態は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子である。
【0009】
本発明の別の形態は、さらに、窒素ドープされている光触媒用酸化チタニウム粒子である。
【0010】
本発明の一形態は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子を製造する方法であって、チタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、有機酸を、有機酸と水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程と、混合溶液を50〜100℃の範囲に保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程と、加水分解・結晶化工程後の溶液から当該溶液に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程と、固体生成物を200〜350℃の範囲で加熱する加熱工程と、を含む光触媒用酸化チタニウム粒子の製造方法である。
【0011】
本発明の別の形態は、さらに、チタニウムアルコキシドをチタニウムテトライソプロポキシドとし、アルコールを2−プロパノールとする光触媒用酸化チタニウム粒子の製造方法である。
【0012】
本発明の別の形態は、混合溶液作製工程において、N−O結合若しくはN−N結合を有する含窒素化合物を有機酸と混合してpHが1.0〜9.0の範囲となる混合溶液を作製する光触媒用酸化チタニウム粒子の製造方法である。
【0013】
本発明の別の形態は、さらに、含窒素化合物をヒドロキシルアミンとする光触媒用酸化チタニウム粒子の製造方法である。
【発明の効果】
【0014】
本発明によれば、光触媒活性の高い酸化チタニウム粒子を得ることができる。
【図面の簡単な説明】
【0015】
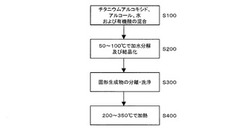
【図1】図1は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【図2】図2は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【図3】図3は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【図4】図4は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【図5】図5は、実験例1にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。
【図6】図6は、実験例1にて作製した酸化チタニウム粒子の一部の細孔径分布を比較して示す。
【図7】図7は、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子の細孔径分布を比較して示す。
【図8】図8は、実験例1にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図9】図9は、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図10】図10は、実験例1にて作製した酸化チタニウム粒子の1種(ギ酸10wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【図11】図11は、実験例1にて作製した酸化チタニウム粒子の1種(酸を使用せずに作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【図12】図12は、実験例2にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。
【図13】図13は、実験例2にて作製した酸化チタニウム粒子の一部(酢酸7wt%使用して作製したもの)の細孔径分布を比較して示す。
【図14】図14は、実験例1,2にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図15】図15は、実験例2にて作製した酸化チタニウム粒子の1種(酢酸7wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【図16】図16は、実験例3にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。
【図17】図17は、実験例1の一部を含め、実験例3にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図18】図18は、実験例4にて作製した2種類の酸化チタニウム粒子と、実験例1にてギ酸無しおよびギ酸10wt%の条件で作製した2種類の酸化チタニウム粒子の合計4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。
【図19】図19は、実験例1の一部を含め、実験例4にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図20】図20は、実験例5にて作製した4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。
【図21】図21は、実験例5にて作製した酸化チタニウム粒子の一部(ギ酸10wt%+ヒドロキシルアミン10wt%の条件で作製したもの)の細孔径分布を示す。
【図22】図22は、実験例5にて作製した4種類の酸化チタニウム粒子およびヒドロキシルアミン1wt%の条件下で溶液Bを用意して作製した酸化チタニウム粒子のそれぞれの光触媒活性を比較して示す。
【図23】図23は、実験例5においてヒドロキシルアミン1wt%の条件にて作製した酸化チタニウム粒子の雰囲気を変えて加熱したときの熱分析結果を示す。
【図24】図24は、実験例5においてギ酸10wt%とヒドロキシルアミン1wt%の条件にて作製した酸化チタニウム粒子の雰囲気を変えて加熱したときの熱分析結果を示す。
【図25】図25は、実験例5においてギ酸10wt%とヒドロキシルアミン10wt%の条件にて作製した酸化チタニウム粒子の雰囲気を変えて加熱したときの熱分析結果を示す。
【図26】図26は、実験例5においてヒドロキシルアミン1wt%、ヒドロキシルアミン1wt%とギ酸10wt%、およびヒドロキシルアミン10wt%とギ酸10wt%の3水準で溶液Bを用意して作製した3種類の酸化チタニウムのXPSチャート(N1s)を示す。
【図27】図27は、図26に示す3種類の酸化チタニウムのXPSチャート(Ti2p)を示す。
【図28】図28は、図26に示す3種類の酸化チタニウムのXPSチャート(O1s)を示す。
【発明を実施するための形態】
【0016】
次に、本発明の光触媒用酸化チタニウム粒子およびその製造方法の好適な実施の形態について説明する。
【0017】
<1.光触媒用酸化チタニウム粒子>
本実施の形態に係る光触媒用酸化チタニウム粒子は、アナターゼ型単一相から成り、比表面積が170m2/g以上であって、主に紫外線応答型の光触媒として用いられる。酸化チタニウム粒子は、その製造に用いる原料由来の有機物を加熱除去する必要から加熱工程を経る。このときの温度に応じて比表面積も上下するが、有機物の除去と光触媒活性を高く維持するように加熱温度を選択すると、170〜220m2/gの範囲の比表面積の酸化チタニウム粒子が好ましい。ここで、比表面積は、窒素吸脱着法により得られるBET値である。光触媒用酸化チタニウム粒子は、ルチル型、ブルッカイト型といった結晶相を含まないアナターゼ型単一相であって、かつ粒子径が小さいため、極めて光触媒活性が高い。アナターゼ型単一相であるか否かは、例えば、CuKα線源を用いた粉末X線回折装置を用いて同定できる。
【0018】
この実施の形態に係る光触媒用酸化チタニウム粒子は、窒素をドープすることによって可視光応答型の光触媒として利用可能である。窒素をドープした光触媒用酸化チタニウム粒子も、アナターゼ型単一相から成る。比表面積は250m2/g以上になる。紫外線応答型と同様、有機物の除去と光触媒活性を高く維持する観点から、250〜300m2/gの範囲の比表面積の酸化チタニウム粒子が好ましい。窒素のドープ量は、例えば、X線光電子分光法にて容易に評価できる。
【0019】
<2.紫外線応答型の光触媒用酸化チタニウム粒子の製造方法>
図1は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【0020】
図1に示すように、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子の製造方法は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子を製造する方法であって、
チタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、有機酸を、有機酸と水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程(ステップS100)と、
混合溶液を50〜100℃の範囲に保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程(ステップS200)と、
加水分解・結晶化工程後の溶液から、当該溶液中に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程(ステップS300)と、
固体生成物を200〜350℃の範囲で加熱する加熱工程(ステップS400)と、
を少なくとも含む。
【0021】
以下、各工程について説明する。
【0022】
(1)混合溶液作製工程(ステップS100)
チタニウムアルコキシドには、チタニウムテトラエトキシド、チタニウムテトラプロポキシド、チタニウムテトライソプロポキシド、チタニウムテトラブトキシド、チタニウムテトライソブトキシド、チタニウムテトライソプロペニルオキシドなどが挙げられる。また、これらのオリゴマーも使用することが出来る。上記の各チタニウムアルコキシドの内、特に好ましい例は、チタニウムテトライソプロポキシドおよびチタニウムテトラブトキシドである。
【0023】
アルコールとしては、メタノール、エタノール、1−プロパノール、1−ブタノール、1−ペンタノール、1−ヘキサノール等の第一級アルコールの他、2−プロパノール、2−ブタノール等の第二級アルコール等を例示できる。上記の各アルコールの内、特に好ましい例は、2−プロパノールおよび1−ブタノールである。アルコールは、チタニウムアルコキシド1モルに対して、3〜20モルの割合で混合されるのが好ましく、特に5〜13モル、より好ましくは8〜11モルの割合で混合される。
【0024】
有機酸は、ギ酸、酢酸またはそれらの混合物であり、チタニウムアルコキシドの加水分解および酸化チタニウムの結晶化の際、酸化チタニウムの結晶化促進剤として機能する。ギ酸または酢酸は、カルボキシル基に結合する部分が水素またはメチル基であるため、炭素数の多いアルキル基を有するカルボン酸に比べて、チタニウムアルコキシドの加水分解・結晶化工程によって生成した固形生成物に炭素化合物として残存することを抑制できる。有機酸としてギ酸を用いる場合、チタニウムアルコキシドが全て酸化チタニウムに変化したときの質量に対する実際に得られた酸化チタニウムの質量の割合(これを、収率または回収率という)は60〜65%であるが、酢酸を用いた場合の該割合は55〜62%である。このように、酸化チタニウム粒子の収率を向上させるという観点では、2種類の有機酸の内、ギ酸を用いるのが好ましい。一方、取り扱い上の安全面を高くするという観点では、有害性の低い酢酸を用いるのが好ましい。
【0025】
有機酸としてギ酸または酢酸を用いる場合、有機酸と水の総量に対して有機酸を5質量%以上にすると、酸化チタニウムの結晶型をアナターゼ型単一相としやすくなる。ギ酸を用いる場合には、ギ酸と水の総量に対してギ酸を好ましくは5〜60質量%、より好ましくは5〜50質量%とする。一方、酢酸を用いる場合には、酢酸と水の総量に対して酢酸を好ましくは5〜10質量%、より好ましくは6〜8質量%とする。有機酸と水の総量は、チタニウムアルコキシドの質量に対して20〜50倍混合するのが好ましく、25〜35倍混合するのが特に好ましく、28〜32倍混合するのがさらに好ましい。
【0026】
(2)加水分解・結晶化工程(ステップS200)
この工程は、有機酸の存在下、チタニウムアルコキシドを加水分解して酸化チタニウムを結晶化する工程である。この工程では、ステップS100により得られた混合溶液を50〜100℃、より好ましくは60〜80℃にて加熱する。加熱時間は、3〜48時間、好ましくは12〜36時間、さらに好ましくは18〜30時間である。従来の水熱法と同様に加圧容器を用いて大気圧より高圧の下で加水分解・結晶化工程を行うことも可能であるが、本実施の形態では、大気圧若しくは大気圧より1〜50%程度高い圧力下でも十分に加水分解および酸化チタニウムの結晶化を行うことができる。加水分解・結晶化工程により得られた酸化チタニウムは、有機酸存在下において、アナターゼ型の結晶化が促進される。
【0027】
(3)分離・洗浄工程(ステップS300)
この工程は、加水分解・結晶化工程(ステップS200)にて得られた溶液(固形生成物である酸化チタニウムを含む)から、固形生成物を分離し、かつ洗浄する工程である。分離および洗浄する方法としては、遠心分離、フィルターを用いて濾過するフィルトレーション等の如何なる方法を用いて実行することができる。分離・洗浄の操作は、1回のみでも良いが、未反応のアルコキシドやアルコール等の不純物の除去と収率向上の両方を考慮すると、5回、10回等の複数回行う方が好ましい。
【0028】
(4)加熱工程(ステップS400)
この工程は、加熱によって、固形生成物である酸化チタニウムに付着あるいは結合する水や有機物を揮発除去する工程である。加熱する温度は、350℃以下、より好ましくは200〜350℃の範囲である。200℃以上の温度で加熱することにより、水や有機物を除去しやすくなる。また、350℃以下の温度で加熱することにより、酸化チタニウム粒子同士の焼結を抑制し、高い比表面積を維持可能である。加熱時間は、好ましくは0.2〜10時間、さらに好ましくは1〜5時間であり、例えば250℃で加熱する場合には、1〜3時間が好ましい。
【0029】
次に、より具体的な酸化チタニウム粒子の製造工程について説明する。
【0030】
図2は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【0031】
図2に示すように、この実施の形態における紫外線応答型の光触媒用酸化チタニウム粒子は、チタニウムアルコキシドとアルコールとを混合して溶液Aを作製する工程(ステップS110)を行い、それと併行して、水(好ましくは、蒸留水やイオン交換水)と有機酸(ギ酸、酢酸、またはそれら両方の混合物)とを混合して溶液Bを作製する工程(ステップS120)を行い、次に、溶液Bを攪拌しながら溶液Aを滴下して両溶液A,Bを混合して懸濁液Cを作製する工程(ステップS130)を行い、次に、懸濁液Cを50〜100℃で所定時間保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程(ステップS200)を行い、次に、加水分解・結晶化工程により得られた溶液を遠心分離して固形生成物と上澄み液とを分離するとともに洗浄を行う遠心分離・洗浄工程(ステップS300a)を繰り返し(例えば、5回)行い、次に、固形生成物を80℃で12時間乾燥する乾燥工程(ステップS310)を行い、次に、乾燥物を粉砕する粉砕工程(ステップS320)を行い、次に、粉砕物を250℃にて2時間加熱する加熱工程(ステップS400)を行うことにより製造できる。
【0032】
図1に示す混合溶液作製工程は、図2に示すステップS110〜ステップS130から成る。ステップS110は、好適には、相対湿度10%未満のグローブボックス内で行う。これは、チタニウムアルコキシドが空気中の水分と反応するのを抑制する必要からであるが、湿度が低い条件であればどのような雰囲気でも良く、例えば、窒素ガス若しくはアルゴンガスフロー雰囲気、それらガスを密閉した雰囲気などでも良い。また、ステップS120にてチタニウムアルコキシド以外のアルコール、水および有機酸の3種溶液を混合し、ステップS130にて、当該混合した溶液にチタニウムアルコキシドを滴下するようにしても良い。
【0033】
図2に示す遠心分離・洗浄工程(ステップS300a)は、図1に示す分離・洗浄工程(ステップS300)の下位概念の工程である。したがって、ステップS300では、遠心分離以外の分離手法を用いることもできる。遠心分離は、例えば、5000〜50000rpm、好ましくは10000〜25000rpmにて行うことができるが、固形生成物の粒度分布に応じて変更できる。また、分離・洗浄の処理は、5回に限らず、1〜4回、または6回以上であっても良い。乾燥工程(ステップS310)では、加熱温度以下の温度であれば、80℃に限定されず、さらに乾燥時間も12時間に限定されない。粉砕工程(ステップS320)は、粉砕の必要性に応じて行う工程であって、ボールミルを用いた方法、乳鉢を用いた方法の他、如何なる手法を用いて行っても良い。
【0034】
<3.可視光応答型の光触媒用酸化チタニウム粒子の製造方法>
図3は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【0035】
図3に示すように、この製造方法は、図1に示す混合溶液作製工程(ステップS100)に代替して、チタニウムアルコキシド、アルコール、水および有機酸に追加して、含窒素化合物を混合する混合溶液作製工程(ステップS150)を実行する点において、図1に示す製造方法と異なる。それ以降の工程は、図1に示すフローと同様の工程である。混合溶液作製工程(ステップS150)において混合する含窒素化合物は、N−O結合若しくはN−N結合を有する化合物である。これらのいずれかの結合を有する含窒素化合物としては、ヒドロキシルアミンおよびヒドラジンを好適に例示でき、特に好ましい例としてヒドロキシアミンを挙げることができる。上記含窒素化合物は、有機酸と混合してpHが1.0〜9.0の範囲となるように混合されるのが好ましい。pHを9.0以下にすることにより、酸化チタニウムの結晶性が良くなる。一方、有機酸を、有機酸と水の総量に対して60質量%まで加えたときであっても、含窒素化合物を添加してpHを最低でも1.0以上にすることにより、光触媒活性の高い酸化チタニウム粒子を得やすい。
【0036】
図4は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【0037】
図4に示すように、この製造方法は、図2に示す溶液Bの作製工程(ステップS120)に代替して、水および有機酸に追加して、含窒素化合物を混合する工程(ステップS160)を実行する点において、図2に示す製造方法と異なる。それ以外の工程は、図2に示すフローと同様の工程である。
【実施例】
【0038】
次に、本発明の実施例について説明する。なお、下記実施例は、本発明の一例にすぎず、本発明は下記実施例に限定されるものではない。
【0039】
1.試料
酸化チタニウム作製用の試料は、以下の通りである。
(1)チタニウムアルコキシド
チタニウムテトライソプロポキシド(「2−プロパノール」ともいう。「TTIP」、供給元: 東京化成工業株式会社)
チタニウムテトラn−ブトキシド(「TTB」、供給元: 和光純薬工業株式会社)
(2)アルコール
イソプロピルアルコール(「IPA」、供給元: 和光純薬工業株式会社)
n−ブタノール(「n−BtOH」、供給元: 和光純薬工業株式会社)
(3)有機酸
ギ酸(供給元: 和光純薬工業株式会社)
酢酸(供給元: 和光純薬工業株式会社)
(4)含窒素化合物
50%ヒドロキシルアミン水溶液(供給元: 和光純薬工業株式会社)
(5)水
蒸留水
【0040】
比較に用いた光触媒は、以下の通りである。
P25(供給元: 日本アエロジル株式会社): 紫外線照射用酸化チタニウム
【0041】
2.評価方法
(1)光触媒活性
石英セル内にて、加熱処理を経た酸化チタニウム粒子20mgを5%酢酸水溶液2gに混ぜて懸濁する。紫外線を照射する評価の場合には、150Wのキセノンランプを光源に用いて、ガラスフィルターによって熱線と270nm未満の波長をカットして、波長が270nm以上の光を上記懸濁液に照射する。光照射開始から10分毎に石英セル内の気相を0.2ml分取して、酢酸の光分解で生成する二酸化炭素の量をガスクロマトグラフィによって定量する。また、可視光を照射する評価の場合には、熱線と440nm未満の波長をカットして、波長が440nm以上の光を上記懸濁液に照射する。その後、光照射開始から60分毎に石英セル内の気相を0.2ml分取して、酢酸の光分解で生成する二酸化炭素の量をガスクロマトグラフィによって定量する。かかる手法は、酢酸の光分解速度をガスクロマトグラフィによって定量化するものである。ガスクロマトグラフィには、ガスクロマトグラフ(株式会社島津製作所製、型式:GC−14B)を用いた。
(2)酸化チタニウムの結晶相の同定
粒子X線回折装置(株式会社リガク製、型式:Rint2500 HF/PC)において、CuKα線源を用いて、加熱処理前の酸化チタニウムの結晶相を同定した。
(3)比表面積、細孔容積および細孔径
窒素吸脱着法により、加熱処理を経た酸化チタニウムを評価した。装置には、高速比表面積/細孔分布測定装置(マイクロメリティクス・インスツルメント・コーポレーション製、型式:ASAP2010)を用いた。
(4)熱分析
TG−DTAにより、乾燥、粉砕後であって加熱処理前の酸化チタニウムを試料として、該試料中の酸触媒等の残留程度を評価した。装置には、差動型示差熱天秤(株式会社リガク製、型式:TG8120)を用いた。
(5)元素分析
加熱処理を経た酸化チタニウム中への窒素ドープ量は、X線光電子分光法により評価した。装置には、X線光電子分析装置(KRATOS社製、型式:AXIS−ULTRA DLD形)を用いた。窒素ドープ量の定量は、次の方法にて行った。Ti2p、O1sおよびN1sに帰属されるピークの面積から各元素の存在比を求め、当該存在比に基づき[N]/[Ti]値を算出し、当該[N]/[Ti]値を窒素ドープ量とした。
(6)収率
チタニウムアルコキシドが全て酸化チタニウムに変化した場合を100として、実際に得られた酸化チタニウムの質量を百分率(%)で示した。具体的には、得られた酸化チタニウムの質量を、チタニウムアルコキシドのモル数と酸化チタニウムの分子量(79.84)を掛けた数値で除し、100を掛けて算出した。
【0042】
3.酸化チタニウム作製方法
3.1 実験例1(ギ酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
3.55g(12.5mmol)のTTIPと、7.51g(125mmol)のIPAを、相対湿度10%未満のグローブボックス内でそれぞれ分取して容器内に入れ、マグネチックスターラーを用いて1時間攪拌して、溶液Aを作製した。次に、ギ酸+水の質量に対するギ酸の質量の百分率(%)を0、0.5、2、5、10、20および40wt%に調整した合計7種類のギ酸水溶液を大気下にて用意し、それぞれの水溶液から100mlを分取して溶液Bを準備した。次に、各溶液Bを激しく攪拌しながら、溶液Aを滴下し、7種類の懸濁液Cを作製した。次に、各懸濁液を密閉容器に入れ、80℃の恒温槽内で24時間静置した。次に、各懸濁液を入れた容器を遠心分離装置にセットして、回転速度15000rpmにて10〜30分間遠心分離を行い、上澄みの除去、蒸留水の添加を行って再度の遠心分離を行う操作を合計5回繰り返した。遠心分離後、容器内の白色沈殿物を掻き出し、別の容器に移して、乾燥機内にて80℃で12時間乾燥した。次に、乾燥後の固形生成物をジルコニア製の乳鉢で約10分間粉砕して粒子化した。次に、粒子化した試料0.3gをアルミナボートに入れ、酸素:窒素=4:1、流速200ml/minの気流雰囲気にて、250℃で2時間の加熱処理を行った。また、ギ酸10wt%の溶液Bを用いた場合については、加熱温度のみを変え、350℃で2時間加熱して酸化チタニウム粒子を作製し、加熱温度による性能の違いも調べた。
【0043】
(2)酸化チタニウム粒子の評価結果
表1に、実験例1にて作製した各酸化チタニウム粒子の一部の比表面積、平均細孔径、細孔容積および結晶相を比較して示す。図5に、実験例1にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。図6に、実験例1にて作製した酸化チタニウム粒子の一部の細孔径分布を比較して示す。図7に、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子の細孔径分布を比較して示す。図8に、実験例1にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。図9に、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。図10に、実験例1にて作製した酸化チタニウム粒子の1種(ギ酸10wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。図11に、実験例1にて作製した酸化チタニウム粒子の1種(酸を使用せずに作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【0044】
【表1】

【0045】
表1に示すように、実験例1にて作製した酸化チタニウム粒子は、いずれも170m2/g以上の比表面積を有する粒子であった。表1に、350℃で加熱した酸化チタニウム粒子の物性を250℃で加熱したものと比較して示すが、350℃で加熱しても比表面積は低下せず、アナターゼ型の結晶相のみを持つ酸化チタニウム粒子を得られることを確認した。また、図5に示すように、ギ酸2wt%(0.5M)まではアナターゼ(Anatase)型の結晶相を主としつつもブルッカイト(Brookite)型の結晶相をも含む酸化チタニウムが得られたが、ギ酸5〜40wt%の範囲ではアナターゼ型単一相の酸化チタニウム粒子が得られた。また、図6および図7に示すように、溶液B中のギ酸の割合が増えると、酸化チタニウム粒子の比表面積が大きく変化せずに細孔径および細孔容積が増大する傾向および加熱温度が上昇してもほぼ同じ細孔径分布を持つ酸化チタニウム粒子を得ることができることが認められた。ギ酸の割合が増えるに伴い細孔径および細孔容積が増大するのは、酸化チタニウム粒子の粒子径分布が小さくなることに起因すると考えられる。図8および図9に示すように、ギ酸の割合の増加に伴い光触媒活性が高くなる傾向、および加熱温度の上昇により光触媒活性が僅かに低くなる傾向が認められた。しかし、いずれの酸化チタニウム粒子も、市販の酸化チタニウム粒子(P25)よりも高い光触媒活性を有していることがわかった。また、ギ酸を用いた場合の酸化チタニウム粒子の収率は、ギ酸0.5wt%のときに62%、ギ酸20wt%のときに65%であった。さらに、ギ酸を用いずに作製した酸化チタニウム粒子およびギ酸を用いて作製した酸化チタニウム粒子では、図10および図11に示すように、250〜450℃の温度域で大きな発熱ピークが認められなかった。このことから、ギ酸は、酸化チタニウムの製造工程において250℃までの加熱で除去され、粒子に残留していないものと考えられる。
【0046】
3.2 実験例2(酢酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
酢酸+水の質量に対する酢酸の質量の百分率(%)を0.7および7wt%に調整した2種類の酢酸水溶液を大気下にて用意し、それぞれの水溶液から100mlを分取して溶液Bを準備した。溶液Bの作製および加熱温度を250℃のみとしたこと以外については、実験例1と同様の作製方法にて、酸化チタニウム粒子を作製した。
【0047】
(2)酸化チタニウム粒子の評価結果
図12に、実験例2にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。図13に、実験例2にて作製した酸化チタニウム粒子の一部(酢酸7wt%使用して作製したもの)の細孔径分布を比較して示す。図14に、実験例1,2にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。図15に、実験例2にて作製した酸化チタニウム粒子の1種(酢酸7wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【0048】
実験例2で作製した酸化チタニウム粒子は、200m2/g以上の比表面積を有する粒子であった。特に、酢酸7wt%(1M)を用いて作製した酸化チタニウム粒子は、212m2/gという高い比表面積を有し、平均細孔径が71オングストローム、細孔容積が0.374cc/gであった。酢酸を用いた方が、ギ酸を用いるよりも、細孔容積および比表面積の大きな酸化チタニウム粒子が得られることがわかった。酢酸0.7wt%(0.1M)を用いて作製した酸化チタニウム粒子は、アナターゼ型の結晶相を主としつつもブルッカイト型の結晶相をも含む酸化チタニウム粒子であったが、酢酸7wt%(1M)を用いて作製した酸化チタニウム粒子は、アナターゼ型単一相の酸化チタニウム粒子であった。酢酸0.7wt%を用いて作製した酸化チタニウム粒子は、ギ酸0.5wt%を用いて作製した酸化チタニウム粒子と同様、市販の酸化チタニウム粒子(P25)よりわずかに高い光触媒活性を有しているに留まったが、酢酸7wt%を用いて作製した酸化チタニウム粒子は、市販の酸化チタニウム粒子(P25)に比べて非常に高い光触媒活性を有していることがわかった。これは、酢酸7wt%を用いて作製した酸化チタニウム粒子がアナターゼ型の結晶相のみから成ることに起因すると考えられる。
【0049】
酢酸を用いて作製した酸化チタニウム粒子(加熱工程前)では、図15に示すように、350℃近傍で大きな発熱ピークが認められた。このことから、酢酸は、酸化チタニウムの製造工程において250℃までの加熱で完全に除去されずに、粒子に残留していると考えられる。また、酢酸0.7wt%および酢酸7wt%を用いてそれぞれ作製した酸化チタニウム粒子の各収率は、61%および57%であった。これらの値は、前述のギ酸を用いたときの収率62%および65%に比べると若干低い。このことから、収率の観点では、ギ酸を用いた方が、若干、有利であると考えられる。
【0050】
3.3 実験例3(比較実験―塩酸、硝酸、硫酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
0.1M、1Mおよび2Mの3種類の塩酸水溶液、1Mの硝酸水溶液および1Mの硫酸水溶液をそれぞれ大気下にて用意して、それぞれから100mlを分取して合計5種類の無機酸水溶液(溶液B)を作製した。溶液Bの作製および加熱温度を250℃のみとしたこと以外の条件については、実験例1と同様の作製方法にて、酸化チタニウム粒子を作製した。
【0051】
(2)酸化チタニウム粒子の評価結果
図16に、実験例3にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。図17に、実験例1の一部を含め、実験例3にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【0052】
1M以上の塩酸水溶液および1Mの硝酸水溶液をそれぞれ用いて作製した酸化チタニウム粒子は、アナターゼ型の結晶相以外にルチル(Rutile)型結晶相を含んでおり、0.1Mの塩酸水溶液を用いて作製した酸化チタニウム粒子はアナターゼ型の結晶相以外にブルッカイト型の結晶相を含んでいた。これに対して、1Mの硫酸水溶液を用いて作製した酸化チタニウム粒子はアナターゼ型の単一相からなっていた。しかし、図17に示すように、塩酸水溶液、硝酸水溶液、硫酸水溶液のいずれを用いて作製した酸化チタニウム粒子も、実験例1でギ酸5wt%(1M)を用いて作製した酸化チタニウム粒子および市販の酸化チタニウム粒子(P25)に比べて、光触媒活性が低いものであった。
【0053】
3.4 実験例4(チタニウムアルコキシドおよびアルコールの種類を変えた製法)
(1)酸化チタニウム粒子の作製方法
実験例1におけるTTIPに代えてTTBを、IPAに代えてn−BtOHを用いて、12.5mmolのTTBと、125mmolのn−BtOHを、相対湿度10%未満のグローブボックス内でそれぞれ分取して容器内に入れ、マグネチックスターラーを用いて1時間攪拌して、溶液Aを作製した。次に、実験例1と同様の手法によって10wt%のギ酸水溶液(溶液B)を作製した。その後の工程は、加熱温度を250℃として実験例1と同様の工程を行い、酸化チタニウム粒子を作製した。なお、ギ酸の有無による性能の違いを確認するため、実験例4の上記工程においてギ酸を加えずに酸化チタニウム粒子を作製した。
【0054】
(2)酸化チタニウム粒子の評価結果
図18に、実験例4にて作製した2種類の酸化チタニウム粒子と、実験例1にてギ酸無しおよびギ酸10wt%の条件で作製した2種類の酸化チタニウム粒子の合計4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。図19に、実験例1の一部を含め、実験例4にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【0055】
図18に示すように、チタニウムアルコキシドとしてTTBを、アルコールとしてn−BtOHを用いても、アナターゼ型の単一相から成る酸化チタニウム粒子が得られることがわかった。また、図19に示すように、チタニウムアルコキシドをTTIPからTTBに、アルコールをIPAからn−BtOHにそれぞれ変えても、市販の酸化チタニウム粒子(P25)および酸を加えずに作製した酸化チタニウム粒子よりも高い光触媒活性を有していることが確認された。
【0056】
3.5 実験例5(ヒドロキシルアミンとギ酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
可視光応答型光触媒用酸化チタニウム粒子を製造するため、実験例1における溶液Bの作製に際して、ギ酸を10wt%に固定し、含窒素化合物であるヒドロキシルアミンを1および10wt%の2水準選択し、ギ酸10wt%とヒドロキシルアミン1wt%を含む溶液と、ギ酸10wt%とヒドロキシルアミン10wt%を含む溶液の2種類の溶液Bを作製した。それ以外の工程については、実験例1と同一条件として、粉砕までの工程を実行した。その後の加熱工程は、実験例1の加熱条件中の雰囲気を、窒素雰囲気および空気雰囲気の2種類とした。この結果、ヒドロキシルアミンの添加量および加熱条件を変えた合計4種類の酸化チタニウム粒子を作製できた。また、比較のため、溶液Bの作製に際して、ギ酸を加えずにヒドロキシルアミン(濃度:1wt%)のみを水に混合する条件とし、かつ空気中で焼成して作製した酸化チタニウム粒子、およびギ酸10wt%のみを水に混合してヒドロキシルアミンを加えずに溶液Bを作製後、空気中で焼成して作製した酸化チタニウム粒子も用意した。
【0057】
(2)酸化チタニウム粒子の評価結果
表2に、実験例5にて作製した3種の溶液Bと、実験例1にて作製した一部の溶液B(4種)のpHを示す。図20に、実験例5にて作製した4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。図21に、実験例5にて作製した4種類の酸化チタニウム粒子の一部(ギ酸10wt%+ヒドロキシルアミン10wt%の条件で作製したもの)の細孔径分布を示す。図22に、実験例5にて作製した4種類の酸化チタニウム粒子およびヒドロキシルアミン1wt%の条件下で溶液Bを用意して作製した酸化チタニウム粒子のそれぞれの光触媒活性を比較して示す。
【0058】
【表2】

【0059】
表2に示すように、実験例1で作製したギ酸5〜40wt%およびヒドロキシルアミン無添加の溶液Bでは、pHは、2.09〜1.09の範囲で変化することがわかった。一方、実験例5にて作製した3種類の溶液Bでは、pHは、2.83〜9.3の範囲で変化することがわかった。ヒドロキシルアミン1wt%のみを加えてギ酸を加えていない溶液Bを用いると、酸化チタニウム粒子の光触媒活性が低すぎるため、pH=9.3となるようにヒドロキシルアミンを加えても、光触媒活性の高い酸化チタニウム粒子は得られないと考えられる。ヒドロキシルアミン1wt%の条件でギ酸10wt%とすると、溶液BのpH=2.83となり、酸化チタニウム粒子の光触媒活性が高くなる。さらに、ギ酸およびヒドロキシルアミンを共に10wt%とすると、溶液BのpH=6.15となり、光触媒活性の高い酸化チタニウム粒子が得られる。また、実験例1で作製した酸化チタニウム粒子のように、ヒドロキシルアミンを加えずにギ酸のみを加えた場合には、溶液BのpH=1.09〜2.09の範囲となり、光触媒活性の高い酸化チタニウム粒子が得られる。この結果から、ヒドロキシルアミンとギ酸とを加えて溶液Bを用意する場合、pH=1〜9の範囲になるようにするのが好ましいことがわかる。また、図20に示すように、ギ酸とヒドロキシルアミンを用いて作製した酸化チタニウム粒子は、ギ酸のみを用いて作製したものと同様、アナターゼ型単一相から成る粒子であった。ギ酸10wt%およびヒドロキシルアミン10wt%を用いて作製した酸化チタニウム粒子の比表面積、平均細孔径および細孔容積は、それぞれ、284m2/g、49オングストロームおよび0.348cc/gであり、非常に粒子径の小さい粒子であることがわかった。なお、ヒドロキシルアミンのみを用い、酸を用いずに酸化チタニウム粒子を作製したが、その結晶性は低かった。ギ酸10wt%とヒドロキシルアミン10wt%の条件で作製した酸化チタニウム粒子は、ヒドロキシルアミンのみの条件で作製した酸化チタニウム粒子、およびギ酸10wt%とヒドロキシルアミン1wt%の条件で作製した酸化チタニウム粒子よりも、可視光照射下において高い光触媒活性を有していた。
【0060】
図23〜図25に、実験例5においてギ酸とヒドロキシルアミンの量を変えて作製した合計6種類の酸化チタニウム粒子(加熱工程前)の雰囲気を変えて加熱したときの熱分析結果を示す。
【0061】
実験例5にて作製したいずれの酸化チタニウム粒子でも、酸素の有無を問わず、250℃までに重量減少が認められることから、250℃にてギ酸およびヒドロキシルアミンを十分に脱離できることが確認された。
【0062】
図26〜図28に、実験例5においてヒドロキシルアミン1wt%、ヒドロキシルアミン1wt%とギ酸10wt%、およびヒドロキシルアミン10wt%とギ酸10wt%の3水準で溶液Bを用意して作製した加熱後(250℃、空気中)の3種類の酸化チタニウムのXPSチャート(N1s、Ti2pおよびO1sの3種類)を示す。
【0063】
ヒドロキシルアミン1wt%、ヒドロキシルアミン1wt%とギ酸10wt%、およびヒドロキシルアミン10wt%とギ酸10wt%の3条件で作製した酸化チタニウム粒子の各窒素ドープ量は、それぞれ、0.082、0.044および0.056であった。いずれの酸化チタニウム粒子にも窒素がドープされていることが確認された。
【産業上の利用可能性】
【0064】
本発明は、光触媒機能を発揮する成形体、塗膜などに利用可能である。
【技術分野】
【0001】
本発明は、光触媒用酸化チタニウム粒子およびその製造方法に関する。
【背景技術】
【0002】
光触媒は、紫外線等の照射によってその表面に発生するヒドロキシラジカル等により、該表面に存在する有害物質を分解する機能を有する触媒である。酸化チタニウムは、光触媒として最もポピュラーな材料であり、アナターゼ型の結晶体の触媒活性が最も大きいことが知られている。酸化チタニウムの製造法は、気相法(塩素法ともいう)、液相法に大別され、液相法も水熱法、硫酸法、ゾル・ゲル法等の多数の製造法に分けられる。
【0003】
例えば、気相法(塩素法)および液相法に属する硫酸法は、共に、酸化チタニウム粒子の工業的製法として確立されている製造法である。塩素法は、四塩化チタニウムを高温で焼成して酸化チタニウム粒子を製造する方法である。硫酸法は、例えば硫酸チタニルを加水分解して含水酸化チタニウムを生成し、これを焼成して酸化チタニウム粒子を製造する方法である。塩素法の場合、800℃以上の高温下で気相反応させる必要から、酸化チタニウム粒子同士の焼結が生じ、比表面積が小さくなり、触媒活性が低くなる。これに対して、硫酸法の場合、塩素法よりも低温で酸化チタニウムを製造できるものの、アナターゼ型の結晶割合を高め、また不純物を揮発除去するには、400℃以上の高温にて焼成する必要がある。加えて、硫酸法の場合には、加熱後に、濾過、洗浄などの工程が必要となり、工程が煩雑となるという問題もある。
【0004】
かかる理由から、塩素法および硫酸法よりも低温にて、アナターゼ型の結晶体を主とする酸化チタニウムを製造できる水熱法が着目されている。例えば、有機溶剤への耐性の低い部材への酸化チタニウム含有スラリーのコーティングを可能とし、低温にて比表面積の大きなアナターゼ型を主とした酸化チタニウム粒子を製造することを目的に、有機溶剤を含まない水系のチタニアゾル水溶液、チタニアゲル体又はチタニアゾル・ゲル混合体を、密閉容器内で加熱および加圧処理し、乾燥することによって酸化チタニウムを製造する方法が知られている(例えば、特許文献1を参照)。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2000−233928号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかし、上記例示の製造法にて得られた酸化チタニウム粒子には、次のような問題がある。上記製造法では、300℃以下の温度で加熱しているため、粒子同士の焼結が抑制され、比較的高い比表面積を有する酸化チタニウム粒子が得られる。しかし、その比表面積は50〜100m2/gの範囲に留まっており、さらなる高比表面積を有し、光触媒活性をより高めた酸化チタニウム粒子が望まれている。また、酸化チタニウム粒子の結晶相がアナターゼ型を主としつつも、ブルッカイト型の結晶相も含まれており、アナターゼ型単一相であって光触媒活性のより高い酸化チタニウム粒子が望まれている。
【0007】
本発明は、上記問題を解決するためになされたものであり、光触媒活性の高い酸化チタニウム粒子およびその製造方法を提供することを目的とする。
【課題を解決するための手段】
【0008】
上記目的を達成するための本発明の一形態は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子である。
【0009】
本発明の別の形態は、さらに、窒素ドープされている光触媒用酸化チタニウム粒子である。
【0010】
本発明の一形態は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子を製造する方法であって、チタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、有機酸を、有機酸と水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程と、混合溶液を50〜100℃の範囲に保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程と、加水分解・結晶化工程後の溶液から当該溶液に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程と、固体生成物を200〜350℃の範囲で加熱する加熱工程と、を含む光触媒用酸化チタニウム粒子の製造方法である。
【0011】
本発明の別の形態は、さらに、チタニウムアルコキシドをチタニウムテトライソプロポキシドとし、アルコールを2−プロパノールとする光触媒用酸化チタニウム粒子の製造方法である。
【0012】
本発明の別の形態は、混合溶液作製工程において、N−O結合若しくはN−N結合を有する含窒素化合物を有機酸と混合してpHが1.0〜9.0の範囲となる混合溶液を作製する光触媒用酸化チタニウム粒子の製造方法である。
【0013】
本発明の別の形態は、さらに、含窒素化合物をヒドロキシルアミンとする光触媒用酸化チタニウム粒子の製造方法である。
【発明の効果】
【0014】
本発明によれば、光触媒活性の高い酸化チタニウム粒子を得ることができる。
【図面の簡単な説明】
【0015】
【図1】図1は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【図2】図2は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【図3】図3は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【図4】図4は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【図5】図5は、実験例1にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。
【図6】図6は、実験例1にて作製した酸化チタニウム粒子の一部の細孔径分布を比較して示す。
【図7】図7は、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子の細孔径分布を比較して示す。
【図8】図8は、実験例1にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図9】図9は、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図10】図10は、実験例1にて作製した酸化チタニウム粒子の1種(ギ酸10wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【図11】図11は、実験例1にて作製した酸化チタニウム粒子の1種(酸を使用せずに作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【図12】図12は、実験例2にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。
【図13】図13は、実験例2にて作製した酸化チタニウム粒子の一部(酢酸7wt%使用して作製したもの)の細孔径分布を比較して示す。
【図14】図14は、実験例1,2にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図15】図15は、実験例2にて作製した酸化チタニウム粒子の1種(酢酸7wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【図16】図16は、実験例3にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。
【図17】図17は、実験例1の一部を含め、実験例3にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図18】図18は、実験例4にて作製した2種類の酸化チタニウム粒子と、実験例1にてギ酸無しおよびギ酸10wt%の条件で作製した2種類の酸化チタニウム粒子の合計4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。
【図19】図19は、実験例1の一部を含め、実験例4にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【図20】図20は、実験例5にて作製した4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。
【図21】図21は、実験例5にて作製した酸化チタニウム粒子の一部(ギ酸10wt%+ヒドロキシルアミン10wt%の条件で作製したもの)の細孔径分布を示す。
【図22】図22は、実験例5にて作製した4種類の酸化チタニウム粒子およびヒドロキシルアミン1wt%の条件下で溶液Bを用意して作製した酸化チタニウム粒子のそれぞれの光触媒活性を比較して示す。
【図23】図23は、実験例5においてヒドロキシルアミン1wt%の条件にて作製した酸化チタニウム粒子の雰囲気を変えて加熱したときの熱分析結果を示す。
【図24】図24は、実験例5においてギ酸10wt%とヒドロキシルアミン1wt%の条件にて作製した酸化チタニウム粒子の雰囲気を変えて加熱したときの熱分析結果を示す。
【図25】図25は、実験例5においてギ酸10wt%とヒドロキシルアミン10wt%の条件にて作製した酸化チタニウム粒子の雰囲気を変えて加熱したときの熱分析結果を示す。
【図26】図26は、実験例5においてヒドロキシルアミン1wt%、ヒドロキシルアミン1wt%とギ酸10wt%、およびヒドロキシルアミン10wt%とギ酸10wt%の3水準で溶液Bを用意して作製した3種類の酸化チタニウムのXPSチャート(N1s)を示す。
【図27】図27は、図26に示す3種類の酸化チタニウムのXPSチャート(Ti2p)を示す。
【図28】図28は、図26に示す3種類の酸化チタニウムのXPSチャート(O1s)を示す。
【発明を実施するための形態】
【0016】
次に、本発明の光触媒用酸化チタニウム粒子およびその製造方法の好適な実施の形態について説明する。
【0017】
<1.光触媒用酸化チタニウム粒子>
本実施の形態に係る光触媒用酸化チタニウム粒子は、アナターゼ型単一相から成り、比表面積が170m2/g以上であって、主に紫外線応答型の光触媒として用いられる。酸化チタニウム粒子は、その製造に用いる原料由来の有機物を加熱除去する必要から加熱工程を経る。このときの温度に応じて比表面積も上下するが、有機物の除去と光触媒活性を高く維持するように加熱温度を選択すると、170〜220m2/gの範囲の比表面積の酸化チタニウム粒子が好ましい。ここで、比表面積は、窒素吸脱着法により得られるBET値である。光触媒用酸化チタニウム粒子は、ルチル型、ブルッカイト型といった結晶相を含まないアナターゼ型単一相であって、かつ粒子径が小さいため、極めて光触媒活性が高い。アナターゼ型単一相であるか否かは、例えば、CuKα線源を用いた粉末X線回折装置を用いて同定できる。
【0018】
この実施の形態に係る光触媒用酸化チタニウム粒子は、窒素をドープすることによって可視光応答型の光触媒として利用可能である。窒素をドープした光触媒用酸化チタニウム粒子も、アナターゼ型単一相から成る。比表面積は250m2/g以上になる。紫外線応答型と同様、有機物の除去と光触媒活性を高く維持する観点から、250〜300m2/gの範囲の比表面積の酸化チタニウム粒子が好ましい。窒素のドープ量は、例えば、X線光電子分光法にて容易に評価できる。
【0019】
<2.紫外線応答型の光触媒用酸化チタニウム粒子の製造方法>
図1は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【0020】
図1に示すように、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子の製造方法は、アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子を製造する方法であって、
チタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、有機酸を、有機酸と水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程(ステップS100)と、
混合溶液を50〜100℃の範囲に保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程(ステップS200)と、
加水分解・結晶化工程後の溶液から、当該溶液中に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程(ステップS300)と、
固体生成物を200〜350℃の範囲で加熱する加熱工程(ステップS400)と、
を少なくとも含む。
【0021】
以下、各工程について説明する。
【0022】
(1)混合溶液作製工程(ステップS100)
チタニウムアルコキシドには、チタニウムテトラエトキシド、チタニウムテトラプロポキシド、チタニウムテトライソプロポキシド、チタニウムテトラブトキシド、チタニウムテトライソブトキシド、チタニウムテトライソプロペニルオキシドなどが挙げられる。また、これらのオリゴマーも使用することが出来る。上記の各チタニウムアルコキシドの内、特に好ましい例は、チタニウムテトライソプロポキシドおよびチタニウムテトラブトキシドである。
【0023】
アルコールとしては、メタノール、エタノール、1−プロパノール、1−ブタノール、1−ペンタノール、1−ヘキサノール等の第一級アルコールの他、2−プロパノール、2−ブタノール等の第二級アルコール等を例示できる。上記の各アルコールの内、特に好ましい例は、2−プロパノールおよび1−ブタノールである。アルコールは、チタニウムアルコキシド1モルに対して、3〜20モルの割合で混合されるのが好ましく、特に5〜13モル、より好ましくは8〜11モルの割合で混合される。
【0024】
有機酸は、ギ酸、酢酸またはそれらの混合物であり、チタニウムアルコキシドの加水分解および酸化チタニウムの結晶化の際、酸化チタニウムの結晶化促進剤として機能する。ギ酸または酢酸は、カルボキシル基に結合する部分が水素またはメチル基であるため、炭素数の多いアルキル基を有するカルボン酸に比べて、チタニウムアルコキシドの加水分解・結晶化工程によって生成した固形生成物に炭素化合物として残存することを抑制できる。有機酸としてギ酸を用いる場合、チタニウムアルコキシドが全て酸化チタニウムに変化したときの質量に対する実際に得られた酸化チタニウムの質量の割合(これを、収率または回収率という)は60〜65%であるが、酢酸を用いた場合の該割合は55〜62%である。このように、酸化チタニウム粒子の収率を向上させるという観点では、2種類の有機酸の内、ギ酸を用いるのが好ましい。一方、取り扱い上の安全面を高くするという観点では、有害性の低い酢酸を用いるのが好ましい。
【0025】
有機酸としてギ酸または酢酸を用いる場合、有機酸と水の総量に対して有機酸を5質量%以上にすると、酸化チタニウムの結晶型をアナターゼ型単一相としやすくなる。ギ酸を用いる場合には、ギ酸と水の総量に対してギ酸を好ましくは5〜60質量%、より好ましくは5〜50質量%とする。一方、酢酸を用いる場合には、酢酸と水の総量に対して酢酸を好ましくは5〜10質量%、より好ましくは6〜8質量%とする。有機酸と水の総量は、チタニウムアルコキシドの質量に対して20〜50倍混合するのが好ましく、25〜35倍混合するのが特に好ましく、28〜32倍混合するのがさらに好ましい。
【0026】
(2)加水分解・結晶化工程(ステップS200)
この工程は、有機酸の存在下、チタニウムアルコキシドを加水分解して酸化チタニウムを結晶化する工程である。この工程では、ステップS100により得られた混合溶液を50〜100℃、より好ましくは60〜80℃にて加熱する。加熱時間は、3〜48時間、好ましくは12〜36時間、さらに好ましくは18〜30時間である。従来の水熱法と同様に加圧容器を用いて大気圧より高圧の下で加水分解・結晶化工程を行うことも可能であるが、本実施の形態では、大気圧若しくは大気圧より1〜50%程度高い圧力下でも十分に加水分解および酸化チタニウムの結晶化を行うことができる。加水分解・結晶化工程により得られた酸化チタニウムは、有機酸存在下において、アナターゼ型の結晶化が促進される。
【0027】
(3)分離・洗浄工程(ステップS300)
この工程は、加水分解・結晶化工程(ステップS200)にて得られた溶液(固形生成物である酸化チタニウムを含む)から、固形生成物を分離し、かつ洗浄する工程である。分離および洗浄する方法としては、遠心分離、フィルターを用いて濾過するフィルトレーション等の如何なる方法を用いて実行することができる。分離・洗浄の操作は、1回のみでも良いが、未反応のアルコキシドやアルコール等の不純物の除去と収率向上の両方を考慮すると、5回、10回等の複数回行う方が好ましい。
【0028】
(4)加熱工程(ステップS400)
この工程は、加熱によって、固形生成物である酸化チタニウムに付着あるいは結合する水や有機物を揮発除去する工程である。加熱する温度は、350℃以下、より好ましくは200〜350℃の範囲である。200℃以上の温度で加熱することにより、水や有機物を除去しやすくなる。また、350℃以下の温度で加熱することにより、酸化チタニウム粒子同士の焼結を抑制し、高い比表面積を維持可能である。加熱時間は、好ましくは0.2〜10時間、さらに好ましくは1〜5時間であり、例えば250℃で加熱する場合には、1〜3時間が好ましい。
【0029】
次に、より具体的な酸化チタニウム粒子の製造工程について説明する。
【0030】
図2は、本実施の形態に係る紫外線応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【0031】
図2に示すように、この実施の形態における紫外線応答型の光触媒用酸化チタニウム粒子は、チタニウムアルコキシドとアルコールとを混合して溶液Aを作製する工程(ステップS110)を行い、それと併行して、水(好ましくは、蒸留水やイオン交換水)と有機酸(ギ酸、酢酸、またはそれら両方の混合物)とを混合して溶液Bを作製する工程(ステップS120)を行い、次に、溶液Bを攪拌しながら溶液Aを滴下して両溶液A,Bを混合して懸濁液Cを作製する工程(ステップS130)を行い、次に、懸濁液Cを50〜100℃で所定時間保持してチタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程(ステップS200)を行い、次に、加水分解・結晶化工程により得られた溶液を遠心分離して固形生成物と上澄み液とを分離するとともに洗浄を行う遠心分離・洗浄工程(ステップS300a)を繰り返し(例えば、5回)行い、次に、固形生成物を80℃で12時間乾燥する乾燥工程(ステップS310)を行い、次に、乾燥物を粉砕する粉砕工程(ステップS320)を行い、次に、粉砕物を250℃にて2時間加熱する加熱工程(ステップS400)を行うことにより製造できる。
【0032】
図1に示す混合溶液作製工程は、図2に示すステップS110〜ステップS130から成る。ステップS110は、好適には、相対湿度10%未満のグローブボックス内で行う。これは、チタニウムアルコキシドが空気中の水分と反応するのを抑制する必要からであるが、湿度が低い条件であればどのような雰囲気でも良く、例えば、窒素ガス若しくはアルゴンガスフロー雰囲気、それらガスを密閉した雰囲気などでも良い。また、ステップS120にてチタニウムアルコキシド以外のアルコール、水および有機酸の3種溶液を混合し、ステップS130にて、当該混合した溶液にチタニウムアルコキシドを滴下するようにしても良い。
【0033】
図2に示す遠心分離・洗浄工程(ステップS300a)は、図1に示す分離・洗浄工程(ステップS300)の下位概念の工程である。したがって、ステップS300では、遠心分離以外の分離手法を用いることもできる。遠心分離は、例えば、5000〜50000rpm、好ましくは10000〜25000rpmにて行うことができるが、固形生成物の粒度分布に応じて変更できる。また、分離・洗浄の処理は、5回に限らず、1〜4回、または6回以上であっても良い。乾燥工程(ステップS310)では、加熱温度以下の温度であれば、80℃に限定されず、さらに乾燥時間も12時間に限定されない。粉砕工程(ステップS320)は、粉砕の必要性に応じて行う工程であって、ボールミルを用いた方法、乳鉢を用いた方法の他、如何なる手法を用いて行っても良い。
【0034】
<3.可視光応答型の光触媒用酸化チタニウム粒子の製造方法>
図3は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子の製造方法の一例の大まかな流れを示すフローチャートである。
【0035】
図3に示すように、この製造方法は、図1に示す混合溶液作製工程(ステップS100)に代替して、チタニウムアルコキシド、アルコール、水および有機酸に追加して、含窒素化合物を混合する混合溶液作製工程(ステップS150)を実行する点において、図1に示す製造方法と異なる。それ以降の工程は、図1に示すフローと同様の工程である。混合溶液作製工程(ステップS150)において混合する含窒素化合物は、N−O結合若しくはN−N結合を有する化合物である。これらのいずれかの結合を有する含窒素化合物としては、ヒドロキシルアミンおよびヒドラジンを好適に例示でき、特に好ましい例としてヒドロキシアミンを挙げることができる。上記含窒素化合物は、有機酸と混合してpHが1.0〜9.0の範囲となるように混合されるのが好ましい。pHを9.0以下にすることにより、酸化チタニウムの結晶性が良くなる。一方、有機酸を、有機酸と水の総量に対して60質量%まで加えたときであっても、含窒素化合物を添加してpHを最低でも1.0以上にすることにより、光触媒活性の高い酸化チタニウム粒子を得やすい。
【0036】
図4は、本実施の形態に係る可視光応答型の光触媒用酸化チタニウム粒子のより具体的な製造工程の一例を示すフローチャートである。
【0037】
図4に示すように、この製造方法は、図2に示す溶液Bの作製工程(ステップS120)に代替して、水および有機酸に追加して、含窒素化合物を混合する工程(ステップS160)を実行する点において、図2に示す製造方法と異なる。それ以外の工程は、図2に示すフローと同様の工程である。
【実施例】
【0038】
次に、本発明の実施例について説明する。なお、下記実施例は、本発明の一例にすぎず、本発明は下記実施例に限定されるものではない。
【0039】
1.試料
酸化チタニウム作製用の試料は、以下の通りである。
(1)チタニウムアルコキシド
チタニウムテトライソプロポキシド(「2−プロパノール」ともいう。「TTIP」、供給元: 東京化成工業株式会社)
チタニウムテトラn−ブトキシド(「TTB」、供給元: 和光純薬工業株式会社)
(2)アルコール
イソプロピルアルコール(「IPA」、供給元: 和光純薬工業株式会社)
n−ブタノール(「n−BtOH」、供給元: 和光純薬工業株式会社)
(3)有機酸
ギ酸(供給元: 和光純薬工業株式会社)
酢酸(供給元: 和光純薬工業株式会社)
(4)含窒素化合物
50%ヒドロキシルアミン水溶液(供給元: 和光純薬工業株式会社)
(5)水
蒸留水
【0040】
比較に用いた光触媒は、以下の通りである。
P25(供給元: 日本アエロジル株式会社): 紫外線照射用酸化チタニウム
【0041】
2.評価方法
(1)光触媒活性
石英セル内にて、加熱処理を経た酸化チタニウム粒子20mgを5%酢酸水溶液2gに混ぜて懸濁する。紫外線を照射する評価の場合には、150Wのキセノンランプを光源に用いて、ガラスフィルターによって熱線と270nm未満の波長をカットして、波長が270nm以上の光を上記懸濁液に照射する。光照射開始から10分毎に石英セル内の気相を0.2ml分取して、酢酸の光分解で生成する二酸化炭素の量をガスクロマトグラフィによって定量する。また、可視光を照射する評価の場合には、熱線と440nm未満の波長をカットして、波長が440nm以上の光を上記懸濁液に照射する。その後、光照射開始から60分毎に石英セル内の気相を0.2ml分取して、酢酸の光分解で生成する二酸化炭素の量をガスクロマトグラフィによって定量する。かかる手法は、酢酸の光分解速度をガスクロマトグラフィによって定量化するものである。ガスクロマトグラフィには、ガスクロマトグラフ(株式会社島津製作所製、型式:GC−14B)を用いた。
(2)酸化チタニウムの結晶相の同定
粒子X線回折装置(株式会社リガク製、型式:Rint2500 HF/PC)において、CuKα線源を用いて、加熱処理前の酸化チタニウムの結晶相を同定した。
(3)比表面積、細孔容積および細孔径
窒素吸脱着法により、加熱処理を経た酸化チタニウムを評価した。装置には、高速比表面積/細孔分布測定装置(マイクロメリティクス・インスツルメント・コーポレーション製、型式:ASAP2010)を用いた。
(4)熱分析
TG−DTAにより、乾燥、粉砕後であって加熱処理前の酸化チタニウムを試料として、該試料中の酸触媒等の残留程度を評価した。装置には、差動型示差熱天秤(株式会社リガク製、型式:TG8120)を用いた。
(5)元素分析
加熱処理を経た酸化チタニウム中への窒素ドープ量は、X線光電子分光法により評価した。装置には、X線光電子分析装置(KRATOS社製、型式:AXIS−ULTRA DLD形)を用いた。窒素ドープ量の定量は、次の方法にて行った。Ti2p、O1sおよびN1sに帰属されるピークの面積から各元素の存在比を求め、当該存在比に基づき[N]/[Ti]値を算出し、当該[N]/[Ti]値を窒素ドープ量とした。
(6)収率
チタニウムアルコキシドが全て酸化チタニウムに変化した場合を100として、実際に得られた酸化チタニウムの質量を百分率(%)で示した。具体的には、得られた酸化チタニウムの質量を、チタニウムアルコキシドのモル数と酸化チタニウムの分子量(79.84)を掛けた数値で除し、100を掛けて算出した。
【0042】
3.酸化チタニウム作製方法
3.1 実験例1(ギ酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
3.55g(12.5mmol)のTTIPと、7.51g(125mmol)のIPAを、相対湿度10%未満のグローブボックス内でそれぞれ分取して容器内に入れ、マグネチックスターラーを用いて1時間攪拌して、溶液Aを作製した。次に、ギ酸+水の質量に対するギ酸の質量の百分率(%)を0、0.5、2、5、10、20および40wt%に調整した合計7種類のギ酸水溶液を大気下にて用意し、それぞれの水溶液から100mlを分取して溶液Bを準備した。次に、各溶液Bを激しく攪拌しながら、溶液Aを滴下し、7種類の懸濁液Cを作製した。次に、各懸濁液を密閉容器に入れ、80℃の恒温槽内で24時間静置した。次に、各懸濁液を入れた容器を遠心分離装置にセットして、回転速度15000rpmにて10〜30分間遠心分離を行い、上澄みの除去、蒸留水の添加を行って再度の遠心分離を行う操作を合計5回繰り返した。遠心分離後、容器内の白色沈殿物を掻き出し、別の容器に移して、乾燥機内にて80℃で12時間乾燥した。次に、乾燥後の固形生成物をジルコニア製の乳鉢で約10分間粉砕して粒子化した。次に、粒子化した試料0.3gをアルミナボートに入れ、酸素:窒素=4:1、流速200ml/minの気流雰囲気にて、250℃で2時間の加熱処理を行った。また、ギ酸10wt%の溶液Bを用いた場合については、加熱温度のみを変え、350℃で2時間加熱して酸化チタニウム粒子を作製し、加熱温度による性能の違いも調べた。
【0043】
(2)酸化チタニウム粒子の評価結果
表1に、実験例1にて作製した各酸化チタニウム粒子の一部の比表面積、平均細孔径、細孔容積および結晶相を比較して示す。図5に、実験例1にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。図6に、実験例1にて作製した酸化チタニウム粒子の一部の細孔径分布を比較して示す。図7に、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子の細孔径分布を比較して示す。図8に、実験例1にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。図9に、実験例1にて加熱温度を変えて作製した2種類の酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。図10に、実験例1にて作製した酸化チタニウム粒子の1種(ギ酸10wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。図11に、実験例1にて作製した酸化チタニウム粒子の1種(酸を使用せずに作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【0044】
【表1】

【0045】
表1に示すように、実験例1にて作製した酸化チタニウム粒子は、いずれも170m2/g以上の比表面積を有する粒子であった。表1に、350℃で加熱した酸化チタニウム粒子の物性を250℃で加熱したものと比較して示すが、350℃で加熱しても比表面積は低下せず、アナターゼ型の結晶相のみを持つ酸化チタニウム粒子を得られることを確認した。また、図5に示すように、ギ酸2wt%(0.5M)まではアナターゼ(Anatase)型の結晶相を主としつつもブルッカイト(Brookite)型の結晶相をも含む酸化チタニウムが得られたが、ギ酸5〜40wt%の範囲ではアナターゼ型単一相の酸化チタニウム粒子が得られた。また、図6および図7に示すように、溶液B中のギ酸の割合が増えると、酸化チタニウム粒子の比表面積が大きく変化せずに細孔径および細孔容積が増大する傾向および加熱温度が上昇してもほぼ同じ細孔径分布を持つ酸化チタニウム粒子を得ることができることが認められた。ギ酸の割合が増えるに伴い細孔径および細孔容積が増大するのは、酸化チタニウム粒子の粒子径分布が小さくなることに起因すると考えられる。図8および図9に示すように、ギ酸の割合の増加に伴い光触媒活性が高くなる傾向、および加熱温度の上昇により光触媒活性が僅かに低くなる傾向が認められた。しかし、いずれの酸化チタニウム粒子も、市販の酸化チタニウム粒子(P25)よりも高い光触媒活性を有していることがわかった。また、ギ酸を用いた場合の酸化チタニウム粒子の収率は、ギ酸0.5wt%のときに62%、ギ酸20wt%のときに65%であった。さらに、ギ酸を用いずに作製した酸化チタニウム粒子およびギ酸を用いて作製した酸化チタニウム粒子では、図10および図11に示すように、250〜450℃の温度域で大きな発熱ピークが認められなかった。このことから、ギ酸は、酸化チタニウムの製造工程において250℃までの加熱で除去され、粒子に残留していないものと考えられる。
【0046】
3.2 実験例2(酢酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
酢酸+水の質量に対する酢酸の質量の百分率(%)を0.7および7wt%に調整した2種類の酢酸水溶液を大気下にて用意し、それぞれの水溶液から100mlを分取して溶液Bを準備した。溶液Bの作製および加熱温度を250℃のみとしたこと以外については、実験例1と同様の作製方法にて、酸化チタニウム粒子を作製した。
【0047】
(2)酸化チタニウム粒子の評価結果
図12に、実験例2にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。図13に、実験例2にて作製した酸化チタニウム粒子の一部(酢酸7wt%使用して作製したもの)の細孔径分布を比較して示す。図14に、実験例1,2にて作製した各酸化チタニウム粒子の一部および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。図15に、実験例2にて作製した酸化チタニウム粒子の1種(酢酸7wt%使用して作製したもの)の250〜800℃の温度域におけるTG−DTAのグラフ(A)およびその一部(点線で囲った部分)の拡大図(B)を示す。
【0048】
実験例2で作製した酸化チタニウム粒子は、200m2/g以上の比表面積を有する粒子であった。特に、酢酸7wt%(1M)を用いて作製した酸化チタニウム粒子は、212m2/gという高い比表面積を有し、平均細孔径が71オングストローム、細孔容積が0.374cc/gであった。酢酸を用いた方が、ギ酸を用いるよりも、細孔容積および比表面積の大きな酸化チタニウム粒子が得られることがわかった。酢酸0.7wt%(0.1M)を用いて作製した酸化チタニウム粒子は、アナターゼ型の結晶相を主としつつもブルッカイト型の結晶相をも含む酸化チタニウム粒子であったが、酢酸7wt%(1M)を用いて作製した酸化チタニウム粒子は、アナターゼ型単一相の酸化チタニウム粒子であった。酢酸0.7wt%を用いて作製した酸化チタニウム粒子は、ギ酸0.5wt%を用いて作製した酸化チタニウム粒子と同様、市販の酸化チタニウム粒子(P25)よりわずかに高い光触媒活性を有しているに留まったが、酢酸7wt%を用いて作製した酸化チタニウム粒子は、市販の酸化チタニウム粒子(P25)に比べて非常に高い光触媒活性を有していることがわかった。これは、酢酸7wt%を用いて作製した酸化チタニウム粒子がアナターゼ型の結晶相のみから成ることに起因すると考えられる。
【0049】
酢酸を用いて作製した酸化チタニウム粒子(加熱工程前)では、図15に示すように、350℃近傍で大きな発熱ピークが認められた。このことから、酢酸は、酸化チタニウムの製造工程において250℃までの加熱で完全に除去されずに、粒子に残留していると考えられる。また、酢酸0.7wt%および酢酸7wt%を用いてそれぞれ作製した酸化チタニウム粒子の各収率は、61%および57%であった。これらの値は、前述のギ酸を用いたときの収率62%および65%に比べると若干低い。このことから、収率の観点では、ギ酸を用いた方が、若干、有利であると考えられる。
【0050】
3.3 実験例3(比較実験―塩酸、硝酸、硫酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
0.1M、1Mおよび2Mの3種類の塩酸水溶液、1Mの硝酸水溶液および1Mの硫酸水溶液をそれぞれ大気下にて用意して、それぞれから100mlを分取して合計5種類の無機酸水溶液(溶液B)を作製した。溶液Bの作製および加熱温度を250℃のみとしたこと以外の条件については、実験例1と同様の作製方法にて、酸化チタニウム粒子を作製した。
【0051】
(2)酸化チタニウム粒子の評価結果
図16に、実験例3にて作製した各酸化チタニウム粒子のX線回折チャートを比較して示す。図17に、実験例1の一部を含め、実験例3にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【0052】
1M以上の塩酸水溶液および1Mの硝酸水溶液をそれぞれ用いて作製した酸化チタニウム粒子は、アナターゼ型の結晶相以外にルチル(Rutile)型結晶相を含んでおり、0.1Mの塩酸水溶液を用いて作製した酸化チタニウム粒子はアナターゼ型の結晶相以外にブルッカイト型の結晶相を含んでいた。これに対して、1Mの硫酸水溶液を用いて作製した酸化チタニウム粒子はアナターゼ型の単一相からなっていた。しかし、図17に示すように、塩酸水溶液、硝酸水溶液、硫酸水溶液のいずれを用いて作製した酸化チタニウム粒子も、実験例1でギ酸5wt%(1M)を用いて作製した酸化チタニウム粒子および市販の酸化チタニウム粒子(P25)に比べて、光触媒活性が低いものであった。
【0053】
3.4 実験例4(チタニウムアルコキシドおよびアルコールの種類を変えた製法)
(1)酸化チタニウム粒子の作製方法
実験例1におけるTTIPに代えてTTBを、IPAに代えてn−BtOHを用いて、12.5mmolのTTBと、125mmolのn−BtOHを、相対湿度10%未満のグローブボックス内でそれぞれ分取して容器内に入れ、マグネチックスターラーを用いて1時間攪拌して、溶液Aを作製した。次に、実験例1と同様の手法によって10wt%のギ酸水溶液(溶液B)を作製した。その後の工程は、加熱温度を250℃として実験例1と同様の工程を行い、酸化チタニウム粒子を作製した。なお、ギ酸の有無による性能の違いを確認するため、実験例4の上記工程においてギ酸を加えずに酸化チタニウム粒子を作製した。
【0054】
(2)酸化チタニウム粒子の評価結果
図18に、実験例4にて作製した2種類の酸化チタニウム粒子と、実験例1にてギ酸無しおよびギ酸10wt%の条件で作製した2種類の酸化チタニウム粒子の合計4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。図19に、実験例1の一部を含め、実験例4にて作製した各酸化チタニウム粒子および比較に用いた市販の酸化チタニウム粒子(P25)のそれぞれの光触媒活性を比較して示す。
【0055】
図18に示すように、チタニウムアルコキシドとしてTTBを、アルコールとしてn−BtOHを用いても、アナターゼ型の単一相から成る酸化チタニウム粒子が得られることがわかった。また、図19に示すように、チタニウムアルコキシドをTTIPからTTBに、アルコールをIPAからn−BtOHにそれぞれ変えても、市販の酸化チタニウム粒子(P25)および酸を加えずに作製した酸化チタニウム粒子よりも高い光触媒活性を有していることが確認された。
【0056】
3.5 実験例5(ヒドロキシルアミンとギ酸を用いた製法)
(1)酸化チタニウム粒子の作製方法
可視光応答型光触媒用酸化チタニウム粒子を製造するため、実験例1における溶液Bの作製に際して、ギ酸を10wt%に固定し、含窒素化合物であるヒドロキシルアミンを1および10wt%の2水準選択し、ギ酸10wt%とヒドロキシルアミン1wt%を含む溶液と、ギ酸10wt%とヒドロキシルアミン10wt%を含む溶液の2種類の溶液Bを作製した。それ以外の工程については、実験例1と同一条件として、粉砕までの工程を実行した。その後の加熱工程は、実験例1の加熱条件中の雰囲気を、窒素雰囲気および空気雰囲気の2種類とした。この結果、ヒドロキシルアミンの添加量および加熱条件を変えた合計4種類の酸化チタニウム粒子を作製できた。また、比較のため、溶液Bの作製に際して、ギ酸を加えずにヒドロキシルアミン(濃度:1wt%)のみを水に混合する条件とし、かつ空気中で焼成して作製した酸化チタニウム粒子、およびギ酸10wt%のみを水に混合してヒドロキシルアミンを加えずに溶液Bを作製後、空気中で焼成して作製した酸化チタニウム粒子も用意した。
【0057】
(2)酸化チタニウム粒子の評価結果
表2に、実験例5にて作製した3種の溶液Bと、実験例1にて作製した一部の溶液B(4種)のpHを示す。図20に、実験例5にて作製した4種類の酸化チタニウム粒子のX線回折チャートを比較して示す。図21に、実験例5にて作製した4種類の酸化チタニウム粒子の一部(ギ酸10wt%+ヒドロキシルアミン10wt%の条件で作製したもの)の細孔径分布を示す。図22に、実験例5にて作製した4種類の酸化チタニウム粒子およびヒドロキシルアミン1wt%の条件下で溶液Bを用意して作製した酸化チタニウム粒子のそれぞれの光触媒活性を比較して示す。
【0058】
【表2】

【0059】
表2に示すように、実験例1で作製したギ酸5〜40wt%およびヒドロキシルアミン無添加の溶液Bでは、pHは、2.09〜1.09の範囲で変化することがわかった。一方、実験例5にて作製した3種類の溶液Bでは、pHは、2.83〜9.3の範囲で変化することがわかった。ヒドロキシルアミン1wt%のみを加えてギ酸を加えていない溶液Bを用いると、酸化チタニウム粒子の光触媒活性が低すぎるため、pH=9.3となるようにヒドロキシルアミンを加えても、光触媒活性の高い酸化チタニウム粒子は得られないと考えられる。ヒドロキシルアミン1wt%の条件でギ酸10wt%とすると、溶液BのpH=2.83となり、酸化チタニウム粒子の光触媒活性が高くなる。さらに、ギ酸およびヒドロキシルアミンを共に10wt%とすると、溶液BのpH=6.15となり、光触媒活性の高い酸化チタニウム粒子が得られる。また、実験例1で作製した酸化チタニウム粒子のように、ヒドロキシルアミンを加えずにギ酸のみを加えた場合には、溶液BのpH=1.09〜2.09の範囲となり、光触媒活性の高い酸化チタニウム粒子が得られる。この結果から、ヒドロキシルアミンとギ酸とを加えて溶液Bを用意する場合、pH=1〜9の範囲になるようにするのが好ましいことがわかる。また、図20に示すように、ギ酸とヒドロキシルアミンを用いて作製した酸化チタニウム粒子は、ギ酸のみを用いて作製したものと同様、アナターゼ型単一相から成る粒子であった。ギ酸10wt%およびヒドロキシルアミン10wt%を用いて作製した酸化チタニウム粒子の比表面積、平均細孔径および細孔容積は、それぞれ、284m2/g、49オングストロームおよび0.348cc/gであり、非常に粒子径の小さい粒子であることがわかった。なお、ヒドロキシルアミンのみを用い、酸を用いずに酸化チタニウム粒子を作製したが、その結晶性は低かった。ギ酸10wt%とヒドロキシルアミン10wt%の条件で作製した酸化チタニウム粒子は、ヒドロキシルアミンのみの条件で作製した酸化チタニウム粒子、およびギ酸10wt%とヒドロキシルアミン1wt%の条件で作製した酸化チタニウム粒子よりも、可視光照射下において高い光触媒活性を有していた。
【0060】
図23〜図25に、実験例5においてギ酸とヒドロキシルアミンの量を変えて作製した合計6種類の酸化チタニウム粒子(加熱工程前)の雰囲気を変えて加熱したときの熱分析結果を示す。
【0061】
実験例5にて作製したいずれの酸化チタニウム粒子でも、酸素の有無を問わず、250℃までに重量減少が認められることから、250℃にてギ酸およびヒドロキシルアミンを十分に脱離できることが確認された。
【0062】
図26〜図28に、実験例5においてヒドロキシルアミン1wt%、ヒドロキシルアミン1wt%とギ酸10wt%、およびヒドロキシルアミン10wt%とギ酸10wt%の3水準で溶液Bを用意して作製した加熱後(250℃、空気中)の3種類の酸化チタニウムのXPSチャート(N1s、Ti2pおよびO1sの3種類)を示す。
【0063】
ヒドロキシルアミン1wt%、ヒドロキシルアミン1wt%とギ酸10wt%、およびヒドロキシルアミン10wt%とギ酸10wt%の3条件で作製した酸化チタニウム粒子の各窒素ドープ量は、それぞれ、0.082、0.044および0.056であった。いずれの酸化チタニウム粒子にも窒素がドープされていることが確認された。
【産業上の利用可能性】
【0064】
本発明は、光触媒機能を発揮する成形体、塗膜などに利用可能である。
【特許請求の範囲】
【請求項1】
アナターゼ型単一相から成り、比表面積が170m2/g以上であることを特徴とする光触媒用酸化チタニウム粒子。
【請求項2】
窒素ドープされていることを特徴とする請求項1に記載の光触媒用酸化チタニウム粒子。
【請求項3】
アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子を製造する方法であって、
チタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、上記有機酸を上記有機酸と上記水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程と、
上記混合溶液を50〜100℃の範囲に保持して上記チタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程と、
上記加水分解・結晶化工程後の溶液から当該溶液に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程と、
上記固体生成物を200〜350℃の範囲で加熱する加熱工程と、
を含む光触媒用酸化チタニウム粒子の製造方法。
【請求項4】
前記チタニウムアルコキシドをチタニウムテトライソプロポキシドとし、
前記アルコールを2−プロパノールとすることを特徴とする請求項3に記載の光触媒用酸化チタニウム粒子の製造方法。
【請求項5】
前記混合溶液作製工程において、N−O結合若しくはN−N結合を有する含窒素化合物を前記有機酸と混合してpHが1.0〜9.0の範囲となる前記混合溶液を作製することを特徴とする請求項3または請求項4に記載の光触媒用酸化チタニウム粒子の製造方法。
【請求項6】
前記含窒素化合物をヒドロキシルアミンとすることを特徴とする請求項5に記載の光触媒用酸化チタニウム粒子の製造方法。
【請求項1】
アナターゼ型単一相から成り、比表面積が170m2/g以上であることを特徴とする光触媒用酸化チタニウム粒子。
【請求項2】
窒素ドープされていることを特徴とする請求項1に記載の光触媒用酸化チタニウム粒子。
【請求項3】
アナターゼ型単一相から成り、比表面積が170m2/g以上の光触媒用酸化チタニウム粒子を製造する方法であって、
チタニウムアルコキシドと、アルコールと、水と、ギ酸と酢酸から1以上選択される有機酸とを混合し、上記有機酸を上記有機酸と上記水の総量に対して5質量%以上含む混合溶液を作製する混合溶液作製工程と、
上記混合溶液を50〜100℃の範囲に保持して上記チタニウムアルコキシドの加水分解および酸化チタニウムの結晶化を行う加水分解・結晶化工程と、
上記加水分解・結晶化工程後の溶液から当該溶液に含まれる固体生成物を分離し、かつ洗浄する分離・洗浄工程と、
上記固体生成物を200〜350℃の範囲で加熱する加熱工程と、
を含む光触媒用酸化チタニウム粒子の製造方法。
【請求項4】
前記チタニウムアルコキシドをチタニウムテトライソプロポキシドとし、
前記アルコールを2−プロパノールとすることを特徴とする請求項3に記載の光触媒用酸化チタニウム粒子の製造方法。
【請求項5】
前記混合溶液作製工程において、N−O結合若しくはN−N結合を有する含窒素化合物を前記有機酸と混合してpHが1.0〜9.0の範囲となる前記混合溶液を作製することを特徴とする請求項3または請求項4に記載の光触媒用酸化チタニウム粒子の製造方法。
【請求項6】
前記含窒素化合物をヒドロキシルアミンとすることを特徴とする請求項5に記載の光触媒用酸化チタニウム粒子の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【公開番号】特開2013−95622(P2013−95622A)
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願番号】特願2011−237785(P2011−237785)
【出願日】平成23年10月28日(2011.10.28)
【出願人】(504180239)国立大学法人信州大学 (759)
【Fターム(参考)】
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願日】平成23年10月28日(2011.10.28)
【出願人】(504180239)国立大学法人信州大学 (759)
【Fターム(参考)】
[ Back to top ]

