内臓脂肪増加抑制効果の評価方法及び評価用キット、並びに、物質のスクリーニング方法
【課題】被験物質が有する内臓脂肪増加抑制効果を評価する方法等を提供する。
【解決手段】被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における11種のマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価する。マーカー物質に対する親和性を有する物質を固定化した担体にマーカー物質を捕捉して、体液中のマーカー物質の濃度を算出する構成が推奨される。該評価方法を用いる物質のスクリーニング方法、該評価方法を簡便に行うことができるキットも提供される。
【解決手段】被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における11種のマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価する。マーカー物質に対する親和性を有する物質を固定化した担体にマーカー物質を捕捉して、体液中のマーカー物質の濃度を算出する構成が推奨される。該評価方法を用いる物質のスクリーニング方法、該評価方法を簡便に行うことができるキットも提供される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、内臓脂肪増加抑制効果の評価方法及び評価用キット、並びに、物質のスクリーニング方法に関し、さらに詳細には、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果を評価する内臓脂肪増加抑制効果の評価方法、該評価方法を簡便に行うことができる内臓脂肪増加抑制効果の評価用キット、並びに、該評価方法を用いて所望も内臓脂肪増加抑制効果を有する物質をスクリーニングする物質のスクリーニング方法に関する。
【背景技術】
【0002】
近年、食生活の欧米化が進み、それに起因すると考えられる肥満、糖尿病、高脂血症、動脈硬化等の生活習慣病が増加している。これらの発症増加は遺伝的なものではなく、主に環境因子によるものである。例えば、高脂肪食や高カロリー食の摂取による脂質代謝異常が、血中脂質上昇、インスリン抵抗性の発症、脂肪細胞肥大化、インスリン分泌不全等の原因となっている。その結果、糖尿病、肥満、動脈硬化等が高確率で発症し、病態の進展へとつながっている。
【0003】
また、これらの生活習慣病には内臓脂肪型肥満が大きく関与していることが明らかになりつつあり、いわゆる「メタボリック症候群」(メタボリックシンドローム、内臓脂肪症候群)に注目が集まっている。メタボリック症候群は、内臓脂肪型肥満に加えて、高血糖、高血圧、脂質異常のうちいずれか2つ以上をあわせもった状態と定義されている。内臓脂肪型肥満をベースとした複合疾患ともいえるメタボリック症候群は、動脈硬化を進行させ、心臓病や脳卒中の危険性を急激に高めることとなる。したがって、メタボリック症候群を予防・改善することが、長寿命ならびに高い生活の質を維持するために重要である。
【0004】
メタボリック症候群を予防・改善するためには、生活習慣を改善することが効果的である。例えば、運動習慣や食生活を改善することが提唱されている。食生活に関しては、内臓脂肪の増加を抑制する効果がある食品を積極的に摂取することで、メタボリック症候群の発症を予防・改善できると考えられる。特許文献1,2には内臓脂肪を減少させる効果がある飲食品の開示がある。一方、内臓脂肪の増加抑制効果を有する物質のスクリーニング系については定かでないが、特許文献3には高コレステロールや高中性脂肪に関係するスクリーニング系についての開示がある。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2008−214253号公報
【特許文献2】特開2008−169147号公報
【特許文献3】特開2007−64747号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
上述のように、メタボリック症候群の予防・改善するための1つの方策として、内臓脂肪の増加抑制効果を有する物質を含有する食品を摂取することが挙げられる。そのためには、物質が有する内臓脂肪の増加抑制効果の評価系や、内臓脂肪の増加抑制効果を有する物質のスクリーニング系を構築することが有用である。例えば、内臓脂肪の状態を反映するバイオマーカー(マーカー物質)を特定できれば、該バイオマーカーを指標とした種々の評価系やスクリーニング系が構築できると考えられる。
【0007】
そこで本発明は、内臓脂肪に関連する新たなバイオマーカーを特定し、該バイオマーカーを用いて被験物質が有する内臓脂肪増加抑制果を評価する方法等を提供することを課題とする。
【課題を解決するための手段】
【0008】
上記した課題を解決するための請求項1に記載の発明は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法である。
(A01)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約4610のイオンピークを生じるタンパク質、
(A02)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約5500のイオンピークを生じるタンパク質、
(A03)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約7050のイオンピークを生じるタンパク質、
(A04)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8330のイオンピークを生じるタンパク質、
(A05)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8840のイオンピークを生じるタンパク質、
(A06)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8930のイオンピークを生じるタンパク質、
(A07)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約9070のイオンピークを生じるタンパク質、
(A08)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約11600のイオンピークを生じるタンパク質、
(A09)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13700のイオンピークを生じるタンパク質、
(A10)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13900のイオンピークを生じるタンパク質、
(A11)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約21400のイオンピークを生じるタンパク質。
【0009】
本発明の内臓脂肪増加抑制効果の評価方法は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における上記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価するものである。上記マーカー物質(A01)〜(A11)は、いずれも内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるタンパク質である。本発明の内臓脂肪増加抑制効果の評価方法によれば、被験物質が有する内臓脂肪増加抑制効果を容易かつ高精度に評価することができる。
【0010】
「内臓脂肪型肥満を発症し得る動物」とは、内臓脂肪型肥満を発症するように設計された動物であって、現時点ではまだ内臓脂肪型肥満をまだ発症していない動物を指す。そして、「内臓脂肪型肥満を発症している又は発症し得る動物」とは「内臓脂肪型肥満を発症している動物」又は「内臓脂肪型肥満を発症し得る動物」を指す。動物の種類としては、ラット等の飼育可能な動物のほか、ヒトも含まれるものとする。
【0011】
ここで、各マーカー物質における質量/電荷比(以下、「m/z」と略記することもある。)の「約4610」、「約8930」、「約21400」等の値は、質量分析における測定値の誤差範囲を考慮した値であり、概ね±0.2%の幅を有する。すなわち、約4610は概ね4610±0.2%、約8930は概ね8930±0.2%、約21400は概ね21400±0.2%を表す。他の質量/電荷比についても全く同様に、概ね±0.2%の幅を有する。また、これらのマーカー物質はいずれも主に血液中に存在するタンパク質である。被験物質が内臓脂肪増加抑制効果を有する場合、動物の体液中のマーカー物質(A01)、(A03)、(A04)、(A05)、(A06)、(A09)、(A10)、及び(A11)の濃度はより低値を示し、(A02)、(A07)、及び(A08)の濃度はより高値を示す。
【0012】
請求項2に記載の発明は、下記(a)〜(i)の少なくとも1つを満たすことを特徴とする請求項1に記載の内臓脂肪増加抑制効果の評価方法である。
(a)マーカー物質(A03)はアポリポタンパク質C1又はその修飾体である、
(b)マーカー物質(A04)はアポリポタンパク質C2又はその修飾体である、
(c)マーカー物質(A05)はアポリポタンパク質A2又はその修飾体である、
(d)マーカー物質(A06)はアポリポタンパク質C3又はその修飾体である、
(e)マーカー物質(A07)は補体C3又はその修飾体である、
(f)マーカー物質(A08)はβ2−ミクログロブリン又はその修飾体である、
(g)マーカー物質(A09)はトランスサイレチン又はその修飾体である、
(h)マーカー物質(A10)はトランスサイレチン又はその修飾体である、
(i)マーカー物質(A11)はアポリポタンパク質M又はその修飾体である。
【0013】
アポリポタンパク質C1、アポリポタンパク質C2、アポリポタンパク質A2、アポリポタンパク質C3、補体C3、β2−ミクログロブリン、トランスサイレチン、アポリポタンパク質Mはいずれも物理化学的性質がよく知られているので、本発明の内臓脂肪増加抑制効果の評価方法によれば、マーカー物質(A03)〜(A11)の解析が容易である。
【0014】
「タンパク質の修飾体」の代表例は、当該タンパク質を構成するアミノ酸残基の少なくとも1つが修飾されたタンパク質である。「修飾」には化合物や官能基の付加(例:リン酸化)のみならず、脱離(例:脱リン酸化)も含まれる。また「タンパク質又はその修飾体」には、当該タンパク質のアイソフォームが含まれる。さらに「タンパク質又はその修飾体」には、当該タンパク質の1次構造において数個のアミノ酸残基が欠失、置換若しくは付加されたような実質的に同一のタンパク質が含まれる。またさらに、「タンパク質又はその修飾体」には、プロテアーゼによる切断を受けた当該タンパク質由来のタンパク質断片が含まれる。なお、複合体タンパク質の場合には「タンパク質又はその修飾体」にはそのサブユニットも含まれるものとする。
【0015】
同様の課題を解決するための請求項3に記載の発明は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法である。
(B1)アポリポタンパク質C1又はその修飾体、
(B2)アポリポタンパク質C2又はその修飾体、
(B3)アポリポタンパク質A2又はその修飾体、
(B4)アポリポタンパク質C3又はその修飾体、
(B5)補体C3又はその修飾体、
(B6)β2−ミクログロブリン又はその修飾体、
(B7)トランスサイレチン又はその修飾体、
(B8)アポリポタンパク質M又はその修飾体。
【0016】
本発明の内臓脂肪増加抑制効果の評価方法は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における上記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価するものである。上記(B1)〜(B8)に属するマーカー物質は、いずれも内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるタンパク質である。本発明の内臓脂肪増加抑制効果の評価方法によれば、被験物質が有する内臓脂肪増加抑制効果を容易かつ高精度に評価することができる。特に、アポリポタンパク質C1、アポリポタンパク質C2、アポリポタンパク質A2、アポリポタンパク質C3、補体C3、β2−ミクログロブリン、トランスサイレチン、アポリポタンパク質Mはいずれも物理化学的性質がよく知られているので、解析が容易である。
【0017】
本発明においても「内臓脂肪型肥満を発症し得る動物」とは、内臓脂肪型肥満を発症するように設計された動物であって、現時点ではまだ内臓脂肪型肥満をまだ発症していない動物を指す。そして、「内臓脂肪型肥満を発症している又は発症し得る動物」とは「内臓脂肪型肥満を発症している動物」又は「内臓脂肪型肥満を発症し得る動物」を指す。動物の種類としては、ラット等の飼育可能な動物のほか、ヒトも含まれるものとする。
【0018】
また、本発明においても「タンパク質の修飾体」の代表例は、当該タンパク質を構成するアミノ酸残基の少なくとも1つが修飾されたタンパク質であり、「修飾」には化合物や官能基の付加のみならず、脱離も含まれる。また「タンパク質又はその修飾体」には、当該タンパク質のアイソフォーム、当該タンパク質の1次構造において数個のアミノ酸残基が欠失、置換若しくは付加されたような実質的に同一のタンパク質、並びに、プロテアーゼによる切断を受けた当該タンパク質由来のタンパク質断片が含まれる。さらに、複合体タンパク質の場合には「タンパク質又はその修飾体」にはそのサブユニットも含まれるものとする。
【0019】
請求項4に記載の発明は、前記動物は、被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物であることを特徴とする請求項1〜3のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0020】
本発明では、「被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物」として「被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物」を採用する。すなわち本発明では、低繊維高脂肪食を摂取させることで「内臓脂肪型肥満を発症している又は発症し得る動物」を設定し、当該動物に被験物質を摂取させる。本発明では、例えば食餌に被験物質や低繊維高脂肪食を含有させて動物を飼育すればよいので、内臓脂肪増加抑制効果の評価がより容易に行える。
【0021】
請求項5に記載の発明は、前記体液は、血液であることを特徴とする請求項1〜4のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0022】
かかる構成により、測定試料となる体液を簡単に採取でき、より簡便かつ迅速に、被験物質が有する内臓脂肪増加抑制効果を評価することができる。
【0023】
請求項6に記載の発明は、前記被験物質は、食品素材であることを特徴とする請求項1〜5のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0024】
かかる構成により、機能性食品の開発を目的として、被験物質が有する内臓脂肪増加抑制効果を評価することができる。
【0025】
請求項7に記載の発明は、前記体液又は体液成分を、前記マーカー物質に対する親和性を有する物質を固定化した担体に接触させて、体液中の前記マーカー物質を担体上に捕捉し、捕捉された前記マーカー物質の量に基づいて体液中の前記マーカー物質の濃度を算出することを特徴とする請求項1〜6のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0026】
本発明の内臓脂肪増加抑制効果の評価方法においては、マーカー物質に対する親和性を有する物質を固定化した担体を使用する。そして、該担体に体液又は体液成分を接触させて、体液又は体液成分に含まれるマーカー物質を、マーカー物質に対する親和性を有する物質を介して担体上に捕捉し、捕捉されたマーカー物質の量に基づいて体液中のマーカー物質の濃度を算出する。本発明の内臓脂肪増加抑制効果の評価方法によれば、担体上に捕捉されたマーカー物質を測定対象とするので、測定試料中に含まれる夾雑物質の影響を低減させることができ、より高感度かつ高精度でマーカー物質の濃度を測定することができる。なお、体液成分の例としては、体液が血液である場合の血清又は血漿が挙げられる。
【0027】
請求項8に記載の発明は、前記担体は平面部分を有し、前記マーカー物質に対する親和性を有する物質は、該平面部分の一部に固定化されていることを特徴とする請求項7に記載の内臓脂肪増加抑制効果の評価方法である。
【0028】
本発明の内臓脂肪増加抑制効果の評価方法では、平面部分を有する担体を用い、マーカー物質に対する親和性を有する物質は該平面部分の一部に固定化されている。かかる構成により、マーカー物質に対する親和性を有する物質を、担体上の複数箇所にスポット的に固定化することができる。その結果、1個の担体で複数の測定試料を同時処理することや、1個の担体で複数のマーカー物質の濃度を同時測定することが可能となり、作業効率がよい。さらに、各スポットの面積を小さくすることにより、微量の測定試料からでもマーカー物質の濃度を測定することができる。なお、平面部分を有する担体の例としては、チップ等の基板が挙げられる。
【0029】
請求項9に記載の発明は、前記マーカー物質に対する親和性を有する物質は、イオン交換体又は抗体であることを特徴とする請求項7又は8に記載の内臓脂肪増加抑制効果の評価方法である。
【0030】
本発明の内臓脂肪増加抑制効果の評価方法においては、マーカー物質に対する親和性を有する物質としてイオン交換体又は抗体を用い、イオン交換体又は抗体を介して測定試料中のマーカー物質を担体上に捕捉する。当該物質がイオン交換体の場合は各種のものが入手容易であり、マーカー物質を捕捉するための担体を容易に調製することができる。また、当該物質が抗体の場合は、より特異的にマーカー物質を捕捉することができる。捕捉されたマーカー物質の量を測定する方法としては、質量分析、イムノアッセイ(抗体の場合)が挙げられる。
【0031】
請求項10に記載の発明は、請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法によって被験物質を評価し、所望の内臓脂肪増加抑制効果を有する物質をスクリーニングすることを特徴とする物質のスクリーニング方法である。
【0032】
本発明は物質のスクリーニング方法にかかり、動物の体液中における上記(A01)〜(A11)の各マーカー物質および上記(B1)〜(B8)に属する各マーカー物質の少なくとも1つの濃度を基準値と比較し、所望の内臓脂肪増加抑制効果の評価を有する物質をスクリーニングするものである。上記(A01)〜(A11)の各マーカー物質および上記(B1)〜(B8)に属する各マーカー物質は、いずれも内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるタンパク質である。本発明の物質のスクリーニング方法によれば、内臓脂肪増加抑制効果の評価を有する物質を、容易かつ高精度にスクリーニングすることができる。特に、被験物質が食品素材の場合は、内臓脂肪増加抑制効果を有する機能性食品の開発に有用な食品素材をスクリーニングすることができる。
【0033】
請求項11に記載の発明は、請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法に用いるためのキットであって、前記マーカー物質に対する親和性を有する物質を固定化した担体を含むことを特徴とする内臓脂肪増加抑制効果の評価用キットである。
【0034】
本発明の内臓脂肪増加抑制効果の評価用キットは、マーカー物質に対する親和性を有する物質を固定化した担体を含む。かかる構成により、マーカー物質の濃度測定に際して当該担体を別途用意する必要がなく、きわめて簡便にマーカー物質の濃度を測定することができる。
【0035】
請求項12に記載の発明は、前記マーカー物質に対する親和性を有する物質は、イオン交換体であることを特徴とする請求項11に記載の内臓脂肪増加抑制効果の評価用キットである。
【0036】
かかる構成により、マーカー物質をより確実に担体上に捕捉することができる。
【0037】
所望の内臓脂肪増加抑制効果を有する物質をスクリーニングするために使用される構成が推奨される(請求項13)。
【発明の効果】
【0038】
本発明の内臓脂肪増加抑制効果の評価方法によれば、被験物質が有する内臓脂肪増加抑制効果の評価を、容易かつ高精度に評価することができる。
【0039】
本発明の物質のスクリーニング方法によれば、内臓脂肪増加抑制効果の評価を有する物質を、容易かつ高精度にスクリーニングすることができる。
【0040】
本発明の内臓脂肪増加抑制効果の評価用キットによれば、マーカー物質の濃度測定に際して当該担体を別途用意する必要がなく、きわめて簡便にマーカー物質の濃度を測定することができる。
【図面の簡単な説明】
【0041】
【図1】各群間で体重を比較したグラフである。
【図2】各群間で内臓脂肪の量を比較したグラフである。
【図3】各群間で皮下脂肪の量を比較したグラフである。
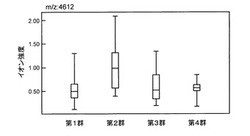
【図4】質量/電荷比が4612(平均値)のイオンピークについての箱髭図である。
【図5】質量/電荷比が5501(平均値)のイオンピークについての箱髭図である。
【図6】質量/電荷比が7054(平均値)のイオンピークについての箱髭図である。
【図7】質量/電荷比が8332(平均値)のイオンピークについての箱髭図である。
【図8】質量/電荷比が8836(平均値)のイオンピークについての箱髭図である。
【図9】質量/電荷比が8931(平均値)のイオンピークについての箱髭図である。
【図10】質量/電荷比が9065(平均値)のイオンピークについての箱髭図である。
【図11】質量/電荷比が11643(平均値)のイオンピークについての箱髭図である。
【図12】質量/電荷比が13733(平均値)のイオンピークについての箱髭図である。
【図13】質量/電荷比が13922(平均値)のイオンピークについての箱髭図である。
【図14】質量/電荷比が21383(平均値)のイオンピークについての箱髭図である。
【図15】実施例2で行ったSDS−PAGEの結果を示す写真である。
【図16】実施例2で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図17】実施例3で行ったSDS−PAGEの結果を示す写真である。
【図18】実施例3で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図19】実施例4で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図20】実施例5で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図21】実施例6で行ったSDS−PAGEの結果を示す写真である。
【図22】実施例6で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図23】実施例7で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図24】実施例8で行ったSDS−PAGEの結果を示す写真である。
【図25】実施例8で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図26】実施例9で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【発明を実施するための形態】
【0042】
以下、本発明を実施するための形態について詳細に説明する。
【0043】
本発明の内臓脂肪増加抑制効果の評価方法は2つの様相を含む。1つの様相では、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価する。
(A01)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約4610のイオンピークを生じるタンパク質、
(A02)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約5500のイオンピークを生じるタンパク質、
(A03)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約7050のイオンピークを生じるタンパク質、
(A04)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8330のイオンピークを生じるタンパク質、
(A05)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8840のイオンピークを生じるタンパク質、
(A06)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8930のイオンピークを生じるタンパク質、
(A07)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約9070のイオンピークを生じるタンパク質、
(A08)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約11600のイオンピークを生じるタンパク質、
(A09)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13700のイオンピークを生じるタンパク質、
(A10)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13900のイオンピークを生じるタンパク質、
(A11)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約21400のイオンピークを生じるタンパク質。
【0044】
これらのマーカー物質はいずれも主に血液中に存在するタンパク質であり、内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるものである。なお、(A01)、(A03)、(A04)、(A05)、(A06)、(A09)、(A10)、及び(A11)の各マーカー物質(以下、これらのマーカー物質からなるグループを「グループ1」と称することがある。)は、内臓脂肪が増加した状態でより高値を示すものであるので、被験物質が内臓脂肪増加抑制効果を有する場合には、当該被験物質を投与した動物においてより低値を示す。一方、(A02)、(A07)、及び(A08)の各マーカー物質(以下、これらのマーカー物質からなるグループを「グループ2」と称することがある。)は、内臓脂肪が増加した状態でより低値を示すものであるので、被験物質が内臓脂肪増加抑制効果を有する場合には、当該被験物質を投与した動物においてより高値を示す。
【0045】
ある条件のペプチドマッピングによれば、マーカー物質(A03)はアポリポタンパク質C1、マーカー物質(A04)はアポリポタンパク質C2、マーカー物質(A05)はアポリポタンパク質A2、マーカー物質(A06)はアポリポタンパク質C3、マーカー物質(A07)は補体C3a(des−Arg)、マーカー物質(A08)はβ2−ミクログロブリン、マーカー物質(A09)はトランスサイレチン、マーカー物質(A10)はトランスサイレチン、マーカー物質(A11)はアポリポタンパク質M、と同定される。すなわち、ある実施形態では、下記(a)〜(i)の少なくとも1つを満たす。
(a)マーカー物質(A03)はアポリポタンパク質C1又はその修飾体である、
(b)マーカー物質(A04)はアポリポタンパク質C2又はその修飾体である、
(c)マーカー物質(A05)はアポリポタンパク質A2又はその修飾体である、
(d)マーカー物質(A06)はアポリポタンパク質C3又はその修飾体である、
(e)マーカー物質(A07)は補体C3又はその修飾体である、
(f)マーカー物質(A08)はβ2−ミクログロブリン又はその修飾体である、
(g)マーカー物質(A09)はトランスサイレチン又はその修飾体である、
(h)マーカー物質(A10)はトランスサイレチン又はその修飾体である、
(i)マーカー物質(A11)はアポリポタンパク質M又はその修飾体である。
【0046】
本発明の内臓脂肪増加抑制効果の評価方法の他の様相では、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価する。
(B1)アポリポタンパク質C1又はその修飾体、
(B2)アポリポタンパク質C2又はその修飾体、
(B3)アポリポタンパク質A2又はその修飾体、
(B4)アポリポタンパク質C3又はその修飾体、
(B5)補体C3又はその修飾体、
(B6)β2−ミクログロブリン又はその修飾体、
(B7)トランスサイレチン又はその修飾体、
(B8)アポリポタンパク質M又はその修飾体。
【0047】
タンパク質の修飾の例としては、N末端αアミノ基やリジンεアミノ基のメチル化、アセチル化、アデニリル化、ミリスチル化等;セリン・スレオニン・アスパラギンへの糖又は糖鎖の付加;セリン・スレオニン・チロシン・アルギニン・ヒスチジンのリン酸化;システインのシステイニル化、ホモシステイニル化、スルホニル化等;グルタミン酸のγ−カルボキシル化;N末端グルタミン酸のピログルタミン酸への変換、等が挙げられる。また、これらの修飾の脱離(脱メチル化、糖又は糖鎖の脱離、脱リン酸化等)も「修飾」に含まれる。
【0048】
「タンパク質又はその修飾体」には、当該タンパク質のアイソフォームが含まれる。アイソフォームとしては、前記した各種の修飾の他、選択的スプライシングによって生じたタンパク質が挙げられる。さらに、「タンパク質又はその修飾体」には、当該タンパク質の1次構造において数個のアミノ酸残基が欠失、置換若しくは付加されたような実質的に同一のタンパク質が含まれる。またさらに、「タンパク質又はその修飾体」には、プロテアーゼによる切断を受けた当該タンパク質由来のタンパク質断片が含まれる。例えば、当該タンパク質由来と認められうる長さのタンパク質断片、例えば20個以上のアミノ酸残基からなるタンパク質断片、分子量が2千以上のタンパク質断片、等が挙げられる。また、複合体タンパク質の場合には「タンパク質又はその修飾体」にはそのサブユニットも含まれるものとする。
【0049】
例えば、アポリポタンパク質C1(配列番号1)のN末端側2アミノ酸残基(Ala−Pro)が欠損したタンパク質断片(配列番号2)は「アポリポタンパク質C1の修飾体」に含まれる。
【0050】
例えば、補体C3のタンパク質断片である補体C3a des Arg(配列番号6)は「補体C3又はその修飾体」に含まれる。
【0051】
トランスサイレチン(配列番号8)については、その唯一のCys残基が修飾を受けた種々の修飾トランスサイレチンが見出されている(Amareth Lim et al., J. Biol. Chem., vol. 258, No. 50, 2003)。例えば、トランスサイレチンのCys残基にシステインが付加した「システイニル化トランスサイレチン」や、グルタチオンが付加した「グルタチオン化トランスサイレチン」は、「トランスサイレチンの修飾体」に含まれる。さらに、トランスサイレチンは4個のサブユニットからなる複合体タンパク質であるので、当該サブユニットは「トランスサイレチン又はその修飾体」に含まれる。
【0052】
本発明の内臓脂肪増加抑制効果の評価方法では、(A01)〜(A11)の各マーカー物質ならびに(B1)〜(B8)に属する各マーカー物質の1つだけを用いてもよいし、複数を組み合わせて用いてもよい。複数を用いる場合の組み合わせ方については特に限定はないが、例えば、グループ1から選択したマーカー物質(1つ又は複数)とグループ2から選択したマーカー物質(1つ又は複数)とを組み合わせることができる。
【0053】
本発明の内臓脂肪増加抑制効果の評価方法では「被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物」を用いる。好ましい実施形態では、当該動物として「被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物」を用いる。例えば、動物に被験物質と低繊維高脂肪食とを同時摂取させた動物を用いればよい。低繊維高脂肪食は、例えば、低繊維飼料に数%〜数十%の動物性脂肪を混合することにより調製することができる。他の実施形態としては、内臓脂肪型肥満を発症する自然発症モデル動物や遺伝子操作モデル動物を用いることも考えられる。例えば、当該自然発症モデル動物や遺伝子操作モデル動物に被験物質を投与し、体液中における各マーカー物質の濃度を指標とすればよい。
【0054】
「内臓脂肪型肥満を発症している又は発症し得る動物」における動物の種類には特に限定はなく、例えば、マウス、ラット、ウサギ、ブタ等を採用することができる。さらに、動物としてヒトを採用することもできる。この場合には、臨床試験の結果によって物質を評価することになる。
【0055】
本発明の内臓脂肪増加抑制効果の評価方法では、動物の体液中におけるマーカー物質の濃度を基準値と比較する。当該基準値としては特に限定はなく、目的に応じて適宜設定すればよい。例えば、「被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物」を採用する場合には、低繊維高脂肪食のみを摂取させた動物の体液中における前記マーカー物質の濃度を用いることができる。低繊維高脂肪食のみを摂取させた動物は、内臓脂肪型肥満を発症している又は発症し得る動物のモデルとなり、その体液中のマーカー物質濃度は「異常値」となる。そして、被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物(例えば同時摂取)における値(測定値)と当該基準値(異常値)とを比較し、測定値が基準値と有意に差がありかつ正常側である場合(正常側に維持された場合)に、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。具体的には、グループ1に属するマーカー物質を指標とする場合は、測定値が当該基準値に比べて有意に低いときに、グループ2に属するマーカー物質を指標とする場合は、測定値が基準値に比べて有意に高いときに、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。
【0056】
さらに、基準値は複数あってもよい。例えば、上記の異常値に加え、通常食を摂取させた動物における値(正常値。陰性対照。)を基準値に加えることができる。具体的には、
(1)通常食を摂取(正常値)、
(2)低繊維高脂肪食を摂取(異常値)、
(3)被験物質と低繊維高脂肪食とを同時摂取、
の3群を設定し、動物を飼育する。そして、各動物の体液中の上記マーカー物質を測定し、各測定値を比較する。このとき、(1)と(2)とで有意差があり、(3)と(2)とで有意差があり、かつ(3)が(2)に比べて正常側((1)に近い側)である場合(正常側に維持された場合)に、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。
【0057】
さらに、基準値として、内臓脂肪増加抑制効果を有する既知物質と低繊維高脂肪食とを同時摂取させた動物における値(陽性対照)を加えることもできる。具体的には、上記(1)〜(3)に加えて、
(4)上記既知物質と低繊維高脂肪食とを同時摂取させる群、
を設定し、動物を飼育する。このとき、(1)と(2)とで有意差があり、(3)と(2)とで有意差があり、かつ(3)が(2)に比べて正常側((1)及び(4)に近い側)である場合に、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。すなわち、このような被験物質は、(4)で採用した上記既知物質と同様の挙動を示し、同様の作用を有する物質といえる。
【0058】
内臓脂肪型肥満を発症する自然発症モデル動物や遺伝子操作モデル動物を用いる場合には、上記(2)の代わりに「内臓脂肪増加抑制効果を有さない既知物質を摂取させる群」、上記(3)の代わりに「被験物質を摂取させる群」を設定すればよい。
【0059】
本発明の内臓脂肪増加抑制効果の評価方法において使用する動物の体液としては、血液が好ましく用いられる。特に、血液から調製した血清又は血漿(体液成分)を測定試料とすることが好ましい。血清又は血漿は遠心分離等の公知の方法で血液から調製することができる。
【0060】
本発明の内臓脂肪増加抑制効果の評価方法における被験物質としては、食品素材、医薬原体などが挙げられる。特に、食品素材を評価対象とする場合は、機能性食品の開発に役立てることができる。
【0061】
本発明の内臓脂肪増加抑制効果の評価方法において、マーカー物質の濃度を測定する方法は、そのマーカー物質の濃度を特異的に測定できる方法であれば、タンパク質の定量に一般に用いられている方法をそのまま用いることができる。例えば、各種のイムノアッセイ、質量分析(MS)、クロマトグラフィー、電気泳動等を用いることができる。
【0062】
イムノアッセイによれば、夾雑物質の多い試料のままでも正確にマーカー物質の濃度を測定することができる。イムノアッセイの例としては、抗原抗体結合物を直接的又は間接的に測定する沈降反応、凝集反応、溶血反応などの古典的な方法や、標識法と組み合わせて検出感度を高めたエンザイムイムノアッセイ(EIA)、ラジオイムノアッセイ(RIA)、蛍光イムノアッセイ(FIA)等の方法が挙げられる。なお、これらのイムノアッセイに用いるマーカー物質に特異的な抗体は、モノクローナルでもよいし、ポリクローナルでもよい。
【0063】
質量分析によれば、各マーカー物質由来のイオンピークを特定し、そのイオンピーク強度をもって各マーカー物質の量(濃度)を測定することができる。質量分析によってマーカー物質の濃度を測定する場合のイオン化の方法としては、マトリクス支援レーザーイオン化(matrix-assisted laser desorption/ionization、MALDI)、エレクトロスプレーイオン化(electrospray ionization、ESI)のいずれも適用可能であるが、多価イオンの生成が少ないMALDIが好ましい。特に、飛行時間質量分析計(time-of-flight mass spectrometer、TOF)と組み合わせたMALDI−TOF−MSによれば、より正確にマーカー物質由来のイオンピークを特定することができる。
【0064】
電気泳動によりマーカー物質の濃度を測定する場合は、例えば、検査材料をSDS−ポリアクリルアミドゲル電気泳動(SDS−PAGE)に供して目的のマーカー物質を分離し、適宜の色素や蛍光物質でゲルを染色し、目的のマーカー物質に相当するバンドの濃さや蛍光強度を測定すればよい。SDS−PAGEだけではマーカー物質の分離が不十分な場合は、等電点電気泳動(IEF)と組み合わせた2次元電気泳動を用いることもできる。さらに、ゲルから直接検出するのではなく、ウエスタンブロッティングを行って膜上のマーカー物質の量を測定することもできる。
【0065】
クロマトグラフィーによってマーカー物質の濃度を測定する場合は、例えば、液体高速クロマトグラフィー(HPLC)による方法を用いることができる。すなわち、試料をHPLCに供して目的のマーカー物質を分離し、そのクロマトグラムのピーク面積を測定することにより試料中のマーカー物質の濃度を測定することができる。
【0066】
好ましい実施形態では、マーカー物質を担体上に捕捉し、その捕捉されたマーカー物質を測定対象とする。すなわち、マーカー物質に対する親和性を有する物質を担体に固定化し、その親和性を有する物質を介してマーカー物質を担体上に捕捉する。そして、捕捉された前記マーカー物質の量に基づいて体液中の前記マーカー物質の濃度を算出する。本実施形態によれば、試料中に含まれる夾雑物質の影響を低減させることができ、より高感度かつ高精度でマーカー物質の濃度を測定することができる。本実施形態において用いることができる担体の例としては、ビーズ、金属、ガラス、樹脂等のような一般的なものの他、基板のような、平面部分を有する担体を用いることができる。基板を用いる場合は、その平面部分の一部にマーカー物質に対する親和性を有する物質を固定化することが好ましい。例としては、基板としてチップを用い、その表面の複数箇所にスポット的にマーカー物質に親和性を有する物質を固定化した担体が挙げられる。なお「親和性」の例としては、イオン結合、金属キレート体とタンパク質中のヒスチジン残基等とのアフィニティ、抗原と抗体、酵素と基質、若しくはホルモンとレセプターのようなバイオアフィニティ、及び、疎水性相互作用のような化学的な相互作用、が挙げられる。
【0067】
イオン結合によってマーカー物質を担体に捕捉する場合は、イオン交換体を担体に固定化する。この場合、イオン交換体には陽イオン交換体、陰イオン交換体のいずれも用いることができ、さらに、強陽イオン交換体、弱陽イオン交換体、強陰イオン交換体、弱陰イオン交換体のいずれも用いることができるが、強陰イオン交換体と弱陽イオン交換体が好ましく用いられる。強陰イオン交換体の例としては、4級アンモニウム(トリメチルアミノメチル)(QA)、4級アミノエチル(ジエチル,モノ・2−ヒドロキシブチルアミノエチル)(QAE)、4級アンモニウム(トリメチルアンモニウム)(QMA)等の強陰イオン交換基を有するものが挙げられる。また、弱陽イオン交換体の例としては、カルボキシメチル(CM)等の弱陽イオン交換基を有するものが挙げられる。また、強陽イオン交換体の例としては、スルホプロピル(SP)等の強陽イオン交換基を有するものが挙げられる。さらに、弱陰イオン交換体の例としては、ジメチルアミノエチル(DE)、ジエチルアミノエチル(DEAE)等の弱陰イオン交換基を有するものが挙げられる。
【0068】
金属キレート体を介してマーカー物質を捕捉する場合は、例えば、Cu2+、Zn2+、Ni2+、Co2+、Al3+、Fe3+、Ga3+等の金属キレート体を固定化した担体を用いることができる。
【0069】
抗体によってマーカー物質を担体に捕捉する場合は、マーカー物質に特異的な抗体を担体に固定化すればよい。
【0070】
疎水性相互作用によってマーカー物質を担体に捕捉する場合は、担体に疎水基をもつ物質を固定化する。疎水基の例としては、C4〜C20のアルキル基、フェニル基等が挙げられる。
【0071】
本実施形態においてマーカー物質の測定方法にイムノアッセイを用いる場合は、抗体を固定化した担体を用いることが好ましい。このようにすれば、担体に固定化された抗体を1次抗体としたイムノアッセイの系を簡単に構築することができる。例えば、マーカー物質に特異的でエピトープの異なる2種類の抗体を用意し、一方を1次抗体として担体に固定化し、他方を2次抗体として酵素標識し、サンドイッチEIAの系を構築することができる。その他、結合阻止法や競合法によるイムノアッセイの系も構築可能である。さらに、担体として基板を用いる場合は、抗体チップによるイムノアッセイが可能である。抗体チップによれば、複数のマーカー物質の濃度を同時に測定でき、迅速な測定が可能である。
【0072】
一方、本実施形態において質量分析を用いる場合は、例えば、抗体の他、イオン交換体、金属キレート体又は疎水基を固定化した担体を用いることができる。なお、これらの物質による結合は抗原と抗体等のバイオアフィニティほどの特異性がないので、これらの物質を固定化した担体を用いる場合はマーカー物質以外の物質も担体上に捕捉されうるが、質量分析によれば分子量を反映した質量分析計スペクトルによって定量するので、問題はない。特に、担体として基板を用い、表面エンハンス型レーザー脱離イオン化(surface-enhanced laser desorption/ionization)−飛行時間質量分析(time-of-flight mass spectrometry)(以下、「SELDI−TOF−MS」と称する)を行うことにより、マーカー物質の濃度をより正確に測定することができる。使用できる基板の種類としては、陽イオン交換基板、陰イオン交換基板、順相基板、逆相基板、金属イオン基板、抗体基板等を用いることができるが、陽イオン交換基板、特に弱陽イオン交換基板と、陰イオン交換基板、特に強陰イオン交換基板が好ましく用いられる。
【0073】
本発明の物質のスクリーニング方法は、本発明の内臓脂肪増加抑制効果の評価方法によって被験物質を評価し、所望の内臓脂肪増加抑制効果を有する物質をスクリーニングするものである。本発明の物質のスクリーニング方法においても、上記した本発明の内臓脂肪増加抑制効果の評価方法の実施形態と全く同様の実施形態をとることができる。
【0074】
本発明の内臓脂肪増加抑制効果の評価方法を簡便に行なうために、必要な試薬類をまとめて評価用キットを構築することができる。当該評価用キットとしては、例えば、マーカー物質に対する親和性を有する物質を固定化した担体を含むものが挙げられる。特に、担体として、CM等の弱陽イオン交換体、あるいはQAやQAE等の強陰イオン交換体を固定化した基板を含めた評価用キットによれば、SELDI−TOF−MS等を簡便に行なうことができる。本キット中には他の試薬類、例えば、標準物質、前処理用の各種緩衝液等を含めてもよい。なお本キットは、内臓脂肪増加抑制効果を有する物質をスクリーニングするためのキットとしても使用できる。本発明のキットの構成例を以下に挙げる。
【0075】
〔キットの構成例〕
(1)弱陽イオン交換基板:1枚
(2)強陰イオン交換基板:1枚
(3)基板洗浄用バッファーA(pH3.0):適量
(4)基板洗浄用バッファーB(pH9.0):適量
(5)各マーカー物質の標準品:各適量
【0076】
以下に、実施例をもって本発明をさらに具体的に説明するが、本発明はこれらの実施例に限定されるものではない。
【実施例1】
【0077】
4週齢のSDラットを1群当たり6〜8匹用意した。第1群のラットには、通常食としてCE−2(日本クレア社)を摂取させた。第2群のラットには、低繊維高脂肪食(低繊維飼料に30%牛脂混餌)を摂取させた。第3群には、前記低繊維高脂肪食と内臓脂肪増加抑制効果を有する既知素材との混合飼料を摂取させた。第4群には、通常飼料と内臓脂肪増加抑制効果を有する既知素材との混合飼料を摂取させた。各飼料は自由摂取とし、3週間(21日)飼育した。飼育終了後、各ラットの体重、体重当たりの内臓脂肪の量(腸間膜、腎、精巣周囲)、体重当たりの皮下脂肪の量(肩甲骨、腰下肢周囲)を測定し、4群比較した。さらに、各ラットから全血を採取して血漿を調製した。
【0078】
図1に体重の測定結果、図2に内臓脂肪の測定結果、図3に皮下脂肪の測定結果を示す。図1〜3において、記号*は第1群に対する有意差、記号#は第2群に対する有意差を示し、「*」「#」は5%有意、「**」「##」は1%有意、「***」「###」は0.1%有意を意味する。まず図1に示すように、第1群と第4群(通常飼料群)に対して、第2群と第3群の方が有意に体重が多かった。また、第3群と第4群との間では有意差はなかった。すなわち、上記既知飼料による体重への影響は見られなかった。また図2に示すように、第1群と第4群(通常飼料群)に対して、第2群と第3群の方が有意に内臓脂肪の量が多かった。さらに、第2群に対して第3群の方が有意に内臓脂肪の量が少なかった。これにより、上記既知飼料による内臓脂肪抑制効果が裏付けられた。なお図3に示すように、皮下脂肪についても内臓脂肪と同様の傾向を示した。以上より、本動物実験の妥当性が裏付けられた。なお、本実験では3週間(21日)という短期間で飼育を終了しており、飼育終了時における第2群のラットは発症初期の内臓脂肪型肥満の状態であったと考えられる。
【0079】
2.プロテインチップによる解析とイオンピークの選抜
各血漿試料20μLに、変性バッファー(9M 尿素、2% CHAPS、50mM Tris−HCl(pH9.0))30μLを加えて前処理を行い、タンパク質を変性させた。次に、前処理した各体液試料を強陰イオン交換樹脂カラム(Q−Sepharose、GEヘルスケア社)にアプライした。次いで、pH9.0の緩衝液(50mM Tris−HCl(pH9.0)、0.1%(w/v)1−o−N−オクチル−β−D−グルコピラノシド(以下、「OGP」と称する。))、pH5.0の緩衝液(100mM 酢酸ナトリウム(pH5.0)、0.1%(w/v)OGP)、pH3.0の緩衝液(50mM クエン酸ナトリウム(pH3.0)、0.1%(w/v)OGP)、及び有機溶媒(0.1%トリフルオロ酢酸、50.0%アセトニトリルからなる混合液)各200μLで順に溶出させ、画分1(pH9.0で溶出、素通り)、画分2(pH5.0で溶出)、画分3(pH3.0で溶出)、画分4(有機溶媒で溶出)の4つの粗分画画分を得た。
【0080】
得られた各画分10μLをpH3.0のプロテインチップ結合バッファー(50mM クエン酸ナトリウム)で10倍希釈した後、弱陽イオン交換チップCM10(バイオラッド社)に添加した。同様に、得られた各画分10μLをpH9.0のプロテインチップ結合バッファー(50mM Tris−HCl(pH9.0))で10倍希釈した後、強陰イオン交換チップQ10(バイオラッド社)に添加した。各チップを各結合バッファーで3回洗浄した後に脱イオン水で1回洗浄し、乾燥させた。次に、エネルギー吸収分子であるシナピン酸(SPA−H、SPA−L)又はα−シアノ−4−ヒドロキシケイ皮酸(CHCA)を添加し、プロテインチップリーダーModel PBS IIc(バイオラッド社)を用いて、SELDI−TOF−MSを行なった。なお、測定分子量範囲(m/z)は、3000〜200000の範囲で行なった。また、測定は2連で行い、m/zの平均値を算出した。データ解析は、Protein Chip Software、CiphergenExpress Data Manager、及びBiomarker Patterns Software(いずれもバイオラッド社)を用いて行なった。具体的には、ベースライン補正、分子量校正、スペクトルの正規化処理を行なった後、シングルマーカー解析及び数本のマーカーを組み合わせたマルチフロー解析を行なった。その結果、粗分画画分の種類、プロテインチップの種類、チップの洗浄条件等の組み合わせによって多数のピークが検出された。各ピークについて、p値(Mann−Whitney検定法)、ROC面積、及びイオンピーク強度を算出し、さらに、以下の(1)〜(4)の条件を指標として11個の候補ピークを選抜した。
【0081】
(1)候補ピーク探索(基本)
第1群と第2群との間でイオン強度に有意差がある(p<0.05)。
(2)上記既知物質の効果検証
第2群と第3群との間でイオン強度に有意差があり(p<0.05またはp<0.1)、かつ第3群の値の方が第2群の値よりも第1群の値に近い(第3群の値が第1群側に復帰している)。
(3)増減パターン解析
第2群のみが高値または低値を示し、第1群、第3群および第4群の間ではあまり差がない。なお、第3群と第4群との間に差があっても、第4群の値の方が第3群の値よりも第2群から離れている場合には本条件を満たすものとして取り扱う。
【0082】
3.マーカー物質(A01)の特定
画分4(有機溶媒)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:CHCA)を行なった場合に、質量/電荷比が4612(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図4に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。図中、髭の上端と下端はそれぞれ最大値と最小値、箱の上辺と下辺はそれぞれ第3四分位(75パーセンタイル)と第1四分位(25パーセンタイル)、箱の中の線は中央値である(図5以降も同じ)。その結果、本ピークのROC面積(第1群vs第2群)は0.750、p値(第1群vs第2群)は0.018、p値(第2群vs第3群)は0.014であった。
【0083】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約4610のピークを生じるタンパク質(マーカー物質(A01))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A01)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約4610のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0084】
4.マーカー物質(A02)の特定
画分1(pH9.0)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が5501(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で高値を示し、第2群で低値を示した。図5に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.833、p値(第1群vs第2群)は0.002、p値(第2群vs第3群)は0.004であった。
【0085】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約5500のピークを生じるタンパク質(マーカー物質(A02))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A02)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約5500のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0086】
5.マーカー物質(A03)の特定
画分3(pH3.0)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−L)を行なった場合に、質量/電荷比が7055(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図6に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.750、p値(第1群vs第2群)は0.029、p値(第2群vs第3群)は0.018であった。
【0087】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約7050のピークを生じるタンパク質(マーカー物質(A03))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A03)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約7050のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0088】
6.マーカー物質(A04)の特定
画分4(有機溶媒)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が8333(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図7に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.984、p値(第1群vs第2群)は0.00002、p値(第2群vs第3群)は0.060であった。
【0089】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約8330のピークを生じるタンパク質(マーカー物質(A04))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A04)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約8330のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0090】
7.マーカー物質(A05)の特定
画分1(pH9.0)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−L)を行なった場合に、質量/電荷比が8337(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図8に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.802、p値(第1群vs第2群)は0.004、p値(第2群vs第3群)は0.090であった。
【0091】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約8340のピークを生じるタンパク質(マーカー物質(A05))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A05)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約8340のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0092】
8.マーカー物質(A06)の特定
画分4(有機溶媒)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が8931(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図9に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.984、p値(第1群vs第2群)は0.00001、p値(第2群vs第3群)は0.001であった。
【0093】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約8930のピークを生じるタンパク質(マーカー物質(A06))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A06)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約8930のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0094】
9.マーカー物質(A07)の特定
画分1(pH9.0)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:CHCA)を行なった場合に、質量/電荷比が9065(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で高値を示し、第2群で低値を示した。図10に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.714、p値(第1群vs第2群)は0.046、p値(第2群vs第3群)は0.018であった。
【0095】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約9070のピークを生じるタンパク質(マーカー物質(A07))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A07)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約9070のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0096】
10.マーカー物質(A08)の特定
画分1(pH9.0)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が11643(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で高値を示し、第2群で低値を示した。図11に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.729、p値(第1群vs第2群)は0.033、p値(第2群vs第3群)は0.090であった。
【0097】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約11600のピークを生じるタンパク質(マーカー物質(A08))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A08)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約11600のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0098】
11.マーカー物質(A09)の特定
画分4(有機溶媒)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−L)を行なった場合に、質量/電荷比が13733(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図12に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.703、p値(第1群vs第2群)は0.046、p値(第2群vs第3群)は0.055であった。
【0099】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約13700のピークを生じるタンパク質(マーカー物質(A09))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A09)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約13700のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0100】
12.マーカー物質(A10)の特定
画分2(pH5.0)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が13922(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図13に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.755、p値(第1群vs第2群)は0.020、p値(第2群vs第3群)は0.042であった。
【0101】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約13900のピークを生じるタンパク質(マーカー物質(A10))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A10)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約13900のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0102】
13.マーカー物質(A11)の特定
画分4(有機溶媒)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が21384(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図14に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.750、p値(第1群vs第2群)は0.011、p値(第2群vs第3群)は0.083であった。
【0103】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約21400のピークを生じるタンパク質(マーカー物質(A11))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A11)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約21400のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0104】
なお、ヒトの体液中にもマーカー物質(A01)〜(A11)と同等のタンパク質が存在する場合には、ヒトの体液中における当該タンパク質の濃度を指標として、内臓脂肪型肥満を診断できる可能性も示唆された。
【実施例2】
【0105】
マーカー物質(A03)の精製と同定
強陰イオン交換樹脂Q-Sepharose HP(GEヘルスケア社)を充填したカラム(5mL)を平衡化バッファー(50mM Tris−HCl pH9.0,1M 尿素,0.22% CHAPS)にて平衡化した。ラット標準血清(ケミコン社)1.5mLに対して変性バッファー(50mM Tris−HCl pH9.0,9M 尿素,2% CHAPS)を450μL加えて変性処理した後、平衡化した前記カラムに添加した。非吸着画分を回収した。回収した画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A03)の質量/電荷比(平均値:7054)と同等の質量/電荷比を示すピークを確認した。
【0106】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図15)。図15中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約7.0kDaのバンド(図15の矢印a)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A03)と同等の質量/電荷比を示すピークを確認した(図16の矢印)。
【0107】
あらためて同様のSDS−PAGEを行って約7.0kDaのバンドを切り出し、還元アルキル化処理した後、0.01μg/μLのトリプシン溶液(50mM 炭酸水素アンモニウム(pH8.0)に溶解)を作用させてゲル内で消化した。消化したサンプル1μLを金属プレート上に滴下し、飽和CHCA溶液0.4μLをさらに滴下して乾燥させた後、質量分析計Proteomics Analyzer 4700(アプライドバイオシステムズ社)で測定したところ、少なくとも5個のピークが検出され、それらの精密質量は「1293.66」、「1052.49」、「1279.62」、「781.45」、及び「1138.54」と算出された。これらのデータを元にMascotデータベース(マトリックスサイエンス社)によって既知タンパク質を検索し、ペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号10〜14で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質C1」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第1表に示す。既報のラットアポリポタンパク質C1(成熟型)のアミノ酸配列を配列番号1に示す。
【0108】
【表1】

【0109】
ここで、ヒト、マウス等において、アポリポタンパク質C1のN末端側2アミノ酸残基が欠損したものが見出されている。全長のラットアポリポタンパク質C1(配列番号1)の質量が7187Daであり、一方、N末端側2アミノ酸残基(Ala−Pro)が欠損したラットアポリポタンパク質C1の断片(配列番号2)の質量が7019Daであることから、マーカー物質(A03)はアポリポタンパク質C1の断片(配列番号2)と最終的に同定された。
【実施例3】
【0110】
マーカー物質(A04)の精製と同定
強陰イオン交換樹脂HiTrap Q HP (5mL)(GEヘルスケア社)を50mM 酢酸ナトリウムバッファー(pH6.0)にて平衡化した。ラット標準血清(ケミコン社)1mLを50mM 酢酸ナトリウムバッファー(pH6.0)で10倍に希釈した後、Millex0.45μLでろ過し、平衡化した前記カラムに添加した。5カラム体積(CV)の50mM 酢酸ナトリウムバッファー(pH6.0)、12CVの50mM 酢酸ナトリウムバッファー(pH6.0)/200mM NaCl、及び5CVの50mM 酢酸ナトリウムバッファー(pH6.0)でカラムを順次洗浄した後、50mM 酢酸ナトリウムバッファー(pH3.0)で溶出し、280nmの吸光度の高い画分を回収した(約1mL)。回収した画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A04)の質量/電荷比(平均値:8333)と同等の質量/電荷比を示すピークを確認した。
【0111】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図17)。図17中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約8.3kDaのバンド(図17の矢印a)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A04)の質量/電荷比(平均値:8333)と同等の質量/電荷比を示すピークを確認した(図18の矢印)。
【0112】
あらためて同様のSDS−PAGEを行って約8.3kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも7個のピークが検出され、それらの精密質量は「950.49」、「1055.54」、「1324.74」、「1964.98」、「928.46」、「2261.18」、及び「2447.26」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号15〜21で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質C2」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第2表に示す。既報のラットアポリポタンパク質C2のアミノ酸配列を配列番号3に示す。
【0113】
【表2】

【実施例4】
【0114】
マーカー物質(A05)の精製と同定
実施例2で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A05)の質量/電荷比(平均値:8837)と同等の質量/電荷比を示すピークを確認した。
【0115】
実施例2で行ったSDS−PAGEで分離された約8.8kDaのバンド(図15の矢印b)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A05)と同等の質量/電荷比を示すピークを確認した(図19)。
【0116】
あらためて同様のSDS−PAGEを行って約8.8kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも3個のピークが検出され、それらの精密質量は「1126.54」、「860.50」、及び「1270.63」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号22〜24で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質A2」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第3表に示す。既報のラットアポリポタンパク質A2のアミノ酸配列を配列番号4に示す。
【0117】
【表3】

【実施例5】
【0118】
マーカー物質(A06)の精製と同定
実施例3で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A06)の質量/電荷比(平均値:8931)と同等の質量/電荷比を示すピークを確認した。
【0119】
実施例3で行ったSDS−PAGEで分離された約8.9kDaのバンド(図17の矢印b)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A06)と同等の質量/電荷比を示すピークを確認した(図20)。
【0120】
あらためて同様のSDS−PAGEを行って約8.9kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも2個のピークが検出され、それらの精密質量は「2262.00」及び「968.53」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号25,26で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質C3」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第4表に示す。既報のラットアポリポタンパク質C3のアミノ酸配列を配列番号5に示す。
【0121】
【表4】

【実施例6】
【0122】
マーカー物質(A07)の精製と同定
強陰イオン交換樹脂Q-Sepharose HP(GEヘルスケア社)を充填したカラム(1mL)を平衡化バッファー(50mM Tris−HCl pH9.0,1M 尿素,0.22% CHAPS)にて平衡化した。ラット標準血清(ケミコン社)500μLに対して変性バッファー(50mM Tris−HCl pH9.0,9M 尿素,2% CHAPS)を750μL加えて4℃で20分間変性処理した。変性処理したサンプルを12,000G、4℃で10分間遠心し、0.45μmのフィルターでろ過した後、平衡化した前記カラムに添加し、非吸着画分を回収した。回収した画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A07)の質量/電荷比(平均値:9065)と同等の質量/電荷比を示すピークを確認した。
【0123】
弱陽イオン交換樹脂HiTrap CM FF 1mL(GEヘルスケア社)を50mM HEPES−NaOH(pH7.0)にて平衡化した。上記の回収画分3mLと100mM酢酸ナトリウムバッファー(pH5.0)2.3mLを混合し、0.45μLのフィルターでろ過した後、平衡化した前記カラムに添加した。50mM HEPES−NaOH(pH7.0)でカラムを洗浄した後、5CVの50mM HEPES−NaOH(pH7.0)/50mM NaCl、5CVの50mM HEPES−NaOH(pH7.0)/100mM NaCl、及び5CVの50mM HEPES−NaOH(pH7.0)/150mM NaClで順次洗浄し、5CVの50mM HEPES−NaOH(pH7.0)/1M NaClで溶出した。溶出画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A07)の質量/電荷比(平均値:9065)と同等の質量/電荷比を示すピークを確認した。
【0124】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図21)。図21中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約9.1kDaのバンド(図21の矢印)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A07)の質量/電荷比(平均値:9065)と同等の質量/電荷比を示すピークを確認した(図22の矢印)。
【0125】
あらためて同様のSDS−PAGEを行って約9.1kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも3個のピークが検出され、それらの精密質量は「1148.43」、「1438.38」、及び「838.34」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号27〜29で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「補体C3a(des−Arg)」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第5表に示す。既報のラット補体C3a(des−Arg)のアミノ酸配列を配列番号6に示す。
【0126】
【表5】

【実施例7】
【0127】
マーカー物質(A08)の精製と同定
実施例2で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A08)の質量/電荷比(平均値:11642)と同等の質量/電荷比を示すピークを確認した。
【0128】
実施例2で行ったSDS−PAGEで分離された約11.6kDaのバンド(図15の矢印c)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A08)と同等の質量/電荷比を示すピークを確認した(図23)。
【0129】
あらためて同様のSDS−PAGEを行って約11.6kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも5個のピークが検出され、それらの精密質量は「1091.59」、「3445.48」、「1496.73」、「2822.17」、及び「777.39」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号30〜34で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「β2−マクログロブリン」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第6表に示す。既報のラットβ2−マクログロブリンのアミノ酸配列を配列番号7に示す。
【0130】
【表6】

【実施例8】
【0131】
マーカー物質(A08)と(A09)の精製と同定
強陰イオン交換樹脂Q-Sepharose HP(GEヘルスケア社)を充填したカラム(5mL)を平衡化バッファー(50mM Tris−HCl pH9.0,1M 尿素,0.22% CHAPS)にて平衡化した。ラット標準血清(ケミコン社)1.5mLに対して変性バッファー(50mM Tris−HCl pH9.0,9M 尿素,2% CHAPS)を450μL加えて変性処理した後、平衡化した前記カラムに添加した。5CVの50mM Tris−HCl(pH9.0)、5CVの50mM 酢酸ナトリウムバッファー(pH5.0)、及び5CVの50mM クエン酸ナトリウムバッファー(pH3.0)で順次洗浄した後、33.3%イソプロパノール/16.7%アセトニトリル/0.1%トリフルオロ酢酸で溶出し、溶出画分を回収した。
【0132】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図24)。図24中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約13.7kDa付近のバンド(図24の矢印a)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A08)と(A09)の質量/電荷比(平均値:13733,13922)と同等の質量/電荷比を含むピークを確認した(図25の矢印)。
【0133】
あらためて同様のSDS−PAGEを行って約13.7kDa付近のバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも7個のピークが検出され、それらの精密質量は「1352.41」、「1587.52」、「2439.83」、「3125.12」、「871.30」、「2516.88」、及び「2596.96」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号35〜41で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「トランスサイレチン」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第7表に示す。既報のラットトランスサイレチンのアミノ酸配列を配列番号8に示す。
【0134】
【表7】

【0135】
上述したように、トランスサイレチンについては、その唯一のCys残基が修飾を受けた種々の修飾トランスサイレチンが見出されている。マーカー物質(A08)、(A09)の各電荷/質量比(平均値:13733,13922)から、マーカー物質(A08)は「システイニル化トランスサイレチン」、マーカー物質(A09)は「グルタチオン化トランスサイレチン」とそれぞれ同定された。
【実施例9】
【0136】
マーカー物質(A11)の精製と同定
実施例8で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A11)の質量/電荷比(平均値:21383)と同等の質量/電荷比を示すピークを確認した。
【0137】
実施例8で行ったSDS−PAGEで分離された約21.4kDaのバンド(図24の矢印b)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A11)と同等の質量/電荷比を示すピークを確認した(図26)。
【0138】
あらためて同様のSDS−PAGEを行って約21.4kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも6個のピークが検出され、それらの精密質量は「1262.49」、「1654.61」、「938.30」、「825.35」、「2635.86」、及び「803.37」、と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号42〜47で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質M」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第8表に示す。既報のラットアポリポタンパク質Mのアミノ酸配列を配列番号9に示す。
【0139】
【表8】

【技術分野】
【0001】
本発明は、内臓脂肪増加抑制効果の評価方法及び評価用キット、並びに、物質のスクリーニング方法に関し、さらに詳細には、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果を評価する内臓脂肪増加抑制効果の評価方法、該評価方法を簡便に行うことができる内臓脂肪増加抑制効果の評価用キット、並びに、該評価方法を用いて所望も内臓脂肪増加抑制効果を有する物質をスクリーニングする物質のスクリーニング方法に関する。
【背景技術】
【0002】
近年、食生活の欧米化が進み、それに起因すると考えられる肥満、糖尿病、高脂血症、動脈硬化等の生活習慣病が増加している。これらの発症増加は遺伝的なものではなく、主に環境因子によるものである。例えば、高脂肪食や高カロリー食の摂取による脂質代謝異常が、血中脂質上昇、インスリン抵抗性の発症、脂肪細胞肥大化、インスリン分泌不全等の原因となっている。その結果、糖尿病、肥満、動脈硬化等が高確率で発症し、病態の進展へとつながっている。
【0003】
また、これらの生活習慣病には内臓脂肪型肥満が大きく関与していることが明らかになりつつあり、いわゆる「メタボリック症候群」(メタボリックシンドローム、内臓脂肪症候群)に注目が集まっている。メタボリック症候群は、内臓脂肪型肥満に加えて、高血糖、高血圧、脂質異常のうちいずれか2つ以上をあわせもった状態と定義されている。内臓脂肪型肥満をベースとした複合疾患ともいえるメタボリック症候群は、動脈硬化を進行させ、心臓病や脳卒中の危険性を急激に高めることとなる。したがって、メタボリック症候群を予防・改善することが、長寿命ならびに高い生活の質を維持するために重要である。
【0004】
メタボリック症候群を予防・改善するためには、生活習慣を改善することが効果的である。例えば、運動習慣や食生活を改善することが提唱されている。食生活に関しては、内臓脂肪の増加を抑制する効果がある食品を積極的に摂取することで、メタボリック症候群の発症を予防・改善できると考えられる。特許文献1,2には内臓脂肪を減少させる効果がある飲食品の開示がある。一方、内臓脂肪の増加抑制効果を有する物質のスクリーニング系については定かでないが、特許文献3には高コレステロールや高中性脂肪に関係するスクリーニング系についての開示がある。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2008−214253号公報
【特許文献2】特開2008−169147号公報
【特許文献3】特開2007−64747号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
上述のように、メタボリック症候群の予防・改善するための1つの方策として、内臓脂肪の増加抑制効果を有する物質を含有する食品を摂取することが挙げられる。そのためには、物質が有する内臓脂肪の増加抑制効果の評価系や、内臓脂肪の増加抑制効果を有する物質のスクリーニング系を構築することが有用である。例えば、内臓脂肪の状態を反映するバイオマーカー(マーカー物質)を特定できれば、該バイオマーカーを指標とした種々の評価系やスクリーニング系が構築できると考えられる。
【0007】
そこで本発明は、内臓脂肪に関連する新たなバイオマーカーを特定し、該バイオマーカーを用いて被験物質が有する内臓脂肪増加抑制果を評価する方法等を提供することを課題とする。
【課題を解決するための手段】
【0008】
上記した課題を解決するための請求項1に記載の発明は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法である。
(A01)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約4610のイオンピークを生じるタンパク質、
(A02)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約5500のイオンピークを生じるタンパク質、
(A03)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約7050のイオンピークを生じるタンパク質、
(A04)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8330のイオンピークを生じるタンパク質、
(A05)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8840のイオンピークを生じるタンパク質、
(A06)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8930のイオンピークを生じるタンパク質、
(A07)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約9070のイオンピークを生じるタンパク質、
(A08)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約11600のイオンピークを生じるタンパク質、
(A09)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13700のイオンピークを生じるタンパク質、
(A10)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13900のイオンピークを生じるタンパク質、
(A11)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約21400のイオンピークを生じるタンパク質。
【0009】
本発明の内臓脂肪増加抑制効果の評価方法は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における上記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価するものである。上記マーカー物質(A01)〜(A11)は、いずれも内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるタンパク質である。本発明の内臓脂肪増加抑制効果の評価方法によれば、被験物質が有する内臓脂肪増加抑制効果を容易かつ高精度に評価することができる。
【0010】
「内臓脂肪型肥満を発症し得る動物」とは、内臓脂肪型肥満を発症するように設計された動物であって、現時点ではまだ内臓脂肪型肥満をまだ発症していない動物を指す。そして、「内臓脂肪型肥満を発症している又は発症し得る動物」とは「内臓脂肪型肥満を発症している動物」又は「内臓脂肪型肥満を発症し得る動物」を指す。動物の種類としては、ラット等の飼育可能な動物のほか、ヒトも含まれるものとする。
【0011】
ここで、各マーカー物質における質量/電荷比(以下、「m/z」と略記することもある。)の「約4610」、「約8930」、「約21400」等の値は、質量分析における測定値の誤差範囲を考慮した値であり、概ね±0.2%の幅を有する。すなわち、約4610は概ね4610±0.2%、約8930は概ね8930±0.2%、約21400は概ね21400±0.2%を表す。他の質量/電荷比についても全く同様に、概ね±0.2%の幅を有する。また、これらのマーカー物質はいずれも主に血液中に存在するタンパク質である。被験物質が内臓脂肪増加抑制効果を有する場合、動物の体液中のマーカー物質(A01)、(A03)、(A04)、(A05)、(A06)、(A09)、(A10)、及び(A11)の濃度はより低値を示し、(A02)、(A07)、及び(A08)の濃度はより高値を示す。
【0012】
請求項2に記載の発明は、下記(a)〜(i)の少なくとも1つを満たすことを特徴とする請求項1に記載の内臓脂肪増加抑制効果の評価方法である。
(a)マーカー物質(A03)はアポリポタンパク質C1又はその修飾体である、
(b)マーカー物質(A04)はアポリポタンパク質C2又はその修飾体である、
(c)マーカー物質(A05)はアポリポタンパク質A2又はその修飾体である、
(d)マーカー物質(A06)はアポリポタンパク質C3又はその修飾体である、
(e)マーカー物質(A07)は補体C3又はその修飾体である、
(f)マーカー物質(A08)はβ2−ミクログロブリン又はその修飾体である、
(g)マーカー物質(A09)はトランスサイレチン又はその修飾体である、
(h)マーカー物質(A10)はトランスサイレチン又はその修飾体である、
(i)マーカー物質(A11)はアポリポタンパク質M又はその修飾体である。
【0013】
アポリポタンパク質C1、アポリポタンパク質C2、アポリポタンパク質A2、アポリポタンパク質C3、補体C3、β2−ミクログロブリン、トランスサイレチン、アポリポタンパク質Mはいずれも物理化学的性質がよく知られているので、本発明の内臓脂肪増加抑制効果の評価方法によれば、マーカー物質(A03)〜(A11)の解析が容易である。
【0014】
「タンパク質の修飾体」の代表例は、当該タンパク質を構成するアミノ酸残基の少なくとも1つが修飾されたタンパク質である。「修飾」には化合物や官能基の付加(例:リン酸化)のみならず、脱離(例:脱リン酸化)も含まれる。また「タンパク質又はその修飾体」には、当該タンパク質のアイソフォームが含まれる。さらに「タンパク質又はその修飾体」には、当該タンパク質の1次構造において数個のアミノ酸残基が欠失、置換若しくは付加されたような実質的に同一のタンパク質が含まれる。またさらに、「タンパク質又はその修飾体」には、プロテアーゼによる切断を受けた当該タンパク質由来のタンパク質断片が含まれる。なお、複合体タンパク質の場合には「タンパク質又はその修飾体」にはそのサブユニットも含まれるものとする。
【0015】
同様の課題を解決するための請求項3に記載の発明は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法である。
(B1)アポリポタンパク質C1又はその修飾体、
(B2)アポリポタンパク質C2又はその修飾体、
(B3)アポリポタンパク質A2又はその修飾体、
(B4)アポリポタンパク質C3又はその修飾体、
(B5)補体C3又はその修飾体、
(B6)β2−ミクログロブリン又はその修飾体、
(B7)トランスサイレチン又はその修飾体、
(B8)アポリポタンパク質M又はその修飾体。
【0016】
本発明の内臓脂肪増加抑制効果の評価方法は、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における上記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価するものである。上記(B1)〜(B8)に属するマーカー物質は、いずれも内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるタンパク質である。本発明の内臓脂肪増加抑制効果の評価方法によれば、被験物質が有する内臓脂肪増加抑制効果を容易かつ高精度に評価することができる。特に、アポリポタンパク質C1、アポリポタンパク質C2、アポリポタンパク質A2、アポリポタンパク質C3、補体C3、β2−ミクログロブリン、トランスサイレチン、アポリポタンパク質Mはいずれも物理化学的性質がよく知られているので、解析が容易である。
【0017】
本発明においても「内臓脂肪型肥満を発症し得る動物」とは、内臓脂肪型肥満を発症するように設計された動物であって、現時点ではまだ内臓脂肪型肥満をまだ発症していない動物を指す。そして、「内臓脂肪型肥満を発症している又は発症し得る動物」とは「内臓脂肪型肥満を発症している動物」又は「内臓脂肪型肥満を発症し得る動物」を指す。動物の種類としては、ラット等の飼育可能な動物のほか、ヒトも含まれるものとする。
【0018】
また、本発明においても「タンパク質の修飾体」の代表例は、当該タンパク質を構成するアミノ酸残基の少なくとも1つが修飾されたタンパク質であり、「修飾」には化合物や官能基の付加のみならず、脱離も含まれる。また「タンパク質又はその修飾体」には、当該タンパク質のアイソフォーム、当該タンパク質の1次構造において数個のアミノ酸残基が欠失、置換若しくは付加されたような実質的に同一のタンパク質、並びに、プロテアーゼによる切断を受けた当該タンパク質由来のタンパク質断片が含まれる。さらに、複合体タンパク質の場合には「タンパク質又はその修飾体」にはそのサブユニットも含まれるものとする。
【0019】
請求項4に記載の発明は、前記動物は、被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物であることを特徴とする請求項1〜3のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0020】
本発明では、「被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物」として「被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物」を採用する。すなわち本発明では、低繊維高脂肪食を摂取させることで「内臓脂肪型肥満を発症している又は発症し得る動物」を設定し、当該動物に被験物質を摂取させる。本発明では、例えば食餌に被験物質や低繊維高脂肪食を含有させて動物を飼育すればよいので、内臓脂肪増加抑制効果の評価がより容易に行える。
【0021】
請求項5に記載の発明は、前記体液は、血液であることを特徴とする請求項1〜4のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0022】
かかる構成により、測定試料となる体液を簡単に採取でき、より簡便かつ迅速に、被験物質が有する内臓脂肪増加抑制効果を評価することができる。
【0023】
請求項6に記載の発明は、前記被験物質は、食品素材であることを特徴とする請求項1〜5のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0024】
かかる構成により、機能性食品の開発を目的として、被験物質が有する内臓脂肪増加抑制効果を評価することができる。
【0025】
請求項7に記載の発明は、前記体液又は体液成分を、前記マーカー物質に対する親和性を有する物質を固定化した担体に接触させて、体液中の前記マーカー物質を担体上に捕捉し、捕捉された前記マーカー物質の量に基づいて体液中の前記マーカー物質の濃度を算出することを特徴とする請求項1〜6のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法である。
【0026】
本発明の内臓脂肪増加抑制効果の評価方法においては、マーカー物質に対する親和性を有する物質を固定化した担体を使用する。そして、該担体に体液又は体液成分を接触させて、体液又は体液成分に含まれるマーカー物質を、マーカー物質に対する親和性を有する物質を介して担体上に捕捉し、捕捉されたマーカー物質の量に基づいて体液中のマーカー物質の濃度を算出する。本発明の内臓脂肪増加抑制効果の評価方法によれば、担体上に捕捉されたマーカー物質を測定対象とするので、測定試料中に含まれる夾雑物質の影響を低減させることができ、より高感度かつ高精度でマーカー物質の濃度を測定することができる。なお、体液成分の例としては、体液が血液である場合の血清又は血漿が挙げられる。
【0027】
請求項8に記載の発明は、前記担体は平面部分を有し、前記マーカー物質に対する親和性を有する物質は、該平面部分の一部に固定化されていることを特徴とする請求項7に記載の内臓脂肪増加抑制効果の評価方法である。
【0028】
本発明の内臓脂肪増加抑制効果の評価方法では、平面部分を有する担体を用い、マーカー物質に対する親和性を有する物質は該平面部分の一部に固定化されている。かかる構成により、マーカー物質に対する親和性を有する物質を、担体上の複数箇所にスポット的に固定化することができる。その結果、1個の担体で複数の測定試料を同時処理することや、1個の担体で複数のマーカー物質の濃度を同時測定することが可能となり、作業効率がよい。さらに、各スポットの面積を小さくすることにより、微量の測定試料からでもマーカー物質の濃度を測定することができる。なお、平面部分を有する担体の例としては、チップ等の基板が挙げられる。
【0029】
請求項9に記載の発明は、前記マーカー物質に対する親和性を有する物質は、イオン交換体又は抗体であることを特徴とする請求項7又は8に記載の内臓脂肪増加抑制効果の評価方法である。
【0030】
本発明の内臓脂肪増加抑制効果の評価方法においては、マーカー物質に対する親和性を有する物質としてイオン交換体又は抗体を用い、イオン交換体又は抗体を介して測定試料中のマーカー物質を担体上に捕捉する。当該物質がイオン交換体の場合は各種のものが入手容易であり、マーカー物質を捕捉するための担体を容易に調製することができる。また、当該物質が抗体の場合は、より特異的にマーカー物質を捕捉することができる。捕捉されたマーカー物質の量を測定する方法としては、質量分析、イムノアッセイ(抗体の場合)が挙げられる。
【0031】
請求項10に記載の発明は、請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法によって被験物質を評価し、所望の内臓脂肪増加抑制効果を有する物質をスクリーニングすることを特徴とする物質のスクリーニング方法である。
【0032】
本発明は物質のスクリーニング方法にかかり、動物の体液中における上記(A01)〜(A11)の各マーカー物質および上記(B1)〜(B8)に属する各マーカー物質の少なくとも1つの濃度を基準値と比較し、所望の内臓脂肪増加抑制効果の評価を有する物質をスクリーニングするものである。上記(A01)〜(A11)の各マーカー物質および上記(B1)〜(B8)に属する各マーカー物質は、いずれも内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるタンパク質である。本発明の物質のスクリーニング方法によれば、内臓脂肪増加抑制効果の評価を有する物質を、容易かつ高精度にスクリーニングすることができる。特に、被験物質が食品素材の場合は、内臓脂肪増加抑制効果を有する機能性食品の開発に有用な食品素材をスクリーニングすることができる。
【0033】
請求項11に記載の発明は、請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法に用いるためのキットであって、前記マーカー物質に対する親和性を有する物質を固定化した担体を含むことを特徴とする内臓脂肪増加抑制効果の評価用キットである。
【0034】
本発明の内臓脂肪増加抑制効果の評価用キットは、マーカー物質に対する親和性を有する物質を固定化した担体を含む。かかる構成により、マーカー物質の濃度測定に際して当該担体を別途用意する必要がなく、きわめて簡便にマーカー物質の濃度を測定することができる。
【0035】
請求項12に記載の発明は、前記マーカー物質に対する親和性を有する物質は、イオン交換体であることを特徴とする請求項11に記載の内臓脂肪増加抑制効果の評価用キットである。
【0036】
かかる構成により、マーカー物質をより確実に担体上に捕捉することができる。
【0037】
所望の内臓脂肪増加抑制効果を有する物質をスクリーニングするために使用される構成が推奨される(請求項13)。
【発明の効果】
【0038】
本発明の内臓脂肪増加抑制効果の評価方法によれば、被験物質が有する内臓脂肪増加抑制効果の評価を、容易かつ高精度に評価することができる。
【0039】
本発明の物質のスクリーニング方法によれば、内臓脂肪増加抑制効果の評価を有する物質を、容易かつ高精度にスクリーニングすることができる。
【0040】
本発明の内臓脂肪増加抑制効果の評価用キットによれば、マーカー物質の濃度測定に際して当該担体を別途用意する必要がなく、きわめて簡便にマーカー物質の濃度を測定することができる。
【図面の簡単な説明】
【0041】
【図1】各群間で体重を比較したグラフである。
【図2】各群間で内臓脂肪の量を比較したグラフである。
【図3】各群間で皮下脂肪の量を比較したグラフである。
【図4】質量/電荷比が4612(平均値)のイオンピークについての箱髭図である。
【図5】質量/電荷比が5501(平均値)のイオンピークについての箱髭図である。
【図6】質量/電荷比が7054(平均値)のイオンピークについての箱髭図である。
【図7】質量/電荷比が8332(平均値)のイオンピークについての箱髭図である。
【図8】質量/電荷比が8836(平均値)のイオンピークについての箱髭図である。
【図9】質量/電荷比が8931(平均値)のイオンピークについての箱髭図である。
【図10】質量/電荷比が9065(平均値)のイオンピークについての箱髭図である。
【図11】質量/電荷比が11643(平均値)のイオンピークについての箱髭図である。
【図12】質量/電荷比が13733(平均値)のイオンピークについての箱髭図である。
【図13】質量/電荷比が13922(平均値)のイオンピークについての箱髭図である。
【図14】質量/電荷比が21383(平均値)のイオンピークについての箱髭図である。
【図15】実施例2で行ったSDS−PAGEの結果を示す写真である。
【図16】実施例2で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図17】実施例3で行ったSDS−PAGEの結果を示す写真である。
【図18】実施例3で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図19】実施例4で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図20】実施例5で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図21】実施例6で行ったSDS−PAGEの結果を示す写真である。
【図22】実施例6で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図23】実施例7で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図24】実施例8で行ったSDS−PAGEの結果を示す写真である。
【図25】実施例8で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【図26】実施例9で行ったSELDI−TOF−MS分析の結果を示すイオンピーク図である。
【発明を実施するための形態】
【0042】
以下、本発明を実施するための形態について詳細に説明する。
【0043】
本発明の内臓脂肪増加抑制効果の評価方法は2つの様相を含む。1つの様相では、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価する。
(A01)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約4610のイオンピークを生じるタンパク質、
(A02)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約5500のイオンピークを生じるタンパク質、
(A03)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約7050のイオンピークを生じるタンパク質、
(A04)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8330のイオンピークを生じるタンパク質、
(A05)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8840のイオンピークを生じるタンパク質、
(A06)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8930のイオンピークを生じるタンパク質、
(A07)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約9070のイオンピークを生じるタンパク質、
(A08)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約11600のイオンピークを生じるタンパク質、
(A09)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13700のイオンピークを生じるタンパク質、
(A10)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13900のイオンピークを生じるタンパク質、
(A11)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約21400のイオンピークを生じるタンパク質。
【0044】
これらのマーカー物質はいずれも主に血液中に存在するタンパク質であり、内臓脂肪型肥満を発症している又は発症し得る動物の体液中で特異的に検出されるものである。なお、(A01)、(A03)、(A04)、(A05)、(A06)、(A09)、(A10)、及び(A11)の各マーカー物質(以下、これらのマーカー物質からなるグループを「グループ1」と称することがある。)は、内臓脂肪が増加した状態でより高値を示すものであるので、被験物質が内臓脂肪増加抑制効果を有する場合には、当該被験物質を投与した動物においてより低値を示す。一方、(A02)、(A07)、及び(A08)の各マーカー物質(以下、これらのマーカー物質からなるグループを「グループ2」と称することがある。)は、内臓脂肪が増加した状態でより低値を示すものであるので、被験物質が内臓脂肪増加抑制効果を有する場合には、当該被験物質を投与した動物においてより高値を示す。
【0045】
ある条件のペプチドマッピングによれば、マーカー物質(A03)はアポリポタンパク質C1、マーカー物質(A04)はアポリポタンパク質C2、マーカー物質(A05)はアポリポタンパク質A2、マーカー物質(A06)はアポリポタンパク質C3、マーカー物質(A07)は補体C3a(des−Arg)、マーカー物質(A08)はβ2−ミクログロブリン、マーカー物質(A09)はトランスサイレチン、マーカー物質(A10)はトランスサイレチン、マーカー物質(A11)はアポリポタンパク質M、と同定される。すなわち、ある実施形態では、下記(a)〜(i)の少なくとも1つを満たす。
(a)マーカー物質(A03)はアポリポタンパク質C1又はその修飾体である、
(b)マーカー物質(A04)はアポリポタンパク質C2又はその修飾体である、
(c)マーカー物質(A05)はアポリポタンパク質A2又はその修飾体である、
(d)マーカー物質(A06)はアポリポタンパク質C3又はその修飾体である、
(e)マーカー物質(A07)は補体C3又はその修飾体である、
(f)マーカー物質(A08)はβ2−ミクログロブリン又はその修飾体である、
(g)マーカー物質(A09)はトランスサイレチン又はその修飾体である、
(h)マーカー物質(A10)はトランスサイレチン又はその修飾体である、
(i)マーカー物質(A11)はアポリポタンパク質M又はその修飾体である。
【0046】
本発明の内臓脂肪増加抑制効果の評価方法の他の様相では、被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価する。
(B1)アポリポタンパク質C1又はその修飾体、
(B2)アポリポタンパク質C2又はその修飾体、
(B3)アポリポタンパク質A2又はその修飾体、
(B4)アポリポタンパク質C3又はその修飾体、
(B5)補体C3又はその修飾体、
(B6)β2−ミクログロブリン又はその修飾体、
(B7)トランスサイレチン又はその修飾体、
(B8)アポリポタンパク質M又はその修飾体。
【0047】
タンパク質の修飾の例としては、N末端αアミノ基やリジンεアミノ基のメチル化、アセチル化、アデニリル化、ミリスチル化等;セリン・スレオニン・アスパラギンへの糖又は糖鎖の付加;セリン・スレオニン・チロシン・アルギニン・ヒスチジンのリン酸化;システインのシステイニル化、ホモシステイニル化、スルホニル化等;グルタミン酸のγ−カルボキシル化;N末端グルタミン酸のピログルタミン酸への変換、等が挙げられる。また、これらの修飾の脱離(脱メチル化、糖又は糖鎖の脱離、脱リン酸化等)も「修飾」に含まれる。
【0048】
「タンパク質又はその修飾体」には、当該タンパク質のアイソフォームが含まれる。アイソフォームとしては、前記した各種の修飾の他、選択的スプライシングによって生じたタンパク質が挙げられる。さらに、「タンパク質又はその修飾体」には、当該タンパク質の1次構造において数個のアミノ酸残基が欠失、置換若しくは付加されたような実質的に同一のタンパク質が含まれる。またさらに、「タンパク質又はその修飾体」には、プロテアーゼによる切断を受けた当該タンパク質由来のタンパク質断片が含まれる。例えば、当該タンパク質由来と認められうる長さのタンパク質断片、例えば20個以上のアミノ酸残基からなるタンパク質断片、分子量が2千以上のタンパク質断片、等が挙げられる。また、複合体タンパク質の場合には「タンパク質又はその修飾体」にはそのサブユニットも含まれるものとする。
【0049】
例えば、アポリポタンパク質C1(配列番号1)のN末端側2アミノ酸残基(Ala−Pro)が欠損したタンパク質断片(配列番号2)は「アポリポタンパク質C1の修飾体」に含まれる。
【0050】
例えば、補体C3のタンパク質断片である補体C3a des Arg(配列番号6)は「補体C3又はその修飾体」に含まれる。
【0051】
トランスサイレチン(配列番号8)については、その唯一のCys残基が修飾を受けた種々の修飾トランスサイレチンが見出されている(Amareth Lim et al., J. Biol. Chem., vol. 258, No. 50, 2003)。例えば、トランスサイレチンのCys残基にシステインが付加した「システイニル化トランスサイレチン」や、グルタチオンが付加した「グルタチオン化トランスサイレチン」は、「トランスサイレチンの修飾体」に含まれる。さらに、トランスサイレチンは4個のサブユニットからなる複合体タンパク質であるので、当該サブユニットは「トランスサイレチン又はその修飾体」に含まれる。
【0052】
本発明の内臓脂肪増加抑制効果の評価方法では、(A01)〜(A11)の各マーカー物質ならびに(B1)〜(B8)に属する各マーカー物質の1つだけを用いてもよいし、複数を組み合わせて用いてもよい。複数を用いる場合の組み合わせ方については特に限定はないが、例えば、グループ1から選択したマーカー物質(1つ又は複数)とグループ2から選択したマーカー物質(1つ又は複数)とを組み合わせることができる。
【0053】
本発明の内臓脂肪増加抑制効果の評価方法では「被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物」を用いる。好ましい実施形態では、当該動物として「被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物」を用いる。例えば、動物に被験物質と低繊維高脂肪食とを同時摂取させた動物を用いればよい。低繊維高脂肪食は、例えば、低繊維飼料に数%〜数十%の動物性脂肪を混合することにより調製することができる。他の実施形態としては、内臓脂肪型肥満を発症する自然発症モデル動物や遺伝子操作モデル動物を用いることも考えられる。例えば、当該自然発症モデル動物や遺伝子操作モデル動物に被験物質を投与し、体液中における各マーカー物質の濃度を指標とすればよい。
【0054】
「内臓脂肪型肥満を発症している又は発症し得る動物」における動物の種類には特に限定はなく、例えば、マウス、ラット、ウサギ、ブタ等を採用することができる。さらに、動物としてヒトを採用することもできる。この場合には、臨床試験の結果によって物質を評価することになる。
【0055】
本発明の内臓脂肪増加抑制効果の評価方法では、動物の体液中におけるマーカー物質の濃度を基準値と比較する。当該基準値としては特に限定はなく、目的に応じて適宜設定すればよい。例えば、「被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物」を採用する場合には、低繊維高脂肪食のみを摂取させた動物の体液中における前記マーカー物質の濃度を用いることができる。低繊維高脂肪食のみを摂取させた動物は、内臓脂肪型肥満を発症している又は発症し得る動物のモデルとなり、その体液中のマーカー物質濃度は「異常値」となる。そして、被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物(例えば同時摂取)における値(測定値)と当該基準値(異常値)とを比較し、測定値が基準値と有意に差がありかつ正常側である場合(正常側に維持された場合)に、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。具体的には、グループ1に属するマーカー物質を指標とする場合は、測定値が当該基準値に比べて有意に低いときに、グループ2に属するマーカー物質を指標とする場合は、測定値が基準値に比べて有意に高いときに、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。
【0056】
さらに、基準値は複数あってもよい。例えば、上記の異常値に加え、通常食を摂取させた動物における値(正常値。陰性対照。)を基準値に加えることができる。具体的には、
(1)通常食を摂取(正常値)、
(2)低繊維高脂肪食を摂取(異常値)、
(3)被験物質と低繊維高脂肪食とを同時摂取、
の3群を設定し、動物を飼育する。そして、各動物の体液中の上記マーカー物質を測定し、各測定値を比較する。このとき、(1)と(2)とで有意差があり、(3)と(2)とで有意差があり、かつ(3)が(2)に比べて正常側((1)に近い側)である場合(正常側に維持された場合)に、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。
【0057】
さらに、基準値として、内臓脂肪増加抑制効果を有する既知物質と低繊維高脂肪食とを同時摂取させた動物における値(陽性対照)を加えることもできる。具体的には、上記(1)〜(3)に加えて、
(4)上記既知物質と低繊維高脂肪食とを同時摂取させる群、
を設定し、動物を飼育する。このとき、(1)と(2)とで有意差があり、(3)と(2)とで有意差があり、かつ(3)が(2)に比べて正常側((1)及び(4)に近い側)である場合に、当該被験物質が内臓脂肪増加抑制効果を有すると評価することができる。すなわち、このような被験物質は、(4)で採用した上記既知物質と同様の挙動を示し、同様の作用を有する物質といえる。
【0058】
内臓脂肪型肥満を発症する自然発症モデル動物や遺伝子操作モデル動物を用いる場合には、上記(2)の代わりに「内臓脂肪増加抑制効果を有さない既知物質を摂取させる群」、上記(3)の代わりに「被験物質を摂取させる群」を設定すればよい。
【0059】
本発明の内臓脂肪増加抑制効果の評価方法において使用する動物の体液としては、血液が好ましく用いられる。特に、血液から調製した血清又は血漿(体液成分)を測定試料とすることが好ましい。血清又は血漿は遠心分離等の公知の方法で血液から調製することができる。
【0060】
本発明の内臓脂肪増加抑制効果の評価方法における被験物質としては、食品素材、医薬原体などが挙げられる。特に、食品素材を評価対象とする場合は、機能性食品の開発に役立てることができる。
【0061】
本発明の内臓脂肪増加抑制効果の評価方法において、マーカー物質の濃度を測定する方法は、そのマーカー物質の濃度を特異的に測定できる方法であれば、タンパク質の定量に一般に用いられている方法をそのまま用いることができる。例えば、各種のイムノアッセイ、質量分析(MS)、クロマトグラフィー、電気泳動等を用いることができる。
【0062】
イムノアッセイによれば、夾雑物質の多い試料のままでも正確にマーカー物質の濃度を測定することができる。イムノアッセイの例としては、抗原抗体結合物を直接的又は間接的に測定する沈降反応、凝集反応、溶血反応などの古典的な方法や、標識法と組み合わせて検出感度を高めたエンザイムイムノアッセイ(EIA)、ラジオイムノアッセイ(RIA)、蛍光イムノアッセイ(FIA)等の方法が挙げられる。なお、これらのイムノアッセイに用いるマーカー物質に特異的な抗体は、モノクローナルでもよいし、ポリクローナルでもよい。
【0063】
質量分析によれば、各マーカー物質由来のイオンピークを特定し、そのイオンピーク強度をもって各マーカー物質の量(濃度)を測定することができる。質量分析によってマーカー物質の濃度を測定する場合のイオン化の方法としては、マトリクス支援レーザーイオン化(matrix-assisted laser desorption/ionization、MALDI)、エレクトロスプレーイオン化(electrospray ionization、ESI)のいずれも適用可能であるが、多価イオンの生成が少ないMALDIが好ましい。特に、飛行時間質量分析計(time-of-flight mass spectrometer、TOF)と組み合わせたMALDI−TOF−MSによれば、より正確にマーカー物質由来のイオンピークを特定することができる。
【0064】
電気泳動によりマーカー物質の濃度を測定する場合は、例えば、検査材料をSDS−ポリアクリルアミドゲル電気泳動(SDS−PAGE)に供して目的のマーカー物質を分離し、適宜の色素や蛍光物質でゲルを染色し、目的のマーカー物質に相当するバンドの濃さや蛍光強度を測定すればよい。SDS−PAGEだけではマーカー物質の分離が不十分な場合は、等電点電気泳動(IEF)と組み合わせた2次元電気泳動を用いることもできる。さらに、ゲルから直接検出するのではなく、ウエスタンブロッティングを行って膜上のマーカー物質の量を測定することもできる。
【0065】
クロマトグラフィーによってマーカー物質の濃度を測定する場合は、例えば、液体高速クロマトグラフィー(HPLC)による方法を用いることができる。すなわち、試料をHPLCに供して目的のマーカー物質を分離し、そのクロマトグラムのピーク面積を測定することにより試料中のマーカー物質の濃度を測定することができる。
【0066】
好ましい実施形態では、マーカー物質を担体上に捕捉し、その捕捉されたマーカー物質を測定対象とする。すなわち、マーカー物質に対する親和性を有する物質を担体に固定化し、その親和性を有する物質を介してマーカー物質を担体上に捕捉する。そして、捕捉された前記マーカー物質の量に基づいて体液中の前記マーカー物質の濃度を算出する。本実施形態によれば、試料中に含まれる夾雑物質の影響を低減させることができ、より高感度かつ高精度でマーカー物質の濃度を測定することができる。本実施形態において用いることができる担体の例としては、ビーズ、金属、ガラス、樹脂等のような一般的なものの他、基板のような、平面部分を有する担体を用いることができる。基板を用いる場合は、その平面部分の一部にマーカー物質に対する親和性を有する物質を固定化することが好ましい。例としては、基板としてチップを用い、その表面の複数箇所にスポット的にマーカー物質に親和性を有する物質を固定化した担体が挙げられる。なお「親和性」の例としては、イオン結合、金属キレート体とタンパク質中のヒスチジン残基等とのアフィニティ、抗原と抗体、酵素と基質、若しくはホルモンとレセプターのようなバイオアフィニティ、及び、疎水性相互作用のような化学的な相互作用、が挙げられる。
【0067】
イオン結合によってマーカー物質を担体に捕捉する場合は、イオン交換体を担体に固定化する。この場合、イオン交換体には陽イオン交換体、陰イオン交換体のいずれも用いることができ、さらに、強陽イオン交換体、弱陽イオン交換体、強陰イオン交換体、弱陰イオン交換体のいずれも用いることができるが、強陰イオン交換体と弱陽イオン交換体が好ましく用いられる。強陰イオン交換体の例としては、4級アンモニウム(トリメチルアミノメチル)(QA)、4級アミノエチル(ジエチル,モノ・2−ヒドロキシブチルアミノエチル)(QAE)、4級アンモニウム(トリメチルアンモニウム)(QMA)等の強陰イオン交換基を有するものが挙げられる。また、弱陽イオン交換体の例としては、カルボキシメチル(CM)等の弱陽イオン交換基を有するものが挙げられる。また、強陽イオン交換体の例としては、スルホプロピル(SP)等の強陽イオン交換基を有するものが挙げられる。さらに、弱陰イオン交換体の例としては、ジメチルアミノエチル(DE)、ジエチルアミノエチル(DEAE)等の弱陰イオン交換基を有するものが挙げられる。
【0068】
金属キレート体を介してマーカー物質を捕捉する場合は、例えば、Cu2+、Zn2+、Ni2+、Co2+、Al3+、Fe3+、Ga3+等の金属キレート体を固定化した担体を用いることができる。
【0069】
抗体によってマーカー物質を担体に捕捉する場合は、マーカー物質に特異的な抗体を担体に固定化すればよい。
【0070】
疎水性相互作用によってマーカー物質を担体に捕捉する場合は、担体に疎水基をもつ物質を固定化する。疎水基の例としては、C4〜C20のアルキル基、フェニル基等が挙げられる。
【0071】
本実施形態においてマーカー物質の測定方法にイムノアッセイを用いる場合は、抗体を固定化した担体を用いることが好ましい。このようにすれば、担体に固定化された抗体を1次抗体としたイムノアッセイの系を簡単に構築することができる。例えば、マーカー物質に特異的でエピトープの異なる2種類の抗体を用意し、一方を1次抗体として担体に固定化し、他方を2次抗体として酵素標識し、サンドイッチEIAの系を構築することができる。その他、結合阻止法や競合法によるイムノアッセイの系も構築可能である。さらに、担体として基板を用いる場合は、抗体チップによるイムノアッセイが可能である。抗体チップによれば、複数のマーカー物質の濃度を同時に測定でき、迅速な測定が可能である。
【0072】
一方、本実施形態において質量分析を用いる場合は、例えば、抗体の他、イオン交換体、金属キレート体又は疎水基を固定化した担体を用いることができる。なお、これらの物質による結合は抗原と抗体等のバイオアフィニティほどの特異性がないので、これらの物質を固定化した担体を用いる場合はマーカー物質以外の物質も担体上に捕捉されうるが、質量分析によれば分子量を反映した質量分析計スペクトルによって定量するので、問題はない。特に、担体として基板を用い、表面エンハンス型レーザー脱離イオン化(surface-enhanced laser desorption/ionization)−飛行時間質量分析(time-of-flight mass spectrometry)(以下、「SELDI−TOF−MS」と称する)を行うことにより、マーカー物質の濃度をより正確に測定することができる。使用できる基板の種類としては、陽イオン交換基板、陰イオン交換基板、順相基板、逆相基板、金属イオン基板、抗体基板等を用いることができるが、陽イオン交換基板、特に弱陽イオン交換基板と、陰イオン交換基板、特に強陰イオン交換基板が好ましく用いられる。
【0073】
本発明の物質のスクリーニング方法は、本発明の内臓脂肪増加抑制効果の評価方法によって被験物質を評価し、所望の内臓脂肪増加抑制効果を有する物質をスクリーニングするものである。本発明の物質のスクリーニング方法においても、上記した本発明の内臓脂肪増加抑制効果の評価方法の実施形態と全く同様の実施形態をとることができる。
【0074】
本発明の内臓脂肪増加抑制効果の評価方法を簡便に行なうために、必要な試薬類をまとめて評価用キットを構築することができる。当該評価用キットとしては、例えば、マーカー物質に対する親和性を有する物質を固定化した担体を含むものが挙げられる。特に、担体として、CM等の弱陽イオン交換体、あるいはQAやQAE等の強陰イオン交換体を固定化した基板を含めた評価用キットによれば、SELDI−TOF−MS等を簡便に行なうことができる。本キット中には他の試薬類、例えば、標準物質、前処理用の各種緩衝液等を含めてもよい。なお本キットは、内臓脂肪増加抑制効果を有する物質をスクリーニングするためのキットとしても使用できる。本発明のキットの構成例を以下に挙げる。
【0075】
〔キットの構成例〕
(1)弱陽イオン交換基板:1枚
(2)強陰イオン交換基板:1枚
(3)基板洗浄用バッファーA(pH3.0):適量
(4)基板洗浄用バッファーB(pH9.0):適量
(5)各マーカー物質の標準品:各適量
【0076】
以下に、実施例をもって本発明をさらに具体的に説明するが、本発明はこれらの実施例に限定されるものではない。
【実施例1】
【0077】
4週齢のSDラットを1群当たり6〜8匹用意した。第1群のラットには、通常食としてCE−2(日本クレア社)を摂取させた。第2群のラットには、低繊維高脂肪食(低繊維飼料に30%牛脂混餌)を摂取させた。第3群には、前記低繊維高脂肪食と内臓脂肪増加抑制効果を有する既知素材との混合飼料を摂取させた。第4群には、通常飼料と内臓脂肪増加抑制効果を有する既知素材との混合飼料を摂取させた。各飼料は自由摂取とし、3週間(21日)飼育した。飼育終了後、各ラットの体重、体重当たりの内臓脂肪の量(腸間膜、腎、精巣周囲)、体重当たりの皮下脂肪の量(肩甲骨、腰下肢周囲)を測定し、4群比較した。さらに、各ラットから全血を採取して血漿を調製した。
【0078】
図1に体重の測定結果、図2に内臓脂肪の測定結果、図3に皮下脂肪の測定結果を示す。図1〜3において、記号*は第1群に対する有意差、記号#は第2群に対する有意差を示し、「*」「#」は5%有意、「**」「##」は1%有意、「***」「###」は0.1%有意を意味する。まず図1に示すように、第1群と第4群(通常飼料群)に対して、第2群と第3群の方が有意に体重が多かった。また、第3群と第4群との間では有意差はなかった。すなわち、上記既知飼料による体重への影響は見られなかった。また図2に示すように、第1群と第4群(通常飼料群)に対して、第2群と第3群の方が有意に内臓脂肪の量が多かった。さらに、第2群に対して第3群の方が有意に内臓脂肪の量が少なかった。これにより、上記既知飼料による内臓脂肪抑制効果が裏付けられた。なお図3に示すように、皮下脂肪についても内臓脂肪と同様の傾向を示した。以上より、本動物実験の妥当性が裏付けられた。なお、本実験では3週間(21日)という短期間で飼育を終了しており、飼育終了時における第2群のラットは発症初期の内臓脂肪型肥満の状態であったと考えられる。
【0079】
2.プロテインチップによる解析とイオンピークの選抜
各血漿試料20μLに、変性バッファー(9M 尿素、2% CHAPS、50mM Tris−HCl(pH9.0))30μLを加えて前処理を行い、タンパク質を変性させた。次に、前処理した各体液試料を強陰イオン交換樹脂カラム(Q−Sepharose、GEヘルスケア社)にアプライした。次いで、pH9.0の緩衝液(50mM Tris−HCl(pH9.0)、0.1%(w/v)1−o−N−オクチル−β−D−グルコピラノシド(以下、「OGP」と称する。))、pH5.0の緩衝液(100mM 酢酸ナトリウム(pH5.0)、0.1%(w/v)OGP)、pH3.0の緩衝液(50mM クエン酸ナトリウム(pH3.0)、0.1%(w/v)OGP)、及び有機溶媒(0.1%トリフルオロ酢酸、50.0%アセトニトリルからなる混合液)各200μLで順に溶出させ、画分1(pH9.0で溶出、素通り)、画分2(pH5.0で溶出)、画分3(pH3.0で溶出)、画分4(有機溶媒で溶出)の4つの粗分画画分を得た。
【0080】
得られた各画分10μLをpH3.0のプロテインチップ結合バッファー(50mM クエン酸ナトリウム)で10倍希釈した後、弱陽イオン交換チップCM10(バイオラッド社)に添加した。同様に、得られた各画分10μLをpH9.0のプロテインチップ結合バッファー(50mM Tris−HCl(pH9.0))で10倍希釈した後、強陰イオン交換チップQ10(バイオラッド社)に添加した。各チップを各結合バッファーで3回洗浄した後に脱イオン水で1回洗浄し、乾燥させた。次に、エネルギー吸収分子であるシナピン酸(SPA−H、SPA−L)又はα−シアノ−4−ヒドロキシケイ皮酸(CHCA)を添加し、プロテインチップリーダーModel PBS IIc(バイオラッド社)を用いて、SELDI−TOF−MSを行なった。なお、測定分子量範囲(m/z)は、3000〜200000の範囲で行なった。また、測定は2連で行い、m/zの平均値を算出した。データ解析は、Protein Chip Software、CiphergenExpress Data Manager、及びBiomarker Patterns Software(いずれもバイオラッド社)を用いて行なった。具体的には、ベースライン補正、分子量校正、スペクトルの正規化処理を行なった後、シングルマーカー解析及び数本のマーカーを組み合わせたマルチフロー解析を行なった。その結果、粗分画画分の種類、プロテインチップの種類、チップの洗浄条件等の組み合わせによって多数のピークが検出された。各ピークについて、p値(Mann−Whitney検定法)、ROC面積、及びイオンピーク強度を算出し、さらに、以下の(1)〜(4)の条件を指標として11個の候補ピークを選抜した。
【0081】
(1)候補ピーク探索(基本)
第1群と第2群との間でイオン強度に有意差がある(p<0.05)。
(2)上記既知物質の効果検証
第2群と第3群との間でイオン強度に有意差があり(p<0.05またはp<0.1)、かつ第3群の値の方が第2群の値よりも第1群の値に近い(第3群の値が第1群側に復帰している)。
(3)増減パターン解析
第2群のみが高値または低値を示し、第1群、第3群および第4群の間ではあまり差がない。なお、第3群と第4群との間に差があっても、第4群の値の方が第3群の値よりも第2群から離れている場合には本条件を満たすものとして取り扱う。
【0082】
3.マーカー物質(A01)の特定
画分4(有機溶媒)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:CHCA)を行なった場合に、質量/電荷比が4612(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図4に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。図中、髭の上端と下端はそれぞれ最大値と最小値、箱の上辺と下辺はそれぞれ第3四分位(75パーセンタイル)と第1四分位(25パーセンタイル)、箱の中の線は中央値である(図5以降も同じ)。その結果、本ピークのROC面積(第1群vs第2群)は0.750、p値(第1群vs第2群)は0.018、p値(第2群vs第3群)は0.014であった。
【0083】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約4610のピークを生じるタンパク質(マーカー物質(A01))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A01)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約4610のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0084】
4.マーカー物質(A02)の特定
画分1(pH9.0)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が5501(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で高値を示し、第2群で低値を示した。図5に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.833、p値(第1群vs第2群)は0.002、p値(第2群vs第3群)は0.004であった。
【0085】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約5500のピークを生じるタンパク質(マーカー物質(A02))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A02)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約5500のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0086】
5.マーカー物質(A03)の特定
画分3(pH3.0)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−L)を行なった場合に、質量/電荷比が7055(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図6に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.750、p値(第1群vs第2群)は0.029、p値(第2群vs第3群)は0.018であった。
【0087】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約7050のピークを生じるタンパク質(マーカー物質(A03))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A03)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約7050のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0088】
6.マーカー物質(A04)の特定
画分4(有機溶媒)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が8333(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図7に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.984、p値(第1群vs第2群)は0.00002、p値(第2群vs第3群)は0.060であった。
【0089】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約8330のピークを生じるタンパク質(マーカー物質(A04))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A04)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約8330のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0090】
7.マーカー物質(A05)の特定
画分1(pH9.0)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−L)を行なった場合に、質量/電荷比が8337(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図8に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.802、p値(第1群vs第2群)は0.004、p値(第2群vs第3群)は0.090であった。
【0091】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約8340のピークを生じるタンパク質(マーカー物質(A05))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A05)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約8340のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0092】
8.マーカー物質(A06)の特定
画分4(有機溶媒)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が8931(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図9に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.984、p値(第1群vs第2群)は0.00001、p値(第2群vs第3群)は0.001であった。
【0093】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約8930のピークを生じるタンパク質(マーカー物質(A06))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A06)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約8930のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0094】
9.マーカー物質(A07)の特定
画分1(pH9.0)を弱陽イオン交換チップCM10に接触させ、pH3.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:CHCA)を行なった場合に、質量/電荷比が9065(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で高値を示し、第2群で低値を示した。図10に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.714、p値(第1群vs第2群)は0.046、p値(第2群vs第3群)は0.018であった。
【0095】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約9070のピークを生じるタンパク質(マーカー物質(A07))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A07)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約9070のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0096】
10.マーカー物質(A08)の特定
画分1(pH9.0)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が11643(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で高値を示し、第2群で低値を示した。図11に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.729、p値(第1群vs第2群)は0.033、p値(第2群vs第3群)は0.090であった。
【0097】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約11600のピークを生じるタンパク質(マーカー物質(A08))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A08)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約11600のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0098】
11.マーカー物質(A09)の特定
画分4(有機溶媒)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−L)を行なった場合に、質量/電荷比が13733(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図12に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.703、p値(第1群vs第2群)は0.046、p値(第2群vs第3群)は0.055であった。
【0099】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約13700のピークを生じるタンパク質(マーカー物質(A09))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A09)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約13700のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0100】
12.マーカー物質(A10)の特定
画分2(pH5.0)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が13922(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図13に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.755、p値(第1群vs第2群)は0.020、p値(第2群vs第3群)は0.042であった。
【0101】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約13900のピークを生じるタンパク質(マーカー物質(A10))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A10)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約13900のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0102】
13.マーカー物質(A11)の特定
画分4(有機溶媒)を強陰イオン交換チップQ10に接触させ、pH9.0のプロテインチップ結合バッファーで洗浄してSELDI−TOF−MS(EAM:SPA−H)を行なった場合に、質量/電荷比が21384(平均値)のイオンピークが検出された。増減パターン解析の結果、本ピークは第1群、第3群および第4群で低値を示し、第2群で高値を示した。図14に、各群に分けて本ピークのピーク強度をプロットした場合の箱髭図を示す。その結果、本ピークのROC面積(第1群vs第2群)は0.750、p値(第1群vs第2群)は0.011、p値(第2群vs第3群)は0.083であった。
【0103】
以上より、SELDI−TOF−MSに供すると質量/電荷比が約21400のピークを生じるタンパク質(マーカー物質(A11))が、内臓脂肪型肥満を発症している又は発症し得る動物に特異的な物質であり、内臓脂肪の状態を反映するマーカーとなり得ることがわかった。これにより、被験物質を投与した内臓脂肪型肥満を発症している又は発症し得る動物の体液中におけるマーカー物質(A11)の濃度を指標として、被験物質が有する内臓脂肪増加抑制効果の評価、並びに、そのような物質のスクリーニングが行なえることが示された。例えば、所望の被験物質を使用して同様の動物実験を行なって体液試料を調製し、同様の手順でSELDI−TOF−MSを行なった場合に、質量/電荷比が約21400のピークを生じるタンパク質の濃度が正常値に維持されたとき、該被験物質は、内臓脂肪増加抑制効果を有すると評価することができる。
【0104】
なお、ヒトの体液中にもマーカー物質(A01)〜(A11)と同等のタンパク質が存在する場合には、ヒトの体液中における当該タンパク質の濃度を指標として、内臓脂肪型肥満を診断できる可能性も示唆された。
【実施例2】
【0105】
マーカー物質(A03)の精製と同定
強陰イオン交換樹脂Q-Sepharose HP(GEヘルスケア社)を充填したカラム(5mL)を平衡化バッファー(50mM Tris−HCl pH9.0,1M 尿素,0.22% CHAPS)にて平衡化した。ラット標準血清(ケミコン社)1.5mLに対して変性バッファー(50mM Tris−HCl pH9.0,9M 尿素,2% CHAPS)を450μL加えて変性処理した後、平衡化した前記カラムに添加した。非吸着画分を回収した。回収した画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A03)の質量/電荷比(平均値:7054)と同等の質量/電荷比を示すピークを確認した。
【0106】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図15)。図15中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約7.0kDaのバンド(図15の矢印a)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A03)と同等の質量/電荷比を示すピークを確認した(図16の矢印)。
【0107】
あらためて同様のSDS−PAGEを行って約7.0kDaのバンドを切り出し、還元アルキル化処理した後、0.01μg/μLのトリプシン溶液(50mM 炭酸水素アンモニウム(pH8.0)に溶解)を作用させてゲル内で消化した。消化したサンプル1μLを金属プレート上に滴下し、飽和CHCA溶液0.4μLをさらに滴下して乾燥させた後、質量分析計Proteomics Analyzer 4700(アプライドバイオシステムズ社)で測定したところ、少なくとも5個のピークが検出され、それらの精密質量は「1293.66」、「1052.49」、「1279.62」、「781.45」、及び「1138.54」と算出された。これらのデータを元にMascotデータベース(マトリックスサイエンス社)によって既知タンパク質を検索し、ペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号10〜14で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質C1」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第1表に示す。既報のラットアポリポタンパク質C1(成熟型)のアミノ酸配列を配列番号1に示す。
【0108】
【表1】

【0109】
ここで、ヒト、マウス等において、アポリポタンパク質C1のN末端側2アミノ酸残基が欠損したものが見出されている。全長のラットアポリポタンパク質C1(配列番号1)の質量が7187Daであり、一方、N末端側2アミノ酸残基(Ala−Pro)が欠損したラットアポリポタンパク質C1の断片(配列番号2)の質量が7019Daであることから、マーカー物質(A03)はアポリポタンパク質C1の断片(配列番号2)と最終的に同定された。
【実施例3】
【0110】
マーカー物質(A04)の精製と同定
強陰イオン交換樹脂HiTrap Q HP (5mL)(GEヘルスケア社)を50mM 酢酸ナトリウムバッファー(pH6.0)にて平衡化した。ラット標準血清(ケミコン社)1mLを50mM 酢酸ナトリウムバッファー(pH6.0)で10倍に希釈した後、Millex0.45μLでろ過し、平衡化した前記カラムに添加した。5カラム体積(CV)の50mM 酢酸ナトリウムバッファー(pH6.0)、12CVの50mM 酢酸ナトリウムバッファー(pH6.0)/200mM NaCl、及び5CVの50mM 酢酸ナトリウムバッファー(pH6.0)でカラムを順次洗浄した後、50mM 酢酸ナトリウムバッファー(pH3.0)で溶出し、280nmの吸光度の高い画分を回収した(約1mL)。回収した画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A04)の質量/電荷比(平均値:8333)と同等の質量/電荷比を示すピークを確認した。
【0111】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図17)。図17中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約8.3kDaのバンド(図17の矢印a)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A04)の質量/電荷比(平均値:8333)と同等の質量/電荷比を示すピークを確認した(図18の矢印)。
【0112】
あらためて同様のSDS−PAGEを行って約8.3kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも7個のピークが検出され、それらの精密質量は「950.49」、「1055.54」、「1324.74」、「1964.98」、「928.46」、「2261.18」、及び「2447.26」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号15〜21で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質C2」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第2表に示す。既報のラットアポリポタンパク質C2のアミノ酸配列を配列番号3に示す。
【0113】
【表2】

【実施例4】
【0114】
マーカー物質(A05)の精製と同定
実施例2で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A05)の質量/電荷比(平均値:8837)と同等の質量/電荷比を示すピークを確認した。
【0115】
実施例2で行ったSDS−PAGEで分離された約8.8kDaのバンド(図15の矢印b)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A05)と同等の質量/電荷比を示すピークを確認した(図19)。
【0116】
あらためて同様のSDS−PAGEを行って約8.8kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも3個のピークが検出され、それらの精密質量は「1126.54」、「860.50」、及び「1270.63」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号22〜24で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質A2」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第3表に示す。既報のラットアポリポタンパク質A2のアミノ酸配列を配列番号4に示す。
【0117】
【表3】

【実施例5】
【0118】
マーカー物質(A06)の精製と同定
実施例3で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A06)の質量/電荷比(平均値:8931)と同等の質量/電荷比を示すピークを確認した。
【0119】
実施例3で行ったSDS−PAGEで分離された約8.9kDaのバンド(図17の矢印b)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A06)と同等の質量/電荷比を示すピークを確認した(図20)。
【0120】
あらためて同様のSDS−PAGEを行って約8.9kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも2個のピークが検出され、それらの精密質量は「2262.00」及び「968.53」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号25,26で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質C3」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第4表に示す。既報のラットアポリポタンパク質C3のアミノ酸配列を配列番号5に示す。
【0121】
【表4】

【実施例6】
【0122】
マーカー物質(A07)の精製と同定
強陰イオン交換樹脂Q-Sepharose HP(GEヘルスケア社)を充填したカラム(1mL)を平衡化バッファー(50mM Tris−HCl pH9.0,1M 尿素,0.22% CHAPS)にて平衡化した。ラット標準血清(ケミコン社)500μLに対して変性バッファー(50mM Tris−HCl pH9.0,9M 尿素,2% CHAPS)を750μL加えて4℃で20分間変性処理した。変性処理したサンプルを12,000G、4℃で10分間遠心し、0.45μmのフィルターでろ過した後、平衡化した前記カラムに添加し、非吸着画分を回収した。回収した画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A07)の質量/電荷比(平均値:9065)と同等の質量/電荷比を示すピークを確認した。
【0123】
弱陽イオン交換樹脂HiTrap CM FF 1mL(GEヘルスケア社)を50mM HEPES−NaOH(pH7.0)にて平衡化した。上記の回収画分3mLと100mM酢酸ナトリウムバッファー(pH5.0)2.3mLを混合し、0.45μLのフィルターでろ過した後、平衡化した前記カラムに添加した。50mM HEPES−NaOH(pH7.0)でカラムを洗浄した後、5CVの50mM HEPES−NaOH(pH7.0)/50mM NaCl、5CVの50mM HEPES−NaOH(pH7.0)/100mM NaCl、及び5CVの50mM HEPES−NaOH(pH7.0)/150mM NaClで順次洗浄し、5CVの50mM HEPES−NaOH(pH7.0)/1M NaClで溶出した。溶出画分に対してSELDI−TOF−MS分析を行い、マーカー物質(A07)の質量/電荷比(平均値:9065)と同等の質量/電荷比を示すピークを確認した。
【0124】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図21)。図21中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約9.1kDaのバンド(図21の矢印)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A07)の質量/電荷比(平均値:9065)と同等の質量/電荷比を示すピークを確認した(図22の矢印)。
【0125】
あらためて同様のSDS−PAGEを行って約9.1kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも3個のピークが検出され、それらの精密質量は「1148.43」、「1438.38」、及び「838.34」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号27〜29で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「補体C3a(des−Arg)」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第5表に示す。既報のラット補体C3a(des−Arg)のアミノ酸配列を配列番号6に示す。
【0126】
【表5】

【実施例7】
【0127】
マーカー物質(A08)の精製と同定
実施例2で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A08)の質量/電荷比(平均値:11642)と同等の質量/電荷比を示すピークを確認した。
【0128】
実施例2で行ったSDS−PAGEで分離された約11.6kDaのバンド(図15の矢印c)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A08)と同等の質量/電荷比を示すピークを確認した(図23)。
【0129】
あらためて同様のSDS−PAGEを行って約11.6kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも5個のピークが検出され、それらの精密質量は「1091.59」、「3445.48」、「1496.73」、「2822.17」、及び「777.39」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号30〜34で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「β2−マクログロブリン」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第6表に示す。既報のラットβ2−マクログロブリンのアミノ酸配列を配列番号7に示す。
【0130】
【表6】

【実施例8】
【0131】
マーカー物質(A08)と(A09)の精製と同定
強陰イオン交換樹脂Q-Sepharose HP(GEヘルスケア社)を充填したカラム(5mL)を平衡化バッファー(50mM Tris−HCl pH9.0,1M 尿素,0.22% CHAPS)にて平衡化した。ラット標準血清(ケミコン社)1.5mLに対して変性バッファー(50mM Tris−HCl pH9.0,9M 尿素,2% CHAPS)を450μL加えて変性処理した後、平衡化した前記カラムに添加した。5CVの50mM Tris−HCl(pH9.0)、5CVの50mM 酢酸ナトリウムバッファー(pH5.0)、及び5CVの50mM クエン酸ナトリウムバッファー(pH3.0)で順次洗浄した後、33.3%イソプロパノール/16.7%アセトニトリル/0.1%トリフルオロ酢酸で溶出し、溶出画分を回収した。
【0132】
回収した画分の一部をアセトン沈殿処理した後、ポリペプチド分離用ゲル(15−20%)NTH−5A0Tゲル(DRC社)を用いてSDS−PAGEを行った(図24)。図24中、レーン1〜6はいずれも回収画分、Mは分子量マーカーである。分離された約13.7kDa付近のバンド(図24の矢印a)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A08)と(A09)の質量/電荷比(平均値:13733,13922)と同等の質量/電荷比を含むピークを確認した(図25の矢印)。
【0133】
あらためて同様のSDS−PAGEを行って約13.7kDa付近のバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも7個のピークが検出され、それらの精密質量は「1352.41」、「1587.52」、「2439.83」、「3125.12」、「871.30」、「2516.88」、及び「2596.96」と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号35〜41で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「トランスサイレチン」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第7表に示す。既報のラットトランスサイレチンのアミノ酸配列を配列番号8に示す。
【0134】
【表7】

【0135】
上述したように、トランスサイレチンについては、その唯一のCys残基が修飾を受けた種々の修飾トランスサイレチンが見出されている。マーカー物質(A08)、(A09)の各電荷/質量比(平均値:13733,13922)から、マーカー物質(A08)は「システイニル化トランスサイレチン」、マーカー物質(A09)は「グルタチオン化トランスサイレチン」とそれぞれ同定された。
【実施例9】
【0136】
マーカー物質(A11)の精製と同定
実施例8で行ったカラム非吸着画分に対するSELDI−TOF−MS分析で、マーカー物質(A11)の質量/電荷比(平均値:21383)と同等の質量/電荷比を示すピークを確認した。
【0137】
実施例8で行ったSDS−PAGEで分離された約21.4kDaのバンド(図24の矢印b)を切り出してタンパク質を抽出し、SELDI−TOF−MS分析を行い、マーカー物質(A11)と同等の質量/電荷比を示すピークを確認した(図26)。
【0138】
あらためて同様のSDS−PAGEを行って約21.4kDaのバンドを切り出し、実施例2と同様にしてゲル内消化及び質量分析を行ったところ、少なくとも6個のピークが検出され、それらの精密質量は「1262.49」、「1654.61」、「938.30」、「825.35」、「2635.86」、及び「803.37」、と算出された。これらのデータを元に実施例2と同様にしてペプチドマスフィンガープリンティングを行ったところ、これらのペプチドはそれぞれ配列番号42〜47で表わされるアミノ酸配列のペプチドと一致し、目的のタンパク質は99%以上の確率で「アポリポタンパク質M」と同定された。各ペプチドの精密質量、アミノ酸配列、及び配列番号の対応関係を第8表に示す。既報のラットアポリポタンパク質Mのアミノ酸配列を配列番号9に示す。
【0139】
【表8】

【特許請求の範囲】
【請求項1】
被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法。
(A01)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約4610のイオンピークを生じるタンパク質、
(A02)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約5500のイオンピークを生じるタンパク質、
(A03)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約7050のイオンピークを生じるタンパク質、
(A04)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8330のイオンピークを生じるタンパク質、
(A05)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8840のイオンピークを生じるタンパク質、
(A06)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8930のイオンピークを生じるタンパク質、
(A07)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約9070のイオンピークを生じるタンパク質、
(A08)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約11600のイオンピークを生じるタンパク質、
(A09)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13700のイオンピークを生じるタンパク質、
(A10)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13900のイオンピークを生じるタンパク質、
(A11)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約21400のイオンピークを生じるタンパク質。
【請求項2】
下記(a)〜(i)の少なくとも1つを満たすことを特徴とする請求項1に記載の内臓脂肪増加抑制効果の評価方法。
(a)マーカー物質(A03)はアポリポタンパク質C1又はその修飾体である、
(b)マーカー物質(A04)はアポリポタンパク質C2又はその修飾体である、
(c)マーカー物質(A05)はアポリポタンパク質A2又はその修飾体である、
(d)マーカー物質(A06)はアポリポタンパク質C3又はその修飾体である、
(e)マーカー物質(A07)は補体C3又はその修飾体である、
(f)マーカー物質(A08)はβ2−ミクログロブリン又はその修飾体である、
(g)マーカー物質(A09)はトランスサイレチン又はその修飾体である、
(h)マーカー物質(A10)はトランスサイレチン又はその修飾体である、
(i)マーカー物質(A11)はアポリポタンパク質M又はその修飾体である。
【請求項3】
被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法。
(B1)アポリポタンパク質C1又はその修飾体、
(B2)アポリポタンパク質C2又はその修飾体、
(B3)アポリポタンパク質A2又はその修飾体、
(B4)アポリポタンパク質C3又はその修飾体、
(B5)補体C3又はその修飾体、
(B6)β2−ミクログロブリン又はその修飾体、
(B7)トランスサイレチン又はその修飾体、
(B8)アポリポタンパク質M又はその修飾体。
【請求項4】
前記動物は、被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物であることを特徴とする請求項1〜3のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項5】
前記体液は、血液であることを特徴とする請求項1〜4のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項6】
前記被験物質は、食品素材であることを特徴とする請求項1〜5のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項7】
前記体液又は体液成分を、前記マーカー物質に対する親和性を有する物質を固定化した担体に接触させて、体液中の前記マーカー物質を担体上に捕捉し、捕捉された前記マーカー物質の量に基づいて体液中の前記マーカー物質の濃度を算出することを特徴とする請求項1〜6のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項8】
前記担体は平面部分を有し、前記マーカー物質に対する親和性を有する物質は、該平面部分の一部に固定化されていることを特徴とする請求項7に記載の内臓脂肪増加抑制効果の評価方法。
【請求項9】
前記マーカー物質に対する親和性を有する物質は、イオン交換体又は抗体であることを特徴とする請求項7又は8に記載の内臓脂肪増加抑制効果の評価方法。
【請求項10】
請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法によって被験物質を評価し、所望の内臓脂肪増加抑制効果を有する物質をスクリーニングすることを特徴とする物質のスクリーニング方法。
【請求項11】
請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法に用いるためのキットであって、前記マーカー物質に対する親和性を有する物質を固定化した担体を含むことを特徴とする内臓脂肪増加抑制効果の評価用キット。
【請求項12】
前記マーカー物質に対する親和性を有する物質は、イオン交換体であることを特徴とする請求項11に記載の内臓脂肪増加抑制効果の評価用キット。
【請求項13】
所望の内臓脂肪増加抑制効果を有する物質をスクリーニングするために使用されることを特徴とする請求項11又は12に記載の内臓脂肪増加抑制効果の評価用キット。
【請求項1】
被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記マーカー物質(A01)〜(A11)の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法。
(A01)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約4610のイオンピークを生じるタンパク質、
(A02)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約5500のイオンピークを生じるタンパク質、
(A03)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約7050のイオンピークを生じるタンパク質、
(A04)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8330のイオンピークを生じるタンパク質、
(A05)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8840のイオンピークを生じるタンパク質、
(A06)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約8930のイオンピークを生じるタンパク質、
(A07)pH3.0で弱陽イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約9070のイオンピークを生じるタンパク質、
(A08)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約11600のイオンピークを生じるタンパク質、
(A09)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13700のイオンピークを生じるタンパク質、
(A10)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約13900のイオンピークを生じるタンパク質、
(A11)pH9.0で強陰イオン交換体に結合し、かつ質量分析に供すると質量/電荷比が約21400のイオンピークを生じるタンパク質。
【請求項2】
下記(a)〜(i)の少なくとも1つを満たすことを特徴とする請求項1に記載の内臓脂肪増加抑制効果の評価方法。
(a)マーカー物質(A03)はアポリポタンパク質C1又はその修飾体である、
(b)マーカー物質(A04)はアポリポタンパク質C2又はその修飾体である、
(c)マーカー物質(A05)はアポリポタンパク質A2又はその修飾体である、
(d)マーカー物質(A06)はアポリポタンパク質C3又はその修飾体である、
(e)マーカー物質(A07)は補体C3又はその修飾体である、
(f)マーカー物質(A08)はβ2−ミクログロブリン又はその修飾体である、
(g)マーカー物質(A09)はトランスサイレチン又はその修飾体である、
(h)マーカー物質(A10)はトランスサイレチン又はその修飾体である、
(i)マーカー物質(A11)はアポリポタンパク質M又はその修飾体である。
【請求項3】
被験物質を投与された内臓脂肪型肥満を発症している又は発症し得る動物の体液中における下記(B1)〜(B8)のいずれかに属するマーカー物質の少なくとも1つの濃度を基準値と比較し、被験物質が有する内臓脂肪増加抑制効果を評価することを特徴とする内臓脂肪増加抑制効果の評価方法。
(B1)アポリポタンパク質C1又はその修飾体、
(B2)アポリポタンパク質C2又はその修飾体、
(B3)アポリポタンパク質A2又はその修飾体、
(B4)アポリポタンパク質C3又はその修飾体、
(B5)補体C3又はその修飾体、
(B6)β2−ミクログロブリン又はその修飾体、
(B7)トランスサイレチン又はその修飾体、
(B8)アポリポタンパク質M又はその修飾体。
【請求項4】
前記動物は、被験物質を摂取させると共に低繊維高脂肪食を摂取させた動物であることを特徴とする請求項1〜3のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項5】
前記体液は、血液であることを特徴とする請求項1〜4のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項6】
前記被験物質は、食品素材であることを特徴とする請求項1〜5のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項7】
前記体液又は体液成分を、前記マーカー物質に対する親和性を有する物質を固定化した担体に接触させて、体液中の前記マーカー物質を担体上に捕捉し、捕捉された前記マーカー物質の量に基づいて体液中の前記マーカー物質の濃度を算出することを特徴とする請求項1〜6のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法。
【請求項8】
前記担体は平面部分を有し、前記マーカー物質に対する親和性を有する物質は、該平面部分の一部に固定化されていることを特徴とする請求項7に記載の内臓脂肪増加抑制効果の評価方法。
【請求項9】
前記マーカー物質に対する親和性を有する物質は、イオン交換体又は抗体であることを特徴とする請求項7又は8に記載の内臓脂肪増加抑制効果の評価方法。
【請求項10】
請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法によって被験物質を評価し、所望の内臓脂肪増加抑制効果を有する物質をスクリーニングすることを特徴とする物質のスクリーニング方法。
【請求項11】
請求項1〜9のいずれか1項に記載の内臓脂肪増加抑制効果の評価方法に用いるためのキットであって、前記マーカー物質に対する親和性を有する物質を固定化した担体を含むことを特徴とする内臓脂肪増加抑制効果の評価用キット。
【請求項12】
前記マーカー物質に対する親和性を有する物質は、イオン交換体であることを特徴とする請求項11に記載の内臓脂肪増加抑制効果の評価用キット。
【請求項13】
所望の内臓脂肪増加抑制効果を有する物質をスクリーニングするために使用されることを特徴とする請求項11又は12に記載の内臓脂肪増加抑制効果の評価用キット。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図16】


【図18】


【図19】


【図20】


【図22】


【図23】


【図25】


【図26】


【図15】


【図17】


【図21】


【図24】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図16】


【図18】


【図19】


【図20】


【図22】


【図23】


【図25】


【図26】


【図15】


【図17】


【図21】


【図24】


【公開番号】特開2010−133947(P2010−133947A)
【公開日】平成22年6月17日(2010.6.17)
【国際特許分類】
【出願番号】特願2009−253628(P2009−253628)
【出願日】平成21年11月5日(2009.11.5)
【出願人】(303058708)株式会社バイオマーカーサイエンス (27)
【出願人】(596156174)
【Fターム(参考)】
【公開日】平成22年6月17日(2010.6.17)
【国際特許分類】
【出願日】平成21年11月5日(2009.11.5)
【出願人】(303058708)株式会社バイオマーカーサイエンス (27)
【出願人】(596156174)

【Fターム(参考)】
[ Back to top ]

