内部に空洞を有するナノ粒子分散微小ガラスビーズ及びその製造方法
【課題】本発明は、内部に空洞を有する微小なケイ素系ガラスビーズであって、ガラス相にナノ粒子を含むケイ素系ガラスビーズ及びその製造方法を提供する。さらに、該ガラスビーズ内部の空洞に、ガラス相中のナノ粒子と同一又は異なる種類のナノ粒子や医薬品分子等の機能性物質(蛍光、磁性、薬効等を有する物質等)を含むケイ素系ガラスビーズ及びその製造方法を提供する。
【解決手段】内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであって、該ケイ素系ガラス相にナノ粒子Aを含むことを特徴とするケイ素系ガラスビーズ、さらに前記ケイ素系ガラスビーズ内部の空洞に機能性物質を含むガラスビーズに関する。
【解決手段】内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであって、該ケイ素系ガラス相にナノ粒子Aを含むことを特徴とするケイ素系ガラスビーズ、さらに前記ケイ素系ガラスビーズ内部の空洞に機能性物質を含むガラスビーズに関する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、内部に空洞を有しガラス相にナノ粒子が分散した微小ガラスビーズ、及びその製造方法に関する。
【0002】
なお、本願明細書では、ゾル−ゲル法を用いて作製したケイ素を含有するマトリックスを「ケイ素系ガラス」と呼ぶ。該ケイ素系ガラスは、一般にエックス線回折で明確なピークを生じない。また、本発明は、微小な(直径が1μm程度以下)概略球形のケイ素系ガラス粒子を対象としており、これを「ケイ素系ガラスビーズ」と呼ぶ。
【背景技術】
【0003】
ガラスは、耐薬品性、機械的特性において高分子より優れており、また、紫外線に対する耐性も良好なので、種々の機能を持つナノ粒子や有機分子を担持するマトリックスとして有用である。
【0004】
このガラスをマトリックスとした微小ビーズについては、多くの研究開発が行われてきており、ケイ素系のガラスをゾル−ゲル法によって作製する方法が数多く報告されている。このとき、アルカリ性条件で、かつ、熱処理温度が低い条件でガラスビーズを作製する場合には、酸化ケイ素の網目状構造の発達が不十分となり、ときには有機物を多く含んだり、1nm程度の微小なシリカ球の集まりとなることがある。
【0005】
このようなケイ素系ガラスビーズですでに製品化されているものとしては、鈴木油脂工業(株)の「無機質球状微粒子」(商品名:ゴッドボール)がある。このガラスビーズには、クロマトグラフィー用の充填剤、化粧用のパウダーなどの用途がある。また、作製法によりビーズの中心付近に中空の構造を作製することができる。この中空部分を有するガラスビーズは、薬品の担持および徐放が可能なのでドラッグデリバリーに用いられる。これらケイ素系ガラスビーズは、多くの場合、粒径1〜100μm程度であり、1μm以下では粒径や中空のコア径の制御が難しくなる。
【0006】
また、特許文献1には、球状粒子の殻の部分(直径0.2〜100μm程度)にマクロ孔(直径60nm〜30μm)を有するケイ素系の殻から構成される中空粒子、とその作製法が記されている。これに関連して、詳細な該中空粒子の作製法が非特許文献1に示されている。
【0007】
一方で、ケイ素系ガラスビーズ中に、ナノ粒子を担持させる研究も進んでいる。ナノ粒子とは、直径2〜20nm程度の大きさの粒子であり、表面積の割合が大きいので注意しないと直ぐに凝集してさまざまな機能を失ってしまうことが多い。このため、適切なマトリックスに担持することが不可欠である。
【0008】
近年、このナノ粒子として半導体ナノ粒子の研究が盛んである。この半導体ナノ粒子は、主にII−VI族またはIII−V族の化合物半導体からなる。これらの半導体ナノ粒子は溶
液法によって作製され、表面の欠陥を除去したものは新しいタイプの蛍光体として知られている。これら半導体ナノ粒子は、いわゆる量子サイズ効果により、同じ材料でできていても粒径が小さくなるほどバンドギャップが広がって短波長側の発光を示すようになる。他に、磁性を示すナノ粒子や金属性のナノ粒子が知られている。
【0009】
特許文献2には、直径数十nmのケイ素系ガラスビーズ中に作製した空隙に、半導体ナノ粒子を含有した構造体、及びその作製方法が記されている。
【0010】
また、本発明者らは、発光する半導体ナノ粒子を分散させたケイ素系ガラスビーズとその作製法について、特許文献3(逆ミセル法)、特許文献4(ストーバー法)、特許文献5(逆ミセル法の改良)に示すように、技術を積み上げてきた。この技術を用いれば、半導体ナノ粒子を発光効率の低下を抑えつつ複数個、およそ直径30nmから1μm程度のガラスビーズに分散させることができる。しかし、いずれの場合もガラスビーズの中に1種類のナノ粒子を分散させる手法である。
【0011】
ガラスビーズ中に1種類のナノ粒子だけでなく、複数の他の種類のナノ粒子や、医薬品分子等の機能性物質を含有させることで、様々な特性を持ったガラスビーズを得ることができる。このような多機能のガラスビーズ作製を狙ったものとして、非特許文献2がある。これには、半導体ナノ粒子と磁性ナノ粒子が同じガラスビーズ中に分散した、蛍光特性と磁性の両方を示すガラスビーズが作製できることが記載されている。
【0012】
このガラスビーズで用いられる半導体ナノ粒子の作製法は、既報の非特許文献3により作製されたとされているが、非特許文献2では該半導体ナノ粒子の発光効率については触れられていない。そこで、非特許文献2で報告されている発光の半値幅(半値全幅(FWHM))を測定すると、赤色発光の場合は65nmと広いため、非特許文献2では、非特許文献3に書かれているサイズ選択処理を行っていないと判定される。この場合には、発光効率は10%の程度である。さらに、磁性粒子と一緒にガラスビーズに導入すると、半値幅が広がり発光のベースラインが大幅に上昇していることから大幅に発光効率が減少したと判断される。
【0013】
一般に、発光するナノ粒子と磁性ナノ粒子を混ぜると、相互作用により発光効率が低下する。例えば、酸化鉄ナノ粒子はプラスに帯電しており、他方、水分散性の多くの半導体ナノ粒子はマイナスに帯電している。このため、ガラスビーズ中に同時に分散させようとして両者を混ぜると、直ぐに凝集体を生じる。
【0014】
また、一般にナノ粒子は、溶液中で周りのイオンと微妙なバランスの上で分散を保っている。このため、他の化学種が加えられるとそのバランスが崩れて、凝集や表面の劣化を伴うことが多い。これを防ぐためには、ナノ粒子と磁性粒子や医薬品分子などを微小なガラスビーズ内の別の領域に閉じ込めることが有効であるが、そのような方法は知られていなかった。
【先行技術文献】
【特許文献】
【0015】
【特許文献1】特開2007−230794号公報
【特許文献2】特開2007−105873号公報
【特許文献3】特許3677538号公報
【特許文献4】特許3755033号公報
【特許文献5】国際公開第2007/034877号パンフレット
【非特許文献】
【0016】
【非特許文献1】藤原他、ケミストリー オブ マテリアルズ、16巻、5420ページ(2004年)
【非特許文献2】ヴェロニカ サルグエリノ−マセイラ他、アドバンスト ファンクショナル マテリアルズ、16巻、509ページ(2006年)
【非特許文献3】ガポーニック他、ジャーナル オブ フィジカルケミストリー ビー、106巻、7177ページ(2002年)
【発明の概要】
【発明が解決しようとする課題】
【0017】
本発明は、上記した如き従来技術の現状に鑑みてなされたものであり、その主な目的は、内部に空洞を有する微小なケイ素系ガラスビーズであって、該ガラスビーズ中の空洞ではない部分(以下、「ガラス相」とも記載する。)にナノ粒子を含むケイ素系ガラスビーズ及びその製造方法を提供することにある。さらに、該ガラスビーズ内部の空洞(ケイ素を含まない部分)に、ガラス相中のナノ粒子と同一又は異なる種類のナノ粒子や医薬品分子等の機能性物質を含むケイ素系ガラスビーズ及びその製造方法を提供することにある。
【課題を解決するための手段】
【0018】
従来の逆ミセル法によるナノ粒子分散ケイ素系ガラスビーズの作製法(特許文献5)は、例えば図1に示される。この逆ミセル法では、疎水性有機溶媒と界面活性剤を含む媒体と、一部が加水分解したケイ素アルコキシドを含むナノ粒子分散水溶液とを混合することにより逆ミセル溶液(W/O型エマルション)を形成する。該逆ミセルの内部の水相に該ナノ粒子分散水溶液が包含される。この逆ミセル溶液にケイ素アルコキシドを添加すると、該アルコキシドは一旦油相に分散され、その後水相に触れることで徐々に加水分解し親水性が増して水相に移動し、そこでゾル−ゲル反応が進行して固化しガラスビーズとなる。このとき、逆ミセルの水相に含まれるナノ粒子も同時にガラス中に取り込まれて、ガラスビーズ中に分散する。
【0019】
しかし、この方法では、ナノ粒子に加えて他のナノ粒子や磁性粒子や医薬品分子などの機能性物質を、微小なガラスビーズ内に導入することは困難である。
【0020】
本発明者は、上記した課題を解決すべく鋭意研究を重ねてきた。その結果、逆ミセル法を用いて半導体ナノ粒子が分散したケイ素系ガラスビーズを形成する過程で、疎水性有機溶媒(シクロヘキサン等)と界面活性剤を含む媒体に、一部加水分解したケイ素アルコキシドとナノ粒子Aを含む水溶液を加えて撹拌し逆ミセル溶液(W/O型エマルション)を形成し、これに機能性物質を含む所定pHのアルカリ性水溶液を加えて撹拌することにより、内部に空洞を有するケイ素系ガラスビーズであって、ガラス相にナノ粒子Aを含み、空洞に機能性物質を含むケイ素系ガラスビーズが得られることを見いだした。しかも、ナノ粒子A及び機能性物質は、その特性を保持したままガラスビーズ内に導入されていることを確認した。
【0021】
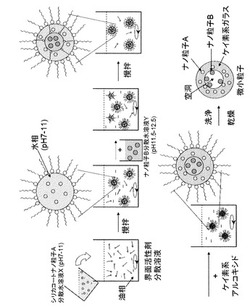
具体的には、本発明の方法では、図2のように、油相に界面活性剤を分散した溶液に、一部が加水分解したケイ素アルコキシドとナノ粒子Aを含む水溶液Xを加えて、該水溶液Xを内包する微小な逆ミセル溶液(W/O型エマルション)を形成する。その溶液に、機能性物質を含むアルカリ性水溶液Yを添加すると、該水溶液Yは一旦、油相中に分散し、やがて一部が水玉となって微小な逆ミセル内の水相(水溶液X)に移動する。
【0022】
このとき、ナノ粒子Aを含む水溶液Xの水素イオン指数をpH1と表し、機能性物質を含む水溶液Yの水素イオン指数をpH2と表した場合に、pH1とpH2の関係を、7<pH1<pH2<14にすることにより、内部に空洞を有するケイ素系ガラスビーズを形成することができる。
【0023】
これは、微小な逆ミセル内の水相(水溶液X)に、アルカリ性の高い水溶液Yの水玉が
入ると、水溶液Yの水玉に接する水溶液Xの表面で急激にゾル−ゲル反応が進行し、逆ミセルの中に水玉の形を保ったままガラスの殻が形成される。これを乾燥することにより内部に空洞を有するケイ素系ガラスビーズが形成されると考えられる。また、必要に応じ、上記逆ミセル溶液にさらにケイ素アルコキシドを添加することができ、これによりゾル−ゲル反応が促進される。
【0024】
このようにして、水溶液Xに含まれるナノ粒子Aはガラス相中に分散・固定され、水溶液Yの水玉中に含まれる機能性物質は空洞の領域に導入される。その結果、ナノ粒子Aと機能性物質は1つのガラスビーズ中で別々の領域に閉じ込められることになる。
【0025】
この方法の利点は、1種類のナノ粒子Aをケイ素系ガラスビーズのガラス相に分散させ、もう1種類の機能性物質を該ガラスビーズ中の空洞(ケイ素を含まない部分)に分散できることである。本発明のケイ素系ガラスビーズは、機能性物質が空洞の内表面に沿って分散し、ガラスビーズの中心部分に空洞を残している場合や、機能性物質が空洞に充填されている場合も含む。この方法では、ナノ粒子Aと機能性物質が直接触れ合うことがないため、分散させる前のナノ粒子Aと機能性物質の特性(蛍光特性や磁性、薬効など)を保持したガラスビーズが作製できる。
【0026】
即ち、本発明のケイ素系ガラスビーズは内部に空洞を有し、ガラス相にナノ粒子Aを含み、且つ、空洞部分にも機能性物質を含ませることができるので、含有されるナノ粒子A及び機能性物質の機能を併せ持った微小なガラスビーズの作製が可能になる。つまり、1つのガラスビーズに複数の機能を持たせたガラスビーズを提供することができる。
【0027】
本発明は、以下のケイ素系ガラスビーズ及びその製造方法を提供する。
【0028】
項1 内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであって、該ケイ素系ガラス相にナノ粒子Aを含むことを特徴とするケイ素系ガラスビーズ。
【0029】
項2 さらに前記ケイ素系ガラスビーズ内部の空洞に機能性物質を含む項1に記載のケイ素系ガラスビーズ。
【0030】
項3 前記機能性物質がナノ粒子Bである項2に記載のケイ素系ガラスビーズ。
【0031】
項4 前記ナノ粒子A及びナノ粒子Bの平均粒径がそれぞれ2〜20nmである項3に記載のケイ素系ガラスビーズ。
【0032】
項5 前記ナノ粒子A及び/又はナノ粒子Bが半導体ナノ粒子である項3又は4に記載のケイ素系ガラスビーズ。
【0033】
項6 前記ナノ粒子A及び/又はナノ粒子Bが、発光効率が20%以上の半導体ナノ粒子である項3〜5のいずれかに記載のケイ素系ガラスビーズ。
【0034】
項7 前記半導体ナノ粒子が、CdTe、CdSe、CdS、ZnSe、ZnSe(1-x)Tex (但し、0 < x <
1)、ZnS、InP、InxGa(1-x)P (但し、0 < x < 1)、及びInAsからなる群より選ばれる少なくとも1種である項5又は6に記載のケイ素系ガラスビーズ。
【0035】
項8 前記ナノ粒子A及び/又はナノ粒子Bが磁性を有するナノ粒子である項3〜7のいずれかに記載のケイ素系ガラスビーズ。
【0036】
項9 前記磁性を有するナノ粒子が、Fe3O4、Fe2O3、CoFe2O4、MnFe2O4、NiFe2O4、CoCrFeO4、Pt、Co、PtCo、FePt、及びFeCoからなる群より選ばれる少なくとも1種である項
8に記載のケイ素系ガラスビーズ。
【0037】
項10 印加磁界5kOeでの磁化が1〜200emu/gである、項8又は9に記載の
ケイ素系ガラスビーズ。
【0038】
項11 前記ナノ粒子A及び/又はナノ粒子Bが金属ナノ粒子である項3〜10のいずれかに記載のケイ素系ガラスビーズ。
【0039】
項12 前記金属ナノ粒子の金属が、金(Au)、銀(Ag)及び銅(Cu)からなる群より選ばれる少なくとも1種である項11に記載のケイ素系ガラスビーズ。
【0040】
項13 前記ケイ素系ガラスビーズ内の空洞の平均内径が10〜500nmである請求項1〜12のいずれかに記載のケイ素系ガラスビーズ。
【0041】
項14 前記機能性物質が薬理活性物質である項2〜13のいずれかに記載のケイ素系ガラスビーズ。
【0042】
項15 前記ケイ素系ガラスビーズの外表面に抗体が接着されてなる項1〜14のいずれかに記載のケイ素系ガラスビーズ。
【0043】
項16 内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであり、該ケイ素系ガラス相にナノ粒子Aを含むケイ素系ガラスビーズの製造方法であって、
(1)疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する工程、及び
(2)上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する工程、
を含む製造方法。
【0044】
項17 前記工程(2)において、アルカリ性水溶液Yが機能性物質を含む項16に記載の製造方法。
【0045】
項18 前記工程(1)のナノ粒子Aを含むケイ素アルコキシド水溶液Xの水素イオン
指数(pH1)がpH1>7であり、かつ、前記工程(2)のアルカリ性水溶液Yの水素イオン指数(pH2)がpH1<pH2<14である項16又は17に記載の製造方法。
【0046】
項19 前記工程(2)が、前記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加した後、さらにケイ素アルコキシドを添加してケイ素系ガラスビーズを形成する工程である項16〜18のいずれかに記載の製造方法。
【0047】
項20 前記項1〜15のいずれかに記載のケイ素系ガラスビーズを含む蛍光試薬。
【0048】
項21 前記項1〜15のいずれかに記載のケイ素系ガラスビーズを含む薬物運搬システム。
【発明の効果】
【0049】
本発明の内部に空洞を有するケイ素系ガラスビーズは、ガラス相にナノ粒子A(例えば、半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)を分散しており、かつ該空洞部分にナノ粒子B(例えば、半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)、薬理活性物質等の機能性物質を担持することができる。該ガラスビーズの合成時に、これらナノ粒子Aと機能性物質の両者が交じり合うことがないので、蛍光性、磁性、薬効など、それぞれの物質の特性を保持したガラスビーズが作製できる。換言すれば、それぞれの物質の特性を同時に発揮するガラスビーズが作製できる。
【0050】
また、ガラスは機械的、化学的特性に優れているので、このガラスビーズは、経時安定
性にも優れている。このため、蛍光試薬、抗原採集、ドラッグデリバリー(人体内での薬物輸送)などの用途に用いることができる。
【図面の簡単な説明】
【0051】
【図1】従来のナノ粒子分散ガラスビーズの作製法の概略を示す図。
【図2】本願発明における空洞を有するナノ粒子分散ガラスビーズの作製法の概略を示す図。この図の場合は、空洞部分にナノ粒子Bを分散させている。
【図3】(a)空洞を含むCdTeナノ粒子分散ガラスビーズ(粒径約160nm)の高角度散乱暗視野法(ハーディフステム、HAADF-STEM)による撮影像。(b)空洞を含むCdTeナノ粒子分散ガラスビーズ(粒径約900nm)の透過電子顕微鏡(TEM)による撮影像。
【図4】CdTeナノ粒子のコロイド溶液と、それを水中のガラスビーズ中に分散させたときの吸収・蛍光スペクトル。
【図5】CdTeナノ粒子を分散したガラスビーズにさらにアビジンを取り付けたときの吸収・蛍光スペクトル。
【図6】磁性ナノ粒子(Fe3O4ナノ粒子)が空洞部分に分散したCdTeナノ粒子分散ガラスビーズの透過電子顕微鏡写真。
【図7】蛍光ナノ粒子(CdTe)と磁性ナノ粒子(Fe3O4)とを分散したガラスビーズのX線回折スペクトル。
【図8】(a)蛍光ナノ粒子(CdTe)と磁性ナノ粒子(Fe3O4)とを分散したガラスビーズの磁気ヒステリシス曲線。(b)磁性ナノ粒子(Fe3O4)単体の磁気ヒステリシス曲線。
【発明を実施するための形態】
【0052】
本発明の内部に空洞を有するケイ素系ガラスビーズは、ガラス相にナノ粒子A(半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)を分散含有しており、かつ該空洞部分に機能性物質を担持することができる。該機能性物質としては、例えばナノ粒子B(半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)、薬理活性物質等が挙げられる。なお、ナノ粒子Aとナノ粒子Bは同一種でも異なる種であってもよい。
【0053】
以下、ガラス相及び/又は空洞部分に導入できるナノ粒子A及びB(半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)並びにその製法について説明し、さらに、ガラス相にナノ粒子Aを含み、空洞部分に該機能性物質(ナノ粒子B、薬理活性物質等)を含むケイ素系ガラスビーズ及びその製法について説明する。
【0054】
1.ナノ粒子の製造方法
ナノ粒子A及びBとして用いられるナノ粒子について以下説明する。該ナノ粒子としては、半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等が挙げられる。
【0055】
1.1 半導体ナノ粒子
半導体ナノ粒子は、II-VI族およびIII-V族がよく知られており、以下に本発明に用いるための作製法を説明する。高い蛍光強度を得るために、作製法が工夫されている。
【0056】
ケイ素系ガラスビーズに含まれるナノ粒子A及びBは、アルカリ水溶液中で安定な半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等を使用するのが好ましい。半導体ナノ粒子は、蛍光性を有するものを用いることが好ましい。
【0057】
(1)II-VI族半導体ナノ粒子
II-VI族半導体ナノ粒子については、可視および赤外領域で発光するもの、例えば、CdTe、CdSe、CdS、ZnSe、ZnSe(1-x)Tex(但し、0 < x < 1)、ZnSなどの半導体ナノ粒子を例示することができ、他にPbS、PbSeなどが挙げられる。これらは皆、以下に説明する公知の
方法で製造できる。
【0058】
水溶液を用いる製造方法として、例えば、II族元素を含む水溶性化合物及び界面活性剤を溶解したアルカリ性水溶液中に、不活性雰囲気下において、VI族元素化合物を導入することによって、II-VI族半導体ナノ粒子を得ることができる。VI族元素化合物は、気体状
のものを用いることもできる。
【0059】
この方法において、II族元素を含む水溶性化合物としては、過塩素酸塩が好ましく、例えば、II族元素がカドミウムである場合には、過塩素酸カドミウムを用いることができる。
【0060】
界面活性剤としては、疎水基であるチオール基と親水基を有するものが好ましい。親水基としては、カルボキシル基などのアニオン性基、アミノ基などのカチオン性基、水酸基などを例示できるが、特に、カルボキシル基などのアニオン性基が好ましい。界面活性剤の具体例としては、チオグリコール酸、チオグリセロール、メルカプトエチルアミン等を例示できる。
【0061】
VI族元素化合物としては、例えばVI族元素の水素化物などを用いることができ、VI族元素がテルルである場合には、テルル化水素を用いることができる。その他、テルル化水素を水酸化ナトリウムと反応させて得られるテルル化水素ナトリウムを水溶液として導入することも可能である。
【0062】
合成時、ナノ粒子作製時に用いる界面活性剤の使用量を、水溶液中に含まれるII族元素に対して、モル比で1〜1.5程度とすると高い発光効率が得られる。
【0063】
不活性雰囲気としては、反応に関与しない気体の雰囲気であればよく、例えば、アルゴンガス、窒素ガス等の不活性ガス雰囲気を好適に利用できる。
【0064】
上記反応は、通常、室温(例えば、10〜30℃程度)において行うことができる。アルカリ性水溶液のpHは、10〜12程度、特に10.5〜11.5であることが好ましい。反応は、通常、VI族化合物を導入後、10分程度以内に終了する。
【0065】
上記した方法で得られる半導体ナノ粒子の粒径は、ナノメートルオーダーであり、多くの場合2〜20nmである。上記した方法で半導体ナノ粒子を作製した後、還流を行うことによって、該ナノ粒子の粒径を制御することが可能であり、還流時間を長くすると、粒径を大きくすることができる。
【0066】
特にCdTeナノ粒子の場合には、文献(村瀬ら、ケミストリー レターズ、34巻、92ページ、2005年)に作製法が説明されている。また、ZnSe系ナノ粒子の場合は、文献(村瀬ら、ジャーナル オブ コロイド アンド インターフェイス サイエンス、321巻、468ページ(2008年))に作製法が説明されている。
【0067】
一方、有機溶液を用いる製造方法として、例えば、トリオクチルフォスフィンやその酸化物を含む溶液にII族元素の化合物を添加して、さらにVI族元素を加える方法が知られている。CdSeは、この方法で作製される最も良く知られたナノ粒子である。用いる溶媒や、II族元素化合物の違いにより、さらに下記のようにいくつかの報告例が知られている。
・タラピンら、ナノ レターズ、1巻、207ページ(2001年)
・ペンら、ジャーナル オブ アメリカン ケミカル ソサエティー、123巻、1389ページ(2001年)
・バベンディーら、ジャーナル オブ フィジカル ケミストリー ビー、101巻、9
463ページ(1997年)
・ペンら、ジャーナル オブ アメリカン ケミカル ソサエティー、124巻、2049ページ(2002年)
・ゾンら、ジャーナル オブ フィジカル ケミストリー シー、111巻、526ページ(2007年)
【0068】
(2)III-V族半導体ナノ粒子
III-V族半導体ナノ粒子としては、アルカリ性水溶液中で発光効率の高いものが好適で
あり、例えば、InP、InxGa(1-x)P(但し、0 < x < 1)、及びInAs等の半導体ナノ粒子を例
示することができる。好ましくは、コアとしてIII-V族半導体ナノ粒子を有し、その表面
にII−VI族半導体の層が付加されたコア/シェル構造を有するナノ粒子が例示される。その作製方法として以下の方法が例示される。
【0069】
(a)コアの作製
公知の文献(村瀬ら、ケミストリー レターズ、37巻、856ページ(2008年))に例示されるように、2種のV族原子が直接に結合した部分構造を持つ化合物をV族元素の供給源とし、さらにソルボサーマル法(耐圧容器に溶媒を入れ、その溶媒の沸点以上の温度にして目的物を合成する手法)を用いることでIII−V族半導体のナノ粒子を比較
的低温で合成する。ソルボサーマル法の温度は、100〜300℃程度、より好ましくは、120〜200℃程度、さらに150〜180℃程度が好ましい。
【0070】
このような2種のV族原子が直接に結合した部分構造を持つ化合物として、好適には、V族原子と窒素原子とが直接に結合した部分構造を持つ化合物が挙げられ、具体的には、一般式(1):
【0071】
【化1】

【0072】
(式中、MはV族元素であり、R1、R2及びR3は同一又は異なって、メチル基、エチル基、n−プロピル基、イソプロピル基、ブチル基、tert−ブチル基等の低級アルキル基である。mは0〜2の整数であり、nは1〜3の整数であって、m+n=3である。)
で表される化合物を例示できる。
【0073】
Mで示されるV族元素としては、P、As、Sb、Bi等が挙げられ、好ましくはPである。R1、R2及びR3で示される低級アルキル基としては、C1−3のアルキル基が好ましく、メチル基がより好ましい。nは3が好ましい。
【0074】
上記一般式で表される化合物の具体例としては、下記(2)〜(7)で表される化合物を挙げることができる。
【0075】
【化2】

【0076】
(式中、M、R1、R2及びR3は前記に同じ。)
上記化合物のうち、(2)、(3)及び(5)で表される化合物が好ましい。R1、R2及びR3はそれぞれ、メチル基であることが好ましい。
【0077】
III族元素の供給源としては、特に限定されないが、In,Ga,Al等のIII族金属、その塩化物、酸化物、硝酸化物、酢酸化物などが例示される。III族元素は一種又は二種
以上混合して用いることができる。具体的なIII族元素化合物としては、InCl3、In2O3、In(OOCCH3)3、AlCl3、Al(NO3)3・9H2O、GaCl3、Ga(NO3)3・nH2Oが挙げられ、好ましくは、InCl3、AlCl3、GaCl3である。
【0078】
溶媒としては、トルエン、クロロホルムなどの疎水性の有機溶媒が例示される。
【0079】
この方法により合成したナノ粒子にアルコールなどの貧溶媒を加えることにより容易にサイズ分布の狭いナノ粒子を得ることができる(サイズ選択的沈降法)。このサイズ選択的沈降法とは、良溶媒に分散しているナノ粒子に、アルコールなどの貧溶媒を徐々に加えていくことで、溶解度の低いナノ粒子(通常は大きなサイズのナノ粒子)から溶解度の順に徐々に沈殿させて分級する手法である。このときの粒径は、1.5〜6nm程度であることが多い。得られたIII-V族半導体ナノ粒子の発光効率を上げるために、この粒子(コ
ア)の表面にさらに以下に記述する方法でシェル層をつける。
【0080】
(b)コア/シェル構造の作製
(b−i)混合液の調製
上記で得られたIII-V族半導体ナノ粒子(コア)を含有する有機溶媒分散液を、II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液に接触させる。この際、水相には界面活性剤を分散させておく。この界面活性剤としては、VI族元素を含む水分散性の分子を用いるのが好都合である。その一例として、チオグリコール酸が挙げられる。この場合は、分子の一端の硫黄原子がナノ粒子の表面に接着し、分子の他端のカルボキシル基が中性からアルカリ性の領域でイオン化して、ナノ粒子の水中での安定分散に寄与する。このとき、界面活性剤に加えて、他のVI族元素を含む化合物を添加しても良い。
【0081】
この工程により、III-V族半導体ナノ粒子の表面にあるIII族およびV族イオンの一部
の脱離反応が起きて、水溶液中のII族およびVI族イオンと置換されると共に、水溶液中に含まれる界面活性剤がナノ粒子表面に結合する。これにより、有機溶媒分散液中に含まれるナノ粒子が親水性となって、水相に移動して、水相中にIII-V族半導体ナノ粒子が分散した状態となる。この際、界面活性剤としては、チオールやアミン、アミノ酸等を用いることができる。チオールを用いた場合には、中に含まれる硫黄がVI族元素なので、他のVI族元素の量を減らすことができる。チオールとしては、チオグリコール酸、チオグリセロール、2−メルカプトエチルアミン、3−メルカプトプロピオン酸、メルカプトコハク酸が例示される。
【0082】
III-V族半導体ナノ粒子を含有する有機溶媒分散液では、有機溶媒としては、一般に疎水性のものを用いることができ、その中でも芳香族炭化水素やハロゲン化炭化水素が好適に用いられる。具体的には、トルエンやクロロホルムが挙げられる。
【0083】
有機溶媒分散液中におけるIII-V族半導体ナノ粒子の濃度については、特に限定的ではないが、例えば、0.5×10−6〜10×10−6mol/L程度とすることが好ましく、1×10−6〜6×10−6mol/L程度とすることがより好ましく、2×10−6〜3×10−6mol/L程度とすることがさらに好ましい。
【0084】
該有機溶媒分散液は、従来のホットソープ法や、上記したソルボサーマル法によって得たIII-V族半導体ナノ粒子が分散した状態の有機溶媒分散液をそのまま用いても良く、或いは、ホットソープ法やソルボサーマル法によって得たIII-V族半導体ナノ粒子を溶媒から分離した後、再度、有機溶媒中に分散させた分散液を用いても良い。
【0085】
水溶液に配合するII族元素を含む化合物としては、Zn,Cd,Hg等のII族元素の少なくとも一種を含む水溶性化合物を用いることができる。この様な水溶性化合物としては、例えば、過塩素酸塩、塩化物、硝酸塩などを用いることができる。
【0086】
水溶液中のII族元素イオンの濃度については、0.01〜0.3mol/L程度とすることが好ましく、0.05〜0.2mol/L程度とすることがより好ましく、0.065〜0.15mol/L程度とすることが更に好ましい。
【0087】
VI族元素を含む化合物としては、S,Se,Te等のVI族元素の少なくとも一種を含む水溶性化合物を用いることができる。この様な水溶性化合物としては、チオグリコール酸、3−メルカプトプロピオン酸、硫化ナトリウム、硫化水素ナトリウム(NaSH)等が挙げられる。その他、セレン化物、テルル化物についても同様の化合物を用いることができる。
【0088】
水溶液中のVI族元素の濃度については、0.01〜0.8mol/L程度とすることが好ましく、0.05〜0.5mol/L程度とすることがより好ましく、0.15〜0.4mol/L程度とすることが更に好ましい。
【0089】
水溶液中におけるII族元素に対するVI族元素のモル比は、VI族/II族元素=1.5〜4.0程度とすることが好ましく、1.8〜3.0程度とすることがより好ましく、1.9〜2.5程度とすることが更に好ましい。
【0090】
さらに、界面活性剤としてチオールを導入する場合には、他のVI族元素の量と合わせて上記の比率となるように添加する。このチオールとしては、チオグリコール酸、チオグリセロール、2−メルカプトエチルアミン、3−メルカプトプロピオン酸、メルカプトコハ
ク酸等が例示される。この界面活性剤の作用で、ナノ粒子の水中での分散性が向上する。
【0091】
II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液のpHは、5〜12程度であることが好ましく、6.5〜11.5程度であることがより好ましく、9〜10程度であることが更に好ましい。
【0092】
III-V族半導体ナノ粒子を含有する有機溶媒分散液と、II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液とを接触させる方法については、特に限定はなく、該有機溶媒分散液と水溶液の一方を含む容器中に他方を加えればよい。この際、該有機溶媒分散液と水溶液の界面において反応が進行するが、該有機溶媒分散液と水溶液を十分に混合することによって、反応の進行を促進することができる。
【0093】
この際、II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液に対するIII-V族半導体ナノ粒子を含有する有機溶媒分散液の体積比は、0.2〜5程度とすることが好ましく、0.7〜1.3程度とすることがより好ましい。
【0094】
混合時の液温は、15〜80℃程度の間であることが好ましく、30〜65℃程度であることがより好ましく、45〜55℃程度であることが最も好ましい。
【0095】
(b−ii)光照射
上記の方法でIII-V族半導体ナノ粒子を水相中に移動させて、水相中に分散した状態とした後、該水相に光を照射する。この工程により、III-V族半導体ナノ粒子の表面において、水溶液中のII族元素とVI族元素との反応が生じてII−VI族半導体の層が形成される。この工程は実際には、光照射によるナノ粒子の溶解と溶液中からのII族およびVI族イオンの供給の競争的な反応である。この反応により、コアとなるIII-V族ナノ粒子の表面が削
られながら新しいII−VI族の層が付加されてコア/シェル構造を有するナノ粒子が得られる。この工程によって、ナノ粒子中の組成において、III族元素がV族元素よりも多くな
る。また、この工程により発光効率が大きく向上して、高い発光効率を有する水分散性のナノ粒子が得られる。
【0096】
この際、VI族元素を含む化合物としてチオグリコール酸を用いた場合には、チオグリコール酸は、VI族元素である硫黄の供給源として作用すると同時に、形成されたシェル部分の表面にチオール基が結合して、カルボキシル基の存在によってナノ粒子に水分散性が付与される。他のチオール(チオグリコール酸、チオグリセロール、2−メルカプトエチルアミン、3−メルカプトプロピオン酸、メルカプトコハク酸等)を用いた場合にも、同様のメカニズムによってナノ粒子が安定化される。
【0097】
照射する光の波長については、光照射による発光効率増大の効果を生じさせるためには、ナノ粒子に光吸収がある波長範囲であればよい。但し、波長が短すぎると溶媒や界面活性剤の吸収の影響が出てくるので望ましくない。また、光吸収の程度が少ないと、反応に時間がかかるので好ましくない。通常は、波長300〜600nm程度の光が好ましく、320〜500nm程度の光がより好ましく、330〜400nm程度の光が更に好ましい。
【0098】
照射光の強度は、0.1〜6W/cm2程度とすることが好ましく、1〜5W/cm2程度とすることがより好ましく、3〜4.5W/cm2程度とすることが更に好ましい。
【0099】
光の照射時間は、照射強度にも依存するが、通常、1分〜12時間程度であり、好ましくは20分〜5時間程度であり、より好ましくは30分〜2時間程度である。上記した光照射によって、ナノ粒子の発光効率が大幅に増大し70%を超える場合もある。
【0100】
上記した方法で得られた、コア部分がIII-V族半導体ナノ粒子からなり、シェル部分がII−VI族半導体からなるコア/シェル構造を有するナノ粒子は、アルコールなどの貧溶媒を加えることで、沈殿させて精製することができる。これを再び、水中に分散させることも可能である。
【0101】
貧溶媒を加えてサイズ選択的沈降法によってナノ粒子を分級するタイミングは、水転換の前でも光照射の直前でも、光照射の直後でも良い。ナノ粒子を水相へ転換した後(光照射の直前または直後)に行うほうが、表面酸化が抑えられてより高い発光効率が得られる傾向にある。
【0102】
これらの半導体ナノ粒子は、高い発光効率を有するものである。様々な応用を考える場合に、発光効率20%を超えることが望ましいが、上記したナノ粒子によれば、それを十分に達成することができる。III-V族半導体ナノ粒子においては、従来、達成されていない水溶液中において50%以上という高い発光効率を有するものも得ることができる。特に、65%以上、更には、70%以上という高い発光効率を有するものも得るとすることができる。
【0103】
なお、本願明細書における「溶液中の半導体ナノ粒子の発光効率」とは、当該技術分野において標準的に用いられる値であり、「内部量子収率」と同義である。以下の、空洞を有するナノ粒子分散ガラスビーズの作製方法の箇所で、詳しく説明する。
【0104】
1.2 磁性ナノ粒子
磁性を有するナノ粒子も、公知の方法で作製できる。典型例として、Fe3O4ナノ粒子の
場合は、既報の文献(ストローブら、ケミストリー オブ マテリアルズ、8巻、2209ページ(1996年))に従って以下の化学式に従って合成できる。
【0105】
【化3】

【0106】
この場合、磁性ナノ粒子は、アルカリ性溶液中(pH11−12)で界面活性剤を用いなくても作製できる。
【0107】
アルカリ性溶液中の磁性ナノ粒子の濃度は、あまり高すぎると凝集を起こす。また、低すぎると、最終的にガラスビーズ中に取り込まれる量が少なくなる。このため、ガラスビーズに含有させる反応に使用する際のナノ粒子の濃度は、1×10−5から5×10−4mol/Lが好ましく、5×10−5から2×10−4mol/Lがさらに好ましい。
【0108】
他に、Fe3O4、Fe2O3、CoFe2O4、MnFe2O4、NiFe2O4、CoCrFeO4、Pt、Co、PtCo、FePt、
及びFeCoからなる群から選ばれる少なくとも1種の磁性ナノ粒子も、既報の文献に従って合成できる。これらの合成法のいくつかが、ウイリアムズら、アカウンツ オブ ケミカルリサーチ、41巻、411ページ(2008年)に解説されている。磁界を印加したときに磁性体に発生する磁化(単位体積あたりの磁気モーメント、単位はemu/g)が大きい
ほど、磁性体は磁石に強く引き付けられる。市販の永久磁石の磁界は大きいものでも5kOe(磁束密度にして0.5T)程度であり、これによって引き付けるためにはガラスビーズの磁化は1emu/g以上必要である。一方で、磁性ナノ粒子としてよく使われるFe3O4磁性ナノ粒子単体では、印加磁界5kOeでの磁化はおよそ40emu/gである。ところが、積層構造を持つPtCoなどでは、その10倍程度の磁化が期待できる。このため、これをガラス
ビーズに導入すれば、重量分率が50%であったとしても200emu/gの磁化が実現でき
る。なお、磁界5kOeは市販の電磁石で容易に発生できる大きさなので、小型の振動試料
型磁力計によってこの磁界での磁化を容易に測定できる。また磁性の種類としては、常磁性、超常磁性、強磁性などが例示されるが、当該ナノ粒子はどの種類の磁性を示してもよい。
【0109】
1.3 金属ナノ粒子
金属ナノ粒子も、公知の方法で作製できる。金属としては、例えば、金(Au)、銀(Ag)、銅(Cu)等が例示される。典型例である金ナノ粒子の場合は、既報の文献(ニーら、ジャーナル オブ アメリカン ケミカル ソサエティ、124巻、9606ページ(2002年))に従って塩化金酸の還元によって合成できる。粒径は、2〜9ナノメートルの範囲で制御できる。また、銀ナノ粒子の場合も、既報の文献(パルら、ジャーナル オブ フィジカルケミストリー、シー、112巻、4874ページ(2008年))に従って合成できる。
【0110】
2.内部に空洞を有するナノ粒子分散ガラスビーズの作製
本発明のケイ素系ガラスビーズは、内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであり、該ガラス相にナノ粒子Aを含むケイ素系ガラスビーズであり、その製造方法の典型例として次の工程を含有する。
(1)疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する工程、及び
(2)上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する工程、
を含む製造方法。
【0111】
以下、図2を参照しながら各工程を具体的に説明する。
【0112】
工程(1)
工程(1)では、疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する(図2)。
【0113】
工程(1)で用いられる疎水性有機溶媒としては、炭素数4〜12の炭化水素が挙げられ、具体的には、炭素数4〜12の直鎖状、分岐状又は環状の脂肪族炭化水素、或いは炭素数6〜12の芳香族炭化水素が挙げられる。上記脂肪族炭化水素は、融点及び沸点が10〜35℃の範囲になく常温で液体であれば、飽和又は不飽和のいずれであってもよく、炭素数5〜10の直鎖状、分岐状又は環状の飽和脂肪族炭化水素が好ましい。より具体的には、ペンタン、シクロペンタン、ヘキサン、シクロヘキサン、ヘプタン、イソヘプタン、オクタン、イソオクタン、ノナン、デカン等が挙げられ、特にシクロヘキサン、イソオクタンが好ましい。上記芳香族炭化水素は、単環又は2環の芳香族炭化水素であり、該芳香環上に脂肪族炭化水素基を有していてもよい。より具体的には、ベンゼン、トルエン、キシレン等が挙げられる。
【0114】
工程(1)で用いられる界面活性剤としては、疎水性有機溶媒に溶解し、溶解した状態において、界面活性剤の疎水基側が外側に配向し、界面活性剤の親水基側が内側に配向した、いわゆる逆ミセルを生成することができるものであれば用いることができる。
【0115】
例えば、親水基や疎水基が電荷を持つイオン性(カチオン性、アニオン性又は両性)界面活性剤、親水基や疎水基が電荷を持たない非イオン性界面活性剤が挙げられる。
【0116】
イオン性(アニオン性)界面活性剤としては、例えば、ビス(2−エチルヘキシル)ス
ルホこはく酸ナトリウム(商品名「エーロゾルOT」、和光純薬工業(株)製)等が例示される。
【0117】
非イオン性界面活性剤としては、例えば、ポリオキシエチレンエーテル型非イオン性界面活性剤が挙げられ、特にポリオキシエチレンアルキルフェニルエーテル型非イオン性界面活性剤が挙げられる。そのうち、ポリオキシエチレン(5)ノニルフェニルエーテル(商
品名「イゲパルCO-520」、シグマ−アルドリッチ社製)、ポリオキシエチレン(2)ノニル
フェニルエーテル(商品名「イゲパルCO-210」、シグマ−アルドリッチ社製)、ポリオキシエチレン(9)ノニルフェニルエーテル(商品名「イゲパルCO-630」、シグマ−アルドリ
ッチ社製)、ポリオキシエチレン(12)ノニルフェニルエーテル(商品名「イゲパルCO-720」、シグマ−アルドリッチ社製)等のポリオキシエチレンノニルフェニルエーテル型非イオン性界面活性剤、ポリオキシエチレン(2)イソオクチルフェニルエーテル(商品名「イ
ゲパルCA-210」、シグマ−アルドリッチ社製)、ポリオキシエチレン(5)イソオクチルフ
ェニルエーテル(商品名「イゲパルCA-520」、シグマ−アルドリッチ社製)、ポリオキシエチレン(12)イソオクチルフェニルエーテル(商品名「イゲパルCA-720」、シグマ−アルドリッチ社製)等のポリオキシエチレンイソオクチルフェニルエーテル型非イオン性界面活性剤などが好ましい。
【0118】
なお、上記のポリオキシエチレンの後に記載した括弧内の数字は、オキシエチレン単位の繰り返し数を意味する。
【0119】
好適な界面活性剤は、非イオン性界面活性剤であり、さらにポリオキシエチレンエーテル型非イオン性界面活性剤、特にポリオキシエチレンノニルフェニルエーテル型非イオン性界面活性剤、とりわけポリオキシエチレン(5)ノニルフェニルエーテルである。これは
、前述したように、逆ミセルとナノ粒子が静電反発を起こさないため、ナノ粒子が逆ミセル中に均一に取り込まれ易いと考えられるからである。
【0120】
疎水性の有機溶媒と界面活性剤を含む媒体は、両者を混合し撹拌することにより製造される。界面活性剤の使用量は、疎水性有機溶媒1molに対し、0.001〜0.1mol程度、好ましくは0.005〜0.02mol程度であればよい。撹拌時の温度は、特に限定はないが、
通常、10〜35℃程度であればよい。
【0121】
ナノ粒子A及びケイ素アルコキシドを含む水溶液Xは、ナノ粒子A分散水溶液とケイ素アルコキシドとを混合して調製される。ケイ素アルコキシドは、一般式(I):
R4r-Si(OR5)4-r (I)
(式中、R4及びR5は同一又は異なって低級アルキル基を示し、rは0,1,2又は3を示す)
で表されるものである。
【0122】
上記一般式(I)で表される化合物の中でも、r=0,1又は2、特にr=0又は1のものが好適
に用いられる。
【0123】
R4及びR5で示される低級アルキル基としては、炭素数1〜6の直鎖又は分岐鎖のアルキル基があげられ、具体的には、メチル、エチル、n−プロピル、イソプロピル等が挙げられ、特にメチル、エチルが好ましい。
【0124】
上記一般式(I)で表される化合物の好ましいものとしては、テトラメトキシシラン、
テトラエトキシシラン(TEOS)、テトライソプロポキシシラン、メチルトリメトキシシラン、エチルトリメトキシシラン等が例示され、特にTEOSが好ましい。
【0125】
ケイ素アルコキシドの配合量は、ケイ素アルコキシドのモル数:半導体ナノ粒子のモル
数が、1000:1〜100000:1程度、好ましくは5000:1〜20000:1程度であればよい。なお、半
導体ナノ粒子のモル数とは、半導体ナノ粒子の個数(半導体分子の数ではない)をアボガドロ数で割った値をモル数として用いるという意味である。半導体ナノ粒子のモル吸光係数は、物質とサイズによって決まっており、いくつもの文献で報告されている。例えば、CdSe、CdTe及びCdSナノ粒子については、文献(ユーら、ケミストリー オブ マテリア
ルズ、15巻、2854ページ(2003年))に詳細に書かれており、さらに特定の大きさのCdTeナノ粒子については、文献(村瀬ら、ナノスケール リサーチ レターズ、2巻、230ページ(2007年))に補足のデータがある。これらの文献に記載された方法を用いることで、対象とする溶液の吸光度から容易に半導体ナノ粒子のモル濃度が算出でき、さらに加える水溶液Xの容量がわかれば、溶液中に含まれる半導体ナノ粒子のモル数が算出できる。
【0126】
なお、ケイ素アルコキシドを溶解した水溶液におけるケイ素アルコキシドと水の混合比率(モル比)は、通常、1:100〜1:10000程度であり、好ましくは1:200〜1:2000程度であ
り、より好ましくは1:300〜1:1000程度である。
【0127】
上記の混合で得たナノ粒子Aとケイ素アルコキシドを含む水溶液中で、ケイ素アルコキシドを部分的に加水分解させる。このようなケイ素アルコキシドの部分的な加水分解は、ナノ粒子Aとケイ素アルコキシドを含む水溶液を撹拌することによって達成される。
【0128】
このとき、必要に応じアルカリ性水溶液を加えても良い。アルカリ性水溶液として好適に用いうるものとして、例えば、アンモニア水の他、水酸化ナトリウム、水酸化カリウム等のアルカリ金属水酸化物の水溶液等が挙げられる。これにより、アルコキシドの部分的加水分解をより促進することができる。これらの中でも、特にアンモニア水又は水酸化ナトリウム水溶液が好ましい。
【0129】
アルカリ性水溶液の添加量は限定的でなく、例えば、ナノ粒子A分散水溶液のpHが7〜11程度(好ましくは8.5〜10程度)となるように、当該水溶液に加えればよい。
【0130】
また、これらアルカリ性水溶液に加え、さらにナノ粒子の劣化を抑制するために、ナノ粒子Aを構成する金属イオン、及び/又はナノ粒子A被覆用界面活性剤を加えてもよい。
【0131】
ナノ粒子Aを構成する金属イオンとしては、上述した半導体ナノ粒子の金属イオンが挙げられ、具体的には、亜鉛イオン、カドミウムイオンが挙げられる。
【0132】
ナノ粒子A被覆用の界面活性剤は、ナノ粒子Aの表面を被覆する性質を有する限り限定的でなく、具体的には、チオグリコール酸、チオグリセロール、2―メルカプト―エチルアミン、グリシン等からなる群より選ばれる少なくとも1種が挙げられる。この中でもチオグリコール酸が好ましい。
【0133】
水溶液Xでは、ケイ素アルコキシドが完全にではなく部分的に加水分解した状態の溶液を得ることが必要である。加水分解を一部進行させたアルコキシドとナノ粒子Aを含む溶液では、ナノ粒子Aの表面がシリカでコートされて安定化されていると考えられる。つまり、ナノ粒子Aが薄いガラス層でコートされるため、ナノ粒子A同士の凝集を防ぐことができる。また、粘度の高まったケイ素アルコキシドの部分的加水分解生成物を用いることにより、半導体ナノ粒子を逆ミセル中に取り込むことができ、その後速やかにケイ素アルコキシドの加水分解を進めてガラス化することができるからである。
【0134】
撹拌の温度は特に限定されないが、通常、室温前後の5〜50℃であり、10〜40℃が好ま
しい。また、第1工程におけるケイ素アルコキシドの部分的加水分解時間(撹拌時間)は
特に限定されないが、通常、1〜6時間であり、2〜4時間が好ましい。
【0135】
次いで、疎水性の有機溶媒と界面活性剤を含む媒体に、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合、撹拌して逆ミセル溶液が調製される(図2)。
【0136】
撹拌の温度は特に限定されないが、通常、室温前後の5〜50℃であり、10〜40℃が好ま
しい。また、撹拌時間は特に限定されないが、通常、1〜6時間であり、2〜4時間が好ましい。
【0137】
なお、均一なサイズの逆ミセルを生成するために、溶液を激しく撹拌することが必要である。これにより平均径(外径)が50〜5000nm程度の微小な逆ミセルが形成される。逆ミセルの平均径(外径)は、界面活性剤の量、水の量、及び疎水性有機溶媒量の相互の比率によって変えることができる。
【0138】
工程(2)
工程(2)では、上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する。なお、アルカリ性水溶液Yには、上記した機能性物質(ナノ粒子B、薬理活性物質等)を含んでいてもよい。
【0139】
このとき、ナノ粒子Aを含む水溶液Xの水素イオン指数をpH1と表し、機能性物質を含んでいてもよいアルカリ性水溶液Yの水素イオン指数をpH2と表した場合に、pH1とpH2の関係を、7<pH1<pH2<14にすることが肝要である。これにより、内部に空洞を有するケイ素系ガラスビーズを形成することができる。
【0140】
pH2とpH1の差は、0.5以上が良く、1.0以上がさらに良く、1.5以上2.5以下が最も好ましい。これは、この範囲であればアルコキシドの加水分解と脱水縮合のスピードが適切になるためである。
【0141】
pH1は7〜10.5が好ましく、さらに8〜10.3が好ましく、9〜10.2が最も好ましい。pH2は上記の条件に加えて、7.5〜14が良く、10〜13がさらに好ましく、11.5〜12.5であれば最も好ましい。pH2のアルカリ性が高いと、ガラスの溶解が起きる場合があるため上記の範囲とすることが好ましい。
【0142】
なお、ナノ粒子Bはアルカリ性領域(pH>7)で安定であるものならば特に限定はない。例えば、上述した磁性ナノ粒子、金属ナノ粒子などが挙げられる。さらに、アルカリ性領域で安定な有機分子や無機材料を分散させた水溶液でも良い。このような有機分子や無機材料が薬理活性物質(医薬品)であれば、その薬効を失わずにガラスビーズ中に分散させることができる。
【0143】
工程(1)で加えたナノ粒子A及びケイ素アルコキシドを含む水溶液Xの添加量(体積:Wx)は、機能性物質を含んでいてもよいアルカリ性水溶液Yの添加量(体積:Wy)よりも多いことが好ましい。具体的には、両者の体積比(Wx/Wy)は、3〜100程度、さらに10〜40程度とすることが好ましく、15〜25程度が最も好ましい。これにより、逆ミセルの内部に形成される水溶液Xの水相(水玉)に、該水相(水玉)より小さい水溶液Yの水相(水玉)を導入することができ、所望の空洞を有するケイ素系ガラスビーズを形成することができるからである。
【0144】
この方法では、図2のように、一部が加水分解したケイ素アルコキシドとナノ粒子Aを含む水溶液Xを内包する微小な逆ミセル溶液(W/O型エマルション)溶液に、アルカリ性水溶液Yを添加すると、該水溶液Yは一旦、疎水性有機溶媒(油相)中に分散し、やが
て一部が水玉となって微小な逆ミセルに内包される水相(水溶液X)に移動する。該アルカリ性溶液には、機能性物質を含んでいてもよい。
【0145】
微小な逆ミセル内の水相(水溶液X)に、アルカリ性の高い水溶液Yの水玉が入ると、水溶液Yの水玉に接する水溶液Xの表面で急激にゾル−ゲル反応が進行し、逆ミセルの中に水玉の形を保ったままガラスの殻が形成される。これを乾燥することにより内部に空洞を有するケイ素系ガラスビーズが形成されると考えられる。
【0146】
また、必要に応じ、上記逆ミセル溶液にさらにケイ素アルコキシドを添加することができる。
【0147】
この方法により、1種類のナノ粒子Aをケイ素系ガラスビーズのガラス相に分散させ、もう1種類の機能性物質を該ガラスビーズ中の空洞に分散できる。この方法では、ナノ粒子Aと機能性物質が直接触れ合うことがないため、分散させる前のナノ粒子Aと機能性物質の特性(蛍光特性や磁性、薬効など)を保持したガラスビーズが作成できる。
【0148】
なお、工程(2)において、撹拌の温度は特に限定されないが、通常、室温前後の5〜50℃であり、10〜40℃が好ましい。また、ケイ素アルコキシドの加水分解時間(撹拌時間
)は特に限定されないが、通常、1〜6時間であり、2〜4時間が好ましい。その後、反応が完了すると、疎水性有機溶媒中に、ケイ素系ガラスビーズが形成される。
【0149】
上記工程(2)で得られた内部に空洞を有する(必要に応じ該空洞に機能性物質を内包する)ケイ素系ガラスビーズを作成した液状媒体から溶媒を除去し、目的のケイ素系ガラスビーズを得る。必要に応じて、生成したケイ素系ガラスビーズの表面に付着している過剰の界面活性剤を適当な溶媒で洗浄してもよく、該ケイ素系ガラスビーズを乾燥してもよい。
【0150】
得られるケイ素系ガラスビーズの形状は、ほぼ球形(例えば、真球、楕円球などを含む。)であり、その平均粒子径は、20nm〜1μm程度となる。また、ケイ素系ガラスビーズ内の空洞の数は、1つであっても、2以上であってもよい。通常、1〜10個である。この空洞の平均内径は、10〜500nm程度が好ましい。なお、ケイ素系ガラスビーズの平均粒子径及び空洞の平均内径は、高角度散乱暗視野(走査透過電子顕微鏡)法(HAADF-STEM)や透過型電子顕微鏡(TEM)を用いて測定できる。
【0151】
この方法で作製できるガラスビーズの粒径Dは、1μmよりも小さくできることが特徴
で、20nm程度まで小さくできる。このため、蛍光試薬や、体内の医薬品運搬(ドラッグデリバリー)などに用いることができる。また、中の空洞の直径dは、添加するアルカリ性溶液YのXに対する比率や攪拌速度に依存して、
D/10≦d≦D/2
の範囲で作製できる。また、ガラスビーズ中の空洞は1個ではなく、複数個作製することも可能である。このためには、アルカリ性溶液Xの体積をWX、アルカリ性溶液Yの体積をWYとしたときに、
10≦WX/WY≦40
とするのが良い。このとき、2〜10個程度の微小な空洞を有するガラスビーズが作製できる。1つのガラスビーズの中のこの空洞の合計の体積をVdとすると、残りの体積VDとの間で、
8≦VD/Vd≦1000
の範囲で調整できる。そして、前記のように、この体積VDの中に予め水溶液Xに含有させ
ておいたナノ粒子を分散させることができる。なお、ガラスビーズおよびその中の空洞は、完全な球形でなくても良く、楕円体の場合は慣性主軸方向の3つの粒径の平均をもって
その粒子の粒径と定義する。
【0152】
先に説明したように、ナノ粒子としては、蛍光を発するもの、磁性をもつもの、金属として強いプラズモン吸収を示すものなどが挙げられる。また、有機物としては薬理活性物質(医薬品)が挙げられ、体内の特定箇所に配置させて目的箇所に集中的に薬物を届け、またガラスの性質を利用することで薬物を徐放し、有効に作用させることができる。
【0153】
さらに、ガラス表面に抗体を取り付けることで、検体中の特定の抗原を接着させることができる。ガラスビーズ中に蛍光性の半導体ナノ粒子および磁性ナノ粒子を分散させておけば、これら抗原を取り付けたあとに磁石を用いて収集し、またその種類を蛍光色で判断することができる。このとき、半導体ナノ粒子は、ガラスビーズに入れても発光効率が低下しないことが望まれ、発光効率として20%以上であることが実用上好ましい。
【0154】
なお、本願明細書におけるガラスビーズの発光効率は、先に蛍光性の半導体ナノ粒子の説明でも触れたように、当該技術分野において標準的に用いられる値であり、「内部量子収率」と同義である。これは、吸収された光子(フォトン)数(ΦA)に対する蛍光(フォトルミネッセンス、PL)として発光される光子(フォトン)数(ΦPL)の割合(ΦPL/ΦA)として定義される。凝集がなく散乱が無視できる場合には、発光効率は溶液の状態で測定する。この場合、発光効率が既知の色素分子を用いて、該色素分子溶液と測定対象物における励起光波長での吸光度と発光強度とを比較することにより算出される。測定時には、色素分子溶液(たとえばキニーネの硫酸0.05mol/L水溶液)と測定対象物の励起波長での吸光度を一致させて比較するのが普通である。粉体や平板、薄膜の場合は、積分球を用いて測定するのが普通であり、そのための装置が市販されている。(例えば、浜松ホトニクスのC9920)本明細書における発光効率の測定の詳細は、発明者らの最近の著作物(村瀬ら、ジャーナル オブ ルミネッセンス、128巻、1896ページ、(2008年))に記されている。この方法によれば、励起波長での吸光度を一致させなくても、正確に発光効率を測定することができる。
【実施例】
【0155】
以下に、実施例に基づいて本発明をより詳細に説明するが、本発明はこれらの実施例により限定されるものではない。なお、溶液の発光効率の測定は、キニーネの硫酸0.05mol/L水溶液(発光効率55%)を標準溶液として用い、400nm励起にて行った。
【0156】
実施例1(蛍光性半導体ナノ粒子が分散した空洞を有するガラスビーズの作製)
(1)CdTeナノ粒子の作製
半導体ナノ粒子であるCdTeナノ粒子は、既報の文献(村瀬ら、ケミストリー レターズ、34巻、92ページ(2005年))に従って合成した。即ち、1.095g(2.61mmol)の過塩素酸カドミウム六水和物(Cd(ClO4)2・6H2O)を200mLの純水に溶解し、さらにナノ粒子用の界面活性剤であるチオグリコール酸をカドミウムとのモル比で1.3となるように加えた。pHを11.4に調整の後、アルゴンガスで脱気してからテルル化水素ガスを導入した。ガス中のテルルの量を、カドミウムの0.47倍となるように調整した。そののち、100℃で100時間還流することで、赤色発光のCdTeナノ粒子(粒径4nm程度)を得た。このナノ粒子の発光効率は約72%であった。
【0157】
(2)ナノ粒子のシリカ層によるコート
上記のCdTeナノ粒子分散液を2.2×10−6mol/Lの濃度として2mL取り出し、アンモニア水溶液(6.25重量%、50μL)とTEOS 20μLを加えて、2時間攪拌した。これにより、表面が薄いシリカ層で覆われたナノ粒子分散水溶液(X1、pH10)が作製された。
【0158】
(3)逆ミセル溶液の作製
界面活性剤(イゲパルCO-520)3.52gをシクロヘキサン25gに添加し、溶液が透明になるまで攪拌した。予め作製したナノ粒子分散水溶液(X1)を2mL取り出し、この溶液に激しく攪拌しながら滴下する。さらに、アンモニア水溶液(Y1)(6.25重量%、pHおよそ12.3、100μL)を滴下する。
【0159】
(4)空洞を含むガラスビーズの作製
上記で作製した逆ミセル溶液に、さらにTEOS 150μLを添加し、24時間攪拌する。
【0160】
これにより、CdTeナノ粒子をガラス相に分散した空洞を含むケイ素系ガラスビーズ分散液が作製された。この段階では、ガラスビーズは、50nmから2μm程度までの広いサイズ分布を持っている。
【0161】
次に、これをフィルタリングと遠心分離の手法により、サイズ選択する。
【0162】
小さいサイズを得る場合には、始めに穴径0.45μmサイズのフィルターでろ過し、ろ液を22000回転で30分間、遠心する。沈殿物をエタノールで洗浄したのち、純水に分散させる。
【0163】
このようにして得たガラスビーズを高角度散乱暗視野(走査透過電子顕微鏡)法(ハーディフステム、HAADF-STEM)によって撮影すると、図3(a)のようになり、直径160n
m程度のガラス球のガラス相部分にCdTeナノ粒子が多数、分散していることが確認された。また、空洞部分の存在も確認された。
【0164】
大きいサイズを得る場合には、始めに5μmサイズのフィルターにてろ過したあと、ろ液を1μmサイズのフィルターにてろ過してフィルターの上部に残った固形物をエタノールで洗浄後、再び水に分散して、1μmサイズのフィルターでろ過する。この作業を10回繰り返す。このようにして得たガラスビーズを透過型電子顕微鏡で観察すると図3(b)
のようになった。矢印で示したように、直径900nmのガラスビーズ中の周辺部分に少なくとも4つの空洞が認められる。このように大きなサイズのガラスビーズでは電子線が通りにくくなるので、中心付近にある空洞は観察されない。また、CdTeナノ粒子(直径4nm程度)も、このような低倍率では観察されない。
【0165】
実施例2(蛍光性半導体ナノ粒子と磁性粒子が分散したガラスビーズの作製)
(1)CdTeナノ粒子とFe3O4ナノ粒子の作製
実施例1と同じ方法で、赤色発光のCdTeナノ粒子(粒径4nm)を得た。作製したCdTeナノ粒子に半導体ナノ粒子用の界面活性剤チオグリコール酸0.005mol/L、過塩素酸カドミウム0.0017mol/Lの水溶液に再分散させてpHを10とし、ナノ粒子の濃度を2.2×10−6mol/Lとした。これを2mL取り出し、アンモニア水溶液(50μL、6.25重量%)とTEOS 20μLを加え、フタをして2時間攪拌する。これによって、薄くシリカコートされたナノ粒子分散液(X2、pH10)が調製できた。
【0166】
また、Fe3O4ナノ粒子(粒径8nm)も、既報の文献(ストローブら、ケミストリー
オブ マテリアルズ、8巻、2209ページ(1996年))に従って合成した。即ち、0.10mLの12規定塩酸と脱気した純水5mLを混ぜ、さらに塩化鉄(II)0.1038gおよび塩化鉄(III)0.26gを攪拌しながら加えて溶解させる。この溶液を、
25mLの1.5mol/Lの水酸化ナトリウム溶液に激しく攪拌しながら加える。生成
した沈殿物を磁石を使って引きつけながら、上澄み液をデカンテーションによって取り除く。分離した沈殿物に純水を加えて4000回転で遠心し、上澄み液を取り除く。これを3回繰り返した後に、500mLの0.01mol/Lの塩酸を攪拌しながら加えて表面のマイナスチャージを除去した後、さらに4000回転で遠心した後、純水中に再分散させてFe3O4ナノ粒子分散溶液とした。
【0167】
(2)逆ミセル溶液の作製
ガラスビーズ用の界面活性剤イゲパルCO-520(3.52g)をシクロヘキサン溶液(25g)に添加し、透明になるまで攪拌した。上記で作製したナノ粒子分散液(X2、pH10)2mLを、この溶液に激しく攪拌しながら一滴ずつ加えた。これにさらに上記で合成した酸化鉄溶液0.3mLにアンモニア水(25重量%)0.1mLを加えた溶液(Y2、アンモニア6.25重量%、pH12.3、100μL)を一滴ずつ添加した。
【0168】
(3)ガラスビーズの作製
上記の逆ミセル溶液にTEOS150μLを加え、24時間攪拌して、反応を進行させた。
【0169】
このようにして得られたガラスビーズは、磁石に接着した。また、赤色の強い蛍光を示した。図4のように、初めのCdTeナノ粒子コロイド溶液とほぼ同じ吸収・蛍光スペクトルが確認された。発光効率を測定すると68%であった。さらにポリエチレングリコールを介してアビジン−ビオチンを付けた場合も、図5に示すように同様の吸収・蛍光スペクトルを示すことがわかった。
【0170】
透過電子顕微鏡で観察すると、図6のようにガラス相にCdTeナノ粒子が多数、分散していることが認められた。また、空洞部分にFe3O4ナノ粒子が塊って分散していることが確
認された。
【0171】
当該ガラスビーズを水溶液中に分散して小さなガラス瓶に入れた後、表面磁束密度0.45Tのネオジム磁石を近づけたところ、ガラスビーズが磁石に吸い付けられることが観察できた。
【0172】
次に、このガラスビーズを乾燥させてX線回折スペクトルを測定すると、図7のようになった。黒丸で示したピークの角度は全て文献によるCdTeの値と一致し、白抜きの四角で示したピークの角度は全て文献によるFe3O4の値と一致した。このため分散しているナノ
粒子は、CdTeナノ粒子とFe3O4ナノ粒子であることが確認できた。また、22度付近に幅
の広い回折ピークが現れているが、これはガラスに特有なものである。この結果から、ナノ粒子を分散させているマトリックスがガラスの性質を示すことも明らかになった。
【0173】
さらに、このガラスビーズおよびFe3O4ナノ粒子単独での磁気ヒステリシス曲線(横軸
が印加磁界、縦軸が磁化)を測定した。測定は、理研電子(株)製の振動試料型磁力計を用いて室温で行った。その結果、図8(a)および(b)に示すように、両者とも超常磁性を示すことがわかった。これは、強磁性体微粒子の集合体で見られる特有の磁性であり、Fe3O4ナノ粒子をガラスビーズ中に分散してもその特性が変わらないことを示している。なお
、縦軸は単位質量あたりの磁化で示しているので、ガラスビーズ中に分散しているFe3O4
ナノ粒子の磁化は、ガラスの質量の分だけFe3O4ナノ粒子単独のものよりも小さくなって
いる。印加磁界5kOeでのFe3O4ナノ粒子単体の磁化が37emu/gであるのに対して、Fe3O4ナノ粒子がCdTeナノ粒子と共に分散したガラスビーズの印加磁界5kOeでの磁化は2.4emu/gであることがわかった。
【0174】
実施例3(異なる種類の蛍光性半導体ナノ粒子を分散したガラスビーズ1)
上記の実施例2を少しだけ変更して、磁性を示すFe3O4ナノ粒子の替わりに、緑色発光
の半導体ナノ粒子を作製した。これは実施例1で100時間の還流をする替わりに30分の還流をすることでCdTeナノ粒子(直径2.6nm)として容易に作製できる。これにより、実施例2でFe3O4ナノ粒子が分散した部分に、CdTeナノ粒子(直径2.6nm)が分
散したガラスビーズを作成することができた。
【0175】
同様に、文献(村瀬ら、ジャーナル オブ コロイド アンド インターフェイス サイエンス、321巻、468ページ(2008年))に従って合成した青色発光のZnSe系ナノ粒子でも、上記の緑色発光のCdTeナノ粒子と同様にガラスビーズ中の空洞部分に分散させることができた。
【0176】
実施例4(異なる種類の蛍光性半導体ナノ粒子を分散したガラスビーズ2)
空洞部分にIII-V族半導体ナノ粒子であるInPナノ粒子を分散したガラスビーズを次のようにして作成した。
【0177】
(1)InPナノ粒子の作製
以下の方法により、III-V族半導体であるInPナノ粒子をソルボサーマル法で作製した。
【0178】
まず、グローブボックスでアルゴンガス雰囲気中、オートクレーブに塩化インジウム(InCl3)0.4g、界面活性剤であるトリオクチルホスフィン(Trioctylphosphine、[CH3(CH2)7]3P、TOP)3mLとドデシルアミン(Dodecylamine、CH3(CH2)11NH2、DDA)2.5gを加えた。さらに、溶媒としてトルエン(Toluene、C6H5CH3)5mLを加え、トリス(ジメチルアミノ)ホスフィン(Tris(dimethylamino)phosphine、C6H18N3P)0.5mLを入れた。
【0179】
オートクレーブを電気炉に移して75℃で1時間保った後、更に180℃に昇温し、24時間でナノ粒子を成長させた。このナノ粒子分散液にトルエン10mLとメタノール6mLを加え、十分に攪拌した後、10分間遠心分離を行い、遠心分離後、透明な上澄み液を取り出すことによって、InPナノ粒子と反応後の副産物を分離した。
【0180】
さらに、この副産物を取り除いたナノ粒子分散液を使用して、サイズ選択的沈降法により異なる粒径のナノ粒子を取り出した。貧溶媒としてはメタノールを利用し、溶液が少し懸濁したら、遠心分離を掛け、得られた沈殿を取り出し、ヘキサンに再分散した。上澄み液に更に貧溶媒を追加することで、溶液が再び懸濁したら、遠心分離を行った。これらの操作を溶液中にナノ粒子が無くなるまで繰り返すことによって、InPナノ粒子をサイズ分布の狭いナノ粒子に分離した。
【0181】
サイズ選択後、ナノ粒子の粒径が揃っていることが第一吸収ピークの位置と幅からも確認された。また、X線回折の結果からも、作製、分離されたものがInPナノ粒子であることが確認された。このときの発光効率は約1%と低いものであった。
【0182】
(2)水分散のInPナノ粒子の作製
上記(1)工程でサイズ選択的沈降法により取り出した異なる粒径のナノ粒子をブタノールとヘキサンの混合溶液(ブタノール:ヘキサンの体積比は1:2)に分散させた。このとき、吸収スペクトルから、既報の文献(アダムら、ジャーナル オブ ケミカル フィジクス、123巻、084706ページ(2005))の吸光係数を用いて算出された溶液中のナノ粒子の濃度は、約0.3×10−5mol/Lであった。ガラス瓶に小型の攪拌子を入れ、ホットスターラーに乗せ、ヒーターの温度を70℃に設定した。このとき、容器中の溶液は約50℃であった。
【0183】
ナノ粒子分散溶液を攪拌しながら、亜鉛イオンと界面活性剤チオグリコール酸が入った混合溶液(ZT溶液)2mLを加えた。このZT溶液中では、亜鉛イオン濃度は0.13mol/L、亜鉛イオンとチオグリコール酸のモル比は1:2.43とした。更に、水酸化ナトリウムでZT溶液のpH値を11.0になるように調整した。
【0184】
攪拌により、有機層のナノ粒子はほぼ全部水層に分配されて、有機層は完全に透明になった。一方で、水層はナノ粒子の粒径によって、黄色や茶色などの色になった。この水溶液をピペットで取り出し、遠沈管に移した。凝集したナノ粒子を取り除くため、遠心分離を掛けた後に、上澄み溶液を採取した。水分散後のナノ粒子はわずかに蛍光(フォトルミネッセンス)を発光した。
【0185】
更に遠沈管に上澄み溶液をいれ、貧溶媒としてメタノールを入れると、溶液が懸濁した。これを遠心分離することで、水分散性ナノ粒子の粉末を取り出すことができた。
【0186】
なお、このInPナノ粒子を水溶液に分散する工程で、水溶液(ZT溶液)の中に界面活性剤が無いと、うまく水溶液に分散できず、沈殿が生じた。また、亜鉛イオンが無いと、溶液攪拌によってナノ粒子が溶解して無くなり、有機層と水層はともに透明になった。
【0187】
(3)コア/シェル構造の半導体ナノ粒子の製造
上記(2)工程で得られた水分散性ナノ粒子の粉末を、(2)工程に記載したZT溶液に溶解し、既報の文献(村瀬ら、コロイズ アンド サーフェスイズ エー、294巻、33ページ(2007))の方法を参照しながら、紫外光照射してInPナノ粒子の上に硫化亜鉛シェルを作製した。
【0188】
まず、ナノ粒子分散溶液に小型の攪拌子を入れて、攪拌しながら、波長365nmの紫外光を強度は4.0W/cm2で20〜120分間照射し、10分間ごとに蛍光と吸収スペクトルを測定した。
【0189】
このように作製したナノ粒子は、発光波長554〜620nm、発光効率は34〜47%であった。得られたナノ粒子の光特性を表1に示す。
【0190】
なお、上記(1)工程でソルボサーマル法の時間を調整することで、発光波長450nmから750nmの広い範囲のナノ粒子を得ることができた。
【0191】
【表1】

【0192】
このようにして作製したInPナノ粒子分散水溶液を実施例1で作製したFe3O4ナノ粒子分散水溶液の替わりに用いることで、空洞部分にInPナノ粒子が分散したガラスビーズを作
製した。
【0193】
実施例5(蛍光性半導体ナノ粒子と金属ナノ粒子が分散したガラスビーズ)
金ナノ粒子を、文献(ニーら、ジャーナル オブ アメリカン ケミカル ソサエティ、124巻、9606ページ(2002年))に従って合成し、粒径を7nmとした。精製後、実施例1と同様にアンモニアを加えてpHを12にした水溶液(Y5)を作製した。
【0194】
実施例1と同様に、界面活性剤イゲパルCO-520をシクロヘキサン溶液に添加、攪拌して、透明溶液を作製した。実施例1のナノ粒子分散液(X5、pH10)2mLを、この透明溶液に激しく攪拌しながら一滴ずつ加えた。これにさらに今回作製した水溶液(Y5)0.1mLを一滴ずつ添加し、24時間攪拌したところ、金属ナノ粒子と半導体ナノ粒子が分散したガラスビーズが得られた。
【0195】
実施例6(金属ナノ粒子と磁性ナノ粒子が分散したガラスビーズ)
(1)金ナノ粒子分散溶液の作製
実施例5で作製した金コロイド溶液(2mL、1×10−5mol/L、pH8.5)、アンモニア水溶液(6.25重量%、50μL)およびTEOS20μLをバイアルビン中で混合し、蓋をしてから2時間、攪拌する。これにより、薄いシリカ層で覆われた金ナノ粒子分散溶液(X6、pH9)が作製される。
【0196】
(2)逆ミセル溶液の作製
界面活性剤(イゲパルCO-520)3.52gをシクロヘキサン25gに加え、溶液が透明になるまで攪拌する。これを2mL取り出して、先の金ナノ粒子分散溶液(X6)に激しく攪拌しながら滴下する。実施例2で作製したFe3O4ナノ粒子(粒径8nm)分散溶液(
Y6、pH11)を100μL取り出して、この逆ミセル溶液に滴下した。
【0197】
(3)ガラスビーズの作製
上記の逆ミセル溶液にTEOS150μLを加え、24時間攪拌して反応を進行させ、ガラスビーズを得た。
【0198】
実施例7(医薬品と半導体ナノ粒子が分散したガラスビーズ)
抗がん剤として知られるイブプロフェン(IBU)を、Flukaより購入した。最近の公知文献(アドバンスト ファンクショナル マテリアルズ、18巻、2780ページ(2008年))を参考にして、IBUをポリビニルアルコールの水溶液に分散させてポリビニルア
ルコールでコートし、アンモニア溶液(pH11)に10重量%となるように分散させた。実施例4の方法で作製したInPナノ粒子を、実施例2の方法でガラス相に分散させ、同時にIBUをガラス球内の空洞部分に分散させることができた。
【0199】
実施例8(抗体を接着したガラスビーズ)
実施例2で作製した蛍光性半導体ナノ粒子と磁性ナノ粒子が分散したガラスビーズ(0.3mL、10mmol/LのPBSバッファー溶液中)に、2−[メトキシ(ポリエチレ
ンオキシ)プロピル]トリメトキシシラン (CH3O(C2H4O)6-9C3H6Si(OCH3)3)を1μL加えて7時間攪拌した。さらに0.2mgのストレプトアビジン−マレイミド(シグマより購入)を10mmol/LのPBSバッファー溶液(20μL)に加えて3時間攪拌した。さ
らに、ビオチン−ストレプトアビジン−アフィニティ純ヤギ抗マウスIgG(重鎖+軽鎖)
(Biotin-SP-conjugatedAffiniPure Goat Anti-Mouse IgG(H+L),Jackson ImmunoResearc Laboratories, Inc.より購入)100μLを加えて5分間、攪拌した。このあと試料を4℃で24時間静置することで、IgGを接着させた。紫外線照射により発光することが、確
かめられた。
【技術分野】
【0001】
本発明は、内部に空洞を有しガラス相にナノ粒子が分散した微小ガラスビーズ、及びその製造方法に関する。
【0002】
なお、本願明細書では、ゾル−ゲル法を用いて作製したケイ素を含有するマトリックスを「ケイ素系ガラス」と呼ぶ。該ケイ素系ガラスは、一般にエックス線回折で明確なピークを生じない。また、本発明は、微小な(直径が1μm程度以下)概略球形のケイ素系ガラス粒子を対象としており、これを「ケイ素系ガラスビーズ」と呼ぶ。
【背景技術】
【0003】
ガラスは、耐薬品性、機械的特性において高分子より優れており、また、紫外線に対する耐性も良好なので、種々の機能を持つナノ粒子や有機分子を担持するマトリックスとして有用である。
【0004】
このガラスをマトリックスとした微小ビーズについては、多くの研究開発が行われてきており、ケイ素系のガラスをゾル−ゲル法によって作製する方法が数多く報告されている。このとき、アルカリ性条件で、かつ、熱処理温度が低い条件でガラスビーズを作製する場合には、酸化ケイ素の網目状構造の発達が不十分となり、ときには有機物を多く含んだり、1nm程度の微小なシリカ球の集まりとなることがある。
【0005】
このようなケイ素系ガラスビーズですでに製品化されているものとしては、鈴木油脂工業(株)の「無機質球状微粒子」(商品名:ゴッドボール)がある。このガラスビーズには、クロマトグラフィー用の充填剤、化粧用のパウダーなどの用途がある。また、作製法によりビーズの中心付近に中空の構造を作製することができる。この中空部分を有するガラスビーズは、薬品の担持および徐放が可能なのでドラッグデリバリーに用いられる。これらケイ素系ガラスビーズは、多くの場合、粒径1〜100μm程度であり、1μm以下では粒径や中空のコア径の制御が難しくなる。
【0006】
また、特許文献1には、球状粒子の殻の部分(直径0.2〜100μm程度)にマクロ孔(直径60nm〜30μm)を有するケイ素系の殻から構成される中空粒子、とその作製法が記されている。これに関連して、詳細な該中空粒子の作製法が非特許文献1に示されている。
【0007】
一方で、ケイ素系ガラスビーズ中に、ナノ粒子を担持させる研究も進んでいる。ナノ粒子とは、直径2〜20nm程度の大きさの粒子であり、表面積の割合が大きいので注意しないと直ぐに凝集してさまざまな機能を失ってしまうことが多い。このため、適切なマトリックスに担持することが不可欠である。
【0008】
近年、このナノ粒子として半導体ナノ粒子の研究が盛んである。この半導体ナノ粒子は、主にII−VI族またはIII−V族の化合物半導体からなる。これらの半導体ナノ粒子は溶
液法によって作製され、表面の欠陥を除去したものは新しいタイプの蛍光体として知られている。これら半導体ナノ粒子は、いわゆる量子サイズ効果により、同じ材料でできていても粒径が小さくなるほどバンドギャップが広がって短波長側の発光を示すようになる。他に、磁性を示すナノ粒子や金属性のナノ粒子が知られている。
【0009】
特許文献2には、直径数十nmのケイ素系ガラスビーズ中に作製した空隙に、半導体ナノ粒子を含有した構造体、及びその作製方法が記されている。
【0010】
また、本発明者らは、発光する半導体ナノ粒子を分散させたケイ素系ガラスビーズとその作製法について、特許文献3(逆ミセル法)、特許文献4(ストーバー法)、特許文献5(逆ミセル法の改良)に示すように、技術を積み上げてきた。この技術を用いれば、半導体ナノ粒子を発光効率の低下を抑えつつ複数個、およそ直径30nmから1μm程度のガラスビーズに分散させることができる。しかし、いずれの場合もガラスビーズの中に1種類のナノ粒子を分散させる手法である。
【0011】
ガラスビーズ中に1種類のナノ粒子だけでなく、複数の他の種類のナノ粒子や、医薬品分子等の機能性物質を含有させることで、様々な特性を持ったガラスビーズを得ることができる。このような多機能のガラスビーズ作製を狙ったものとして、非特許文献2がある。これには、半導体ナノ粒子と磁性ナノ粒子が同じガラスビーズ中に分散した、蛍光特性と磁性の両方を示すガラスビーズが作製できることが記載されている。
【0012】
このガラスビーズで用いられる半導体ナノ粒子の作製法は、既報の非特許文献3により作製されたとされているが、非特許文献2では該半導体ナノ粒子の発光効率については触れられていない。そこで、非特許文献2で報告されている発光の半値幅(半値全幅(FWHM))を測定すると、赤色発光の場合は65nmと広いため、非特許文献2では、非特許文献3に書かれているサイズ選択処理を行っていないと判定される。この場合には、発光効率は10%の程度である。さらに、磁性粒子と一緒にガラスビーズに導入すると、半値幅が広がり発光のベースラインが大幅に上昇していることから大幅に発光効率が減少したと判断される。
【0013】
一般に、発光するナノ粒子と磁性ナノ粒子を混ぜると、相互作用により発光効率が低下する。例えば、酸化鉄ナノ粒子はプラスに帯電しており、他方、水分散性の多くの半導体ナノ粒子はマイナスに帯電している。このため、ガラスビーズ中に同時に分散させようとして両者を混ぜると、直ぐに凝集体を生じる。
【0014】
また、一般にナノ粒子は、溶液中で周りのイオンと微妙なバランスの上で分散を保っている。このため、他の化学種が加えられるとそのバランスが崩れて、凝集や表面の劣化を伴うことが多い。これを防ぐためには、ナノ粒子と磁性粒子や医薬品分子などを微小なガラスビーズ内の別の領域に閉じ込めることが有効であるが、そのような方法は知られていなかった。
【先行技術文献】
【特許文献】
【0015】
【特許文献1】特開2007−230794号公報
【特許文献2】特開2007−105873号公報
【特許文献3】特許3677538号公報
【特許文献4】特許3755033号公報
【特許文献5】国際公開第2007/034877号パンフレット
【非特許文献】
【0016】
【非特許文献1】藤原他、ケミストリー オブ マテリアルズ、16巻、5420ページ(2004年)
【非特許文献2】ヴェロニカ サルグエリノ−マセイラ他、アドバンスト ファンクショナル マテリアルズ、16巻、509ページ(2006年)
【非特許文献3】ガポーニック他、ジャーナル オブ フィジカルケミストリー ビー、106巻、7177ページ(2002年)
【発明の概要】
【発明が解決しようとする課題】
【0017】
本発明は、上記した如き従来技術の現状に鑑みてなされたものであり、その主な目的は、内部に空洞を有する微小なケイ素系ガラスビーズであって、該ガラスビーズ中の空洞ではない部分(以下、「ガラス相」とも記載する。)にナノ粒子を含むケイ素系ガラスビーズ及びその製造方法を提供することにある。さらに、該ガラスビーズ内部の空洞(ケイ素を含まない部分)に、ガラス相中のナノ粒子と同一又は異なる種類のナノ粒子や医薬品分子等の機能性物質を含むケイ素系ガラスビーズ及びその製造方法を提供することにある。
【課題を解決するための手段】
【0018】
従来の逆ミセル法によるナノ粒子分散ケイ素系ガラスビーズの作製法(特許文献5)は、例えば図1に示される。この逆ミセル法では、疎水性有機溶媒と界面活性剤を含む媒体と、一部が加水分解したケイ素アルコキシドを含むナノ粒子分散水溶液とを混合することにより逆ミセル溶液(W/O型エマルション)を形成する。該逆ミセルの内部の水相に該ナノ粒子分散水溶液が包含される。この逆ミセル溶液にケイ素アルコキシドを添加すると、該アルコキシドは一旦油相に分散され、その後水相に触れることで徐々に加水分解し親水性が増して水相に移動し、そこでゾル−ゲル反応が進行して固化しガラスビーズとなる。このとき、逆ミセルの水相に含まれるナノ粒子も同時にガラス中に取り込まれて、ガラスビーズ中に分散する。
【0019】
しかし、この方法では、ナノ粒子に加えて他のナノ粒子や磁性粒子や医薬品分子などの機能性物質を、微小なガラスビーズ内に導入することは困難である。
【0020】
本発明者は、上記した課題を解決すべく鋭意研究を重ねてきた。その結果、逆ミセル法を用いて半導体ナノ粒子が分散したケイ素系ガラスビーズを形成する過程で、疎水性有機溶媒(シクロヘキサン等)と界面活性剤を含む媒体に、一部加水分解したケイ素アルコキシドとナノ粒子Aを含む水溶液を加えて撹拌し逆ミセル溶液(W/O型エマルション)を形成し、これに機能性物質を含む所定pHのアルカリ性水溶液を加えて撹拌することにより、内部に空洞を有するケイ素系ガラスビーズであって、ガラス相にナノ粒子Aを含み、空洞に機能性物質を含むケイ素系ガラスビーズが得られることを見いだした。しかも、ナノ粒子A及び機能性物質は、その特性を保持したままガラスビーズ内に導入されていることを確認した。
【0021】
具体的には、本発明の方法では、図2のように、油相に界面活性剤を分散した溶液に、一部が加水分解したケイ素アルコキシドとナノ粒子Aを含む水溶液Xを加えて、該水溶液Xを内包する微小な逆ミセル溶液(W/O型エマルション)を形成する。その溶液に、機能性物質を含むアルカリ性水溶液Yを添加すると、該水溶液Yは一旦、油相中に分散し、やがて一部が水玉となって微小な逆ミセル内の水相(水溶液X)に移動する。
【0022】
このとき、ナノ粒子Aを含む水溶液Xの水素イオン指数をpH1と表し、機能性物質を含む水溶液Yの水素イオン指数をpH2と表した場合に、pH1とpH2の関係を、7<pH1<pH2<14にすることにより、内部に空洞を有するケイ素系ガラスビーズを形成することができる。
【0023】
これは、微小な逆ミセル内の水相(水溶液X)に、アルカリ性の高い水溶液Yの水玉が
入ると、水溶液Yの水玉に接する水溶液Xの表面で急激にゾル−ゲル反応が進行し、逆ミセルの中に水玉の形を保ったままガラスの殻が形成される。これを乾燥することにより内部に空洞を有するケイ素系ガラスビーズが形成されると考えられる。また、必要に応じ、上記逆ミセル溶液にさらにケイ素アルコキシドを添加することができ、これによりゾル−ゲル反応が促進される。
【0024】
このようにして、水溶液Xに含まれるナノ粒子Aはガラス相中に分散・固定され、水溶液Yの水玉中に含まれる機能性物質は空洞の領域に導入される。その結果、ナノ粒子Aと機能性物質は1つのガラスビーズ中で別々の領域に閉じ込められることになる。
【0025】
この方法の利点は、1種類のナノ粒子Aをケイ素系ガラスビーズのガラス相に分散させ、もう1種類の機能性物質を該ガラスビーズ中の空洞(ケイ素を含まない部分)に分散できることである。本発明のケイ素系ガラスビーズは、機能性物質が空洞の内表面に沿って分散し、ガラスビーズの中心部分に空洞を残している場合や、機能性物質が空洞に充填されている場合も含む。この方法では、ナノ粒子Aと機能性物質が直接触れ合うことがないため、分散させる前のナノ粒子Aと機能性物質の特性(蛍光特性や磁性、薬効など)を保持したガラスビーズが作製できる。
【0026】
即ち、本発明のケイ素系ガラスビーズは内部に空洞を有し、ガラス相にナノ粒子Aを含み、且つ、空洞部分にも機能性物質を含ませることができるので、含有されるナノ粒子A及び機能性物質の機能を併せ持った微小なガラスビーズの作製が可能になる。つまり、1つのガラスビーズに複数の機能を持たせたガラスビーズを提供することができる。
【0027】
本発明は、以下のケイ素系ガラスビーズ及びその製造方法を提供する。
【0028】
項1 内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであって、該ケイ素系ガラス相にナノ粒子Aを含むことを特徴とするケイ素系ガラスビーズ。
【0029】
項2 さらに前記ケイ素系ガラスビーズ内部の空洞に機能性物質を含む項1に記載のケイ素系ガラスビーズ。
【0030】
項3 前記機能性物質がナノ粒子Bである項2に記載のケイ素系ガラスビーズ。
【0031】
項4 前記ナノ粒子A及びナノ粒子Bの平均粒径がそれぞれ2〜20nmである項3に記載のケイ素系ガラスビーズ。
【0032】
項5 前記ナノ粒子A及び/又はナノ粒子Bが半導体ナノ粒子である項3又は4に記載のケイ素系ガラスビーズ。
【0033】
項6 前記ナノ粒子A及び/又はナノ粒子Bが、発光効率が20%以上の半導体ナノ粒子である項3〜5のいずれかに記載のケイ素系ガラスビーズ。
【0034】
項7 前記半導体ナノ粒子が、CdTe、CdSe、CdS、ZnSe、ZnSe(1-x)Tex (但し、0 < x <
1)、ZnS、InP、InxGa(1-x)P (但し、0 < x < 1)、及びInAsからなる群より選ばれる少なくとも1種である項5又は6に記載のケイ素系ガラスビーズ。
【0035】
項8 前記ナノ粒子A及び/又はナノ粒子Bが磁性を有するナノ粒子である項3〜7のいずれかに記載のケイ素系ガラスビーズ。
【0036】
項9 前記磁性を有するナノ粒子が、Fe3O4、Fe2O3、CoFe2O4、MnFe2O4、NiFe2O4、CoCrFeO4、Pt、Co、PtCo、FePt、及びFeCoからなる群より選ばれる少なくとも1種である項
8に記載のケイ素系ガラスビーズ。
【0037】
項10 印加磁界5kOeでの磁化が1〜200emu/gである、項8又は9に記載の
ケイ素系ガラスビーズ。
【0038】
項11 前記ナノ粒子A及び/又はナノ粒子Bが金属ナノ粒子である項3〜10のいずれかに記載のケイ素系ガラスビーズ。
【0039】
項12 前記金属ナノ粒子の金属が、金(Au)、銀(Ag)及び銅(Cu)からなる群より選ばれる少なくとも1種である項11に記載のケイ素系ガラスビーズ。
【0040】
項13 前記ケイ素系ガラスビーズ内の空洞の平均内径が10〜500nmである請求項1〜12のいずれかに記載のケイ素系ガラスビーズ。
【0041】
項14 前記機能性物質が薬理活性物質である項2〜13のいずれかに記載のケイ素系ガラスビーズ。
【0042】
項15 前記ケイ素系ガラスビーズの外表面に抗体が接着されてなる項1〜14のいずれかに記載のケイ素系ガラスビーズ。
【0043】
項16 内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであり、該ケイ素系ガラス相にナノ粒子Aを含むケイ素系ガラスビーズの製造方法であって、
(1)疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する工程、及び
(2)上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する工程、
を含む製造方法。
【0044】
項17 前記工程(2)において、アルカリ性水溶液Yが機能性物質を含む項16に記載の製造方法。
【0045】
項18 前記工程(1)のナノ粒子Aを含むケイ素アルコキシド水溶液Xの水素イオン
指数(pH1)がpH1>7であり、かつ、前記工程(2)のアルカリ性水溶液Yの水素イオン指数(pH2)がpH1<pH2<14である項16又は17に記載の製造方法。
【0046】
項19 前記工程(2)が、前記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加した後、さらにケイ素アルコキシドを添加してケイ素系ガラスビーズを形成する工程である項16〜18のいずれかに記載の製造方法。
【0047】
項20 前記項1〜15のいずれかに記載のケイ素系ガラスビーズを含む蛍光試薬。
【0048】
項21 前記項1〜15のいずれかに記載のケイ素系ガラスビーズを含む薬物運搬システム。
【発明の効果】
【0049】
本発明の内部に空洞を有するケイ素系ガラスビーズは、ガラス相にナノ粒子A(例えば、半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)を分散しており、かつ該空洞部分にナノ粒子B(例えば、半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)、薬理活性物質等の機能性物質を担持することができる。該ガラスビーズの合成時に、これらナノ粒子Aと機能性物質の両者が交じり合うことがないので、蛍光性、磁性、薬効など、それぞれの物質の特性を保持したガラスビーズが作製できる。換言すれば、それぞれの物質の特性を同時に発揮するガラスビーズが作製できる。
【0050】
また、ガラスは機械的、化学的特性に優れているので、このガラスビーズは、経時安定
性にも優れている。このため、蛍光試薬、抗原採集、ドラッグデリバリー(人体内での薬物輸送)などの用途に用いることができる。
【図面の簡単な説明】
【0051】
【図1】従来のナノ粒子分散ガラスビーズの作製法の概略を示す図。
【図2】本願発明における空洞を有するナノ粒子分散ガラスビーズの作製法の概略を示す図。この図の場合は、空洞部分にナノ粒子Bを分散させている。
【図3】(a)空洞を含むCdTeナノ粒子分散ガラスビーズ(粒径約160nm)の高角度散乱暗視野法(ハーディフステム、HAADF-STEM)による撮影像。(b)空洞を含むCdTeナノ粒子分散ガラスビーズ(粒径約900nm)の透過電子顕微鏡(TEM)による撮影像。
【図4】CdTeナノ粒子のコロイド溶液と、それを水中のガラスビーズ中に分散させたときの吸収・蛍光スペクトル。
【図5】CdTeナノ粒子を分散したガラスビーズにさらにアビジンを取り付けたときの吸収・蛍光スペクトル。
【図6】磁性ナノ粒子(Fe3O4ナノ粒子)が空洞部分に分散したCdTeナノ粒子分散ガラスビーズの透過電子顕微鏡写真。
【図7】蛍光ナノ粒子(CdTe)と磁性ナノ粒子(Fe3O4)とを分散したガラスビーズのX線回折スペクトル。
【図8】(a)蛍光ナノ粒子(CdTe)と磁性ナノ粒子(Fe3O4)とを分散したガラスビーズの磁気ヒステリシス曲線。(b)磁性ナノ粒子(Fe3O4)単体の磁気ヒステリシス曲線。
【発明を実施するための形態】
【0052】
本発明の内部に空洞を有するケイ素系ガラスビーズは、ガラス相にナノ粒子A(半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)を分散含有しており、かつ該空洞部分に機能性物質を担持することができる。該機能性物質としては、例えばナノ粒子B(半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)、薬理活性物質等が挙げられる。なお、ナノ粒子Aとナノ粒子Bは同一種でも異なる種であってもよい。
【0053】
以下、ガラス相及び/又は空洞部分に導入できるナノ粒子A及びB(半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等)並びにその製法について説明し、さらに、ガラス相にナノ粒子Aを含み、空洞部分に該機能性物質(ナノ粒子B、薬理活性物質等)を含むケイ素系ガラスビーズ及びその製法について説明する。
【0054】
1.ナノ粒子の製造方法
ナノ粒子A及びBとして用いられるナノ粒子について以下説明する。該ナノ粒子としては、半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等が挙げられる。
【0055】
1.1 半導体ナノ粒子
半導体ナノ粒子は、II-VI族およびIII-V族がよく知られており、以下に本発明に用いるための作製法を説明する。高い蛍光強度を得るために、作製法が工夫されている。
【0056】
ケイ素系ガラスビーズに含まれるナノ粒子A及びBは、アルカリ水溶液中で安定な半導体ナノ粒子、磁性ナノ粒子、金属ナノ粒子等を使用するのが好ましい。半導体ナノ粒子は、蛍光性を有するものを用いることが好ましい。
【0057】
(1)II-VI族半導体ナノ粒子
II-VI族半導体ナノ粒子については、可視および赤外領域で発光するもの、例えば、CdTe、CdSe、CdS、ZnSe、ZnSe(1-x)Tex(但し、0 < x < 1)、ZnSなどの半導体ナノ粒子を例示することができ、他にPbS、PbSeなどが挙げられる。これらは皆、以下に説明する公知の
方法で製造できる。
【0058】
水溶液を用いる製造方法として、例えば、II族元素を含む水溶性化合物及び界面活性剤を溶解したアルカリ性水溶液中に、不活性雰囲気下において、VI族元素化合物を導入することによって、II-VI族半導体ナノ粒子を得ることができる。VI族元素化合物は、気体状
のものを用いることもできる。
【0059】
この方法において、II族元素を含む水溶性化合物としては、過塩素酸塩が好ましく、例えば、II族元素がカドミウムである場合には、過塩素酸カドミウムを用いることができる。
【0060】
界面活性剤としては、疎水基であるチオール基と親水基を有するものが好ましい。親水基としては、カルボキシル基などのアニオン性基、アミノ基などのカチオン性基、水酸基などを例示できるが、特に、カルボキシル基などのアニオン性基が好ましい。界面活性剤の具体例としては、チオグリコール酸、チオグリセロール、メルカプトエチルアミン等を例示できる。
【0061】
VI族元素化合物としては、例えばVI族元素の水素化物などを用いることができ、VI族元素がテルルである場合には、テルル化水素を用いることができる。その他、テルル化水素を水酸化ナトリウムと反応させて得られるテルル化水素ナトリウムを水溶液として導入することも可能である。
【0062】
合成時、ナノ粒子作製時に用いる界面活性剤の使用量を、水溶液中に含まれるII族元素に対して、モル比で1〜1.5程度とすると高い発光効率が得られる。
【0063】
不活性雰囲気としては、反応に関与しない気体の雰囲気であればよく、例えば、アルゴンガス、窒素ガス等の不活性ガス雰囲気を好適に利用できる。
【0064】
上記反応は、通常、室温(例えば、10〜30℃程度)において行うことができる。アルカリ性水溶液のpHは、10〜12程度、特に10.5〜11.5であることが好ましい。反応は、通常、VI族化合物を導入後、10分程度以内に終了する。
【0065】
上記した方法で得られる半導体ナノ粒子の粒径は、ナノメートルオーダーであり、多くの場合2〜20nmである。上記した方法で半導体ナノ粒子を作製した後、還流を行うことによって、該ナノ粒子の粒径を制御することが可能であり、還流時間を長くすると、粒径を大きくすることができる。
【0066】
特にCdTeナノ粒子の場合には、文献(村瀬ら、ケミストリー レターズ、34巻、92ページ、2005年)に作製法が説明されている。また、ZnSe系ナノ粒子の場合は、文献(村瀬ら、ジャーナル オブ コロイド アンド インターフェイス サイエンス、321巻、468ページ(2008年))に作製法が説明されている。
【0067】
一方、有機溶液を用いる製造方法として、例えば、トリオクチルフォスフィンやその酸化物を含む溶液にII族元素の化合物を添加して、さらにVI族元素を加える方法が知られている。CdSeは、この方法で作製される最も良く知られたナノ粒子である。用いる溶媒や、II族元素化合物の違いにより、さらに下記のようにいくつかの報告例が知られている。
・タラピンら、ナノ レターズ、1巻、207ページ(2001年)
・ペンら、ジャーナル オブ アメリカン ケミカル ソサエティー、123巻、1389ページ(2001年)
・バベンディーら、ジャーナル オブ フィジカル ケミストリー ビー、101巻、9
463ページ(1997年)
・ペンら、ジャーナル オブ アメリカン ケミカル ソサエティー、124巻、2049ページ(2002年)
・ゾンら、ジャーナル オブ フィジカル ケミストリー シー、111巻、526ページ(2007年)
【0068】
(2)III-V族半導体ナノ粒子
III-V族半導体ナノ粒子としては、アルカリ性水溶液中で発光効率の高いものが好適で
あり、例えば、InP、InxGa(1-x)P(但し、0 < x < 1)、及びInAs等の半導体ナノ粒子を例
示することができる。好ましくは、コアとしてIII-V族半導体ナノ粒子を有し、その表面
にII−VI族半導体の層が付加されたコア/シェル構造を有するナノ粒子が例示される。その作製方法として以下の方法が例示される。
【0069】
(a)コアの作製
公知の文献(村瀬ら、ケミストリー レターズ、37巻、856ページ(2008年))に例示されるように、2種のV族原子が直接に結合した部分構造を持つ化合物をV族元素の供給源とし、さらにソルボサーマル法(耐圧容器に溶媒を入れ、その溶媒の沸点以上の温度にして目的物を合成する手法)を用いることでIII−V族半導体のナノ粒子を比較
的低温で合成する。ソルボサーマル法の温度は、100〜300℃程度、より好ましくは、120〜200℃程度、さらに150〜180℃程度が好ましい。
【0070】
このような2種のV族原子が直接に結合した部分構造を持つ化合物として、好適には、V族原子と窒素原子とが直接に結合した部分構造を持つ化合物が挙げられ、具体的には、一般式(1):
【0071】
【化1】

【0072】
(式中、MはV族元素であり、R1、R2及びR3は同一又は異なって、メチル基、エチル基、n−プロピル基、イソプロピル基、ブチル基、tert−ブチル基等の低級アルキル基である。mは0〜2の整数であり、nは1〜3の整数であって、m+n=3である。)
で表される化合物を例示できる。
【0073】
Mで示されるV族元素としては、P、As、Sb、Bi等が挙げられ、好ましくはPである。R1、R2及びR3で示される低級アルキル基としては、C1−3のアルキル基が好ましく、メチル基がより好ましい。nは3が好ましい。
【0074】
上記一般式で表される化合物の具体例としては、下記(2)〜(7)で表される化合物を挙げることができる。
【0075】
【化2】

【0076】
(式中、M、R1、R2及びR3は前記に同じ。)
上記化合物のうち、(2)、(3)及び(5)で表される化合物が好ましい。R1、R2及びR3はそれぞれ、メチル基であることが好ましい。
【0077】
III族元素の供給源としては、特に限定されないが、In,Ga,Al等のIII族金属、その塩化物、酸化物、硝酸化物、酢酸化物などが例示される。III族元素は一種又は二種
以上混合して用いることができる。具体的なIII族元素化合物としては、InCl3、In2O3、In(OOCCH3)3、AlCl3、Al(NO3)3・9H2O、GaCl3、Ga(NO3)3・nH2Oが挙げられ、好ましくは、InCl3、AlCl3、GaCl3である。
【0078】
溶媒としては、トルエン、クロロホルムなどの疎水性の有機溶媒が例示される。
【0079】
この方法により合成したナノ粒子にアルコールなどの貧溶媒を加えることにより容易にサイズ分布の狭いナノ粒子を得ることができる(サイズ選択的沈降法)。このサイズ選択的沈降法とは、良溶媒に分散しているナノ粒子に、アルコールなどの貧溶媒を徐々に加えていくことで、溶解度の低いナノ粒子(通常は大きなサイズのナノ粒子)から溶解度の順に徐々に沈殿させて分級する手法である。このときの粒径は、1.5〜6nm程度であることが多い。得られたIII-V族半導体ナノ粒子の発光効率を上げるために、この粒子(コ
ア)の表面にさらに以下に記述する方法でシェル層をつける。
【0080】
(b)コア/シェル構造の作製
(b−i)混合液の調製
上記で得られたIII-V族半導体ナノ粒子(コア)を含有する有機溶媒分散液を、II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液に接触させる。この際、水相には界面活性剤を分散させておく。この界面活性剤としては、VI族元素を含む水分散性の分子を用いるのが好都合である。その一例として、チオグリコール酸が挙げられる。この場合は、分子の一端の硫黄原子がナノ粒子の表面に接着し、分子の他端のカルボキシル基が中性からアルカリ性の領域でイオン化して、ナノ粒子の水中での安定分散に寄与する。このとき、界面活性剤に加えて、他のVI族元素を含む化合物を添加しても良い。
【0081】
この工程により、III-V族半導体ナノ粒子の表面にあるIII族およびV族イオンの一部
の脱離反応が起きて、水溶液中のII族およびVI族イオンと置換されると共に、水溶液中に含まれる界面活性剤がナノ粒子表面に結合する。これにより、有機溶媒分散液中に含まれるナノ粒子が親水性となって、水相に移動して、水相中にIII-V族半導体ナノ粒子が分散した状態となる。この際、界面活性剤としては、チオールやアミン、アミノ酸等を用いることができる。チオールを用いた場合には、中に含まれる硫黄がVI族元素なので、他のVI族元素の量を減らすことができる。チオールとしては、チオグリコール酸、チオグリセロール、2−メルカプトエチルアミン、3−メルカプトプロピオン酸、メルカプトコハク酸が例示される。
【0082】
III-V族半導体ナノ粒子を含有する有機溶媒分散液では、有機溶媒としては、一般に疎水性のものを用いることができ、その中でも芳香族炭化水素やハロゲン化炭化水素が好適に用いられる。具体的には、トルエンやクロロホルムが挙げられる。
【0083】
有機溶媒分散液中におけるIII-V族半導体ナノ粒子の濃度については、特に限定的ではないが、例えば、0.5×10−6〜10×10−6mol/L程度とすることが好ましく、1×10−6〜6×10−6mol/L程度とすることがより好ましく、2×10−6〜3×10−6mol/L程度とすることがさらに好ましい。
【0084】
該有機溶媒分散液は、従来のホットソープ法や、上記したソルボサーマル法によって得たIII-V族半導体ナノ粒子が分散した状態の有機溶媒分散液をそのまま用いても良く、或いは、ホットソープ法やソルボサーマル法によって得たIII-V族半導体ナノ粒子を溶媒から分離した後、再度、有機溶媒中に分散させた分散液を用いても良い。
【0085】
水溶液に配合するII族元素を含む化合物としては、Zn,Cd,Hg等のII族元素の少なくとも一種を含む水溶性化合物を用いることができる。この様な水溶性化合物としては、例えば、過塩素酸塩、塩化物、硝酸塩などを用いることができる。
【0086】
水溶液中のII族元素イオンの濃度については、0.01〜0.3mol/L程度とすることが好ましく、0.05〜0.2mol/L程度とすることがより好ましく、0.065〜0.15mol/L程度とすることが更に好ましい。
【0087】
VI族元素を含む化合物としては、S,Se,Te等のVI族元素の少なくとも一種を含む水溶性化合物を用いることができる。この様な水溶性化合物としては、チオグリコール酸、3−メルカプトプロピオン酸、硫化ナトリウム、硫化水素ナトリウム(NaSH)等が挙げられる。その他、セレン化物、テルル化物についても同様の化合物を用いることができる。
【0088】
水溶液中のVI族元素の濃度については、0.01〜0.8mol/L程度とすることが好ましく、0.05〜0.5mol/L程度とすることがより好ましく、0.15〜0.4mol/L程度とすることが更に好ましい。
【0089】
水溶液中におけるII族元素に対するVI族元素のモル比は、VI族/II族元素=1.5〜4.0程度とすることが好ましく、1.8〜3.0程度とすることがより好ましく、1.9〜2.5程度とすることが更に好ましい。
【0090】
さらに、界面活性剤としてチオールを導入する場合には、他のVI族元素の量と合わせて上記の比率となるように添加する。このチオールとしては、チオグリコール酸、チオグリセロール、2−メルカプトエチルアミン、3−メルカプトプロピオン酸、メルカプトコハ
ク酸等が例示される。この界面活性剤の作用で、ナノ粒子の水中での分散性が向上する。
【0091】
II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液のpHは、5〜12程度であることが好ましく、6.5〜11.5程度であることがより好ましく、9〜10程度であることが更に好ましい。
【0092】
III-V族半導体ナノ粒子を含有する有機溶媒分散液と、II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液とを接触させる方法については、特に限定はなく、該有機溶媒分散液と水溶液の一方を含む容器中に他方を加えればよい。この際、該有機溶媒分散液と水溶液の界面において反応が進行するが、該有機溶媒分散液と水溶液を十分に混合することによって、反応の進行を促進することができる。
【0093】
この際、II族元素を含む化合物及びVI族元素を含む化合物を含有する水溶液に対するIII-V族半導体ナノ粒子を含有する有機溶媒分散液の体積比は、0.2〜5程度とすることが好ましく、0.7〜1.3程度とすることがより好ましい。
【0094】
混合時の液温は、15〜80℃程度の間であることが好ましく、30〜65℃程度であることがより好ましく、45〜55℃程度であることが最も好ましい。
【0095】
(b−ii)光照射
上記の方法でIII-V族半導体ナノ粒子を水相中に移動させて、水相中に分散した状態とした後、該水相に光を照射する。この工程により、III-V族半導体ナノ粒子の表面において、水溶液中のII族元素とVI族元素との反応が生じてII−VI族半導体の層が形成される。この工程は実際には、光照射によるナノ粒子の溶解と溶液中からのII族およびVI族イオンの供給の競争的な反応である。この反応により、コアとなるIII-V族ナノ粒子の表面が削
られながら新しいII−VI族の層が付加されてコア/シェル構造を有するナノ粒子が得られる。この工程によって、ナノ粒子中の組成において、III族元素がV族元素よりも多くな
る。また、この工程により発光効率が大きく向上して、高い発光効率を有する水分散性のナノ粒子が得られる。
【0096】
この際、VI族元素を含む化合物としてチオグリコール酸を用いた場合には、チオグリコール酸は、VI族元素である硫黄の供給源として作用すると同時に、形成されたシェル部分の表面にチオール基が結合して、カルボキシル基の存在によってナノ粒子に水分散性が付与される。他のチオール(チオグリコール酸、チオグリセロール、2−メルカプトエチルアミン、3−メルカプトプロピオン酸、メルカプトコハク酸等)を用いた場合にも、同様のメカニズムによってナノ粒子が安定化される。
【0097】
照射する光の波長については、光照射による発光効率増大の効果を生じさせるためには、ナノ粒子に光吸収がある波長範囲であればよい。但し、波長が短すぎると溶媒や界面活性剤の吸収の影響が出てくるので望ましくない。また、光吸収の程度が少ないと、反応に時間がかかるので好ましくない。通常は、波長300〜600nm程度の光が好ましく、320〜500nm程度の光がより好ましく、330〜400nm程度の光が更に好ましい。
【0098】
照射光の強度は、0.1〜6W/cm2程度とすることが好ましく、1〜5W/cm2程度とすることがより好ましく、3〜4.5W/cm2程度とすることが更に好ましい。
【0099】
光の照射時間は、照射強度にも依存するが、通常、1分〜12時間程度であり、好ましくは20分〜5時間程度であり、より好ましくは30分〜2時間程度である。上記した光照射によって、ナノ粒子の発光効率が大幅に増大し70%を超える場合もある。
【0100】
上記した方法で得られた、コア部分がIII-V族半導体ナノ粒子からなり、シェル部分がII−VI族半導体からなるコア/シェル構造を有するナノ粒子は、アルコールなどの貧溶媒を加えることで、沈殿させて精製することができる。これを再び、水中に分散させることも可能である。
【0101】
貧溶媒を加えてサイズ選択的沈降法によってナノ粒子を分級するタイミングは、水転換の前でも光照射の直前でも、光照射の直後でも良い。ナノ粒子を水相へ転換した後(光照射の直前または直後)に行うほうが、表面酸化が抑えられてより高い発光効率が得られる傾向にある。
【0102】
これらの半導体ナノ粒子は、高い発光効率を有するものである。様々な応用を考える場合に、発光効率20%を超えることが望ましいが、上記したナノ粒子によれば、それを十分に達成することができる。III-V族半導体ナノ粒子においては、従来、達成されていない水溶液中において50%以上という高い発光効率を有するものも得ることができる。特に、65%以上、更には、70%以上という高い発光効率を有するものも得るとすることができる。
【0103】
なお、本願明細書における「溶液中の半導体ナノ粒子の発光効率」とは、当該技術分野において標準的に用いられる値であり、「内部量子収率」と同義である。以下の、空洞を有するナノ粒子分散ガラスビーズの作製方法の箇所で、詳しく説明する。
【0104】
1.2 磁性ナノ粒子
磁性を有するナノ粒子も、公知の方法で作製できる。典型例として、Fe3O4ナノ粒子の
場合は、既報の文献(ストローブら、ケミストリー オブ マテリアルズ、8巻、2209ページ(1996年))に従って以下の化学式に従って合成できる。
【0105】
【化3】

【0106】
この場合、磁性ナノ粒子は、アルカリ性溶液中(pH11−12)で界面活性剤を用いなくても作製できる。
【0107】
アルカリ性溶液中の磁性ナノ粒子の濃度は、あまり高すぎると凝集を起こす。また、低すぎると、最終的にガラスビーズ中に取り込まれる量が少なくなる。このため、ガラスビーズに含有させる反応に使用する際のナノ粒子の濃度は、1×10−5から5×10−4mol/Lが好ましく、5×10−5から2×10−4mol/Lがさらに好ましい。
【0108】
他に、Fe3O4、Fe2O3、CoFe2O4、MnFe2O4、NiFe2O4、CoCrFeO4、Pt、Co、PtCo、FePt、
及びFeCoからなる群から選ばれる少なくとも1種の磁性ナノ粒子も、既報の文献に従って合成できる。これらの合成法のいくつかが、ウイリアムズら、アカウンツ オブ ケミカルリサーチ、41巻、411ページ(2008年)に解説されている。磁界を印加したときに磁性体に発生する磁化(単位体積あたりの磁気モーメント、単位はemu/g)が大きい
ほど、磁性体は磁石に強く引き付けられる。市販の永久磁石の磁界は大きいものでも5kOe(磁束密度にして0.5T)程度であり、これによって引き付けるためにはガラスビーズの磁化は1emu/g以上必要である。一方で、磁性ナノ粒子としてよく使われるFe3O4磁性ナノ粒子単体では、印加磁界5kOeでの磁化はおよそ40emu/gである。ところが、積層構造を持つPtCoなどでは、その10倍程度の磁化が期待できる。このため、これをガラス
ビーズに導入すれば、重量分率が50%であったとしても200emu/gの磁化が実現でき
る。なお、磁界5kOeは市販の電磁石で容易に発生できる大きさなので、小型の振動試料
型磁力計によってこの磁界での磁化を容易に測定できる。また磁性の種類としては、常磁性、超常磁性、強磁性などが例示されるが、当該ナノ粒子はどの種類の磁性を示してもよい。
【0109】
1.3 金属ナノ粒子
金属ナノ粒子も、公知の方法で作製できる。金属としては、例えば、金(Au)、銀(Ag)、銅(Cu)等が例示される。典型例である金ナノ粒子の場合は、既報の文献(ニーら、ジャーナル オブ アメリカン ケミカル ソサエティ、124巻、9606ページ(2002年))に従って塩化金酸の還元によって合成できる。粒径は、2〜9ナノメートルの範囲で制御できる。また、銀ナノ粒子の場合も、既報の文献(パルら、ジャーナル オブ フィジカルケミストリー、シー、112巻、4874ページ(2008年))に従って合成できる。
【0110】
2.内部に空洞を有するナノ粒子分散ガラスビーズの作製
本発明のケイ素系ガラスビーズは、内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであり、該ガラス相にナノ粒子Aを含むケイ素系ガラスビーズであり、その製造方法の典型例として次の工程を含有する。
(1)疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する工程、及び
(2)上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する工程、
を含む製造方法。
【0111】
以下、図2を参照しながら各工程を具体的に説明する。
【0112】
工程(1)
工程(1)では、疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する(図2)。
【0113】
工程(1)で用いられる疎水性有機溶媒としては、炭素数4〜12の炭化水素が挙げられ、具体的には、炭素数4〜12の直鎖状、分岐状又は環状の脂肪族炭化水素、或いは炭素数6〜12の芳香族炭化水素が挙げられる。上記脂肪族炭化水素は、融点及び沸点が10〜35℃の範囲になく常温で液体であれば、飽和又は不飽和のいずれであってもよく、炭素数5〜10の直鎖状、分岐状又は環状の飽和脂肪族炭化水素が好ましい。より具体的には、ペンタン、シクロペンタン、ヘキサン、シクロヘキサン、ヘプタン、イソヘプタン、オクタン、イソオクタン、ノナン、デカン等が挙げられ、特にシクロヘキサン、イソオクタンが好ましい。上記芳香族炭化水素は、単環又は2環の芳香族炭化水素であり、該芳香環上に脂肪族炭化水素基を有していてもよい。より具体的には、ベンゼン、トルエン、キシレン等が挙げられる。
【0114】
工程(1)で用いられる界面活性剤としては、疎水性有機溶媒に溶解し、溶解した状態において、界面活性剤の疎水基側が外側に配向し、界面活性剤の親水基側が内側に配向した、いわゆる逆ミセルを生成することができるものであれば用いることができる。
【0115】
例えば、親水基や疎水基が電荷を持つイオン性(カチオン性、アニオン性又は両性)界面活性剤、親水基や疎水基が電荷を持たない非イオン性界面活性剤が挙げられる。
【0116】
イオン性(アニオン性)界面活性剤としては、例えば、ビス(2−エチルヘキシル)ス
ルホこはく酸ナトリウム(商品名「エーロゾルOT」、和光純薬工業(株)製)等が例示される。
【0117】
非イオン性界面活性剤としては、例えば、ポリオキシエチレンエーテル型非イオン性界面活性剤が挙げられ、特にポリオキシエチレンアルキルフェニルエーテル型非イオン性界面活性剤が挙げられる。そのうち、ポリオキシエチレン(5)ノニルフェニルエーテル(商
品名「イゲパルCO-520」、シグマ−アルドリッチ社製)、ポリオキシエチレン(2)ノニル
フェニルエーテル(商品名「イゲパルCO-210」、シグマ−アルドリッチ社製)、ポリオキシエチレン(9)ノニルフェニルエーテル(商品名「イゲパルCO-630」、シグマ−アルドリ
ッチ社製)、ポリオキシエチレン(12)ノニルフェニルエーテル(商品名「イゲパルCO-720」、シグマ−アルドリッチ社製)等のポリオキシエチレンノニルフェニルエーテル型非イオン性界面活性剤、ポリオキシエチレン(2)イソオクチルフェニルエーテル(商品名「イ
ゲパルCA-210」、シグマ−アルドリッチ社製)、ポリオキシエチレン(5)イソオクチルフ
ェニルエーテル(商品名「イゲパルCA-520」、シグマ−アルドリッチ社製)、ポリオキシエチレン(12)イソオクチルフェニルエーテル(商品名「イゲパルCA-720」、シグマ−アルドリッチ社製)等のポリオキシエチレンイソオクチルフェニルエーテル型非イオン性界面活性剤などが好ましい。
【0118】
なお、上記のポリオキシエチレンの後に記載した括弧内の数字は、オキシエチレン単位の繰り返し数を意味する。
【0119】
好適な界面活性剤は、非イオン性界面活性剤であり、さらにポリオキシエチレンエーテル型非イオン性界面活性剤、特にポリオキシエチレンノニルフェニルエーテル型非イオン性界面活性剤、とりわけポリオキシエチレン(5)ノニルフェニルエーテルである。これは
、前述したように、逆ミセルとナノ粒子が静電反発を起こさないため、ナノ粒子が逆ミセル中に均一に取り込まれ易いと考えられるからである。
【0120】
疎水性の有機溶媒と界面活性剤を含む媒体は、両者を混合し撹拌することにより製造される。界面活性剤の使用量は、疎水性有機溶媒1molに対し、0.001〜0.1mol程度、好ましくは0.005〜0.02mol程度であればよい。撹拌時の温度は、特に限定はないが、
通常、10〜35℃程度であればよい。
【0121】
ナノ粒子A及びケイ素アルコキシドを含む水溶液Xは、ナノ粒子A分散水溶液とケイ素アルコキシドとを混合して調製される。ケイ素アルコキシドは、一般式(I):
R4r-Si(OR5)4-r (I)
(式中、R4及びR5は同一又は異なって低級アルキル基を示し、rは0,1,2又は3を示す)
で表されるものである。
【0122】
上記一般式(I)で表される化合物の中でも、r=0,1又は2、特にr=0又は1のものが好適
に用いられる。
【0123】
R4及びR5で示される低級アルキル基としては、炭素数1〜6の直鎖又は分岐鎖のアルキル基があげられ、具体的には、メチル、エチル、n−プロピル、イソプロピル等が挙げられ、特にメチル、エチルが好ましい。
【0124】
上記一般式(I)で表される化合物の好ましいものとしては、テトラメトキシシラン、
テトラエトキシシラン(TEOS)、テトライソプロポキシシラン、メチルトリメトキシシラン、エチルトリメトキシシラン等が例示され、特にTEOSが好ましい。
【0125】
ケイ素アルコキシドの配合量は、ケイ素アルコキシドのモル数:半導体ナノ粒子のモル
数が、1000:1〜100000:1程度、好ましくは5000:1〜20000:1程度であればよい。なお、半
導体ナノ粒子のモル数とは、半導体ナノ粒子の個数(半導体分子の数ではない)をアボガドロ数で割った値をモル数として用いるという意味である。半導体ナノ粒子のモル吸光係数は、物質とサイズによって決まっており、いくつもの文献で報告されている。例えば、CdSe、CdTe及びCdSナノ粒子については、文献(ユーら、ケミストリー オブ マテリア
ルズ、15巻、2854ページ(2003年))に詳細に書かれており、さらに特定の大きさのCdTeナノ粒子については、文献(村瀬ら、ナノスケール リサーチ レターズ、2巻、230ページ(2007年))に補足のデータがある。これらの文献に記載された方法を用いることで、対象とする溶液の吸光度から容易に半導体ナノ粒子のモル濃度が算出でき、さらに加える水溶液Xの容量がわかれば、溶液中に含まれる半導体ナノ粒子のモル数が算出できる。
【0126】
なお、ケイ素アルコキシドを溶解した水溶液におけるケイ素アルコキシドと水の混合比率(モル比)は、通常、1:100〜1:10000程度であり、好ましくは1:200〜1:2000程度であ
り、より好ましくは1:300〜1:1000程度である。
【0127】
上記の混合で得たナノ粒子Aとケイ素アルコキシドを含む水溶液中で、ケイ素アルコキシドを部分的に加水分解させる。このようなケイ素アルコキシドの部分的な加水分解は、ナノ粒子Aとケイ素アルコキシドを含む水溶液を撹拌することによって達成される。
【0128】
このとき、必要に応じアルカリ性水溶液を加えても良い。アルカリ性水溶液として好適に用いうるものとして、例えば、アンモニア水の他、水酸化ナトリウム、水酸化カリウム等のアルカリ金属水酸化物の水溶液等が挙げられる。これにより、アルコキシドの部分的加水分解をより促進することができる。これらの中でも、特にアンモニア水又は水酸化ナトリウム水溶液が好ましい。
【0129】
アルカリ性水溶液の添加量は限定的でなく、例えば、ナノ粒子A分散水溶液のpHが7〜11程度(好ましくは8.5〜10程度)となるように、当該水溶液に加えればよい。
【0130】
また、これらアルカリ性水溶液に加え、さらにナノ粒子の劣化を抑制するために、ナノ粒子Aを構成する金属イオン、及び/又はナノ粒子A被覆用界面活性剤を加えてもよい。
【0131】
ナノ粒子Aを構成する金属イオンとしては、上述した半導体ナノ粒子の金属イオンが挙げられ、具体的には、亜鉛イオン、カドミウムイオンが挙げられる。
【0132】
ナノ粒子A被覆用の界面活性剤は、ナノ粒子Aの表面を被覆する性質を有する限り限定的でなく、具体的には、チオグリコール酸、チオグリセロール、2―メルカプト―エチルアミン、グリシン等からなる群より選ばれる少なくとも1種が挙げられる。この中でもチオグリコール酸が好ましい。
【0133】
水溶液Xでは、ケイ素アルコキシドが完全にではなく部分的に加水分解した状態の溶液を得ることが必要である。加水分解を一部進行させたアルコキシドとナノ粒子Aを含む溶液では、ナノ粒子Aの表面がシリカでコートされて安定化されていると考えられる。つまり、ナノ粒子Aが薄いガラス層でコートされるため、ナノ粒子A同士の凝集を防ぐことができる。また、粘度の高まったケイ素アルコキシドの部分的加水分解生成物を用いることにより、半導体ナノ粒子を逆ミセル中に取り込むことができ、その後速やかにケイ素アルコキシドの加水分解を進めてガラス化することができるからである。
【0134】
撹拌の温度は特に限定されないが、通常、室温前後の5〜50℃であり、10〜40℃が好ま
しい。また、第1工程におけるケイ素アルコキシドの部分的加水分解時間(撹拌時間)は
特に限定されないが、通常、1〜6時間であり、2〜4時間が好ましい。
【0135】
次いで、疎水性の有機溶媒と界面活性剤を含む媒体に、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合、撹拌して逆ミセル溶液が調製される(図2)。
【0136】
撹拌の温度は特に限定されないが、通常、室温前後の5〜50℃であり、10〜40℃が好ま
しい。また、撹拌時間は特に限定されないが、通常、1〜6時間であり、2〜4時間が好ましい。
【0137】
なお、均一なサイズの逆ミセルを生成するために、溶液を激しく撹拌することが必要である。これにより平均径(外径)が50〜5000nm程度の微小な逆ミセルが形成される。逆ミセルの平均径(外径)は、界面活性剤の量、水の量、及び疎水性有機溶媒量の相互の比率によって変えることができる。
【0138】
工程(2)
工程(2)では、上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する。なお、アルカリ性水溶液Yには、上記した機能性物質(ナノ粒子B、薬理活性物質等)を含んでいてもよい。
【0139】
このとき、ナノ粒子Aを含む水溶液Xの水素イオン指数をpH1と表し、機能性物質を含んでいてもよいアルカリ性水溶液Yの水素イオン指数をpH2と表した場合に、pH1とpH2の関係を、7<pH1<pH2<14にすることが肝要である。これにより、内部に空洞を有するケイ素系ガラスビーズを形成することができる。
【0140】
pH2とpH1の差は、0.5以上が良く、1.0以上がさらに良く、1.5以上2.5以下が最も好ましい。これは、この範囲であればアルコキシドの加水分解と脱水縮合のスピードが適切になるためである。
【0141】
pH1は7〜10.5が好ましく、さらに8〜10.3が好ましく、9〜10.2が最も好ましい。pH2は上記の条件に加えて、7.5〜14が良く、10〜13がさらに好ましく、11.5〜12.5であれば最も好ましい。pH2のアルカリ性が高いと、ガラスの溶解が起きる場合があるため上記の範囲とすることが好ましい。
【0142】
なお、ナノ粒子Bはアルカリ性領域(pH>7)で安定であるものならば特に限定はない。例えば、上述した磁性ナノ粒子、金属ナノ粒子などが挙げられる。さらに、アルカリ性領域で安定な有機分子や無機材料を分散させた水溶液でも良い。このような有機分子や無機材料が薬理活性物質(医薬品)であれば、その薬効を失わずにガラスビーズ中に分散させることができる。
【0143】
工程(1)で加えたナノ粒子A及びケイ素アルコキシドを含む水溶液Xの添加量(体積:Wx)は、機能性物質を含んでいてもよいアルカリ性水溶液Yの添加量(体積:Wy)よりも多いことが好ましい。具体的には、両者の体積比(Wx/Wy)は、3〜100程度、さらに10〜40程度とすることが好ましく、15〜25程度が最も好ましい。これにより、逆ミセルの内部に形成される水溶液Xの水相(水玉)に、該水相(水玉)より小さい水溶液Yの水相(水玉)を導入することができ、所望の空洞を有するケイ素系ガラスビーズを形成することができるからである。
【0144】
この方法では、図2のように、一部が加水分解したケイ素アルコキシドとナノ粒子Aを含む水溶液Xを内包する微小な逆ミセル溶液(W/O型エマルション)溶液に、アルカリ性水溶液Yを添加すると、該水溶液Yは一旦、疎水性有機溶媒(油相)中に分散し、やが
て一部が水玉となって微小な逆ミセルに内包される水相(水溶液X)に移動する。該アルカリ性溶液には、機能性物質を含んでいてもよい。
【0145】
微小な逆ミセル内の水相(水溶液X)に、アルカリ性の高い水溶液Yの水玉が入ると、水溶液Yの水玉に接する水溶液Xの表面で急激にゾル−ゲル反応が進行し、逆ミセルの中に水玉の形を保ったままガラスの殻が形成される。これを乾燥することにより内部に空洞を有するケイ素系ガラスビーズが形成されると考えられる。
【0146】
また、必要に応じ、上記逆ミセル溶液にさらにケイ素アルコキシドを添加することができる。
【0147】
この方法により、1種類のナノ粒子Aをケイ素系ガラスビーズのガラス相に分散させ、もう1種類の機能性物質を該ガラスビーズ中の空洞に分散できる。この方法では、ナノ粒子Aと機能性物質が直接触れ合うことがないため、分散させる前のナノ粒子Aと機能性物質の特性(蛍光特性や磁性、薬効など)を保持したガラスビーズが作成できる。
【0148】
なお、工程(2)において、撹拌の温度は特に限定されないが、通常、室温前後の5〜50℃であり、10〜40℃が好ましい。また、ケイ素アルコキシドの加水分解時間(撹拌時間
)は特に限定されないが、通常、1〜6時間であり、2〜4時間が好ましい。その後、反応が完了すると、疎水性有機溶媒中に、ケイ素系ガラスビーズが形成される。
【0149】
上記工程(2)で得られた内部に空洞を有する(必要に応じ該空洞に機能性物質を内包する)ケイ素系ガラスビーズを作成した液状媒体から溶媒を除去し、目的のケイ素系ガラスビーズを得る。必要に応じて、生成したケイ素系ガラスビーズの表面に付着している過剰の界面活性剤を適当な溶媒で洗浄してもよく、該ケイ素系ガラスビーズを乾燥してもよい。
【0150】
得られるケイ素系ガラスビーズの形状は、ほぼ球形(例えば、真球、楕円球などを含む。)であり、その平均粒子径は、20nm〜1μm程度となる。また、ケイ素系ガラスビーズ内の空洞の数は、1つであっても、2以上であってもよい。通常、1〜10個である。この空洞の平均内径は、10〜500nm程度が好ましい。なお、ケイ素系ガラスビーズの平均粒子径及び空洞の平均内径は、高角度散乱暗視野(走査透過電子顕微鏡)法(HAADF-STEM)や透過型電子顕微鏡(TEM)を用いて測定できる。
【0151】
この方法で作製できるガラスビーズの粒径Dは、1μmよりも小さくできることが特徴
で、20nm程度まで小さくできる。このため、蛍光試薬や、体内の医薬品運搬(ドラッグデリバリー)などに用いることができる。また、中の空洞の直径dは、添加するアルカリ性溶液YのXに対する比率や攪拌速度に依存して、
D/10≦d≦D/2
の範囲で作製できる。また、ガラスビーズ中の空洞は1個ではなく、複数個作製することも可能である。このためには、アルカリ性溶液Xの体積をWX、アルカリ性溶液Yの体積をWYとしたときに、
10≦WX/WY≦40
とするのが良い。このとき、2〜10個程度の微小な空洞を有するガラスビーズが作製できる。1つのガラスビーズの中のこの空洞の合計の体積をVdとすると、残りの体積VDとの間で、
8≦VD/Vd≦1000
の範囲で調整できる。そして、前記のように、この体積VDの中に予め水溶液Xに含有させ
ておいたナノ粒子を分散させることができる。なお、ガラスビーズおよびその中の空洞は、完全な球形でなくても良く、楕円体の場合は慣性主軸方向の3つの粒径の平均をもって
その粒子の粒径と定義する。
【0152】
先に説明したように、ナノ粒子としては、蛍光を発するもの、磁性をもつもの、金属として強いプラズモン吸収を示すものなどが挙げられる。また、有機物としては薬理活性物質(医薬品)が挙げられ、体内の特定箇所に配置させて目的箇所に集中的に薬物を届け、またガラスの性質を利用することで薬物を徐放し、有効に作用させることができる。
【0153】
さらに、ガラス表面に抗体を取り付けることで、検体中の特定の抗原を接着させることができる。ガラスビーズ中に蛍光性の半導体ナノ粒子および磁性ナノ粒子を分散させておけば、これら抗原を取り付けたあとに磁石を用いて収集し、またその種類を蛍光色で判断することができる。このとき、半導体ナノ粒子は、ガラスビーズに入れても発光効率が低下しないことが望まれ、発光効率として20%以上であることが実用上好ましい。
【0154】
なお、本願明細書におけるガラスビーズの発光効率は、先に蛍光性の半導体ナノ粒子の説明でも触れたように、当該技術分野において標準的に用いられる値であり、「内部量子収率」と同義である。これは、吸収された光子(フォトン)数(ΦA)に対する蛍光(フォトルミネッセンス、PL)として発光される光子(フォトン)数(ΦPL)の割合(ΦPL/ΦA)として定義される。凝集がなく散乱が無視できる場合には、発光効率は溶液の状態で測定する。この場合、発光効率が既知の色素分子を用いて、該色素分子溶液と測定対象物における励起光波長での吸光度と発光強度とを比較することにより算出される。測定時には、色素分子溶液(たとえばキニーネの硫酸0.05mol/L水溶液)と測定対象物の励起波長での吸光度を一致させて比較するのが普通である。粉体や平板、薄膜の場合は、積分球を用いて測定するのが普通であり、そのための装置が市販されている。(例えば、浜松ホトニクスのC9920)本明細書における発光効率の測定の詳細は、発明者らの最近の著作物(村瀬ら、ジャーナル オブ ルミネッセンス、128巻、1896ページ、(2008年))に記されている。この方法によれば、励起波長での吸光度を一致させなくても、正確に発光効率を測定することができる。
【実施例】
【0155】
以下に、実施例に基づいて本発明をより詳細に説明するが、本発明はこれらの実施例により限定されるものではない。なお、溶液の発光効率の測定は、キニーネの硫酸0.05mol/L水溶液(発光効率55%)を標準溶液として用い、400nm励起にて行った。
【0156】
実施例1(蛍光性半導体ナノ粒子が分散した空洞を有するガラスビーズの作製)
(1)CdTeナノ粒子の作製
半導体ナノ粒子であるCdTeナノ粒子は、既報の文献(村瀬ら、ケミストリー レターズ、34巻、92ページ(2005年))に従って合成した。即ち、1.095g(2.61mmol)の過塩素酸カドミウム六水和物(Cd(ClO4)2・6H2O)を200mLの純水に溶解し、さらにナノ粒子用の界面活性剤であるチオグリコール酸をカドミウムとのモル比で1.3となるように加えた。pHを11.4に調整の後、アルゴンガスで脱気してからテルル化水素ガスを導入した。ガス中のテルルの量を、カドミウムの0.47倍となるように調整した。そののち、100℃で100時間還流することで、赤色発光のCdTeナノ粒子(粒径4nm程度)を得た。このナノ粒子の発光効率は約72%であった。
【0157】
(2)ナノ粒子のシリカ層によるコート
上記のCdTeナノ粒子分散液を2.2×10−6mol/Lの濃度として2mL取り出し、アンモニア水溶液(6.25重量%、50μL)とTEOS 20μLを加えて、2時間攪拌した。これにより、表面が薄いシリカ層で覆われたナノ粒子分散水溶液(X1、pH10)が作製された。
【0158】
(3)逆ミセル溶液の作製
界面活性剤(イゲパルCO-520)3.52gをシクロヘキサン25gに添加し、溶液が透明になるまで攪拌した。予め作製したナノ粒子分散水溶液(X1)を2mL取り出し、この溶液に激しく攪拌しながら滴下する。さらに、アンモニア水溶液(Y1)(6.25重量%、pHおよそ12.3、100μL)を滴下する。
【0159】
(4)空洞を含むガラスビーズの作製
上記で作製した逆ミセル溶液に、さらにTEOS 150μLを添加し、24時間攪拌する。
【0160】
これにより、CdTeナノ粒子をガラス相に分散した空洞を含むケイ素系ガラスビーズ分散液が作製された。この段階では、ガラスビーズは、50nmから2μm程度までの広いサイズ分布を持っている。
【0161】
次に、これをフィルタリングと遠心分離の手法により、サイズ選択する。
【0162】
小さいサイズを得る場合には、始めに穴径0.45μmサイズのフィルターでろ過し、ろ液を22000回転で30分間、遠心する。沈殿物をエタノールで洗浄したのち、純水に分散させる。
【0163】
このようにして得たガラスビーズを高角度散乱暗視野(走査透過電子顕微鏡)法(ハーディフステム、HAADF-STEM)によって撮影すると、図3(a)のようになり、直径160n
m程度のガラス球のガラス相部分にCdTeナノ粒子が多数、分散していることが確認された。また、空洞部分の存在も確認された。
【0164】
大きいサイズを得る場合には、始めに5μmサイズのフィルターにてろ過したあと、ろ液を1μmサイズのフィルターにてろ過してフィルターの上部に残った固形物をエタノールで洗浄後、再び水に分散して、1μmサイズのフィルターでろ過する。この作業を10回繰り返す。このようにして得たガラスビーズを透過型電子顕微鏡で観察すると図3(b)
のようになった。矢印で示したように、直径900nmのガラスビーズ中の周辺部分に少なくとも4つの空洞が認められる。このように大きなサイズのガラスビーズでは電子線が通りにくくなるので、中心付近にある空洞は観察されない。また、CdTeナノ粒子(直径4nm程度)も、このような低倍率では観察されない。
【0165】
実施例2(蛍光性半導体ナノ粒子と磁性粒子が分散したガラスビーズの作製)
(1)CdTeナノ粒子とFe3O4ナノ粒子の作製
実施例1と同じ方法で、赤色発光のCdTeナノ粒子(粒径4nm)を得た。作製したCdTeナノ粒子に半導体ナノ粒子用の界面活性剤チオグリコール酸0.005mol/L、過塩素酸カドミウム0.0017mol/Lの水溶液に再分散させてpHを10とし、ナノ粒子の濃度を2.2×10−6mol/Lとした。これを2mL取り出し、アンモニア水溶液(50μL、6.25重量%)とTEOS 20μLを加え、フタをして2時間攪拌する。これによって、薄くシリカコートされたナノ粒子分散液(X2、pH10)が調製できた。
【0166】
また、Fe3O4ナノ粒子(粒径8nm)も、既報の文献(ストローブら、ケミストリー
オブ マテリアルズ、8巻、2209ページ(1996年))に従って合成した。即ち、0.10mLの12規定塩酸と脱気した純水5mLを混ぜ、さらに塩化鉄(II)0.1038gおよび塩化鉄(III)0.26gを攪拌しながら加えて溶解させる。この溶液を、
25mLの1.5mol/Lの水酸化ナトリウム溶液に激しく攪拌しながら加える。生成
した沈殿物を磁石を使って引きつけながら、上澄み液をデカンテーションによって取り除く。分離した沈殿物に純水を加えて4000回転で遠心し、上澄み液を取り除く。これを3回繰り返した後に、500mLの0.01mol/Lの塩酸を攪拌しながら加えて表面のマイナスチャージを除去した後、さらに4000回転で遠心した後、純水中に再分散させてFe3O4ナノ粒子分散溶液とした。
【0167】
(2)逆ミセル溶液の作製
ガラスビーズ用の界面活性剤イゲパルCO-520(3.52g)をシクロヘキサン溶液(25g)に添加し、透明になるまで攪拌した。上記で作製したナノ粒子分散液(X2、pH10)2mLを、この溶液に激しく攪拌しながら一滴ずつ加えた。これにさらに上記で合成した酸化鉄溶液0.3mLにアンモニア水(25重量%)0.1mLを加えた溶液(Y2、アンモニア6.25重量%、pH12.3、100μL)を一滴ずつ添加した。
【0168】
(3)ガラスビーズの作製
上記の逆ミセル溶液にTEOS150μLを加え、24時間攪拌して、反応を進行させた。
【0169】
このようにして得られたガラスビーズは、磁石に接着した。また、赤色の強い蛍光を示した。図4のように、初めのCdTeナノ粒子コロイド溶液とほぼ同じ吸収・蛍光スペクトルが確認された。発光効率を測定すると68%であった。さらにポリエチレングリコールを介してアビジン−ビオチンを付けた場合も、図5に示すように同様の吸収・蛍光スペクトルを示すことがわかった。
【0170】
透過電子顕微鏡で観察すると、図6のようにガラス相にCdTeナノ粒子が多数、分散していることが認められた。また、空洞部分にFe3O4ナノ粒子が塊って分散していることが確
認された。
【0171】
当該ガラスビーズを水溶液中に分散して小さなガラス瓶に入れた後、表面磁束密度0.45Tのネオジム磁石を近づけたところ、ガラスビーズが磁石に吸い付けられることが観察できた。
【0172】
次に、このガラスビーズを乾燥させてX線回折スペクトルを測定すると、図7のようになった。黒丸で示したピークの角度は全て文献によるCdTeの値と一致し、白抜きの四角で示したピークの角度は全て文献によるFe3O4の値と一致した。このため分散しているナノ
粒子は、CdTeナノ粒子とFe3O4ナノ粒子であることが確認できた。また、22度付近に幅
の広い回折ピークが現れているが、これはガラスに特有なものである。この結果から、ナノ粒子を分散させているマトリックスがガラスの性質を示すことも明らかになった。
【0173】
さらに、このガラスビーズおよびFe3O4ナノ粒子単独での磁気ヒステリシス曲線(横軸
が印加磁界、縦軸が磁化)を測定した。測定は、理研電子(株)製の振動試料型磁力計を用いて室温で行った。その結果、図8(a)および(b)に示すように、両者とも超常磁性を示すことがわかった。これは、強磁性体微粒子の集合体で見られる特有の磁性であり、Fe3O4ナノ粒子をガラスビーズ中に分散してもその特性が変わらないことを示している。なお
、縦軸は単位質量あたりの磁化で示しているので、ガラスビーズ中に分散しているFe3O4
ナノ粒子の磁化は、ガラスの質量の分だけFe3O4ナノ粒子単独のものよりも小さくなって
いる。印加磁界5kOeでのFe3O4ナノ粒子単体の磁化が37emu/gであるのに対して、Fe3O4ナノ粒子がCdTeナノ粒子と共に分散したガラスビーズの印加磁界5kOeでの磁化は2.4emu/gであることがわかった。
【0174】
実施例3(異なる種類の蛍光性半導体ナノ粒子を分散したガラスビーズ1)
上記の実施例2を少しだけ変更して、磁性を示すFe3O4ナノ粒子の替わりに、緑色発光
の半導体ナノ粒子を作製した。これは実施例1で100時間の還流をする替わりに30分の還流をすることでCdTeナノ粒子(直径2.6nm)として容易に作製できる。これにより、実施例2でFe3O4ナノ粒子が分散した部分に、CdTeナノ粒子(直径2.6nm)が分
散したガラスビーズを作成することができた。
【0175】
同様に、文献(村瀬ら、ジャーナル オブ コロイド アンド インターフェイス サイエンス、321巻、468ページ(2008年))に従って合成した青色発光のZnSe系ナノ粒子でも、上記の緑色発光のCdTeナノ粒子と同様にガラスビーズ中の空洞部分に分散させることができた。
【0176】
実施例4(異なる種類の蛍光性半導体ナノ粒子を分散したガラスビーズ2)
空洞部分にIII-V族半導体ナノ粒子であるInPナノ粒子を分散したガラスビーズを次のようにして作成した。
【0177】
(1)InPナノ粒子の作製
以下の方法により、III-V族半導体であるInPナノ粒子をソルボサーマル法で作製した。
【0178】
まず、グローブボックスでアルゴンガス雰囲気中、オートクレーブに塩化インジウム(InCl3)0.4g、界面活性剤であるトリオクチルホスフィン(Trioctylphosphine、[CH3(CH2)7]3P、TOP)3mLとドデシルアミン(Dodecylamine、CH3(CH2)11NH2、DDA)2.5gを加えた。さらに、溶媒としてトルエン(Toluene、C6H5CH3)5mLを加え、トリス(ジメチルアミノ)ホスフィン(Tris(dimethylamino)phosphine、C6H18N3P)0.5mLを入れた。
【0179】
オートクレーブを電気炉に移して75℃で1時間保った後、更に180℃に昇温し、24時間でナノ粒子を成長させた。このナノ粒子分散液にトルエン10mLとメタノール6mLを加え、十分に攪拌した後、10分間遠心分離を行い、遠心分離後、透明な上澄み液を取り出すことによって、InPナノ粒子と反応後の副産物を分離した。
【0180】
さらに、この副産物を取り除いたナノ粒子分散液を使用して、サイズ選択的沈降法により異なる粒径のナノ粒子を取り出した。貧溶媒としてはメタノールを利用し、溶液が少し懸濁したら、遠心分離を掛け、得られた沈殿を取り出し、ヘキサンに再分散した。上澄み液に更に貧溶媒を追加することで、溶液が再び懸濁したら、遠心分離を行った。これらの操作を溶液中にナノ粒子が無くなるまで繰り返すことによって、InPナノ粒子をサイズ分布の狭いナノ粒子に分離した。
【0181】
サイズ選択後、ナノ粒子の粒径が揃っていることが第一吸収ピークの位置と幅からも確認された。また、X線回折の結果からも、作製、分離されたものがInPナノ粒子であることが確認された。このときの発光効率は約1%と低いものであった。
【0182】
(2)水分散のInPナノ粒子の作製
上記(1)工程でサイズ選択的沈降法により取り出した異なる粒径のナノ粒子をブタノールとヘキサンの混合溶液(ブタノール:ヘキサンの体積比は1:2)に分散させた。このとき、吸収スペクトルから、既報の文献(アダムら、ジャーナル オブ ケミカル フィジクス、123巻、084706ページ(2005))の吸光係数を用いて算出された溶液中のナノ粒子の濃度は、約0.3×10−5mol/Lであった。ガラス瓶に小型の攪拌子を入れ、ホットスターラーに乗せ、ヒーターの温度を70℃に設定した。このとき、容器中の溶液は約50℃であった。
【0183】
ナノ粒子分散溶液を攪拌しながら、亜鉛イオンと界面活性剤チオグリコール酸が入った混合溶液(ZT溶液)2mLを加えた。このZT溶液中では、亜鉛イオン濃度は0.13mol/L、亜鉛イオンとチオグリコール酸のモル比は1:2.43とした。更に、水酸化ナトリウムでZT溶液のpH値を11.0になるように調整した。
【0184】
攪拌により、有機層のナノ粒子はほぼ全部水層に分配されて、有機層は完全に透明になった。一方で、水層はナノ粒子の粒径によって、黄色や茶色などの色になった。この水溶液をピペットで取り出し、遠沈管に移した。凝集したナノ粒子を取り除くため、遠心分離を掛けた後に、上澄み溶液を採取した。水分散後のナノ粒子はわずかに蛍光(フォトルミネッセンス)を発光した。
【0185】
更に遠沈管に上澄み溶液をいれ、貧溶媒としてメタノールを入れると、溶液が懸濁した。これを遠心分離することで、水分散性ナノ粒子の粉末を取り出すことができた。
【0186】
なお、このInPナノ粒子を水溶液に分散する工程で、水溶液(ZT溶液)の中に界面活性剤が無いと、うまく水溶液に分散できず、沈殿が生じた。また、亜鉛イオンが無いと、溶液攪拌によってナノ粒子が溶解して無くなり、有機層と水層はともに透明になった。
【0187】
(3)コア/シェル構造の半導体ナノ粒子の製造
上記(2)工程で得られた水分散性ナノ粒子の粉末を、(2)工程に記載したZT溶液に溶解し、既報の文献(村瀬ら、コロイズ アンド サーフェスイズ エー、294巻、33ページ(2007))の方法を参照しながら、紫外光照射してInPナノ粒子の上に硫化亜鉛シェルを作製した。
【0188】
まず、ナノ粒子分散溶液に小型の攪拌子を入れて、攪拌しながら、波長365nmの紫外光を強度は4.0W/cm2で20〜120分間照射し、10分間ごとに蛍光と吸収スペクトルを測定した。
【0189】
このように作製したナノ粒子は、発光波長554〜620nm、発光効率は34〜47%であった。得られたナノ粒子の光特性を表1に示す。
【0190】
なお、上記(1)工程でソルボサーマル法の時間を調整することで、発光波長450nmから750nmの広い範囲のナノ粒子を得ることができた。
【0191】
【表1】

【0192】
このようにして作製したInPナノ粒子分散水溶液を実施例1で作製したFe3O4ナノ粒子分散水溶液の替わりに用いることで、空洞部分にInPナノ粒子が分散したガラスビーズを作
製した。
【0193】
実施例5(蛍光性半導体ナノ粒子と金属ナノ粒子が分散したガラスビーズ)
金ナノ粒子を、文献(ニーら、ジャーナル オブ アメリカン ケミカル ソサエティ、124巻、9606ページ(2002年))に従って合成し、粒径を7nmとした。精製後、実施例1と同様にアンモニアを加えてpHを12にした水溶液(Y5)を作製した。
【0194】
実施例1と同様に、界面活性剤イゲパルCO-520をシクロヘキサン溶液に添加、攪拌して、透明溶液を作製した。実施例1のナノ粒子分散液(X5、pH10)2mLを、この透明溶液に激しく攪拌しながら一滴ずつ加えた。これにさらに今回作製した水溶液(Y5)0.1mLを一滴ずつ添加し、24時間攪拌したところ、金属ナノ粒子と半導体ナノ粒子が分散したガラスビーズが得られた。
【0195】
実施例6(金属ナノ粒子と磁性ナノ粒子が分散したガラスビーズ)
(1)金ナノ粒子分散溶液の作製
実施例5で作製した金コロイド溶液(2mL、1×10−5mol/L、pH8.5)、アンモニア水溶液(6.25重量%、50μL)およびTEOS20μLをバイアルビン中で混合し、蓋をしてから2時間、攪拌する。これにより、薄いシリカ層で覆われた金ナノ粒子分散溶液(X6、pH9)が作製される。
【0196】
(2)逆ミセル溶液の作製
界面活性剤(イゲパルCO-520)3.52gをシクロヘキサン25gに加え、溶液が透明になるまで攪拌する。これを2mL取り出して、先の金ナノ粒子分散溶液(X6)に激しく攪拌しながら滴下する。実施例2で作製したFe3O4ナノ粒子(粒径8nm)分散溶液(
Y6、pH11)を100μL取り出して、この逆ミセル溶液に滴下した。
【0197】
(3)ガラスビーズの作製
上記の逆ミセル溶液にTEOS150μLを加え、24時間攪拌して反応を進行させ、ガラスビーズを得た。
【0198】
実施例7(医薬品と半導体ナノ粒子が分散したガラスビーズ)
抗がん剤として知られるイブプロフェン(IBU)を、Flukaより購入した。最近の公知文献(アドバンスト ファンクショナル マテリアルズ、18巻、2780ページ(2008年))を参考にして、IBUをポリビニルアルコールの水溶液に分散させてポリビニルア
ルコールでコートし、アンモニア溶液(pH11)に10重量%となるように分散させた。実施例4の方法で作製したInPナノ粒子を、実施例2の方法でガラス相に分散させ、同時にIBUをガラス球内の空洞部分に分散させることができた。
【0199】
実施例8(抗体を接着したガラスビーズ)
実施例2で作製した蛍光性半導体ナノ粒子と磁性ナノ粒子が分散したガラスビーズ(0.3mL、10mmol/LのPBSバッファー溶液中)に、2−[メトキシ(ポリエチレ
ンオキシ)プロピル]トリメトキシシラン (CH3O(C2H4O)6-9C3H6Si(OCH3)3)を1μL加えて7時間攪拌した。さらに0.2mgのストレプトアビジン−マレイミド(シグマより購入)を10mmol/LのPBSバッファー溶液(20μL)に加えて3時間攪拌した。さ
らに、ビオチン−ストレプトアビジン−アフィニティ純ヤギ抗マウスIgG(重鎖+軽鎖)
(Biotin-SP-conjugatedAffiniPure Goat Anti-Mouse IgG(H+L),Jackson ImmunoResearc Laboratories, Inc.より購入)100μLを加えて5分間、攪拌した。このあと試料を4℃で24時間静置することで、IgGを接着させた。紫外線照射により発光することが、確
かめられた。
【特許請求の範囲】
【請求項1】
内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであって、該ケイ素系ガラス相にナノ粒子Aを含むことを特徴とするケイ素系ガラスビーズ。
【請求項2】
さらに前記ケイ素系ガラスビーズ内部の空洞に機能性物質を含む請求項1に記載のケイ素系ガラスビーズ。
【請求項3】
前記機能性物質がナノ粒子Bである請求項2に記載のケイ素系ガラスビーズ。
【請求項4】
前記ナノ粒子A及びナノ粒子Bの平均粒径がそれぞれ2〜20nmである請求項3に記載のケイ素系ガラスビーズ。
【請求項5】
前記ナノ粒子A及び/又はナノ粒子Bが半導体ナノ粒子である請求項3又は4に記載のケイ素系ガラスビーズ。
【請求項6】
前記ナノ粒子A及び/又はナノ粒子Bが、発光効率が20%以上の半導体ナノ粒子である請求項3〜5のいずれかに記載のケイ素系ガラスビーズ。
【請求項7】
前記半導体ナノ粒子が、CdTe、CdSe、CdS、ZnSe、ZnSe(1-x)Tex (但し、0 < x < 1)、ZnS、InP、InxGa(1-x)P (但し、0 < x < 1)、及びInAsからなる群より選ばれる少なくとも1種である請求項5又は6に記載のケイ素系ガラスビーズ。
【請求項8】
前記ナノ粒子A及び/又はナノ粒子Bが磁性を有するナノ粒子である請求項3〜7のいずれかに記載のケイ素系ガラスビーズ。
【請求項9】
前記磁性を有するナノ粒子が、Fe3O4、Fe2O3、CoFe2O4、MnFe2O4、NiFe2O4、CoCrFeO4、Pt、Co、PtCo、FePt、及びFeCoからなる群より選ばれる少なくとも1種である請求項8に
記載のケイ素系ガラスビーズ。
【請求項10】
印加磁界5kOeでの磁化が1〜200emu/gである、請求項8又は9に記載のケイ素
系ガラスビーズ。
【請求項11】
前記ナノ粒子A及び/又はナノ粒子Bが金属ナノ粒子である請求項3〜10のいずれかに記載のケイ素系ガラスビーズ。
【請求項12】
前記金属ナノ粒子の金属が、金(Au)、銀(Ag)及び銅(Cu)からなる群より選ばれる少なくとも1種である請求項11に記載のケイ素系ガラスビーズ。
【請求項13】
前記ケイ素系ガラスビーズ内の空洞の平均内径が10〜500nmである請求項1〜12のいずれかに記載のケイ素系ガラスビーズ。
【請求項14】
前記機能性物質が薬理活性物質である請求項2〜13のいずれかに記載のケイ素系ガラスビーズ。
【請求項15】
前記ケイ素系ガラスビーズの外表面に抗体が接着されてなる請求項1〜14のいずれかに記載のケイ素系ガラスビーズ。
【請求項16】
内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであり、該ケイ素系ガラス相にナノ粒子Aを含むケイ素系ガラスビーズの製造方法であって、
(1)疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する工程、及び
(2)上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する工程、
を含む製造方法。
【請求項17】
前記工程(2)において、アルカリ性水溶液Yが機能性物質を含む請求項16に記載の製造方法。
【請求項18】
前記工程(1)のナノ粒子Aを含むケイ素アルコキシド水溶液Xの水素イオン指数(pH
1)がpH1>7であり、かつ、前記工程(2)のアルカリ性水溶液Yの水素イオン指数(pH2)がpH1<pH2<14である請求項16又は17に記載の製造方法。
【請求項19】
前記工程(2)が、前記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加した後、さらにケイ素アルコキシドを添加してケイ素系ガラスビーズを形成する工程である請求項16〜18のいずれかに記載の製造方法。
【請求項20】
前記請求項1〜15のいずれかに記載のケイ素系ガラスビーズを含む蛍光試薬。
【請求項21】
前記請求項1〜15のいずれかに記載のケイ素系ガラスビーズを含む薬物運搬システム。
【請求項1】
内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであって、該ケイ素系ガラス相にナノ粒子Aを含むことを特徴とするケイ素系ガラスビーズ。
【請求項2】
さらに前記ケイ素系ガラスビーズ内部の空洞に機能性物質を含む請求項1に記載のケイ素系ガラスビーズ。
【請求項3】
前記機能性物質がナノ粒子Bである請求項2に記載のケイ素系ガラスビーズ。
【請求項4】
前記ナノ粒子A及びナノ粒子Bの平均粒径がそれぞれ2〜20nmである請求項3に記載のケイ素系ガラスビーズ。
【請求項5】
前記ナノ粒子A及び/又はナノ粒子Bが半導体ナノ粒子である請求項3又は4に記載のケイ素系ガラスビーズ。
【請求項6】
前記ナノ粒子A及び/又はナノ粒子Bが、発光効率が20%以上の半導体ナノ粒子である請求項3〜5のいずれかに記載のケイ素系ガラスビーズ。
【請求項7】
前記半導体ナノ粒子が、CdTe、CdSe、CdS、ZnSe、ZnSe(1-x)Tex (但し、0 < x < 1)、ZnS、InP、InxGa(1-x)P (但し、0 < x < 1)、及びInAsからなる群より選ばれる少なくとも1種である請求項5又は6に記載のケイ素系ガラスビーズ。
【請求項8】
前記ナノ粒子A及び/又はナノ粒子Bが磁性を有するナノ粒子である請求項3〜7のいずれかに記載のケイ素系ガラスビーズ。
【請求項9】
前記磁性を有するナノ粒子が、Fe3O4、Fe2O3、CoFe2O4、MnFe2O4、NiFe2O4、CoCrFeO4、Pt、Co、PtCo、FePt、及びFeCoからなる群より選ばれる少なくとも1種である請求項8に
記載のケイ素系ガラスビーズ。
【請求項10】
印加磁界5kOeでの磁化が1〜200emu/gである、請求項8又は9に記載のケイ素
系ガラスビーズ。
【請求項11】
前記ナノ粒子A及び/又はナノ粒子Bが金属ナノ粒子である請求項3〜10のいずれかに記載のケイ素系ガラスビーズ。
【請求項12】
前記金属ナノ粒子の金属が、金(Au)、銀(Ag)及び銅(Cu)からなる群より選ばれる少なくとも1種である請求項11に記載のケイ素系ガラスビーズ。
【請求項13】
前記ケイ素系ガラスビーズ内の空洞の平均内径が10〜500nmである請求項1〜12のいずれかに記載のケイ素系ガラスビーズ。
【請求項14】
前記機能性物質が薬理活性物質である請求項2〜13のいずれかに記載のケイ素系ガラスビーズ。
【請求項15】
前記ケイ素系ガラスビーズの外表面に抗体が接着されてなる請求項1〜14のいずれかに記載のケイ素系ガラスビーズ。
【請求項16】
内部に空洞を有する平均粒径20nm〜1μmのケイ素系ガラスビーズであり、該ケイ素系ガラス相にナノ粒子Aを含むケイ素系ガラスビーズの製造方法であって、
(1)疎水性有機溶媒及び界面活性剤を含む媒体と、ナノ粒子A及びケイ素アルコキシドを含む水溶液Xとを混合して逆ミセル溶液を調製する工程、及び
(2)上記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加してケイ素系ガラスビーズを形成する工程、
を含む製造方法。
【請求項17】
前記工程(2)において、アルカリ性水溶液Yが機能性物質を含む請求項16に記載の製造方法。
【請求項18】
前記工程(1)のナノ粒子Aを含むケイ素アルコキシド水溶液Xの水素イオン指数(pH
1)がpH1>7であり、かつ、前記工程(2)のアルカリ性水溶液Yの水素イオン指数(pH2)がpH1<pH2<14である請求項16又は17に記載の製造方法。
【請求項19】
前記工程(2)が、前記工程(1)の逆ミセル溶液に、アルカリ性水溶液Yを添加した後、さらにケイ素アルコキシドを添加してケイ素系ガラスビーズを形成する工程である請求項16〜18のいずれかに記載の製造方法。
【請求項20】
前記請求項1〜15のいずれかに記載のケイ素系ガラスビーズを含む蛍光試薬。
【請求項21】
前記請求項1〜15のいずれかに記載のケイ素系ガラスビーズを含む薬物運搬システム。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公開番号】特開2010−285335(P2010−285335A)
【公開日】平成22年12月24日(2010.12.24)
【国際特許分類】
【出願番号】特願2009−237846(P2009−237846)
【出願日】平成21年10月15日(2009.10.15)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成21年度独立行政法人科学技術振興機構「蛍光試薬用高輝度ナノ粒子分散ガラスビーズの開発」委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【Fターム(参考)】
【公開日】平成22年12月24日(2010.12.24)
【国際特許分類】
【出願日】平成21年10月15日(2009.10.15)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成21年度独立行政法人科学技術振興機構「蛍光試薬用高輝度ナノ粒子分散ガラスビーズの開発」委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【Fターム(参考)】
[ Back to top ]

