分析方法、粘着テープ及びペン
【課題】本発明は、DART又はDESIを用いて、試料に付着している化学物質の位置を検出するための基準の位置を設定すると共に、質量分析計を校正することが可能な分析方法並びに該分析方法に用いられる粘着テープ及びペンを提供することを目的とする。
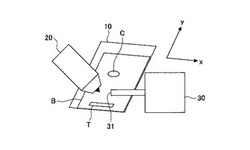
【解決手段】分析方法は、化学物質Cが付着している平板Bのx軸方向の化学物質Cを含む領域に、校正用試薬を含む粘着テープTを貼付する工程と、粘着テープTが貼付された平板Bを移動させながら、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンを平板Bの化学物質C及び粘着テープTに含まれる校正用試薬に付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析する工程を有する。
【解決手段】分析方法は、化学物質Cが付着している平板Bのx軸方向の化学物質Cを含む領域に、校正用試薬を含む粘着テープTを貼付する工程と、粘着テープTが貼付された平板Bを移動させながら、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンを平板Bの化学物質C及び粘着テープTに含まれる校正用試薬に付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析する工程を有する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、分析方法、粘着テープ及びペンに関する。
【背景技術】
【0002】
大気圧イオン化法として、種々の方法が知られているが、近年、DART(Direct Analysis in Real Time)や、DESI(Desorption Electrospray Ionization)が注目されている(特許文献1参照)。
【0003】
DARTは、電子励起状態の原子又は分子を大気中の水に衝突させてペニングイオン化させて生成したプロトンを試料に付加してイオン化する方法である。例えば、準安定励起状態のヘリウムHe*(23S)を用いると、以下のようにして、試料Mをイオン化することができる。
【0004】
He*(23S)+H2O→H2O+*+He(11S)+e−
H2O+*+H2O→H3O++OH*
H3O++nH2O→[(H2O)nH]+
[(H2O)nH]++M→MH++nH2O
DESIは、イオン化した溶媒を試料に付着させてイオンを脱離させる方法である。
【0005】
しかしながら、DART又はDESIを用いて、試料を測定する前に、校正用試薬を用いて質量分析計を校正しなければならないという問題がある。また、DART又はDESIを用いて、化学物質が付着している試料を移動させながら、化学物質の位置を検出する場合に、基準の位置を任意に設定することができないという問題がある。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2008−180659号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明は、上記の従来技術が有する問題に鑑み、DART又はDESIを用いて、試料に付着している化学物質の位置を検出するための基準の位置を設定すると共に、質量分析計を校正することが可能な分析方法並びに該分析方法に用いられる粘着テープ及びペンを提供することを目的とする。
【課題を解決するための手段】
【0008】
請求項1に記載の発明は、分析方法において、試料の所定の領域に、校正用試薬を含む層を形成する工程と、前記層が形成された試料を移動させながら、DART又はDESIを用いて、前記試料の前記層を含む領域から生成したイオンを質量分析する工程を有することを特徴とする。
【0009】
請求項2に記載の発明は、請求項1に記載の分析方法において、前記校正用試薬を含む粘着テープを貼付して前記校正用試薬を含む層を形成することを特徴とする。
【0010】
請求項3に記載の発明は、請求項1に記載の分析方法において、前記校正用試薬を含むインクが充填されているペンを用いて前記校正用試薬を含む層を形成することを特徴とする。
【0011】
請求項4に記載の発明は、粘着テープにおいて、校正用試薬を含むことを特徴とする。
【0012】
請求項5に記載の発明は、ペンにおいて、校正用試薬を含むインクが充填されていることを特徴とする。
【発明の効果】
【0013】
本発明によれば、DART又はDESIを用いて、試料に付着している化学物質の位置を検出するための基準の位置を設定すると共に、質量分析計を校正することが可能な分析方法並びに該分析方法に用いられる粘着テープ及びペンを提供することができる。
【図面の簡単な説明】
【0014】
【図1】本発明の分析方法の一例を示す模式図である。
【図2】本発明の分析方法の他の例を示す模式図である。
【図3】実施例1のマスクロマトグラムを示す図である。
【図4】図3の1.0minにおけるマススペクトルを示す図である。
【図5】図3の5.5minにおけるマススペクトルを示す図である。
【図6】実施例2のマスクロマトグラムを示す図である。
【図7】図6の3.2minにおけるマススペクトルを示す図である。
【図8】実施例3のマスクロマトグラムを示す図である。
【図9】図8の5.2minにおけるマススペクトルを示す図である。
【図10】実施例4のマスクロマトグラムを示す図である。
【図11】図10の1.1minにおけるマススペクトルを示す図である。
【図12】図10の2.0minにおけるマススペクトルを示す図である。
【発明を実施するための形態】
【0015】
次に、本発明を実施するための形態を図面と共に説明する。
【0016】
図1に、本発明の分析方法の一例を示す。まず、x軸方向及びy軸方向に移動することが可能なサンプルステージ10に、化学物質Cが付着している長方形の平板Bを載せる。次に、平板Bのx軸方向の化学物質Cを含む領域に、校正用試薬を含む粘着テープTを貼付する。さらに、サンプルステージ10をy軸方向に移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンを平板Bの化学物質C及び粘着テープTに含まれる校正用試薬に付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析する。このとき、サンプルステージ10をy軸方向に移動させる速度をv[mm/s]、x=xiにおけるマスクロマトグラムの校正用試薬由来のピークの頂点及び化学物質C由来のピークの開始点をそれぞれyi0[s]及びyi[s]とすると、x=xiにおける化学物質Cと粘着テープTのy軸方向の中点の間の間隔giは、式
gi=v(yi−yi0)
で表される。このとき、マスクロマトグラムの校正用試薬由来のピークにおけるマススペクトルを用いて、質量分析計30を校正することができる。
【0017】
校正用試薬としては、DARTイオン源20を用いてイオンを生成させることが可能であれば、特に限定されないが、校正の精度を考慮すると、マススペクトルのピークが等間隔で存在するポリエチレングリコール(PEG60〜PEG2000)、炭素数が4〜36の脂肪酸等が挙げられ、二種以上併用してもよい。
【0018】
校正用試薬を含む粘着テープTは、例えば、校正用試薬を溶媒に溶解させた溶液を公知の粘着テープに塗布することにより得られる。
【0019】
準安定励起状態のヘリウムHe*(23S)の代わりに、準安定励起状態のネオン、準安定励起状態のアルゴン、準安定励起状態の窒素等を用いてもよい。
【0020】
試料としては、DARTイオン源20を用いてイオンを生成させることが可能であれば、化学物質Cが付着している長方形の平板Bに限定されない。
【0021】
図2に、本発明の分析方法の他の例を示す。まず、x軸方向及びy軸方向に移動することが可能なサンプルステージ10に、化学物質Cが付着している長方形の平板Bを載せる。次に、平板Bのx軸方向の化学物質Cを含む領域に、校正用試薬を含むインクが充填されているペンPを用いて基準線Lを描画する。さらに、サンプルステージ10を移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンを平板Bの化学物質C及び基準線Lに含まれる校正用試薬に付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析する。
【0022】
校正用試薬を含むインクは、例えば、校正用試薬を溶媒に溶解させた溶液を公知のインクに添加することにより得られる。また、ペンPは、例えば、校正用試薬を含むインクを公知のペンに充填することにより得られる。
【0023】
本発明において、校正用試薬を含む層を形成する方法としては、図1又は図2に示す方法に限定されず、筆を用いて塗布する方法等が挙げられる。
【0024】
また、DARTイオン源20の代わりに、DESIイオン源を用いて、イオン化した溶媒を試料に付着させてイオンを脱離させてもよい。
【0025】
イオン化させる溶媒としては、特に限定されないが、メタノール、メタノール水溶液、アセトニトリル、アセトニトリル水溶液等が挙げられる。
【0026】
なお、イオン化させる溶媒は、酸性物質や塩基性物質を含んでいてもよい。
【0027】
校正用試薬としては、DESIイオン源を用いてイオンを生成させることが可能であれば、特に限定されないが、校正の精度を考慮すると、マススペクトルのピークが等間隔で存在するポリエチレングリコール(PEG60〜PEG2000)、炭素数が4〜36の脂肪酸等が挙げられ、二種以上併用してもよい。
【0028】
試料としては、DESIイオン源を用いてイオンを生成させることが可能であれば、特に限定されない。
【実施例】
【0029】
[粘着テープTの作製]
インクジェットプリンタ用ラベルシート(コクヨ社製)に、1mm×17mmの切り込みを複数入れた後、平均分子量が180〜220のポリエチレングリコール200(和光純薬社製)の1g/Lメタノール溶液5mL及び平均分子量が380〜420のポリエチレングリコール400(関東化学社製)の1g/Lメタノール溶液5mLの混合液を均等に噴霧し、粘着テープTを得た。
【0030】
[ペンPの作製]
アートライン ウエットライト 補充インキ(赤色)(シャチハタ社製)1mLに、平均分子量が180〜220のポリエチレングリコール200(和光純薬社製)0.5mL及び平均分子量が380〜420のポリエチレングリコール400(関東化学社製)0.5mLを添加して攪拌し、インクを得た。
【0031】
得られたインクを、アートライン ウエットライト(赤色)(シャチハタ社製)に充填し、ペンPを得た。
【0032】
[実施例1]
スライドガラスに、尿素、リドカイン、ジフェンヒドラミンを含む医薬品外用剤1を塗布した後、図1の分析方法を用いて分析した。具体的には、まず、医薬品外用剤1が塗布されたスライドガラスをサンプルステージ10に載せた後、スライドガラスのx軸方向の医薬品外用剤1が塗布された領域を含む領域に、医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔が48mmとなるように粘着テープTを貼付した。次に、サンプルステージ10をy軸方向に0.2mm/sで移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンをスライドガラスの医薬品外用剤1に含まれる尿素、リドカイン、ジフェンヒドラミン及び粘着テープTに含まれるポリエチレングリコールに付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析した。
【0033】
このとき、DARTイオン源20として、DART SVP(エーエムアール社製)を用い、ガスヒーターの温度を500℃とした。また、質量分析計30として、MicrOTOFQII(ブルカー ダルトニクス社製)を用い、測定モードをpositive ion modeとした。
【0034】
図3に、得られたマスクロマトグラムを示す。なお、図3(a)、(b)、(c)及び(d)は、それぞれポリエチレングリコール(m/z=195)、尿素(m/z=61)、リドカイン(m/z=235)及びジフェンヒドラミン(m/z=256)のマスクロマトグラムである。
【0035】
図3から、ポリエチレングリコール由来のピークの頂点、尿素由来のピークの開始点、リドカイン由来のピークの開始点及びジフェンヒドラミン由来のピークの開始点は、それぞれ1min、5min、5min及び5minであることがわかる。このことから、医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔は48mmとなり、精度よく測定できることがわかる。
【0036】
図4及び図5に、それぞれ図3の1.0min及び5.5minにおけるマススペクトルを示す。
【0037】
図4から、ポリエチレングリコール由来のピーク(m/z=151、195、239、283)が存在していることがわかる。なお、これらのピークを用いて、質量分析計30を校正した。
【0038】
図5から、尿素由来のピーク(m/z=61)、リドカイン由来のピーク(m/z=235)及びジフェンヒドラミン由来のピーク(m/z=256)が存在していることがわかる。
【0039】
[実施例2]
スライドガラスの代わりに、軍手を用い、y軸方向の医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔が24mmとなるように粘着テープTを貼付した以外は、実施例1と同様にして、分析した。
【0040】
図6に、得られたマスクロマトグラムを示す。なお、図6(a)、(b)、(c)及び(d)は、それぞれポリエチレングリコール(m/z=195)、尿素(m/z=61)、リドカイン(m/z=235)及びジフェンヒドラミン(m/z=256)のマスクロマトグラムである。
【0041】
図6から、ポリエチレングリコール由来のピークの頂点、尿素由来のピークの開始点、リドカイン由来のピークの開始点及びジフェンヒドラミン由来のピークの開始点は、それぞれ1min、3min、3min及び3minであることがわかる。このことから、医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔は24mmとなり、精度よく測定できることがわかる。
【0042】
図7に、図6の3.2minにおけるマススペクトルを示す。
【0043】
図7から、尿素由来のピーク(m/z=61)、リドカイン由来のピーク(m/z=235)及びジフェンヒドラミン由来のピーク(m/z=256)が存在していることがわかる。
【0044】
[実施例3]
スライドガラス及び医薬品外用剤1の代わりに、それぞれ箱及びジフェンヒドラミンを含む医薬品外用剤2を用い、y軸方向の医薬品外用剤2が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔が40.8mmとなるように粘着テープTを貼付した以外は、実施例1と同様にして、分析した。
【0045】
図8に、得られたマスクロマトグラムを示す。なお、図8(a)及び(b)は、それぞれポリエチレングリコール(m/z=195)及びジフェンヒドラミン(m/z=256)のマスクロマトグラムである。
【0046】
図8から、ポリエチレングリコール由来のピークの頂点及びジフェンヒドラミン由来のピークの開始点は、それぞれ1.3min及び4.7minであることがわかる。このことから、医薬品外用剤2が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔は40.8mmとなり、精度よく測定できることがわかる。
【0047】
図9に、図8の5.2minにおけるマススペクトルを示す。
【0048】
図9から、ジフェンヒドラミン由来のピーク(m/z=256)が存在していることがわかる。
【0049】
[実施例4]
スライドガラスに、フタル酸ジメチルの1g/Lメタノール溶液(以下、溶液1という)10μL、フタル酸ジエチルの1g/Lメタノール溶液(以下、溶液2という)10μL及びフタル酸ジイソプロピルの1g/Lメタノール溶液(以下、溶液3という)10μLを24mm間隔で直線状に塗布した。次に、図2に示す分析方法を用いて分析した。具体的には、まず、溶液1〜3が塗布されたスライドガラスをサンプルステージ10に載せた後、スライドガラスのx軸方向の溶液1〜3が塗布された領域を含む領域に、溶液1が塗布された領域と基準線Lのy軸方向の中点の間のy軸方向の間隔が7.2mmとなるようにペンPを用いて基準線Lを描画した。次に、サンプルステージ10をy軸方向に0.2mm/sで移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンをスライドガラスのフタル酸ジメチル、フタル酸ジエチル、フタル酸ジイソプロピル及び基準線Lに含まれるポリエチレングリコールに付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析した。
【0050】
図10に、得られたマスクロマトグラムを示す。なお、図10(a)、(b)、(c)及び(d)は、それぞれポリエチレングリコール(m/z=327)、フタル酸ジメチル(m/z=195)、フタル酸ジエチル(m/z=223)及びフタル酸ジイソプロピル(m/z=251)のマスクロマトグラムである。
【0051】
図10から、ポリエチレングリコール由来のピークの頂点、フタル酸ジメチル由来のピークの開始点、フタル酸ジエチル由来のピークの開始点及びフタル酸ジイソプロピル由来のピークの開始点は、それぞれ1.1min、1.7min、3.7min及び5.7minであることがわかる。このことから、溶液1が塗布された領域、溶液2が塗布された領域及び溶液3が塗布された領域と、基準線Lのy軸方向の中点の間のy軸方向の間隔は、それぞれ7.2mm、31.2mm及び55.2mmとなり、溶液1、溶液2及び溶液3が24mm間隔で塗布されていることが確認され、精度よく測定できることがわかる。
【0052】
図11及び図12に、それぞれ図10の1.1min及び2.0minにおけるマススペクトルを示す。
【0053】
図11から、ポリエチレングリコール由来のピーク(m/z=195、239、283、327)が存在していることがわかる。なお、これらのピークを用いて、質量分析計30を校正した。
【0054】
図12から、フタル酸ジメチル由来のピーク(m/z=195)が存在していることがわかる。
【符号の説明】
【0055】
10 サンプルステージ
20 DARTイオン源
30 質量分析計
31 イオン導入口
B 平板
C 化学物質
T 粘着テープ
L 基準線
P ペン
【技術分野】
【0001】
本発明は、分析方法、粘着テープ及びペンに関する。
【背景技術】
【0002】
大気圧イオン化法として、種々の方法が知られているが、近年、DART(Direct Analysis in Real Time)や、DESI(Desorption Electrospray Ionization)が注目されている(特許文献1参照)。
【0003】
DARTは、電子励起状態の原子又は分子を大気中の水に衝突させてペニングイオン化させて生成したプロトンを試料に付加してイオン化する方法である。例えば、準安定励起状態のヘリウムHe*(23S)を用いると、以下のようにして、試料Mをイオン化することができる。
【0004】
He*(23S)+H2O→H2O+*+He(11S)+e−
H2O+*+H2O→H3O++OH*
H3O++nH2O→[(H2O)nH]+
[(H2O)nH]++M→MH++nH2O
DESIは、イオン化した溶媒を試料に付着させてイオンを脱離させる方法である。
【0005】
しかしながら、DART又はDESIを用いて、試料を測定する前に、校正用試薬を用いて質量分析計を校正しなければならないという問題がある。また、DART又はDESIを用いて、化学物質が付着している試料を移動させながら、化学物質の位置を検出する場合に、基準の位置を任意に設定することができないという問題がある。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2008−180659号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明は、上記の従来技術が有する問題に鑑み、DART又はDESIを用いて、試料に付着している化学物質の位置を検出するための基準の位置を設定すると共に、質量分析計を校正することが可能な分析方法並びに該分析方法に用いられる粘着テープ及びペンを提供することを目的とする。
【課題を解決するための手段】
【0008】
請求項1に記載の発明は、分析方法において、試料の所定の領域に、校正用試薬を含む層を形成する工程と、前記層が形成された試料を移動させながら、DART又はDESIを用いて、前記試料の前記層を含む領域から生成したイオンを質量分析する工程を有することを特徴とする。
【0009】
請求項2に記載の発明は、請求項1に記載の分析方法において、前記校正用試薬を含む粘着テープを貼付して前記校正用試薬を含む層を形成することを特徴とする。
【0010】
請求項3に記載の発明は、請求項1に記載の分析方法において、前記校正用試薬を含むインクが充填されているペンを用いて前記校正用試薬を含む層を形成することを特徴とする。
【0011】
請求項4に記載の発明は、粘着テープにおいて、校正用試薬を含むことを特徴とする。
【0012】
請求項5に記載の発明は、ペンにおいて、校正用試薬を含むインクが充填されていることを特徴とする。
【発明の効果】
【0013】
本発明によれば、DART又はDESIを用いて、試料に付着している化学物質の位置を検出するための基準の位置を設定すると共に、質量分析計を校正することが可能な分析方法並びに該分析方法に用いられる粘着テープ及びペンを提供することができる。
【図面の簡単な説明】
【0014】
【図1】本発明の分析方法の一例を示す模式図である。
【図2】本発明の分析方法の他の例を示す模式図である。
【図3】実施例1のマスクロマトグラムを示す図である。
【図4】図3の1.0minにおけるマススペクトルを示す図である。
【図5】図3の5.5minにおけるマススペクトルを示す図である。
【図6】実施例2のマスクロマトグラムを示す図である。
【図7】図6の3.2minにおけるマススペクトルを示す図である。
【図8】実施例3のマスクロマトグラムを示す図である。
【図9】図8の5.2minにおけるマススペクトルを示す図である。
【図10】実施例4のマスクロマトグラムを示す図である。
【図11】図10の1.1minにおけるマススペクトルを示す図である。
【図12】図10の2.0minにおけるマススペクトルを示す図である。
【発明を実施するための形態】
【0015】
次に、本発明を実施するための形態を図面と共に説明する。
【0016】
図1に、本発明の分析方法の一例を示す。まず、x軸方向及びy軸方向に移動することが可能なサンプルステージ10に、化学物質Cが付着している長方形の平板Bを載せる。次に、平板Bのx軸方向の化学物質Cを含む領域に、校正用試薬を含む粘着テープTを貼付する。さらに、サンプルステージ10をy軸方向に移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンを平板Bの化学物質C及び粘着テープTに含まれる校正用試薬に付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析する。このとき、サンプルステージ10をy軸方向に移動させる速度をv[mm/s]、x=xiにおけるマスクロマトグラムの校正用試薬由来のピークの頂点及び化学物質C由来のピークの開始点をそれぞれyi0[s]及びyi[s]とすると、x=xiにおける化学物質Cと粘着テープTのy軸方向の中点の間の間隔giは、式
gi=v(yi−yi0)
で表される。このとき、マスクロマトグラムの校正用試薬由来のピークにおけるマススペクトルを用いて、質量分析計30を校正することができる。
【0017】
校正用試薬としては、DARTイオン源20を用いてイオンを生成させることが可能であれば、特に限定されないが、校正の精度を考慮すると、マススペクトルのピークが等間隔で存在するポリエチレングリコール(PEG60〜PEG2000)、炭素数が4〜36の脂肪酸等が挙げられ、二種以上併用してもよい。
【0018】
校正用試薬を含む粘着テープTは、例えば、校正用試薬を溶媒に溶解させた溶液を公知の粘着テープに塗布することにより得られる。
【0019】
準安定励起状態のヘリウムHe*(23S)の代わりに、準安定励起状態のネオン、準安定励起状態のアルゴン、準安定励起状態の窒素等を用いてもよい。
【0020】
試料としては、DARTイオン源20を用いてイオンを生成させることが可能であれば、化学物質Cが付着している長方形の平板Bに限定されない。
【0021】
図2に、本発明の分析方法の他の例を示す。まず、x軸方向及びy軸方向に移動することが可能なサンプルステージ10に、化学物質Cが付着している長方形の平板Bを載せる。次に、平板Bのx軸方向の化学物質Cを含む領域に、校正用試薬を含むインクが充填されているペンPを用いて基準線Lを描画する。さらに、サンプルステージ10を移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンを平板Bの化学物質C及び基準線Lに含まれる校正用試薬に付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析する。
【0022】
校正用試薬を含むインクは、例えば、校正用試薬を溶媒に溶解させた溶液を公知のインクに添加することにより得られる。また、ペンPは、例えば、校正用試薬を含むインクを公知のペンに充填することにより得られる。
【0023】
本発明において、校正用試薬を含む層を形成する方法としては、図1又は図2に示す方法に限定されず、筆を用いて塗布する方法等が挙げられる。
【0024】
また、DARTイオン源20の代わりに、DESIイオン源を用いて、イオン化した溶媒を試料に付着させてイオンを脱離させてもよい。
【0025】
イオン化させる溶媒としては、特に限定されないが、メタノール、メタノール水溶液、アセトニトリル、アセトニトリル水溶液等が挙げられる。
【0026】
なお、イオン化させる溶媒は、酸性物質や塩基性物質を含んでいてもよい。
【0027】
校正用試薬としては、DESIイオン源を用いてイオンを生成させることが可能であれば、特に限定されないが、校正の精度を考慮すると、マススペクトルのピークが等間隔で存在するポリエチレングリコール(PEG60〜PEG2000)、炭素数が4〜36の脂肪酸等が挙げられ、二種以上併用してもよい。
【0028】
試料としては、DESIイオン源を用いてイオンを生成させることが可能であれば、特に限定されない。
【実施例】
【0029】
[粘着テープTの作製]
インクジェットプリンタ用ラベルシート(コクヨ社製)に、1mm×17mmの切り込みを複数入れた後、平均分子量が180〜220のポリエチレングリコール200(和光純薬社製)の1g/Lメタノール溶液5mL及び平均分子量が380〜420のポリエチレングリコール400(関東化学社製)の1g/Lメタノール溶液5mLの混合液を均等に噴霧し、粘着テープTを得た。
【0030】
[ペンPの作製]
アートライン ウエットライト 補充インキ(赤色)(シャチハタ社製)1mLに、平均分子量が180〜220のポリエチレングリコール200(和光純薬社製)0.5mL及び平均分子量が380〜420のポリエチレングリコール400(関東化学社製)0.5mLを添加して攪拌し、インクを得た。
【0031】
得られたインクを、アートライン ウエットライト(赤色)(シャチハタ社製)に充填し、ペンPを得た。
【0032】
[実施例1]
スライドガラスに、尿素、リドカイン、ジフェンヒドラミンを含む医薬品外用剤1を塗布した後、図1の分析方法を用いて分析した。具体的には、まず、医薬品外用剤1が塗布されたスライドガラスをサンプルステージ10に載せた後、スライドガラスのx軸方向の医薬品外用剤1が塗布された領域を含む領域に、医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔が48mmとなるように粘着テープTを貼付した。次に、サンプルステージ10をy軸方向に0.2mm/sで移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンをスライドガラスの医薬品外用剤1に含まれる尿素、リドカイン、ジフェンヒドラミン及び粘着テープTに含まれるポリエチレングリコールに付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析した。
【0033】
このとき、DARTイオン源20として、DART SVP(エーエムアール社製)を用い、ガスヒーターの温度を500℃とした。また、質量分析計30として、MicrOTOFQII(ブルカー ダルトニクス社製)を用い、測定モードをpositive ion modeとした。
【0034】
図3に、得られたマスクロマトグラムを示す。なお、図3(a)、(b)、(c)及び(d)は、それぞれポリエチレングリコール(m/z=195)、尿素(m/z=61)、リドカイン(m/z=235)及びジフェンヒドラミン(m/z=256)のマスクロマトグラムである。
【0035】
図3から、ポリエチレングリコール由来のピークの頂点、尿素由来のピークの開始点、リドカイン由来のピークの開始点及びジフェンヒドラミン由来のピークの開始点は、それぞれ1min、5min、5min及び5minであることがわかる。このことから、医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔は48mmとなり、精度よく測定できることがわかる。
【0036】
図4及び図5に、それぞれ図3の1.0min及び5.5minにおけるマススペクトルを示す。
【0037】
図4から、ポリエチレングリコール由来のピーク(m/z=151、195、239、283)が存在していることがわかる。なお、これらのピークを用いて、質量分析計30を校正した。
【0038】
図5から、尿素由来のピーク(m/z=61)、リドカイン由来のピーク(m/z=235)及びジフェンヒドラミン由来のピーク(m/z=256)が存在していることがわかる。
【0039】
[実施例2]
スライドガラスの代わりに、軍手を用い、y軸方向の医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔が24mmとなるように粘着テープTを貼付した以外は、実施例1と同様にして、分析した。
【0040】
図6に、得られたマスクロマトグラムを示す。なお、図6(a)、(b)、(c)及び(d)は、それぞれポリエチレングリコール(m/z=195)、尿素(m/z=61)、リドカイン(m/z=235)及びジフェンヒドラミン(m/z=256)のマスクロマトグラムである。
【0041】
図6から、ポリエチレングリコール由来のピークの頂点、尿素由来のピークの開始点、リドカイン由来のピークの開始点及びジフェンヒドラミン由来のピークの開始点は、それぞれ1min、3min、3min及び3minであることがわかる。このことから、医薬品外用剤1が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔は24mmとなり、精度よく測定できることがわかる。
【0042】
図7に、図6の3.2minにおけるマススペクトルを示す。
【0043】
図7から、尿素由来のピーク(m/z=61)、リドカイン由来のピーク(m/z=235)及びジフェンヒドラミン由来のピーク(m/z=256)が存在していることがわかる。
【0044】
[実施例3]
スライドガラス及び医薬品外用剤1の代わりに、それぞれ箱及びジフェンヒドラミンを含む医薬品外用剤2を用い、y軸方向の医薬品外用剤2が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔が40.8mmとなるように粘着テープTを貼付した以外は、実施例1と同様にして、分析した。
【0045】
図8に、得られたマスクロマトグラムを示す。なお、図8(a)及び(b)は、それぞれポリエチレングリコール(m/z=195)及びジフェンヒドラミン(m/z=256)のマスクロマトグラムである。
【0046】
図8から、ポリエチレングリコール由来のピークの頂点及びジフェンヒドラミン由来のピークの開始点は、それぞれ1.3min及び4.7minであることがわかる。このことから、医薬品外用剤2が塗布された領域と粘着テープTのy軸方向の中点の間のy軸方向の間隔は40.8mmとなり、精度よく測定できることがわかる。
【0047】
図9に、図8の5.2minにおけるマススペクトルを示す。
【0048】
図9から、ジフェンヒドラミン由来のピーク(m/z=256)が存在していることがわかる。
【0049】
[実施例4]
スライドガラスに、フタル酸ジメチルの1g/Lメタノール溶液(以下、溶液1という)10μL、フタル酸ジエチルの1g/Lメタノール溶液(以下、溶液2という)10μL及びフタル酸ジイソプロピルの1g/Lメタノール溶液(以下、溶液3という)10μLを24mm間隔で直線状に塗布した。次に、図2に示す分析方法を用いて分析した。具体的には、まず、溶液1〜3が塗布されたスライドガラスをサンプルステージ10に載せた後、スライドガラスのx軸方向の溶液1〜3が塗布された領域を含む領域に、溶液1が塗布された領域と基準線Lのy軸方向の中点の間のy軸方向の間隔が7.2mmとなるようにペンPを用いて基準線Lを描画した。次に、サンプルステージ10をy軸方向に0.2mm/sで移動させながら、DARTイオン源20を用いて、準安定励起状態のヘリウムHe*(23S)を大気中の水に衝突させてペニングイオン化させて生成したプロトンをスライドガラスのフタル酸ジメチル、フタル酸ジエチル、フタル酸ジイソプロピル及び基準線Lに含まれるポリエチレングリコールに付加して生成したイオンを、質量分析計30のイオン導入口31に導入して質量分析した。
【0050】
図10に、得られたマスクロマトグラムを示す。なお、図10(a)、(b)、(c)及び(d)は、それぞれポリエチレングリコール(m/z=327)、フタル酸ジメチル(m/z=195)、フタル酸ジエチル(m/z=223)及びフタル酸ジイソプロピル(m/z=251)のマスクロマトグラムである。
【0051】
図10から、ポリエチレングリコール由来のピークの頂点、フタル酸ジメチル由来のピークの開始点、フタル酸ジエチル由来のピークの開始点及びフタル酸ジイソプロピル由来のピークの開始点は、それぞれ1.1min、1.7min、3.7min及び5.7minであることがわかる。このことから、溶液1が塗布された領域、溶液2が塗布された領域及び溶液3が塗布された領域と、基準線Lのy軸方向の中点の間のy軸方向の間隔は、それぞれ7.2mm、31.2mm及び55.2mmとなり、溶液1、溶液2及び溶液3が24mm間隔で塗布されていることが確認され、精度よく測定できることがわかる。
【0052】
図11及び図12に、それぞれ図10の1.1min及び2.0minにおけるマススペクトルを示す。
【0053】
図11から、ポリエチレングリコール由来のピーク(m/z=195、239、283、327)が存在していることがわかる。なお、これらのピークを用いて、質量分析計30を校正した。
【0054】
図12から、フタル酸ジメチル由来のピーク(m/z=195)が存在していることがわかる。
【符号の説明】
【0055】
10 サンプルステージ
20 DARTイオン源
30 質量分析計
31 イオン導入口
B 平板
C 化学物質
T 粘着テープ
L 基準線
P ペン
【特許請求の範囲】
【請求項1】
試料の所定の領域に、校正用試薬を含む層を形成する工程と、
前記層が形成された試料を移動させながら、DART又はDESIを用いて、前記試料の前記層を含む領域から生成したイオンを質量分析する工程を有することを特徴とする分析方法。
【請求項2】
前記校正用試薬を含む粘着テープを貼付して前記校正用試薬を含む層を形成することを特徴とする請求項1に記載の分析方法。
【請求項3】
前記校正用試薬を含むインクが充填されているペンを用いて前記校正用試薬を含む層を形成することを特徴とする請求項1に記載の分析方法。
【請求項4】
校正用試薬を含むことを特徴とする粘着テープ。
【請求項5】
校正用試薬を含むインクが充填されていることを特徴とするペン。
【請求項1】
試料の所定の領域に、校正用試薬を含む層を形成する工程と、
前記層が形成された試料を移動させながら、DART又はDESIを用いて、前記試料の前記層を含む領域から生成したイオンを質量分析する工程を有することを特徴とする分析方法。
【請求項2】
前記校正用試薬を含む粘着テープを貼付して前記校正用試薬を含む層を形成することを特徴とする請求項1に記載の分析方法。
【請求項3】
前記校正用試薬を含むインクが充填されているペンを用いて前記校正用試薬を含む層を形成することを特徴とする請求項1に記載の分析方法。
【請求項4】
校正用試薬を含むことを特徴とする粘着テープ。
【請求項5】
校正用試薬を含むインクが充填されていることを特徴とするペン。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【公開番号】特開2012−83138(P2012−83138A)
【公開日】平成24年4月26日(2012.4.26)
【国際特許分類】
【出願番号】特願2010−227728(P2010−227728)
【出願日】平成22年10月7日(2010.10.7)
【出願人】(000001959)株式会社 資生堂 (1,748)
【Fターム(参考)】
【公開日】平成24年4月26日(2012.4.26)
【国際特許分類】
【出願日】平成22年10月7日(2010.10.7)
【出願人】(000001959)株式会社 資生堂 (1,748)
【Fターム(参考)】
[ Back to top ]

