分離膜、これを備える水素分離膜、および該水素分離膜を備える水素分離装置
【課題】水素透過特性および酸化安定性に優れており、水素脆性破壊が抑制された分離膜を提供する。
【解決手段】少なくとも1種の5族元素およびIrを含む合金を含み、前記合金は体心立方型結晶構造を含む分離膜、該分離膜を含む水素分離膜、および該水素分離膜を備える装置。
【解決手段】少なくとも1種の5族元素およびIrを含む合金を含み、前記合金は体心立方型結晶構造を含む分離膜、該分離膜を含む水素分離膜、および該水素分離膜を備える装置。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、分離膜、これを備える水素分離膜、および該水素分離膜を備える水素分離装置に関する。
【背景技術】
【0002】
水素ガスが含有されているガス混合物から水素ガスのみを選択的に分離する分離膜として、既存のPd系金属がよく知られている。Pd系金属は、面心立方構造(FCC: face−centered cubic)を形成して、単位格子内の空間を用いた水素の溶解および拡散により水素の選択的な分離が行われる。しかしながら、Pd系金属が高コストであること、および水素透過度を向上させ難いことは、相溶化の制限要因として働く。
【0003】
これに伴い、Pd系金属と同じ程度の優れた水素透過性能を有し、かつ価格競争力のある水素分離膜への要求が急増している。
【0004】
Pdに代替する分離膜として、多孔性分離膜、非晶質系金属分離膜、または4族元素もしくは5族元素を用いた分離膜への取り組みが行われている。
【0005】
多孔性分離膜は、気孔径によりガスを分離するものである。しかしながら、現実的に、気孔径を同じ寸法に、しかも、完璧な球状に製造することは困難であるため、選択度、例えば、二酸化炭素の透過度に対する水素ガスの透過度の比が低いという問題がある。
【0006】
非晶質系金属分離膜の場合、金属を溶融状態で急冷して製造するため、急冷可能な組成および工程が制限されるという欠点を有している。実際に、分離膜の使用温度が250〜500℃と高温であるため、非晶質系金属分離膜は高温下での結晶化に伴う耐久性の低下の問題があり、これを解消するための技術が望まれる。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2006−95521号公報
【特許文献2】特開2003−1381号公報
【特許文献3】米国特許出願公開第2010/0247944号明細書
【特許文献4】米国特許出願公開第2004/0129135号明細書
【非特許文献】
【0008】
【非特許文献1】M.D. Dolan, J. Membrane Science, 362, 12−28, 2010
【発明の概要】
【発明が解決しようとする課題】
【0009】
本発明の目的は、水素透過特性および酸化安定性に優れており、水素脆性破壊が抑制された分離膜を提供することである。
【0010】
本発明の他の目的は、前記分離膜を備える水素分離膜を提供することである。
【0011】
本発明のさらに他の目的は、前記水素分離膜を備える水素分離装置を提供することである。
【課題を解決するための手段】
【0012】
本発明の一実施形態によれば、少なくとも1種の5族元素およびIrを含む合金を含み、前記合金は体心立方型結晶構造を含む、分離膜を提供する。
【発明の効果】
【0013】
本発明によれば、水素透過特性および酸化安定性に優れており、水素脆性破壊が抑制された分離膜が提供される。なお、これを備える水素分離膜によれば、高純度の水素を分離することができ、耐久性が効果的に改善される。
【図面の簡単な説明】
【0014】
【図1A】本発明の一実施形態に係る分離膜が形成可能な結晶格子を示す模式図である。
【図1B】本発明の一実施形態に係る分離膜が形成可能な結晶格子を示す模式図である。
【図2】本発明の他の実施形態に係る水素分離膜を通過して、水素ガスが分離されるメカニズムを示す模式図である。
【図3】実施例2〜4、および比較例1に従い製造された水素分離膜に対するPCT(pressure−concentration−temperature)評価結果を示すグラフである。
【図4】実施例5〜8に従い製造された水素分離膜の組成に対するX線回折(XRD:X−ray diffraction analysis)測定結果を示すグラフである。
【図5】実施例2〜3および比較例1に従い製造された水素分離膜に対するXRD評価結果を示すグラフである。
【図6A】比較例1に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図6B】比較例1に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図7A】実施例6に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図7B】実施例6に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図8】実施例2および比較例2に従い製造された水素分離膜に対する水素透過特性の測定結果を示すグラフである。
【図9】実施例6および比較例3に従い製造された水素分離膜に対する水素透過特性の測定結果を示すグラフである。
【図10A】実施例2に従い製造された水素分離膜に対する、熱重量分析法(Thermo Gravimetric Analysis;TGA)による評価結果を示すグラフである。
【図10B】実施例2に従い製造された水素分離膜に対する、熱重量分析法(Thermo Gravimetric Analysis;TGA)による評価結果を示すグラフである。
【図11A】実施例4に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図11B】実施例4に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図12A】比較例1に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図12B】比較例1に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図13】本発明の一実施形態に係る水素分離装置の模式図である。
【図14】本発明の他の実施形態に係る管状の水素分離膜を備える水素分離装置の模式図である。
【発明を実施するための形態】
【0015】
以下、本発明の一実施形態について本発明が属する技術分野において通常の知識を有する者が容易に実施できる程度に詳細に説明する。しかしながら、本発明は種々の異なる形態に実現可能であり、ここで説明する実施形態に限定されるものではない。
【0016】
本発明は種々の異なる形態に実現可能であり、必要に応じて、図面に基づいて説明され、ここで説明する実施形態に限定されない。本明細書の図面に示す各構成要素の大きさおよび厚さは説明の便宜のために任意に示されており、本発明が必ずしも図示のところに限定されるとは限らない。なお、図示した各構成要素の大きさおよび厚さは説明の便宜のために任意に誇張されており、本発明が必ずしも図示のところに限定されるとは限らない。
【0017】
本発明の一実施形態によれば、少なくとも1種の5族元素およびIrを含む合金を含み、前記合金が体心立方型(BCC:body−centered cubic)結晶構造を含む分離膜を提供する。
【0018】
前記分離膜は、特定のガスを選択的に分離するための分離膜として用いられることが好ましい。
【0019】
4族元素または5族元素の金属分離膜の場合、高い水素固溶による水素耐久性の低下を引き起こす脆性破壊が発生する虞がある。また、金属系の分離膜は高温下で酸化されるため、性能が低下する虞がある。このため、4族元素または5族元素の金属分離膜は水素固溶による金属水素化物の生成を抑えて水素脆性破壊を克服し、同時に高い透過度を維持するための研究が必要である。
【0020】
本発明の一実施形態に係る分離膜は、前記のような合金を含むことにより、ポリマー製の分離膜に比べて高温条件下で作動可能であるというメリットがある。また、本発明の分離膜は、5族系の金属を用いるにも拘わらず、低い水素固溶度を維持し、これにより、水素脆性破壊を抑えるとともに、高い水素透過度を維持することができる。なお、本発明の分離膜は、結晶構造が形成可能な合金を含むことにより、非晶質系金属分離膜に比べて非晶質の結晶化による性能低下の問題点がなく、耐久性の面で有利である。
【0021】
本発明の一実施形態によれば、前記合金は、5族元素およびIrを含み、これもまた結晶構造を形成することができる。
【0022】
前記合金の前記結晶構造は、体心立方型(BCC:body−centered cubic)構造に加えて、面心立方型(FCC:face−centered cubic)構造、六方最密充填型(HCP:hexagonal closed packed)構造またはこれらの組み合わせとすることができる。
【0023】
5族金属は、体心立方型(BCC:body−centered cubic)の結晶構造を取り得ることが知られており、これは、結晶系の表面に相当する特定のX線回折(XRD)ピークによって確認することができる。
【0024】
本発明の一実施形態に係る合金は5族金属およびIrを含み、前記合金が、5族金属だけではなく、Irを含むにも拘わらず、依然として体心立方型(BCC)構造を含む結晶構造を形成することができる(図4参照)。
【0025】
本発明に係る合金が10原子%以下のIrを含む場合、本発明に係る合金は、ほとんどが体心立方型(BCC)の結晶構造を形成することができる。
【0026】
Irの量が増えるに従って、本発明に係る合金は、面心立方構造(FCC)、六方最密充填構造(HCP)またはこれらの組み合わせをさらに含むことができる。
【0027】
このため、本発明の一実施形態に係る分離膜内の合金は、好ましくは50体積%、より好ましくは70体積%以上、さらに好ましくは80体積%以上が体心立方型(BCC)構造である。なお上限値は特に制限されないが、好ましくは99体積%以下、より好ましくは98体積%以下が体心立方型(BCC)構造である。
【0028】
本発明の他の実施形態によれば、本発明の分離膜を備える水素分離膜(hydrogen separation membrane)を提供する。この水素分離膜は、水素ガスが含有されているガス混合物から水素ガスのみを選択的に分離する分離膜であって、水素を拡散させ易い体心立方型(BCC)の結晶構造を含むことにより、高い水素透過特性を有する。その結果、本発明の水素分離膜は、高純度の水素分離を行うことができる。例えば、本発明の水素分離膜は、本発明に係る合金の好ましくは50体積%以上、より好ましくは70体積%以上、さらに好ましくは80体積%以上が体心立方型(BCC)の結晶構造である。なお上限値は特に制限されないが、好ましくは99体積%以下、より好ましくは98体積%以下が体心立方型(BCC)の結晶構造である。前記のような範囲の高いレベルの結晶構造を有する分離膜は、水素分離膜として好適である。
【0029】
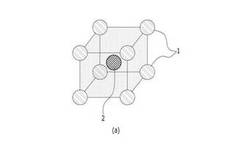
図1Aおよび図1Bは、本発明の分離膜が含み得る結晶格子の類型を示す模式図であり、少なくとも1種の5族元素およびIrを含む合金が形成可能な結晶格子を示している。5族元素は体心立方型(BCC)構造を形成するが、図1Aは、5族元素が形成する体心立方型(BCC)構造の体心にIrが置換された場合を示すものであり、図1Bは、5族元素が形成する体心立方型(BCC)構造の頂点にIrが置換された場合を示すものである。すなわち、本発明の分離膜は、5族元素およびIrが一緒に形成した体心立方型(BCC)の結晶構造を有する。
【0030】
本発明に係る合金は、空隙率が好ましくは10体積%未満、より好ましくは5体積%未満、さらに好ましくは1体積%未満である非多孔性膜の形態に製造され得る。また、空隙率の下限値は特に制限されないが、0.01体積%以上であることが好ましく0.1体積%以上であることがより好ましい。
【0031】
また、本発明の分離膜は、空隙率が好ましくは10体積%未満、より好ましくは5体積%未満、さらに好ましくは1体積%未満である非多孔性膜の形態に製造され得る。また、空隙率の下限値は特に制限されないが、0.01体積%以上であることが好ましく、0.1体積%以上であることがより好ましい。
【0032】
ここで、「非多孔性」とは、膜の厚さ方向に延びる気孔(空隙)が実質的に存在しないことにより、そのような気孔(空隙)を介して非選択的にガス、例えば、水素(H2)、酸素(O2)、二酸化炭素(CO2)または窒素(N2)などのガス分子が通過できないことを意味する。
【0033】
一方、空隙率は、下記数式(1)のように定義することができる。
【0034】
【数1】

【0035】
すなわち、空隙率は物質内の空隙(すなわち、空いている部分)を測定するものであり、全体の体積に対する空隙の体積の比であり、0〜1または0〜100%の値で表わされる。
【0036】
非多孔性膜を備える本発明の分離膜は、分離対象となる物質のみを選択的に透過して分離することができる。本発明の分離膜を水素分離膜として形成する場合、非多孔性膜構造にして水素のみを選択的に透過して分離する。
【0037】
本発明の分離膜のIrの含量を変化させて、応用しようとする膜の特性に合わせて設計することができる。具体的に、本発明の分離膜中のIr含量は、0.1〜40原子%が好ましく、0.1〜30原子%がより好ましく、5〜15原子%がさらに好ましい。前記のような含量の範囲のIrを含む分離膜は、水素透過特性に優れており、しかも、耐久性が向上して水素分離膜として用いて好適である。
【0038】
前記5族元素は、V、Nb、およびTaからなる群より選択される少なくとも1種が好ましい。本発明の一実施形態によれば、前記5族元素は、VおよびNbの少なくとも1種がより好ましい。本発明の他の実施形態によれば、前記5族元素は、Nbがさらに好ましい。
【0039】
本発明の分離膜は、例えば、NbおよびIrの合金、VおよびIrの合金、Nb、VおよびIrの合金、またはNb、TaおよびIrの合金を含むことが好ましい。
【0040】
本発明の分離膜は、5族元素およびIrに加えて、他の金属をさらに含む合金であることが好ましく、例えば、3成分系合金または4成分系合金であることが好ましい。このような他の金属は、Zr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種であることが好ましい。他の金属がさらに含まれる結果、本発明の分離膜の柔軟性が高まる。
【0041】
上記のような他の金属もまた、本発明に係る合金において、5族元素およびIrと共に体心立方型(BCC)の結晶構造を形成することができる。他の金属をさらに含む合金は、合金内に存在する金属間化合物(intermetallic compound)を形成することができるが、ほとんどの合金が体心立方型(BCC)の結晶構造を形成することにより、上記の他の金属をさらに含む合金製の分離膜においても、合金の好ましくは50体積%以上、より好ましくは50〜99体積%、さらに好ましくは60〜98体積%が体心立方型(BCC)の結晶構造を有する。
【0042】
本発明の分離膜が上記のような他の金属をさらに含む場合、本発明の分離膜は、0.1〜40原子%のIrと、0.1〜30原子%のZr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種の金属と、を含むことが好ましい。
【0043】
5族元素のみからなる分離膜は、水素の透過時に金属水素化物を形成して脆化が起こることがあるが、これを「水素脆性」と呼ぶ。このように脆化された部分に外部応力が加えられると、水素脆性破壊が発生する。水素脆性破壊を抑えるためには、水素固溶度を下げることを余儀なくされる。本発明の分離膜は、5族元素にIrが合金化されることにより、純粋な5族元素のみからなる膜に比べて水素固溶度が下がる。図1(a)および図1(b)に示す結晶構造を形成するようにIrが合金化されると、水素原子と5族元素との結合エネルギーを変化させる結果、水素固溶度が下がる。水素固溶度とは、金属内において固溶された水素の濃度のことをいい、固溶された水素(H)および金属(M)のモル比(H/M)により計算される。
【0044】
例えば、Irを約6原子%含むNb−Ir合金に対して、高水素濃度領域(H/Nbのモル比が約0.5である)における水素の固溶エネルギー(heat of H solution)を密度汎関数理論(DFT:Density Functional Theory)を用いて計算すれば、約−0.25eVであり、これは、純粋なNbの場合の約−0.4eVに比べてその絶対値が小さいため、水素固溶度が下がる。このように本発明の分離膜は、5族元素にIrを添加して合金化させて水素固溶度を下げたものである。
【0045】
全体的には、計算はDFTに基づく平面疑似ポテンシャル法で行われ、そのプログラムはVienna ab initio simulation package(VASP)内にある。Perdew、Burke、およびErnzerhofによって提案された密度勾配近似(GGA)は、(Phys. Rev. Lett.77, 3865(1996)参照)、電子交換相関関係可能性のために採用される。平面波分離エネルギーとMornkhorst−Pack k点サンプリングは慎重にテストされ、そして、最後に、計算の正確さと計算努力との間の妥協を成し遂げるために、300evの最適化された区分のエネルギーとk点メッシュとのための6×6×6格子が選ばれた。16のNb原子の1つを合金になっている金属原子と取り替えることによって、合金構造はモデル化される。そして、15のNb原子と1つの合金になっている金属原子とからなるスーパーセルになる。金属のH濃度(c=H/(Nb+M))は、計算において、1/16〜1/2まで変化する。すべての原子位置と格子定数とは、残りの力が0.02eV/Åより小さくなり、トータルのエネルギーの収束が1meV/スーパーセルになるまで、完全に弱まる。
【0046】
Nb合金の水素の固溶エネルギーは、次の式で定義される:
Esol=(1/n)[E[Nb15M1−nH]−E[Nb15M1]}−E[H2]/2
E[Nb15M1−nH]とE[Nb15M1]とがn中間部のH原子による、そして、それのないNb15M1スーパーセルの全エネルギーであって、E[H2]は、真空で水素分子の全エネルギーを意味する。水素が非常に軽い元素であるので、零点エネルギー(ΔEZPE)の補正は非常に重要である。金属と水素分子とのHの振動方法は、密度機能摂動理論を使って計算される。Nbの四面体の介在性(HTと定義される)のHのための振動波数は1400、1400、1037cm-1である。ところが、水素分子の振動頻度を考慮に入れた後に、NbのHTのための計算されたΔEZPEは106meV/Hである。Nb−M合金のために、計算されたΔEZPEは、75〜125meVにわたる。ΔEZPEの上での合金原子の影響はほとんど同じことで、零点エネルギー訂正はH固溶エネルギーの計算においてもはや必要ではない。
【0047】
上述したように、本発明の分離膜を用いて製造された水素分離膜は、低い水素固溶度を有することになり、具体的に、0.1〜1MPaの水素圧および400℃の条件下で測定した水素固溶度が0.01〜0.6であることが好ましく、0.05〜0.5であることがより好ましい。さらに具体的には、0.7MPa(約7bar)の水素圧および400℃の条件下で測定した水素固溶度が、0.1〜0.4であることが好ましい。
【0048】
また、このようにして製造された分離膜を用いて製造された水素分離膜は、水素透過度に優れている。水素透過度は、下記の数式(2)により計算することができる。
【0049】
【数2】

【0050】
式中、Permeabilityは水素透過度であり、Jは単位面積当たりの水素透過速度(Flux)であり、Lは分離膜の厚さであり、PH2、inは供給水素の圧力であり、PH2、outは透過水素の圧力である。
【0051】
本発明の分離膜の水素透過度は、400℃の条件下で1.0×10-8〜15.0×10-8mol/m・s・Pa1/2であることが好ましく、1.2×10-8〜12.0×10-8mol/m・s・Pa1/2であることがより好ましく、1.5×10-8〜10.0×10-8mol/m・s・Pa1/2であることがさらに好ましい。
【0052】
本発明の分離膜の厚さは、1〜500μmであることが好ましく、10〜100μmであることがより好ましい。分離膜は、前記のような範囲の厚さを有するときに、分離膜として用いて好適な水素透過度を有する。この厚さは、図13に示す水素分離膜23の厚さまたは図14の管状の水素分離膜33の厚さであることが好ましい。
【0053】
本発明の分離膜は、公知の合金の製造方法によって製造することができ、その方法に特に制限はない。例えば、アーク融解法(arc melting)、誘導溶解法(induction melting)などによって各金属を均一に溶解し、所望の厚さの膜を製作するために熱間圧延(hot rolling)、冷間圧延(cold rolling)、蒸着およびメッキ工程を施して分離膜を製造することができる。
【0054】
本発明の水素分離膜は、本発明の分離膜の片面または両面に触媒層がさらに形成されたものであることが好ましい。図2は、分離膜11の両面に触媒層12が形成された水素分離膜10を示すものであり、水素ガス(H2)が水素分離膜を通過するメカニズムを示す模式図である。上述したように、水素分離膜10を用いた水素の透過は水素原子によって行われるため、水素分子(H2)の水素原子(H)への解離が必要である。触媒層12は、このような水素分子の解離を補助する触媒として働く。水素分離膜10を通過して選択的に透過された水素は、さらに水素分子に再結合される必要があり、このような再結合も触媒層12によって促される。
【0055】
触媒層12は、上述したように、水素分離膜10の表面において水素分子を解離したり水素分子に再結合させたりする反応の触媒作用をする物質を含む。その物質としては、特に制限はなく、具体的には、Pd、Pt、Ru、Ir、Cu、Ag、Au、およびRhからなる群より選択される少なくとも1種の金属を含むことが好ましい。
【0056】
触媒層12の厚さは、例えば、好ましくは20〜1,000nm、より好ましくは50〜500nmである。触媒層12が上記の範囲の厚さを有するときに、全体の水素分離膜10の透過度を阻害せず、円滑な触媒作用を行うことができる。
【0057】
本発明の水素分離膜は、触媒層12および分離膜11の間の反応および拡散を防ぐ遮断層をさらに備えることが好ましい。
【0058】
または、水素分離膜は、分離膜の一方の面または両面に触媒層はなくてもよい。その代わりに、水素分離膜は、水素分子の分離を助けるために、触媒活性を有する化合物が表面にドープされている分離膜からなってもよい。水素分子の分離のための触媒活性を有する化合物としては、特に制限なく、Pb、Pt、Ru、Ir、Cu、Ag、Au、Rhまたはその組合せが挙げられる。
【0059】
本発明の水素分離膜は、スチーム改質反応(steam reforming)、石炭ガス化反応(coal gasification)、水性ガス転化反応(WGS:Water gas shift reaction)などにより生成されたH2、CO2、COなどを含むガスのうち、H2ガスのみを選択的に透過して分離する技術分野に適用可能である。例えば、高純度水素生成機、燃料電池用の水素再生機、ガス化複合火力発電所用の混合ガスの水素分離用分離膜、H2/CO2分離用分離膜などの分野に適用可能である。
【0060】
このようにして分離された水素は、清浄エネルギー源である電気発電用、化学原料(NH4、オレフィンなど)用、または石油精製用に用いられる。一方、水素を除去してから残留するガスは、高濃度のCO2成分からなるガスであるため、このようなCO2濃厚ガス(CO2 rich gas)を選択的に捕集および貯蔵してCO2を除去する用途に用いてもよい。
【0061】
本発明の水素分離膜は、まず、水素をはじめとする各種のガスのうち水素ガス(H2)を吸着し、吸着された水素ガス(H2)は水素分離膜の表面において水素原子(H)に解離され、解離された水素原子(H)は分離膜を透過する。分離膜の単位格子の四面体または八面体の格子内空間を通じて水素原子(H)が溶解(あるいは固溶)され、かつ拡散されて透過が行われる(M.D. Dolan, J. membrane science 362, 12−28(2010)参照)。膜を透過した水素原子(H)はさらに再結合して水素ガス(H2)になった後、水素分離膜から脱離される。
【0062】
本発明のさらに他の実施形態は、本発明の水素分離膜を備える水素分離装置を提供する。
【0063】
本発明の水素分離装置は、水素ガスを含む混合ガスが流入する流入口および分離された水素ガスが流出される流出口を有するチャンバと、本発明の水素分離膜と、を備え、このとき、水素分離装置は、前記チャンバを第1の部分および第2の部分の両部分に画成するように前記チャンバ内に配設されるが、前記第1の部分は、前記水素ガスを含む混合ガスが流入する流入口が設けられた部分であり、前記第2の部分は、前記分離された水素ガスが流出される流出口が設けられた部分であることが好ましい。
【0064】
図13は、本発明の一実施形態に係る水素分離装置20を概略的に示す模式図である。水素ガスを含む混合ガスの供給手段21を介して水素ガスを含む混合ガスがチャンバ22に投入されると、混合ガスのうち水素ガスのみが選択的に水素分離膜23を介して排出室24に分離される。分離された水素ガスは、排出手段25を介して回収される。水素分離装置20は、水素ガスの分離された残りのガスを回収するための回収手段26が、チャンバにさらに設けられていてもよい。水素分離装置20は、説明の便宜のために簡略に示されており、用途に応じて、他の構成要素をさらに備えてもよい。
【0065】
図14は、水素分離装置30が管状に形成された他の実施形態を示す模式図である。水素分離装置30は、管状の水素分離膜33を備え、水素分離膜33の外部に管状の水素分離膜33の直径よりも大きい径の筒状のチャンバ隔壁36が形成されて、チャンバ隔壁36と水素分離膜33との間の空間がチャンバ32として形成され、管状の水素分離膜33の内部は水素が排出される排出室34として形成される。チャンバ32に水素ガスを含む混合ガスの供給手段(図示せず)、および水素ガスが分離された残留ガスの回収手段(図示せず)がさらに設けられていてもよい。なお、分離された水素ガスを排出室34に排出する排出手段(図示せず)がさらに設けられていてもよい。
【0066】
本発明は、さらに他の実施形態において、管状の水素分離膜33は、図14の場合とは逆に、管状の水素分離膜33の内部に混合ガスが供給され、混合ガスのうち水素が管状の水素分離膜33を通過して管状の水素分離膜33の外部に分離されて水素が排出されるように形成されてもよい。すなわち、水素分離膜33の内部は、混合ガスが供給されるチャンバとして形成され、水素分離膜33の外部は水素が排出される排出室として形成される。
【実施例】
【0067】
以下、本発明の具体的な実施例を提示する。但し、後述する実施例は本発明を具体的に例示もしくは説明するためのものに過ぎず、これら実施例により本発明が制限されることはない。
【0068】
実施例1
NbおよびIrを、アーク融解法を用いて均一に溶解して合金化を行い、50μmの厚さの分離膜を備える水素分離膜を製造した。具体的には、Nb 97原子%およびIr 3原子%を秤量して材料を準備し、この材料を高真空(5Pa以下(5×10-5torr以下))の状態でArガスを注入して酸化防止条件を形成し、次いで、電流を増加させて上記の材料を溶かした後に十分に冷却した。製造したインゴットは50μmの厚さにし、真空下で熱処理を施して転位などの欠陥を除去した後、膜の両面にPdをコーティングして水素分離膜を製造した。
【0069】
実施例2
Nb 95原子%およびIr 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0070】
実施例3
Nb 92.5原子%およびIr 7.5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0071】
実施例4
Nb 90原子%およびIr 10原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0072】
実施例5
V 97.5原子%およびIr 2.5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0073】
実施例6
V 95原子%およびIr 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0074】
実施例7
V 92.5原子%およびIr 7.5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0075】
実施例8
V 90原子%、Ir 5原子%、およびNi 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0076】
比較例1
純粋なNbからなる50μmの厚さの水素分離膜を製造した。
【0077】
比較例2
Pd 74原子%およびAg 26原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0078】
比較例3
純粋なPd材料を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0079】
比較例4
V 95原子%およびTi 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0080】
評価例1:水素固溶度の評価
実施例2〜4、および比較例1に従い製造された水素分離膜に対して、JIS H7201:2007の規格に準拠して、400℃において水素圧力別に水素固溶度を評価した。評価は、Sievert Type PCT(pressure−concentration−temperature)装置を用いて行った。その結果を図3に示す。400℃、0.7MPa(7bar)の条件下で、Irが少量(2.5〜7.5原子%)添加されても、有効に水素固溶度が下がる。下記表1に示すように、実施例6は、400℃、0.7MPa(7bar)の条件下で水素固溶度が0.25であり、比較例1の0.67に比べて小さな値を有する。
【0081】
評価例2:体心立方型(BCC)の維持
図4は、実施例5〜8に従い製造された水素分離膜の組成に対するX線回折(XRD)測定結果を示すグラフである。
【0082】
あらゆる組成において、体心立方型(BCC)の結晶構造を維持していることが分かる。体心立方型(BCC)の結晶構造を維持すれば、水素の拡散係数が面心立方型(FCC)の結晶構造に比べて大きいため、透過度が増加するというメリットがある。
【0083】
評価例3:体心立方型(BCC)の維持および金属水素化物の生成有無の評価
実施例2〜3および比較例1に従い製造された水素分離膜に対して、10MPaまで水素固溶を行った後に、常温(約25℃)に冷却してX線回折分析(XRD)を行い、金属水素化物に相当するピークが生成されるか否かを評価した。その結果を表1に示す。図5は、実施例2〜3および比較例1に従い製造された水素分離膜に対するX線回折(XRD)評価結果を示すグラフである。実施例2および実施例3において、体心立方型(BCC)構造を良好に維持していることを確認することができる。一方、比較例1の水素分離膜において、金属水素化物が生成されたことを示すピークを確認し(X線回折(XRD)ピーク内に点線で囲まれた円にて表示される)、比較例1の水素分離膜の水素固溶前のX線回折(XRD)評価結果(図4参照)を測定して、金属水素化物が水素固溶前に存在しないことを確認した。
【0084】
下記表1に、実施例1、実施例2、実施例3、実施例6、および比較例1に従い製造された水素分離膜に対して、金属水素化物の生成有無を評価した結果を示す。水素固溶度と金属水素化物の生成との関係を調べるために、上記の評価例1の方法と同様にして、0.7MPa(約7bar)の水素圧および400℃の条件下で測定された水素固溶度を表1に併記する。
【0085】
【表1】

【0086】
上記表1の結果から、水素固溶度が高い比較例1においては、金属水素化物が生成されるものの、それよりも水素固溶度が低い実施例1、実施例2、実施例3、および実施例6においては、金属水素化物の生成の度合いが僅かであるか、あるいは、無視できる程度であることを確認することができた。その結果、水素固溶度が金属水素化物の生成に直接的に影響することが分かる。
【0087】
評価例4:水素脆性の評価
実施例1〜3および比較例1に従い製造された水素分離膜を、水素が加減圧可能な装置に入れた。次いで、水素の圧力を1Mpa(10bar)、2Mpa(20bar)、および3Mpa(30bar)に上げた後に常圧まで下げ、試験片を取り出して表面にひび割れが発生したか否かを観察した。その結果を下記表2に示す。
【0088】
【表2】

【0089】
下記表3は、水素ガス入力部の圧力を増大させながら、分離膜の水素透過度の変化および破壊の有無を観察した結果を示すものである。比較例1(Pure Nb)および比較例4の場合、加圧と同時に破壊が行われて水素透過度を測定することが困難であった。これに対し、実施例6の場合、水素圧力を加えることにより破壊無しに安定的な水素透過度の値を維持した。したがって、Irの添加による耐脆性の改善効果に優れていることが分かる。
【0090】
【表3】

【0091】
評価例5:過酷サイクル評価
400℃の温度条件下で5MPa(50bar)および常圧状態を30分間2回繰り返した後に得られた水素透過膜を、走査型電子顕微鏡(SEM)により写真撮影し、写真から外観を比較しかつ検査した。図6は、比較例1の場合であって、図6Aは100倍拡大した写真であり、図6Bは、500倍拡大した写真であり、脆性破壊が多く見られた。図7は、実施例3の場合であって、図7Aは100倍拡大した写真であり、図7Bは500倍拡大した写真であり、脆性破壊がほとんど見られなかった。
【0092】
ひび割れ密度(crack density)を下記の方法により計算した。結果を下記表4に示す。評価例5の過酷サイクル評価を行った後、サンプルの走査型電子顕微鏡(SEM)写真を100倍にて撮り、5cm×5cmの断面に対してひび割れの長さを測定した(ひび割れの長さ/サンプルの面積、破壊された面も長さに含める)。
【0093】
【表4】

【0094】
評価例6:水素透過特性の評価
上記の結果に基づき、実施例2、実施例6、比較例2、および比較例3に従い製造された水素分離膜に対して、下記の数式(2)により水素透過度を測定した。ここで、((PH2、in)1/2−(PH2、out)1/2)は、水素分離膜の水素入力時および水素出力時の水素分圧の平方根の差分である。
【0095】
【数3】

【0096】
式中、Permeabilityは水素透過度であり、Jは単位面積当たりの水素透過速度(Flux)であり、Lは水素分離膜の厚さであり、PH2、inは供給水素の圧力であり、PH2、outは透過水素の圧力である。
【0097】
図8および図9は、上記数式(1)により計算された水素透過特性を示すグラフである。図8から、実施例2は比較例2よりも優れた水素透過特性を有することが分かり、図9から、実施例6は比較例3よりも優れた水素透過特性を有することが分かる。
【0098】
水素透過度(実施例6):9.8×10-8mol/m・s・Pa1/2
水素透過度(比較例3):1.6×10-8mol/m・s・Pa1/2。
【0099】
評価例7:酸化安定性の評価
実施例2、実施例4、および比較例1に従い製造された水素分離膜に対して、大気中において5℃/分の昇温速度にて常温(25℃)から800℃まで昇温しながら熱重量分析法(Thermo Gravimetric Analysis;TGA)により評価して重さの変化を観察した。その結果を図10〜図12に示す。図10中、図10Aは実施例2に対する熱重量分析(Thermo Gravimetric Analysis;TGA)グラフであり、図10Bは実施例2に対する微分熱重量分析(Derivative Thermo Gravimetry;DTG)グラフである。図11中、図11Aは実施例4に対するTGAグラフであり、図11Bは実施例4に対するDTGグラフである。図12中、図12Aは比較例1に対するTGAグラフであり、図12Bは比較例1に対するDTGグラフである。
【0100】
熱重量分析のグラフから、実施例2、実施例4、および比較例1に従い製造された水素分離膜の酸化開始温度を評価した結果を下記表5に示す。
【0101】
【表5】

【0102】
上記表5の結果から、実施例2および実施例4の場合、比較例1に比べて酸化安定性が増加することが分かる。
【0103】
以上、本発明の好適な実施例について詳細に説明したが、本発明の権利範囲はこれに何ら限定されるものではなく、下記の特許請求の範囲において定義している本発明の基本概念を用いた当業者の種々の変形および改良もまた本発明の権利範囲に属するものである。
【符号の説明】
【0104】
1 5族元素、
2 Ir原子、
10 水素分離膜、
11 分離膜、
12 触媒層、
20、30 水素分離装置、
21 水素ガスを含む混合ガスの供給手段、
22、32 チャンバ、
23、33 水素分離膜、
24、34 排出室、
25 分離された水素ガスの排出手段、
26 回収手段、
36 チャンバ隔壁。
【技術分野】
【0001】
本発明は、分離膜、これを備える水素分離膜、および該水素分離膜を備える水素分離装置に関する。
【背景技術】
【0002】
水素ガスが含有されているガス混合物から水素ガスのみを選択的に分離する分離膜として、既存のPd系金属がよく知られている。Pd系金属は、面心立方構造(FCC: face−centered cubic)を形成して、単位格子内の空間を用いた水素の溶解および拡散により水素の選択的な分離が行われる。しかしながら、Pd系金属が高コストであること、および水素透過度を向上させ難いことは、相溶化の制限要因として働く。
【0003】
これに伴い、Pd系金属と同じ程度の優れた水素透過性能を有し、かつ価格競争力のある水素分離膜への要求が急増している。
【0004】
Pdに代替する分離膜として、多孔性分離膜、非晶質系金属分離膜、または4族元素もしくは5族元素を用いた分離膜への取り組みが行われている。
【0005】
多孔性分離膜は、気孔径によりガスを分離するものである。しかしながら、現実的に、気孔径を同じ寸法に、しかも、完璧な球状に製造することは困難であるため、選択度、例えば、二酸化炭素の透過度に対する水素ガスの透過度の比が低いという問題がある。
【0006】
非晶質系金属分離膜の場合、金属を溶融状態で急冷して製造するため、急冷可能な組成および工程が制限されるという欠点を有している。実際に、分離膜の使用温度が250〜500℃と高温であるため、非晶質系金属分離膜は高温下での結晶化に伴う耐久性の低下の問題があり、これを解消するための技術が望まれる。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2006−95521号公報
【特許文献2】特開2003−1381号公報
【特許文献3】米国特許出願公開第2010/0247944号明細書
【特許文献4】米国特許出願公開第2004/0129135号明細書
【非特許文献】
【0008】
【非特許文献1】M.D. Dolan, J. Membrane Science, 362, 12−28, 2010
【発明の概要】
【発明が解決しようとする課題】
【0009】
本発明の目的は、水素透過特性および酸化安定性に優れており、水素脆性破壊が抑制された分離膜を提供することである。
【0010】
本発明の他の目的は、前記分離膜を備える水素分離膜を提供することである。
【0011】
本発明のさらに他の目的は、前記水素分離膜を備える水素分離装置を提供することである。
【課題を解決するための手段】
【0012】
本発明の一実施形態によれば、少なくとも1種の5族元素およびIrを含む合金を含み、前記合金は体心立方型結晶構造を含む、分離膜を提供する。
【発明の効果】
【0013】
本発明によれば、水素透過特性および酸化安定性に優れており、水素脆性破壊が抑制された分離膜が提供される。なお、これを備える水素分離膜によれば、高純度の水素を分離することができ、耐久性が効果的に改善される。
【図面の簡単な説明】
【0014】
【図1A】本発明の一実施形態に係る分離膜が形成可能な結晶格子を示す模式図である。
【図1B】本発明の一実施形態に係る分離膜が形成可能な結晶格子を示す模式図である。
【図2】本発明の他の実施形態に係る水素分離膜を通過して、水素ガスが分離されるメカニズムを示す模式図である。
【図3】実施例2〜4、および比較例1に従い製造された水素分離膜に対するPCT(pressure−concentration−temperature)評価結果を示すグラフである。
【図4】実施例5〜8に従い製造された水素分離膜の組成に対するX線回折(XRD:X−ray diffraction analysis)測定結果を示すグラフである。
【図5】実施例2〜3および比較例1に従い製造された水素分離膜に対するXRD評価結果を示すグラフである。
【図6A】比較例1に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図6B】比較例1に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図7A】実施例6に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図7B】実施例6に従い製造された水素分離膜に対して過酷条件下でのサイクルを行った後の表面の走査型電子顕微鏡(SEM)写真である。
【図8】実施例2および比較例2に従い製造された水素分離膜に対する水素透過特性の測定結果を示すグラフである。
【図9】実施例6および比較例3に従い製造された水素分離膜に対する水素透過特性の測定結果を示すグラフである。
【図10A】実施例2に従い製造された水素分離膜に対する、熱重量分析法(Thermo Gravimetric Analysis;TGA)による評価結果を示すグラフである。
【図10B】実施例2に従い製造された水素分離膜に対する、熱重量分析法(Thermo Gravimetric Analysis;TGA)による評価結果を示すグラフである。
【図11A】実施例4に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図11B】実施例4に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図12A】比較例1に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図12B】比較例1に従い製造された水素分離膜に対する、熱重量分析法(TGA)による評価結果を示すグラフである。
【図13】本発明の一実施形態に係る水素分離装置の模式図である。
【図14】本発明の他の実施形態に係る管状の水素分離膜を備える水素分離装置の模式図である。
【発明を実施するための形態】
【0015】
以下、本発明の一実施形態について本発明が属する技術分野において通常の知識を有する者が容易に実施できる程度に詳細に説明する。しかしながら、本発明は種々の異なる形態に実現可能であり、ここで説明する実施形態に限定されるものではない。
【0016】
本発明は種々の異なる形態に実現可能であり、必要に応じて、図面に基づいて説明され、ここで説明する実施形態に限定されない。本明細書の図面に示す各構成要素の大きさおよび厚さは説明の便宜のために任意に示されており、本発明が必ずしも図示のところに限定されるとは限らない。なお、図示した各構成要素の大きさおよび厚さは説明の便宜のために任意に誇張されており、本発明が必ずしも図示のところに限定されるとは限らない。
【0017】
本発明の一実施形態によれば、少なくとも1種の5族元素およびIrを含む合金を含み、前記合金が体心立方型(BCC:body−centered cubic)結晶構造を含む分離膜を提供する。
【0018】
前記分離膜は、特定のガスを選択的に分離するための分離膜として用いられることが好ましい。
【0019】
4族元素または5族元素の金属分離膜の場合、高い水素固溶による水素耐久性の低下を引き起こす脆性破壊が発生する虞がある。また、金属系の分離膜は高温下で酸化されるため、性能が低下する虞がある。このため、4族元素または5族元素の金属分離膜は水素固溶による金属水素化物の生成を抑えて水素脆性破壊を克服し、同時に高い透過度を維持するための研究が必要である。
【0020】
本発明の一実施形態に係る分離膜は、前記のような合金を含むことにより、ポリマー製の分離膜に比べて高温条件下で作動可能であるというメリットがある。また、本発明の分離膜は、5族系の金属を用いるにも拘わらず、低い水素固溶度を維持し、これにより、水素脆性破壊を抑えるとともに、高い水素透過度を維持することができる。なお、本発明の分離膜は、結晶構造が形成可能な合金を含むことにより、非晶質系金属分離膜に比べて非晶質の結晶化による性能低下の問題点がなく、耐久性の面で有利である。
【0021】
本発明の一実施形態によれば、前記合金は、5族元素およびIrを含み、これもまた結晶構造を形成することができる。
【0022】
前記合金の前記結晶構造は、体心立方型(BCC:body−centered cubic)構造に加えて、面心立方型(FCC:face−centered cubic)構造、六方最密充填型(HCP:hexagonal closed packed)構造またはこれらの組み合わせとすることができる。
【0023】
5族金属は、体心立方型(BCC:body−centered cubic)の結晶構造を取り得ることが知られており、これは、結晶系の表面に相当する特定のX線回折(XRD)ピークによって確認することができる。
【0024】
本発明の一実施形態に係る合金は5族金属およびIrを含み、前記合金が、5族金属だけではなく、Irを含むにも拘わらず、依然として体心立方型(BCC)構造を含む結晶構造を形成することができる(図4参照)。
【0025】
本発明に係る合金が10原子%以下のIrを含む場合、本発明に係る合金は、ほとんどが体心立方型(BCC)の結晶構造を形成することができる。
【0026】
Irの量が増えるに従って、本発明に係る合金は、面心立方構造(FCC)、六方最密充填構造(HCP)またはこれらの組み合わせをさらに含むことができる。
【0027】
このため、本発明の一実施形態に係る分離膜内の合金は、好ましくは50体積%、より好ましくは70体積%以上、さらに好ましくは80体積%以上が体心立方型(BCC)構造である。なお上限値は特に制限されないが、好ましくは99体積%以下、より好ましくは98体積%以下が体心立方型(BCC)構造である。
【0028】
本発明の他の実施形態によれば、本発明の分離膜を備える水素分離膜(hydrogen separation membrane)を提供する。この水素分離膜は、水素ガスが含有されているガス混合物から水素ガスのみを選択的に分離する分離膜であって、水素を拡散させ易い体心立方型(BCC)の結晶構造を含むことにより、高い水素透過特性を有する。その結果、本発明の水素分離膜は、高純度の水素分離を行うことができる。例えば、本発明の水素分離膜は、本発明に係る合金の好ましくは50体積%以上、より好ましくは70体積%以上、さらに好ましくは80体積%以上が体心立方型(BCC)の結晶構造である。なお上限値は特に制限されないが、好ましくは99体積%以下、より好ましくは98体積%以下が体心立方型(BCC)の結晶構造である。前記のような範囲の高いレベルの結晶構造を有する分離膜は、水素分離膜として好適である。
【0029】
図1Aおよび図1Bは、本発明の分離膜が含み得る結晶格子の類型を示す模式図であり、少なくとも1種の5族元素およびIrを含む合金が形成可能な結晶格子を示している。5族元素は体心立方型(BCC)構造を形成するが、図1Aは、5族元素が形成する体心立方型(BCC)構造の体心にIrが置換された場合を示すものであり、図1Bは、5族元素が形成する体心立方型(BCC)構造の頂点にIrが置換された場合を示すものである。すなわち、本発明の分離膜は、5族元素およびIrが一緒に形成した体心立方型(BCC)の結晶構造を有する。
【0030】
本発明に係る合金は、空隙率が好ましくは10体積%未満、より好ましくは5体積%未満、さらに好ましくは1体積%未満である非多孔性膜の形態に製造され得る。また、空隙率の下限値は特に制限されないが、0.01体積%以上であることが好ましく0.1体積%以上であることがより好ましい。
【0031】
また、本発明の分離膜は、空隙率が好ましくは10体積%未満、より好ましくは5体積%未満、さらに好ましくは1体積%未満である非多孔性膜の形態に製造され得る。また、空隙率の下限値は特に制限されないが、0.01体積%以上であることが好ましく、0.1体積%以上であることがより好ましい。
【0032】
ここで、「非多孔性」とは、膜の厚さ方向に延びる気孔(空隙)が実質的に存在しないことにより、そのような気孔(空隙)を介して非選択的にガス、例えば、水素(H2)、酸素(O2)、二酸化炭素(CO2)または窒素(N2)などのガス分子が通過できないことを意味する。
【0033】
一方、空隙率は、下記数式(1)のように定義することができる。
【0034】
【数1】

【0035】
すなわち、空隙率は物質内の空隙(すなわち、空いている部分)を測定するものであり、全体の体積に対する空隙の体積の比であり、0〜1または0〜100%の値で表わされる。
【0036】
非多孔性膜を備える本発明の分離膜は、分離対象となる物質のみを選択的に透過して分離することができる。本発明の分離膜を水素分離膜として形成する場合、非多孔性膜構造にして水素のみを選択的に透過して分離する。
【0037】
本発明の分離膜のIrの含量を変化させて、応用しようとする膜の特性に合わせて設計することができる。具体的に、本発明の分離膜中のIr含量は、0.1〜40原子%が好ましく、0.1〜30原子%がより好ましく、5〜15原子%がさらに好ましい。前記のような含量の範囲のIrを含む分離膜は、水素透過特性に優れており、しかも、耐久性が向上して水素分離膜として用いて好適である。
【0038】
前記5族元素は、V、Nb、およびTaからなる群より選択される少なくとも1種が好ましい。本発明の一実施形態によれば、前記5族元素は、VおよびNbの少なくとも1種がより好ましい。本発明の他の実施形態によれば、前記5族元素は、Nbがさらに好ましい。
【0039】
本発明の分離膜は、例えば、NbおよびIrの合金、VおよびIrの合金、Nb、VおよびIrの合金、またはNb、TaおよびIrの合金を含むことが好ましい。
【0040】
本発明の分離膜は、5族元素およびIrに加えて、他の金属をさらに含む合金であることが好ましく、例えば、3成分系合金または4成分系合金であることが好ましい。このような他の金属は、Zr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種であることが好ましい。他の金属がさらに含まれる結果、本発明の分離膜の柔軟性が高まる。
【0041】
上記のような他の金属もまた、本発明に係る合金において、5族元素およびIrと共に体心立方型(BCC)の結晶構造を形成することができる。他の金属をさらに含む合金は、合金内に存在する金属間化合物(intermetallic compound)を形成することができるが、ほとんどの合金が体心立方型(BCC)の結晶構造を形成することにより、上記の他の金属をさらに含む合金製の分離膜においても、合金の好ましくは50体積%以上、より好ましくは50〜99体積%、さらに好ましくは60〜98体積%が体心立方型(BCC)の結晶構造を有する。
【0042】
本発明の分離膜が上記のような他の金属をさらに含む場合、本発明の分離膜は、0.1〜40原子%のIrと、0.1〜30原子%のZr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種の金属と、を含むことが好ましい。
【0043】
5族元素のみからなる分離膜は、水素の透過時に金属水素化物を形成して脆化が起こることがあるが、これを「水素脆性」と呼ぶ。このように脆化された部分に外部応力が加えられると、水素脆性破壊が発生する。水素脆性破壊を抑えるためには、水素固溶度を下げることを余儀なくされる。本発明の分離膜は、5族元素にIrが合金化されることにより、純粋な5族元素のみからなる膜に比べて水素固溶度が下がる。図1(a)および図1(b)に示す結晶構造を形成するようにIrが合金化されると、水素原子と5族元素との結合エネルギーを変化させる結果、水素固溶度が下がる。水素固溶度とは、金属内において固溶された水素の濃度のことをいい、固溶された水素(H)および金属(M)のモル比(H/M)により計算される。
【0044】
例えば、Irを約6原子%含むNb−Ir合金に対して、高水素濃度領域(H/Nbのモル比が約0.5である)における水素の固溶エネルギー(heat of H solution)を密度汎関数理論(DFT:Density Functional Theory)を用いて計算すれば、約−0.25eVであり、これは、純粋なNbの場合の約−0.4eVに比べてその絶対値が小さいため、水素固溶度が下がる。このように本発明の分離膜は、5族元素にIrを添加して合金化させて水素固溶度を下げたものである。
【0045】
全体的には、計算はDFTに基づく平面疑似ポテンシャル法で行われ、そのプログラムはVienna ab initio simulation package(VASP)内にある。Perdew、Burke、およびErnzerhofによって提案された密度勾配近似(GGA)は、(Phys. Rev. Lett.77, 3865(1996)参照)、電子交換相関関係可能性のために採用される。平面波分離エネルギーとMornkhorst−Pack k点サンプリングは慎重にテストされ、そして、最後に、計算の正確さと計算努力との間の妥協を成し遂げるために、300evの最適化された区分のエネルギーとk点メッシュとのための6×6×6格子が選ばれた。16のNb原子の1つを合金になっている金属原子と取り替えることによって、合金構造はモデル化される。そして、15のNb原子と1つの合金になっている金属原子とからなるスーパーセルになる。金属のH濃度(c=H/(Nb+M))は、計算において、1/16〜1/2まで変化する。すべての原子位置と格子定数とは、残りの力が0.02eV/Åより小さくなり、トータルのエネルギーの収束が1meV/スーパーセルになるまで、完全に弱まる。
【0046】
Nb合金の水素の固溶エネルギーは、次の式で定義される:
Esol=(1/n)[E[Nb15M1−nH]−E[Nb15M1]}−E[H2]/2
E[Nb15M1−nH]とE[Nb15M1]とがn中間部のH原子による、そして、それのないNb15M1スーパーセルの全エネルギーであって、E[H2]は、真空で水素分子の全エネルギーを意味する。水素が非常に軽い元素であるので、零点エネルギー(ΔEZPE)の補正は非常に重要である。金属と水素分子とのHの振動方法は、密度機能摂動理論を使って計算される。Nbの四面体の介在性(HTと定義される)のHのための振動波数は1400、1400、1037cm-1である。ところが、水素分子の振動頻度を考慮に入れた後に、NbのHTのための計算されたΔEZPEは106meV/Hである。Nb−M合金のために、計算されたΔEZPEは、75〜125meVにわたる。ΔEZPEの上での合金原子の影響はほとんど同じことで、零点エネルギー訂正はH固溶エネルギーの計算においてもはや必要ではない。
【0047】
上述したように、本発明の分離膜を用いて製造された水素分離膜は、低い水素固溶度を有することになり、具体的に、0.1〜1MPaの水素圧および400℃の条件下で測定した水素固溶度が0.01〜0.6であることが好ましく、0.05〜0.5であることがより好ましい。さらに具体的には、0.7MPa(約7bar)の水素圧および400℃の条件下で測定した水素固溶度が、0.1〜0.4であることが好ましい。
【0048】
また、このようにして製造された分離膜を用いて製造された水素分離膜は、水素透過度に優れている。水素透過度は、下記の数式(2)により計算することができる。
【0049】
【数2】

【0050】
式中、Permeabilityは水素透過度であり、Jは単位面積当たりの水素透過速度(Flux)であり、Lは分離膜の厚さであり、PH2、inは供給水素の圧力であり、PH2、outは透過水素の圧力である。
【0051】
本発明の分離膜の水素透過度は、400℃の条件下で1.0×10-8〜15.0×10-8mol/m・s・Pa1/2であることが好ましく、1.2×10-8〜12.0×10-8mol/m・s・Pa1/2であることがより好ましく、1.5×10-8〜10.0×10-8mol/m・s・Pa1/2であることがさらに好ましい。
【0052】
本発明の分離膜の厚さは、1〜500μmであることが好ましく、10〜100μmであることがより好ましい。分離膜は、前記のような範囲の厚さを有するときに、分離膜として用いて好適な水素透過度を有する。この厚さは、図13に示す水素分離膜23の厚さまたは図14の管状の水素分離膜33の厚さであることが好ましい。
【0053】
本発明の分離膜は、公知の合金の製造方法によって製造することができ、その方法に特に制限はない。例えば、アーク融解法(arc melting)、誘導溶解法(induction melting)などによって各金属を均一に溶解し、所望の厚さの膜を製作するために熱間圧延(hot rolling)、冷間圧延(cold rolling)、蒸着およびメッキ工程を施して分離膜を製造することができる。
【0054】
本発明の水素分離膜は、本発明の分離膜の片面または両面に触媒層がさらに形成されたものであることが好ましい。図2は、分離膜11の両面に触媒層12が形成された水素分離膜10を示すものであり、水素ガス(H2)が水素分離膜を通過するメカニズムを示す模式図である。上述したように、水素分離膜10を用いた水素の透過は水素原子によって行われるため、水素分子(H2)の水素原子(H)への解離が必要である。触媒層12は、このような水素分子の解離を補助する触媒として働く。水素分離膜10を通過して選択的に透過された水素は、さらに水素分子に再結合される必要があり、このような再結合も触媒層12によって促される。
【0055】
触媒層12は、上述したように、水素分離膜10の表面において水素分子を解離したり水素分子に再結合させたりする反応の触媒作用をする物質を含む。その物質としては、特に制限はなく、具体的には、Pd、Pt、Ru、Ir、Cu、Ag、Au、およびRhからなる群より選択される少なくとも1種の金属を含むことが好ましい。
【0056】
触媒層12の厚さは、例えば、好ましくは20〜1,000nm、より好ましくは50〜500nmである。触媒層12が上記の範囲の厚さを有するときに、全体の水素分離膜10の透過度を阻害せず、円滑な触媒作用を行うことができる。
【0057】
本発明の水素分離膜は、触媒層12および分離膜11の間の反応および拡散を防ぐ遮断層をさらに備えることが好ましい。
【0058】
または、水素分離膜は、分離膜の一方の面または両面に触媒層はなくてもよい。その代わりに、水素分離膜は、水素分子の分離を助けるために、触媒活性を有する化合物が表面にドープされている分離膜からなってもよい。水素分子の分離のための触媒活性を有する化合物としては、特に制限なく、Pb、Pt、Ru、Ir、Cu、Ag、Au、Rhまたはその組合せが挙げられる。
【0059】
本発明の水素分離膜は、スチーム改質反応(steam reforming)、石炭ガス化反応(coal gasification)、水性ガス転化反応(WGS:Water gas shift reaction)などにより生成されたH2、CO2、COなどを含むガスのうち、H2ガスのみを選択的に透過して分離する技術分野に適用可能である。例えば、高純度水素生成機、燃料電池用の水素再生機、ガス化複合火力発電所用の混合ガスの水素分離用分離膜、H2/CO2分離用分離膜などの分野に適用可能である。
【0060】
このようにして分離された水素は、清浄エネルギー源である電気発電用、化学原料(NH4、オレフィンなど)用、または石油精製用に用いられる。一方、水素を除去してから残留するガスは、高濃度のCO2成分からなるガスであるため、このようなCO2濃厚ガス(CO2 rich gas)を選択的に捕集および貯蔵してCO2を除去する用途に用いてもよい。
【0061】
本発明の水素分離膜は、まず、水素をはじめとする各種のガスのうち水素ガス(H2)を吸着し、吸着された水素ガス(H2)は水素分離膜の表面において水素原子(H)に解離され、解離された水素原子(H)は分離膜を透過する。分離膜の単位格子の四面体または八面体の格子内空間を通じて水素原子(H)が溶解(あるいは固溶)され、かつ拡散されて透過が行われる(M.D. Dolan, J. membrane science 362, 12−28(2010)参照)。膜を透過した水素原子(H)はさらに再結合して水素ガス(H2)になった後、水素分離膜から脱離される。
【0062】
本発明のさらに他の実施形態は、本発明の水素分離膜を備える水素分離装置を提供する。
【0063】
本発明の水素分離装置は、水素ガスを含む混合ガスが流入する流入口および分離された水素ガスが流出される流出口を有するチャンバと、本発明の水素分離膜と、を備え、このとき、水素分離装置は、前記チャンバを第1の部分および第2の部分の両部分に画成するように前記チャンバ内に配設されるが、前記第1の部分は、前記水素ガスを含む混合ガスが流入する流入口が設けられた部分であり、前記第2の部分は、前記分離された水素ガスが流出される流出口が設けられた部分であることが好ましい。
【0064】
図13は、本発明の一実施形態に係る水素分離装置20を概略的に示す模式図である。水素ガスを含む混合ガスの供給手段21を介して水素ガスを含む混合ガスがチャンバ22に投入されると、混合ガスのうち水素ガスのみが選択的に水素分離膜23を介して排出室24に分離される。分離された水素ガスは、排出手段25を介して回収される。水素分離装置20は、水素ガスの分離された残りのガスを回収するための回収手段26が、チャンバにさらに設けられていてもよい。水素分離装置20は、説明の便宜のために簡略に示されており、用途に応じて、他の構成要素をさらに備えてもよい。
【0065】
図14は、水素分離装置30が管状に形成された他の実施形態を示す模式図である。水素分離装置30は、管状の水素分離膜33を備え、水素分離膜33の外部に管状の水素分離膜33の直径よりも大きい径の筒状のチャンバ隔壁36が形成されて、チャンバ隔壁36と水素分離膜33との間の空間がチャンバ32として形成され、管状の水素分離膜33の内部は水素が排出される排出室34として形成される。チャンバ32に水素ガスを含む混合ガスの供給手段(図示せず)、および水素ガスが分離された残留ガスの回収手段(図示せず)がさらに設けられていてもよい。なお、分離された水素ガスを排出室34に排出する排出手段(図示せず)がさらに設けられていてもよい。
【0066】
本発明は、さらに他の実施形態において、管状の水素分離膜33は、図14の場合とは逆に、管状の水素分離膜33の内部に混合ガスが供給され、混合ガスのうち水素が管状の水素分離膜33を通過して管状の水素分離膜33の外部に分離されて水素が排出されるように形成されてもよい。すなわち、水素分離膜33の内部は、混合ガスが供給されるチャンバとして形成され、水素分離膜33の外部は水素が排出される排出室として形成される。
【実施例】
【0067】
以下、本発明の具体的な実施例を提示する。但し、後述する実施例は本発明を具体的に例示もしくは説明するためのものに過ぎず、これら実施例により本発明が制限されることはない。
【0068】
実施例1
NbおよびIrを、アーク融解法を用いて均一に溶解して合金化を行い、50μmの厚さの分離膜を備える水素分離膜を製造した。具体的には、Nb 97原子%およびIr 3原子%を秤量して材料を準備し、この材料を高真空(5Pa以下(5×10-5torr以下))の状態でArガスを注入して酸化防止条件を形成し、次いで、電流を増加させて上記の材料を溶かした後に十分に冷却した。製造したインゴットは50μmの厚さにし、真空下で熱処理を施して転位などの欠陥を除去した後、膜の両面にPdをコーティングして水素分離膜を製造した。
【0069】
実施例2
Nb 95原子%およびIr 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0070】
実施例3
Nb 92.5原子%およびIr 7.5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0071】
実施例4
Nb 90原子%およびIr 10原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0072】
実施例5
V 97.5原子%およびIr 2.5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0073】
実施例6
V 95原子%およびIr 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0074】
実施例7
V 92.5原子%およびIr 7.5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0075】
実施例8
V 90原子%、Ir 5原子%、およびNi 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0076】
比較例1
純粋なNbからなる50μmの厚さの水素分離膜を製造した。
【0077】
比較例2
Pd 74原子%およびAg 26原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0078】
比較例3
純粋なPd材料を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0079】
比較例4
V 95原子%およびTi 5原子%を用いて膜を製造したこと以外は、実施例1の方法と同様にして水素分離膜を製造した。
【0080】
評価例1:水素固溶度の評価
実施例2〜4、および比較例1に従い製造された水素分離膜に対して、JIS H7201:2007の規格に準拠して、400℃において水素圧力別に水素固溶度を評価した。評価は、Sievert Type PCT(pressure−concentration−temperature)装置を用いて行った。その結果を図3に示す。400℃、0.7MPa(7bar)の条件下で、Irが少量(2.5〜7.5原子%)添加されても、有効に水素固溶度が下がる。下記表1に示すように、実施例6は、400℃、0.7MPa(7bar)の条件下で水素固溶度が0.25であり、比較例1の0.67に比べて小さな値を有する。
【0081】
評価例2:体心立方型(BCC)の維持
図4は、実施例5〜8に従い製造された水素分離膜の組成に対するX線回折(XRD)測定結果を示すグラフである。
【0082】
あらゆる組成において、体心立方型(BCC)の結晶構造を維持していることが分かる。体心立方型(BCC)の結晶構造を維持すれば、水素の拡散係数が面心立方型(FCC)の結晶構造に比べて大きいため、透過度が増加するというメリットがある。
【0083】
評価例3:体心立方型(BCC)の維持および金属水素化物の生成有無の評価
実施例2〜3および比較例1に従い製造された水素分離膜に対して、10MPaまで水素固溶を行った後に、常温(約25℃)に冷却してX線回折分析(XRD)を行い、金属水素化物に相当するピークが生成されるか否かを評価した。その結果を表1に示す。図5は、実施例2〜3および比較例1に従い製造された水素分離膜に対するX線回折(XRD)評価結果を示すグラフである。実施例2および実施例3において、体心立方型(BCC)構造を良好に維持していることを確認することができる。一方、比較例1の水素分離膜において、金属水素化物が生成されたことを示すピークを確認し(X線回折(XRD)ピーク内に点線で囲まれた円にて表示される)、比較例1の水素分離膜の水素固溶前のX線回折(XRD)評価結果(図4参照)を測定して、金属水素化物が水素固溶前に存在しないことを確認した。
【0084】
下記表1に、実施例1、実施例2、実施例3、実施例6、および比較例1に従い製造された水素分離膜に対して、金属水素化物の生成有無を評価した結果を示す。水素固溶度と金属水素化物の生成との関係を調べるために、上記の評価例1の方法と同様にして、0.7MPa(約7bar)の水素圧および400℃の条件下で測定された水素固溶度を表1に併記する。
【0085】
【表1】

【0086】
上記表1の結果から、水素固溶度が高い比較例1においては、金属水素化物が生成されるものの、それよりも水素固溶度が低い実施例1、実施例2、実施例3、および実施例6においては、金属水素化物の生成の度合いが僅かであるか、あるいは、無視できる程度であることを確認することができた。その結果、水素固溶度が金属水素化物の生成に直接的に影響することが分かる。
【0087】
評価例4:水素脆性の評価
実施例1〜3および比較例1に従い製造された水素分離膜を、水素が加減圧可能な装置に入れた。次いで、水素の圧力を1Mpa(10bar)、2Mpa(20bar)、および3Mpa(30bar)に上げた後に常圧まで下げ、試験片を取り出して表面にひび割れが発生したか否かを観察した。その結果を下記表2に示す。
【0088】
【表2】

【0089】
下記表3は、水素ガス入力部の圧力を増大させながら、分離膜の水素透過度の変化および破壊の有無を観察した結果を示すものである。比較例1(Pure Nb)および比較例4の場合、加圧と同時に破壊が行われて水素透過度を測定することが困難であった。これに対し、実施例6の場合、水素圧力を加えることにより破壊無しに安定的な水素透過度の値を維持した。したがって、Irの添加による耐脆性の改善効果に優れていることが分かる。
【0090】
【表3】

【0091】
評価例5:過酷サイクル評価
400℃の温度条件下で5MPa(50bar)および常圧状態を30分間2回繰り返した後に得られた水素透過膜を、走査型電子顕微鏡(SEM)により写真撮影し、写真から外観を比較しかつ検査した。図6は、比較例1の場合であって、図6Aは100倍拡大した写真であり、図6Bは、500倍拡大した写真であり、脆性破壊が多く見られた。図7は、実施例3の場合であって、図7Aは100倍拡大した写真であり、図7Bは500倍拡大した写真であり、脆性破壊がほとんど見られなかった。
【0092】
ひび割れ密度(crack density)を下記の方法により計算した。結果を下記表4に示す。評価例5の過酷サイクル評価を行った後、サンプルの走査型電子顕微鏡(SEM)写真を100倍にて撮り、5cm×5cmの断面に対してひび割れの長さを測定した(ひび割れの長さ/サンプルの面積、破壊された面も長さに含める)。
【0093】
【表4】

【0094】
評価例6:水素透過特性の評価
上記の結果に基づき、実施例2、実施例6、比較例2、および比較例3に従い製造された水素分離膜に対して、下記の数式(2)により水素透過度を測定した。ここで、((PH2、in)1/2−(PH2、out)1/2)は、水素分離膜の水素入力時および水素出力時の水素分圧の平方根の差分である。
【0095】
【数3】

【0096】
式中、Permeabilityは水素透過度であり、Jは単位面積当たりの水素透過速度(Flux)であり、Lは水素分離膜の厚さであり、PH2、inは供給水素の圧力であり、PH2、outは透過水素の圧力である。
【0097】
図8および図9は、上記数式(1)により計算された水素透過特性を示すグラフである。図8から、実施例2は比較例2よりも優れた水素透過特性を有することが分かり、図9から、実施例6は比較例3よりも優れた水素透過特性を有することが分かる。
【0098】
水素透過度(実施例6):9.8×10-8mol/m・s・Pa1/2
水素透過度(比較例3):1.6×10-8mol/m・s・Pa1/2。
【0099】
評価例7:酸化安定性の評価
実施例2、実施例4、および比較例1に従い製造された水素分離膜に対して、大気中において5℃/分の昇温速度にて常温(25℃)から800℃まで昇温しながら熱重量分析法(Thermo Gravimetric Analysis;TGA)により評価して重さの変化を観察した。その結果を図10〜図12に示す。図10中、図10Aは実施例2に対する熱重量分析(Thermo Gravimetric Analysis;TGA)グラフであり、図10Bは実施例2に対する微分熱重量分析(Derivative Thermo Gravimetry;DTG)グラフである。図11中、図11Aは実施例4に対するTGAグラフであり、図11Bは実施例4に対するDTGグラフである。図12中、図12Aは比較例1に対するTGAグラフであり、図12Bは比較例1に対するDTGグラフである。
【0100】
熱重量分析のグラフから、実施例2、実施例4、および比較例1に従い製造された水素分離膜の酸化開始温度を評価した結果を下記表5に示す。
【0101】
【表5】

【0102】
上記表5の結果から、実施例2および実施例4の場合、比較例1に比べて酸化安定性が増加することが分かる。
【0103】
以上、本発明の好適な実施例について詳細に説明したが、本発明の権利範囲はこれに何ら限定されるものではなく、下記の特許請求の範囲において定義している本発明の基本概念を用いた当業者の種々の変形および改良もまた本発明の権利範囲に属するものである。
【符号の説明】
【0104】
1 5族元素、
2 Ir原子、
10 水素分離膜、
11 分離膜、
12 触媒層、
20、30 水素分離装置、
21 水素ガスを含む混合ガスの供給手段、
22、32 チャンバ、
23、33 水素分離膜、
24、34 排出室、
25 分離された水素ガスの排出手段、
26 回収手段、
36 チャンバ隔壁。
【特許請求の範囲】
【請求項1】
少なくとも1種の5族元素およびIrを含む合金を含み、前記合金は体心立方型結晶構造を含む、分離膜。
【請求項2】
前記5族元素は、V、Nb、およびTaからなる群より選択される少なくとも1種である、請求項1に記載の分離膜。
【請求項3】
10体積%未満の空隙率を有する膜である、請求項1または2に記載の分離膜。
【請求項4】
5体積%未満の空隙率を有する膜である、請求項3に記載の分離膜。
【請求項5】
1体積%未満の空隙率を有する膜である、請求項3または4に記載の分離膜。
【請求項6】
前記合金は、前記Irを0.1〜40原子%含む、請求項1〜5のいずれか1項に記載の分離膜。
【請求項7】
前記合金は、前記体心立方型結晶構造において、前記Irが前記5族元素を置換した置換合金である、請求項1〜6のいずれか1項に記載の分離膜。
【請求項8】
前記合金は、面心立方型構造、六方最密充填型構造またはこれらの組み合わせの結晶構造をさらに含む、請求項1〜7のいずれか1項に記載の分離膜。
【請求項9】
前記合金は、Zr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種の金属をさらに含む、請求項1〜8のいずれか1項に記載の分離膜。
【請求項10】
前記合金は、
0.1〜40原子%のIrと、
0.1〜30原子%のZr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種の金属と、
を含む、請求項9に記載の分離膜。
【請求項11】
厚さが1〜500μmである、請求項1〜10のいずれか1項に記載の分離膜。
【請求項12】
請求項1〜11のいずれか1項に記載の分離膜を備える、水素分離膜。
【請求項13】
0.1〜1MPaの水素圧および400℃の温度条件下で測定した水素固溶度が0.01〜0.6である、請求項12に記載の水素分離膜。
【請求項14】
0.7MPaの水素圧および400℃の温度条件下で測定した水素固溶度が0.1〜0.4である、請求項12または13に記載の水素分離膜。
【請求項15】
400℃の温度条件下での水素透過度が1.0×10-8〜15.0×10-8mol/m・s・Pa1/2である、請求項12〜14のいずれか1項に記載の水素分離膜。
【請求項16】
触媒層をさらに備える、請求項12〜15のいずれか1項に記載の水素分離膜。
【請求項17】
前記触媒層は、Pd、Pt、Ru、Ir、Cu、Ag、Au、およびRhからなる群より選択される少なくとも1種の金属を含む、請求項16に記載の水素分離膜。
【請求項18】
請求項12〜17のいずれか1項に記載の水素分離膜を備える、装置。
【請求項19】
水素ガスを含む混合ガスが流入する流入口および分離された水素ガスが流出される流出口を有するチャンバをさらに備え、
前記水素分離膜は、前記チャンバを第1の部分および第2の部分に画成するように前記チャンバ内に配設され、
前記第1の部分は、前記水素ガスを含む混合ガスが流入する流入口が設けられた部分であり、
前記第2の部分は、前記分離された水素ガスが流出される流出口が設けられた部分である、請求項18に記載の装置。
【請求項1】
少なくとも1種の5族元素およびIrを含む合金を含み、前記合金は体心立方型結晶構造を含む、分離膜。
【請求項2】
前記5族元素は、V、Nb、およびTaからなる群より選択される少なくとも1種である、請求項1に記載の分離膜。
【請求項3】
10体積%未満の空隙率を有する膜である、請求項1または2に記載の分離膜。
【請求項4】
5体積%未満の空隙率を有する膜である、請求項3に記載の分離膜。
【請求項5】
1体積%未満の空隙率を有する膜である、請求項3または4に記載の分離膜。
【請求項6】
前記合金は、前記Irを0.1〜40原子%含む、請求項1〜5のいずれか1項に記載の分離膜。
【請求項7】
前記合金は、前記体心立方型結晶構造において、前記Irが前記5族元素を置換した置換合金である、請求項1〜6のいずれか1項に記載の分離膜。
【請求項8】
前記合金は、面心立方型構造、六方最密充填型構造またはこれらの組み合わせの結晶構造をさらに含む、請求項1〜7のいずれか1項に記載の分離膜。
【請求項9】
前記合金は、Zr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種の金属をさらに含む、請求項1〜8のいずれか1項に記載の分離膜。
【請求項10】
前記合金は、
0.1〜40原子%のIrと、
0.1〜30原子%のZr、Cu、Y、Ni、Al、およびMnからなる群より選択される少なくとも1種の金属と、
を含む、請求項9に記載の分離膜。
【請求項11】
厚さが1〜500μmである、請求項1〜10のいずれか1項に記載の分離膜。
【請求項12】
請求項1〜11のいずれか1項に記載の分離膜を備える、水素分離膜。
【請求項13】
0.1〜1MPaの水素圧および400℃の温度条件下で測定した水素固溶度が0.01〜0.6である、請求項12に記載の水素分離膜。
【請求項14】
0.7MPaの水素圧および400℃の温度条件下で測定した水素固溶度が0.1〜0.4である、請求項12または13に記載の水素分離膜。
【請求項15】
400℃の温度条件下での水素透過度が1.0×10-8〜15.0×10-8mol/m・s・Pa1/2である、請求項12〜14のいずれか1項に記載の水素分離膜。
【請求項16】
触媒層をさらに備える、請求項12〜15のいずれか1項に記載の水素分離膜。
【請求項17】
前記触媒層は、Pd、Pt、Ru、Ir、Cu、Ag、Au、およびRhからなる群より選択される少なくとも1種の金属を含む、請求項16に記載の水素分離膜。
【請求項18】
請求項12〜17のいずれか1項に記載の水素分離膜を備える、装置。
【請求項19】
水素ガスを含む混合ガスが流入する流入口および分離された水素ガスが流出される流出口を有するチャンバをさらに備え、
前記水素分離膜は、前記チャンバを第1の部分および第2の部分に画成するように前記チャンバ内に配設され、
前記第1の部分は、前記水素ガスを含む混合ガスが流入する流入口が設けられた部分であり、
前記第2の部分は、前記分離された水素ガスが流出される流出口が設けられた部分である、請求項18に記載の装置。
【図1A】


【図1B】


【図2】


【図3】


【図4】


【図5】


【図6A】


【図6B】


【図7A】


【図7B】


【図8】


【図9】


【図10A】


【図10B】


【図11A】


【図11B】


【図12A】


【図12B】


【図13】


【図14】




【図1B】


【図2】


【図3】


【図4】


【図5】


【図6A】


【図6B】


【図7A】


【図7B】


【図8】


【図9】


【図10A】


【図10B】


【図11A】


【図11B】


【図12A】


【図12B】


【図13】


【図14】


【公開番号】特開2013−111576(P2013−111576A)
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願番号】特願2012−257399(P2012−257399)
【出願日】平成24年11月26日(2012.11.26)
【出願人】(390019839)三星電子株式会社 (8,520)
【氏名又は名称原語表記】Samsung Electronics Co.,Ltd.
【住所又は居所原語表記】129,Samsung−ro,Yeongtong−gu,Suwon−si,Gyeonggi−do,Republic of Korea
【Fターム(参考)】
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願日】平成24年11月26日(2012.11.26)
【出願人】(390019839)三星電子株式会社 (8,520)
【氏名又は名称原語表記】Samsung Electronics Co.,Ltd.
【住所又は居所原語表記】129,Samsung−ro,Yeongtong−gu,Suwon−si,Gyeonggi−do,Republic of Korea
【Fターム(参考)】
[ Back to top ]

