分離膜の製造方法およびその分離膜を用いた分離膜モジュールの製造方法
【課題】
血液適合性に優れ、タンパク質や有機物の付着が少ない分離膜の製造方法を提供することにある。
【解決手段】
下記一般式(I)で示される繰り返し単位を1分子中に60モル%以上含有する高分子の溶液が、抱液率20%以上、600%以下の割合で含まれた分離膜を、放射線照射により処理することを特徴とする。
−[CH2−C(R1){CO−O−(R2)}]− (I)
血液適合性に優れ、タンパク質や有機物の付着が少ない分離膜の製造方法を提供することにある。
【解決手段】
下記一般式(I)で示される繰り返し単位を1分子中に60モル%以上含有する高分子の溶液が、抱液率20%以上、600%以下の割合で含まれた分離膜を、放射線照射により処理することを特徴とする。
−[CH2−C(R1){CO−O−(R2)}]− (I)
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、高分子溶液を抱液率20〜600%の割合で含まれた分離膜を放射線照射により処理することを特徴とする分離膜の製造方法に関する。
【背景技術】
【0002】
体液や血液と接触する医療用の分離膜は、タンパク質や血小板が付着すると分離膜の性能低下や、生体反応を引き起こす原因となり、深刻な問題となる。また、浄水器などの水処理膜においても、タンパク質や有機物の付着が、分離膜の性能低下を引き起こす。このような問題に対して、分離膜を親水化することによって解決しようとして、様々な検討がなされている。例えば、ポリスルホンに親水性高分子であるポリビニルピロリドンを、製膜原液の段階で混合させて成形することで、膜に親水性を与え、汚れを抑制する方法が特許文献1、特許文献2に開示されている。しかしながら、これらの方法では、表面に親水性を付与するには、製膜原液中の親水性高分子量を多くする必要があることや、基材となる高分子と相溶性のある親水性高分子に限定されることや、材料の使用用途に合わせて、最適な原液組成を検討しなければならないなどの制約を受ける。
【0003】
また、高分子表面に、ラジカル重合性モノマーを作用させて表面にグラフト重合層を形成させる方法も広く用いられている。例えば、非特許文献1には、放射線を用いたグラフト重合が、また非特許文献2には、アルゴンプラズマを用いたポリエチレン表面上へのアクリルアミドのグラフト重合が提案されている。しかしながら、これらの方法は、基材や重合性モノマーに限定があることや、未反応の重合性モノマーが残存することが懸念される。
【0004】
さらに、高分子表面にグロー放電やコロナ放電等によるプラズマ処理で、表面に親水性の官能基を導入する方法も広く用いられている。しかしながら、この方法では官能基しか導入できないため、血液適合性を導入するには不十分であり、さらには、基材の原料や形状などに限定がある。
【0005】
また、血液適合性能を上げるために、ポリスルホン系の分離膜をポリビニルピロリドンなどの親水性高分子溶液と接触させ、物理吸着させる方法(特許文献3)も開示されているが、この方法では血液と接触した際に、親水性高分子が血中に溶出してくる可能性が考えられる。
【0006】
さらには、製膜の工程中で放射線または熱により、水不溶化するポリビニルピロリドンなどの親水性成分を導入する方法(特許文献4)や、ポリスルホン系の分離膜をポリビニルピロリドンなどの親水性高分子溶液と接触させた後、放射線架橋により不溶化した被膜層を形成する方法(特許文献5)が開示されている。しかしながら、本発明者らが鋭意検討した結果、親水性高分子の被膜層を形成させる方法は、ある程度の改善が認められるが、多くの例外があった。
【0007】
すなわち、簡便にかつ血液適合性を満たす基材の処理法は未だ確立されていない。
【特許文献1】特公平2−18695号公報
【特許文献2】特開昭61−238834号公報
【特許文献3】特開平10−118472
【特許文献4】特公平8−9668
【特許文献5】特開平6−238139
【非特許文献1】A.Henglein, Angew. Chem., 70,461(1955)
【非特許文献2】筏;工材,31,62(1983)
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明の目的は、かかる従来技術の欠点を改良し、血液適合性に優れ、タンパク質や有機物の付着が少ない分離膜の製造方法を提供することにある。
【課題を解決するための手段】
【0009】
本発明者らは上記課題を達成するため鋭意検討を進めた結果、血液適合性に優れ、タンパク質や有機物の付着が少ない分離膜の製造方法は、下記の(1)〜(9)の構成によって達成される。
(1) 下記一般式(I)で示される繰り返し単位を1分子中に60モル%以上含有する高分子の溶液が、抱液率20%以上、600%以下の割合で含まれた分離膜を、放射線照射により処理することを特徴とする分離膜の製造方法。
−[CH2−C(R1){CO−O−(R2)}]− (I)
但し、式中、R1が水素原子、メチル基のいずれかを示す。R2は炭化水素基もしくは炭化水素基に、水酸基、エーテル基、エステル基から選ばれるいずれか一つが結合した構造体を表す。
【0010】
(2)前記一般式(I)におけるR2が、炭素数2〜10個の炭化水素基もしくは炭素数が2〜10個までの炭化水素基に、水酸基、エーテル基、エステル基の中から選ばれる官能基を一個有する構造を有することを特徴とする1に記載の分離膜の製造方法。
(3) 前記一般式(I)で表される繰り返し単位が、2−ヒドロキシエチルメタクリレートもしくは、2−エチルヘキシルアクリレートであることを特徴とする1または2に記載の分離膜の製造方法。
(4) 前記分離膜が中空糸膜であることを特徴とする1〜3のいずれかに記載の分離膜の製造方法。
(5) 1〜4のいずれかに記載の方法により製造された分離膜をモジュールに内蔵することを特徴とする分離膜モジュールの製造方法。
(6) 前記分離膜モジュールが、医療用モジュールであることを特徴とする5に記載の分離膜モジュールの製造方法。
(7) 前記医療用モジュールが血液浄化用モジュールであることを特徴とする6に記載の分離膜モジュールの製造方法。
(8) 前記医療用モジュールが人工腎臓用モジュールであることを特徴とする7に記載の分離膜モジュールの製造方法。
(9) 前記分離膜モジュール内の酸素濃度が10%以下の状態において、放射線照射することを特徴とする5〜8のいずれかに記載の分離膜モジュールの製造方法。
【発明の効果】
【0011】
本発明の方法は、分離膜に上記特定の高分子溶液が接触した状態で放射線照射により処理することにより、分離膜に血液適合性やタンパク質・有機物の付着しにくい性質が要求される用途に幅広く用いることができる分離膜を提供できるものである。
【発明を実施するための最良の形態】
【0012】
本発明でいうところの分離膜とは溶媒中に含まれる物質をろ過・除去する膜のことで、高分子材料が主成分であることが好ましい。高分子材料の例としては、医療用に用いられている素材が好ましく、ポリ塩化ビニル、ポリスルホンやポリエーテルスルホンなどのポリスルホン系ポリマーやポリスチレン、ポリ弗化ビニリデン、ポリイミド、ポリエーテルイミド、ポリアミドイミド、ポリアリレート、ポリエーテルエーテルケトン、ポリアクリロニトリル、ポリウレタン、ポリカーボネート、ポリエチレン、ポリプロピレン、ポリメタクリル酸メチル、ポリアミド、セルロース系ポリマーなどが挙げられる。この中でも特にポリスルホンは成形が容易で、膜にしたときの物質透過性能に優れているため、好適に用いられる。
【0013】
本発明で用いられるポリスルホン系ポリマーは、主鎖に芳香環、スルフォニル基およびエーテル基をもつもので、例えば、次式(1)、(2)の化学式で示されるポリスルホンが好適に使用されるが、本発明ではこれらに限定されない。式中のnは、例えば50〜80の如き整数である。
【0014】
【化1】

【0015】
ポリスルホン系ポリマーの具体例としては、ユーデル(登録商標)、レーデル(登録商標)AおよびR(ソルベイアドバンストポリマーズ社製)、ウルトラゾーン(登録商標)S3010およびEシリーズ(BASF社製)等のポリスルホンが挙げられる。又、本発明で用いられるポリスルホンは上記式(1)及び/又は(2)で表される繰り返し単位のみからなるポリマーが好適ではあるが、本発明の効果を妨げない範囲で他のモノマーと共重合していても良い。ただし、特に限定するものではないが、他の共重合モノマーは10重量%以下であることが好ましい。
【0016】
しかし、分離膜が医療用分離膜である場合、体液や血液が高分子材料と接触すると、タンパク質の吸着や血栓の形成などの生体反応を引き起こすため、親水性を付与して血液適合性を向上させる必要がある。また、分離膜が水処理用分離膜である場合、タンパク質や有機物などが高分子材料に吸着し、分離能を低下させるおそれがあるため、同様に親水性が要求される。
【0017】
そこで、本発明の方法においては、一般式(I)で示される繰り返し単位を60モル%以上、より好ましくは80%以上含有する高分子の溶液を、抱液率が20〜600%となるように抱液させた分離膜に放射線照射することにより、該高分子が分離膜に好適に導入され、タンパク質や血小板などの吸着を抑制することができる。
【0018】
本発明の方法は、抱液率が20〜600%の分離膜に対して用いることができる。すなわち、抱液率がこの範囲にある場合、分離膜の親水化処理後、膜を再度乾燥させて湿潤状態にする必要がないため、製造コスト的にも有利である。さらに、医療用分離膜であるならば、本発明による方法は、放射線照射により処理することで効果を発揮するものであるが、かかる処理操作により、滅菌処理操作を兼ねることができるため、好ましい。
【0019】
また、抱液とは、分離膜に液体が含まれる状態をいう。抱液率とは、膜である基材の乾燥重量に対してどの程度の液体を含むかを表すもので、分離膜に含まれる液体量(乾燥前の全重量−分離膜の絶乾重量)と乾燥重量から、次の計算式で与えられる。ここでいう、分離膜の絶乾重量とは、実施例にて後述するように、分離膜を乾燥させて、乾燥中の1時間での重量変化率が2%以内になった状態の重量をいう。なお、ここでいう「液体」とは、特に断りがない限り、本発明における「一般式(I)で示される繰り返し単位を60モル%以上含有する高分子の溶液」を意味する。
【0020】
抱液率 = (分離膜の液体量/分離膜の絶乾重量)×100 [%]
抱液率が小さいと、膜からの体液、血液等への溶出物(以下、単に溶出物という。)が増加するため、抱液率は20%以上がよく、100%以上が好ましい。例えば、抱液のための溶液として水もしくは水溶液を用いた場合、放射線照射時には、水からヒドロキシラジカルが発生し、これが起点となって高分子や分離膜の素材もラジカル化し、高分子が膜へ架橋するものと考えられる。したがって、抱液率が低いと、発生するヒドロキシラジカル量が少ないために架橋反応が不十分になり、溶出物が増加すると考えられる。また、抱液率が600%を超えても、溶出物が増加することがあるため、別途モジュールの洗浄処理が必要となり、コスト的に不利である。これは、大量の水が存在すると、過剰のヒドロキシラジカルが発生し、架橋反応だけでなく、分解反応も進行するためと考えられる。従って、分離膜の抱液率が20〜600%の範囲に入ることがよく、100〜300%の範囲に入ることが好ましい。水以外の溶媒を用いた場合でも、同じことが言える。
【0021】
本発明において、20〜600%の範囲で抱液した分離膜を製造する方法としては、例えば、分離膜をモジュール内に充填した後、モジュール内を上記溶液で満たし、次いで分離膜に含まれる溶液を気体を用いて吹き飛ばす方法が挙げられる。人工腎臓用モジュールの場合には、例えば分離膜をモジュールケースに充填した後、上記溶液を血液側入り口から血液側出口に通液し、次いで透析液側入り口から透析液側出口に通液する順でモジュール内に溶液を充填する。その後、空気、窒素などの気体を用いて所定の圧力、時間でモジュール内の透析液側、血液側に充填された溶液をそれぞれ吹き飛ばすことにより、溶液の抱液率が20〜600%である分離膜を得ることができる。
【0022】
抱液させる溶液の溶媒としては、安全性の面から水もしくは水溶液が好ましく用いられるが、本発明の効果を阻害せず、安全性や膜素材への影響がなければ、その他の溶媒を用いてもよい。当然のことではあるが、有機溶媒を選択する場合には、膜を変形させないようにする必要がある。
【0023】
本発明で用いる高分子が水に難溶な物質である場合は、その高分子を溶解できる溶媒、例えばアルコールなど有機溶媒に溶解する方法が考えられる。その溶媒を用いて抱液させて放射線照射することについて安全性に関する懸念があるならば、高分子溶液を分離膜に接触させたのちに、水もしくは水溶液で置換してから放射線照射してもよい。例えば、有機溶媒に高分子が溶解した高分子溶液をモジュールに通液し、その後水または水溶液で洗浄して、20〜600%の範囲で抱液した分離膜を製造する方法が挙げられる。
【0024】
また、分離膜の抱液率のコントロールの方法としては、減圧乾燥、高温乾燥、低温送風乾燥、ブロー乾燥など、様々な方法が考えられるが、これらに限定されるものではない。それぞれの条件を変えることによって、20〜600%の抱液率を達成できる。例えば、ブロー乾燥では、気体を用いてモジュール中の溶液を吹き飛ばす際に、その時間や、圧力を調整することによって所定の抱液率を示す分離膜を製造できる。気体による吹き飛ばし時間は、短すぎると十分に溶液が除去できず抱液率が高くなり、長すぎると溶液を吹き飛ばしすぎて抱液率が低くなる。気体による溶液の吹き飛ばし時間としては、10秒以上がよく、30秒以上がより好ましい。また、5分以下が好適に採用され、さらには2分以下が望ましい。また、圧力に関しても、溶液の残存度合を左右するため、弱すぎても強すぎても目的の抱液率は得られない。かかる観点から、気体の圧力としては、10kPa以上がよく、50kPa以上がより好ましい。また、500kPa以下が好適に採用され、さらには200kPa以下がより好適に用いられる。
【0025】
なお、モジュールケース内部の酸素濃度が高い分離膜モジュールに放射線を照射すると、モジュールケース内部に存在する空気中の酸素に起因してラジカルが発生しやすく、分離膜素材の高分子材料が分解することがあると考えられ、その場合溶出物が増加することがある。従って、酸素濃度はモジュール内に存在する気体中において10%以下であることが望ましい。
【0026】
上記のように湿潤状態をコントロールすることで、溶出物が低く、安全性の高い分離膜が提供できる。
【0027】
また、本発明の効果を損なうことがなければ、高分子溶液中に本発明における高分子以外の成分、例えば、抗酸化剤を添加しても良い。
【0028】
抗酸化剤を添加することで、発生するヒドロキシラジカル量を適正に調整することができる。例えば、医療用分離膜で、本発明の放射線照射と滅菌を兼ねる際に、通常の滅菌線量では分離膜などが劣化する場合、その防止のために抗酸化剤を併用しても良い。ここで、抗酸化剤とは、他の分子に電子を与えやすい性質を有する分子のことを言うが、ポリマーが放射線によりラジカル反応を起こす際、その反応を抑制する性質を有するものである。例えば、ビタミンCなどの水溶性ビタミン類、ポリフェノール類、メタノール、エタノール、プロパノール、エチレングリコール、グリセリンなどのアルコール類、グルコース、ガラクトース、マンノース、トレハロースなどの糖類、ソジウムハイドロサルファイト、ピロ亜硫酸ナトリウム、二チオン酸ナトリウムなどの無機塩類、尿酸、システイン、グルタチオン、酸素などが挙げられるが、これらに限定されるものではない。これらの抗酸化剤は単独で用いてもよいし、2種類以上混合して用いてもよい。本発明の方法により医療用具を製造する際は、用具の安全性を考慮する必要があるため、抗酸化剤として毒性の低いものが好適に用いられる。
【0029】
溶液中における抗酸化剤の濃度については、含有する抗酸化剤の種類、放射線の照射線量などにより異なる。抗酸化剤の濃度が低すぎると、溶媒から発生する過剰なラジカルの消去が十分にできないため、分離膜などの劣化を防ぐことができないことがある。また、抗酸化剤を多量に入れると、ラジカルが必要以上に消去されてしまうために、高分子の分離膜への導入効率が低下するために、溶出物が増加し、またタンパク質や血小板などの付着抑制効果も十分に得られないことがある。
【0030】
本発明において、高分子として代表的な親水性高分子であるポリエチレングリコールや、ポリビニルピロリドンを用いても、血液適合性やタンパク質付着抑制性を持った分離膜を得ることができない。本発明による処理を行った分離膜が血液適合性やタンパク質付着抑制性に優れているのは、高分子における親水性部分と疎水性部分とのバランス性に理由があるものと考えられる。
【0031】
すなわち、本発明における高分子を使用することによって血液適合性やタンパク質付着抑制性を示す理由は、次のように考えられる。まず、高分子の親水性部分が周囲の水分子と相互作用し、水和層を形成することで、タンパク質などの付着を抑制するものと考えられる。しかしながら、水和層は膜表面全体を覆っていなければ、タンパク質が吸着する。本発明の高分子は、分子内に疎水性部分も併せ持つため、疎水性部分が、膜表面の疎水性部分と相互作用することで、膜表面の疎水性部分の露出がなくなり、親水性の膜表面を作りだすのではないかと考えられる。つまり、高分子と膜表面の疎水性部分が膜表面の疎水性部分に対してのりのような役目を果たすことで、膜表面が効率的に高分子で覆われ、かつ、高分子中の親水性部分が水和するために、膜表面全体が水和層で覆われた状態になっているのではないかと考えられる。
【0032】
一般式(I)において、親水性部分は基本骨格のうちのエステル基(CO−O−)である。また、疎水性部分としてはR2の炭化水素部分である。ただし、親水性部分が、R2に含まれていても良い。R2における親水性部分が多すぎると親水性・疎水性のバランスが悪くなるため、R2に存在する親水性基は、水酸基、エーテル基、エステル基の中から選ばれる一個のみであることが好ましい。また、疎水性部分としてのR2の炭化水素部分については、炭素数が少なくても、また多くても、高分子における親水性部分と疎水性部分とのバランスが悪くなるため、炭素数は2〜10個が好ましく、さらには2〜8個が好ましい。炭化水素としては芳香族炭化水素であっても、脂肪族炭化水素であっても良い。このように、一般式(I)は、同一繰り返し単位内に、親水性部分と疎水性部分を併せ持つ高分子である。
【0033】
本発明で用いる高分子は、一般式(I)の繰り返し単位のみ、すなわちホモポリマーであることが好ましいが、本発明によって得られるタンパク質などの付着抑制効果を損なわない程度であれば、共重合体ポリマーであってもよい。具体的には一般式(I)の繰り返し単位が60モル%以上、さらに好ましくは90モル%以上のものが好適に用いられる。
【0034】
本発明で用いる他の高分子の例としては、入手のしやすさなどから、ポリ(2−ヒドロキシエチルメタクリレート)、ポリ(2−エチルヘキシルアクリレート)、ポリ(エチルアクリレート)などが好適に用いられ、特にタンパク質付着抑制などの効果が高いポリ(2−ヒドロキシエチルメタクリレート)が好ましい。
【0035】
放射線としてはα線、β線、γ線、X線、紫外線、電子線などが用いられる。また、人工腎臓などの医療用具は滅菌することが必要であり、近年は残留毒性の少なさや簡便さの点から、放射線滅菌法が多用されており、特に、γ線や電子線が好適に用いられている。すなわち、本発明の方法を用いることにより、滅菌を兼ねることができるので、医療用分離膜および分離膜モジュールに用いることは好ましい。例えば、血液浄化用モジュールをγ線で滅菌するには15kGy以上の線量照射が好ましい。ただし、滅菌が不要な用途に用いる場合は、この線量に限定されない。
【0036】
なお、本発明によって処理される分離膜が利用される用途としては、医療用分離膜、特に血液浄化用モジュール、人工腎臓用モジュール、生体成分分離用モジュールなどが挙げられるが、これらに限定されるものではない。また、水処理用分離膜としては、浄水器用膜、上水浄化膜、下水浄化膜、逆浸透膜などが挙げられる。
【0037】
特に、近年は分離膜モジュールの軽量化や、寒冷地での凍結防止を図るため、抱液率の低い湿潤タイプやドライタイプの分離膜が注目されてきている。
【0038】
本発明の血液浄化用モジュールとは、血液を体外に循環させる際に、吸着や濾過、拡散によって血中の老廃物や有害物質を取り除く機能を有したモジュールのことをいい、具体例としては、人工腎臓や外毒素吸着カラムなどがある。
【0039】
血液浄化用モジュールに内蔵される分離膜の形態は特に限定されるものではなく、平膜、中空糸膜などの形態で用いられる。しかし、処理効率すなわち血液と接触する表面積の確保などを考慮すると中空糸膜型であることが好ましい。
【0040】
本発明にかかる分離膜モジュールの製造方法としては、その用途により、種々の方法があるが、大まかな工程としては、分離膜の製造工程と、その分離膜をモジュールに組み込むという工程にわけることができる。放射線照射による処理を、分離膜をモジュールに組み込む工程の前に用いてもよいし、分離膜をモジュールに組み込んだ後に用いてもよい。モジュール化した後にγ線照射するのであれば、医療用に用いる場合、滅菌も同時に行うことができるので好ましい。
【0041】
人工腎臓に用いられる中空糸膜モジュールの製造方法についての一例を示す。
【0042】
人工腎臓に内蔵される中空糸膜の製造方法としては、一方法としてつぎのような方法がある。すなわち、ポリスルホンとポリビニルピロリドン(重量比率20:1〜1:5が好ましく、5:1〜1:1がより好ましい)をポリスルホンの良溶媒(N,N−ジメチルアセトアミド、ジメチルスルホキシド、ジメチルホルムアミド、N−メチルピロリドン、ジオキサンなどが好ましい)および貧溶媒の混合溶液に溶解させた製膜原液(濃度は、10〜30重量%が好ましく、15〜25重量%がより好ましい)を二重環状口金の外側の管内から吐出させる。その際、二重環状口金の内側の管内に注入液(芯液)を流し、ともに乾式部を走行させた後凝固浴へ導く。この際、乾式部の湿度が影響を与えるために、相対湿度が低い場合は乾式部走行中に膜外表面からの水分補給によって、外表面近傍での相分離挙動を速め、孔径拡大し、結果として透析の際の透過・拡散抵抗を減らすことも可能である。ただし、相対湿度が高すぎると外表面での原液凝固が支配的になり、かえって孔径が小さくなり、結果として透析の際の透過・拡散抵抗を増大する傾向がある。そのため、相対湿度としては60〜90%が好適である。また、注入液組成としてはプロセス適性から原液に用いた溶媒を基本とする組成からなるものを用いることが好ましい。注入液濃度としては、例えばジメチルアセトアミドを用いたときは、45〜80重量%、さらには60〜75重量%の水溶液が好適に用いられる。
【0043】
中空糸膜をモジュールに内蔵する方法としては、特に限定されないが、一例を示すと次の通りである。まず、中空糸膜を必要な長さに切断し、必要本数を束ねた後、筒状ケースに入れる。その後両端に仮のキャップをし、中空糸膜両端部にポッティング剤を充填させる。ポッティング剤の材料としては、ウレタン樹脂等が好ましい。このとき遠心機でモジュールを回転させながらポッティング剤を中空糸膜両端よりも中央側から注入して、遠心力により両端部に移動させ、固化させる方法は、ポッティング剤が均一に充填されるために好ましい方法である。ポッティング剤が固化した後、中空糸膜の両端が開口するように両端部を切断し、中空糸膜モジュールを得ることができる。
【0044】
本発明の製造方法において、上記のようにして得られた中空糸膜を高分子溶液で抱液率を20〜600%に調整し、γ線等で照射したのち、モジュールに組み込んでもよい。もしくは、モジュール化を行った後に、上記した方法により分離膜の抱液率を20〜600%に調整し、γ線照射してもよい。モジュール化の後にγ線照射すれば、滅菌も同時に行うことができるので好ましい。
【0045】
以下実施例を挙げて本発明を説明するが、本発明はこれらの例によって限定されるものではない。
【実施例】
【0046】
以下実施例と比較例を挙げて本発明を説明するが、本発明はこれらの例によって限定されるものではない。また、特に断りのない限り、部とは重量部を示す。
1.中空糸膜モジュールの作製
ポリスルホン(アモコ社 Udel−P3500)16部、ポリビニルピロリドン(インターナショナルスペシャルプロダクツ社;以下ISP社と略す)K30 3部、ポリビニルピロリドン(ISP社K90)3部をジメチルアセトアミド77部、水1部を加熱溶解し、製膜原液とした。
【0047】
この原液を温度50℃の紡糸口金部へ送り、外径0.35mm、内径0.25mmの二重スリット管の外側の管から、芯液としてジメチルアセトアミド63部、水37部からなる溶液を内側の管から吐出させたものとともに口金を通して吐出させ、中空糸膜を形成させた後、温度30℃、露点29℃の、350mmのドライゾーン雰囲気(乾式部)を経て、ジメチルアセトアミド20重量%、水80重量%からなる温度40℃の凝固浴を通過させ、60〜75℃で90秒洗浄する水洗工程、130℃での乾燥工程を2分通過させ、160℃で行うクリンプ工程を経て得られた中空糸膜を巻き取り束とした。得られた中空糸分離膜の内径は0.2mmであり 、膜厚は0.04mmであった。この中空糸12000本を図1に示すような、透析液入口および透析液出口を有する円筒状のプラスチックケースに挿入し、両端部を樹脂で封止して、有効膜面積1.6m2の人工腎臓用中空糸膜モジュールを作成した。
2.測定方法
(1)中空糸膜のヒト血小板付着試験方法
18mmφのポリスチレン製の円形フィルムに両面テープを貼り付け、そこに中空糸膜を固定した。貼り付けた中空糸膜を片刃で半円筒状にそぎ切り、中空糸膜の内表面を露出させた(中空糸内表面に汚れや傷、折り目などがあると、その部分に血小板が付着し、正しい評価ができないことがあるのでこのような部分はできるだけ用いないよう注意を要する。)。
【0048】
筒状に切ったFalcon(登録商標)チューブ(18mmφ、No.2051)に該円形フィルムを、中空糸膜を貼り付けた面が円筒内部に入るように取り付け、パラフィルム(登録商標)で取り付け部分の隙間を埋めてカップ状の試験サンプルを作成した。この円筒管内を生理食塩水で洗浄後、生理食塩水で満たした。成人健常者の静脈血を採血後、直ちにヘパリンナトリウム注射液(味の素社製)を50U/mlになるように添加した。前記円筒管内の生理食塩水を廃棄後、前記血液を、採血後10分以内に、円筒管内に1.0ml入れ、37℃で1時間振盪させた。その後、円筒管内を10mlの生理食塩水で洗浄し、2.5容積%グルタルアルデヒド(ナカライテスク社製)生理食塩水溶液で血液成分の固定を行い、20mlの蒸留水にて洗浄した。円筒管から洗浄した円形フィルムを取り外し、走査型電子顕微鏡の試料台に両面テープで貼り付けた。該試料台を常温66Paにて10時間減圧乾燥した。その後、スパッタリングにより、白金/パラジウムの薄膜を円形フィルム上の中空糸膜表面に形成させて、試料とした。この中空糸膜の内表面をフィールドエミッション型走査型電子顕微鏡(日立社製S800)にて、倍率1500倍で試料の内表面を観察し、1視野中(4.3×103μm2)の付着血小板数を数えた。中空糸長手方向における中央付近で、異なる10視野での付着血小板数の平均値を血小板付着数(個/4.3×103μm2)とした。中空糸の長手方向における端の部分は、血液溜まりができやすいため付着数の計測対象からはずした。
(2)抱液率の測定方法
抱液処理を行った中空糸膜モジュールから中空糸を取り出し、重量を測定した。その後、常温66Paにて常温10時間減圧乾燥したのち、分離膜の乾燥重量を測定した。次にもう1時間同様の方法で減圧乾燥して乾燥重量を測定し、重量変化率を測定するという手順を繰り返し、重量変化率が2%以内になった状態の重量を絶乾重量とし、乾燥前の重量と絶乾重量との差を中空糸膜の液体量とした。下式にて抱液率を求めた。
【0049】
抱液率 = (分離膜の液体量/分離膜の絶乾重量)×100 [%]
(3)酸素濃度の測定方法
東レ・テクノ(株)にて、中空糸膜モジュールを窒素雰囲気内に入れ、モジュール内ガスを採取し、島津製作所社製GC−14Bを用いて、GC−TCD法にて、ケース内の酸素濃度を測定した。
【0050】
分析条件を下記に示した。
【0051】
使用機器:島津製作所社製GC−14B
カラム:Molecular sieve 5A 2.0m
カラム温度:60℃
入口温度:150℃
出口温度:200℃
キャリアガス:ヘリウム 0.8kg/cm2
ディテクター:TCD
電流:50mA
(4)溶出物の測定方法
中空糸膜モジュールの血液側(膜の内側)に初期洗浄液として常温下で水を流量100mL/minで流し、最初に流出される50mLをサンプリングした。このサンプルから任意の10mLを取り出し、2.0×10−3mol/L過マンガン酸カリウム水溶液20mL、希塩酸1mLを加え、250℃のホットプレート上で3分間煮沸、撹拌した。室温まで冷却し、ヨウ化カリウム水溶液1mLを加え、よく撹拌後10分放置し、1.0×10−2mol/Lチオ硫酸ナトリウム水溶液で滴定した。別途、中空糸膜モジュールを通さなかった水について、測定サンプルと同様の操作をした。中空糸膜モジュールを通さない水の滴定に要したチオ硫酸ナトリウム水溶液量と、サンプルの滴定に要したチオ硫酸ナトリウム水溶液量との差を、溶出物により消費された2.0×10−3mol/L過マンガン酸カリウム水溶液量(過マンガン酸カリウム水溶液の消費量)とした。これを溶出物量(mL)とした。
(実施例1)
高分子としてポリ(2−ヒドロキシエチルメタクリレート)(シグマ・アルドリッチ社製、P3932 粉末,culture tested)を使用した。ポリ(2−ヒドロキシエチルメタクリレート)が0.1重量%の濃度のメタノール溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側(膜の外側)入り口から透析液側出口に通液する順で流して充填した。その後、純水にて同様に通液し、洗浄を行った。さらに100kPaの圧縮空気を透析液側ノズルから血液側に1分間流して充填液を押しだし、次に血液側ノズルから同様に圧縮空気を流して充填液を1分間吹き飛ばした。さらに窒素で透析液側、血液側それぞれを100kPaで1分間ブローし、抱液率270%、酸素濃度3%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、付着血小板数が少なく、血液適合性に優れた分離膜を得た。また、溶出物も少ない人工腎臓モジュールが得られた。
(実施例2)
高分子としてポリ(2−エチルヘキシルアクリレート)(シグマ・アルドリッチ社製、R157023 secondary standard)を使用した。ポリ(2−エチルヘキシルアクリレート)が0.1重量%の濃度のメタノール溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。その後、純水にて同様に通液し、洗浄を行った。さらに、実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率270%、酸素濃度3%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、付着血小板数が少なく、血液適合性に優れた分離膜を得た。また、溶出物も少ない人工腎臓モジュールが得られた。
(比較例1)
高分子としてポリビニルピロリドン(BASF社製、重量平均分子量10000)を使用した。ポリビニルピロリドンが0.1重量%の濃度の水溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。さらに実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率275%、酸素濃度4%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、溶出物は少ないが、付着血小板数が多くなった。高分子の親水・疎水バランスに偏りがあるためと考えられる。
(比較例2)
高分子としてポリエチレングリコール(日本油脂社製、重量平均分子量2000)を使用した。ポリエチレングリコールが0.1重量%の濃度の水溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。さらに実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率270%、酸素濃度4%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、溶出物は少ないが、付着血小板数が多くなった。高分子の親水・疎水バランスに偏りがあるためと考えられる。
(比較例3)
高分子としてポリアクリル酸(和光純薬工業社製、重量平均分子量25000)を使用した。ポリアクリル酸が0.1重量%の濃度の水溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。さらに実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率260%、酸素濃度4%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、溶出物は少ないが、付着血小板数が多くなった。高分子の親水・疎水バランスに偏りがあるためと考えられる。
【0052】
【表1】

【産業上の利用可能性】
【0053】
本発明は血液適合性やタンパク質や有機物の非付着が要求される用途に好適に用いられる。例えば、血液浄化用の分離膜では血液適合性やタンパク質の非付着が要求されるし、浄水器用膜、上水浄化膜、下水浄化膜、逆浸透膜や、生体成分分離用膜などではタンパク質や有機物の非付着が要求されるため、好適に用いられる。また、これらの分離膜を内蔵したモジュールの製造時にも好適に用いられる。特に、血液適合性が要求される血液浄化用モジュールの製造時には好適に用いられる。
【図面の簡単な説明】
【0054】
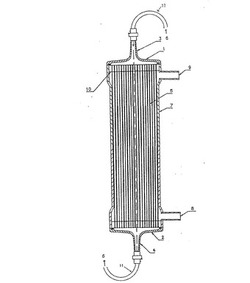
【図1】本発明に用いられる人工腎臓の一態様を示す。
【符号の説明】
【0055】
1.動脈側ヘッダー
2.静脈側ヘッダー
3.血液導入口
4.血液導出口
5.中空糸膜
6.血液
7.モジュールケース
8.透析液導入口
9.透析液導出口
10.ポッティング部
11.血液回路
【技術分野】
【0001】
本発明は、高分子溶液を抱液率20〜600%の割合で含まれた分離膜を放射線照射により処理することを特徴とする分離膜の製造方法に関する。
【背景技術】
【0002】
体液や血液と接触する医療用の分離膜は、タンパク質や血小板が付着すると分離膜の性能低下や、生体反応を引き起こす原因となり、深刻な問題となる。また、浄水器などの水処理膜においても、タンパク質や有機物の付着が、分離膜の性能低下を引き起こす。このような問題に対して、分離膜を親水化することによって解決しようとして、様々な検討がなされている。例えば、ポリスルホンに親水性高分子であるポリビニルピロリドンを、製膜原液の段階で混合させて成形することで、膜に親水性を与え、汚れを抑制する方法が特許文献1、特許文献2に開示されている。しかしながら、これらの方法では、表面に親水性を付与するには、製膜原液中の親水性高分子量を多くする必要があることや、基材となる高分子と相溶性のある親水性高分子に限定されることや、材料の使用用途に合わせて、最適な原液組成を検討しなければならないなどの制約を受ける。
【0003】
また、高分子表面に、ラジカル重合性モノマーを作用させて表面にグラフト重合層を形成させる方法も広く用いられている。例えば、非特許文献1には、放射線を用いたグラフト重合が、また非特許文献2には、アルゴンプラズマを用いたポリエチレン表面上へのアクリルアミドのグラフト重合が提案されている。しかしながら、これらの方法は、基材や重合性モノマーに限定があることや、未反応の重合性モノマーが残存することが懸念される。
【0004】
さらに、高分子表面にグロー放電やコロナ放電等によるプラズマ処理で、表面に親水性の官能基を導入する方法も広く用いられている。しかしながら、この方法では官能基しか導入できないため、血液適合性を導入するには不十分であり、さらには、基材の原料や形状などに限定がある。
【0005】
また、血液適合性能を上げるために、ポリスルホン系の分離膜をポリビニルピロリドンなどの親水性高分子溶液と接触させ、物理吸着させる方法(特許文献3)も開示されているが、この方法では血液と接触した際に、親水性高分子が血中に溶出してくる可能性が考えられる。
【0006】
さらには、製膜の工程中で放射線または熱により、水不溶化するポリビニルピロリドンなどの親水性成分を導入する方法(特許文献4)や、ポリスルホン系の分離膜をポリビニルピロリドンなどの親水性高分子溶液と接触させた後、放射線架橋により不溶化した被膜層を形成する方法(特許文献5)が開示されている。しかしながら、本発明者らが鋭意検討した結果、親水性高分子の被膜層を形成させる方法は、ある程度の改善が認められるが、多くの例外があった。
【0007】
すなわち、簡便にかつ血液適合性を満たす基材の処理法は未だ確立されていない。
【特許文献1】特公平2−18695号公報
【特許文献2】特開昭61−238834号公報
【特許文献3】特開平10−118472
【特許文献4】特公平8−9668
【特許文献5】特開平6−238139
【非特許文献1】A.Henglein, Angew. Chem., 70,461(1955)
【非特許文献2】筏;工材,31,62(1983)
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明の目的は、かかる従来技術の欠点を改良し、血液適合性に優れ、タンパク質や有機物の付着が少ない分離膜の製造方法を提供することにある。
【課題を解決するための手段】
【0009】
本発明者らは上記課題を達成するため鋭意検討を進めた結果、血液適合性に優れ、タンパク質や有機物の付着が少ない分離膜の製造方法は、下記の(1)〜(9)の構成によって達成される。
(1) 下記一般式(I)で示される繰り返し単位を1分子中に60モル%以上含有する高分子の溶液が、抱液率20%以上、600%以下の割合で含まれた分離膜を、放射線照射により処理することを特徴とする分離膜の製造方法。
−[CH2−C(R1){CO−O−(R2)}]− (I)
但し、式中、R1が水素原子、メチル基のいずれかを示す。R2は炭化水素基もしくは炭化水素基に、水酸基、エーテル基、エステル基から選ばれるいずれか一つが結合した構造体を表す。
【0010】
(2)前記一般式(I)におけるR2が、炭素数2〜10個の炭化水素基もしくは炭素数が2〜10個までの炭化水素基に、水酸基、エーテル基、エステル基の中から選ばれる官能基を一個有する構造を有することを特徴とする1に記載の分離膜の製造方法。
(3) 前記一般式(I)で表される繰り返し単位が、2−ヒドロキシエチルメタクリレートもしくは、2−エチルヘキシルアクリレートであることを特徴とする1または2に記載の分離膜の製造方法。
(4) 前記分離膜が中空糸膜であることを特徴とする1〜3のいずれかに記載の分離膜の製造方法。
(5) 1〜4のいずれかに記載の方法により製造された分離膜をモジュールに内蔵することを特徴とする分離膜モジュールの製造方法。
(6) 前記分離膜モジュールが、医療用モジュールであることを特徴とする5に記載の分離膜モジュールの製造方法。
(7) 前記医療用モジュールが血液浄化用モジュールであることを特徴とする6に記載の分離膜モジュールの製造方法。
(8) 前記医療用モジュールが人工腎臓用モジュールであることを特徴とする7に記載の分離膜モジュールの製造方法。
(9) 前記分離膜モジュール内の酸素濃度が10%以下の状態において、放射線照射することを特徴とする5〜8のいずれかに記載の分離膜モジュールの製造方法。
【発明の効果】
【0011】
本発明の方法は、分離膜に上記特定の高分子溶液が接触した状態で放射線照射により処理することにより、分離膜に血液適合性やタンパク質・有機物の付着しにくい性質が要求される用途に幅広く用いることができる分離膜を提供できるものである。
【発明を実施するための最良の形態】
【0012】
本発明でいうところの分離膜とは溶媒中に含まれる物質をろ過・除去する膜のことで、高分子材料が主成分であることが好ましい。高分子材料の例としては、医療用に用いられている素材が好ましく、ポリ塩化ビニル、ポリスルホンやポリエーテルスルホンなどのポリスルホン系ポリマーやポリスチレン、ポリ弗化ビニリデン、ポリイミド、ポリエーテルイミド、ポリアミドイミド、ポリアリレート、ポリエーテルエーテルケトン、ポリアクリロニトリル、ポリウレタン、ポリカーボネート、ポリエチレン、ポリプロピレン、ポリメタクリル酸メチル、ポリアミド、セルロース系ポリマーなどが挙げられる。この中でも特にポリスルホンは成形が容易で、膜にしたときの物質透過性能に優れているため、好適に用いられる。
【0013】
本発明で用いられるポリスルホン系ポリマーは、主鎖に芳香環、スルフォニル基およびエーテル基をもつもので、例えば、次式(1)、(2)の化学式で示されるポリスルホンが好適に使用されるが、本発明ではこれらに限定されない。式中のnは、例えば50〜80の如き整数である。
【0014】
【化1】

【0015】
ポリスルホン系ポリマーの具体例としては、ユーデル(登録商標)、レーデル(登録商標)AおよびR(ソルベイアドバンストポリマーズ社製)、ウルトラゾーン(登録商標)S3010およびEシリーズ(BASF社製)等のポリスルホンが挙げられる。又、本発明で用いられるポリスルホンは上記式(1)及び/又は(2)で表される繰り返し単位のみからなるポリマーが好適ではあるが、本発明の効果を妨げない範囲で他のモノマーと共重合していても良い。ただし、特に限定するものではないが、他の共重合モノマーは10重量%以下であることが好ましい。
【0016】
しかし、分離膜が医療用分離膜である場合、体液や血液が高分子材料と接触すると、タンパク質の吸着や血栓の形成などの生体反応を引き起こすため、親水性を付与して血液適合性を向上させる必要がある。また、分離膜が水処理用分離膜である場合、タンパク質や有機物などが高分子材料に吸着し、分離能を低下させるおそれがあるため、同様に親水性が要求される。
【0017】
そこで、本発明の方法においては、一般式(I)で示される繰り返し単位を60モル%以上、より好ましくは80%以上含有する高分子の溶液を、抱液率が20〜600%となるように抱液させた分離膜に放射線照射することにより、該高分子が分離膜に好適に導入され、タンパク質や血小板などの吸着を抑制することができる。
【0018】
本発明の方法は、抱液率が20〜600%の分離膜に対して用いることができる。すなわち、抱液率がこの範囲にある場合、分離膜の親水化処理後、膜を再度乾燥させて湿潤状態にする必要がないため、製造コスト的にも有利である。さらに、医療用分離膜であるならば、本発明による方法は、放射線照射により処理することで効果を発揮するものであるが、かかる処理操作により、滅菌処理操作を兼ねることができるため、好ましい。
【0019】
また、抱液とは、分離膜に液体が含まれる状態をいう。抱液率とは、膜である基材の乾燥重量に対してどの程度の液体を含むかを表すもので、分離膜に含まれる液体量(乾燥前の全重量−分離膜の絶乾重量)と乾燥重量から、次の計算式で与えられる。ここでいう、分離膜の絶乾重量とは、実施例にて後述するように、分離膜を乾燥させて、乾燥中の1時間での重量変化率が2%以内になった状態の重量をいう。なお、ここでいう「液体」とは、特に断りがない限り、本発明における「一般式(I)で示される繰り返し単位を60モル%以上含有する高分子の溶液」を意味する。
【0020】
抱液率 = (分離膜の液体量/分離膜の絶乾重量)×100 [%]
抱液率が小さいと、膜からの体液、血液等への溶出物(以下、単に溶出物という。)が増加するため、抱液率は20%以上がよく、100%以上が好ましい。例えば、抱液のための溶液として水もしくは水溶液を用いた場合、放射線照射時には、水からヒドロキシラジカルが発生し、これが起点となって高分子や分離膜の素材もラジカル化し、高分子が膜へ架橋するものと考えられる。したがって、抱液率が低いと、発生するヒドロキシラジカル量が少ないために架橋反応が不十分になり、溶出物が増加すると考えられる。また、抱液率が600%を超えても、溶出物が増加することがあるため、別途モジュールの洗浄処理が必要となり、コスト的に不利である。これは、大量の水が存在すると、過剰のヒドロキシラジカルが発生し、架橋反応だけでなく、分解反応も進行するためと考えられる。従って、分離膜の抱液率が20〜600%の範囲に入ることがよく、100〜300%の範囲に入ることが好ましい。水以外の溶媒を用いた場合でも、同じことが言える。
【0021】
本発明において、20〜600%の範囲で抱液した分離膜を製造する方法としては、例えば、分離膜をモジュール内に充填した後、モジュール内を上記溶液で満たし、次いで分離膜に含まれる溶液を気体を用いて吹き飛ばす方法が挙げられる。人工腎臓用モジュールの場合には、例えば分離膜をモジュールケースに充填した後、上記溶液を血液側入り口から血液側出口に通液し、次いで透析液側入り口から透析液側出口に通液する順でモジュール内に溶液を充填する。その後、空気、窒素などの気体を用いて所定の圧力、時間でモジュール内の透析液側、血液側に充填された溶液をそれぞれ吹き飛ばすことにより、溶液の抱液率が20〜600%である分離膜を得ることができる。
【0022】
抱液させる溶液の溶媒としては、安全性の面から水もしくは水溶液が好ましく用いられるが、本発明の効果を阻害せず、安全性や膜素材への影響がなければ、その他の溶媒を用いてもよい。当然のことではあるが、有機溶媒を選択する場合には、膜を変形させないようにする必要がある。
【0023】
本発明で用いる高分子が水に難溶な物質である場合は、その高分子を溶解できる溶媒、例えばアルコールなど有機溶媒に溶解する方法が考えられる。その溶媒を用いて抱液させて放射線照射することについて安全性に関する懸念があるならば、高分子溶液を分離膜に接触させたのちに、水もしくは水溶液で置換してから放射線照射してもよい。例えば、有機溶媒に高分子が溶解した高分子溶液をモジュールに通液し、その後水または水溶液で洗浄して、20〜600%の範囲で抱液した分離膜を製造する方法が挙げられる。
【0024】
また、分離膜の抱液率のコントロールの方法としては、減圧乾燥、高温乾燥、低温送風乾燥、ブロー乾燥など、様々な方法が考えられるが、これらに限定されるものではない。それぞれの条件を変えることによって、20〜600%の抱液率を達成できる。例えば、ブロー乾燥では、気体を用いてモジュール中の溶液を吹き飛ばす際に、その時間や、圧力を調整することによって所定の抱液率を示す分離膜を製造できる。気体による吹き飛ばし時間は、短すぎると十分に溶液が除去できず抱液率が高くなり、長すぎると溶液を吹き飛ばしすぎて抱液率が低くなる。気体による溶液の吹き飛ばし時間としては、10秒以上がよく、30秒以上がより好ましい。また、5分以下が好適に採用され、さらには2分以下が望ましい。また、圧力に関しても、溶液の残存度合を左右するため、弱すぎても強すぎても目的の抱液率は得られない。かかる観点から、気体の圧力としては、10kPa以上がよく、50kPa以上がより好ましい。また、500kPa以下が好適に採用され、さらには200kPa以下がより好適に用いられる。
【0025】
なお、モジュールケース内部の酸素濃度が高い分離膜モジュールに放射線を照射すると、モジュールケース内部に存在する空気中の酸素に起因してラジカルが発生しやすく、分離膜素材の高分子材料が分解することがあると考えられ、その場合溶出物が増加することがある。従って、酸素濃度はモジュール内に存在する気体中において10%以下であることが望ましい。
【0026】
上記のように湿潤状態をコントロールすることで、溶出物が低く、安全性の高い分離膜が提供できる。
【0027】
また、本発明の効果を損なうことがなければ、高分子溶液中に本発明における高分子以外の成分、例えば、抗酸化剤を添加しても良い。
【0028】
抗酸化剤を添加することで、発生するヒドロキシラジカル量を適正に調整することができる。例えば、医療用分離膜で、本発明の放射線照射と滅菌を兼ねる際に、通常の滅菌線量では分離膜などが劣化する場合、その防止のために抗酸化剤を併用しても良い。ここで、抗酸化剤とは、他の分子に電子を与えやすい性質を有する分子のことを言うが、ポリマーが放射線によりラジカル反応を起こす際、その反応を抑制する性質を有するものである。例えば、ビタミンCなどの水溶性ビタミン類、ポリフェノール類、メタノール、エタノール、プロパノール、エチレングリコール、グリセリンなどのアルコール類、グルコース、ガラクトース、マンノース、トレハロースなどの糖類、ソジウムハイドロサルファイト、ピロ亜硫酸ナトリウム、二チオン酸ナトリウムなどの無機塩類、尿酸、システイン、グルタチオン、酸素などが挙げられるが、これらに限定されるものではない。これらの抗酸化剤は単独で用いてもよいし、2種類以上混合して用いてもよい。本発明の方法により医療用具を製造する際は、用具の安全性を考慮する必要があるため、抗酸化剤として毒性の低いものが好適に用いられる。
【0029】
溶液中における抗酸化剤の濃度については、含有する抗酸化剤の種類、放射線の照射線量などにより異なる。抗酸化剤の濃度が低すぎると、溶媒から発生する過剰なラジカルの消去が十分にできないため、分離膜などの劣化を防ぐことができないことがある。また、抗酸化剤を多量に入れると、ラジカルが必要以上に消去されてしまうために、高分子の分離膜への導入効率が低下するために、溶出物が増加し、またタンパク質や血小板などの付着抑制効果も十分に得られないことがある。
【0030】
本発明において、高分子として代表的な親水性高分子であるポリエチレングリコールや、ポリビニルピロリドンを用いても、血液適合性やタンパク質付着抑制性を持った分離膜を得ることができない。本発明による処理を行った分離膜が血液適合性やタンパク質付着抑制性に優れているのは、高分子における親水性部分と疎水性部分とのバランス性に理由があるものと考えられる。
【0031】
すなわち、本発明における高分子を使用することによって血液適合性やタンパク質付着抑制性を示す理由は、次のように考えられる。まず、高分子の親水性部分が周囲の水分子と相互作用し、水和層を形成することで、タンパク質などの付着を抑制するものと考えられる。しかしながら、水和層は膜表面全体を覆っていなければ、タンパク質が吸着する。本発明の高分子は、分子内に疎水性部分も併せ持つため、疎水性部分が、膜表面の疎水性部分と相互作用することで、膜表面の疎水性部分の露出がなくなり、親水性の膜表面を作りだすのではないかと考えられる。つまり、高分子と膜表面の疎水性部分が膜表面の疎水性部分に対してのりのような役目を果たすことで、膜表面が効率的に高分子で覆われ、かつ、高分子中の親水性部分が水和するために、膜表面全体が水和層で覆われた状態になっているのではないかと考えられる。
【0032】
一般式(I)において、親水性部分は基本骨格のうちのエステル基(CO−O−)である。また、疎水性部分としてはR2の炭化水素部分である。ただし、親水性部分が、R2に含まれていても良い。R2における親水性部分が多すぎると親水性・疎水性のバランスが悪くなるため、R2に存在する親水性基は、水酸基、エーテル基、エステル基の中から選ばれる一個のみであることが好ましい。また、疎水性部分としてのR2の炭化水素部分については、炭素数が少なくても、また多くても、高分子における親水性部分と疎水性部分とのバランスが悪くなるため、炭素数は2〜10個が好ましく、さらには2〜8個が好ましい。炭化水素としては芳香族炭化水素であっても、脂肪族炭化水素であっても良い。このように、一般式(I)は、同一繰り返し単位内に、親水性部分と疎水性部分を併せ持つ高分子である。
【0033】
本発明で用いる高分子は、一般式(I)の繰り返し単位のみ、すなわちホモポリマーであることが好ましいが、本発明によって得られるタンパク質などの付着抑制効果を損なわない程度であれば、共重合体ポリマーであってもよい。具体的には一般式(I)の繰り返し単位が60モル%以上、さらに好ましくは90モル%以上のものが好適に用いられる。
【0034】
本発明で用いる他の高分子の例としては、入手のしやすさなどから、ポリ(2−ヒドロキシエチルメタクリレート)、ポリ(2−エチルヘキシルアクリレート)、ポリ(エチルアクリレート)などが好適に用いられ、特にタンパク質付着抑制などの効果が高いポリ(2−ヒドロキシエチルメタクリレート)が好ましい。
【0035】
放射線としてはα線、β線、γ線、X線、紫外線、電子線などが用いられる。また、人工腎臓などの医療用具は滅菌することが必要であり、近年は残留毒性の少なさや簡便さの点から、放射線滅菌法が多用されており、特に、γ線や電子線が好適に用いられている。すなわち、本発明の方法を用いることにより、滅菌を兼ねることができるので、医療用分離膜および分離膜モジュールに用いることは好ましい。例えば、血液浄化用モジュールをγ線で滅菌するには15kGy以上の線量照射が好ましい。ただし、滅菌が不要な用途に用いる場合は、この線量に限定されない。
【0036】
なお、本発明によって処理される分離膜が利用される用途としては、医療用分離膜、特に血液浄化用モジュール、人工腎臓用モジュール、生体成分分離用モジュールなどが挙げられるが、これらに限定されるものではない。また、水処理用分離膜としては、浄水器用膜、上水浄化膜、下水浄化膜、逆浸透膜などが挙げられる。
【0037】
特に、近年は分離膜モジュールの軽量化や、寒冷地での凍結防止を図るため、抱液率の低い湿潤タイプやドライタイプの分離膜が注目されてきている。
【0038】
本発明の血液浄化用モジュールとは、血液を体外に循環させる際に、吸着や濾過、拡散によって血中の老廃物や有害物質を取り除く機能を有したモジュールのことをいい、具体例としては、人工腎臓や外毒素吸着カラムなどがある。
【0039】
血液浄化用モジュールに内蔵される分離膜の形態は特に限定されるものではなく、平膜、中空糸膜などの形態で用いられる。しかし、処理効率すなわち血液と接触する表面積の確保などを考慮すると中空糸膜型であることが好ましい。
【0040】
本発明にかかる分離膜モジュールの製造方法としては、その用途により、種々の方法があるが、大まかな工程としては、分離膜の製造工程と、その分離膜をモジュールに組み込むという工程にわけることができる。放射線照射による処理を、分離膜をモジュールに組み込む工程の前に用いてもよいし、分離膜をモジュールに組み込んだ後に用いてもよい。モジュール化した後にγ線照射するのであれば、医療用に用いる場合、滅菌も同時に行うことができるので好ましい。
【0041】
人工腎臓に用いられる中空糸膜モジュールの製造方法についての一例を示す。
【0042】
人工腎臓に内蔵される中空糸膜の製造方法としては、一方法としてつぎのような方法がある。すなわち、ポリスルホンとポリビニルピロリドン(重量比率20:1〜1:5が好ましく、5:1〜1:1がより好ましい)をポリスルホンの良溶媒(N,N−ジメチルアセトアミド、ジメチルスルホキシド、ジメチルホルムアミド、N−メチルピロリドン、ジオキサンなどが好ましい)および貧溶媒の混合溶液に溶解させた製膜原液(濃度は、10〜30重量%が好ましく、15〜25重量%がより好ましい)を二重環状口金の外側の管内から吐出させる。その際、二重環状口金の内側の管内に注入液(芯液)を流し、ともに乾式部を走行させた後凝固浴へ導く。この際、乾式部の湿度が影響を与えるために、相対湿度が低い場合は乾式部走行中に膜外表面からの水分補給によって、外表面近傍での相分離挙動を速め、孔径拡大し、結果として透析の際の透過・拡散抵抗を減らすことも可能である。ただし、相対湿度が高すぎると外表面での原液凝固が支配的になり、かえって孔径が小さくなり、結果として透析の際の透過・拡散抵抗を増大する傾向がある。そのため、相対湿度としては60〜90%が好適である。また、注入液組成としてはプロセス適性から原液に用いた溶媒を基本とする組成からなるものを用いることが好ましい。注入液濃度としては、例えばジメチルアセトアミドを用いたときは、45〜80重量%、さらには60〜75重量%の水溶液が好適に用いられる。
【0043】
中空糸膜をモジュールに内蔵する方法としては、特に限定されないが、一例を示すと次の通りである。まず、中空糸膜を必要な長さに切断し、必要本数を束ねた後、筒状ケースに入れる。その後両端に仮のキャップをし、中空糸膜両端部にポッティング剤を充填させる。ポッティング剤の材料としては、ウレタン樹脂等が好ましい。このとき遠心機でモジュールを回転させながらポッティング剤を中空糸膜両端よりも中央側から注入して、遠心力により両端部に移動させ、固化させる方法は、ポッティング剤が均一に充填されるために好ましい方法である。ポッティング剤が固化した後、中空糸膜の両端が開口するように両端部を切断し、中空糸膜モジュールを得ることができる。
【0044】
本発明の製造方法において、上記のようにして得られた中空糸膜を高分子溶液で抱液率を20〜600%に調整し、γ線等で照射したのち、モジュールに組み込んでもよい。もしくは、モジュール化を行った後に、上記した方法により分離膜の抱液率を20〜600%に調整し、γ線照射してもよい。モジュール化の後にγ線照射すれば、滅菌も同時に行うことができるので好ましい。
【0045】
以下実施例を挙げて本発明を説明するが、本発明はこれらの例によって限定されるものではない。
【実施例】
【0046】
以下実施例と比較例を挙げて本発明を説明するが、本発明はこれらの例によって限定されるものではない。また、特に断りのない限り、部とは重量部を示す。
1.中空糸膜モジュールの作製
ポリスルホン(アモコ社 Udel−P3500)16部、ポリビニルピロリドン(インターナショナルスペシャルプロダクツ社;以下ISP社と略す)K30 3部、ポリビニルピロリドン(ISP社K90)3部をジメチルアセトアミド77部、水1部を加熱溶解し、製膜原液とした。
【0047】
この原液を温度50℃の紡糸口金部へ送り、外径0.35mm、内径0.25mmの二重スリット管の外側の管から、芯液としてジメチルアセトアミド63部、水37部からなる溶液を内側の管から吐出させたものとともに口金を通して吐出させ、中空糸膜を形成させた後、温度30℃、露点29℃の、350mmのドライゾーン雰囲気(乾式部)を経て、ジメチルアセトアミド20重量%、水80重量%からなる温度40℃の凝固浴を通過させ、60〜75℃で90秒洗浄する水洗工程、130℃での乾燥工程を2分通過させ、160℃で行うクリンプ工程を経て得られた中空糸膜を巻き取り束とした。得られた中空糸分離膜の内径は0.2mmであり 、膜厚は0.04mmであった。この中空糸12000本を図1に示すような、透析液入口および透析液出口を有する円筒状のプラスチックケースに挿入し、両端部を樹脂で封止して、有効膜面積1.6m2の人工腎臓用中空糸膜モジュールを作成した。
2.測定方法
(1)中空糸膜のヒト血小板付着試験方法
18mmφのポリスチレン製の円形フィルムに両面テープを貼り付け、そこに中空糸膜を固定した。貼り付けた中空糸膜を片刃で半円筒状にそぎ切り、中空糸膜の内表面を露出させた(中空糸内表面に汚れや傷、折り目などがあると、その部分に血小板が付着し、正しい評価ができないことがあるのでこのような部分はできるだけ用いないよう注意を要する。)。
【0048】
筒状に切ったFalcon(登録商標)チューブ(18mmφ、No.2051)に該円形フィルムを、中空糸膜を貼り付けた面が円筒内部に入るように取り付け、パラフィルム(登録商標)で取り付け部分の隙間を埋めてカップ状の試験サンプルを作成した。この円筒管内を生理食塩水で洗浄後、生理食塩水で満たした。成人健常者の静脈血を採血後、直ちにヘパリンナトリウム注射液(味の素社製)を50U/mlになるように添加した。前記円筒管内の生理食塩水を廃棄後、前記血液を、採血後10分以内に、円筒管内に1.0ml入れ、37℃で1時間振盪させた。その後、円筒管内を10mlの生理食塩水で洗浄し、2.5容積%グルタルアルデヒド(ナカライテスク社製)生理食塩水溶液で血液成分の固定を行い、20mlの蒸留水にて洗浄した。円筒管から洗浄した円形フィルムを取り外し、走査型電子顕微鏡の試料台に両面テープで貼り付けた。該試料台を常温66Paにて10時間減圧乾燥した。その後、スパッタリングにより、白金/パラジウムの薄膜を円形フィルム上の中空糸膜表面に形成させて、試料とした。この中空糸膜の内表面をフィールドエミッション型走査型電子顕微鏡(日立社製S800)にて、倍率1500倍で試料の内表面を観察し、1視野中(4.3×103μm2)の付着血小板数を数えた。中空糸長手方向における中央付近で、異なる10視野での付着血小板数の平均値を血小板付着数(個/4.3×103μm2)とした。中空糸の長手方向における端の部分は、血液溜まりができやすいため付着数の計測対象からはずした。
(2)抱液率の測定方法
抱液処理を行った中空糸膜モジュールから中空糸を取り出し、重量を測定した。その後、常温66Paにて常温10時間減圧乾燥したのち、分離膜の乾燥重量を測定した。次にもう1時間同様の方法で減圧乾燥して乾燥重量を測定し、重量変化率を測定するという手順を繰り返し、重量変化率が2%以内になった状態の重量を絶乾重量とし、乾燥前の重量と絶乾重量との差を中空糸膜の液体量とした。下式にて抱液率を求めた。
【0049】
抱液率 = (分離膜の液体量/分離膜の絶乾重量)×100 [%]
(3)酸素濃度の測定方法
東レ・テクノ(株)にて、中空糸膜モジュールを窒素雰囲気内に入れ、モジュール内ガスを採取し、島津製作所社製GC−14Bを用いて、GC−TCD法にて、ケース内の酸素濃度を測定した。
【0050】
分析条件を下記に示した。
【0051】
使用機器:島津製作所社製GC−14B
カラム:Molecular sieve 5A 2.0m
カラム温度:60℃
入口温度:150℃
出口温度:200℃
キャリアガス:ヘリウム 0.8kg/cm2
ディテクター:TCD
電流:50mA
(4)溶出物の測定方法
中空糸膜モジュールの血液側(膜の内側)に初期洗浄液として常温下で水を流量100mL/minで流し、最初に流出される50mLをサンプリングした。このサンプルから任意の10mLを取り出し、2.0×10−3mol/L過マンガン酸カリウム水溶液20mL、希塩酸1mLを加え、250℃のホットプレート上で3分間煮沸、撹拌した。室温まで冷却し、ヨウ化カリウム水溶液1mLを加え、よく撹拌後10分放置し、1.0×10−2mol/Lチオ硫酸ナトリウム水溶液で滴定した。別途、中空糸膜モジュールを通さなかった水について、測定サンプルと同様の操作をした。中空糸膜モジュールを通さない水の滴定に要したチオ硫酸ナトリウム水溶液量と、サンプルの滴定に要したチオ硫酸ナトリウム水溶液量との差を、溶出物により消費された2.0×10−3mol/L過マンガン酸カリウム水溶液量(過マンガン酸カリウム水溶液の消費量)とした。これを溶出物量(mL)とした。
(実施例1)
高分子としてポリ(2−ヒドロキシエチルメタクリレート)(シグマ・アルドリッチ社製、P3932 粉末,culture tested)を使用した。ポリ(2−ヒドロキシエチルメタクリレート)が0.1重量%の濃度のメタノール溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側(膜の外側)入り口から透析液側出口に通液する順で流して充填した。その後、純水にて同様に通液し、洗浄を行った。さらに100kPaの圧縮空気を透析液側ノズルから血液側に1分間流して充填液を押しだし、次に血液側ノズルから同様に圧縮空気を流して充填液を1分間吹き飛ばした。さらに窒素で透析液側、血液側それぞれを100kPaで1分間ブローし、抱液率270%、酸素濃度3%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、付着血小板数が少なく、血液適合性に優れた分離膜を得た。また、溶出物も少ない人工腎臓モジュールが得られた。
(実施例2)
高分子としてポリ(2−エチルヘキシルアクリレート)(シグマ・アルドリッチ社製、R157023 secondary standard)を使用した。ポリ(2−エチルヘキシルアクリレート)が0.1重量%の濃度のメタノール溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。その後、純水にて同様に通液し、洗浄を行った。さらに、実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率270%、酸素濃度3%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、付着血小板数が少なく、血液適合性に優れた分離膜を得た。また、溶出物も少ない人工腎臓モジュールが得られた。
(比較例1)
高分子としてポリビニルピロリドン(BASF社製、重量平均分子量10000)を使用した。ポリビニルピロリドンが0.1重量%の濃度の水溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。さらに実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率275%、酸素濃度4%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、溶出物は少ないが、付着血小板数が多くなった。高分子の親水・疎水バランスに偏りがあるためと考えられる。
(比較例2)
高分子としてポリエチレングリコール(日本油脂社製、重量平均分子量2000)を使用した。ポリエチレングリコールが0.1重量%の濃度の水溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。さらに実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率270%、酸素濃度4%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、溶出物は少ないが、付着血小板数が多くなった。高分子の親水・疎水バランスに偏りがあるためと考えられる。
(比較例3)
高分子としてポリアクリル酸(和光純薬工業社製、重量平均分子量25000)を使用した。ポリアクリル酸が0.1重量%の濃度の水溶液を中空糸膜モジュールの血液側入口から血液側出口に通液し、次に透析液側入り口から透析液側出口に通液する順で流して充填した。さらに実施例1と同様の方法で充填液を除去した。さらに窒素で透析液側、血液側それぞれをブローし、抱液率260%、酸素濃度4%にした。その後、該モジュールの中空糸膜にγ線を照射した。γ線照射線量は27kGyであった。該モジュールの中空糸を切り出し、血小板付着試験を行った。結果は表1の通りであり、溶出物は少ないが、付着血小板数が多くなった。高分子の親水・疎水バランスに偏りがあるためと考えられる。
【0052】
【表1】

【産業上の利用可能性】
【0053】
本発明は血液適合性やタンパク質や有機物の非付着が要求される用途に好適に用いられる。例えば、血液浄化用の分離膜では血液適合性やタンパク質の非付着が要求されるし、浄水器用膜、上水浄化膜、下水浄化膜、逆浸透膜や、生体成分分離用膜などではタンパク質や有機物の非付着が要求されるため、好適に用いられる。また、これらの分離膜を内蔵したモジュールの製造時にも好適に用いられる。特に、血液適合性が要求される血液浄化用モジュールの製造時には好適に用いられる。
【図面の簡単な説明】
【0054】
【図1】本発明に用いられる人工腎臓の一態様を示す。
【符号の説明】
【0055】
1.動脈側ヘッダー
2.静脈側ヘッダー
3.血液導入口
4.血液導出口
5.中空糸膜
6.血液
7.モジュールケース
8.透析液導入口
9.透析液導出口
10.ポッティング部
11.血液回路
【特許請求の範囲】
【請求項1】
下記一般式(I)で示される繰り返し単位を1分子中に60モル%以上含有する高分子の溶液が、抱液率20%以上、600%以下の割合で含まれた分離膜を、放射線照射により処理することを特徴とする分離膜の製造方法。
−[CH2−C(R1){CO−O−(R2)}]− (I)
但し、式中、R1が水素原子、メチル基のいずれかを示す。R2は炭化水素基もしくは炭化水素基に、水酸基、エーテル基、エステル基から選ばれるいずれか一つが結合した構造体を表す。
【請求項2】
前記一般式(I)におけるR2が、炭素数2〜10個の炭化水素基もしくは炭素数が2〜10個までの炭化水素基に、水酸基、エーテル基、エステル基の中から選ばれる官能基を一個有する構造を有することを特徴とする請求項1に記載の分離膜の製造方法。
【請求項3】
前記一般式(I)で表される繰り返し単位が、2−ヒドロキシエチルメタクリレートもしくは2−エチルヘキシルアクリレートであることを特徴とする請求項1または2に記載の分離膜の製造方法。
【請求項4】
前記分離膜が中空糸膜であることを特徴とする請求項1〜3のいずれかに記載の分離膜の製造方法。
【請求項5】
請求項1〜4のいずれかに記載の方法により製造された分離膜をモジュールに内蔵することを特徴とする分離膜モジュールの製造方法。
【請求項6】
前記分離膜モジュールが、医療用モジュールであることを特徴とする請求項5に記載の分離膜モジュールの製造方法。
【請求項7】
前記医療用モジュールが血液浄化用モジュールであることを特徴とする請求項6に記載の分離膜モジュールの製造方法。
【請求項8】
前記医療用モジュールが人工腎臓用モジュールであることを特徴とする請求項7に記載の分離膜モジュールの製造方法。
【請求項9】
前記分離膜モジュール内の酸素濃度が10%以下の状態において、放射線照射することを特徴とする請求項5〜8のいずれかに記載の分離膜モジュールの製造方法。
【請求項1】
下記一般式(I)で示される繰り返し単位を1分子中に60モル%以上含有する高分子の溶液が、抱液率20%以上、600%以下の割合で含まれた分離膜を、放射線照射により処理することを特徴とする分離膜の製造方法。
−[CH2−C(R1){CO−O−(R2)}]− (I)
但し、式中、R1が水素原子、メチル基のいずれかを示す。R2は炭化水素基もしくは炭化水素基に、水酸基、エーテル基、エステル基から選ばれるいずれか一つが結合した構造体を表す。
【請求項2】
前記一般式(I)におけるR2が、炭素数2〜10個の炭化水素基もしくは炭素数が2〜10個までの炭化水素基に、水酸基、エーテル基、エステル基の中から選ばれる官能基を一個有する構造を有することを特徴とする請求項1に記載の分離膜の製造方法。
【請求項3】
前記一般式(I)で表される繰り返し単位が、2−ヒドロキシエチルメタクリレートもしくは2−エチルヘキシルアクリレートであることを特徴とする請求項1または2に記載の分離膜の製造方法。
【請求項4】
前記分離膜が中空糸膜であることを特徴とする請求項1〜3のいずれかに記載の分離膜の製造方法。
【請求項5】
請求項1〜4のいずれかに記載の方法により製造された分離膜をモジュールに内蔵することを特徴とする分離膜モジュールの製造方法。
【請求項6】
前記分離膜モジュールが、医療用モジュールであることを特徴とする請求項5に記載の分離膜モジュールの製造方法。
【請求項7】
前記医療用モジュールが血液浄化用モジュールであることを特徴とする請求項6に記載の分離膜モジュールの製造方法。
【請求項8】
前記医療用モジュールが人工腎臓用モジュールであることを特徴とする請求項7に記載の分離膜モジュールの製造方法。
【請求項9】
前記分離膜モジュール内の酸素濃度が10%以下の状態において、放射線照射することを特徴とする請求項5〜8のいずれかに記載の分離膜モジュールの製造方法。
【図1】




【公開番号】特開2007−260592(P2007−260592A)
【公開日】平成19年10月11日(2007.10.11)
【国際特許分類】
【出願番号】特願2006−90626(P2006−90626)
【出願日】平成18年3月29日(2006.3.29)
【出願人】(000003159)東レ株式会社 (7,677)
【Fターム(参考)】
【公開日】平成19年10月11日(2007.10.11)
【国際特許分類】
【出願日】平成18年3月29日(2006.3.29)
【出願人】(000003159)東レ株式会社 (7,677)
【Fターム(参考)】
[ Back to top ]

