初期充填速度に基づく全血ヘマトクリット値を測定するためのシステム、デバイス、及び方法
【課題】血液サンプルのヘマトクリット値を決定するための方法、並びに併せて使用するデバイス及びシステムを提供する。
【解決手段】作用電極及び対電極を有するサンプル分析デバイスに血液サンプルを供給する際、電極間に電位を印加し電流を求める事により、サンプルのデバイスへの初期充填速度を計算する。次いで、求められた初期充填速度を考慮して、ヘマトクリット値並びに分析物の濃度を決定する。
【解決手段】作用電極及び対電極を有するサンプル分析デバイスに血液サンプルを供給する際、電極間に電位を印加し電流を求める事により、サンプルのデバイスへの初期充填速度を計算する。次いで、求められた初期充填速度を考慮して、ヘマトクリット値並びに分析物の濃度を決定する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、サンプル中の分析物の濃度を決定する工程に関し、より具体的には、サンプルの初期充填速度に基づいて濃度をより正確に決定する工程に関する。
【背景技術】
【0002】
生理学的流体、例えば、血液又は血液由来の生成物中の分析物検出は、今日の社会では、今まで以上に重要性を増している。分析物検出の分析は、臨床検査、家庭検査などを含めて、多様な用途に利用法が見出され、そのような検査の結果は、様々な病状の診断及び処置において主要な役割を果たしている。目的の分析物には、糖尿病管理のためのグルコース、コレステロールなどが挙げられる。こうした分析物検出の重要性の高まりに応じて、臨床での使用及び家庭での使用の両方に対応する多様な分析物検出の手順及びデバイスが開発されてきた。これらのデバイスのいくつかには、電気化学セル、電気化学センサ、ヘモグロビンセンサ、酸化防止剤センサ、バイオセンサ、及び免疫センサが挙げられる。
【0003】
分析物検出に影響を及ぼし得る血液の1つの特性は、ヘマトクリットである。ヘマトクリットのレベルは、様々な人により、非常に異なり得る。非限定的な例として、貧血を罹患する人は、約20%のヘマトクリットレベルを有し得る一方、新生児は、約65%のヘマトクリットレベルを有し得る。一定期間にわたって、同一の個人から摂取されたサンプルでさえ、異なるヘマトクリットレベルを有する場合がある。更に、高いヘマトクリットは、血液の粘度を増加させることもでき、その粘度が次には、分析物検出に付随する他のパラメータに影響を及ぼす場合があるため、ヘマトクリットのサンプルへの影響を明らかにすることが、正確な分析物濃度決定を行う上で重要になる場合がある。
【0004】
血液サンプル中のヘマトクリットの異なるレベルを明らかにしてきた1つの方法は、血液から血漿を分離し、次いで、調節された血漿量に対して抗原の濃度を再計算することによるものである。分離は、例えば、遠心分離工程を実施することによって達成されてきた。血液サンプル中のヘマトクリットの異なるレベルを明らかにしてきた他の方法には、計算に平均メハトクリットを使用する工程、又は別個の工程においてヘマトクリットを測定し、次いで、血漿値に対する抗原の濃度を計算する工程が挙げられる。しかしながら、これらの方法は、少なくとも、それらが不必要なサンプルの取り扱いを伴い、更なる時間を要し、最終決定において実質的な誤差を引き起こすため、望ましくないと考えられている。更に、サンプルが分析される環境の温度は、分析物濃度決定の精度に負の影響を及ぼし得る。
【発明の概要】
【発明が解決しようとする課題】
【0005】
したがって、広範なヘマトクリットレベル及び温度を明らかにする、より正確な分析物濃度測定を得る方法を開発することが望ましいであろう。ヘマトクリットレベルを迅速に決定する方法を開発することも望ましいであろう。
【課題を解決するための手段】
【0006】
出願者は、前述の付随問題がほとんどないか、又はそれが全くない、広範なヘマトクリットレベル及び温度を明らかにする、より正確な分析物濃度測定を得る方法を開発することが望ましいであろうことを理解している。出願者は、ヘマトクリットレベルを迅速に決定する方法を開発することも望ましいであろうことも理解している。したがって、システム、デバイス、及び方法は、概して、血液サンプルのヘマトクリット値を決定し、かつサンプル中の分析物の濃度を決定するために提供される。全血サンプルのヘマトクリット値を決定するための方法の例示的な一実施例において、該方法は、全血のサンプルを、毛管空隙を有するサンプル分析デバイスに提供する工程と、毛管空隙の少なくとも一部分内のサンプルの初期充填速度を測定する工程と、初期充填速度からサンプルのヘマトクリット値を決定する工程と、を含む。初期充填速度を測定する工程は、電位を印加する工程と、電流を測定する工程と、初期電流量を決定する工程と、を含むことができる。一実施形態において、電流測定は、約10ミリ秒毎に少なくとも約50ミリ秒間実施され、平均電流は、電流測定値に基づき計算される。別の代替的実施形態において、初期充填速度を測定する工程は、光信号を検出する工程を含むことができる。一実施形態において、初期充填速度を測定する工程は、サンプルが毛管空隙に進入した直後に生じる。更に別の実施形態において、初期充填速度を測定する工程は、サンプルが、検出信号が生成されるサンプル分析デバイスの毛管空隙の領域内に横断した後に生じる。サンプルの温度は、測定するか、又は推測することができる。測定又は推測された温度は、サンプルのヘマトクリット値を決定するために使用することができる。例示的な一実施形態において、サンプル分析デバイスは、免疫センサを含む。
【0007】
ヘマトクリットレベルを測定する工程の他に、該方法は、サンプル中の分析物の濃度を決定するために使用することもできる。例えば、ヘマトクリット値を決定するための方法は、決定されたヘマトクリット値を考慮して、分析物の濃度を計算する工程を含むことができる。これは、例えば、電位を印加し、電位を印加した後の初期電流を測定し、電位を逆転させることによって達成することができる。一定期間にわたる電流の変化は、電位の逆転後、測定することができる。一定期間にわたる、測定された電流の変化は、分析物の濃度を計算するためにも使用することができる。一実施形態では、サンプルの温度は、測定するか、又は推測することができる。かかる実施形態において、一定期間にわたる、測定された電流の変化、及びサンプルの温度は、分析物の濃度を計算するために使用することができる。
【0008】
サンプル中の分析物の濃度を決定するための方法の例示的な一実施形態において、該方法は、分析物を含有するサンプルを、作用電極及び対電極を有するサンプル分析デバイスに提供する工程と、作用電極と対電極との間に電位を印加する工程と、サンプルの初期充填速度を決定する工程と、初期充填速度を考慮して、分析物の濃度を計算する工程と、を含む。一実施形態において、初期充填速度は、光信号における変化率を決定することによって決定することができる。別の実施形態において、初期充填速度は、初期電流量を決定することによって決定することができる。初期電流量は、例えば、約10ミリ秒毎に少なくとも約50ミリ秒間電流測定を実施し、次いで、電流測定値に基づき平均電流を計算することによって決定することができる。更に別の実施形態において、初期充填速度は、電位を印加した後の初期電流を測定し、サンプル中のヘマトクリットのレベルを決定し、作用電極と対電極との間で電位を逆転させることによって決定することができる。更に、分析物の濃度は、決定されたヘマトクリットのレベルに基づき、算定することができる。
【0009】
分析物の濃度を決定するための方法は、電位の逆転後、一定期間にわたって、電流の変化、即ち、電流対時間のグラフの勾配mを測定する工程を更に含むことができる。その結果、分析物の濃度、COは、一定期間にわたる、電流の変化を考慮して、計算することができる。例えば、分析物の濃度は、以下の等式を使用して、計算することができる:
【数1】

式中、
【数2】

であり、Hは、ヘマトクリットのレベルである。ヘマトクリットのレベルHは、以下の等式を使用して決定することができる:
【数3】

式中、
【数4】

は、初期電流の絶対値である。
【0010】
サンプル分析デバイスは、免疫センサであってもよい。濃度が分析される分析物は、C反応性タンパク質であってもよい。分析物は、血液であってもよい。一実施形態において、血液は、全血を含む。該方法は、全血の温度Tを測定する工程か、あるいは、周辺温度を測定し、それを使用して血液の温度Tを推測する工程を更に含むことができる。該方法は、電位の逆転後、一定期間にわたって、電流の変化、即ち、電流対時間のグラフの勾配mを測定する工程も更に含むことができる。その結果、分析物の濃度、COは、一定期間にわたる、電流の変化を考慮して、計算することができる。例えば、分析物の濃度は、以下の等式を使用して、計算することができる:
【数5】

式中、
【数6】

であり、Hは、ヘマトクリットのレベルである。ヘマトクリットのレベルHは、以下の等式によって決定することができる:
【数7】

式中、
【数8】

は、初期電流の絶対値である。
【0011】
電気化学システムの例示的な一実施形態において、システムは、下部電極及び上部電極を有する免疫センサと、免疫センサの下部電極と上部電極との間に電位を印加するように構成された計器と、免疫センサ内に導入されたサンプルの開始充填速度を測定するように構成された制御ユニットと、を含む。制御ユニットは、開始充填速度を使用して、サンプルが血液を含むときのサンプルのヘマトクリット値及びサンプル中の分析物の濃度のうちの少なくとも1つを計算するように更に構成される。システムは、免疫センサの少なくとも一部分を加熱するように構成された加熱要素も含むことができる。
【0012】
免疫センサは、第1の液体試薬と、第2の液体試薬と、抗原と抱合した磁気ビーズと、を含むことができる。一実施形態において、第1の液体試薬は、緩衝液中の酵素と抱合した抗体を含むことができる。第1の液体試薬は、下部電極上に縞模様に付けることができ、乾燥させることができる。第2の液体試薬は、フェリシアン化物と、酵素のための基質と、希酸溶液中のメディエータとを含むことができる。第2の液体試薬は、下部電極上に縞模様に付けることができ、乾燥させることができる。一方、磁気ビーズは、上部電極上に縞模様に付けることができ、乾燥させることができる。
【0013】
免疫センサは、複数のチャンバーと、セパレータと、通気孔と、1つ以上の封止用構成要素とを更に含むことができる。セパレータは、下部電極と上部電極との間に配設することができる。複数のチャンバーは、反応チャンバーと、検出チャンバーと、充填チャンバーと、を含むことができる。反応チャンバーは、セパレータ内に形成されることができ、第1の試薬、及び抗原と抱合した磁気ビーズがその中に配設されることができる。検出チャンバーも、セパレータ内に形成されることができ、第2の試薬がその中に配設されることができる。充填チャンバーは、セパレータ、並びに下部電極及び上部電極の一方に少なくとも部分的に形成されることができ、検出チャンバーからある距離だけ離間されることができ、反応チャンバーの少なくとも一部分に重なり合うことができる。通気孔は、セパレータ、下部電極、及び上部電極の各々において少なくとも部分的に形成されることができ、反応チャンバーからある距離だけ離間されることができ、検出チャンバーの少なくとも一部分に重なり合うことができる。一実施形態において、1つ以上の封止用構成要素は、第1の封止用構成要素及び第2の封止用構成要素であることができる。第1の封止用構成要素は、下部電極及び上部電極のうちの一方に取り付けられた、組み込まれた抗凝固剤を有することができ、通気孔の上に配設されることができ、充填チャンバーの壁を形成すると共に通気孔を封止するように構成されることができる。第2の封止用構成要素は、下部電極及び上部電極のうちのもう一方に取り付けることができ、通気孔の上に配設されることができ、通気孔を封止するように構成されることができる。一実施形態において、第1の封止用構成要素は、親水性接着テープを含む。
【0014】
一実施形態において、電気化学システムの制御ユニットは、サンプルの初期充填速度を測定するために、光信号における変化率を測定するように構成された光信号検出器を含むことができる。別の実施形態において、制御ユニットは、サンプルの初期充填速度を測定するために、初期電流量を測定するように構成された電流量検出器を含むことができる。更に別の実施形態において、制御ユニットは、サンプルが免疫センサの毛管空隙に進入した直後のサンプルの初期充填速度を測定するように構成されることができる。更に別の実施形態において、制御ユニットは、サンプルが、検出信号が生成される免疫センサの毛管空隙の領域内に横断した後の初期充填速度を測定するように構成されることができる。制御ユニット、免疫センサ、及び計器のうちの少なくとも1つは、サンプルの温度を測定するか、又はサンプルの温度を推測するように構成されることができる。
【0015】
システムが濃度を計算する分析物は、C反応性タンパク質であってよい。免疫センサ内に導入されるサンプルは、血液であってよい。一実施形態において、血液は、全血を含む。
【0016】
サンプル分析デバイスはまた、非限定的な例として、電気化学セル、電気化学センサ、グルコースセンサ、グルコース計器、ヘモグロビンセンサ、酸化防止剤センサ、及びバイオセンサを含む、多数の他の分析デバイスであってよい。一実施形態において、サンプル分析デバイスは、グルコースセンサを含む。グルコースセンサは、作用電極及び対又は対/基準電極を有する電気化学セルを含むことができる。作用電極及び対又は対/基準電極は、約500マイクロメートル以下で離間することができる。一実施形態において、電極間の間隔は、約80マイクロメートル〜約200マイクロメートルの範囲である。間隔は、所望の結果を達成するため、例えば、実質的に、所望時間内に定常状態の電流を達成するために決定することができる。一実施形態において、電極間の間隔は、対電極からの反応生成物が作用電極に到達するように選択される。
【0017】
作用電極及び対又は対/基準電極は、様々な構成を有することができる。例えば、電極は、互いに面することができるか、それらは、実質的に互いに面することができるか、又は、それらは、電極がほぼ同じ平面上に位置付けられる隣接構造を有することができる。電極は、実質的に同一の対応領域を有することができる。電極は、平面的であってもよい。一実施形態において、電気化学セルは、作用電極、対電極、及び別個の基準電極を含む。別の実施形態において、電気化学セルは、2つの電極対を有することができる。電極対は、作用電極、対電極、対/基準電極、及び別個の基準電極のうちの任意の組み合わせを含むことができるが、例示的な一実施形態において、各対は、作用電極及び対又は対/基準電極を含む。更に別の実施形態において、電気化学セルは、約1.5マイクロリットル以下の有効なセル量を有することができる。あるいは、電気化学セルは、中空であってもよい。
【0018】
電位は、非限定的な例として計器を含む、多数の異なる機構によって、セルの電極に印加することができる。電位の規模は、非限定的な例として、セル内のサンプルの所望の反応を含む、多数の異なる要因による可能性がある。一実施形態において、電位の規模は、サンプルの還元された形態の電解酸化、又は酸化された形態の電解還元が、実質的に拡散律速であるように、選択することができる。
【0019】
サンプルは、毛管現象によりセルに進入することができる。制御ユニットは、セルに進入するサンプルの初期速度を決定するために使用することができる。一実施形態において、制御ユニットは、サンプルの初期充填速度を測定するために、光信号における変化率を測定するように構成される、光信号検出器を含むことができる。別の実施形態において、制御ユニットは、サンプルの初期充填速度を測定するために、初期電流量を測定するように構成される、電流量検出器を含むことができる。更に別の実施形態において、制御ユニットは、サンプルが電気化学セルの毛管空隙に進入した直後のサンプルの初期充填速度を測定するように構成されることができる。更に別の実施形態において、制御ユニットは、サンプルが、検出信号が生成される電気化学セルの毛管空隙の領域内に横断した後の初期充填速度を測定するように構成されることができる。制御ユニット、電気化学セル、及び計器のうちの少なくとも1つは、サンプルの温度を測定するか、又はサンプルの温度を推測するように構成されることができる。
【0020】
血液サンプル中の抗原を測定するための方法の例示的な一実施形態は、2つの電極を有する免疫センサ及び免疫センサの2つの電極との間に電位を印加するように構成された計器を提供する工程を含むことができる。該方法は、抗原を含有する血液サンプルを免疫センサ内に導入する工程と、2つの電極間に電位を印加する工程と、血液サンプルの初期充填速度を決定する工程と、初期充填速度を考慮して、抗原の濃度を計算する工程とを更に含むことができる。代替的実施形態において、該方法は、血液のヘマトクリットレベルのみを測定するか、又は血液のヘマトクリットレベル及び血中の抗原の濃度の両方を測定するように設定することができる。免疫センサは、2つの電極間に配設されたセパレータ内に形成された反応チャンバー及び検出チャンバーと、セパレータ及び2つの電極のうちの1つ内に少なくとも部分的に形成された充填チャンバーと、セパレータ及び2つの電極内に少なくとも部分的に形成された通気孔と、を更に含むことができる。充填チャンバーは、検出チャンバーからある距離だけ離間されることができ、反応チャンバーの少なくとも一部分に重なり合うことができる。通気孔は、反応チャンバーからある距離だけ離間されることができ、検出チャンバーの少なくとも一部分に重なり合うことができる。血液サンプルの抗原は、C反応性タンパク質であってよい。該方法は、血液サンプルの温度を測定する工程、あるいは血液サンプルの温度を推測する工程、及び、次いで、電位を逆転させる工程後に、一定期間にわたって、電流の変化を測定する工程を更に含むことができる。その結果、抗原の濃度は、一定期間にわたる電流の変化及び測定又は推測された温度を考慮して、計算することができる。
【0021】
血液サンプルを測定するための方法は、第1の緩衝液中の抗体酵素複合体及び第2の緩衝液中の抗原に連結した磁気ビーズを反応チャンバー内に提供する工程を更に含むことができる。希酸中のフェリシアン化物、グリコース、及びメディエータは、検出チャンバー内に提供することができる。第1の封止は、充填チャンバーの壁を形成する通気孔の第1の側面上に提供することができ、第2の封止は、通気孔の第2の側面上に提供することができる。免疫センサ内に導入される血液サンプルの少なくとも一部分は、それが免疫センサ内に導入されるときに、充填チャンバーから反応チャンバーに移動する。
【0022】
該方法は、封止のうちの少なくとも1つを穿孔することによって、所定時間後に、通気孔を開口する工程を更に含むことができる。封止のうちの少なくとも1つを穿孔することで、磁気ビーズに拘束されていない抗原酵素複合体を含有する血液サンプルの一部分が、検出チャンバーに移動するのを可能にする。更に、該方法は、検出チャンバー内でグルコースの酸化を触媒する工程を含むことができ、これは、フェロシアン化物の形成をもたらすことができる。電流は、フェロシアン化物から電気化学的に検出することができ、血液サンプル中の抗原の濃度は、検出した信号を考慮して、計算することができる。
【0023】
一実施形態において、初期充填速度を決定する工程は、電位を印加した後の初期電流を測定する工程と、サンプル中のヘマトクリットのレベルを決定する工程と、作用電極と対電極との間の電位を逆転させる工程と、を含むことができる。したがって、分析物の濃度は、決定されたヘマトクリットのレベルに基づき、算定することができる。該方法は、電位の逆転後、一定期間にわたって、電流の変化を測定する工程を更に含むことができる。したがって、分析物の濃度は、一定期間にわたる電流の変化を考慮して、計算することができる。別の実施形態において、初期充填速度を決定する工程は、初期充填速度を決定するために、光信号における変化率を決定する工程を含むことができる。更に別の実施形態において、初期充填速度を決定する工程は、初期充填速度を決定するために、初期電流量を決定する工程を含むことができる。初期充填速度は、血液サンプルが免疫センサの毛管空隙に進入した直後に決定することができる。あるいは、初期充填速度は、血液サンプルが、検出信号が生成される免疫センサの毛管空隙の領域内に横断した後に決定することができる。
【0024】
本発明は、以下の詳細な説明を付属の図面と併せ読むことでより詳細に理解されるであろう。
【図面の簡単な説明】
【0025】
【図1】本発明に従う、免疫センサ、及び初期充填速度を計算するための光検出器を有する制御ユニットの一実施形態の斜視図。
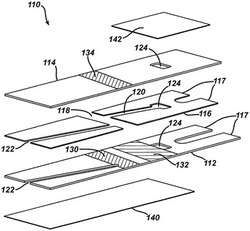
【図2】本発明に従う、免疫センサの別の例示的実施形態の分解図。免疫センサは、初期充填速度を計算するための電気化学検出システムを有する制御ユニットと共に使用するように構成される。
【図3】本発明に従う、電気化学セルの例示的な一実施形態の概略側面図(原寸に比例しない)。
【図4】上から見た図3の電気化学セルの平面図。
【図5】本発明に従う、中空の電気化学セルの例示的な一実施形態の概略断面図(原寸に比例しない)。
【図6】本明細書に提供される様々な血液サンプルを試験するための例示的な一実施例と併せて、図2のデバイスを使用して実施された電流対時間遷移のプロット。
【図7】電流に対しての図6に関連した実施例に関連して使用された、各血液サンプルに関するヘマトクリット濃度レベルのプロット。
【図8】図6に関連した各血液サンプルの決定されたヘマトクリット濃度レベルに対する、図6に関連した各血液サンプルに関して決定されたヘマトクリット濃度レベルの誤差割合のプロット。
【図9】図6に関連した各血液サンプルの計算されたC反応性タンパク質のレベルの、従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値に対するプロット。
【図10】本明細書に提供される様々な血液サンプルを試験するための別の例示的実施例と併せて、図2の免疫センサを使用して実施した、血液サンプルが配設される免疫センサの検出チャンバーの電流対温度のプロット。
【図11】図10に関連した各血液サンプルの決定されたヘマトクリット濃度レベルに対する、図10に関連した各血液サンプルに関して決定されたヘマトクリット濃度レベルの誤差割合のプロット。
【図12】図10に関連した各血液サンプルに関する、経時的な電流の変化に基づき決定された勾配の、血液サンプルが配設される免疫センサの検出チャンバーの温度に対するプロット。
【図13】従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値に対して、約33.5%のヘマトクリットレベル及び約47.5%のヘマトクリットレベルを有する、図10に関連した血液サンプルの計算されたC反応性タンパク質レベルのプロット。
【発明を実施するための形態】
【0026】
本明細書で開示される装置及び方法の構造、機能、製造、及び使用の原理が総括的に理解されるように、特定の例示的実施形態について、これから説明することにする。これらの実施形態の1つ以上の実施例を添付の図面に示す。本明細書で詳細に説明し、添付の図面に示す装置及び方法は、非限定的な例示的実施形態であること、並びに、本発明の範囲は、特許請求の範囲のみによって定義されることが、当業者には理解されよう。ある例示的実施形態に関連して例示又は説明される特徴は、他の実施形態の特徴と組み合わされてもよい。そのような修正及び変形は、本発明の範囲に含まれることを意図したものである。更に、いくつかの実施形態は、サンプルのヘマトクリットの値を決定する工程を論じ、他の実施形態は、サンプル中の分析物の濃度を決定する工程を論じるが、各種類の実施形態に付随する教示は、他の種類の実施形態に同様に適用可能であることは、当業者には理解されるであろう。即ち、ヘマトクリット値を決定する工程を対象とした実施形態は、サンプル中の分析物の濃度を決定するために使用することもでき、分析物の濃度を決定する工程を対象とした実施形態は、サンプルのヘマトクリット値を単に決定するために使用することができる。更に、実施形態は、両方、サンプルのヘマトクリット値を決定し、サンプル中の分析物の濃度を決定するために使用することができる。
【0027】
本明細書に開示する、サンプル中のヘマトクリットの値を決定し、サンプル中の分析物の濃度を決定するための方法は、任意のサンプル分析デバイス及び/又はシステムと共に使用することができる。デバイスは、毛管空隙を有することができる。該デバイスは、少なくとも1つの作用電極及び電位をそれらの間に印加することができる1つの対電極を含むことができる。サンプル分析デバイスは、一般的に、計器等の電極間に電位を印加するための構成要素に関連付けられることができる。サンプル分析デバイスは、サンプルがデバイスに導入されるときに、サンプルの初期充填速度を測定することが可能な、1つ以上の構成要素に関連付けられることもできる。かかる構成要素は、初期充填速度を考慮して、サンプル中の分析物の濃度を計算することも可能である。かかる構成要素は、概して、本明細書において制御ユニットとして言及される。更に、分析物、抗原、及び抗体という用語は、その中で同じ意味で使用され、したがって、1つの用語の使用は、当業者によって他に指示されないか、又は道理にかなって知られていない限り、3つのすべての用語に同様に適用可能である。
【0028】
全血サンプルのヘマトクリット値を決定するための方法の例示的な一実施形態において、全血のサンプルを、毛管空隙を有するサンプル分析デバイスに提供する。毛管の少なくとも一部分内のサンプルの初期充填速度を測定する。次いで、サンプルのヘマトクリット値を、初期充填速度から決定する。サンプル中の分析物又は抗原の濃度は、決定されたヘマトクリットの値を考慮して、決定することができる。初期充填速度を使用してヘマトクリット値を計算することにより、精度の改善を可能にすることができる。ヘマトクリット値を決定するための方法は、以下に詳細に論じるとおり、温度の効果も明らかにすることができる。更に、付随する分析物濃度を参照せずに、ヘマトクリットの値のみを測定することによって、決定値を、ほぼ瞬時に、しばしば、1秒未満で達成することができる。例えば、一滴の血液のヘマトクリットレベルは、血液をサンプル分析デバイスのセンサストリップ上に単に液滴することによって、1秒未満で決定することができる。血液がストリップ上に配設されると、ヘマトクリットレベルのデジタル読み出しを、ほぼ瞬時に提供することができる。その結果は、ヘマトクリットレベルの迅速かつ正確な決定値であり、これは、様々な医療評価において、例えば、貧血等の症状に関連する評価を行う上で有用である。
【0029】
サンプル中の分析物の濃度を決定するための方法の別の例示的実施形態において、サンプルを、作用電極及び対電極を有するサンプル分析デバイスに提供する。電位は、サンプル分析デバイスの作用電極と対電極との間に印加することができ、サンプル分析デバイスの毛管空隙内へのサンプルの初期充填速度を決定することができる。サンプル中の分析物の濃度は、決定された初期充填速度を考慮して、計算することができる。初期充填速度を考慮して濃度を計算することによって、各サンプルで異なるヘマトクリットレベルから生じ得る誤差等の誤差を明らかにすることができ、それによって、サンプル中の分析物の濃度のより正確な決定値をもたらす。該方法は、以下に詳細に論じるとおり、温度の影響を明らかにすることもできる。サンプル中の分析物の濃度を検出するための代替的実施形態において、誤差は、決定された初期充填速度ではなくむしろ、決定された充填時間に基づき訂正される。かかるデバイスの一例は、「Systems,Devices,and Methods for Improving Accuracy of Biosensors Using Fill Time」と題する、2009年12月30日に本出願と同時に出願されたRonald C.Chatelier及びAlastair M.Hodges(代理人整理番号104978−458)の同時係属特許出願に開示されており、これは、参照によって、その全体が本願に組み込まれる。代替的実施形態において、血漿相内の抗原の濃度及びヘマトクリットレベルの推定レベルを決定することができる。
【0030】
初期充填速度は、分析物の濃度を決定するための様々な方法に使用することができる。例えば、サンプルが全血を含み、サンプルがサンプル分析デバイス内で分析される位置の温度が既知である場合、初期充填速度は、決定されたヘマトクリットレベルに関連付けられることができる。例えば、サンプル分析デバイスのチャンバーが所望温度まで予熱される場合、サンプルの温度は既知であり得る。温度が不明な場合、計算は、依然として実施され、これは、温度を反応中に測定又は推測するのを可能にする。かかる例では、温度及びヘマトクリットレベルは、両方とも、より正確な分析物濃度決定値を提供するために明らかにすることができる。更に、初期充填速度は、同様に、血液サンプルのヘマトクリットレベルを決定するための様々な方法に使用することができる。
【0031】
サンプル分析デバイスに進入するサンプルに関連付けられる初期充填速度を決定するための様々な方法が存在する。初期充填速度を決定することは、ひいては、液体の粘度を予測することを可能にすることができる。液体の粘度を予測することは、より正確な濃度決定を行う上で役立つことができる。図1に示すとおり、例示的な一実施形態において、免疫センサ10は、一般的に免疫センサ10の進入ポート21付近から充填チャンバー22まで位置する光検出器52を有する制御ユニット50を含む。光検出器52は、任意の形状又は寸法を有することができ、また、例えば、免疫センサ10の上部の上又は免疫センサ10の進入ポート21のすぐ内側に位置することができる。図示の実施形態において、光センサは、進入ポート21に隣接する、免疫センサ10の上部プレート14に取り付けられる。光センサ52は、サンプルがセンサ52を通過するときに変化する光信号を含むことができる。したがって、サンプルが免疫センサ10に提供されると、光信号の変化率を検出することができ、それは、ひいては、初期充填速度を予測するために使用することができる。変化率は、免疫センサ10の毛管空隙の少なくとも一部分内で測定することができる。次いで、初期充填速度は、多くの異なるパラメータを計算するために使用することができる。非限定的な例として、初期充填速度は、サンプル中の抗原の濃度又は全血サンプルのヘマトクリットレベルを計算するために使用することができる。
【0032】
別の例示的実施形態において、電気化学検出システムは、初期電流量の規模を測定するために使用することができる。規模は、サンプルがサンプル分析デバイスの毛管空隙に進入するとすぐに測定することができる。毛管空隙は、例えば、充填チャンバー内への初期の進入前に、充填チャンバーと反応チャンバーとの間、及び/又は反応チャンバーと検出チャンバーとの間に位置することができる。例示的な一実施形態において、初期電流量は、充填チャンバーと反応チャンバーとの間で決定される。別の例示的実施形態において、初期電流量は、まず、サンプルが、検出チャンバー等の検出信号が生成されるサンプル分析デバイスの毛管空隙の領域内に横断するときに測定される。
【0033】
多くの異なる技術を、電流量を測定するために使用することができる。例えば、所望数の測定を、所望の期間にわたって行うことができる。例示的な一実施形態において、測定は、約1ミリ秒毎〜約25ミリ秒毎の範囲にほぼ少なくとも約10ミリ秒間〜約300ミリ秒間、行われる。別の実施形態において、測定は、ほぼ約10ミリ秒毎にほぼ少なくとも50ミリ秒間行われる。単一の測定を行うこともできるが、典型的に、初期速度のより正確な結果は、短期間にわたって複数の測定を行うことによって得ることができる。いくつかを以下に詳細に開示するが、サンプルの初期電流及び/又は初期速度を決定することができる様々な他の方法が存在することは、当業者には理解されるであろう。
【0034】
本明細書に開示する方法のうちの少なくともいくつか及び免疫センサ110と併せて使用するためのサンプル分析デバイスの別の例示的実施形態が図2に図示され、「Adhesive Compositions for Use in an Immunosensor」と題する、2009年9月30日に出願された、Chatelierらの米国特許出願第12/570,268号に記載されており、これは、参照によって、その全体が本願に組み込まれる。複数のチャンバーは、サンプルを免疫センサの中に導入することができる充填チャンバー、サンプルを1つ以上の所望の物質と反応させることができる反応チャンバー、及びサンプルの特定の構成成分の濃度を決定することができる検出チャンバーを含む、免疫センサ内に形成されることができる。これらのチャンバーは、免疫センサの下部電極、上部電極、及びセパレータのうちの少なくとも一部分内に形成されることができる。免疫センサは、必要に応じて、空気が免疫センサに進入及びそれから漏れることを可能にし、また第1及び第2の封止用構成要素が通気孔の第1及び第2の側面を選択的に封止することを可能にする、通気孔を含むこともできる。第1の封止用構成要素は、充填チャンバーの壁を形成することもできる。
【0035】
図示するとおり、免疫センサ110は、その上に縞模様に付けられた2つの液体試薬130、132を有する下部電極112を含む。下部電極112は、電極を形成するために使用される任意の数の技術を使用して形成されることができるが、一実施形態では、硫酸バリウムで充填されたポリエチレンテレフタレート(PET)のシートは、例えば、金等の好適な伝導体でスパッタコーティングされる。電極を形成する他の非限定的な例が、「Electrochemical Cell」と題され、2000年11月10日に出願された、Hodgesらの米国特許第6,521,110号において開示されており、その内容は、参照によって、その全体が本願に組み込まれる。
【0036】
同様に、液体試薬130、132は、多くの異なる組成物を有し得る。一実施形態において、第1の液体試薬130は、スクロース、並びにポロキサマー(例えば、Pluronics(登録商標)ブロックコポリマー等)、抗凝結剤(シトラコン酸塩)、及びカルシウムイオンを含有する緩衝液中の酵素と抱合した抗体(例えば、GDH−PQQ等)を含む。一実施形態において、第2の液体試薬132は、酸性緩衝液(希釈シトラコン酸溶液等)中のフェリシアン化物、グルコース、及び第2のメディエータ(フェナジンエトサルフェート等)の混合物を含む。第1及び第2の液体試薬130、132は、下部電極112の上で乾燥させることができる。試薬130、132を乾燥させるために多くの技法を使用することができるが、一実施形態において、下部電極112の上に試薬130、132が縞模様で付けられた後に、1つ以上の赤外線乾燥器を試薬130、132に適用することができる。また、例えば、1つ以上の空気乾燥器が赤外線乾燥器に続いて使用されることもできる。本明細書における、第1の試薬と第1の液体試薬、及び第2の試薬と第2の液体試薬についての言及は、同じ意味で用いられており、特定の実施形態に対して試薬が所与の時点で液体の又は乾燥した形態にあることを必ずしも示唆するものではない。更に、第1及び第2の液体試薬に付随する構成成分のいくつかは、交換可能に、かつ/又は、所望に応じて第1の液体試薬と第2の液体試薬の両方において使用されることができる。非限定的な例として、抗凝固剤は、第1の液体試薬130及び第2の液体試薬132のうちの一方又は両方に付随することができる。
【0037】
1本の線が、試薬130、132の一方の縁部がその線に近接するか又は接するように、試薬130と132との間のスパッタコーティングされた金として形成されることができる。図示の実施形態において、線は、試薬132の縁部が通気孔124における線に接するように、形成される。この線は、レーザーアブレーションを利用して、又は鋭利な金属の縁部を用いて施されることができる。一実施形態において、線は、試薬130、132が電極上に縞模様で付けられる前に施されることができる。この線は、下部電極112の検出チャンバーの下にある部分を、反応チャンバーの下に位置する部分から電気的に絶縁するように設計されることができる。これにより、電気化学的分析の間、作用電極の範囲がより良好に画定されることができる。
【0038】
また、免疫センサ110は、1つ以上の磁気ビーズ134を有する上部電極114を含むことができ、磁気ビーズ134は、表面結合型抗原をその上に含有している。これらの抗原は、以下で更に詳細に説明するように、下部電極112に配設された抗体及び反応チャンバー118内のサンプルと反応するように構成されることができる。下部電極112の上及び上部電極114の上に配設された構成要素が相互に交換可能であることが、当業者には理解されよう。したがって、下部電極112は1つ以上の磁気ビーズ134を有することができ、上部電極114は、上部電極132上に縞模様で付けられた2種類の液体試薬130、132を有することができる。更に、図示の実施形態において、電極112の長さは、免疫センサ110の全体の長さを形成しているが、他の実施形態において、電極は、免疫センサの層のうちの下部又は上部電極として働く一部分のみとされることができ、あるいは、複数の電極が、免疫センサの単一の層に配置されることができる。更に、免疫センサに印加される電位は、反転及び/又は交番することがあるため、下部及び上部電極の各々は、異なる段階において作用電極及び対電極又は対電極/基準電極として働くことができる。説明を容易にする目的で、本願において、下部電極は作用電極と見なし、上部電極は対電極又は対電極/基準電極と見なす。
【0039】
下部電極112と上部電極114との間に配置されるセパレータ116は、多様な形状及び寸法を有することができるが、一般的には、望ましくは下部及び上部電極112、114と係合して免疫センサ110を形成するように構成される。例示的な一実施形態において、セパレータ116は、両側で接着特性を含む。セパレータ116は、セパレータ116の2面の各々の側に剥離ライナーを更に有することができる。セパレータ116は、少なくとも2つの空洞を形成する方式で切断されることができる。第1の空洞は、反応チャンバー118として働くように形成されることができ、第2の空洞は、検出チャンバー120として働くように形成されることができる。一実施形態において、反応チャンバー118は、電極112、114と整列して反応チャンバー内での抗原抗体反応を可能にし、一方で検出チャンバー120は、電極112、114と整列して検出チャンバー内でのフェロシアン化物の電気化学的測定を可能にするように、セパレータ116がキスカット(kiss−cut)されることができる。
【0040】
一実施形態において、セパレータ116は、上部電極114の磁気ビーズ134及び下部電極112の第1の試薬130を少なくとも部分的に反応チャンバー118内に配設することが可能となり、かつ下部電極112の第2の試薬132のフェロシアン化物とグルコースとの組み合わせを少なくとも部分的に検出チャンバー120内に配設することが可能となるような方式で、下部電極112上に配置されることができる第1及び第2の液体試薬130、132の各々に抗凝固剤を含めて、抗凝固剤が反応チャンバー118及び検出チャンバー120の各々に付随するようにすると有利となり得る。いくつかの実施形態では、上部電極112及び下部電極114の一方とセパレータ116との組み合わせが、互いに積層されて二層積層体を形成することができ、一方で、他の実施形態では、下部電極112、上部電極114、及びセパレータ116の各々の組み合わせが、互いに積層されて三層積層体を形成することができる。あるいは、更なる層も追加し得る。
【0041】
充填チャンバー122は、下部電極112及び上部電極114の一方及びセパレータ116に孔を打抜きすることによって形成されることができる。図示の実施形態において、充填チャンバーは、下部電極112の孔が反応チャンバー118と重なり合うように、下部電極112及びセパレータ116に孔を打抜きすることによって形成されている。図示されるように、充填チャンバー122は、検出チャンバー120から一定の距離だけ離されることができる。そのような構成により、サンプルは、検出チャンバー120に進入することなしに、充填チャンバー122を通じて免疫センサ110に進入し、反応チャンバー118の中に流入して、例えば、第1の電極112上の、酵素と抱合した抗体を緩衝液中に含む第1の液体試薬130、及び上部電極114上に縞模様で付けられた磁気ビーズ134と反応することが可能となる。サンプルの充填チャンバー122への進入は、毛管現象として生じることができ、充填チャンバー122、反応チャンバー118、及びそれらの間の位置のうちの少なくとも1つを、毛管空隙と見なすことができる。サンプルが反応したら、そのサンプルは、次いで、第2の液体試薬132、例えば、フェリシアン化物、グルコース、及び酸性の緩衝液中の第2のメディエータの混合物と相互作用するために、検出チャンバー120の中に流入することができる。
【0042】
通気孔124が免疫センサ110の全体を通じて延びるように、通気孔124は、2つの電極112、114の各々及びセパレータ116を貫いて孔を打抜きすることによって形成されることができる。孔は、例えば、多数の異なる位置でドリル又は打抜き等の好適な方法で形成されることができるが、例示的な一実施形態では、それは、反応チャンバー118から離間される検出チャンバー120の領域と重なり合うことができる。
【0043】
通気孔124は、多数の異なる方法で封止することができる。図示の実施形態において、第1の封止用構成要素140は、下部電極112上に位置して、通気孔124の第1の側面を封止し、第2の封止用構成要素142は、上部電極114上に位置して、通機孔124の第2の側面を封止する。封止用構成要素は、任意の数の材料から作製することができ、及び/又は任意の数の材料を含むことができる。非限定的な例として、封止用構成要素のいずれか一方、又はそれらの両方は、親水性接着テープ又はスコッチ(Scotch)(登録商標)テープであってよい。封止用構成要素の接着側は、免疫センサ110に面することができる。図示されるように、第1の封止用構成要素140は、通気孔124に対する封止を形成できるだけでなく、サンプルが中に収容されることができるように、充填チャンバー122の壁を形成することもできる。第1の封止用構成要素140の接着側上に組み込まれた特性は、充填チャンバー122に関連付けられることができる。例えば、第1の封止用構成要素140が、それを親水性及び/又は水溶性にする特性を含む場合、充填チャンバーは、サンプルがその中に配設されるときに、よく濡れた状態のままであることができる。更に、封止用構成要素140、142は、免疫センサ110及びその中に配設された構成成分に対して所望に応じて通気及び/又は封止をなすように、免疫センサ110に選択的に関連し、かつ切り離すことができる。
【0044】
接着剤は、一般的に、免疫センサの構造に使用することができる。接着剤を本開示の免疫センサ及び他のサンプル分析デバイス内に組み込むことができる方法の非限定的な例は、「Adhesive Compositions for Use in an Immunosensor」と題し、2009年9月30日に出願された、Chatelierらの米国特許出願第12/570,268号で確認することができ、この内容は、既に、参照によって、その全体が本願に組み込まれている。
【0045】
本開示は、免疫センサに関連する様々な異なる実施形態を論じるが、免疫センサの他の実施形態も、本開示の方法と共に使用することができる。そのような実施形態の非限定的な例には、「Direct Immunosensor Assay」と題され2002年3月21日に出願されたHodgesらの米国特許出願公開第2003/0180814号、「Immunosensor」と題され2004年4月22日に出願されたHodgesらの米国特許出願公開第2004/0203137号、「Biosensor Apparatus and Methods of Use」と題され2005年11月21日に出願されたRylattらの米国特許出願公開第2006/0134713号、並びに米国特許出願公開第2003/0180814号及び同第2004/0203137号の各々に対する優先権を主張する米国特許出願第12/563,091号に記載されたものが挙げられ、これらのそれぞれは、参照によって、その全体が本願に組み込まれる。
【0046】
一実施形態において、免疫センサ110は、電極112、114に電位を印加し、その電位を印加した結果として生じる電流を測定するように構成された計器の中に配設されるように構成されることができる。一実施形態において、免疫センサは、計器と係合するための1つ以上のタブ117を含む。他の特性も、免疫センサ110を計器に係合するために使用することができる。その計器は、多くの種々の特徴を有することができる。例えば、計器は、免疫センサ110の特定の構成成分をあるチャンバー内に維持し、その一方で他の構成成分が他のチャンバーに流れるように構成された、磁石を含むことができる。例示的な一実施形態において、計器の磁石は、免疫センサ110を計器内に配設すると磁石が反応チャンバー118の下方に配置されるように位置する。これにより、磁石は、任意の磁気ビーズ134、より具体的には、ビーズ134に拘束されている任意の抗体酵素複合体が、検出チャンバー120の中に流入するのを防ぐのを助けることができる。
【0047】
計器の別の特徴には、加熱要素が挙げられる。加熱要素は、反応速度を速めるのを助け、また、粘度を減じることによってサンプルが所望の方式で免疫センサ110を通じて流動するのを助けることができる。加熱要素は、1つ以上のチャンバー及び/又はその中に配置されたサンプルが所定温度まで加熱されるのを可能にすることもできる。所定温度まで加熱することで、例えば、反応が生じる際の温度変化の影響を減少又は除去することによって、精度を提供するのを助けることができる。
【0048】
更に、穿孔装置は、計器に関連付けられることもできる。穿孔装置は、空気が通気孔から流出し、液体が反応チャンバーから検出チャンバーに流動することができるように、所望時間に第1及び第2の封止用構成要素のうちの少なくとも1つを穿孔するように構成することができる。
【0049】
免疫センサ110は、制御ユニットに関連付けられるように構成することもできる。制御ユニットは、様々な機能を実行するように構成することができる。例示的な一実施形態において、制御ユニットは、サンプルがデバイスに導入されたときに、サンプルの初期充填速度を測定することが可能である。別の実施形態において、制御ユニットは、血液サンプルのヘマトクリット値を決定するように構成される。更に別の実施形態において、制御ユニットは、初期充填速度を考慮して、サンプル中の分析物の濃度を計算するように構成される。実際、制御ユニットは、少なくとも部分的に、望ましいとされる機能性、及びシステムが初期充填速度を測定するように設計される方法に応じて、多数の異なる特徴を含むことができる。
【0050】
非限定的な例として、システムが初期充填速度を光学的に測定するように設計される場合、制御ユニットは、光信号検出器を含むことができる。光信号検出器は、検出器によって感知された光信号における変化率に基づき初期充填速度を測定することができる。あるいは、システムが電流量に基づき所期充填速度を測定するように設計される場合、制御ユニットは、電流量検出器を含むことができる。電流量検出器は、サンプルが免疫センサに進入する結果として生じる電流の変化に基づき初期充填速度を測定することができる。この変化のタイミングは、多くの異なる方法で生じ得るが、例示的な一実施形態では、電流は、サンプルが、検出信号が生成される免疫センサの毛管空隙の領域内に横断した後、例えば、サンプルが反応チャンバーから検出チャンバーに横断するときに測定される。別の実施形態では、電流は、サンプルが免疫センサの毛管空隙に進入した直後、例えば、サンプルが反応チャンバーに進入したときに測定される。
【0051】
制御ユニットは、システムの他の特徴を測定することもできる。非限定的な例として、制御ユニットは、免疫センサの1つ以上のチャンバーの温度を測定するように構成されることができる。また、例えば、直接、又は周辺温度を測定し、それを使用してサンプルの温度、サンプルの色、又はサンプル及び/又はシステムの様々な他の特徴及び/又は特性を推測することによって、サンプルの温度を測定するように構成されることもできる。更なる非限定的な例として、制御ユニットは、初期充填速度決定の結果、ヘマトクリット値決定の結果、及び/又は分析物濃度決定の結果を外部装置に伝達するように構成されることができる。これは、任意の数の方法で実現することができる。一実施形態において、制御ユニットは、マイクロプロセッサ及び/又はディスプレイデバイスに配線することができる。別の実施形態において、制御ユニットは、制御ユニットからのデータをマイクロプロセッサ及び/又はディスプレイデバイスに無線で送信するように構成されることができる。
【0052】
システムの他の構成要素も、そのような測定を行うように構成されることができる。例えば、免疫センサ又は計器は、免疫センサの1つ以上のチャンバーの温度を測定するか、サンプルの温度を測定若しくは推測するか、又はサンプル及び/若しくはシステムの様々な他の特徴及び/若しくは特性を測定、決定、若しくは推測するように構成されることができる。更に、制御ユニットのこれらの特徴が、単一の制御ユニット内で交換及び選択的に組み合わせることができることは、当業者には理解されよう。例えば、制御ユニットは、初期充填速度を決定し、かつチャンバーの温度を測定することができる。他の実施形態において、複数の制御ユニットは、様々な制御ユニットの構成及び実行される所望機能に少なくとも部分的に基づき、様々な機能を実行するために共に使用することができる。
【0053】
他の種類のサンプル分析デバイスを、本明細書に開示するシステム及び方法のうちの少なくともいくつかと併せて使用することができる。これらのデバイスには、非限定的な例として、電気化学セル、電気化学センサ、グルコースセンサ、グルコース計器、ヘモグロビンセンサ、酸化防止剤センサ、及びバイオセンサが挙げられる。一実施形態において、サンプル分析デバイスは、グルコースセンサを含む。グルコースセンサは、図3及び4に図示するセル等の電気化学セルを含むことができる。セルは、上部表面及び下部表面202、203を有する薄いストリップ膜201を含むことができ、また下部表面203上に配設された作用電極206と上部表面202上に配設された対/基準電極205との間に画定されたセル領域204を含むこともできる。膜の厚さは、反応生成物が対電極から作用電極に到達する等の所望の結果を達成するように選択することができる。例えば、膜の厚さは、電極が距離tによって分離されるように選択することができ、その距離は、対電極における電気化学反応の生成物が、試験期間中に作用電極に移動することができ、定常状態の拡散プロファイルを実質的に達成することができるように、十分に近接してもよい。典型的に、tは、約500マイクロメートル未満、あるいは、約10マイクロメートル〜約400マイクロメートルの範囲、より具体的には、約80マイクロメートル〜約200マイクロメートルの範囲であってよい。一実施形態において、電極間の間隔は、対電極からの反応生成物が作用電極に到達するように選択することができる。
【0054】
電極は、様々な構成を有することもできる。例えば、電極は、平面的であってもよい。更に、図示の実施形態では、電極205、206は互いに面し、実質的に対向する一方、他の実施形態では、電極は、互いに単に面することができ、それらは、実質的に互いに対向するか、又はそれらは、電極がほぼ同じ平面上に位置付けられる隣接構造を有することができる。異なる電極構成の例は、「Electrochemical Cell」と題し2003年10月14日に出願された、Hodgesの米国特許第7,431,820号において少なくとも確認することができ、その内容は、参照によって、その全体が本願に組み込まれる。
【0055】
サンプル付着又は「標的」領域207は、膜201の上部表面202上に画定することができ、セル領域204から膜の厚さを超える距離で離間することができる。膜201は、標的領域207とセル領域204との間に延在することができる拡散領域208を有することができる。好適な試薬は、酸化還元メディエータM、酵素E、及びpH緩衝液Bを含むことができ、これらの各々は、膜のセル領域204内、及び/又はセル領域204と標的領域207との間に含まれることができる。試薬は、安定剤等を含むこともできる。
【0056】
センサの使用中、一滴の血液を標的領域207上に設置することができ、血液の構成要素を、セル領域204に向かって吸上げることができる。血液が標的領域207を覆う初期速度は、少なくともヘマトクリットに依存し得る。
【0057】
電極205、206の各々は、所定領域を有することができる。図3及び4の実施形態において、セル領域204は、膜の縁部209、210、211によって画定することができ、それは、電極の縁部212、213を(標的領域207に対して)誘導することによって、電極205、206の縁部に対応させることができる。本例において、電極は、約60nm(600オングストローム)の厚さであってよく、また約1mm〜5mmの幅であってよいが、様々な他の寸法及びパラメータを、本発明の範囲から逸脱することなく使用することができる。
【0058】
あるいは、膜の両側を、標的領域207を除いて、サンプルからの水の蒸発を防止しかつ装置に機械的ロバスト性を提供する機能を果たすことができる層を積層することによって、被覆することができる。水の蒸発は、それがサンプルを濃縮し、電極が乾燥するのを可能にし、溶液が冷却するのを可能にするため、望ましくないと考えられており、それによって、拡散係数に影響を及ぼし、酵素動態を遅くするが、拡散係数は、上記のとおり推測することができる。
【0059】
図5に図示する代替的実施形態において、本明細書に開示するシステム及び方法と共に使用するための中空の電気化学セルを提供する。電極305、306は、離間されたポリマー壁330によって担持されることができ、それによって中空セルを画定する。開口部331を、セルの1つの側面上に提供することができ、それによって、サンプルを空洞332内に受け入れることができる。本実施形態では膜を使用しないが、いくつかの実施形態では膜を含むことができる。電極は、少なくとも上述のとおり、様々な構成を有することができる。非限定的な例として、電極は、約500マイクロメートル未満、好ましくは、約10マイクロメートル又は約20マイクロメートル〜約400マイクロメートルの範囲、より好ましくは、約100マイクロメートル〜約200マイクロメートルの範囲で離間することができる。有効なセル量は、約1.5マイクロリットル以下であり得る。
【0060】
図3〜5の電気化学セルは、計器、制御ユニット、並びに本明細書に開示するデバイス、システム、及び方法の他の構成要素及び工程と併せて使用することができる。図3〜5の電気化学セルに関連する更なる開示は、「Electrochemical cell」と題し1998年4月17日に出願された、Hodgesらの米国特許第6,284,125号で確認することができ、この内容は、参照によって、その全体が本願に組み込まれる。例えば、本開示と併せて使用される電気化学セルは、2つの電極対を有することができる。電極対は、作用電極、対電極、対/基準電極、及び別個の基準電極のうちの任意の組み合わせを含むことができる。
【実施例】
【0061】
(実施例1)
測定する電流量に基づき初期充填速度を測定するための電気化学システムの使用を、以下の実施例によって示す。以下の実施例において、システムは、サンプル分析デバイス、特に、図2の免疫センサ110、電位を印加するように構成された計器、及び初期充填速度を決定するように構成された制御ユニットを含んだ。特に、電位を、免疫センサ110の電極に印加し、ヘマトクリットのレベルを決定し、次いで、電位を逆転させた。分析物の濃度を、決定されたヘマトクリットのレベルを考慮して、その後決定した。ヘマトクリットのレベルを、計算された初期充填速度を考慮して、決定した。
【0062】
複数のサンプルを、本明細書に開示するシステム、デバイス、及び方法の性能を試験するための分析に提供した。サンプルは、C反応性タンパク質を含有する血液サンプルであり、したがって、決定される分析物の濃度は、C反応性タンパク質の濃度であった。試験結果の比較として既知の、4つの異なるレベルのヘマトクリットを含有したサンプルを、実際の結果と比較して、システム、デバイス、及び方法の精度を決定することができるであろう。ヘマトクリットの4つのレベルは、約33%、約41.5%、約47.5%、及び約55%であった。4つのレベルのヘマトクリットを試験することは、開示したシステム、デバイス及び方法の精度が広範囲におよぶ濃度レベルにわたり確認されるのを可能にした。
【0063】
この第1の実施例において、免疫センサを、サンプルが導入される前に、約37℃まで予熱した。免疫センサに関連付けられる計器を、予熱を実行するように構成したが、他の代替物を使用することもできた。次いでサンプルを免疫センサ内に導入した。サンプルの免疫センサ内への導入は様々な方法で達成することができるが、該実施例では、充填チャンバーへの毛管現象により、各サンプルを個別に受け入れた。
【0064】
約2分間が経過した後、第1の封止用構成要素を穿孔することによって、免疫センサの通気孔にアクセスした。計器の穿孔装置を使用して穿孔動作を実行し、それが次には、血液が免疫センサの反応チャンバーから免疫センサの検出チャンバー内に流動するのを可能にした。血液が検出チャンバーに進入し始めるとすぐに、計器により約4秒間、約300mVの電位を電極に印加した。あるいは、電位を、血液が検出チャンバーに到達する前、又は到達している間に印加することもできた。その後、電位を、約10秒間、中断し逆転させた。本実施例から得られた電流対時間遷移のプロットを図6に図示する。本実施例において、約10ミリ秒毎に測定され、次いで、最初の50ミリ秒間において平均化された各サンプルの初期電流は、特定のサンプルのヘマトクリットレベルに関連する。ヘマトクリットのレベルを、第1の電位の印加中に初期電流から決定する一方、C反応性タンパク質のレベルを、電位の逆転後、電流対時間プロットの勾配及び決定されたヘマトクリットのレベルに基づき計算する。
【0065】
上述のとおり、いくつかの実施形態において、ヘマトクリットのレベルのみを測定することが望ましい場合がある。したがって、初期電流に基づく第1の計算は、その計算を行うのに必要とされる唯一の工程であり得る。本実施例において、この決定を、4秒間の電位印加の結果として行う一方、ヘマトクリットレベルの実際の決定は、初期電流を計算できるのと同じほど迅速に決定することができる。したがって、非限定的な例として、初期電流が、最初の約50ミリ秒間の平均に基づき計算される場合、ヘマトクリットのレベルは、最初の約50ミリ秒後に決定することができる。したがって、血液サンプルのヘマトクリットレベルの測定は、1秒未満で実施することができる。
【0066】
決定された各サンプルのヘマトクリットレベルを、図7に図示する。図7は、各サンプルのヘマトクリットの濃度レベル対決定された初期電流のプロットを図示する。プロットは、4つの異なるレベルのヘマトクリットを含有するサンプルが試験されたことを明確に示し、それは、既知の濃度レベルと相関する。更に、図示するとおり、より高いレベルのヘマトクリットは、一般的に、測定された初期電流のより低い絶対値をもたらした。例えば、約33%であったヘマトクリットの濃度を有するサンプルは、ほぼ、約38マイクロアンペア〜約33マイクロアンペアの範囲であった初期電流絶対値を有した一方、約47.5%であったヘマトクリットの濃度を有するサンプルは、ほぼ、約31マイクロアンペア〜約26マイクロアンペアの範囲であった初期電流絶対値を有した。すべての結果の最適合線を決定し、それも図7に図示する。最適合線と相関する等式は、
【数9】

であり、ここでHは、ヘマトクリットのレベルであり、
【数10】

は、初期電流である。ヘマトクリットレベル対初期電流の結果を表す等式と実際の結果との間の誤差を、図8に図示する。より具体的には、図8は、各試験サンプル対実際の測定されたヘマトクリットレベルに存在した誤差割合をプロットする。2つを除いたすべての実際の結果は、計算された範囲の約±5%内であり、かなりの量は約±2.5%の範囲であった。
【0067】
ヘマトクリットレベルが決定したら、その結果を図6の電流対約9秒〜約14秒の時間遷移の勾配と共に使用して、サンプル中のC反応性タンパク質の値を計算した。C反応性タンパク質のレベルを以下の等式で決定した:
【数11】

式中、COは、C反応性タンパク質の濃度であり、yは、前述の勾配及びヘマトクリットのレベルに基づく。より具体的には、yは、勾配へのヘマトクリットの影響を除去し、以下の等式によって計算した:
【数12】

式中、mは、電流対約9秒〜約14秒の時間遷移の勾配であり、Hは、決定されたヘマトクリットレベルである。図9は、血液サンプル各々の計算されたC反応性タンパク質のレベル対従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値のプロットを図示する。図9の最適合線は、決定されたC反応性タンパク質のレベルと、同等の参照値との間の正確な相関関係を図示する。
【0068】
(実施例2)
測定する電流量に基づき初期充填速度を測定するための電気化学システムの使用を、別の実施例によって更に示した。本実施例に使用したサンプル分析デバイスもまた、図2の免疫センサ110、電位を印加するように構成された計器、及び初期充填速度を決定するように構成された制御ユニットであった。特に、電位を、免疫センサ110の電極に印加し、ヘマトクリットのレベルを決定し、次いで、電位を逆転させた。分析物の濃度を、決定されたヘマトクリットのレベルを考慮して、その後決定した。前述の実施例と同様に、異なるヘマトクリットレベルを有する多くのサンプルを、システムの能力を実証するために、システムと共に使用した。ヘマトクリット濃度の既知のレベルは、約33.5%、約41%、約47.5%、及び約56.5%であった。
【0069】
サンプルを、毛管現象により、未加熱の免疫センサに導入した。サンプルは、充填チャンバーに進入し、反応チャンバーに移動し、そこで約5分間、滞留した。第1の封止用構成要素を穿孔することによって、免疫センサの通気孔を、その後開口し、それによって、免疫センサ内に配設されたサンプルの血液が免疫センサの反応チャンバーから免疫センサの検出チャンバーへの流動するのを可能にした。封止用構成要素のうちの少なくとも1つを穿孔する前に、サンプルをより長い時間待機させることによって、特に未加熱の反応チャンバーを考慮して、免疫センサの抗原及び抗体酵素複合体が拡散し反応するのに十分な時間を提供した。上記の実施例1に示すとおり、免疫センサを予熱することで、この時間を速めることができる。しかしながら、本実施例において、加熱要素は含まれず、それは、システムに加熱要素を組み込むことに付随した複雑な問題及び費用を除去する利点をもたらした。しかしながら、チャンバーの温度が不明又は一定ではないそのような例では、ヘマトクリットのレベル及び/又はC反応性タンパク質のレベルを決定するために実行する計算は、より正確な結果を提供するために、異なる周辺温度の影響を明らかにしなければならない。そのような計算法を、この第2の実施例に提供した。一実施形態では、サンプルの温度を推測することができる。
【0070】
以前の実施例と同様に、血液が検出チャンバーに進入し始めると、約300mVの電位を、計器により約4秒間、電極に印加した。その後、電位を約10秒間、中断し逆転させた。得られた電流対時間遷移のプロットを、図6に図示したプロットと同様の方法で作製した。得られたプロットから、ヘマトクリットのレベルを電位の第1の印加中の初期電流から決定した。その後、C反応性タンパク質のレベルを、電位の逆転後に計算した。計算されたC反応性タンパク質のレベルは、電流対時間プロットの勾配、及び決定されたヘマトクリットのレベルに基づいた。本実施例の温度を明らかにすることによって、以下に示すとおり、更なる精度を提供した。
【0071】
各サンプル用に決定された初期電流を、図10に図示する。図10は、サンプルが配設された免疫センサの検出チャンバーの決定された初期電流対温度のプロットを図示する。4つの種類のサンプル(即ち、4つの異なるレベルのヘマトクリット)の初期電流を、約20℃〜約37℃の範囲にわたり、測定した。一般的に、ヘマトクリットのより高いレベルは、初期電流のより低い絶対値をもたらした。チャンバー内の温度が上昇すると、初期電流の絶対値も通常上昇した。示すとおり、初期電流は、ヘマトクリットが固定されたときに、温度と線形的に異なった。チャンバーの温度及び初期電流を考慮して、ヘマトクリットのレベルを以下の等式によって決定した:
【数13】

式中、Hは、ヘマトクリットのレベルであり、
【数14】

は、初期電流であり、Tは、検出チャンバーの温度である。以前の実施例と同様に、図11に示すとおり、ヘマトクリットの予測レベルにおける誤差は、約±5%以内であった。図11は、各試験サンプル対そのサンプルの参照ヘマトクリットレベルに存在した誤差割合をプロットする。やはり以前の実施例と同様に、いくつかの実施形態において、ヘマトクリット値の決定のみが行われ、それによって、ヘマトクリット値の決定値に基づき評価することができる、様々な医学的状態の迅速な評価が可能になる。
【0072】
ヘマトクリットレベルが決定したら、その結果を電流対約9秒〜約14秒の時間遷移の勾配及び検出チャンバーの温度と共に使用して、サンプル中のC反応性タンパク質の値を計算した。C反応性タンパク質のレベルを以下の等式によって決定した:
【数15】

式中、COは、C反応性タンパク質の濃度であり、y’は、検出チャンバーの温度及び変数に基づき、それがひいては前述の勾配及びヘマトクリットのレベルに基づく。より具体的には、y’は、勾配への温度の影響を除去し、以下の等式によって計算した:
【数16】

式中、Tは、免疫センサの検出チャンバーの温度であり、yは、勾配へのヘマトクリットの影響を除去する条件である。y’に対する等式は、勾配が、約1℃毎の温度の変化に対して、一定の割合、典型的に約4〜約7パーセントの範囲で変化すると仮定する。更に、条件T−25は、y’のすべての値を25℃の標準温度に修正する。異なる温度を修正しなければならない場合、この条件は、適宜に調整することができる。実際に、他のサンプル、温度等のために、この等式及びこの開示全体に開示される他の等式をうまく利用するための多くの方法が、当業者には理解されるであろう。
【0073】
変数yを以下の等式によって計算した:
【数17】

式中、mは、電流対約9秒〜約14秒の時間遷移の勾配であり、Hは、決定されたヘマトクリットレベルである。条件(1−0.01H)は、次いで任意電力まで上昇される、血漿である容量の一部を表す。電力を較正係数として得ることができる。
【0074】
ほぼ、約9秒〜約14秒の遷移の勾配は、C反応性タンパク質、ヘマトクリットレベル、及び温度の関数である。C反応性タンパク質の濃度が約0.15mg/Lに固定されたときに、図12に示すとおり、ヘマトクリット及び温度に対する勾配のかなりの変動が依然として存在した。図12は、サンプルが配設された免疫センサの検出チャンバーの決定された勾配対温度のプロットを図示する。4つのヘマトクリットレベルのサンプルの各々の初期電流を、約20℃〜約37℃の範囲にわたり、測定した。一般的に、サンプル中のヘマトクリットのレベルが大きいほど、勾配の値は小さくなる。チャンバー内の温度が上昇すると、勾配の値は、通常上昇した。
【0075】
図13は、約33.5%又は約47.5%のいずれかのヘマトクリットレベルを有するサンプル各々の計算されたC反応性タンパク質レベル対従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値のプロットを図示する。図13の最適合線は、決定されたC反応性タンパク質のレベルと、同等の参照値との間の正確な相関関係を図示する。
【0076】
これらの2つの実施例は、本明細書に含まれる教示をどのように実行し、かつ使用することができるかという、多くの実施例のうちの2つにすぎないことは、当業者には理解されよう。更に、本明細書に開示する方法、システム、及びデバイスは、血液サンプルの分析物の濃度を決定する工程と併せて主に使用され、血液サンプル中の異なるレベルのヘマトクリットから生じる場合がある誤差を明らかにする工程に主に焦点を置くが、本明細書に含まれる開示は、分析物を含有する様々な他のサンプルのために使用することもでき、サンプル内に含有される様々な抗原及び/又は抗体に対して試験することができることは、当業者には理解されよう。
【0077】
様々な方法、システム、デバイスが特定の等式に頼るという点では、提供される等式は、一般的に、等式が適用された実施例に基づくことも、当業者には理解されよう。本開示を考慮して、本発明の範囲から逸脱することなく、他の状況に対して、開示した等式を調整することは、当業者には可能であろう。
【0078】
更に、濃度を決定する工程並びにシステム及びデバイスを使用する工程に関する方法等の本明細書に論じる方法は、指示される場所を除き、特定の工程又は工程の順序によっても制限されない。当業者には、それらの方法を実施することができる様々な順序が理解され、また、それらの工程が本発明の範囲から逸脱することなく修正又は追加されることができることは、理解されよう。
【0079】
本明細書に開示する方法を使用することができる、他の種類のデバイスのいくつかの非限定的な例が、「Electrochemical Method」と題され1997年5月7日に出願されたHodgesらの米国特許第5,942,102号、「Electrochemical Cell」と題され1999年5月18日に出願されたHodgesらの米国特許第6,174,420号、「Sensor Connection Means」と題され1999年9月20日に出願されたChambersらの米国特許第6,379,513号、「Heated Electrochemical Cell」と題され2000年9月11日に出願されたHodgesらの米国特許第6,475,360号、「Hemoglobin Sensor」と題され2000年7月14日に出願されたHodgesらの米国特許第6,632,349号、「Antioxidant Sensor」と題され2000年7月14日に出願されたHodgesらの米国特許第6,638,415号、「Method of Forming an Electrical Connection Between an Electrochemical Cell and a Meter」と題され2002年12月9日に出願されたHodgesらの米国特許第6,946,067号、「Method of Preventing Short Sampling of a Capillary or Wicking Fill Device」と題され2003年4月3日に出願されたHodgesらの米国特許第7,043,821号、及び「Electrochemical Cell」と題され2002年10月1日に出願されたHodgesらの米国特許第7,431,820号において、より詳細に論じられており、これらの各々は、参照によって、その全体が本願に組み込まれる。
【0080】
更に、特定の構成を有するデバイスと共に使用するための本明細書における開示について論じる限りにおいて、任意の数の構成が使用されることができる。例えば、本開示と共に使用され得るいくつかの構成は、互いに面する2つの電極を有するセンサ、同じ平面上に2つの電極を有するセンサ、及び3つの電極を有し、それらの電極のうちの2つが対向し、それらの電極のうちの2つが同じ平面上にあるセンサを含む。これらの異なる構成は、免疫センサを含む任意のデバイス及び他の前述のデバイス内で生じることができる。
【0081】
デバイス、システム、及び方法の様々な態様は、本発明の範囲から逸脱することなく、様々な決定値に関して、必要に応じて、適合させる及び変更することができる。更に、上述の実施形態に基づいた本発明の更なる特徴及び利点が、当業者には理解されよう。したがって、本発明は、添付の請求項に示された内容を除き、本明細書に特に示され記述されたものに限定されることはない。本明細書に記載の全ての参考文献は、その全体が参照により本明細書に明示的に組み込まれる。
【技術分野】
【0001】
本発明は、サンプル中の分析物の濃度を決定する工程に関し、より具体的には、サンプルの初期充填速度に基づいて濃度をより正確に決定する工程に関する。
【背景技術】
【0002】
生理学的流体、例えば、血液又は血液由来の生成物中の分析物検出は、今日の社会では、今まで以上に重要性を増している。分析物検出の分析は、臨床検査、家庭検査などを含めて、多様な用途に利用法が見出され、そのような検査の結果は、様々な病状の診断及び処置において主要な役割を果たしている。目的の分析物には、糖尿病管理のためのグルコース、コレステロールなどが挙げられる。こうした分析物検出の重要性の高まりに応じて、臨床での使用及び家庭での使用の両方に対応する多様な分析物検出の手順及びデバイスが開発されてきた。これらのデバイスのいくつかには、電気化学セル、電気化学センサ、ヘモグロビンセンサ、酸化防止剤センサ、バイオセンサ、及び免疫センサが挙げられる。
【0003】
分析物検出に影響を及ぼし得る血液の1つの特性は、ヘマトクリットである。ヘマトクリットのレベルは、様々な人により、非常に異なり得る。非限定的な例として、貧血を罹患する人は、約20%のヘマトクリットレベルを有し得る一方、新生児は、約65%のヘマトクリットレベルを有し得る。一定期間にわたって、同一の個人から摂取されたサンプルでさえ、異なるヘマトクリットレベルを有する場合がある。更に、高いヘマトクリットは、血液の粘度を増加させることもでき、その粘度が次には、分析物検出に付随する他のパラメータに影響を及ぼす場合があるため、ヘマトクリットのサンプルへの影響を明らかにすることが、正確な分析物濃度決定を行う上で重要になる場合がある。
【0004】
血液サンプル中のヘマトクリットの異なるレベルを明らかにしてきた1つの方法は、血液から血漿を分離し、次いで、調節された血漿量に対して抗原の濃度を再計算することによるものである。分離は、例えば、遠心分離工程を実施することによって達成されてきた。血液サンプル中のヘマトクリットの異なるレベルを明らかにしてきた他の方法には、計算に平均メハトクリットを使用する工程、又は別個の工程においてヘマトクリットを測定し、次いで、血漿値に対する抗原の濃度を計算する工程が挙げられる。しかしながら、これらの方法は、少なくとも、それらが不必要なサンプルの取り扱いを伴い、更なる時間を要し、最終決定において実質的な誤差を引き起こすため、望ましくないと考えられている。更に、サンプルが分析される環境の温度は、分析物濃度決定の精度に負の影響を及ぼし得る。
【発明の概要】
【発明が解決しようとする課題】
【0005】
したがって、広範なヘマトクリットレベル及び温度を明らかにする、より正確な分析物濃度測定を得る方法を開発することが望ましいであろう。ヘマトクリットレベルを迅速に決定する方法を開発することも望ましいであろう。
【課題を解決するための手段】
【0006】
出願者は、前述の付随問題がほとんどないか、又はそれが全くない、広範なヘマトクリットレベル及び温度を明らかにする、より正確な分析物濃度測定を得る方法を開発することが望ましいであろうことを理解している。出願者は、ヘマトクリットレベルを迅速に決定する方法を開発することも望ましいであろうことも理解している。したがって、システム、デバイス、及び方法は、概して、血液サンプルのヘマトクリット値を決定し、かつサンプル中の分析物の濃度を決定するために提供される。全血サンプルのヘマトクリット値を決定するための方法の例示的な一実施例において、該方法は、全血のサンプルを、毛管空隙を有するサンプル分析デバイスに提供する工程と、毛管空隙の少なくとも一部分内のサンプルの初期充填速度を測定する工程と、初期充填速度からサンプルのヘマトクリット値を決定する工程と、を含む。初期充填速度を測定する工程は、電位を印加する工程と、電流を測定する工程と、初期電流量を決定する工程と、を含むことができる。一実施形態において、電流測定は、約10ミリ秒毎に少なくとも約50ミリ秒間実施され、平均電流は、電流測定値に基づき計算される。別の代替的実施形態において、初期充填速度を測定する工程は、光信号を検出する工程を含むことができる。一実施形態において、初期充填速度を測定する工程は、サンプルが毛管空隙に進入した直後に生じる。更に別の実施形態において、初期充填速度を測定する工程は、サンプルが、検出信号が生成されるサンプル分析デバイスの毛管空隙の領域内に横断した後に生じる。サンプルの温度は、測定するか、又は推測することができる。測定又は推測された温度は、サンプルのヘマトクリット値を決定するために使用することができる。例示的な一実施形態において、サンプル分析デバイスは、免疫センサを含む。
【0007】
ヘマトクリットレベルを測定する工程の他に、該方法は、サンプル中の分析物の濃度を決定するために使用することもできる。例えば、ヘマトクリット値を決定するための方法は、決定されたヘマトクリット値を考慮して、分析物の濃度を計算する工程を含むことができる。これは、例えば、電位を印加し、電位を印加した後の初期電流を測定し、電位を逆転させることによって達成することができる。一定期間にわたる電流の変化は、電位の逆転後、測定することができる。一定期間にわたる、測定された電流の変化は、分析物の濃度を計算するためにも使用することができる。一実施形態では、サンプルの温度は、測定するか、又は推測することができる。かかる実施形態において、一定期間にわたる、測定された電流の変化、及びサンプルの温度は、分析物の濃度を計算するために使用することができる。
【0008】
サンプル中の分析物の濃度を決定するための方法の例示的な一実施形態において、該方法は、分析物を含有するサンプルを、作用電極及び対電極を有するサンプル分析デバイスに提供する工程と、作用電極と対電極との間に電位を印加する工程と、サンプルの初期充填速度を決定する工程と、初期充填速度を考慮して、分析物の濃度を計算する工程と、を含む。一実施形態において、初期充填速度は、光信号における変化率を決定することによって決定することができる。別の実施形態において、初期充填速度は、初期電流量を決定することによって決定することができる。初期電流量は、例えば、約10ミリ秒毎に少なくとも約50ミリ秒間電流測定を実施し、次いで、電流測定値に基づき平均電流を計算することによって決定することができる。更に別の実施形態において、初期充填速度は、電位を印加した後の初期電流を測定し、サンプル中のヘマトクリットのレベルを決定し、作用電極と対電極との間で電位を逆転させることによって決定することができる。更に、分析物の濃度は、決定されたヘマトクリットのレベルに基づき、算定することができる。
【0009】
分析物の濃度を決定するための方法は、電位の逆転後、一定期間にわたって、電流の変化、即ち、電流対時間のグラフの勾配mを測定する工程を更に含むことができる。その結果、分析物の濃度、COは、一定期間にわたる、電流の変化を考慮して、計算することができる。例えば、分析物の濃度は、以下の等式を使用して、計算することができる:
【数1】

式中、
【数2】

であり、Hは、ヘマトクリットのレベルである。ヘマトクリットのレベルHは、以下の等式を使用して決定することができる:
【数3】

式中、
【数4】

は、初期電流の絶対値である。
【0010】
サンプル分析デバイスは、免疫センサであってもよい。濃度が分析される分析物は、C反応性タンパク質であってもよい。分析物は、血液であってもよい。一実施形態において、血液は、全血を含む。該方法は、全血の温度Tを測定する工程か、あるいは、周辺温度を測定し、それを使用して血液の温度Tを推測する工程を更に含むことができる。該方法は、電位の逆転後、一定期間にわたって、電流の変化、即ち、電流対時間のグラフの勾配mを測定する工程も更に含むことができる。その結果、分析物の濃度、COは、一定期間にわたる、電流の変化を考慮して、計算することができる。例えば、分析物の濃度は、以下の等式を使用して、計算することができる:
【数5】

式中、
【数6】

であり、Hは、ヘマトクリットのレベルである。ヘマトクリットのレベルHは、以下の等式によって決定することができる:
【数7】

式中、
【数8】

は、初期電流の絶対値である。
【0011】
電気化学システムの例示的な一実施形態において、システムは、下部電極及び上部電極を有する免疫センサと、免疫センサの下部電極と上部電極との間に電位を印加するように構成された計器と、免疫センサ内に導入されたサンプルの開始充填速度を測定するように構成された制御ユニットと、を含む。制御ユニットは、開始充填速度を使用して、サンプルが血液を含むときのサンプルのヘマトクリット値及びサンプル中の分析物の濃度のうちの少なくとも1つを計算するように更に構成される。システムは、免疫センサの少なくとも一部分を加熱するように構成された加熱要素も含むことができる。
【0012】
免疫センサは、第1の液体試薬と、第2の液体試薬と、抗原と抱合した磁気ビーズと、を含むことができる。一実施形態において、第1の液体試薬は、緩衝液中の酵素と抱合した抗体を含むことができる。第1の液体試薬は、下部電極上に縞模様に付けることができ、乾燥させることができる。第2の液体試薬は、フェリシアン化物と、酵素のための基質と、希酸溶液中のメディエータとを含むことができる。第2の液体試薬は、下部電極上に縞模様に付けることができ、乾燥させることができる。一方、磁気ビーズは、上部電極上に縞模様に付けることができ、乾燥させることができる。
【0013】
免疫センサは、複数のチャンバーと、セパレータと、通気孔と、1つ以上の封止用構成要素とを更に含むことができる。セパレータは、下部電極と上部電極との間に配設することができる。複数のチャンバーは、反応チャンバーと、検出チャンバーと、充填チャンバーと、を含むことができる。反応チャンバーは、セパレータ内に形成されることができ、第1の試薬、及び抗原と抱合した磁気ビーズがその中に配設されることができる。検出チャンバーも、セパレータ内に形成されることができ、第2の試薬がその中に配設されることができる。充填チャンバーは、セパレータ、並びに下部電極及び上部電極の一方に少なくとも部分的に形成されることができ、検出チャンバーからある距離だけ離間されることができ、反応チャンバーの少なくとも一部分に重なり合うことができる。通気孔は、セパレータ、下部電極、及び上部電極の各々において少なくとも部分的に形成されることができ、反応チャンバーからある距離だけ離間されることができ、検出チャンバーの少なくとも一部分に重なり合うことができる。一実施形態において、1つ以上の封止用構成要素は、第1の封止用構成要素及び第2の封止用構成要素であることができる。第1の封止用構成要素は、下部電極及び上部電極のうちの一方に取り付けられた、組み込まれた抗凝固剤を有することができ、通気孔の上に配設されることができ、充填チャンバーの壁を形成すると共に通気孔を封止するように構成されることができる。第2の封止用構成要素は、下部電極及び上部電極のうちのもう一方に取り付けることができ、通気孔の上に配設されることができ、通気孔を封止するように構成されることができる。一実施形態において、第1の封止用構成要素は、親水性接着テープを含む。
【0014】
一実施形態において、電気化学システムの制御ユニットは、サンプルの初期充填速度を測定するために、光信号における変化率を測定するように構成された光信号検出器を含むことができる。別の実施形態において、制御ユニットは、サンプルの初期充填速度を測定するために、初期電流量を測定するように構成された電流量検出器を含むことができる。更に別の実施形態において、制御ユニットは、サンプルが免疫センサの毛管空隙に進入した直後のサンプルの初期充填速度を測定するように構成されることができる。更に別の実施形態において、制御ユニットは、サンプルが、検出信号が生成される免疫センサの毛管空隙の領域内に横断した後の初期充填速度を測定するように構成されることができる。制御ユニット、免疫センサ、及び計器のうちの少なくとも1つは、サンプルの温度を測定するか、又はサンプルの温度を推測するように構成されることができる。
【0015】
システムが濃度を計算する分析物は、C反応性タンパク質であってよい。免疫センサ内に導入されるサンプルは、血液であってよい。一実施形態において、血液は、全血を含む。
【0016】
サンプル分析デバイスはまた、非限定的な例として、電気化学セル、電気化学センサ、グルコースセンサ、グルコース計器、ヘモグロビンセンサ、酸化防止剤センサ、及びバイオセンサを含む、多数の他の分析デバイスであってよい。一実施形態において、サンプル分析デバイスは、グルコースセンサを含む。グルコースセンサは、作用電極及び対又は対/基準電極を有する電気化学セルを含むことができる。作用電極及び対又は対/基準電極は、約500マイクロメートル以下で離間することができる。一実施形態において、電極間の間隔は、約80マイクロメートル〜約200マイクロメートルの範囲である。間隔は、所望の結果を達成するため、例えば、実質的に、所望時間内に定常状態の電流を達成するために決定することができる。一実施形態において、電極間の間隔は、対電極からの反応生成物が作用電極に到達するように選択される。
【0017】
作用電極及び対又は対/基準電極は、様々な構成を有することができる。例えば、電極は、互いに面することができるか、それらは、実質的に互いに面することができるか、又は、それらは、電極がほぼ同じ平面上に位置付けられる隣接構造を有することができる。電極は、実質的に同一の対応領域を有することができる。電極は、平面的であってもよい。一実施形態において、電気化学セルは、作用電極、対電極、及び別個の基準電極を含む。別の実施形態において、電気化学セルは、2つの電極対を有することができる。電極対は、作用電極、対電極、対/基準電極、及び別個の基準電極のうちの任意の組み合わせを含むことができるが、例示的な一実施形態において、各対は、作用電極及び対又は対/基準電極を含む。更に別の実施形態において、電気化学セルは、約1.5マイクロリットル以下の有効なセル量を有することができる。あるいは、電気化学セルは、中空であってもよい。
【0018】
電位は、非限定的な例として計器を含む、多数の異なる機構によって、セルの電極に印加することができる。電位の規模は、非限定的な例として、セル内のサンプルの所望の反応を含む、多数の異なる要因による可能性がある。一実施形態において、電位の規模は、サンプルの還元された形態の電解酸化、又は酸化された形態の電解還元が、実質的に拡散律速であるように、選択することができる。
【0019】
サンプルは、毛管現象によりセルに進入することができる。制御ユニットは、セルに進入するサンプルの初期速度を決定するために使用することができる。一実施形態において、制御ユニットは、サンプルの初期充填速度を測定するために、光信号における変化率を測定するように構成される、光信号検出器を含むことができる。別の実施形態において、制御ユニットは、サンプルの初期充填速度を測定するために、初期電流量を測定するように構成される、電流量検出器を含むことができる。更に別の実施形態において、制御ユニットは、サンプルが電気化学セルの毛管空隙に進入した直後のサンプルの初期充填速度を測定するように構成されることができる。更に別の実施形態において、制御ユニットは、サンプルが、検出信号が生成される電気化学セルの毛管空隙の領域内に横断した後の初期充填速度を測定するように構成されることができる。制御ユニット、電気化学セル、及び計器のうちの少なくとも1つは、サンプルの温度を測定するか、又はサンプルの温度を推測するように構成されることができる。
【0020】
血液サンプル中の抗原を測定するための方法の例示的な一実施形態は、2つの電極を有する免疫センサ及び免疫センサの2つの電極との間に電位を印加するように構成された計器を提供する工程を含むことができる。該方法は、抗原を含有する血液サンプルを免疫センサ内に導入する工程と、2つの電極間に電位を印加する工程と、血液サンプルの初期充填速度を決定する工程と、初期充填速度を考慮して、抗原の濃度を計算する工程とを更に含むことができる。代替的実施形態において、該方法は、血液のヘマトクリットレベルのみを測定するか、又は血液のヘマトクリットレベル及び血中の抗原の濃度の両方を測定するように設定することができる。免疫センサは、2つの電極間に配設されたセパレータ内に形成された反応チャンバー及び検出チャンバーと、セパレータ及び2つの電極のうちの1つ内に少なくとも部分的に形成された充填チャンバーと、セパレータ及び2つの電極内に少なくとも部分的に形成された通気孔と、を更に含むことができる。充填チャンバーは、検出チャンバーからある距離だけ離間されることができ、反応チャンバーの少なくとも一部分に重なり合うことができる。通気孔は、反応チャンバーからある距離だけ離間されることができ、検出チャンバーの少なくとも一部分に重なり合うことができる。血液サンプルの抗原は、C反応性タンパク質であってよい。該方法は、血液サンプルの温度を測定する工程、あるいは血液サンプルの温度を推測する工程、及び、次いで、電位を逆転させる工程後に、一定期間にわたって、電流の変化を測定する工程を更に含むことができる。その結果、抗原の濃度は、一定期間にわたる電流の変化及び測定又は推測された温度を考慮して、計算することができる。
【0021】
血液サンプルを測定するための方法は、第1の緩衝液中の抗体酵素複合体及び第2の緩衝液中の抗原に連結した磁気ビーズを反応チャンバー内に提供する工程を更に含むことができる。希酸中のフェリシアン化物、グリコース、及びメディエータは、検出チャンバー内に提供することができる。第1の封止は、充填チャンバーの壁を形成する通気孔の第1の側面上に提供することができ、第2の封止は、通気孔の第2の側面上に提供することができる。免疫センサ内に導入される血液サンプルの少なくとも一部分は、それが免疫センサ内に導入されるときに、充填チャンバーから反応チャンバーに移動する。
【0022】
該方法は、封止のうちの少なくとも1つを穿孔することによって、所定時間後に、通気孔を開口する工程を更に含むことができる。封止のうちの少なくとも1つを穿孔することで、磁気ビーズに拘束されていない抗原酵素複合体を含有する血液サンプルの一部分が、検出チャンバーに移動するのを可能にする。更に、該方法は、検出チャンバー内でグルコースの酸化を触媒する工程を含むことができ、これは、フェロシアン化物の形成をもたらすことができる。電流は、フェロシアン化物から電気化学的に検出することができ、血液サンプル中の抗原の濃度は、検出した信号を考慮して、計算することができる。
【0023】
一実施形態において、初期充填速度を決定する工程は、電位を印加した後の初期電流を測定する工程と、サンプル中のヘマトクリットのレベルを決定する工程と、作用電極と対電極との間の電位を逆転させる工程と、を含むことができる。したがって、分析物の濃度は、決定されたヘマトクリットのレベルに基づき、算定することができる。該方法は、電位の逆転後、一定期間にわたって、電流の変化を測定する工程を更に含むことができる。したがって、分析物の濃度は、一定期間にわたる電流の変化を考慮して、計算することができる。別の実施形態において、初期充填速度を決定する工程は、初期充填速度を決定するために、光信号における変化率を決定する工程を含むことができる。更に別の実施形態において、初期充填速度を決定する工程は、初期充填速度を決定するために、初期電流量を決定する工程を含むことができる。初期充填速度は、血液サンプルが免疫センサの毛管空隙に進入した直後に決定することができる。あるいは、初期充填速度は、血液サンプルが、検出信号が生成される免疫センサの毛管空隙の領域内に横断した後に決定することができる。
【0024】
本発明は、以下の詳細な説明を付属の図面と併せ読むことでより詳細に理解されるであろう。
【図面の簡単な説明】
【0025】
【図1】本発明に従う、免疫センサ、及び初期充填速度を計算するための光検出器を有する制御ユニットの一実施形態の斜視図。
【図2】本発明に従う、免疫センサの別の例示的実施形態の分解図。免疫センサは、初期充填速度を計算するための電気化学検出システムを有する制御ユニットと共に使用するように構成される。
【図3】本発明に従う、電気化学セルの例示的な一実施形態の概略側面図(原寸に比例しない)。
【図4】上から見た図3の電気化学セルの平面図。
【図5】本発明に従う、中空の電気化学セルの例示的な一実施形態の概略断面図(原寸に比例しない)。
【図6】本明細書に提供される様々な血液サンプルを試験するための例示的な一実施例と併せて、図2のデバイスを使用して実施された電流対時間遷移のプロット。
【図7】電流に対しての図6に関連した実施例に関連して使用された、各血液サンプルに関するヘマトクリット濃度レベルのプロット。
【図8】図6に関連した各血液サンプルの決定されたヘマトクリット濃度レベルに対する、図6に関連した各血液サンプルに関して決定されたヘマトクリット濃度レベルの誤差割合のプロット。
【図9】図6に関連した各血液サンプルの計算されたC反応性タンパク質のレベルの、従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値に対するプロット。
【図10】本明細書に提供される様々な血液サンプルを試験するための別の例示的実施例と併せて、図2の免疫センサを使用して実施した、血液サンプルが配設される免疫センサの検出チャンバーの電流対温度のプロット。
【図11】図10に関連した各血液サンプルの決定されたヘマトクリット濃度レベルに対する、図10に関連した各血液サンプルに関して決定されたヘマトクリット濃度レベルの誤差割合のプロット。
【図12】図10に関連した各血液サンプルに関する、経時的な電流の変化に基づき決定された勾配の、血液サンプルが配設される免疫センサの検出チャンバーの温度に対するプロット。
【図13】従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値に対して、約33.5%のヘマトクリットレベル及び約47.5%のヘマトクリットレベルを有する、図10に関連した血液サンプルの計算されたC反応性タンパク質レベルのプロット。
【発明を実施するための形態】
【0026】
本明細書で開示される装置及び方法の構造、機能、製造、及び使用の原理が総括的に理解されるように、特定の例示的実施形態について、これから説明することにする。これらの実施形態の1つ以上の実施例を添付の図面に示す。本明細書で詳細に説明し、添付の図面に示す装置及び方法は、非限定的な例示的実施形態であること、並びに、本発明の範囲は、特許請求の範囲のみによって定義されることが、当業者には理解されよう。ある例示的実施形態に関連して例示又は説明される特徴は、他の実施形態の特徴と組み合わされてもよい。そのような修正及び変形は、本発明の範囲に含まれることを意図したものである。更に、いくつかの実施形態は、サンプルのヘマトクリットの値を決定する工程を論じ、他の実施形態は、サンプル中の分析物の濃度を決定する工程を論じるが、各種類の実施形態に付随する教示は、他の種類の実施形態に同様に適用可能であることは、当業者には理解されるであろう。即ち、ヘマトクリット値を決定する工程を対象とした実施形態は、サンプル中の分析物の濃度を決定するために使用することもでき、分析物の濃度を決定する工程を対象とした実施形態は、サンプルのヘマトクリット値を単に決定するために使用することができる。更に、実施形態は、両方、サンプルのヘマトクリット値を決定し、サンプル中の分析物の濃度を決定するために使用することができる。
【0027】
本明細書に開示する、サンプル中のヘマトクリットの値を決定し、サンプル中の分析物の濃度を決定するための方法は、任意のサンプル分析デバイス及び/又はシステムと共に使用することができる。デバイスは、毛管空隙を有することができる。該デバイスは、少なくとも1つの作用電極及び電位をそれらの間に印加することができる1つの対電極を含むことができる。サンプル分析デバイスは、一般的に、計器等の電極間に電位を印加するための構成要素に関連付けられることができる。サンプル分析デバイスは、サンプルがデバイスに導入されるときに、サンプルの初期充填速度を測定することが可能な、1つ以上の構成要素に関連付けられることもできる。かかる構成要素は、初期充填速度を考慮して、サンプル中の分析物の濃度を計算することも可能である。かかる構成要素は、概して、本明細書において制御ユニットとして言及される。更に、分析物、抗原、及び抗体という用語は、その中で同じ意味で使用され、したがって、1つの用語の使用は、当業者によって他に指示されないか、又は道理にかなって知られていない限り、3つのすべての用語に同様に適用可能である。
【0028】
全血サンプルのヘマトクリット値を決定するための方法の例示的な一実施形態において、全血のサンプルを、毛管空隙を有するサンプル分析デバイスに提供する。毛管の少なくとも一部分内のサンプルの初期充填速度を測定する。次いで、サンプルのヘマトクリット値を、初期充填速度から決定する。サンプル中の分析物又は抗原の濃度は、決定されたヘマトクリットの値を考慮して、決定することができる。初期充填速度を使用してヘマトクリット値を計算することにより、精度の改善を可能にすることができる。ヘマトクリット値を決定するための方法は、以下に詳細に論じるとおり、温度の効果も明らかにすることができる。更に、付随する分析物濃度を参照せずに、ヘマトクリットの値のみを測定することによって、決定値を、ほぼ瞬時に、しばしば、1秒未満で達成することができる。例えば、一滴の血液のヘマトクリットレベルは、血液をサンプル分析デバイスのセンサストリップ上に単に液滴することによって、1秒未満で決定することができる。血液がストリップ上に配設されると、ヘマトクリットレベルのデジタル読み出しを、ほぼ瞬時に提供することができる。その結果は、ヘマトクリットレベルの迅速かつ正確な決定値であり、これは、様々な医療評価において、例えば、貧血等の症状に関連する評価を行う上で有用である。
【0029】
サンプル中の分析物の濃度を決定するための方法の別の例示的実施形態において、サンプルを、作用電極及び対電極を有するサンプル分析デバイスに提供する。電位は、サンプル分析デバイスの作用電極と対電極との間に印加することができ、サンプル分析デバイスの毛管空隙内へのサンプルの初期充填速度を決定することができる。サンプル中の分析物の濃度は、決定された初期充填速度を考慮して、計算することができる。初期充填速度を考慮して濃度を計算することによって、各サンプルで異なるヘマトクリットレベルから生じ得る誤差等の誤差を明らかにすることができ、それによって、サンプル中の分析物の濃度のより正確な決定値をもたらす。該方法は、以下に詳細に論じるとおり、温度の影響を明らかにすることもできる。サンプル中の分析物の濃度を検出するための代替的実施形態において、誤差は、決定された初期充填速度ではなくむしろ、決定された充填時間に基づき訂正される。かかるデバイスの一例は、「Systems,Devices,and Methods for Improving Accuracy of Biosensors Using Fill Time」と題する、2009年12月30日に本出願と同時に出願されたRonald C.Chatelier及びAlastair M.Hodges(代理人整理番号104978−458)の同時係属特許出願に開示されており、これは、参照によって、その全体が本願に組み込まれる。代替的実施形態において、血漿相内の抗原の濃度及びヘマトクリットレベルの推定レベルを決定することができる。
【0030】
初期充填速度は、分析物の濃度を決定するための様々な方法に使用することができる。例えば、サンプルが全血を含み、サンプルがサンプル分析デバイス内で分析される位置の温度が既知である場合、初期充填速度は、決定されたヘマトクリットレベルに関連付けられることができる。例えば、サンプル分析デバイスのチャンバーが所望温度まで予熱される場合、サンプルの温度は既知であり得る。温度が不明な場合、計算は、依然として実施され、これは、温度を反応中に測定又は推測するのを可能にする。かかる例では、温度及びヘマトクリットレベルは、両方とも、より正確な分析物濃度決定値を提供するために明らかにすることができる。更に、初期充填速度は、同様に、血液サンプルのヘマトクリットレベルを決定するための様々な方法に使用することができる。
【0031】
サンプル分析デバイスに進入するサンプルに関連付けられる初期充填速度を決定するための様々な方法が存在する。初期充填速度を決定することは、ひいては、液体の粘度を予測することを可能にすることができる。液体の粘度を予測することは、より正確な濃度決定を行う上で役立つことができる。図1に示すとおり、例示的な一実施形態において、免疫センサ10は、一般的に免疫センサ10の進入ポート21付近から充填チャンバー22まで位置する光検出器52を有する制御ユニット50を含む。光検出器52は、任意の形状又は寸法を有することができ、また、例えば、免疫センサ10の上部の上又は免疫センサ10の進入ポート21のすぐ内側に位置することができる。図示の実施形態において、光センサは、進入ポート21に隣接する、免疫センサ10の上部プレート14に取り付けられる。光センサ52は、サンプルがセンサ52を通過するときに変化する光信号を含むことができる。したがって、サンプルが免疫センサ10に提供されると、光信号の変化率を検出することができ、それは、ひいては、初期充填速度を予測するために使用することができる。変化率は、免疫センサ10の毛管空隙の少なくとも一部分内で測定することができる。次いで、初期充填速度は、多くの異なるパラメータを計算するために使用することができる。非限定的な例として、初期充填速度は、サンプル中の抗原の濃度又は全血サンプルのヘマトクリットレベルを計算するために使用することができる。
【0032】
別の例示的実施形態において、電気化学検出システムは、初期電流量の規模を測定するために使用することができる。規模は、サンプルがサンプル分析デバイスの毛管空隙に進入するとすぐに測定することができる。毛管空隙は、例えば、充填チャンバー内への初期の進入前に、充填チャンバーと反応チャンバーとの間、及び/又は反応チャンバーと検出チャンバーとの間に位置することができる。例示的な一実施形態において、初期電流量は、充填チャンバーと反応チャンバーとの間で決定される。別の例示的実施形態において、初期電流量は、まず、サンプルが、検出チャンバー等の検出信号が生成されるサンプル分析デバイスの毛管空隙の領域内に横断するときに測定される。
【0033】
多くの異なる技術を、電流量を測定するために使用することができる。例えば、所望数の測定を、所望の期間にわたって行うことができる。例示的な一実施形態において、測定は、約1ミリ秒毎〜約25ミリ秒毎の範囲にほぼ少なくとも約10ミリ秒間〜約300ミリ秒間、行われる。別の実施形態において、測定は、ほぼ約10ミリ秒毎にほぼ少なくとも50ミリ秒間行われる。単一の測定を行うこともできるが、典型的に、初期速度のより正確な結果は、短期間にわたって複数の測定を行うことによって得ることができる。いくつかを以下に詳細に開示するが、サンプルの初期電流及び/又は初期速度を決定することができる様々な他の方法が存在することは、当業者には理解されるであろう。
【0034】
本明細書に開示する方法のうちの少なくともいくつか及び免疫センサ110と併せて使用するためのサンプル分析デバイスの別の例示的実施形態が図2に図示され、「Adhesive Compositions for Use in an Immunosensor」と題する、2009年9月30日に出願された、Chatelierらの米国特許出願第12/570,268号に記載されており、これは、参照によって、その全体が本願に組み込まれる。複数のチャンバーは、サンプルを免疫センサの中に導入することができる充填チャンバー、サンプルを1つ以上の所望の物質と反応させることができる反応チャンバー、及びサンプルの特定の構成成分の濃度を決定することができる検出チャンバーを含む、免疫センサ内に形成されることができる。これらのチャンバーは、免疫センサの下部電極、上部電極、及びセパレータのうちの少なくとも一部分内に形成されることができる。免疫センサは、必要に応じて、空気が免疫センサに進入及びそれから漏れることを可能にし、また第1及び第2の封止用構成要素が通気孔の第1及び第2の側面を選択的に封止することを可能にする、通気孔を含むこともできる。第1の封止用構成要素は、充填チャンバーの壁を形成することもできる。
【0035】
図示するとおり、免疫センサ110は、その上に縞模様に付けられた2つの液体試薬130、132を有する下部電極112を含む。下部電極112は、電極を形成するために使用される任意の数の技術を使用して形成されることができるが、一実施形態では、硫酸バリウムで充填されたポリエチレンテレフタレート(PET)のシートは、例えば、金等の好適な伝導体でスパッタコーティングされる。電極を形成する他の非限定的な例が、「Electrochemical Cell」と題され、2000年11月10日に出願された、Hodgesらの米国特許第6,521,110号において開示されており、その内容は、参照によって、その全体が本願に組み込まれる。
【0036】
同様に、液体試薬130、132は、多くの異なる組成物を有し得る。一実施形態において、第1の液体試薬130は、スクロース、並びにポロキサマー(例えば、Pluronics(登録商標)ブロックコポリマー等)、抗凝結剤(シトラコン酸塩)、及びカルシウムイオンを含有する緩衝液中の酵素と抱合した抗体(例えば、GDH−PQQ等)を含む。一実施形態において、第2の液体試薬132は、酸性緩衝液(希釈シトラコン酸溶液等)中のフェリシアン化物、グルコース、及び第2のメディエータ(フェナジンエトサルフェート等)の混合物を含む。第1及び第2の液体試薬130、132は、下部電極112の上で乾燥させることができる。試薬130、132を乾燥させるために多くの技法を使用することができるが、一実施形態において、下部電極112の上に試薬130、132が縞模様で付けられた後に、1つ以上の赤外線乾燥器を試薬130、132に適用することができる。また、例えば、1つ以上の空気乾燥器が赤外線乾燥器に続いて使用されることもできる。本明細書における、第1の試薬と第1の液体試薬、及び第2の試薬と第2の液体試薬についての言及は、同じ意味で用いられており、特定の実施形態に対して試薬が所与の時点で液体の又は乾燥した形態にあることを必ずしも示唆するものではない。更に、第1及び第2の液体試薬に付随する構成成分のいくつかは、交換可能に、かつ/又は、所望に応じて第1の液体試薬と第2の液体試薬の両方において使用されることができる。非限定的な例として、抗凝固剤は、第1の液体試薬130及び第2の液体試薬132のうちの一方又は両方に付随することができる。
【0037】
1本の線が、試薬130、132の一方の縁部がその線に近接するか又は接するように、試薬130と132との間のスパッタコーティングされた金として形成されることができる。図示の実施形態において、線は、試薬132の縁部が通気孔124における線に接するように、形成される。この線は、レーザーアブレーションを利用して、又は鋭利な金属の縁部を用いて施されることができる。一実施形態において、線は、試薬130、132が電極上に縞模様で付けられる前に施されることができる。この線は、下部電極112の検出チャンバーの下にある部分を、反応チャンバーの下に位置する部分から電気的に絶縁するように設計されることができる。これにより、電気化学的分析の間、作用電極の範囲がより良好に画定されることができる。
【0038】
また、免疫センサ110は、1つ以上の磁気ビーズ134を有する上部電極114を含むことができ、磁気ビーズ134は、表面結合型抗原をその上に含有している。これらの抗原は、以下で更に詳細に説明するように、下部電極112に配設された抗体及び反応チャンバー118内のサンプルと反応するように構成されることができる。下部電極112の上及び上部電極114の上に配設された構成要素が相互に交換可能であることが、当業者には理解されよう。したがって、下部電極112は1つ以上の磁気ビーズ134を有することができ、上部電極114は、上部電極132上に縞模様で付けられた2種類の液体試薬130、132を有することができる。更に、図示の実施形態において、電極112の長さは、免疫センサ110の全体の長さを形成しているが、他の実施形態において、電極は、免疫センサの層のうちの下部又は上部電極として働く一部分のみとされることができ、あるいは、複数の電極が、免疫センサの単一の層に配置されることができる。更に、免疫センサに印加される電位は、反転及び/又は交番することがあるため、下部及び上部電極の各々は、異なる段階において作用電極及び対電極又は対電極/基準電極として働くことができる。説明を容易にする目的で、本願において、下部電極は作用電極と見なし、上部電極は対電極又は対電極/基準電極と見なす。
【0039】
下部電極112と上部電極114との間に配置されるセパレータ116は、多様な形状及び寸法を有することができるが、一般的には、望ましくは下部及び上部電極112、114と係合して免疫センサ110を形成するように構成される。例示的な一実施形態において、セパレータ116は、両側で接着特性を含む。セパレータ116は、セパレータ116の2面の各々の側に剥離ライナーを更に有することができる。セパレータ116は、少なくとも2つの空洞を形成する方式で切断されることができる。第1の空洞は、反応チャンバー118として働くように形成されることができ、第2の空洞は、検出チャンバー120として働くように形成されることができる。一実施形態において、反応チャンバー118は、電極112、114と整列して反応チャンバー内での抗原抗体反応を可能にし、一方で検出チャンバー120は、電極112、114と整列して検出チャンバー内でのフェロシアン化物の電気化学的測定を可能にするように、セパレータ116がキスカット(kiss−cut)されることができる。
【0040】
一実施形態において、セパレータ116は、上部電極114の磁気ビーズ134及び下部電極112の第1の試薬130を少なくとも部分的に反応チャンバー118内に配設することが可能となり、かつ下部電極112の第2の試薬132のフェロシアン化物とグルコースとの組み合わせを少なくとも部分的に検出チャンバー120内に配設することが可能となるような方式で、下部電極112上に配置されることができる第1及び第2の液体試薬130、132の各々に抗凝固剤を含めて、抗凝固剤が反応チャンバー118及び検出チャンバー120の各々に付随するようにすると有利となり得る。いくつかの実施形態では、上部電極112及び下部電極114の一方とセパレータ116との組み合わせが、互いに積層されて二層積層体を形成することができ、一方で、他の実施形態では、下部電極112、上部電極114、及びセパレータ116の各々の組み合わせが、互いに積層されて三層積層体を形成することができる。あるいは、更なる層も追加し得る。
【0041】
充填チャンバー122は、下部電極112及び上部電極114の一方及びセパレータ116に孔を打抜きすることによって形成されることができる。図示の実施形態において、充填チャンバーは、下部電極112の孔が反応チャンバー118と重なり合うように、下部電極112及びセパレータ116に孔を打抜きすることによって形成されている。図示されるように、充填チャンバー122は、検出チャンバー120から一定の距離だけ離されることができる。そのような構成により、サンプルは、検出チャンバー120に進入することなしに、充填チャンバー122を通じて免疫センサ110に進入し、反応チャンバー118の中に流入して、例えば、第1の電極112上の、酵素と抱合した抗体を緩衝液中に含む第1の液体試薬130、及び上部電極114上に縞模様で付けられた磁気ビーズ134と反応することが可能となる。サンプルの充填チャンバー122への進入は、毛管現象として生じることができ、充填チャンバー122、反応チャンバー118、及びそれらの間の位置のうちの少なくとも1つを、毛管空隙と見なすことができる。サンプルが反応したら、そのサンプルは、次いで、第2の液体試薬132、例えば、フェリシアン化物、グルコース、及び酸性の緩衝液中の第2のメディエータの混合物と相互作用するために、検出チャンバー120の中に流入することができる。
【0042】
通気孔124が免疫センサ110の全体を通じて延びるように、通気孔124は、2つの電極112、114の各々及びセパレータ116を貫いて孔を打抜きすることによって形成されることができる。孔は、例えば、多数の異なる位置でドリル又は打抜き等の好適な方法で形成されることができるが、例示的な一実施形態では、それは、反応チャンバー118から離間される検出チャンバー120の領域と重なり合うことができる。
【0043】
通気孔124は、多数の異なる方法で封止することができる。図示の実施形態において、第1の封止用構成要素140は、下部電極112上に位置して、通気孔124の第1の側面を封止し、第2の封止用構成要素142は、上部電極114上に位置して、通機孔124の第2の側面を封止する。封止用構成要素は、任意の数の材料から作製することができ、及び/又は任意の数の材料を含むことができる。非限定的な例として、封止用構成要素のいずれか一方、又はそれらの両方は、親水性接着テープ又はスコッチ(Scotch)(登録商標)テープであってよい。封止用構成要素の接着側は、免疫センサ110に面することができる。図示されるように、第1の封止用構成要素140は、通気孔124に対する封止を形成できるだけでなく、サンプルが中に収容されることができるように、充填チャンバー122の壁を形成することもできる。第1の封止用構成要素140の接着側上に組み込まれた特性は、充填チャンバー122に関連付けられることができる。例えば、第1の封止用構成要素140が、それを親水性及び/又は水溶性にする特性を含む場合、充填チャンバーは、サンプルがその中に配設されるときに、よく濡れた状態のままであることができる。更に、封止用構成要素140、142は、免疫センサ110及びその中に配設された構成成分に対して所望に応じて通気及び/又は封止をなすように、免疫センサ110に選択的に関連し、かつ切り離すことができる。
【0044】
接着剤は、一般的に、免疫センサの構造に使用することができる。接着剤を本開示の免疫センサ及び他のサンプル分析デバイス内に組み込むことができる方法の非限定的な例は、「Adhesive Compositions for Use in an Immunosensor」と題し、2009年9月30日に出願された、Chatelierらの米国特許出願第12/570,268号で確認することができ、この内容は、既に、参照によって、その全体が本願に組み込まれている。
【0045】
本開示は、免疫センサに関連する様々な異なる実施形態を論じるが、免疫センサの他の実施形態も、本開示の方法と共に使用することができる。そのような実施形態の非限定的な例には、「Direct Immunosensor Assay」と題され2002年3月21日に出願されたHodgesらの米国特許出願公開第2003/0180814号、「Immunosensor」と題され2004年4月22日に出願されたHodgesらの米国特許出願公開第2004/0203137号、「Biosensor Apparatus and Methods of Use」と題され2005年11月21日に出願されたRylattらの米国特許出願公開第2006/0134713号、並びに米国特許出願公開第2003/0180814号及び同第2004/0203137号の各々に対する優先権を主張する米国特許出願第12/563,091号に記載されたものが挙げられ、これらのそれぞれは、参照によって、その全体が本願に組み込まれる。
【0046】
一実施形態において、免疫センサ110は、電極112、114に電位を印加し、その電位を印加した結果として生じる電流を測定するように構成された計器の中に配設されるように構成されることができる。一実施形態において、免疫センサは、計器と係合するための1つ以上のタブ117を含む。他の特性も、免疫センサ110を計器に係合するために使用することができる。その計器は、多くの種々の特徴を有することができる。例えば、計器は、免疫センサ110の特定の構成成分をあるチャンバー内に維持し、その一方で他の構成成分が他のチャンバーに流れるように構成された、磁石を含むことができる。例示的な一実施形態において、計器の磁石は、免疫センサ110を計器内に配設すると磁石が反応チャンバー118の下方に配置されるように位置する。これにより、磁石は、任意の磁気ビーズ134、より具体的には、ビーズ134に拘束されている任意の抗体酵素複合体が、検出チャンバー120の中に流入するのを防ぐのを助けることができる。
【0047】
計器の別の特徴には、加熱要素が挙げられる。加熱要素は、反応速度を速めるのを助け、また、粘度を減じることによってサンプルが所望の方式で免疫センサ110を通じて流動するのを助けることができる。加熱要素は、1つ以上のチャンバー及び/又はその中に配置されたサンプルが所定温度まで加熱されるのを可能にすることもできる。所定温度まで加熱することで、例えば、反応が生じる際の温度変化の影響を減少又は除去することによって、精度を提供するのを助けることができる。
【0048】
更に、穿孔装置は、計器に関連付けられることもできる。穿孔装置は、空気が通気孔から流出し、液体が反応チャンバーから検出チャンバーに流動することができるように、所望時間に第1及び第2の封止用構成要素のうちの少なくとも1つを穿孔するように構成することができる。
【0049】
免疫センサ110は、制御ユニットに関連付けられるように構成することもできる。制御ユニットは、様々な機能を実行するように構成することができる。例示的な一実施形態において、制御ユニットは、サンプルがデバイスに導入されたときに、サンプルの初期充填速度を測定することが可能である。別の実施形態において、制御ユニットは、血液サンプルのヘマトクリット値を決定するように構成される。更に別の実施形態において、制御ユニットは、初期充填速度を考慮して、サンプル中の分析物の濃度を計算するように構成される。実際、制御ユニットは、少なくとも部分的に、望ましいとされる機能性、及びシステムが初期充填速度を測定するように設計される方法に応じて、多数の異なる特徴を含むことができる。
【0050】
非限定的な例として、システムが初期充填速度を光学的に測定するように設計される場合、制御ユニットは、光信号検出器を含むことができる。光信号検出器は、検出器によって感知された光信号における変化率に基づき初期充填速度を測定することができる。あるいは、システムが電流量に基づき所期充填速度を測定するように設計される場合、制御ユニットは、電流量検出器を含むことができる。電流量検出器は、サンプルが免疫センサに進入する結果として生じる電流の変化に基づき初期充填速度を測定することができる。この変化のタイミングは、多くの異なる方法で生じ得るが、例示的な一実施形態では、電流は、サンプルが、検出信号が生成される免疫センサの毛管空隙の領域内に横断した後、例えば、サンプルが反応チャンバーから検出チャンバーに横断するときに測定される。別の実施形態では、電流は、サンプルが免疫センサの毛管空隙に進入した直後、例えば、サンプルが反応チャンバーに進入したときに測定される。
【0051】
制御ユニットは、システムの他の特徴を測定することもできる。非限定的な例として、制御ユニットは、免疫センサの1つ以上のチャンバーの温度を測定するように構成されることができる。また、例えば、直接、又は周辺温度を測定し、それを使用してサンプルの温度、サンプルの色、又はサンプル及び/又はシステムの様々な他の特徴及び/又は特性を推測することによって、サンプルの温度を測定するように構成されることもできる。更なる非限定的な例として、制御ユニットは、初期充填速度決定の結果、ヘマトクリット値決定の結果、及び/又は分析物濃度決定の結果を外部装置に伝達するように構成されることができる。これは、任意の数の方法で実現することができる。一実施形態において、制御ユニットは、マイクロプロセッサ及び/又はディスプレイデバイスに配線することができる。別の実施形態において、制御ユニットは、制御ユニットからのデータをマイクロプロセッサ及び/又はディスプレイデバイスに無線で送信するように構成されることができる。
【0052】
システムの他の構成要素も、そのような測定を行うように構成されることができる。例えば、免疫センサ又は計器は、免疫センサの1つ以上のチャンバーの温度を測定するか、サンプルの温度を測定若しくは推測するか、又はサンプル及び/若しくはシステムの様々な他の特徴及び/若しくは特性を測定、決定、若しくは推測するように構成されることができる。更に、制御ユニットのこれらの特徴が、単一の制御ユニット内で交換及び選択的に組み合わせることができることは、当業者には理解されよう。例えば、制御ユニットは、初期充填速度を決定し、かつチャンバーの温度を測定することができる。他の実施形態において、複数の制御ユニットは、様々な制御ユニットの構成及び実行される所望機能に少なくとも部分的に基づき、様々な機能を実行するために共に使用することができる。
【0053】
他の種類のサンプル分析デバイスを、本明細書に開示するシステム及び方法のうちの少なくともいくつかと併せて使用することができる。これらのデバイスには、非限定的な例として、電気化学セル、電気化学センサ、グルコースセンサ、グルコース計器、ヘモグロビンセンサ、酸化防止剤センサ、及びバイオセンサが挙げられる。一実施形態において、サンプル分析デバイスは、グルコースセンサを含む。グルコースセンサは、図3及び4に図示するセル等の電気化学セルを含むことができる。セルは、上部表面及び下部表面202、203を有する薄いストリップ膜201を含むことができ、また下部表面203上に配設された作用電極206と上部表面202上に配設された対/基準電極205との間に画定されたセル領域204を含むこともできる。膜の厚さは、反応生成物が対電極から作用電極に到達する等の所望の結果を達成するように選択することができる。例えば、膜の厚さは、電極が距離tによって分離されるように選択することができ、その距離は、対電極における電気化学反応の生成物が、試験期間中に作用電極に移動することができ、定常状態の拡散プロファイルを実質的に達成することができるように、十分に近接してもよい。典型的に、tは、約500マイクロメートル未満、あるいは、約10マイクロメートル〜約400マイクロメートルの範囲、より具体的には、約80マイクロメートル〜約200マイクロメートルの範囲であってよい。一実施形態において、電極間の間隔は、対電極からの反応生成物が作用電極に到達するように選択することができる。
【0054】
電極は、様々な構成を有することもできる。例えば、電極は、平面的であってもよい。更に、図示の実施形態では、電極205、206は互いに面し、実質的に対向する一方、他の実施形態では、電極は、互いに単に面することができ、それらは、実質的に互いに対向するか、又はそれらは、電極がほぼ同じ平面上に位置付けられる隣接構造を有することができる。異なる電極構成の例は、「Electrochemical Cell」と題し2003年10月14日に出願された、Hodgesの米国特許第7,431,820号において少なくとも確認することができ、その内容は、参照によって、その全体が本願に組み込まれる。
【0055】
サンプル付着又は「標的」領域207は、膜201の上部表面202上に画定することができ、セル領域204から膜の厚さを超える距離で離間することができる。膜201は、標的領域207とセル領域204との間に延在することができる拡散領域208を有することができる。好適な試薬は、酸化還元メディエータM、酵素E、及びpH緩衝液Bを含むことができ、これらの各々は、膜のセル領域204内、及び/又はセル領域204と標的領域207との間に含まれることができる。試薬は、安定剤等を含むこともできる。
【0056】
センサの使用中、一滴の血液を標的領域207上に設置することができ、血液の構成要素を、セル領域204に向かって吸上げることができる。血液が標的領域207を覆う初期速度は、少なくともヘマトクリットに依存し得る。
【0057】
電極205、206の各々は、所定領域を有することができる。図3及び4の実施形態において、セル領域204は、膜の縁部209、210、211によって画定することができ、それは、電極の縁部212、213を(標的領域207に対して)誘導することによって、電極205、206の縁部に対応させることができる。本例において、電極は、約60nm(600オングストローム)の厚さであってよく、また約1mm〜5mmの幅であってよいが、様々な他の寸法及びパラメータを、本発明の範囲から逸脱することなく使用することができる。
【0058】
あるいは、膜の両側を、標的領域207を除いて、サンプルからの水の蒸発を防止しかつ装置に機械的ロバスト性を提供する機能を果たすことができる層を積層することによって、被覆することができる。水の蒸発は、それがサンプルを濃縮し、電極が乾燥するのを可能にし、溶液が冷却するのを可能にするため、望ましくないと考えられており、それによって、拡散係数に影響を及ぼし、酵素動態を遅くするが、拡散係数は、上記のとおり推測することができる。
【0059】
図5に図示する代替的実施形態において、本明細書に開示するシステム及び方法と共に使用するための中空の電気化学セルを提供する。電極305、306は、離間されたポリマー壁330によって担持されることができ、それによって中空セルを画定する。開口部331を、セルの1つの側面上に提供することができ、それによって、サンプルを空洞332内に受け入れることができる。本実施形態では膜を使用しないが、いくつかの実施形態では膜を含むことができる。電極は、少なくとも上述のとおり、様々な構成を有することができる。非限定的な例として、電極は、約500マイクロメートル未満、好ましくは、約10マイクロメートル又は約20マイクロメートル〜約400マイクロメートルの範囲、より好ましくは、約100マイクロメートル〜約200マイクロメートルの範囲で離間することができる。有効なセル量は、約1.5マイクロリットル以下であり得る。
【0060】
図3〜5の電気化学セルは、計器、制御ユニット、並びに本明細書に開示するデバイス、システム、及び方法の他の構成要素及び工程と併せて使用することができる。図3〜5の電気化学セルに関連する更なる開示は、「Electrochemical cell」と題し1998年4月17日に出願された、Hodgesらの米国特許第6,284,125号で確認することができ、この内容は、参照によって、その全体が本願に組み込まれる。例えば、本開示と併せて使用される電気化学セルは、2つの電極対を有することができる。電極対は、作用電極、対電極、対/基準電極、及び別個の基準電極のうちの任意の組み合わせを含むことができる。
【実施例】
【0061】
(実施例1)
測定する電流量に基づき初期充填速度を測定するための電気化学システムの使用を、以下の実施例によって示す。以下の実施例において、システムは、サンプル分析デバイス、特に、図2の免疫センサ110、電位を印加するように構成された計器、及び初期充填速度を決定するように構成された制御ユニットを含んだ。特に、電位を、免疫センサ110の電極に印加し、ヘマトクリットのレベルを決定し、次いで、電位を逆転させた。分析物の濃度を、決定されたヘマトクリットのレベルを考慮して、その後決定した。ヘマトクリットのレベルを、計算された初期充填速度を考慮して、決定した。
【0062】
複数のサンプルを、本明細書に開示するシステム、デバイス、及び方法の性能を試験するための分析に提供した。サンプルは、C反応性タンパク質を含有する血液サンプルであり、したがって、決定される分析物の濃度は、C反応性タンパク質の濃度であった。試験結果の比較として既知の、4つの異なるレベルのヘマトクリットを含有したサンプルを、実際の結果と比較して、システム、デバイス、及び方法の精度を決定することができるであろう。ヘマトクリットの4つのレベルは、約33%、約41.5%、約47.5%、及び約55%であった。4つのレベルのヘマトクリットを試験することは、開示したシステム、デバイス及び方法の精度が広範囲におよぶ濃度レベルにわたり確認されるのを可能にした。
【0063】
この第1の実施例において、免疫センサを、サンプルが導入される前に、約37℃まで予熱した。免疫センサに関連付けられる計器を、予熱を実行するように構成したが、他の代替物を使用することもできた。次いでサンプルを免疫センサ内に導入した。サンプルの免疫センサ内への導入は様々な方法で達成することができるが、該実施例では、充填チャンバーへの毛管現象により、各サンプルを個別に受け入れた。
【0064】
約2分間が経過した後、第1の封止用構成要素を穿孔することによって、免疫センサの通気孔にアクセスした。計器の穿孔装置を使用して穿孔動作を実行し、それが次には、血液が免疫センサの反応チャンバーから免疫センサの検出チャンバー内に流動するのを可能にした。血液が検出チャンバーに進入し始めるとすぐに、計器により約4秒間、約300mVの電位を電極に印加した。あるいは、電位を、血液が検出チャンバーに到達する前、又は到達している間に印加することもできた。その後、電位を、約10秒間、中断し逆転させた。本実施例から得られた電流対時間遷移のプロットを図6に図示する。本実施例において、約10ミリ秒毎に測定され、次いで、最初の50ミリ秒間において平均化された各サンプルの初期電流は、特定のサンプルのヘマトクリットレベルに関連する。ヘマトクリットのレベルを、第1の電位の印加中に初期電流から決定する一方、C反応性タンパク質のレベルを、電位の逆転後、電流対時間プロットの勾配及び決定されたヘマトクリットのレベルに基づき計算する。
【0065】
上述のとおり、いくつかの実施形態において、ヘマトクリットのレベルのみを測定することが望ましい場合がある。したがって、初期電流に基づく第1の計算は、その計算を行うのに必要とされる唯一の工程であり得る。本実施例において、この決定を、4秒間の電位印加の結果として行う一方、ヘマトクリットレベルの実際の決定は、初期電流を計算できるのと同じほど迅速に決定することができる。したがって、非限定的な例として、初期電流が、最初の約50ミリ秒間の平均に基づき計算される場合、ヘマトクリットのレベルは、最初の約50ミリ秒後に決定することができる。したがって、血液サンプルのヘマトクリットレベルの測定は、1秒未満で実施することができる。
【0066】
決定された各サンプルのヘマトクリットレベルを、図7に図示する。図7は、各サンプルのヘマトクリットの濃度レベル対決定された初期電流のプロットを図示する。プロットは、4つの異なるレベルのヘマトクリットを含有するサンプルが試験されたことを明確に示し、それは、既知の濃度レベルと相関する。更に、図示するとおり、より高いレベルのヘマトクリットは、一般的に、測定された初期電流のより低い絶対値をもたらした。例えば、約33%であったヘマトクリットの濃度を有するサンプルは、ほぼ、約38マイクロアンペア〜約33マイクロアンペアの範囲であった初期電流絶対値を有した一方、約47.5%であったヘマトクリットの濃度を有するサンプルは、ほぼ、約31マイクロアンペア〜約26マイクロアンペアの範囲であった初期電流絶対値を有した。すべての結果の最適合線を決定し、それも図7に図示する。最適合線と相関する等式は、
【数9】

であり、ここでHは、ヘマトクリットのレベルであり、
【数10】

は、初期電流である。ヘマトクリットレベル対初期電流の結果を表す等式と実際の結果との間の誤差を、図8に図示する。より具体的には、図8は、各試験サンプル対実際の測定されたヘマトクリットレベルに存在した誤差割合をプロットする。2つを除いたすべての実際の結果は、計算された範囲の約±5%内であり、かなりの量は約±2.5%の範囲であった。
【0067】
ヘマトクリットレベルが決定したら、その結果を図6の電流対約9秒〜約14秒の時間遷移の勾配と共に使用して、サンプル中のC反応性タンパク質の値を計算した。C反応性タンパク質のレベルを以下の等式で決定した:
【数11】

式中、COは、C反応性タンパク質の濃度であり、yは、前述の勾配及びヘマトクリットのレベルに基づく。より具体的には、yは、勾配へのヘマトクリットの影響を除去し、以下の等式によって計算した:
【数12】

式中、mは、電流対約9秒〜約14秒の時間遷移の勾配であり、Hは、決定されたヘマトクリットレベルである。図9は、血液サンプル各々の計算されたC反応性タンパク質のレベル対従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値のプロットを図示する。図9の最適合線は、決定されたC反応性タンパク質のレベルと、同等の参照値との間の正確な相関関係を図示する。
【0068】
(実施例2)
測定する電流量に基づき初期充填速度を測定するための電気化学システムの使用を、別の実施例によって更に示した。本実施例に使用したサンプル分析デバイスもまた、図2の免疫センサ110、電位を印加するように構成された計器、及び初期充填速度を決定するように構成された制御ユニットであった。特に、電位を、免疫センサ110の電極に印加し、ヘマトクリットのレベルを決定し、次いで、電位を逆転させた。分析物の濃度を、決定されたヘマトクリットのレベルを考慮して、その後決定した。前述の実施例と同様に、異なるヘマトクリットレベルを有する多くのサンプルを、システムの能力を実証するために、システムと共に使用した。ヘマトクリット濃度の既知のレベルは、約33.5%、約41%、約47.5%、及び約56.5%であった。
【0069】
サンプルを、毛管現象により、未加熱の免疫センサに導入した。サンプルは、充填チャンバーに進入し、反応チャンバーに移動し、そこで約5分間、滞留した。第1の封止用構成要素を穿孔することによって、免疫センサの通気孔を、その後開口し、それによって、免疫センサ内に配設されたサンプルの血液が免疫センサの反応チャンバーから免疫センサの検出チャンバーへの流動するのを可能にした。封止用構成要素のうちの少なくとも1つを穿孔する前に、サンプルをより長い時間待機させることによって、特に未加熱の反応チャンバーを考慮して、免疫センサの抗原及び抗体酵素複合体が拡散し反応するのに十分な時間を提供した。上記の実施例1に示すとおり、免疫センサを予熱することで、この時間を速めることができる。しかしながら、本実施例において、加熱要素は含まれず、それは、システムに加熱要素を組み込むことに付随した複雑な問題及び費用を除去する利点をもたらした。しかしながら、チャンバーの温度が不明又は一定ではないそのような例では、ヘマトクリットのレベル及び/又はC反応性タンパク質のレベルを決定するために実行する計算は、より正確な結果を提供するために、異なる周辺温度の影響を明らかにしなければならない。そのような計算法を、この第2の実施例に提供した。一実施形態では、サンプルの温度を推測することができる。
【0070】
以前の実施例と同様に、血液が検出チャンバーに進入し始めると、約300mVの電位を、計器により約4秒間、電極に印加した。その後、電位を約10秒間、中断し逆転させた。得られた電流対時間遷移のプロットを、図6に図示したプロットと同様の方法で作製した。得られたプロットから、ヘマトクリットのレベルを電位の第1の印加中の初期電流から決定した。その後、C反応性タンパク質のレベルを、電位の逆転後に計算した。計算されたC反応性タンパク質のレベルは、電流対時間プロットの勾配、及び決定されたヘマトクリットのレベルに基づいた。本実施例の温度を明らかにすることによって、以下に示すとおり、更なる精度を提供した。
【0071】
各サンプル用に決定された初期電流を、図10に図示する。図10は、サンプルが配設された免疫センサの検出チャンバーの決定された初期電流対温度のプロットを図示する。4つの種類のサンプル(即ち、4つの異なるレベルのヘマトクリット)の初期電流を、約20℃〜約37℃の範囲にわたり、測定した。一般的に、ヘマトクリットのより高いレベルは、初期電流のより低い絶対値をもたらした。チャンバー内の温度が上昇すると、初期電流の絶対値も通常上昇した。示すとおり、初期電流は、ヘマトクリットが固定されたときに、温度と線形的に異なった。チャンバーの温度及び初期電流を考慮して、ヘマトクリットのレベルを以下の等式によって決定した:
【数13】

式中、Hは、ヘマトクリットのレベルであり、
【数14】

は、初期電流であり、Tは、検出チャンバーの温度である。以前の実施例と同様に、図11に示すとおり、ヘマトクリットの予測レベルにおける誤差は、約±5%以内であった。図11は、各試験サンプル対そのサンプルの参照ヘマトクリットレベルに存在した誤差割合をプロットする。やはり以前の実施例と同様に、いくつかの実施形態において、ヘマトクリット値の決定のみが行われ、それによって、ヘマトクリット値の決定値に基づき評価することができる、様々な医学的状態の迅速な評価が可能になる。
【0072】
ヘマトクリットレベルが決定したら、その結果を電流対約9秒〜約14秒の時間遷移の勾配及び検出チャンバーの温度と共に使用して、サンプル中のC反応性タンパク質の値を計算した。C反応性タンパク質のレベルを以下の等式によって決定した:
【数15】

式中、COは、C反応性タンパク質の濃度であり、y’は、検出チャンバーの温度及び変数に基づき、それがひいては前述の勾配及びヘマトクリットのレベルに基づく。より具体的には、y’は、勾配への温度の影響を除去し、以下の等式によって計算した:
【数16】

式中、Tは、免疫センサの検出チャンバーの温度であり、yは、勾配へのヘマトクリットの影響を除去する条件である。y’に対する等式は、勾配が、約1℃毎の温度の変化に対して、一定の割合、典型的に約4〜約7パーセントの範囲で変化すると仮定する。更に、条件T−25は、y’のすべての値を25℃の標準温度に修正する。異なる温度を修正しなければならない場合、この条件は、適宜に調整することができる。実際に、他のサンプル、温度等のために、この等式及びこの開示全体に開示される他の等式をうまく利用するための多くの方法が、当業者には理解されるであろう。
【0073】
変数yを以下の等式によって計算した:
【数17】

式中、mは、電流対約9秒〜約14秒の時間遷移の勾配であり、Hは、決定されたヘマトクリットレベルである。条件(1−0.01H)は、次いで任意電力まで上昇される、血漿である容量の一部を表す。電力を較正係数として得ることができる。
【0074】
ほぼ、約9秒〜約14秒の遷移の勾配は、C反応性タンパク質、ヘマトクリットレベル、及び温度の関数である。C反応性タンパク質の濃度が約0.15mg/Lに固定されたときに、図12に示すとおり、ヘマトクリット及び温度に対する勾配のかなりの変動が依然として存在した。図12は、サンプルが配設された免疫センサの検出チャンバーの決定された勾配対温度のプロットを図示する。4つのヘマトクリットレベルのサンプルの各々の初期電流を、約20℃〜約37℃の範囲にわたり、測定した。一般的に、サンプル中のヘマトクリットのレベルが大きいほど、勾配の値は小さくなる。チャンバー内の温度が上昇すると、勾配の値は、通常上昇した。
【0075】
図13は、約33.5%又は約47.5%のいずれかのヘマトクリットレベルを有するサンプル各々の計算されたC反応性タンパク質レベル対従来の酵素イムノアッセイによって決定される血漿C反応性タンパク質の参照値のプロットを図示する。図13の最適合線は、決定されたC反応性タンパク質のレベルと、同等の参照値との間の正確な相関関係を図示する。
【0076】
これらの2つの実施例は、本明細書に含まれる教示をどのように実行し、かつ使用することができるかという、多くの実施例のうちの2つにすぎないことは、当業者には理解されよう。更に、本明細書に開示する方法、システム、及びデバイスは、血液サンプルの分析物の濃度を決定する工程と併せて主に使用され、血液サンプル中の異なるレベルのヘマトクリットから生じる場合がある誤差を明らかにする工程に主に焦点を置くが、本明細書に含まれる開示は、分析物を含有する様々な他のサンプルのために使用することもでき、サンプル内に含有される様々な抗原及び/又は抗体に対して試験することができることは、当業者には理解されよう。
【0077】
様々な方法、システム、デバイスが特定の等式に頼るという点では、提供される等式は、一般的に、等式が適用された実施例に基づくことも、当業者には理解されよう。本開示を考慮して、本発明の範囲から逸脱することなく、他の状況に対して、開示した等式を調整することは、当業者には可能であろう。
【0078】
更に、濃度を決定する工程並びにシステム及びデバイスを使用する工程に関する方法等の本明細書に論じる方法は、指示される場所を除き、特定の工程又は工程の順序によっても制限されない。当業者には、それらの方法を実施することができる様々な順序が理解され、また、それらの工程が本発明の範囲から逸脱することなく修正又は追加されることができることは、理解されよう。
【0079】
本明細書に開示する方法を使用することができる、他の種類のデバイスのいくつかの非限定的な例が、「Electrochemical Method」と題され1997年5月7日に出願されたHodgesらの米国特許第5,942,102号、「Electrochemical Cell」と題され1999年5月18日に出願されたHodgesらの米国特許第6,174,420号、「Sensor Connection Means」と題され1999年9月20日に出願されたChambersらの米国特許第6,379,513号、「Heated Electrochemical Cell」と題され2000年9月11日に出願されたHodgesらの米国特許第6,475,360号、「Hemoglobin Sensor」と題され2000年7月14日に出願されたHodgesらの米国特許第6,632,349号、「Antioxidant Sensor」と題され2000年7月14日に出願されたHodgesらの米国特許第6,638,415号、「Method of Forming an Electrical Connection Between an Electrochemical Cell and a Meter」と題され2002年12月9日に出願されたHodgesらの米国特許第6,946,067号、「Method of Preventing Short Sampling of a Capillary or Wicking Fill Device」と題され2003年4月3日に出願されたHodgesらの米国特許第7,043,821号、及び「Electrochemical Cell」と題され2002年10月1日に出願されたHodgesらの米国特許第7,431,820号において、より詳細に論じられており、これらの各々は、参照によって、その全体が本願に組み込まれる。
【0080】
更に、特定の構成を有するデバイスと共に使用するための本明細書における開示について論じる限りにおいて、任意の数の構成が使用されることができる。例えば、本開示と共に使用され得るいくつかの構成は、互いに面する2つの電極を有するセンサ、同じ平面上に2つの電極を有するセンサ、及び3つの電極を有し、それらの電極のうちの2つが対向し、それらの電極のうちの2つが同じ平面上にあるセンサを含む。これらの異なる構成は、免疫センサを含む任意のデバイス及び他の前述のデバイス内で生じることができる。
【0081】
デバイス、システム、及び方法の様々な態様は、本発明の範囲から逸脱することなく、様々な決定値に関して、必要に応じて、適合させる及び変更することができる。更に、上述の実施形態に基づいた本発明の更なる特徴及び利点が、当業者には理解されよう。したがって、本発明は、添付の請求項に示された内容を除き、本明細書に特に示され記述されたものに限定されることはない。本明細書に記載の全ての参考文献は、その全体が参照により本明細書に明示的に組み込まれる。
【特許請求の範囲】
【請求項1】
全血サンプルのヘマトクリット値を決定するための方法において、
全血サンプルを、毛管空隙を有するサンプル分析デバイスに提供する工程と、
前記毛管空隙の少なくとも一部分内の前記サンプルの初期充填速度を測定する工程と、
前記初期充填速度から前記サンプルのヘマトクリット値を決定する工程と、
を含む、方法。
【請求項2】
前記サンプルの初期充填速度を測定する工程が、
電位を印加する工程と、
電流を測定する工程と、
初期電流量を決定する工程と、
を更に含む、請求項1に記載の方法。
【請求項3】
初期充填速度を測定する工程が、
約10ミリ秒毎に少なくとも約50ミリ秒間電流測定を実施する工程と、
前記電流測定値に基づき平均電流を計算する工程と、
を更に含む、請求項2に記載の方法。
【請求項4】
前記サンプルの初期充填速度を測定する工程が、光信号を検出する工程を更に含む、請求項1に記載の方法。
【請求項5】
前記サンプルの初期充填速度を測定する工程が、前記サンプルが前記毛管空隙に進入した直後に生じる、請求項1に記載の方法。
【請求項6】
前記サンプルの初期充填速度を測定する工程が、前記サンプルが、検出信号が生成される前記サンプル分析デバイスの前記毛管空隙の領域内に横断した後に生じる、請求項1に記載の方法。
【請求項7】
前記サンプルの温度を測定する工程、又は前記サンプルの温度を推測する工程のうちの少なくとも1つを更に含む、請求項1に記載の方法。
【請求項8】
前記サンプル分析デバイスが、免疫センサである、請求項1に記載の方法。
【請求項9】
前記サンプルが、分析物を含み、前記方法が、
前記決定されたヘマトクリット値を考慮して、前記分析物の濃度を計算する工程を更に含む、請求項1に記載の方法。
【請求項10】
電位を印加する工程と、
前記電位を印加した後の初期電流を測定する工程と、
前記電位を逆転させる工程と、
を更に含む、請求項9に記載の方法。
【請求項11】
前記電位を逆転させる工程後、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を測定する工程は、前記一定期間の電流の前記変化を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項10に記載の方法。
【請求項12】
前記サンプルの温度を測定する工程、又は前記サンプルの温度を推測する工程のうちの少なくとも1つを更に含む、請求項10に記載の方法。
【請求項13】
前記電位を逆転させる工程の後に、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を測定する工程は、一定期間の電流の前記変化及び前記サンプルの前記温度を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項12に記載の方法。
【請求項14】
サンプル中の分析物の濃度を決定するための方法において、
分析物を含むサンプルを、作用電極及び対電極を有するサンプル分析デバイスに提供する工程と、
前記作用電極と前記対電極との間に電位を印加する工程と、
前記サンプルの初期充填速度を決定する工程と、
前記初期充填速度を考慮して、前記分析物の濃度を計算する工程と、
を含む、方法。
【請求項15】
初期充填速度を決定する工程が、
前記電位を印加した後の初期電流を測定する工程と、
前記サンプル中のヘマトクリットのレベルを決定する工程と、
前記作用電極と前記対電極との間の前記電位を逆転させる工程と、
を更に含む、請求項14に記載の方法。
【請求項16】
前記分析物の前記濃度を計算する工程が、前記決定されたヘマトクリットのレベルに基づき、前記濃度を算定する工程を更に含む、請求項15に記載の方法。
【請求項17】
前記電位を逆転させる工程後、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を計算する工程は、前記一定期間の電流における前記変化を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項16に記載の方法。
【請求項18】
前記サンプルが、全血を含み、前記方法が、前記全血の温度を測定する工程、又は前記全血の温度を推測する工程のうちの少なくとも1つを更に含む、請求項16に記載の方法。
【請求項19】
初期充填速度を決定する工程が、前記初期充填速度を計算するために、光信号における変化率を決定する工程を更に含む、請求項14に記載の方法。
【請求項20】
初期充填速度を決定する工程が、前記初期充填速度を決定するために、初期電流量を決定する工程を更に含む、請求項14に記載の方法。
【請求項21】
初期電流量を決定する工程が、
約10ミリ秒毎に少なくとも約50ミリ秒間電流測定を実施する工程と、
前記電流測定値に基づき平均電流を計算する工程と、
を更に含む、請求項20に記載の方法。
【請求項22】
初期充填速度を決定する工程が、前記サンプルが、前記サンプル分析デバイスの毛管空隙に進入した直後の初期充填速度を決定する工程を更に含む、請求項14に記載の方法。
【請求項23】
初期充填速度を決定する工程が、前記サンプルが、検出信号が生成される前記サンプル分析装置の毛管空隙の領域内に横断した後の初期充填速度を決定する工程を更に含む、請求項14に記載の方法。
【請求項24】
前記サンプル分析デバイスが、免疫センサを含む、請求項14に記載の方法。
【請求項25】
前記電位を逆転させる工程後、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を計算する工程は、前記一定期間の電流における前記変化を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項18に記載の方法。
【請求項26】
下部電極及び上部電極を有する免疫センサと、
前記免疫センサの前記下部電極と前記上部電極との間に電位を印加するように構成された計器と、
前記計器に接続された制御ユニットであって、前記制御ユニットは、前記免疫センサ内に導入されたサンプルの初期充填速度を測定し、前記初期充填速度を使用して、前記サンプルが血液であるときの前記サンプルのヘマトクリット値、及び前記サンプル中の分析物の濃度のうちの少なくとも1つを計算するような、制御ユニットと、
を含む、電気化学システム。
【請求項27】
前記免疫センサの少なくとも一部分を加熱するように構成された加熱要素を更に含む、請求項26に記載の電気化学システム。
【請求項28】
前記免疫センサが、
緩衝液中の酵素と抱合した抗体を含む第1の液体試薬であって、前記下部電極上に縞模様に付けられ、乾燥された、第1の液体試薬と、
フェリシアン化物と、前記酵素のための基質と、希酸溶液中のメディエータとを含む第2の液体試薬であって、前記下部電極上に縞模様に付けられ、乾燥された、第2の液体試薬と、
抗原と抱合した磁気ビーズであって、前記上部電極上に縞模様に付けられ、その上で乾燥された、磁気ビーズと、
前記下部電極と上部電極との間に配設されたセパレータと、
前記セパレータ内に形成された反応チャンバーであって、前記第1の試薬、及び前記抗原と抱合した前記磁気ビーズがその中に配設された、反応チャンバーと、
前記セパレータ内に形成された検出チャンバーであって、前記第2の試薬がその中に配設された検出チャンバーと、
前記セパレータ、並びに前記下部電極及び上部電極の一方に少なくとも部分的に形成され、前記検出チャンバーからある距離だけ離間され、前記反応チャンバーの少なくとも一部分に重なり合う充填チャンバーと、
前記セパレータ、前記下部電極、及び前記上部電極の各々に少なくとも部分的に形成され、前記反応チャンバーからある距離だけ離間され、前記検出チャンバーの少なくとも一部分に重なり合う通気孔と、
前記下部電極及び上部電極のうちの一方に取り付けられ、前記通気孔の上に配設され、前記充填チャンバーの壁を形成すると共に前記通気孔を封止するように構成された、組み込まれた抗凝固剤を有する第1の封止用構成要素と、
前記下部電極及び上部電極のうちのもう一方に取り付けられ、前記通気孔の上に配設され、前記通気孔を封止するように構成された、第2の封止用構成要素と、
を更に含む、請求項26に記載の電気化学システム。
【請求項29】
前記第1の封止用構成要素が、親水性接着テープを含む、請求項28に記載の電気化学システム。
【請求項30】
前記制御ユニットが、前記サンプルの前記初期充填速度を測定するために、光信号における変化率を測定するように構成された光信号検出器を更に含む、請求項28に記載の電気化学システム。
【請求項31】
前記制御ユニットが、前記初期充填速度を測定するために、初期電流量を測定するように構成された電流量検出器を更に含む、請求項28に記載の電気化学システム。
【請求項32】
前記制御ユニットが、前記サンプルが、前記免疫センサの毛管空隙に進入した直後の前記サンプルの前記初期充填速度を測定するための構成を含む、請求項28に記載の電気化学システム。
【請求項33】
前記制御ユニットが、前記サンプルが、検出信号が生成される前記免疫センサの毛管空隙の領域内に横断した後の前記サンプルの初期充填速度を測定するための構成を含む、請求項28に記載の電気化学システム。
【請求項34】
前記免疫センサ、前記計器、及び前記制御ユニットのうちの少なくとも1つが、前記サンプルの温度を測定する機能、又は前記サンプルの温度を推測する機能のうちの少なくとも1つを実施するように構成される、請求項28に記載の電気化学システム。
【請求項1】
全血サンプルのヘマトクリット値を決定するための方法において、
全血サンプルを、毛管空隙を有するサンプル分析デバイスに提供する工程と、
前記毛管空隙の少なくとも一部分内の前記サンプルの初期充填速度を測定する工程と、
前記初期充填速度から前記サンプルのヘマトクリット値を決定する工程と、
を含む、方法。
【請求項2】
前記サンプルの初期充填速度を測定する工程が、
電位を印加する工程と、
電流を測定する工程と、
初期電流量を決定する工程と、
を更に含む、請求項1に記載の方法。
【請求項3】
初期充填速度を測定する工程が、
約10ミリ秒毎に少なくとも約50ミリ秒間電流測定を実施する工程と、
前記電流測定値に基づき平均電流を計算する工程と、
を更に含む、請求項2に記載の方法。
【請求項4】
前記サンプルの初期充填速度を測定する工程が、光信号を検出する工程を更に含む、請求項1に記載の方法。
【請求項5】
前記サンプルの初期充填速度を測定する工程が、前記サンプルが前記毛管空隙に進入した直後に生じる、請求項1に記載の方法。
【請求項6】
前記サンプルの初期充填速度を測定する工程が、前記サンプルが、検出信号が生成される前記サンプル分析デバイスの前記毛管空隙の領域内に横断した後に生じる、請求項1に記載の方法。
【請求項7】
前記サンプルの温度を測定する工程、又は前記サンプルの温度を推測する工程のうちの少なくとも1つを更に含む、請求項1に記載の方法。
【請求項8】
前記サンプル分析デバイスが、免疫センサである、請求項1に記載の方法。
【請求項9】
前記サンプルが、分析物を含み、前記方法が、
前記決定されたヘマトクリット値を考慮して、前記分析物の濃度を計算する工程を更に含む、請求項1に記載の方法。
【請求項10】
電位を印加する工程と、
前記電位を印加した後の初期電流を測定する工程と、
前記電位を逆転させる工程と、
を更に含む、請求項9に記載の方法。
【請求項11】
前記電位を逆転させる工程後、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を測定する工程は、前記一定期間の電流の前記変化を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項10に記載の方法。
【請求項12】
前記サンプルの温度を測定する工程、又は前記サンプルの温度を推測する工程のうちの少なくとも1つを更に含む、請求項10に記載の方法。
【請求項13】
前記電位を逆転させる工程の後に、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を測定する工程は、一定期間の電流の前記変化及び前記サンプルの前記温度を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項12に記載の方法。
【請求項14】
サンプル中の分析物の濃度を決定するための方法において、
分析物を含むサンプルを、作用電極及び対電極を有するサンプル分析デバイスに提供する工程と、
前記作用電極と前記対電極との間に電位を印加する工程と、
前記サンプルの初期充填速度を決定する工程と、
前記初期充填速度を考慮して、前記分析物の濃度を計算する工程と、
を含む、方法。
【請求項15】
初期充填速度を決定する工程が、
前記電位を印加した後の初期電流を測定する工程と、
前記サンプル中のヘマトクリットのレベルを決定する工程と、
前記作用電極と前記対電極との間の前記電位を逆転させる工程と、
を更に含む、請求項14に記載の方法。
【請求項16】
前記分析物の前記濃度を計算する工程が、前記決定されたヘマトクリットのレベルに基づき、前記濃度を算定する工程を更に含む、請求項15に記載の方法。
【請求項17】
前記電位を逆転させる工程後、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を計算する工程は、前記一定期間の電流における前記変化を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項16に記載の方法。
【請求項18】
前記サンプルが、全血を含み、前記方法が、前記全血の温度を測定する工程、又は前記全血の温度を推測する工程のうちの少なくとも1つを更に含む、請求項16に記載の方法。
【請求項19】
初期充填速度を決定する工程が、前記初期充填速度を計算するために、光信号における変化率を決定する工程を更に含む、請求項14に記載の方法。
【請求項20】
初期充填速度を決定する工程が、前記初期充填速度を決定するために、初期電流量を決定する工程を更に含む、請求項14に記載の方法。
【請求項21】
初期電流量を決定する工程が、
約10ミリ秒毎に少なくとも約50ミリ秒間電流測定を実施する工程と、
前記電流測定値に基づき平均電流を計算する工程と、
を更に含む、請求項20に記載の方法。
【請求項22】
初期充填速度を決定する工程が、前記サンプルが、前記サンプル分析デバイスの毛管空隙に進入した直後の初期充填速度を決定する工程を更に含む、請求項14に記載の方法。
【請求項23】
初期充填速度を決定する工程が、前記サンプルが、検出信号が生成される前記サンプル分析装置の毛管空隙の領域内に横断した後の初期充填速度を決定する工程を更に含む、請求項14に記載の方法。
【請求項24】
前記サンプル分析デバイスが、免疫センサを含む、請求項14に記載の方法。
【請求項25】
前記電位を逆転させる工程後、一定期間にわたって、電流の変化を測定する工程を更に含み、前記分析物の濃度を計算する工程は、前記一定期間の電流における前記変化を考慮して、前記分析物の前記濃度を計算する工程を更に含む、請求項18に記載の方法。
【請求項26】
下部電極及び上部電極を有する免疫センサと、
前記免疫センサの前記下部電極と前記上部電極との間に電位を印加するように構成された計器と、
前記計器に接続された制御ユニットであって、前記制御ユニットは、前記免疫センサ内に導入されたサンプルの初期充填速度を測定し、前記初期充填速度を使用して、前記サンプルが血液であるときの前記サンプルのヘマトクリット値、及び前記サンプル中の分析物の濃度のうちの少なくとも1つを計算するような、制御ユニットと、
を含む、電気化学システム。
【請求項27】
前記免疫センサの少なくとも一部分を加熱するように構成された加熱要素を更に含む、請求項26に記載の電気化学システム。
【請求項28】
前記免疫センサが、
緩衝液中の酵素と抱合した抗体を含む第1の液体試薬であって、前記下部電極上に縞模様に付けられ、乾燥された、第1の液体試薬と、
フェリシアン化物と、前記酵素のための基質と、希酸溶液中のメディエータとを含む第2の液体試薬であって、前記下部電極上に縞模様に付けられ、乾燥された、第2の液体試薬と、
抗原と抱合した磁気ビーズであって、前記上部電極上に縞模様に付けられ、その上で乾燥された、磁気ビーズと、
前記下部電極と上部電極との間に配設されたセパレータと、
前記セパレータ内に形成された反応チャンバーであって、前記第1の試薬、及び前記抗原と抱合した前記磁気ビーズがその中に配設された、反応チャンバーと、
前記セパレータ内に形成された検出チャンバーであって、前記第2の試薬がその中に配設された検出チャンバーと、
前記セパレータ、並びに前記下部電極及び上部電極の一方に少なくとも部分的に形成され、前記検出チャンバーからある距離だけ離間され、前記反応チャンバーの少なくとも一部分に重なり合う充填チャンバーと、
前記セパレータ、前記下部電極、及び前記上部電極の各々に少なくとも部分的に形成され、前記反応チャンバーからある距離だけ離間され、前記検出チャンバーの少なくとも一部分に重なり合う通気孔と、
前記下部電極及び上部電極のうちの一方に取り付けられ、前記通気孔の上に配設され、前記充填チャンバーの壁を形成すると共に前記通気孔を封止するように構成された、組み込まれた抗凝固剤を有する第1の封止用構成要素と、
前記下部電極及び上部電極のうちのもう一方に取り付けられ、前記通気孔の上に配設され、前記通気孔を封止するように構成された、第2の封止用構成要素と、
を更に含む、請求項26に記載の電気化学システム。
【請求項29】
前記第1の封止用構成要素が、親水性接着テープを含む、請求項28に記載の電気化学システム。
【請求項30】
前記制御ユニットが、前記サンプルの前記初期充填速度を測定するために、光信号における変化率を測定するように構成された光信号検出器を更に含む、請求項28に記載の電気化学システム。
【請求項31】
前記制御ユニットが、前記初期充填速度を測定するために、初期電流量を測定するように構成された電流量検出器を更に含む、請求項28に記載の電気化学システム。
【請求項32】
前記制御ユニットが、前記サンプルが、前記免疫センサの毛管空隙に進入した直後の前記サンプルの前記初期充填速度を測定するための構成を含む、請求項28に記載の電気化学システム。
【請求項33】
前記制御ユニットが、前記サンプルが、検出信号が生成される前記免疫センサの毛管空隙の領域内に横断した後の前記サンプルの初期充填速度を測定するための構成を含む、請求項28に記載の電気化学システム。
【請求項34】
前記免疫センサ、前記計器、及び前記制御ユニットのうちの少なくとも1つが、前記サンプルの温度を測定する機能、又は前記サンプルの温度を推測する機能のうちの少なくとも1つを実施するように構成される、請求項28に記載の電気化学システム。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2011−137816(P2011−137816A)
【公開日】平成23年7月14日(2011.7.14)
【国際特許分類】
【出願番号】特願2010−285718(P2010−285718)
【出願日】平成22年12月22日(2010.12.22)
【出願人】(596159500)ライフスキャン・インコーポレイテッド (100)
【氏名又は名称原語表記】Lifescan,Inc.
【住所又は居所原語表記】1000 Gibraltar Drive,Milpitas,California 95035,United States of America
【Fターム(参考)】
【公開日】平成23年7月14日(2011.7.14)
【国際特許分類】
【出願日】平成22年12月22日(2010.12.22)
【出願人】(596159500)ライフスキャン・インコーポレイテッド (100)
【氏名又は名称原語表記】Lifescan,Inc.
【住所又は居所原語表記】1000 Gibraltar Drive,Milpitas,California 95035,United States of America
【Fターム(参考)】
[ Back to top ]

