包摂マトリックスを用いたMALDI法
【課題】通常マトリックス剤としては、固体の有機酸が用いられ、このマトリックス剤の分子量が大体500Da以下であることから、500Da以下の質量領域には、マトリックス由来の多数のピークが存在しており、500Da以下の分子量を持つ測定対象試料は、測定できないという欠点があった。本願発明の課題は、マトリックスが存在するにも関わらず、マトリックスの本体のピーク及びフラグメントのピークを抑制して、測定試料の明瞭なピークを検出する方法を提供することである。
【解決手段】本願発明は、包摂特性を有する分子(ホスト分子)に従来のマトリックス剤(例えば、DHB、CHCA、FA、SA又はTHAP)をゲストとして包摂させることにより、マトリックス由来のピークを完全に消去した。
【解決手段】本願発明は、包摂特性を有する分子(ホスト分子)に従来のマトリックス剤(例えば、DHB、CHCA、FA、SA又はTHAP)をゲストとして包摂させることにより、マトリックス由来のピークを完全に消去した。
【発明の詳細な説明】
【技術分野】
【0001】
本願発明は、質量分析、特に、マトリックス支援レーザー脱離イオン化質量分析法(MALDI−MS(Matrix Assisted Laser Desorption/Ionization-Mass Spectrometry))に関する。
【背景技術】
【0002】
レーザー脱離-質量分析法(Laser Desorption Mass Spectrometry:LD-MS)は、1980年代に注目され、主に金属や半導体などの表面分析に用いられてきた。レーザーを用いているため、レンズを用いて容易に集光が可能であり、微小領域の分析が可能である。
【0003】
しかしながら、イオン化効率が低く、また、目的分子を解離させてしまうなどの欠点を持っており、巨大分子の測定が不可能とされていた。
【0004】
そのような背景の中、たんぱく質などの巨大分子を分析する手法の一つとして、2002年のノーベル化学賞受賞者である田中耕一氏が開発したMALDI―TOF―MS(マトリックス支援レーザー脱離-飛行時間型-質量分析)測定装置が注目を浴びている。
【0005】
MALDI法の最大の特徴は、試料に対してマトリックスと総称される化合物を大過剰(百倍から千倍)に混合し、混晶状態とした試料を用いることである。大過剰に混合されたマトリックス分子は、レーザーエネルギーを吸収することにより熱エネルギー(ミクロには振動エネルギー)に変換するため、照射レーザー(MALDI法では一般的に数ns程度のパルス幅が用いられる)の到達領域(深さ:数μm、径:数100μm)に含まれるマトリックス分子の一部が、パルス幅が数nsという短パルスレーザーの照射により急速加熱され、気化あるいは昇華される。
【0006】
このMALDI法を飛行時間型の質量分析装置TOF-MSと組み合わせたMALDI-TOF-MSには以下の利点が存在する。
(1)150万Da(ダルトン=原子質量単位)の高分子まで測定可能である。
(2)10-5から10-6といった精度で質量分析ができるため、分子量だけで分子構造の推定も可能である。
(3)不純物の混入に寛容である。
(4)一価のチャージを持ったイオンだけが基本的に測れるのでスペクトルがシンプルである。
(5)装置が簡単である。
【0007】
このように、MALDI−MSは、非常に有用な技術であるが、欠点の一つとして上げられるのが、マトリックス剤のフラグメントピークである。通常マトリックス剤は、固体の有機酸が用いられ、この分子量が大体500Da以下であることから、500Da以下の質量領域には、マトリックス由来の多数のピークが存在し、例えば500Da以下の分子量を持つ測定対象試料は、測定できないという欠点があった。
【0008】
これまでに低分子量分子をMALDI法により測定する試みとしては、金などの金属及び金属酸化物微粒子を混入させる方法がある(下記非特許文献1参照)。しかし、この方法は、金属微粒子と測定対象試料を「同居」させるために流動パラフィンなどを用いる必要があり、レーザーパワーを上げると結果的に流動パラフィンなどのフラグメント成分が多数検出されてしまうという欠点がある。
【0009】
また、ポーラスシリコン基板を用いる方法も報告されている(下記非特許文献2参照)。しかしながら、この方法は、感度が絶対的に弱いという欠点がある。
【0010】
また、ナノ構造基板を用いる方法もある(下記非特許文献3参照)。しかしながら、この方法は、感度が弱いこと及びこの方法に適する分子が限られる点に欠点を有している。
【0011】
また、IR-UV光同時照射による方法も知られている(下記非特許文献4参照)。しかしながら、この方法は、低分子量領域を有効的に消せるが、赤外光源として自由電子レーザーを用いており、装置自体が非常に大掛かりであり汎用性はない。
【0012】
さらに、MALDI法を用いて低分子量の質量を測る手法として、測定対象試料(測りたい分子)+分子量の大きいマトリックスの複合体(コンプレックス)のマスピークを観測して、マトリックス由来のピークが多く出る領域から避ける手法がある(下記非特許文献5参照)。
【0013】
上記手法に基づく実験において、βシクロデキストリンを用いて行っている。測定対象試料RDX(hexahydro1,3,5-trinitro-1,3,5-triazine)をβシクロデキストリン中に入れたものを、新たに測定対象試料と考えて、この試料を、シナピン酸(SA)をマトリックスとしてMALDI-MS測定を行った。結果として、βCD(RDX) + SA のピークを観測して、SA関連のピークが多数出る領域からRDXのピークを移動させて測定した。
【0014】
この手法の欠点は、結果としてSAをそのままマトリックス剤として用いているため、マトリックスは、ソフトイオン化になっていない。このため通常のMALDIと同じように低分子量領域にマトリックス由来のピークが多数出ており、根本的な解決にはなっていない。
【非特許文献1】T. Kinumi, T. Saisu, M.Takayama, H. Niwa, J. Mass Spectrom. 35 (2000) 417-22.
【非特許文献2】R. Arakawa, Y. Shimomae, H.Morikawa, K. Ohara, S. Okuno, J. Mass Spectrom. 39 (2004) 961-65.)
【非特許文献3】H. Masuda, H. Yamada, M.Satoh, H. Asoh, M. Nakao, T. Tamamura, Appl. Phys. Lett. 71 (1997) 2770-72.
【非特許文献4】Y. Niito, S.Y. Suzuki, K.Ishii, K. Awazu, Nucl. Instrum. Meth. A 528 (2004) 614-18.
【非特許文献5】Min Zhang et al, J. Am. Soc.Mass Spectrom, 2006, 17, 189-193
【発明の開示】
【発明が解決しようとする課題】
【0015】
通常マトリックス剤としては、固体の有機酸が用いられ、このマトリックス剤の分子量が大体500Da以下であることから、500Da以下の質量領域には、マトリックス由来の多数のピークが存在しており、500Da以下の分子量を持つ測定対象試料は、測定できないという欠点があった。本願発明の課題は、マトリックスが存在するにも関わらず、マトリックスの本体のピーク及びフラグメントのピークを抑制して、測定試料の明瞭なピークを検出する方法を提供することである。
【課題を解決するための手段】
【0016】
本願発明は、包摂特性を有する分子(ホスト分子)に従来のマトリックス剤(例えば、DHB、CHCA、FA、SA又はTHAP)をゲストとして包摂させることにより、マトリックス由来のピークを完全に消去した。
【0017】
図1(a)に、ホスト分子としてよく知られているα−シクロデキストリン(以下「αCD」という。)の分子構造を示す。αCD分子の内部は、疎水性であり、外側は、親水性である。包摂される分子(ゲスト分子)の性質を安定化させる働きがある。例えば、揮発性物質を難揮発性にしたり、酸化されやすいものを耐酸化性にする働きがある。
【0018】
図1(b)に、αCDだけのLDI-MS (Laser Desorption Ionization)結果を示す。すなわち、ステンレス基板の上にαCDを滴下し(乾燥させ)、レーザー照射(266nm)によってイオン化し、質量分析したものである。αCDは、266 nmに吸光係数をほとんど持たないので、図から明らかなように、αCDのイオンは、観測されない。
【0019】
図2に、従来のマトリックスであるTHAP(2,4,6トリヒドロキシアセトフェノン、2,4,6trihydroxyacetophenone;168Da)の分子構造を示す。
【0020】
図3(a)に、このTHAPのLDI-MSスペクトルを示す。この図から明らかなように、THAPのLDIからは、プロトン付加体だけでなく、アルカリ金属イオン付加体、二量体、フラグメント(OHロス)が観測される。従って、従来のLDI法では、ソフトイオン化は実現できない。
【0021】
図3(b)に、THAPをαCDに包摂させたもののLDI-MSスペクトルを示す。この図から明らかなように、包摂された分子(THAP)のイオン強度が減少し、アルカリ金属が付着した際に生じるイオンが消え単純化されている。また非常にわずかなフラグメント(OHロス)ピークのみが検出されているにすぎず、αCDがソフトイオン化に効果があることが示されている。
【0022】
図4(a)に、参考のために、マトリックスとしてTHAP、測定対象試料としてポリペプチドのサブスタンスP(以下「SubP」という。)とした通常のMALDI-MSスペクトルを示す。励起光波長は266nmである。インセットには、親分子ピーク付近を拡大したものを示す。プロトン付加体のほかに、アルカリ金属イオンが付着したピークが確認できる。また500Da以下の領域では、マトリックスとして用いたTHAP関連のマスピークが多数存在している。従って、この領域に、サブスタンスP関連のピーク(フラグメント)があったとしても、判別は困難である。
【発明の効果】
【0023】
本願発明は、包摂特性を有する分子(ホスト分子)に従来のマトリックス剤(例えば、DHB、CHCA、FA、SA又はTHAP)を包摂させることにより、マトリックス由来のピークを完全に消去することができ、試料のみのピークを観測可能であり、雑音を極めて削除することに成功した。
【発明を実施するための最良の形態】
【0024】
以下に、本願発明を実施するための最良の形態を示す。
【実施例1】
【0025】
マトリックス剤として用いたTHAP及びCHCAは、試薬会社から購入し、メタノールで3回再結晶を行い純度の高い結晶を得た。
【0026】
包摂マトリックスの作成手順は、以下のとおりである。
まず、αCDを蒸留水に溶かして、10 mmoldm-3の溶液を作成する。
【0027】
次に、THAP(またはCHCA)を体積比にして7:3のアセトニトリル・水混合溶液に溶かし、約75 mmoldm-3の溶液を作成する。
【0028】
α-CD溶液(溶媒:水,10 mmol/l)120 μlとマトリックス溶液(溶媒:アセトニトリル/水=7/3にTFA(トリフルオロ酢酸)0.1%添加,60 mmol/l)20 μlをマイクロチューブに入れ攪拌,静置しα-CD:マトリックス=1:1(モル比)の溶液を得る。
【0029】
得られた溶液を試料台に0.5 μl滴下し,乾燥前にサンプル溶液(約0.5 μmol/l)0.5 μlを重ねて滴下後,乾燥させ測定した。
【0030】
このときのレーザーの照射条件は、Nd:YAGレーザー(NewWave Polaris ST,4 ns,10 Hz)の四倍波(266 nm)を使用し,照射パワー約10 μJ,レーザー径5 mmを約0.5mm(目視)に集光し測定を行った。
【0031】
図4(b)に、シクロデキストリン包摂マトリックスαCD(THAP)を新たにMALDI用のマトリックスとしてとらえ、SubPを測定対象試料としてMALDI-MSスペクトルを観測した例を示す。500Da以下の領域において、先に示したようなマトリックス由来のピーク強度・数が激減したことが分かる。また親分子の領域においても、アルカリ金属由来のマスピークが消え、プロトン付加体のピークのみが検出されていることがわかる。従って包摂マトリックスは、マトリックスのピークの単純化だけでなく、測定対象試料のピークの単純化も行う能力があることが分かる。
【0032】
上述においては、包摂マトリックス(ゲスト)としてTHAPを用いていたが、よりプロトン親和力の弱い分子CHCA(cyano-4-hydroxyl-cinnamic acid)(構造は、図5参照)をマトリックス剤として用いてみた。プロトン親和力が弱いためピーク強度の減少が見込まれる。
【0033】
図4(c)に、CHCAをシクロデキストリンに包摂させたαCD(CHCA)を使って、SubPのMALDI-MSスペクトルを観測した結果を示す。この図から明らかなように、完全にマトリックス由来のピークを消すことができた。
【0034】
また、図6に、試料として、N-Acetylchitobiose(分子量:424.5)を測定した結果を示す。図6の上段に、通常のMALDI法により測定した結果(マトリックス:THAP)を示す。この図から明らかなように、該試料のプロトン付加体は検出されず、試料のナトリウム付加体およびマトリックス(THAP)のプロトン付加体しか検出されなかった。
【0035】
図6の下段に、THAPをαCDにより包摂し、上記試料を測定した結果を示す。この図から明らかなように、試料関連のプロトン付加体およびアルカリ金属付加体は検出されず、マトリックス(THAP)のプロトン付加体しか検出されなかった。これは本願発明の方法においては、ナトリウムやカリウム付加体が検出されにくいことを示唆する結果である。
【図面の簡単な説明】
【0036】
【図1】(a)に包摂特性を有するα−シクロデキストリン(αCD)の分子構造を示す。(b)は、該αCDだけのLDI-MS (Laser Desorption Ionization)スペクトルを示す。
【図2】マトリックスであるTHAP(2,4,6トリヒドロキシアセトフェノン、2,4,6trihydroxyacetophenone;168Da)の分子構造を示す。
【図3】(a)にTHAPのLDI-MSスペクトルを示す。(b)にTHAPをαCDにより包摂させたもののLDI-MSスペクトルを示す。
【図4】(a)に、マトリックスとしてTHAP、測定対象試料としてポリペプチドのサブスタンスP(SubP)とした通常のMALDI-MSスペクトルを示す。(b)に、THAPをαCDにより包摂し、SubPを測定したMALDI-MSスペクトルを示す。(c)に、CHCAをαCDにより包摂し、SubPを測定したMALDI-MSスペクトルを示す。
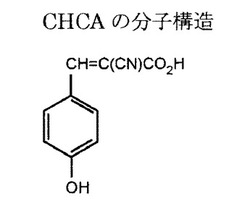
【図5】THAPよりプロトン親和力の弱いマトリックスであるCHCA構造式を示す。
【図6】上段に、マトリックスとしてTHAPを用い、試料として、N-Acetylchitobioseを通常のMALDI法により測定した結果を示す。下段に、THAPをαCDにより包摂し、上記試料を測定した結果を示す。
【技術分野】
【0001】
本願発明は、質量分析、特に、マトリックス支援レーザー脱離イオン化質量分析法(MALDI−MS(Matrix Assisted Laser Desorption/Ionization-Mass Spectrometry))に関する。
【背景技術】
【0002】
レーザー脱離-質量分析法(Laser Desorption Mass Spectrometry:LD-MS)は、1980年代に注目され、主に金属や半導体などの表面分析に用いられてきた。レーザーを用いているため、レンズを用いて容易に集光が可能であり、微小領域の分析が可能である。
【0003】
しかしながら、イオン化効率が低く、また、目的分子を解離させてしまうなどの欠点を持っており、巨大分子の測定が不可能とされていた。
【0004】
そのような背景の中、たんぱく質などの巨大分子を分析する手法の一つとして、2002年のノーベル化学賞受賞者である田中耕一氏が開発したMALDI―TOF―MS(マトリックス支援レーザー脱離-飛行時間型-質量分析)測定装置が注目を浴びている。
【0005】
MALDI法の最大の特徴は、試料に対してマトリックスと総称される化合物を大過剰(百倍から千倍)に混合し、混晶状態とした試料を用いることである。大過剰に混合されたマトリックス分子は、レーザーエネルギーを吸収することにより熱エネルギー(ミクロには振動エネルギー)に変換するため、照射レーザー(MALDI法では一般的に数ns程度のパルス幅が用いられる)の到達領域(深さ:数μm、径:数100μm)に含まれるマトリックス分子の一部が、パルス幅が数nsという短パルスレーザーの照射により急速加熱され、気化あるいは昇華される。
【0006】
このMALDI法を飛行時間型の質量分析装置TOF-MSと組み合わせたMALDI-TOF-MSには以下の利点が存在する。
(1)150万Da(ダルトン=原子質量単位)の高分子まで測定可能である。
(2)10-5から10-6といった精度で質量分析ができるため、分子量だけで分子構造の推定も可能である。
(3)不純物の混入に寛容である。
(4)一価のチャージを持ったイオンだけが基本的に測れるのでスペクトルがシンプルである。
(5)装置が簡単である。
【0007】
このように、MALDI−MSは、非常に有用な技術であるが、欠点の一つとして上げられるのが、マトリックス剤のフラグメントピークである。通常マトリックス剤は、固体の有機酸が用いられ、この分子量が大体500Da以下であることから、500Da以下の質量領域には、マトリックス由来の多数のピークが存在し、例えば500Da以下の分子量を持つ測定対象試料は、測定できないという欠点があった。
【0008】
これまでに低分子量分子をMALDI法により測定する試みとしては、金などの金属及び金属酸化物微粒子を混入させる方法がある(下記非特許文献1参照)。しかし、この方法は、金属微粒子と測定対象試料を「同居」させるために流動パラフィンなどを用いる必要があり、レーザーパワーを上げると結果的に流動パラフィンなどのフラグメント成分が多数検出されてしまうという欠点がある。
【0009】
また、ポーラスシリコン基板を用いる方法も報告されている(下記非特許文献2参照)。しかしながら、この方法は、感度が絶対的に弱いという欠点がある。
【0010】
また、ナノ構造基板を用いる方法もある(下記非特許文献3参照)。しかしながら、この方法は、感度が弱いこと及びこの方法に適する分子が限られる点に欠点を有している。
【0011】
また、IR-UV光同時照射による方法も知られている(下記非特許文献4参照)。しかしながら、この方法は、低分子量領域を有効的に消せるが、赤外光源として自由電子レーザーを用いており、装置自体が非常に大掛かりであり汎用性はない。
【0012】
さらに、MALDI法を用いて低分子量の質量を測る手法として、測定対象試料(測りたい分子)+分子量の大きいマトリックスの複合体(コンプレックス)のマスピークを観測して、マトリックス由来のピークが多く出る領域から避ける手法がある(下記非特許文献5参照)。
【0013】
上記手法に基づく実験において、βシクロデキストリンを用いて行っている。測定対象試料RDX(hexahydro1,3,5-trinitro-1,3,5-triazine)をβシクロデキストリン中に入れたものを、新たに測定対象試料と考えて、この試料を、シナピン酸(SA)をマトリックスとしてMALDI-MS測定を行った。結果として、βCD(RDX) + SA のピークを観測して、SA関連のピークが多数出る領域からRDXのピークを移動させて測定した。
【0014】
この手法の欠点は、結果としてSAをそのままマトリックス剤として用いているため、マトリックスは、ソフトイオン化になっていない。このため通常のMALDIと同じように低分子量領域にマトリックス由来のピークが多数出ており、根本的な解決にはなっていない。
【非特許文献1】T. Kinumi, T. Saisu, M.Takayama, H. Niwa, J. Mass Spectrom. 35 (2000) 417-22.
【非特許文献2】R. Arakawa, Y. Shimomae, H.Morikawa, K. Ohara, S. Okuno, J. Mass Spectrom. 39 (2004) 961-65.)
【非特許文献3】H. Masuda, H. Yamada, M.Satoh, H. Asoh, M. Nakao, T. Tamamura, Appl. Phys. Lett. 71 (1997) 2770-72.
【非特許文献4】Y. Niito, S.Y. Suzuki, K.Ishii, K. Awazu, Nucl. Instrum. Meth. A 528 (2004) 614-18.
【非特許文献5】Min Zhang et al, J. Am. Soc.Mass Spectrom, 2006, 17, 189-193
【発明の開示】
【発明が解決しようとする課題】
【0015】
通常マトリックス剤としては、固体の有機酸が用いられ、このマトリックス剤の分子量が大体500Da以下であることから、500Da以下の質量領域には、マトリックス由来の多数のピークが存在しており、500Da以下の分子量を持つ測定対象試料は、測定できないという欠点があった。本願発明の課題は、マトリックスが存在するにも関わらず、マトリックスの本体のピーク及びフラグメントのピークを抑制して、測定試料の明瞭なピークを検出する方法を提供することである。
【課題を解決するための手段】
【0016】
本願発明は、包摂特性を有する分子(ホスト分子)に従来のマトリックス剤(例えば、DHB、CHCA、FA、SA又はTHAP)をゲストとして包摂させることにより、マトリックス由来のピークを完全に消去した。
【0017】
図1(a)に、ホスト分子としてよく知られているα−シクロデキストリン(以下「αCD」という。)の分子構造を示す。αCD分子の内部は、疎水性であり、外側は、親水性である。包摂される分子(ゲスト分子)の性質を安定化させる働きがある。例えば、揮発性物質を難揮発性にしたり、酸化されやすいものを耐酸化性にする働きがある。
【0018】
図1(b)に、αCDだけのLDI-MS (Laser Desorption Ionization)結果を示す。すなわち、ステンレス基板の上にαCDを滴下し(乾燥させ)、レーザー照射(266nm)によってイオン化し、質量分析したものである。αCDは、266 nmに吸光係数をほとんど持たないので、図から明らかなように、αCDのイオンは、観測されない。
【0019】
図2に、従来のマトリックスであるTHAP(2,4,6トリヒドロキシアセトフェノン、2,4,6trihydroxyacetophenone;168Da)の分子構造を示す。
【0020】
図3(a)に、このTHAPのLDI-MSスペクトルを示す。この図から明らかなように、THAPのLDIからは、プロトン付加体だけでなく、アルカリ金属イオン付加体、二量体、フラグメント(OHロス)が観測される。従って、従来のLDI法では、ソフトイオン化は実現できない。
【0021】
図3(b)に、THAPをαCDに包摂させたもののLDI-MSスペクトルを示す。この図から明らかなように、包摂された分子(THAP)のイオン強度が減少し、アルカリ金属が付着した際に生じるイオンが消え単純化されている。また非常にわずかなフラグメント(OHロス)ピークのみが検出されているにすぎず、αCDがソフトイオン化に効果があることが示されている。
【0022】
図4(a)に、参考のために、マトリックスとしてTHAP、測定対象試料としてポリペプチドのサブスタンスP(以下「SubP」という。)とした通常のMALDI-MSスペクトルを示す。励起光波長は266nmである。インセットには、親分子ピーク付近を拡大したものを示す。プロトン付加体のほかに、アルカリ金属イオンが付着したピークが確認できる。また500Da以下の領域では、マトリックスとして用いたTHAP関連のマスピークが多数存在している。従って、この領域に、サブスタンスP関連のピーク(フラグメント)があったとしても、判別は困難である。
【発明の効果】
【0023】
本願発明は、包摂特性を有する分子(ホスト分子)に従来のマトリックス剤(例えば、DHB、CHCA、FA、SA又はTHAP)を包摂させることにより、マトリックス由来のピークを完全に消去することができ、試料のみのピークを観測可能であり、雑音を極めて削除することに成功した。
【発明を実施するための最良の形態】
【0024】
以下に、本願発明を実施するための最良の形態を示す。
【実施例1】
【0025】
マトリックス剤として用いたTHAP及びCHCAは、試薬会社から購入し、メタノールで3回再結晶を行い純度の高い結晶を得た。
【0026】
包摂マトリックスの作成手順は、以下のとおりである。
まず、αCDを蒸留水に溶かして、10 mmoldm-3の溶液を作成する。
【0027】
次に、THAP(またはCHCA)を体積比にして7:3のアセトニトリル・水混合溶液に溶かし、約75 mmoldm-3の溶液を作成する。
【0028】
α-CD溶液(溶媒:水,10 mmol/l)120 μlとマトリックス溶液(溶媒:アセトニトリル/水=7/3にTFA(トリフルオロ酢酸)0.1%添加,60 mmol/l)20 μlをマイクロチューブに入れ攪拌,静置しα-CD:マトリックス=1:1(モル比)の溶液を得る。
【0029】
得られた溶液を試料台に0.5 μl滴下し,乾燥前にサンプル溶液(約0.5 μmol/l)0.5 μlを重ねて滴下後,乾燥させ測定した。
【0030】
このときのレーザーの照射条件は、Nd:YAGレーザー(NewWave Polaris ST,4 ns,10 Hz)の四倍波(266 nm)を使用し,照射パワー約10 μJ,レーザー径5 mmを約0.5mm(目視)に集光し測定を行った。
【0031】
図4(b)に、シクロデキストリン包摂マトリックスαCD(THAP)を新たにMALDI用のマトリックスとしてとらえ、SubPを測定対象試料としてMALDI-MSスペクトルを観測した例を示す。500Da以下の領域において、先に示したようなマトリックス由来のピーク強度・数が激減したことが分かる。また親分子の領域においても、アルカリ金属由来のマスピークが消え、プロトン付加体のピークのみが検出されていることがわかる。従って包摂マトリックスは、マトリックスのピークの単純化だけでなく、測定対象試料のピークの単純化も行う能力があることが分かる。
【0032】
上述においては、包摂マトリックス(ゲスト)としてTHAPを用いていたが、よりプロトン親和力の弱い分子CHCA(cyano-4-hydroxyl-cinnamic acid)(構造は、図5参照)をマトリックス剤として用いてみた。プロトン親和力が弱いためピーク強度の減少が見込まれる。
【0033】
図4(c)に、CHCAをシクロデキストリンに包摂させたαCD(CHCA)を使って、SubPのMALDI-MSスペクトルを観測した結果を示す。この図から明らかなように、完全にマトリックス由来のピークを消すことができた。
【0034】
また、図6に、試料として、N-Acetylchitobiose(分子量:424.5)を測定した結果を示す。図6の上段に、通常のMALDI法により測定した結果(マトリックス:THAP)を示す。この図から明らかなように、該試料のプロトン付加体は検出されず、試料のナトリウム付加体およびマトリックス(THAP)のプロトン付加体しか検出されなかった。
【0035】
図6の下段に、THAPをαCDにより包摂し、上記試料を測定した結果を示す。この図から明らかなように、試料関連のプロトン付加体およびアルカリ金属付加体は検出されず、マトリックス(THAP)のプロトン付加体しか検出されなかった。これは本願発明の方法においては、ナトリウムやカリウム付加体が検出されにくいことを示唆する結果である。
【図面の簡単な説明】
【0036】
【図1】(a)に包摂特性を有するα−シクロデキストリン(αCD)の分子構造を示す。(b)は、該αCDだけのLDI-MS (Laser Desorption Ionization)スペクトルを示す。
【図2】マトリックスであるTHAP(2,4,6トリヒドロキシアセトフェノン、2,4,6trihydroxyacetophenone;168Da)の分子構造を示す。
【図3】(a)にTHAPのLDI-MSスペクトルを示す。(b)にTHAPをαCDにより包摂させたもののLDI-MSスペクトルを示す。
【図4】(a)に、マトリックスとしてTHAP、測定対象試料としてポリペプチドのサブスタンスP(SubP)とした通常のMALDI-MSスペクトルを示す。(b)に、THAPをαCDにより包摂し、SubPを測定したMALDI-MSスペクトルを示す。(c)に、CHCAをαCDにより包摂し、SubPを測定したMALDI-MSスペクトルを示す。
【図5】THAPよりプロトン親和力の弱いマトリックスであるCHCA構造式を示す。
【図6】上段に、マトリックスとしてTHAPを用い、試料として、N-Acetylchitobioseを通常のMALDI法により測定した結果を示す。下段に、THAPをαCDにより包摂し、上記試料を測定した結果を示す。
【特許請求の範囲】
【請求項1】
マトリックス支援レーザー脱離イオン化質量分析法であって、他の物質を包摂する特性を有する化合物により、試料とマトリックスを包摂し、該包摂した状態において、レーザーを照射することにより、試料をイオン化し、質量分析することを特徴とするマトリックス支援レーザー脱離イオン化質量分析法。
【請求項2】
上記マトリックスを包摂する化合物は、シクロデキストリンであることを特徴とする請求項1に記載のマトリックス支援レーザー脱離イオン化質量分析法。
【請求項3】
上記マトリックスは、THAPであることを特徴とする請求項1に記載のマトリックス支援レーザー脱離イオン化質量分析法。
【請求項4】
上記マトリックスは、CHCAであることを特徴とする請求項1に記載のマトリックス支援レーザー脱離イオン化質量分析法。
【請求項1】
マトリックス支援レーザー脱離イオン化質量分析法であって、他の物質を包摂する特性を有する化合物により、試料とマトリックスを包摂し、該包摂した状態において、レーザーを照射することにより、試料をイオン化し、質量分析することを特徴とするマトリックス支援レーザー脱離イオン化質量分析法。
【請求項2】
上記マトリックスを包摂する化合物は、シクロデキストリンであることを特徴とする請求項1に記載のマトリックス支援レーザー脱離イオン化質量分析法。
【請求項3】
上記マトリックスは、THAPであることを特徴とする請求項1に記載のマトリックス支援レーザー脱離イオン化質量分析法。
【請求項4】
上記マトリックスは、CHCAであることを特徴とする請求項1に記載のマトリックス支援レーザー脱離イオン化質量分析法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2009−186298(P2009−186298A)
【公開日】平成21年8月20日(2009.8.20)
【国際特許分類】
【出願番号】特願2008−25881(P2008−25881)
【出願日】平成20年2月6日(2008.2.6)
【出願人】(305027401)公立大学法人首都大学東京 (385)
【Fターム(参考)】
【公開日】平成21年8月20日(2009.8.20)
【国際特許分類】
【出願日】平成20年2月6日(2008.2.6)
【出願人】(305027401)公立大学法人首都大学東京 (385)
【Fターム(参考)】
[ Back to top ]

