化学物質検出センサおよび化学物質検出方法
【課題】高感度であり、小型であり、かつ安価な化学物質検出センサおよび化学物質検出方法を提供する。
【解決手段】本発明の一の態様によれば、特定の化学物質を検出する化学物質検出センサであって、生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質を備えることを特徴とする、化学物質検出センサが提供される。
【解決手段】本発明の一の態様によれば、特定の化学物質を検出する化学物質検出センサであって、生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質を備えることを特徴とする、化学物質検出センサが提供される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、イオンチャネル型受容体タンパク質を用いて特定の化学物質の検出を行う化学物質検出センサ、および化学物質検出方法に関する。
【背景技術】
【0002】
化学物質の種類を同定しあるいはその濃度を定量化することは、様々な局面において要請されている。例えば、半導体装置の製造プロセスにおいては、製造歩止まりを向上して高品質の半導体装置を製造するために、製造過程にある半導体基板上に付着した有機汚染物質などの化学物質を検出および管理することなどが必要である。
【0003】
このような化学物質を検出する装置としては、例えば、キャビティリングダウン(CRD)方式を用いた検出装置、イオン移動度スペクトル(IMS)方式を用いた検出装置、半導体検出器がある。
【0004】
CRD方式を用いた検出装置は、多重反射を用いて、化学物質の光吸収スペクトルを光学的に検出して、化学物質の検出を行うものである。この検出装置は、高感度であるが、非常に高価であり、かつ巨大であるという問題がある。
【0005】
IMS方式を用いた検出装置は、放射性同位体を用いて化学物質をイオン化し、そのイオンの移動度によって、化学物質の検出を行うものである。この検出装置も、高感度であるが、非常に高価であり、かつ巨大であるという問題がある。また、放射性同位体を扱うため、危険性を伴う。
【0006】
半導体検出器は、気体中に存在する分子を、アルミナ基板上に形成された金属酸化物半導体の表面に吸着させ、金属酸化物半導体の電気伝導度の変化を電気的に検出することにより化学物質の検出を行うものである。この検出器は、比較的安価であるが、感度が低いという問題がある。
【0007】
したがって、高感度、小型および安価の全ての条件を満たす検出装置はまだ開発されていないのが現状である。
【0008】
なお、非特許文献1、2には、キイロショウジョウバエの触角において特異的に発現している63種類のタンパク質について、これらのタンパク質が匂い受容体として機能していることが開示されている。新たに受容体であることが確認されたこれらのタンパク質は、その分子構造が既知の受容体タンパク質である「イオンチャネル型グルタミン酸受容体(ionotropic Glutamate Receptor : iGluR)」に似ていることから、「イオンチャネル型受容体(Ionotropic Receptor : IR)」と命名されている。このイオンチャネル型受容体は、既知である他の匂い受容体、嗅覚受容体や味覚受容体とは明確に異なるタンパク質の分子構造を持つ匂い受容体である。
【先行技術文献】
【非特許文献】
【0009】
【非特許文献1】Richard Benton et al., “Variant Ionotropic Glutamate Receptors as Chemosensory Receptors in Drosophila”, Cell, Elsevier Inc, January 9, 2009, 136, p149-162
【非特許文献2】Liliane Abuin et al.,“Functional Architecture of Olfactory Ionotropic Glutamate Receptors”,Neuron,Elsevier Inc,January 13,2011,69,p44-60
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、上記課題を解決するためになされたものである。すなわち、高感度であり、小型であり、かつ安価な化学物質検出センサおよび化学物質検出方法を提供する。
【課題を解決するための手段】
【0011】
本発明者らは、イオンチャネル型受容体タンパク質が特定の化学物質を検出するセンサとして使用できることを見出した。本発明は、かかる知見に基づいてなされたものである。
【0012】
本発明の一の態様によれば、特定の化学物質を検出する化学物質検出センサであって、生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質を備えることを特徴とする、化学物質検出センサが提供される。
【0013】
本発明の他の態様によれば、特定の化学物質を検出する化学物質検出方法であって、生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質に、少なくともイオンを含む液体試料または気体試料を供給して、前記液体試料または気体試料中に特定の化学物質が含まれているか否かの検出を行うことを特徴とする、化学物質検出方法が提供される。
【発明の効果】
【0014】
本発明の一および他の態様の化学物質検出センサによれば、高感度であり、小型であり、かつ安価な化学物質検出センサを提供することができる。本発明の他の態様の化学物質検出方法によれば、高感度であり、小型であり、かつ安価で行い得る化学物質検出方法を提供することができる。
【図面の簡単な説明】
【0015】
【図1】第1の実施形態に係る化学物質検出センサの概略構成図である。
【図2】図1に示される溶出器を構成する基材の平面図である。
【図3】図1に示される溶出器の縦断面図である。
【図4】第2の実施形態に係る化学物質検出センサの概略構成図である。
【図5】第3の実施形態に係る化学物質検出センサの概略構成図である。
【図6】第4の実施形態に係る化学物質検出センサの概略構成図である。
【図7】検出部の一例を示した概略構成図である。
【図8】第5の実施形態に係る化学物質検出センサの概略構成図である。
【図9】第5の実施形態に係る他の箇所に電極を配置した図である。
【図10】実施例1に係るイオンチャネル型受容体タンパク質が発現したアフリカツメガエルの卵母細胞における各化学物質に対する電流応答を示すグラフである。
【図11】実施例2および比較例1係るイオンチャネル型受容体タンパク質が発現している複数のアフリカツメガエルの卵母細胞における各化学物質に対する電流応答を示すグラフである。
【図12】カイコガが匂い源の探索行動を発現させていることを、目視ではなく、球と光学マウスを使用することで電気的に検知できることを示したグラフである。
【発明を実施するための形態】
【0016】
(第1の実施形態)
以下、本発明による化学物質検出センサおよび化学物質検出方法について、説明する。
【0017】
<化学物質検出センサ>
化学物質検出センサは、特定の化学物質と結合し、かつ生物から採取したイオンチャネル型受容体タンパク質を備えるものである。本明細書における「イオンチャネル型受容体」とは、嗅覚受容細胞に存在する、イオンチャネル共役型受容体のカテゴリに属する匂い受容体の一種を指す。ここで言う「イオンチャネル共役型受容体」とは、対応する分子の特異的な結合によってチャネルを開く作用を持った、受容体タンパク質の一群を指すものである。「イオンチャネル型受容体」はその中の一種であるが、例えば、同じく匂い受容体として機能する昆虫の嗅覚受容体や、神経伝達に関係するイオンチャネル型グルタミン酸受容体などの同じイオンチャネル共役型受容体のカテゴリに属する既知の受容体とは異なるものである。開示されている文献によっては、本明細書において「イオンチャネル共役型受容体」と呼称している、「リガンド分子の結合によりチャネル部分が開口するイオンチャネル」を「イオンチャネル型受容体」と記しているものもあるが、本明細書においては両者を明確に区別する。「イオンチャネル型受容体」は、あくまでも「イオンチャネル共役型受容体」の中の1カテゴリに過ぎず、嗅覚受容体や味覚受容体等と同列に表記されるべき匂い受容体の1カテゴリとして取り扱う。
【0018】
「生物」としては、例えば動物界、旧口動物枝に属する動物が挙げられるが、イオンチャネル型受容体タンパク質を有する生物であれば限定されない。ただし、本明細書における「生物」とは、ヒトを除くものとする。
【0019】
旧口動物枝に属する動物としては、昆虫が挙げられる。「昆虫」とは、動物界、旧口動物枝、脱皮動物上門、節足動物門、昆虫綱に属する動物である。昆虫としては、例えば、原尾目、粘菅目、双尾目、総尾目、蜉蝣目、蜻蛉目、積翅目、欠翅目、直翅目、ナナフシ目、革翅目、蟷螂目、網翅目、シロアリ目、紡脚目、噛虫目、食毛目、シラミ目、アザミウマ目、半翅目、脈翅目、長翅目、毛翅目、鱗翅目、鞘翅目、双翅目、膜翅目、隠翅目、撚翅目等に属するものが挙げられる。昆虫の具体的な例示としては、双翅目短角亜目ハエ下目ショウジョウバエ科に属するキイロショウジョウバエ等が挙げられる。
【0020】
例えば、キイロショウジョウバエの場合、イオンチャネル型受容体タンパク質の一つである、DmIR84a遺伝子がコードするイオンチャネル型受容体タンパク質は配列番号1(別紙)に記載のアミノ酸配列で表わすことができ、このイオンチャネル型受容体タンパク質をコードする遺伝子、DmIR84aは配列番号2(別紙)に記載の塩基配列で表すことができる。このDmIR84a遺伝子からコードされるイオンチャネル型受容体タンパク質は下記式(1)で示されるフェニルアセトアルデヒドと選択的に結合する。
【化1】

【0021】
なお、DmIR84a遺伝子がコードするイオンチャネル型受容体タンパク質には、配列番号1に記載されるアミノ酸配列からなるタンパク質の他、(i)配列番号1で表されるアミノ酸配列において、1もしくは複数個のアミノ酸が欠失、置換、挿入もしくは付加されたアミノ酸配列を含んでなり、かつ配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するタンパク質、(ii)配列番号1で表されるアミノ酸配列をコードする遺伝子とストリンジェントな条件でハイブリダイズする遺伝子によりコードされ、かつ配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するタンパク質、または(iii)配列番号1で表されるアミノ酸配列と70%以上の同一性を有するアミノ酸配列を含んでなり、かつ配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するタンパク質が含まれる。
【0022】
本明細書において、「アミノ酸配列において、1もしくは複数個のアミノ酸が欠失、置換、挿入もしくは付加されたアミノ酸配列」とは、部位特異的突然変異誘発法等の周知の方法により、または天然に生じ得る程度の複数個の数のアミノ酸の置換等により改変がなされたことを意味する。アミノ酸の改変の個数は、好ましくは1〜50個、より好ましくは1〜30個、さらに好ましくは1〜10個、さらにより好ましくは1〜5個、最も好ましくは1〜2個である。
【0023】
受容体タンパク質の改変アミノ酸配列の例は、好ましくは、そのアミノ酸が、1または複数個(好ましくは、1ないし数個あるいは1、2、3、または4個)の保存的置換を有する配列番号1で表されるアミノ酸配列であることができる。
【0024】
本明細書において、「保存的置換」とは、1若しくは複数個のアミノ酸残基を、別の化学的に類似したアミノ酸残基で置き換えることを意味する。例えば、ある疎水性残基を別の疎水性残基によって置換する場合、ある極性残基を同じ電荷を有する別の極性残基によって置換する場合などが挙げられる。このような置換を行うことができる機能的に類似のアミノ酸は、アミノ酸毎に該技術分野において公知である。具体例を挙げると、非極性(疎水性)アミノ酸としては、アラニン、バリン、イソロイシン、ロイシン、プロリン、トリプトファン、フェニルアラニン、メチオニンなどが挙げられる。極性(中性)アミノ酸としては、グリシン、セリン、スレオニン、チロシン、グルタミン、アスパラギン、システインなどが挙げられる。陽電荷をもつ(塩基性)アミノ酸としては、アルギニン、ヒスチジン、リジンなどが挙げられる。負電荷をもつ(酸性)アミノ酸としては、アスパラギン酸、グルタミン酸などが挙げられる。
【0025】
本明細書において「ストリンジェントな条件」とは、ハイブリダイゼーション後のメンブレンの洗浄操作を、高温下低塩濃度溶液中で行うことを意味し、例えば、0.5×SSC濃度(1×SSC:15mMクエン酸3ナトリウム、150mM塩化ナトリウム)、60℃、15分間の洗浄条件、好ましくは0.5×SSC濃度、0.1%SDS溶液中で60℃、15分間の洗浄条件、を意味する。
【0026】
ハイブリダイゼーションは、公知の方法に従って行うことができる。また、市販のライブラリーを使用する場合、添付の使用説明書に記載の方法に従って行うことができる。
【0027】
本明細書において、塩基配列またはアミノ酸配列についての「同一性」とは、比較される配列間において、各々の配列を構成する塩基またはアミノ酸残基の一致の程度の意味で用いられる。本明細書において示した「同一性」の数値はいずれも、当業者に公知の相同性検索プログラムを用いて算出される数値であればよく、例えばFASTA、BLAST等においてデフォルト(初期設定)のパラメータを用いることにより、容易に算出することができる。
【0028】
配列番号1で表されるアミノ酸配列と70%以上の同一性を有するアミノ酸配列は、好ましくは、80%以上、より好ましくは85%以上、さらに好ましくは90%以上、さらにより好ましくは95%以上、特に好ましくは98%以上、そして最も好ましくは99%以上の同一性を有するアミノ酸配列であることができる。
【0029】
本明細書において、配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するかどうかは配列番号1で表されるアミノ酸配列からなるタンパク質の発現と関連する生体現象あるいは機能を評価することにより決定することができ、例えば、そのタンパク質を遺伝子組み換え技術により発現させることができるかどうかを評価することにより決定することができる。
【0030】
イオンチャネル型受容体と言うカテゴリに含まれるタンパク質をコードする遺伝子であるならば、上記において例示したものと発現に至る形態が同一であるために機能を発現させることは可能である。
【0031】
このようなイオンチャネル型受容体タンパク質は、例えば細胞や無細胞タンパク質発現系を用いて発現させることができる。無細胞タンパク質発現系としては、例えば大腸菌抽出物を用いたキット等が挙げられる。イオンチャネル型受容体タンパク質は、例えば、細胞で発現した状態または脂質二重膜に組み込まれた状態で使用される。
【0032】
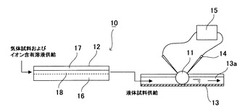
以下、イオンチャネル型受容体タンパク質が発現している細胞を備えた化学物質検出センサについて説明する。図1は本実施形態に係る化学物質検出センサの概略構成図である。図2は図1に示される溶出器を構成する基材の平面図であり、図3は図1に示される溶出器の縦断面図である。
【0033】
図1に示されるように化学物質検出センサ10は、細胞11を備えるものである。また、図1に示される化学物質検出センサ10は、さらに、溶出器12と、流路形成部材13と、電極14と、電流測定器15とを備えるものである。
【0034】
細胞
細胞11は、生物から採取した、特定の化学物質と結合するイオンチャネル型受容体タンパク質が発現しているものである。細胞11としては、特に限定されないが、アフリカツメガエルの卵母細胞、培養細胞、大腸菌、酵母、カイコガの触角に存在するボンビコール受容細胞、ショウジョウバエのエンプティニューロン(内在性の嗅覚受容体を欠く遺伝子組み換えショウジョウバエを用いた発現系)、その他の動物細胞、および植物細胞等が挙げられる。化学物質検出センサ10においては、細胞に電極を刺入する必要があるので、これらの細胞の中でも、直径が約1mm程度であり、細胞に電極を比較的刺入しやすいアフリカツメガエルの卵母細胞が好ましい。
【0035】
細胞11のイオンチャネル型受容体タンパク質は、イオンチャネル型受容体タンパク質をコードする遺伝子を導入することにより、発現しているものである。遺伝子の導入方法は、用いる細胞によって適宜選択することが望ましい。遺伝子の導入方としては、例えば、マイクロインジェクション法、リポフェクション法、ウイルス感染を用いた方法、ヒートショック法、エレクトロポレーション法、リチウム法、GAL4-UASシステムを利用した方法、アクロバクテリウム法等の公知の遺伝子導入技術により得ることができる。
【0036】
例えば、細胞11として、アフリカツメガエルの卵母細胞を用いる場合には、マイクロインジェクション法を用いることが可能である。この場合、例えば昆虫から単離したイオンチャネル型受容体タンパク質をコードするRNAを含む溶液をマイクロインジェクターでアフリカツメガエルの卵母細胞に導入する。これにより、アフリカツメガエルの卵母細胞にて昆虫のイオンチャネル型受容体タンパク質を発現させることができる。
【0037】
細胞11として、培養細胞を用いる場合には、リポフェクション法またはウイルス感染を用いた方法を用いることが可能である。リポフェクション法の場合、リポソーム内に例えば昆虫から単離したイオンチャネル型受容体タンパク質をコードするRNAを導入し、このRNAが導入されたリポソームを培養細胞に融合する。これにより、培養細胞にて昆虫のイオンチャネル型受容体タンパク質を発現させることができる。
【0038】
細胞11として、大腸菌を用いる場合にはヒートショック法やエレクトロポレーション法を用いることが可能であり、酵母を用いる場合には酢酸リチウム法を用いることが可能であり、カイコガの触角に存在するボンビコール受容細胞やショウジョウバエのエンプティニューロンを用いる場合にはGAL4-UASシステムを利用した方法を用いることが可能である。その他の動物細胞を用いる場合にはエレクトロポレーション法が一般的であるが、ウイルス感染を用いた方法やリポフェクション法なども使用することが可能である。また、植物細胞を用いる場合にはアクロバクテリウム法を用いることが可能である。
【0039】
溶出器
溶出器12は、気体試料(サンプルガス)に含まれる化学物質を、イオン含有溶液中に溶出させて、液体試料を得るためのものである。イオン含有溶液は、例えばNa+、Ka+、Ca2+のような陽イオンを含む液体であり、イオン含有溶液としては、例えばバース液が挙げられる。
【0040】
溶出器12としては、例えば、マイクロ化学チップ、フローセル、インピンジャー、スクラバー等が挙げられるが、使用する気体試料やイオン含有溶液が少量で済む観点から例えばマイクロ化学チップ等が好ましい。本実施の形態では、溶出器12が、マイクロ化学チップである例について説明する。
【0041】
溶出器12は、基材16と、基材16を覆うカバー部材17とから構成されている。基材16には、図2に示されるように両端が二股に分岐した形状、すなわち両端がY字状に流路18が形成されている。ここで、注入口18a、18bから合流地点Aまでを注入用流路18c、18dとし、排出口18e、18fから合流地点Bまでを排出用流路18g、18hとし、合流地点Aから合流地点Bまでを溶出用流路18i、18jとする。
【0042】
溶出用流路18iと溶出用流路18jは、溶出用流路18iを流れるサンプルガスと溶出用流路18jを流れるイオン含有溶液が一部において互いに接触するように通じている。溶出用流路18iと溶出用流路18jとの間には、安定した層流を得るために図3に示されるようにガイド18kが設けられていてもよい。
【0043】
注入口18aから気体試料を流すと、気体試料は、注入用流路18c、溶出用流路18i、排出用流路18gを介して排出口18eから排出される。また、注入口18bからイオン含有溶液を流すと、イオン含有溶液は、注入用流路18d、溶出用流路18j、排出用流路18hを介して排出口18fから排出される。ここで、並行かつ接触している2つの微小流路を流れる流体においては、安定で直線的な層流の流れになる傾向が強く、2つの流体を合流させても、実際には互いに混じり合わず、それぞれの流れを維持するような現象が起こる。その一方で、2つの流体の距離が非常に近く、体積から見ると互いが接する界面の面積が非常に大きいことから、拡散によって、一方の流体から他方の流体に分子を移動させることができる。このような原理により、溶出用流路18iを流れる気体試料に含まれる化学物質が、溶出用流路18jを流れるイオン含有溶液に溶出して、液体試料が得られる。
【0044】
流路形成部材
流路形成部材13は、細胞11が設置されるとともに、排出口18fから排出された液体試料を流すための流路13aを備えている。流路形成部材13は、流路13aが形成されていれば、特に限定されない。流路形成部材13としては、例えば、流路が形成された基板等が挙げられる。
【0045】
電極および電流測定器
電極14は、細胞11に刺入されるものである。電極14としては、例えばガラス電極が挙げられる。電流測定器15は、電極14に電気的に接続されている。
【0046】
このような化学物質検出センサ10によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、気体試料から気体試料に含まれる化学物質を溶出器12によりイオン含有溶液に溶出させて、液体試料を得る。そして、流路13aを介して、溶出した化学物質およびイオンを含む液体試料を電極14が刺入された細胞11に供給する。液体試料に含まれている化学物質が、検出対象である特定の化学物質ではない場合、すなわちイオンチャネル型受容体が結合する化学物質でない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、イオンが細胞11内に流入せず、電流変化はほぼ生じない。これに対し、液体試料に含まれている化学物質が、検出対象である特定の化学物質である場合、すなわちイオンチャネル型受容体が結合する化学物質である場合には、化学物質との結合によりイオンチャネル型受容体のイオンチャネルが開き、液体試料に含まれているイオンが細胞11内に流入する。そして、このイオンの流入により、電極14間に流れる電流が変化するので、この電流変化を、電流測定器15を用いて測定することにより検出対象である特定の化学物質を検出することができるとともに、この化学物質の濃度を測定することができる。
【0047】
イオンチャネル型受容体は選択性が高く、また非常に高感度であるので、目的とする化学物質が少量存在すれば、検出することができる。また、イオンチャネル型受容体は非常に小さいので、小型のセンサを得ることができる。さらに、イオンチャネル型受容体タンパク質は例えば一度、生物の組織から遺伝子の形で採取してしまえば、遺伝子工学技術により容易に増幅、およびタンパク質へと合成することができるので、非常に安価で得ることができる。したがって、本実施の形態によれば、高感度であり、小型であり、かつ安価な化学物質検出センサを提供することができる。
【0048】
<化学物質検出方法>
本実施形態の化学物質検出方法は、生物から採取され、かつ特定の化学物質と結合するイオンチャネル型受容体タンパク質に、少なくともイオンを含む液体試料または気体試料を供給して、液体試料または気体試料中に特定の化学物質が含まれているか否かの検出を行うものである。イオンチャネル型受容体タンパク質は、上記と同様のものであるので、ここでは説明を省略するものとする。
【0049】
イオンチャネル型受容体タンパク質を用いて行う化学物質検出方法によれば、上述したように、液体試料または気体試料中に検出対象である特定の化学物質が含まれている場合には、イオンチャネル型受容体タンパク質が特定の化学物質と結合することにより、イオンチャネルが開き、化学物質検出センサの内部にイオンチャネル型受容体タンパク質を介してイオンが流入する。このイオンの流れを例えば電流変化または電圧変化として捉えることによって、検出対象である特定の化学物質を検出することができる。
【0050】
(第2の実施形態)
以下、本発明による第2の実施形態について、図面を参照しながら説明する。図4は本実施形態に係る化学物質検出センサの概略構成図である。
【0051】
図4に示されるように化学物質検出センサ20は、細胞21を備えるものである。また、図4に示される化学物質検出センサ20は、さらに、溶出器22と、流路形成部材23とを備えるものである。
【0052】
細胞
細胞21は、細胞11と同様に、特定の化学物質と結合し、かつ生物から採取したイオンチャネル型受容体タンパク質を備えるものであるが、細胞21には更に例えばイオンの濃度によって蛍光強度が変化する蛍光物質(図示せず)が導入されている。細胞21としては、第1の実施形態で列挙されたものと同様のものが挙げられる。
【0053】
蛍光物質としては、例えば、Na+に応答して蛍光強度が変化するナトリウムイオン感受性蛍光色素、Ka+に応答して蛍光強度が変化するカリウムイオン感受性蛍光色素、Ca2+に応答して蛍光強度が変化するカルシウムイオン感受性蛍光色素等が挙げられる。ナトリウムイオン感受性蛍光色素としては例えばSBFI、CoroNa等が挙げられ、カリウムイオン感受性蛍光色素としては例えばPBFI等が挙げられ、カルシウムイオン感受性蛍光色素としては例えばFura-2、Fluo-3、Fluo-4等が挙げられる。
【0054】
溶出器および流路形成部材
溶出器22は溶出器12と同様のものであり、また流路形成部材23は流路形成部材13と同様のものであるので、説明を省略する。
【0055】
このような化学物質検出センサ20によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、気体試料から気体試料に含まれる化学物質を溶出器22によりイオン含有溶液に溶出させて、液体試料を得る。そして、流路23aを介して、溶出した化学物質およびイオンを含む液体試料を、蛍光物質が導入された細胞21に供給する。液体試料に含まれている化学物質が、検出対象である特定の化学物質ではない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、液体試料に含まれているイオンが細胞21内に流入せず、蛍光強度の変化はほぼ生じない。これに対し、液体試料に含まれている化学物質が、検出対象である特定の化学物質である場合には、化学物質との結合によりイオンチャネル型受容体のイオンチャネルが開き、液体試料に含まれているイオンが細胞21内に流入する。そして、このイオンの流入により、蛍光物質の蛍光強度が変化するので、この蛍光強度の変化を計測することにより、検出対象である特定の目的とする化学物質を検出することができるとともに、この特定の化学物質の濃度を測定することができる。
【0056】
本実施形態によれば、電極を細胞21に刺入する必要がないので、培養細胞のような大きさが非常に小さい細胞であっても、容易に化学物質の検出を行うことができる。
【0057】
(第3の実施形態)
以下、本発明による第3の実施形態について、図面を参照しながら説明する。図5は本実施形態に係る化学物質検出センサの概略構成図である。
【0058】
図5に示されるように化学物質検出センサ30は、脂質二重膜31を備えるものである。また、図5に示される化学物質検出センサ30は、さらに、溶出器32と、流路形成部材33、34と、電流測定器35を備えるものである。
【0059】
脂質二重膜
脂質二重膜31には、イオンチャネル型受容体タンパク質が組み込まれている。このような脂質二重膜31は、無細胞タンパク質発現系によるイオンチャネル型受容体タンパク質の合成と脂質二重膜の形成を同時に行うことにより得ることができる。
【0060】
溶出器
溶出器32は溶出器12と同様であるので説明を省略する。
【0061】
流路形成部材および電流測定器
流路形成部材33、34は脂質二重膜31を挟持するように、流路形成部材33は脂質二重膜31の上側に配置されており、流路形成部材34は脂質二重膜の下側に配置されている。流路形成部材33、34は、流路33a、34aを有し、流路形成部材33、34は流路33a、34aが向かい合わせとなるように配置されている。すなわち、流路33a、34aに、溶出器32によって溶出させた化学物質およびイオンを含む液体試料を流すと、液体試料は脂質二重膜31に接触する。電流測定器35は、流路33a、34a内を流れるイオン含有溶液間の電流を測定するものである。
【0062】
このような化学物質検出センサ30によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、気体試料から気体試料に含まれる化学物質を溶出器35によりイオン含有溶液に溶出させて、液体試料を得る。そして、流路33、34に、溶出した化学物質およびイオンを含む液体試料を流す。液体試料に含まれている化学物質が、検出対象である特定の化学物質ではない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、液体試料に含まれているイオンが流路34aに流入せず、電流変化はほぼ生じない。これに対し、液体試料に含まれている化学物質が、検出対象である特定の化学物質である場合には、化学物質との結合によりイオンチャネル型受容体のイオンチャネルが開き、流路33a内の液体試料に含まれているイオンが脂質二重膜31を介して、流路34aに流入する。このイオンの流入により、液体試料間に流れる電流が変化するので、この電流変化を電流測定器35により測定することにより検出対象である特定の化学物質を検出することができるとともに、この特定の化学物質の濃度を測定することができる。
【0063】
(第4の実施形態)
以下、本発明による第4の実施形態について、図面を参照しながら説明する。図6は、第4の実施形態に係る化学物質検出センサの概略構成図であり、図7は検知部の一例を示した概略構成図である。
【0064】
図6に示されるように化学物質検出センサ40は、トランスジェニックカイコガ41を備えるものである。また、図6に示される化学物質検出センサ40は、さらに、トランスジェニックカイコガ41を収容する筺体42と、外気を筺体42内に取り込む吸引ポンプ43、およびトランスジェニックカイコガ41の動作を検知する検知部44とを備えるものである。
【0065】
トランスジェニックカイコガ
トランスジェニックカイコガ41は、カイコガ以外の生物のイオンチャネル型受容体タンパク質をコードする遺伝子が導入され、ボンビコール受容細胞でイオンチャネル型受容体タンパク質が発現しているものである。なお、本実施形態では、トランスジェニックカイコガ41を用いているが、ショウジョウバエのエンプティニューロンなどを用いてもよい。
【0066】
このようなトランスジェニックカイコガ41は、例えば、マイクロインジェクション法、ウイルス感染を用いた方法等の公知の遺伝子導入技術により得ることができる。これらの中でも、次代への導入遺伝子の伝達効率の点からマイクロインジェクション法が好ましい。
【0067】
具体的には、トランスジェニックカイコガ41は、以下の方法により作製することができる。例えば、野生型のカイコガの性フェロモン受容体に対応する遺伝子であるBmOR1上流配列の下流部に転写制御因子であるGAL4遺伝子を配置させたDNAコンストラクトを作成し、野生型のカイコガの卵のゲノム領域に組み込み、育成する。組み込まれたBmOR1のプロモーターにより、性フェロモン受容細胞でのみGAL4が発現する。
【0068】
また、導入するイオンチャネル型受容体に対応する遺伝子の上流部にUAS(Upstream Activator Sequence)を組み込んだDNAコンストラクトを作成し、野生型のカイコガの卵のゲノム領域に組み込み、育成する。UASはGAL4の認識配列であり、GAL4の存在下においてUASの下流の任意の遺伝子の発現を誘導する。
【0069】
そして、それぞれ育成した、GAL4トランスジェニックカイコガと、UASトランスジェニックカイコガとを交配させて、二重トランスジェニック個体であるトランスジェニックカイコガ41を得る。この方法により作製したトランスジェニックカイコガ41は、GAL4が発現している性フェロモン受容細胞においてのみ、UASの下流に存在する目的のイオンチャネル型受容体タンパク質を発現させることができる。また、この方法で作製したトランスジェニックカイコガにおいては、一度このカイコガの育成を行なえば、次代以降のカイコガは全て同じトランスジェニックカイコガとして育成できる。
【0070】
野生型の雄のカイコガは、雌のカイコガから発生されるフェロモン物質である下記式(2)で示されるボンビコール(Bombykol)を特異的に認識し、匂い源の探索行動が発現する。匂い源の探索行動とは、具体的には、普段は静止状態にあるカイコガが、羽ばたきを始め、化学物質の源を探索し動き始める行動のことを指す。この探索行動は、普段の静止状態とは明確に区別し得る。このボンビコールは、カイコガの触角に存在する嗅覚感覚子内にあるボンビコール受容細胞によって受容される。ボンビコールの受容によってボンビコール受容細胞の神経興奮が発生したときだけ匂い源の探索行動が発現する。なお、特異的に認識するとは、特定の化学物質にのみ匂い源の探索行動が発現することを示し、他の化学物質に関してはその探索行動が発現しないことを意味する。したがって、野生型のカイコガはボンビコールでは匂い源の探索行動が発現するが、他の化学物質には探索行動は発現しない。
【化2】

【0071】
これに対し、トランスジェニックカイコガ41は、ボンビコール受容細胞にボンビコール以外の化学物質と結合するイオンチャネル型受容体タンパク質をコードする遺伝子が導入され、かつこのイオンチャネル型受容体タンパク質が発現しているものであるので、導入したイオンチャネル型受容体タンパク質が結合する化学物質に対してボンビコール受容細胞の神経興奮が起こり、匂い源の探索行動が発現する。具体的には、トランスジェニックカイコガ41が、導入したイオンチャネル型受容体タンパク質が結合する化学物質を受容すると、イオンチャネルが開き、リンパ液に含まれるイオンが流入して、ボンビコール受容細胞の神経興奮が起こる。これにより、トランスジェニックカイコガ41は、羽ばたきを始めて、化学物質の源を探索し始める。したがって、この挙動をモニタリングすることによって、化学物質の検出が可能になる。
【0072】
筺体
筺体42は、少なくとも1匹のトランスジェニックカイコガ41を収容することができれば特に限定されないが、複数匹のトランスジェニックカイコガ41を収容できるものが好ましい。複数匹のトランスジェニックカイコガ41を用いることにより、化学物質を検出するセンサとしての正確性を向上させることができる。筺体42は吸気口42aおよび排気口42bを備えている。
【0073】
吸引ポンプ
吸引ポンプ43は、排気口42bに接続されている。吸引ポンプ43を作動させることにより、吸気口42aを介して外気を筺体42内に取入れることができる。
【0074】
検知部
検知部44としては、トランスジェニックカイコガ41の動作を直接的または間接的に検知することができれば特に限定されない。検知部44として、例えば、動体センサ、トランスジェニックカイコガ41の動作に伴う振動を検知する振動センサ、トランスジェニックカイコガ41の動作に伴う音を検知する音センサ等を用いることができる。なお、検知部44を設けずに目視によりトランスジェニックカイコガ41の動作を検知してもよい。
【0075】
また、検知部44として、図7に示されるようなトランスジェニックカイコガ41を吊下げる吊下部材44aと、吊下部材44aで吊下げられたトランスジェニックカイコガ41の足に接触し、かつ回転可能に設置された球44bと、球44bの動きを検知する例えば光学マウス等の動体センサ44cとを備えるものを使用してもよい。なお、球44bと動体センサ44cとを備えるトラックボールを用いてもよい。このような検知部44を用いることにより、トランスジェニックカイコガ41の動作を検知できるだけでなく、トランスジェニックカイコガ41の行動解析を行うことができる。
【0076】
このような化学物質検出センサ40によれば、以下のようにして、目的とする化学物質を検出することができる。まず、吸引ポンプ43を作動させて、筺体42内に外気を取り込む。取り込まれた外気(気体試料)に検出対象である特定の化学物質が含まれていない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、トランスジェニックカイコガ41は特異的な挙動は示さない。これに対して、取り込まれた外気に検出対象である特定の化学物質が含まれていた場合には、イオンチャネル型受容体のイオンチャネルが開き、トランスジェニックカイコガ41は羽ばたきを始め、化学物質の源の探索を始める。そして、この際の動作やこの際に発生する振動や音を検知部44で検知することにより、検出対象である特定の化学物質を検出することができる。
【0077】
カイコガの触角は非常に高感度であるので、トランスジェニックカイコガ41においても、検出対象である特定の化学物質が例えば気体中に数100分子程度存在すれば、検知することができる。さらに、例えばマイクロインジェクション法等により子孫に導入遺伝子を伝達させることができる場合には、一度遺伝子をカイコガに導入すればよいので、トランスジェニックカイコガ41の飼育費用等を考慮しても、トランスジェニックカイコガ41を非常に安価で得ることができる。さらに、トランスジェニックカイコガ41は野生型のカイコガと同様に体長3cm程度であるので、小型のセンサを得ることができる。したがって、本実施の形態によれば、トランスジェニックカイコガ41を用いているので、高感度であり、小型であり、かつ安価な化学物質検出センサ40を提供することができる。
【0078】
また、空気中での化学物質の分布は、単純に拡散して連続的になっておらず、小さい多数の断続的な塊となって浮遊している。すなわち、発生源の近くでは濃度が高く、遠ざかるにつれて低くなるという単純な分布ではない。このため、化学物質の発生源の探索は困難であり、発生源の特定を行うには、濃度の高い方向へただ遡って行くだけでは不十分であり、高度な行動アルゴリズムが必要となる。
【0079】
一方で、野生型の雄のカイコガは非常に高度な行動アルゴリズムを用いて雌のカイコガを探索している。本実施形態によるトランスジェニックカイコガ41は、この高度な行動アルゴリズムを用いることができるので、目的とする化学物質の発生源を探索することができる。
【0080】
(第5の実施形態)
以下、本発明による第5の実施形態について、図面を参照しながら説明する。図8は、第5の実施形態に係る化学物質検出センサの概略構成図であり、図9は第5の実施形態に係る他の箇所に電極を配置した図である。
【0081】
図8に示される化学物質検出センサ50は、トランスジェニックカイコガの触角51と、一対の電極52と、電位測定器53とを備えている。図8に示される化学物質検出センサ50は、さらに、触角51を収容する筺体54と、外気を筺体54内に取り込む吸引ポンプ55とを備えている。
【0082】
触角
触角51は、第4の実施形態で説明したトランスジェニックカイコガ41から切り取られたものである。
【0083】
電極
一対の電極52は、触角51に接続されている。図8に示される化学物質検出センサ50においては、一方の電極52(記録電極)が触角51の先端部51aに接続されており、他方の電極52(不関電極)は触角51の根元部51b、すなわち脳に繋がる神経の軸策部位に接続されている。なお、先端部51aは、電極52を接続する前に多少先端が切り落とされたものである。この場合には、その触角51に存在する全ての嗅覚感覚子からの電位の総和が得られる。
【0084】
また、電極52は、図9に示されるように触角51中に存在する一つの嗅覚感覚子51cに接続してもよい。この場合には、一つの嗅覚感覚子51cから電位が得られる。
【0085】
電位測定器
電位測定器53は、嗅覚感覚子が目的とする化学物質を受容したとき、触角全体または一つの嗅覚感覚子から発生する電位を測定するものである。図8のように触角51全体から発生する電位を測定する場合には、電位測定装置53としては、触角電図法(EAG: electroantennogram recording)を用いた装置が挙げられる。また、図9のように一つの嗅覚感覚子51cから発生する電位を測定する場合には、単一感覚子記録法(single sensillum recording)を用いた装置が挙げられる。
【0086】
筺体および吸引ポンプ
筺体54は、吸気口54aおよび排気口54bを備えている。また、吸引ポンプ55は、排気口54bに接続されている。吸引ポンプ55を作動させることにより、吸気口54aを介して外気を筺体54内に取入れることができる。
【0087】
このような化学物質検出センサ50によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、吸引ポンプ55を作動させて、筺体54内に外気を取り込む。取り込まれた外気に検出対象である特定の化学物質が含まれていない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であり、触角51は電気応答を示さない。これに対して、取り込まれた外気に目的とする化学物質が含まれていた場合には、イオンチャネル型受容体のイオンチャネルが開き、触角51は電気応答を示し、電位が検知される。これにより、検出対象である特定の化学物質を検出することができる。
【0088】
本実施の形態によれば、トランスジェニックカイコガから切り取った触角51を用いているので、高感度であり、安価であり、さらにより小型の化学物質検出センサ10を提供することができる。
【0089】
また、触角電図法では目的とする化学物質の濃度が高いほど、検知される電位が大きくなるので、電位の大きさによって目的とする化学物質の濃度を測定することができる。また、単一感覚子記録法では目的とする化学物質の濃度が高いほど、検知される活動電位数が増加するので、活動電位数の数によって目的とする化学物質の濃度を測定することができる。
【実施例】
【0090】
以下、実施例により本発明を更に詳細に説明するが、これら実施例に本発明が限定されるものではない。
【0091】
実施例1
まず、アフリカツメガエルの卵母細胞に、キイロショウジョウバエの触角から単離したイオンチャネル型受容体タンパク質をコードする遺伝子DmIR84aをマイクロインジェクション法により導入して、イオンチャネル型受容体タンパク質が発現した卵母細胞を得た。ここで、このキイロショウジョウバエのイオンチャネル型受容体タンパク質は、フェニルアセトアルデヒドと選択的に結合するものである。
【0092】
また、化学物質検出センサを用意した。具体的には、上記卵母細胞の他、流路形成部材、電極としてのガラス電極、ガラス電極に電気的に接続された電流測定器を用意した。そして、流路形成部材に形成された流路内に上記イオンチャネル型受容体タンパク質が発現した卵母細胞を1つ配置し、この卵母細胞にガラス電極を刺入した。流路には、1ml/min程度のバッファ(緩衝液)を流し、常に新鮮なバッファが卵母細胞に供給されるようにした。また、流路の上流より、バッファ、および10μMに希釈したアンモニア、ブチルアミン、ペンチルアミン、p−クレゾール、フェニルアセトアルデヒドを、1種類ずつ所定時間をおいてピペットにより順次供給した。そして、そのときのガラス電極間に流れる電流を電流測定器により測定した。
【0093】
以下、結果について述べる。図10は実施例1に係る卵母細胞の各化学物質に対する電流応答を示したグラフである。図10に示されるように卵母細胞は、フェニルアセトアルデヒドに対して電流応答を示したが、バッファ、アンモニア、ブチルアミン、ペンチルアミン、p−クレゾールに対して電流応答を示さなかった。
【0094】
この結果から、アフリカツメガエルの卵母細胞にキイロショウジョウバエ由来のイオンチャネル型受容体タンパク質をコードする遺伝子、DmIR84aを導入して、卵母細胞にてDmIR84a遺伝子のコードするイオンチャネル型受容体タンパク質を発現させた場合、導入した受容体が結合するフェニルアセトアルデヒドを卵母細胞で応答させることができることが確認された。
【0095】
実施例2
実施例1においては、1個のアフリカツメガエルの卵母細胞を用いて実験が行われたが、実施例2においては、5個のアフリカツメガエルの卵母細胞を用いて実験が行われた。
【0096】
それぞれのアフリカツメガエルの卵母細胞に、実施例1と同様に、キイロショウジョウバエの触角から単離したイオンチャネル型受容体タンパク質をコードする遺伝子、DmIR84aをマイクロインジェクション法により導入して、DmIR84a遺伝子のコードするイオンチャネル型受容体タンパク質が発現した卵母細胞を得た。
【0097】
比較例1
複数のアフリカツメガエルの卵母細胞のそれぞれに、キイロショウジョウバエの触角から単離した、先程とは別種のイオンチャネル型受容体をコードする遺伝子、DmIR31aをマイクロインジェクション法により導入し、DmIR31a遺伝子のコードするイオンチャネル型受容体タンパク質が発現した卵母細胞を得た。
【0098】
そして、実施例2に係る卵母細胞と、比較例1に係る卵母細胞に対して、実施例1と同様の実験を行った。
【0099】
以下、結果について述べる。図11は実施例2および比較例1に係る卵母細胞の各化学物質に対する電流応答を示したグラフである。図11に示されるように比較例1に係る全ての卵母細胞は、バッファ、アンモニア、ブチルアミン、ペンチルアミン、p−クレゾール、およびフェニルアセトアルデヒドの全ての化学物質に対してほぼ電流応答を示さなかった。これに対し、実施例2に係る卵母細胞の内、5個中の4個については、バッファ、アンモニア、ブチルアミン、ペンチルアミン、p−クレゾールに対しては電流応答を示さなかったが、フェニルアセトアルデヒドに対しては電流応答を示した。
【0100】
これらの結果から、まさしく導入したキイロショウジョウバエ由来のイオンチャネル型受容体タンパク質DmIR84aによって、フェニルアセトアルデヒドに対する応答機能が発現されることができることが確認された。ここで、キイロショウジョウバエ触角においては、DmIR84a遺伝子がコードするイオンチャネル型受容体タンパク質の存在する細胞はフェニルアセトアルデヒドに応答を示すが、DmIR31a遺伝子がコードするイオンチャネル型受容体タンパク質の存在する細胞はフェニルアセトアルデヒドに応答を示さないことが知られている。以上の結果は、キイロショウジョウバエの触角における匂いに対する応答を、卵母細胞上で再現できたことを意味している。
【0101】
実施例3
野生型のカイコガを発砲スチロールの球の上に置き、吊下部材により野生型のカイコガを吊下げて固定した。その後、前方から野生型のカイコガのフェロモン物質であるボンビコールを吹き付けた。そして、野生型のカイコガの動きを光学マウスにより読み取り、野生型のカイコガの行動を解析した。
【0102】
以下、結果について述べる。図12は実施例3に係る野生型のカイコガのボンビコールに対する挙動を示したグラフである。
【0103】
図12から、フェロモン物質を受容したことによる匂い源の探索行動の発現を、目視ではなく、球と光学マウスを用いることで電気的に検出できることが確認された。
【符号の説明】
【0104】
10、20、30、40、50…化学物質検出センサ、11、21…細胞、12、22、32…溶出器、13、23、33、34…流路形成部材、13a、23a、33a、34a…流路、15、35…電流測定器、31…脂質二重膜、41…トランスジェニックカイコガ、44…検知部、51…触角、52…電極、53…電位測定器。
【技術分野】
【0001】
本発明は、イオンチャネル型受容体タンパク質を用いて特定の化学物質の検出を行う化学物質検出センサ、および化学物質検出方法に関する。
【背景技術】
【0002】
化学物質の種類を同定しあるいはその濃度を定量化することは、様々な局面において要請されている。例えば、半導体装置の製造プロセスにおいては、製造歩止まりを向上して高品質の半導体装置を製造するために、製造過程にある半導体基板上に付着した有機汚染物質などの化学物質を検出および管理することなどが必要である。
【0003】
このような化学物質を検出する装置としては、例えば、キャビティリングダウン(CRD)方式を用いた検出装置、イオン移動度スペクトル(IMS)方式を用いた検出装置、半導体検出器がある。
【0004】
CRD方式を用いた検出装置は、多重反射を用いて、化学物質の光吸収スペクトルを光学的に検出して、化学物質の検出を行うものである。この検出装置は、高感度であるが、非常に高価であり、かつ巨大であるという問題がある。
【0005】
IMS方式を用いた検出装置は、放射性同位体を用いて化学物質をイオン化し、そのイオンの移動度によって、化学物質の検出を行うものである。この検出装置も、高感度であるが、非常に高価であり、かつ巨大であるという問題がある。また、放射性同位体を扱うため、危険性を伴う。
【0006】
半導体検出器は、気体中に存在する分子を、アルミナ基板上に形成された金属酸化物半導体の表面に吸着させ、金属酸化物半導体の電気伝導度の変化を電気的に検出することにより化学物質の検出を行うものである。この検出器は、比較的安価であるが、感度が低いという問題がある。
【0007】
したがって、高感度、小型および安価の全ての条件を満たす検出装置はまだ開発されていないのが現状である。
【0008】
なお、非特許文献1、2には、キイロショウジョウバエの触角において特異的に発現している63種類のタンパク質について、これらのタンパク質が匂い受容体として機能していることが開示されている。新たに受容体であることが確認されたこれらのタンパク質は、その分子構造が既知の受容体タンパク質である「イオンチャネル型グルタミン酸受容体(ionotropic Glutamate Receptor : iGluR)」に似ていることから、「イオンチャネル型受容体(Ionotropic Receptor : IR)」と命名されている。このイオンチャネル型受容体は、既知である他の匂い受容体、嗅覚受容体や味覚受容体とは明確に異なるタンパク質の分子構造を持つ匂い受容体である。
【先行技術文献】
【非特許文献】
【0009】
【非特許文献1】Richard Benton et al., “Variant Ionotropic Glutamate Receptors as Chemosensory Receptors in Drosophila”, Cell, Elsevier Inc, January 9, 2009, 136, p149-162
【非特許文献2】Liliane Abuin et al.,“Functional Architecture of Olfactory Ionotropic Glutamate Receptors”,Neuron,Elsevier Inc,January 13,2011,69,p44-60
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、上記課題を解決するためになされたものである。すなわち、高感度であり、小型であり、かつ安価な化学物質検出センサおよび化学物質検出方法を提供する。
【課題を解決するための手段】
【0011】
本発明者らは、イオンチャネル型受容体タンパク質が特定の化学物質を検出するセンサとして使用できることを見出した。本発明は、かかる知見に基づいてなされたものである。
【0012】
本発明の一の態様によれば、特定の化学物質を検出する化学物質検出センサであって、生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質を備えることを特徴とする、化学物質検出センサが提供される。
【0013】
本発明の他の態様によれば、特定の化学物質を検出する化学物質検出方法であって、生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質に、少なくともイオンを含む液体試料または気体試料を供給して、前記液体試料または気体試料中に特定の化学物質が含まれているか否かの検出を行うことを特徴とする、化学物質検出方法が提供される。
【発明の効果】
【0014】
本発明の一および他の態様の化学物質検出センサによれば、高感度であり、小型であり、かつ安価な化学物質検出センサを提供することができる。本発明の他の態様の化学物質検出方法によれば、高感度であり、小型であり、かつ安価で行い得る化学物質検出方法を提供することができる。
【図面の簡単な説明】
【0015】
【図1】第1の実施形態に係る化学物質検出センサの概略構成図である。
【図2】図1に示される溶出器を構成する基材の平面図である。
【図3】図1に示される溶出器の縦断面図である。
【図4】第2の実施形態に係る化学物質検出センサの概略構成図である。
【図5】第3の実施形態に係る化学物質検出センサの概略構成図である。
【図6】第4の実施形態に係る化学物質検出センサの概略構成図である。
【図7】検出部の一例を示した概略構成図である。
【図8】第5の実施形態に係る化学物質検出センサの概略構成図である。
【図9】第5の実施形態に係る他の箇所に電極を配置した図である。
【図10】実施例1に係るイオンチャネル型受容体タンパク質が発現したアフリカツメガエルの卵母細胞における各化学物質に対する電流応答を示すグラフである。
【図11】実施例2および比較例1係るイオンチャネル型受容体タンパク質が発現している複数のアフリカツメガエルの卵母細胞における各化学物質に対する電流応答を示すグラフである。
【図12】カイコガが匂い源の探索行動を発現させていることを、目視ではなく、球と光学マウスを使用することで電気的に検知できることを示したグラフである。
【発明を実施するための形態】
【0016】
(第1の実施形態)
以下、本発明による化学物質検出センサおよび化学物質検出方法について、説明する。
【0017】
<化学物質検出センサ>
化学物質検出センサは、特定の化学物質と結合し、かつ生物から採取したイオンチャネル型受容体タンパク質を備えるものである。本明細書における「イオンチャネル型受容体」とは、嗅覚受容細胞に存在する、イオンチャネル共役型受容体のカテゴリに属する匂い受容体の一種を指す。ここで言う「イオンチャネル共役型受容体」とは、対応する分子の特異的な結合によってチャネルを開く作用を持った、受容体タンパク質の一群を指すものである。「イオンチャネル型受容体」はその中の一種であるが、例えば、同じく匂い受容体として機能する昆虫の嗅覚受容体や、神経伝達に関係するイオンチャネル型グルタミン酸受容体などの同じイオンチャネル共役型受容体のカテゴリに属する既知の受容体とは異なるものである。開示されている文献によっては、本明細書において「イオンチャネル共役型受容体」と呼称している、「リガンド分子の結合によりチャネル部分が開口するイオンチャネル」を「イオンチャネル型受容体」と記しているものもあるが、本明細書においては両者を明確に区別する。「イオンチャネル型受容体」は、あくまでも「イオンチャネル共役型受容体」の中の1カテゴリに過ぎず、嗅覚受容体や味覚受容体等と同列に表記されるべき匂い受容体の1カテゴリとして取り扱う。
【0018】
「生物」としては、例えば動物界、旧口動物枝に属する動物が挙げられるが、イオンチャネル型受容体タンパク質を有する生物であれば限定されない。ただし、本明細書における「生物」とは、ヒトを除くものとする。
【0019】
旧口動物枝に属する動物としては、昆虫が挙げられる。「昆虫」とは、動物界、旧口動物枝、脱皮動物上門、節足動物門、昆虫綱に属する動物である。昆虫としては、例えば、原尾目、粘菅目、双尾目、総尾目、蜉蝣目、蜻蛉目、積翅目、欠翅目、直翅目、ナナフシ目、革翅目、蟷螂目、網翅目、シロアリ目、紡脚目、噛虫目、食毛目、シラミ目、アザミウマ目、半翅目、脈翅目、長翅目、毛翅目、鱗翅目、鞘翅目、双翅目、膜翅目、隠翅目、撚翅目等に属するものが挙げられる。昆虫の具体的な例示としては、双翅目短角亜目ハエ下目ショウジョウバエ科に属するキイロショウジョウバエ等が挙げられる。
【0020】
例えば、キイロショウジョウバエの場合、イオンチャネル型受容体タンパク質の一つである、DmIR84a遺伝子がコードするイオンチャネル型受容体タンパク質は配列番号1(別紙)に記載のアミノ酸配列で表わすことができ、このイオンチャネル型受容体タンパク質をコードする遺伝子、DmIR84aは配列番号2(別紙)に記載の塩基配列で表すことができる。このDmIR84a遺伝子からコードされるイオンチャネル型受容体タンパク質は下記式(1)で示されるフェニルアセトアルデヒドと選択的に結合する。
【化1】

【0021】
なお、DmIR84a遺伝子がコードするイオンチャネル型受容体タンパク質には、配列番号1に記載されるアミノ酸配列からなるタンパク質の他、(i)配列番号1で表されるアミノ酸配列において、1もしくは複数個のアミノ酸が欠失、置換、挿入もしくは付加されたアミノ酸配列を含んでなり、かつ配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するタンパク質、(ii)配列番号1で表されるアミノ酸配列をコードする遺伝子とストリンジェントな条件でハイブリダイズする遺伝子によりコードされ、かつ配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するタンパク質、または(iii)配列番号1で表されるアミノ酸配列と70%以上の同一性を有するアミノ酸配列を含んでなり、かつ配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するタンパク質が含まれる。
【0022】
本明細書において、「アミノ酸配列において、1もしくは複数個のアミノ酸が欠失、置換、挿入もしくは付加されたアミノ酸配列」とは、部位特異的突然変異誘発法等の周知の方法により、または天然に生じ得る程度の複数個の数のアミノ酸の置換等により改変がなされたことを意味する。アミノ酸の改変の個数は、好ましくは1〜50個、より好ましくは1〜30個、さらに好ましくは1〜10個、さらにより好ましくは1〜5個、最も好ましくは1〜2個である。
【0023】
受容体タンパク質の改変アミノ酸配列の例は、好ましくは、そのアミノ酸が、1または複数個(好ましくは、1ないし数個あるいは1、2、3、または4個)の保存的置換を有する配列番号1で表されるアミノ酸配列であることができる。
【0024】
本明細書において、「保存的置換」とは、1若しくは複数個のアミノ酸残基を、別の化学的に類似したアミノ酸残基で置き換えることを意味する。例えば、ある疎水性残基を別の疎水性残基によって置換する場合、ある極性残基を同じ電荷を有する別の極性残基によって置換する場合などが挙げられる。このような置換を行うことができる機能的に類似のアミノ酸は、アミノ酸毎に該技術分野において公知である。具体例を挙げると、非極性(疎水性)アミノ酸としては、アラニン、バリン、イソロイシン、ロイシン、プロリン、トリプトファン、フェニルアラニン、メチオニンなどが挙げられる。極性(中性)アミノ酸としては、グリシン、セリン、スレオニン、チロシン、グルタミン、アスパラギン、システインなどが挙げられる。陽電荷をもつ(塩基性)アミノ酸としては、アルギニン、ヒスチジン、リジンなどが挙げられる。負電荷をもつ(酸性)アミノ酸としては、アスパラギン酸、グルタミン酸などが挙げられる。
【0025】
本明細書において「ストリンジェントな条件」とは、ハイブリダイゼーション後のメンブレンの洗浄操作を、高温下低塩濃度溶液中で行うことを意味し、例えば、0.5×SSC濃度(1×SSC:15mMクエン酸3ナトリウム、150mM塩化ナトリウム)、60℃、15分間の洗浄条件、好ましくは0.5×SSC濃度、0.1%SDS溶液中で60℃、15分間の洗浄条件、を意味する。
【0026】
ハイブリダイゼーションは、公知の方法に従って行うことができる。また、市販のライブラリーを使用する場合、添付の使用説明書に記載の方法に従って行うことができる。
【0027】
本明細書において、塩基配列またはアミノ酸配列についての「同一性」とは、比較される配列間において、各々の配列を構成する塩基またはアミノ酸残基の一致の程度の意味で用いられる。本明細書において示した「同一性」の数値はいずれも、当業者に公知の相同性検索プログラムを用いて算出される数値であればよく、例えばFASTA、BLAST等においてデフォルト(初期設定)のパラメータを用いることにより、容易に算出することができる。
【0028】
配列番号1で表されるアミノ酸配列と70%以上の同一性を有するアミノ酸配列は、好ましくは、80%以上、より好ましくは85%以上、さらに好ましくは90%以上、さらにより好ましくは95%以上、特に好ましくは98%以上、そして最も好ましくは99%以上の同一性を有するアミノ酸配列であることができる。
【0029】
本明細書において、配列番号1で表されるアミノ酸配列からなるタンパク質と同等の機能を有するかどうかは配列番号1で表されるアミノ酸配列からなるタンパク質の発現と関連する生体現象あるいは機能を評価することにより決定することができ、例えば、そのタンパク質を遺伝子組み換え技術により発現させることができるかどうかを評価することにより決定することができる。
【0030】
イオンチャネル型受容体と言うカテゴリに含まれるタンパク質をコードする遺伝子であるならば、上記において例示したものと発現に至る形態が同一であるために機能を発現させることは可能である。
【0031】
このようなイオンチャネル型受容体タンパク質は、例えば細胞や無細胞タンパク質発現系を用いて発現させることができる。無細胞タンパク質発現系としては、例えば大腸菌抽出物を用いたキット等が挙げられる。イオンチャネル型受容体タンパク質は、例えば、細胞で発現した状態または脂質二重膜に組み込まれた状態で使用される。
【0032】
以下、イオンチャネル型受容体タンパク質が発現している細胞を備えた化学物質検出センサについて説明する。図1は本実施形態に係る化学物質検出センサの概略構成図である。図2は図1に示される溶出器を構成する基材の平面図であり、図3は図1に示される溶出器の縦断面図である。
【0033】
図1に示されるように化学物質検出センサ10は、細胞11を備えるものである。また、図1に示される化学物質検出センサ10は、さらに、溶出器12と、流路形成部材13と、電極14と、電流測定器15とを備えるものである。
【0034】
細胞
細胞11は、生物から採取した、特定の化学物質と結合するイオンチャネル型受容体タンパク質が発現しているものである。細胞11としては、特に限定されないが、アフリカツメガエルの卵母細胞、培養細胞、大腸菌、酵母、カイコガの触角に存在するボンビコール受容細胞、ショウジョウバエのエンプティニューロン(内在性の嗅覚受容体を欠く遺伝子組み換えショウジョウバエを用いた発現系)、その他の動物細胞、および植物細胞等が挙げられる。化学物質検出センサ10においては、細胞に電極を刺入する必要があるので、これらの細胞の中でも、直径が約1mm程度であり、細胞に電極を比較的刺入しやすいアフリカツメガエルの卵母細胞が好ましい。
【0035】
細胞11のイオンチャネル型受容体タンパク質は、イオンチャネル型受容体タンパク質をコードする遺伝子を導入することにより、発現しているものである。遺伝子の導入方法は、用いる細胞によって適宜選択することが望ましい。遺伝子の導入方としては、例えば、マイクロインジェクション法、リポフェクション法、ウイルス感染を用いた方法、ヒートショック法、エレクトロポレーション法、リチウム法、GAL4-UASシステムを利用した方法、アクロバクテリウム法等の公知の遺伝子導入技術により得ることができる。
【0036】
例えば、細胞11として、アフリカツメガエルの卵母細胞を用いる場合には、マイクロインジェクション法を用いることが可能である。この場合、例えば昆虫から単離したイオンチャネル型受容体タンパク質をコードするRNAを含む溶液をマイクロインジェクターでアフリカツメガエルの卵母細胞に導入する。これにより、アフリカツメガエルの卵母細胞にて昆虫のイオンチャネル型受容体タンパク質を発現させることができる。
【0037】
細胞11として、培養細胞を用いる場合には、リポフェクション法またはウイルス感染を用いた方法を用いることが可能である。リポフェクション法の場合、リポソーム内に例えば昆虫から単離したイオンチャネル型受容体タンパク質をコードするRNAを導入し、このRNAが導入されたリポソームを培養細胞に融合する。これにより、培養細胞にて昆虫のイオンチャネル型受容体タンパク質を発現させることができる。
【0038】
細胞11として、大腸菌を用いる場合にはヒートショック法やエレクトロポレーション法を用いることが可能であり、酵母を用いる場合には酢酸リチウム法を用いることが可能であり、カイコガの触角に存在するボンビコール受容細胞やショウジョウバエのエンプティニューロンを用いる場合にはGAL4-UASシステムを利用した方法を用いることが可能である。その他の動物細胞を用いる場合にはエレクトロポレーション法が一般的であるが、ウイルス感染を用いた方法やリポフェクション法なども使用することが可能である。また、植物細胞を用いる場合にはアクロバクテリウム法を用いることが可能である。
【0039】
溶出器
溶出器12は、気体試料(サンプルガス)に含まれる化学物質を、イオン含有溶液中に溶出させて、液体試料を得るためのものである。イオン含有溶液は、例えばNa+、Ka+、Ca2+のような陽イオンを含む液体であり、イオン含有溶液としては、例えばバース液が挙げられる。
【0040】
溶出器12としては、例えば、マイクロ化学チップ、フローセル、インピンジャー、スクラバー等が挙げられるが、使用する気体試料やイオン含有溶液が少量で済む観点から例えばマイクロ化学チップ等が好ましい。本実施の形態では、溶出器12が、マイクロ化学チップである例について説明する。
【0041】
溶出器12は、基材16と、基材16を覆うカバー部材17とから構成されている。基材16には、図2に示されるように両端が二股に分岐した形状、すなわち両端がY字状に流路18が形成されている。ここで、注入口18a、18bから合流地点Aまでを注入用流路18c、18dとし、排出口18e、18fから合流地点Bまでを排出用流路18g、18hとし、合流地点Aから合流地点Bまでを溶出用流路18i、18jとする。
【0042】
溶出用流路18iと溶出用流路18jは、溶出用流路18iを流れるサンプルガスと溶出用流路18jを流れるイオン含有溶液が一部において互いに接触するように通じている。溶出用流路18iと溶出用流路18jとの間には、安定した層流を得るために図3に示されるようにガイド18kが設けられていてもよい。
【0043】
注入口18aから気体試料を流すと、気体試料は、注入用流路18c、溶出用流路18i、排出用流路18gを介して排出口18eから排出される。また、注入口18bからイオン含有溶液を流すと、イオン含有溶液は、注入用流路18d、溶出用流路18j、排出用流路18hを介して排出口18fから排出される。ここで、並行かつ接触している2つの微小流路を流れる流体においては、安定で直線的な層流の流れになる傾向が強く、2つの流体を合流させても、実際には互いに混じり合わず、それぞれの流れを維持するような現象が起こる。その一方で、2つの流体の距離が非常に近く、体積から見ると互いが接する界面の面積が非常に大きいことから、拡散によって、一方の流体から他方の流体に分子を移動させることができる。このような原理により、溶出用流路18iを流れる気体試料に含まれる化学物質が、溶出用流路18jを流れるイオン含有溶液に溶出して、液体試料が得られる。
【0044】
流路形成部材
流路形成部材13は、細胞11が設置されるとともに、排出口18fから排出された液体試料を流すための流路13aを備えている。流路形成部材13は、流路13aが形成されていれば、特に限定されない。流路形成部材13としては、例えば、流路が形成された基板等が挙げられる。
【0045】
電極および電流測定器
電極14は、細胞11に刺入されるものである。電極14としては、例えばガラス電極が挙げられる。電流測定器15は、電極14に電気的に接続されている。
【0046】
このような化学物質検出センサ10によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、気体試料から気体試料に含まれる化学物質を溶出器12によりイオン含有溶液に溶出させて、液体試料を得る。そして、流路13aを介して、溶出した化学物質およびイオンを含む液体試料を電極14が刺入された細胞11に供給する。液体試料に含まれている化学物質が、検出対象である特定の化学物質ではない場合、すなわちイオンチャネル型受容体が結合する化学物質でない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、イオンが細胞11内に流入せず、電流変化はほぼ生じない。これに対し、液体試料に含まれている化学物質が、検出対象である特定の化学物質である場合、すなわちイオンチャネル型受容体が結合する化学物質である場合には、化学物質との結合によりイオンチャネル型受容体のイオンチャネルが開き、液体試料に含まれているイオンが細胞11内に流入する。そして、このイオンの流入により、電極14間に流れる電流が変化するので、この電流変化を、電流測定器15を用いて測定することにより検出対象である特定の化学物質を検出することができるとともに、この化学物質の濃度を測定することができる。
【0047】
イオンチャネル型受容体は選択性が高く、また非常に高感度であるので、目的とする化学物質が少量存在すれば、検出することができる。また、イオンチャネル型受容体は非常に小さいので、小型のセンサを得ることができる。さらに、イオンチャネル型受容体タンパク質は例えば一度、生物の組織から遺伝子の形で採取してしまえば、遺伝子工学技術により容易に増幅、およびタンパク質へと合成することができるので、非常に安価で得ることができる。したがって、本実施の形態によれば、高感度であり、小型であり、かつ安価な化学物質検出センサを提供することができる。
【0048】
<化学物質検出方法>
本実施形態の化学物質検出方法は、生物から採取され、かつ特定の化学物質と結合するイオンチャネル型受容体タンパク質に、少なくともイオンを含む液体試料または気体試料を供給して、液体試料または気体試料中に特定の化学物質が含まれているか否かの検出を行うものである。イオンチャネル型受容体タンパク質は、上記と同様のものであるので、ここでは説明を省略するものとする。
【0049】
イオンチャネル型受容体タンパク質を用いて行う化学物質検出方法によれば、上述したように、液体試料または気体試料中に検出対象である特定の化学物質が含まれている場合には、イオンチャネル型受容体タンパク質が特定の化学物質と結合することにより、イオンチャネルが開き、化学物質検出センサの内部にイオンチャネル型受容体タンパク質を介してイオンが流入する。このイオンの流れを例えば電流変化または電圧変化として捉えることによって、検出対象である特定の化学物質を検出することができる。
【0050】
(第2の実施形態)
以下、本発明による第2の実施形態について、図面を参照しながら説明する。図4は本実施形態に係る化学物質検出センサの概略構成図である。
【0051】
図4に示されるように化学物質検出センサ20は、細胞21を備えるものである。また、図4に示される化学物質検出センサ20は、さらに、溶出器22と、流路形成部材23とを備えるものである。
【0052】
細胞
細胞21は、細胞11と同様に、特定の化学物質と結合し、かつ生物から採取したイオンチャネル型受容体タンパク質を備えるものであるが、細胞21には更に例えばイオンの濃度によって蛍光強度が変化する蛍光物質(図示せず)が導入されている。細胞21としては、第1の実施形態で列挙されたものと同様のものが挙げられる。
【0053】
蛍光物質としては、例えば、Na+に応答して蛍光強度が変化するナトリウムイオン感受性蛍光色素、Ka+に応答して蛍光強度が変化するカリウムイオン感受性蛍光色素、Ca2+に応答して蛍光強度が変化するカルシウムイオン感受性蛍光色素等が挙げられる。ナトリウムイオン感受性蛍光色素としては例えばSBFI、CoroNa等が挙げられ、カリウムイオン感受性蛍光色素としては例えばPBFI等が挙げられ、カルシウムイオン感受性蛍光色素としては例えばFura-2、Fluo-3、Fluo-4等が挙げられる。
【0054】
溶出器および流路形成部材
溶出器22は溶出器12と同様のものであり、また流路形成部材23は流路形成部材13と同様のものであるので、説明を省略する。
【0055】
このような化学物質検出センサ20によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、気体試料から気体試料に含まれる化学物質を溶出器22によりイオン含有溶液に溶出させて、液体試料を得る。そして、流路23aを介して、溶出した化学物質およびイオンを含む液体試料を、蛍光物質が導入された細胞21に供給する。液体試料に含まれている化学物質が、検出対象である特定の化学物質ではない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、液体試料に含まれているイオンが細胞21内に流入せず、蛍光強度の変化はほぼ生じない。これに対し、液体試料に含まれている化学物質が、検出対象である特定の化学物質である場合には、化学物質との結合によりイオンチャネル型受容体のイオンチャネルが開き、液体試料に含まれているイオンが細胞21内に流入する。そして、このイオンの流入により、蛍光物質の蛍光強度が変化するので、この蛍光強度の変化を計測することにより、検出対象である特定の目的とする化学物質を検出することができるとともに、この特定の化学物質の濃度を測定することができる。
【0056】
本実施形態によれば、電極を細胞21に刺入する必要がないので、培養細胞のような大きさが非常に小さい細胞であっても、容易に化学物質の検出を行うことができる。
【0057】
(第3の実施形態)
以下、本発明による第3の実施形態について、図面を参照しながら説明する。図5は本実施形態に係る化学物質検出センサの概略構成図である。
【0058】
図5に示されるように化学物質検出センサ30は、脂質二重膜31を備えるものである。また、図5に示される化学物質検出センサ30は、さらに、溶出器32と、流路形成部材33、34と、電流測定器35を備えるものである。
【0059】
脂質二重膜
脂質二重膜31には、イオンチャネル型受容体タンパク質が組み込まれている。このような脂質二重膜31は、無細胞タンパク質発現系によるイオンチャネル型受容体タンパク質の合成と脂質二重膜の形成を同時に行うことにより得ることができる。
【0060】
溶出器
溶出器32は溶出器12と同様であるので説明を省略する。
【0061】
流路形成部材および電流測定器
流路形成部材33、34は脂質二重膜31を挟持するように、流路形成部材33は脂質二重膜31の上側に配置されており、流路形成部材34は脂質二重膜の下側に配置されている。流路形成部材33、34は、流路33a、34aを有し、流路形成部材33、34は流路33a、34aが向かい合わせとなるように配置されている。すなわち、流路33a、34aに、溶出器32によって溶出させた化学物質およびイオンを含む液体試料を流すと、液体試料は脂質二重膜31に接触する。電流測定器35は、流路33a、34a内を流れるイオン含有溶液間の電流を測定するものである。
【0062】
このような化学物質検出センサ30によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、気体試料から気体試料に含まれる化学物質を溶出器35によりイオン含有溶液に溶出させて、液体試料を得る。そして、流路33、34に、溶出した化学物質およびイオンを含む液体試料を流す。液体試料に含まれている化学物質が、検出対象である特定の化学物質ではない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、液体試料に含まれているイオンが流路34aに流入せず、電流変化はほぼ生じない。これに対し、液体試料に含まれている化学物質が、検出対象である特定の化学物質である場合には、化学物質との結合によりイオンチャネル型受容体のイオンチャネルが開き、流路33a内の液体試料に含まれているイオンが脂質二重膜31を介して、流路34aに流入する。このイオンの流入により、液体試料間に流れる電流が変化するので、この電流変化を電流測定器35により測定することにより検出対象である特定の化学物質を検出することができるとともに、この特定の化学物質の濃度を測定することができる。
【0063】
(第4の実施形態)
以下、本発明による第4の実施形態について、図面を参照しながら説明する。図6は、第4の実施形態に係る化学物質検出センサの概略構成図であり、図7は検知部の一例を示した概略構成図である。
【0064】
図6に示されるように化学物質検出センサ40は、トランスジェニックカイコガ41を備えるものである。また、図6に示される化学物質検出センサ40は、さらに、トランスジェニックカイコガ41を収容する筺体42と、外気を筺体42内に取り込む吸引ポンプ43、およびトランスジェニックカイコガ41の動作を検知する検知部44とを備えるものである。
【0065】
トランスジェニックカイコガ
トランスジェニックカイコガ41は、カイコガ以外の生物のイオンチャネル型受容体タンパク質をコードする遺伝子が導入され、ボンビコール受容細胞でイオンチャネル型受容体タンパク質が発現しているものである。なお、本実施形態では、トランスジェニックカイコガ41を用いているが、ショウジョウバエのエンプティニューロンなどを用いてもよい。
【0066】
このようなトランスジェニックカイコガ41は、例えば、マイクロインジェクション法、ウイルス感染を用いた方法等の公知の遺伝子導入技術により得ることができる。これらの中でも、次代への導入遺伝子の伝達効率の点からマイクロインジェクション法が好ましい。
【0067】
具体的には、トランスジェニックカイコガ41は、以下の方法により作製することができる。例えば、野生型のカイコガの性フェロモン受容体に対応する遺伝子であるBmOR1上流配列の下流部に転写制御因子であるGAL4遺伝子を配置させたDNAコンストラクトを作成し、野生型のカイコガの卵のゲノム領域に組み込み、育成する。組み込まれたBmOR1のプロモーターにより、性フェロモン受容細胞でのみGAL4が発現する。
【0068】
また、導入するイオンチャネル型受容体に対応する遺伝子の上流部にUAS(Upstream Activator Sequence)を組み込んだDNAコンストラクトを作成し、野生型のカイコガの卵のゲノム領域に組み込み、育成する。UASはGAL4の認識配列であり、GAL4の存在下においてUASの下流の任意の遺伝子の発現を誘導する。
【0069】
そして、それぞれ育成した、GAL4トランスジェニックカイコガと、UASトランスジェニックカイコガとを交配させて、二重トランスジェニック個体であるトランスジェニックカイコガ41を得る。この方法により作製したトランスジェニックカイコガ41は、GAL4が発現している性フェロモン受容細胞においてのみ、UASの下流に存在する目的のイオンチャネル型受容体タンパク質を発現させることができる。また、この方法で作製したトランスジェニックカイコガにおいては、一度このカイコガの育成を行なえば、次代以降のカイコガは全て同じトランスジェニックカイコガとして育成できる。
【0070】
野生型の雄のカイコガは、雌のカイコガから発生されるフェロモン物質である下記式(2)で示されるボンビコール(Bombykol)を特異的に認識し、匂い源の探索行動が発現する。匂い源の探索行動とは、具体的には、普段は静止状態にあるカイコガが、羽ばたきを始め、化学物質の源を探索し動き始める行動のことを指す。この探索行動は、普段の静止状態とは明確に区別し得る。このボンビコールは、カイコガの触角に存在する嗅覚感覚子内にあるボンビコール受容細胞によって受容される。ボンビコールの受容によってボンビコール受容細胞の神経興奮が発生したときだけ匂い源の探索行動が発現する。なお、特異的に認識するとは、特定の化学物質にのみ匂い源の探索行動が発現することを示し、他の化学物質に関してはその探索行動が発現しないことを意味する。したがって、野生型のカイコガはボンビコールでは匂い源の探索行動が発現するが、他の化学物質には探索行動は発現しない。
【化2】

【0071】
これに対し、トランスジェニックカイコガ41は、ボンビコール受容細胞にボンビコール以外の化学物質と結合するイオンチャネル型受容体タンパク質をコードする遺伝子が導入され、かつこのイオンチャネル型受容体タンパク質が発現しているものであるので、導入したイオンチャネル型受容体タンパク質が結合する化学物質に対してボンビコール受容細胞の神経興奮が起こり、匂い源の探索行動が発現する。具体的には、トランスジェニックカイコガ41が、導入したイオンチャネル型受容体タンパク質が結合する化学物質を受容すると、イオンチャネルが開き、リンパ液に含まれるイオンが流入して、ボンビコール受容細胞の神経興奮が起こる。これにより、トランスジェニックカイコガ41は、羽ばたきを始めて、化学物質の源を探索し始める。したがって、この挙動をモニタリングすることによって、化学物質の検出が可能になる。
【0072】
筺体
筺体42は、少なくとも1匹のトランスジェニックカイコガ41を収容することができれば特に限定されないが、複数匹のトランスジェニックカイコガ41を収容できるものが好ましい。複数匹のトランスジェニックカイコガ41を用いることにより、化学物質を検出するセンサとしての正確性を向上させることができる。筺体42は吸気口42aおよび排気口42bを備えている。
【0073】
吸引ポンプ
吸引ポンプ43は、排気口42bに接続されている。吸引ポンプ43を作動させることにより、吸気口42aを介して外気を筺体42内に取入れることができる。
【0074】
検知部
検知部44としては、トランスジェニックカイコガ41の動作を直接的または間接的に検知することができれば特に限定されない。検知部44として、例えば、動体センサ、トランスジェニックカイコガ41の動作に伴う振動を検知する振動センサ、トランスジェニックカイコガ41の動作に伴う音を検知する音センサ等を用いることができる。なお、検知部44を設けずに目視によりトランスジェニックカイコガ41の動作を検知してもよい。
【0075】
また、検知部44として、図7に示されるようなトランスジェニックカイコガ41を吊下げる吊下部材44aと、吊下部材44aで吊下げられたトランスジェニックカイコガ41の足に接触し、かつ回転可能に設置された球44bと、球44bの動きを検知する例えば光学マウス等の動体センサ44cとを備えるものを使用してもよい。なお、球44bと動体センサ44cとを備えるトラックボールを用いてもよい。このような検知部44を用いることにより、トランスジェニックカイコガ41の動作を検知できるだけでなく、トランスジェニックカイコガ41の行動解析を行うことができる。
【0076】
このような化学物質検出センサ40によれば、以下のようにして、目的とする化学物質を検出することができる。まず、吸引ポンプ43を作動させて、筺体42内に外気を取り込む。取り込まれた外気(気体試料)に検出対象である特定の化学物質が含まれていない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であるので、トランスジェニックカイコガ41は特異的な挙動は示さない。これに対して、取り込まれた外気に検出対象である特定の化学物質が含まれていた場合には、イオンチャネル型受容体のイオンチャネルが開き、トランスジェニックカイコガ41は羽ばたきを始め、化学物質の源の探索を始める。そして、この際の動作やこの際に発生する振動や音を検知部44で検知することにより、検出対象である特定の化学物質を検出することができる。
【0077】
カイコガの触角は非常に高感度であるので、トランスジェニックカイコガ41においても、検出対象である特定の化学物質が例えば気体中に数100分子程度存在すれば、検知することができる。さらに、例えばマイクロインジェクション法等により子孫に導入遺伝子を伝達させることができる場合には、一度遺伝子をカイコガに導入すればよいので、トランスジェニックカイコガ41の飼育費用等を考慮しても、トランスジェニックカイコガ41を非常に安価で得ることができる。さらに、トランスジェニックカイコガ41は野生型のカイコガと同様に体長3cm程度であるので、小型のセンサを得ることができる。したがって、本実施の形態によれば、トランスジェニックカイコガ41を用いているので、高感度であり、小型であり、かつ安価な化学物質検出センサ40を提供することができる。
【0078】
また、空気中での化学物質の分布は、単純に拡散して連続的になっておらず、小さい多数の断続的な塊となって浮遊している。すなわち、発生源の近くでは濃度が高く、遠ざかるにつれて低くなるという単純な分布ではない。このため、化学物質の発生源の探索は困難であり、発生源の特定を行うには、濃度の高い方向へただ遡って行くだけでは不十分であり、高度な行動アルゴリズムが必要となる。
【0079】
一方で、野生型の雄のカイコガは非常に高度な行動アルゴリズムを用いて雌のカイコガを探索している。本実施形態によるトランスジェニックカイコガ41は、この高度な行動アルゴリズムを用いることができるので、目的とする化学物質の発生源を探索することができる。
【0080】
(第5の実施形態)
以下、本発明による第5の実施形態について、図面を参照しながら説明する。図8は、第5の実施形態に係る化学物質検出センサの概略構成図であり、図9は第5の実施形態に係る他の箇所に電極を配置した図である。
【0081】
図8に示される化学物質検出センサ50は、トランスジェニックカイコガの触角51と、一対の電極52と、電位測定器53とを備えている。図8に示される化学物質検出センサ50は、さらに、触角51を収容する筺体54と、外気を筺体54内に取り込む吸引ポンプ55とを備えている。
【0082】
触角
触角51は、第4の実施形態で説明したトランスジェニックカイコガ41から切り取られたものである。
【0083】
電極
一対の電極52は、触角51に接続されている。図8に示される化学物質検出センサ50においては、一方の電極52(記録電極)が触角51の先端部51aに接続されており、他方の電極52(不関電極)は触角51の根元部51b、すなわち脳に繋がる神経の軸策部位に接続されている。なお、先端部51aは、電極52を接続する前に多少先端が切り落とされたものである。この場合には、その触角51に存在する全ての嗅覚感覚子からの電位の総和が得られる。
【0084】
また、電極52は、図9に示されるように触角51中に存在する一つの嗅覚感覚子51cに接続してもよい。この場合には、一つの嗅覚感覚子51cから電位が得られる。
【0085】
電位測定器
電位測定器53は、嗅覚感覚子が目的とする化学物質を受容したとき、触角全体または一つの嗅覚感覚子から発生する電位を測定するものである。図8のように触角51全体から発生する電位を測定する場合には、電位測定装置53としては、触角電図法(EAG: electroantennogram recording)を用いた装置が挙げられる。また、図9のように一つの嗅覚感覚子51cから発生する電位を測定する場合には、単一感覚子記録法(single sensillum recording)を用いた装置が挙げられる。
【0086】
筺体および吸引ポンプ
筺体54は、吸気口54aおよび排気口54bを備えている。また、吸引ポンプ55は、排気口54bに接続されている。吸引ポンプ55を作動させることにより、吸気口54aを介して外気を筺体54内に取入れることができる。
【0087】
このような化学物質検出センサ50によれば、以下のようにして、検出対象である特定の化学物質を検出することができる。まず、吸引ポンプ55を作動させて、筺体54内に外気を取り込む。取り込まれた外気に検出対象である特定の化学物質が含まれていない場合には、イオンチャネル型受容体のイオンチャネルは閉じたままの状態であり、触角51は電気応答を示さない。これに対して、取り込まれた外気に目的とする化学物質が含まれていた場合には、イオンチャネル型受容体のイオンチャネルが開き、触角51は電気応答を示し、電位が検知される。これにより、検出対象である特定の化学物質を検出することができる。
【0088】
本実施の形態によれば、トランスジェニックカイコガから切り取った触角51を用いているので、高感度であり、安価であり、さらにより小型の化学物質検出センサ10を提供することができる。
【0089】
また、触角電図法では目的とする化学物質の濃度が高いほど、検知される電位が大きくなるので、電位の大きさによって目的とする化学物質の濃度を測定することができる。また、単一感覚子記録法では目的とする化学物質の濃度が高いほど、検知される活動電位数が増加するので、活動電位数の数によって目的とする化学物質の濃度を測定することができる。
【実施例】
【0090】
以下、実施例により本発明を更に詳細に説明するが、これら実施例に本発明が限定されるものではない。
【0091】
実施例1
まず、アフリカツメガエルの卵母細胞に、キイロショウジョウバエの触角から単離したイオンチャネル型受容体タンパク質をコードする遺伝子DmIR84aをマイクロインジェクション法により導入して、イオンチャネル型受容体タンパク質が発現した卵母細胞を得た。ここで、このキイロショウジョウバエのイオンチャネル型受容体タンパク質は、フェニルアセトアルデヒドと選択的に結合するものである。
【0092】
また、化学物質検出センサを用意した。具体的には、上記卵母細胞の他、流路形成部材、電極としてのガラス電極、ガラス電極に電気的に接続された電流測定器を用意した。そして、流路形成部材に形成された流路内に上記イオンチャネル型受容体タンパク質が発現した卵母細胞を1つ配置し、この卵母細胞にガラス電極を刺入した。流路には、1ml/min程度のバッファ(緩衝液)を流し、常に新鮮なバッファが卵母細胞に供給されるようにした。また、流路の上流より、バッファ、および10μMに希釈したアンモニア、ブチルアミン、ペンチルアミン、p−クレゾール、フェニルアセトアルデヒドを、1種類ずつ所定時間をおいてピペットにより順次供給した。そして、そのときのガラス電極間に流れる電流を電流測定器により測定した。
【0093】
以下、結果について述べる。図10は実施例1に係る卵母細胞の各化学物質に対する電流応答を示したグラフである。図10に示されるように卵母細胞は、フェニルアセトアルデヒドに対して電流応答を示したが、バッファ、アンモニア、ブチルアミン、ペンチルアミン、p−クレゾールに対して電流応答を示さなかった。
【0094】
この結果から、アフリカツメガエルの卵母細胞にキイロショウジョウバエ由来のイオンチャネル型受容体タンパク質をコードする遺伝子、DmIR84aを導入して、卵母細胞にてDmIR84a遺伝子のコードするイオンチャネル型受容体タンパク質を発現させた場合、導入した受容体が結合するフェニルアセトアルデヒドを卵母細胞で応答させることができることが確認された。
【0095】
実施例2
実施例1においては、1個のアフリカツメガエルの卵母細胞を用いて実験が行われたが、実施例2においては、5個のアフリカツメガエルの卵母細胞を用いて実験が行われた。
【0096】
それぞれのアフリカツメガエルの卵母細胞に、実施例1と同様に、キイロショウジョウバエの触角から単離したイオンチャネル型受容体タンパク質をコードする遺伝子、DmIR84aをマイクロインジェクション法により導入して、DmIR84a遺伝子のコードするイオンチャネル型受容体タンパク質が発現した卵母細胞を得た。
【0097】
比較例1
複数のアフリカツメガエルの卵母細胞のそれぞれに、キイロショウジョウバエの触角から単離した、先程とは別種のイオンチャネル型受容体をコードする遺伝子、DmIR31aをマイクロインジェクション法により導入し、DmIR31a遺伝子のコードするイオンチャネル型受容体タンパク質が発現した卵母細胞を得た。
【0098】
そして、実施例2に係る卵母細胞と、比較例1に係る卵母細胞に対して、実施例1と同様の実験を行った。
【0099】
以下、結果について述べる。図11は実施例2および比較例1に係る卵母細胞の各化学物質に対する電流応答を示したグラフである。図11に示されるように比較例1に係る全ての卵母細胞は、バッファ、アンモニア、ブチルアミン、ペンチルアミン、p−クレゾール、およびフェニルアセトアルデヒドの全ての化学物質に対してほぼ電流応答を示さなかった。これに対し、実施例2に係る卵母細胞の内、5個中の4個については、バッファ、アンモニア、ブチルアミン、ペンチルアミン、p−クレゾールに対しては電流応答を示さなかったが、フェニルアセトアルデヒドに対しては電流応答を示した。
【0100】
これらの結果から、まさしく導入したキイロショウジョウバエ由来のイオンチャネル型受容体タンパク質DmIR84aによって、フェニルアセトアルデヒドに対する応答機能が発現されることができることが確認された。ここで、キイロショウジョウバエ触角においては、DmIR84a遺伝子がコードするイオンチャネル型受容体タンパク質の存在する細胞はフェニルアセトアルデヒドに応答を示すが、DmIR31a遺伝子がコードするイオンチャネル型受容体タンパク質の存在する細胞はフェニルアセトアルデヒドに応答を示さないことが知られている。以上の結果は、キイロショウジョウバエの触角における匂いに対する応答を、卵母細胞上で再現できたことを意味している。
【0101】
実施例3
野生型のカイコガを発砲スチロールの球の上に置き、吊下部材により野生型のカイコガを吊下げて固定した。その後、前方から野生型のカイコガのフェロモン物質であるボンビコールを吹き付けた。そして、野生型のカイコガの動きを光学マウスにより読み取り、野生型のカイコガの行動を解析した。
【0102】
以下、結果について述べる。図12は実施例3に係る野生型のカイコガのボンビコールに対する挙動を示したグラフである。
【0103】
図12から、フェロモン物質を受容したことによる匂い源の探索行動の発現を、目視ではなく、球と光学マウスを用いることで電気的に検出できることが確認された。
【符号の説明】
【0104】
10、20、30、40、50…化学物質検出センサ、11、21…細胞、12、22、32…溶出器、13、23、33、34…流路形成部材、13a、23a、33a、34a…流路、15、35…電流測定器、31…脂質二重膜、41…トランスジェニックカイコガ、44…検知部、51…触角、52…電極、53…電位測定器。
【特許請求の範囲】
【請求項1】
特定の化学物質を検出する化学物質検出センサであって、
生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質を備えることを特徴とする、化学物質検出センサ。
【請求項2】
前記イオンチャネル型受容体タンパク質が昆虫から採取されたものである、請求項1のいずれか1項に記載の化学物質検出センサ。
【請求項3】
前記昆虫が双翅目に属する昆虫である、請求項2に記載の化学物質検出センサ。
【請求項4】
前記昆虫が双翅目短角亜目ハエ下目ショウジョウバエ科に属する昆虫である、請求項3に記載の化学物質検出センサ。
【請求項5】
前記昆虫がキイロショウジョウバエである、請求項4に記載の化学物質検出センサ。
【請求項6】
前記化学物質がフェニルアセトアルデヒドであり、前記イオンチャネル型受容体タンパク質がキイロショウジョウバエ由来のDmIR84a遺伝子によりコードされるものである、請求項5に記載の化学物質検出センサ。
【請求項7】
前記イオンチャネル型受容体タンパク質が、前記イオンチャネル型受容体タンパク質をコードする遺伝子が導入された細胞において発現している、請求項1ないし6のいずれか1項に記載の化学物質検出センサ。
【請求項8】
前記細胞が、アフリカツメガエルの卵母細胞、培養細胞、大腸菌、酵母、カイコガの触角に存在するボンビコール受容細胞、ショウジョウバエのエンプティニューロン、および植物細胞からなる群から選択される、請求項7に記載の化学物質検出センサ。
【請求項9】
少なくともイオンを含む液体試料が流れ、かつ前記細胞が配置される流路を有する流路形成部材と、
前記流路の内部に配置された前記細胞に刺入される一対の電極と、
前記電極間に流れる電流を測定する電流測定器とをさらに備える、請求項7または8に記載の化学物質検出センサ。
【請求項10】
前記細胞がイオンの濃度によって蛍光強度が変化する蛍光物質を含み、
少なくともイオンを含む液体試料が流れ、かつ前記細胞が配置される流路を有する流路形成部材をさらに備える、請求項7または8に記載の化学物質検出センサ。
【請求項11】
気体に含まれる化学物質をイオン含有溶液に溶出させて、前記液体試料を得るための溶出器をさらに備える、請求項9または10に記載の化学物質検出センサ。
【請求項12】
前記イオンチャネル型受容体タンパク質が発現している細胞が、トランスジェニックカイコガの触角に存在するボンビコール受容細胞またはショウジョウバエのエンプティニューロンであり、
前記触角と、
前記触角に刺入される一対の電極と、
前記電極の電位を測定する電位測定器とをさらに備える、請求項7に記載の化学物質検出センサ。
【請求項13】
前記イオンチャネル型受容体タンパク質が発現している細胞が、トランスジェニックカイコガの触角に存在するボンビコール受容細胞またはショウジョウバエのエンプティニューロンであり、
前記トランスジェニックカイコガまたはショウジョウバエの動作を検知する検知部をさらに備える、請求項7に記載の化学物質検出センサ。
【請求項14】
前記イオンチャネル型受容体タンパク質が、脂質二重膜に組み込まれている、請求項1ないし6のいずれか1項に記載の化学物質検出センサ。
【請求項15】
少なくともイオンを含む液体試料が流れる流路をそれぞれ有する2つの流路形成部材と、
前記流路内を流れる前記液体試料間の電流を測定する電流測定器とをさらに備え、
前記2つの流路形成部材が、前記流路が向かい合うように前記脂質二重膜を介して配置されている、請求項14に記載の化学物質検出センサ。
【請求項16】
気体に含まれる化学物質をイオン含有溶液に溶出させて、前記液体試料を得るための溶出器をさらに備える、請求項15に記載の化学物質検出センサ。
【請求項17】
特定の化学物質を検出する化学物質検出方法であって、
生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質に、少なくともイオンを含む液体試料または気体試料を供給して、前記液体試料または気体試料中に特定の化学物質が含まれているか否かの検出を行うことを特徴とする、化学物質検出方法。
【請求項1】
特定の化学物質を検出する化学物質検出センサであって、
生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質を備えることを特徴とする、化学物質検出センサ。
【請求項2】
前記イオンチャネル型受容体タンパク質が昆虫から採取されたものである、請求項1のいずれか1項に記載の化学物質検出センサ。
【請求項3】
前記昆虫が双翅目に属する昆虫である、請求項2に記載の化学物質検出センサ。
【請求項4】
前記昆虫が双翅目短角亜目ハエ下目ショウジョウバエ科に属する昆虫である、請求項3に記載の化学物質検出センサ。
【請求項5】
前記昆虫がキイロショウジョウバエである、請求項4に記載の化学物質検出センサ。
【請求項6】
前記化学物質がフェニルアセトアルデヒドであり、前記イオンチャネル型受容体タンパク質がキイロショウジョウバエ由来のDmIR84a遺伝子によりコードされるものである、請求項5に記載の化学物質検出センサ。
【請求項7】
前記イオンチャネル型受容体タンパク質が、前記イオンチャネル型受容体タンパク質をコードする遺伝子が導入された細胞において発現している、請求項1ないし6のいずれか1項に記載の化学物質検出センサ。
【請求項8】
前記細胞が、アフリカツメガエルの卵母細胞、培養細胞、大腸菌、酵母、カイコガの触角に存在するボンビコール受容細胞、ショウジョウバエのエンプティニューロン、および植物細胞からなる群から選択される、請求項7に記載の化学物質検出センサ。
【請求項9】
少なくともイオンを含む液体試料が流れ、かつ前記細胞が配置される流路を有する流路形成部材と、
前記流路の内部に配置された前記細胞に刺入される一対の電極と、
前記電極間に流れる電流を測定する電流測定器とをさらに備える、請求項7または8に記載の化学物質検出センサ。
【請求項10】
前記細胞がイオンの濃度によって蛍光強度が変化する蛍光物質を含み、
少なくともイオンを含む液体試料が流れ、かつ前記細胞が配置される流路を有する流路形成部材をさらに備える、請求項7または8に記載の化学物質検出センサ。
【請求項11】
気体に含まれる化学物質をイオン含有溶液に溶出させて、前記液体試料を得るための溶出器をさらに備える、請求項9または10に記載の化学物質検出センサ。
【請求項12】
前記イオンチャネル型受容体タンパク質が発現している細胞が、トランスジェニックカイコガの触角に存在するボンビコール受容細胞またはショウジョウバエのエンプティニューロンであり、
前記触角と、
前記触角に刺入される一対の電極と、
前記電極の電位を測定する電位測定器とをさらに備える、請求項7に記載の化学物質検出センサ。
【請求項13】
前記イオンチャネル型受容体タンパク質が発現している細胞が、トランスジェニックカイコガの触角に存在するボンビコール受容細胞またはショウジョウバエのエンプティニューロンであり、
前記トランスジェニックカイコガまたはショウジョウバエの動作を検知する検知部をさらに備える、請求項7に記載の化学物質検出センサ。
【請求項14】
前記イオンチャネル型受容体タンパク質が、脂質二重膜に組み込まれている、請求項1ないし6のいずれか1項に記載の化学物質検出センサ。
【請求項15】
少なくともイオンを含む液体試料が流れる流路をそれぞれ有する2つの流路形成部材と、
前記流路内を流れる前記液体試料間の電流を測定する電流測定器とをさらに備え、
前記2つの流路形成部材が、前記流路が向かい合うように前記脂質二重膜を介して配置されている、請求項14に記載の化学物質検出センサ。
【請求項16】
気体に含まれる化学物質をイオン含有溶液に溶出させて、前記液体試料を得るための溶出器をさらに備える、請求項15に記載の化学物質検出センサ。
【請求項17】
特定の化学物質を検出する化学物質検出方法であって、
生物から採取され、かつ前記特定の化学物質と結合するイオンチャネル型受容体タンパク質に、少なくともイオンを含む液体試料または気体試料を供給して、前記液体試料または気体試料中に特定の化学物質が含まれているか否かの検出を行うことを特徴とする、化学物質検出方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図12】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図12】


【図10】


【図11】


【公開番号】特開2012−191904(P2012−191904A)
【公開日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願番号】特願2011−59370(P2011−59370)
【出願日】平成23年3月17日(2011.3.17)
【出願人】(000219967)東京エレクトロン株式会社 (5,184)
【出願人】(511070123)
【出願人】(511070134)
【出願人】(511070145)
【Fターム(参考)】
【公開日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願日】平成23年3月17日(2011.3.17)
【出願人】(000219967)東京エレクトロン株式会社 (5,184)
【出願人】(511070123)

【出願人】(511070134)

【出願人】(511070145)

【Fターム(参考)】
[ Back to top ]

