化粧品分野におけるエステル交換オリーブ油の使用
化粧品活性成分及び/又は皮膚科学的活性成分の浸透速度を増大させるための、又は化粧品モイスチャライザーとしての、エステル交換オリーブ油の使用が開示される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、皮膚浸透特性の向上のための、化粧品分野におけるエステル交換オリーブ油の使用に関する。
【背景技術】
【0002】
皮膚中に活性成分を浸透させるという課題は、化粧品において、さらにはおそらく皮膚科学においても劇的な重要性を有している。しかし、ほとんどの活性成分の自然浸透の速度は、その活性成分の作用の有効性を低下させ、又はさらには該作用を完全に無効にする場合があるものであることが多い。これを克服するために、それ自体の中に活性成分を埋め込むことにより、活性成分をその自然の速度より大きな速度で皮膚中に浸透させ、その結果その効果を十分且つ適時なものとする薬剤を見出すことが有用である。それにより多くの場合では、活性成分の濃度を低減することにより、任意の考え得る副作用を最小限まで低減することも可能であろう。原理としては、送達の促進により、角質層を通り抜けることを可能とするために本来化学的に変換する必要がある活性成分を使用することも、可能となるだろう。この種の浸透向上剤での課題は、該浸透向上剤は、活性成分の作用を無効にすることもその特性を損なうこともないように、その活性成分と有意に相互作用することなく、このような促進をもたらさなければならないことである。
【0003】
1つの方法は、細胞を或る程度破壊することにより浸透抵抗性を低減する少量の毒性物質を、化粧品製品に添加することであろう。しかしこの方法は、皮膚を不可逆的に損傷する危険があるので、回避すべきである。
【0004】
また、モイスチャライザーの塗布は、良好な皮膚浸透特性を必要とする。皮膚の水和及びその変動は、皮膚の健康及び皮膚の外観と相関することが多い。したがって、正常な皮膚の水和を欠くことは、潜在的に重大な美容上の関心事と関連することが多く、苦痛とさらには皮膚障害とを引き起こし得る。皮膚による2つの生理学的調節メカニズムが存在する:1)天然の加湿因子、及び2)角化細胞の間に位置する細胞間脂質層。上記角化細胞は、親油性であり、表皮を通じた過剰な水の蒸発を防ぐ。表皮角化細胞及び細胞間脂質層が皮膚のバリア機能を確定するが、脂質部分は主たる役割を果たす。したがって表皮の正常な生理学的バリア機能は、細胞間脂質が浸透する高度に規則的な薄膜に基づく。実際には、表皮角質層においては、細胞間脂質は、層状のゲル相中、及び層状の液晶中に集積している。
【0005】
皮膚水和を調節するための最も慣用されている方法は、エモリエント又は保湿剤の局所塗布にある。
【0006】
エモリエントは細孔の部分的な閉塞をもたらし、皮膚の角質層を軟化し、加湿し、その外観を向上させることができる。
【0007】
他方、保湿剤は概して、大気中の水分と結合することができる例えば尿素又はグリセロール等の吸湿性の分子であり、皮膚の水分を適度なバランスに維持するのを助ける。
【0008】
しかし、エモリエントも保湿剤も、皮膚のバリア機能の完全性(integrity)に影響を与えない。
【0009】
概して、皮膚は、身体の表面上に存在し、内部器官を保護する覆いの役割を果たし、内部器官が環境と直接接触するのを防ぐ。いずれにせよ、皮膚は極めて複雑であり、細胞内分泌(intracrinous)能及びパラ分泌(paracrinous)能の両方を有する。したがって、皮膚は、紫外線(メラニン形成)から保護し、免疫保護をもたらし、外来粒子の浸透を防ぐバリア機能を有する。皮膚はまた、内部の水分のレベルの管理に動的に関与する。皮膚は、ビタミンDの光生成、及び栄養として導入したビタミンEの分布の場所でもある。
【0010】
主要な皮膚の層は、真皮及び表皮である。真皮は、コラーゲン、エラスチン等の細胞外成分、及び分散した常在線維芽細胞により産生及び分泌されるグリコサミノグリカンの合成の部位である。他方、表皮の細胞密度は非常に高く、主に角化細胞により代表される。表皮は、外側への流れと、表皮基底層から角質層(SC)までに由来する細胞の分化とにより、常に自己再生する。表皮の最外層である角質層は、透過性バリアのほとんどを供給し、該透過性バリアは、脂質に富む細胞外マトリクス中への組織立った角化細胞の埋め込みにより主に供給されている。
【0011】
化学的分析により、角質層の細胞間脂質は、主にセラミド、コレステロール、コレステロールエステル及び脂肪酸から成る(それら自体は角化細胞により合成される)ことが示されている。これらの脂質の三次元構成は、種々の異なるモデルの示唆をもたらす種々の研究の対象となっている(非特許文献1)。最近のモデル(非特許文献2)では、角質層の脂肪(モルタル)が、角化細胞(ブリック)の間に見出される多層状の系として配置される、結晶性ゲルの形態で存在することが示唆されている。角質層及び角化細胞の脂質の構成を可視化する方法は、ブリック壁(ここで、角化細胞を表すブリックはモルタルの脂質層中に、整然と並置され且つ挟まれて(chelated)いる)を画像化(imagine)することである。細胞成分の完全性は既知であり、特に角質層の脂質層はバリア機能の完全性を必然的に維持するはずである。角質層のバリア機能の破壊は、経皮水分喪失量の増大と、その結果として皮膚水和レベルの低減とを引き起こし、既に上で示した負の結果をもたらす。
【0012】
細胞間脂質の薄膜(結晶性ゲル)に加えて、皮脂由来の他の種類の脂質も、角質層中で重要な役割を果たす。皮脂中に見出される主要な脂質は、コレステロール、ステロール及びワックスエステル、トリグリセリド、並びにスクアレン(非特許文献3)である。トリグリセリドは、皮脂腺の内側で産生され、遊離脂肪酸の形態で放出され得る。角質層の外表面における沈着後、皮脂の脂肪(又は皮膚の表面脂質)は、一過性の抗酸化剤(α−トコフェロール)として(非特許文献4)、抗微生物(anti-microbic)作用を発揮する(非特許文献5及び非特許文献6)と共に、標的となる生物学的目的を有する重要な分子を供給する。例えば、トリグリセリドの加水分解により得られる可能性がより高いグリセロールは、吸湿剤として働き、角質層の水を保持する能力に関与する(非特許文献7)。オレイン酸及びリノール酸等の幾つかの脂肪酸は、ペルオキシソーム増殖因子活性化受容体(PPAR)の結合因子として振る舞う。PPARの活性化は、角膜実質細胞分化(非特許文献8)に、及びバリアを急速に排除した後の加速バリア機能の回復(非特許文献9、非特許文献10)に関与することが示されている。角質層の外表面上で分泌されるにもかかわらず、さらなる深層の脂質形状の完全性の維持において、皮脂の脂肪は顕著に影響され得る。多数の研究により、脂質のカテゴリーに依存して、皮膚の皮脂表面脂質の勾配が角質層を通じて検出されることが証明されている(非特許文献11、非特許文献12、非特許文献13、非特許文献14、非特許文献15、非特許文献16)。
【0013】
角化細胞の表皮での役目は、落屑(desquamation)プロセスにより終了する。角化細胞(又は角質細胞)の剥離は、表皮の再生に必要なプロセスであり、種々の酵素のタンパク質加水分解作用により得られ得る(非特許文献17)。落屑現象が、角質層の細胞間脂質層状マトリクスにおいて、或る特定の程度の構造崩壊を引き起こし得ることが示唆されている(非特許文献18、非特許文献19)。剥離プロセスは、(壁からのブリックの除去が周囲のモルタルを粉砕するのと同様に)基礎となる脂質マトリクス中に小さい隙間を開ける、不安定化させる操作として表すことができる。このような微小孔は、皮脂の脂質を角質層の脂質対応物と混合する径路となり得る。角質層の内層のこれらの特徴部と皮脂の脂質との混合が、その後起こり得る。まとめると、これらの研究により、皮膚表面中における、及び表皮全体のための、皮脂生成物の生理学的重要性が確立されている。
【先行技術文献】
【非特許文献】
【0014】
【非特許文献1】Madison, 2003
【非特許文献2】Norlen, 2001
【非特許文献3】Stewart, 1992
【非特許文献4】Thiele, 1999
【非特許文献5】Georgel, 2005
【非特許文献6】Willie, 2003
【非特許文献7】Fluhr, 2003
【非特許文献8】Komuves, 2000
【非特許文献9】Schurer, 2002
【非特許文献10】Mao Qiang, 2004
【非特許文献11】Blanc, 1989
【非特許文献12】Norlen, 1998
【非特許文献13】Sheu, 1999
【非特許文献14】Thiele, 1999
【非特許文献15】Norlen, 2001
【非特許文献16】Yagi, 2007
【非特許文献17】Houben, 2007
【非特許文献18】Norlen, 2001
【非特許文献19】Sheu, 1999
【発明の概要】
【発明が解決しようとする課題】
【0015】
本発明の目的は、高浸透皮膚科学的薬剤であって、一方で活性成分の皮膚中へのより速い浸透を可能にし、他方で生体模倣再構築剤として働く、高浸透皮膚科学的薬剤を設計することである。本発明は、角質層の細胞間脂質の薄膜の分子構成を模倣する(mimike)ように、皮膚適合性液晶を生成するための、皮膚中で見出される脂肪酸組成に類似する脂肪酸組成に主に基づく。このように形成される液晶は、皮膚層を高速で通過し、皮膚の脂質バリア中で生理学的に集積し、その完全性を強化する可能性を有するはずである。
【課題を解決するための手段】
【0016】
上で述べた目的は、皮膚浸透特性の向上のための、化粧品分野におけるエステル交換オリーブ油の使用に関する本発明により、見事に達成される。
【0017】
ここで、本発明を、以下の添付の図面を参照して、さらに詳細に示す。
【図面の簡単な説明】
【0018】
【図1】RHEの組織切片(表皮−多孔質膜)のヘマトキシリン・エオシン染色結果を示す図である。
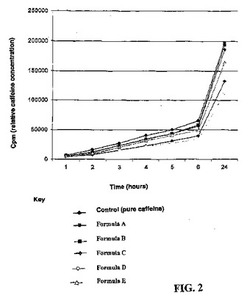
【図2】多孔質膜の他方の側におけるカフェインの蓄積を示す図である。
【図3】セテアリルオリベート、ソルビタンオリベートの液晶構造を示す走査電子顕微鏡(SEM)画像である。
【図4】皮膚バリア完全性に対する、セテアリルオリベート、ソルビタンオリベートの存在の、及び他の脂質組成物の存在の効果を示す図である。
【図5】グリセリンの水和特性と、セテアリルオリベート、ソルビタンオリベートの水和特性との間の比較を示す図である。
【図6】セテアリルオリベート、ソルビタンオリベートの皮膚水和に関する機能的有効性を示す図である。
【図7】本発明によるエステルの作用メカニズムのイラストである。
【発明を実施するための形態】
【0019】
言うなれば、オリーブ油は、その起源と、年数及び加工方法に依存する、オリーブ油を得るのに利用したオリーブの種類とに従って変化する、脂肪酸エステルの混合物である。しかし、種々のエステルの百分率は、或る特定の変動度ではあるが、十分に規定され且つ広範に知られた範囲内で変化するので、オリーブ油は、或る規定された組成物とみなすことができる。
【0020】
オリーブ油のエステル交換は、有機化学の通常の手順に従って、任意のアルコール又はアルコール混合物により行うことができる。特に、セテアリルアルコール及び/又はソルビトールでエステル交換を行うことにより、妥当な結果が得られている。
【0021】
これらのアルコールの両方でオリーブ油のエステル交換を行うことにより、INCI命名法に従いセテアリルオリベート、ソルビタンオリベートと特定される生成物が形成される。この生成物は、液晶の形態で見出される。
【0022】
特に効果的な製造プロセスに従い、オリーブ油を最初に、通常の条件下でけん化する(undergopes saponification)。得られた脂肪酸を、その後部分的にセテアリルアルコールで、部分的にソルビタンでエステル化し、得られた生成物を最終的に共に混合する。
【0023】
本出願人は、オリーブ油のエステル交換により得られる、セテアリルオリベート、ソルビタンオリベートにより生成される皮膚適合性液晶の経皮浸透における有効性を検証した。これは、一方で強力な水和効果を得るように水の蒸散を抑える能力、及び他方でこのような結晶が生物活性分子の経皮浸透を向上させるのに使用することができることを含む。
【0024】
本発明はオリーブ油をエステル交換することにより得ることができる全ての生成物に関するが、以下の本発明の例示的な説明において使用される成分(INCI:セテアリルオリベート、ソルビタンオリベート)は、親水性又は親油性の意味において特徴的な自己乳化特性を有する、皮膚表面の脂質組成と化学的に関連する、脂肪酸の複雑な組合せである。したがってセテアリルオリベート、ソルビタンオリベートは、1)皮膚バリア完全性を再構築及び維持する、並びに2)それ自体が乳化基剤をもたらすという2本立て(double feature)が期待される単一の生体模倣再構築剤を表す。これにより、塗布後に「生理学的に」自然な皮膚の感覚をもたらす、生物学的に機能的な化粧品製剤の創出がもたらされる。
【0025】
これらの成分の特殊性は、これらの成分が、これらの生成物の皮脂との類似性により、皮膚表面上で見出されている脂肪酸組成(表1)を化学的に(及び生理学的に)十分に再現する脂肪酸の組合せから成ることである。先に言及したように、皮膚表面の脂肪(皮脂脂肪酸)は、角質層の内層中に浸透し、角質層の細胞間脂質の層状マトリクスに埋め込み、且つバリア層の一部分となるこの能力を有する。したがって、皮脂を再現する脂肪酸組成を使用して、角質層の内層に接近するためのその天然の「エントリーカード」を利用することが可能になる。したがって、オリーブ油を出発材料として使用することにより、本出願人は、角質層の脂質の層状の系に対するその天然の親和性を通じて生理学的作用が委ねられる、セテアリルオリベート、ソルビタンオリベート等の化粧品成分を得ることに成功した。
【0026】
【表1】

【0027】
単一の脂肪酸組成を有することに加えて、その成分であるセテアリルオリベート、ソルビタンオリベートは、図3において強調したように、乳化されると液晶形状をとる。これらの液晶は、角質層の脂質薄膜において観察される分子構造と類似する分子構造を有する。実際には、液晶の壁は、脂肪酸及び水の交互の層から成るので、角質層の標準的な細胞間脂質のマトリクス構造を再現している(Norlen, 2001)。したがって、セテアリルオリベート、ソルビタンオリベートの生体模倣は、1)皮膚表面の脂質組成を有する化学的模倣、及び2)角質層の、細胞間脂質の層状の構成を有する構造上の模倣という2つの側面がある。以下で、セテアリルオリベート、ソルビタンオリベートにより形成されるこれらの構造(例えば生体適合性液晶)に言及する。
【0028】
第1の態様によれば、エステル交換オリーブ油の皮膚浸透特性と、その特徴的な構造とにより、皮膚の最内層中に化粧品活性分子及び/又は皮膚科学的活性分子を到達させてより顕著な及び/又はより適時な効果を得ることを可能とするために、化粧品活性分子及び/又は皮膚科学的活性分子を上記構造中に埋め込むことが可能となる。
【0029】
第2の態様によれば、エステル交換オリーブ油自体は、皮膚の最内層中に浸透すると、それ自体が埋め込まれてバリアとして働くことが可能であり、それにより皮膚を通じた水の過剰な蒸発を回避し、いかなる負の結果ももたらさずに最適な水和効果をもたらす。
【0030】
本発明の両方の態様が同じ現象(エステル交換オリーブ油の皮膚中への高い浸透速度)の直接の結果であることは明らかである。
【0031】
ここで本発明を、以下の非限定的な実施例に基づきさらに示す。
【実施例】
【0032】
実施例1
in vitroの再構築ヒト表皮(RHE)系を使用した。生物活性分子としてカフェインを選択した。RHE表面に塗布すると、カフェインは、表皮層中に浸透する能力を有する。カフェインの経皮浸透は、放射性マーカーを使用することにより定量化することができる。カフェインはまた、経皮浸透速度を向上させる際の上記薬剤の効果を検証するために、種々の製剤(エマルション)中に組み込むことができる。
【0033】
ヒト皮膚角化細胞を人工多孔質膜上に分散させ、上記角化細胞の分化を13日と報告される時期まで誘導した。再構築ヒト表皮(RHE)は、水−空気界面環境において規定の培養培地中で成長させる。RHEの組織学的構成が図1に示され、角質層の層を有する表皮の典型的な形状を示す。
【0034】
RHEを、37℃、5%CO2で、1mlの維持培地の存在下で、各々12ウェルを備えるプレート中に配置する。各々のウェル中のRHEは、個々の実験条件を代表するものとした。経皮的に浸透する能力を有する、RHEのチップに塗布した任意の物質は、RHEの下の培養培地中で収集し、好適な検出方法を使用して定量化することができる。
【0035】
表2に従い、様々な製剤を調製した。セテアリルオリベート、ソルビタンオリベート(Olivem 1000 Crystal Skin)を、種々の製剤環境中において形成された液晶として使用した(表2、A、B及びC)。対照処方も検証した(表2、D及びE)。
【0036】
放射性カフェイン(14C−カフェイン、1mCi/m、0.04mM、0.339mMの非放射性の(cold)カフェインに添加)をマーカーとして使用する。この混合物(他に特に記載がない限り、以下「カフェイン」と称する)は、水溶性生物活性分子を代表する。カフェインを、純品で(pure)又は種々の処方に組み込んで、試験した。カフェインを、緩やかに振とうしながら処方中に組み込み、試験前に終夜室温で維持した。
【0037】
【表2】

【0038】
処方A、処方B、処方C、処方D若しくは処方E又は純粋なカフェイン(対照)を、各ウェル中のRHE表面に塗布した。全条件をn=3で実施した。速度論的試料を、1時間、2時間、3時間、4時間、5時間、6時間及び24時間の7つの速度論的時間で、RHEの下の培養培地に配置した。収集した試料中に含有される放射能を、液体シンチレーションを使用して測定した。結果は、放出されたカフェインのcpm(1分当たりのカウント数)として表現し、表皮中のカフェインの相対濃度を表す。
【0039】
角化細胞の生存度を、MTTアッセイを使用して確認した:MTT塩(3−(4,5−ジメチル(dimetil)−チアゾール(tiaol)−2−イル(il))−2,5ジフェニルテトラゾリウムブロミド)は、生細胞に見出されるミトコンドリア酵素スクシネートデヒドロゲナーゼにより還元され得る。還元生成物ホルマザン結晶は、540mmでの光学密度により定量化することができ、生細胞数に比例する。MTTアッセイを、24時間時点で直ちに、RHEに対して実施した。
【0040】
これらの実験条件では、A製剤、B製剤、C製剤及びE製剤が、表皮中へのカフェイン通過を促進した。効果は、製剤で処理せず純粋なカフェインで処理した対照表皮と比較して、統計的に有意であった(p<0.05)。例えば、24時間時点直後では、処方A、処方B及び処方Cのみが、純粋なカフェイン(対照)と比較して、カフェインの浸透を有意に増大させた(p>0.01)。D処方及びE処方は、純粋なカフェイン(対照)と比較して、有意な効果を示さなかった(p>0.05)。処方Eの主成分(セテアリルアルコール及びセテアリルグルコシド)が液晶を生成することに留意しなければならない。これらの結果により、セテアリルオリベート、ソルビタンオリベートにより生成した液晶(皮膚適合性液晶)の化学的組成が独特であり、経皮浸透を有意に増大させるのに重要であることが証明される。さらに、このアッセイで観察された浸透増大効果は、MTTアッセイの結果は正常な生存度(細胞生存度100%)を示している(表3)ため、細胞生存度に対する負の効果で単純に説明することはできない。
【0041】
【表3】

【0042】
実施例2
セテアリルオリベート、ソルビタンオリベートにより生成される生体適合性液晶の臨床的効率性を、臨床的に検証した。最初に、その皮膚生体適合性を、他の脂質組成物との関連で、経皮水分喪失量(TEWL)に対するその効果に関する研究において検証した。TEWLは、皮膚透過性バリア機能を評価するための、バリデーションされた(convalidated)方法である(Fluhr, 2006)。10人のボランティアが、同一の濃度(5%)の以下の成分を局所的に塗布した:セテアリルオリベート、ソルビタンオリベート;セテアリルアルコール、セテアリルグルコシド;及びポリグリセリル(poliglyceril)−3メチルグルコースジステアレート。結果(図4を参照されたい)により、セテアリルオリベート、ソルビタンオリベートの塗布が、対照処方に対してTEWLの増大を29%低減したことが示されている(図2)。
【0043】
これらの結果は、局所的に塗布した脂質組成物と皮膚との間の生理学的適合性に関する必要性を支持する。セテアリルアルコール、セテアリルグルコシド、及びポリグリセリル−3メチルグルコースジステアレートは、塗布後の過剰の水分喪失をそれらが活性化するという事実により、非適合性脂質組成物としてのカテゴリーにおいて特定することができる。このことは、それを通じて水が出てくることができる微小孔の形成をもたらす、バリア完全性の一過性の不安定化と解釈することができる。TEWLは、バリア完全性が回復すると、徐々にベースライン値を取り戻す。適切な皮膚適合性脂質の組成及び比から成る、脂質組成の重要性は、証明されている(Mao Qiang, 1995、De Paepe, 2002)。皮膚の脂質組成を有するセテアリルオリベート、ソルビタンオリベートの適合性は、導いたTEWLの相対的に低いレベルで検出される。皮膚に塗布した成分の脂質組成は、形成した三次元形状よりも大きな重要性を有するようである。セテアリルオリベート、ソルビタンオリベートが液晶を生成することは、既に証明されている(図1)。興味深いことに、セテアリルアルコール及びセテアリルグルコシドも、乳化すると液晶を形成する能力を有する。化粧品製剤における液晶の利点は既知であるが、脂肪酸組成の観点では、その化学的製造によってのみ、液晶が皮膚と生理学的に適合性となる。セテアリルオリベート、ソルビタンオリベートにより得られた結果は、液晶構造を形成することの重要性のみでなく、それらを皮膚との化学的適合性を有する(非常に類似する)ものにして、所望の浸透効果及びモイスチャライジング効果をもたらし、最適なバリア完全性を維持すること(今日まで従来技術に基づいて予測することは不可能であった)の重要性をも明示している。
実施例3
全体の皮膚水和レベルはバリア機能及び水分保持能力に依存するので、セテアリルオリベート、ソルビタンオリベートの皮膚水和効果を、コルネオメトリー(corneometry)を利用してグリセリンの皮膚水和効果と比較した。グリセリンは皮脂腺により産生及び分泌され、天然皮膚保湿剤として働く(Fluhr, 2003)。10人のボランティアが、2%グリセリン及び0.4%キサンタンガムから成る溶液、並びに4%セテアリルオリベート、ソルビタンオリベートのエマルションを、前腕の手掌側の異なる部位に塗布した。期待した通り、図5において明らかなように、グリセリン溶液は、皮膚表面の水和の迅速な増大をもたらした。
【0044】
図5に示したグリセリンの皮膚水和ピークは徐々に消失し、塗布後45分から7時間まで、セテアリルオリベート、ソルビタンオリベートよりも有意に低い値に到達した。セテアリルオリベート、ソルビタンオリベートのエマルションは、水和の一過性のピークはもたらさなかったが、より安定な長期的効果をもたらした。この効果は、セテアリルオリベート、ソルビタンオリベートにより形成される皮膚適合性液晶の生理学的浸透及び集積により、角質層の完全性が増大したと解釈することができる。セテアリルオリベート、ソルビタンオリベートの「バリア」効果は、グリセリンの保湿挙動と明らかに異なる。したがって、協調的作用で、天然皮膚保湿剤としてのグリセリンと、角質層バリアの天然成分としてのセテアリルオリベート、ソルビタンオリベートとは、例えばその両方を含有する水和キット中に相互に組み込まれ、2つの重要な補完的皮膚水和メカニズムを活性化することができる。
実施例4
セテアリルオリベート、ソルビタンオリベートの有効性を、その機能的水和効果に関して、さらに臨床的に解析した。10人のボランティアが、半数の顔にセテアリルオリベート、ソルビタンオリベートから成るエマルションを、他の半数の顔にCeteareth−20、セテアリルアルコールから成るエマルションを、1日2回、最大45日の期間、塗布した。
【0045】
図6に示すように、セテアリルオリベート、ソルビタンオリベートの塗布の後、皮膚の水和は、15日及び45日後にそれぞれ24.7%及び27.3%高まった(p<0.05)。対照としてのceteareth−20、セテアリルアルコールでは、2.2%(15日)及び4.5%(45日)という有意でない効果が観察された。同時に、2.5% セテアリルオリベート、ソルビタンオリベートを含有する製剤は、同一の被験者で判断した知覚レベルを40%上昇させた。この試験で得られた結果は、より長期の水和をもたらす、セテアリルオリベート、ソルビタンオリベートにより形成される皮膚適合性液晶の塗布後の角質層バリアの効果の向上と矛盾しない。
【0046】
皮膚の恒常性は、脂質に富むマトリクス中に埋め込まれた角化細胞から成る、角質層バリアの完全性に、高度に基づく。その完全性は、環境の攻撃からの保護を確実にし、過剰の経皮水分喪失を回避する。そのバリア機能は、結果として水蒸発速度、皮膚の感受性レベル、及び細胞機能に影響を及ぼす、汚染物質、強力な洗浄剤、及び加齢要因等の有害な外部作用因子により破壊されることがある。最終的にこのことが、皮膚の乾燥、皮膚刺激、及び生理学的応答の減弱を引き起こすことがある。
【0047】
本発明により、皮膚表面の脂質組成と、角質層の細胞間脂質の薄膜の分子構成との両方を模倣する、皮膚適合性液晶を生成した。セテアリルオリベート、ソルビタンオリベートの液晶は、脂質の皮膚バリア中に生理学的に集積する特性を有する。セテアリルオリベート、ソルビタンオリベートの液晶は、生体模倣再構築剤として働き、皮膚のバリア機能の最適な完全性を回復する。さらに、皮膚表面の脂質組成とのその類似性により、これらの液晶が製剤の一部分との知覚を向上させることが可能になる。
【0048】
セテアリルオリベート、ソルビタンオリベートの液晶の示唆された皮膚作用は、図7にまとめることができる。皮膚の液晶表面に塗布すると、表面脂質組成とのその化学的適合性により、該液晶は角質層の上層に浸透及び定着することによりバリア機能を強化するはずである。セテアリルオリベート、ソルビタンオリベートの生理学的及び生体模倣の再構築の作用により、バリア完全性の向上、及び皮膚の水分レベルの増大がもたらされる。
【0049】
セテアリルオリベート、ソルビタンオリベートの皮膚科学的適合性は、それらを脂質皮膚バリアの化学的な及び構造上の恒常性に関連する生成物の製剤における主要成分たらしめるので、生理学的に非常に好適である。この皮膚科学的適合性は、表皮を通じた活性物質(actives)の送達の生理学的な促進も支持している。
【0050】
活性成分を皮膚中に浸透させる能力をカフェインで検証したが、このような特性は、任意の活性成分、例えば抗酸化剤、フリーラジカルスカベンジャ、ヒアルロン酸、コラーゲン、ボツリヌス毒素、コルチゾン様薬(cortison-like drugs)、抗生物質、化学療法剤、創傷治癒薬、ペプチドで示される。
【技術分野】
【0001】
本発明は、皮膚浸透特性の向上のための、化粧品分野におけるエステル交換オリーブ油の使用に関する。
【背景技術】
【0002】
皮膚中に活性成分を浸透させるという課題は、化粧品において、さらにはおそらく皮膚科学においても劇的な重要性を有している。しかし、ほとんどの活性成分の自然浸透の速度は、その活性成分の作用の有効性を低下させ、又はさらには該作用を完全に無効にする場合があるものであることが多い。これを克服するために、それ自体の中に活性成分を埋め込むことにより、活性成分をその自然の速度より大きな速度で皮膚中に浸透させ、その結果その効果を十分且つ適時なものとする薬剤を見出すことが有用である。それにより多くの場合では、活性成分の濃度を低減することにより、任意の考え得る副作用を最小限まで低減することも可能であろう。原理としては、送達の促進により、角質層を通り抜けることを可能とするために本来化学的に変換する必要がある活性成分を使用することも、可能となるだろう。この種の浸透向上剤での課題は、該浸透向上剤は、活性成分の作用を無効にすることもその特性を損なうこともないように、その活性成分と有意に相互作用することなく、このような促進をもたらさなければならないことである。
【0003】
1つの方法は、細胞を或る程度破壊することにより浸透抵抗性を低減する少量の毒性物質を、化粧品製品に添加することであろう。しかしこの方法は、皮膚を不可逆的に損傷する危険があるので、回避すべきである。
【0004】
また、モイスチャライザーの塗布は、良好な皮膚浸透特性を必要とする。皮膚の水和及びその変動は、皮膚の健康及び皮膚の外観と相関することが多い。したがって、正常な皮膚の水和を欠くことは、潜在的に重大な美容上の関心事と関連することが多く、苦痛とさらには皮膚障害とを引き起こし得る。皮膚による2つの生理学的調節メカニズムが存在する:1)天然の加湿因子、及び2)角化細胞の間に位置する細胞間脂質層。上記角化細胞は、親油性であり、表皮を通じた過剰な水の蒸発を防ぐ。表皮角化細胞及び細胞間脂質層が皮膚のバリア機能を確定するが、脂質部分は主たる役割を果たす。したがって表皮の正常な生理学的バリア機能は、細胞間脂質が浸透する高度に規則的な薄膜に基づく。実際には、表皮角質層においては、細胞間脂質は、層状のゲル相中、及び層状の液晶中に集積している。
【0005】
皮膚水和を調節するための最も慣用されている方法は、エモリエント又は保湿剤の局所塗布にある。
【0006】
エモリエントは細孔の部分的な閉塞をもたらし、皮膚の角質層を軟化し、加湿し、その外観を向上させることができる。
【0007】
他方、保湿剤は概して、大気中の水分と結合することができる例えば尿素又はグリセロール等の吸湿性の分子であり、皮膚の水分を適度なバランスに維持するのを助ける。
【0008】
しかし、エモリエントも保湿剤も、皮膚のバリア機能の完全性(integrity)に影響を与えない。
【0009】
概して、皮膚は、身体の表面上に存在し、内部器官を保護する覆いの役割を果たし、内部器官が環境と直接接触するのを防ぐ。いずれにせよ、皮膚は極めて複雑であり、細胞内分泌(intracrinous)能及びパラ分泌(paracrinous)能の両方を有する。したがって、皮膚は、紫外線(メラニン形成)から保護し、免疫保護をもたらし、外来粒子の浸透を防ぐバリア機能を有する。皮膚はまた、内部の水分のレベルの管理に動的に関与する。皮膚は、ビタミンDの光生成、及び栄養として導入したビタミンEの分布の場所でもある。
【0010】
主要な皮膚の層は、真皮及び表皮である。真皮は、コラーゲン、エラスチン等の細胞外成分、及び分散した常在線維芽細胞により産生及び分泌されるグリコサミノグリカンの合成の部位である。他方、表皮の細胞密度は非常に高く、主に角化細胞により代表される。表皮は、外側への流れと、表皮基底層から角質層(SC)までに由来する細胞の分化とにより、常に自己再生する。表皮の最外層である角質層は、透過性バリアのほとんどを供給し、該透過性バリアは、脂質に富む細胞外マトリクス中への組織立った角化細胞の埋め込みにより主に供給されている。
【0011】
化学的分析により、角質層の細胞間脂質は、主にセラミド、コレステロール、コレステロールエステル及び脂肪酸から成る(それら自体は角化細胞により合成される)ことが示されている。これらの脂質の三次元構成は、種々の異なるモデルの示唆をもたらす種々の研究の対象となっている(非特許文献1)。最近のモデル(非特許文献2)では、角質層の脂肪(モルタル)が、角化細胞(ブリック)の間に見出される多層状の系として配置される、結晶性ゲルの形態で存在することが示唆されている。角質層及び角化細胞の脂質の構成を可視化する方法は、ブリック壁(ここで、角化細胞を表すブリックはモルタルの脂質層中に、整然と並置され且つ挟まれて(chelated)いる)を画像化(imagine)することである。細胞成分の完全性は既知であり、特に角質層の脂質層はバリア機能の完全性を必然的に維持するはずである。角質層のバリア機能の破壊は、経皮水分喪失量の増大と、その結果として皮膚水和レベルの低減とを引き起こし、既に上で示した負の結果をもたらす。
【0012】
細胞間脂質の薄膜(結晶性ゲル)に加えて、皮脂由来の他の種類の脂質も、角質層中で重要な役割を果たす。皮脂中に見出される主要な脂質は、コレステロール、ステロール及びワックスエステル、トリグリセリド、並びにスクアレン(非特許文献3)である。トリグリセリドは、皮脂腺の内側で産生され、遊離脂肪酸の形態で放出され得る。角質層の外表面における沈着後、皮脂の脂肪(又は皮膚の表面脂質)は、一過性の抗酸化剤(α−トコフェロール)として(非特許文献4)、抗微生物(anti-microbic)作用を発揮する(非特許文献5及び非特許文献6)と共に、標的となる生物学的目的を有する重要な分子を供給する。例えば、トリグリセリドの加水分解により得られる可能性がより高いグリセロールは、吸湿剤として働き、角質層の水を保持する能力に関与する(非特許文献7)。オレイン酸及びリノール酸等の幾つかの脂肪酸は、ペルオキシソーム増殖因子活性化受容体(PPAR)の結合因子として振る舞う。PPARの活性化は、角膜実質細胞分化(非特許文献8)に、及びバリアを急速に排除した後の加速バリア機能の回復(非特許文献9、非特許文献10)に関与することが示されている。角質層の外表面上で分泌されるにもかかわらず、さらなる深層の脂質形状の完全性の維持において、皮脂の脂肪は顕著に影響され得る。多数の研究により、脂質のカテゴリーに依存して、皮膚の皮脂表面脂質の勾配が角質層を通じて検出されることが証明されている(非特許文献11、非特許文献12、非特許文献13、非特許文献14、非特許文献15、非特許文献16)。
【0013】
角化細胞の表皮での役目は、落屑(desquamation)プロセスにより終了する。角化細胞(又は角質細胞)の剥離は、表皮の再生に必要なプロセスであり、種々の酵素のタンパク質加水分解作用により得られ得る(非特許文献17)。落屑現象が、角質層の細胞間脂質層状マトリクスにおいて、或る特定の程度の構造崩壊を引き起こし得ることが示唆されている(非特許文献18、非特許文献19)。剥離プロセスは、(壁からのブリックの除去が周囲のモルタルを粉砕するのと同様に)基礎となる脂質マトリクス中に小さい隙間を開ける、不安定化させる操作として表すことができる。このような微小孔は、皮脂の脂質を角質層の脂質対応物と混合する径路となり得る。角質層の内層のこれらの特徴部と皮脂の脂質との混合が、その後起こり得る。まとめると、これらの研究により、皮膚表面中における、及び表皮全体のための、皮脂生成物の生理学的重要性が確立されている。
【先行技術文献】
【非特許文献】
【0014】
【非特許文献1】Madison, 2003
【非特許文献2】Norlen, 2001
【非特許文献3】Stewart, 1992
【非特許文献4】Thiele, 1999
【非特許文献5】Georgel, 2005
【非特許文献6】Willie, 2003
【非特許文献7】Fluhr, 2003
【非特許文献8】Komuves, 2000
【非特許文献9】Schurer, 2002
【非特許文献10】Mao Qiang, 2004
【非特許文献11】Blanc, 1989
【非特許文献12】Norlen, 1998
【非特許文献13】Sheu, 1999
【非特許文献14】Thiele, 1999
【非特許文献15】Norlen, 2001
【非特許文献16】Yagi, 2007
【非特許文献17】Houben, 2007
【非特許文献18】Norlen, 2001
【非特許文献19】Sheu, 1999
【発明の概要】
【発明が解決しようとする課題】
【0015】
本発明の目的は、高浸透皮膚科学的薬剤であって、一方で活性成分の皮膚中へのより速い浸透を可能にし、他方で生体模倣再構築剤として働く、高浸透皮膚科学的薬剤を設計することである。本発明は、角質層の細胞間脂質の薄膜の分子構成を模倣する(mimike)ように、皮膚適合性液晶を生成するための、皮膚中で見出される脂肪酸組成に類似する脂肪酸組成に主に基づく。このように形成される液晶は、皮膚層を高速で通過し、皮膚の脂質バリア中で生理学的に集積し、その完全性を強化する可能性を有するはずである。
【課題を解決するための手段】
【0016】
上で述べた目的は、皮膚浸透特性の向上のための、化粧品分野におけるエステル交換オリーブ油の使用に関する本発明により、見事に達成される。
【0017】
ここで、本発明を、以下の添付の図面を参照して、さらに詳細に示す。
【図面の簡単な説明】
【0018】
【図1】RHEの組織切片(表皮−多孔質膜)のヘマトキシリン・エオシン染色結果を示す図である。
【図2】多孔質膜の他方の側におけるカフェインの蓄積を示す図である。
【図3】セテアリルオリベート、ソルビタンオリベートの液晶構造を示す走査電子顕微鏡(SEM)画像である。
【図4】皮膚バリア完全性に対する、セテアリルオリベート、ソルビタンオリベートの存在の、及び他の脂質組成物の存在の効果を示す図である。
【図5】グリセリンの水和特性と、セテアリルオリベート、ソルビタンオリベートの水和特性との間の比較を示す図である。
【図6】セテアリルオリベート、ソルビタンオリベートの皮膚水和に関する機能的有効性を示す図である。
【図7】本発明によるエステルの作用メカニズムのイラストである。
【発明を実施するための形態】
【0019】
言うなれば、オリーブ油は、その起源と、年数及び加工方法に依存する、オリーブ油を得るのに利用したオリーブの種類とに従って変化する、脂肪酸エステルの混合物である。しかし、種々のエステルの百分率は、或る特定の変動度ではあるが、十分に規定され且つ広範に知られた範囲内で変化するので、オリーブ油は、或る規定された組成物とみなすことができる。
【0020】
オリーブ油のエステル交換は、有機化学の通常の手順に従って、任意のアルコール又はアルコール混合物により行うことができる。特に、セテアリルアルコール及び/又はソルビトールでエステル交換を行うことにより、妥当な結果が得られている。
【0021】
これらのアルコールの両方でオリーブ油のエステル交換を行うことにより、INCI命名法に従いセテアリルオリベート、ソルビタンオリベートと特定される生成物が形成される。この生成物は、液晶の形態で見出される。
【0022】
特に効果的な製造プロセスに従い、オリーブ油を最初に、通常の条件下でけん化する(undergopes saponification)。得られた脂肪酸を、その後部分的にセテアリルアルコールで、部分的にソルビタンでエステル化し、得られた生成物を最終的に共に混合する。
【0023】
本出願人は、オリーブ油のエステル交換により得られる、セテアリルオリベート、ソルビタンオリベートにより生成される皮膚適合性液晶の経皮浸透における有効性を検証した。これは、一方で強力な水和効果を得るように水の蒸散を抑える能力、及び他方でこのような結晶が生物活性分子の経皮浸透を向上させるのに使用することができることを含む。
【0024】
本発明はオリーブ油をエステル交換することにより得ることができる全ての生成物に関するが、以下の本発明の例示的な説明において使用される成分(INCI:セテアリルオリベート、ソルビタンオリベート)は、親水性又は親油性の意味において特徴的な自己乳化特性を有する、皮膚表面の脂質組成と化学的に関連する、脂肪酸の複雑な組合せである。したがってセテアリルオリベート、ソルビタンオリベートは、1)皮膚バリア完全性を再構築及び維持する、並びに2)それ自体が乳化基剤をもたらすという2本立て(double feature)が期待される単一の生体模倣再構築剤を表す。これにより、塗布後に「生理学的に」自然な皮膚の感覚をもたらす、生物学的に機能的な化粧品製剤の創出がもたらされる。
【0025】
これらの成分の特殊性は、これらの成分が、これらの生成物の皮脂との類似性により、皮膚表面上で見出されている脂肪酸組成(表1)を化学的に(及び生理学的に)十分に再現する脂肪酸の組合せから成ることである。先に言及したように、皮膚表面の脂肪(皮脂脂肪酸)は、角質層の内層中に浸透し、角質層の細胞間脂質の層状マトリクスに埋め込み、且つバリア層の一部分となるこの能力を有する。したがって、皮脂を再現する脂肪酸組成を使用して、角質層の内層に接近するためのその天然の「エントリーカード」を利用することが可能になる。したがって、オリーブ油を出発材料として使用することにより、本出願人は、角質層の脂質の層状の系に対するその天然の親和性を通じて生理学的作用が委ねられる、セテアリルオリベート、ソルビタンオリベート等の化粧品成分を得ることに成功した。
【0026】
【表1】

【0027】
単一の脂肪酸組成を有することに加えて、その成分であるセテアリルオリベート、ソルビタンオリベートは、図3において強調したように、乳化されると液晶形状をとる。これらの液晶は、角質層の脂質薄膜において観察される分子構造と類似する分子構造を有する。実際には、液晶の壁は、脂肪酸及び水の交互の層から成るので、角質層の標準的な細胞間脂質のマトリクス構造を再現している(Norlen, 2001)。したがって、セテアリルオリベート、ソルビタンオリベートの生体模倣は、1)皮膚表面の脂質組成を有する化学的模倣、及び2)角質層の、細胞間脂質の層状の構成を有する構造上の模倣という2つの側面がある。以下で、セテアリルオリベート、ソルビタンオリベートにより形成されるこれらの構造(例えば生体適合性液晶)に言及する。
【0028】
第1の態様によれば、エステル交換オリーブ油の皮膚浸透特性と、その特徴的な構造とにより、皮膚の最内層中に化粧品活性分子及び/又は皮膚科学的活性分子を到達させてより顕著な及び/又はより適時な効果を得ることを可能とするために、化粧品活性分子及び/又は皮膚科学的活性分子を上記構造中に埋め込むことが可能となる。
【0029】
第2の態様によれば、エステル交換オリーブ油自体は、皮膚の最内層中に浸透すると、それ自体が埋め込まれてバリアとして働くことが可能であり、それにより皮膚を通じた水の過剰な蒸発を回避し、いかなる負の結果ももたらさずに最適な水和効果をもたらす。
【0030】
本発明の両方の態様が同じ現象(エステル交換オリーブ油の皮膚中への高い浸透速度)の直接の結果であることは明らかである。
【0031】
ここで本発明を、以下の非限定的な実施例に基づきさらに示す。
【実施例】
【0032】
実施例1
in vitroの再構築ヒト表皮(RHE)系を使用した。生物活性分子としてカフェインを選択した。RHE表面に塗布すると、カフェインは、表皮層中に浸透する能力を有する。カフェインの経皮浸透は、放射性マーカーを使用することにより定量化することができる。カフェインはまた、経皮浸透速度を向上させる際の上記薬剤の効果を検証するために、種々の製剤(エマルション)中に組み込むことができる。
【0033】
ヒト皮膚角化細胞を人工多孔質膜上に分散させ、上記角化細胞の分化を13日と報告される時期まで誘導した。再構築ヒト表皮(RHE)は、水−空気界面環境において規定の培養培地中で成長させる。RHEの組織学的構成が図1に示され、角質層の層を有する表皮の典型的な形状を示す。
【0034】
RHEを、37℃、5%CO2で、1mlの維持培地の存在下で、各々12ウェルを備えるプレート中に配置する。各々のウェル中のRHEは、個々の実験条件を代表するものとした。経皮的に浸透する能力を有する、RHEのチップに塗布した任意の物質は、RHEの下の培養培地中で収集し、好適な検出方法を使用して定量化することができる。
【0035】
表2に従い、様々な製剤を調製した。セテアリルオリベート、ソルビタンオリベート(Olivem 1000 Crystal Skin)を、種々の製剤環境中において形成された液晶として使用した(表2、A、B及びC)。対照処方も検証した(表2、D及びE)。
【0036】
放射性カフェイン(14C−カフェイン、1mCi/m、0.04mM、0.339mMの非放射性の(cold)カフェインに添加)をマーカーとして使用する。この混合物(他に特に記載がない限り、以下「カフェイン」と称する)は、水溶性生物活性分子を代表する。カフェインを、純品で(pure)又は種々の処方に組み込んで、試験した。カフェインを、緩やかに振とうしながら処方中に組み込み、試験前に終夜室温で維持した。
【0037】
【表2】

【0038】
処方A、処方B、処方C、処方D若しくは処方E又は純粋なカフェイン(対照)を、各ウェル中のRHE表面に塗布した。全条件をn=3で実施した。速度論的試料を、1時間、2時間、3時間、4時間、5時間、6時間及び24時間の7つの速度論的時間で、RHEの下の培養培地に配置した。収集した試料中に含有される放射能を、液体シンチレーションを使用して測定した。結果は、放出されたカフェインのcpm(1分当たりのカウント数)として表現し、表皮中のカフェインの相対濃度を表す。
【0039】
角化細胞の生存度を、MTTアッセイを使用して確認した:MTT塩(3−(4,5−ジメチル(dimetil)−チアゾール(tiaol)−2−イル(il))−2,5ジフェニルテトラゾリウムブロミド)は、生細胞に見出されるミトコンドリア酵素スクシネートデヒドロゲナーゼにより還元され得る。還元生成物ホルマザン結晶は、540mmでの光学密度により定量化することができ、生細胞数に比例する。MTTアッセイを、24時間時点で直ちに、RHEに対して実施した。
【0040】
これらの実験条件では、A製剤、B製剤、C製剤及びE製剤が、表皮中へのカフェイン通過を促進した。効果は、製剤で処理せず純粋なカフェインで処理した対照表皮と比較して、統計的に有意であった(p<0.05)。例えば、24時間時点直後では、処方A、処方B及び処方Cのみが、純粋なカフェイン(対照)と比較して、カフェインの浸透を有意に増大させた(p>0.01)。D処方及びE処方は、純粋なカフェイン(対照)と比較して、有意な効果を示さなかった(p>0.05)。処方Eの主成分(セテアリルアルコール及びセテアリルグルコシド)が液晶を生成することに留意しなければならない。これらの結果により、セテアリルオリベート、ソルビタンオリベートにより生成した液晶(皮膚適合性液晶)の化学的組成が独特であり、経皮浸透を有意に増大させるのに重要であることが証明される。さらに、このアッセイで観察された浸透増大効果は、MTTアッセイの結果は正常な生存度(細胞生存度100%)を示している(表3)ため、細胞生存度に対する負の効果で単純に説明することはできない。
【0041】
【表3】

【0042】
実施例2
セテアリルオリベート、ソルビタンオリベートにより生成される生体適合性液晶の臨床的効率性を、臨床的に検証した。最初に、その皮膚生体適合性を、他の脂質組成物との関連で、経皮水分喪失量(TEWL)に対するその効果に関する研究において検証した。TEWLは、皮膚透過性バリア機能を評価するための、バリデーションされた(convalidated)方法である(Fluhr, 2006)。10人のボランティアが、同一の濃度(5%)の以下の成分を局所的に塗布した:セテアリルオリベート、ソルビタンオリベート;セテアリルアルコール、セテアリルグルコシド;及びポリグリセリル(poliglyceril)−3メチルグルコースジステアレート。結果(図4を参照されたい)により、セテアリルオリベート、ソルビタンオリベートの塗布が、対照処方に対してTEWLの増大を29%低減したことが示されている(図2)。
【0043】
これらの結果は、局所的に塗布した脂質組成物と皮膚との間の生理学的適合性に関する必要性を支持する。セテアリルアルコール、セテアリルグルコシド、及びポリグリセリル−3メチルグルコースジステアレートは、塗布後の過剰の水分喪失をそれらが活性化するという事実により、非適合性脂質組成物としてのカテゴリーにおいて特定することができる。このことは、それを通じて水が出てくることができる微小孔の形成をもたらす、バリア完全性の一過性の不安定化と解釈することができる。TEWLは、バリア完全性が回復すると、徐々にベースライン値を取り戻す。適切な皮膚適合性脂質の組成及び比から成る、脂質組成の重要性は、証明されている(Mao Qiang, 1995、De Paepe, 2002)。皮膚の脂質組成を有するセテアリルオリベート、ソルビタンオリベートの適合性は、導いたTEWLの相対的に低いレベルで検出される。皮膚に塗布した成分の脂質組成は、形成した三次元形状よりも大きな重要性を有するようである。セテアリルオリベート、ソルビタンオリベートが液晶を生成することは、既に証明されている(図1)。興味深いことに、セテアリルアルコール及びセテアリルグルコシドも、乳化すると液晶を形成する能力を有する。化粧品製剤における液晶の利点は既知であるが、脂肪酸組成の観点では、その化学的製造によってのみ、液晶が皮膚と生理学的に適合性となる。セテアリルオリベート、ソルビタンオリベートにより得られた結果は、液晶構造を形成することの重要性のみでなく、それらを皮膚との化学的適合性を有する(非常に類似する)ものにして、所望の浸透効果及びモイスチャライジング効果をもたらし、最適なバリア完全性を維持すること(今日まで従来技術に基づいて予測することは不可能であった)の重要性をも明示している。
実施例3
全体の皮膚水和レベルはバリア機能及び水分保持能力に依存するので、セテアリルオリベート、ソルビタンオリベートの皮膚水和効果を、コルネオメトリー(corneometry)を利用してグリセリンの皮膚水和効果と比較した。グリセリンは皮脂腺により産生及び分泌され、天然皮膚保湿剤として働く(Fluhr, 2003)。10人のボランティアが、2%グリセリン及び0.4%キサンタンガムから成る溶液、並びに4%セテアリルオリベート、ソルビタンオリベートのエマルションを、前腕の手掌側の異なる部位に塗布した。期待した通り、図5において明らかなように、グリセリン溶液は、皮膚表面の水和の迅速な増大をもたらした。
【0044】
図5に示したグリセリンの皮膚水和ピークは徐々に消失し、塗布後45分から7時間まで、セテアリルオリベート、ソルビタンオリベートよりも有意に低い値に到達した。セテアリルオリベート、ソルビタンオリベートのエマルションは、水和の一過性のピークはもたらさなかったが、より安定な長期的効果をもたらした。この効果は、セテアリルオリベート、ソルビタンオリベートにより形成される皮膚適合性液晶の生理学的浸透及び集積により、角質層の完全性が増大したと解釈することができる。セテアリルオリベート、ソルビタンオリベートの「バリア」効果は、グリセリンの保湿挙動と明らかに異なる。したがって、協調的作用で、天然皮膚保湿剤としてのグリセリンと、角質層バリアの天然成分としてのセテアリルオリベート、ソルビタンオリベートとは、例えばその両方を含有する水和キット中に相互に組み込まれ、2つの重要な補完的皮膚水和メカニズムを活性化することができる。
実施例4
セテアリルオリベート、ソルビタンオリベートの有効性を、その機能的水和効果に関して、さらに臨床的に解析した。10人のボランティアが、半数の顔にセテアリルオリベート、ソルビタンオリベートから成るエマルションを、他の半数の顔にCeteareth−20、セテアリルアルコールから成るエマルションを、1日2回、最大45日の期間、塗布した。
【0045】
図6に示すように、セテアリルオリベート、ソルビタンオリベートの塗布の後、皮膚の水和は、15日及び45日後にそれぞれ24.7%及び27.3%高まった(p<0.05)。対照としてのceteareth−20、セテアリルアルコールでは、2.2%(15日)及び4.5%(45日)という有意でない効果が観察された。同時に、2.5% セテアリルオリベート、ソルビタンオリベートを含有する製剤は、同一の被験者で判断した知覚レベルを40%上昇させた。この試験で得られた結果は、より長期の水和をもたらす、セテアリルオリベート、ソルビタンオリベートにより形成される皮膚適合性液晶の塗布後の角質層バリアの効果の向上と矛盾しない。
【0046】
皮膚の恒常性は、脂質に富むマトリクス中に埋め込まれた角化細胞から成る、角質層バリアの完全性に、高度に基づく。その完全性は、環境の攻撃からの保護を確実にし、過剰の経皮水分喪失を回避する。そのバリア機能は、結果として水蒸発速度、皮膚の感受性レベル、及び細胞機能に影響を及ぼす、汚染物質、強力な洗浄剤、及び加齢要因等の有害な外部作用因子により破壊されることがある。最終的にこのことが、皮膚の乾燥、皮膚刺激、及び生理学的応答の減弱を引き起こすことがある。
【0047】
本発明により、皮膚表面の脂質組成と、角質層の細胞間脂質の薄膜の分子構成との両方を模倣する、皮膚適合性液晶を生成した。セテアリルオリベート、ソルビタンオリベートの液晶は、脂質の皮膚バリア中に生理学的に集積する特性を有する。セテアリルオリベート、ソルビタンオリベートの液晶は、生体模倣再構築剤として働き、皮膚のバリア機能の最適な完全性を回復する。さらに、皮膚表面の脂質組成とのその類似性により、これらの液晶が製剤の一部分との知覚を向上させることが可能になる。
【0048】
セテアリルオリベート、ソルビタンオリベートの液晶の示唆された皮膚作用は、図7にまとめることができる。皮膚の液晶表面に塗布すると、表面脂質組成とのその化学的適合性により、該液晶は角質層の上層に浸透及び定着することによりバリア機能を強化するはずである。セテアリルオリベート、ソルビタンオリベートの生理学的及び生体模倣の再構築の作用により、バリア完全性の向上、及び皮膚の水分レベルの増大がもたらされる。
【0049】
セテアリルオリベート、ソルビタンオリベートの皮膚科学的適合性は、それらを脂質皮膚バリアの化学的な及び構造上の恒常性に関連する生成物の製剤における主要成分たらしめるので、生理学的に非常に好適である。この皮膚科学的適合性は、表皮を通じた活性物質(actives)の送達の生理学的な促進も支持している。
【0050】
活性成分を皮膚中に浸透させる能力をカフェインで検証したが、このような特性は、任意の活性成分、例えば抗酸化剤、フリーラジカルスカベンジャ、ヒアルロン酸、コラーゲン、ボツリヌス毒素、コルチゾン様薬(cortison-like drugs)、抗生物質、化学療法剤、創傷治癒薬、ペプチドで示される。
【特許請求の範囲】
【請求項1】
皮膚浸透特性の向上のための、化粧品分野におけるエステル交換オリーブ油の使用。
【請求項2】
セテアリルアルコール及び/又はソルビトールでエステル交換を行うことを特徴とする、請求項1に記載のエステル交換オリーブ油の使用。
【請求項3】
前記エステル交換オリーブ油がセテアリルオリベート、ソルビタンオリベートであることを特徴とする、請求項2に記載の使用。
【請求項4】
化粧品活性分子及び/又は皮膚科学的活性分子が前記エステル交換オリーブ油に埋め込まれることを特徴とする、請求項1〜3のいずれか一項に記載の使用。
【請求項5】
前記化粧品活性分子及び/又は前記皮膚科学的活性分子がカフェインであることを特徴とする、請求項4に記載の使用。
【請求項6】
前記化粧品活性分子及び/又は前記皮膚科学的活性分子が、抗酸化剤、フリーラジカルスカベンジャ、ヒアルロン酸(ialuronic acid)、コラーゲン、ボツリヌス毒素、コルチゾン様薬、抗生物質、化学療法剤、創傷治癒薬、ペプチドから成る群から選択されることを特徴とする、請求項4に記載の使用。
【請求項7】
皮膚モイスチャライザーを製造するための、請求項1〜3のいずれか一項に記載の使用。
【請求項8】
前記生成物がグリセリンと共にモイスチャライジングキットを構成することを特徴とする、請求項7に記載の使用。
【請求項1】
皮膚浸透特性の向上のための、化粧品分野におけるエステル交換オリーブ油の使用。
【請求項2】
セテアリルアルコール及び/又はソルビトールでエステル交換を行うことを特徴とする、請求項1に記載のエステル交換オリーブ油の使用。
【請求項3】
前記エステル交換オリーブ油がセテアリルオリベート、ソルビタンオリベートであることを特徴とする、請求項2に記載の使用。
【請求項4】
化粧品活性分子及び/又は皮膚科学的活性分子が前記エステル交換オリーブ油に埋め込まれることを特徴とする、請求項1〜3のいずれか一項に記載の使用。
【請求項5】
前記化粧品活性分子及び/又は前記皮膚科学的活性分子がカフェインであることを特徴とする、請求項4に記載の使用。
【請求項6】
前記化粧品活性分子及び/又は前記皮膚科学的活性分子が、抗酸化剤、フリーラジカルスカベンジャ、ヒアルロン酸(ialuronic acid)、コラーゲン、ボツリヌス毒素、コルチゾン様薬、抗生物質、化学療法剤、創傷治癒薬、ペプチドから成る群から選択されることを特徴とする、請求項4に記載の使用。
【請求項7】
皮膚モイスチャライザーを製造するための、請求項1〜3のいずれか一項に記載の使用。
【請求項8】
前記生成物がグリセリンと共にモイスチャライジングキットを構成することを特徴とする、請求項7に記載の使用。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公表番号】特表2011−510059(P2011−510059A)
【公表日】平成23年3月31日(2011.3.31)
【国際特許分類】
【出願番号】特願2010−543583(P2010−543583)
【出願日】平成20年10月21日(2008.10.21)
【国際出願番号】PCT/IB2008/054327
【国際公開番号】WO2009/093104
【国際公開日】平成21年7月30日(2009.7.30)
【出願人】(510199557)
【Fターム(参考)】
【公表日】平成23年3月31日(2011.3.31)
【国際特許分類】
【出願日】平成20年10月21日(2008.10.21)
【国際出願番号】PCT/IB2008/054327
【国際公開番号】WO2009/093104
【国際公開日】平成21年7月30日(2009.7.30)
【出願人】(510199557)

【Fターム(参考)】
[ Back to top ]

