医用材料
ケイ素及び3価カチオンを含む、合成リン酸カルシウム系医用材料。
【発明の詳細な説明】
【発明の詳細な説明】
【0001】
本発明は、医用材料、特に人工骨として使用される置換リン酸カルシウム(例えばアパタイト及びヒドロキシアパタイト)材料に関する。
【0002】
人口の老齢化と、生活の質に関して高まる期待との複合作用により、損傷した骨及び関節の置換又は増強用の整形外科用埋込み材への世界的な需要が増加する結果となった。骨移植術における現在の標準は、自家移植片及び同種移植片の使用を含むが、これらの方法は、供給及び整合性に制限があるため、非理想的であるという認識が増している。セラミックスは、過去30年間に渡り、従来の骨移植片に取って代わる、又はそれを拡大適用するための、骨移植片補填材としての使用が検討されてきた。特にヒドロキシアパタイトなどのリン酸カルシウム類は、それらの骨伝導能の特性のために奨励されてきた。
【0003】
したがって、外科技術及び医学知識が継続して進歩するにつれて、人工骨補填材への需要が増えている。必然的に、関節及び顔の復元などにおける、荷重有りと無しの両方の場合の骨欠損部の補填のための、人工骨補填材の開発への関心が高まっている。
【0004】
ヒドロキシアパタイトの生体適合性は、ヒドロキシアパタイトの結晶構造が骨のミネラル分と類似していることも相まって、ヒドロキシアパタイトが骨欠損部の増強用材料として多大な関心を集めるきっかけとなった。ミネラル類のアパタイト群は、リン酸カルシウムを基礎とし、化学量論的ヒドロキシアパタイトのCa/Pのモル比は、1.67である。ヒドロキシアパタイトの化学式は、Ca10(PO4)6(OH)2である。
【0005】
シリケート置換のヒドロキシアパタイト組成物は、骨補填材としての化学量論的ヒドロキシアパタイトの興味深い代替となる。ケイ素は、リン酸カルシウムの骨移植片と組み合わせると、骨の治癒の速度及び質を向上させ、その結果埋込み材と宿主との間の骨結合が速まることが判明している。PCT/GB97/02325は、シリケート置換のヒドロキシアパタイト材料を記載している。
【0006】
しかし、問題が存在する。なぜなら、シリケートのヒドロキシアパタイトへの置換には、組成上の限度があるからである。シリケート置換の程度がこの限度を超えたとき、ヒドロキシアパタイトは、一般的な焼結温度(例えば、約1200℃以上)で、熱的に不安定になる恐れがある。これは、例えば、ある用途には望ましくないリン酸三カルシウム(TCP)などの二次相の形成を生じ得る。ヒドロキシアパタイト結晶格子へのシリケート置換の置換限度は、約5.3重量%である(1.6重量%のケイ素に相当)。
【0007】
本発明は、従来技術に関連する少なくとも幾つかの問題の解決に当たること、及び/又は様々なリン酸カルシウム材料に基づく新規な医用材料を提供することを目的とする。
【0008】
したがって、本発明は、ケイ素及び3価カチオンを含む、合成リン酸カルシウム系医用材料を提供する。
【0009】
本発明による医用材料は、例えばヒドロキシアパタイト又はアパタイトなどのリン酸カルシウム材料に基づく。
【0010】
本発明による医用材料は、好ましくは、以下の一般化学式を有する化合物を含む。
Ca10−yMy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、Mは3価カチオンであり、0<x<1.3及び0<y<1.3である。好ましくは、0<x<1.1、より好ましくは0.5<x<1.1である。好ましくは、0<y<1.1、より好ましくは0.5<y<1.1である。また好ましくはx≧yである。)
【0011】
3価カチオンは、好ましくは、イットリウム、スカンジウム、アルミニウム及びランタニド元素のうちの1種又は複数から選択される。好ましくは、3価カチオンはイットリウムであるか、又はイットリウムを含む。
【0012】
3価カチオンは、ヒドロキシアパタイト結晶格子内で、カルシウムイオンを置換すると考えられている。ケイ酸イオンは、ヒドロキシアパタイト結晶格子内で、リン酸イオンを置換すると考えられている。
【0013】
不明確さを避けるため、本明細書で使用する場合、シリケート置換という用語は、ケイ素置換をも包含する。同様に、本明細書で使用する場合、ケイ素置換という用語は、シリケート置換をも包含する。
【0014】
本質的に純相な材料が必要とされる、本発明の一実施形態において、材料の相純度は、好ましくは少なくとも95%、より好ましくは少なくとも97%、さらにより好ましくは少なくとも99%である。この場合、該材料は、実質的にいかなる二次相も含まない。しかし、避けられない不純物が存在し得ることは理解されよう。医用材料の相純度が、従来のX線回折技術で測定できることは理解されよう。
【0015】
二次相の存在が問題とならない別の実施態様において、該材料はさらに、例えばリン酸三カルシウム(例えばα−TCP及び/又はβ−TCP)などの1つ又は複数の二次相を含んでもよい。したがって本発明は、二相及び多相の材料も提供する。二次相は、60重量%まで、より一般的には40重量%まで、さらにより一般的には20重量%までの量で存在してもよい。
【0016】
本発明による医用材料は、人工骨材、骨の埋入み材、骨移植片、骨代替物、骨の足場材、充填材、被覆材又はセメントとして使用してもよい。該医用材料は、多孔性又は無孔性の形で提供してもよい。該医用材料は、例えば生体適合性ポリマーと組み合わせて、複合材の形で提供してもよい。
【0017】
本発明はまた、3価カチオン−シリケート共置換の合成リン酸カルシウム系材料を含む医用材料も提供する。例として挙げられるのは、3価カチオン−シリケート共置換のヒドロキシアパタイト及びアパタイト材料である。3価カチオンは好ましくは、イットリウム、スカンジウム、アルミニウム及びランタニド元素のうちの1種又は複数から選択される。さらに好ましくは、3価カチオンはイットリウムであるか、又はイットリウムを含む。上記に記載の好ましい特徴は、単独で、又は組み合わせて、本発明のこの態様に適用することもできる。
【0018】
本発明による医用材料は、水沈殿法又は固相法、例えば水熱法などによって調製し得る。しかし、水沈殿法が好ましい。したがって、本発明はまた、カルシウム又はカルシウム含有化合物、3価カチオン含有化合物、リン含有化合物及びケイ素含有化合物を用意するステップと、アルカリ性pHで水相の化合物を反応させることによって、沈殿物を形成するステップとを含む、ケイ素及び3価カチオンを含むリン酸カルシウム系医用材料を合成するための方法を提供する。
【0019】
該方法を使用して、ケイ素及び3価カチオンを含むヒドロキシアパタイト及びアパタイト材料を合成してもよい。
【0020】
本発明による方法は、好ましくは水沈殿法である。
【0021】
好ましくは、カルシウム含有化合物は、カルシウム塩を含む。カルシウム塩は、例えば水酸化カルシウム、塩化カルシウム、硝酸カルシウム及び/又は硝酸カルシウム水和物のうちの1種又は複数から選択してもよい。
【0022】
好ましくは、3価カチオン含有化合物は、イットリウムの化合物を含む。イットリウム含有化合物は、例えば塩化イットリウム及び/又は硝酸イットリウムの一方又は両方から選択され、好ましくはY(NO3)3.XH2Oであってよい。
【0023】
イットリウムは、好ましくは、13重量%まで、より好ましくは12重量%までの量で、医用材料(すなわち最終製品)内に存在する。上記考察のように該材料が本質的に純相材料である場合には、これは一般的である。一方、該材料が1つ又は複数の二次相を含む場合、材料中のイットリウムの量は、13重量%を超え、20重量%までの量で存在し得る。
【0024】
好ましくは、ケイ素含有化合物は、シリケートを含有する。さらに好ましくは、シリケートは、オルトケイ酸テトラエチル(TEOS)及び/又は酢酸ケイ素の一方又は両方から選択される。
【0025】
好ましくは、シリケートは13重量%まで(ケイ素として4重量%に相応)、さらに好ましくは12重量%まで(3.66重量%のケイ素に相応)の量で、該材料(すなわち最終製品)内に存在する。上記と同様に、上記考察の材料が本質的に純相材料である場合には、これが一般的である。一方、材料が1つ又は複数の二次相を含む場合は、材料中のシリケートの量は、13重量%を超えてもよく、20重量%までの量で存在し得る。
【0026】
好ましくは、リン含有化合物は、リン酸塩及び/又はリン酸の一方又は両方から選択される。より好ましくは、リン含有化合物は、リン酸アンモニウム及び/又はリン酸の一方又は両方から選択される。
【0027】
一実施形態において、ケイ素含有化合物及び3価カチオン含有化合物は、好ましくはケイ素の量及び3価カチオンの量に対して実質的に等モル量で供給する。代替の実施形態においては、ケイ素含有化合物が、ケイ素の量及び3価カチオンの量に対して、3価カチオン化合物よりも大きなモル量で供給される。
【0028】
本発明の第2の実施形態による方法は、好ましくはアルカリ性pHで実施される。好ましくは、pHは8〜13である。より好ましくは、pHは10〜12である。
【0029】
溶液のpHを所望するpHに調整するために、好ましくはアルカリを溶液に添加する。該アルカリは、例えば水酸化アンモニウム又は濃縮アンモニアであってよい。
【0030】
本発明による方法は、好ましくは、最初に周囲条件下で(但し、このステップは、約100℃までの温度で実施できる)カルシウム又はカルシウム含有化合物(例えばCa(OH)2)及び3価カチオン含有化合物(例えばY(NO3)3.XH2O)を含む水性懸濁液を形成するステップを含む。次に、リン含有化合物(例えばH3PO4)の水溶液を撹拌しながら懸濁液にゆっくりと添加する。最後に、ケイ素含有化合物の水溶液(例えばSi(OC2H5)4=TEOS)を撹拌しながらゆっくりと添加する(代わりに、リン含有化合物の水溶液をケイ素含有化合物の水溶液と混合することもでき、次いでこの配合物を撹拌しながら懸濁液にゆっくりと添加することもできる)。pHを監視し、例えば濃縮アンモニア溶液を用いて、好ましくは11〜13のアルカリ性pHに維持する。全混合物は、次いでそのまま放置、熟成し、沈殿させるが、これには通常12〜24時間かかる。
【0031】
沈殿物が一度形成され、熟成されると、それを乾燥、加熱及び/又は焼結させてもよい。好ましくは、最初にそれを100℃までの温度に加熱することによって、乾燥させる。次いで、800℃〜1500℃、より好ましくは1000℃〜1350℃、さらにより好ましくは1200℃〜1300℃の範囲の温度に加熱して、材料を焼結させてもよい。乾燥した沈殿物は、好ましくは焼結ステップの前に、粉砕して粉末にする。
【0032】
上記のプロセスを使用して、本明細書に記載の本質的に純相の材料を調製してもよい。
【0033】
例えば、単相のイットリア/シリケート共置換のヒドロキシアパタイトよりもイットリア/シリケート共置換による2相の組成物などの、2相又は多相材料の生成が所望される場合、幾つかのステップを単独で又は組み合わせて使用してもよい。以下にその例を挙げる。最初に、沈殿物のpHを11〜13から8〜10に低下させる。これにより、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿が促進され、加熱によって2相のイットリア/シリケート共置換の組成物が形成されることが判明した。第2に、カルシウム塩若しくはイットリウム塩のいずれか、又はこれら2つの組合せであるカチオンを添加し、その相対量が低下するように反応混合物を調整することによって、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進させる。上記と同様に、これは、加熱によって、2相のイットリア/シリケート共置換の組成物を形成することになる。第3に、リン酸塩若しくはケイ酸塩のいずれか、又はこれら2つの組合せであるアニオンを添加し、その相対量が低下するように反応混合物を調整することによって、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進させてもよく、これは加熱によって2相のイットリア/シリケート共置換の組成物を形成することになる。第4に、反応混合組成物の改変と共に、pHを低下させることによって、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物を生成してもよく、これは加熱によって2相のイットリア/シリケート共置換の組成物を形成することになる。イットリアは、例として参照したことを理解されたい。
【0034】
これらの方法に加え、単相のヒドロキシアパタイト様組成物を生成するのに示した限度を超えてシリケート/イットリアの置換量を増加させることによっても、2相のイットリア/シリケート共置換の組成物を加熱により生成することになる。さらに、十分に高い温度(≧1400℃)で、又は高温でより長い加熱時間で、任意の組成物を加熱することによっても、一般に、2相のイットリア/シリケート共置換の組成物が、加熱により生成される結果になるであろう。上記と同様に、イットリアは例として参照したことを理解されたい。
【0035】
本発明はまた、ケイ素置換ヒドロキシアパタイト材料を安定化する方法であって、3価カチオンを結晶格子に共置換するステップを含む方法を提供した。好ましくは、3価カチオンは、イットリウム、スカンジウム、アルミニウム、及びランタニド元素のうちの1種又は複数から選択される。好ましくは、3価カチオンは、イットリウムである。
【0036】
本発明を、以下の好ましい実施形態を参照してこれからさらに説明する。これらの実施形態、実施例及び付属する図は、例として提供される。
【0037】
より多くのシリケートを置換によりリン酸カルシウム結晶格子(例えばヒドロキシアパタイト又はアパタイト)に入れることができるよう、本発明は共置換法を提供しているが、この方法によりイットリウム(又はカルシウムイオンへの置換に適切である他の3価カチオン)は、ケイ酸イオンで共置換される。2つの異なるメカニズムが可能である。第1のメカニズムは、ヒドロキシル(OH)基が、電荷の平衡を保つために、ヒドロキシアパタイト結晶格子から失われることを本質的に否定している。なぜならイットリウム及びケイ酸のイオンのカルシウム及びリン酸のイオンへの等モル置換によって、電荷の平衡が保たれるからである。
(1)Y3+ + SiO44− → Ca2+ + PO43−
これは、以下の一般式にまとめることができる。
Ca10−xYx(PO4)6−x(SiO4)x(OH)2
【0038】
第2の置換においては、比例的により少ないイットリウムイオンが、ケイ酸イオンで共置換され、その結果電荷の平衡を保つためにOH基の程度が減ることになる(例えば、イットリウムのモル量は、置換されたシリケートの半分のモル量である)。
(2) 0.5Y3++SiO44− → 0.5Ca2++PO43−+0.5OH−
これは、以下の一般式にまとめることができる。
Ca10―yYy(PO4)6−x(SiO4)x(OH)2−x+y
(このメカニズムでは、y<x)
【0039】
ヒドロキシアパタイトの結晶格子における他のイオン置換に関しては、置換の限度がある。置換の程度がこれらの限度を超えると、組成物は、焼結中に熱的に不安定になり、ヒドロキシアパタイトの相分解が起こり、二次相の形成を起こす。本発明による共置換法を使用することによって、一般的な温度(約1200℃以上)での焼結の後で相分解が発生しないように、ヒドロキシアパタイト結晶格子のシリケートによる置換の限度を、最大約12重量%のケイ酸イオン(又はケイ素3.66重量%)まで上げてもよい。この限度まで到達した後で、二次相が生成される。ある用途に対しては、本質的に純相の材料が所望され、そのために最大約12重量%のケイ酸イオンが導入される。他の用途に対しては、二次相の存在が実際には所望される(又は問題とならない)こともあり、この場合約12重量%のシリケートという限度を超えてもよい。
【0040】
本発明はさらに、これより以下の実施例及び付属する図面をさらに参照することによって説明される。
【実施例】
【0041】
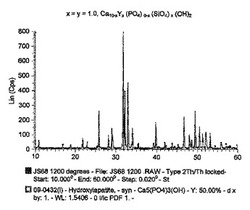
実施例1: Y3+/SiO44−共置換ヒドロキシアパタイト(x=y=1.0)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法による、Y3+/SiO44−共置換のヒドロキシアパタイト約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=y=1.0である)
【0042】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.0782gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、3.8361gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNH溶液を、Ca(OH)2懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0043】
5.7703gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈した。この溶液を滴下漏斗に注ぎ、約30分間の間、撹拌しているCa(OH)2/YNH懸濁液に滴下添加した。H3PO4溶液を完全に添加した後、2.1278gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注ぎ、約30分間の間、撹拌しているCa(OH)2/YNH/H3PO4混合液に滴下添加した。撹拌している溶液のpHは、H3PO4及びTEOS溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約37.5mlを添加した。TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ICDD標準ピークと一致し、追加的なピークは観察されず、この方法で生成した組成物が、ヒドロキシアパタイト様構造を有する単相材料であることが示された(図1を参照)。
【0044】
実施例2:Y3+/SiO44−共置換ヒドロキシアパタイト(x=1.0、y=0.5)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=1.0、y=0.5である)
【0045】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.3601gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、1.9162gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0046】
5.7708gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。2.1281gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約40mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ICDD標準のピークと一致し、追加的なピークは観察されず、この方法で生成した組成物が、ヒドロキシアパタイト様構造を有する単相材料であることが示された(図2を参照)。
【0047】
実施例3: Y3+/SiO44−共置換ヒドロキシアパタイト(x=y=1.0)の合成
この実施例の合成は、実施例1に記載の合成方法の通りで、唯一異なるのが、H3PO4及びTEOS溶液(それぞれ約100ml)を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に、一緒に混合し、同時に滴下したことであった。この違いは別として、沈殿及び次の加工ステップは、実施例1に記載のステップと同一であった。この方法により生成した焼結試料のX線回折パターンは、実施例1で観察したものと同一であった。
【0048】
実施例4: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=0.6、y=0.6)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=y=0.6である)
【0049】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例1に記載)ではなく、イットリア/シリケート共置換の2相組成物を生成するために、沈殿物のpHを10に低下させ、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。これから、2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0050】
最初に、CaCO3を一晩(16時間)、約900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.2735gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、2.2993gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0051】
6.2286gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。1.2764gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNH懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOS溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH10に維持した。合計で約10mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0052】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両方においてICDD標準のピークと一致し、この方法で生成した組成物が、2相材料であることが示された(図3を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が70%、リン酸三カルシウムの量が30%であると見積もられる。
【0053】
実施例5: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=0.6、y=0.3)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウム2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=0.6、y=0.3である)
【0054】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例2に記載)ではなく、イットリア/シリケート共置換の、y<xである2相組成物を生成するために、沈殿物のpHを10に低下させ、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。これによって、2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0055】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.4461gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、1.1508gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0056】
6.2264gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。1.2817gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH10に維持した。合計で約10mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0057】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8線回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両相においてICDD標準のピークと一致し、この方法で生成した組成物が、2相材料であることが示された(図4を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が85%、リン酸三カルシウムの量が15%であると見積もられる。
【0058】
実施例6: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=y=1.3)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=y=1.3である)
【0059】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例1に記載)ではなく、イットリア/シリケート共置換の2相組成物を生成するために、但しこの場合pH12で、Ca(OH)2及びYNHの不足量を添加し、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。こうして2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0060】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、4.9054gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、4.9807gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0061】
5.4277gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。2.7679gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約40mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0062】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ICDD標準のピークと、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両方において一致し、この方法で生成した組成物が、2相材料であることが示された(図5を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が90%、リン酸三カルシウムの量が10%であると見積もられる。
【0063】
実施例7: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=1.0、y=0.5)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=1.0、y=0.5である)
【0064】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例2に記載)ではなく、y<xである、イットリア/シリケート共置換の2相組成物を生成するために、但しこの場合pH12で、Ca(OH)2及びYNHの不足量を添加し、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。こうして2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0065】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.3299gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、1.9170gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0066】
5.7719gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。2.1259gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約40mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0067】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両方においてICDD標準のピークと一致し、この方法で生成した組成物が、2相材料であることが示された(図6を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が80%、リン酸三カルシウムの量が20%であると見積もられる。
【0068】
本発明により、一般的な焼結温度、例えば≧1200℃で有意な層分解をまったく起こさずに、より多くのケイ酸イオン(又はケイ素)によるリン酸カルシウム(例えばヒドロキシアパタイト又はアパタイト)結晶格子の置換が可能となる。その結果、現在の置換限界であるシリケート5.3重量%(又はケイ素1.6重量%)を増加させることができ、骨のミネラルの化学組成とよりぴったりと一致する合成医用材料を生成し得る。本発明はケイ素含有量のさらにより高い2相及び多相材料の生成をも可能にする。
【図面の簡単な説明】
【0069】
【図1】図1は、実施例1に対応するX線回折データを示す図である。
【図2】図2は、実施例2に対応するX線回折データを示す図である。
【図3】図3は、実施例4に対応するX線回折データを示す図である。
【図4】図4は、実施例5に対応するX線回折データを示す図である。
【図5】図5は、実施例6に対応するX線回折データを示す図である。
【図6】図6は、実施例7に対応するX線回折データを示す図である。
【発明の詳細な説明】
【0001】
本発明は、医用材料、特に人工骨として使用される置換リン酸カルシウム(例えばアパタイト及びヒドロキシアパタイト)材料に関する。
【0002】
人口の老齢化と、生活の質に関して高まる期待との複合作用により、損傷した骨及び関節の置換又は増強用の整形外科用埋込み材への世界的な需要が増加する結果となった。骨移植術における現在の標準は、自家移植片及び同種移植片の使用を含むが、これらの方法は、供給及び整合性に制限があるため、非理想的であるという認識が増している。セラミックスは、過去30年間に渡り、従来の骨移植片に取って代わる、又はそれを拡大適用するための、骨移植片補填材としての使用が検討されてきた。特にヒドロキシアパタイトなどのリン酸カルシウム類は、それらの骨伝導能の特性のために奨励されてきた。
【0003】
したがって、外科技術及び医学知識が継続して進歩するにつれて、人工骨補填材への需要が増えている。必然的に、関節及び顔の復元などにおける、荷重有りと無しの両方の場合の骨欠損部の補填のための、人工骨補填材の開発への関心が高まっている。
【0004】
ヒドロキシアパタイトの生体適合性は、ヒドロキシアパタイトの結晶構造が骨のミネラル分と類似していることも相まって、ヒドロキシアパタイトが骨欠損部の増強用材料として多大な関心を集めるきっかけとなった。ミネラル類のアパタイト群は、リン酸カルシウムを基礎とし、化学量論的ヒドロキシアパタイトのCa/Pのモル比は、1.67である。ヒドロキシアパタイトの化学式は、Ca10(PO4)6(OH)2である。
【0005】
シリケート置換のヒドロキシアパタイト組成物は、骨補填材としての化学量論的ヒドロキシアパタイトの興味深い代替となる。ケイ素は、リン酸カルシウムの骨移植片と組み合わせると、骨の治癒の速度及び質を向上させ、その結果埋込み材と宿主との間の骨結合が速まることが判明している。PCT/GB97/02325は、シリケート置換のヒドロキシアパタイト材料を記載している。
【0006】
しかし、問題が存在する。なぜなら、シリケートのヒドロキシアパタイトへの置換には、組成上の限度があるからである。シリケート置換の程度がこの限度を超えたとき、ヒドロキシアパタイトは、一般的な焼結温度(例えば、約1200℃以上)で、熱的に不安定になる恐れがある。これは、例えば、ある用途には望ましくないリン酸三カルシウム(TCP)などの二次相の形成を生じ得る。ヒドロキシアパタイト結晶格子へのシリケート置換の置換限度は、約5.3重量%である(1.6重量%のケイ素に相当)。
【0007】
本発明は、従来技術に関連する少なくとも幾つかの問題の解決に当たること、及び/又は様々なリン酸カルシウム材料に基づく新規な医用材料を提供することを目的とする。
【0008】
したがって、本発明は、ケイ素及び3価カチオンを含む、合成リン酸カルシウム系医用材料を提供する。
【0009】
本発明による医用材料は、例えばヒドロキシアパタイト又はアパタイトなどのリン酸カルシウム材料に基づく。
【0010】
本発明による医用材料は、好ましくは、以下の一般化学式を有する化合物を含む。
Ca10−yMy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、Mは3価カチオンであり、0<x<1.3及び0<y<1.3である。好ましくは、0<x<1.1、より好ましくは0.5<x<1.1である。好ましくは、0<y<1.1、より好ましくは0.5<y<1.1である。また好ましくはx≧yである。)
【0011】
3価カチオンは、好ましくは、イットリウム、スカンジウム、アルミニウム及びランタニド元素のうちの1種又は複数から選択される。好ましくは、3価カチオンはイットリウムであるか、又はイットリウムを含む。
【0012】
3価カチオンは、ヒドロキシアパタイト結晶格子内で、カルシウムイオンを置換すると考えられている。ケイ酸イオンは、ヒドロキシアパタイト結晶格子内で、リン酸イオンを置換すると考えられている。
【0013】
不明確さを避けるため、本明細書で使用する場合、シリケート置換という用語は、ケイ素置換をも包含する。同様に、本明細書で使用する場合、ケイ素置換という用語は、シリケート置換をも包含する。
【0014】
本質的に純相な材料が必要とされる、本発明の一実施形態において、材料の相純度は、好ましくは少なくとも95%、より好ましくは少なくとも97%、さらにより好ましくは少なくとも99%である。この場合、該材料は、実質的にいかなる二次相も含まない。しかし、避けられない不純物が存在し得ることは理解されよう。医用材料の相純度が、従来のX線回折技術で測定できることは理解されよう。
【0015】
二次相の存在が問題とならない別の実施態様において、該材料はさらに、例えばリン酸三カルシウム(例えばα−TCP及び/又はβ−TCP)などの1つ又は複数の二次相を含んでもよい。したがって本発明は、二相及び多相の材料も提供する。二次相は、60重量%まで、より一般的には40重量%まで、さらにより一般的には20重量%までの量で存在してもよい。
【0016】
本発明による医用材料は、人工骨材、骨の埋入み材、骨移植片、骨代替物、骨の足場材、充填材、被覆材又はセメントとして使用してもよい。該医用材料は、多孔性又は無孔性の形で提供してもよい。該医用材料は、例えば生体適合性ポリマーと組み合わせて、複合材の形で提供してもよい。
【0017】
本発明はまた、3価カチオン−シリケート共置換の合成リン酸カルシウム系材料を含む医用材料も提供する。例として挙げられるのは、3価カチオン−シリケート共置換のヒドロキシアパタイト及びアパタイト材料である。3価カチオンは好ましくは、イットリウム、スカンジウム、アルミニウム及びランタニド元素のうちの1種又は複数から選択される。さらに好ましくは、3価カチオンはイットリウムであるか、又はイットリウムを含む。上記に記載の好ましい特徴は、単独で、又は組み合わせて、本発明のこの態様に適用することもできる。
【0018】
本発明による医用材料は、水沈殿法又は固相法、例えば水熱法などによって調製し得る。しかし、水沈殿法が好ましい。したがって、本発明はまた、カルシウム又はカルシウム含有化合物、3価カチオン含有化合物、リン含有化合物及びケイ素含有化合物を用意するステップと、アルカリ性pHで水相の化合物を反応させることによって、沈殿物を形成するステップとを含む、ケイ素及び3価カチオンを含むリン酸カルシウム系医用材料を合成するための方法を提供する。
【0019】
該方法を使用して、ケイ素及び3価カチオンを含むヒドロキシアパタイト及びアパタイト材料を合成してもよい。
【0020】
本発明による方法は、好ましくは水沈殿法である。
【0021】
好ましくは、カルシウム含有化合物は、カルシウム塩を含む。カルシウム塩は、例えば水酸化カルシウム、塩化カルシウム、硝酸カルシウム及び/又は硝酸カルシウム水和物のうちの1種又は複数から選択してもよい。
【0022】
好ましくは、3価カチオン含有化合物は、イットリウムの化合物を含む。イットリウム含有化合物は、例えば塩化イットリウム及び/又は硝酸イットリウムの一方又は両方から選択され、好ましくはY(NO3)3.XH2Oであってよい。
【0023】
イットリウムは、好ましくは、13重量%まで、より好ましくは12重量%までの量で、医用材料(すなわち最終製品)内に存在する。上記考察のように該材料が本質的に純相材料である場合には、これは一般的である。一方、該材料が1つ又は複数の二次相を含む場合、材料中のイットリウムの量は、13重量%を超え、20重量%までの量で存在し得る。
【0024】
好ましくは、ケイ素含有化合物は、シリケートを含有する。さらに好ましくは、シリケートは、オルトケイ酸テトラエチル(TEOS)及び/又は酢酸ケイ素の一方又は両方から選択される。
【0025】
好ましくは、シリケートは13重量%まで(ケイ素として4重量%に相応)、さらに好ましくは12重量%まで(3.66重量%のケイ素に相応)の量で、該材料(すなわち最終製品)内に存在する。上記と同様に、上記考察の材料が本質的に純相材料である場合には、これが一般的である。一方、材料が1つ又は複数の二次相を含む場合は、材料中のシリケートの量は、13重量%を超えてもよく、20重量%までの量で存在し得る。
【0026】
好ましくは、リン含有化合物は、リン酸塩及び/又はリン酸の一方又は両方から選択される。より好ましくは、リン含有化合物は、リン酸アンモニウム及び/又はリン酸の一方又は両方から選択される。
【0027】
一実施形態において、ケイ素含有化合物及び3価カチオン含有化合物は、好ましくはケイ素の量及び3価カチオンの量に対して実質的に等モル量で供給する。代替の実施形態においては、ケイ素含有化合物が、ケイ素の量及び3価カチオンの量に対して、3価カチオン化合物よりも大きなモル量で供給される。
【0028】
本発明の第2の実施形態による方法は、好ましくはアルカリ性pHで実施される。好ましくは、pHは8〜13である。より好ましくは、pHは10〜12である。
【0029】
溶液のpHを所望するpHに調整するために、好ましくはアルカリを溶液に添加する。該アルカリは、例えば水酸化アンモニウム又は濃縮アンモニアであってよい。
【0030】
本発明による方法は、好ましくは、最初に周囲条件下で(但し、このステップは、約100℃までの温度で実施できる)カルシウム又はカルシウム含有化合物(例えばCa(OH)2)及び3価カチオン含有化合物(例えばY(NO3)3.XH2O)を含む水性懸濁液を形成するステップを含む。次に、リン含有化合物(例えばH3PO4)の水溶液を撹拌しながら懸濁液にゆっくりと添加する。最後に、ケイ素含有化合物の水溶液(例えばSi(OC2H5)4=TEOS)を撹拌しながらゆっくりと添加する(代わりに、リン含有化合物の水溶液をケイ素含有化合物の水溶液と混合することもでき、次いでこの配合物を撹拌しながら懸濁液にゆっくりと添加することもできる)。pHを監視し、例えば濃縮アンモニア溶液を用いて、好ましくは11〜13のアルカリ性pHに維持する。全混合物は、次いでそのまま放置、熟成し、沈殿させるが、これには通常12〜24時間かかる。
【0031】
沈殿物が一度形成され、熟成されると、それを乾燥、加熱及び/又は焼結させてもよい。好ましくは、最初にそれを100℃までの温度に加熱することによって、乾燥させる。次いで、800℃〜1500℃、より好ましくは1000℃〜1350℃、さらにより好ましくは1200℃〜1300℃の範囲の温度に加熱して、材料を焼結させてもよい。乾燥した沈殿物は、好ましくは焼結ステップの前に、粉砕して粉末にする。
【0032】
上記のプロセスを使用して、本明細書に記載の本質的に純相の材料を調製してもよい。
【0033】
例えば、単相のイットリア/シリケート共置換のヒドロキシアパタイトよりもイットリア/シリケート共置換による2相の組成物などの、2相又は多相材料の生成が所望される場合、幾つかのステップを単独で又は組み合わせて使用してもよい。以下にその例を挙げる。最初に、沈殿物のpHを11〜13から8〜10に低下させる。これにより、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿が促進され、加熱によって2相のイットリア/シリケート共置換の組成物が形成されることが判明した。第2に、カルシウム塩若しくはイットリウム塩のいずれか、又はこれら2つの組合せであるカチオンを添加し、その相対量が低下するように反応混合物を調整することによって、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進させる。上記と同様に、これは、加熱によって、2相のイットリア/シリケート共置換の組成物を形成することになる。第3に、リン酸塩若しくはケイ酸塩のいずれか、又はこれら2つの組合せであるアニオンを添加し、その相対量が低下するように反応混合物を調整することによって、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進させてもよく、これは加熱によって2相のイットリア/シリケート共置換の組成物を形成することになる。第4に、反応混合組成物の改変と共に、pHを低下させることによって、イットリア/シリケート共置換の、カチオン欠損アパタイト組成物を生成してもよく、これは加熱によって2相のイットリア/シリケート共置換の組成物を形成することになる。イットリアは、例として参照したことを理解されたい。
【0034】
これらの方法に加え、単相のヒドロキシアパタイト様組成物を生成するのに示した限度を超えてシリケート/イットリアの置換量を増加させることによっても、2相のイットリア/シリケート共置換の組成物を加熱により生成することになる。さらに、十分に高い温度(≧1400℃)で、又は高温でより長い加熱時間で、任意の組成物を加熱することによっても、一般に、2相のイットリア/シリケート共置換の組成物が、加熱により生成される結果になるであろう。上記と同様に、イットリアは例として参照したことを理解されたい。
【0035】
本発明はまた、ケイ素置換ヒドロキシアパタイト材料を安定化する方法であって、3価カチオンを結晶格子に共置換するステップを含む方法を提供した。好ましくは、3価カチオンは、イットリウム、スカンジウム、アルミニウム、及びランタニド元素のうちの1種又は複数から選択される。好ましくは、3価カチオンは、イットリウムである。
【0036】
本発明を、以下の好ましい実施形態を参照してこれからさらに説明する。これらの実施形態、実施例及び付属する図は、例として提供される。
【0037】
より多くのシリケートを置換によりリン酸カルシウム結晶格子(例えばヒドロキシアパタイト又はアパタイト)に入れることができるよう、本発明は共置換法を提供しているが、この方法によりイットリウム(又はカルシウムイオンへの置換に適切である他の3価カチオン)は、ケイ酸イオンで共置換される。2つの異なるメカニズムが可能である。第1のメカニズムは、ヒドロキシル(OH)基が、電荷の平衡を保つために、ヒドロキシアパタイト結晶格子から失われることを本質的に否定している。なぜならイットリウム及びケイ酸のイオンのカルシウム及びリン酸のイオンへの等モル置換によって、電荷の平衡が保たれるからである。
(1)Y3+ + SiO44− → Ca2+ + PO43−
これは、以下の一般式にまとめることができる。
Ca10−xYx(PO4)6−x(SiO4)x(OH)2
【0038】
第2の置換においては、比例的により少ないイットリウムイオンが、ケイ酸イオンで共置換され、その結果電荷の平衡を保つためにOH基の程度が減ることになる(例えば、イットリウムのモル量は、置換されたシリケートの半分のモル量である)。
(2) 0.5Y3++SiO44− → 0.5Ca2++PO43−+0.5OH−
これは、以下の一般式にまとめることができる。
Ca10―yYy(PO4)6−x(SiO4)x(OH)2−x+y
(このメカニズムでは、y<x)
【0039】
ヒドロキシアパタイトの結晶格子における他のイオン置換に関しては、置換の限度がある。置換の程度がこれらの限度を超えると、組成物は、焼結中に熱的に不安定になり、ヒドロキシアパタイトの相分解が起こり、二次相の形成を起こす。本発明による共置換法を使用することによって、一般的な温度(約1200℃以上)での焼結の後で相分解が発生しないように、ヒドロキシアパタイト結晶格子のシリケートによる置換の限度を、最大約12重量%のケイ酸イオン(又はケイ素3.66重量%)まで上げてもよい。この限度まで到達した後で、二次相が生成される。ある用途に対しては、本質的に純相の材料が所望され、そのために最大約12重量%のケイ酸イオンが導入される。他の用途に対しては、二次相の存在が実際には所望される(又は問題とならない)こともあり、この場合約12重量%のシリケートという限度を超えてもよい。
【0040】
本発明はさらに、これより以下の実施例及び付属する図面をさらに参照することによって説明される。
【実施例】
【0041】
実施例1: Y3+/SiO44−共置換ヒドロキシアパタイト(x=y=1.0)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法による、Y3+/SiO44−共置換のヒドロキシアパタイト約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=y=1.0である)
【0042】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.0782gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、3.8361gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNH溶液を、Ca(OH)2懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0043】
5.7703gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈した。この溶液を滴下漏斗に注ぎ、約30分間の間、撹拌しているCa(OH)2/YNH懸濁液に滴下添加した。H3PO4溶液を完全に添加した後、2.1278gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注ぎ、約30分間の間、撹拌しているCa(OH)2/YNH/H3PO4混合液に滴下添加した。撹拌している溶液のpHは、H3PO4及びTEOS溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約37.5mlを添加した。TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ICDD標準ピークと一致し、追加的なピークは観察されず、この方法で生成した組成物が、ヒドロキシアパタイト様構造を有する単相材料であることが示された(図1を参照)。
【0044】
実施例2:Y3+/SiO44−共置換ヒドロキシアパタイト(x=1.0、y=0.5)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=1.0、y=0.5である)
【0045】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.3601gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、1.9162gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0046】
5.7708gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。2.1281gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約40mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ICDD標準のピークと一致し、追加的なピークは観察されず、この方法で生成した組成物が、ヒドロキシアパタイト様構造を有する単相材料であることが示された(図2を参照)。
【0047】
実施例3: Y3+/SiO44−共置換ヒドロキシアパタイト(x=y=1.0)の合成
この実施例の合成は、実施例1に記載の合成方法の通りで、唯一異なるのが、H3PO4及びTEOS溶液(それぞれ約100ml)を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に、一緒に混合し、同時に滴下したことであった。この違いは別として、沈殿及び次の加工ステップは、実施例1に記載のステップと同一であった。この方法により生成した焼結試料のX線回折パターンは、実施例1で観察したものと同一であった。
【0048】
実施例4: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=0.6、y=0.6)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=y=0.6である)
【0049】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例1に記載)ではなく、イットリア/シリケート共置換の2相組成物を生成するために、沈殿物のpHを10に低下させ、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。これから、2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0050】
最初に、CaCO3を一晩(16時間)、約900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.2735gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、2.2993gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0051】
6.2286gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。1.2764gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNH懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOS溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH10に維持した。合計で約10mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0052】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両方においてICDD標準のピークと一致し、この方法で生成した組成物が、2相材料であることが示された(図3を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が70%、リン酸三カルシウムの量が30%であると見積もられる。
【0053】
実施例5: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=0.6、y=0.3)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウム2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=0.6、y=0.3である)
【0054】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例2に記載)ではなく、イットリア/シリケート共置換の、y<xである2相組成物を生成するために、沈殿物のpHを10に低下させ、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。これによって、2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0055】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.4461gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、1.1508gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0056】
6.2264gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。1.2817gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH10に維持した。合計で約10mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0057】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8線回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両相においてICDD標準のピークと一致し、この方法で生成した組成物が、2相材料であることが示された(図4を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が85%、リン酸三カルシウムの量が15%であると見積もられる。
【0058】
実施例6: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=y=1.3)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=y=1.3である)
【0059】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例1に記載)ではなく、イットリア/シリケート共置換の2相組成物を生成するために、但しこの場合pH12で、Ca(OH)2及びYNHの不足量を添加し、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。こうして2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0060】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、4.9054gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、4.9807gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0061】
5.4277gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。2.7679gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約40mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0062】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ICDD標準のピークと、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両方において一致し、この方法で生成した組成物が、2相材料であることが示された(図5を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が90%、リン酸三カルシウムの量が10%であると見積もられる。
【0063】
実施例7: Y3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物(x=1.0、y=0.5)の合成
以下の方法は、以下の置換メカニズムに基づく、水沈殿法によるY3+/SiO44−共置換ヒドロキシアパタイト/リン酸三カルシウムの2相混合物約10gの合成を記載するものである。
Ca10−yYy(PO4)6−x(SiO4)x(OH)2−x+y
(式中、x=1.0、y=0.5である)
【0064】
単相のイットリア/シリケート共置換のヒドロキシアパタイト組成物(実施例2に記載)ではなく、y<xである、イットリア/シリケート共置換の2相組成物を生成するために、但しこの場合pH12で、Ca(OH)2及びYNHの不足量を添加し、これによってイットリア/シリケート共置換の、カチオン欠損アパタイト組成物の沈殿を促進した。こうして2相のイットリア/シリケート共置換の組成物が加熱によって形成することになる。
【0065】
最初に、CaCO3を一晩(16時間)900℃の炉の中で脱炭酸した。生成したCaOは、次いで炉から取り出し、デシケーターの中で冷却した。氷浴内で約100mlの脱イオン水を含有するビーカーに、5.3299gのCaOを添加した。CaOが完全に添加された後、氷浴からビーカーを取り除き、撹拌機上に置いた。懸濁液は、約10分間撹拌放置した。CaOは水和してCa(OH)2を形成すると思われる。その一方で、1.9170gのY(NO3)3.6H2O(YNH)を、約100mlの脱イオン水を含有するビーカーに添加し、YNHが完全に溶解するまで混合した。次いでこのYNHの溶液を、Ca(OH)2の懸濁液にゆっくりと注ぎ、この懸濁液を約30分間撹拌放置した。
【0066】
5.7719gのH3PO4(アッセイ濃度85%)を、約100mlの脱イオン水で希釈し、この溶液を滴下漏斗に注いだ。2.1259gのSi(OC2H5)4(TEOS)を約100mlの脱イオン水で希釈し、この溶液を、H3PO4溶液を含有する滴下漏斗に注ぎ、このH3PO4/TEOS溶液を、約60分間の間、撹拌しているCa(OH)2/YNHの懸濁液に滴下添加した。撹拌している溶液のpHは、H3PO4/TEOSの溶液の添加中はずっと監視し、濃縮アンモニア溶液の添加によってpH12に維持した。合計で約40mlを添加した。H3PO4/TEOS溶液を完全に添加した後、全部の混合液をさらに2時間撹拌放置し、その後一晩熟成及び沈殿させた(約16時間)。次いで沈殿物を濾過し、80℃で24時間乾燥し、粉砕して、微粉末を形成した。約3gの乾燥粉末を白金るつぼに置いて、それぞれ2.5°/分及び10°/分の加熱速度及び冷却速度を用いて、炉の中で1200℃で2時間焼結した。
【0067】
次いで、焼結した粉末は、X線回折を用いて分析することにより、相純度を確認した。Bruker D8回折装置を用いて、ステップサイズ0.02°、及びカウント時間1.5秒/ステップで、10〜60°2θのデータを収集した。取得した回折パターンを、ヒドロキシアパタイトのICDD標準パターン(#09−0432)及びα−リン酸三カルシウムの標準パターン(#09−0348)と比較した。焼結したY3+/SiO44−共置換ヒドロキシアパタイトのすべての回折ピークは、ヒドロキシアパタイト相及びα−リン酸三カルシウム相の両方においてICDD標準のピークと一致し、この方法で生成した組成物が、2相材料であることが示された(図6を参照)。ヒドロキシアパタイト相及びα−リン酸三カルシウム相の最も強いピークの強度を比較すると、ヒドロキシアパタイトの量が80%、リン酸三カルシウムの量が20%であると見積もられる。
【0068】
本発明により、一般的な焼結温度、例えば≧1200℃で有意な層分解をまったく起こさずに、より多くのケイ酸イオン(又はケイ素)によるリン酸カルシウム(例えばヒドロキシアパタイト又はアパタイト)結晶格子の置換が可能となる。その結果、現在の置換限界であるシリケート5.3重量%(又はケイ素1.6重量%)を増加させることができ、骨のミネラルの化学組成とよりぴったりと一致する合成医用材料を生成し得る。本発明はケイ素含有量のさらにより高い2相及び多相材料の生成をも可能にする。
【図面の簡単な説明】
【0069】
【図1】図1は、実施例1に対応するX線回折データを示す図である。
【図2】図2は、実施例2に対応するX線回折データを示す図である。
【図3】図3は、実施例4に対応するX線回折データを示す図である。
【図4】図4は、実施例5に対応するX線回折データを示す図である。
【図5】図5は、実施例6に対応するX線回折データを示す図である。
【図6】図6は、実施例7に対応するX線回折データを示す図である。
【特許請求の範囲】
【請求項1】
ケイ素及び3価カチオンを含む、合成リン酸カルシウム系医用材料。
【請求項2】
リン酸カルシウム系医用材料が、ヒドロキシアパタイト又はアパタイトを含む、請求項1に記載の医用材料。
【請求項3】
一般化学式を有する化合物を含む、請求項1又は請求項2に記載の医用材料。
Ca10−yMy(PO4)6−x(SiO4)x(OH)2−x+y
[式中、Mは3価カチオンであり、0<x<1.3、及び0<y<1.3である。]
【請求項4】
0<x<1.1である、請求項3に記載の医用材料。
【請求項5】
0.5<x<1.1である、請求項4に記載の医用材料。
【請求項6】
0<y<1.1である、請求項3〜5のいずれか一項に記載の医用材料。
【請求項7】
0.5<y<1.1である、請求項6に記載の医用材料。
【請求項8】
x≧yである、請求項3〜7のいずれか一項に記載の医用材料。
【請求項9】
y≧xである、請求項3〜7のいずれか一項に記載の医用材料。
【請求項10】
3価カチオンが、イットリウム、スカンジウム、アルミニウム及びランタニド元素のうちの1種又は複数から選択される、請求項1〜9のいずれか一項に記載の医用材料。
【請求項11】
X線回折により測定された医用材料の相純度が、少なくとも95%、好ましくは少なくとも97%、より好ましくは少なくとも99%である、請求項1〜10のいずれか一項に記載の医用材料。
【請求項12】
医用材料が1つ又は複数の二次相を含む、請求項1〜10のいずれか一項に記載の医用材料。
【請求項13】
二次相が、リン酸三カルシウム、そのα又はβ多形、ケイ酸カルシウム、リン酸四カルシウム、炭酸カルシウム、酸化カルシウム、モネタイト、ブルシャイト、ピロリン酸カルシウム、及びリン酸八カルシウムのうちの1種又は複数を含む、請求項12に記載の医用材料。
【請求項14】
3価カチオンが、リン酸カルシウム結晶格子内のカルシウムイオンを置換する、請求項1〜13のいずれか一項に記載の医用材料。
【請求項15】
ケイ酸イオンがリン酸カルシウム結晶格子内のリン酸イオンを置換する、請求項1〜14のいずれか一項に記載の医用材料。
【請求項16】
3価カチオン−シリケート共置換の合成リン酸カルシウム系材料を含む医用材料。
【請求項17】
3価カチオンがイットリウムである、請求項16に記載の医用材料。
【請求項18】
請求項1〜17のいずれか一項に記載の医用材料を含む、人工骨材、骨埋入み材、骨移植片、骨代替物、骨の足場材、充填材、被覆材又はセメント。
【請求項19】
カルシウム又はカルシウム含有化合物、3価カチオン含有化合物、リン含有化合物及びケイ素含有化合物を用意するステップと、
アルカリ性のpHで、水相の化合物を反応させることによって、沈殿物を形成するステップと
を含む、ケイ素及び3価カチオンを含むリン酸カルシウム系材料を合成するための方法。
【請求項20】
リン酸カルシウム系材料が、ヒドロキシアパタイト又はアパタイトを含む、請求項19に記載の方法。
【請求項21】
カルシウム含有化合物が、カルシウム塩を含む、請求項19又は請求項20に記載の方法。
【請求項22】
カルシウム塩が、水酸化カルシウム、塩化カルシウム、硝酸カルシウム及び/又は硝酸カルシウム水和物のうちの1種又は複数から選択される、請求項21に記載の方法。
【請求項23】
3価カチオン含有化合物がイットリウム化合物を含む、請求項19〜22のいずれか一項に記載の方法。
【請求項24】
イットリウム化合物が、塩化イットリウム及び/又は硝酸イットリウムの一方又は両方から選択される、請求項23に記載の方法。
【請求項25】
イットリウムが、13重量%まで、好ましくは12重量%までの量で前記材料に存在する、請求項23又は請求項24に記載の方法。
【請求項26】
イットリウムが、20重量%までの量で前記材料に存在する、請求項23又は請求項24に記載の方法。
【請求項27】
リン含有化合物が、リン酸塩及び/又はリン酸の一方又は両方から選択される、請求項19〜26のいずれか一項に記載の方法。
【請求項28】
リン含有化合物が、リン酸アンモニウム及び/又はリン酸の一方又は両方から選択される、請求項27に記載の方法。
【請求項29】
ケイ素含有化合物が、シリケートを含む、請求項19〜27のいずれか一項に記載の方法。
【請求項30】
シリケートが、オルトケイ酸テトラエチル(TEOS)及び/又は酢酸ケイ素の一方又は両方から選択される、請求項29に記載の方法。
【請求項31】
シリケートが、13重量%まで、好ましくは12重量%までの量で前記材料内に存在する、請求項29又は請求項30に記載の方法。
【請求項32】
シリケートが20重量%までの量で前記材料内に存在する、請求項29又は請求項30に記載の方法。
【請求項33】
pHが8〜13である、請求項19〜32のいずれか一項に記載の方法。
【請求項34】
pHが10〜12である、請求項33に記載の方法。
【請求項35】
アルカリを添加することによって、溶液のpHを所望のpHに調整する、請求項19〜34のいずれか一項に記載の方法。
【請求項36】
アルカリが、水酸化アンモニウム又は濃縮アンモニアである、請求項35に記載の方法。
【請求項37】
沈殿物を、その形成後に乾燥、加熱、及び/又は焼結する、請求項19〜36のいずれか一項に記載の方法。
【請求項38】
沈殿物が800℃〜1500℃の範囲の温度に加熱及び/又は焼結される、請求項37に記載の方法。
【請求項39】
沈殿物が1000℃〜1350℃、好ましくは1200℃〜1300℃の範囲の温度に加熱及び/又は焼結される、請求項38に記載の方法。
【請求項40】
ケイ素含有化合物及び3価カチオン含有化合物が、ケイ素の量及び3価カチオンの量に対して等モル量で供給される、請求項19〜39のいずれか一項に記載の方法。
【請求項41】
ケイ素含有化合物が、ケイ素の量及び3価カチオンの量に対して、3価カチオン化合物より多い量で供給される、請求項19〜39のいずれか一項に記載の方法。
【請求項42】
ケイ素含有化合物が、ケイ素の量及び3価カチオンの量に対して、3価カチオン化合物より少ない量で供給される、請求項19〜39のいずれか一項に記載の方法。
【請求項43】
3価カチオンを置換により結晶格子に入れることを特徴とする、ケイ素置換リン酸カルシウム材料を安定化する方法。
【請求項44】
リン酸カルシウム材料が、ヒドロキシアパタイト又はアパタイトを含む、請求項43に記載の方法。
【請求項45】
3価カチオンがイットリウムである、請求項43又は請求項44に記載の方法。
【請求項1】
ケイ素及び3価カチオンを含む、合成リン酸カルシウム系医用材料。
【請求項2】
リン酸カルシウム系医用材料が、ヒドロキシアパタイト又はアパタイトを含む、請求項1に記載の医用材料。
【請求項3】
一般化学式を有する化合物を含む、請求項1又は請求項2に記載の医用材料。
Ca10−yMy(PO4)6−x(SiO4)x(OH)2−x+y
[式中、Mは3価カチオンであり、0<x<1.3、及び0<y<1.3である。]
【請求項4】
0<x<1.1である、請求項3に記載の医用材料。
【請求項5】
0.5<x<1.1である、請求項4に記載の医用材料。
【請求項6】
0<y<1.1である、請求項3〜5のいずれか一項に記載の医用材料。
【請求項7】
0.5<y<1.1である、請求項6に記載の医用材料。
【請求項8】
x≧yである、請求項3〜7のいずれか一項に記載の医用材料。
【請求項9】
y≧xである、請求項3〜7のいずれか一項に記載の医用材料。
【請求項10】
3価カチオンが、イットリウム、スカンジウム、アルミニウム及びランタニド元素のうちの1種又は複数から選択される、請求項1〜9のいずれか一項に記載の医用材料。
【請求項11】
X線回折により測定された医用材料の相純度が、少なくとも95%、好ましくは少なくとも97%、より好ましくは少なくとも99%である、請求項1〜10のいずれか一項に記載の医用材料。
【請求項12】
医用材料が1つ又は複数の二次相を含む、請求項1〜10のいずれか一項に記載の医用材料。
【請求項13】
二次相が、リン酸三カルシウム、そのα又はβ多形、ケイ酸カルシウム、リン酸四カルシウム、炭酸カルシウム、酸化カルシウム、モネタイト、ブルシャイト、ピロリン酸カルシウム、及びリン酸八カルシウムのうちの1種又は複数を含む、請求項12に記載の医用材料。
【請求項14】
3価カチオンが、リン酸カルシウム結晶格子内のカルシウムイオンを置換する、請求項1〜13のいずれか一項に記載の医用材料。
【請求項15】
ケイ酸イオンがリン酸カルシウム結晶格子内のリン酸イオンを置換する、請求項1〜14のいずれか一項に記載の医用材料。
【請求項16】
3価カチオン−シリケート共置換の合成リン酸カルシウム系材料を含む医用材料。
【請求項17】
3価カチオンがイットリウムである、請求項16に記載の医用材料。
【請求項18】
請求項1〜17のいずれか一項に記載の医用材料を含む、人工骨材、骨埋入み材、骨移植片、骨代替物、骨の足場材、充填材、被覆材又はセメント。
【請求項19】
カルシウム又はカルシウム含有化合物、3価カチオン含有化合物、リン含有化合物及びケイ素含有化合物を用意するステップと、
アルカリ性のpHで、水相の化合物を反応させることによって、沈殿物を形成するステップと
を含む、ケイ素及び3価カチオンを含むリン酸カルシウム系材料を合成するための方法。
【請求項20】
リン酸カルシウム系材料が、ヒドロキシアパタイト又はアパタイトを含む、請求項19に記載の方法。
【請求項21】
カルシウム含有化合物が、カルシウム塩を含む、請求項19又は請求項20に記載の方法。
【請求項22】
カルシウム塩が、水酸化カルシウム、塩化カルシウム、硝酸カルシウム及び/又は硝酸カルシウム水和物のうちの1種又は複数から選択される、請求項21に記載の方法。
【請求項23】
3価カチオン含有化合物がイットリウム化合物を含む、請求項19〜22のいずれか一項に記載の方法。
【請求項24】
イットリウム化合物が、塩化イットリウム及び/又は硝酸イットリウムの一方又は両方から選択される、請求項23に記載の方法。
【請求項25】
イットリウムが、13重量%まで、好ましくは12重量%までの量で前記材料に存在する、請求項23又は請求項24に記載の方法。
【請求項26】
イットリウムが、20重量%までの量で前記材料に存在する、請求項23又は請求項24に記載の方法。
【請求項27】
リン含有化合物が、リン酸塩及び/又はリン酸の一方又は両方から選択される、請求項19〜26のいずれか一項に記載の方法。
【請求項28】
リン含有化合物が、リン酸アンモニウム及び/又はリン酸の一方又は両方から選択される、請求項27に記載の方法。
【請求項29】
ケイ素含有化合物が、シリケートを含む、請求項19〜27のいずれか一項に記載の方法。
【請求項30】
シリケートが、オルトケイ酸テトラエチル(TEOS)及び/又は酢酸ケイ素の一方又は両方から選択される、請求項29に記載の方法。
【請求項31】
シリケートが、13重量%まで、好ましくは12重量%までの量で前記材料内に存在する、請求項29又は請求項30に記載の方法。
【請求項32】
シリケートが20重量%までの量で前記材料内に存在する、請求項29又は請求項30に記載の方法。
【請求項33】
pHが8〜13である、請求項19〜32のいずれか一項に記載の方法。
【請求項34】
pHが10〜12である、請求項33に記載の方法。
【請求項35】
アルカリを添加することによって、溶液のpHを所望のpHに調整する、請求項19〜34のいずれか一項に記載の方法。
【請求項36】
アルカリが、水酸化アンモニウム又は濃縮アンモニアである、請求項35に記載の方法。
【請求項37】
沈殿物を、その形成後に乾燥、加熱、及び/又は焼結する、請求項19〜36のいずれか一項に記載の方法。
【請求項38】
沈殿物が800℃〜1500℃の範囲の温度に加熱及び/又は焼結される、請求項37に記載の方法。
【請求項39】
沈殿物が1000℃〜1350℃、好ましくは1200℃〜1300℃の範囲の温度に加熱及び/又は焼結される、請求項38に記載の方法。
【請求項40】
ケイ素含有化合物及び3価カチオン含有化合物が、ケイ素の量及び3価カチオンの量に対して等モル量で供給される、請求項19〜39のいずれか一項に記載の方法。
【請求項41】
ケイ素含有化合物が、ケイ素の量及び3価カチオンの量に対して、3価カチオン化合物より多い量で供給される、請求項19〜39のいずれか一項に記載の方法。
【請求項42】
ケイ素含有化合物が、ケイ素の量及び3価カチオンの量に対して、3価カチオン化合物より少ない量で供給される、請求項19〜39のいずれか一項に記載の方法。
【請求項43】
3価カチオンを置換により結晶格子に入れることを特徴とする、ケイ素置換リン酸カルシウム材料を安定化する方法。
【請求項44】
リン酸カルシウム材料が、ヒドロキシアパタイト又はアパタイトを含む、請求項43に記載の方法。
【請求項45】
3価カチオンがイットリウムである、請求項43又は請求項44に記載の方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公表番号】特表2008−544792(P2008−544792A)
【公表日】平成20年12月11日(2008.12.11)
【国際特許分類】
【出願番号】特願2008−518967(P2008−518967)
【出願日】平成18年6月29日(2006.6.29)
【国際出願番号】PCT/GB2006/002411
【国際公開番号】WO2007/000608
【国際公開日】平成19年1月4日(2007.1.4)
【出願人】(501306999)ザ・ユニバーシティ・コート・オブ・ザ・ユニバーシティ・オブ・アバディーン (6)
【出願人】(508004557)アパテック リミテッド (6)
【Fターム(参考)】
【公表日】平成20年12月11日(2008.12.11)
【国際特許分類】
【出願日】平成18年6月29日(2006.6.29)
【国際出願番号】PCT/GB2006/002411
【国際公開番号】WO2007/000608
【国際公開日】平成19年1月4日(2007.1.4)
【出願人】(501306999)ザ・ユニバーシティ・コート・オブ・ザ・ユニバーシティ・オブ・アバディーン (6)
【出願人】(508004557)アパテック リミテッド (6)
【Fターム(参考)】
[ Back to top ]

