医療装置のための樹状突起状で星形の造影剤、および生体吸収性で放射線不透過性のバルク材料、およびこれらを製造するための方法
【課題】高強度の放射線不透過性の造影剤を提供する。
【解決手段】この造影剤はバルク材料の上に被覆するかその中に組み込むことができ、この材料はさらにその後に放射線不透過性の医療装置を作るために利用できる。化学的性質による主要な効果はその放射線不透過性の要素または物質の単位重量当たりの比較的に高い放射線不透過性の濃度を含む。また、二次的な効果はその放射線不透過性の要素の選択的な配置を含み、このことはさらに、その放射線不透過性の物質の必要性の減少により、その装置の放射線不透過性を高めることができる。このような放射線不透過性の造影剤は、樹状突起体等のような、種々の形態で製造でき、さらに/または、高分子鎖の端部の基として組み込むことができる。加えて、本発明との組み合わせにおいて、生物学的な、さらに/または、薬剤用の、物質を組み込むことも可能である。
【解決手段】この造影剤はバルク材料の上に被覆するかその中に組み込むことができ、この材料はさらにその後に放射線不透過性の医療装置を作るために利用できる。化学的性質による主要な効果はその放射線不透過性の要素または物質の単位重量当たりの比較的に高い放射線不透過性の濃度を含む。また、二次的な効果はその放射線不透過性の要素の選択的な配置を含み、このことはさらに、その放射線不透過性の物質の必要性の減少により、その装置の放射線不透過性を高めることができる。このような放射線不透過性の造影剤は、樹状突起体等のような、種々の形態で製造でき、さらに/または、高分子鎖の端部の基として組み込むことができる。加えて、本発明との組み合わせにおいて、生物学的な、さらに/または、薬剤用の、物質を組み込むことも可能である。
【発明の詳細な説明】
【開示の内容】
【0001】
〔関連の出願に対するクロス・リファレンス〕
本特許出願は米国特許法第119(e)条に基いて、2005年、3月18日に出願されている米国仮特許出願第60/662,957号の優先権を主張している。
【0002】
〔発明の分野〕
本発明は医療の治療および処置において用いる脈管内装置に関連している。さらに具体的に言えば、本発明は、医療装置、特に、ポリマーの一端部または両端部において結合されている、内部に造影剤が分散されているポリマーにより作られている高分子の医療装置および高分子の被膜、の画像化を向上させるために適している新しい種類の有機性の高強度X線造影剤、ならびに、これらの材料および装置の製造の方法に関連している。
【0003】
〔関連技術の論述〕
最近において、経管プロテーゼが血管、胆管、またはその他の生体の類似の器官の中における移植のための医療技術において広く用いられている。これらのプロテーゼはステントとして一般的に知られており、管状の構造を維持して、開口させるか、拡張するために用いられている。一般的に用いられているステントの例が、参照により、本明細書に組み入れられている、1985年11月7日にパルマズ(Palmaz)により出願されている、米国特許第4,733,665号において記載されている。これらのステントはバルーン式の拡張可能なステントとして呼ばれる場合が多い。一般的に、ステントはステンレス鋼の固体の管により作成されているが、別の金属材料も利用されている。その後、そのステントの壁部に一連の切り込みが作成される。このステントは第1の比較的に小さい直径を有しており、この第1の直径は、ステントが、バルーン・カテーテルの上に圧着されることにより、人間の脈管の中を通して送達されることを可能にする。このステントはまた、その管状に造形された部材の内部から、バルーン・カテーテルにより、半径方向に、外側に向けられた力の供給時に、第2の拡張された直径も有する。
【0004】
しかしながら、上記のステントに伴う一つの問題はこれらが頸動脈等のような一部の脈管の中の使用において実用的でない場合が多いことである。この頸動脈は人間の体の外部から容易に接近可能であり、皮膚の表面に近い。ステンレス鋼等により作成されているバルーン拡張式のステントを頚動脈に有している患者は日々の活動を通して深刻な傷害を受ける可能性が高い。例えば、患者の首に十分な力が加わることにより、そのステントが崩壊して、その患者に対する傷害を生じる可能性がある。このことを防ぐために、自己拡張式のステントが上記のような脈管の中における使用のために提案されている。これらの自己拡張式のステントはばねのように作用して、つぶされた後に、拡張および埋め込まれた形態に戻る。
【0005】
自己拡張式ステントの一つの種類が米国特許第4,655,771号において開示されており、このステントは半径方向および軸方向に柔軟で弾性的な管状の本体部分を有しており、この本体部分は当該本体部分の両端部の互いに対する軸方向の移動において可変である所定の直径を伴っていて、半径方向に自己拡張性のらせんを定めている複数の個々に剛性であるが柔軟で弾性的な糸状の要素により構成されている。この種のステントは「編組型ステント」として当業界において知られており、本明細書においてこのように示されている。体内の脈管の中におけるこのようなステントの配置は、先端部においてそのステントを保持するための外側のカテーテルと、ステントが配置された後にそのステントを前方に押し出す内側のピストンとを備えている装置により、達成できる。
【0006】
しかしながら、編組型ステントは多くの不都合を有している。これらは一般的に病気の脈管を開口した状態に有効に維持するために必要な半径方向の強度を有していない。加えて、これらのステントを作成するために用いられている複数のワイヤまたはファイバーは、ステントの本体部分から分離されると、危険になる可能性があり、このような場合に、これらは脈管を突き刺すことも有り得る。それゆえ、市場において入手可能な多くのバルーン拡張式ステントのための一般的な製造方法である、金属の管から切り出された自己拡張式ステントを有することに対する要望が存在している。管から切り出された自己拡張式ステントを製造するために、用いられる合金は、好ましくは、体温において、超弾性または擬弾性の特性を示し、これにより、回復可能につぶれる。
【0007】
先行技術はニチノール(Nitinol)(ニッケル−チタン合金)等のような合金の使用を参考にしており、この合金は、患者の体内に挿入されるように設計されている医療装置の中において、形状記憶および/または超弾性の特性を有する。この形状記憶特性は、上記の装置が体内の内腔またはキャビティの中へのこれらの挿入を容易にするために変形された後に、その装置がその元の形状に戻るように、その体内において加熱されること、を可能にする。一方、超弾性特性は一般に、患者の体内への上記の金属を含有している医療装置の挿入を容易にするように変形されている状態に、その金属が変形して拘束されることを可能にし、このような変形は相転移を生じる。いったん、体内腔の中に入ると、上記の超弾性の部材における拘束は解除でき、これにより、応力が減少して、その超弾性の部材はその元の相に戻る転移により、その元の変形されていない形状に戻ることができる。
【0008】
上記の形状記憶/超弾性の特性を有する合金は一般に少なくとも2種類の相を有している。これらの相は、比較的に小さい引張強さを有していて比較的に低い温度において安定であるマルテンサイト相(martensite phase)と、比較的に大きい引張強さを有していてマルテンサイト相よりも高い温度において安定であるオーステナイト相(austenite phase)である。
【0009】
形状記憶特性は、マルテンサイト相からオーステナイト相への転移が完全になる温度よりも高い温度、すなわち、オーステナイト相が安定である温度よりも高い温度(Af 温度)において、上記の金属を加熱することにより、その合金に賦与される。この熱処理の間における上記の金属の形状が「記憶された」形状である。その後、この熱処理された金属はマルテンサイト相が安定である温度まで冷却され、オーステナイト相をマルテンサイト相に転移させる。次に、このマルテンサイト相の金属は、例えば、患者の体内へのその導入を容易にするために、可塑的に変形される。その後、この変形されたマルテンサイト相をそのマルテンサイト相からオーステナイト相への転移温度よりも高い温度まで加熱することにより、その変形されたマルテンサイト相がオーステナイト相に転移し、この相転移の間に、その金属は、拘束されていなければ、その元の形状に戻る。しかし、拘束されていれば、その金属は、その拘束が解除されるまで、マルテンサイト相を維持する。
【0010】
患者の体内に置くことを目的としている医療装置において上記の合金の形状記憶特性を用いる方法は動作上の困難さをもたらしている。例えば、体温よりも低い安定なマルテンサイト温度を有する形状記憶合金を用いれば、上記の医療装置が患者の体内に挿入されている時に、マルテンサイト相からオーステナイト相への転移を阻止するために、そのような合金を含有しているその医療装置の温度を体温よりも十分に低く維持することが困難になる場合が多い。一方、体温よりも十分に高いマルテンサイト相からオーステナイト相への転移温度を有する形状記憶合金により形成されている脈管内装置を用いると、これらの装置は、ほとんどまたは全く問題を伴わずに、患者の体内に導入できるが、これらはマルテンサイト相からオーステナイト相への転移温度まで加熱する必要があり、この温度は組織の損傷を引き起こすのに十分に高い場合が多い。
【0011】
オーステナイト相が安定である温度(すなわち、マルテンサイト相からオーステナイト相への転移が完全になる温度)よりも高い温度において超弾性特性を示すニチノール等のような金属の試料に応力が加えられると、その試料は、その合金がさらにオーステナイト相からマルテンサイト相への応力誘発型の相転移を生じる段階における特定の応力レベルに到達するまで、弾性的に変形する。さらに、上記の相転移が進行すると、上記の合金はひずみにおけるかなりの増加を生じるが、応力においてはほとんどまたは全く付随する増加を生じない。その後、このひずみは増加するが、応力は、オーステナイト相からマルテンサイト相への転移が完全になるまで、実質的に一定に保たれる。その後は、応力におけるさらなる増加がさらなる変形を引き起こすために必要になる。この場合に、マルテンサイト相の金属は、追加の応力の供給時に、最初に弾性的に変形し、その後、永久的な残留変形により可塑的に変形する。
【0012】
何らかの永久的な変形が生じる前に上記の試料における負荷が除去されると、そのマルテンサイト相の試料はオーステナイト相に弾性的に戻って転移する。この応力の減少は最初にひずみの減少を引き起こす。その後、この応力の減少が、マルテンサイト相がオーステナイト相に転移して戻るレベルに到達すると、その試料における応力のレベルは、そのオーステナイト相に戻る転移が完全になるまで、すなわち、付随する応力が無視できる程度にしか減少せずに、ひずみにおけるかなりの回復が生じるまで、(オーステナイト相がマルテンサイト相に転移する一定の応力のレベルよりは実質的に低いが)実質的に一定に維持される。このオーステナイト相に戻る転移が完全になると、さらなる応力の減少が弾性ひずみの減少を生じる。このような負荷の供給時に、比較的に一定の応力において、かなりのひずみを生じて、その負荷の除去時に変形から回復するための能力は、超弾性または擬弾性と一般的に呼ばれている。上記の管切断型の自己拡張式ステントの製造において材料を有用にしているのは、このような材料の特性である。
【0013】
先行技術は、患者の体内に挿入するかその他の様式で使用することを目的としている医療装置における、超弾性の特性を有する金属の合金の使用を参考にしている。例えば、米国特許第4,665,905号(ジャービス(Jervis))および米国特許第4,925,445号(サカモト(Sakamoto)他)を参照されたい。しかしながら、このような先行技術は依然として適当な管切断型の自己拡張式ステントを全く開示していない。加えて、先行技術のステントの多くは身体の脈管を開口状態に維持するために必要な剛性またはフープの強度を欠いていた。さらに、先行技術のステントの多くはそれぞれの拡張された直径において大きな開口部を有する。この拡張されたステントにおける開口部が小さいほど、そのステントと脈管の壁部との間にその開口部が捕捉できるプラークまたはその他の堆積物の量が多くなる。これらの堆積物の捕捉は、この捕捉が、脈管内へのプラークの脱出、ステントが植え込まれている脈管の再狭窄、および血流内への塞栓形成性の粒子の放出により生じる発作、を阻止することに役立つ点において、患者の健康状態の継続にとって重要である。
【0014】
これらのステント、およびその他の医療装置に伴う一つの付加的な問題は、これらがX線透視下において低下された放射線不透過性を示す可能性があることである。この問題を解消するために、高度に放射線不透過性の材料により作成した標識をステントに取り付けること、またはめっきまたは塗布の方法で放射線不透過性の材料を使用することが一般的な実施方法である。このような材料は一般的に金、プラチナ、またはタンタルである。さらに、先行技術は米国特許第5,632,771号(ボートマン(Boatman)他)、米国特許第6,022,374号(イムラン(Imran))、米国特許第5,741,327号(フランツェン(Frantzen)、米国特許第5,725,572号(ラム(Lam)他)、および米国特許第5,800,526号(アンダーソン(Anderson)他)における上記のような標識または方法を参考にしている。しかしながら、ガルバニ列におけるステントの基材の位置に対するガルバニ列における上記の材料の相対的な位置により、解消すべき特定の課題、すなわち、電解腐食、が存在している。
【0015】
加えて、金属材料の使用を避けている、生体分解性のステント、および高分子材料により作られているステントはさらにX線透視下において可視化されることが可能である必要がある。これらの種類の装置においては、放射線不透過性の標識または被膜の使用を伴わずにこれらの装置における放射線不透過性を賦与/増加する方法において、重大な課題が存在している。先行技術は米国特許第4,935,019号(パップ(Papp))における一例のこのような方法を参考にしており、この場合に、外科用の布地の上に印刷するために適している放射線不透過性で高分子の組成物がX線検出可能な標識を構成しており、この標識は液体のポリマーのキャリアの中に、硫酸バリウム等のような、重金属の塩を分散させることにより得られる。このパップ(Papp)において、上記の硫酸バリウムは約5ミクロンよりも大きい平均の粒度を有しており、上記の組成物の全体の固形物の約15〜90重量%の量で存在している。さらに、パップ(Papp)は上記の組成物の約60〜90重量%を占める硫酸バリウムが好ましいことを示している。しかしながら、このように大きな割合の量での硫酸バリウムの添加は基材の構造の完全性に悪影響を及ぼす可能性があり、強度を低下させ、その他の機械的な特性および特徴に有害に影響する。また、生体分解性のポリマーにおいて、放射線不透過性の添加物の影響力は、生体吸収性のポリマーの分解速度、弾性等のような特性にも有害な影響を及ぼす可能性があると共に、材料の中における何らかの局在化された濃度の硫酸バリウム粒子の中またはそれらの周囲における応力の増加因子の存在を潜在的に加える。さらに、硫酸バリウムおよび酸化ジルコニウム等のような、無機の造影剤は有機溶媒中に容易に溶解せず、あるいは、容易に分散せず、これらは非分解性で生体分解性のポリマーを溶解するために一般的に用いられている。
【0016】
従って、結果として得られる組成物の材料が適当に放射線不透過性になるように、ポリマーの中に容易に溶解して、その材料自体に、または放射線不透過性にすることを望む材料の機械的な特性に、有害な影響を及ぼさずに、生体安定性の高分子および生体分解性の高分子の材料に、容易に添加できる放射線不透過性の材料または物質に対する要望が存在している。
【0017】
〔発明の概要〕
本発明による高強度X線造影剤は現在において利用可能であるものの不都合点および欠点を解消して、一次的および二次的な両方の作用により、X線造影剤の強度を最大にすることにより、画像化用の医療装置、特に、非金属の医療装置、における満たされていない要望を満足させている。主要な作用は放射線不透過性の要素を組み込んで、化学的性質により造影剤の中のその要素の含有量を最大にすることを含み、二次的な作用はポリマーの中の放射線不透過性の要素の位置を最適化することを含む。本質的に、ポリマーの中全体に亘って分散しているヨウ素の含有量を選択的に最大にして組み込むことにより、高分子材料の放射線不透過性を、以前には利用可能でなかったレベルまで調整することが可能になる。さらに、このような造影剤の形成および最適化は高分子材料に対して組み込まれる時に改善された処理特性を与え、したがって、製造費用をさらに減少させると共に、十分な分解特性と共に改善された高強度の放射線不透過性を伴う高分子材料を提供することを可能にする。
【0018】
本発明は植え込み可能な高分子の医療装置と共に使用するために、または植え込み可能な医療装置の高分子の被膜のために適している高強度の樹状突起状のまたは星形の造影剤に関連している。ペンタエリスリトール(pentaerythritol)、ビス−ペンタエリスリトール・グリセロール(bis-pentaerythritol glycerol)、多価のモノ−およびジ−サッカリド等の、多価のヒドロキシルまたはアミンを含んでいる有機化合物は、ヨウ素含有の2,3,5−トリヨード安息香酸(2,3,4-triiodobenzoic acid)等のような芳香族化合物と共に反応させて、上記のような高濃度のヨウ素含有の化合物を形成するために使用できる。それぞれのこのような化合物は3個の倍数のヨウ素原子を含むことができ、このような化合物を含んでいる材料により作られた医療装置のX線画像を強く増感させる。このような高強度の樹状突起状の造影剤におけるヨウ素の含有量は、市場において入手可能な樹状突起状のポリアミン前駆体を用いて、85%程度の高さにすることができる。
【0019】
本発明の例示的な実施形態において、上記の造影剤は、上記の装置を作るかその装置に被膜として供給される材料の全体に亘ってその造影剤を分散させることにより作られるX線画像を向上させるために、単一の分子の中に多数のヨウ素原子または臭素原子またはこれらの両方の組み合わせを含むことができる。本発明によれば、上記の造影剤は、アミン、ヒドロキシル、スルフヒドリル、イソシアネート等のような、遊離の官能基を含んでいる樹状突起体の任意のコアにより構成することができ、トリヨード安息香酸(triiodobenzoic acid)またはトリヨード安息香酸の塩化物(triiodobenzoic acid chloride)等のような、少量のヨウ素または臭素を含んでいるビルディング・ブロックにおけるそれぞれの付加的な結合を伴って、3個の倍数のヨウ素または臭素またはこれらの両方の原子の組み合わせを含んでいる分子を結果として形成できる。このような様式で構成される場合に、上記の造影剤は、アセトン、ジメチルアセトアミド(dimethylacetamide)(DMA)、ジメチルスルホキシド(dimethylsulfoxide)(DMSO)、アセトン、THF、1,4−ジオキサン(1,4-dioxane)、DCM等のような、一般的な有機溶媒の中で実質的に溶けることができ、PLGA、PLA等のような、一般的な有機ポリマーに対して実質的に良好な混和性も有している。本発明による造影剤は、ポリマー基材により固溶体を形成して、これにより医療装置の基材を形成できる。本発明による造影剤は実質的に生体適合性であり、材料のX線画像品質を高めるために、ポリマーまたはポリマーの混合物、および/または無機/有機の組成物の材料に添加できる。
【0020】
本発明の別の例示的な実施形態において、上記の造影剤は、医療装置または医療装置の被膜を形成するために、溶液流延、射出成形および/または圧縮成形等のような、種々の手段によりバルク材料と共に混合できる。その後、このバルクの形態は従来の製造方法により最終的な大きさおよび形状に加工できる。あるいは、上記の造影剤を含んでいる高分子の被膜は従来の塗布方法を用いて植え込み可能な医療装置の表面に供給できる。
【0021】
本発明のさらに別の例示的な実施形態において、高分子の構造に対する上記の造影剤の選択的な組み込みは多数の方法で達成できる。このポリマー構造の特定の領域内であって、他の領域内にはない、造影剤の配置を確実にすることにより、放射線不透過性における付加的で二次的な改善が材料および/または機械的な特性に有害な影響を及ぼさずに実現できる。一つのこのような例はポリマー鎖の基端部および先端部における造影剤の組み込みである。例えば、ポリマーの中においてポリマー鎖の高度な分子の配向状態を与えることのできる、オリエントルージョン(orientrusion)等のような方法を利用することにより、そのバルク材料の選択的な部分において高強度の放射線不透過性を伴う高分子材料を形成することができ、これらの部分は、造影剤が存在していない周りの領域よりも、かなり高い放射線不透過性になると考えられる。同様に、被膜材料の中における上記の造影剤の選択的な配置は、バルク材料の中における造影剤の選択的な配置により得られる利点と、同様の二次的な利点を与えることができる。
【0022】
本発明のさらに別の例示的な実施形態において、高分子の構造に対する上記の造影剤の選択的な組み込みは、生体安定性および/または生体分解性のポリマー鎖の先端部および基端部のいずれか、またはこれらの両方の端部における共有結合法により達成できる。このような固有の放射線不透過性を伴うポリマーは、植え込み可能な医療装置を構築するために、あるいは、植え込み可能な医療装置のための被膜として、使用できる。
【0023】
さらに、上記材料を伴うまたはその材料の上における生物学的なさらに/または薬剤用の物質の組み込みまたは供給は、本発明との組み合わせにおいて用いられる場合に、付加的な利点を与えることができ、したがって本発明のさらに別の目的でもある。以下において定められているような化合物は上記の装置の上に被膜として供給するか、上記のポリマーの中に組み込むことが可能であり、治療用および薬剤用の物質を送達するために使用でき、これらの物質は、ビンカ・アルカロイド(vinca alkaloids)(すなわち、ビンブラスチン(vinblastine)、ビンクリスチン(vincristine)、およびビノレルビン(vinorelbine))、パクリタキセル(paclitaxel)、エピジポドフィロトキシン(epidipodophyllotoxins)(すなわち、エトポシド(etoposide)、テニポシド(teniposide))、抗生物質(antibiotics)(ダクチノマイシン(dactinomycin)(アクチノマイシンD(actinomycin D))、ダウノルビシン(daunorubicin)、ドキソルビシン(doxorubicin)およびイダルビシン(idarubicin))、アントラサイクリン(anthracyclines)、ミトキザントロン(mitoxantrone)、ブレオマイシン(bleomycins)、プリカマイシン(plicamycin)(ミトラマイシン(mithramycin))およびマイトマイシン(mitomycin)、酵素(L−アスパラギン(L-asparagine)を全身系的に代謝し、固有のアスパラギンを合成する能力を有していない細胞を奪取する、L−アスパラギナーゼ(L-asparaginase))等のような天然産物を含む抗増殖/抗有糸分裂剤、G(GP)IIb /IIIa 抑制因子およびビトロネクチン・レセプタ(vitronectin receptor)拮抗質等のような抗血小板剤、ナイトロジェン・マスタード(nitrogen mustards)(メクロレタミン(meclorethamine)、シクロホスファミド(cyclophosphamide)および類似体、メルファラン(melphalan)、クロラムブシル(chlorambucil))、エチレンイミン(ethylenimines)およびメチルメラミン(methylmelamines)(ヘキサメチルメラミン(hexamethylmelamine)およびチオテパ(thiotepa))、アルキル・スルホネート−ブスルファン(alkyl sulfonates-busulfan)、ニトロソウレア(nitrosoureas)(カルムスチン(carmustine)(BCNU)および類似体、ストレプトゾシン(streptozocin))、トラゼン−ダカルバジニン(trazenes-dacarbazinine)(DTIC)等のような抗増殖/抗有糸分裂性のアルキル化剤、葉酸類似体(メトトレキセート(methotrexate))、ピリミジン類似体(フルオロウラシル(fluorouracil)、フロクスウリジン(floxuridine)、およびシタラビン(cytarabine))、プリン類似体および関連の抑制因子(メルカプトプリン(mercaptopurine)、チオグアニン(thioguanine)、ペントスタチン(pentostatin)および2−クロロデオキシアデノシン(2-chlorodeoxyadenosine)(クラドリビン(cladribine)))等のような抗増殖/抗有糸分裂性の代謝拮抗物質、プラチナ配位錯体(シスプラチン(cisplatin)、カルボプラチン(carboplatin))、プロカルバジン(procarbazine)、ヒドロキシウレア(hydroxyurea)、ミトーテン(mitotane)、アミノグルテチミド(aminoglutethimide)、ホルモン(すなわち、エストロゲン(estrogen))、抗凝固薬(ヘパリン(heparin)、合成ヘパリン(heparin)の塩およびトロンビン(thrombin)の他の抑制因子)、フィブリン溶解剤(組織プラスミノゲン(plasminogen)活性薬、ストレプトキナーゼ(streptokinase)およびウロキナーゼ(urokinase)等)、アスピリン(aspirin)、ジピリダモール(dipyridamole)、チクロピジン(ticlopidine)、クロピドグレル(clopidogrel)、アブシキシマブ(abciximab)、抗遊走薬(antimigratory)、抗分泌薬(antisecretory)(ブレベルジン(breveldin))、アドレノコルチカル・ステロイド(コルチソル(cortisol)、コルチゾン(cortison)、フルドロコルチゾン(fludrocortisone)、プレドニソン(prednisone)、プレドニソロン(prednisolone)、6α−メチルプレドニソロン(6α-methylprednisolone)、トリアムシノロン(triamcinolone)、ベタメタゾン(betamethasone)、およびデキサメタゾン(dexamethasone))等のような抗炎症薬、非ステロイド薬(サリチル酸(salicylic acid)誘導体、すなわち、アスピリン(aspirin)、パラ−アミノフェノール(para-aminophenol)誘導体、すなわち、アセトアミノフェン(acetaminophen)、インドール(indole)およびインデン(indene)酢酸(インドメタシン(indomethacin)、スリンダク(sulindac)、およびエトダラク(etodalac))、ヘテロアリール酢酸(トルメチン(tolmetin)、ジクロフェナク(diclofenac)、およびケトロラク(ketorolac)、アリールプロピオン酸(arylpropionic acid)(イブプロフェン(ibuprofen)および誘導体)、アントラニル酸(anthranilic acid)(メフェナム酸(mefenamic acid)、およびメクロフェナム酸(meclofenamic acid))、エノール酸(enolic acid)(ピロキシカム(piroxicam)、テノキシカム(tenoxicam)、フェニルブタゾン(phenylbutazone)、およびオキシフェンタトラゾン(oxyphenthatrazone))、ナブメトン(nabmetone)、金化合物(オーラノフィン(auranofin)、オーロチオグルコース(aurothioglucose)、金−ナトリウム・チオマレート(gold sodium thiomalate))、免疫抑制薬(シクロスポリン(cyclosporine)、タクロリムス(tacrolimus)(FK−506)、シロリムス(sirolimus)(ラパマイシン(rapamycin))、アザチオプリン(azathioprine)、マイコフェノレート・モフェチル(mycophenolate mofetil))、脈管形成剤、脈管内皮増殖因子(VEGF)、線維芽細胞増殖因子(FGF)、アンギオテンシン・レセプタ遮断薬、一酸化窒素ドナー、アンチセンス・オリゴヌクレオチドおよびこれらの組み合わせ、細胞周期抑制因子、mTOR抑制因子、および増殖因子レセプタ信号導入キナーゼ抑制因子、レテノイド(retenoids)、サイクリン(cyclin)/CDK抑制因子、HMGコエンザイム・レダクターゼ抑制因子(スタチン(statins))、およびプロテアーゼ抑制因子、を含むことができる。
【0024】
本発明に関連する化合物の使用は既存の療法および/または装置に明らかな臨床上の利点を与えることができる。さらに具体的に言えば、塞栓性の破片の溶解または分裂を生じることのできる化合物を本発明の濾過用の部分の中に組み込むことができる。上記のような化合物の選択において考慮すべき要因は、その破片の発端が血栓、プラーク、アテローム、または何らかの他の塞栓を表わす形態のいずれであるかである。本発明の濾過の態様のメッシュまたは気孔の大きさが減少するほど、多くの塞栓性の物質が本発明の濾過機構の中に捕捉できるようになり、これにより、その濾過部分における負荷が増加する。小さな塞栓(一般的に100ミクロンよりも小さい)は、その塞栓を酵素により分解して、消化または溶解する体の自然な能力により、大きな問題にはならないが、フィルター自体における塞栓性の負荷は過剰負荷になって、血流が血栓の形成を可能にする程度まで著しく遅くなると、結果として血栓を形成する可能性がある。このような状況において、捕捉された塞栓を分解できる化合物の組み込みまたは供給は有益になると考えられる。一部の例示的で適当な化合物は、ティシュー・プラスミノゲン・アクチベータ(Tissue Plasminogen activator)(TPA)、ストレプトキナーゼ(Streptokinase)(SK)、レテプラーゼ(Reteplase)、テネクテプラーゼ(Tenecteplase)、ウロキナーゼ(Urokinase)、ラノテプラーゼ(Lanoteplase)、スタフィロキナーゼ(Staphylokinase)、および/またはナドロパリン(Nadroparin)(アンチ−ファクターXa(anti-factor Xa))、を含むことができる。加えて、本発明の濾過部分は塞栓の形成を防ぐための抗血栓性および/または抗トロンボゲン形成性の物質を組み込むことができる。一部の例示的な化合物は、ヘパリン(Heparin)、フラグミン(Fragmin)(ダルテパリン(dalteparin)、低分子量ヘパリン(low MW Heparin))、レオプロ(ReoPro)(商標)(アブシキシマブ(abciximab)、抗血小板抗体)アセノクマロール(Acenocoumarol)等のようなモノクローナル抗体、アニシンジオン(Anisindione)、ジクマロール(Dicumarol)、ワルファリン(Warfarin)、エノキサパリン(Enoxaparin)(ロベノックス(Lovenox))、アナグレリド(Anagrelide)(アグリリン(Agrylin))、インドメタシン(Indomethacin)(インドシン(Indocin))、ジピリダモール(Dipyridamole)、クロピドグレル(Clopidogrel)、アグレノックス(Aggrenox)、および/またはクマジン(Coumadin)、を含むことができる。さらに、親和結合性の化合物もまた、それ自体で、あるいは、他の化合物との組み合わせにおいて、本発明の濾過の態様に組み込むことができる。これらの親和結合性の化合物は塞栓性の物質の結合および/または付着を促進することができ、これにより、塞栓性の物質の捕捉を促進し、これに続いて血流から除去できる。化学的な表面処理、ボンバードメント、貯蔵器の中への配置等のような方法により支柱部または膜の中に組み込みまれるか、あるいは、高分子の支柱部または膜の場合に、その材料自体と共に混合されるか、あるいは、化合物を支柱部および/または膜に塗布する供給により、あらゆる確認された化合物または確認された化合物の組み合わせが使用できる。さらに、多数の化合物が熟練者にとって思いつくことができ、本発明に関連して、単独でまたは他の化合物との組み合わせにおいて利用できる。
【0025】
本発明の以上の例示的な実施形態は、例えば、被膜として、独立して使用可能であり、あるいは、後に本発明による医療装置に製造されることになる高分子材料の中に組み込むことのできる、高強度の放射線不透過性の造影剤を提供している。さらに、上記の薬物および/または薬剤の組み込みは、付加的な相乗効果の有益な作用を実現するために、高強度の造影剤と組み合わせることができる。上述のように、本発明による生物学的なさらに/または薬剤として活性な物質の組み込みは、血栓の形成の阻止、結合の促進、血栓の分解、という付加的な目的のために利用可能であり、これらの全ては患者に有益な作用を与える。
【0026】
本発明の態様ならびに上述の情報は、添付の例示的な図面と共に、以下の詳細な説明を参照することにより、最良に理解できるであろう。
【0027】
〔好ましい実施形態の詳細な説明〕
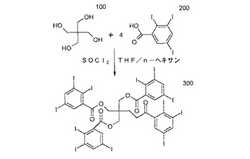
図1において示されているように、SOCl2 (触媒)およびTHF/ヘキサン(反応媒体)の存在下に、ペンタエリスリトール(pentaerythritol)(100)をトリヨード安息香酸(triiodobenzoic acid)(200)と共に反応させると、結果として得られる造影剤(300)は、商品名をウルトラビスト(Ultravist)(登録商標)とする物質等のような市場において入手可能な物質(50)のほぼ2倍の高さである、85%の高いヨウ素の含有量を有することができる。図示の反応において、トリヨード安息香酸(triiodobenzoic acid)(200)はレベル1の樹状突起体と当量であり、SOCl2 は触媒であり、THF/ヘキサンは反応のための反応媒体である(図式1)。従って、比較的に高レベルの樹状突起体を使用できる。図2はレベル4の樹状突起状のポリアミン(400)の化学的な構造を示しており、アミン基(401)の合計数は2n である。図示のそれぞれのアミン基(401)は、高められた造影強度のために、トリヨード安息香酸(triiodobenzoic acid)の部分(200)に対して潜在的に結合できる。例えば、図3において示されているような、3個のヨウ素原子を含んでいるトリヨード安息香酸(triiodobenzoic acid)の基(200)が結合している場合に示されるレベル4の樹状突起状のポリアミン(400)においては、その結果は48個のヨウ素原子を含んでいる構造(500)になり、高強度の造影剤が結果として得られる。これらのヨウ素原子または放射線不透過性の特性を示す他の適当な原子の数は2n ×3までの数として表わすことができ、nは反応において用いられる樹状突起体の前駆体(400)のレベルの数である。同様に、カルボキシル、ヒドロキシル、スルフヒドリルの基等のような、他の官能基を含んでいる樹状突起体も本発明による高強度の造影剤のビルディング・ブロックとして使用できる。ウルトラビスト(Ultravist)(登録商標)の化学的な構造において示されているように、それぞれのこのような分子はコアのベンゼン環に共有結合の状態で連結している3個のヨウ素原子を含んでいる。この場合のヨウ素−炭素の結合は生理学的なおよび照射の条件下において安定であることが立証されている。なお、上記の化合物は腎透析により主に排除される。
【0028】
図4は商品名をウルトラビスト(Ultravist)(登録商標)として知られている、市場において入手可能な造影剤(50)を示している。このイオプロミド(Iopromide)化合物の特徴は、この化合物を水に可溶性にする多数のヒドロキシル基を有していることである。この物質の水に対する溶解度はこの物質を注入可能な造影剤としての使用に適するものにしているが、放射線不透過性の被膜として、あるいは、ポリマー基材中の放射線不透過性の添加物として用いられる場合に、機能しなくなる可能性もある。このような側方の基の増加はその分子の中のヨウ素の重量の割合を比較的に低くしている。これに対して、本発明によれば、それぞれの分子内のヨウ素含有量を最大にするような、多数のトリヨード・ベンゼン環(triiodobenzene ring)の構造の、コアの樹状突起構造に対する連結は、ポリマー基材に対する被膜および添加物の両方としての放射線不透過性の添加物として、ならびに、当業者において知られている別の用法において、適している高強度の造影剤を形成できる。図5において示されているように、上記のような高いヨウ素の含有量の造影剤の最も単純な形態が、Fmoc保護された1−アミノ−2,2−ジヒドロキシメチル−3−プロパノール(1-amino-2,2-dihydroxymethyl-3-propanol)(110)と3個の2,3,5−トリヨード安息香酸(2,3,5-triiodobenzoic acid)の塩化物(210)との間の反応を通して、合成されている。この結果として得られる造影剤(310)は約74%のヨウ素の含有量を有しており、ウルトラビスト(Ultravist)(登録商標)の48%(50)よりもはるかに高い。本発明による造影剤の別の利点は、全ての原材料が容易に入手可能であり、それぞれの結合反応が総じて高い収率であるということである。多層の樹状突起体のコアは費用を増す可能性があるが、さらに高いヨウ素の含有量と、十分な画像のコントラストを達成するために医療装置の中において必要とされる物質の減少された量とより、このことは相殺できる。さらに、高められた分子量は移動性を減少させて、造影剤が医療装置からにじみ出る可能性を低下させる。
【0029】
触媒を伴う、ヒドロキシル基またはアミン基を含んでいる化合物とヨウ素含有の芳香族カルボン酸またはカルボン酸の塩化物の化合物との反応は、ヨウ素含有の造影剤を合成するために使用できる。本発明によれば、この反応は、エチレン・グリコール(ethylene glycol)、プロピレン・グリコール(propylene glycol)、グリセロール(glycerol)、およびペンタエリスリトール(pentaerythritol)、ビス−ペンタエリスリトール(bis-pentaerythritol)等のような、2個、3個または4個のヒドロキシル基を含んでいる化合物をさらに用いることにより、多数のヨウ素原子を伴う単一の反応性の造影剤に拡張されており、このことはその分子の放射線不透過性を結果として最大にできる。
【0030】
社内の研究により、商品名をウルトラビスト(Ultravist)(登録商標)(50)(ウルトラビスト(Ultravist)はシャーリング・エー・ジー(Schering AG)の登録商標である)(それぞれのウルトラビスト(Ultravist)の分子中に3個のヨウ素原子を含んでいるイオプロミド(iopromide))とする物質等のような、市場において入手可能の注入可能な造影剤は硫酸バリウムに匹敵するX線のコントラストを示すことが分かっている。一方、本発明による造影剤は造影剤の単位重量当たりに2倍までの多いヨウ素原子を含んでおり、このことは推定される4倍のさらに鮮明なコントラストの画像品質を得ることが可能である。加えて、この提案されている造影剤は水溶性が低く、医療装置のポリマー基材を膨潤させることがなく、したがって、医療装置の機械特性を比較的に良好に維持する。さらに、膨潤を制限することに加えて、物質のにじみ出しも最小限になる。
【0031】
本発明によれば、多数のヨウ素含有の分子が単一の造影剤の中に組み込まれて、その造影剤の放射線不透過性を結果として最大にしている。さらに、一般的な有機溶媒の中において上記の造影剤は良好な溶解度を示すので、固溶体を形成するための一般的なポリマーまたはポリマー混合物に対して良好な混和性が得られる。この結果、バルク材料の高められた機械特性が、結果として応力の増加因子になる可能性のある結晶性の添加物の排除により、維持されると共に、比較的に低い水に対する溶解度が長い存在時間およびバルク材料の分解の速度を確実にしている。
【0032】
上記の反応における種々のヒドロキシルまたはアミンを含んでいる官能性の分子の使用等のような、本発明に従う付加的な変更も有益になる可能性がある。一般的な例は、エチレン・グリコール(ethylene glycol)、プロピレン・グリコール(propylene glycol)、グリセロール(glycerol)、ペンタエリスリトール(pentaerythritol)を含む。さらに、カルボキシル基等のような、別の官能基を含んでいる化合物も高強度の造影剤の化合物の合成のために使用可能であり、ソルビトール(sorbitol)、トレハロース(trehalose)等のような、天然に誘導されるアミンまたは多価アルコールも上記のような造影剤を構成するために使用でき、加えて、良好な生体適合性を賦与できる。既に示されているように、溶液流延、浸漬塗布、射出成形等のような、種々の処理方法が上記の造影剤およびバルク材料を混合するために使用可能である。
【0033】
本発明によれば、薬物溶出用のステント等のような、植え込まれた医療装置を画像化するために適している新種の高分子の高強度X線造影剤の組成物が配合されている。樹状突起体の合成において一般的に用いられている、保護された多価アルコールまたはアミンを含んでいる有機化合物が、上記のような高いヨウ素の含有量の開始剤を形成するために、2,3,5−トリヨード安息香酸(2,3,5-triiodobenzoic acid)等のような、ヨウ素含有の芳香族化合物をと共に反応させるために使用できる。それぞれのこのような開始剤は3個の倍数のヨウ素原子を含むことができる。脱保護において、図6において示されているように、上記のヨウ素に富んでいる化合物は、生体吸収性のポリマーを形成するために、ラクチド、グリコリド等のような、環状ジラクトンの開環反応のための開始剤として作用できる。さらに、ジラクタム、混合ジラクトン、混合シクロホスホエステル等のような、別の官能性の二量体も上記の反応において使用可能である。随意的に、図7および図8において示されているように、合成の生体吸収性のポリマーは開始剤(330)の誘導体によりエンド・キャップすることができ、1個のポリマー当たりにヨウ素原子を2倍にして、X線画像のコントラストをさらに高めることができる。同様に、二官能性のヨウ素に富んでいる化合物は、ポリウレタンおよびポリウレア等のような、別の種類のポリマーを構築することにおいて使用できる。上記のような化合物の特有の利点は、薬物溶出用のステント等のような、医療装置の基材を作成するために用いる生体吸収性のポリマーと同様に作用するヨウ素含有の生体吸収性のポリマーを含むがこれらに限定されず、これらの化合物は一般的な有機溶媒に可溶性であり、このようなヨウ素含有の生体吸収性のポリマーの分子量およびその他の特性は、分解時間、機械強度、および1個のポリマー当たりのコントラストの強度、を変えるために調節でき、本発明によるこれらのヨウ素含有のポリマーは医療装置を構成するために用いるバルク材料に対して混和性であり、分解時間および機械強度の変化を避けることができ、水溶性ではなく、製造過程の間および初期の植え込み期間ににじみ出さない。
【0034】
図9Aおよび図9Bは高分子基材におけるポリマーのストランドの配向を示している。ポリマー基材(10)の中のポリマー鎖の通常の配向は不規則であるが、その構造(11)の中におけるポリマー鎖の整列状態を形成するために力および/または処理条件を加えることができ、このことは異方性の材料の特性を結果として生じることができ、改善された材料および/または機械特性につながることができる。本発明によれば、上記の高強度のコントラスト特性を有するポリマーは所望の機械特性を達成するために同様に処理できる。
【0035】
同様に、グリコリド(GA)、カプロラクトン(CL)、p−ジオキサノン(DO)、トリメチルカーボネート(TMC)等のような、開環反応のための、図10において示されているような別の一般的に用いられている二量体も全て上記の重合反応において用いることができる。このような二量体は単独で、生体吸収性のポリグリコリド(PGA)の開環反応、およびヨウ素含有の官能性の部分を伴うエンド・キャップ反応を示している図11におけるように、あるいはこれらの組み合わせにおいて、最終のコポリマーの物理的および化学的な特性を調節するために使用することも可能である。
【0036】
付加的な実施形態および/または変更例は、ラクチド、グリコリド、カプロラクトン、またはこれらの混合物等のような、生体吸収性のポリマーの開環反応を開始するために用いる一連の官能性のヨウ素または臭素含有の開始剤を含む。二官能性のヨウ素または臭素に富んでいる化合物は、ポリウレタンおよびポリウレア等のような、非分解性のポリマーのビルディング・ブロックとして作用できる。これらの高分子の構造はポリマー鎖の一端部または両端部において多数のヨウ素原子を含んでいる生体分解性および/または生体安定性のポリマーを有することにより、さらに改質できる。このことは、ポリマー鎖の中においてヨウ素原子を2倍にするために、反応の終了時にヨウ素または臭素を含んでいる生体分解性および/または生体安定性のポリマーをエンド・キャップするための本発明による方法を利用することにより、達成される。さらに、この本発明による方法は、必要な放射線不透過性を賦与する上記のようなヨウ素または臭素を含んでいる生体吸収性のポリマーを用いて、医療装置のX線により見えるバルク材料を形成するために使用できる。あるいは、本発明による方法は、上記のようなヨウ素または臭素を含んでいる生体吸収性のポリマーを添加することにおいて、医療装置のバルク材料におけるX線のコントラスト強度を高めるために使用できる。さらに、本発明による方法は、上記のようなヨウ素または臭素を含んでいる非分解性または生体安定性のポリマーを用いることにおいても、医療装置におけるX線により見えるバルク材料を形成するために利用できるので、生体吸収性のポリマーに限定されない。また、この本発明による方法は、医療装置のバルク材料に上記のようなヨウ素または臭素を含んでいる非分解性または生体安定性のポリマーを添加することにより、その医療装置のバルク材料におけるX線のコントラスト強度を高めることも可能である。
【0037】
ヨウ素含有量の簡単な計算により、ヨウ素に富んでいる化合物の一例が72.7%のヨウ素含有量を有していることを示すことができた。200の重合度(DP)を有する最終のポリマー(分子量は計算値で30KDである)の中に組み込むと、その最終のポリマーの中のヨウ素の含有量はおよそ3.81%になり、この値は通常のX線の動作条件下における可視性のために十分である。さらに、本発明による最終のエンド・キャップ工程を用いると、最終のポリマーにおけるヨウ素の含有量は7.25%まで2倍にすることができ、許容可能であるX線の不透過性のために必要とされる3.0%〜5.0%よりもはるかに高い値を達成できる。あるいは、上記のポリマーは本発明のエンド・キャップ処理により十分なX線の不透過性を保つと考えられるので、そのポリマーの分子量も、放射線不透過性に不利な影響を及ぼさずに、およそ60キロ・ダルトン(KD)まで、2倍にすることができる。
【0038】
米国特許第6,475,477号(この特許文献は、参照により、このように、本明細書に組み入れられている)において開示されているような、それぞれの反復しているモノマーの中にヨウ素または臭素の原子を導入するための方法は、その高分子材料の全体に亘り分布されるヨウ素または臭素の導入の結果として、そのバルク・ポリマーの特性を変える可能性がある。また、上記の一連の特許はヨウ素または臭素を含んでいるポリカーボネートに限定されている。これに比べて、本発明による方法はポリマー鎖の一端部または両端部にヨウ素原子を集中させるか、これらの原子を選択的に配置しており、そのポリマー鎖のバルクの部分は、その医療装置としての役割のために、手をつけないままにしているので、その装置の性能に影響する可能性のあるバルク材料の特性に変化を生じない。
【0039】
上記の開示されている発明は分解性で生体吸収性のポリマーの合成と共に、非分解性で生体安定性のポリマーにも適用できる。これらのX線不透過性のポリマーは、最終の製品または装置を形成するバルク材料を備えている医療装置としての異なる形態および形状に、さらに処理することができる。これらのポリマーはまた、装置と薬物の組み合わせの製品のための高分子被膜または薬物放出用のバリアとして、あるいは、その材料が上部に塗布されているか内部に組み込まれている装置の放射線不透過性を単に高めるために、用いることも可能である。
【0040】
ヒドロキシル基を含んでいる化合物とヨウ素含有の芳香族化合物との間の反応はヨウ素含有の造影剤を合成するために処理することができる。本発明はこの概念をさらに拡張しており、官能性の開始剤を作成するために、保護されている2個、3個または4個のヒドロキシル基を含んでいる化合物を用いている。図6において示されているような、Fmoc(9−フルオレニルメトキシカルボニル(9-fluorenylmethoxycarbonyl))の脱保護において、ヨウ素含有のポリマーを形成するために、ラクチドまたはグリコリド等のような、環状ラクトンの開環反応を開始する、開始剤が使用できる。さらに、Fmoc以外にも、Boc−、Z−、Ddz−、ターシャリー−ブチル、Cbz等のような、アミンおよびヒドロキシルの基に対応する、別の一般的に用いられている保護基を、上記の反応における適当な保護基としてFmocの代わりに特別に用いることができる。上記の開環反応は十分に研究されており、吸収性の縫合糸等のような、別の生体適合性の材料の製造において用いられている。図8において示されているような最終のエンド・キャップ工程は、上記の生体吸収性のポリマーにおけるさらに高いヨウ素含有量を与えるための、メタノールの通常のエンド・キャップ処理の変形である。
【0041】
本発明によれば、多数のヨウ素分子が開環反応の単一の開始剤の中に組み込まれている。生体吸収性のポリマーはバルク材料の機械特性を犠牲にすることなく、多数のヨウ素原子を含んでおり、例えば、このような生体吸収性のポリマーは、ヨウ素含有の官能性の開始剤の誘導体によるエンド・キャップ処理により、2倍の数のヨウ素原子を含有できる。このようなヨウ素含有の生体吸収性のポリマーは、はるかに高められたX線のコントラストを伴う医療装置を形成するために通常のバルク材料と共に混合することができ、処理の間および植え込みの初期においてにじみ出さず、所望の分解および生体適合性を確実にする。さらに、医療装置のコントラスト強度はその基材中のヨウ素含有のポリマーの分子量および割合を変更することにより調節できる。このヨウ素の導入方法は、本発明に従って、放射線不透過性で非分解性のポリマーの合成においても、使用可能である。
【0042】
変更例は種々のヒドロキシルまたはアミンを含んでいる官能性の分子の使用を含み、これらの分子は適当に保護されていると、上記の官能性の開始剤の合成において使用できる。その後、脱保護により、上記の官能性の開始剤は対応するエンド・キャップ用のヨウ素含有の官能性の化合物に変換できる。ラクチド、グリコリド、カプロラクトン、ジオキサノン、トリメチレン・カーボネート等、またはこれらのモノマーの組み合わせのような、生体吸収性のポリマーのための、任意の一般的なモノマーが上記のヨウ素含有の分解性のポリマーを構成するために使用できる。さらに、ポリウレタンまたはポリウレア等のような、非分解性のポリマーも、上記と同一または類似の化学作用を用いて、さらに高い放射線不透過性にすることができる。
【0043】
以上において図示および説明されているものは本発明の最も実用的で好ましい実施形態であると考えられるものであるが、これらの説明および図示されている特定の設計の別の形態またはこれらからの変形は当業者において想到し得るものとなり、本発明の趣旨、範囲または本質的な特徴から逸脱することなく使用可能になるであろう。本発明は上記の説明されている実施形態に制限または限定されず、むしろ、添付の特許請求の範囲における各請求項に該当し得る全ての変形、組み合わせ、および変更に一貫していると解釈されるべきである。
【0044】
〔実施の態様〕
(1)以下の化学式を有する化合物において、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
(2)以下の化学式を有する化合物において、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
(3)以下の化学式を有する化合物において、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、
前記R′はポリマーである、
化合物。
(4)放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
(5)放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖の基端部または先端部のいずれかに共有結合している、
放射線不透過性の材料。
【0045】
(6)放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、
前記R′はポリマーである、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
(7)実施態様1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、化合物。
(8)実施態様1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる星形の有機性の部分である、化合物。
(9)実施態様4,5または6のいずれかに記載の材料から作られている、医療装置。
(10)実施態様1,2または3のいずれかに記載の化合物により、放射線不透過性が高められている、医療装置。
【0046】
(11)実施態様7に記載の化合物により、放射線不透過性が高められている、医療装置。
(12)実施態様8に記載の化合物により、放射線不透過性が高められている、医療装置。
(13)実施態様4,5または6のいずれかに記載の材料により作られている被膜により、放射線不透過性が高められている、医療装置。
(14)実施態様3に記載の化合物において、
前記ポリマーは生体安定性のポリマーである、化合物。
(15)実施態様3に記載の化合物において、
前記ポリマーは生体分解性のポリマーである、化合物。
【0047】
(16)実施態様6に記載の放射線不透過性の材料において、
前記ポリマーは生体安定性のポリマーである、放射線不透過性の材料。
(17)実施態様6に記載の放射線不透過性の材料において、
前記ポリマーは生体分解性のポリマーである、放射線不透過性の材料。
(18)実施態様9に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(19)実施態様10に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(20)実施態様11に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【0048】
(21)実施態様12に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(22)実施態様13に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(23)実施態様16に記載の放射線不透過性の材料において、
前記生体安定性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
(24)実施態様17に記載の放射線不透過性の材料において、
前記生体分解性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
(25)実施態様18に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【0049】
(26)実施態様19に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
(27)実施態様20に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
(28)実施態様21に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
(29)実施態様22に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【図面の簡単な説明】
【0050】
【図1】化学反応の生成物を示しており、SOCl2 は触媒または活性化用の物質であり、THF/ヘキサンは反応のための反応媒体または溶媒である。
【図2】レベル4の樹状突起状のポリアミンの化学的な構造ならびにその構造に重ねられているレベル1〜3も示している。
【図3】レベル4の樹状突起状のポリアミンの化学的な構造から誘導された高強度造影剤を示している。
【図4】商品名をウルトラビスト(Ultravist)(登録商標)として、当業界において知られている市場において入手可能な水溶性の造影剤の化学的な構造を示している。
【図5】化学的な反応を示しており、高いヨウ素の含有量の造影剤が、ペンタエリスリトール(pentaerythritol)と3個の2,3,5−トリヨード安息香酸(2,3,5-triiodobenzoic acid)の分子との間の反応を通して、合成されている。
【図6】保護されている開始剤の脱保護を表わしている反応を示している。
【図7】ヨウ素含有のエンド・キャップ基の合成反応を示している。
【図8】生体吸収性のポリマーの開環反応およびヨウ素含有の官能基によるエンド・キャップを結果として生じている反応を示している。
【図9A】配列において、図式的に不規則な配向のポリマーのストランド/鎖を示している。
【図9B】オリエントルージョンの処理を受けているポリマーの中のポリマーのストランド/鎖の整列された配向を示している。
【図10】生体吸収性のポリマーおよび/またはコポリマーを作成するために用いられる例示的な二量体の化学的な構造を示している。
【図11】生体吸収性のポリグリコリド(polyglycolide)(PGA)の開環、およびヨウ素含有の官能性の部分によるエンド・キャップ反応を、結果として生じている反応を示している。
【開示の内容】
【0001】
〔関連の出願に対するクロス・リファレンス〕
本特許出願は米国特許法第119(e)条に基いて、2005年、3月18日に出願されている米国仮特許出願第60/662,957号の優先権を主張している。
【0002】
〔発明の分野〕
本発明は医療の治療および処置において用いる脈管内装置に関連している。さらに具体的に言えば、本発明は、医療装置、特に、ポリマーの一端部または両端部において結合されている、内部に造影剤が分散されているポリマーにより作られている高分子の医療装置および高分子の被膜、の画像化を向上させるために適している新しい種類の有機性の高強度X線造影剤、ならびに、これらの材料および装置の製造の方法に関連している。
【0003】
〔関連技術の論述〕
最近において、経管プロテーゼが血管、胆管、またはその他の生体の類似の器官の中における移植のための医療技術において広く用いられている。これらのプロテーゼはステントとして一般的に知られており、管状の構造を維持して、開口させるか、拡張するために用いられている。一般的に用いられているステントの例が、参照により、本明細書に組み入れられている、1985年11月7日にパルマズ(Palmaz)により出願されている、米国特許第4,733,665号において記載されている。これらのステントはバルーン式の拡張可能なステントとして呼ばれる場合が多い。一般的に、ステントはステンレス鋼の固体の管により作成されているが、別の金属材料も利用されている。その後、そのステントの壁部に一連の切り込みが作成される。このステントは第1の比較的に小さい直径を有しており、この第1の直径は、ステントが、バルーン・カテーテルの上に圧着されることにより、人間の脈管の中を通して送達されることを可能にする。このステントはまた、その管状に造形された部材の内部から、バルーン・カテーテルにより、半径方向に、外側に向けられた力の供給時に、第2の拡張された直径も有する。
【0004】
しかしながら、上記のステントに伴う一つの問題はこれらが頸動脈等のような一部の脈管の中の使用において実用的でない場合が多いことである。この頸動脈は人間の体の外部から容易に接近可能であり、皮膚の表面に近い。ステンレス鋼等により作成されているバルーン拡張式のステントを頚動脈に有している患者は日々の活動を通して深刻な傷害を受ける可能性が高い。例えば、患者の首に十分な力が加わることにより、そのステントが崩壊して、その患者に対する傷害を生じる可能性がある。このことを防ぐために、自己拡張式のステントが上記のような脈管の中における使用のために提案されている。これらの自己拡張式のステントはばねのように作用して、つぶされた後に、拡張および埋め込まれた形態に戻る。
【0005】
自己拡張式ステントの一つの種類が米国特許第4,655,771号において開示されており、このステントは半径方向および軸方向に柔軟で弾性的な管状の本体部分を有しており、この本体部分は当該本体部分の両端部の互いに対する軸方向の移動において可変である所定の直径を伴っていて、半径方向に自己拡張性のらせんを定めている複数の個々に剛性であるが柔軟で弾性的な糸状の要素により構成されている。この種のステントは「編組型ステント」として当業界において知られており、本明細書においてこのように示されている。体内の脈管の中におけるこのようなステントの配置は、先端部においてそのステントを保持するための外側のカテーテルと、ステントが配置された後にそのステントを前方に押し出す内側のピストンとを備えている装置により、達成できる。
【0006】
しかしながら、編組型ステントは多くの不都合を有している。これらは一般的に病気の脈管を開口した状態に有効に維持するために必要な半径方向の強度を有していない。加えて、これらのステントを作成するために用いられている複数のワイヤまたはファイバーは、ステントの本体部分から分離されると、危険になる可能性があり、このような場合に、これらは脈管を突き刺すことも有り得る。それゆえ、市場において入手可能な多くのバルーン拡張式ステントのための一般的な製造方法である、金属の管から切り出された自己拡張式ステントを有することに対する要望が存在している。管から切り出された自己拡張式ステントを製造するために、用いられる合金は、好ましくは、体温において、超弾性または擬弾性の特性を示し、これにより、回復可能につぶれる。
【0007】
先行技術はニチノール(Nitinol)(ニッケル−チタン合金)等のような合金の使用を参考にしており、この合金は、患者の体内に挿入されるように設計されている医療装置の中において、形状記憶および/または超弾性の特性を有する。この形状記憶特性は、上記の装置が体内の内腔またはキャビティの中へのこれらの挿入を容易にするために変形された後に、その装置がその元の形状に戻るように、その体内において加熱されること、を可能にする。一方、超弾性特性は一般に、患者の体内への上記の金属を含有している医療装置の挿入を容易にするように変形されている状態に、その金属が変形して拘束されることを可能にし、このような変形は相転移を生じる。いったん、体内腔の中に入ると、上記の超弾性の部材における拘束は解除でき、これにより、応力が減少して、その超弾性の部材はその元の相に戻る転移により、その元の変形されていない形状に戻ることができる。
【0008】
上記の形状記憶/超弾性の特性を有する合金は一般に少なくとも2種類の相を有している。これらの相は、比較的に小さい引張強さを有していて比較的に低い温度において安定であるマルテンサイト相(martensite phase)と、比較的に大きい引張強さを有していてマルテンサイト相よりも高い温度において安定であるオーステナイト相(austenite phase)である。
【0009】
形状記憶特性は、マルテンサイト相からオーステナイト相への転移が完全になる温度よりも高い温度、すなわち、オーステナイト相が安定である温度よりも高い温度(Af 温度)において、上記の金属を加熱することにより、その合金に賦与される。この熱処理の間における上記の金属の形状が「記憶された」形状である。その後、この熱処理された金属はマルテンサイト相が安定である温度まで冷却され、オーステナイト相をマルテンサイト相に転移させる。次に、このマルテンサイト相の金属は、例えば、患者の体内へのその導入を容易にするために、可塑的に変形される。その後、この変形されたマルテンサイト相をそのマルテンサイト相からオーステナイト相への転移温度よりも高い温度まで加熱することにより、その変形されたマルテンサイト相がオーステナイト相に転移し、この相転移の間に、その金属は、拘束されていなければ、その元の形状に戻る。しかし、拘束されていれば、その金属は、その拘束が解除されるまで、マルテンサイト相を維持する。
【0010】
患者の体内に置くことを目的としている医療装置において上記の合金の形状記憶特性を用いる方法は動作上の困難さをもたらしている。例えば、体温よりも低い安定なマルテンサイト温度を有する形状記憶合金を用いれば、上記の医療装置が患者の体内に挿入されている時に、マルテンサイト相からオーステナイト相への転移を阻止するために、そのような合金を含有しているその医療装置の温度を体温よりも十分に低く維持することが困難になる場合が多い。一方、体温よりも十分に高いマルテンサイト相からオーステナイト相への転移温度を有する形状記憶合金により形成されている脈管内装置を用いると、これらの装置は、ほとんどまたは全く問題を伴わずに、患者の体内に導入できるが、これらはマルテンサイト相からオーステナイト相への転移温度まで加熱する必要があり、この温度は組織の損傷を引き起こすのに十分に高い場合が多い。
【0011】
オーステナイト相が安定である温度(すなわち、マルテンサイト相からオーステナイト相への転移が完全になる温度)よりも高い温度において超弾性特性を示すニチノール等のような金属の試料に応力が加えられると、その試料は、その合金がさらにオーステナイト相からマルテンサイト相への応力誘発型の相転移を生じる段階における特定の応力レベルに到達するまで、弾性的に変形する。さらに、上記の相転移が進行すると、上記の合金はひずみにおけるかなりの増加を生じるが、応力においてはほとんどまたは全く付随する増加を生じない。その後、このひずみは増加するが、応力は、オーステナイト相からマルテンサイト相への転移が完全になるまで、実質的に一定に保たれる。その後は、応力におけるさらなる増加がさらなる変形を引き起こすために必要になる。この場合に、マルテンサイト相の金属は、追加の応力の供給時に、最初に弾性的に変形し、その後、永久的な残留変形により可塑的に変形する。
【0012】
何らかの永久的な変形が生じる前に上記の試料における負荷が除去されると、そのマルテンサイト相の試料はオーステナイト相に弾性的に戻って転移する。この応力の減少は最初にひずみの減少を引き起こす。その後、この応力の減少が、マルテンサイト相がオーステナイト相に転移して戻るレベルに到達すると、その試料における応力のレベルは、そのオーステナイト相に戻る転移が完全になるまで、すなわち、付随する応力が無視できる程度にしか減少せずに、ひずみにおけるかなりの回復が生じるまで、(オーステナイト相がマルテンサイト相に転移する一定の応力のレベルよりは実質的に低いが)実質的に一定に維持される。このオーステナイト相に戻る転移が完全になると、さらなる応力の減少が弾性ひずみの減少を生じる。このような負荷の供給時に、比較的に一定の応力において、かなりのひずみを生じて、その負荷の除去時に変形から回復するための能力は、超弾性または擬弾性と一般的に呼ばれている。上記の管切断型の自己拡張式ステントの製造において材料を有用にしているのは、このような材料の特性である。
【0013】
先行技術は、患者の体内に挿入するかその他の様式で使用することを目的としている医療装置における、超弾性の特性を有する金属の合金の使用を参考にしている。例えば、米国特許第4,665,905号(ジャービス(Jervis))および米国特許第4,925,445号(サカモト(Sakamoto)他)を参照されたい。しかしながら、このような先行技術は依然として適当な管切断型の自己拡張式ステントを全く開示していない。加えて、先行技術のステントの多くは身体の脈管を開口状態に維持するために必要な剛性またはフープの強度を欠いていた。さらに、先行技術のステントの多くはそれぞれの拡張された直径において大きな開口部を有する。この拡張されたステントにおける開口部が小さいほど、そのステントと脈管の壁部との間にその開口部が捕捉できるプラークまたはその他の堆積物の量が多くなる。これらの堆積物の捕捉は、この捕捉が、脈管内へのプラークの脱出、ステントが植え込まれている脈管の再狭窄、および血流内への塞栓形成性の粒子の放出により生じる発作、を阻止することに役立つ点において、患者の健康状態の継続にとって重要である。
【0014】
これらのステント、およびその他の医療装置に伴う一つの付加的な問題は、これらがX線透視下において低下された放射線不透過性を示す可能性があることである。この問題を解消するために、高度に放射線不透過性の材料により作成した標識をステントに取り付けること、またはめっきまたは塗布の方法で放射線不透過性の材料を使用することが一般的な実施方法である。このような材料は一般的に金、プラチナ、またはタンタルである。さらに、先行技術は米国特許第5,632,771号(ボートマン(Boatman)他)、米国特許第6,022,374号(イムラン(Imran))、米国特許第5,741,327号(フランツェン(Frantzen)、米国特許第5,725,572号(ラム(Lam)他)、および米国特許第5,800,526号(アンダーソン(Anderson)他)における上記のような標識または方法を参考にしている。しかしながら、ガルバニ列におけるステントの基材の位置に対するガルバニ列における上記の材料の相対的な位置により、解消すべき特定の課題、すなわち、電解腐食、が存在している。
【0015】
加えて、金属材料の使用を避けている、生体分解性のステント、および高分子材料により作られているステントはさらにX線透視下において可視化されることが可能である必要がある。これらの種類の装置においては、放射線不透過性の標識または被膜の使用を伴わずにこれらの装置における放射線不透過性を賦与/増加する方法において、重大な課題が存在している。先行技術は米国特許第4,935,019号(パップ(Papp))における一例のこのような方法を参考にしており、この場合に、外科用の布地の上に印刷するために適している放射線不透過性で高分子の組成物がX線検出可能な標識を構成しており、この標識は液体のポリマーのキャリアの中に、硫酸バリウム等のような、重金属の塩を分散させることにより得られる。このパップ(Papp)において、上記の硫酸バリウムは約5ミクロンよりも大きい平均の粒度を有しており、上記の組成物の全体の固形物の約15〜90重量%の量で存在している。さらに、パップ(Papp)は上記の組成物の約60〜90重量%を占める硫酸バリウムが好ましいことを示している。しかしながら、このように大きな割合の量での硫酸バリウムの添加は基材の構造の完全性に悪影響を及ぼす可能性があり、強度を低下させ、その他の機械的な特性および特徴に有害に影響する。また、生体分解性のポリマーにおいて、放射線不透過性の添加物の影響力は、生体吸収性のポリマーの分解速度、弾性等のような特性にも有害な影響を及ぼす可能性があると共に、材料の中における何らかの局在化された濃度の硫酸バリウム粒子の中またはそれらの周囲における応力の増加因子の存在を潜在的に加える。さらに、硫酸バリウムおよび酸化ジルコニウム等のような、無機の造影剤は有機溶媒中に容易に溶解せず、あるいは、容易に分散せず、これらは非分解性で生体分解性のポリマーを溶解するために一般的に用いられている。
【0016】
従って、結果として得られる組成物の材料が適当に放射線不透過性になるように、ポリマーの中に容易に溶解して、その材料自体に、または放射線不透過性にすることを望む材料の機械的な特性に、有害な影響を及ぼさずに、生体安定性の高分子および生体分解性の高分子の材料に、容易に添加できる放射線不透過性の材料または物質に対する要望が存在している。
【0017】
〔発明の概要〕
本発明による高強度X線造影剤は現在において利用可能であるものの不都合点および欠点を解消して、一次的および二次的な両方の作用により、X線造影剤の強度を最大にすることにより、画像化用の医療装置、特に、非金属の医療装置、における満たされていない要望を満足させている。主要な作用は放射線不透過性の要素を組み込んで、化学的性質により造影剤の中のその要素の含有量を最大にすることを含み、二次的な作用はポリマーの中の放射線不透過性の要素の位置を最適化することを含む。本質的に、ポリマーの中全体に亘って分散しているヨウ素の含有量を選択的に最大にして組み込むことにより、高分子材料の放射線不透過性を、以前には利用可能でなかったレベルまで調整することが可能になる。さらに、このような造影剤の形成および最適化は高分子材料に対して組み込まれる時に改善された処理特性を与え、したがって、製造費用をさらに減少させると共に、十分な分解特性と共に改善された高強度の放射線不透過性を伴う高分子材料を提供することを可能にする。
【0018】
本発明は植え込み可能な高分子の医療装置と共に使用するために、または植え込み可能な医療装置の高分子の被膜のために適している高強度の樹状突起状のまたは星形の造影剤に関連している。ペンタエリスリトール(pentaerythritol)、ビス−ペンタエリスリトール・グリセロール(bis-pentaerythritol glycerol)、多価のモノ−およびジ−サッカリド等の、多価のヒドロキシルまたはアミンを含んでいる有機化合物は、ヨウ素含有の2,3,5−トリヨード安息香酸(2,3,4-triiodobenzoic acid)等のような芳香族化合物と共に反応させて、上記のような高濃度のヨウ素含有の化合物を形成するために使用できる。それぞれのこのような化合物は3個の倍数のヨウ素原子を含むことができ、このような化合物を含んでいる材料により作られた医療装置のX線画像を強く増感させる。このような高強度の樹状突起状の造影剤におけるヨウ素の含有量は、市場において入手可能な樹状突起状のポリアミン前駆体を用いて、85%程度の高さにすることができる。
【0019】
本発明の例示的な実施形態において、上記の造影剤は、上記の装置を作るかその装置に被膜として供給される材料の全体に亘ってその造影剤を分散させることにより作られるX線画像を向上させるために、単一の分子の中に多数のヨウ素原子または臭素原子またはこれらの両方の組み合わせを含むことができる。本発明によれば、上記の造影剤は、アミン、ヒドロキシル、スルフヒドリル、イソシアネート等のような、遊離の官能基を含んでいる樹状突起体の任意のコアにより構成することができ、トリヨード安息香酸(triiodobenzoic acid)またはトリヨード安息香酸の塩化物(triiodobenzoic acid chloride)等のような、少量のヨウ素または臭素を含んでいるビルディング・ブロックにおけるそれぞれの付加的な結合を伴って、3個の倍数のヨウ素または臭素またはこれらの両方の原子の組み合わせを含んでいる分子を結果として形成できる。このような様式で構成される場合に、上記の造影剤は、アセトン、ジメチルアセトアミド(dimethylacetamide)(DMA)、ジメチルスルホキシド(dimethylsulfoxide)(DMSO)、アセトン、THF、1,4−ジオキサン(1,4-dioxane)、DCM等のような、一般的な有機溶媒の中で実質的に溶けることができ、PLGA、PLA等のような、一般的な有機ポリマーに対して実質的に良好な混和性も有している。本発明による造影剤は、ポリマー基材により固溶体を形成して、これにより医療装置の基材を形成できる。本発明による造影剤は実質的に生体適合性であり、材料のX線画像品質を高めるために、ポリマーまたはポリマーの混合物、および/または無機/有機の組成物の材料に添加できる。
【0020】
本発明の別の例示的な実施形態において、上記の造影剤は、医療装置または医療装置の被膜を形成するために、溶液流延、射出成形および/または圧縮成形等のような、種々の手段によりバルク材料と共に混合できる。その後、このバルクの形態は従来の製造方法により最終的な大きさおよび形状に加工できる。あるいは、上記の造影剤を含んでいる高分子の被膜は従来の塗布方法を用いて植え込み可能な医療装置の表面に供給できる。
【0021】
本発明のさらに別の例示的な実施形態において、高分子の構造に対する上記の造影剤の選択的な組み込みは多数の方法で達成できる。このポリマー構造の特定の領域内であって、他の領域内にはない、造影剤の配置を確実にすることにより、放射線不透過性における付加的で二次的な改善が材料および/または機械的な特性に有害な影響を及ぼさずに実現できる。一つのこのような例はポリマー鎖の基端部および先端部における造影剤の組み込みである。例えば、ポリマーの中においてポリマー鎖の高度な分子の配向状態を与えることのできる、オリエントルージョン(orientrusion)等のような方法を利用することにより、そのバルク材料の選択的な部分において高強度の放射線不透過性を伴う高分子材料を形成することができ、これらの部分は、造影剤が存在していない周りの領域よりも、かなり高い放射線不透過性になると考えられる。同様に、被膜材料の中における上記の造影剤の選択的な配置は、バルク材料の中における造影剤の選択的な配置により得られる利点と、同様の二次的な利点を与えることができる。
【0022】
本発明のさらに別の例示的な実施形態において、高分子の構造に対する上記の造影剤の選択的な組み込みは、生体安定性および/または生体分解性のポリマー鎖の先端部および基端部のいずれか、またはこれらの両方の端部における共有結合法により達成できる。このような固有の放射線不透過性を伴うポリマーは、植え込み可能な医療装置を構築するために、あるいは、植え込み可能な医療装置のための被膜として、使用できる。
【0023】
さらに、上記材料を伴うまたはその材料の上における生物学的なさらに/または薬剤用の物質の組み込みまたは供給は、本発明との組み合わせにおいて用いられる場合に、付加的な利点を与えることができ、したがって本発明のさらに別の目的でもある。以下において定められているような化合物は上記の装置の上に被膜として供給するか、上記のポリマーの中に組み込むことが可能であり、治療用および薬剤用の物質を送達するために使用でき、これらの物質は、ビンカ・アルカロイド(vinca alkaloids)(すなわち、ビンブラスチン(vinblastine)、ビンクリスチン(vincristine)、およびビノレルビン(vinorelbine))、パクリタキセル(paclitaxel)、エピジポドフィロトキシン(epidipodophyllotoxins)(すなわち、エトポシド(etoposide)、テニポシド(teniposide))、抗生物質(antibiotics)(ダクチノマイシン(dactinomycin)(アクチノマイシンD(actinomycin D))、ダウノルビシン(daunorubicin)、ドキソルビシン(doxorubicin)およびイダルビシン(idarubicin))、アントラサイクリン(anthracyclines)、ミトキザントロン(mitoxantrone)、ブレオマイシン(bleomycins)、プリカマイシン(plicamycin)(ミトラマイシン(mithramycin))およびマイトマイシン(mitomycin)、酵素(L−アスパラギン(L-asparagine)を全身系的に代謝し、固有のアスパラギンを合成する能力を有していない細胞を奪取する、L−アスパラギナーゼ(L-asparaginase))等のような天然産物を含む抗増殖/抗有糸分裂剤、G(GP)IIb /IIIa 抑制因子およびビトロネクチン・レセプタ(vitronectin receptor)拮抗質等のような抗血小板剤、ナイトロジェン・マスタード(nitrogen mustards)(メクロレタミン(meclorethamine)、シクロホスファミド(cyclophosphamide)および類似体、メルファラン(melphalan)、クロラムブシル(chlorambucil))、エチレンイミン(ethylenimines)およびメチルメラミン(methylmelamines)(ヘキサメチルメラミン(hexamethylmelamine)およびチオテパ(thiotepa))、アルキル・スルホネート−ブスルファン(alkyl sulfonates-busulfan)、ニトロソウレア(nitrosoureas)(カルムスチン(carmustine)(BCNU)および類似体、ストレプトゾシン(streptozocin))、トラゼン−ダカルバジニン(trazenes-dacarbazinine)(DTIC)等のような抗増殖/抗有糸分裂性のアルキル化剤、葉酸類似体(メトトレキセート(methotrexate))、ピリミジン類似体(フルオロウラシル(fluorouracil)、フロクスウリジン(floxuridine)、およびシタラビン(cytarabine))、プリン類似体および関連の抑制因子(メルカプトプリン(mercaptopurine)、チオグアニン(thioguanine)、ペントスタチン(pentostatin)および2−クロロデオキシアデノシン(2-chlorodeoxyadenosine)(クラドリビン(cladribine)))等のような抗増殖/抗有糸分裂性の代謝拮抗物質、プラチナ配位錯体(シスプラチン(cisplatin)、カルボプラチン(carboplatin))、プロカルバジン(procarbazine)、ヒドロキシウレア(hydroxyurea)、ミトーテン(mitotane)、アミノグルテチミド(aminoglutethimide)、ホルモン(すなわち、エストロゲン(estrogen))、抗凝固薬(ヘパリン(heparin)、合成ヘパリン(heparin)の塩およびトロンビン(thrombin)の他の抑制因子)、フィブリン溶解剤(組織プラスミノゲン(plasminogen)活性薬、ストレプトキナーゼ(streptokinase)およびウロキナーゼ(urokinase)等)、アスピリン(aspirin)、ジピリダモール(dipyridamole)、チクロピジン(ticlopidine)、クロピドグレル(clopidogrel)、アブシキシマブ(abciximab)、抗遊走薬(antimigratory)、抗分泌薬(antisecretory)(ブレベルジン(breveldin))、アドレノコルチカル・ステロイド(コルチソル(cortisol)、コルチゾン(cortison)、フルドロコルチゾン(fludrocortisone)、プレドニソン(prednisone)、プレドニソロン(prednisolone)、6α−メチルプレドニソロン(6α-methylprednisolone)、トリアムシノロン(triamcinolone)、ベタメタゾン(betamethasone)、およびデキサメタゾン(dexamethasone))等のような抗炎症薬、非ステロイド薬(サリチル酸(salicylic acid)誘導体、すなわち、アスピリン(aspirin)、パラ−アミノフェノール(para-aminophenol)誘導体、すなわち、アセトアミノフェン(acetaminophen)、インドール(indole)およびインデン(indene)酢酸(インドメタシン(indomethacin)、スリンダク(sulindac)、およびエトダラク(etodalac))、ヘテロアリール酢酸(トルメチン(tolmetin)、ジクロフェナク(diclofenac)、およびケトロラク(ketorolac)、アリールプロピオン酸(arylpropionic acid)(イブプロフェン(ibuprofen)および誘導体)、アントラニル酸(anthranilic acid)(メフェナム酸(mefenamic acid)、およびメクロフェナム酸(meclofenamic acid))、エノール酸(enolic acid)(ピロキシカム(piroxicam)、テノキシカム(tenoxicam)、フェニルブタゾン(phenylbutazone)、およびオキシフェンタトラゾン(oxyphenthatrazone))、ナブメトン(nabmetone)、金化合物(オーラノフィン(auranofin)、オーロチオグルコース(aurothioglucose)、金−ナトリウム・チオマレート(gold sodium thiomalate))、免疫抑制薬(シクロスポリン(cyclosporine)、タクロリムス(tacrolimus)(FK−506)、シロリムス(sirolimus)(ラパマイシン(rapamycin))、アザチオプリン(azathioprine)、マイコフェノレート・モフェチル(mycophenolate mofetil))、脈管形成剤、脈管内皮増殖因子(VEGF)、線維芽細胞増殖因子(FGF)、アンギオテンシン・レセプタ遮断薬、一酸化窒素ドナー、アンチセンス・オリゴヌクレオチドおよびこれらの組み合わせ、細胞周期抑制因子、mTOR抑制因子、および増殖因子レセプタ信号導入キナーゼ抑制因子、レテノイド(retenoids)、サイクリン(cyclin)/CDK抑制因子、HMGコエンザイム・レダクターゼ抑制因子(スタチン(statins))、およびプロテアーゼ抑制因子、を含むことができる。
【0024】
本発明に関連する化合物の使用は既存の療法および/または装置に明らかな臨床上の利点を与えることができる。さらに具体的に言えば、塞栓性の破片の溶解または分裂を生じることのできる化合物を本発明の濾過用の部分の中に組み込むことができる。上記のような化合物の選択において考慮すべき要因は、その破片の発端が血栓、プラーク、アテローム、または何らかの他の塞栓を表わす形態のいずれであるかである。本発明の濾過の態様のメッシュまたは気孔の大きさが減少するほど、多くの塞栓性の物質が本発明の濾過機構の中に捕捉できるようになり、これにより、その濾過部分における負荷が増加する。小さな塞栓(一般的に100ミクロンよりも小さい)は、その塞栓を酵素により分解して、消化または溶解する体の自然な能力により、大きな問題にはならないが、フィルター自体における塞栓性の負荷は過剰負荷になって、血流が血栓の形成を可能にする程度まで著しく遅くなると、結果として血栓を形成する可能性がある。このような状況において、捕捉された塞栓を分解できる化合物の組み込みまたは供給は有益になると考えられる。一部の例示的で適当な化合物は、ティシュー・プラスミノゲン・アクチベータ(Tissue Plasminogen activator)(TPA)、ストレプトキナーゼ(Streptokinase)(SK)、レテプラーゼ(Reteplase)、テネクテプラーゼ(Tenecteplase)、ウロキナーゼ(Urokinase)、ラノテプラーゼ(Lanoteplase)、スタフィロキナーゼ(Staphylokinase)、および/またはナドロパリン(Nadroparin)(アンチ−ファクターXa(anti-factor Xa))、を含むことができる。加えて、本発明の濾過部分は塞栓の形成を防ぐための抗血栓性および/または抗トロンボゲン形成性の物質を組み込むことができる。一部の例示的な化合物は、ヘパリン(Heparin)、フラグミン(Fragmin)(ダルテパリン(dalteparin)、低分子量ヘパリン(low MW Heparin))、レオプロ(ReoPro)(商標)(アブシキシマブ(abciximab)、抗血小板抗体)アセノクマロール(Acenocoumarol)等のようなモノクローナル抗体、アニシンジオン(Anisindione)、ジクマロール(Dicumarol)、ワルファリン(Warfarin)、エノキサパリン(Enoxaparin)(ロベノックス(Lovenox))、アナグレリド(Anagrelide)(アグリリン(Agrylin))、インドメタシン(Indomethacin)(インドシン(Indocin))、ジピリダモール(Dipyridamole)、クロピドグレル(Clopidogrel)、アグレノックス(Aggrenox)、および/またはクマジン(Coumadin)、を含むことができる。さらに、親和結合性の化合物もまた、それ自体で、あるいは、他の化合物との組み合わせにおいて、本発明の濾過の態様に組み込むことができる。これらの親和結合性の化合物は塞栓性の物質の結合および/または付着を促進することができ、これにより、塞栓性の物質の捕捉を促進し、これに続いて血流から除去できる。化学的な表面処理、ボンバードメント、貯蔵器の中への配置等のような方法により支柱部または膜の中に組み込みまれるか、あるいは、高分子の支柱部または膜の場合に、その材料自体と共に混合されるか、あるいは、化合物を支柱部および/または膜に塗布する供給により、あらゆる確認された化合物または確認された化合物の組み合わせが使用できる。さらに、多数の化合物が熟練者にとって思いつくことができ、本発明に関連して、単独でまたは他の化合物との組み合わせにおいて利用できる。
【0025】
本発明の以上の例示的な実施形態は、例えば、被膜として、独立して使用可能であり、あるいは、後に本発明による医療装置に製造されることになる高分子材料の中に組み込むことのできる、高強度の放射線不透過性の造影剤を提供している。さらに、上記の薬物および/または薬剤の組み込みは、付加的な相乗効果の有益な作用を実現するために、高強度の造影剤と組み合わせることができる。上述のように、本発明による生物学的なさらに/または薬剤として活性な物質の組み込みは、血栓の形成の阻止、結合の促進、血栓の分解、という付加的な目的のために利用可能であり、これらの全ては患者に有益な作用を与える。
【0026】
本発明の態様ならびに上述の情報は、添付の例示的な図面と共に、以下の詳細な説明を参照することにより、最良に理解できるであろう。
【0027】
〔好ましい実施形態の詳細な説明〕
図1において示されているように、SOCl2 (触媒)およびTHF/ヘキサン(反応媒体)の存在下に、ペンタエリスリトール(pentaerythritol)(100)をトリヨード安息香酸(triiodobenzoic acid)(200)と共に反応させると、結果として得られる造影剤(300)は、商品名をウルトラビスト(Ultravist)(登録商標)とする物質等のような市場において入手可能な物質(50)のほぼ2倍の高さである、85%の高いヨウ素の含有量を有することができる。図示の反応において、トリヨード安息香酸(triiodobenzoic acid)(200)はレベル1の樹状突起体と当量であり、SOCl2 は触媒であり、THF/ヘキサンは反応のための反応媒体である(図式1)。従って、比較的に高レベルの樹状突起体を使用できる。図2はレベル4の樹状突起状のポリアミン(400)の化学的な構造を示しており、アミン基(401)の合計数は2n である。図示のそれぞれのアミン基(401)は、高められた造影強度のために、トリヨード安息香酸(triiodobenzoic acid)の部分(200)に対して潜在的に結合できる。例えば、図3において示されているような、3個のヨウ素原子を含んでいるトリヨード安息香酸(triiodobenzoic acid)の基(200)が結合している場合に示されるレベル4の樹状突起状のポリアミン(400)においては、その結果は48個のヨウ素原子を含んでいる構造(500)になり、高強度の造影剤が結果として得られる。これらのヨウ素原子または放射線不透過性の特性を示す他の適当な原子の数は2n ×3までの数として表わすことができ、nは反応において用いられる樹状突起体の前駆体(400)のレベルの数である。同様に、カルボキシル、ヒドロキシル、スルフヒドリルの基等のような、他の官能基を含んでいる樹状突起体も本発明による高強度の造影剤のビルディング・ブロックとして使用できる。ウルトラビスト(Ultravist)(登録商標)の化学的な構造において示されているように、それぞれのこのような分子はコアのベンゼン環に共有結合の状態で連結している3個のヨウ素原子を含んでいる。この場合のヨウ素−炭素の結合は生理学的なおよび照射の条件下において安定であることが立証されている。なお、上記の化合物は腎透析により主に排除される。
【0028】
図4は商品名をウルトラビスト(Ultravist)(登録商標)として知られている、市場において入手可能な造影剤(50)を示している。このイオプロミド(Iopromide)化合物の特徴は、この化合物を水に可溶性にする多数のヒドロキシル基を有していることである。この物質の水に対する溶解度はこの物質を注入可能な造影剤としての使用に適するものにしているが、放射線不透過性の被膜として、あるいは、ポリマー基材中の放射線不透過性の添加物として用いられる場合に、機能しなくなる可能性もある。このような側方の基の増加はその分子の中のヨウ素の重量の割合を比較的に低くしている。これに対して、本発明によれば、それぞれの分子内のヨウ素含有量を最大にするような、多数のトリヨード・ベンゼン環(triiodobenzene ring)の構造の、コアの樹状突起構造に対する連結は、ポリマー基材に対する被膜および添加物の両方としての放射線不透過性の添加物として、ならびに、当業者において知られている別の用法において、適している高強度の造影剤を形成できる。図5において示されているように、上記のような高いヨウ素の含有量の造影剤の最も単純な形態が、Fmoc保護された1−アミノ−2,2−ジヒドロキシメチル−3−プロパノール(1-amino-2,2-dihydroxymethyl-3-propanol)(110)と3個の2,3,5−トリヨード安息香酸(2,3,5-triiodobenzoic acid)の塩化物(210)との間の反応を通して、合成されている。この結果として得られる造影剤(310)は約74%のヨウ素の含有量を有しており、ウルトラビスト(Ultravist)(登録商標)の48%(50)よりもはるかに高い。本発明による造影剤の別の利点は、全ての原材料が容易に入手可能であり、それぞれの結合反応が総じて高い収率であるということである。多層の樹状突起体のコアは費用を増す可能性があるが、さらに高いヨウ素の含有量と、十分な画像のコントラストを達成するために医療装置の中において必要とされる物質の減少された量とより、このことは相殺できる。さらに、高められた分子量は移動性を減少させて、造影剤が医療装置からにじみ出る可能性を低下させる。
【0029】
触媒を伴う、ヒドロキシル基またはアミン基を含んでいる化合物とヨウ素含有の芳香族カルボン酸またはカルボン酸の塩化物の化合物との反応は、ヨウ素含有の造影剤を合成するために使用できる。本発明によれば、この反応は、エチレン・グリコール(ethylene glycol)、プロピレン・グリコール(propylene glycol)、グリセロール(glycerol)、およびペンタエリスリトール(pentaerythritol)、ビス−ペンタエリスリトール(bis-pentaerythritol)等のような、2個、3個または4個のヒドロキシル基を含んでいる化合物をさらに用いることにより、多数のヨウ素原子を伴う単一の反応性の造影剤に拡張されており、このことはその分子の放射線不透過性を結果として最大にできる。
【0030】
社内の研究により、商品名をウルトラビスト(Ultravist)(登録商標)(50)(ウルトラビスト(Ultravist)はシャーリング・エー・ジー(Schering AG)の登録商標である)(それぞれのウルトラビスト(Ultravist)の分子中に3個のヨウ素原子を含んでいるイオプロミド(iopromide))とする物質等のような、市場において入手可能の注入可能な造影剤は硫酸バリウムに匹敵するX線のコントラストを示すことが分かっている。一方、本発明による造影剤は造影剤の単位重量当たりに2倍までの多いヨウ素原子を含んでおり、このことは推定される4倍のさらに鮮明なコントラストの画像品質を得ることが可能である。加えて、この提案されている造影剤は水溶性が低く、医療装置のポリマー基材を膨潤させることがなく、したがって、医療装置の機械特性を比較的に良好に維持する。さらに、膨潤を制限することに加えて、物質のにじみ出しも最小限になる。
【0031】
本発明によれば、多数のヨウ素含有の分子が単一の造影剤の中に組み込まれて、その造影剤の放射線不透過性を結果として最大にしている。さらに、一般的な有機溶媒の中において上記の造影剤は良好な溶解度を示すので、固溶体を形成するための一般的なポリマーまたはポリマー混合物に対して良好な混和性が得られる。この結果、バルク材料の高められた機械特性が、結果として応力の増加因子になる可能性のある結晶性の添加物の排除により、維持されると共に、比較的に低い水に対する溶解度が長い存在時間およびバルク材料の分解の速度を確実にしている。
【0032】
上記の反応における種々のヒドロキシルまたはアミンを含んでいる官能性の分子の使用等のような、本発明に従う付加的な変更も有益になる可能性がある。一般的な例は、エチレン・グリコール(ethylene glycol)、プロピレン・グリコール(propylene glycol)、グリセロール(glycerol)、ペンタエリスリトール(pentaerythritol)を含む。さらに、カルボキシル基等のような、別の官能基を含んでいる化合物も高強度の造影剤の化合物の合成のために使用可能であり、ソルビトール(sorbitol)、トレハロース(trehalose)等のような、天然に誘導されるアミンまたは多価アルコールも上記のような造影剤を構成するために使用でき、加えて、良好な生体適合性を賦与できる。既に示されているように、溶液流延、浸漬塗布、射出成形等のような、種々の処理方法が上記の造影剤およびバルク材料を混合するために使用可能である。
【0033】
本発明によれば、薬物溶出用のステント等のような、植え込まれた医療装置を画像化するために適している新種の高分子の高強度X線造影剤の組成物が配合されている。樹状突起体の合成において一般的に用いられている、保護された多価アルコールまたはアミンを含んでいる有機化合物が、上記のような高いヨウ素の含有量の開始剤を形成するために、2,3,5−トリヨード安息香酸(2,3,5-triiodobenzoic acid)等のような、ヨウ素含有の芳香族化合物をと共に反応させるために使用できる。それぞれのこのような開始剤は3個の倍数のヨウ素原子を含むことができる。脱保護において、図6において示されているように、上記のヨウ素に富んでいる化合物は、生体吸収性のポリマーを形成するために、ラクチド、グリコリド等のような、環状ジラクトンの開環反応のための開始剤として作用できる。さらに、ジラクタム、混合ジラクトン、混合シクロホスホエステル等のような、別の官能性の二量体も上記の反応において使用可能である。随意的に、図7および図8において示されているように、合成の生体吸収性のポリマーは開始剤(330)の誘導体によりエンド・キャップすることができ、1個のポリマー当たりにヨウ素原子を2倍にして、X線画像のコントラストをさらに高めることができる。同様に、二官能性のヨウ素に富んでいる化合物は、ポリウレタンおよびポリウレア等のような、別の種類のポリマーを構築することにおいて使用できる。上記のような化合物の特有の利点は、薬物溶出用のステント等のような、医療装置の基材を作成するために用いる生体吸収性のポリマーと同様に作用するヨウ素含有の生体吸収性のポリマーを含むがこれらに限定されず、これらの化合物は一般的な有機溶媒に可溶性であり、このようなヨウ素含有の生体吸収性のポリマーの分子量およびその他の特性は、分解時間、機械強度、および1個のポリマー当たりのコントラストの強度、を変えるために調節でき、本発明によるこれらのヨウ素含有のポリマーは医療装置を構成するために用いるバルク材料に対して混和性であり、分解時間および機械強度の変化を避けることができ、水溶性ではなく、製造過程の間および初期の植え込み期間ににじみ出さない。
【0034】
図9Aおよび図9Bは高分子基材におけるポリマーのストランドの配向を示している。ポリマー基材(10)の中のポリマー鎖の通常の配向は不規則であるが、その構造(11)の中におけるポリマー鎖の整列状態を形成するために力および/または処理条件を加えることができ、このことは異方性の材料の特性を結果として生じることができ、改善された材料および/または機械特性につながることができる。本発明によれば、上記の高強度のコントラスト特性を有するポリマーは所望の機械特性を達成するために同様に処理できる。
【0035】
同様に、グリコリド(GA)、カプロラクトン(CL)、p−ジオキサノン(DO)、トリメチルカーボネート(TMC)等のような、開環反応のための、図10において示されているような別の一般的に用いられている二量体も全て上記の重合反応において用いることができる。このような二量体は単独で、生体吸収性のポリグリコリド(PGA)の開環反応、およびヨウ素含有の官能性の部分を伴うエンド・キャップ反応を示している図11におけるように、あるいはこれらの組み合わせにおいて、最終のコポリマーの物理的および化学的な特性を調節するために使用することも可能である。
【0036】
付加的な実施形態および/または変更例は、ラクチド、グリコリド、カプロラクトン、またはこれらの混合物等のような、生体吸収性のポリマーの開環反応を開始するために用いる一連の官能性のヨウ素または臭素含有の開始剤を含む。二官能性のヨウ素または臭素に富んでいる化合物は、ポリウレタンおよびポリウレア等のような、非分解性のポリマーのビルディング・ブロックとして作用できる。これらの高分子の構造はポリマー鎖の一端部または両端部において多数のヨウ素原子を含んでいる生体分解性および/または生体安定性のポリマーを有することにより、さらに改質できる。このことは、ポリマー鎖の中においてヨウ素原子を2倍にするために、反応の終了時にヨウ素または臭素を含んでいる生体分解性および/または生体安定性のポリマーをエンド・キャップするための本発明による方法を利用することにより、達成される。さらに、この本発明による方法は、必要な放射線不透過性を賦与する上記のようなヨウ素または臭素を含んでいる生体吸収性のポリマーを用いて、医療装置のX線により見えるバルク材料を形成するために使用できる。あるいは、本発明による方法は、上記のようなヨウ素または臭素を含んでいる生体吸収性のポリマーを添加することにおいて、医療装置のバルク材料におけるX線のコントラスト強度を高めるために使用できる。さらに、本発明による方法は、上記のようなヨウ素または臭素を含んでいる非分解性または生体安定性のポリマーを用いることにおいても、医療装置におけるX線により見えるバルク材料を形成するために利用できるので、生体吸収性のポリマーに限定されない。また、この本発明による方法は、医療装置のバルク材料に上記のようなヨウ素または臭素を含んでいる非分解性または生体安定性のポリマーを添加することにより、その医療装置のバルク材料におけるX線のコントラスト強度を高めることも可能である。
【0037】
ヨウ素含有量の簡単な計算により、ヨウ素に富んでいる化合物の一例が72.7%のヨウ素含有量を有していることを示すことができた。200の重合度(DP)を有する最終のポリマー(分子量は計算値で30KDである)の中に組み込むと、その最終のポリマーの中のヨウ素の含有量はおよそ3.81%になり、この値は通常のX線の動作条件下における可視性のために十分である。さらに、本発明による最終のエンド・キャップ工程を用いると、最終のポリマーにおけるヨウ素の含有量は7.25%まで2倍にすることができ、許容可能であるX線の不透過性のために必要とされる3.0%〜5.0%よりもはるかに高い値を達成できる。あるいは、上記のポリマーは本発明のエンド・キャップ処理により十分なX線の不透過性を保つと考えられるので、そのポリマーの分子量も、放射線不透過性に不利な影響を及ぼさずに、およそ60キロ・ダルトン(KD)まで、2倍にすることができる。
【0038】
米国特許第6,475,477号(この特許文献は、参照により、このように、本明細書に組み入れられている)において開示されているような、それぞれの反復しているモノマーの中にヨウ素または臭素の原子を導入するための方法は、その高分子材料の全体に亘り分布されるヨウ素または臭素の導入の結果として、そのバルク・ポリマーの特性を変える可能性がある。また、上記の一連の特許はヨウ素または臭素を含んでいるポリカーボネートに限定されている。これに比べて、本発明による方法はポリマー鎖の一端部または両端部にヨウ素原子を集中させるか、これらの原子を選択的に配置しており、そのポリマー鎖のバルクの部分は、その医療装置としての役割のために、手をつけないままにしているので、その装置の性能に影響する可能性のあるバルク材料の特性に変化を生じない。
【0039】
上記の開示されている発明は分解性で生体吸収性のポリマーの合成と共に、非分解性で生体安定性のポリマーにも適用できる。これらのX線不透過性のポリマーは、最終の製品または装置を形成するバルク材料を備えている医療装置としての異なる形態および形状に、さらに処理することができる。これらのポリマーはまた、装置と薬物の組み合わせの製品のための高分子被膜または薬物放出用のバリアとして、あるいは、その材料が上部に塗布されているか内部に組み込まれている装置の放射線不透過性を単に高めるために、用いることも可能である。
【0040】
ヒドロキシル基を含んでいる化合物とヨウ素含有の芳香族化合物との間の反応はヨウ素含有の造影剤を合成するために処理することができる。本発明はこの概念をさらに拡張しており、官能性の開始剤を作成するために、保護されている2個、3個または4個のヒドロキシル基を含んでいる化合物を用いている。図6において示されているような、Fmoc(9−フルオレニルメトキシカルボニル(9-fluorenylmethoxycarbonyl))の脱保護において、ヨウ素含有のポリマーを形成するために、ラクチドまたはグリコリド等のような、環状ラクトンの開環反応を開始する、開始剤が使用できる。さらに、Fmoc以外にも、Boc−、Z−、Ddz−、ターシャリー−ブチル、Cbz等のような、アミンおよびヒドロキシルの基に対応する、別の一般的に用いられている保護基を、上記の反応における適当な保護基としてFmocの代わりに特別に用いることができる。上記の開環反応は十分に研究されており、吸収性の縫合糸等のような、別の生体適合性の材料の製造において用いられている。図8において示されているような最終のエンド・キャップ工程は、上記の生体吸収性のポリマーにおけるさらに高いヨウ素含有量を与えるための、メタノールの通常のエンド・キャップ処理の変形である。
【0041】
本発明によれば、多数のヨウ素分子が開環反応の単一の開始剤の中に組み込まれている。生体吸収性のポリマーはバルク材料の機械特性を犠牲にすることなく、多数のヨウ素原子を含んでおり、例えば、このような生体吸収性のポリマーは、ヨウ素含有の官能性の開始剤の誘導体によるエンド・キャップ処理により、2倍の数のヨウ素原子を含有できる。このようなヨウ素含有の生体吸収性のポリマーは、はるかに高められたX線のコントラストを伴う医療装置を形成するために通常のバルク材料と共に混合することができ、処理の間および植え込みの初期においてにじみ出さず、所望の分解および生体適合性を確実にする。さらに、医療装置のコントラスト強度はその基材中のヨウ素含有のポリマーの分子量および割合を変更することにより調節できる。このヨウ素の導入方法は、本発明に従って、放射線不透過性で非分解性のポリマーの合成においても、使用可能である。
【0042】
変更例は種々のヒドロキシルまたはアミンを含んでいる官能性の分子の使用を含み、これらの分子は適当に保護されていると、上記の官能性の開始剤の合成において使用できる。その後、脱保護により、上記の官能性の開始剤は対応するエンド・キャップ用のヨウ素含有の官能性の化合物に変換できる。ラクチド、グリコリド、カプロラクトン、ジオキサノン、トリメチレン・カーボネート等、またはこれらのモノマーの組み合わせのような、生体吸収性のポリマーのための、任意の一般的なモノマーが上記のヨウ素含有の分解性のポリマーを構成するために使用できる。さらに、ポリウレタンまたはポリウレア等のような、非分解性のポリマーも、上記と同一または類似の化学作用を用いて、さらに高い放射線不透過性にすることができる。
【0043】
以上において図示および説明されているものは本発明の最も実用的で好ましい実施形態であると考えられるものであるが、これらの説明および図示されている特定の設計の別の形態またはこれらからの変形は当業者において想到し得るものとなり、本発明の趣旨、範囲または本質的な特徴から逸脱することなく使用可能になるであろう。本発明は上記の説明されている実施形態に制限または限定されず、むしろ、添付の特許請求の範囲における各請求項に該当し得る全ての変形、組み合わせ、および変更に一貫していると解釈されるべきである。
【0044】
〔実施の態様〕
(1)以下の化学式を有する化合物において、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
(2)以下の化学式を有する化合物において、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
(3)以下の化学式を有する化合物において、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、
前記R′はポリマーである、
化合物。
(4)放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
(5)放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖の基端部または先端部のいずれかに共有結合している、
放射線不透過性の材料。
【0045】
(6)放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、
前記R′はポリマーである、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
(7)実施態様1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、化合物。
(8)実施態様1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる星形の有機性の部分である、化合物。
(9)実施態様4,5または6のいずれかに記載の材料から作られている、医療装置。
(10)実施態様1,2または3のいずれかに記載の化合物により、放射線不透過性が高められている、医療装置。
【0046】
(11)実施態様7に記載の化合物により、放射線不透過性が高められている、医療装置。
(12)実施態様8に記載の化合物により、放射線不透過性が高められている、医療装置。
(13)実施態様4,5または6のいずれかに記載の材料により作られている被膜により、放射線不透過性が高められている、医療装置。
(14)実施態様3に記載の化合物において、
前記ポリマーは生体安定性のポリマーである、化合物。
(15)実施態様3に記載の化合物において、
前記ポリマーは生体分解性のポリマーである、化合物。
【0047】
(16)実施態様6に記載の放射線不透過性の材料において、
前記ポリマーは生体安定性のポリマーである、放射線不透過性の材料。
(17)実施態様6に記載の放射線不透過性の材料において、
前記ポリマーは生体分解性のポリマーである、放射線不透過性の材料。
(18)実施態様9に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(19)実施態様10に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(20)実施態様11に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【0048】
(21)実施態様12に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(22)実施態様13に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
(23)実施態様16に記載の放射線不透過性の材料において、
前記生体安定性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
(24)実施態様17に記載の放射線不透過性の材料において、
前記生体分解性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
(25)実施態様18に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【0049】
(26)実施態様19に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
(27)実施態様20に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
(28)実施態様21に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
(29)実施態様22に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【図面の簡単な説明】
【0050】
【図1】化学反応の生成物を示しており、SOCl2 は触媒または活性化用の物質であり、THF/ヘキサンは反応のための反応媒体または溶媒である。
【図2】レベル4の樹状突起状のポリアミンの化学的な構造ならびにその構造に重ねられているレベル1〜3も示している。
【図3】レベル4の樹状突起状のポリアミンの化学的な構造から誘導された高強度造影剤を示している。
【図4】商品名をウルトラビスト(Ultravist)(登録商標)として、当業界において知られている市場において入手可能な水溶性の造影剤の化学的な構造を示している。
【図5】化学的な反応を示しており、高いヨウ素の含有量の造影剤が、ペンタエリスリトール(pentaerythritol)と3個の2,3,5−トリヨード安息香酸(2,3,5-triiodobenzoic acid)の分子との間の反応を通して、合成されている。
【図6】保護されている開始剤の脱保護を表わしている反応を示している。
【図7】ヨウ素含有のエンド・キャップ基の合成反応を示している。
【図8】生体吸収性のポリマーの開環反応およびヨウ素含有の官能基によるエンド・キャップを結果として生じている反応を示している。
【図9A】配列において、図式的に不規則な配向のポリマーのストランド/鎖を示している。
【図9B】オリエントルージョンの処理を受けているポリマーの中のポリマーのストランド/鎖の整列された配向を示している。
【図10】生体吸収性のポリマーおよび/またはコポリマーを作成するために用いられる例示的な二量体の化学的な構造を示している。
【図11】生体吸収性のポリグリコリド(polyglycolide)(PGA)の開環、およびヨウ素含有の官能性の部分によるエンド・キャップ反応を、結果として生じている反応を示している。
【特許請求の範囲】
【請求項1】
以下の化学式を有する化合物において、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
【請求項2】
以下の化学式を有する化合物において、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
【請求項3】
以下の化学式を有する化合物において、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、R′はポリマーである、
化合物。
【請求項4】
放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
【請求項5】
放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖の基端部または先端部のいずれかに共有結合している、
放射線不透過性の材料。
【請求項6】
放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、
前記R′はポリマーである、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
【請求項7】
請求項1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、化合物。
【請求項8】
請求項1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる星形の有機性の部分である、化合物。
【請求項9】
請求項4,5または6のいずれかに記載の材料から作られている、医療装置。
【請求項10】
請求項1,2または3のいずれかに記載の化合物により、放射線不透過性が高められている、医療装置。
【請求項11】
請求項7に記載の化合物により、放射線不透過性が高められている、医療装置。
【請求項12】
請求項8に記載の化合物により、放射線不透過性が高められている、医療装置。
【請求項13】
請求項4,5または6のいずれかに記載の材料により作られている被膜により、放射線不透過性が高められている、医療装置。
【請求項14】
請求項3に記載の化合物において、
前記ポリマーは生体安定性のポリマーである、化合物。
【請求項15】
請求項3に記載の化合物において、
前記ポリマーは生体分解性のポリマーである、化合物。
【請求項16】
請求項6に記載の放射線不透過性の材料において、
前記ポリマーは生体安定性のポリマーである、放射線不透過性の材料。
【請求項17】
請求項6に記載の放射線不透過性の材料において、
前記ポリマーは生体分解性のポリマーである、放射線不透過性の材料。
【請求項18】
請求項9に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項19】
請求項10に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項20】
請求項11に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項21】
請求項12に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項22】
請求項13に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項23】
請求項16に記載の放射線不透過性の材料において、
前記生体安定性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
【請求項24】
請求項17に記載の放射線不透過性の材料において、
前記生体分解性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
【請求項25】
請求項18に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項26】
請求項19に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項27】
請求項20に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項28】
請求項21に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項29】
請求項22に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項1】
以下の化学式を有する化合物において、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
【請求項2】
以下の化学式を有する化合物において、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物。
【請求項3】
以下の化学式を有する化合物において、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、R′はポリマーである、
化合物。
【請求項4】
放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NHFmoc
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
【請求項5】
放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH2
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖の基端部または先端部のいずれかに共有結合している、
放射線不透過性の材料。
【請求項6】
放射線不透過性の材料において、
基端部と先端部とを有する、有機性の高分子鎖と、
以下の化学式を有する化合物であって、
R−NH−R′
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも1個のハロゲン原子を含んでいる樹状突起状の有機性の部分であり、
前記R′はポリマーである、
化合物と、
を含んでおり、
この化合物が前記有機性の高分子鎖と共に混合されている、
放射線不透過性の材料。
【請求項7】
請求項1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる樹状突起状の有機性の部分である、化合物。
【請求項8】
請求項1,2または3のいずれかに記載の化合物において、
前記Rは、ヨウ素、塩素、および臭素、から成る群から選択される少なくとも3個のハロゲン原子を含んでいる星形の有機性の部分である、化合物。
【請求項9】
請求項4,5または6のいずれかに記載の材料から作られている、医療装置。
【請求項10】
請求項1,2または3のいずれかに記載の化合物により、放射線不透過性が高められている、医療装置。
【請求項11】
請求項7に記載の化合物により、放射線不透過性が高められている、医療装置。
【請求項12】
請求項8に記載の化合物により、放射線不透過性が高められている、医療装置。
【請求項13】
請求項4,5または6のいずれかに記載の材料により作られている被膜により、放射線不透過性が高められている、医療装置。
【請求項14】
請求項3に記載の化合物において、
前記ポリマーは生体安定性のポリマーである、化合物。
【請求項15】
請求項3に記載の化合物において、
前記ポリマーは生体分解性のポリマーである、化合物。
【請求項16】
請求項6に記載の放射線不透過性の材料において、
前記ポリマーは生体安定性のポリマーである、放射線不透過性の材料。
【請求項17】
請求項6に記載の放射線不透過性の材料において、
前記ポリマーは生体分解性のポリマーである、放射線不透過性の材料。
【請求項18】
請求項9に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項19】
請求項10に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項20】
請求項11に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項21】
請求項12に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項22】
請求項13に記載の医療装置において、
薬剤用の物質をさらに含んでいる、医療装置。
【請求項23】
請求項16に記載の放射線不透過性の材料において、
前記生体安定性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
【請求項24】
請求項17に記載の放射線不透過性の材料において、
前記生体分解性のポリマーは高分子鎖を有しており、
それらの高分子鎖の分子の配向が実質的に整列されている、
放射線不透過性の材料。
【請求項25】
請求項18に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項26】
請求項19に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項27】
請求項20に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項28】
請求項21に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【請求項29】
請求項22に記載の医療装置において、
この医療装置は内腔型の医療装置である、医療装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9A】


【図9B】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9A】


【図9B】


【図10】


【図11】


【公開番号】特開2006−298904(P2006−298904A)
【公開日】平成18年11月2日(2006.11.2)
【国際特許分類】
【外国語出願】
【出願番号】特願2006−75049(P2006−75049)
【出願日】平成18年3月17日(2006.3.17)
【出願人】(597041828)コーディス・コーポレイション (206)
【氏名又は名称原語表記】Cordis Corporation
【Fターム(参考)】
【公開日】平成18年11月2日(2006.11.2)
【国際特許分類】
【出願番号】特願2006−75049(P2006−75049)
【出願日】平成18年3月17日(2006.3.17)
【出願人】(597041828)コーディス・コーポレイション (206)
【氏名又は名称原語表記】Cordis Corporation
【Fターム(参考)】
[ Back to top ]

