反応容器
【課題】 試薬または試料を収容する複数の収容部を備えた反応容器において、前記収容部のそれぞれに収容した試薬または試料を密閉状態で混合し反応させることが可能で、かつ従来の容器と比較し簡単な構成または小型化可能な容器を提供すること。
【解決手段】 第一の試薬または試料を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な、第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉する蓋部と、を備え、かつ第二の収容部が、第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部と、を設けたである反応容器、および前記容器を用いた試料中の特定成分の測定方法により、前記課題を解決する。
【解決手段】 第一の試薬または試料を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な、第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉する蓋部と、を備え、かつ第二の収容部が、第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部と、を設けたである反応容器、および前記容器を用いた試料中の特定成分の測定方法により、前記課題を解決する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、試薬または試料を収容する複数の収容部を備えた反応容器に関する。特に本発明は、収容部のそれぞれに収容した試薬または試料を密閉状態で混合するのに適した反応容器に関する。
【背景技術】
【0002】
従来、生化学分野において、液体同士または液体と固体とを混合する際は、あらかじめ固体または液体を入れた容器に、ピペットやシリンジなどを用いて液体を添加し、液体同士または液体と固体とを接触させて混合する。しかしながら、ピペットやシリンジなどを用いて容器に液体を添加/混合する際、容器は開放された状態(蓋の開いた状態)である。そのため、混合すべき液体同士または液体と固体とが接触した時点で反応が開始する場合、すぐに容器を密閉したとしても添加してから容器を密閉状態にするときまでの間、反応物が大気中に拡散してしまう恐れがある。特に遺伝子検査試薬の場合、反応開始と同時に核酸が指数関数的に増幅するため、増幅した核酸が大気中に拡散することによるコンタミネーションの恐れがある。
【0003】
特許文献1は、遺伝子検査で用いる各試薬を密閉状態で混合する遺伝子検出用具を開示している。この遺伝子検出用具は、反応室としての容器と開封自在の隔壁部を有した検出室としての容器とを備え、かつ検出室としての容器と反応室としての容器とが嵌合可能となっている。特許文献1の容器を用いて遺伝子検査を行なう際は、
(1)反応室としての容器に遺伝子検査を行なうのに必要な第一の試薬および試料(例えば検体からの核酸抽出物)を、検出室としての容器に遺伝子検査を行なうのに必要な第二の試薬を、それぞれ収容し、
(2)反応室としての容器と検出室としての容器とを嵌合し、
(3)検出室としての容器が密閉された状態で、当該容器の外側から隔壁部を押しつぶして破開することで反応室としての容器と検出室としての容器とを連通し、
(4)両容器に収容した第一の試薬および試料と第二の試薬とを接触/混合し、適切な温度条件下で遺伝子増幅および検出を行なう、
ことで遺伝子検査を行なう。ただし、特許文献1の容器は、連通させる際、隔壁部を押しつぶし破開させる必要があるため、検出室としての容器は適度に変形可能な材質とする必要がある。また、隔壁部を破開させる際、反応室としての容器と検出室としての容器との嵌合部分が外れないようにするため、前記嵌合部分と前記隔壁部との間は十分な間隔をとる必要がある。そのため、容器全体の小型化が困難である。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特許第3642574号公報
【特許文献2】特開2000−014400号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
本発明の目的は、試薬または試料を収容する複数の収容部を備えた反応容器において、前記収容部のそれぞれに収容した試薬または試料を密閉状態で混合し反応させることが可能で、かつ従来の容器と比較し簡単な構成または小型化可能な容器を提供することにある。
【課題を解決するための手段】
【0006】
前記目的を達成するためになされた本発明は、以下の態様を包含する:
第一の態様は、
第一の試薬または試料を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な、第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉する蓋部と、を備えた反応容器であって、
第二の収容部が、第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部と、を設けた収容部である、
前記反応容器である。
【0007】
第二の態様は、第二の収容部に設けた保持部の形状が、略半球状、略半偏心球面状または略錐状の凹部をなす、前記第一の態様に記載の反応容器である。
【0008】
第三の態様は、少なくとも第一の収容部の前記底部が光透過性を有している、前記第一または第二の態様に記載の反応容器である。
【0009】
第四の態様は、
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、および
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、を含む、
前記第一から第三の態様のいずれかに記載の反応容器を用いた、試料に含まれる特定成分の測定方法である。
【0010】
第五の態様は、
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、および
(7)第一の収容部の底部を通じて、反応生成物を光学的手法により検出する操作、
を含む、前記第三の態様に記載の反応容器を用いた、試料に含まれる特定成分の測定方法である。
【0011】
第六の態様は、第一の試薬が凍結乾燥試薬である、前記第四または第五の態様に記載の測定方法である。
【0012】
第七の態様は、
試料中に含まれる特定成分が特定核酸であり、
第一の試薬が試料に含まれる特定核酸を増幅するためのオリゴヌクレオチドプライマー、前記特定核酸を検出するためのオリゴヌクレオチドプローブおよび反応基質を含み、
第二の試薬が特定核酸を増幅するための酵素を含む、
前記第四から第六の態様のいずれかに記載の測定方法である。
【発明の効果】
【0013】
本発明の反応容器は、第一の試薬を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉可能な蓋部とを備え、かつ、第二の収容部が第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部とを設けていることを特徴としている。本発明の反応容器は、接触および混合すべき第一の試薬および第二の試薬を各収容部に収容し、試料を添加後、密閉した状態で接触および混合が可能である。また、本発明の反応容器は、第二の収容部に収容した第二の試薬を、第二の収容部が第一の収容部内に挿入した状態(第二の収容部に設けた嵌合部が第一の収容部の内壁と嵌合した状態)で、第二の収容部に設けた開口部より第一の収容部に移送させることができる。このため、試薬を混合させる際、特許文献1のように隔壁部を破開させる操作が不要となり、反応容器全体を小型化することができる。例えば、遺伝子増幅反応で用いる市販の蓋付マイクロチューブの蓋を本発明の反応容器における蓋部に、マイクロチューブ本体を第一の収容部に、それぞれみなし、マイクロチューブ本体内に挿入可能な第二の収容部を新たに作製することで、混合撹拌して得られた反応液をそのまま市販の遺伝子増幅検出装置にセットすることができる。
【0014】
特に、PCR(Polymerase Chain Reaction)法、RT−PCR(Reverse−Transcription PCR)法、NASBA(Nucleic Acid Sequence Based Amplification)法、TMA(Transcription−Mediated Amplification)法、TRC(Transcription Reverse−transcription Concerted reaction)法(特許文献2)などの核酸増幅法では、試料と各試薬とを混合し一定温度下で反応させると、速やかに特定核酸の増幅が開始される。そのため、各試薬と試料との混合操作や反応操作(核酸増幅操作)を大気中に開放された状態で実施すると、当該増幅した核酸が大気中に拡散することによるコンタミネーションリスクが発生し得る。本発明の反応容器は、各試薬と試料との混合操作および核酸増幅反応を密閉状態で行なうことができる。そのため、前記コンタミネーションリスクを低減させることができる。さらに、本発明の反応容器のうち、少なくとも第一の収容部の底部を光透過性を有する材料で作製すると、核酸増幅の有無を光学的手法を用いて検出することができる。よって、蛍光色素などで標識した、特定核酸を特異的に検出するオリゴヌクレオチドプローブを試薬に添加すると、試薬と試料との混合操作、核酸増幅反応および核酸検出操作をいずれも密閉状態で行なえるため、前記コンタミネーションリスクをさらに低減させることができる。
【図面の簡単な説明】
【0015】
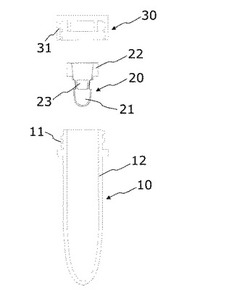
【図1】本発明の反応容器の一例を示した図(分解図)である。
【図2】図1の反応容器に備えた各収容部に各試薬を収容した態様を示した図である。
【図3】回転により、第二の収容部に収容した液体を、開口部から第一の収容部へ移送する態様を示した図である。
【図4】ミキサーを用いて、第二の収容部に収容した液体を、開口部から第一の収容部へ移送する態様を示した図である。
【図5】本発明の反応容器内で反応させた反応液を、光学的手法で測定する態様の一例を示した図である。
【発明を実施するための形態】
【0016】
本発明の反応容器を、図を用いて詳細に説明する。
【0017】
図1および2に示す本発明の反応容器は、
第一の試薬41を収容するための第一の収容部10と、
第一の収容部10内に挿入可能な、第二の試薬42を収容するための第二の収容部20と、
第二の収容部20を挿入した状態で第一の収容部10を密閉可能な蓋部30とを備えており、
第一の収容部10の外壁には蓋部30により密閉可能な手段(図1では螺合手段11)を設けており、
第二の収容部20は、第二の試薬42を収容し保持するための保持部21と、第一の収容部の内壁12と嵌合可能な嵌合部22と、嵌合部22で第一の収容部の内壁12と嵌合した状態で保持部21に保持した第二の試薬42を第一の収容部10に移送可能な開口部23とを設けている。
【0018】
図1および2に示す本発明の反応容器では、第二の収容部20を第一の収容部10内に圧入により挿入することで、嵌合部22を第一の収容部の内壁12と嵌合させている。なお、嵌合部22と第一の収容部の内壁12との嵌合をより確実にするために、第一の収容部の内壁12のうち当該嵌合位置の直下に突起などを設けてもよい。
【0019】
図1および2に示す本発明の反応容器において、第二の試薬42を収容し保持するための保持部21は、第一の収容部10に試料を添加する場合は少なくとも反応に必要な量の第二の試薬42を、第二の収容部20に試料を添加する場合は少なくとも反応に必要な量の第二の試薬42と添加する試料との合計量を、それぞれ収容し保持可能であればよく、その形状に限定はない。ただし、保持部21の内底面の形状を、略半球状、略半偏心球面状または略円錐状や略角錐状といった略錐状の凹部をなす形状とすると、後述の開口部23を用いた第二の試薬42の第一の収容部10への移送をスムーズに行なうことができ、かつ移送後に残留する試薬の量(デッドボリューム)も最小にできるため好ましい。
【0020】
図1および2に示す本発明の反応容器では、保持部21と嵌合部22との間に移送のための開口部23を設けており、第一の収容部10内に第二の収容部20を挿入した状態(嵌合部22で第一の収容部の内壁12と嵌合した状態)で保持部21に収容した第二の試薬42を第一の収容部10に移送させることができる。また、第二の収容部20を挿入した状態で第一の収容部10を蓋部30により密閉すれば、第一の試薬41と第二の試薬42との混合を密閉状態で行なうことが可能となる。なお、図1および2に示す本発明の反応容器は、蓋部30による第一の収容部10の密閉を螺合手段(11、31)による螺合で行なっているが、市販の蓋付マイクロチューブ(例えば、Individual Dome Cap PCR Tube(SSI社製))の蓋を本発明の反応容器における蓋部30に、マイクロチューブ本体を第一の収容部10に、それぞれみなし、当該蓋を圧入によりマイクロチューブ本体に挿入し密閉させる態様であってもよい。
【0021】
保持部21に収容した第二の試薬42の第一の収容部10への移送方法としては、転倒混和による方法や、遠心力を利用した方法があげられる。後者の方法は、移送後に保持部21や第一の収容部の内壁12に残留する試薬の量(デッドボリューム)を最小にできる点で好ましい。
【0022】
後者の方法による第二の試薬の移送方法を図3を用いて詳細に説明する。
(1)回転軸50を中心に回転させることで、本発明の反応容器に遠心力を与え、第二の試薬42を保持部21内壁に沿って上方へ移送させ、開口部23を経由し、第一の収容部の内壁12に移送させる。
(2)第二の試薬42を第一の収容部の内壁12まで移送させた時点で、遠心力を弱め(例えば回転数を減少させ)、重力により第二の試薬42を第一の収容部の内壁12に沿って底部へ移送させる。
(3)移送された第二の試薬42と第一の収容部10に収容された第一の試薬41とを接触させる。なお、第一の試薬41が凍結乾燥体などの固体形状である場合は、この時点で第二の試薬42による第一の試薬41の溶解操作も行なわれる。
(4)第一の試薬41と第二の試薬42との接触後、遠心力の強弱(例えば回転数の増加と減少)を繰り返し、第一の収容部の内壁12に沿って上下に移動させて撹拌することで、均一な混合液を得ることができる。
なお、後者の方法で使用する、遠心力を与える手段としては特に限定はなく、例えば、マイクロチューブ用遠心分離機(卓上遠心機)や、Vortex−Genie 2(Scientific Industries社製)といった回転力を与えることができるミキサーがあげられる。
【実施例】
【0023】
以下、本発明の反応容器をTRC法を用いた遺伝子検査に適用した場合を例として、本発明をさらに詳細に説明するが、当該実施例は本発明を限定するものではない。なおTRC法は、試料に含まれる特定RNAを増幅し検出する遺伝子検査法である(特許文献2)。具体的には、反応基質を含む基質試薬と、特定RNAを増幅するためのオリゴヌクレオチドプライマーおよび前記特定RNAを検出するためのオリゴヌクレオチドプローブを含むプライマー試薬をあらかじめ混合し、当該混合液に特定RNAを増幅するための酵素を含む酵素試薬および試料を添加後、40℃から50℃(好ましくは43℃から46℃)の一定温度下で反応させることで特定RNAの増幅を行ない、それと同時に前記プローブによる特定RNAの検出も行なう。前記プローブにはあらかじめ蛍光色素を修飾させており、当該蛍光色素による蛍光強度の変化をモニタリングすることで、試料中に特定RNAが含まれている否かを反応開始後30分以内に判定することができる。
【0024】
実施例1
本発明の反応容器を用いた遺伝子検査法の一例を以下に示す。
(1)図1および2に示す本発明の反応容器に備えた第一の収容部10に、第一の試薬41として反応基質を含む基質試薬ならびに特定RNAを増幅するためのオリゴヌクレオチドプライマーおよび前記特定RNAを検出するためのオリゴヌクレオチドプローブを含むプライマー試薬の混合試薬を収容する。前記第一の試薬は液体試薬であってもよいし、凍結乾燥などで固化させた試薬であってもよい。
(2)第二の収容部20を第一の収容部10に圧入することで、嵌合部22と第一の収容部の内壁12とを嵌合させる。
(3)保持部21に特定RNAを増幅するための酵素を含む酵素試薬(第二の試薬)42と試料との混合液を収容する。なお、試料としては、菌体培養液、糞便、喀痰、細胞などの検体から核酸抽出試薬(例えば、Extragen IIやExtragen MB(いずれも東ソー社製))を用いて得られる核酸抽出液が好ましい。
(4)螺合手段(11、31)により蓋部30と第一の収容部10とを螺合させることで密閉する。
(5)密閉した本発明の反応容器を一定温度条件下(たとえば43℃から46℃)で加温する。
(6)モーター52でホルダー51を回転させることで、ホルダー51に保持した本発明の反応容器を回転させ、遠心力を与える(図4)。
(7)遠心力により、保持部21に収容された第二の試薬42と試料との混合液が、開口部23を経由し、第一の収容部の内壁12に移送される。
(8)移送後、モーター52による回転を停止し、遠心力をなくすことで、重力により第二の試薬42と試料との混合液を第一の収容部10の底部に移送させ、第一の試薬41と接触させる。なお、第一の試薬41が凍結乾燥などで固化させた試薬である場合は、この時点で第二の試薬42と試料との混合液による第一の試薬41の溶解操作も行なわれる。また、当該混合液が有する粘度などが原因で第一の収容部10の底面への移送速度が遅い場合は、卓上遠心機などを用い、強制的に移送させてもよい。
(9)引き続きミキサーを用いて均一な混合液を調製する。なお、混合はモーター52による断続的な回転で行なってもよい。
(10)均一な混合液を収容した本発明の反応容器を、温調機能付き蛍光分光光度計(例えば、TRCRapid−160(東ソー社製))にセットして再び一定温度条件下(たとえば43℃から46℃)で加温することで、特定RNAを増幅させると同時に、第一の収容部10の底部から反応液43に励起光61を照射して得られる蛍光62の強度変化を検出器63で経時的に検出することで、試料中に特定RNAが存在するか確認できる(図5)。
【0025】
実施例2
実施例1では試料を第二の収容部に設けた保持部21に収容したが、第一の収容部10に収容してもよい、その場合の操作を下記に示す。
(1)図1および2に示す本発明の反応容器に備えた第一の収容部10に、反応基質を含む基質試薬と特定RNAを増幅するためのオリゴヌクレオチドプライマーおよび前記特定RNAを検出するためのオリゴヌクレオチドプローブを含むプライマー試薬の混合試薬(第一の試薬)41と試料を収容する。第一の試薬41は液体試薬であってもよいし、凍結乾燥などで固化させた試薬であってもよい。なお、第一の試薬41が固化させた試薬の場合、試料による第一の試薬41の溶解現象が発生するが、コンタミネーション防止のため、この時点での混合撹拌操作は行なわない。また、試料としては、菌体培養液、糞便、喀痰、細胞などの検体から核酸抽出試薬(例えば、Extragen IIやExtragen MB(いずれも東ソー社製))を用いて得られる核酸抽出液が好ましい。
(2)第二の収容部20を第一の収容部10に圧入することで、嵌合部22と第一の収容部10の内壁11とを嵌合させ、保持部21に特定RNAを増幅するための酵素を含む酵素試薬(第二の試薬)42を収容する。
(3)螺合手段(11、31)により蓋部30と第一の収容部10とを螺合させることで密閉する。
(4)密閉した本発明の反応容器を一定温度条件下(たとえば43℃から46℃)で加温する。
(5)モーター52でホルダー51を回転させることで、ホルダー51に保持した本発明の反応容器を回転させ、遠心力を与える(図4)。
(6)遠心力により、保持部21に収容された第二の試薬42が、開口部23を経由し、第一の収容部の内壁12に移送される。
(7)移送後、モーター52による回転を停止し、遠心力をなくすことで、重力により第二の試薬42を第一の収容部10の底部に移送させ、第一の試薬41および試料と接触させる。なお、当該混合液が有する粘度などが原因で第一の収容部10の底面への移送速度が遅い場合は、卓上遠心機などを用い、強制的に移送させてもよい。
(8)引き続きミキサーを用いて均一な混合液を調製する。また、混合はモーター52による断続的な回転で行なってもよい。
(9)均一な混合液を収容した本発明の反応容器を、温調機能付き蛍光分光光度計(例えば、TRCRapid−160(東ソー社製))にセットして再び一定温度条件下(たとえば43℃から46℃)で加温することで、特定RNAを増幅させると同時に、第一の収容部10の底部から反応液43に励起光61を照射して得られる蛍光62の強度変化を検出器63で経時的に検出することで、試料中に特定RNAが存在するか確認できる(図5)。
【符号の説明】
【0026】
10:第一の収容部
11、31:螺合手段
12:内壁
20:第二の収容部
21:保持部
22:嵌合部
23:開口部
30:蓋
41:第一の試薬
42:第二の試薬
43:反応液
50:回転軸
51:ミキサーホルダー
52:ミキサーモーター
61:励起光
62:蛍光
63:蛍光検出器
【技術分野】
【0001】
本発明は、試薬または試料を収容する複数の収容部を備えた反応容器に関する。特に本発明は、収容部のそれぞれに収容した試薬または試料を密閉状態で混合するのに適した反応容器に関する。
【背景技術】
【0002】
従来、生化学分野において、液体同士または液体と固体とを混合する際は、あらかじめ固体または液体を入れた容器に、ピペットやシリンジなどを用いて液体を添加し、液体同士または液体と固体とを接触させて混合する。しかしながら、ピペットやシリンジなどを用いて容器に液体を添加/混合する際、容器は開放された状態(蓋の開いた状態)である。そのため、混合すべき液体同士または液体と固体とが接触した時点で反応が開始する場合、すぐに容器を密閉したとしても添加してから容器を密閉状態にするときまでの間、反応物が大気中に拡散してしまう恐れがある。特に遺伝子検査試薬の場合、反応開始と同時に核酸が指数関数的に増幅するため、増幅した核酸が大気中に拡散することによるコンタミネーションの恐れがある。
【0003】
特許文献1は、遺伝子検査で用いる各試薬を密閉状態で混合する遺伝子検出用具を開示している。この遺伝子検出用具は、反応室としての容器と開封自在の隔壁部を有した検出室としての容器とを備え、かつ検出室としての容器と反応室としての容器とが嵌合可能となっている。特許文献1の容器を用いて遺伝子検査を行なう際は、
(1)反応室としての容器に遺伝子検査を行なうのに必要な第一の試薬および試料(例えば検体からの核酸抽出物)を、検出室としての容器に遺伝子検査を行なうのに必要な第二の試薬を、それぞれ収容し、
(2)反応室としての容器と検出室としての容器とを嵌合し、
(3)検出室としての容器が密閉された状態で、当該容器の外側から隔壁部を押しつぶして破開することで反応室としての容器と検出室としての容器とを連通し、
(4)両容器に収容した第一の試薬および試料と第二の試薬とを接触/混合し、適切な温度条件下で遺伝子増幅および検出を行なう、
ことで遺伝子検査を行なう。ただし、特許文献1の容器は、連通させる際、隔壁部を押しつぶし破開させる必要があるため、検出室としての容器は適度に変形可能な材質とする必要がある。また、隔壁部を破開させる際、反応室としての容器と検出室としての容器との嵌合部分が外れないようにするため、前記嵌合部分と前記隔壁部との間は十分な間隔をとる必要がある。そのため、容器全体の小型化が困難である。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特許第3642574号公報
【特許文献2】特開2000−014400号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
本発明の目的は、試薬または試料を収容する複数の収容部を備えた反応容器において、前記収容部のそれぞれに収容した試薬または試料を密閉状態で混合し反応させることが可能で、かつ従来の容器と比較し簡単な構成または小型化可能な容器を提供することにある。
【課題を解決するための手段】
【0006】
前記目的を達成するためになされた本発明は、以下の態様を包含する:
第一の態様は、
第一の試薬または試料を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な、第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉する蓋部と、を備えた反応容器であって、
第二の収容部が、第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部と、を設けた収容部である、
前記反応容器である。
【0007】
第二の態様は、第二の収容部に設けた保持部の形状が、略半球状、略半偏心球面状または略錐状の凹部をなす、前記第一の態様に記載の反応容器である。
【0008】
第三の態様は、少なくとも第一の収容部の前記底部が光透過性を有している、前記第一または第二の態様に記載の反応容器である。
【0009】
第四の態様は、
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、および
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、を含む、
前記第一から第三の態様のいずれかに記載の反応容器を用いた、試料に含まれる特定成分の測定方法である。
【0010】
第五の態様は、
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、および
(7)第一の収容部の底部を通じて、反応生成物を光学的手法により検出する操作、
を含む、前記第三の態様に記載の反応容器を用いた、試料に含まれる特定成分の測定方法である。
【0011】
第六の態様は、第一の試薬が凍結乾燥試薬である、前記第四または第五の態様に記載の測定方法である。
【0012】
第七の態様は、
試料中に含まれる特定成分が特定核酸であり、
第一の試薬が試料に含まれる特定核酸を増幅するためのオリゴヌクレオチドプライマー、前記特定核酸を検出するためのオリゴヌクレオチドプローブおよび反応基質を含み、
第二の試薬が特定核酸を増幅するための酵素を含む、
前記第四から第六の態様のいずれかに記載の測定方法である。
【発明の効果】
【0013】
本発明の反応容器は、第一の試薬を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉可能な蓋部とを備え、かつ、第二の収容部が第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部とを設けていることを特徴としている。本発明の反応容器は、接触および混合すべき第一の試薬および第二の試薬を各収容部に収容し、試料を添加後、密閉した状態で接触および混合が可能である。また、本発明の反応容器は、第二の収容部に収容した第二の試薬を、第二の収容部が第一の収容部内に挿入した状態(第二の収容部に設けた嵌合部が第一の収容部の内壁と嵌合した状態)で、第二の収容部に設けた開口部より第一の収容部に移送させることができる。このため、試薬を混合させる際、特許文献1のように隔壁部を破開させる操作が不要となり、反応容器全体を小型化することができる。例えば、遺伝子増幅反応で用いる市販の蓋付マイクロチューブの蓋を本発明の反応容器における蓋部に、マイクロチューブ本体を第一の収容部に、それぞれみなし、マイクロチューブ本体内に挿入可能な第二の収容部を新たに作製することで、混合撹拌して得られた反応液をそのまま市販の遺伝子増幅検出装置にセットすることができる。
【0014】
特に、PCR(Polymerase Chain Reaction)法、RT−PCR(Reverse−Transcription PCR)法、NASBA(Nucleic Acid Sequence Based Amplification)法、TMA(Transcription−Mediated Amplification)法、TRC(Transcription Reverse−transcription Concerted reaction)法(特許文献2)などの核酸増幅法では、試料と各試薬とを混合し一定温度下で反応させると、速やかに特定核酸の増幅が開始される。そのため、各試薬と試料との混合操作や反応操作(核酸増幅操作)を大気中に開放された状態で実施すると、当該増幅した核酸が大気中に拡散することによるコンタミネーションリスクが発生し得る。本発明の反応容器は、各試薬と試料との混合操作および核酸増幅反応を密閉状態で行なうことができる。そのため、前記コンタミネーションリスクを低減させることができる。さらに、本発明の反応容器のうち、少なくとも第一の収容部の底部を光透過性を有する材料で作製すると、核酸増幅の有無を光学的手法を用いて検出することができる。よって、蛍光色素などで標識した、特定核酸を特異的に検出するオリゴヌクレオチドプローブを試薬に添加すると、試薬と試料との混合操作、核酸増幅反応および核酸検出操作をいずれも密閉状態で行なえるため、前記コンタミネーションリスクをさらに低減させることができる。
【図面の簡単な説明】
【0015】
【図1】本発明の反応容器の一例を示した図(分解図)である。
【図2】図1の反応容器に備えた各収容部に各試薬を収容した態様を示した図である。
【図3】回転により、第二の収容部に収容した液体を、開口部から第一の収容部へ移送する態様を示した図である。
【図4】ミキサーを用いて、第二の収容部に収容した液体を、開口部から第一の収容部へ移送する態様を示した図である。
【図5】本発明の反応容器内で反応させた反応液を、光学的手法で測定する態様の一例を示した図である。
【発明を実施するための形態】
【0016】
本発明の反応容器を、図を用いて詳細に説明する。
【0017】
図1および2に示す本発明の反応容器は、
第一の試薬41を収容するための第一の収容部10と、
第一の収容部10内に挿入可能な、第二の試薬42を収容するための第二の収容部20と、
第二の収容部20を挿入した状態で第一の収容部10を密閉可能な蓋部30とを備えており、
第一の収容部10の外壁には蓋部30により密閉可能な手段(図1では螺合手段11)を設けており、
第二の収容部20は、第二の試薬42を収容し保持するための保持部21と、第一の収容部の内壁12と嵌合可能な嵌合部22と、嵌合部22で第一の収容部の内壁12と嵌合した状態で保持部21に保持した第二の試薬42を第一の収容部10に移送可能な開口部23とを設けている。
【0018】
図1および2に示す本発明の反応容器では、第二の収容部20を第一の収容部10内に圧入により挿入することで、嵌合部22を第一の収容部の内壁12と嵌合させている。なお、嵌合部22と第一の収容部の内壁12との嵌合をより確実にするために、第一の収容部の内壁12のうち当該嵌合位置の直下に突起などを設けてもよい。
【0019】
図1および2に示す本発明の反応容器において、第二の試薬42を収容し保持するための保持部21は、第一の収容部10に試料を添加する場合は少なくとも反応に必要な量の第二の試薬42を、第二の収容部20に試料を添加する場合は少なくとも反応に必要な量の第二の試薬42と添加する試料との合計量を、それぞれ収容し保持可能であればよく、その形状に限定はない。ただし、保持部21の内底面の形状を、略半球状、略半偏心球面状または略円錐状や略角錐状といった略錐状の凹部をなす形状とすると、後述の開口部23を用いた第二の試薬42の第一の収容部10への移送をスムーズに行なうことができ、かつ移送後に残留する試薬の量(デッドボリューム)も最小にできるため好ましい。
【0020】
図1および2に示す本発明の反応容器では、保持部21と嵌合部22との間に移送のための開口部23を設けており、第一の収容部10内に第二の収容部20を挿入した状態(嵌合部22で第一の収容部の内壁12と嵌合した状態)で保持部21に収容した第二の試薬42を第一の収容部10に移送させることができる。また、第二の収容部20を挿入した状態で第一の収容部10を蓋部30により密閉すれば、第一の試薬41と第二の試薬42との混合を密閉状態で行なうことが可能となる。なお、図1および2に示す本発明の反応容器は、蓋部30による第一の収容部10の密閉を螺合手段(11、31)による螺合で行なっているが、市販の蓋付マイクロチューブ(例えば、Individual Dome Cap PCR Tube(SSI社製))の蓋を本発明の反応容器における蓋部30に、マイクロチューブ本体を第一の収容部10に、それぞれみなし、当該蓋を圧入によりマイクロチューブ本体に挿入し密閉させる態様であってもよい。
【0021】
保持部21に収容した第二の試薬42の第一の収容部10への移送方法としては、転倒混和による方法や、遠心力を利用した方法があげられる。後者の方法は、移送後に保持部21や第一の収容部の内壁12に残留する試薬の量(デッドボリューム)を最小にできる点で好ましい。
【0022】
後者の方法による第二の試薬の移送方法を図3を用いて詳細に説明する。
(1)回転軸50を中心に回転させることで、本発明の反応容器に遠心力を与え、第二の試薬42を保持部21内壁に沿って上方へ移送させ、開口部23を経由し、第一の収容部の内壁12に移送させる。
(2)第二の試薬42を第一の収容部の内壁12まで移送させた時点で、遠心力を弱め(例えば回転数を減少させ)、重力により第二の試薬42を第一の収容部の内壁12に沿って底部へ移送させる。
(3)移送された第二の試薬42と第一の収容部10に収容された第一の試薬41とを接触させる。なお、第一の試薬41が凍結乾燥体などの固体形状である場合は、この時点で第二の試薬42による第一の試薬41の溶解操作も行なわれる。
(4)第一の試薬41と第二の試薬42との接触後、遠心力の強弱(例えば回転数の増加と減少)を繰り返し、第一の収容部の内壁12に沿って上下に移動させて撹拌することで、均一な混合液を得ることができる。
なお、後者の方法で使用する、遠心力を与える手段としては特に限定はなく、例えば、マイクロチューブ用遠心分離機(卓上遠心機)や、Vortex−Genie 2(Scientific Industries社製)といった回転力を与えることができるミキサーがあげられる。
【実施例】
【0023】
以下、本発明の反応容器をTRC法を用いた遺伝子検査に適用した場合を例として、本発明をさらに詳細に説明するが、当該実施例は本発明を限定するものではない。なおTRC法は、試料に含まれる特定RNAを増幅し検出する遺伝子検査法である(特許文献2)。具体的には、反応基質を含む基質試薬と、特定RNAを増幅するためのオリゴヌクレオチドプライマーおよび前記特定RNAを検出するためのオリゴヌクレオチドプローブを含むプライマー試薬をあらかじめ混合し、当該混合液に特定RNAを増幅するための酵素を含む酵素試薬および試料を添加後、40℃から50℃(好ましくは43℃から46℃)の一定温度下で反応させることで特定RNAの増幅を行ない、それと同時に前記プローブによる特定RNAの検出も行なう。前記プローブにはあらかじめ蛍光色素を修飾させており、当該蛍光色素による蛍光強度の変化をモニタリングすることで、試料中に特定RNAが含まれている否かを反応開始後30分以内に判定することができる。
【0024】
実施例1
本発明の反応容器を用いた遺伝子検査法の一例を以下に示す。
(1)図1および2に示す本発明の反応容器に備えた第一の収容部10に、第一の試薬41として反応基質を含む基質試薬ならびに特定RNAを増幅するためのオリゴヌクレオチドプライマーおよび前記特定RNAを検出するためのオリゴヌクレオチドプローブを含むプライマー試薬の混合試薬を収容する。前記第一の試薬は液体試薬であってもよいし、凍結乾燥などで固化させた試薬であってもよい。
(2)第二の収容部20を第一の収容部10に圧入することで、嵌合部22と第一の収容部の内壁12とを嵌合させる。
(3)保持部21に特定RNAを増幅するための酵素を含む酵素試薬(第二の試薬)42と試料との混合液を収容する。なお、試料としては、菌体培養液、糞便、喀痰、細胞などの検体から核酸抽出試薬(例えば、Extragen IIやExtragen MB(いずれも東ソー社製))を用いて得られる核酸抽出液が好ましい。
(4)螺合手段(11、31)により蓋部30と第一の収容部10とを螺合させることで密閉する。
(5)密閉した本発明の反応容器を一定温度条件下(たとえば43℃から46℃)で加温する。
(6)モーター52でホルダー51を回転させることで、ホルダー51に保持した本発明の反応容器を回転させ、遠心力を与える(図4)。
(7)遠心力により、保持部21に収容された第二の試薬42と試料との混合液が、開口部23を経由し、第一の収容部の内壁12に移送される。
(8)移送後、モーター52による回転を停止し、遠心力をなくすことで、重力により第二の試薬42と試料との混合液を第一の収容部10の底部に移送させ、第一の試薬41と接触させる。なお、第一の試薬41が凍結乾燥などで固化させた試薬である場合は、この時点で第二の試薬42と試料との混合液による第一の試薬41の溶解操作も行なわれる。また、当該混合液が有する粘度などが原因で第一の収容部10の底面への移送速度が遅い場合は、卓上遠心機などを用い、強制的に移送させてもよい。
(9)引き続きミキサーを用いて均一な混合液を調製する。なお、混合はモーター52による断続的な回転で行なってもよい。
(10)均一な混合液を収容した本発明の反応容器を、温調機能付き蛍光分光光度計(例えば、TRCRapid−160(東ソー社製))にセットして再び一定温度条件下(たとえば43℃から46℃)で加温することで、特定RNAを増幅させると同時に、第一の収容部10の底部から反応液43に励起光61を照射して得られる蛍光62の強度変化を検出器63で経時的に検出することで、試料中に特定RNAが存在するか確認できる(図5)。
【0025】
実施例2
実施例1では試料を第二の収容部に設けた保持部21に収容したが、第一の収容部10に収容してもよい、その場合の操作を下記に示す。
(1)図1および2に示す本発明の反応容器に備えた第一の収容部10に、反応基質を含む基質試薬と特定RNAを増幅するためのオリゴヌクレオチドプライマーおよび前記特定RNAを検出するためのオリゴヌクレオチドプローブを含むプライマー試薬の混合試薬(第一の試薬)41と試料を収容する。第一の試薬41は液体試薬であってもよいし、凍結乾燥などで固化させた試薬であってもよい。なお、第一の試薬41が固化させた試薬の場合、試料による第一の試薬41の溶解現象が発生するが、コンタミネーション防止のため、この時点での混合撹拌操作は行なわない。また、試料としては、菌体培養液、糞便、喀痰、細胞などの検体から核酸抽出試薬(例えば、Extragen IIやExtragen MB(いずれも東ソー社製))を用いて得られる核酸抽出液が好ましい。
(2)第二の収容部20を第一の収容部10に圧入することで、嵌合部22と第一の収容部10の内壁11とを嵌合させ、保持部21に特定RNAを増幅するための酵素を含む酵素試薬(第二の試薬)42を収容する。
(3)螺合手段(11、31)により蓋部30と第一の収容部10とを螺合させることで密閉する。
(4)密閉した本発明の反応容器を一定温度条件下(たとえば43℃から46℃)で加温する。
(5)モーター52でホルダー51を回転させることで、ホルダー51に保持した本発明の反応容器を回転させ、遠心力を与える(図4)。
(6)遠心力により、保持部21に収容された第二の試薬42が、開口部23を経由し、第一の収容部の内壁12に移送される。
(7)移送後、モーター52による回転を停止し、遠心力をなくすことで、重力により第二の試薬42を第一の収容部10の底部に移送させ、第一の試薬41および試料と接触させる。なお、当該混合液が有する粘度などが原因で第一の収容部10の底面への移送速度が遅い場合は、卓上遠心機などを用い、強制的に移送させてもよい。
(8)引き続きミキサーを用いて均一な混合液を調製する。また、混合はモーター52による断続的な回転で行なってもよい。
(9)均一な混合液を収容した本発明の反応容器を、温調機能付き蛍光分光光度計(例えば、TRCRapid−160(東ソー社製))にセットして再び一定温度条件下(たとえば43℃から46℃)で加温することで、特定RNAを増幅させると同時に、第一の収容部10の底部から反応液43に励起光61を照射して得られる蛍光62の強度変化を検出器63で経時的に検出することで、試料中に特定RNAが存在するか確認できる(図5)。
【符号の説明】
【0026】
10:第一の収容部
11、31:螺合手段
12:内壁
20:第二の収容部
21:保持部
22:嵌合部
23:開口部
30:蓋
41:第一の試薬
42:第二の試薬
43:反応液
50:回転軸
51:ミキサーホルダー
52:ミキサーモーター
61:励起光
62:蛍光
63:蛍光検出器
【特許請求の範囲】
【請求項1】
第一の試薬または試料を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な、第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉する蓋部と、を備えた反応容器であって、
第二の収容部が、第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部と、を設けた収容部である、
前記反応容器。
【請求項2】
第二の収容部に設けた保持部の形状が、略半球状、略半偏心球面状または略錐状の凹部をなす、請求項1に記載の反応容器。
【請求項3】
少なくとも第一の収容部の前記底部が光透過性を有している、請求項1または2に記載の反応容器。
【請求項4】
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、および
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、を含む、
請求項1から3のいずれかに記載の反応容器を用いた、試料に含まれる特定成分の測定方法。
【請求項5】
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、および
(7)第一の収容部の底部を通じて、反応生成物を光学的手法により検出する操作、
を含む、請求項3に記載の反応容器を用いた、試料に含まれる特定成分の測定方法。
【請求項6】
第一の試薬が凍結乾燥試薬である、請求項4または5に記載の測定方法。
【請求項7】
試料中に含まれる特定成分が特定核酸であり、
第一の試薬が試料に含まれる特定核酸を増幅するためのオリゴヌクレオチドプライマー、前記特定核酸を検出するためのオリゴヌクレオチドプローブおよび反応基質を含み、
第二の試薬が特定核酸を増幅するための酵素を含む、
請求項4から6のいずれかに記載の測定方法。
【請求項1】
第一の試薬または試料を収容するための底部および内壁を有する第一の収容部と、第一の収容部内に挿入可能な、第二の試薬または試料を収容するための第二の収容部と、第一の収容部を密閉する蓋部と、を備えた反応容器であって、
第二の収容部が、第二の試薬または試料を収容し保持するための保持部と、第一の収容部の前記内壁と嵌合可能な嵌合部と、前記保持部に保持した第二の試薬または試料を第一の収容部に移送可能とする開口部と、を設けた収容部である、
前記反応容器。
【請求項2】
第二の収容部に設けた保持部の形状が、略半球状、略半偏心球面状または略錐状の凹部をなす、請求項1に記載の反応容器。
【請求項3】
少なくとも第一の収容部の前記底部が光透過性を有している、請求項1または2に記載の反応容器。
【請求項4】
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、および
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、を含む、
請求項1から3のいずれかに記載の反応容器を用いた、試料に含まれる特定成分の測定方法。
【請求項5】
(1)第一の収容部に第一の試薬を、第二の収容部に設けた保持部に第二の試薬を、それぞれ収容する操作、
(2)第一の収容部または第二の収容部に試料を添加する操作、
(3)第二の収容部を、その嵌合部が第一の収容部の内壁と嵌合するよう、挿入する操作、
(4)蓋部により、第一の収容部を密閉する操作、
(5)第二の収容部に設けた保持部に収容された第二の試薬、または第二の試薬および試料を、開口部を通じて第一の収容部に移送する操作、
(6)移送された第二の試薬と第一の収容部に収容された第一の試薬および試料、または移送された第二の試薬および試料と第一の収容部に収容された第一の試薬、とを反応させる操作、および
(7)第一の収容部の底部を通じて、反応生成物を光学的手法により検出する操作、
を含む、請求項3に記載の反応容器を用いた、試料に含まれる特定成分の測定方法。
【請求項6】
第一の試薬が凍結乾燥試薬である、請求項4または5に記載の測定方法。
【請求項7】
試料中に含まれる特定成分が特定核酸であり、
第一の試薬が試料に含まれる特定核酸を増幅するためのオリゴヌクレオチドプライマー、前記特定核酸を検出するためのオリゴヌクレオチドプローブおよび反応基質を含み、
第二の試薬が特定核酸を増幅するための酵素を含む、
請求項4から6のいずれかに記載の測定方法。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2013−42713(P2013−42713A)
【公開日】平成25年3月4日(2013.3.4)
【国際特許分類】
【出願番号】特願2011−183339(P2011−183339)
【出願日】平成23年8月25日(2011.8.25)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
【公開日】平成25年3月4日(2013.3.4)
【国際特許分類】
【出願日】平成23年8月25日(2011.8.25)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
[ Back to top ]

