口部材及び内容物収納容器
【課題】 中心領域に向かっての押圧力を高い状態にすることにより、針を刺した状態での気密性及び液密性又は針を抜いた状態での気密性及び液密性を担保する手段の提供。
【解決手段】 弾性体から構成される栓体部材と、前記栓体部材が挿入可能な第一開口部が形成されており、かつ、当該開口部から挿入された前記栓体部材を収納可能な内部空間が形成されたベース部材と、前記ベース部材の前記第一開口部を覆うように前記ベース部材に装着可能な、前記第一開口部よりも小さく設定された第二開口部を有する冠体部材と、を備えた口部材であって、前記栓体部材が前記内部空間に収納された状態で前記冠体部材を前記ベース部材に装着した際、前記栓体部材は、前記冠体部材及び前記ベース部材の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記内部空間を形成する内壁からも圧縮力を受ける一方、前記圧縮力による弾性変形の結果、前記栓体部材の一部が前記第二開口部から凸状に露出する口部材。
【解決手段】 弾性体から構成される栓体部材と、前記栓体部材が挿入可能な第一開口部が形成されており、かつ、当該開口部から挿入された前記栓体部材を収納可能な内部空間が形成されたベース部材と、前記ベース部材の前記第一開口部を覆うように前記ベース部材に装着可能な、前記第一開口部よりも小さく設定された第二開口部を有する冠体部材と、を備えた口部材であって、前記栓体部材が前記内部空間に収納された状態で前記冠体部材を前記ベース部材に装着した際、前記栓体部材は、前記冠体部材及び前記ベース部材の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記内部空間を形成する内壁からも圧縮力を受ける一方、前記圧縮力による弾性変形の結果、前記栓体部材の一部が前記第二開口部から凸状に露出する口部材。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、例えば、分析システムにおいて使用される薬液バッグに適用可能な、気密性・液密性に優れた口部材及びそれを用いた内容物収納容器に関する。
【背景技術】
【0002】
近年、様々な分野で、極微量成分の定量又は半定量分析技術が検討されている。例えば、半導体の製造工程においては、Siウエハの洗浄その他の洗浄工程、露光・現像工程、エッチング工程において、様々な薬液が用いられる。これらの薬液に金属不純物が混入している場合、サブppb乃至pptオーダーであっても、製品性能・歩留まりに深刻な悪影響を及ぼすことがあるので、当該濃度の不純物測定は極めて重要である。
【0003】
更に、前記薬液の分析は、(1)各薬液毎にサンプルを採取し、(2)別の場所の分析室等において、濃縮等のバッチ方式でのみ適用できる方法で検出感度を高める処理を行った後、(3)ICP-MS(Inductively coupled plasma-mass spectrometer:誘導結合プラズマ質量分析)などの高感度分析方法に委ねていた。このような方法では、試料濃縮などの処理が必要なために、分析結果が出るまでに最短でも一日程度要し、その結果、薬液の不純物濃度が高いと判断された場合は、それにかかる製品をすべて廃棄するなどの無駄を生じ、結果として、歩留まりの低下を引き起こしていた。加えて、前記手法では、サンプルが測定されるまでの間、濃縮プロセス等の複数の工程を介在させるので、汚染の機会が増え、必ずしも超微量分析に適した手法とはいえない。そこで、微量の金属元素をオンサイトで分析する手法として、フロー分析(フローインジェクション分析)を適用する手法が提案されている(特許文献1)。この手法によれば、サンプルがリアルタイムかつ自動的に反応系に導かれるので、汚染の危険性が相当低減される。
【0004】
ここで、フロー分析は、溶液バッグを用いることにより、完全閉鎖系測定システムとすることが可能で、測定環境からの汚染を遮断することができる。これに加え、測定後、瞬時に測定結果が得られ、手軽に持ち運びでき、更には装置調整も簡単なことから、オンサイト分析が可能である。そのため、例えば、半導体の製造工程中に設置し、その結果を半導体製造工程に直ちに反映できる。ここで、測定環境からの汚染防止の観点からは、溶液バックを如何に密閉系にできるかが重要であり、当該密閉を担う一部材が、収容体の開口部を閉塞するように取着され収容体中の液体の出入れに利用される口部材(スパウト)である。ここで、図44及び図45に従来の薬液バッグに使用されている口部材の一例を示す(特許文献1)。この口部材1は、弾性体15が封入される内部空間7を具備し、収容物吸出し用の液路6に連通する口部8と、この口部8を覆うように装着可能であり、収容物吸出し用の針が差し込まれる冠体20と、を有し、前記冠体20には、冠体20を前記口部8に装着した際に前記内部空間7に封入された弾性体15を押圧して、弾性体15を前記口部8の内周壁に付勢する押圧部22が形成されている。ここで、図45に示すように、弾性体15は、矢印方向から押圧した場合に全体的に半径方向に膨らむように、軸方向に膨らんだ形状に構成されている。そして、弾性体15は、内部空間7の径よりも僅かに小さいため、内部空間7に容易に封入することができる。
【特許文献1】特許第2519871号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
ここで、上記口部材は、冠体部材の押圧により弾性体を口部内周壁に付勢するという構成を採っているので、口部の径よりも大きな径を有するゴムを封入することによりゴム自体に強い押圧力を付与する構成と比較すると、作製工程が容易であるという優れた利点があるものの、他方で、弾性体の材質や形状等によっては、中心領域に向かっての押圧力が不十分になり、針を刺した状態での気密性及び液密性又は針を抜いた状態での気密性及び液密性が担保できないという問題がある。更に、上記口部材を使用するに際しては、上部から穿刺針を膜体22aに突き刺す操作を行なうが、この際、当該突き刺しにより切断した膜体22aの一部が該針内に侵入することが多々あり、偽結果の原因となったり分析装置の故障の原因になることが危惧されている。
【課題を解決するための手段】
【0006】
本発明者らは、上記課題を解決するために鋭意研究した結果、本発明(1)〜(8)を完成させたものである。
【0007】
本発明(1)は、弾性体から構成される栓体部材(栓体部材131b〜331b)と、
前記栓体部材(栓体部材131b〜331b)が挿入可能な第一開口部(開口部131a1〜331a1)が形成されており、かつ、当該開口部(開口部131a1〜331a1)から挿入された前記栓体部材(栓体部材131b〜331b)を収納可能な内部空間(内部空間131a5〜331a5)が形成されたベース部材(ベース部材131a〜331a)と、
前記ベース部材(ベース部材131a〜331a)の前記第一開口部(開口部131a1〜331a1)を覆うように前記ベース部材(ベース部材131a〜331a)に装着可能な、前記第一開口部(開口部131a1〜331a1)よりも小さく設定された第二開口部(開口部131c1〜331c1)を有する冠体部材(冠体部材131c〜331c)と、
を備えた口部材(口部材130〜330)であって、
前記栓体部材(栓体部材131b〜331b)が前記内部空間(内部空間131a5〜331a5)に装着された状態で前記冠体部材(冠体部材131c〜331c)を前記ベース部材(ベース部材131a〜331a)に嵌合した際、前記栓体部材(栓体部材131b〜331b)は、前記冠体部材(冠体部材131c〜331c)及び前記ベース部材(ベース部材131a〜331a)の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記内部空間(内部空間131a5〜331a5)を形成する内壁(内壁131a2〜331a2)からも圧縮力を受ける一方、前記圧縮力による弾性変形の結果、前記栓体部材(栓体部材131b〜331b)の一部(凸部131b1〜331b1)が前記第二開口部(開口部131c1〜331c1)から凸状に露出する口部材(口部材130〜330)である。
【0008】
本発明(2)は、前記装着が、冠体部材(冠体部材231c、冠体部材331c)と前記ベース部材(ベース部材231a、ベース部材331a)との螺合により達成されると共に、前記螺合の程度に応じて、前記圧縮力が可変するよう構成されている、前記発明(1)の口部材(口部材230、口部材330)である。
【0009】
本発明(3)は、前記ベース部材(ベース部材331a)が、前記第一開口部(開口部331a1)とは反対側に、前記第一開口部(開口部331a1)よりも小さく設定された第三開口部(開口部331a3−1)を更に有しており、
前記栓体部材(栓体部材331b)が前記内部空間(内部空間331a5)に収納された状態で前記冠体部材(冠体部材331c)を前記ベース部材(ベース部材331a)に装着した際、前記栓体部材(栓体部材331b)は、前記冠体部材(冠体部材331c)及び前記ベース部材(ベース部材331a)の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記栓体部材(栓体部材331b)の一部が前記第三開口部(開口部331a3−1)から凸状に露出するよう構成されている、前記発明(1)又は(2)の口部材(口部材330)である。
【0010】
本発明(4)は、前記発明(1)〜(3)のいずれか一つの口部材を備えた内容物収納容器(口部材130〜330)である。
【0011】
本発明(5)は、前記内容物が化学分析用薬液である、前記発明(4)の内容物収納容器(薬液バッグ100〜300)である。
【0012】
本発明(6)は、前記化学分析がフロー分析である、前記発明(5)の内容物収納容器(薬液バッグ100〜300)である。
【0013】
本発明(7)は、前記内容物が酸素易変性成分を含有する、前記発明(4)〜(6)のいずれか一つの内容物収納容器(薬液バッグ100〜300)である。
【0014】
本発明(8)は、前記収納容器が酸素バリア性素材から構成されている、前記発明(7)の内容物収納容器(薬液バッグ100〜300)である。
【発明の効果】
【0015】
本発明(1)によれば、上方向から栓体部材を圧縮すると共に、当該圧縮による弾性変形に基づく横方向の変形を規制した結果、横方向から間接的に圧縮される構成を採った上で、冠体部材に開口部を設けたことにより、応力が集中する凸部が形成される。その結果、従来の圧縮型で問題となっていた、針を刺した状態での気密性及び液密性並びに針を抜いた状態での気密性及び液密性がより確実に保証できるという効果を奏する。更には、冠体部材に開口部が設けられているので、従来冠体部材の膜体を突き破る際に問題となり得る、冠体部材由来の膜体による悪影響を回避することができるという効果も奏する。
【0016】
本発明(2)によれば、前記効果に加え、どのような材質の栓体部材を採用しても、螺合の程度を変更することにより、最適な圧縮力を前記栓体部材に与えることが可能になる。その結果、栓体部材の材質を変更しても、ベース部材や冠体部材の形状等を変更する必要がないので、製造コストを顕著に低減できるという効果を奏する。加えて、使用日数の経過につれて穿刺針の突き刺し部分から液漏れが生じた場合であっても、螺合の程度を変更することにより、当該液漏れの問題を解消することができるという効果も奏する。更には、螺合の程度を適宜調整することにより、どのような材質の栓体部材を採用しても、破断した栓体部材が針の内部に侵入することも防止することができる。その結果、偽結果や分析装置の故障を未然に防止することが可能になるという効果も奏する。
【0017】
本発明(3)によれば、前記効果に加えて、ベース部材の底部に開口部が設けられているので、従来ベース部材の底部の膜体を突き破る際に問題となった、ベース部材由来の膜体による悪影響を回避することができるという効果も奏する。
【0018】
本発明(4)〜(8)も前記効果と同じ効果を奏する。尚、保存時・使用時とも高い気密性・液密性を担保できるので、特に、酸素が極微量でも容器内に侵入すると分析結果に悪影響を及ぼすような場合(特に、サブppb乃至pptオーダーといった超微量分析の場合)に有効である。
【発明を実施するための最良の形態】
【0019】
以下、図1〜図9を参照しながら、最良形態として薬液バッグを例にとり、本発明の第一の最良形態について説明する。尚、本発明の権利範囲は、以下の最良形態に限定されるものではない。即ち、上記最良形態は、あくまでも例示であり、本発明の特許請求の範囲に記載された技術的思想と実質的に同一な構成を有し、同様な作用効果を奏するものは、いかなるものであっても本発明の権利範囲に包含される。例えば、本発明に係る口部材を輸液バックに使用する場合も本発明の権利範囲内である。
【0020】
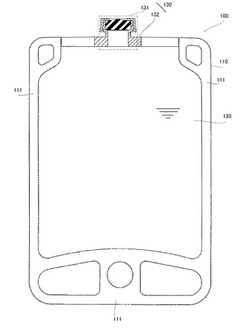
はじめに、本最良形態に係る薬液バッグ100の構造について説明する。まず、図1は、本最良形態に係る薬液バッグ100の断面図を示した図である。薬液バッグ100は、シート状又はフィルム状の合成樹脂を貼り合わせて袋状に形成した容器110と、前記容器110内に収納された薬液120と、前記容器110をヒートシールする等により、気密的・液密的に当該容器110に固定された口部材130とから構成されている。以下、各要素について詳述する。
【0021】
まず、図1〜図8を参照しながら、本最良形態に係る口部材130の構造について説明する。はじめに、図1に示すように、口部材130は、口部材130を容器110の口部に取り付けた際、容器110内の薬液120を吸い出す取出口として機能する略円筒状の口部材本体131と、前記口部材本体131と一体化したフランジ部132とから構成される。ここで、図2及び図3は、夫々、図1の状態での口部材130の上面図及び側断面図である。図2及び図3から分かるように、略円筒状を成す口部材本体131は、後述するように、ベース部材131a、栓体部材131b及び冠体部材131cとから構成され、栓体部材131bがベース部材131aと冠体部材131cとにより圧縮状態を保ちながら挟まれた構造を採っている。加えて、口部材130の、容器110の口部に接続される側に、略菱形状のフランジ部132が、ベース部材131aと一体形成されている。ここで、当該フランジ部132は、容器110の口部との取り付け部として機能する(当該フランジ部132の四側面が容器110裏の両面と熱融着する)と共に、菱形状である故、特にフランジ部132の両端部における容器110同士の気密的・液密的なヒートシールを担保することが可能となる。
【0022】
次に、口部材本体131を構成する各要素(ベース部材131a、栓体部材131b及び冠体部材131c)について詳述する。尚、理解の容易上、まず、各要素を別々に説明し、次いでこれらを組み立てた際に構築される口部材本体131を説明する。はじめに、図4及び図5を参照しながら、ベース部材131aを詳述する。ここで、図4(1)、図4(2)及び図5は、夫々、ベース部材131aの側断面図、側面図及び上面図である。まず、ベース部材131aは、円形の開口部131a1をその上面に有すると共に、円筒状の内壁131a2と円形の底面131a3が内部に形成されている。即ち、円柱状の空間131a5がベース部材131aの内部に形成されている。ここで、前記底面131a3の一部(131a3−1)は、使用の際に穿刺針を突き刺した際に貫通可能な程度の厚さに設定されている(例えば、0.5mm程度の膜状)。そして、ベース部材131aの上部外周面には、フランジ状の凸部131a4が形成されている。尚、当該凸部131a4は、後述するように、冠体部材131cの内壁に形成された円周状の凹部131c2(図6参照)と嵌合するよう機能する。
【0023】
次に、図6を参照しながら、栓体部材131bについて詳述する。ここで、図6は、冠体部材131cをベース部材131aに嵌合する前の口部材130の状態を示した図である。栓体部材131bは、ベース部材131の内部に形成された空間131a5と略同一の径を成す円柱体である。但し、後述のように冠体部材131cとベース部材131aとを嵌合した際、両者の挟み込みにより栓体部材131bに圧縮力が作用するよう、栓体部材131の高さは、前記空間131a5のそれよりも大きく設定されている(図6参照)。
【0024】
次に、図2及び図6を参照しながら、冠体部材131cについて詳述する。図2及び図6に示すように、円筒状を成す冠体部材131cは、中央部に開口部131c1を有すると共に、その内壁には円周状の凹部131c2が形成されている。そして、冠体部材131cの裏面には、後述する嵌合時には、栓体部材131b上面の円周縁部に当接すると共に、当該当接部を介して、ベース部材131aの底面131a3と協働して栓体部材131bに対して圧縮力を印加する、略平面の当接部131c3が形成されている。
【0025】
次に、図6〜図8を参照しながら、前記各要素(ベース部材131a、栓体部材131b及び冠体部材131c)を組み立てたことにより構築される口部材本体131について説明する。まず、図7に示す状態は、図6に示す状態から、冠体部材131cをベース部材131aに嵌合することにより構築される。この嵌合操作により、弾性部材である栓体部材131bは、冠体部材131cとベース部材131aとの間に挟まれ圧縮される。ここで、縦方向(図6の矢印方向)での圧縮に伴い、冠体部材131cは横方向に変形しようとするが、横方向の変形はベース部材131aの内壁131a2の存在により規制されるため、横方向からも圧縮される。更に、図7に示すように、栓体部材131bの一部(131b1)が、抗力が生じない開口部131c1に逃げる結果、開口部131c1から凸状に露出する。ここで、図8は、図7の状態における、冠体部材131cとベース部材131a間に挟まれた栓体部材131bの応力分布図である。図8に示されるように、栓体部材131bには、特に冠体部材131c及びベース部材131aの当接部分において、弾性復元力に基づく応力が生じている。この応力に基づく高い気密性及び液密性が、口部材本体131を介しての外部からの空気侵入防止を担保すると共に、外部への液漏れ防止を担保する。
【0026】
次に、図1を参照しながら、本最良形態に係る容器110を説明する。本容器110は、最内層がシーラント層である2枚の積層体を三方ヒートシールして得られた袋体である。ここで、当該袋体は、収納した薬液の量に追従して変形可能であり、薬液の量が減少するに従い扁平状に変形する。
【0027】
次に、上記各要素の材質等について説明する。まず、口部材130を構成する要素の内、栓体部材131b以外の要素(口部材本体131、フランジ部132、冠体部材131c)は、例えば、従来公知の種々のプラスチックを用いて形成可能である。特に熱可塑性樹脂を用いたときは、口部材本体等を射出成形によって簡易に形成することができる。具体的には、ポリエチレン、ポリプロピレン、ポリ4−メチルペンテン〔例えば、三井化学(株)の商品名「TPX」〕、ポリテトラフルオロエチレン等のポリオレフィン;エチレン−テトラシクロドデセン共重合体〔例えば、三井化学(株)の商品名「アペル」〕等のポリ環状オレフィン;ポリアセタール(POM);アクリロニトリル−ブタジエン−スチレン共重合体(ABS);ポリエチレンナフタレート(PEN)、ポリエチレンテレフタレート(PET)、ポリアリレート等のポリエステル;ポリフェニレンサルファイド(PPS)等のベンゼン系重合体等が挙げられる。
【0028】
次に、口部材130を構成する要素の内、弾性体である栓体部材131bは、例えば、従来公知の種々のゴムやエラストマー(例えば、ブチルゴムやSBR等の加硫ゴム)を用いて形成することができる。具体的には、天然ゴム、シリコーンゴム等のゴムや、スチレン系エラストマー(例えば、スチレン−ブタジエン系、スチレン−イソプレン系及びこれらに水素添加物)、オレフィン系エラストマー、ポリウレタン系エラストマー等の熱可塑性エラストマーを挙げることができる。加えて、特に限定されないが、例えば、そのJIS硬度は、40〜55度程度、肉厚は約1〜10mm程度、直径は15〜20mm程度の短円柱状のものが使用可能である。尚、当該栓体部材131bは、例えば熱可塑性エラストマーを用いたときは、射出成形によって形成可能である。
【0029】
次に、容器110を構成する積層体は、好適には、酸素透過度(25℃×80%RH)が10fmol/m2s・Pa以下のガスバリア性素材からなる。ここで、ガスバリア性素材としては、プラスチック基材の表面に、酸化珪素、酸化アルミニウム、酸化マグネシウム、その他等の無機酸化物を使用し、真空蒸着法、スパッタリング法又はイオンプレ−ティング法等の物理気相成長法(PVD法)、或いは、プラズマ化学気相成長法、熱化学気相成長法又は光化学気相成長法等の化学気相成長法(CVD法)等を利用して、その無機酸化物の蒸着薄膜を形成してなる透明ガスバリア性フィルムが好適である。
【0030】
ここでまず、プラスチック基材としては、無機酸化物の蒸着薄膜を設ける点で、物理的及び化学的に優れた強度及び耐熱性を有することが好適である。具体的には、当該プラスチック基材としては、例えば、ポリエチレン系樹脂、ポリプロピレン系樹脂、環状ポリオレフィン系樹脂、フッ素系樹脂、ポリスチレン系樹脂、アクリロニトリル−スチレン共重合体(AS樹脂)、アクリロニトリル−ブタジエン−スチレン共重合体(ABS樹脂)、ポリ塩化ビニル系樹脂、フッ素系樹脂、ポリ(メタ)アクリル系樹脂、ポリカ−ボネ−ト系樹脂、ポリエチレンテレフタレ−ト、ポリエチレンナフタレ−ト等のポリエステル系樹脂、各種のナイロン等のポリアミド系樹脂、ポリイミド系樹脂、ポリアミドイミド系樹脂、ポリアリ−ルフタレ−ト系樹脂、シリコ−ン系樹脂、ポリスルホン系樹脂、ポリフェニレンスルフィド系樹脂、ポリエ−テルスルホン系樹脂、ポリウレタン系樹脂、アセタ−ル系樹脂、セルロ−ス系樹脂、その他等の各種の樹脂のフィルム又はシ−トを挙げることができる。尚、膜厚は、6〜100μmが好適であり、9〜50μmがより好適である。
【0031】
次に、最内層に形成されるシーラント層としては、例えば、熱によって溶融し相互に融着し得る各種のヒ−トシ−ル性を有するポリオレフィン系樹脂が好適である。具体的には、例えば、低密度ポリエチレン、中密度ポリエチレン、高密度ポリエチレン、直鎖状(線状)低密度ポリエチレン、メタロセン触媒を使用して重合したエチレン−α・オレフィン共重合体、ポリプロピレン、エチレン−酢酸ビニル共重合体、アイオノマ−樹脂、エチレン−アクリル酸共重合体、エチレン−アクリル酸エチル共重合体、エチレン−メタクリル酸共重合体、エチレン−メタクリル酸メチル共重合体、エチレン−プロピレン共重合体、メチルペンテンポリマ−、ポリブテンポリマ−、ポリエチレンまたはポリプロピレン等のポリオレフィン系樹脂をアクリル酸、メタクリル酸、マレイン酸、無水マレイン酸、フマ−ル酸、イタコン酸等の不飽和カルボン酸で変性した酸変性ポリオレフィン樹脂、ポリ酢酸ビニル系樹脂、ポリ(メタ)アクリル系樹脂、ポリ塩化ビニル系樹脂、熱可塑性ポリエステル系樹脂、ポリアミド系樹脂等を挙げることができる。尚、当該層の厚さは、5〜200μmであることが好適であり、10〜100μmがより好適である。
【0032】
尚、積層材を形成する材料として、その他、例えば、水蒸気や水等のバリア−性を有する低密度ポリエチレン、中密度ポリエチレン、高密度ポリエチレン、直鎖状低密度ポリエチレン、ポリプロピレン、エチレン−プロピレン共重合体等の樹脂のフィルム又はシ−ト、或いは、酸素や水蒸気等に対するバリア−性を有するポリ塩化ビニリデン系樹脂、ポリビニルアルコ−ル系樹脂、エチレン−ビニルアルコ−ル共重合体、MXDポリアミド系樹脂、ポリナフタレンテレフタレ−ト系樹脂等の樹脂のフィルム又はシ−トの一種又はそれ以上を組み合わせて使用してもよい。尚、当該フィルム又はシ−トの厚さは、特に限定されないが、5μm〜300μmが好適であり、10μm〜100μmがより好適である。
【0033】
次に、本最良形態に係る薬液バッグの性質を説明する。前記のように、薬液バッグ100は、容器110が酸素透過度(25℃×80%RH)が10fmol/m2s・Pa以下の素材から構成されている。加えて、口部材130の栓体部材131bが、内部で上下左右方向から圧縮された状態にある結果、当該栓体部材131bとベース部材131a及び冠体部材131cとで協働し、高い気密・液密性が担保されている。そして、冠体部材131cの開口部に弾性部材の凸部が形成されているので、当該部分に針を刺した場合でも、強力な圧縮力が働き、当該部分で極めて高い気密・液密性が保証される。
【0034】
次に、図9を参照しながら、本最良形態に係る薬液バッグの使用方法を説明する。はじめに、一端側が分析装置(不図示)に連通する薬液チューブの他端に設けられたプラスチック瓶針やステンレス針等の穿刺針Aを、栓体部材131bの凸部131b1に穿刺する。この際、薄膜状の底部131a3−1が穿孔し、その結果、穿刺針Aは薬液容器100の内部に到達する。これにより、上記薬液容器内の薬液が上記チューブを介して分析装置に導入される。
【0035】
以下、次に、図面を参照しながら、本発明の第二の最良形態及び第三の最良形態について説明する。ここで、第一の最良形態と第二の最良形態及び第三の最良形態との相違点は、冠体をベース部材に装着する態様が、前者が嵌合であるのに対し、後者は螺合である点である。更に、第二の最良形態と第三の最良形態との相違点は、前者が栓体部材下が膜状であるのに対し、後者が栓体部材下に開口部が設けられている点である。以下、第一の最良形態との相違部分について説明する。
【0036】
はじめに、図10〜図18を参照しながら、第二の最良形態に係る薬液バッグ200の構造について説明する。まず、図10は、本最良形態に係る薬液バッグ200の断面図を示した図である。薬液バッグ200は、シート状又はフィルム状の合成樹脂を貼り合わせて袋状に形成した容器210と、前記容器210内に収納された薬液220と、前記容器210をヒートシールする等により、気密的・液密的に当該容器210に固定された口部材230とから構成されている。以下、各要素について詳述する。
【0037】
まず、図10〜図17を参照しながら、第二の最良形態に係る口部材230の構造について説明する。はじめに、図10に示すように、口部材230は、口部材230を容器210の口部に取り付けた際、容器210内の薬液220を吸い出す取出口として機能する口部材本体231と、前記口部材231と一体化したフランジ部232とから構成される。ここで、図11及び図12は、夫々、図10の状態での口部材230の上面図及び側断面図である。図11及び図12から分かるように、略円筒状を成す口部材本体231は、後述するように、ベース部材231a、栓体部材231b及び冠体部材231cとから構成され、栓体部材231bがベース部材231aと冠体部材231cとにより圧縮状態を担保しながら挟まれた構造を採っている。加えて、口部材本体230の、容器210の口部に接続される側に、略偏平なフランジ部232が、ベース部材231aと一体形成されている。ここで、当該フランジ部232は、容器210の口部との取り付け部として機能する(当該フランジ部232の両側面が容器210裏の両面と熱融着する)と共に、略偏平状である故、特にフランジ部232の両端部における容器210同士の気密的・液密的なヒートシールを担保することが可能となる。
【0038】
次に、口部材本体231を構成する各要素(ベース部材231a、栓体部材231b及び冠体部材231c)について詳述する。尚、理解の容易上、まず、各要素を別々に説明し、次いでこれらを組み立てた際に構築される口部材本体231を説明する。はじめに、図13及び図14を参照しながら、ベース部材231aを詳述する。ここで、図13及び図14は、夫々、ベース部材231aの側断面図及び上面図である。まず、ベース部材231aは、円形の開口部231a1をその上面に有すると共に、円筒状の内壁231a2と円形の底面231a3が内部に形成されている。即ち、円柱状の空間231a5がベース部材231aの内部に形成されている。ここで、前記底面231a3の一部(231a3−1)は、使用の際に穿刺針を突き刺した際に貫通可能な程度の厚さに設定されている(例えば、0.5mm程度の膜状)。そして、外周面には、螺子状に切り込まれた螺子部231a4が設けられている。尚、当該螺子部231a4は、後述するように、冠体部材231cの内壁に形成された螺子係合部231c2(図15参照)と係合するよう機能する。
【0039】
次に、図15を参照しながら、栓体部材231bについて詳述する。ここで、図15は、冠体部材231cをベース部材231aに螺合する前の口部材230の状態を示した図である。栓体部材231bは、ベース部材231の内部に形成された空間231a5と略同一の径を成す円柱体である。但し、後述のように冠体部材231cとベース部材231aとで挟み込んだ際、栓体部材231に圧縮力が作用するよう、栓体部材231の高さは、前記空間231a5のそれよりも大きく設定されている(図15参照)。
【0040】
次に、図11及び図15を参照しながら、冠体部材231cについて詳述する。図11及び図15に示すように、円筒状を成す冠体部材231cは、中央部に開口部231c1を有すると共に、その内壁には螺子係合部231c2が形成されている。そして、冠体部材231cの裏面には、後述する取付時には、栓体部材231b上面の円周縁部に当接すると共に、当該当接部を介して、ベース部材231aの底面231a3と協働して栓体部材231に対して圧縮力を印加する、略平面の当接部231c3が形成されている。
【0041】
次に、図15〜図17を参照しながら、前記各要素(ベース部材231a、栓体部材231b及び冠体部材231c)を組み立てたことにより構築される口部材本体231について説明する。まず、図16に示す状態は、図15に示す状態から、冠体部材231cをベース部材231aに螺合することにより構築される。この螺合操作に従い、弾性部材である栓体部材231bは、冠体部材231cとベース部材231aとの間に挟まれ徐々に圧縮される。即ち、螺合するにつれ、弾性部材に付与される圧縮力が大きくなる。ここで、縦方向(図15の矢印方向)での圧縮に伴い、冠体部材231cは横方向に膨張しようとするが、横方向の膨張はベース部材231aの内壁231a2の存在により規制されるため、図16に示すように、抗力が生じない開口部231c1で冠体部材231cは凸状に露出する。ここで、図17は、図16の状態における、冠体部材231cとベース部材231a間に挟まれた栓体部材231bの応力分布図である。図17に示されるように、栓体部材231bには、特に冠体部材231c及びベース部材231aの当接部分において、弾性復元力に基づく応力が生じている。この応力に基づく高い気密性及び液密性が、口部材本体231を介しての外部からの空気侵入防止を担保すると共に、外部への液漏れ防止を担保する。
【0042】
次に、図18を参照しながら、本最良形態に係る薬液バッグの使用方法を説明する。はじめに、一端側が分析装置(不図示)に連通する薬液チューブの他端に設けられたプラスチック瓶針やステンレス針等の穿刺針Aを、栓体部材231bの凸部231b1に穿刺する。この際、薄膜状の底部231a3−1が穿孔し、その結果、穿刺針Aは薬液容器200の内部に到達する。これにより、上記薬液容器内の薬液が上記チューブを介して分析装置に導入される。
【0043】
本最良形態に係る薬液バッグは、前記性質に基づき、保存・使用時における、容器200内の薬液220への酸素混入を問題量以下まで低減させることが可能になる。したがって、極微量の酸素混入ですら偽結果をもたらす化学分析、例えば、半導体プロセスにおける洗浄液やプロセス液中の超微量金属を定量・半定量分析する際の薬液バッグとして有用である。
【0044】
次に、第三の最良形態に係る薬液バッグ300について詳述する。以下、図19〜図27を参照しながら、第三の最良形態に係る薬液バッグ300の構造について説明する。はじめに、図19は、本最良形態に係る薬液バッグ300の断面図を示した図である。薬液バッグ300は、シート状又はフィルム状の合成樹脂を貼り合わせて袋状に形成した容器310と、前記容器310内に収納された薬液320と、前記容器310をヒートシールする等により、気密的・液密的に当該容器310に固定された口部材330とから構成されている。以下、各要素について詳述する。
【0045】
まず、図19〜図26を参照しながら、第三の最良形態に係る口部材330の構造について説明する。はじめに、図19に示すように、口部材330は、口部材330を容器310の口部に取り付けた際、容器310内の薬液320を吸い出す取出口として機能する口部材本体331と、前記口部材本体331と一体化したフランジ部332とから構成される。ここで、図20及び図21は、夫々、図19の状態での口部材330の上面図及び側断面図である。図20及び図21から分かるように、略円筒状を成す口部材本体331は、後述するように、ベース部材331a、栓体部材331b及び冠体部材331cとから構成され、栓体部材331bがベース部材331aと冠体部材331cとにより圧縮状態を担保しながら挟まれた構造を採っている。加えて、口部材本体330の、容器310の口部に接続される側に、略偏平なフランジ部332が、ベース部材331aと一体形成されている。ここで、当該フランジ部332は、容器310の口部との取り付け部として機能する(当該フランジ部332の両側面が容器310の裏の両面と熱融着する)と共に、略偏平状である故、特にフランジ部332の端部における容器310同士の気密的・液密的なヒートシールを担保することが可能となる。
【0046】
次に、口部材本体331を構成する各要素(ベース部材331a、栓体部材331b及び冠体部材331c)について詳述する。尚、理解の容易上、まず、各要素を別々に説明し、次いでこれらを組み立てた際に構築される口部材本体331を説明する。はじめに、図22及び図23を参照しながら、ベース部材331aを詳述する。ここで、図22及び図23は、夫々、ベース部材331aの側断面図及び上面図である。まず、ベース部材331aは、円形の開口部331a1をその上面に有すると共に、円筒状の内壁331a2と円形の底面331a3が内部に形成されている。即ち、円柱状の空間331a5がベース部材331aの内部に形成されている。ここで、前記底面331a3は、円形の開口部331a3−1を更に有する。そして、外周面には、螺子状に切り込まれた螺子部331a4が設けられている。尚、当該螺子部331a4は、後述するように、冠体部材331cの内壁に形成された螺子係合部331c2(図24参照)と係合するよう機能する。
【0047】
次に、図24を参照しながら、栓体部材331bについて詳述する。ここで、図24は、冠体部材331cをベース部材331aに螺合する前の口部材330の状態を示した図である。栓体部材331bは、ベース部材331の内部に形成された空間331a5と略同一の径を成す円柱体である。但し、後述のように冠体部材331cとベース部材331aとで挟み込んだ際、栓体部材331に圧縮力が作用するよう、栓体部材331の高さは、前記空間331a5のそれよりも大きく設定されている(図24参照)。
【0048】
次に、図20及び図24を参照しながら、冠体部材331cについて詳述する。図20及び図24に示すように、円筒状を成す冠体部材331cは、中央部に開口部331c1を有すると共に、その内壁には螺子係合部331c2が形成されている。そして、冠体部材331cの裏面には、後述する取付時には、栓体部材331b上面の円周縁部に当接すると共に、当該当接部を介して、ベース部材331aの底面331a3と協働して栓体部材331に対して圧縮力を印加する、略平面の当接部331c3が形成されている。
【0049】
次に、図24〜図26を参照しながら、前記各要素(ベース部材331a、栓体部材331b及び冠体部材331c)を組み立てたことにより構築される口部材本体331について説明する。まず、図25に示す状態は、図24に示す状態から、冠体部材331cをベース部材331aに螺合することにより構築される。この螺合操作に従い、弾性部材である栓体部材331bは、冠体部材331cとベース部材331aとの間に挟まれ徐々に圧縮される。即ち、螺合するにつれ、弾性部材に付与される圧縮力が大きくなる。ここで、縦方向(図24の矢印方向)での圧縮に伴い、冠体部材331cは横方向に膨張しようとするが、横方向の膨張はベース部材331aの内壁331a2の存在により規制されるため、図25に示すように、抗力が生じない開口部331c1及び331a3−1で冠体部材331cは凸状に露出する。ここで、図26は、図25の状態における、冠体部材331cとベース部材331a間に挟まれた栓体部材331bの応力分布図である。図26に示されるように、栓体部材331bには、特に冠体部材331c及びベース部材331aの当接部分において、弾性復元力に基づく応力が生じている。この応力に基づく高い気密性及び液密性が、口部材本体331を介しての外部からの空気侵入防止を担保すると共に、外部への液漏れ防止を担保する。
【0050】
次に、図27を参照しながら、本最良形態に係る薬液バッグの使用方法を説明する。はじめに、一端側が分析装置(不図示)に連通する薬液チューブの他端に設けられたプラスチック瓶針やステンレス針等の穿刺針Aを、栓体部材331bの凸部331b1に穿刺する。そして、穿刺し続けると、穿刺針Aは開口部331a3−1から突出し、その結果、穿刺針Aは薬液容器300の内部に到達する。これにより、上記薬液容器内の薬液が上記チューブを介して分析装置に導入される。
【0051】
本最良形態に係る薬液バッグは、前記性質に基づき、保存・使用時における、容器300内の薬液320への酸素混入を問題量以下まで低減させることが可能になる。したがって、極微量の酸素混入ですら偽結果をもたらす化学分析、例えば、半導体プロセスにおける洗浄液やプロセス液中の超微量金属を定量・半定量分析する際の薬液バッグとして有用である。
【0052】
そこで、サンプル液中に含まれている分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムを例にとり、本最良形態に係る薬液バッグの好適な使用例を挙げる。ここで、このフロー分析(FA)とは、例えば、サンプルを流路内に流しておいて、連続的又は適当な間隔で薬液を注入し、当該反応液からの応答を検出し、前記サンプル内の分析対象物濃度を定量的に測定する手法である。図28を参照しながら説明すると、サンプル液導入部2(2)から導入されたサンプル液Sは、図示しないポンプにより連続的に流路内に送液される。そして、流路内にサンプル液Sが存在する状況下、限定された時間だけポンプ(図示せず)をシンクロ作動させることにより、発色液R(2)及び発色補助液{酸化液O(2)、緩衝液B(2)}が同時に流路内に注入される。これにより、流路内のある一部分だけサンプルと薬液が混合した状態となり、当該混合液が発色反応を起こす。そして、当該混合液は、やがて下流の測定部17(2)に到達し、ここで吸光度が測定される。他方、混合していない部分(即ち、サンプル液のみ)の吸光度も測定され、差Δに基づき、サンプル液中の分析対象物の濃度を決定する。
【0053】
また、フローインジェクション分析(FIA)とは、フロー分析の一種であり、流路にキャリア(試料を運ぶ流体)を流しておき、適時、キャリア中を分析試料に置きかえて、これら検出元素が発色する反応試薬と反応させて、キャリアの吸光度と分析試料の吸光度との差△を検出して元素濃度を分析する方法である。すなわち、FIAにおいては、キャリアと反応試薬を混合して、これを攪拌・分散等によってよく混ぜた後に、元素濃度を検出する検出器によって濃度検出(典型的には吸光度分析による吸光度の測定)を行うのであるが、キャリアをある時点において、試料に置き換えることによって、吸光度の差分を測定することによって試料濃度を測定するものである。尚、特開2004−163191号公報(特願2002−327720号)の内容は、本明細書に組み込まれるものとする。
【0054】
ここで、FIAの原理図を図29及び図30に示す。図29を参照すると、キャリアと反応試薬が定常的に攪拌混入され、検出器において測定対象元素の検出が行われる。このときに、キャリアに切り替えバルブを設けておき、適時、分析対象サンプルをキャリアと置換する。
【0055】
図30は、このような状態で検出される吸光度のチャートである。キャリアに対する吸光度測定時は空試験値として表されている。これに対し、分析対象サンプル(試料)は、空試験値からΔで表される分、吸光度特性に差分が観察される。この差分Δがすなわち、キャリア中に含まれる分析対象元素濃度(0であると推定される)と、サンプル中に含まれる分析対象元素濃度の差分による吸光度の差である。通常、Δは小さいので、これを100〜1000倍に拡大することによって、分析精度を向上させる手法が採用される。なお、吸光度の代わりに蛍光測定でもよく、この場合は発色試薬ではなく蛍光を発する試薬を用いる。
【0056】
また、FIAにおいては、キャリアと試料による吸光度の差分を電気的手法により増幅し、これによって、分析感度を高める方法がとられることもある。このためには、ノイズが小さく、安定したバックグラウンドが得られる反応系、装置等をクリアしなければならない。
【0057】
ここで、超高純度分析においては、検出対象となる元素が費消されて発色が生じる型の反応ではなく、検出対象となる元素が発色反応の触媒となり、それ自体は費消されることなく発色が生じる型(接触型)の反応を前提とすることが好ましい。かかる前提下においては、一定温度、一定時間、その他pHなどの一定条件下において、比較材(本明細書においてはキャリア)とサンプル材との反応を制御し、前者と後者とのS/N比を最適化した測定条件にて発色程度の測定を行うことにより感度のよい分析が可能となる。そして、一定条件下を実現するためには、分析に使用する容器の汚染度が一回ごとに異なるバッチ式の分析方法を採用するよりも、連続式の分析方法を採用する方が、様々な条件を分析毎に統一することができるので好ましい。本例においては、オンサイト型分析方法であるFAやFIAに接触型の反応試薬を適用することが好ましい。
【0058】
微量分析を実現するためには、測定環境からの汚染を防止することが重要である。検出対象元素が鉄のような一般的な元素の場合、大気中に浮遊していたり、用いる実験器具、容器、配管から混入する場合も考えられる。そのため、本例に係る測定システムは、外環境からなるべく閉鎖されたシステムであることが望ましい。
【0059】
さらに、S/N比を向上させるために、本例においては、比較材(キャリア)中に含まれる検出対象元素(不純物)の発色を低減させることが好ましい。
【0060】
これらの発想の一部又は全部を組み合わせて分析感度を高めた結果、pptオーダーの超高純度元素分析が可能となる。
【0061】
より具体的な例として第1例〜第14例を挙げる。
【0062】
第1例は、サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器が接続されている、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記試薬液が封入された密封容器として本発明に係る内容物収納容器を使用した、フロー分析システム又はフローインジェクション分析システムである。
【0063】
ここで、第1例の一態様は、サンプル液を流路内に導入するためのサンプル液導入部と、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器が接続されている、前記試薬液を前記流路内に導入するための試薬液導入部と、前記サンプル液導入部及び前記試薬液導入部より前記流路の下流に位置する、前記応答を測定するための応答測定部とを有し、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答と、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記試薬液が封入された密封容器が、本発明に係る内容物収納容器である、フロー分析システム又はフローインジェクション分析システムである。
【0064】
第2例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が更に接続されており、前記補助液が密封された密封容器が、本発明に係る内容物収納容器である、前記第1例のフロー分析システム又はフローインジェクション分析システムである。
【0065】
第2例の一態様は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入するための補助液導入部を更に有し、前記補助液が密封された密封容器が、本発明に係る内容物収納容器である、前記第1例のフロー分析システム又はフローインジェクション分析システムである。
【0066】
第3例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第3例のフロー分析システム又はフローインジェクション分析システムである。
【0067】
第4例は、前記密封容器に封入された状態の試薬液又は補助液中に含まれる酸素含有量が、5ppm以下である、前記第1例〜第3例のいずれか一つのフロー分析システム又はフローインジェクション分析システムである。
【0068】
第5例は、前記第1例〜第4例のいずれか一つのフロー分析システム又はフローインジェクション分析システムにおいて使用される、本発明に係る内容物収納容器である。
【0069】
第6例は、前記密封容器に封入された状態の試薬液又は補助液中に含まれる酸素含有量が、5ppm以下である、前記第5例の密封容器である。
【0070】
第7例は、サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)が接続されている、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下であるフロー分析システム又はフローインジェクション分析システムである。
【0071】
第7例の一態様は、サンプル液を流路内に導入するためのサンプル液導入部と、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)が接続されている、前記試薬液を前記流路内に導入するための試薬液導入部と、前記サンプル液導入部及び前記試薬液導入部より前記流路の下流に位置する、前記応答を測定するための応答測定部とを有し、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答と、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下であるフロー分析システム又はフローインジェクション分析システムである。
【0072】
第8例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入するための補助液導入部を更に有し、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下である、前記第7例のフロー分析システム又はフローインジェクション分析システムである。
【0073】
第9例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第8例のフロー分析システム又はフローインジェクション分析システムである。
【0074】
第10例は、前記試薬液又は前記補助液が封入された密封容器が、本発明に係る内容物収納容器である、前記第7例〜第9例のいずれか一つのフロー分析システム又はフローインジェクション分析システムである。
【0075】
第11例は、前記第7例〜第10例のいずれか一つのフロー分析システム又はフローインジェクション分析システムにおいて使用される、酸素含有量が5ppm以下の試薬液又は補助液が封入された密封容器である。
【0076】
第12例は、前記密封容器が、本発明に係る内容物収納容器である、前記第11例の密封容器である。
【0077】
第13例は、流路内を流れる第一の液に関する第一の応答と、前記流路内を流れる第二の液に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている分析対象元素を定量又は半定量的に測定可能なフロー分析システムであって、前記流路内を流れる前記第二の液が、前記試薬液による応答を抑制する作用を有する応答抑制物質を含有するフロー分析システム又はフローインジェクション分析システムである。
【0078】
第13例の一態様は、サンプル液を流路内に導入するためのサンプル液導入部と、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)が接続されている、前記試薬液を前記流路内に導入するための試薬液導入部と、前記サンプル液導入部及び前記試薬液導入部より前記流路の下流に位置する、前記応答を測定するための応答測定部とを有し、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答と、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システムであって、前記流路内を流れる第二の液が、前記試薬液による応答を抑制する作用を有する応答抑制物質を含有するフロー分析システム又はフローインジェクション分析システムである。
【0079】
第14例は、サンプル液を流路内に導入するステップと、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器から、前記試薬液を流路内に導入するステップと、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答を検出すると共に、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答を検出又は入力するステップとを有する、前記第一の応答と前記第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析方法又はフローインジェクション分析方法であって、前記試薬液が封入された密封容器が、本発明に係る内容物収納容器である、フロー分析方法又はフローインジェクション分析方法である。
【0080】
ここで、第二の液に関するベース値としての第二の応答は、正確さの観点からは、検出して取得することが好適であるが、通常、その値は第一の応答よりも低いので、規定値(例えば、過去の測定値に基づく平均値)として記録しておき、当該規定値を入力する形で取得してもよい。尚、以下の発明における「第二の応答を検出又は入力するステップ」という用語の意味も同様である。
【0081】
第15例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入ステップを更に有し、前記補助液が密封された密封容器が、本発明に係る内容物収納容器である、前記第14例のフロー分析方法又はフローインジェクション分析方法である。
【0082】
第16例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第14例のフロー分析方法又はフローインジェクション分析方法である。
【0083】
第17例は、前記密封容器に封入された状態の試薬液又は補助液中に含まれる酸素含有量が、5ppm以下である、前記第14例〜第16例のいずれか一つのフロー分析方法又はフローインジェクション分析方法である。
【0084】
第18例は、サンプル液を流路内に導入するステップと、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)から、前記試薬液を流路内に導入するステップと、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答を検出すると共に、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答を検出又は入力するステップとを有する、前記第一の応答と前記第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析方法又はフローインジェクション分析方法であって、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下であるフロー分析方法又はフローインジェクション分析方法である。
【0085】
第19例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入するための補助液導入部を更に有し、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下である、前記第18例のフロー分析方法又はフローインジェクション分析方法である。
【0086】
第20例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第19例のフロー分析方法又はフローインジェクション分析方法である。
【0087】
第21例は、前記試薬液又は前記補助液が封入された密封容器が、本発明に係る内容物収納容器である、前記第18例〜第20例のいずれか一つのフロー分析方法又はフローインジェクション分析方法である。
【0088】
第22例は、サンプル液を流路内に導入するステップと、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)から、前記試薬液を流路内に導入するステップと、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答を検出すると共に、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答を検出又は入力するステップとを有し、前記第一の応答と前記第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析方法又はフローインジェクション分析方法であって、前記流路内を流れる前記第二の液が、前記試薬液による応答を抑制する作用を有する応答抑制物質を含有するフロー分析方法又はフローインジェクション分析方法である。
【0089】
ここで、本例における各用語の意義について説明する。「サンプル液」とは、分析対象元素を含んでいるか否かが問題となる液をいい、例えば、各プロセス(例えば半導体洗浄プロセス)で使用するプロセス液(洗浄液)や、当該プロセス液の原液(新液)を挙げることができる。「検出可能な応答」とは、例えば、変色(例えば発色や減色)、光信号(例えば蛍光)、電気信号等を挙げることができ、検出可能である限り特に限定されない。「第一の液」とは、好適な応答反応条件の下、サンプル液中に存在する分析対象元素の存在により応答反応を起した液を指し、例えば、サンプル液と試薬液との混合液や、サンプル液と試薬液と補助液(例えば、酸化液、中和液、緩衝液、補触媒液等)との混合液を挙げることができる。「第二の液」とは、サンプル液を含有しない液や、サンプル液を含有していても第一の液と比較して応答反応を起し難い状態にある液を指し、例えば、サンプル液を含有しない液としては、例えば、キャリア液と試薬液の混合液や、キャリア液と試薬液と他の補助液(例えば、酸化液、緩衝液、補触媒液等)}との混合液を挙げることができ、サンプル液を含有していても第一の液と比較して応答反応を起し難い状態にある液としては、例えば、サンプル液のみ、応答反応に適したpH範囲にない状態のサンプル液と試薬液との混合液、応答反応に必要な補触媒が存在しない状態のサンプル液と試薬液との混合液を挙げることができる。「システム」とは、装置のみならずプラントのようなものも包含する概念であり、また、各構成要素が物理的に一体的又は集約的なもののみならず、各構成要素が物理的に分割しているものや分散しているものも包含する。「元素」とは、特に限定されず、例えば金属元素である。「フロー分析」とは、自動分析を含む流れ分析を意味し、フローインジェクション分析を包含する概念である。
【0090】
以下、本発明に係る内容物収納容器の適用例を更に具体的に説明する。尚、以下のシステム及び方法は、好適には、微量元素を測定対象とし、より好適には超微量元素を測定対象とする。ここで、「微量」とは、対象元素の含有量が10−7オーダー(ppb)以下である場合を指し、「超微量」とは、対象元素の含有量が10−8オーダー(サブppb)以下(より好適には10−9オーダー以下)である場合を指す。尚、下限値は特に制限されないが、通常、10−12オーダー(ppt)である。更に、以下のシステム及び方法は、オンサイト分析用に適しているが、オンサイト分析用に限定されるものではなく、これ以外の用途も適用可能であり、本発明の権利範囲に属する。
【0091】
まず、図31及び図32を参照しながら、第一の適用具体例(新液用モニター)について詳述する。ここで、「新液」とは、実際の洗浄時に使用されるプロセス液を作るための高濃度の原液であり、例えば、98%硫酸や29%アンモニア水である。図31は、当該FIAの各工程に係るフローチャート図である。図31に示すように、半導体工程等、分析対象となる薬品から、連続的に、又は、一定時間毎にサンプルを採取するサンプル採取工程(ステップ1)と、前記サンプル採取工程で採取されたサンプルを中和してpHを調整する中和工程(ステップ2)と、前記中和工程後のサンプルに、金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬を注入する発色試薬注入工程(ステップ3)と、前記発色試薬注入工程後のサンプルの吸光度を測定する吸光度測定工程(ステップ4)とを含む。以下、各工程について詳述する。
【0092】
(1)サンプル採取工程(S1)
サンプル採取工程S1は、被検出溶液たる薬品中からサンプルを採取する工程である。ここで、一定時間毎にサンプルを採取することが好適であり、更に、一定時間毎に一定量のサンプルを採取することがより好適である。尚、サンプル採取の具体的方法は特に限定されない。
【0093】
被検出溶液たる薬品としては、例えば、強酸、弱酸及び強アルカリ、弱アルカリ薬品のいずれであっても、金属の検出が可能である。具体的には、強酸薬品としては、塩酸、硫酸、硝酸、又はこれらを混合したものなど、弱酸薬品としては、酢酸、フッ酸、リン酸などを挙げることができる。また、強アルカリ薬品としては、水酸化カリウム溶液、水酸化ナトリウム溶液、水酸化テトラブチルアンモニウム、水酸化テトラメチルアンモニウム、又はこれらを混合したものなど、弱アルカリ薬品としては、アンモニア水などを挙げることができる。
【0094】
(2)中和工程(S2)
中和工程S2とは、採取したサンプルに中和剤を注入することにより中和させる工程である。尚、発熱反応による発泡現象を防止するために、中和工程を冷却下で行なったり、並びに/或いは、中和剤及び/又はサンプルを予め冷却しておくことが好適である。このような構成を採ることにより、中和剤の希釈度を低く抑えることが可能となる結果、感度上昇に繋がる。但し、本工程は、中和しないと測定ができない場合にのみ必要であり、中和しなくても測定可能なサンプルの場合には省略される。
【0095】
この中和工程S2において用いられる中和剤は、被検出溶液たる薬品の種類及びpHにより適宜選択して使用すればよい。例えば、被検出溶液が塩酸の場合には、アンモニア水や水酸化ナトリウムを好適に用いることができ、また被検出溶液が水酸化カリウムの場合には、塩酸や酢酸などを好適に用いることができる。尚、中和剤としては、金属を含有しないものを用いることが、感度上昇の観点から好適である。
【0096】
(3)発色試薬注入工程(S3)
発色試薬注入工程S3とは、中和されたサンプル中に、検出対象である金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬を注入する工程である。尚、本適用具体例では、吸光度測定法に基づいて測定を行なうため、分析試薬として発色試薬を選択したが、例えば、分析手法として蛍光測定法を選択した場合には、分析試薬として蛍光試薬を選択することになる。
【0097】
発色試薬は、検出しようとする金属に合わせて適宜選択する。例えば、薬品中の鉄を検出する場合には、発色試薬としてはN,N−ジメチル−p−フェニレンジアミンや還元体のマラカイトグリーン、メチレンブルーなどが好適であり、また、銅、マンガン、コバルトなどを検出する場合にも、これらの試薬が使用可能である。尚、分析対象金属に応じ、温度、pH、濃度などの条件を適宜変更する。
【0098】
具体的には、例えば、N,N-ジメチル-p-フェニレンジアミン、N,N-ジエチル-p-フェニレンジアミン、N-(p-メトキシフェニル)-p-フェニレンジアミン、N-(p-メトキシフェニル-N,N-ジメチル)-p-フェニレンジアミン、4−ヒドロキシベンズアルデヒドセミカルパゾン、N-フェニル-p-フェニレンジアミン、2-ニトロソ-5-(Nプロピル-N-スルホプロピルアミノ)フェノール、2-(5-ブロム-2-ピリジルアゾ)-5-(N-プロピル-N-スルホプロピルアミノ)アニリン、2-(5-ブロム-2-ピリジルアゾ)-5-(N-プロピル-N-スルホプロピルアミノ)フェノール、2-(5-ニトロ-2-ピリジルアゾ)-5-(N-プロピル-N-スルホプロピルアミノ)フェノールなどを挙げることができる。
【0099】
また、発色試薬注入工程S3において、前記発色試薬に加えて酸化剤(酸化液)や緩衝剤(緩衝液)を注入することもできる。使用される発色試薬は、酸化反応により発色を呈する試薬であるため、当該酸化反応を促進することにより感度を上げることができる。例えば、鉄イオンは、酸化剤である過酸化水素の酸化反応を促進する触媒として働くことができる。しかも、酸化剤である過酸化水素は、発色試薬と鉄(III)の酸化還元反応の化学量論量よりもかなり多量に加えられており、鉄(III)が消費され、鉄(II)が生成されると、過酸化水素により鉄(III)が再生される(鉄の触媒作用)。このような触媒作用を利用することにより、少量の測定対象物質(例えば鉄)が存在すれば、十分な酸化剤が存在し、時間を制限しなければ、無限に酸化反応は進行する。すなわち、酸化による生成物の発色を検出に利用する場合には、感度の大幅な向上が期待できる。しかし、生成物量が測定対象物質量と明瞭な相関関係(直線関係が好ましい)にあることが保障される測定装置、測定手法でなければならない。このためには、詳細な実験的裏付けが必須である。注入する酸化剤は、特に限定されないが、例えば、発色試薬として、N,N−ジメチル−p−フェニレンジアミンを用いた場合には、酸化剤としては過酸化水素が好適である。また、使用される緩衝剤は、当該発色強度が最も高くなるpH域に緩衝するものである限り特に限定されない。
【0100】
(4)吸光度測定工程(S4)
吸光度測定工程S4とは、前記発色試薬注入工程S3後のサンプルの吸光度を測定する工程であり、当該測定結果により被検出溶液たる薬品中に存在する金属を定量することができる。尚、本最良形態では、吸光度測定法に基づいて測定を行なうものを挙げたが、分析手法はこれに限定されず、例えば、蛍光測定法も採用可能である。
【0101】
吸光度測定の具体的な方法は特に限定されることなく、従来公知の検出装置などを用いることができる。また測定波長についても前記発色試薬により適宜設定すればよい。例えば、発色試薬としてN,N−ジメチル−p−フェニレンジアミンを用いた場合には、測定波長は510nm〜530nm付近である。
【0102】
以下、図32を参照しながら、半導体製造工程を例にとり、本適用具体例をより詳細に説明する。半導体製造工程の場合、使用される薬液は強酸・強アルカリであり、取扱がきわめて難しいという問題がある。また、例えば、濃硫酸の場合は、濃度が極めて高いので中和が必要であるが、中和すると不純物元素の濃度も低下するので、一層の検出感度が必要となる。
【0103】
また、半導体製造工程の配管の多くは、鉄系素材に四フッ化樹脂などの耐薬品性樹脂をライニングしたものなどからなり、このライニング樹脂の破れなどの欠陥は、鉄などの金属汚染の原因となっている。したがって、濃硫酸を対象として、検出対象元素を鉄(Fe)とした例を以下に説明する。しかし、本発明において、試薬等鉄固有の条件要素ではない部分は、他の金属元素を微量分析する場合にも適用可能であり、本明細書において鉄を適用具体例として説明するからといって、他の元素に対する適用が否定されたり、本願発明の権利範囲が限定されると解釈されてはならない。
【0104】
図32に示す検出装置は、フローインジェクション分析装置の一種であり、半導体製造工程において使用される薬品から、一定時間毎にサンプルを採取するサンプル採取手段2と、前記サンプル採取手段2により採取されたサンプルと、当該サンプルを中和してpHを調整するための中和試薬とを混合して、当該サンプルを中和する中和手段3と、前記中和手段により中和されたサンプルと、金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬と酸化剤を所定の割合で混合して、発色反応を起こさせる反応手段4と、前記反応装置により発色反応を呈したサンプルの吸光度を測定する吸光光度測定手段5とを少なくとも含む。
【0105】
まず、サンプル採取手段2は、半導体製造工程において使用される薬品が流通する薬品流通管50に設けられており、当該薬品流通管50から一定時間毎に一定量のサンプルSを採取する。
【0106】
そして、サンプル採取手段2により採取されたサンプルは、サンプル流通管5に流入される。サンプル流通管5は、中和手段3として機能する中和管7に接続されている。
【0107】
中和試薬Nは、本発明に係る内容物収納容器(薬液バック又は試薬バック)8aに封入されており、当該試薬バック8aが接続されている中和試薬流通管9により前記中和管7に注入される。このように中和試薬Nをはじめ、本発明の装置において使用される試薬を本発明に係る内容物収納容器に封入して使用することにより、装置外部から不純物が混入することを防止することができ、より感度の高い分析を行うことができる。
【0108】
中和手段3にかかる中和管7に流入されたサンプルと中和試薬Nは、中和管7を流通する間に中和される。この際、中和管7に流入されるサンプルの流量、および中和試薬Nの流量を適宜調節することにより簡便に再現性よく中和をすることができる。
【0109】
中和管7は、自動切り替えバルブBに接続されている。当該自動切り替えバルブBには、一定量のサンプルを保持することができるサンプル計量管10を設けてある。
【0110】
切り替えバルブBには、キャリア流通管11が接続されている。当該キャリア流通管11の端部にはキャリアCを封入するための試薬バック8bが接続されている。
【0111】
キャリアCをキャリア流通管11に流入せしめながら、適当なタイミングで自動切り替えバルブBを切り替えることにより、キャリアCはサンプル保持管10内に流入する。その結果サンプル保持管10内に保持されたサンプルはキャリアCによって押し出されて、反応手段4にかかる反応管12へ流入する。
【0112】
反応手段4の上流側には、当該反応管に金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬Rを封入した試薬バッグ8cに接続された発色試薬流通管13、酸化剤Oを封入した試薬バッグ8dに接続された酸化剤流通管14、および緩衝溶液Bを封入した試薬バッグ8eに接続された緩衝溶液流通管15が接続されている。
【0113】
反応管4は、サンプルSまたはキャリアCに、発色試薬R、酸化剤O、および必要に応じて用いられる緩衝溶液Bをそれぞれ混合し、酸化反応を促進する。フローインジェクション分析装置においては、当該反応管12の長さを調節することにより反応時間をコントロールすることが出来る。また、当該反応管12(特に下流側)を温度調節器16内に設けることにより、反応温度を調節することも可能である。
【0114】
上述したように各試薬は、それぞれ試薬バック8a〜8eに封入されていることが好ましい。
【0115】
更に、それぞれの流通管には、試薬の流量を調節する機構が設けられている(図示せず)。したがって、それぞれの流通管を流れる溶液のpHや濃度等により、それぞれの流通管の流量を調節することによって、発色試薬が最も発色し易い条件を容易に作り出すことができる。
【0116】
反応管12は、吸光光度測定手段である吸光光度計17に接続されている。吸光光度計17は、サンプルSまたはキャリアCの吸光度を測定する。吸光度が測定されたサンプルは排出管18より排出される。
【0117】
上記説明においては、中和剤、酸化剤、緩衝剤の順序でサンプルに対して適用しているが、この順序については発色を実現するものであれば特にこだわるものではない。
【0118】
次に、図28及び図33を参照しながら、第二の適用具体例(プロセス液用モニター)について説明する。ここで、「プロセス液」とは、新液を希釈して実際の洗浄に使用される液を意味し、例えば過酸化水素等が添加されているものである(例えば、36%塩酸:30%過酸化水素:超純水=1:5:400)。まず、図31は、当該FAの各工程に係るフローチャート図である。図31に示すように、まず、ステップ11でサンプルを採取する。この際、FIAと異なり、サンプルは採取し続け、基本的には常に流路内に流れている状態となる。次に、ステップ12で、発色試薬(及び場合により酸化剤や緩衝剤)をある期間注入する。その結果、発色試薬が注入されたサンプル部分は、発色反応を起こし得る状態となる。そして、ステップ13で、当該発色試薬が注入されたサンプル部分と、当該発色試薬が注入されていないサンプル部分の両方について吸光度を測定する。
【0119】
次に、図28は、本具体例に係る装置の概略図である。ここで、第一適用具体例(FIA)との相違点は、キャリア液が存在しない点、サンプル液が流路内を流れ続ける点、及び、発色試薬(及び酸化剤や緩衝剤のような補助液)がある期間シンクロしてサンプル液に注入される点である。それ以外は、第一適用具体例と同一であり、同一機能を有する部材の番号の後に「(2)」を付している。相違点について説明すると、サンプル液導入部2(2)は、洗浄流路100(2)から継続的にサンプル液Sを採取し、図示しないポンプにより流路5(2)内にサンプル液Sを流し続ける。そして、酸化液O(2)、試薬液R(2)及び緩衝液B(2)は、図示しないポンプをシンクロ作動させることにより、ある期間、サンプル液S内にこれら試薬液や補助液を同時注入する。
【0120】
前記第一適用具体例(FIA)及び前記第二適用具体例(FA)のような検出装置において、その検出感度は、検出バックグランド値とサンプルピーク値との差分であるΔを大きくすることによって向上する。FAやFIAによる検出感度を上げるための工夫としては大きく分けると以下の二つのアプローチがあり得る。
【0121】
第一は、検出バックグランドを低下させることにより、ノイズを小さく安定させ、微少なΔを大きくし、またはこれを拡大して正確に測定する方法である。第二は、検出対象元素の発色効率を向上させることによって、サンプルピークを実質的に大きくし、S/N比を向上することによってΔを大きくする方法である。
【0122】
本発明においては、それぞれのアプローチに関して、以下の手法を採用した。
【0123】
検出バックグランドは、主として(1)流路において、分析サンプル以外から検出対象元素が混入すること、(2)検出対象元素以外の元素に発色剤が反応して発色が生じること、によって上昇する。本例においては、この二つの要因を低下させることによって、検出バックグランドの低下を図る。
【0124】
まず、(1)については、分析サンプル以外からの検出対象元素の混入量を低減するとともに、バックグランドを構成するキャリア液中に分析対象元素の発色を抑制する物質(発色抑制物質)を混入することによって解決した。
【0125】
本例によれば、試薬バッグ8bに封入されたキャリアCの中にかかる発色抑制物質を混入する。発色抑制物質としては、通常のキレート試薬、例えば、エチレンジアミン四酢酸、エチレングリコールビス(2−アミノエチル)エーテルジアミン四酢酸、ジエチレントリアミン五酢酸、トリエチレンテトラミン六酢酸その他の塩、ピロリン酸の無機錯化剤などが考えられる。
【0126】
発色抑制物質の濃度は、10-13M(mol/l)〜10-3M(mol/l)が好ましい。10-13M(mol/l)未満であると発色抑制の効果が低下し、10-3M(mol/l)以上入れてもそれ以上の効果がないからである。
【0127】
発色抑制物質をキャリア中に入れることにより、キャリアにかかる検出バックグランドが低下し、ノイズが小さくなり、バックグランドが安定するので微少なΔも拡大して正確に測定できる。よって、相対的にサンプルの検出レベルとの差異Δが大きくなるので、検出感度が向上する。
【0128】
尚、当該発色抑制物質は、キャリア中だけでなく、試薬液や他の補助液(例えば、酸化液、緩衝液、中和液)に入れてもよい。
【0129】
また、上記(2)の点について、本発明者は、FAやFIAでサブppbオーダー乃至pptオーダーで測定を行なう際に、最も重要な偽発色原因物質が酸素であることを見出した。更に、FAやFIAで高感度な超微量分析を可能にする上で、所定値以下の酸素透過性(酸素透過度)のバックで各種薬剤(特に発色剤溶液)を封入することが重要であることも見出した。具体的には、当該バッグの酸素透過度は、25℃で相対湿度80%において、10fmol/m2.s.Pa(2cc/m2・d・atm)以下であることが重要であり、5fmol/m2・s・Pa(1cc/m2・d・atm)以下であることが好適であり、2.5fmol/m2・s・Pa(0.5cc/m2・d・atm)以下であることがより好適である。
【0130】
更に、口部材の栓体部材が、内部で上下左右方向から圧縮された状態にある結果、当該栓体部材とベース部材及び冠体部とで協働し、高い気密・液密性が担保されている。そして、冠体部材の開口部に弾性部材の凸部が形成されているので、当該部分に針を刺した場合でも、強力な圧縮力が働き、当該部分で極めて高い気密・液密性が保証される。
【0131】
以上の工夫を施したバッグに薬剤を封入することにより、FAやFIAでサブppbオーダー乃至pptオーダーで測定を行なう際に従来問題となっていた、発色液の保管・運搬中における発色剤の発色を、本目的を達成するために問題とならない程度まで抑制できる。更に、発色剤溶液のみならず、他の補助剤(キャリア、酸化剤、中和剤、緩衝剤)も同様のバッグに封入することにより、発色剤と混合した際の偽発色も抑制できる。ここで、前記バッグに各種液を封入するに際し、これら薬剤を十分に脱気してから封入する必要があることはいうまでもない。
【0132】
また、別の手段(又は前記手段との組み合わせ)として、本発明者らは、FAやFIAでサブppbオーダー乃至pptオーダーで測定を行なう際、液中に僅かにでも存在する気泡が大きな問題となることを発見した。当該発見に基づき、鋭意検討した結果、各種液(特に発色液)中の酸素含有量が、5ppm以下に維持することが好適であることを見出した。ここで、5ppm以下に維持する手法としては、例えば、減圧して溶存酸素を除去する手法を挙げることができる。
【0133】
なお、本明細書における数値を規定するにあたって、酸素含有量については、例えば、溶存酸素測定法(JIS K 0400−32−30)に記載された水質―溶存酸素の定量―電気化学プローブ法による。また、酸素透過率については、例えば、JIS K7126に記載のプラスチックフィルム及びシートの気体透過度試験方法により測定することができる。
【0134】
次に、検出精度を高めるための第二のアプローチについて述べる。
【0135】
検出精度を高めるためには、サンプル中に含まれる検出対象元素の触媒効果がもっとも発現反応しやすい条件となり、発色に寄与することが望ましい。検出対象元素がFeであり、発色剤がN,N−ジメチル−p−フェニレンジアミンの場合、発色反応を呈するためには、好ましくは、pH3.0乃至9.0に一定時間維持することが望ましい。このような維持は、吸光度測定器に連接された恒温層において、または、吸光度測定器の直前において実現されることが好ましい。
【実施例】
【0136】
実施例1{FIA法(鉄分析)}
まず、図34を参照しながら、本実施例に係る装置及び分析方法について説明する。サンプルSと中和液NSの送液にはCavro Scientific Instruments,Inc.製CavroXL3000モジュラー・デジタル・ポンプ(1”h、1”v)を用いた。サンプルSとしては、5種類の97%(18.2mol/l)硫酸(鉄濃度=0、30、60、80、100ppt)を300μl用い、流量50μl/minで流した。中和液NSとしては、密封容器(酸素透過度:0.8cc/m2・d・atm)に封入されている2.85%(1.65mol/l)のアンモニア水(酸素含有量:2.5ppm)を5500μl用い、流量916.7μl/minで流した。キャリア液CS、酸化剤OS、発色試薬液RS,緩衝液BSの送液には、旭テクネイオン株式会社製APZ−2000ダブルプランジャーポンプ1”bを用いた。キャリア液CSとしては、密封容器(詳細情報が必要)に封入されている0.97mol/lの硫酸アンモニウム水溶液(酸素含有量:2.5ppm)を用い、流量0.8ml/minで流した。また、キャリア中には発色を抑える抑制剤として10−6mol/lのエチレンジアミン四酢酸を混ぜている。酸化液OSには、密封容器(詳細情報が必要)に封入されている0.3%の過酸化水素水(酸素含有量:2.5ppm)を用い、流量0.8ml/minで流した。発色試薬液RSには、密封容器(詳細情報が必要)に封入されている4mmol/lのN,N−ジメチル−p−フェニレンジアミン(酸素含有量:2.5ppm)を用い流量0.5ml/minで流した。緩衝液BSには、密封容器(詳細情報が必要)に封入されている1.3mol/lの酢酸アンモニウム水溶液(酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。サンプル計量管(インジェクションバルブ1”i)には、内径0.8mm、長さ160cmのチューブを用いた。中和管(冷却部1”g)で中和された液、酸化液OS、発色試薬液RS、緩衝液BSを、内径0.8mm、長さ2mの反応管で混合した。この混合液を温度調節器1”kで35℃に保った。そして、空冷部1”qを介した後、この着色溶液の吸光度を検出器(吸光光度計1”m)により最大吸収波長514nmで測定を行った。流路構成には内径0.8mmのチューブを用いた。
【0137】
図35に、上記方法で濃硫酸中における30ppt乃至100pptの濃度の鉄を測定した場合の検量線を示す。なお、この例においては、発色反応を呈するためにpHを5.5に維持した。この結果、図35に示すように、Blankと表示されたキャリアにおける発色と30ppt乃至100pptの濃度の鉄を含んだサンプルとの間には、発色度に応じた差Δ(キャリアの発色度とサンプルの発色度との差)が観察された。また、図36にΔと鉄濃度との相関を示す。図36に示すように、この相関は、良好な直線関係を示しており、本発明にかかる方法によって、pptオーダーの鉄が測定可能であることが立証された。
【0138】
実施例2{FA法(鉄、銅及び各種元素分析)}
まず、図37を参照しながら、本実施例に係る装置及び分析方法について説明する。サンプルSの送液には旭テクネイオン株式会社製APZ−2000の2連式プランジャーポンプ1hを用いた。サンプルSとしては、以下の表に示す所定量の金属を添加した0.01M塩酸を300μl用い、流量50μl/minで流した。
【表1】

酸化液OS、発色試薬液RS及び緩衝液BSの送液には、シリンジポンプ1bを用いた。酸化液OSには、密封容器(詳細情報が必要)に封入されている0.3%の過酸化水素水(酸素含有量:2.5ppm)を用い、流量0.8ml/minで流した。発色試薬液RSには、密封容器(詳細情報が必要)に封入されている4mmol/lのN,N−ジメチル−p−フェニレンジアミン(酸素含有量:2.5ppm)を用い流量0.5ml/minで流した。緩衝液BSには、密封容器(詳細情報が必要)に封入されている1.3mol/lの酢酸アンモニウム水溶液(酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。尚、これら3個のシリンジポンプ1bは、流れるサンプルSの同じ場所にすべてが注入されるよう、相互にシンクロして作動させた。サンプルS、酸化液OS、発色試薬液RS,緩衝液BSは、内径0.8mm、長さ2mの反応管で混合した。この混合液を温度調節器1kで35℃に保った。この着色溶液の吸光度を検出器(吸光光度計)1mにより最大吸収波長514nmで測定を行った。流路構成には内径0.8mmのチューブを用いた。
【0139】
尚、濃度決定の際には、検量線を作成する必要があるため、標準液SSやブランク液BLSが、インジェクションバルブ1iによりサンプル液Sと切替可能に構成されている。尚、図19は、サンプル液Sと標準液SSやブランク液BLSとの切替をインジェクションバルブ1iで行なう態様であるが、図38に、切替弁1’wで切替を行なう態様を示す。
【0140】
結果を図39〜図42及び表2に示す。図39は、波長514nmにおける鉄1ppbの吸光度ピークを示すチャートである。図40は、波長514nmにおける銅1ppbの吸光度ピークを示すチャートである。図41は、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。図42は、波長514nmにおける吸光度と銅濃度との関係を示す検量線である。図39及び図40に示されるように、検出バックグラウンドが十分に低下しているので、ppbオーダーでも、検出バックグランド値とサンプルピーク値との差分であるΔが大きくなった。尚、鉄の感度は銅の3倍近くであることが確認された。また、図41及び図42に示されるように、鉄及び銅のいずれに関しても、相関定数が0.999程度と、ppbオーダーでも極めて高い相関関係を示すことが確認された。更に、表2に示されるように、鉄(1ppb)+銅(1ppb)を添加した場合には、吸光度(0.0860)は、鉄1ppbに基づく吸光度(0.0652)と銅1ppbに基づく吸光度(0.0208)とを合計した値となり、鉄と銅の総量を測定できることが確認された。更に、鉄+銅+他の金属(すべて1ppb)を添加した場合、測定された吸光度(0.0857)は、ほぼ鉄+銅(1ppb)の吸光度(0.0860)と同程度であることから、他の金属の影響は無視できることが確認された。
【表2】

【0141】
実施例3{FIA法(鉄分析)}
まず、図34を参照しながら、本実施例に係る装置及び分析方法について説明する。尚、本実施例に関しては、中和液を用いないので、図34中の「NS」及びそのラインは存在しないものとする。サンプルSの送液にはCavro Scientific Instruments,Inc.製CavroXL3000モジュラー・デジタル・ポンプ(1”h、1”v)を用いた。サンプルSとしては、APM液(29% アンモニア:30%過酸化水素:超純水=1:5:400)に鉄を0、0.5、1.0ppb加えたものを0.8ml用いた。キャリア液CS、酸化液OS、発色試薬液RS、緩衝液BSの送液には、旭テクネイオン株式会社製APZ−2000ダブルプランジャーポンプ1”bを用いた。キャリア液CSとしては、密封容器(詳細情報が必要)に封入されている0.037 M (0.071 %) アンモニア+0.11 M (0.37 %) 過酸化水素(pH 10.86)を用い、流量0.8ml/minで流した。酸化液OSには、密封容器(詳細情報が必要)に封入されている0.88 M (3.0 %) 過酸化水素+0.05 M (0.15 %) 塩酸(pH 1.26)を用い(酸素含有量:2.5ppm)、流量0.8ml/minで流した。発色試薬液RSには、密封容器(詳細情報が必要)に封入されている4 mM (0.084%)のN,N−ジメチル−p−フェニレンジアミン(DPD,pH 1.87)(酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。緩衝液BSには、密封容器(詳細情報が必要)に封入されている1.3mol/lの酢酸アンモニウム水溶液(pH6.34、酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。サンプル計量管(インジェクションバルブ1”i)には、内径0.8mm、長さ160cmのチューブを用いた。流路を流れるキャリア液S又はサンプル液と、酸化液OS、発色試薬液RS及び緩衝液BSとを、内径0.8mm、長さ2mの反応管で混合した。この混合液を温度調節器1”kで35℃に保った。そして、空冷部1”qを介した後、この着色溶液の吸光度を検出器(吸光光度計1”m)により最大吸収波長514nmで測定を行った。流路構成には内径0.8mmのチューブを用いた。
【0142】
結果を図43に示す。図43は、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。図43に示されるように、調製当日は鉄の濃度に比例して吸光度が増加し、鉄1 ppbで吸光度0.032を示しているので、塩酸中の鉄などと同程度の充分な感度が得られることが分かった。以上の結果から、希薄APM液中の鉄の測定でも、塩酸中の鉄と同程度の感度で得られたので、希薄APM液中の鉄を中和等の前処理工程を経ず、充分な感度で定量出来ることが判明した。
【0143】
本明細書においては、pptオーダーの微量元素を分析することを前提として記述したが、本願発明はppbオーダーの元素分析にも適用可能である。かかる場合も本発明の射程範囲内であり、その権利範囲が及ぶことは当然である。
【0144】
本明細書の最良形態及び実施例においては、発色反応を前提として説明を行ったが、蛍光反応を前提としても本発明を適用可能である。この場合、発色試薬ではなく、サンプル及びキャリアに含まれる分析対象元素の濃度に応じて蛍光光度が変化する蛍光物質(蛍光試薬)を用いる。また、キャリア中に加える物質としては、発色抑制物質の代わりに、蛍光反応を抑制する物質を添加すればよい。
【図面の簡単な説明】
【0145】
【図1】本最良形態に係る薬液バッグの断面図である。
【図2】本最良形態に係る薬液バッグの、口部材の上面図である。
【図3】本最良形態に係る薬液バッグの、口部材の側断面図である。
【図4】本最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の側断面図である。
【図5】本最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の上面図である。
【図6】本最良形態に係る薬液バッグの、冠体部材装着前の口部材の側断面図である。
【図7】本最良形態に係る薬液バッグの、口部材の側断面図である。
【図8】本最良形態に係る薬液バッグの、口部材内の栓体部材の応力分布図であ る。
【図9】使用時における、本最良形態に係る薬液バッグの断面図である。
【図10】第二の最良形態に係る薬液バッグの断面図である。
【図11】第二の最良形態に係る薬液バッグの、口部材の上面図である。
【図12】第二の最良形態に係る薬液バッグの、口部材の側断面図である。
【図13】第二の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の側断面図である。
【図14】第二の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の上面図である。
【図15】第二の最良形態に係る薬液バッグの、冠体部材装着前の口部材の側断面図である。
【図16】第二の最良形態に係る薬液バッグの、口部材の側断面図である。
【図17】第二の最良形態に係る薬液バッグの、口部材内の栓体部材の応力分布図である。
【図18】使用時における、第二の最良形態に係る薬液バッグの断面図である。
【図19】第三の最良形態に係る薬液バッグの断面図である。
【図20】第三の最良形態に係る薬液バッグの、口部材の上面図である。
【図21】第三の最良形態に係る薬液バッグの、口部材の側断面図である。
【図22】第三の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の側断面図である。
【図23】第三の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の上面図である。
【図24】第三の最良形態に係る薬液バッグの、冠体部材装着前の口部材の側断面図である。
【図25】第三の最良形態に係る薬液バッグの、口部材の側断面図である。
【図26】第三の最良形態に係る薬液バッグの、口部材内の栓体部材の応力分布図である。
【図27】使用時における、第三の最良形態に係る薬液バッグの断面図である。
【図28】本適用具体例にかかるFA装置を模式的に示した図である。
【図29】本適用具体例にかかるFIA測定装置を簡略的に示した図である。
【図30】本適用具体例にかかるFIA測定原理を示す測定チャートである。
【図31】本適用具体例にかかるFIA測定ステップを示すフロー図である。
【図32】本適用具体例に用いられるFIA装置を模式的に示した図である。
【図33】本適用具体例にかかるFA測定ステップを示すフロー図である。
【図34】実施例1及び実施例3における、FIA装置を模式的に示した図である。
【図35】実施例1における、濃硫酸中の微量鉄を測定したときのデータ図である。
【図36】実施例1における、濃硫酸中の微量鉄を測定したときの鉄濃度と発色度との相関を示すデータ図である。
【図37】実施例2における、FA装置を模式的に示した図である。
【図38】図37のFA装置の変更態様を模式的に示した図である。
【図39】実施例2における、波長514nmでの鉄1ppbの吸光度ピークを示すチャートである。
【図40】実施例2における、波長514nmでの銅1ppbの吸光度ピークを示すチャートである。
【図41】実施例2における、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。
【図42】実施例2における、波長514nmにおける吸光度と銅濃度との関係を示す検量線である。
【図43】実施例3における、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。
【図44】従来の口部材の側断面図である。
【図45】従来の弾性部材の上面図及び側断面図である。
【符号の説明】
【0146】
1 FA装置、1b シリンジポンプ、1c 混合器、1d 洗浄水切替弁、1e 気液分離器、1f サンプル入口弁、1g 冷却器(ラジエター)、1h 2連式プランジャーポンプ、1i インジェクションバルブ、1j 標準液切替弁、1k 恒温槽、1m 吸光光度計、1n チェック弁、1p シリンジポンプ、1r エア抜き電磁弁、1s 廃液、1t エアトラップ(外付け)、1x 洗浄水導入部、1y サンプル導入部、1z サンプル排出部、2 検出薬カートリッジ(保冷庫)
【0147】
1’ FA装置、1’b シリンジポンプ、1’c 混合器、1’d 洗浄水切替弁、1’e 気液分離器、1’f サンプル入口弁、1’g 冷却器(ラジエター)、1’h 2連式プランジャーポンプ、1’j 標準液切替弁、1’k 恒温槽、1’m 吸光光度計、1’n チェック弁、1’p シリンジポンプ、1’r エア抜き電磁弁、1’s 廃液、1’t エアトラップ(外付け)、1’w 標準液切替弁、1’x 洗浄水導入部、1’y サンプル導入部、1’z サンプル排出部、2’ 検出薬カートリッジ(保冷庫)
【0148】
1” FA装置、1”b プランジャーポンプ、1”f サンプル入口弁、1”g 冷却器(ラジエター)、1”h サンプルポンプ、1”i インジェクションバルブ、1”j サンプル吸引弁、1”k 恒温槽、1”m 吸光光度計、1”n チェック弁、1”p シリンジポンプ、1”r エア抜き電磁弁、1”s 廃液、1”t エアトラップ(外付け)、1”u 線浄水ポンプ、1”v 中和液ポンプ、1”x 洗浄水導入部、1”y サンプル導入部、1”z サンプル排出部、2” 検出薬カートリッジ(保冷庫)
【技術分野】
【0001】
本発明は、例えば、分析システムにおいて使用される薬液バッグに適用可能な、気密性・液密性に優れた口部材及びそれを用いた内容物収納容器に関する。
【背景技術】
【0002】
近年、様々な分野で、極微量成分の定量又は半定量分析技術が検討されている。例えば、半導体の製造工程においては、Siウエハの洗浄その他の洗浄工程、露光・現像工程、エッチング工程において、様々な薬液が用いられる。これらの薬液に金属不純物が混入している場合、サブppb乃至pptオーダーであっても、製品性能・歩留まりに深刻な悪影響を及ぼすことがあるので、当該濃度の不純物測定は極めて重要である。
【0003】
更に、前記薬液の分析は、(1)各薬液毎にサンプルを採取し、(2)別の場所の分析室等において、濃縮等のバッチ方式でのみ適用できる方法で検出感度を高める処理を行った後、(3)ICP-MS(Inductively coupled plasma-mass spectrometer:誘導結合プラズマ質量分析)などの高感度分析方法に委ねていた。このような方法では、試料濃縮などの処理が必要なために、分析結果が出るまでに最短でも一日程度要し、その結果、薬液の不純物濃度が高いと判断された場合は、それにかかる製品をすべて廃棄するなどの無駄を生じ、結果として、歩留まりの低下を引き起こしていた。加えて、前記手法では、サンプルが測定されるまでの間、濃縮プロセス等の複数の工程を介在させるので、汚染の機会が増え、必ずしも超微量分析に適した手法とはいえない。そこで、微量の金属元素をオンサイトで分析する手法として、フロー分析(フローインジェクション分析)を適用する手法が提案されている(特許文献1)。この手法によれば、サンプルがリアルタイムかつ自動的に反応系に導かれるので、汚染の危険性が相当低減される。
【0004】
ここで、フロー分析は、溶液バッグを用いることにより、完全閉鎖系測定システムとすることが可能で、測定環境からの汚染を遮断することができる。これに加え、測定後、瞬時に測定結果が得られ、手軽に持ち運びでき、更には装置調整も簡単なことから、オンサイト分析が可能である。そのため、例えば、半導体の製造工程中に設置し、その結果を半導体製造工程に直ちに反映できる。ここで、測定環境からの汚染防止の観点からは、溶液バックを如何に密閉系にできるかが重要であり、当該密閉を担う一部材が、収容体の開口部を閉塞するように取着され収容体中の液体の出入れに利用される口部材(スパウト)である。ここで、図44及び図45に従来の薬液バッグに使用されている口部材の一例を示す(特許文献1)。この口部材1は、弾性体15が封入される内部空間7を具備し、収容物吸出し用の液路6に連通する口部8と、この口部8を覆うように装着可能であり、収容物吸出し用の針が差し込まれる冠体20と、を有し、前記冠体20には、冠体20を前記口部8に装着した際に前記内部空間7に封入された弾性体15を押圧して、弾性体15を前記口部8の内周壁に付勢する押圧部22が形成されている。ここで、図45に示すように、弾性体15は、矢印方向から押圧した場合に全体的に半径方向に膨らむように、軸方向に膨らんだ形状に構成されている。そして、弾性体15は、内部空間7の径よりも僅かに小さいため、内部空間7に容易に封入することができる。
【特許文献1】特許第2519871号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
ここで、上記口部材は、冠体部材の押圧により弾性体を口部内周壁に付勢するという構成を採っているので、口部の径よりも大きな径を有するゴムを封入することによりゴム自体に強い押圧力を付与する構成と比較すると、作製工程が容易であるという優れた利点があるものの、他方で、弾性体の材質や形状等によっては、中心領域に向かっての押圧力が不十分になり、針を刺した状態での気密性及び液密性又は針を抜いた状態での気密性及び液密性が担保できないという問題がある。更に、上記口部材を使用するに際しては、上部から穿刺針を膜体22aに突き刺す操作を行なうが、この際、当該突き刺しにより切断した膜体22aの一部が該針内に侵入することが多々あり、偽結果の原因となったり分析装置の故障の原因になることが危惧されている。
【課題を解決するための手段】
【0006】
本発明者らは、上記課題を解決するために鋭意研究した結果、本発明(1)〜(8)を完成させたものである。
【0007】
本発明(1)は、弾性体から構成される栓体部材(栓体部材131b〜331b)と、
前記栓体部材(栓体部材131b〜331b)が挿入可能な第一開口部(開口部131a1〜331a1)が形成されており、かつ、当該開口部(開口部131a1〜331a1)から挿入された前記栓体部材(栓体部材131b〜331b)を収納可能な内部空間(内部空間131a5〜331a5)が形成されたベース部材(ベース部材131a〜331a)と、
前記ベース部材(ベース部材131a〜331a)の前記第一開口部(開口部131a1〜331a1)を覆うように前記ベース部材(ベース部材131a〜331a)に装着可能な、前記第一開口部(開口部131a1〜331a1)よりも小さく設定された第二開口部(開口部131c1〜331c1)を有する冠体部材(冠体部材131c〜331c)と、
を備えた口部材(口部材130〜330)であって、
前記栓体部材(栓体部材131b〜331b)が前記内部空間(内部空間131a5〜331a5)に装着された状態で前記冠体部材(冠体部材131c〜331c)を前記ベース部材(ベース部材131a〜331a)に嵌合した際、前記栓体部材(栓体部材131b〜331b)は、前記冠体部材(冠体部材131c〜331c)及び前記ベース部材(ベース部材131a〜331a)の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記内部空間(内部空間131a5〜331a5)を形成する内壁(内壁131a2〜331a2)からも圧縮力を受ける一方、前記圧縮力による弾性変形の結果、前記栓体部材(栓体部材131b〜331b)の一部(凸部131b1〜331b1)が前記第二開口部(開口部131c1〜331c1)から凸状に露出する口部材(口部材130〜330)である。
【0008】
本発明(2)は、前記装着が、冠体部材(冠体部材231c、冠体部材331c)と前記ベース部材(ベース部材231a、ベース部材331a)との螺合により達成されると共に、前記螺合の程度に応じて、前記圧縮力が可変するよう構成されている、前記発明(1)の口部材(口部材230、口部材330)である。
【0009】
本発明(3)は、前記ベース部材(ベース部材331a)が、前記第一開口部(開口部331a1)とは反対側に、前記第一開口部(開口部331a1)よりも小さく設定された第三開口部(開口部331a3−1)を更に有しており、
前記栓体部材(栓体部材331b)が前記内部空間(内部空間331a5)に収納された状態で前記冠体部材(冠体部材331c)を前記ベース部材(ベース部材331a)に装着した際、前記栓体部材(栓体部材331b)は、前記冠体部材(冠体部材331c)及び前記ベース部材(ベース部材331a)の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記栓体部材(栓体部材331b)の一部が前記第三開口部(開口部331a3−1)から凸状に露出するよう構成されている、前記発明(1)又は(2)の口部材(口部材330)である。
【0010】
本発明(4)は、前記発明(1)〜(3)のいずれか一つの口部材を備えた内容物収納容器(口部材130〜330)である。
【0011】
本発明(5)は、前記内容物が化学分析用薬液である、前記発明(4)の内容物収納容器(薬液バッグ100〜300)である。
【0012】
本発明(6)は、前記化学分析がフロー分析である、前記発明(5)の内容物収納容器(薬液バッグ100〜300)である。
【0013】
本発明(7)は、前記内容物が酸素易変性成分を含有する、前記発明(4)〜(6)のいずれか一つの内容物収納容器(薬液バッグ100〜300)である。
【0014】
本発明(8)は、前記収納容器が酸素バリア性素材から構成されている、前記発明(7)の内容物収納容器(薬液バッグ100〜300)である。
【発明の効果】
【0015】
本発明(1)によれば、上方向から栓体部材を圧縮すると共に、当該圧縮による弾性変形に基づく横方向の変形を規制した結果、横方向から間接的に圧縮される構成を採った上で、冠体部材に開口部を設けたことにより、応力が集中する凸部が形成される。その結果、従来の圧縮型で問題となっていた、針を刺した状態での気密性及び液密性並びに針を抜いた状態での気密性及び液密性がより確実に保証できるという効果を奏する。更には、冠体部材に開口部が設けられているので、従来冠体部材の膜体を突き破る際に問題となり得る、冠体部材由来の膜体による悪影響を回避することができるという効果も奏する。
【0016】
本発明(2)によれば、前記効果に加え、どのような材質の栓体部材を採用しても、螺合の程度を変更することにより、最適な圧縮力を前記栓体部材に与えることが可能になる。その結果、栓体部材の材質を変更しても、ベース部材や冠体部材の形状等を変更する必要がないので、製造コストを顕著に低減できるという効果を奏する。加えて、使用日数の経過につれて穿刺針の突き刺し部分から液漏れが生じた場合であっても、螺合の程度を変更することにより、当該液漏れの問題を解消することができるという効果も奏する。更には、螺合の程度を適宜調整することにより、どのような材質の栓体部材を採用しても、破断した栓体部材が針の内部に侵入することも防止することができる。その結果、偽結果や分析装置の故障を未然に防止することが可能になるという効果も奏する。
【0017】
本発明(3)によれば、前記効果に加えて、ベース部材の底部に開口部が設けられているので、従来ベース部材の底部の膜体を突き破る際に問題となった、ベース部材由来の膜体による悪影響を回避することができるという効果も奏する。
【0018】
本発明(4)〜(8)も前記効果と同じ効果を奏する。尚、保存時・使用時とも高い気密性・液密性を担保できるので、特に、酸素が極微量でも容器内に侵入すると分析結果に悪影響を及ぼすような場合(特に、サブppb乃至pptオーダーといった超微量分析の場合)に有効である。
【発明を実施するための最良の形態】
【0019】
以下、図1〜図9を参照しながら、最良形態として薬液バッグを例にとり、本発明の第一の最良形態について説明する。尚、本発明の権利範囲は、以下の最良形態に限定されるものではない。即ち、上記最良形態は、あくまでも例示であり、本発明の特許請求の範囲に記載された技術的思想と実質的に同一な構成を有し、同様な作用効果を奏するものは、いかなるものであっても本発明の権利範囲に包含される。例えば、本発明に係る口部材を輸液バックに使用する場合も本発明の権利範囲内である。
【0020】
はじめに、本最良形態に係る薬液バッグ100の構造について説明する。まず、図1は、本最良形態に係る薬液バッグ100の断面図を示した図である。薬液バッグ100は、シート状又はフィルム状の合成樹脂を貼り合わせて袋状に形成した容器110と、前記容器110内に収納された薬液120と、前記容器110をヒートシールする等により、気密的・液密的に当該容器110に固定された口部材130とから構成されている。以下、各要素について詳述する。
【0021】
まず、図1〜図8を参照しながら、本最良形態に係る口部材130の構造について説明する。はじめに、図1に示すように、口部材130は、口部材130を容器110の口部に取り付けた際、容器110内の薬液120を吸い出す取出口として機能する略円筒状の口部材本体131と、前記口部材本体131と一体化したフランジ部132とから構成される。ここで、図2及び図3は、夫々、図1の状態での口部材130の上面図及び側断面図である。図2及び図3から分かるように、略円筒状を成す口部材本体131は、後述するように、ベース部材131a、栓体部材131b及び冠体部材131cとから構成され、栓体部材131bがベース部材131aと冠体部材131cとにより圧縮状態を保ちながら挟まれた構造を採っている。加えて、口部材130の、容器110の口部に接続される側に、略菱形状のフランジ部132が、ベース部材131aと一体形成されている。ここで、当該フランジ部132は、容器110の口部との取り付け部として機能する(当該フランジ部132の四側面が容器110裏の両面と熱融着する)と共に、菱形状である故、特にフランジ部132の両端部における容器110同士の気密的・液密的なヒートシールを担保することが可能となる。
【0022】
次に、口部材本体131を構成する各要素(ベース部材131a、栓体部材131b及び冠体部材131c)について詳述する。尚、理解の容易上、まず、各要素を別々に説明し、次いでこれらを組み立てた際に構築される口部材本体131を説明する。はじめに、図4及び図5を参照しながら、ベース部材131aを詳述する。ここで、図4(1)、図4(2)及び図5は、夫々、ベース部材131aの側断面図、側面図及び上面図である。まず、ベース部材131aは、円形の開口部131a1をその上面に有すると共に、円筒状の内壁131a2と円形の底面131a3が内部に形成されている。即ち、円柱状の空間131a5がベース部材131aの内部に形成されている。ここで、前記底面131a3の一部(131a3−1)は、使用の際に穿刺針を突き刺した際に貫通可能な程度の厚さに設定されている(例えば、0.5mm程度の膜状)。そして、ベース部材131aの上部外周面には、フランジ状の凸部131a4が形成されている。尚、当該凸部131a4は、後述するように、冠体部材131cの内壁に形成された円周状の凹部131c2(図6参照)と嵌合するよう機能する。
【0023】
次に、図6を参照しながら、栓体部材131bについて詳述する。ここで、図6は、冠体部材131cをベース部材131aに嵌合する前の口部材130の状態を示した図である。栓体部材131bは、ベース部材131の内部に形成された空間131a5と略同一の径を成す円柱体である。但し、後述のように冠体部材131cとベース部材131aとを嵌合した際、両者の挟み込みにより栓体部材131bに圧縮力が作用するよう、栓体部材131の高さは、前記空間131a5のそれよりも大きく設定されている(図6参照)。
【0024】
次に、図2及び図6を参照しながら、冠体部材131cについて詳述する。図2及び図6に示すように、円筒状を成す冠体部材131cは、中央部に開口部131c1を有すると共に、その内壁には円周状の凹部131c2が形成されている。そして、冠体部材131cの裏面には、後述する嵌合時には、栓体部材131b上面の円周縁部に当接すると共に、当該当接部を介して、ベース部材131aの底面131a3と協働して栓体部材131bに対して圧縮力を印加する、略平面の当接部131c3が形成されている。
【0025】
次に、図6〜図8を参照しながら、前記各要素(ベース部材131a、栓体部材131b及び冠体部材131c)を組み立てたことにより構築される口部材本体131について説明する。まず、図7に示す状態は、図6に示す状態から、冠体部材131cをベース部材131aに嵌合することにより構築される。この嵌合操作により、弾性部材である栓体部材131bは、冠体部材131cとベース部材131aとの間に挟まれ圧縮される。ここで、縦方向(図6の矢印方向)での圧縮に伴い、冠体部材131cは横方向に変形しようとするが、横方向の変形はベース部材131aの内壁131a2の存在により規制されるため、横方向からも圧縮される。更に、図7に示すように、栓体部材131bの一部(131b1)が、抗力が生じない開口部131c1に逃げる結果、開口部131c1から凸状に露出する。ここで、図8は、図7の状態における、冠体部材131cとベース部材131a間に挟まれた栓体部材131bの応力分布図である。図8に示されるように、栓体部材131bには、特に冠体部材131c及びベース部材131aの当接部分において、弾性復元力に基づく応力が生じている。この応力に基づく高い気密性及び液密性が、口部材本体131を介しての外部からの空気侵入防止を担保すると共に、外部への液漏れ防止を担保する。
【0026】
次に、図1を参照しながら、本最良形態に係る容器110を説明する。本容器110は、最内層がシーラント層である2枚の積層体を三方ヒートシールして得られた袋体である。ここで、当該袋体は、収納した薬液の量に追従して変形可能であり、薬液の量が減少するに従い扁平状に変形する。
【0027】
次に、上記各要素の材質等について説明する。まず、口部材130を構成する要素の内、栓体部材131b以外の要素(口部材本体131、フランジ部132、冠体部材131c)は、例えば、従来公知の種々のプラスチックを用いて形成可能である。特に熱可塑性樹脂を用いたときは、口部材本体等を射出成形によって簡易に形成することができる。具体的には、ポリエチレン、ポリプロピレン、ポリ4−メチルペンテン〔例えば、三井化学(株)の商品名「TPX」〕、ポリテトラフルオロエチレン等のポリオレフィン;エチレン−テトラシクロドデセン共重合体〔例えば、三井化学(株)の商品名「アペル」〕等のポリ環状オレフィン;ポリアセタール(POM);アクリロニトリル−ブタジエン−スチレン共重合体(ABS);ポリエチレンナフタレート(PEN)、ポリエチレンテレフタレート(PET)、ポリアリレート等のポリエステル;ポリフェニレンサルファイド(PPS)等のベンゼン系重合体等が挙げられる。
【0028】
次に、口部材130を構成する要素の内、弾性体である栓体部材131bは、例えば、従来公知の種々のゴムやエラストマー(例えば、ブチルゴムやSBR等の加硫ゴム)を用いて形成することができる。具体的には、天然ゴム、シリコーンゴム等のゴムや、スチレン系エラストマー(例えば、スチレン−ブタジエン系、スチレン−イソプレン系及びこれらに水素添加物)、オレフィン系エラストマー、ポリウレタン系エラストマー等の熱可塑性エラストマーを挙げることができる。加えて、特に限定されないが、例えば、そのJIS硬度は、40〜55度程度、肉厚は約1〜10mm程度、直径は15〜20mm程度の短円柱状のものが使用可能である。尚、当該栓体部材131bは、例えば熱可塑性エラストマーを用いたときは、射出成形によって形成可能である。
【0029】
次に、容器110を構成する積層体は、好適には、酸素透過度(25℃×80%RH)が10fmol/m2s・Pa以下のガスバリア性素材からなる。ここで、ガスバリア性素材としては、プラスチック基材の表面に、酸化珪素、酸化アルミニウム、酸化マグネシウム、その他等の無機酸化物を使用し、真空蒸着法、スパッタリング法又はイオンプレ−ティング法等の物理気相成長法(PVD法)、或いは、プラズマ化学気相成長法、熱化学気相成長法又は光化学気相成長法等の化学気相成長法(CVD法)等を利用して、その無機酸化物の蒸着薄膜を形成してなる透明ガスバリア性フィルムが好適である。
【0030】
ここでまず、プラスチック基材としては、無機酸化物の蒸着薄膜を設ける点で、物理的及び化学的に優れた強度及び耐熱性を有することが好適である。具体的には、当該プラスチック基材としては、例えば、ポリエチレン系樹脂、ポリプロピレン系樹脂、環状ポリオレフィン系樹脂、フッ素系樹脂、ポリスチレン系樹脂、アクリロニトリル−スチレン共重合体(AS樹脂)、アクリロニトリル−ブタジエン−スチレン共重合体(ABS樹脂)、ポリ塩化ビニル系樹脂、フッ素系樹脂、ポリ(メタ)アクリル系樹脂、ポリカ−ボネ−ト系樹脂、ポリエチレンテレフタレ−ト、ポリエチレンナフタレ−ト等のポリエステル系樹脂、各種のナイロン等のポリアミド系樹脂、ポリイミド系樹脂、ポリアミドイミド系樹脂、ポリアリ−ルフタレ−ト系樹脂、シリコ−ン系樹脂、ポリスルホン系樹脂、ポリフェニレンスルフィド系樹脂、ポリエ−テルスルホン系樹脂、ポリウレタン系樹脂、アセタ−ル系樹脂、セルロ−ス系樹脂、その他等の各種の樹脂のフィルム又はシ−トを挙げることができる。尚、膜厚は、6〜100μmが好適であり、9〜50μmがより好適である。
【0031】
次に、最内層に形成されるシーラント層としては、例えば、熱によって溶融し相互に融着し得る各種のヒ−トシ−ル性を有するポリオレフィン系樹脂が好適である。具体的には、例えば、低密度ポリエチレン、中密度ポリエチレン、高密度ポリエチレン、直鎖状(線状)低密度ポリエチレン、メタロセン触媒を使用して重合したエチレン−α・オレフィン共重合体、ポリプロピレン、エチレン−酢酸ビニル共重合体、アイオノマ−樹脂、エチレン−アクリル酸共重合体、エチレン−アクリル酸エチル共重合体、エチレン−メタクリル酸共重合体、エチレン−メタクリル酸メチル共重合体、エチレン−プロピレン共重合体、メチルペンテンポリマ−、ポリブテンポリマ−、ポリエチレンまたはポリプロピレン等のポリオレフィン系樹脂をアクリル酸、メタクリル酸、マレイン酸、無水マレイン酸、フマ−ル酸、イタコン酸等の不飽和カルボン酸で変性した酸変性ポリオレフィン樹脂、ポリ酢酸ビニル系樹脂、ポリ(メタ)アクリル系樹脂、ポリ塩化ビニル系樹脂、熱可塑性ポリエステル系樹脂、ポリアミド系樹脂等を挙げることができる。尚、当該層の厚さは、5〜200μmであることが好適であり、10〜100μmがより好適である。
【0032】
尚、積層材を形成する材料として、その他、例えば、水蒸気や水等のバリア−性を有する低密度ポリエチレン、中密度ポリエチレン、高密度ポリエチレン、直鎖状低密度ポリエチレン、ポリプロピレン、エチレン−プロピレン共重合体等の樹脂のフィルム又はシ−ト、或いは、酸素や水蒸気等に対するバリア−性を有するポリ塩化ビニリデン系樹脂、ポリビニルアルコ−ル系樹脂、エチレン−ビニルアルコ−ル共重合体、MXDポリアミド系樹脂、ポリナフタレンテレフタレ−ト系樹脂等の樹脂のフィルム又はシ−トの一種又はそれ以上を組み合わせて使用してもよい。尚、当該フィルム又はシ−トの厚さは、特に限定されないが、5μm〜300μmが好適であり、10μm〜100μmがより好適である。
【0033】
次に、本最良形態に係る薬液バッグの性質を説明する。前記のように、薬液バッグ100は、容器110が酸素透過度(25℃×80%RH)が10fmol/m2s・Pa以下の素材から構成されている。加えて、口部材130の栓体部材131bが、内部で上下左右方向から圧縮された状態にある結果、当該栓体部材131bとベース部材131a及び冠体部材131cとで協働し、高い気密・液密性が担保されている。そして、冠体部材131cの開口部に弾性部材の凸部が形成されているので、当該部分に針を刺した場合でも、強力な圧縮力が働き、当該部分で極めて高い気密・液密性が保証される。
【0034】
次に、図9を参照しながら、本最良形態に係る薬液バッグの使用方法を説明する。はじめに、一端側が分析装置(不図示)に連通する薬液チューブの他端に設けられたプラスチック瓶針やステンレス針等の穿刺針Aを、栓体部材131bの凸部131b1に穿刺する。この際、薄膜状の底部131a3−1が穿孔し、その結果、穿刺針Aは薬液容器100の内部に到達する。これにより、上記薬液容器内の薬液が上記チューブを介して分析装置に導入される。
【0035】
以下、次に、図面を参照しながら、本発明の第二の最良形態及び第三の最良形態について説明する。ここで、第一の最良形態と第二の最良形態及び第三の最良形態との相違点は、冠体をベース部材に装着する態様が、前者が嵌合であるのに対し、後者は螺合である点である。更に、第二の最良形態と第三の最良形態との相違点は、前者が栓体部材下が膜状であるのに対し、後者が栓体部材下に開口部が設けられている点である。以下、第一の最良形態との相違部分について説明する。
【0036】
はじめに、図10〜図18を参照しながら、第二の最良形態に係る薬液バッグ200の構造について説明する。まず、図10は、本最良形態に係る薬液バッグ200の断面図を示した図である。薬液バッグ200は、シート状又はフィルム状の合成樹脂を貼り合わせて袋状に形成した容器210と、前記容器210内に収納された薬液220と、前記容器210をヒートシールする等により、気密的・液密的に当該容器210に固定された口部材230とから構成されている。以下、各要素について詳述する。
【0037】
まず、図10〜図17を参照しながら、第二の最良形態に係る口部材230の構造について説明する。はじめに、図10に示すように、口部材230は、口部材230を容器210の口部に取り付けた際、容器210内の薬液220を吸い出す取出口として機能する口部材本体231と、前記口部材231と一体化したフランジ部232とから構成される。ここで、図11及び図12は、夫々、図10の状態での口部材230の上面図及び側断面図である。図11及び図12から分かるように、略円筒状を成す口部材本体231は、後述するように、ベース部材231a、栓体部材231b及び冠体部材231cとから構成され、栓体部材231bがベース部材231aと冠体部材231cとにより圧縮状態を担保しながら挟まれた構造を採っている。加えて、口部材本体230の、容器210の口部に接続される側に、略偏平なフランジ部232が、ベース部材231aと一体形成されている。ここで、当該フランジ部232は、容器210の口部との取り付け部として機能する(当該フランジ部232の両側面が容器210裏の両面と熱融着する)と共に、略偏平状である故、特にフランジ部232の両端部における容器210同士の気密的・液密的なヒートシールを担保することが可能となる。
【0038】
次に、口部材本体231を構成する各要素(ベース部材231a、栓体部材231b及び冠体部材231c)について詳述する。尚、理解の容易上、まず、各要素を別々に説明し、次いでこれらを組み立てた際に構築される口部材本体231を説明する。はじめに、図13及び図14を参照しながら、ベース部材231aを詳述する。ここで、図13及び図14は、夫々、ベース部材231aの側断面図及び上面図である。まず、ベース部材231aは、円形の開口部231a1をその上面に有すると共に、円筒状の内壁231a2と円形の底面231a3が内部に形成されている。即ち、円柱状の空間231a5がベース部材231aの内部に形成されている。ここで、前記底面231a3の一部(231a3−1)は、使用の際に穿刺針を突き刺した際に貫通可能な程度の厚さに設定されている(例えば、0.5mm程度の膜状)。そして、外周面には、螺子状に切り込まれた螺子部231a4が設けられている。尚、当該螺子部231a4は、後述するように、冠体部材231cの内壁に形成された螺子係合部231c2(図15参照)と係合するよう機能する。
【0039】
次に、図15を参照しながら、栓体部材231bについて詳述する。ここで、図15は、冠体部材231cをベース部材231aに螺合する前の口部材230の状態を示した図である。栓体部材231bは、ベース部材231の内部に形成された空間231a5と略同一の径を成す円柱体である。但し、後述のように冠体部材231cとベース部材231aとで挟み込んだ際、栓体部材231に圧縮力が作用するよう、栓体部材231の高さは、前記空間231a5のそれよりも大きく設定されている(図15参照)。
【0040】
次に、図11及び図15を参照しながら、冠体部材231cについて詳述する。図11及び図15に示すように、円筒状を成す冠体部材231cは、中央部に開口部231c1を有すると共に、その内壁には螺子係合部231c2が形成されている。そして、冠体部材231cの裏面には、後述する取付時には、栓体部材231b上面の円周縁部に当接すると共に、当該当接部を介して、ベース部材231aの底面231a3と協働して栓体部材231に対して圧縮力を印加する、略平面の当接部231c3が形成されている。
【0041】
次に、図15〜図17を参照しながら、前記各要素(ベース部材231a、栓体部材231b及び冠体部材231c)を組み立てたことにより構築される口部材本体231について説明する。まず、図16に示す状態は、図15に示す状態から、冠体部材231cをベース部材231aに螺合することにより構築される。この螺合操作に従い、弾性部材である栓体部材231bは、冠体部材231cとベース部材231aとの間に挟まれ徐々に圧縮される。即ち、螺合するにつれ、弾性部材に付与される圧縮力が大きくなる。ここで、縦方向(図15の矢印方向)での圧縮に伴い、冠体部材231cは横方向に膨張しようとするが、横方向の膨張はベース部材231aの内壁231a2の存在により規制されるため、図16に示すように、抗力が生じない開口部231c1で冠体部材231cは凸状に露出する。ここで、図17は、図16の状態における、冠体部材231cとベース部材231a間に挟まれた栓体部材231bの応力分布図である。図17に示されるように、栓体部材231bには、特に冠体部材231c及びベース部材231aの当接部分において、弾性復元力に基づく応力が生じている。この応力に基づく高い気密性及び液密性が、口部材本体231を介しての外部からの空気侵入防止を担保すると共に、外部への液漏れ防止を担保する。
【0042】
次に、図18を参照しながら、本最良形態に係る薬液バッグの使用方法を説明する。はじめに、一端側が分析装置(不図示)に連通する薬液チューブの他端に設けられたプラスチック瓶針やステンレス針等の穿刺針Aを、栓体部材231bの凸部231b1に穿刺する。この際、薄膜状の底部231a3−1が穿孔し、その結果、穿刺針Aは薬液容器200の内部に到達する。これにより、上記薬液容器内の薬液が上記チューブを介して分析装置に導入される。
【0043】
本最良形態に係る薬液バッグは、前記性質に基づき、保存・使用時における、容器200内の薬液220への酸素混入を問題量以下まで低減させることが可能になる。したがって、極微量の酸素混入ですら偽結果をもたらす化学分析、例えば、半導体プロセスにおける洗浄液やプロセス液中の超微量金属を定量・半定量分析する際の薬液バッグとして有用である。
【0044】
次に、第三の最良形態に係る薬液バッグ300について詳述する。以下、図19〜図27を参照しながら、第三の最良形態に係る薬液バッグ300の構造について説明する。はじめに、図19は、本最良形態に係る薬液バッグ300の断面図を示した図である。薬液バッグ300は、シート状又はフィルム状の合成樹脂を貼り合わせて袋状に形成した容器310と、前記容器310内に収納された薬液320と、前記容器310をヒートシールする等により、気密的・液密的に当該容器310に固定された口部材330とから構成されている。以下、各要素について詳述する。
【0045】
まず、図19〜図26を参照しながら、第三の最良形態に係る口部材330の構造について説明する。はじめに、図19に示すように、口部材330は、口部材330を容器310の口部に取り付けた際、容器310内の薬液320を吸い出す取出口として機能する口部材本体331と、前記口部材本体331と一体化したフランジ部332とから構成される。ここで、図20及び図21は、夫々、図19の状態での口部材330の上面図及び側断面図である。図20及び図21から分かるように、略円筒状を成す口部材本体331は、後述するように、ベース部材331a、栓体部材331b及び冠体部材331cとから構成され、栓体部材331bがベース部材331aと冠体部材331cとにより圧縮状態を担保しながら挟まれた構造を採っている。加えて、口部材本体330の、容器310の口部に接続される側に、略偏平なフランジ部332が、ベース部材331aと一体形成されている。ここで、当該フランジ部332は、容器310の口部との取り付け部として機能する(当該フランジ部332の両側面が容器310の裏の両面と熱融着する)と共に、略偏平状である故、特にフランジ部332の端部における容器310同士の気密的・液密的なヒートシールを担保することが可能となる。
【0046】
次に、口部材本体331を構成する各要素(ベース部材331a、栓体部材331b及び冠体部材331c)について詳述する。尚、理解の容易上、まず、各要素を別々に説明し、次いでこれらを組み立てた際に構築される口部材本体331を説明する。はじめに、図22及び図23を参照しながら、ベース部材331aを詳述する。ここで、図22及び図23は、夫々、ベース部材331aの側断面図及び上面図である。まず、ベース部材331aは、円形の開口部331a1をその上面に有すると共に、円筒状の内壁331a2と円形の底面331a3が内部に形成されている。即ち、円柱状の空間331a5がベース部材331aの内部に形成されている。ここで、前記底面331a3は、円形の開口部331a3−1を更に有する。そして、外周面には、螺子状に切り込まれた螺子部331a4が設けられている。尚、当該螺子部331a4は、後述するように、冠体部材331cの内壁に形成された螺子係合部331c2(図24参照)と係合するよう機能する。
【0047】
次に、図24を参照しながら、栓体部材331bについて詳述する。ここで、図24は、冠体部材331cをベース部材331aに螺合する前の口部材330の状態を示した図である。栓体部材331bは、ベース部材331の内部に形成された空間331a5と略同一の径を成す円柱体である。但し、後述のように冠体部材331cとベース部材331aとで挟み込んだ際、栓体部材331に圧縮力が作用するよう、栓体部材331の高さは、前記空間331a5のそれよりも大きく設定されている(図24参照)。
【0048】
次に、図20及び図24を参照しながら、冠体部材331cについて詳述する。図20及び図24に示すように、円筒状を成す冠体部材331cは、中央部に開口部331c1を有すると共に、その内壁には螺子係合部331c2が形成されている。そして、冠体部材331cの裏面には、後述する取付時には、栓体部材331b上面の円周縁部に当接すると共に、当該当接部を介して、ベース部材331aの底面331a3と協働して栓体部材331に対して圧縮力を印加する、略平面の当接部331c3が形成されている。
【0049】
次に、図24〜図26を参照しながら、前記各要素(ベース部材331a、栓体部材331b及び冠体部材331c)を組み立てたことにより構築される口部材本体331について説明する。まず、図25に示す状態は、図24に示す状態から、冠体部材331cをベース部材331aに螺合することにより構築される。この螺合操作に従い、弾性部材である栓体部材331bは、冠体部材331cとベース部材331aとの間に挟まれ徐々に圧縮される。即ち、螺合するにつれ、弾性部材に付与される圧縮力が大きくなる。ここで、縦方向(図24の矢印方向)での圧縮に伴い、冠体部材331cは横方向に膨張しようとするが、横方向の膨張はベース部材331aの内壁331a2の存在により規制されるため、図25に示すように、抗力が生じない開口部331c1及び331a3−1で冠体部材331cは凸状に露出する。ここで、図26は、図25の状態における、冠体部材331cとベース部材331a間に挟まれた栓体部材331bの応力分布図である。図26に示されるように、栓体部材331bには、特に冠体部材331c及びベース部材331aの当接部分において、弾性復元力に基づく応力が生じている。この応力に基づく高い気密性及び液密性が、口部材本体331を介しての外部からの空気侵入防止を担保すると共に、外部への液漏れ防止を担保する。
【0050】
次に、図27を参照しながら、本最良形態に係る薬液バッグの使用方法を説明する。はじめに、一端側が分析装置(不図示)に連通する薬液チューブの他端に設けられたプラスチック瓶針やステンレス針等の穿刺針Aを、栓体部材331bの凸部331b1に穿刺する。そして、穿刺し続けると、穿刺針Aは開口部331a3−1から突出し、その結果、穿刺針Aは薬液容器300の内部に到達する。これにより、上記薬液容器内の薬液が上記チューブを介して分析装置に導入される。
【0051】
本最良形態に係る薬液バッグは、前記性質に基づき、保存・使用時における、容器300内の薬液320への酸素混入を問題量以下まで低減させることが可能になる。したがって、極微量の酸素混入ですら偽結果をもたらす化学分析、例えば、半導体プロセスにおける洗浄液やプロセス液中の超微量金属を定量・半定量分析する際の薬液バッグとして有用である。
【0052】
そこで、サンプル液中に含まれている分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムを例にとり、本最良形態に係る薬液バッグの好適な使用例を挙げる。ここで、このフロー分析(FA)とは、例えば、サンプルを流路内に流しておいて、連続的又は適当な間隔で薬液を注入し、当該反応液からの応答を検出し、前記サンプル内の分析対象物濃度を定量的に測定する手法である。図28を参照しながら説明すると、サンプル液導入部2(2)から導入されたサンプル液Sは、図示しないポンプにより連続的に流路内に送液される。そして、流路内にサンプル液Sが存在する状況下、限定された時間だけポンプ(図示せず)をシンクロ作動させることにより、発色液R(2)及び発色補助液{酸化液O(2)、緩衝液B(2)}が同時に流路内に注入される。これにより、流路内のある一部分だけサンプルと薬液が混合した状態となり、当該混合液が発色反応を起こす。そして、当該混合液は、やがて下流の測定部17(2)に到達し、ここで吸光度が測定される。他方、混合していない部分(即ち、サンプル液のみ)の吸光度も測定され、差Δに基づき、サンプル液中の分析対象物の濃度を決定する。
【0053】
また、フローインジェクション分析(FIA)とは、フロー分析の一種であり、流路にキャリア(試料を運ぶ流体)を流しておき、適時、キャリア中を分析試料に置きかえて、これら検出元素が発色する反応試薬と反応させて、キャリアの吸光度と分析試料の吸光度との差△を検出して元素濃度を分析する方法である。すなわち、FIAにおいては、キャリアと反応試薬を混合して、これを攪拌・分散等によってよく混ぜた後に、元素濃度を検出する検出器によって濃度検出(典型的には吸光度分析による吸光度の測定)を行うのであるが、キャリアをある時点において、試料に置き換えることによって、吸光度の差分を測定することによって試料濃度を測定するものである。尚、特開2004−163191号公報(特願2002−327720号)の内容は、本明細書に組み込まれるものとする。
【0054】
ここで、FIAの原理図を図29及び図30に示す。図29を参照すると、キャリアと反応試薬が定常的に攪拌混入され、検出器において測定対象元素の検出が行われる。このときに、キャリアに切り替えバルブを設けておき、適時、分析対象サンプルをキャリアと置換する。
【0055】
図30は、このような状態で検出される吸光度のチャートである。キャリアに対する吸光度測定時は空試験値として表されている。これに対し、分析対象サンプル(試料)は、空試験値からΔで表される分、吸光度特性に差分が観察される。この差分Δがすなわち、キャリア中に含まれる分析対象元素濃度(0であると推定される)と、サンプル中に含まれる分析対象元素濃度の差分による吸光度の差である。通常、Δは小さいので、これを100〜1000倍に拡大することによって、分析精度を向上させる手法が採用される。なお、吸光度の代わりに蛍光測定でもよく、この場合は発色試薬ではなく蛍光を発する試薬を用いる。
【0056】
また、FIAにおいては、キャリアと試料による吸光度の差分を電気的手法により増幅し、これによって、分析感度を高める方法がとられることもある。このためには、ノイズが小さく、安定したバックグラウンドが得られる反応系、装置等をクリアしなければならない。
【0057】
ここで、超高純度分析においては、検出対象となる元素が費消されて発色が生じる型の反応ではなく、検出対象となる元素が発色反応の触媒となり、それ自体は費消されることなく発色が生じる型(接触型)の反応を前提とすることが好ましい。かかる前提下においては、一定温度、一定時間、その他pHなどの一定条件下において、比較材(本明細書においてはキャリア)とサンプル材との反応を制御し、前者と後者とのS/N比を最適化した測定条件にて発色程度の測定を行うことにより感度のよい分析が可能となる。そして、一定条件下を実現するためには、分析に使用する容器の汚染度が一回ごとに異なるバッチ式の分析方法を採用するよりも、連続式の分析方法を採用する方が、様々な条件を分析毎に統一することができるので好ましい。本例においては、オンサイト型分析方法であるFAやFIAに接触型の反応試薬を適用することが好ましい。
【0058】
微量分析を実現するためには、測定環境からの汚染を防止することが重要である。検出対象元素が鉄のような一般的な元素の場合、大気中に浮遊していたり、用いる実験器具、容器、配管から混入する場合も考えられる。そのため、本例に係る測定システムは、外環境からなるべく閉鎖されたシステムであることが望ましい。
【0059】
さらに、S/N比を向上させるために、本例においては、比較材(キャリア)中に含まれる検出対象元素(不純物)の発色を低減させることが好ましい。
【0060】
これらの発想の一部又は全部を組み合わせて分析感度を高めた結果、pptオーダーの超高純度元素分析が可能となる。
【0061】
より具体的な例として第1例〜第14例を挙げる。
【0062】
第1例は、サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器が接続されている、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記試薬液が封入された密封容器として本発明に係る内容物収納容器を使用した、フロー分析システム又はフローインジェクション分析システムである。
【0063】
ここで、第1例の一態様は、サンプル液を流路内に導入するためのサンプル液導入部と、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器が接続されている、前記試薬液を前記流路内に導入するための試薬液導入部と、前記サンプル液導入部及び前記試薬液導入部より前記流路の下流に位置する、前記応答を測定するための応答測定部とを有し、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答と、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記試薬液が封入された密封容器が、本発明に係る内容物収納容器である、フロー分析システム又はフローインジェクション分析システムである。
【0064】
第2例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が更に接続されており、前記補助液が密封された密封容器が、本発明に係る内容物収納容器である、前記第1例のフロー分析システム又はフローインジェクション分析システムである。
【0065】
第2例の一態様は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入するための補助液導入部を更に有し、前記補助液が密封された密封容器が、本発明に係る内容物収納容器である、前記第1例のフロー分析システム又はフローインジェクション分析システムである。
【0066】
第3例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第3例のフロー分析システム又はフローインジェクション分析システムである。
【0067】
第4例は、前記密封容器に封入された状態の試薬液又は補助液中に含まれる酸素含有量が、5ppm以下である、前記第1例〜第3例のいずれか一つのフロー分析システム又はフローインジェクション分析システムである。
【0068】
第5例は、前記第1例〜第4例のいずれか一つのフロー分析システム又はフローインジェクション分析システムにおいて使用される、本発明に係る内容物収納容器である。
【0069】
第6例は、前記密封容器に封入された状態の試薬液又は補助液中に含まれる酸素含有量が、5ppm以下である、前記第5例の密封容器である。
【0070】
第7例は、サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)が接続されている、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下であるフロー分析システム又はフローインジェクション分析システムである。
【0071】
第7例の一態様は、サンプル液を流路内に導入するためのサンプル液導入部と、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)が接続されている、前記試薬液を前記流路内に導入するための試薬液導入部と、前記サンプル液導入部及び前記試薬液導入部より前記流路の下流に位置する、前記応答を測定するための応答測定部とを有し、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答と、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システム又はフローインジェクション分析システムであって、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下であるフロー分析システム又はフローインジェクション分析システムである。
【0072】
第8例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入するための補助液導入部を更に有し、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下である、前記第7例のフロー分析システム又はフローインジェクション分析システムである。
【0073】
第9例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第8例のフロー分析システム又はフローインジェクション分析システムである。
【0074】
第10例は、前記試薬液又は前記補助液が封入された密封容器が、本発明に係る内容物収納容器である、前記第7例〜第9例のいずれか一つのフロー分析システム又はフローインジェクション分析システムである。
【0075】
第11例は、前記第7例〜第10例のいずれか一つのフロー分析システム又はフローインジェクション分析システムにおいて使用される、酸素含有量が5ppm以下の試薬液又は補助液が封入された密封容器である。
【0076】
第12例は、前記密封容器が、本発明に係る内容物収納容器である、前記第11例の密封容器である。
【0077】
第13例は、流路内を流れる第一の液に関する第一の応答と、前記流路内を流れる第二の液に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている分析対象元素を定量又は半定量的に測定可能なフロー分析システムであって、前記流路内を流れる前記第二の液が、前記試薬液による応答を抑制する作用を有する応答抑制物質を含有するフロー分析システム又はフローインジェクション分析システムである。
【0078】
第13例の一態様は、サンプル液を流路内に導入するためのサンプル液導入部と、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)が接続されている、前記試薬液を前記流路内に導入するための試薬液導入部と、前記サンプル液導入部及び前記試薬液導入部より前記流路の下流に位置する、前記応答を測定するための応答測定部とを有し、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答と、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析システムであって、前記流路内を流れる第二の液が、前記試薬液による応答を抑制する作用を有する応答抑制物質を含有するフロー分析システム又はフローインジェクション分析システムである。
【0079】
第14例は、サンプル液を流路内に導入するステップと、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器から、前記試薬液を流路内に導入するステップと、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答を検出すると共に、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答を検出又は入力するステップとを有する、前記第一の応答と前記第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析方法又はフローインジェクション分析方法であって、前記試薬液が封入された密封容器が、本発明に係る内容物収納容器である、フロー分析方法又はフローインジェクション分析方法である。
【0080】
ここで、第二の液に関するベース値としての第二の応答は、正確さの観点からは、検出して取得することが好適であるが、通常、その値は第一の応答よりも低いので、規定値(例えば、過去の測定値に基づく平均値)として記録しておき、当該規定値を入力する形で取得してもよい。尚、以下の発明における「第二の応答を検出又は入力するステップ」という用語の意味も同様である。
【0081】
第15例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入ステップを更に有し、前記補助液が密封された密封容器が、本発明に係る内容物収納容器である、前記第14例のフロー分析方法又はフローインジェクション分析方法である。
【0082】
第16例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第14例のフロー分析方法又はフローインジェクション分析方法である。
【0083】
第17例は、前記密封容器に封入された状態の試薬液又は補助液中に含まれる酸素含有量が、5ppm以下である、前記第14例〜第16例のいずれか一つのフロー分析方法又はフローインジェクション分析方法である。
【0084】
第18例は、サンプル液を流路内に導入するステップと、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)から、前記試薬液を流路内に導入するステップと、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答を検出すると共に、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答を検出又は入力するステップとを有する、前記第一の応答と前記第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析方法又はフローインジェクション分析方法であって、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下であるフロー分析方法又はフローインジェクション分析方法である。
【0085】
第19例は、試薬液以外の、前記応答測定に必要な補助液が封入された密封容器が接続されている、前記補助液を前記流路内に導入するための補助液導入部を更に有し、前記密封容器に封入された状態の試薬液中に含まれる酸素含有量が、5ppm以下である、前記第18例のフロー分析方法又はフローインジェクション分析方法である。
【0086】
第20例は、前記補助液が、キャリア液、中和液、酸化液、緩衝液、前記分析対象元素の標準液及びブランク液から選択される少なくとも一種である、前記第19例のフロー分析方法又はフローインジェクション分析方法である。
【0087】
第21例は、前記試薬液又は前記補助液が封入された密封容器が、本発明に係る内容物収納容器である、前記第18例〜第20例のいずれか一つのフロー分析方法又はフローインジェクション分析方法である。
【0088】
第22例は、サンプル液を流路内に導入するステップと、前記サンプル液中の分析対象元素の濃度に応じて検出可能な応答を発する試薬液が封入された密封容器(本発明に係る内容物収納容器)から、前記試薬液を流路内に導入するステップと、前記流路内を流れる第一の液(例えば、前記サンプル液と前記試薬液との混合液)に関する第一の応答を検出すると共に、前記流路内を流れる第二の液(例えば、前記混合液以外の液)に関するベース値としての第二の応答を検出又は入力するステップとを有し、前記第一の応答と前記第二の応答との差Δに基づき、サンプル液中に含まれている前記分析対象元素を定量又は半定量的に測定可能なフロー分析方法又はフローインジェクション分析方法であって、前記流路内を流れる前記第二の液が、前記試薬液による応答を抑制する作用を有する応答抑制物質を含有するフロー分析方法又はフローインジェクション分析方法である。
【0089】
ここで、本例における各用語の意義について説明する。「サンプル液」とは、分析対象元素を含んでいるか否かが問題となる液をいい、例えば、各プロセス(例えば半導体洗浄プロセス)で使用するプロセス液(洗浄液)や、当該プロセス液の原液(新液)を挙げることができる。「検出可能な応答」とは、例えば、変色(例えば発色や減色)、光信号(例えば蛍光)、電気信号等を挙げることができ、検出可能である限り特に限定されない。「第一の液」とは、好適な応答反応条件の下、サンプル液中に存在する分析対象元素の存在により応答反応を起した液を指し、例えば、サンプル液と試薬液との混合液や、サンプル液と試薬液と補助液(例えば、酸化液、中和液、緩衝液、補触媒液等)との混合液を挙げることができる。「第二の液」とは、サンプル液を含有しない液や、サンプル液を含有していても第一の液と比較して応答反応を起し難い状態にある液を指し、例えば、サンプル液を含有しない液としては、例えば、キャリア液と試薬液の混合液や、キャリア液と試薬液と他の補助液(例えば、酸化液、緩衝液、補触媒液等)}との混合液を挙げることができ、サンプル液を含有していても第一の液と比較して応答反応を起し難い状態にある液としては、例えば、サンプル液のみ、応答反応に適したpH範囲にない状態のサンプル液と試薬液との混合液、応答反応に必要な補触媒が存在しない状態のサンプル液と試薬液との混合液を挙げることができる。「システム」とは、装置のみならずプラントのようなものも包含する概念であり、また、各構成要素が物理的に一体的又は集約的なもののみならず、各構成要素が物理的に分割しているものや分散しているものも包含する。「元素」とは、特に限定されず、例えば金属元素である。「フロー分析」とは、自動分析を含む流れ分析を意味し、フローインジェクション分析を包含する概念である。
【0090】
以下、本発明に係る内容物収納容器の適用例を更に具体的に説明する。尚、以下のシステム及び方法は、好適には、微量元素を測定対象とし、より好適には超微量元素を測定対象とする。ここで、「微量」とは、対象元素の含有量が10−7オーダー(ppb)以下である場合を指し、「超微量」とは、対象元素の含有量が10−8オーダー(サブppb)以下(より好適には10−9オーダー以下)である場合を指す。尚、下限値は特に制限されないが、通常、10−12オーダー(ppt)である。更に、以下のシステム及び方法は、オンサイト分析用に適しているが、オンサイト分析用に限定されるものではなく、これ以外の用途も適用可能であり、本発明の権利範囲に属する。
【0091】
まず、図31及び図32を参照しながら、第一の適用具体例(新液用モニター)について詳述する。ここで、「新液」とは、実際の洗浄時に使用されるプロセス液を作るための高濃度の原液であり、例えば、98%硫酸や29%アンモニア水である。図31は、当該FIAの各工程に係るフローチャート図である。図31に示すように、半導体工程等、分析対象となる薬品から、連続的に、又は、一定時間毎にサンプルを採取するサンプル採取工程(ステップ1)と、前記サンプル採取工程で採取されたサンプルを中和してpHを調整する中和工程(ステップ2)と、前記中和工程後のサンプルに、金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬を注入する発色試薬注入工程(ステップ3)と、前記発色試薬注入工程後のサンプルの吸光度を測定する吸光度測定工程(ステップ4)とを含む。以下、各工程について詳述する。
【0092】
(1)サンプル採取工程(S1)
サンプル採取工程S1は、被検出溶液たる薬品中からサンプルを採取する工程である。ここで、一定時間毎にサンプルを採取することが好適であり、更に、一定時間毎に一定量のサンプルを採取することがより好適である。尚、サンプル採取の具体的方法は特に限定されない。
【0093】
被検出溶液たる薬品としては、例えば、強酸、弱酸及び強アルカリ、弱アルカリ薬品のいずれであっても、金属の検出が可能である。具体的には、強酸薬品としては、塩酸、硫酸、硝酸、又はこれらを混合したものなど、弱酸薬品としては、酢酸、フッ酸、リン酸などを挙げることができる。また、強アルカリ薬品としては、水酸化カリウム溶液、水酸化ナトリウム溶液、水酸化テトラブチルアンモニウム、水酸化テトラメチルアンモニウム、又はこれらを混合したものなど、弱アルカリ薬品としては、アンモニア水などを挙げることができる。
【0094】
(2)中和工程(S2)
中和工程S2とは、採取したサンプルに中和剤を注入することにより中和させる工程である。尚、発熱反応による発泡現象を防止するために、中和工程を冷却下で行なったり、並びに/或いは、中和剤及び/又はサンプルを予め冷却しておくことが好適である。このような構成を採ることにより、中和剤の希釈度を低く抑えることが可能となる結果、感度上昇に繋がる。但し、本工程は、中和しないと測定ができない場合にのみ必要であり、中和しなくても測定可能なサンプルの場合には省略される。
【0095】
この中和工程S2において用いられる中和剤は、被検出溶液たる薬品の種類及びpHにより適宜選択して使用すればよい。例えば、被検出溶液が塩酸の場合には、アンモニア水や水酸化ナトリウムを好適に用いることができ、また被検出溶液が水酸化カリウムの場合には、塩酸や酢酸などを好適に用いることができる。尚、中和剤としては、金属を含有しないものを用いることが、感度上昇の観点から好適である。
【0096】
(3)発色試薬注入工程(S3)
発色試薬注入工程S3とは、中和されたサンプル中に、検出対象である金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬を注入する工程である。尚、本適用具体例では、吸光度測定法に基づいて測定を行なうため、分析試薬として発色試薬を選択したが、例えば、分析手法として蛍光測定法を選択した場合には、分析試薬として蛍光試薬を選択することになる。
【0097】
発色試薬は、検出しようとする金属に合わせて適宜選択する。例えば、薬品中の鉄を検出する場合には、発色試薬としてはN,N−ジメチル−p−フェニレンジアミンや還元体のマラカイトグリーン、メチレンブルーなどが好適であり、また、銅、マンガン、コバルトなどを検出する場合にも、これらの試薬が使用可能である。尚、分析対象金属に応じ、温度、pH、濃度などの条件を適宜変更する。
【0098】
具体的には、例えば、N,N-ジメチル-p-フェニレンジアミン、N,N-ジエチル-p-フェニレンジアミン、N-(p-メトキシフェニル)-p-フェニレンジアミン、N-(p-メトキシフェニル-N,N-ジメチル)-p-フェニレンジアミン、4−ヒドロキシベンズアルデヒドセミカルパゾン、N-フェニル-p-フェニレンジアミン、2-ニトロソ-5-(Nプロピル-N-スルホプロピルアミノ)フェノール、2-(5-ブロム-2-ピリジルアゾ)-5-(N-プロピル-N-スルホプロピルアミノ)アニリン、2-(5-ブロム-2-ピリジルアゾ)-5-(N-プロピル-N-スルホプロピルアミノ)フェノール、2-(5-ニトロ-2-ピリジルアゾ)-5-(N-プロピル-N-スルホプロピルアミノ)フェノールなどを挙げることができる。
【0099】
また、発色試薬注入工程S3において、前記発色試薬に加えて酸化剤(酸化液)や緩衝剤(緩衝液)を注入することもできる。使用される発色試薬は、酸化反応により発色を呈する試薬であるため、当該酸化反応を促進することにより感度を上げることができる。例えば、鉄イオンは、酸化剤である過酸化水素の酸化反応を促進する触媒として働くことができる。しかも、酸化剤である過酸化水素は、発色試薬と鉄(III)の酸化還元反応の化学量論量よりもかなり多量に加えられており、鉄(III)が消費され、鉄(II)が生成されると、過酸化水素により鉄(III)が再生される(鉄の触媒作用)。このような触媒作用を利用することにより、少量の測定対象物質(例えば鉄)が存在すれば、十分な酸化剤が存在し、時間を制限しなければ、無限に酸化反応は進行する。すなわち、酸化による生成物の発色を検出に利用する場合には、感度の大幅な向上が期待できる。しかし、生成物量が測定対象物質量と明瞭な相関関係(直線関係が好ましい)にあることが保障される測定装置、測定手法でなければならない。このためには、詳細な実験的裏付けが必須である。注入する酸化剤は、特に限定されないが、例えば、発色試薬として、N,N−ジメチル−p−フェニレンジアミンを用いた場合には、酸化剤としては過酸化水素が好適である。また、使用される緩衝剤は、当該発色強度が最も高くなるpH域に緩衝するものである限り特に限定されない。
【0100】
(4)吸光度測定工程(S4)
吸光度測定工程S4とは、前記発色試薬注入工程S3後のサンプルの吸光度を測定する工程であり、当該測定結果により被検出溶液たる薬品中に存在する金属を定量することができる。尚、本最良形態では、吸光度測定法に基づいて測定を行なうものを挙げたが、分析手法はこれに限定されず、例えば、蛍光測定法も採用可能である。
【0101】
吸光度測定の具体的な方法は特に限定されることなく、従来公知の検出装置などを用いることができる。また測定波長についても前記発色試薬により適宜設定すればよい。例えば、発色試薬としてN,N−ジメチル−p−フェニレンジアミンを用いた場合には、測定波長は510nm〜530nm付近である。
【0102】
以下、図32を参照しながら、半導体製造工程を例にとり、本適用具体例をより詳細に説明する。半導体製造工程の場合、使用される薬液は強酸・強アルカリであり、取扱がきわめて難しいという問題がある。また、例えば、濃硫酸の場合は、濃度が極めて高いので中和が必要であるが、中和すると不純物元素の濃度も低下するので、一層の検出感度が必要となる。
【0103】
また、半導体製造工程の配管の多くは、鉄系素材に四フッ化樹脂などの耐薬品性樹脂をライニングしたものなどからなり、このライニング樹脂の破れなどの欠陥は、鉄などの金属汚染の原因となっている。したがって、濃硫酸を対象として、検出対象元素を鉄(Fe)とした例を以下に説明する。しかし、本発明において、試薬等鉄固有の条件要素ではない部分は、他の金属元素を微量分析する場合にも適用可能であり、本明細書において鉄を適用具体例として説明するからといって、他の元素に対する適用が否定されたり、本願発明の権利範囲が限定されると解釈されてはならない。
【0104】
図32に示す検出装置は、フローインジェクション分析装置の一種であり、半導体製造工程において使用される薬品から、一定時間毎にサンプルを採取するサンプル採取手段2と、前記サンプル採取手段2により採取されたサンプルと、当該サンプルを中和してpHを調整するための中和試薬とを混合して、当該サンプルを中和する中和手段3と、前記中和手段により中和されたサンプルと、金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬と酸化剤を所定の割合で混合して、発色反応を起こさせる反応手段4と、前記反応装置により発色反応を呈したサンプルの吸光度を測定する吸光光度測定手段5とを少なくとも含む。
【0105】
まず、サンプル採取手段2は、半導体製造工程において使用される薬品が流通する薬品流通管50に設けられており、当該薬品流通管50から一定時間毎に一定量のサンプルSを採取する。
【0106】
そして、サンプル採取手段2により採取されたサンプルは、サンプル流通管5に流入される。サンプル流通管5は、中和手段3として機能する中和管7に接続されている。
【0107】
中和試薬Nは、本発明に係る内容物収納容器(薬液バック又は試薬バック)8aに封入されており、当該試薬バック8aが接続されている中和試薬流通管9により前記中和管7に注入される。このように中和試薬Nをはじめ、本発明の装置において使用される試薬を本発明に係る内容物収納容器に封入して使用することにより、装置外部から不純物が混入することを防止することができ、より感度の高い分析を行うことができる。
【0108】
中和手段3にかかる中和管7に流入されたサンプルと中和試薬Nは、中和管7を流通する間に中和される。この際、中和管7に流入されるサンプルの流量、および中和試薬Nの流量を適宜調節することにより簡便に再現性よく中和をすることができる。
【0109】
中和管7は、自動切り替えバルブBに接続されている。当該自動切り替えバルブBには、一定量のサンプルを保持することができるサンプル計量管10を設けてある。
【0110】
切り替えバルブBには、キャリア流通管11が接続されている。当該キャリア流通管11の端部にはキャリアCを封入するための試薬バック8bが接続されている。
【0111】
キャリアCをキャリア流通管11に流入せしめながら、適当なタイミングで自動切り替えバルブBを切り替えることにより、キャリアCはサンプル保持管10内に流入する。その結果サンプル保持管10内に保持されたサンプルはキャリアCによって押し出されて、反応手段4にかかる反応管12へ流入する。
【0112】
反応手段4の上流側には、当該反応管に金属イオンを触媒として酸化反応を起こすことにより発色を呈する発色試薬Rを封入した試薬バッグ8cに接続された発色試薬流通管13、酸化剤Oを封入した試薬バッグ8dに接続された酸化剤流通管14、および緩衝溶液Bを封入した試薬バッグ8eに接続された緩衝溶液流通管15が接続されている。
【0113】
反応管4は、サンプルSまたはキャリアCに、発色試薬R、酸化剤O、および必要に応じて用いられる緩衝溶液Bをそれぞれ混合し、酸化反応を促進する。フローインジェクション分析装置においては、当該反応管12の長さを調節することにより反応時間をコントロールすることが出来る。また、当該反応管12(特に下流側)を温度調節器16内に設けることにより、反応温度を調節することも可能である。
【0114】
上述したように各試薬は、それぞれ試薬バック8a〜8eに封入されていることが好ましい。
【0115】
更に、それぞれの流通管には、試薬の流量を調節する機構が設けられている(図示せず)。したがって、それぞれの流通管を流れる溶液のpHや濃度等により、それぞれの流通管の流量を調節することによって、発色試薬が最も発色し易い条件を容易に作り出すことができる。
【0116】
反応管12は、吸光光度測定手段である吸光光度計17に接続されている。吸光光度計17は、サンプルSまたはキャリアCの吸光度を測定する。吸光度が測定されたサンプルは排出管18より排出される。
【0117】
上記説明においては、中和剤、酸化剤、緩衝剤の順序でサンプルに対して適用しているが、この順序については発色を実現するものであれば特にこだわるものではない。
【0118】
次に、図28及び図33を参照しながら、第二の適用具体例(プロセス液用モニター)について説明する。ここで、「プロセス液」とは、新液を希釈して実際の洗浄に使用される液を意味し、例えば過酸化水素等が添加されているものである(例えば、36%塩酸:30%過酸化水素:超純水=1:5:400)。まず、図31は、当該FAの各工程に係るフローチャート図である。図31に示すように、まず、ステップ11でサンプルを採取する。この際、FIAと異なり、サンプルは採取し続け、基本的には常に流路内に流れている状態となる。次に、ステップ12で、発色試薬(及び場合により酸化剤や緩衝剤)をある期間注入する。その結果、発色試薬が注入されたサンプル部分は、発色反応を起こし得る状態となる。そして、ステップ13で、当該発色試薬が注入されたサンプル部分と、当該発色試薬が注入されていないサンプル部分の両方について吸光度を測定する。
【0119】
次に、図28は、本具体例に係る装置の概略図である。ここで、第一適用具体例(FIA)との相違点は、キャリア液が存在しない点、サンプル液が流路内を流れ続ける点、及び、発色試薬(及び酸化剤や緩衝剤のような補助液)がある期間シンクロしてサンプル液に注入される点である。それ以外は、第一適用具体例と同一であり、同一機能を有する部材の番号の後に「(2)」を付している。相違点について説明すると、サンプル液導入部2(2)は、洗浄流路100(2)から継続的にサンプル液Sを採取し、図示しないポンプにより流路5(2)内にサンプル液Sを流し続ける。そして、酸化液O(2)、試薬液R(2)及び緩衝液B(2)は、図示しないポンプをシンクロ作動させることにより、ある期間、サンプル液S内にこれら試薬液や補助液を同時注入する。
【0120】
前記第一適用具体例(FIA)及び前記第二適用具体例(FA)のような検出装置において、その検出感度は、検出バックグランド値とサンプルピーク値との差分であるΔを大きくすることによって向上する。FAやFIAによる検出感度を上げるための工夫としては大きく分けると以下の二つのアプローチがあり得る。
【0121】
第一は、検出バックグランドを低下させることにより、ノイズを小さく安定させ、微少なΔを大きくし、またはこれを拡大して正確に測定する方法である。第二は、検出対象元素の発色効率を向上させることによって、サンプルピークを実質的に大きくし、S/N比を向上することによってΔを大きくする方法である。
【0122】
本発明においては、それぞれのアプローチに関して、以下の手法を採用した。
【0123】
検出バックグランドは、主として(1)流路において、分析サンプル以外から検出対象元素が混入すること、(2)検出対象元素以外の元素に発色剤が反応して発色が生じること、によって上昇する。本例においては、この二つの要因を低下させることによって、検出バックグランドの低下を図る。
【0124】
まず、(1)については、分析サンプル以外からの検出対象元素の混入量を低減するとともに、バックグランドを構成するキャリア液中に分析対象元素の発色を抑制する物質(発色抑制物質)を混入することによって解決した。
【0125】
本例によれば、試薬バッグ8bに封入されたキャリアCの中にかかる発色抑制物質を混入する。発色抑制物質としては、通常のキレート試薬、例えば、エチレンジアミン四酢酸、エチレングリコールビス(2−アミノエチル)エーテルジアミン四酢酸、ジエチレントリアミン五酢酸、トリエチレンテトラミン六酢酸その他の塩、ピロリン酸の無機錯化剤などが考えられる。
【0126】
発色抑制物質の濃度は、10-13M(mol/l)〜10-3M(mol/l)が好ましい。10-13M(mol/l)未満であると発色抑制の効果が低下し、10-3M(mol/l)以上入れてもそれ以上の効果がないからである。
【0127】
発色抑制物質をキャリア中に入れることにより、キャリアにかかる検出バックグランドが低下し、ノイズが小さくなり、バックグランドが安定するので微少なΔも拡大して正確に測定できる。よって、相対的にサンプルの検出レベルとの差異Δが大きくなるので、検出感度が向上する。
【0128】
尚、当該発色抑制物質は、キャリア中だけでなく、試薬液や他の補助液(例えば、酸化液、緩衝液、中和液)に入れてもよい。
【0129】
また、上記(2)の点について、本発明者は、FAやFIAでサブppbオーダー乃至pptオーダーで測定を行なう際に、最も重要な偽発色原因物質が酸素であることを見出した。更に、FAやFIAで高感度な超微量分析を可能にする上で、所定値以下の酸素透過性(酸素透過度)のバックで各種薬剤(特に発色剤溶液)を封入することが重要であることも見出した。具体的には、当該バッグの酸素透過度は、25℃で相対湿度80%において、10fmol/m2.s.Pa(2cc/m2・d・atm)以下であることが重要であり、5fmol/m2・s・Pa(1cc/m2・d・atm)以下であることが好適であり、2.5fmol/m2・s・Pa(0.5cc/m2・d・atm)以下であることがより好適である。
【0130】
更に、口部材の栓体部材が、内部で上下左右方向から圧縮された状態にある結果、当該栓体部材とベース部材及び冠体部とで協働し、高い気密・液密性が担保されている。そして、冠体部材の開口部に弾性部材の凸部が形成されているので、当該部分に針を刺した場合でも、強力な圧縮力が働き、当該部分で極めて高い気密・液密性が保証される。
【0131】
以上の工夫を施したバッグに薬剤を封入することにより、FAやFIAでサブppbオーダー乃至pptオーダーで測定を行なう際に従来問題となっていた、発色液の保管・運搬中における発色剤の発色を、本目的を達成するために問題とならない程度まで抑制できる。更に、発色剤溶液のみならず、他の補助剤(キャリア、酸化剤、中和剤、緩衝剤)も同様のバッグに封入することにより、発色剤と混合した際の偽発色も抑制できる。ここで、前記バッグに各種液を封入するに際し、これら薬剤を十分に脱気してから封入する必要があることはいうまでもない。
【0132】
また、別の手段(又は前記手段との組み合わせ)として、本発明者らは、FAやFIAでサブppbオーダー乃至pptオーダーで測定を行なう際、液中に僅かにでも存在する気泡が大きな問題となることを発見した。当該発見に基づき、鋭意検討した結果、各種液(特に発色液)中の酸素含有量が、5ppm以下に維持することが好適であることを見出した。ここで、5ppm以下に維持する手法としては、例えば、減圧して溶存酸素を除去する手法を挙げることができる。
【0133】
なお、本明細書における数値を規定するにあたって、酸素含有量については、例えば、溶存酸素測定法(JIS K 0400−32−30)に記載された水質―溶存酸素の定量―電気化学プローブ法による。また、酸素透過率については、例えば、JIS K7126に記載のプラスチックフィルム及びシートの気体透過度試験方法により測定することができる。
【0134】
次に、検出精度を高めるための第二のアプローチについて述べる。
【0135】
検出精度を高めるためには、サンプル中に含まれる検出対象元素の触媒効果がもっとも発現反応しやすい条件となり、発色に寄与することが望ましい。検出対象元素がFeであり、発色剤がN,N−ジメチル−p−フェニレンジアミンの場合、発色反応を呈するためには、好ましくは、pH3.0乃至9.0に一定時間維持することが望ましい。このような維持は、吸光度測定器に連接された恒温層において、または、吸光度測定器の直前において実現されることが好ましい。
【実施例】
【0136】
実施例1{FIA法(鉄分析)}
まず、図34を参照しながら、本実施例に係る装置及び分析方法について説明する。サンプルSと中和液NSの送液にはCavro Scientific Instruments,Inc.製CavroXL3000モジュラー・デジタル・ポンプ(1”h、1”v)を用いた。サンプルSとしては、5種類の97%(18.2mol/l)硫酸(鉄濃度=0、30、60、80、100ppt)を300μl用い、流量50μl/minで流した。中和液NSとしては、密封容器(酸素透過度:0.8cc/m2・d・atm)に封入されている2.85%(1.65mol/l)のアンモニア水(酸素含有量:2.5ppm)を5500μl用い、流量916.7μl/minで流した。キャリア液CS、酸化剤OS、発色試薬液RS,緩衝液BSの送液には、旭テクネイオン株式会社製APZ−2000ダブルプランジャーポンプ1”bを用いた。キャリア液CSとしては、密封容器(詳細情報が必要)に封入されている0.97mol/lの硫酸アンモニウム水溶液(酸素含有量:2.5ppm)を用い、流量0.8ml/minで流した。また、キャリア中には発色を抑える抑制剤として10−6mol/lのエチレンジアミン四酢酸を混ぜている。酸化液OSには、密封容器(詳細情報が必要)に封入されている0.3%の過酸化水素水(酸素含有量:2.5ppm)を用い、流量0.8ml/minで流した。発色試薬液RSには、密封容器(詳細情報が必要)に封入されている4mmol/lのN,N−ジメチル−p−フェニレンジアミン(酸素含有量:2.5ppm)を用い流量0.5ml/minで流した。緩衝液BSには、密封容器(詳細情報が必要)に封入されている1.3mol/lの酢酸アンモニウム水溶液(酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。サンプル計量管(インジェクションバルブ1”i)には、内径0.8mm、長さ160cmのチューブを用いた。中和管(冷却部1”g)で中和された液、酸化液OS、発色試薬液RS、緩衝液BSを、内径0.8mm、長さ2mの反応管で混合した。この混合液を温度調節器1”kで35℃に保った。そして、空冷部1”qを介した後、この着色溶液の吸光度を検出器(吸光光度計1”m)により最大吸収波長514nmで測定を行った。流路構成には内径0.8mmのチューブを用いた。
【0137】
図35に、上記方法で濃硫酸中における30ppt乃至100pptの濃度の鉄を測定した場合の検量線を示す。なお、この例においては、発色反応を呈するためにpHを5.5に維持した。この結果、図35に示すように、Blankと表示されたキャリアにおける発色と30ppt乃至100pptの濃度の鉄を含んだサンプルとの間には、発色度に応じた差Δ(キャリアの発色度とサンプルの発色度との差)が観察された。また、図36にΔと鉄濃度との相関を示す。図36に示すように、この相関は、良好な直線関係を示しており、本発明にかかる方法によって、pptオーダーの鉄が測定可能であることが立証された。
【0138】
実施例2{FA法(鉄、銅及び各種元素分析)}
まず、図37を参照しながら、本実施例に係る装置及び分析方法について説明する。サンプルSの送液には旭テクネイオン株式会社製APZ−2000の2連式プランジャーポンプ1hを用いた。サンプルSとしては、以下の表に示す所定量の金属を添加した0.01M塩酸を300μl用い、流量50μl/minで流した。
【表1】

酸化液OS、発色試薬液RS及び緩衝液BSの送液には、シリンジポンプ1bを用いた。酸化液OSには、密封容器(詳細情報が必要)に封入されている0.3%の過酸化水素水(酸素含有量:2.5ppm)を用い、流量0.8ml/minで流した。発色試薬液RSには、密封容器(詳細情報が必要)に封入されている4mmol/lのN,N−ジメチル−p−フェニレンジアミン(酸素含有量:2.5ppm)を用い流量0.5ml/minで流した。緩衝液BSには、密封容器(詳細情報が必要)に封入されている1.3mol/lの酢酸アンモニウム水溶液(酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。尚、これら3個のシリンジポンプ1bは、流れるサンプルSの同じ場所にすべてが注入されるよう、相互にシンクロして作動させた。サンプルS、酸化液OS、発色試薬液RS,緩衝液BSは、内径0.8mm、長さ2mの反応管で混合した。この混合液を温度調節器1kで35℃に保った。この着色溶液の吸光度を検出器(吸光光度計)1mにより最大吸収波長514nmで測定を行った。流路構成には内径0.8mmのチューブを用いた。
【0139】
尚、濃度決定の際には、検量線を作成する必要があるため、標準液SSやブランク液BLSが、インジェクションバルブ1iによりサンプル液Sと切替可能に構成されている。尚、図19は、サンプル液Sと標準液SSやブランク液BLSとの切替をインジェクションバルブ1iで行なう態様であるが、図38に、切替弁1’wで切替を行なう態様を示す。
【0140】
結果を図39〜図42及び表2に示す。図39は、波長514nmにおける鉄1ppbの吸光度ピークを示すチャートである。図40は、波長514nmにおける銅1ppbの吸光度ピークを示すチャートである。図41は、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。図42は、波長514nmにおける吸光度と銅濃度との関係を示す検量線である。図39及び図40に示されるように、検出バックグラウンドが十分に低下しているので、ppbオーダーでも、検出バックグランド値とサンプルピーク値との差分であるΔが大きくなった。尚、鉄の感度は銅の3倍近くであることが確認された。また、図41及び図42に示されるように、鉄及び銅のいずれに関しても、相関定数が0.999程度と、ppbオーダーでも極めて高い相関関係を示すことが確認された。更に、表2に示されるように、鉄(1ppb)+銅(1ppb)を添加した場合には、吸光度(0.0860)は、鉄1ppbに基づく吸光度(0.0652)と銅1ppbに基づく吸光度(0.0208)とを合計した値となり、鉄と銅の総量を測定できることが確認された。更に、鉄+銅+他の金属(すべて1ppb)を添加した場合、測定された吸光度(0.0857)は、ほぼ鉄+銅(1ppb)の吸光度(0.0860)と同程度であることから、他の金属の影響は無視できることが確認された。
【表2】

【0141】
実施例3{FIA法(鉄分析)}
まず、図34を参照しながら、本実施例に係る装置及び分析方法について説明する。尚、本実施例に関しては、中和液を用いないので、図34中の「NS」及びそのラインは存在しないものとする。サンプルSの送液にはCavro Scientific Instruments,Inc.製CavroXL3000モジュラー・デジタル・ポンプ(1”h、1”v)を用いた。サンプルSとしては、APM液(29% アンモニア:30%過酸化水素:超純水=1:5:400)に鉄を0、0.5、1.0ppb加えたものを0.8ml用いた。キャリア液CS、酸化液OS、発色試薬液RS、緩衝液BSの送液には、旭テクネイオン株式会社製APZ−2000ダブルプランジャーポンプ1”bを用いた。キャリア液CSとしては、密封容器(詳細情報が必要)に封入されている0.037 M (0.071 %) アンモニア+0.11 M (0.37 %) 過酸化水素(pH 10.86)を用い、流量0.8ml/minで流した。酸化液OSには、密封容器(詳細情報が必要)に封入されている0.88 M (3.0 %) 過酸化水素+0.05 M (0.15 %) 塩酸(pH 1.26)を用い(酸素含有量:2.5ppm)、流量0.8ml/minで流した。発色試薬液RSには、密封容器(詳細情報が必要)に封入されている4 mM (0.084%)のN,N−ジメチル−p−フェニレンジアミン(DPD,pH 1.87)(酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。緩衝液BSには、密封容器(詳細情報が必要)に封入されている1.3mol/lの酢酸アンモニウム水溶液(pH6.34、酸素含有量:2.5ppm)を用い、流量0.5ml/minで流した。サンプル計量管(インジェクションバルブ1”i)には、内径0.8mm、長さ160cmのチューブを用いた。流路を流れるキャリア液S又はサンプル液と、酸化液OS、発色試薬液RS及び緩衝液BSとを、内径0.8mm、長さ2mの反応管で混合した。この混合液を温度調節器1”kで35℃に保った。そして、空冷部1”qを介した後、この着色溶液の吸光度を検出器(吸光光度計1”m)により最大吸収波長514nmで測定を行った。流路構成には内径0.8mmのチューブを用いた。
【0142】
結果を図43に示す。図43は、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。図43に示されるように、調製当日は鉄の濃度に比例して吸光度が増加し、鉄1 ppbで吸光度0.032を示しているので、塩酸中の鉄などと同程度の充分な感度が得られることが分かった。以上の結果から、希薄APM液中の鉄の測定でも、塩酸中の鉄と同程度の感度で得られたので、希薄APM液中の鉄を中和等の前処理工程を経ず、充分な感度で定量出来ることが判明した。
【0143】
本明細書においては、pptオーダーの微量元素を分析することを前提として記述したが、本願発明はppbオーダーの元素分析にも適用可能である。かかる場合も本発明の射程範囲内であり、その権利範囲が及ぶことは当然である。
【0144】
本明細書の最良形態及び実施例においては、発色反応を前提として説明を行ったが、蛍光反応を前提としても本発明を適用可能である。この場合、発色試薬ではなく、サンプル及びキャリアに含まれる分析対象元素の濃度に応じて蛍光光度が変化する蛍光物質(蛍光試薬)を用いる。また、キャリア中に加える物質としては、発色抑制物質の代わりに、蛍光反応を抑制する物質を添加すればよい。
【図面の簡単な説明】
【0145】
【図1】本最良形態に係る薬液バッグの断面図である。
【図2】本最良形態に係る薬液バッグの、口部材の上面図である。
【図3】本最良形態に係る薬液バッグの、口部材の側断面図である。
【図4】本最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の側断面図である。
【図5】本最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の上面図である。
【図6】本最良形態に係る薬液バッグの、冠体部材装着前の口部材の側断面図である。
【図7】本最良形態に係る薬液バッグの、口部材の側断面図である。
【図8】本最良形態に係る薬液バッグの、口部材内の栓体部材の応力分布図であ る。
【図9】使用時における、本最良形態に係る薬液バッグの断面図である。
【図10】第二の最良形態に係る薬液バッグの断面図である。
【図11】第二の最良形態に係る薬液バッグの、口部材の上面図である。
【図12】第二の最良形態に係る薬液バッグの、口部材の側断面図である。
【図13】第二の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の側断面図である。
【図14】第二の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の上面図である。
【図15】第二の最良形態に係る薬液バッグの、冠体部材装着前の口部材の側断面図である。
【図16】第二の最良形態に係る薬液バッグの、口部材の側断面図である。
【図17】第二の最良形態に係る薬液バッグの、口部材内の栓体部材の応力分布図である。
【図18】使用時における、第二の最良形態に係る薬液バッグの断面図である。
【図19】第三の最良形態に係る薬液バッグの断面図である。
【図20】第三の最良形態に係る薬液バッグの、口部材の上面図である。
【図21】第三の最良形態に係る薬液バッグの、口部材の側断面図である。
【図22】第三の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の側断面図である。
【図23】第三の最良形態に係る薬液バッグの、冠体部材装着前の口部材(ベース部材及びフランジ部)の上面図である。
【図24】第三の最良形態に係る薬液バッグの、冠体部材装着前の口部材の側断面図である。
【図25】第三の最良形態に係る薬液バッグの、口部材の側断面図である。
【図26】第三の最良形態に係る薬液バッグの、口部材内の栓体部材の応力分布図である。
【図27】使用時における、第三の最良形態に係る薬液バッグの断面図である。
【図28】本適用具体例にかかるFA装置を模式的に示した図である。
【図29】本適用具体例にかかるFIA測定装置を簡略的に示した図である。
【図30】本適用具体例にかかるFIA測定原理を示す測定チャートである。
【図31】本適用具体例にかかるFIA測定ステップを示すフロー図である。
【図32】本適用具体例に用いられるFIA装置を模式的に示した図である。
【図33】本適用具体例にかかるFA測定ステップを示すフロー図である。
【図34】実施例1及び実施例3における、FIA装置を模式的に示した図である。
【図35】実施例1における、濃硫酸中の微量鉄を測定したときのデータ図である。
【図36】実施例1における、濃硫酸中の微量鉄を測定したときの鉄濃度と発色度との相関を示すデータ図である。
【図37】実施例2における、FA装置を模式的に示した図である。
【図38】図37のFA装置の変更態様を模式的に示した図である。
【図39】実施例2における、波長514nmでの鉄1ppbの吸光度ピークを示すチャートである。
【図40】実施例2における、波長514nmでの銅1ppbの吸光度ピークを示すチャートである。
【図41】実施例2における、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。
【図42】実施例2における、波長514nmにおける吸光度と銅濃度との関係を示す検量線である。
【図43】実施例3における、波長514nmにおける吸光度と鉄濃度との関係を示す検量線である。
【図44】従来の口部材の側断面図である。
【図45】従来の弾性部材の上面図及び側断面図である。
【符号の説明】
【0146】
1 FA装置、1b シリンジポンプ、1c 混合器、1d 洗浄水切替弁、1e 気液分離器、1f サンプル入口弁、1g 冷却器(ラジエター)、1h 2連式プランジャーポンプ、1i インジェクションバルブ、1j 標準液切替弁、1k 恒温槽、1m 吸光光度計、1n チェック弁、1p シリンジポンプ、1r エア抜き電磁弁、1s 廃液、1t エアトラップ(外付け)、1x 洗浄水導入部、1y サンプル導入部、1z サンプル排出部、2 検出薬カートリッジ(保冷庫)
【0147】
1’ FA装置、1’b シリンジポンプ、1’c 混合器、1’d 洗浄水切替弁、1’e 気液分離器、1’f サンプル入口弁、1’g 冷却器(ラジエター)、1’h 2連式プランジャーポンプ、1’j 標準液切替弁、1’k 恒温槽、1’m 吸光光度計、1’n チェック弁、1’p シリンジポンプ、1’r エア抜き電磁弁、1’s 廃液、1’t エアトラップ(外付け)、1’w 標準液切替弁、1’x 洗浄水導入部、1’y サンプル導入部、1’z サンプル排出部、2’ 検出薬カートリッジ(保冷庫)
【0148】
1” FA装置、1”b プランジャーポンプ、1”f サンプル入口弁、1”g 冷却器(ラジエター)、1”h サンプルポンプ、1”i インジェクションバルブ、1”j サンプル吸引弁、1”k 恒温槽、1”m 吸光光度計、1”n チェック弁、1”p シリンジポンプ、1”r エア抜き電磁弁、1”s 廃液、1”t エアトラップ(外付け)、1”u 線浄水ポンプ、1”v 中和液ポンプ、1”x 洗浄水導入部、1”y サンプル導入部、1”z サンプル排出部、2” 検出薬カートリッジ(保冷庫)
【特許請求の範囲】
【請求項1】
弾性体から構成される栓体部材と、
前記栓体部材が挿入可能な第一開口部が形成されており、かつ、当該開口部から挿入された前記栓体部材を収納可能な内部空間が形成されたベース部材と、
前記ベース部材の前記第一開口部を覆うように前記ベース部材に装着可能な、前記第一開口部よりも小さく設定された第二開口部を有する冠体部材と、
を備えた口部材であって、
前記栓体部材が前記内部空間に収納された状態で前記冠体部材を前記ベース部材に装着した際、前記栓体部材は、前記冠体部材及び前記ベース部材の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記内部空間を形成する内壁からも圧縮力を受ける一方、前記圧縮力による弾性変形の結果、前記栓体部材の一部が前記第二開口部から凸状に露出する口部材。
【請求項2】
前記装着が、冠体部材と前記ベース部材との螺合により達成されると共に、前記螺合の程度に応じて、前記圧縮力が可変するよう構成されている、請求項1記載の口部材。
【請求項3】
前記ベース部材が、前記第一開口部とは反対側に、前記第一開口部よりも小さく設定された第三開口部を更に有しており、
前記栓体部材が前記内部空間に収納された状態で前記冠体部材を前記ベース部材に装着した際、前記栓体部材は、前記冠体部材及び前記ベース部材の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記栓体部材の一部が前記第三開口部から凸状に露出するよう構成されている、請求項1又は2記載の口部材。
【請求項4】
請求項1〜3のいずれか一項記載の口部材を備えた内容物収納容器。
【請求項5】
前記内容物が化学分析用薬液である、請求項4記載の内容物収納容器。
【請求項6】
前記化学分析がフロー分析である、請求項5記載の内容物収納容器。
【請求項7】
前記内容物が酸素易変性成分を含有する、請求項4〜6のいずれか一項記載の内容物収納容器。
【請求項8】
前記収納容器が酸素バリア性素材から構成されている、請求項7記載の内容物収納容器。
【請求項1】
弾性体から構成される栓体部材と、
前記栓体部材が挿入可能な第一開口部が形成されており、かつ、当該開口部から挿入された前記栓体部材を収納可能な内部空間が形成されたベース部材と、
前記ベース部材の前記第一開口部を覆うように前記ベース部材に装着可能な、前記第一開口部よりも小さく設定された第二開口部を有する冠体部材と、
を備えた口部材であって、
前記栓体部材が前記内部空間に収納された状態で前記冠体部材を前記ベース部材に装着した際、前記栓体部材は、前記冠体部材及び前記ベース部材の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記内部空間を形成する内壁からも圧縮力を受ける一方、前記圧縮力による弾性変形の結果、前記栓体部材の一部が前記第二開口部から凸状に露出する口部材。
【請求項2】
前記装着が、冠体部材と前記ベース部材との螺合により達成されると共に、前記螺合の程度に応じて、前記圧縮力が可変するよう構成されている、請求項1記載の口部材。
【請求項3】
前記ベース部材が、前記第一開口部とは反対側に、前記第一開口部よりも小さく設定された第三開口部を更に有しており、
前記栓体部材が前記内部空間に収納された状態で前記冠体部材を前記ベース部材に装着した際、前記栓体部材は、前記冠体部材及び前記ベース部材の挟み込みにより圧縮力を受けると共に、前記圧縮力による弾性変形の結果、前記栓体部材の一部が前記第三開口部から凸状に露出するよう構成されている、請求項1又は2記載の口部材。
【請求項4】
請求項1〜3のいずれか一項記載の口部材を備えた内容物収納容器。
【請求項5】
前記内容物が化学分析用薬液である、請求項4記載の内容物収納容器。
【請求項6】
前記化学分析がフロー分析である、請求項5記載の内容物収納容器。
【請求項7】
前記内容物が酸素易変性成分を含有する、請求項4〜6のいずれか一項記載の内容物収納容器。
【請求項8】
前記収納容器が酸素バリア性素材から構成されている、請求項7記載の内容物収納容器。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】


【公開番号】特開2006−347604(P2006−347604A)
【公開日】平成18年12月28日(2006.12.28)
【国際特許分類】
【出願番号】特願2005−177756(P2005−177756)
【出願日】平成17年6月17日(2005.6.17)
【出願人】(501210065)株式会社フィアモ (8)
【Fターム(参考)】
【公開日】平成18年12月28日(2006.12.28)
【国際特許分類】
【出願日】平成17年6月17日(2005.6.17)
【出願人】(501210065)株式会社フィアモ (8)
【Fターム(参考)】
[ Back to top ]

