可視光応答型光触媒の製造方法、及び可視光応答型光触媒
【課題】 簡便かつ工業的に有効な金属イオンを酸化チタン結晶へ直接ドーピングする製造方法、及び該製造方法で得られる全紫外線領域から約600nmまでの強い吸収を示す金属ドーピング酸化チタンからなる可視光応答型光触媒を提供すること。
【解決手段】 アナターゼ/ルチル混晶型酸化チタン(A)に、金属イオンの水溶液(B)を接触させた後、固体を取りだし、300〜900℃で焼成することを特徴とする可視光応答型光触媒の製造方法、及びアナターゼ/ルチル混晶型酸化チタン(A)に遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)がドーピングしてなることを特徴とする可視光応答型光触媒。
【解決手段】 アナターゼ/ルチル混晶型酸化チタン(A)に、金属イオンの水溶液(B)を接触させた後、固体を取りだし、300〜900℃で焼成することを特徴とする可視光応答型光触媒の製造方法、及びアナターゼ/ルチル混晶型酸化チタン(A)に遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)がドーピングしてなることを特徴とする可視光応答型光触媒。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、可視光応答型光触媒に関し、詳しくは、アナターゼとルチルの二つの結晶相が混在する混晶型酸化チタンに金属イオンがドーピングされてなる金属イオンドーピング型の可視光応答型光触媒とその簡便な製造方法に関するものである。
【背景技術】
【0002】
先端材料において、酸化チタンは従来の白色顔料、高屈折率材料と異なる応用物性を示すことで、ますます注目を集めている(非特許文献1参照。)。例えば、光触媒又は色素増感電荷分離機能では、酸化チタンは群を抜いた触媒材料であり、次世代型光触媒デバイス、太陽電池への応用分野での期待が大きい。また、エネルギー問題で大きな注目を集める燃料電池でも、酸化チタンに白金ナノ粒子を埋め込んだ電極層研究開発が脚光を浴びている。燃料電池の実用化には、水素製造が要求されるが、その水素製造用触媒でも、酸化チタン・白金のコンポジットが有力な候補となっている。
【0003】
近年、酸化チタンによる汚れや有害物質等を自発分解し無害化する光触媒機能が非常に注目されている。その応用分野は、住宅、車、医療、土地処理などへと広がり、循環型社会構築の不可欠技術として位置付けられている。しかしながら、酸化チタンの該光触媒機能を発現させるためには、紫外線を光源とすることが前提条件である。自然光(太陽光)にはわずか3%程度の紫外線しか含まれておらず、その大部分は可視光であることを鑑みると、紫外線のみを吸収する光触媒では、太陽光線の利用はほとんど無意味となる。即ち、酸化チタンを有効な光触媒として用いるためには、酸化チタンそのものの吸収範囲を可視光へ変換させることが最も重要である。従って、多くの研究では、酸化チタン中に不純物ともいわれるほどの原子ドーピング、例えばアニオン(窒素原子、炭素原子、硫黄原子、リン原子)ドーピング、またはカチオン(遷移金属、希土類金属、半金属等の金属イオン)ドーピング等が検討されてきた。
【0004】
酸化チタンにこれらのドーピングを行うには、いくつかの代表的な方法が知られている。例えば、チタン化合物のゾルゲル反応で酸化チタンを調製する際に、金属イオン化合物を同時に加え、得られた加水分解物を熱焼成することで着色酸化チタンを製造する方法が挙げられる(例えば、非特許文献2〜4参照。)。このような方法はもっとも簡易なゾルゲル反応であるので、多くの研究者に安易に利用されて来たが、実験条件により全く異なる結果になることが多く、再現性はほとんど保証できないと認識されている。したがって、その光触媒作用にも再現性が得られず、工業的な利用に用いるドーピング酸化チタンの製造方法とは言いがたいものが多い。
【0005】
このような状況から脱皮するため、加速電圧によるイオン注入法を用いることが開発されている(例えば、特許文献1参照)。前記特許文献1では、加速エネルギーにて金属イオンを酸化チタン結晶面に注入することで、酸化チタン結晶面に金属イオンをドーピングするものである。この手法は、注入イオンの量、種類などをコントロールできることから、ドーピング反応を目的にあわせて制御する方法としては確かに有効である。また、該手法にて得られるドーピング酸化チタンは可視光領域である400〜500nmの領域に吸収を示し、可視光応答型光触媒として機能することも確認されている。
【0006】
また、超高温ガスプラズマ法を用い、酸化チタン結晶格子中に鉄やアルミニウムなどの不純物準位の比較的高い原子をドーピングさせることも提案されている(例えば、特許文献2参照。)。しかしながら、これらの加速エネルギーイオン注入法、超高温プラズマ法はそのプロセス自体の生産コストが高く、循環型社会へ可視光応答型光触媒を供給することには全く不向きであるといっても過言ではない。
【0007】
可視光応答型光触媒として有用な金属ドーピング酸化チタンについてはその有効性が予測されるものの、いまだ工業的な簡便な製造方法は見出されておらず、可視光応答型として市販される酸化チタンであっても、室内の蛍光灯下では光触媒機能すら示さないことが多い。酸化チタンそのものに信頼性ある可視光応答性を付与することは重要な技術的課題である。
【0008】
【非特許文献1】A.L.Linsebiger et al.、Chem.Rev.1995年、第95巻、735頁
【非特許文献2】E.Borgarello et al.、J.Am.Chem.Soc.,1982年、第104巻、2996頁
【非特許文献3】L.Zang et al.、J.Phys.Chem.B 1998年、第102巻、10765頁
【非特許文献4】H.Kisch et al.、Angew.Chem.Int.Ed.,1998年、第37巻、3034頁
【非特許文献5】S.Sakthivel et al.、Angew.Chem..Int.Ed.、2003年、第42巻,4908頁
【特許文献1】特開平9−262482号公報
【発明の開示】
【発明が解決しようとする課題】
【0009】
上記実情を鑑み、本発明が解決しようとする課題は、簡便かつ工業的に有効な金属イオンを酸化チタン結晶へ直接ドーピングする製造方法、及び該製造方法で得られる全紫外線領域から約600nmまでの強い吸収を示す金属ドーピング酸化チタンからなる可視光応答型光触媒を提供することにある。
【課題を解決するための手段】
【0010】
本発明者は、前記課題を解決するために鋭意検討を重ねた結果、アナターゼ型結晶性とルチル型結晶性とを有するアナターゼ/ルチル混晶型酸化チタンに、金属イオンの水溶液を接触させた後、固体を取りだし、熱焼成させることで、金属イオンがドーピングした酸化チタンが容易に且つ再現性良く得られること、また、得られた金属イオンドーピング酸化チタンが可視光に応答する光触媒として機能することを見出し、本発明を完成した。
【0011】
即ち本発明は、アナターゼ/ルチル混晶型酸化チタンに、金属イオンの水溶液を接触させた後、固体を取りだし、300〜900℃で焼成することを特徴とする可視光応答型光触媒の製造方法を提供するものである。
【0012】
更に本発明は、アナターゼ/ルチル混晶型酸化チタンに遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオンがドーピングしてなることを特徴とする可視光応答型光触媒をも提供するものである。
【発明の効果】
【0013】
本発明の可視光応答型光触媒は、可視光への応答性が高く、色素類など有機物の分解能に優れる。また、その製造方法は、工業的汎用の整備のみで製造可能であり、再現性も高く工業的有用性が高い。
【0014】
また、本発明の製造方法では、単一種類の金属イオンに限らず、複数種のイオンを同時にドーピングすることも可能であり、可視光において広い吸収範囲を有する金属イオンドーピング酸化チタンが得られる。従って、本発明の製造方法で得られる金属イオンドーピング酸化チタンは、自然光(太陽光)のみならず、室内の蛍光灯下での有効利用の面からも期待できる。
【発明を実施するための最良の形態】
【0015】
酸化チタンに金属イオンをドープする際、もっとも広く用いられる方法は、アルコキシチタンのゾルゲル反応液中に、遷移金属塩を混合し、不純物が含まれた酸化チタン前駆体を調製し、その前駆体を一定温度にて加熱する方法である。このような方法では、金属イオンが酸化チタン本体と表面に分布した状態でドープされるが、金属イオンがドープされるドメインの構造制御には不向きである。
【0016】
金属イオンドーピング酸化チタンにおいては、出来る限り、酸化チタン結晶の表面層に金属イオンが存在し、それが結晶格子中欠陥または結晶表面にて異物同士の共融体を形成することができれば、可視光応答性触媒機能発現にはもっと有効となると考えられる。本発明は、酸化チタン形成のゾルゲル反応中に金属化合物を混合することではなく、酸化チタン結晶そのものを出発原料とし、その結晶表面に金属イオン化合物を吸着させた後、これを焼成することによって、金属イオンをドープすることを着想し、完成したものである。
【0017】
[酸化チタン]
本発明で用いる酸化チタンは、アナターゼ型結晶単独またはルチル型結晶単独ではなく、二つの結晶相が混在したアナターゼ/ルチル混晶型酸化チタン(A)を用いることを特徴とする。
【0018】
ルチル型結晶相は高温で安定的に形成する特徴を有することから、アナターゼ型とルチル型の結晶相が混在した混晶型酸化チタン(A)は、例えば、市販のアナターゼ型結晶性の酸化チタンまたはアルコキシチタンのゾルゲル反応から得た酸化チタンを一定温度で焼成し、それにルチル結晶相を成長させることで調製できる。
【0019】
上記アナターゼ型結晶性酸化チタンを焼成する際の温度条件としては、650〜800℃の範囲であればルチル型結晶相を好適に誘導出来る。焼成時間は、温度条件にもよるが、ルチル型結晶相の成長が行き過ぎることを避けるために、概ね1〜4時間の範囲であることが望ましい。
【0020】
また、異なる結晶相を有する酸化チタンを用いる場合には、アナターゼ型結晶性酸化チタン(a1)とルチル型結晶性酸化チタン(a2)とを一定割合で混合した後、後述する方法で金属イオンをドーピングする方法であってもよく、またはそれを300〜500℃の範囲で1〜3時間加熱処理して予め、アナターゼ/ルチル混晶型酸化チタン(A)としてから、後の工程に供しても良い。このとき、アナターゼ型結晶性酸化チタンとルチル型結晶性酸化チタンとを水またはアルコール中分散し、攪拌またはミーリングした後、濾過、乾燥する方法であっても、粉末のまま混合する方法であっても良い。
【0021】
また、アナターゼ/ルチル混晶型酸化チタン(A)の市販品、例えば、日本アエロジル株式会社で販売している触媒用酸化チタンP25等は、そのまま用いることができる。
【0022】
本発明において、可視光応答型光触媒機能を効率よく発現させるためには、アナターゼ/ルチル混晶型酸化チタン(A)中のアナターゼ型結晶性の酸化チタン(a1)とルチル型結晶性の酸化チタン(a2)との存在割合(a1):(a2)が99/1〜60/40(質量比)の範囲であることが好ましく、85/15〜70/30の範囲であることがより好ましい。
【0023】
[酸化チタン結晶の金属イオン吸着]
二つの結晶相が混在したアナターゼ/ルチル混晶型酸化チタン(A)に、金属イオンの水溶液(B)を接触させることにより、該酸化チタン(A)に金属イオンを吸着させる。このとき、酸化チタン表面のTi−OH結合部分と金属イオンとの相互作用を促進させることが重要である。
【0024】
通常酸化チタンの表面は極性が強く、またルイス酸性を示している。このため、金属イオンの水溶液(B)としては遷移金属イオンの水溶液、又は希土類金属イオンの水溶液であることが好ましい。即ち、金属イオンの水溶液(B)中における金属種が、遷移金属及び希土類金属からなる群から選ばれる一種以上の金属であることが好ましい。
【0025】
前記遷移金属としては、例えば、バナジウム、クロム、マンガン、鉄、コバルト、ニッケル、銅、モリブデン、タングステン、亜鉛等を好ましく用いることができ、その中でも、クロムとニッケルは可視光触媒活性をもっとも高めることができるので更に好適に用いることができる。
【0026】
前記希土類金属としては、ランタンを用いることが好ましい。希土類金属の場合は単独使用よりも、遷移金属と混合して用いることが好ましく、このとき希土類金属と遷移金属とのモル比が1/99〜5/95の範囲であれば好適である。
【0027】
金属イオンの水溶液(B)としては、金属の2価、3価の塩類、または高価の金属酸根の化合物を水中溶解させることで得ることができる。金属イオン化合物としては、例えば、上記遷移金属イオンの硝酸塩、硫酸塩、リン酸塩、塩酸塩、酢酸塩などを挙げることができる。また、金属イオン化合物として、金属酸根のアンモニウム化合物であるクロム酸アンモニウム、モリブデン酸アンモニウム、タングステン酸アンモニウム、コバルト酸アンモニウム、バナジウム酸アンモニウムなどを用いても良い。
【0028】
金属イオンの使用量は、前記酸化チタン(A)の質量に合わせて調製することが望ましく、酸化チタン/金属イオンで表される質量比で80/20〜99.5/0.5の範囲であることが好ましく、特に80/20〜98/2の範囲であれば好適である。
【0029】
金属イオンの水溶液(B)の濃度としては、特に限定する必要がないが、0.1〜0.5mol/Lの範囲であれば好適である。
【0030】
前記酸化チタン(A)と前記金属イオンの水溶液(B)とを接触させるだけで、酸化チタン(A)表面に金属イオンの吸着が行なわれるものであるが、金属イオンと錯体を形成出来るポリアミン類を介して吸着させても良い。例えば、ポリエチレンイミン、ポリアリルアミン、ポリビニルアミン、ポリリシンなどの塩基性ポリマーを金属イオンの水溶液(B)と混合し、予め錯体を形成させた後、そのポリマー錯体溶液に酸化チタン(A)を混合させることで金属イオンを酸化チタン表面に効率的に吸着させることもできる。
【0031】
接触させる方法としては、酸化チタン(A)と金属イオンの水溶液(B)を一定割合で混合した後、それを室温(20〜30℃)で1〜24時間攪拌することで十分効果的に吸着を行なうことができる。
【0032】
吸着後の酸化チタン(A)の固体は蒸留水で洗浄した後、それを室温で乾燥させることで金属イオンが吸着した酸化チタン粉末を得ることができる。
【0033】
[酸化チタン結晶表面での金属イオンのドープ]
上記で得られた金属イオンを吸着したアナターゼ/ルチル混晶型酸化チタンを加熱焼成することで、酸化チタンの結晶表面に金属イオンをドープさせることができる。
【0034】
加熱焼成温度は300〜900℃の範囲であれば良く、アナターゼ結晶相のルチル結晶相への過度な変換を抑制するためには、焼成温度を500〜700℃に設定することが好ましい。
【0035】
焼成時間は通常2〜8時間であればよく、温度上昇をプログラム的に制御することが好ましい。例えば、室温から300℃まで1時間をかけて上昇させ、その後、30分かけて500℃まで上昇させた後、その温度で3時間保持させること等、段階的な焼成であることが好ましい。
【0036】
温度上昇プログラムは得られる金属イオンドーピング酸化チタンの光触媒活性に影響を与えるが、金属イオン(B’)の種類によってもそのプログラムを都度調整することが好ましい。
【0037】
また、加熱焼成過程を空気雰囲気下で行なうことが好ましいが、不活性ガス、例えば、窒素雰囲気下で行なうこともできる。
【0038】
ドーピング後の金属イオンの量は、基本的に吸着された金属イオンの量により決まるが、酸化チタンと金属イオンとの質量比で80/20〜99.5/0.5に調製することができる。
【0039】
本発明でドーピングされた金属イオンが酸化チタンのどの結晶相に局在するのかは不明である。しかし、単一結晶相の酸化チタンで同様な手法を用いて金属イオンをドープしても、光触媒としての可視光応答性が発現しないことから、可視光応答型光触媒として機能するには、アナターゼ型結晶相とルチル型結晶相の二つの結晶間で形成したインターフェースのところに存在すると推察される。
【0040】
本発明の可視光応答型光触媒は、前述の手法で得られたものであり、その触媒機能に優れることから、アナターゼ/ルチル混晶型酸化チタン(A)に遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)がドーピングしてなるものであることが好ましい。
【0041】
[可視光応答型光触媒機能]
本発明での可視光というのは、蛍光灯下440nm以下の光をカットした前提での光源を指す。このような条件下、特に色素水溶液の脱色または、光触媒に吸着された状態の色素の分解反応において有効であることを本発明では可視光応答性という。
【0042】
従って、本発明での可視光触媒活性は、一定濃度の色素水溶液中に本発明の光触媒の粉末を混合し、その混合液に可視光照射することで、色素濃度が光照射時間に伴う変化から見積もることができる。
【0043】
用いる色素の初期濃度は5〜20ppmであればよく、触媒粉末の使用量は水溶液の体積に対して5〜100mg/20mL範囲であれば好適である。
【0044】
色素としては、特に限定することではなく、水溶性染料全般を用いることができる。また、溶剤溶解型色素でもそれが光触媒粉末の表面に吸着されうるものであれば、可視光下で脱色(分解反応)を行なうことができる。更に、色素以外の有機化合物であっても、光触媒の表面に付着可能であれば、可視光によって分解反応を行うことができる。
【0045】
光照射時間は、色素濃度または色素構造により異なるが、10時間〜1週間の範囲であることが望ましい。
【0046】
室内蛍光灯は、一定の紫外光線を有するが、それをカットしていない状態で用いると紫外光と可視光の両方を光源とすることができるため、紫外光線をカットせずに本発明の光触媒を用いることでも、触媒活性は効果的に発現させることができる。
【0047】
また、本発明の光触媒は、紫外線単独でも触媒活性を示し、太陽光、キセノンランプ、水銀ランプ、ハロゲンランプなど、種々の光源下でも光触媒として用いることができる。
【0048】
本発明の可視光応答型光触媒を用いる際には、本発明の金属イオンドーピング酸化チタンを用いること以外になんら制限されるものではなく、その他の光触媒と併用しても、様々な基材等を含有していても良い。また、可視光応答型光触媒として用いるときの形状としても制限されず、例えば、粉末、粒子、ペレット、膜などの形状で用いることができ、使用する環境下に応じて適宜選択することが好ましい。また、コーティング剤に混合して用いることにより、光触媒機能を有する塗膜とすることも可能である。
【実施例】
【0049】
以下、実施例および参考例によって本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。特に断らない限り、「%」は「質量%」を表す。
【0050】
〔X線回折法(XRD)による酸化チタンの分析〕
酸化チタンを測定試料用ホルダーにのせ、それを株式会社リガク製広角X線回折装置「Rint−ultma」にセットし、Cu/Kα線、40kV/30mA、スキャンスピード1.0°/分、走査範囲20〜40°の条件で行った。
【0051】
〔UV−vis反射スペクトル〕
UV−vis反射スペクトルはOceanOptics製のUSB−4000分光器、DH−2000ランプを使用した。
【0052】
〔透過型電子顕微鏡による触媒構造観察〕
透過型電子顕微鏡はJEOL製のTEM2200FSを使用し、電圧200keVの条件で行った。
【0053】
〔X線光電子スペクトル〕
X線光電子スペクトルはULVAC製のPH1、Quantera SXMを用い、電圧1.0V、電流20μA、ビーム直径105μmの条件で行った。
【0054】
〔蛍光X線スペクトルによるドープ金属含有量測定〕
蛍光X線測定は株式会社リガク製のZSXを用いて、真空条件下で行った。
【0055】
〔吸光度スペクトル〕
吸光度スペクトルは日立製作所製のU−3500分光光度計により測定した。
【0056】
〔光触媒活性評価〕
光触媒活性はメチレンブルー水溶液の脱色反応速度から評価した。メチレンブルー水溶液は20ml、濃度は10ppmのものを用い、触媒は0.03gを使用し、20mlスクリュー管に封入した状態で光照射を行った。光源は蛍光灯を440nm以下の波長の光をカットするフィルターで包んだもの使用し、光量は約5,500lxで行った。メチレンブルーの脱色は吸収スペクトルの664nmにおける吸光度変化から評価した。
【0057】
実施例1
<アナターゼ型結晶性酸化チタンとルチル型結晶性酸化チタンとを原料として用いる金属イオンドーピング酸化チタンの合成>
アナターゼ型結晶性酸化チタン(a1、関東化学株式会社製)とルチル型結晶性酸化チタン(a2、和光純薬工業株式会社製)を合計1.85gになるように表中記載の割合で乳鉢を用いて良く混合した。二つの結晶構造が同時に存在していることをX線回折パターンから確認した(図1)。ドーピング用の金属化合物としてはCr、Co、Cu、Fe、V、Mnイオンの硝酸塩を用い、各々の水溶液(0.1M)を調製した。上記水溶液1.5mLに蒸留水を48.5mL加えた後、それに酸化チタン粉末1.85gを混合した。
【0058】
超音波洗浄器にて、1時間照射した後、1晩静置した。遠心分離機を用いて上澄みを除去し、固体部分を蒸留水で洗浄し余分な金属元素を取り除く作業を3回繰り返した。金属イオンの吸着した酸化チタン沈殿物を、真空乾燥機を用いて乾燥させた。乾燥した粉末を、空気雰囲気下、電気炉を用いて室温から300℃まで30分加熱し、300℃/1時間保持後、さらに30分かけて600℃まで温度を上げ、その温度で30分保持した後、自然冷却した。この焼成プログラムにより、金属イオンドーピング酸化チタンの粉末を得た。これらの金属イオンドーピング酸化チタンを表1に示した
【0059】
【表1】

【0060】
上記の金属イオンドーピング酸化チタン粉末のUV−vis反射スペクトルを測定したところ約600nm付近までの吸収波長領域の拡大が見られた(図2)。
【0061】
比較例1
実施例1と同様にして、アナターゼ型結晶性酸化チタン(a1)とルチル型結晶性酸化チタン(a2)それぞれにCrイオンのドーピングを行なった。Crの含有率は両者とも0.26質量%であることを確認した。
【0062】
実施例2
<P25酸化チタンを用いた金属イオンドーピング酸化チタンの合成>
酸化チタンとして、P25(アナターゼ型結晶性とルチル型結晶性の混晶物、デグサ社製)を用い、上記実施例1と同様な方法で金属イオンのドーピングを行い、金属イオンドーピング酸化チタンを得た。これらの結果を表2に示した。
【0063】
【表2】

【0064】
原料として用いた酸化チタンP25の結晶構造を、X線回折測定を用いて調べたところ、アナターゼ結晶相とルチル結晶相が4/1の割合で存在していることが確認できた。更に試料No.T21では、金属イオンドーピングによる酸化チタンの格子定数の変化に起因する高角度側へのピークシフトが見られた(図3)。また、P25とNo.T21における可視光吸収を比較すると、No.T21では大きく可視光側への吸収領域の拡大が確認できた(図4)。吸収領域は約600nm付近まで拡大しており、可視光吸収能力が顕著に向上したことがわかる。更に、TEM撮影の結果、酸化チタンP25の単体結晶とは明らかに異なった構造の存在が確認できた(図5)。このことからP25の表面にクロムイオン由来の結晶表面変化が形成されていることがわかった。この結晶表面変化がクロム由来であることをXPS測定から調査した。測定の結果、クロムの2pに由来する強いピークが確認できた(図6)。クロム含有量が0.3%程度である点を考慮に入れると、P25の浅い表面付近にクロムイオンがドープされているものと考えられる。
【0065】
実施例3
<クロムのドーピング量が異なる酸化チタンの合成>
硝酸クロムの使用量を変えた以外、実施例2に示した同様な方法でドーピングし、クロム含有量が異なるクロムイオンドーピング酸化チタンを調製した。これらの結果を表3に示した。
【0066】
【表3】

【0067】
実施例4
<酸化チタンP25表面におけるポリマー金属イオン錯体吸着を経由する金属イオンドーピング酸化チタンの合成>
ポリエチレンイミン(分子量20,000;日本触媒製)1gを48.5mLの蒸留水中に溶解させた後、その溶液に1.5mL(0.1M)硝酸クロム水溶液を加え、ポリマー金属錯体溶液を調製した。この金属錯体溶液に、1.85gのP25を加え、1時間攪拌した後、1晩静置した。混合物を遠心分離機にて洗浄し、上澄みを除去した。この作業を3回繰り返した。得られた沈殿物を、40℃にて真空乾燥した。その粉末を、大気雰囲気下電気炉にて、室温から300℃まで30分加熱し、300℃/1時間保持後、さらに30分かけて600℃まで温度を上げ、その温度で30分保持した後、自然冷却した。この焼成プログラムにより、得たクロムイオンドーピング酸化チタン(T41)のCrの含有率が0.63質量%であった。また、アナターゼ型結晶相とルチル型結晶相との比は4/1であった。
【0068】
実施例5
<クロムとランタンとの共ドープの酸化チタンの合成>
P25を用いて、上記実施例2と同様な方法でクロムとランタンの二種類の金属イオンドープを行い、二種類の金属イオンが共ドープされた酸化チタンを得た。これらの結果を表4に示した。
【0069】
【表4】

【0070】
実施例6
<触媒No.T11を用いる可視光下でのメチレンブルーの脱色>
上記実施例1で得たクロムイオンドーピング酸化チタン粉末であるNo.T11(30mg)を用い、メチレンブルーの水溶液(20mL)と混合し、暗所で12時間放置した後、溶液を取り出し、そこに新たに新鮮なメチレンブルー水溶液(20mL)を加えた。一方、蛍光灯(10W)に管状の光フィルター(440nm以下をカット、ANNAKA社製)を被せた状態で、可視光の光量が5500lxの条件下、上記混合物中メチレンブルーの脱色反応を行った。一定時間毎に、上澄みの溶液を取り出し、それの吸収スペクトルを測定することで、光照射時間によるメチレンブルーの濃度変化を追跡した。メチレンブルーの濃度低下を図7に示した。比較に、比較例1で得たアナターゼ型結晶酸化チタン単独、またはルチル型結晶酸化チタン単独にクロムドープしたものを触媒として用いたが、いずれも可視光触媒活性は非常に低いレベルであった。このことは、アナターゼ型とルチル型の混晶体であるNo.T11を用いた場合のみ、可視光照射下でメチレンブルーの分解反応が確実に進行していることを強く示唆する。
【0071】
実施例7
<触媒No.T21を用いる可視光下でのメチレンブルーの脱色>
上記実施例2で得たクロムイオンドーピング酸化チタン粉末であるNo.T21(30mg)を用い、メチレンブルーの水溶液(20mL)と混合し、暗所で00時間放置した後、溶液を取り出し、そこに新たに新鮮なメチレンブルー水溶液(20mL)を加えた。一方、蛍光灯(10W)に管状の光フィルター(440nm以下をカット、ANNAKA社製)を被せた状態で、可視光の光量が5500lxの条件下、上記混合物中メチレンブルーの脱色反応を行った。メチレンブルーの濃度低下を図8に示した。比較に、窒素ドープ型酸化チタン(V−cat豊田中央研究所製)を触媒として用いたが、440nm以下光をカットした条件下、メチレンブルーの脱色はほとんど進行しなかった。図9に96時間照射後のメチレンブルーの吸収スペクトルを示した。反応初期から明確なピークシフトが起きた。このことは、可視光照射下でメチレンブルーの分解反応が確実に進行していることを強く示唆する。
【0072】
実施例8
<触媒No.T21を用いる可視光下でのトリパンブルーの脱色>
上記実施例7において、メチレンブルーの代わりにトリパンブルーを用いる以外、実施例7と同様にしてトリパンブルーの脱色反応を行った。トリパンブルーの濃度低下を図10に示した。トリパンブルーの吸収スペクトルにおいて、明確なピークシフト(図11)が起きた。このことは、可視光照射下でトリパンブルーの分解反応が確実に進行していることを強く示唆する。
【0073】
実施例9
<触媒No.T21を用いる可視光下でのクロロフェノールの分解>
上記実施例7において、メチレンブルーの代わりにクロロフェノール水溶液(20mL)を用い、クロロフェノール水溶液のpH変化の調査を行った。光照射に伴うクロロフェノール水溶液のpHの低下を図12に示した。これはクロロフェノールの塩素部分が光触媒の分解効果により脱離し、塩化水素を生成したためである。このことは、可視光照射下でクロロフェノールの分解反応が確実に進んでいることを強く示唆する。
【0074】
実施例10
<蛍光灯照射距離によるメチレンブルー脱色>
上記実施例5で得たクロム、ランタン共ドープの酸化チタンである粉末No.T54(30mg)を用いメチレンブルーの水溶液(20mL)と混合し、暗所で12時間静置した後、溶液を取り出し、そこに新たに新鮮なメチレンブルー水溶液(20mL)を加えた。一方、蛍光灯(10W、紫外線カットせず)とサンプル管距離を8cm(光量が6000lx)、28cm(1500lx)、160cm(500lx)の条件下、上記混合物中メチレンブルーの脱色反応を行った。一定時間毎に、上澄みの溶液を取り出し、それの吸収スペクトルを測定することで、光照射時間によるメチレンブルーの濃度変化を追跡した。各々の光量下でのメチレンブルーの濃度低下を図13−図15に示した。窒素ドープ型酸化チタンとの触媒活性と比較したところ、光量が大きい時は、両者の活性は同等レベルであった。しかし、光量が小さくなるにつれて窒素ドープ型酸化チタンの触媒活性はT54の触媒活性よりも大きく下回った。これは触媒No.T54が可視光線を効率良く利用していることを強く示している。紫外線は可視光線と比較して大気中を移動する際に空気によって大きく散乱、減衰を受ける。そのため触媒と光源との距離が大きくなるにつれて、紫外線頼りの触媒の全体光子吸収が弱く、結果的には触媒活性は低下する。替わりに可視光線を効率良く利用できる触媒は、可視光の光量に比例した触媒活性を示すことになる。本実施例の比較結果は、No.T54が優れた可視光応答型光触媒であることを強く示唆する。
【0075】
実施例11及び比較例2
<T22を用いるメチレンブルーの脱色反応>
上記実施例2で、No.T22を調製する際の焼成前クロムイオン担持体と、それを焼成してから得るNo.T22を用い、実施例7と同様な条件下、メチレンブルーの脱色反応を行なった。図16に照射時間に伴うメチレンブルーの残存率を示した。焼成後のNo.T22ではメチレンブルーが顕著に減少したが、それの前駆体である未焼成状態のクロムイオン担持体ではほとんど脱色が進まなかった。このことは、クロムイオン担持では可視光触媒活性は発現せず、焼成処理後において(即ち、酸化チタンにドーピングされた状態)で可視光触媒活性が発現できることを強く示唆する。
【図面の簡単な説明】
【0076】
【図1】実施例1での酸化チタン混合物のX線回折パターンである。
【図2】実施例1で得られた金属イオンドーピング酸化チタンT14(Feドープ)、T15(Vドープ)、T11(Crドープ)のUV−vis拡散反射スペクトルである。
【図3】実施例2で得たT21と原料P25のX線回折パターンである。
【図4】実施例2で得たT21と原料P25のUV−vis拡散反射スペクトルである。
【図5】実施例2で得たT21のTEM写真である。点線に囲まれた部分は酸化チタンと異なる構造である。
【図6】実施例2で得たT21のXPSスペクトルである。クロムの存在を示す結合エネルギーが観察された。
【図7】実施例1で得たT11及び比較例1で得た単一結晶系酸化チタンにクロムイオンをドーピングした酸化チタンを触媒として用いた時のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。
【図8】実施例2で得たT21を触媒として用いた時(実線)と、市販の窒素ドープ型酸化チタンを触媒として用いた時(破線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。
【図9】実施例2で得たT21を触媒として用いた時のメチレンブルー脱色に伴う吸収スペクトルである。
【図10】実施例2で得たT21を触媒として用いた時のトリパンブルーの残存率(650nm吸光度)対光照射時間のプロットである。
【図11】実施例2で得たT21を触媒として用いた時のトリパンブルーの脱色に伴う吸収スペクトルである。
【図12】実施例2で得たT21を触媒として用いた時のクロロフェノール溶液のpH対光照射時間のプロットである。
【図13】実施例5で得たT54を触媒として用いた時(破線)と、市販の窒素ドープ型酸化チタンを触媒として用いたとき(実線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。(照射条件:蛍光灯そのまま、光量6000lx)。
【図14】実施例5で得たT54を触媒として用いた時(破線)と、市販の窒素ドープ型酸化チタンを触媒として用いた時(実線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。(照射条件:蛍光灯そのまま、光量1500lx)。
【図15】実施例5で得たT54を触媒として用いた時(破線)と、市販の窒素ドープ型酸化チタンを触媒として用いた時(実線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。(照射条件:蛍光灯そのまま、光量500lx)。
【技術分野】
【0001】
本発明は、可視光応答型光触媒に関し、詳しくは、アナターゼとルチルの二つの結晶相が混在する混晶型酸化チタンに金属イオンがドーピングされてなる金属イオンドーピング型の可視光応答型光触媒とその簡便な製造方法に関するものである。
【背景技術】
【0002】
先端材料において、酸化チタンは従来の白色顔料、高屈折率材料と異なる応用物性を示すことで、ますます注目を集めている(非特許文献1参照。)。例えば、光触媒又は色素増感電荷分離機能では、酸化チタンは群を抜いた触媒材料であり、次世代型光触媒デバイス、太陽電池への応用分野での期待が大きい。また、エネルギー問題で大きな注目を集める燃料電池でも、酸化チタンに白金ナノ粒子を埋め込んだ電極層研究開発が脚光を浴びている。燃料電池の実用化には、水素製造が要求されるが、その水素製造用触媒でも、酸化チタン・白金のコンポジットが有力な候補となっている。
【0003】
近年、酸化チタンによる汚れや有害物質等を自発分解し無害化する光触媒機能が非常に注目されている。その応用分野は、住宅、車、医療、土地処理などへと広がり、循環型社会構築の不可欠技術として位置付けられている。しかしながら、酸化チタンの該光触媒機能を発現させるためには、紫外線を光源とすることが前提条件である。自然光(太陽光)にはわずか3%程度の紫外線しか含まれておらず、その大部分は可視光であることを鑑みると、紫外線のみを吸収する光触媒では、太陽光線の利用はほとんど無意味となる。即ち、酸化チタンを有効な光触媒として用いるためには、酸化チタンそのものの吸収範囲を可視光へ変換させることが最も重要である。従って、多くの研究では、酸化チタン中に不純物ともいわれるほどの原子ドーピング、例えばアニオン(窒素原子、炭素原子、硫黄原子、リン原子)ドーピング、またはカチオン(遷移金属、希土類金属、半金属等の金属イオン)ドーピング等が検討されてきた。
【0004】
酸化チタンにこれらのドーピングを行うには、いくつかの代表的な方法が知られている。例えば、チタン化合物のゾルゲル反応で酸化チタンを調製する際に、金属イオン化合物を同時に加え、得られた加水分解物を熱焼成することで着色酸化チタンを製造する方法が挙げられる(例えば、非特許文献2〜4参照。)。このような方法はもっとも簡易なゾルゲル反応であるので、多くの研究者に安易に利用されて来たが、実験条件により全く異なる結果になることが多く、再現性はほとんど保証できないと認識されている。したがって、その光触媒作用にも再現性が得られず、工業的な利用に用いるドーピング酸化チタンの製造方法とは言いがたいものが多い。
【0005】
このような状況から脱皮するため、加速電圧によるイオン注入法を用いることが開発されている(例えば、特許文献1参照)。前記特許文献1では、加速エネルギーにて金属イオンを酸化チタン結晶面に注入することで、酸化チタン結晶面に金属イオンをドーピングするものである。この手法は、注入イオンの量、種類などをコントロールできることから、ドーピング反応を目的にあわせて制御する方法としては確かに有効である。また、該手法にて得られるドーピング酸化チタンは可視光領域である400〜500nmの領域に吸収を示し、可視光応答型光触媒として機能することも確認されている。
【0006】
また、超高温ガスプラズマ法を用い、酸化チタン結晶格子中に鉄やアルミニウムなどの不純物準位の比較的高い原子をドーピングさせることも提案されている(例えば、特許文献2参照。)。しかしながら、これらの加速エネルギーイオン注入法、超高温プラズマ法はそのプロセス自体の生産コストが高く、循環型社会へ可視光応答型光触媒を供給することには全く不向きであるといっても過言ではない。
【0007】
可視光応答型光触媒として有用な金属ドーピング酸化チタンについてはその有効性が予測されるものの、いまだ工業的な簡便な製造方法は見出されておらず、可視光応答型として市販される酸化チタンであっても、室内の蛍光灯下では光触媒機能すら示さないことが多い。酸化チタンそのものに信頼性ある可視光応答性を付与することは重要な技術的課題である。
【0008】
【非特許文献1】A.L.Linsebiger et al.、Chem.Rev.1995年、第95巻、735頁
【非特許文献2】E.Borgarello et al.、J.Am.Chem.Soc.,1982年、第104巻、2996頁
【非特許文献3】L.Zang et al.、J.Phys.Chem.B 1998年、第102巻、10765頁
【非特許文献4】H.Kisch et al.、Angew.Chem.Int.Ed.,1998年、第37巻、3034頁
【非特許文献5】S.Sakthivel et al.、Angew.Chem..Int.Ed.、2003年、第42巻,4908頁
【特許文献1】特開平9−262482号公報
【発明の開示】
【発明が解決しようとする課題】
【0009】
上記実情を鑑み、本発明が解決しようとする課題は、簡便かつ工業的に有効な金属イオンを酸化チタン結晶へ直接ドーピングする製造方法、及び該製造方法で得られる全紫外線領域から約600nmまでの強い吸収を示す金属ドーピング酸化チタンからなる可視光応答型光触媒を提供することにある。
【課題を解決するための手段】
【0010】
本発明者は、前記課題を解決するために鋭意検討を重ねた結果、アナターゼ型結晶性とルチル型結晶性とを有するアナターゼ/ルチル混晶型酸化チタンに、金属イオンの水溶液を接触させた後、固体を取りだし、熱焼成させることで、金属イオンがドーピングした酸化チタンが容易に且つ再現性良く得られること、また、得られた金属イオンドーピング酸化チタンが可視光に応答する光触媒として機能することを見出し、本発明を完成した。
【0011】
即ち本発明は、アナターゼ/ルチル混晶型酸化チタンに、金属イオンの水溶液を接触させた後、固体を取りだし、300〜900℃で焼成することを特徴とする可視光応答型光触媒の製造方法を提供するものである。
【0012】
更に本発明は、アナターゼ/ルチル混晶型酸化チタンに遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオンがドーピングしてなることを特徴とする可視光応答型光触媒をも提供するものである。
【発明の効果】
【0013】
本発明の可視光応答型光触媒は、可視光への応答性が高く、色素類など有機物の分解能に優れる。また、その製造方法は、工業的汎用の整備のみで製造可能であり、再現性も高く工業的有用性が高い。
【0014】
また、本発明の製造方法では、単一種類の金属イオンに限らず、複数種のイオンを同時にドーピングすることも可能であり、可視光において広い吸収範囲を有する金属イオンドーピング酸化チタンが得られる。従って、本発明の製造方法で得られる金属イオンドーピング酸化チタンは、自然光(太陽光)のみならず、室内の蛍光灯下での有効利用の面からも期待できる。
【発明を実施するための最良の形態】
【0015】
酸化チタンに金属イオンをドープする際、もっとも広く用いられる方法は、アルコキシチタンのゾルゲル反応液中に、遷移金属塩を混合し、不純物が含まれた酸化チタン前駆体を調製し、その前駆体を一定温度にて加熱する方法である。このような方法では、金属イオンが酸化チタン本体と表面に分布した状態でドープされるが、金属イオンがドープされるドメインの構造制御には不向きである。
【0016】
金属イオンドーピング酸化チタンにおいては、出来る限り、酸化チタン結晶の表面層に金属イオンが存在し、それが結晶格子中欠陥または結晶表面にて異物同士の共融体を形成することができれば、可視光応答性触媒機能発現にはもっと有効となると考えられる。本発明は、酸化チタン形成のゾルゲル反応中に金属化合物を混合することではなく、酸化チタン結晶そのものを出発原料とし、その結晶表面に金属イオン化合物を吸着させた後、これを焼成することによって、金属イオンをドープすることを着想し、完成したものである。
【0017】
[酸化チタン]
本発明で用いる酸化チタンは、アナターゼ型結晶単独またはルチル型結晶単独ではなく、二つの結晶相が混在したアナターゼ/ルチル混晶型酸化チタン(A)を用いることを特徴とする。
【0018】
ルチル型結晶相は高温で安定的に形成する特徴を有することから、アナターゼ型とルチル型の結晶相が混在した混晶型酸化チタン(A)は、例えば、市販のアナターゼ型結晶性の酸化チタンまたはアルコキシチタンのゾルゲル反応から得た酸化チタンを一定温度で焼成し、それにルチル結晶相を成長させることで調製できる。
【0019】
上記アナターゼ型結晶性酸化チタンを焼成する際の温度条件としては、650〜800℃の範囲であればルチル型結晶相を好適に誘導出来る。焼成時間は、温度条件にもよるが、ルチル型結晶相の成長が行き過ぎることを避けるために、概ね1〜4時間の範囲であることが望ましい。
【0020】
また、異なる結晶相を有する酸化チタンを用いる場合には、アナターゼ型結晶性酸化チタン(a1)とルチル型結晶性酸化チタン(a2)とを一定割合で混合した後、後述する方法で金属イオンをドーピングする方法であってもよく、またはそれを300〜500℃の範囲で1〜3時間加熱処理して予め、アナターゼ/ルチル混晶型酸化チタン(A)としてから、後の工程に供しても良い。このとき、アナターゼ型結晶性酸化チタンとルチル型結晶性酸化チタンとを水またはアルコール中分散し、攪拌またはミーリングした後、濾過、乾燥する方法であっても、粉末のまま混合する方法であっても良い。
【0021】
また、アナターゼ/ルチル混晶型酸化チタン(A)の市販品、例えば、日本アエロジル株式会社で販売している触媒用酸化チタンP25等は、そのまま用いることができる。
【0022】
本発明において、可視光応答型光触媒機能を効率よく発現させるためには、アナターゼ/ルチル混晶型酸化チタン(A)中のアナターゼ型結晶性の酸化チタン(a1)とルチル型結晶性の酸化チタン(a2)との存在割合(a1):(a2)が99/1〜60/40(質量比)の範囲であることが好ましく、85/15〜70/30の範囲であることがより好ましい。
【0023】
[酸化チタン結晶の金属イオン吸着]
二つの結晶相が混在したアナターゼ/ルチル混晶型酸化チタン(A)に、金属イオンの水溶液(B)を接触させることにより、該酸化チタン(A)に金属イオンを吸着させる。このとき、酸化チタン表面のTi−OH結合部分と金属イオンとの相互作用を促進させることが重要である。
【0024】
通常酸化チタンの表面は極性が強く、またルイス酸性を示している。このため、金属イオンの水溶液(B)としては遷移金属イオンの水溶液、又は希土類金属イオンの水溶液であることが好ましい。即ち、金属イオンの水溶液(B)中における金属種が、遷移金属及び希土類金属からなる群から選ばれる一種以上の金属であることが好ましい。
【0025】
前記遷移金属としては、例えば、バナジウム、クロム、マンガン、鉄、コバルト、ニッケル、銅、モリブデン、タングステン、亜鉛等を好ましく用いることができ、その中でも、クロムとニッケルは可視光触媒活性をもっとも高めることができるので更に好適に用いることができる。
【0026】
前記希土類金属としては、ランタンを用いることが好ましい。希土類金属の場合は単独使用よりも、遷移金属と混合して用いることが好ましく、このとき希土類金属と遷移金属とのモル比が1/99〜5/95の範囲であれば好適である。
【0027】
金属イオンの水溶液(B)としては、金属の2価、3価の塩類、または高価の金属酸根の化合物を水中溶解させることで得ることができる。金属イオン化合物としては、例えば、上記遷移金属イオンの硝酸塩、硫酸塩、リン酸塩、塩酸塩、酢酸塩などを挙げることができる。また、金属イオン化合物として、金属酸根のアンモニウム化合物であるクロム酸アンモニウム、モリブデン酸アンモニウム、タングステン酸アンモニウム、コバルト酸アンモニウム、バナジウム酸アンモニウムなどを用いても良い。
【0028】
金属イオンの使用量は、前記酸化チタン(A)の質量に合わせて調製することが望ましく、酸化チタン/金属イオンで表される質量比で80/20〜99.5/0.5の範囲であることが好ましく、特に80/20〜98/2の範囲であれば好適である。
【0029】
金属イオンの水溶液(B)の濃度としては、特に限定する必要がないが、0.1〜0.5mol/Lの範囲であれば好適である。
【0030】
前記酸化チタン(A)と前記金属イオンの水溶液(B)とを接触させるだけで、酸化チタン(A)表面に金属イオンの吸着が行なわれるものであるが、金属イオンと錯体を形成出来るポリアミン類を介して吸着させても良い。例えば、ポリエチレンイミン、ポリアリルアミン、ポリビニルアミン、ポリリシンなどの塩基性ポリマーを金属イオンの水溶液(B)と混合し、予め錯体を形成させた後、そのポリマー錯体溶液に酸化チタン(A)を混合させることで金属イオンを酸化チタン表面に効率的に吸着させることもできる。
【0031】
接触させる方法としては、酸化チタン(A)と金属イオンの水溶液(B)を一定割合で混合した後、それを室温(20〜30℃)で1〜24時間攪拌することで十分効果的に吸着を行なうことができる。
【0032】
吸着後の酸化チタン(A)の固体は蒸留水で洗浄した後、それを室温で乾燥させることで金属イオンが吸着した酸化チタン粉末を得ることができる。
【0033】
[酸化チタン結晶表面での金属イオンのドープ]
上記で得られた金属イオンを吸着したアナターゼ/ルチル混晶型酸化チタンを加熱焼成することで、酸化チタンの結晶表面に金属イオンをドープさせることができる。
【0034】
加熱焼成温度は300〜900℃の範囲であれば良く、アナターゼ結晶相のルチル結晶相への過度な変換を抑制するためには、焼成温度を500〜700℃に設定することが好ましい。
【0035】
焼成時間は通常2〜8時間であればよく、温度上昇をプログラム的に制御することが好ましい。例えば、室温から300℃まで1時間をかけて上昇させ、その後、30分かけて500℃まで上昇させた後、その温度で3時間保持させること等、段階的な焼成であることが好ましい。
【0036】
温度上昇プログラムは得られる金属イオンドーピング酸化チタンの光触媒活性に影響を与えるが、金属イオン(B’)の種類によってもそのプログラムを都度調整することが好ましい。
【0037】
また、加熱焼成過程を空気雰囲気下で行なうことが好ましいが、不活性ガス、例えば、窒素雰囲気下で行なうこともできる。
【0038】
ドーピング後の金属イオンの量は、基本的に吸着された金属イオンの量により決まるが、酸化チタンと金属イオンとの質量比で80/20〜99.5/0.5に調製することができる。
【0039】
本発明でドーピングされた金属イオンが酸化チタンのどの結晶相に局在するのかは不明である。しかし、単一結晶相の酸化チタンで同様な手法を用いて金属イオンをドープしても、光触媒としての可視光応答性が発現しないことから、可視光応答型光触媒として機能するには、アナターゼ型結晶相とルチル型結晶相の二つの結晶間で形成したインターフェースのところに存在すると推察される。
【0040】
本発明の可視光応答型光触媒は、前述の手法で得られたものであり、その触媒機能に優れることから、アナターゼ/ルチル混晶型酸化チタン(A)に遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)がドーピングしてなるものであることが好ましい。
【0041】
[可視光応答型光触媒機能]
本発明での可視光というのは、蛍光灯下440nm以下の光をカットした前提での光源を指す。このような条件下、特に色素水溶液の脱色または、光触媒に吸着された状態の色素の分解反応において有効であることを本発明では可視光応答性という。
【0042】
従って、本発明での可視光触媒活性は、一定濃度の色素水溶液中に本発明の光触媒の粉末を混合し、その混合液に可視光照射することで、色素濃度が光照射時間に伴う変化から見積もることができる。
【0043】
用いる色素の初期濃度は5〜20ppmであればよく、触媒粉末の使用量は水溶液の体積に対して5〜100mg/20mL範囲であれば好適である。
【0044】
色素としては、特に限定することではなく、水溶性染料全般を用いることができる。また、溶剤溶解型色素でもそれが光触媒粉末の表面に吸着されうるものであれば、可視光下で脱色(分解反応)を行なうことができる。更に、色素以外の有機化合物であっても、光触媒の表面に付着可能であれば、可視光によって分解反応を行うことができる。
【0045】
光照射時間は、色素濃度または色素構造により異なるが、10時間〜1週間の範囲であることが望ましい。
【0046】
室内蛍光灯は、一定の紫外光線を有するが、それをカットしていない状態で用いると紫外光と可視光の両方を光源とすることができるため、紫外光線をカットせずに本発明の光触媒を用いることでも、触媒活性は効果的に発現させることができる。
【0047】
また、本発明の光触媒は、紫外線単独でも触媒活性を示し、太陽光、キセノンランプ、水銀ランプ、ハロゲンランプなど、種々の光源下でも光触媒として用いることができる。
【0048】
本発明の可視光応答型光触媒を用いる際には、本発明の金属イオンドーピング酸化チタンを用いること以外になんら制限されるものではなく、その他の光触媒と併用しても、様々な基材等を含有していても良い。また、可視光応答型光触媒として用いるときの形状としても制限されず、例えば、粉末、粒子、ペレット、膜などの形状で用いることができ、使用する環境下に応じて適宜選択することが好ましい。また、コーティング剤に混合して用いることにより、光触媒機能を有する塗膜とすることも可能である。
【実施例】
【0049】
以下、実施例および参考例によって本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。特に断らない限り、「%」は「質量%」を表す。
【0050】
〔X線回折法(XRD)による酸化チタンの分析〕
酸化チタンを測定試料用ホルダーにのせ、それを株式会社リガク製広角X線回折装置「Rint−ultma」にセットし、Cu/Kα線、40kV/30mA、スキャンスピード1.0°/分、走査範囲20〜40°の条件で行った。
【0051】
〔UV−vis反射スペクトル〕
UV−vis反射スペクトルはOceanOptics製のUSB−4000分光器、DH−2000ランプを使用した。
【0052】
〔透過型電子顕微鏡による触媒構造観察〕
透過型電子顕微鏡はJEOL製のTEM2200FSを使用し、電圧200keVの条件で行った。
【0053】
〔X線光電子スペクトル〕
X線光電子スペクトルはULVAC製のPH1、Quantera SXMを用い、電圧1.0V、電流20μA、ビーム直径105μmの条件で行った。
【0054】
〔蛍光X線スペクトルによるドープ金属含有量測定〕
蛍光X線測定は株式会社リガク製のZSXを用いて、真空条件下で行った。
【0055】
〔吸光度スペクトル〕
吸光度スペクトルは日立製作所製のU−3500分光光度計により測定した。
【0056】
〔光触媒活性評価〕
光触媒活性はメチレンブルー水溶液の脱色反応速度から評価した。メチレンブルー水溶液は20ml、濃度は10ppmのものを用い、触媒は0.03gを使用し、20mlスクリュー管に封入した状態で光照射を行った。光源は蛍光灯を440nm以下の波長の光をカットするフィルターで包んだもの使用し、光量は約5,500lxで行った。メチレンブルーの脱色は吸収スペクトルの664nmにおける吸光度変化から評価した。
【0057】
実施例1
<アナターゼ型結晶性酸化チタンとルチル型結晶性酸化チタンとを原料として用いる金属イオンドーピング酸化チタンの合成>
アナターゼ型結晶性酸化チタン(a1、関東化学株式会社製)とルチル型結晶性酸化チタン(a2、和光純薬工業株式会社製)を合計1.85gになるように表中記載の割合で乳鉢を用いて良く混合した。二つの結晶構造が同時に存在していることをX線回折パターンから確認した(図1)。ドーピング用の金属化合物としてはCr、Co、Cu、Fe、V、Mnイオンの硝酸塩を用い、各々の水溶液(0.1M)を調製した。上記水溶液1.5mLに蒸留水を48.5mL加えた後、それに酸化チタン粉末1.85gを混合した。
【0058】
超音波洗浄器にて、1時間照射した後、1晩静置した。遠心分離機を用いて上澄みを除去し、固体部分を蒸留水で洗浄し余分な金属元素を取り除く作業を3回繰り返した。金属イオンの吸着した酸化チタン沈殿物を、真空乾燥機を用いて乾燥させた。乾燥した粉末を、空気雰囲気下、電気炉を用いて室温から300℃まで30分加熱し、300℃/1時間保持後、さらに30分かけて600℃まで温度を上げ、その温度で30分保持した後、自然冷却した。この焼成プログラムにより、金属イオンドーピング酸化チタンの粉末を得た。これらの金属イオンドーピング酸化チタンを表1に示した
【0059】
【表1】

【0060】
上記の金属イオンドーピング酸化チタン粉末のUV−vis反射スペクトルを測定したところ約600nm付近までの吸収波長領域の拡大が見られた(図2)。
【0061】
比較例1
実施例1と同様にして、アナターゼ型結晶性酸化チタン(a1)とルチル型結晶性酸化チタン(a2)それぞれにCrイオンのドーピングを行なった。Crの含有率は両者とも0.26質量%であることを確認した。
【0062】
実施例2
<P25酸化チタンを用いた金属イオンドーピング酸化チタンの合成>
酸化チタンとして、P25(アナターゼ型結晶性とルチル型結晶性の混晶物、デグサ社製)を用い、上記実施例1と同様な方法で金属イオンのドーピングを行い、金属イオンドーピング酸化チタンを得た。これらの結果を表2に示した。
【0063】
【表2】

【0064】
原料として用いた酸化チタンP25の結晶構造を、X線回折測定を用いて調べたところ、アナターゼ結晶相とルチル結晶相が4/1の割合で存在していることが確認できた。更に試料No.T21では、金属イオンドーピングによる酸化チタンの格子定数の変化に起因する高角度側へのピークシフトが見られた(図3)。また、P25とNo.T21における可視光吸収を比較すると、No.T21では大きく可視光側への吸収領域の拡大が確認できた(図4)。吸収領域は約600nm付近まで拡大しており、可視光吸収能力が顕著に向上したことがわかる。更に、TEM撮影の結果、酸化チタンP25の単体結晶とは明らかに異なった構造の存在が確認できた(図5)。このことからP25の表面にクロムイオン由来の結晶表面変化が形成されていることがわかった。この結晶表面変化がクロム由来であることをXPS測定から調査した。測定の結果、クロムの2pに由来する強いピークが確認できた(図6)。クロム含有量が0.3%程度である点を考慮に入れると、P25の浅い表面付近にクロムイオンがドープされているものと考えられる。
【0065】
実施例3
<クロムのドーピング量が異なる酸化チタンの合成>
硝酸クロムの使用量を変えた以外、実施例2に示した同様な方法でドーピングし、クロム含有量が異なるクロムイオンドーピング酸化チタンを調製した。これらの結果を表3に示した。
【0066】
【表3】

【0067】
実施例4
<酸化チタンP25表面におけるポリマー金属イオン錯体吸着を経由する金属イオンドーピング酸化チタンの合成>
ポリエチレンイミン(分子量20,000;日本触媒製)1gを48.5mLの蒸留水中に溶解させた後、その溶液に1.5mL(0.1M)硝酸クロム水溶液を加え、ポリマー金属錯体溶液を調製した。この金属錯体溶液に、1.85gのP25を加え、1時間攪拌した後、1晩静置した。混合物を遠心分離機にて洗浄し、上澄みを除去した。この作業を3回繰り返した。得られた沈殿物を、40℃にて真空乾燥した。その粉末を、大気雰囲気下電気炉にて、室温から300℃まで30分加熱し、300℃/1時間保持後、さらに30分かけて600℃まで温度を上げ、その温度で30分保持した後、自然冷却した。この焼成プログラムにより、得たクロムイオンドーピング酸化チタン(T41)のCrの含有率が0.63質量%であった。また、アナターゼ型結晶相とルチル型結晶相との比は4/1であった。
【0068】
実施例5
<クロムとランタンとの共ドープの酸化チタンの合成>
P25を用いて、上記実施例2と同様な方法でクロムとランタンの二種類の金属イオンドープを行い、二種類の金属イオンが共ドープされた酸化チタンを得た。これらの結果を表4に示した。
【0069】
【表4】

【0070】
実施例6
<触媒No.T11を用いる可視光下でのメチレンブルーの脱色>
上記実施例1で得たクロムイオンドーピング酸化チタン粉末であるNo.T11(30mg)を用い、メチレンブルーの水溶液(20mL)と混合し、暗所で12時間放置した後、溶液を取り出し、そこに新たに新鮮なメチレンブルー水溶液(20mL)を加えた。一方、蛍光灯(10W)に管状の光フィルター(440nm以下をカット、ANNAKA社製)を被せた状態で、可視光の光量が5500lxの条件下、上記混合物中メチレンブルーの脱色反応を行った。一定時間毎に、上澄みの溶液を取り出し、それの吸収スペクトルを測定することで、光照射時間によるメチレンブルーの濃度変化を追跡した。メチレンブルーの濃度低下を図7に示した。比較に、比較例1で得たアナターゼ型結晶酸化チタン単独、またはルチル型結晶酸化チタン単独にクロムドープしたものを触媒として用いたが、いずれも可視光触媒活性は非常に低いレベルであった。このことは、アナターゼ型とルチル型の混晶体であるNo.T11を用いた場合のみ、可視光照射下でメチレンブルーの分解反応が確実に進行していることを強く示唆する。
【0071】
実施例7
<触媒No.T21を用いる可視光下でのメチレンブルーの脱色>
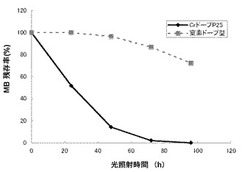
上記実施例2で得たクロムイオンドーピング酸化チタン粉末であるNo.T21(30mg)を用い、メチレンブルーの水溶液(20mL)と混合し、暗所で00時間放置した後、溶液を取り出し、そこに新たに新鮮なメチレンブルー水溶液(20mL)を加えた。一方、蛍光灯(10W)に管状の光フィルター(440nm以下をカット、ANNAKA社製)を被せた状態で、可視光の光量が5500lxの条件下、上記混合物中メチレンブルーの脱色反応を行った。メチレンブルーの濃度低下を図8に示した。比較に、窒素ドープ型酸化チタン(V−cat豊田中央研究所製)を触媒として用いたが、440nm以下光をカットした条件下、メチレンブルーの脱色はほとんど進行しなかった。図9に96時間照射後のメチレンブルーの吸収スペクトルを示した。反応初期から明確なピークシフトが起きた。このことは、可視光照射下でメチレンブルーの分解反応が確実に進行していることを強く示唆する。
【0072】
実施例8
<触媒No.T21を用いる可視光下でのトリパンブルーの脱色>
上記実施例7において、メチレンブルーの代わりにトリパンブルーを用いる以外、実施例7と同様にしてトリパンブルーの脱色反応を行った。トリパンブルーの濃度低下を図10に示した。トリパンブルーの吸収スペクトルにおいて、明確なピークシフト(図11)が起きた。このことは、可視光照射下でトリパンブルーの分解反応が確実に進行していることを強く示唆する。
【0073】
実施例9
<触媒No.T21を用いる可視光下でのクロロフェノールの分解>
上記実施例7において、メチレンブルーの代わりにクロロフェノール水溶液(20mL)を用い、クロロフェノール水溶液のpH変化の調査を行った。光照射に伴うクロロフェノール水溶液のpHの低下を図12に示した。これはクロロフェノールの塩素部分が光触媒の分解効果により脱離し、塩化水素を生成したためである。このことは、可視光照射下でクロロフェノールの分解反応が確実に進んでいることを強く示唆する。
【0074】
実施例10
<蛍光灯照射距離によるメチレンブルー脱色>
上記実施例5で得たクロム、ランタン共ドープの酸化チタンである粉末No.T54(30mg)を用いメチレンブルーの水溶液(20mL)と混合し、暗所で12時間静置した後、溶液を取り出し、そこに新たに新鮮なメチレンブルー水溶液(20mL)を加えた。一方、蛍光灯(10W、紫外線カットせず)とサンプル管距離を8cm(光量が6000lx)、28cm(1500lx)、160cm(500lx)の条件下、上記混合物中メチレンブルーの脱色反応を行った。一定時間毎に、上澄みの溶液を取り出し、それの吸収スペクトルを測定することで、光照射時間によるメチレンブルーの濃度変化を追跡した。各々の光量下でのメチレンブルーの濃度低下を図13−図15に示した。窒素ドープ型酸化チタンとの触媒活性と比較したところ、光量が大きい時は、両者の活性は同等レベルであった。しかし、光量が小さくなるにつれて窒素ドープ型酸化チタンの触媒活性はT54の触媒活性よりも大きく下回った。これは触媒No.T54が可視光線を効率良く利用していることを強く示している。紫外線は可視光線と比較して大気中を移動する際に空気によって大きく散乱、減衰を受ける。そのため触媒と光源との距離が大きくなるにつれて、紫外線頼りの触媒の全体光子吸収が弱く、結果的には触媒活性は低下する。替わりに可視光線を効率良く利用できる触媒は、可視光の光量に比例した触媒活性を示すことになる。本実施例の比較結果は、No.T54が優れた可視光応答型光触媒であることを強く示唆する。
【0075】
実施例11及び比較例2
<T22を用いるメチレンブルーの脱色反応>
上記実施例2で、No.T22を調製する際の焼成前クロムイオン担持体と、それを焼成してから得るNo.T22を用い、実施例7と同様な条件下、メチレンブルーの脱色反応を行なった。図16に照射時間に伴うメチレンブルーの残存率を示した。焼成後のNo.T22ではメチレンブルーが顕著に減少したが、それの前駆体である未焼成状態のクロムイオン担持体ではほとんど脱色が進まなかった。このことは、クロムイオン担持では可視光触媒活性は発現せず、焼成処理後において(即ち、酸化チタンにドーピングされた状態)で可視光触媒活性が発現できることを強く示唆する。
【図面の簡単な説明】
【0076】
【図1】実施例1での酸化チタン混合物のX線回折パターンである。
【図2】実施例1で得られた金属イオンドーピング酸化チタンT14(Feドープ)、T15(Vドープ)、T11(Crドープ)のUV−vis拡散反射スペクトルである。
【図3】実施例2で得たT21と原料P25のX線回折パターンである。
【図4】実施例2で得たT21と原料P25のUV−vis拡散反射スペクトルである。
【図5】実施例2で得たT21のTEM写真である。点線に囲まれた部分は酸化チタンと異なる構造である。
【図6】実施例2で得たT21のXPSスペクトルである。クロムの存在を示す結合エネルギーが観察された。
【図7】実施例1で得たT11及び比較例1で得た単一結晶系酸化チタンにクロムイオンをドーピングした酸化チタンを触媒として用いた時のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。
【図8】実施例2で得たT21を触媒として用いた時(実線)と、市販の窒素ドープ型酸化チタンを触媒として用いた時(破線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。
【図9】実施例2で得たT21を触媒として用いた時のメチレンブルー脱色に伴う吸収スペクトルである。
【図10】実施例2で得たT21を触媒として用いた時のトリパンブルーの残存率(650nm吸光度)対光照射時間のプロットである。
【図11】実施例2で得たT21を触媒として用いた時のトリパンブルーの脱色に伴う吸収スペクトルである。
【図12】実施例2で得たT21を触媒として用いた時のクロロフェノール溶液のpH対光照射時間のプロットである。
【図13】実施例5で得たT54を触媒として用いた時(破線)と、市販の窒素ドープ型酸化チタンを触媒として用いたとき(実線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。(照射条件:蛍光灯そのまま、光量6000lx)。
【図14】実施例5で得たT54を触媒として用いた時(破線)と、市販の窒素ドープ型酸化チタンを触媒として用いた時(実線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。(照射条件:蛍光灯そのまま、光量1500lx)。
【図15】実施例5で得たT54を触媒として用いた時(破線)と、市販の窒素ドープ型酸化チタンを触媒として用いた時(実線)のメチレンブルーの残存率(664nm吸光度)対光照射時間のプロットである。(照射条件:蛍光灯そのまま、光量500lx)。
【特許請求の範囲】
【請求項1】
アナターゼ/ルチル混晶型酸化チタン(A)に、金属イオンの水溶液(B)を接触させた後、固体を取りだし、300〜900℃で焼成することを特徴とする可視光応答型光触媒の製造方法。
【請求項2】
アナターゼ/ルチル混晶型酸化チタン(A)におけるアナターゼ型結晶性の酸化チタン(a1)とルチル型結晶性の酸化チタンとの存在割合(a1):(a2)が99/1〜60/1(質量比)の範囲である請求項1記載の可視光応答型光触媒の製造方法。
【請求項3】
金属イオンの水溶液(B)中における金属種が、遷移金属及び希土類金属からなる群から選ばれる一種以上の金属である請求項1又は2記載の可視光応答型光触媒の製造方法
【請求項4】
焼成を空気雰囲気下で行なうものである請求項1〜3の何れか1項記載の可視光応答型光触媒の製造方法。
【請求項5】
アナターゼ/ルチル混晶型酸化チタン(A)と、金属イオンの水溶液(B)との混合比が、酸化チタン/金属イオンで表される質量比で80/20〜99.5/0.5である請求項1〜4の何れか1項記載の可視光応答型光触媒の製造方法。
【請求項6】
アナターゼ/ルチル混晶型酸化チタン(A)に遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)がドーピングしてなることを特徴とする可視光応答型光触媒。
【請求項7】
アナターゼ/ルチル混晶型酸化チタン(A)と、遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)との存在割合が、(A)/(B’)で表される質量比で80/20〜99.5/0.5である請求項6記載の可視光応答型光触媒。
【請求項1】
アナターゼ/ルチル混晶型酸化チタン(A)に、金属イオンの水溶液(B)を接触させた後、固体を取りだし、300〜900℃で焼成することを特徴とする可視光応答型光触媒の製造方法。
【請求項2】
アナターゼ/ルチル混晶型酸化チタン(A)におけるアナターゼ型結晶性の酸化チタン(a1)とルチル型結晶性の酸化チタンとの存在割合(a1):(a2)が99/1〜60/1(質量比)の範囲である請求項1記載の可視光応答型光触媒の製造方法。
【請求項3】
金属イオンの水溶液(B)中における金属種が、遷移金属及び希土類金属からなる群から選ばれる一種以上の金属である請求項1又は2記載の可視光応答型光触媒の製造方法
【請求項4】
焼成を空気雰囲気下で行なうものである請求項1〜3の何れか1項記載の可視光応答型光触媒の製造方法。
【請求項5】
アナターゼ/ルチル混晶型酸化チタン(A)と、金属イオンの水溶液(B)との混合比が、酸化チタン/金属イオンで表される質量比で80/20〜99.5/0.5である請求項1〜4の何れか1項記載の可視光応答型光触媒の製造方法。
【請求項6】
アナターゼ/ルチル混晶型酸化チタン(A)に遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)がドーピングしてなることを特徴とする可視光応答型光触媒。
【請求項7】
アナターゼ/ルチル混晶型酸化チタン(A)と、遷移金属及び希土類金属からなる群から選ばれる一種以上の金属のイオン(B’)との存在割合が、(A)/(B’)で表される質量比で80/20〜99.5/0.5である請求項6記載の可視光応答型光触媒。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【公開番号】特開2010−149046(P2010−149046A)
【公開日】平成22年7月8日(2010.7.8)
【国際特許分類】
【出願番号】特願2008−329861(P2008−329861)
【出願日】平成20年12月25日(2008.12.25)
【出願人】(000002886)DIC株式会社 (2,597)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
【公開日】平成22年7月8日(2010.7.8)
【国際特許分類】
【出願日】平成20年12月25日(2008.12.25)
【出願人】(000002886)DIC株式会社 (2,597)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
[ Back to top ]

